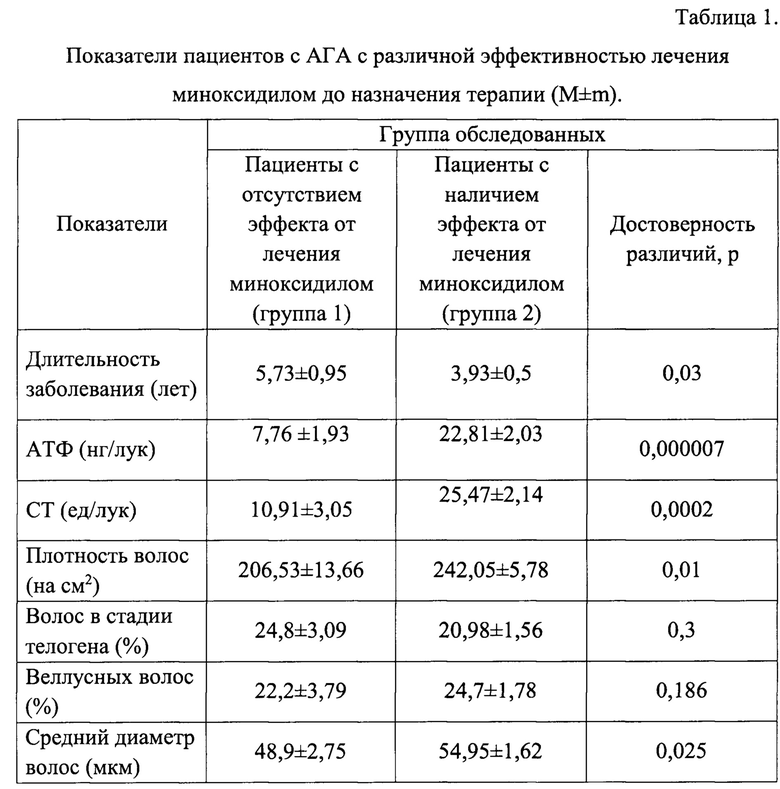
Изобретение относится к области медицины, а именно дерматовенерологии и косметологии, и может быть использовано в лечебно-профилактических учреждениях, имеющих в структуре отделение дерматовенерологии, косметологии, в кожно-венерологических диспансерах и специализированных отделениях профильных больниц, госпиталей, а также в медицинских учреждениях косметологической направленности для прогноза эффективности лечения андрогенетической алопеции.
Андрогенетическая алопеция (АГА) - естественный прогрессирующий процесс уменьшения плотности и толщины волос в лобно-теменной зоне, развивающийся в результате постепенного превращения терминальных волос1 (1Терминальные волосы - стержневые волосы, диаметром более 30 мкм) в веллюсные2 (2Веллюсные волосы - пушковые волосы, диаметром менее 30 мкм.) у людей с генетической предрасположенностью [1]. Эти нарушения вызваны миниатюризацией фолликулов в течение нескольких лет, проявляющейся в виде их уменьшения в размере и глубине залегания. Помимо изменения самого фолликула, происходит патологический сдвиг в цикле роста волоса с укорочением фазы анагена3 (3Фаза анагена - стадия роста волоса.) и преждевременным наступлением фазы телогена4 (4Стадия телогена - стадия выпадения волоса.) волоса [2]. При этом увеличивается доля телогеновых волос5 (5 Телогеновые волосы - волосы в стадии телогена, в норме их доля не превышает 15%.) в пораженной зоне скальпа.
В целом, хотя точные молекулярные механизмы, лежащие в основе предрасположенности к АГА, остаются неизвестными, наиболее вероятным механизмом реализации процесса считается воздействие на волосяные фолликулы гормона дигидротестостерона, активного метаболита тестостерона, образующегося из тестостерона с участием фермента 5-альфаредуктаза.
Различные степени андрогенетического поредения волос переживают около 50% мужчин и женщин старше 40 лет [3, 4]. Длительное прогрессирующее течение АГА, усиленное выпадение волос, поредение волосяного покрова в косметически важных зонах значительно снижают качество жизни пациентов [5, 6].
Основной целью лечения АГА является стабилизация процесса прогрессирующего истончения волос и/или стимуляция их роста.
В настоящее время единственным терапевтически эффективным наружным лечением АГА с высокой степенью достоверности является препарат миноксидил (2-5% лосьон и 5% пена), продемонстрировавший высокие результаты при нанесении на лобную и теменную зоны [7] и включенный в руководство по лечению андрогенетической алопеции [8].
Миноксидил - это пролекарство, превращающееся в наружной корневой оболочке волосяного фолликула в сульфат миноксидила с помощью фермента сульфотрансферазы (СТ) [9]. Миноксидил сульфат открывает АТФ-чувствительные калиевые каналы в клеточных мембранах, что оказывает сосудорасширяющее действие [10]. Точный механизм, с помощью которого он эффективен при АГА, еще до конца не изучен, но возможными механизмами его действия являются сосудорасширяющие и способствующие ангиогенезу эффекты, а также способность стимулировать фактор роста эндотелия сосудов (VEGF) [11]. Миноксидил способствует росту волос, продлевая продолжительность анагена, укорачивая телоген и увеличивая миниатюризованные фолликулы [12].
В клинической практике эффективность терапии АГА основана на динамическом наблюдении за выраженностью клинических симптомов заболевания - рост волос начинается в течение трех-восьми месяцев и стабилизируется через 12-18 месяцев; таким образом, рекомендуется год лечения, прежде чем оценивать его эффективность [15], тогда при отсутствии положительного лечебного эффекта лекарственного средства или незначительном улучшении состояния пациента лечащий врач меняет терапевтическую тактику. В связи с этим чрезвычайно актуальным в настоящее время является индивидуальное прогнозирование эффективности терапии заболеваний вообще и АГА в частности и оптимизация лечения путем применения персонифицированного подхода, позволяющего снизить как потенциальные риски применяемой терапии, так и экономические затраты на лечение.
При этом успешное персонифицированное лечение больных АГА возможно на основе учета не только клинических данных, но и более объективных, параклинических прогностических критериев, которые могут быть тесно связаны с патогенетическими механизмами АГА.
Аденозинтрифосфат (АТФ) известен как универсальный источник энергии для всех биохимических процессов, протекающих в живых системах, в том числе как важнейший источник энергии [16], в том числе, и для синтеза белков-кератинов. В клетках волосяного фолликула внутриклеточный АТФ участвует в работе сигнальных путей [17] и трансмембранных каналов [18], а выделяемый вовне - в межклеточной коммуникации через пуринергические рецепторы [19]. Потребность волосяного фолликула в АТФ может изменяться в зависимости от стадии роста волоса, возрастая в период активного клеточного деления (фаза анагена) [20, 21]. В то же время, дигидротестостерон может останавливать превращение АТФ в циклический АМФ (цАМФ) за счет ингибирования аденилатциклазы, и в этом случае снижение уровня содержания цАМФ сопровождается временным повышением содержания АТФ на фоне выпадения волос [22]. У пациентов с АГА отмечено снижение уровня АТФ в луковицах волос, эпилированных с теменной зоны [23]. Таким образом, определение АТФ в луковицах волос, возможно, могло бы быть использовано, как для оценки тяжести АГА, так и для прогнозирования эффективности терапии АГА.
Эффективность терапии АГА зависит от многих факторов, в том числе от активности фермента СТ, причем рост волос прямо пропорционален его активности [9]. Предполагается, что эта изменчивость является результатом генетических и экологических факторов, способствующих переменной активности ферментов в фолликулах, что затрудняет достижение универсального подхода. Препараты, повышающие концентрацию СТ, такие как третиноин, усиливают эффект миноксидила при местном применении, в то время как средства, снижающие концентрацию СТ, такие как аспирин, снижают эффективность миноксидила. Только у 40% пациентов наблюдается косметически значимое улучшение, и, таким образом, определение количества фермента СТ для исключения нечувствительных к терапии пациентов может иметь клиническую значимость [13]. Таким образом, определение концентрации СТ в луковицах волос, возможно, могло бы быть использовано, для прогнозирования эффективности терапии АГА.
Использование различных показателей для оценки качества лечения пациентов с андрогенетической алопецией миноксидилом отражено в единичных сообщениях.
В исследовании De Villez и др. было продемонстрировано, что наибольшая эффективность при лечении миноксидилом отмечается у пациентов с небольшой продолжительностью АГА (длительность до 10 лет), в случаях формирования ограниченных зон поредения (до 10 см в диаметре), сохранного роста миниатюризированных волос длиной 1 см и более [14].
В исследовании D. Whiting продемонстрировано отсутствие эффекта от лечения 2% миноксидилом у мужчин с АГА, в гистологических образцах которых выявлялось снижение плотности фолликулярных структур до 2 единиц на мм2. Кроме этого, выявление в биоптатах значительного перифолликулярного воспаления и фиброза также приводило к снижению ответа на миноксидил [24].
Описан способ прогнозирования реакции пациента на лекарственное средство для лечения андроген-индуцированных заболеваний кожи, таких как алопеция, акне и гирсутизм. Вероятный ответ на применение лекарственного средства, а именно антиандрогенов и ингибиторов 5-альфа-редуктазы может быть определен путем создания генетического профиля пациента и сравнения его со стандартизированными значениями, каждое из которых представляет либо высокий, либо низкий ожидаемый эффект от применения антиандрогенных препаратов. [25].
Известен способ прогнозирования лечения миноксидилом пациентов с АГА, включающий локальное измерение кровотока на коже головы до и после нанесения препарата 5% миноксидила, заключающийся в том, что при изменении кровотока ниже порогового значения результат идентифицируется как маловероятный ответ на препарат 5% миноксидила, если изменение кровотока является положительным, пациенту рекомендован препарат миноксидила [27].
Задачей предлагаемого изобретения является разработка критериев прогноза эффективности терапии миноксидилом с использованием совокупности анамнестических, клинических и метаболических маркеров.
Одним из возможных подходов к прогнозированию различных исходов терапии АГА может являться математический подход, осуществляемый с использованием многофакторного (множественного, или многомерного) дискриминантного анализа (МДА).
Сущность МДА заключается в поиске новых признаков, называемых дискриминантными функциями (ДФ), на основе использования совокупности исходных показателей. При этом полученные новые признаки (переменные) обладают свойством максимально хорошо (с высокой точностью) разделять друг от друга группы пациентов с разными диагнозами или, например, с разными исходами терапии, по отношению к которым решается задача дискриминации. Число ДФ при этом равно числу выборок. Каждой группе пациентов соответствует своя ДФ, имеющая следующий общий вид:
Y(1)=a11X1+a12X2+…+a1mXm+C1
Y(2)=a21X1+a22X2+…+a2mXm+C2,
где Y(1) и Y(2) - новые переменные, называемые дискриминантными функциями;
a11, a12, …, a1m - это коэффициенты 1-ой ДФ на каждый из признаков (1, 2, …, m);
a21, а22, …, a2m - это коэффициенты 2-ой ДФ на каждый из признаков (1, 2, …, m).
При этом отнесение пациента к той или иной группе выполняется по максимальному значению ДФ после расчета значений ДФ для каждой группы по набору переменных (X1, Х2, …, X12). Набор ДФ позволяет отнести любого пациента по значению его исходных показателей к той или иной группе пациентов [28].
В дерматологии методология дискриминантного анализа применялась, в частности, для дифференциации клинико-иммунологических особенностей аллергических заболеваний кожи [29], а также в сифилидологии [30, 31].
Для прогнозирования эффективности терапии АГА методология дискриминантного анализа до настоящего времени не использовалась.
В связи с этим задачей настоящего изобретения явилась разработка способа прогнозирования эффективности терапии АГА на основе совокупности анамнестических, клинических и метаболических маркеров, доступных практическому здравоохранению, с использованием математического подхода, основанного на применении многофакторного дискриминантного анализа, который ранее для этой цели не использовался.
Известен способ прогнозирования ответа на лечение миноксидилом у пациентов с АГА на основе колориметрического анализа активности СТ в луковицах эпилированных волос. В частности, активность SULT1A1 может быть использована в качестве индикатора реакции на миноксидил. Для обеспечения более персонализированной терапии авторы предлагают проведение генетического теста на аллели гена SULT1A [32].
Недостатком данного способа является то, что авторы для прогнозирования эффективности терапии используют только один фактор, влияющий на эффективность терапии, а именно колориметрический анализ активности СТ в луковицах эпилированных волос, в то время как данный способ не учитывает другие факторы, как клинические, так и метаболические, не использует математический анализ комплекса полученных результатов с использованием современных статистических методов многомерного анализа.
В ретроспективном исследовании A. Goren 2014 и соавт. оценивалась активность ферментов СТ SULT1A1 в волосяном фолликуле для прогнозирования ответа на миноксидил у пациентов с андрогенетической алопецией. Авторы продемонстрировали, что тест для определения активности СТ может использоваться как предикторный с чувствительностью 95% и специфичностью 73% [26].
Недостатком данного способа является то, что авторы для прогнозирования эффективности терапии используют только единичный фактор, влияющий на эффективность терапии, а именно чувствительность пациента к миноксидилу на основании определения активности ферментов СТ SULT1A1 в волосяном фолликуле, в то время как данный способ не учитывает влияние совокупности признаков (анамнестические, клинические, биохимические/метаболические признаки) на основе использования современных статистических методов многомерного анализа.
Данные способы являются наиболее близкими к заявленному и выбраны в качестве прототипов.
Отличие предлагаемого способа от прототипов заключается в том, что в предлагаемом изобретении для персонализированной оценки прогноза эффективности лечения АГА у каждого конкретного пациента определяют не только комплекс общепринятых показателей (пол, возраст, стадия заболевания, данные трихоскопии), но проводят ряд дополнительных информативных лабораторных тестов (концентрация АТФ, активность СТ в луковице волоса), а также определяют ряд анамнестических и клинических показателей (длительность заболевания, плотность волос на см2, средний диаметр волоса), которые до настоящего времени для этой цели не применялись. Кроме того, в предлагаемом изобретении используется математический инструмент - многофакторный/многомерный дискриминантный анализ, с помощью которого рассчитываются значения двух линейных дискриминантных функций ДФ1 и ДФ2 для показателей двух групп пациентов (1-я - пациенты, у которых эффект лечения АГА миноксидилом отсутствует, 2-я - пациенты, у которых терапия АГА миноксидилом оказывается эффективной), и при значении ДФ1 больше ДФ2 пациенту прогнозируют отсутствие эффекта терапии миноксидилом, а при ДФ2 больше ДФ1 прогнозируют эффективность терапии и целесообразность проведения терапии миноксидилом.
Применение способа расширяет возможности для персонализации прогнозирования эффективности терапии АГА благодаря применению дополнительных высокоинформативных тестов (методология определения АТФ и СТ в луковице волоса), а также использованию технологии обработки результатов исследований методом многомерного дискриминантного анализа, позволяющим объединить разноплановые показатели и перевести их в интегральный показатель дискриминантной функции.
Способ позволяет повысить эффективность терапии АГА у пациентов с различными стадиями АГА, улучшить качество жизни пациентов при одновременном снижении потенциальных рисков и экономических затрат на лечение (если необходимость в нем отсутствует), внедрить в практику эффективные протоколы персонифицированного подхода к терапии АГА.
Основания для создания изобретения
Основанием для создания изобретения явились результаты, полученные в ходе выполнения НИР «Разработка и внедрение в московское здравоохранение инновационных методов и подходов к профилактике, диагностике и терапии заболеваний кожи и подкожно-жировой клетчатки», №государственной регистрации темы: АААА-А17-117122290023-8, фрагмент «Персонализированная терапия пациентов с андрогенетической алопецией в зависимости от результатов морфометрических и биохимических исследований волос».
Целью исследования явился отбор наиболее информативных показателей для прогнозирования эффективности терапии АГА миноксидилом, а также изучение возможности использования для целей персонализации терапии многофакторного дискриминантного анализа.
Объектом исследования явились 55 пациентов с АГА (13 мужчин, 42 женщины) в возрасте от 19 до 45 лет.
Для проведения исследований методом многофакторного (множественного, многомерного) дискриминантного анализа (МДА) пациенты были разделены на 2 группы:
1-я - пациенты, у которых эффект лечения АГА миноксидилом отсутствует (15 чел., 27%);
2-я - пациенты, у которых терапия АГА миноксидилом оказывается эффективной (40 чел., 73%).
При выполнении НИР применялись методы:
- клинического обследования пациентов;
- лабораторной диагностики (определение содержания АТФ и активности СТ в луковицах эпилированных волос);
- инструментального исследования (фототрихограмма с подсчетом плотности волос на см2, % волос в стадии телогена, % веллусных волос, среднего диаметра волос).
Полученные данные обработаны с использованием пакета статистических программ «Statistica 10.0». Различия между группами и подгруппами считались статистически значимыми при значении р<0,05, для оценки достоверности различий использовался критерий Манна-Уитни.
Для осуществления прогнозирования эффективности терапии АГА миноксидилом с использованием совокупности наиболее информативных показателей и расчетом дискриминантных функций был проведен многофакторный дискриминантный анализ. Расчет показателей МДА проводился с использованием пакета программ «Statistica 10.0». Проверка точности отнесения пациентов к той или иной группе с помощью МДА (чувствительность решающих правил) проводилась с помощью линейных классификационных функций; проверка различимости групп - путем подсчета Биквадрата расстояния Махалонобиса. Оценка достоверности разделения пациентов на 2 группы и информативности признаков оценивалась по F-критерию Фишера (критический уровень значимости при проверке статистических гипотез р=0,05).
В результате проведения исследований было установлено, что из всех применявшихся показателей (длительность заболевания, концентрация АТФ и активность СТ в луковице волоса, плотность волос на см2, % волос в стадии телогена, % веллусных волос, средний диаметр волоса) наиболее информативными (р<0,05) для разделения пациентов с АГА на 2 подгруппы (с эффективностью лечения миноксидилом и с отсутствием эффекта от лечения) явились следующие 5 показателей: длительность заболевания, концентрация АТФ и активность СТ в луковице волоса, плотность волос и средний диаметр волоса.
Результаты сравнительного изучения информативности показателей в зависимости от эффективности терапии миноксидилом
Результаты применения МДА
В ходе выполнения МДА для двух групп пациентов (1-я - пациенты, у которых эффект лечения АГА миноксидилом отсутствует, 2-я - пациенты, у которых терапия АГА миноксидилом оказывается эффективной), были определены коэффициенты линейных классификационных функций для каждого из 5-ти использованных показателей (таблица 2)
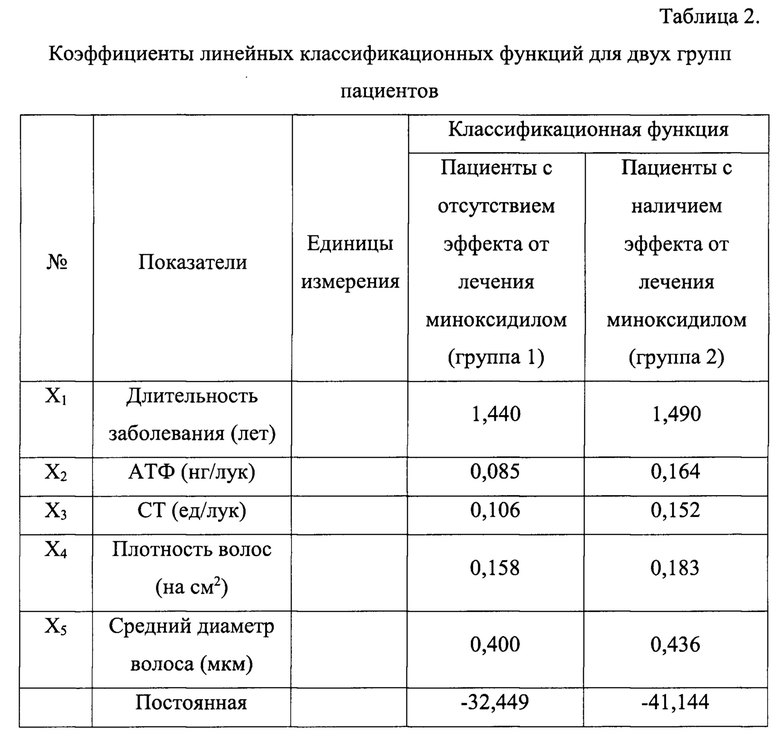
При этом были получены следующие значения дискриминантных функций:
ДФ1 = 1,44 х длительность заболевания + 0,085 х АТФ + 0,106 х СТ + 0,158 х плотность волос + 0,4 х средний диаметр волоса - 32,449
ДФ2 = 1,49 х длительность заболевания + 0,164 х АТФ + 0,152 х СТ + 0,183 х плотность волос + 0,436 х средний диаметр волоса - 41,144
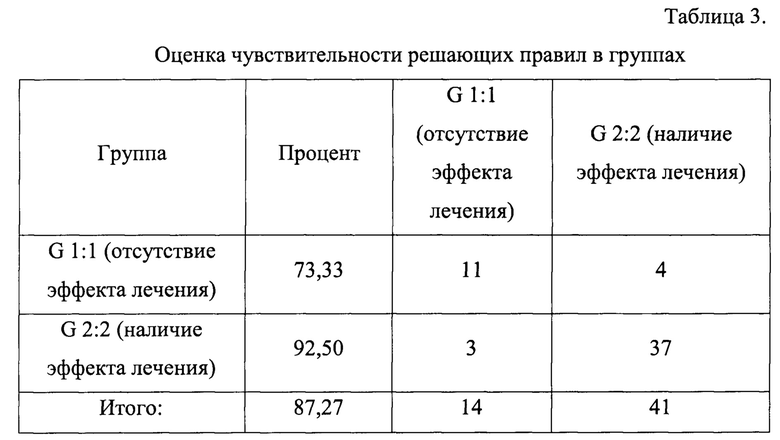
Оценка чувствительности решающих правил в двух группах пациентов показала, что при проверке линейными классифицирующими функциями к 1 группе было неверно отнесено 4 объекта (пациента), ко 2 группе - 3 объекта (пациента). При этом правильное отнесение к группе 2 (пациенты, у которых лечение оказалось эффективным) классифицировалось в 92,50% случаев, а правильное отнесение к группе 1 (пациенты, у которых лечение оказалось неэффективным) - в 73,33% случаев. Точность дифференциации пациентов на предмет наличия/отсутствия эффекта от лечения в целом составила 87,27% (таблица 3).
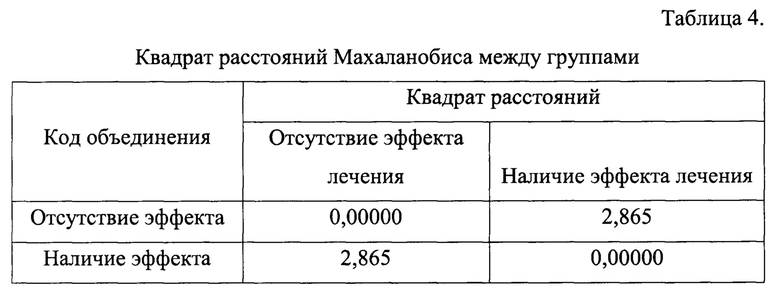
Расчет квадрата расстояний Махаланобиса показал наличие существенных различий между группами (расстояние Махалонобиса = 2,865, таблица 4).
Оценка различий между группами по F-критерию показала высокую достоверность (F-критерий между 1 и 2 группами составил 5,779; р<0,0003). Оценка информативности каждого из признаков в двух группах показала, что наиболее информативным признаком для диагностики эффекта/отсутствие эффекта лечения является показатель количества волос (на см2) (F=5,942; р=0,018). Следующими по значимости для диагностики признаками являются АТФ и СТ (таблица 5).
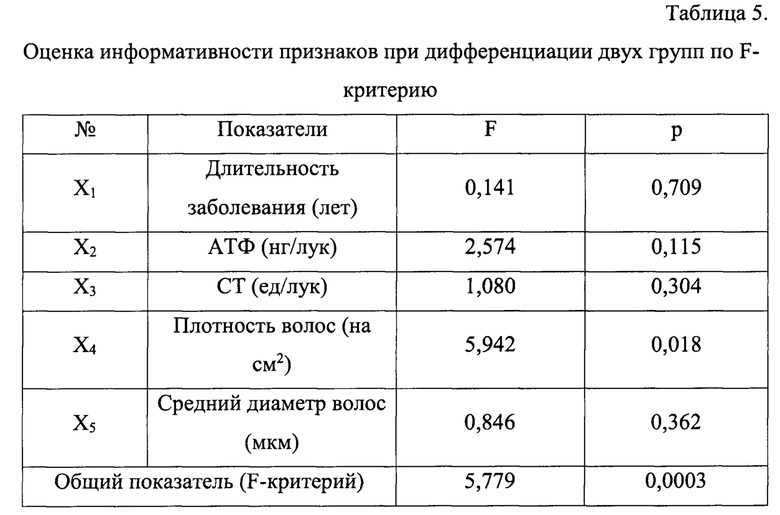
Таким образом, для определения принадлежности пациента к одной из групп по отсутствию/наличию эффекта лечения на основании проведения МДА рассчитываются значения двух ДФ по индивидуальным данным для 5-ти показателей. При этом пациент относится к той группе, для которой получена наибольшая величина ДФ. При значении ДФ1>ДФ2 прогнозируют отсутствие эффекта от лечения миноксидилом, а при значении ДФ2>ДФ1 - наличие эффекта лечения этим препаратом.
Значения дискриминантных функций и дискриминантных коэффициентов, полученные на основании обработки результатов исследования пациентов с АГА методом многомерного дискриминантного анализа, могут рассматриваться в качестве математической модели прогнозирования персонализации эффективности терапии АГА.
Раскрытие настоящего изобретения
Предлагаемый Способ осуществляется следующим образом.
Пациент с АГА проходит клинико-анамнестическое и лабораторное обследование.
При этом определяются значения следующих показателей:
1. Длительность заболевания (лет) (анамнестические данные)
2. Содержание АТФ в луковицах эпилированных волос. Эпилированные луковицы получают вручную, извлекая волосы из зоны алопеции с помощью пинцета. С помощью микроскопии отбирается 5 луковиц волос в стадии анагена. Содержание АТФ измеряется с использованием метода хемилюминесценции. Для проведения реакции луковицы эпилированных волос инкубируют в буферном растворе, что приводит к экстракции АТФ. Оценка содержания АТФ проводится на хемилюминометре с использованием реагента на основе смеси люциферин-люциферазы (Sigma). Расчет проводится по калибровочной зависимости, полученной для стандартного раствора АТФ (Sigma).
3. Содержание СТ в луковицах эпилированных волос. Эпилированные луковицы получают вручную, извлекая волосы из зоны алопеции с помощью пинцета. С помощью микроскопии отбирается 5 луковиц волос в стадии анагена. Содержание СТ оценивается при помощи метода спектрофотометрии. Для проведения реакции луковицы волос инкубируют в буферном растворе. Определение активности сульфотрансфераз в луковицах проводят с помощью пара-нитрофенилсульфата. Сульфотрансферазная активность в луковицах волос оценивается количеству образовавшегося паранитрофенола, который поглощает при длине волны 405-414 нм. Измеряемый показатель - оптическое поглощение буферного раствора при 414 нм.
4. Плотность волос (на 1 см2). Определяется путем анализа изображений, полученных с помощью цифрового видеодерматоскопа Fotofinder с использованием специализированной программы Trchoscience Pro.
5. Средний диаметр волоса (мкм). Определяется путем анализа изображений, полученных с помощью цифрового видеодерматоскопа Fotofinder с использованием специализированной программы Trchoscience Pro.
После получения результатов изучения всех перечисленных параметров у данного конкретного пациента вычисляют значения дискриминантных функций по формулам, полученным в ходе проведения многомерного дискриминантного анализа:
ДФ1 = 1,44 х длительность заболевания + 0,085 х АТФ + 0,106 х СТ + 0,158 х плотность волос + 0,4 х средний диаметр волоса - 32,449
ДФ2 = 1,49 х длительность заболевания + 0,16 4х АТФ + 0,152 х СТ + 0,183 х плотность волос + 0,436 х средний диаметр волоса - 41,144
Рассчитываются значения двух ДФ по индивидуальным данным результатов исследований пациента, и при значении ДФ1>ДФ2 у пациента прогнозируют отсутствие эффекта терапии миноксидилом, а при значении ДФ2>ДФ1 прогнозируют эффективность терапии миноксидилом.
Примеры осуществления Способа
Пример 1.
Пациентка №17, женщина, 30 лет. Длительность потери волос 6 лет. При первичном приеме на основании наружного осмотра и анализа фототрихограммы диагностирована I стадия АГА по классификации Людвига. По результатам фототрихограммы в теменной зоне определены плотность волос - 224,0 на 1 см2 и средний диаметр волос - 61 мкм. Определены биохимические показатели волос: содержание АТФ - 37,3 нг/лук, активность сульфотрансферазы - 57,5 ед/лук.
Полученные данные использованы для вычисления значения дискриминантных функций по формулам, полученным в ходе проведения многомерного дискриминантного анализа, а именно:
ДФ1 = 1,44 х 6 + 0,085 х 37,3 + 0,106 х 57,5 + 0,158 х 224 + 0,4 х 61 - 32,449 = 45,25;
ДФ2 = 1,49 х 6 + 0,16 4х 37,3 + 0,152 х 57,5 + 0,183 х 224 + 0,436 х 61 - 41,144 = 50,24.
Полученное значение ДФ2>ДФ1 прогнозирует эффективность терапии миноксидилом.
Пациентке была проведена терапия миноксидилом 5% наружно, путем нанесения 1 мл раствора на область алопеции 2 раза в день. На 2-м визите (через 3 месяца терапии) пациентка продемонстрировала значимое улучшение: наблюдалось увеличение плотности волос до 264 на 1 см2, увеличение среднего диаметра волос до 68 мкм. По обзорным фотографиям отмечалось клиническое улучшение - уменьшение степени поредения волос.
Таким образом, на основании определения обозначенных выше 5-ти показателей до лечения и применения метода многомерного дискриминационного анализа по сравнению значений двух дискриминантных функций была спрогнозирована эффективность терапии миноксидилом, и данная терапия действительно оказала положительный эффект при лечении пациентки.
Пример 2.
Пациент №40, мужчина, 36 лет. Длительность потери волос 5 лет. При первичном приеме на основе наружного осмотра и анализа фототрихограммы диагностирована 2 стадия АГА по классификации Норвуда-Гамильтона. По результатам фототрихограммы в теменной зоне определены плотность волос - 206,0 на см2 и средний диаметр волос - 64 мкм. Определены биохимические показатели волос: содержание АТФ 20,5 нг/лук, активность сульфотрансферазы - 41 ед/лук.
Полученные данные использованы для вычисления значения дискриминантных функций по формулам, полученным в ходе проведения многомерного дискриминантного анализа, а именно:
ДФ1 = 1,44 х 5 + 0,085 х 20,5 + 0,106 х 41 + 0,158 х 206 + 0,4 х 64 - 32,449 = 39;
ДФ2 = 1,49 х 6 + 0,16 4х 37,3 + 0,152 х 57,5 + 0,183 х 224 + 0,436 х 61 - 41,144 = 41,5.
Полученное значение ДФ2>ДФ1 прогнозировало эффективность терапии миноксидилом.
Пациенту была проведена терапия миноксидилом 5% наружно, путем нанесения 1 мл раствора на область алопеции 2 раза в день. На 2-м визите (через 3 месяца терапии) пациент продемонстрировал значимое улучшение: наблюдалось увеличение плотности волос до 225 на 1 см2, увеличение среднего диаметра волос до 72 мкм. По обзорным фотографиям отмечалось клиническое улучшение - увеличение густоты волос и уменьшение выраженности поредения волос.
Таким образом, у данного пациента на основании определения обозначенных выше 5-ти показателей до лечения и применения метода многомерного дискриминационного анализа по сравнению значений двух дискриминантных функций была спрогнозирована эффективность терапии миноксидилом, и данная терапия действительно оказала положительный эффект при его лечении.
Пример 3.
Пациентка №48, женщина, 34 года. Длительность потери волос 5 лет. При первичном приеме на основе наружного осмотра и анализа фототрихограммы диагностирована II стадия АГА по классификации Людвига. По результатам фототрихограммы в теменной зоне определены плотность волос - 202,0 на см2 и средний диаметр волос - 59 мкм. Определены биохимические показатели волос: содержание АТФ - 3,3 нг/лук, активность сульфотрансферазы - 4,3 ед/лук.
Полученные данные использованы для вычисления значения дискриминантных функций по формулам, полученным в ходе проведения многомерного дискриминантного анализа, а именно:
ДФ1 = 1,44 х 5 + 0,085 х 3,3 + 0,106 х 4,3 + 0,158 х 202 + 0,4 х 59 - 32,449 = 31;
ДФ2 = 1,49 х 3 + 0,16 4х 3,3 + 0,152 х 4,3 + 0,183 х 202 + 0,436 х 59 - 41,144 = 30,19.
Полученное значение ДФ1>ДФ2 у пациентки прогнозировало отсутствие эффекта терапии миноксидилом.
Пациентке была проведена терапия миноксидилом 5% наружно, путем нанесения 1 мл раствора на область алопеции 2 раза в день. На 2-м визите (через 3 месяца терапии) у пациентки было отмечено отсутствие эффекта терапии: плотность волос не увеличилась и осталась равной 202 на 1 см2, диаметр волос снизился и составил 55 мкм. По обзорным фотографиям отмечалось сохранение поредения волос II ст. АГА по классификации Людвига.
Таким образом, у данной пациентки на основании определения обозначенных выше 5-ти показателей до лечения и применения метода многомерного дискриминационного анализа по сравнению значений двух дискриминантных функций было спрогнозировано отсутствие эффективности терапии миноксидилом, и данная терапия действительно оказалась неэффективной.
Пример 4.
Пациент №47, мужчина, 32 года. Длительность потери волос 12 лет. При первичном приеме на основе наружного осмотра и анализа фототрихограммы диагностирована 3 стадия АГА по классификации Норвуда-Гамильтона. По результатам фототрихограммы в теменной зоне определены плотность волос - 165,0 на 1 см2 и средний диаметр волос 48 мкм. Определены биохимические показатели волос: содержание АТФ - 4 нг/лук, активность сульфотрансферазы - 12,8 ед/лук.
Полученные данные были использованы для вычисления значения дискриминантных функций по формулам, полученным в ходе проведения многомерного дискриминантного анализа, а именно:
ДФ1 = 1,44 х 12 + 0,085 х 4 + 0,106 х 12,8 + 0,158 х 165 + 0,4 х 48 - 32,449 = 31,8;
ДФ2 = 1,49 х 12 + 0,164х 4 + 0,152 х 12,8 + 0,183 х 165 + 0,436 х 48 - 41,144 = 30,46.
Полученное значение ДФ1>ДФ2 у пациента прогнозировало отсутствие эффекта терапии миноксидилом.
Пациенту была проведена терапия миноксидилом 5% наружно, путем нанесения 1 мл раствора на область алопеции 2 раза в день. На 2-м визите (через 3 месяца терапии) пациент продемонстрировал отсутствие улучшений: наблюдалось снижение плотности волос до 160 на 1 см2, диаметр волос практически не изменился и составил 47 мкм. По обзорным фотографиям отмечалось ухудшение состояния волос, снижение их густоты.
Таким образом, у данного пациента на основании определения обозначенных выше 5-ти показателей до лечения и применения метода многомерного дискриминационного анализа по сравнению значений двух дискриминантных функций было спрогнозировано отсутствие эффективности терапии миноксидилом, и данная терапия действительно оказалась неэффективной.
Источники информации
1. Blumeyer A, Tosti A, Messenger A, et al. Evidence-based (S3) guideline for the treatment of androgenetic alopecia in women and in men. J Dtsch Dermatol Ges. 2011 Oct;9 Suppl 6:S1-S57.
2. Alsantali A, Shapiro J. Androgens and hair loss. Curr Opin Endocrinol Diabetes Obes. 2009 Jun;16(3):246-253.
3. Shapiro J. Clinical practice: Hair loss in women. N Engl J Med. 2007;357(16): 1620-1630.
4. Rhodes T, Girman CJ, Savin RC, et al. Prevalence of male pattern hair loss in 18-49 year old men. Dermatol Surg. 1998;24:1330-1332.
5. Cash TF. The psychological effects of androgenetic alopecia in men. J Am Acad Dermatol. 1992;26:926-931.
6. Girman C, Rhodes T, Lilly F, et al. Effects of self-perceived hair loss in a community sample of men. Dermatology. 1998;197:223-229.
7. Blumeyer A, Tosti A, Messenger A, et al. Evidence-based (S3) guideline for the treatment of androgenetic alopecia in women and in men. J Dtsch Dermatol Ges. 2011 Oct;9 Suppl 6:S1-S57.
8. Kanti V, Messenger A et al. Evidence based (s3) guidelines for the treatment of androgenetic alopecia in women and in men, 2017.
9. Roberts J, Desai N, McCoy J, et al. Sulfotransferase activity in plucked hair follicles predicts response to topical minoxidil in the treatment of female androgenetic alopecia. Dermatol Ther. 2014;27:252-254.
10. Jahangir A, Terzic A. KATP channel therapeutics at the bedside. J Mol Cell Cardiol. 2005;39:99-112.
11. Marubayashi A, Nakaya Y, Fukui K, et al. Minoxidil-induced hair growth is mediated by adenosine in cultured dermal papilla cells: possible involvement of sulfonylurea receptor 2B as a target of minoxidil. J Invest Dermatol. 2001;117:1594-1600.
12. York K, Meah N, Bhoyrul B, Sinclair R. A review of the treatment of male pattern hair loss. Expert Opin Pharmacother. 2020 Apr;21(5):603-612. doi: 10.1080/14656566.2020.1721463. Epub 2020 Feb 17.
13. Goren A, Shapiro J, Roberts J, et al. Clinical utility and validity of minoxidil response testing in androgenetic alopecia. Dermatol Ther. 2015;28:13-16.
14. De Villez RL. Topical minoxidil therapy in hereditary androgenetic alopecia. Arch Dermatol. 1985;121:197-202.
15. Olsen EA, Weiner MS. Topical minoxidil in male pattern baldness: effects of discontinuation of treatment. J Am Acad Dermatol. 1987;17:97-101.
16. Adachi K., Takayasu S., Takashima I., Takashima I, Kano M., Kondo S. Human hair follicles: metabolism and control mechanisms. J. Soc Cosmet Chem. 1970, V. 21, p.901-924.
17. Rogers G.E. Hair follicle differentiation and regulation. Int. J. Dev. Biol. 2004, V. 48, №2-3, p.163-170.
18. Shorter K., Farjo N., Picksley S.M., Randall V.A. Human hair follicles contain two forms of ATP-sensitive potassium channels, only one of which is sensitive to minoxidil. FASEB. J. 2008, V. 22, №6, p.1725-1736.
19. Greig A.V.N., Linge C., Burnstock G. Purinergic receptors are part of a signalling system for proliferation and differentiation in distinct cell lineages in human anagen hair follicles. Purinergic Signalling. 2008, V. 4, №4, p.331-338.
20. Adachi K., Takayasu S., Takashima I., Takashima I, Kano M., Kondo S. Human hair follicles: metabolism and control mechanisms. J. Soc.Cosmet.Chem. 1970, V. 21, p.901-924.
21. Cipriani C., Moretti G., Rampini E., Divano C. Adenyl-cyclase activity in rat-hair-cycle. Arch. Derm. Res. 1976, V. 256, №3, p.319-325.
22. Gazzani G., Roncoroni S., Corsi M., Falchi M., Ferrero M.E. Increased cAMP levels in human hair follicles due to local treatment with trichoriboside. Int. J. Tissue React. 1994. Vol.16, №2, p.73-77.
23. Михальчик E.B., Смолина H.B., Гаджигороева А.Г., и др. Комплекс показателей для оценки состояния волоса человека / Методические рекомендации. 2014 г.
24. Whiting DA. Diagnostic and predictive value of horizontal sections of scalp biopsy specimens in male pattern androgenetic alopecia. J Am Acad Dermatol. 1993 May;28(5 Pt 1):755-63. doi: 10.1016/0190-9622(93)70106-4. Erratum in: J Am Acad Dermatol 1993 Oct;29(4):554. PMID: 8496421.
25. Патент US 20120232045 A1. Andy Ofer GOREN, Sharon Keene. Methods and systems for prognosis of a patient's response to treatment of androgenetic skin disorders.
26. Goren A, Castano JA, McCoy J, Bermudez F, Lotti T. Novel enzymatic assay predicts minoxidil response in the treatment of androgenetic alopecia. Dermatol Ther. 2014 May-Jun;27(3): 171-3. doi: 10.1111/dth. 12111. Epub 2013 Nov 27. PMID: 24283387.
27. Патент WO 2017007921 A2. Andy Ofer Goren, John Mccoy. Systems and methods for treatment of androgenetic alopecia with minoxidil based on noninvasive predictive response testing.
28. Михалевич И.М. Основы прикладной статистики: методические рекомендации / И.М. Михалевич, Н.Ю. Рожкова ИГИУВ. Иркутск, 2006. - 90 с.; Кузнецов Е.А., Негашева М.А., Анохин В.Н., Волов Н.А., Ли Е.Д., Бычкова О.П. Математическая модель диагностики ишемической болезни сердца методом многофакторного дискриминантного анализа. Российский кардиологический журнал. М., 2001, №5, стр. 60-65.
29. Бибарсова Г.И. Клинико-иммунологические особенности аллергических заболеваний кожи. Автореф. дисс. канд. мед. наук.; М., 2017.
30. Е.В. Соколовский Серологическая резистентность после лечения сифилиса (причины и факторы развития, профилактика и лечение) Автореф. дисс. докт. мед. наук.; СПб., 1995.
31. Фриго Н.В. Современные критерии дифференциальной диагностики раннего скрытого сифилиса и ложноположительных результатов стандартных серологических реакций на сифилис Автореф. дисс. докт. мед. наук.; М., 2001.
32. Патент US 20140220609 A1. Andy Ofer GOREN, John McCoy. Systems and methods for predicting response to minoxidil for the treatment of androgenetic alopecia.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ АНДРОГЕНЕТИЧЕСКОЙ АЛОПЕЦИИ | 2020 |
|
RU2751214C1 |
| СПОСОБ ЛЕЧЕНИЯ АЛОПЕЦИЙ С СОПУТСТВУЮЩИМИ ПСИХОСОМАТИЧЕСКИМИ РАССТРОЙСТВАМИ | 2020 |
|
RU2756002C1 |
| МЕТОД ЛЕЧЕНИЯ АНДРОГЕННОЙ АЛОПЕЦИИ: МЕСТНОЕ НАНЕСЕНИЕ НА ОЧАГИ ОБЛЫСЕНИЯ ГЕПАРИНА (В СОСТАВЕ ПРЕПАРАТОВ ДЛЯ МЕСТНОГО ЛЕЧЕНИЯ) | 2011 |
|
RU2517087C2 |
| Способ лечения нерубцовой алопеции | 2023 |
|
RU2823154C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ АНДРОГЕННОЙ АЛОПЕЦИИ У МУЖЧИН | 2018 |
|
RU2713374C1 |
| Средство для лечения алопеции на основе четвертичного аммониевого соединения, содержащего фрагмент пиридоксина | 2023 |
|
RU2813104C1 |
| СПОСОБ ДИАГНОСТИКИ НЕЙРОСИФИЛИСА | 2018 |
|
RU2699057C1 |
| Способ комплексной коррекции нерубцовых алопеций в эксперименте | 2023 |
|
RU2821779C1 |
| ДЕРМАТОЛОГИЧЕСКОЕ И/ИЛИ КОСМЕТОЛОГИЧЕСКОЕ СРЕДСТВО, СТИМУЛИРУЮЩЕЕ РОСТ ВОЛОС, СРЕДСТВО, ВЛИЯЮЩЕЕ НА РАЗМНОЖЕНИЕ КЛЕТОК ВОЛОСЯНЫХ ФОЛЛИКУЛОВ | 2007 |
|
RU2357722C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕРУБЦОВОЙ АЛОПЕЦИИ | 2018 |
|
RU2681854C1 |
Изобретение относится к области медицины, а именно дерматовенерологии и косметологии. Перед назначением лечения определяют анамнестические данные: длительность заболевания, в годах, плотность волос на 1 см2, средний диаметр волос и биохимические показатели: содержание АТФ и активность сульфотрансферазы (СТ) в луковицах волос, при этом эффективность терапии миноксидилом прогнозируют по значениям дискриминантных функций: ДФ1 и ДФ2. При значении ДФ1 больше ДФ2 пациенту прогнозируют отсутствие эффекта терапии миноксидилом. При значении ДФ2 больше ДФ1 прогнозируют эффективность терапии и целесообразность проведения терапии миноксидилом. Способ позволяет повысить эффективность терапии андрогенетической алопеции (АГА) у пациентов с различными стадиями АГА, улучшить качество жизни пациентов при одновременном снижении потенциальных рисков и экономических затрат на лечение, если необходимость в нем отсутствует, внедрить в практику эффективные протоколы персонифицированного подхода к терапии АГА. 5 табл., 4 пр.
Способ прогнозирования эффективности лечения андрогенетической алопеции миноксидилом путем исследования анамнестических, клинических и метаболических показателей, отличающийся тем, что перед назначением лечения миноксидилом у пациента дополнительно определяют длительность заболевания, содержание АТФ и активность сульфотрансферазы (СТ) в луковицах волос, плотность волос на 1 см2, средний диаметр волос и прогнозируют эффективность терапии миноксидилом по следующим значениям дискриминантных функций многомерного дискриминантного анализа:
ДФ1 = 1,44 х длительность заболевания + 0,085 х АТФ + 0,106 х СТ + 0,158 х плотность волос + 0,4 х средний диаметр волос - 32,449
ДФ2 = 1,49 х длительность заболевания + 0,16 4х АТФ + 0,152 х СТ + 0,183 х плотность волос + 0,436 х средний диаметр волос - 41,144,
При значении ДФ1 больше ДФ2 пациенту прогнозируют отсутствие эффекта терапии миноксидилом, а при значении ДФ2 больше ДФ1 прогнозируют эффективность терапии и целесообразность проведения терапии миноксидилом.
| СПОСОБ ЛЕЧЕНИЯ АНДРОГЕНЕТИЧЕСКОЙ АЛОПЕЦИИ | 2018 |
|
RU2682763C1 |
| СПОСОБ ЛЕЧЕНИЯ АЛОПЕЦИЙ С СОПУТСТВУЮЩИМИ ПСИХОСОМАТИЧЕСКИМИ РАССТРОЙСТВАМИ | 2020 |
|
RU2756002C1 |
| СПОСОБ ЛЕЧЕНИЯ ОБЛЫСЕНИЯ | 2010 |
|
RU2448682C2 |
| WO 2013049258 A1, 04.04.2013 | |||
| WO 2017007921 A2, 12.01.2017 | |||
| US 2014220609 A1, 07.08.2014 | |||
| CN 104435884 A, 25.03.2015 | |||
| Гаджигороева А | |||
| Г., Нечаева Н | |||
| П | |||
| Применение трихограммы для оценки эффективности лечения выпадения волос / II Всероссийский конгресс | |||
Авторы
Даты
2022-06-21—Публикация
2021-12-29—Подача