Область техники
Изобретение относится к области радиационного воздействия на живые белковые молекулы и может быть использовано для получения молекул с улучшенными свойствами.
Известен способ, [1], Патент РФ 2 512 679 С1, 10.04.2014 «Способ досмотра и досмотровый комплекс», в котором через образец пропускается рентгеновское излучение, которое детектируется и, по результатам измерений, восстанавливается внутренняя картина образца.
Сущность изобретения заключается в том, что выполняют двустороннее сканирование досматриваемого человека тонкими пучками рентгеновского излучения из двух, размещенных по разные стороны досматриваемого человека, источников рентгеновского излучения путем вертикальной развертки за счет их линейного вертикального перемещения посредством снабженных электроприводом кареток и горизонтальной развертки посредством коллиматоров и регистрацию обратно рассеянного рентгеновского излучения посредством установленного на каждой из кареток приемного детектора для формирования растровых изображений досматриваемого человека за один цикл сканирования, при этом линейное вертикальное перемещение обоих источников рентгеновского излучения осуществляют одновременно и асинхронно с задержкой начала сканирования одного относительно другого, а рассеянное рентгеновское излучение, прошедшее от противоположного источника рентгеновского излучения, поглощают посредством защитных экранов на каждом из приемных детекторов.
Вместо рентгеновского в этом методе может быть использовано гамма излучение, [2], Патент РФ, 2 742 632 С1, 09.02.2021, «Гамма - дефектоскоп затворного типа».
Технический результат, получаемый при реализации этого метода анализа внутренней структуры образца, заключается в его устойчивой радиационной безопасности в условиях хранения, эксплуатации и транспортирования, в том числе аварийного (с вероятностью динамического смещения центра тяжести), модификации системы блокирования затворного узла в виде сегмента радиационной защиты, скрепленного с поворотной кулисой, для его автоматизированного циклического силового удержания в соответствующем конструктивном пространстве в закрытом состоянии после завершения рабочего цикла, а деблокирование в процессе эксплуатации выполняют исключительно перед выпуском пучка излучения по команде оператора в ручном режиме.
Вместо рентгеновского и гамма излучения могут использоваться электроны или протоны [3], Патент РФ, 2 573178 С1, 20.01.2016 «Способ формирования изображения быстропротекающего изображения с помощью протонного излучения».
Принципиальная схема здесь остается той же - просвечивание тела излучением.
Сущность изобретения заключается в том, что способ включает ввод протонного пучка, по крайней мере, в один магнитооптический канал, изменение ширины протонного пучка на разные величины, которое осуществляют последовательно в одном и том же магнитооптическом канале, для этого либо после прохождения части протонных сгустков через рассеиватель его удаляют или изменяют толщину, а затем пропускают оставшуюся часть протонных сгустков, либо следующие друг за другом протонные сгустки смещают относительно друг друга с помощью магнитных линз и, используя разнотолщинный рассеиватель, смещенные протонные сгустки пропускают через области рассеивателя с разной толщиной, после прохождения рассеивателя с помощью системы согласующих магнитных линз формируют протонный пучок с параметрами, соответствующими параметрам области исследования и последующей магнитооптической системы формирования протонного изображения, и просвечивают область исследования, пропуская поочередно протонные сгустки различной ширины, при использовании нескольких магнитооптических каналов просвечивание области исследования осуществляют под разными углами, после чего прошедший протонный пучок направляют в магнитооптическую систему формирования протонного изображения, состоящую, по крайней мере, из двух различных по апертуре линзовых систем, апертура каждого набора соответствует протонному пучку определенной ширины, оба набора линз системы формирования теневого протонного изображения размещают последовательно в одном магнитооптическом канале.
В способе [4], Патент РФ 2 502 986 С1, 27.12.2013 «Способ нейтронной радиографии», просвечивание образца предложено проводить с помощью нейтронов.
Суть предложения заключается в том, что информацию о структуре и вещественном составе просвечиваемого объекта получают путем обработки данных по ослаблению первичного пучка, по соотношению и количеству нейтронов, рассеянных вперед и назад, а также по спектру гамма-излучения, возникающего в объекте. Технический результат: расширение области применения радиографического контроля внутренней структуры и идентификации вещественного состава просвечиваемых объектов, уменьшение влияния рассеянного излучения и увеличение контраста изображения, упрощение процедуры идентификации.
Немного особняком стоит Полезная модель РФ 195 097 U1 «Устройство для обнаружения взрывчатых, отравляющих и делящихся веществ на морском дне», [5].
Здесь облучение ведут нейтронами, а регистрируется вторичное излучение - гамма кванты, которые испускают, образовавшиеся при поглощении нейтронов, ядра. Этим способом можно обнаруживать взрывчатые, отравляющие и делящиеся вещества на морском дне. Устройство для обнаружения содержит импульсный нейтронный дейтерий-дейтериевый генератор, сцинтилляционные гамма-детекторы и амплитудный анализатор с временным окном для измерения гамма-квантов радиационного захвата нейтронов, сцинтилляционные гамма-детекторы и импульсный нейтронный дейтерий-дейтериевый генератор присоединены к амплитудному анализатору, сцинтилляционные гамма-детекторы размещены во фторсодержащем веществе, окружающем сцинтилляционные гамма-детекторы, амплитудный анализатор имеет временное окно для измерения гамма-квантов изотопа 16N, образующихся при взаимодействии нейтронов деления, испускаемых при облучении нейтронами объекта исследования, содержащего делящееся вещество, с фторсодержащим веществом, причем объем и расположение фторсодержащего вещества, а также объем и расположение сцинтилляционных гамма-детекторов должны быть такими, чтобы произведение скорости наработки изотопа 16N во фторсодержащем веществе нейтронами деления и вероятности регистрации гамма-квантов с энергией 6,13 МэВ, выходящих из фторсодержащего вещества, сцинтилляционными гамма-детекторами было не менее 6,25/Т0, где Т0 - время обнаружения.
Недостатком всех указанных выше способов является то, что неразрушающий контроль относится ко всему телу, как целому, а не к отдельным белковым молекулам, находящимся внутри образца. К тому же в отношении белковых молекул, которые являются живыми, такой контроль вряд ли можно назвать неразрушающим. Как раз излучение повреждает структуру молекул и может полностью парализовать их работу в качестве биологического катализатора.
В качестве прототипа выбран ЯМР способ экспресс регистрации химических сдвигов в белковых молекулах [6], Тарасевич Б.Н. «Первоначальные сведения о методах ЯМР, масс спектрометрии и ИК спектрометрии», МГУ им. М.В. Ломоносова, Химический факультет, кафедра органической химии, 2014 год, который может проводиться in vivo, то есть на живой молекуле непосредственно в процессе ее жизнедеятельности.
Реально это означает, что исследуются химические сдвиги в живых белковых молекулах. Для проведения такого анализа биологический образец помещают в сильное магнитное поле. В этом поле в ядрах, имеющих полуцелый спин, становятся возможны переходы между различными спиновыми состояниями. В результате происходит сдвиг характерной частоты Δf, с характерной величиной Δf/f лежащей в диапазоне Δf/f≈10-6. Сложная белковая молекула, каковой является, например, биологический катализатор, содержит в своем спектре сотни характерных частот, каждая из которых очень точно известна. Чрезвычайно важным здесь является то, что величина сдвига зависит от наличия той или иной химической связи в белковой молекуле, так что, проводя спектроскопию поглощенного в молекуле излучения, можно определить какие химические связи появились вновь, а какие разрушились. И, как было сказано выше, этот анализ можно проводить непосредственно на живой молекуле, в то время как она активно действует. Непосредственно в процессе проведения спектроскопического анализа, можно видеть, как повреждение той или иной химической связи в молекуле влияет на скорость биохимической реакции. Недостатком такого способа исследования влияния энзимов на скорость биохимических реакций, является то обстоятельство, что в данном случае проводится ЯМР анализ молекулы с уже нанесенными ей повреждениями. Настоятельно требуется разработка экспресс анализа влияния разрушения определенных химических связей в белковых молекулах на активирование или ингибирование их действия, то есть на скорость протекания заданной биохимической реакции.
Задачей изобретения является создание такого способа, который позволит быстро, непосредственно в процессе протекания химической реакции, под воздействием радиационного облучения биологических молекул, производит и определять химические сдвиги в живых белковых молекулах с помощью ЯМР-спектроскопии.
Технический результат заключается в том, что одновременно с ЯМР-спектроскопией живых белковых молекул ведут их радиационное облучение, сравнивают скорость выхода химической реакции с контрольным образцом и, по результатам измерений, получают информацию о влиянии поглощенной дозы радиации на скорость протекания биохимической реакции.
Описание фигур
Фиг. 1. Схема установки по экспресс анализу ингибирования живых белковых молекул. (1) - источник радиации, (2) - исследуемый образец, (3-5) - измерители концентрации исходного вещества и продуктов реакции: глюкометр (3), алкометр (4), газовый анализатор (5); (6) - сверхпроводящий соленоид, (7) - узкополосный генератор радиоизлучения, (8) - приемник, настроенный на частоту генератора
Осуществление способа
Осуществление способа проведем на примере расщепления молекулы сахара на две молекулы этилового спирта и две молекулы углекислого газа, [7], Джамеев В.Ю. Химия. Биология, Эксмо, Москва, 2015, стр. 48.
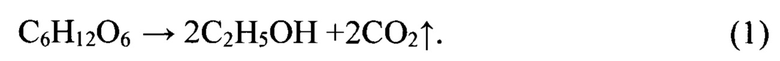
Схема соответствующей установки приведена на Фиг. 1. Если просто растворить сахар в теплой воде, то никакой реакции расщепления сахара идти не будет. Получится просто сладкая вода. Реакция пойдет только тогда, когда в раствор будут добавлены дрожжи. Дрожжи содержат биологический катализатор - фермент зимазу. Это большая белковая молекула, которая захватывает молекулу сахара и ее просто разрывает. Эта, и другие реакции, в которых участвуют ферменты, может идти быстрее или медленнее при облучении раствора определенной дозой радиации, поскольку радиация разрушает электронные связи в ферменте. На Фиг. 1. этот источник радиации обозначен цифрой (1). Точно известно, что если живую молекулу фермента каким-либо образом убить, то реакция расщепления сахара прекратится. Она пойдет снова, если добавить новую порцию фермента.
В данном случае, контролировать скорость протекания реакции можно с помощью обычных приборов. На Фиг. 1. контейнер в котором протекает реакция, обозначен цифрой (2). Уровень сахара в растворе можно контролировать глюкометром, позиция (3) на Фиг. 1, концентрацию спирта - алкометром, позиция (4), Фиг. 1. и количество выделившегося углекислого - газовым анализатором, позиция (5) на Фиг. 1. Таким образом, можно непосредственно в ходе радиационного облучения контролировать скорость этой химической реакции. Эту скорость реакции можно сравнивать со скоростью реакции нескольких контрольных образцов, которые находятся в таких условиях, как и испытуемый образец, но которые не подвергаются радиационному облучению.
Это дает нам информацию о влиянии поглощенной дозы радиации на скорость протекания биохимической реакции, но при этом остается не известным -какие именно разрушения в белковой молекуле привели к этому результату. Это можно узнать, если поместить исследуемое вещество внутрь ЯМР спектрометра. На Фиг. 1. Этот спектрометр показан в виде отдельных составных частей.
Позицией (6) на Фиг. 1. обозначен сверхпроводящий магнит, в поле которого изотопы водорода, углерода и азота с нечетным числом нуклонов испытывают зеемановский сдвиг. Этот резонансный сдвиг узкой линии поглощения можно зарегистрировать, если облучать вещество, находящееся в контейнере, с помощью перестраиваемого узкополосного радио излучателя, позиция (7) на Фиг. 1. и настроенного на ту же частоту узкополосного радиоприемника, позиция (8) на Фиг. 1.
Рассмотрим детально работу приборов, изображенных на Фиг. 1. Концентрацию сахара, растворенного в воде, можно контролировать с помощью обычного глюкометра. Исходя из уравнения (1), можно ожидать линейного во времени уменьшения концентрации сахара. Содержание спирта в растворе можно контролировать спиртометром. Количество выделившегося углекислого газа можно контролировать, собирая газ в отдельном объеме и используя датчик давления.
Таким образом, концентрацию всех трех молекул, участвующих в реакции (1), можно измерять независимо.
Прохождение γ-излучения через раствор сахара
Интенсивность пучка γ-квантов при прохождении через вещество убывает экспоненциально. В таблице на стр. 965 книги «Таблицы физических величин, справочник под ред. И.К. Кикоина, Москва, Атомиздат, 1976» [8], приведена толщина слоя воды, для которой достигается соответствующая кратность ослабления пучка в зависимости от энергии γ-квантов. Так, для кратности ослабления равной 2, для энергии γ-квантов равной ε=1 МэВ требуется слой воды с толщиной lw=26 см. Это означает, что слой воды с толщиной 10 cm будет равномерно облучаться γ-квантами с энергией ε=1 МэВ.
Механизм работы ферментов
Собственно, работа ферментов похожа на действия человека, играющего в тетрис. В этой игре сверху падают состоящие из четырех квадратиков фигурки. Задача человека состоит в том, чтобы направить фигурку соответствующей формы в нужное место, при этом фигурку с помощью кнопок надо требуемым образом развернуть. После того, как фигурками заполнен целый слой, слой исчезает. Задача человека состоит в том, чтобы заполнить за конечное время возможно большее количество слоев. Фермент зимаза, где-то на своей поверхности размещает соответствующим образом молекулу сахара, после чего разрывает ее на составные части. Скорее всего, фермент это делает с помощью электрических полей. Тогда, наложение внешнего электрического поля будет сильным ингибитором (внешнее электрическое поле будет уменьшать скорость биохимической реакции). Это будет происходить по двум причинам. С одной стороны - полярная молекула глюкозы будет занимать пространственную ориентацию, определяемую внешним электрическим полем, а не полем фермента зимазы. В результате молекула глюкозы не будет ориентирована (развернута) соответствующим образом не будет разорвана зимазой на отдельные части. С другой стороны, внешнее электрическое поле поляризует молекулы воды, которые потеряют подвижность. В результате, в такой среде «замороженных» молекул воды, молекуле глюкозы будет труднее развернуться в пространстве. После того как молекула глюкозы расположилась правильным образом на поверхности молекулы зимазы включаются дополнительные электрические поля, которые и разрывают молекулу глюкозы на части. Безусловно, и поток нейтронов и поток γ-излучения будут ингибиторами, то есть они будут повреждать молекулы зимазы, что уменьшит скорость катализа. Процессом катализа управляет живая молекула зимазы. По-видимому, это белковая цепная молекула, свернутая в глобулу. По мере нанесения молекуле зимазы повреждений глобула будет превращаться в клубок, то есть будут разрушены в первую очередь поперечные химические связи, форма молекулы немного изменится - она распухнет.
Раненая молекула скорость катализа уменьшит, мертвая молекула в процессе катализа участвовать не будет. Интересно связать степень повреждения молекулы зимазы со скоростью катализа.
Облучение биологических ферментов нейтронами
Будем, для определенности, считать, что объем раствора равен 1 дм3 и что он представляет собой куб со стороной 10 см. Количество молекул воды в одном сантиметре кубическом можно найти из соотношения Авогадро:


Откуда находим, что n=3*1022 мол/см3. График полного нейтронного сечения на воде в интервале энергий 0.01 - 107eV приведен в книге [8], стр. 914. Из этого графика видно, что в широком диапазоне энергий нейтронов полное сечение постоянно и равно: σ=40 бн.
Тогда, длина свободного пробега нейтрона в воде равна:

И это, в свою очередь, означает, что нейтронным потоком будет облучаться почти равномерно весь исследуемый объем раствора сахара в воде. Взаимодействие нейтронов с ядрами атомов зимазы
Рассмотрим процесс облучения зимазы на нейтронном пучке реактора ИБР - 2, расположенного в Дубне. Временная структура нейтронного пучка реактора ИБР -2 следующая. Собственно, реактор выдает импульсы с длительностью 200 микросекунд, следующие с частотой 5 Гц. Реактор дает нейтроны быстрые, средняя энергия которых равна ε=2 МэВ. Средняя плотность потока нейтронов достигает (в зависимости от места расположения мишени) 1014 n/см2*с.
Облучая молекулы зимазы потоком нейтронов, можно будет видеть, как скорость катализа зависит от величины поглощенной дозы нейтронов и восстанавливается ли скорость катализа после снятия облучения. Тем самым будет дан ответ на вопрос - обратимы ли радиационные повреждения, нанесенные зимазе потоком нейтронов.
Изменение свойств белковой молекулы под воздействием внешних неблагоприятных факторов, в частности радиации, называется денатурацией. Предлагаемый способ экспресс анализа позволит связывать степень радиационного повреждения белковой молекулы с изменением ее свойств непосредственно в процессе радиационного облучения белковой молекулы.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНАЛИЗАТОР МНОГОФАЗНОЙ ЖИДКОСТИ | 2013 |
|
RU2530460C1 |
| КОНТЕЙНЕР | 2006 |
|
RU2310831C1 |
| КОНСТРУКЦИЯ ФОТОЭЛЕКТРИЧЕСКОГО МОДУЛЯ КОСМИЧЕСКОГО БАЗИРОВАНИЯ | 2014 |
|
RU2584184C1 |
| ДЕТЕКТОР ПРОНИКАЮЩИХ ИЗЛУЧЕНИЙ | 2005 |
|
RU2290664C1 |
| СПОСОБ И УСТРОЙСТВО ГЕНЕРАЦИИ КВАНТОВЫХ ПУЧКОВ | 2010 |
|
RU2433493C1 |
| СПОСОБ ПОВЫШЕНИЯ ЧАСТОТЫ ОБРАЗОВАНИЯ ДВУНИТЕВЫХ РАЗРЫВОВ ДНК В КЛЕТКАХ ЧЕЛОВЕКА ПРИ ДЕЙСТВИИ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ В УСЛОВИЯХ ВЛИЯНИЯ РАДИОМОДИФИКАТОРОВ | 2018 |
|
RU2699670C1 |
| Способ определения поглощенной дозы ядер отдачи | 2020 |
|
RU2743417C1 |
| ЭКРАН-ПРЕОБРАЗОВАТЕЛЬ ПРОНИКАЮЩИХ ИЗЛУЧЕНИЙ | 2005 |
|
RU2290665C1 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ СПЕКТРОСКОПИИ ЖИВОЙ ТКАНИ | 2019 |
|
RU2752711C2 |
| СЦИНТИЛЛЯЦИОННЫЙ ДЕТЕКТОР НЕЙТРОННОГО И ГАММА-ИЗЛУЧЕНИЯ | 2000 |
|
RU2189057C2 |

Использование: для экспресс-анализа ингибирования живых белковых молекул. Сущность изобретения заключается в том, что выполняют ЯМР-спектроскопию живых молекул, при этом одновременно с ЯМР-спектроскопией живых белковых молекул ведут их радиационное облучение, сравнивают скорость выхода химической реакции с контрольным образцом и по результатам измерений получают информацию о влиянии поглощенной дозы радиации на скорость протекания биохимической реакции. Технический результат: обеспечение возможности быстро, непосредственно в процессе протекания химической реакции, под воздействием радиационного облучения белковых молекул осуществлять и определять химические сдвиги в живых белковых молекулах с помощью ЯМР-спектроскопии. 1 ил.
Способ экспресс анализа ингибирования живых белковых молекул, включающий ЯМР-спектроскопию живых молекул, отличающийся тем, что одновременно с ЯМР-спектроскопией живых белковых молекул ведут их радиационное облучение, сравнивают скорость выхода химической реакции с контрольным образцом и по результатам измерений получают информацию о влиянии поглощенной дозы радиации на скорость протекания биохимической реакции.
| Тарасевич Б.Н | |||
| Первоначальные сведения о методах ЯМР, масс спектрометрии и ИК спектрометрии, МГУ им | |||
| М.В | |||
| Ломоносова, Химический факультет, кафедра органической химии, 2014 | |||
| Jian Zhi Hu, Xiongjie, Mary Y Hu, NMR Metabolomics in Ionizing Radiation, HHS Public Access, Clin Oncol (Belmont), 2016, pp | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Changhyun Roh, Metabolomics in | |||
Авторы
Даты
2022-07-18—Публикация
2021-09-14—Подача