ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка заявляет приоритет по предварительной заявке на патент США №62/501981, поданной 5 мая 2017 г., которая включена в данное описание в качестве ссылки в полном объеме.
УРОВЕНЬ ТЕХНИКИ
[0002] Семафорин 4D (SEMA4D), также известный как CD100, представляет собой трансмембранный белок, который принадлежит к семейству генов семафорина. SEMA4D экспрессируется на клеточной мембране в виде гомодимера, но при активации клеток SEMA4D может быть освобожден от клеточной мембраны с помощью протеолитического расщепления для создания sSEMA4D - растворимой формы белка, которая также является биологически активной. См. Suzuki et al., Nature Rev. Immunol. 3:159-167 (2003); Kikutani et al., Nature Immunol. 9:17-23 (2008).
[0003] SEMA4D экспрессируется на высоком уровне в лимфоидных органах, в том числе селезенке, тимусе и лимфатических узлах, и в органах, не являющихся лимфоидными, таких как мозг и почки. В лимфоидных органах, SEMA4D обильно экспрессируются на покоящихся Т-клетках, но лишь слабо экспрессируются на покоящихся В-клетках и антиген-презентирующих клетках (АРС), таких как дендритные клетки (DC). Однако, их экспрессия, активируется в этих клетках после активации различных иммунологических раздражителей. Высвобождение растворимого SEMA4D из иммунных клеток также увеличивается за счет активации клеток.
[0004] SEMA4D участвует в развитии некоторых видов рака (Ch'ng et al., Cancer 110:164-72 (2007); Campos et al., Oncology Letters 5:1527-35 (2013); Kato et al., Cancer Sci. 102:2029-37 (2011)) и несколько источником предполагают, что одним из механизмов этого влияния является роль SEMA4D в развитии ангиогенеза опухоли (Conrotto et al., Blood 105:4321-4329 (2005). Basile et al., J Biol Chem. 282:34888-34895 (2007); Sierra et. al. J. Exp. Med. 205:1673 (2008); Zhou et al., Angiogenesis 15:391-407 (2012)). Рост и метастазирование опухоли включают сложный процесс перекрестного взаимодействия среди опухолевых клеток, стромы и иммунного инфильтрата, а также эндотелиальных клеток и сосудов. SEMA4D сверхэкспрессируется в широком спектре типов опухолей и также продуцируется воспалительными клетками, рекрутируемыми на микроокружение опухоли. Последние работы показывают, что SEMA4D играет важную роль в миграции, выживании, дифференциации и организации различных типов клеток, которые составляют строму опухоли (Evans et al., Cancer Immunol. Res. 3:689-701 (2015)).
[0005] SEMA4D участвует в нейродегенеративных расстройств, аутоиммунных заболеваниях, демиелинизирующих заболеваний и раке. В центральной нервной системе (ЦНС), SEMA4D экспрессируется на, например, инфильтрующих иммунных клетка и клетках-предшественниках олигодендроцитов, а его рецепторы экспрессируются на, например, нейронах, олигодендроцитах, астроцитах и эндотелиальных клетках (Okuno, Т., et al., J. Immunol. 184:1499-1506 (2010)). SEMA4D может служить в качестве аксональной молекулы наведения (Swiercz et al., Neuron 35:51-63 (2002)) и может стать посредником развития ГАМКергического и глутаматергического синапсов (Paradis et al., Neuron 53:217-232 (2007)) среди других активностей.
[0006] Также было показано, что SEMA4D, играют роль в миграции и дифференцировке нейронов и клеток-предшественников олигодендроцитов, воспалении ЦНС и нейродегенерации. Например, SEMA4D-дефицитные мыши устойчивы к развитию экспериментального аутоиммунного энцефаломиелита (ЕАЕ) (Kumanogoh A et al., Immunity 13:621-631 (2000)), и блокада SEMA4D может ингибировать активацию микроглии и нейровоспаления при ЕАЕ (Okuno, Т., et al., J. Immunol. 184:1499-1506 (2010)). Точно так же, стимуляция SEMA4D эндотелиальных клеток может привести к образованию провоспалительного цитокина IL-8 (Yang, YH et al., PLoS One 6:e25826 (2011)).
[0007] Недавние публикации показали эффективность связывающих молекул против SEMA4D, например, антитела или его антигенсвязывающих фрагментов в лечении как рака, так и нейровоспалительных/нейродегенеративных заболеваний. Например, последние фазы клинических испытаний с антителом против SEMA4D VX15/2503 продемонстрировали безопасность и эффективность при лечении солидных опухолей. См., например, Patnaik, A., et al. Clin. Cancer Res. 22:827-836 (2016) и Southwell AL., et al., Neurobiol. Dis 76:46-56 (2015). Тем не менее остается потребность в дополнительных антителах против SEMA4D с модифицированными и/или улучшенными профилями, например, по отношению к характеристикам связывания, иммуногенности и/или активности.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] Данное изобретение относится к композициям и способам лечения заболеваний, связанных с патологиями семафорина-4 В (SEMA4D), таким как аутоиммунные заболевания, воспалительные заболевания, рак, нейровоспалительные заболевания и нейродегенеративные расстройства. Согласно аспектам данного изобретения, проиллюстрированным в данном описании, предложено антитело или антигенсвязывающие фрагменты, которые специфически связываются с SEMA4D. Согласно другим аспектам данного изобретения, представленным в данном документе, предложен способ лечения субъекта с аутоиммунным заболеванием, воспалительные заболевания, раком, нейровоспалительным заболеванием и нейродегенеративным расстройством, включающий введение субъекту эффективного количества антитела, или его антигенсвязывающего фрагмента, которое специфически связывается с SEMA4D и нейтрализует активность SEMA4D.
[0009] В определенных аспектах, антитело или его антигенсвязывающий фрагмент, которое специфически связывается с SEMA4D, содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL); причем VH содержит области, определяющие комплементарность (HCDR) HCDR1, HCDR2 и HCDR3, содержащие аминокислотные последовательности, идентичные или идентичные за исключением одной, двух, трех или четырех аминокислотных замен в одной, двух или трех HCDR SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 4, соответственно; при этом VL содержит области, определяющие комплементарность (LCDR) LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности, идентичные или идентичные за исключением одной, двух, трех или четырех аминокислотных замен в одной, двух или трех LCDR SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно.
[00010] В определенных аспектах антитело против SEMA4D, или его антигенсвязывающий фрагмент, содержит области, определяющие комплементарность VH HCDR1, HCDR2 и HCDR3, которые содержат аминокислотные последовательности идентичные SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 4, соответственно, и VL области, определяющие комплементарность LCDR1, LCDR2 и LCDR3, которые содержат аминокислотные последовательности идентичные SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно.
[00011] В определенных аспектах антитело против SEMA4D, или его антигенсвязывающий фрагмент, содержит VH, которая содержит каркасные области (HFW) HFW1, HFW2, HFW3 и HFW4, и VL, которая содержит каркасные области (LFW) LFW1, LFW2, LFW3 и LFW4. В определенных аспектах, каркасные области могут быть получены из антитела человека или из антитела, не являющегося антителом человека.
[00012] В определенных аспектах, антитело против SEMA4D или его антигенсвязывающий фрагмент содержит VH, которая содержит аминокислотную последовательность SEQ ID NO: 1. В определенных аспектах, антитело против SEMA4D или его антигенсвязывающий фрагмент содержит VL, которая содержит аминокислотную последовательность SEQ ID NO: 5. В определенных аспектах, антитело против SEMA4D или его антигенсвязывающий фрагмент содержит VH и VL, которые содержат аминокислотные последовательности SEQ ID NO: 1 и SEQ ID NO: 5, соответственно.
[00013] В определенных аспектах VH антитела против SEMA4D или его антигенсвязывающего фрагмента, представленная в данном описании, содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95% или 100% идентичную SEQ ID NO: 1. В определенных аспектах VL антитела против SEMA4D или его антигенсвязывающего фрагмента, представленная в данном описании, содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95% или 100% идентичную SEQ ID NO: 5. В определенных аспектах VH может содержать аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95% или 100% идентичную SEQ ID NO: 1; a VL может содержать аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95% или 100% идентичную SEQ ID NO: 5.
[00014] В определенных аспектах антитело против SEMA4D, или его фрагмент, раскрытое в данном документе, содержит константную область тяжелой цепи, или ее фрагмент, слитую с С-концом VH. В определенных аспектах константная область тяжелой цепи, или ее фрагмент, представляет собой константную область тяжелой цепи человека. В определенных аспектах константная область тяжелой цепи, или ее фрагмент, может представлять собой константную область IgG4. В определенных аспектах константная область тяжелой цепи, или ее фрагмент, представляет собой константную область тяжелой цепи не являющейся тяжелой цепью человека. В определенных аспектах константная область тяжелой цепи, или ее фрагмент, представляет собой константную область IgG1 мыши. В определенных аспектах антитело против SEMA4D, или его фрагмент, содержит VH и VL, причем константная область легкой цепи, или ее фрагмент, слита с С-концом VL. В определенных аспектах антитело против SEMA4D, или его фрагмент, раскрытое в данном документе, содержит константную область легкой цепи, или ее фрагмент, слитую с С-концом VL. В определенных аспектах константная область легкой цепи представляет собой константную область легкой цепи человека, например, константную область легкой цепи лямбда человека или каппа человека. В определенных аспектах константная область легкой цепи представляет собой константную область легкой цепи, не являющейся легкой цепью человека, например, константную область легкой цепи лямбда мыши.
[00015] В определенных аспектах антитело против SEMA4D или его фрагмент, предложенные в данном документе, могут представлять собой фрагмент Fab, фрагмент Fab', фрагмент F(ab')2, фрагмент Fd, одноцепочечный фрагмент Fv (scFv) или дисульфид-связанный фрагмент Fv (sdFv). В некоторых аспектах антитело против SEMA4D, или его фрагмент, может быть мультиспецифическим, например, биспецифическим.
[00016] В определенных аспектах, антитело против SEMA4D, или его фрагмент, представленные в данном документе, может специфически связываться с SEMA4D человека, SEMA4D мыши, SEMA4D крысы и/или SEMA4D примата, не являющегося человеком, например, SEMA4D макака и/или SEMA4D мармозетки. В определенных аспектах антитело SEMA4D, или его фрагмент, предложенное в данном документе, может связываться с SEMA4D, например, SEMA4D человека, SEMA4D мыши, SEMA4D крысы и/или SEMA4D примата, отличного от человека, например, SEMA4D яванского макака и/или SEMA4D мармозетки, с аффинностью, характеризующейся константой диссоциации KD не более чем 500 нМ, 100 нМ, 50,0 нМ, 40,0 нМ, 30,0 нМ, 20,0 нМ, 10,0 нМ, 9,0 нМ, 8,0 нМ, 7,0 нМ, 6,0 нМ, 5,0 нМ, 4,0 нМ, 3,0 нМ, 2,0 нМ, 1,0 нМ, 0,50 нМ, 0,10 нМ, 0,050 нМ, 0,01 нМ, 0,005 нМ или 0,001 нМ.
[00017] В определенных аспектах, антитело против SEMA4D, или его фрагмент, предложенное в данном документе, может ингибировать связывание SEMA4D с рецептором SEMA4D, например, плексином-В1, плексином-В2, CD72 или любой их комбинацией.
[00018] В определенных аспектах, антитело против SEMA4D, или его фрагмент, вызывает минимальный ответ или отсутствие иммунного ответа на антитело при введении субъекту.
[00019] В определенных аспектах, антитело против SEMA4D, или его фрагмент, содержит гетерологичный фрагмент, слитый или конъюгированный с ним. В некоторых аспектах гетерологичный фрагмент может представлять собой полипептид, цитотоксический агент, терапевтический агент, пролекарство, липид, углевод, нуклеиновую кислоту, детектируемую метку, полимер или любую их комбинацию. В определенных аспектах гетерологический фрагмент может включать связывающую молекулу, фермент, цитокин, лимфокин, гормональный пептид или любую их комбинацию. В определенных аспектах гетерологический фрагмент может включать радионуклид, биологический токсин, ферментативно активный токсин или любую их комбинацию. В определенных аспектах гетерологический фрагмент может включать фермент, флуоресцентную метку, хемилюминесцентную метку, биолюминесцентную метку, радиоактивную метку или любую их комбинацию.
[00020] В определенных аспектах в данном изобретении предложена фармацевтическая композиция, содержащая антитело против SEMA4D, или его фрагмент, предложенное в данном описании, и носитель.
[00021] В определенных аспектах в данном изобретении предложен выделенный полинуклеотид, или комбинация полинуклеотидов, содержащий одну или более последовательностей нуклеиновых кислот, кодирующих антитело против SEMA4D, или его фрагмент. В другом аспекте полинуклеотид или комбинация полинуклеотидов, содержит последовательность нуклеиновой кислоты, кодирующую VH, антитела против SEMA4D, или его фрагмента. В другом аспекте полинуклеотид или комбинация полинуклеотидов, содержит последовательность нуклеиновой кислоты, кодирующую VL, антитела против SEMA4D, или его фрагмента. В другом аспекте полинуклеотид или комбинация полинуклеотидов, содержит последовательность нуклеиновой кислоты, кодирующую VH и VL, антитела против SEMA4D, или его фрагмента. В еще одном аспекте в данном изобретении предложен вектор, содержащий полинуклеотид, который содержит одну или более последовательностей нуклеиновых кислот, кодирующих антитело против SEMA4D, или его фрагмент. В другом аспекте в данном изобретении предложена клетка-хозяин, содержащая вектор. В другом аспекте в данном изобретении предложен способ получения антитела против SEMA4D, или его фрагмента.
[00022] В определенном аспекте предложенного способа антитело против SEMA4D, или его антигенсвязывающий фрагмент, нейтрализует SEMA4D у субъекта-человека.
[00023] В соответствии с аспектами, проиллюстрированных в данном описании, в данном изобретении предложен способ лечения субъекта с аутоиммунным заболеванием или расстройством, воспалительным заболеванием или расстройствами, раком, нейровоспалительным заболеванием или расстройством, нейродегенеративным заболеванием или расстройством, или любыми их комбинациями, включая введение субъекту эффективного количества антитела или его антигенсвязывающего фрагмента, которое специфически связывается с SEMA4D и нейтрализует активность SEMA4D. В определенных аспектах нейровоспалительное заболевание или расстройство представляет собой рассеянный склероз. В определенных аспектах нейродегенеративное заболевание или расстройство представляет собой инсульт, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, синдром Дауна, атаксию, боковой амиотрофический склероз (ALS), лобно-височную деменцию (FTD), связанное с ВИЧ когнитивное нарушение, волчанку ЦНС, умеренное когнитивное нарушение или их комбинацию. В определенных аспектах аутоиммунное заболевание или воспалительное заболевание представляет собой артрит. В определенных аспектах аутоиммунное заболевание или воспалительное заболевание представляет собой ревматоидный артрит.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ/ФИГУР
[00024] На Фиг. 1А представлено сравнение связывания MAbD2517 и MAbVX15/2503 (оба растворены в PBS) с SEMA4D человека, измеренное с помощью ИФА.
[00025] На Фиг. 1В представлено сравнение связывания MAbD2517 и MAbVX15/2503 (оба растворены в PBS) с SEMA4D яванского макака, измеренное с помощью ИФА.
[00026] На Фиг. 1С представлено сравнение связывания MAbD2517 и MAbVX15/2503 (оба растворены в PBS) с SEMA4D мармозетки, измеренное с помощью ИФА.
[00027] На Фиг. 1D представлено сравнение связывания MAbD2517 и MAbVX15/2503 (оба растворены в PBS) с SEMA4D мыши, измеренное с помощью ИФА.
[00028] На Фиг. 2А представлена способность MAbD2517 блокировать связывание SEMA4D человека с клетками 293PLXNB1 по сравнению с MAbVX15/2503.
[00029] На Фиг. 2В представлена способность MAbD2517 блокировать связывание SEMA4D яванского макака с клетками 293PLXNB1 по сравнению с MAbVX15/2503.
[00030] На Фиг. 2С представлена способность MAbD2517 блокировать связывание SEMA4D мыши с клетками 293PLXNB1 по сравнению с MAbVX15/2503.
[00031] На Фиг. 2D представлена способность MAbD2517 блокировать связывание SEMA4D крысы с клетками 293PLXNB1 по сравнению с MAbVX15/2503.
[00032] На Фиг. 3А представлено измерение объема опухоли у Balb/c мышей, получавших лечение или контрольным IgG1/2B8 мыши, или химерным антителом MAbD2585 (10 мг/кг, ИП, еженедельно Х5).
[00033] На Фиг. 3В представлено время выживания мышей Balb/c, получавших лечение или контрольным IgG1/2B8 мыши, или химерным антителом MAbD2585.
[00034] На Фиг. 3С представлена частота регрессий опухолей у мышей Balb/c, получавших лечение или контрольным IgG1/2B8 мыши, или химерным антителом MAbD2585.
ДЕТАЛЬНОЕ ОПИСАНИЕ
Определения
[00035] Следует отметить, что использование определений в единственном числе не исключает возможности наличия определений во множественном числе, например, «связывающая молекула» представляет собой одну или более связывающих молекул. Таким образом, термины «один или более» и «по меньшей мере один» могут быть использованы в данном документе взаимозаменяемо.
[00036] Кроме того, «и/или», используемые в данном документе, следует рассматривать как конкретное раскрытие каждого из двух указанных признаков или компонентов с другим, или без другого. Таким образом, термин «и/или», используемый во фразе, такой как «А и/или В» в данном описании предназначен для включения «А и В», «А или В» «А (отдельно)» и «В (отдельно)». Аналогично, термин «и/или», используемый в фразе, например, «А, В и/или С» предназначен для охвата каждого из следующих вариантов: А, В и С; А, В или С; А или С; А или В; В или С; А и С; А и В; В и С; А (отдельно); В (отдельно) и С (отдельно).
[00037] Если не указано иное, технические и научные термины, используемые в данном документе, имеют такое же значение, которое обычно понимается обычным специалистом в данной области техники к которой относится данное описание. Например, Concise Dictionary of Biomedicine and Molecular Biology, Juo, Pei-Show, 2nd ed., 2002, CRC Press; The Dictionary of Cell and Molecular Biology, 3rd ed., 1999, Academic Press и the Oxford Dictionary of Biochemistry and Molecular Biology, Revised, 2000, Oxford University Press, предлагают специалистам в данной области техники словари многих терминов, используемых в данном описании.
[00038] Единицы, префиксы и символы обозначены в форме международной системы СИ (SI). Числовые диапазоны включают числа, определяющие диапазон. Если не указано иное, аминокислотные последовательности записываются слева направо в направлении от аминогруппы до карбоксильной группы. Заголовки, представленные в данном документе, не являются ограничениями различных аспектов или аспектов данного изобретения, которые могут быть ссылкой на описание в целом. Соответственно, термины, определенные непосредственно ниже, более полно определяются ссылкой на описание в полном объеме.
[00039] Все варианты осуществления, описанные с термином «содержит», являются аналогичными вариантами осуществления, описанным с терминами «состоит из» и/или «состоит по существу из».
[00040] Аминокислоты называют в данном документе с помощью их общеизвестных трехбуквенных символов или с помощью однобуквенных символов, рекомендованных комиссией по биохимической номенклатуре IUPAC-IUB. Нуклеотиды, также, называют их общепринятыми однобуквенными кодами.
[00041] Используемые в данном описании термины «рак» и «раковый» относятся или описывают физиологическое состояние у млекопитающих, в котором популяция клеток, характеризуются неконтролируемым ростом клеток. Раки могут быть классифицированы, например, в виде солидных опухолей или злокачественных новообразований, или гематологических злокачественных опухолей или злокачественных новообразований. Оба типа могут мигрировать на удаленные органы, как метастазы. Солидные опухоли могут быть классифицированы, например, как саркомы, карциномы, меланомы или их метастазы.
[00042] «Опухоль» и «новообразование», используемые в данном документе, относятся к любой массе ткани, которые являются результатом чрезмерного роста или пролиферации клеток, как доброкачественные (нераковые) так и злокачественные (раковые), включая предраковые поражения. В определенных вариантах осуществления, опухоли, описанные в данном документе экспрессируют рецептор SEMA4D, например, плексин-В1, плексин-В2 и/или CD72, и/или может экспрессировать SEMA4D.
[00043] Используемый в данном описании термин «полипептид» предназначен для охвата одиночного «полипептида», а также множественных «полипептидов» и относится к молекуле, состоящей из мономеров (аминокислот), линейно связанных амидными связями (также известными, как пептидные связи). Термин «полипептид» относится к любой цепи или цепи из двух или более аминокислот и не относится к конкретной длине продукта. Таким образом, пептиды, дипептиды, трипептиды, олигопептиды, «белок», «аминокислотная цепь» или любой другой термин, используемый для обозначения цепи или цепей из двух или более аминокислот, включены в определении «полипептид», а термин «полипептид» может быть использован вместо или наравне с каким-либо из этих терминов. Термин «полипептид» также предназначен для обозначения продуктов пост-экспрессионных модификаций полипептида, в том числе, без ограничения, гликозилирование, ацетилирование, фосфорилирование, амидирование, дериватизацию и при помощи известных защитных/блокирующих групп, протеолитического расщепления или модификации с помощью не встречающихся в природе аминокислот. Полипептид может быть получен из биологического источника или получен с помощью рекомбинантной технологии, но не обязательно транслируется из обозначенной последовательности нуклеиновой кислоты. Он может быть создан любым способом, в том числе путем химического синтеза.
[00044] Полипептид, описанный в данном документе, может иметь размер, равный около 3 или более, 5 или более, 10 или более, 20 или более, 25 или более, 50 или более, 75 или более, 100 или более, 200 или более, 500 или более, 1000 или более или 2000 или более аминокислот. Полипептиды могут иметь определенную трехмерную структуру, хотя они не обязательно имеют такую структуру. Полипептиды с определенной трехмерной структурой, называются сложенными, а полипептиды, которые не обладают определенной трехмерной структурой, а может принимать множество различных конформаций и называется разложенным. Используемый в данном описании термин гликопротеин относится к белку, соединенному с по меньшей мере одним углеводным фрагментом, который присоединен к белку посредством кислородсодержащей или азотсодержащей боковой цепи аминокислоты, например, серина или аспарагина.
[00045] Под «выделенным» полипептидом или его фрагментом, вариантом, или производным подразумевают полипептид, который находится не в своей естественной среде. Конкретный уровень очистки не требуется. Например, выделенный полипептид может быть удален из его нативной или природной среды. Рекомбинантно полученные полипептиды и белки, экспрессированные в клетках-хозяевах, считаются выделенными, как описано в данном документе, так же как и нативные или рекомбинантные полипептиды, которые были отделены, фракционированных, или частично или, по существу, очищенные с помощью любого подходящего способа.
[00046] Используемый в данном описании, термин «не встречающийся в природе полипептид» или любой его грамматические варианты, представляет собой условное определение, которое явно исключает, но только исключает, эти формы полипептида, которые являются, или могут быть, определяемые или интерпретируемыми судьей или административным судьей, или судебным органом, как «природные».
[00047] Другие полипептиды, описанные в данном документе, представляют собой фрагменты, производные, аналоги или варианты указанных выше полипептидов, а также любую их комбинацию. Термины «фрагмент», «вариант», «производное» и «аналог», раскрытые в данном описании, включают любые полипептиды, которые сохраняют по меньшей мере, некоторые из свойств соответствующего нативного полипептида, антитела или, например, специфически связываться с антигеном. Фрагменты полипептидов включают, например, протеолитические фрагменты, а также фрагменты делеции, в дополнении к определенным фрагментам антител, обсуждаемых в данном документе в другом месте. Варианты, например, полипептид, включают фрагменты, описанные выше, а также полипептиды с измененными аминокислотными последовательностями из-за аминокислотных замен, делеций или инсерций. В определенных аспектах варианты могут быть не неприродными. Неприродные варианты могут быть получены с использованием известных методов мутагенеза. Варианты полипептидов могут содержать консервативные или неконсервативные аминокислотные замены, делеции или инсерций. Производные полипептидов, которые были изменены таким образом, чтобы продемонстрировать дополнительные функции, которых нет у оригинального полипептида. Примеры включают слитые белки. Варианты полипептидов могут также упоминаться в данном документе как «аналоги полипептидов». Используемый в данном документе термин «производное» полипептида может также относиться к конкретному полипептиду, имеющему одну или более аминокислот, химически дериватизированных посредством реакции функциональной боковой группы. Также в качестве «производных» включены пептиды, которые содержат одно или более производных двадцати стандартных аминокислот. Так, например, 4-гидроксипролин может быть заменен на пролин, 5-гидроксилизин может быть заменен на лизин, 3-метилгистидин может быть заменен на гистидин, гомосерин может быть заменен на серии, а орнитина может быть заменен на лизин.
[00048] «Консервативная аминокислотная замена» является той, в котором одна аминокислота заменена другой аминокислотой, имеющей подобную боковую цепь. Семейства аминокислот, имеющих сходные боковые цепи, были определены в данной области техники, включая основные боковые цепи (например, лизин, аргинин, гистидин), кислотные боковые цепи (например, аспарагиновая кислота, глутаминовая кислота), незаряженные полярные боковые цепи (например, аспарагин, глутамин, серии, треонин, тирозин, цистеин), неполярные боковые цепи (например, глицин, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленные боковые цепи (например, треонин, валин, изолейцин) и ароматические боковые цепи (например, тирозин, фенилаланин, триптофан, гистидин). Например, замена фенилаланина на тирозин является консервативной заменой. В определенных вариантах осуществления, консервативные замены в последовательности полипептидов и антител по данному изобретению не отменяют связывание полипептида или антитела, содержащих аминокислотную последовательность, с антигеном, с которым связывается связывающая молекула. Методы идентификации нуклеотидных и аминокислотных консервативных замен, которые не исключают связывания с антигеном, хорошо известны в данной области техники (см, например, Brummell et al., Biochem. 32:1180-1187 (1993); Kobayashi et al., Protein Eng. 12(10):879-884 (1999) и Burks et al., Proc. Natl. Acad. Sci. USA 94:.412-417 (1997)).
[00049] Термин «полинуклеотид» предназначен для охвата одиночной нуклеиновой кислоты, а также множественных нуклеиновых кислот, и относится к выделенной молекуле нуклеиновой кислоты или конструкции, например, матричной РНК (мРНК), кДНК или плазмидной ДНК (пДНК). Полинуклеотид может содержать обычную фосфодиэфирную связь или нетрадиционную связь (например, амидную связь, например, пептидные нуклеиновые кислоты (ПНК)). Термины «нуклеиновая кислота» или «последовательность нуклеиновой кислоты» относится к любому одному или более сегментам нуклеиновых кислот, например, фрагментам ДНК или РНК, присутствующим в полинуклеотиде.
[00050] Под «выделенной» нуклеиновой кислотой или полинуклеотидом подразумевают любую форму нуклеиновой кислоты или полинуклеотида, которая отделена от ее родной среды. Так, например, гель-очищенный полинуклеотид, или рекомбинантный полинуклеотид, кодирующий полипептид, содержащийся в векторе, будет считаться «выделенным». Кроме того, сегмент полинуклеотида, например, ПЦР-продукт, который был модифицирован, чтобы иметь сайты рестрикции для клонирования считается «выделенным». Другие примеры выделенного полинуклеотида включают рекомбинантные полинуклеотиды, поддерживаемые в гетерологичных клетках-хозяевах или очищенные (частично или в значительной степени) полинуклеотиды в неродном растворе, такие как буфер или физиологический раствор. Выделенные молекулы РНК включают in vivo или in vitro РНК-транскрипты полинуклеотидов, в которых транскрипт не является таким, который может быть найден в природе. Выделенные полинуклеотиды или нуклеиновые кислоты дополнительно включают такие молекулы, полученные синтетическим путем. Кроме того, полинуклеотид или нуклеиновая кислота может быть или может содержать регуляторный элемент, такой как промотор, сайт связывания рибосом или терминатор транскрипции.
[00051] Используемый в данном описании, термин «не встречающийся в природе полинуклеотид» или любой его грамматические варианты, представляет собой условное определение, которое явно исключает, но только исключает, эти формы нуклеиновой кислоты или полинуклеотида, которые являются, или могут быть, определяемые или интерпретируемыми судьей или административным судьей, или судебным органом, как «природные».
[00052] Используемый в данном описании термин «кодирующая область» представляет собой часть нуклеиновой кислоты, которая состоит из кодонов, транслированных в аминокислоты. Хотя «стоп-кодон» (TAG, ТГ, или ТАА) не транслируется в аминокислоты, он может рассматриваться как часть кодирующей области, но любые фланкирующие последовательности, например, промоторы, участки связывания рибосомы, терминаторов транскрипции, интроны и т.п., не являются частью кодирующей области. Двк или более кодирующие области могут присутствовать в одной полинуклеотидной конструкции, например, на одном векторе, или в отдельных полинуклеотидных конструкциях, например, на отдельных (различных) векторах. Кроме того, любой вектор может содержать одну кодирующую область, или может содержать две или более кодирующих областей, например, один вектор может отдельно кодировать вариабельную область тяжелой цепи иммуноглобулина и вариабельную область легкой цепи иммуноглобулина. Кроме того, вектор, полинуклеотид или нуклеиновая кислота могут содержать гетерологичные кодирующие области, либо слитые или не слитые с другой кодирующей областью. Гетерологические кодирующие области включают, без ограничения, эти кодирующие специализированные элементы или мотивы, такие как секреторный сигнальный пептид или гетерологичный функциональный домен.
[00053] В определенных вариантах осуществления полинуклеотид или нуклеиновая кислота представляет собой ДНК. В случае ДНК, полинуклеотид, содержащий нуклеиновую кислоту, которая кодирует полипептид, как правило, может содержать промотор и/или другие транскрипционные или управляющие элементы трансляции функционально связанные с одной или более кодирующей областью. Функциональная ассоциация, когда участок, кодирующий генный продукт, например, полипептид, связан с одной или более регуляторными последовательностями таким образом, чтобы поместить экспрессию продукта гена под влияние или контроль регуляторной последовательности(ей). Два фрагмента ДНК (например, область, кодирующая полипептид и промотор, связанный с ней) являются «функционально связанными», если индукция функции промотора приводит к транскрипции мРНК, кодирующей нужный генный продукт, и если природа связи между этими двумя фрагментами ДНК не мешает способности регуляторных последовательностей экспрессии направлять экспрессию продукта гена или не препятствует способности ДНК-матрицы осуществлять транскрипцию. Таким образом, область промотора будет функционально связана с нуклеиновой кислотой, кодирующей полипептид, если промотор был способен осуществлять транскрипцию этой нуклеиновой кислоты. Промотор может представлять собой клетка-специфический промотор, который направляет значительную транскрипцию ДНК в заранее определенных клетках. Другие элементы управления транскрипцией, помимо промотора, например, энхансеры, операторы, репрессоры и сигналы терминации транскрипции, могут быть функционально связаны с полинуклеотидом для управления клеточно-специфической транскрипцией.
[00054] Разнообразие областей контроля транскрипции известно специалистам в данной области техники. Оно включает, без ограничения, области контроля транскрипции, которые функционируют в клетках позвоночных, таких как, без ограничения, сегменты промотора и энхансера от цитомегаловирусов (непосредственный ранний промотор, в сочетании с интроном-А), вирус обезьяны 40 (ранний промотор), и ретровирусы (например, вирус саркомы Рауса). Другие области контроля транскрипции включают те, которые получены из генов позвоночных, таких как актин, белок теплового шока, бычий гормон роста и бета-глобин кролика, а также другие последовательности, способные контролировать экспрессию генов в эукариотических клетках. Дополнительные подходящие области контроля транскрипции включают ткань-специфические промоторы и энхансеры, а также лимфокин-индуцируемые промоторы (например, промоторы, индуцируемые интерферонами или интерлейкинами).
[00055] Кроме того, различные элементы управления трансляции известны обычным специалистам в данной области техники. Они включают, но не ограничиваются ими, сайты связывания рибосом, кодоны инициации трансляции и терминации и элементы, полученные из пикорнавирусов (в частности, внутренний сайт записи рибосомы или IRES, также упоминаемый как последовательность Cite).
[00056] В других вариантах осуществления полинуклеотид может представлять собой РНК, например, в виде матричной РНК (мРНК), транспортной РНК или рибосомальной РНК.
[00057] Полинуклеотид и кодирующие области нуклеиновых кислот, могут быть связаны с дополнительными кодирующими областями, которые кодируют секреторные или сигнальные пептиды, которые направляют секрецию полипептида, кодируемого полинуклеотидом, как описано в данном документе. Согласно гипотезе сигнала, белки секретируемые клетками млекопитающих имеют сигнальный пептид или секреторную лидерную последовательность, которая отщепляется от зрелого белка, как только начинается экспорт растущей белковой цепи через шероховатой эндоплазматической сети. Так, специалистам в данной области техники известно, что полипептиды, секретируемые клетками позвоночных, могут иметь сигнальный пептид, слитый с N-концом полипептида, который расщепляется от полного или «полноразмерного» полипептида, чтобы произвести секретируемую или «зрелую» форму полипептида. В некоторых вариантах осуществления используют, например, нативный сигнальный пептид, тяжелой цепи иммуноглобулина или легкой цепи сигнального пептида, или функциональное производное этой последовательности, которая сохраняет способность направлять секрецию полипептида, который функционально связанный с ним. В качестве альтернативы, можно использовать гетерологичный сигнальный пептид млекопитающего, или его функциональное производное. Так, например, лидерная последовательность дикого типа может быть замещена лидерной последовательностью активатора тканевого плазминогена человека (TPA) или бета-глюкуронидазы мыши.
[00058] В данном описании раскрыты определенные связывающие молекулы, или их антигенсвязывающие фрагменты, варианты или их производные. Если конкретно, в отношении полноразмерного антитела, термин «связывающая молекула» включает полноразмерные антитела, а также антигенсвязывающие субъединицы, фрагменты, варианты, аналоги или производные таких антител, например, сконструированные молекулы антитела или фрагменты, которые связываются с антигеном аналогичной молекулы антитела, но которые используют различный каркас.
[00059] Используемый в данном описании, термин «связывающая молекула» относится в широком смысле к молекуле, которая специфически связывается с рецептором, например, эпитопом или антигенной детерминантой. Как описано далее в данном описании, связывающая молекула может содержать один или более «антигенсвязывающих доменов», описанных в данной заявке. Неограничивающий пример связывающей молекулы, представляет собой антитело или его фрагмент, который сохраняет антигенспецифическое связывание.
[00060] Используемые в данном описании термины «связывающий домен» или «антигенсвязывающий домен» относятся к области связывания молекулы, которая является необходимой и достаточной, для специфического связывания с эпитопом. Например, «Fv», например, вариабельная тяжелая цепь и вариабельная легкая цепь антитела, либо в виде двух отдельных полипептидных субъединиц, либо в виде одной цепи, считаются «связывающим доменом». Другие связывающие домены включают, без ограничения, вариабельную тяжелую цепь (VHH) антител, полученную из видов верблюжьих или шесть, областей, определяющих комплементарность иммуноглобулина (CDR), экспрессированных в каркасе фибронектина. «Связывающая молекула», описанная в данном документе, может содержать один, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать или более «антигенсвязывающих доменов».
[00061] Термины «антитело» и «иммуноглобулин» могут быть использованы в данном документе взаимозаменяемо. Антитело (или фрагмент, вариант, или его производное, описанные в данном документе) содержит по меньшей мере вариабельную область тяжелой цепи (для видов верблюжьих) или по меньшей мере вариабельную область тяжелой цепи и легкой цепи. Основные структуры иммуноглобулина в системах позвоночных относительно хорошо изучены. См., например, Harlow et al., Antibodies: A Laboratory Manual. (Cold Spring Harbor Laboratory Press, 2nd ed. 1988). Если не указано иное, термин «антитело» охватывает все, начиная от небольшого антигенсвязывающего фрагмента антитела к полноразмерным антителам, например, антителам IgG, которые содержат две полных тяжелых цепи и две полных легкие цепи, антителам IgA, которые содержат четыре полных тяжелые цепи и четыре полных легких цепей и, необязательно, содержат J цепь и/или секреторный компонент, или антителам IgM, которые содержат десять или двенадцать полных тяжелых цепей и десять или двенадцать полных легких цепей и, необязательно, содержат J цепь.
[00062] Как будет обсуждено более подробно ниже, термин «иммуноглобулин» включает различные широкие классы полипептидов, которые можно отличить биохимически. Специалисты в данной области техники будет понятно, что тяжелые цепи классифицируются как гамма, мю, альфа, дельта, эпсилон (γ, μ, α, δ, ε) с некоторыми подклассами среди них (например, γ1-γ4 или α1-α2). Природа этой цепи, которая определяет «класс» антитела как IgG, IgM, IgA IgG или IgE, соответственно. Подклассы иммуноглобулинов (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, и т.д., хорошо охарактеризованы и, как известно, обладают функциональной специализацией. Модифицированные версии каждого из этих классов и изотипов легко различимы специалисту в данной области техники в свете данного описания, и, соответственно, находятся в пределах объема данного изобретения.
[00063] Легкие цепи классифицируются как каппа или лямбда (κ, λ). Каждый класс тяжелой цепи может быть связан либо с легкой цепью каппа, либо с легкой цепью лямбда. В общем, легкие и тяжелые цепи ковалентно связаны друг с другом, а «хвостовые» участки двух тяжелых цепей связаны друг с другом посредством ковалентных дисульфидных связей или нековалентных связей, когда иммуноглобулины генерируются гибридомами, В клетками или генетически сконструированными клетками-хозяевами. В тяжелой цепи, аминокислотные последовательности начинаются от N-конца на разветвленных концах Y конфигурации к С-концу в нижней части каждой цепи. Базовая структура некоторых антител, например, антитела IgG, содержит две субъединицы тяжелой цепи и две субъединицы легкой цепи, ковалентно соединенных с помощью дисульфидных связей с образованием «Y» структуры, также называемой в данном документе как структура «H2L2».
[00064] И легкие и тяжелые цепи разделены на области структурной и функциональной гомологии. Термины «константные» и «вариабельные» используются функционально. В связи с этим следует иметь в виду, что вариабельные области как вариабельных легких (VL), так и вариабельных тяжелых (VH) участков цепей определяют распознавание и специфичность антигена. И наоборот, константные области легкой цепи (CL) и тяжелой цепи (CH1, СН2 или СН3) придают биологические свойства, такие как секреция, трансплацентарная подвижность, связывание Fc-рецептора, связывание комплемента и тому подобное. Считается, что нумерации константных областей возрастает, поскольку они становятся более дистальны от сайта связывания антигена или амино-конца антитела. N-концевой участок представляет собой вариабельную область, а С-концевой участок представляет собой константную область; СН3 (или СН4 в случае IgM), а домены CL фактически содержат карбокси-конец тяжелой и легкой цепи соответственно.
[00065] Как было указано выше, вариабельная область (то есть, «связывающий домен») позволяет связывающей молекуле избирательно распознавать и специфически связывать эпитопы на антигенах. То есть, область VL и область VH, или подмножество областей, определяющих комплементарность (CDR), связывающей молекулы, например, антитела, объединены с образованием вариабельной области, которая определяет трехмерный сайт связывания антигена. Более конкретно, сайт связывания антигена определяются три CDR, на каждой из цепей VH и VL. Некоторые антитела образуют более крупные структуры. Так, например, IgA, может образовать молекулу, которая содержит две единицы H2L2, J цепь, и секреторный компонент, все ковалентно соединенные через дисульфидные связи, а IgM, может образовывать пентамерную или гексамерную молекулу, которая содержит пять или шесть единиц H2L2 и необязательно J цепь, ковалентно соединенные с помощью дисульфидных связей.
[00066] Шесть «областей, определяющих комплементарность» или «CDR,» присутствующие в антигенсвязывающем домене антитела представляют собой короткие, несмежные последовательности аминокислот, которые специально расположены, чтобы сформировать связывающий домен, когда антитело принимает свою трехмерную конфигурацию, в водной окружающей обстановке. Остальная часть аминокислот в связывающем домене, именуемые «каркасные» области, демонстрируют меньшую межмолекулярную вариабельность. Каркасные области в значительной степени принимают β-складчатую конформацию и CDR, образуют петли, соединяющие и в некоторых случаях образуют часть данной β-складчатой структуры. Таким образом, каркасные области действуют таким образом, чтобы сформировать каркас, который обеспечивает позиционирование CDR в правильной ориентации посредством межцепочечных, нековалентных взаимодействий. Связывающий домен, образованный расположенными CDR, определяет поверхность, комплементарную эпитопу на иммунореактивном антигене. Эта комплементарная поверхность способствует нековалентному связыванию антитела с его родственным эпитопом. Аминокислоты, входящие в составе CDR, и каркасных областей, соответственно, могут быть легко идентифицированы для любой тяжелой или легкой цепи вариабельной области рядовым специалистом в данной области техники, так как они были определены различными способами (см., "Sequences of Proteins of Immunological Interest," Kabat, E., et al., U.S. Department of Health and Human Services, (1983); and Chothia and Lesk, J. Mol. Biol., 796:901-917 (1987), которые целиком включены в данный документ посредством ссылки).
[00067] В случае, когда существует два или более определений термина, которые используются и/или приняты в данной области техники, определение термина, используемого в данном описании, включают все такие значения, если явно не указано иное. Конкретным примером является использование термина «области, определяющие комплементарность» («CDR»), чтобы описать несмежные антиген объединяющие сайты, найденных в вариабельной области обоих тяжелых и легких цепей полипептидов. Эти конкретные области были описаны, например, в Kabat et al., U.S. Dept. of Health and Human Services, "Sequences of Proteins of Immunological Interest" (1983) и by Chothia et al., J. Mol. Biol. 196:901-917 (1987), которые включены в данное описание в качестве ссылки. Определения Kabat и Chothia включают перекрывание или подмножество аминокислот при сравнении друг против друга. Тем не менее, применение определения (или других определений, известным специалистам в данной области техники), чтобы обратиться к CDR антитела или его варианту предназначен, чтобы быть в пределах объема этого термина, как определено и используется данном документе, если не указано иное. Соответствующие аминокислоты, которые охватывают CDR, как определено каждой из приведенных выше цитируемых ссылок, приведены ниже в таблице 1 в качестве сравнения. Количества точных аминокислот, которые охватывает конкретный CDR будет варьировать в зависимости от последовательности и размера CDR. Специалисты в данной области техники может определить, какие обычно аминокислоты содержит конкретный CDR с учетом аминокислотной последовательности вариабельной области антитела.
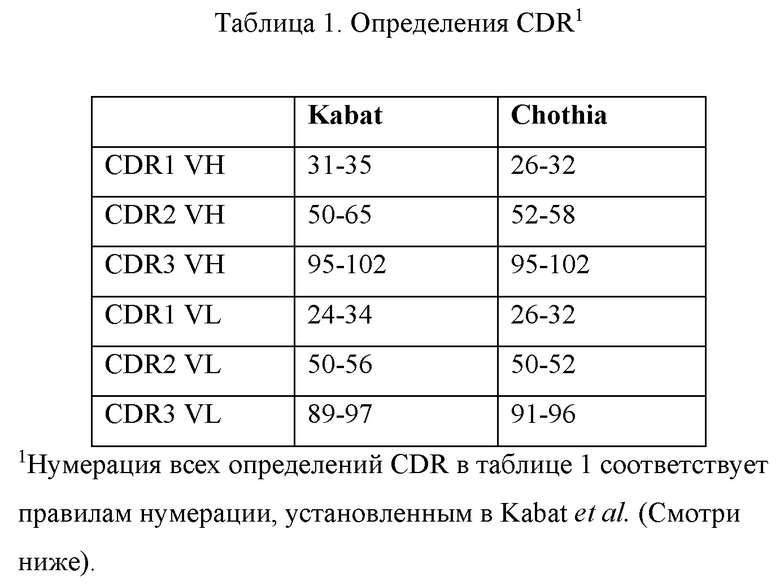
[00068] Вариабельные области иммуноглобулина также могут быть проанализированы с использованием информационной системы IMGT (www://imgt.cines.fr/) (EVIGT®/V-Quest) для идентификации сегментов вариабельной области, в том числе CDR. См., например, Brochet, X. et al., Nucl. Acids Res. 36:W503-508 (2008).
[00069] В Kabat et al. также определена система нумерации для последовательностей вариабельной области, которая применима к любому антителу. Специалист в данной области техники может однозначно присвоить эту систему «нумерации Kabat» любой последовательности вариабельной области, без опоры на любые экспериментальные данные, помимо самой последовательности. Использованная в данном описании «нумерация Kabat» относится к системе нумерации, предложенной в Kabat et al., U.S. Dept. of Health and Human Services, "Sequence of Proteins of Immunological Interest" (1983). Однако, если использование системы нумерации Kabat явно не отмечено, последовательная нумерация используется для всех аминокислотных последовательностей в данном описании.
[00070] Связывающие молекулы, например, антитела или антигенсвязывающие фрагменты, варианты или их производные, включают, но не ограничиваются ими, поликлональные, моноклональные, гуманизированные, человеческие или химерные антитела, одноцепочечные антитела, эпитоп-связывающие фрагменты, например, Fab, Fab' и F(ab')2, Fd, Fvs, одноцепочечные Fvs (scFv), одноцепочечные антитела, дисульфидсвязанные Fvs (sdFv), фрагменты, содержащие либо область VL, либо VH, а фрагменты получают путем библиотеки экспрессии Fab. Молекулы ScFv известны в данной области техники и описаны, например, в патенте США №5892019. Молекулы иммуноглобулина или антитела, охватываемые данным описанием, могут быть любого типа (например, IgG, IgE, IgM, IgD, IgA и IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса молекулы иммуноглобулина.
[00071] Под термином «специфически связывается» обычно понимают, что связывающая молекула, например, антитело или фрагмент, вариант, или его производное связывается с эпитопом через его антигенсвязывающий домен, а также о том, что связывание влечет за собой некоторую комплементарности между антигенсвязывающим доменом и эпитоп .Согласно этому определению, связывающая молекула называется «специфически связывающей» с эпитопом, когда она связывается с этим эпитопом, с помощью ее антигенсвязывающего домена более легко, чем она связывалась бы со случайным, несвязанным эпитопом. Термин «специфичность» используется в данном документе, чтобы квалифицировать относительное аффинность, с помощью которой определенная связывающая молекула связывается с определенным эпитопом. Так, например, можно считать, что связывающая молекула «А» имеет более высокую специфичность для данного эпитопа, чем связующая молекула «В», или связывающая молекула «А», можно сказать, связываться с эпитопом «С» с более высокой специфичностью, чем она это делает с соответствующим эпитопом «D».
[00072] Можно сказать, что связывающая молекула, например, антитело или его фрагмент, вариант, или производное описанные в данном документе, связывает антиген- мишень с константой диссоциации (k(off)) меньшей или равной 5×10-2 сек-1, 10-2 сек-1, 5×10-3 сек-1, 10-3 сек-1, 5×10-4 сек-1, 10-4 сек-1, 5×10-5 сек-1 или 10-5 сек-1 5×10-6 сек-1, 10-6 сек-1, 5×10-7 сек-1 или 10-7 сек-1.
[00073] Можно сказать, что связывающая молекула, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное описанные в данном документе, связывает антиген-мишень с константой ассоциации (k(on)) большей или равной 103 М-1 сек-1, 5×103 М-1 сек-1, 104 М-1 сек-1, 5×104 М-1 сек-1, 105 М-1 сек-1, 5×105 М-1 сек-1, 106 М-1 сек-1 или 5×106 М-1 сек-1, или 107 М-1 сек-1.
[00074] Можно сказать, что связывающая молекула, например, антитело или его фрагмент, вариант, или его производное, конкурентно ингибирует связывание эталонное антитело или его антигенсвязывающий фрагмента к данному эпитопу, если оно преимущественно связывается с этим эпитопом в той степени, что блокирует, до некоторой степень, связывание эталонного антитела или его антигенсвязывающего фрагмента с эпитопом. Конкурентное ингибирование может быть определено любым способом, известным в данной области техники, например, конкурентным ИФА. Можно сказать, что связывающая молекула, конкурентно ингибирует за связывание контрольного антитела или его антигенсвязывающего фрагмента с данным эпитопом на по меньшей мере 90%, по меньшей мере 80%, по меньшей мере 70%, по меньшей мере 60% или по меньшей мере 50%.
[00075] Использованный в данном описании, термин «аффинность» относится к измерению силы связывания отдельного эпитопа с одним или более связывающими доменами, например, молекулы иммуноглобулина. См., например, Harlow et al., Antibodies: A Laboratory Manual., (Cold Spring Harbor Laboratory Press, 2nd ed. 1988) на станицах 27-28. Использованный в данном описании, термин «авидность» относится к общей стабильности комплекса между популяциями связывающих доменов и антигеном. См., например, Harlow на страницах 29-34. Авидность связана как с аффинностью отдельных связывающих доменов в популяции с конкретными эпитопами, так и с валентностью иммуноглобулинов и антигена. Так, например, взаимодействие между двухвалентным моноклональным антителом и антигеном с высоко повторяющейся структурой эпитопа, такой как полимер, имело бы высокую авидность. Взаимодействие между двухвалентным моноклональным антителом с рецептором, присутствующим при высокой плотности на клеточной поверхности также будет обладать высокой авидностью.
[00076] Связывание молекул или антигенсвязывающие фрагментом, вариантов или их производных, описанных в данном описании, также могут быть описаны или определены с точки зрения их перекрестной реактивности. Использованный в данном описании, термин «перекрестная реактивность» относится к способности связывающей молекулы, например, антитела или его фрагмента, варианта или производного, специфичного для одного антигена, вступать в реакцию со вторым антигеном; мера связанности между двумя различными антигенными веществами. Таким образом, связывающая молекула является перекрестно реактивной, если она связывается с эпитопом, отличным от того, что индуцирует ее формирования. Перекрестно реактивный эпитоп обычно содержит многие из тех же дополнительных структурных особенностей, как индуцирующий эпитоп, а в некоторых случаях, может на самом деле подходит лучше, чем оригинал.
[00077] Связывающая молекула, например, антитело или его фрагмент, вариант, или производное могут быть также описаны или определены с точки зрения их аффинности связывания с антигеном. Например, связывающая молекула может связываться с антигеном с константой диссоциации или KD не более, чем 5×10-2 М, 10-2 М, 5×10-3 М, 10-3 М, 5×10-4 М, 10-4 М, 5×10-5 М, 10-5 М, 5×10-6 М, 10-6 М, 5×10-7 М, 10-7 М, 5×10-8 М, 10-8 М, 5×10-9 М, 10-9 М, 5×10-10 М, 10-10 M, 5×10-11 М, 10-11 М, 5×10-12 М, 10-12 М, 5×10-13 М, 10-13 М, 5×10-14 М, 10-14 М, 5×10-15 М или 10-15 М.
[00078] Фрагменты антител, включая одноцепочечные антитела или другие связывающие домены могут существовать по отдельности или в комбинации с одним или более из следующих компонентов: шарнирная область, домены CH1, СН2, СН3 или СН4, цепь J или секреторный компонент. Кроме того, включены антигенсвязывающие фрагменты, которые могут содержать любую комбинацию из вариабельной области(ей) с одним или более компонентами из шарнирной области, доменов CH1, СН2, СН3, СН4, цепи J или секреторного компонента. Связывание молекулы, например, антитела или антигенсвязывающие фрагменты могут быть любого животного происхождения, включая птиц и млекопитающих. Антитела могут быть получены из антител человека, мыши, осла, кролика, козы, морской свинки, верблюда, ламы, лошади или курицы. В другом варианте осуществления вариабельной область может происходит от хрящевых рыб (например, от акул). Используемый в данном описании термин антитела «человека» включают антитела, имеющие аминокислотную последовательность иммуноглобулина человека, и включают антитела, выделенные из библиотек иммуноглобулинов человека или из животных, трансгенных по одному или более иммуноглобулинам человека и может в некоторых случаях экспрессировать эндогенные иммуноглобулины, а некоторые нет, как описанные ниже и, например, в патенте США. №5939598 от Kucherlapati et al.
[00079] Используемый в данном описании термин «субъединица тяжелой цепи» включает аминокислотные последовательности, полученные из тяжелой цепи иммуноглобулина, связывающей молекулы, например, антитела, содержащего субъединицу тяжелой цепи, содержащую по меньшей мере одну из: область VH, СН1 домен, шарнирный домен (например, верхняя, средняя и/или нижняя шарнирная область), домен СН2, домен СН3, домен СН4, или их вариант или фрагмент. Например, связывающие молекулы, например, антитело или его фрагмент, вариант, или производное может содержать, в дополнение к области VH, домен СН1; домен СН1, шарнир и домен СН2; домен СН1 и домен СН3; домен СН1, шарнир и домен СН3 или домен СН1, шарнирный домен, домен СН2 и домен СН3. В определенных аспектах связывающая молекула, например, антитело или его фрагмент, вариант, или производное может содержать, в дополнение к VH области, домен СН3 и домен СН4 или домен СН3, домен СН4 и цепь J. Кроме того, связывающая молекула для применения в данном документе может не иметь частей константной области, например, всего или части домена СН2. Это будет понятно любому специалисту в данной области техники, что эти домены (например, субъединица тяжелой цепи) может быть изменена таким образом, что они различаются по аминокислотной последовательности относительно исходной молекулы иммуноглобулина.
[00080] Субъединица тяжелой цепи связывающей молекулы, например, антитела или его фрагмента, могут содержать домены, полученные из различных молекул иммуноглобулина. Например, субъединица тяжелой цепи полипептида может содержать домен СН1, полученный из молекулы IgG1 и шарнирную область, полученную из молекулы IgG3. В другом примере субъединица тяжелой цепи может содержать шарнирную область, полученную, частично, из молекулы IgG1 и, частично, из молекулы IgG3. В другом примере субъединица тяжелой цепи может содержать химерную шарнирную область, полученную, частично, из молекулы IgG1 и, частично, из молекулы IgG4.
[00081] Используемый в данном описании, термин «субъединица легкой цепи» включает аминокислотные последовательности, полученные из легкой цепи иммуноглобулина. Субъединица легкой цепи содержит по меньшей мере один из доменов VL или CL (например, Сκ или Сλ).
[00082] Связывающие молекулы, например, антитела или их антигенсвязывающие фрагменты, варианты или производные могут быть описаны или определены в терминах эпитопа(ов) или части(ей) антигена, которые они распознают или специфически связывают. Часть антигена-мишени, которая специфический взаимодействует с антигенсвязывающим доменом антитела представляет собой «эпитоп» или «антигенную детерминанту». Антиген-мишень может содержать один эпитоп или не менее двух эпитопов, и может содержать любое количество эпитопов, в зависимости от размера, конформации и тип антигена.
[00083] Как было указано ранее, структуры субъединиц и трехмерные конфигурации константных областей различных классов иммуноглобулинов хорошо известны. Использованный в данном описании термин «область VH» включает аминоконцевую вариабельную область тяжелой цепи иммуноглобулина, а термин «домен СН1» включает первый (наиболее аминоконцевой) домен константной области тяжелой цепи иммуноглобулина. Домен СН1 примыкает к области VH и является аминоконцевым к шарнирной области типичной молекулы тяжелой цепи иммуноглобулина.
[00084] Используемый в данном описании термин «домен СН2» включает часть тяжелой цепной молекулы, которая проходит, например, от около 244 аминокислоты до аминокислоты 360 антитела IgG с использованием обычных схем нумерации (аминокислоты 244 до 360, система нумерации Kabat; и аминокислоты 231-340), система нумерации EU; см. Kabat ЕА et al. op. cit. Домен СН3 начинается от домена СН2 к С-концу молекулы IgG и содержит приблизительно 108 аминокислот. Определенные классы иммуноглобулинов, например, IgM, дополнительно содержат область СН4.
[00085] Использованный в данном описании термин «шарнирная область» включает часть тяжелой цепи молекулы, которая соединяет домен СН1 с доменом СН2. Эта шарнирная область содержит около 25 аминокислот и является гибкой, позволяя, таким образом, двум N-концевым антигенсвязывающим областям двигаться независимо друг от друга.
[00086] Используемый в данном документе термин «дисульфидную связь» включает ковалентную связь, образованную между двумя атомами серы. Аминокислота цистеин содержит тиольную группу, которая может образовывать дисульфидную связь или мостик со второй тиольной группой. В определенных молекулах IgG области СН1 и CL связаны дисульфидной связью, а две тяжелые цепи связаны двумя дисульфидными связями в положениях, соответствующими 239 и 242 с использованием системы нумерации Kabat (позиция 226 или 229, системы нумерации EU).
[00087] Используемый в данном описании термин «гибридное антитело» означает антитело, в котором иммунореактивная область или сайт получен или происходит из первого вида, а константную область (которая может быть интактной, частичной или модифицированной) получают из второго вида. В некоторых вариантах осуществления целевая область связывания или сайт будут происходить из источника, отличного от человека (например, мыши или примата), а константная областью является человеческой.
[00088] Термины «мультиспецифическое антитело, или «биспецифическое антитело» относятся к антителу, которое имеет связывающие домены для двух или более различных эпитопов в пределах одной молекулы антитела. Другие связывающие молекулы в дополнении к канонической структуре антитела может быть сконструированы с двойной специфичностью связывания. Связывание эпитопа биспецифическими или мультиспецифическими антителами может быть одновременным или последовательным. Триомы и гибридные гибридомы являются двумя примерами клеточных линий, которые могут секретируют биспецифические антитела. Биспецифические антитела также могут быть сконструированы с помощью рекомбинантных средств. ( and Heiss, Future Oncol. (5:1387-94 (2010); Mabry and Snavely, IDrugs. 13:543-9 (2010)). Биспецифическое антитело может также представлять собой диатело.
and Heiss, Future Oncol. (5:1387-94 (2010); Mabry and Snavely, IDrugs. 13:543-9 (2010)). Биспецифическое антитело может также представлять собой диатело.
[00089] Используемый в данном описании термин «сконструированное антитело» означает антитело, в котором вариабельна области или тяжелой и легкой цепи или обеих цепей изменялась посредством по меньшей мере частичной замены одной или более аминокислот, либо в CDR, либо в каркасных областях. В определенных аспектах целые CDR, от антитела известной специфичности может быть привит к каркасным областям гетерологичного антитела. Хотя альтернативные CDR, могут быть получены из антитела того же класса или подкласса даже в качестве антитела, из которого получены каркасные участки, CDR могут быть также получены из антитела другого класса, например, из антитела от другого вида. Сконструированное антитело, в котором одна или более «донорная» CDR из антитела, не являющегося антителом человека, известной специфичности привиты к каркасной области тяжелой или легкой цепи человека упоминается в данном описании как «гуманизированное антитело». В некоторых аспектах, не все CDR, заменяются на полные CDR из донорной вариабельной области, и все же антигенсвязывающий потенциал донора по-прежнему может быть передан в вариабельные области реципиентов. Принимая во внимание объяснения изложенные, например, в патентах США №5585089, 5693761, 5693762 и 6180370, это будет понятно в пределах компетенции специалистов в данной области техники, либо путем проведения рутинных экспериментов или проверки методом проб и ошибок для получения функционального сконструированного или гуманизированного антитела.
[00090] Используемый в данном описании термин «сконструированное» включает манипулирование нуклеотидными или полипептидными молекулами синтетическими способами (например, с помощью рекомбинантных методик, пептидного синтеза in vitro, путем ферментативного или химического связывания пептидов или некоторой комбинации этих методов).
[00091] Использованные в данном описании, термины «связанный», «слитый» или «слияние» или другие грамматические эквиваленты могут быть использованы взаимозаменяемо. Эти термины относятся к соединению друг с другом более двух элементов или компонентов, любыми средствами, в том числе химической конъюгации или рекомбинантными способами. «Слитый в рамке считывания» относится к соединению двух или более полинуклеотидных открытых рамок считывания (ОРС) с образованием непрерывной более длинной ОРС, таким образом, что поддерживается транслируемая рамка считывания исходных ОРС. Таким образом, рекомбинантный слитый белок представляет собой один белок, содержащий два или более сегментов, которые соответствуют полипептидам, кодируемым исходными ОРС (сегменты которых обычно не соединенны в природе.) Несмотря на то, что рамка считывания, таким образом, производится непрерывно в течение слившихся сегментов, сегменты могут быть физически или пространственно разделены, например, последовательности линкера в рамке считывания. Так, например, полинуклеотиды, кодирующие CDR вариабельной области иммуноглобулина могут быть слиты в рамке считывания, но быть разделены с помощью полинуклеотида, кодирующего, по меньшей мере одну область каркаса иммуноглобулина или дополнительные области CDR, а также «слитые» CDR являются ко-транслированными как часть непрерывного полипептида.
[00092] В контексте полипептидов, «линейная последовательность» или «последовательность» представляет собой порядок аминокислот в полипептиде в направлении от аминоконца до карбоксильного конца, в котором аминокислоты, которые граничат друг с другом в последовательности является смежным в первичной структуре полипептида. Часть полипептида, которая является «аминоконцевой» или «N-концевой» к другой части полипептида является той частью, которая располагается раньше в последовательной полипептидной цепи. Аналогично, часть полипептида, которая является «карбоксиконцевой» или «С-концевой» к другой части полипептида является той частью, которая располагается позже в последовательной полипептидной цепи. Например, в типичном антителе, вариабельная область является «N-концевой» к константной области, а константная область является «С-концевой» к вариабельной области.
[00093] Термин «экспрессия», используемый в данном описании, относится к способу, с помощью которого ген производит биохимическое вещество, например, полипептид. Процесс включает в себя любое проявление функционального присутствие гена в клетке, включая, без ограничения, нокдаун гена, а также временную экспрессию и стабильную экспрессию. Он включает, без ограничения транскрипции гена в матричную РНК (мРНК), и трансляцию таких мРНК в полипептид(ы). Если конечный желаемый продукт является биохимическим, экспрессия включает создание биохимических веществ и каких-либо предшественников. Экспрессия гена производит «генный продукт». Используемый в данном описании продукт гена может представлять собой или нуклеиновую кислоту, например, матричную РНК полученную путем транскрипции гена, или полипептид, который транслируется из транскрипта. Генные продукты, описанные в данном документе, дополнительно включают нуклеиновые кислоты с посттранскрипционными модификациями, например, полиаденилирование, или полипептиды с посттрансляционными модификациями, например, метилирование, гликозилирование, добавление липидов, ассоциацию с другими белковыми субъединицами, протеолитическое расщепление, и тому подобное.
[00094] Использованный в данном описании термин «связывающая молекула против SEMA4D» относится к молекуле, которая специфически связывается с SEMA4D, например, антителу или его антигенсвязывающему фрагменту, варианту или производному. Если конкретно со ссылкой на полноразмерное антитело, такое как встречающееся в природе антитело, термин «антитело против SEMA4D» включает полноразмерные антитела, а также антигенсвязывающие фрагменты, а также антигенсвязывающие фрагменты, варианты, аналоги или производные, таких антител, например, природные антитела или молекулы иммуноглобулина или сконструированные молекулы антитела или фрагменты, которые связываются с антигеном способом, аналогичным с таковым у молекул антител.
[00095] Такие термины, как «лечение» или «процесс лечения» или «лечить» или «облегчение», или «улучшать» относится к терапевтическим мерам, которые излечивают, замедляют, уменьшают симптомы, и/или останавливают или замедляют прогрессирование существующего диагноза патологического состояния или расстройства. Такие термины, как «предотвратить», «предотвращение», «избегание», «сдерживание» и т.п. относятся к профилактическим или превентивным мерам, которые предотвращают развитие недиагностированного целевого патологического состояния или расстройства. Таким образом, «тот, кто нуждается в лечении» может включать тех, кто уже имеет расстройство; склонны иметь расстройство; и тех, у кого расстройство должно быть предотвращено. Используемая в данном документе фраза, такая как «субъект, который будет иметь пользу от терапии» и «животные, нуждающиеся в лечении» включает субъекты, такие, как субъекты-млекопитающие, которые будут иметь пользу от введения терапии, как описано в данном документе.
[00096] Термин «терапевтически эффективное количество» относится к количеству антитела, полипептида, полинуклеотида, небольшой органической молекулы, или другого лекарственного средства, эффективного для «лечения» заболевания или расстройства у субъекта или млекопитающего.
[00097] Под термином «субъект» или «индивид», или «животное», или «пациент», или «млекопитающее» подразумевается любой субъект, в частности млекопитающее, для которого желателен диагноз, прогноз, или терапия. Субъекты-млекопитающие включают людей, домашних животных, сельскохозяйственных животных, и животных, содержащихся в зоопарках, спортивных животных или животных-спутников, таких как собаки, кошки, морские свинки, кролики, крысы, мыши, лошади, свиньи, коровы, медведи, и так далее.
Описание целевого полипептида - SEMA4D
[00098] Использованные в данном описании термины «семафорин-4D», «SEMA4D» и «полипептид SEMA4D» используются взаимозаменяемо, так же как «SEMA4D» и «Sema4D». В некоторых вариантах осуществления SEMA4D экспрессируется на поверхности или секретируется клеткой. В другом варианте осуществления SEMA4D является связанным с мембраной. В другом варианте осуществления SEMA4D является растворимым, например, sSEMA4D. В другом варианте осуществления SEMA4D может включать полноразмерный SEMA4D или его фрагмент, или вариант полипептида SEMA4D, причем фрагмент SEMA4D или вариант полипептида SEMA4D сохраняет некоторые или все функциональные свойства полноразмерного SEMA4D.
[00099] Полноразмерный белок SEMA4D человека представляет собой гомодимер трансмембранного белка, состоящий из двух полипептидных цепей, размером 150 к Да. SEMA4D принадлежит к семейству семафоринов рецепторов клеточной поверхности и также упоминается как CD100. Оба SEMA4D/Sema4D человека и мыши могут быть протеолитически расщеплены из их трансмембранной формы для создания 120 кДа растворимых форм, что приведет к образованию двух изоформ Sema4D (Kumanogoh et al., J. Cell Science 116:3464 (2003)). Семафорины состоят из растворимых и мембраносвязанных белков, которые первоначально были определены как факторы аксонального наведения, которые играют важную роль в установлении точных соединений между нейронами и их соответствующей мишенью. Структурно считающийся семафорином IV класса, SEMA4D состоит из сигнальной аминоконцевой последовательности с расположенным далее характерным доменом «Sema», который содержит 17 остатков цистеина, lg-подобный домен, лизин-богатая вытягивающая последовательность, гидрофобная трансмембранная область и цитоплазматический хвост.
[000100] Полипептид SEMA4D содержит сигнальную последовательность из около 13 аминокислот, за которой следует домен семафорина из около 512 аминокислот, иммуноглобулин-подобный (Ig-подобный) домен из около 65 аминокислот, лизин-богатая вытягивающая последовательность из 104 аминокислот, гидрофобная трансмембранная область из около 19 аминокислот и цитоплазматический хвост из 110 аминокислот. Консенсусный сайт для фосфорилирования тирозина в цитоплазматическом хвосте поддерживает предсказанную ассоциацию SEMA4D с тирозинкиназой (Schlossman et al., Eds. (1995) Leucocyte Typing V (Oxford University Press, Oxford).
[000101] SEMA4D, как известно, имеют по меньшей мере три функциональных рецептора, плексин-В1, плексин-В2 и CD72. Плексин-В1, экспрессируется в нелимфоидных тканях, и демонстрирует высокую аффинность (1 нМ) с рецептором SEMA4D (Tamagnone et al., Cell 99:71-80 (1999)). Стимуляция при помощи SEMA4D сигналинга плексина-В1 продемонстрировала индукцию коллапс конуса роста нейронов, и индуцирует процесс расширения коллапса и апоптоз олигодендроцитов (Giraudon et al., J. Immunol. 172:1246-1255 (2004); Giraudon et al., NeuroMolecular Med. 7:207-216 (2005)). После связывания с SEMA4D, сигналинг плексина-В1 опосредует инактивацию R-Ras, что приводит к уменьшению интегрин-опосредованного прикрепления к внеклеточному матриксу, а также к активации RhoA, что приводит к коллапсу клеток путем реорганизации цитоскелета (Kruger et al., Nature Rev. Mol. Cell Biol. 6:789-800 (2005); Pasterkamp, TRENDS in Cell Biology 15:61-64 (2005)). Плексин-В2 имеет промежуточную аффинность с SEMA4D и недавнее сообщение указывает на то, что плексин-В2 экспрессируется на кератиноцитах и активирует SEMA4D-позитивные γδ Т-клетки, для способствования эпителиальной репарации (Witherden et al., Immunity 37:314-25 (2012)).
[000102] В лимфоидной ткани, CD72 используются в качестве рецептора SEMA4D с низкой аффинностью (300 нМ) (Kumanogoh et al., Immunity 13:621-631 (2000)). В-клетки и антигенпрезентирующие клетки (АРС) экспрессируют CD72, а антитело против CD72 имеет многие из тех же эффектов, что и sSEMA4D, такие как усиление CD40-индуцированных В-клеточных ответов и шеддинг CD23 В-клетками. CD72 как полагают, действует как негативный регулятор В-клеточных ответов посредством рекрутинга тирозинфосфатазы SHP-1, которая может ассоциировать с многими ингибиторными рецепторами. Взаимодействие SEMA4D с CD72 приводит к диссоциации SHP-1, и потере этого отрицательного сигнала активации. Было показано, что SEMA4D способствует стимуляции Т-клеток и агрегации и выживанию клеток В in vitro. Добавление SEMA4D-экспрессирующих клеток или sSEMA4D усиливает CD40-индуцированную пролиферацию В-клеток и продукцию иммуноглобулина in vitro, и ускоряется ответы антител in vivo (Ishida et al., Inter. Immunol. 15:1027-1034 (2003); Kumanogoh и H. Kukutani, Trends in Immunol. 22:670-676 (2001)). sSEMA4D усиливает CD40 индуцированное созревание ДК, в том числе увеличение активности костимуляторных молекул и повышенной секреции IL-12. Кроме того, sSEMA4D может ингибировать миграцию иммунных клеток, которое может быть отменено путем добавления блокирующих антител мыши против SEMA4D (Elhabazi et al., J. Immunol. 166:4341-4347 (2001); Delaire et al., J. Immunol. 166:4348-4354 (2001)).
[000103] Sema4D экспрессируется на высоком уровне в лимфоидных органах, в том числе селезенке, тимусе и лимфатических узлах, и в органах, не являющихся лимфоидными, таких как мозг, сердце и почки. В лимфоидных органах, Sema4D обильно экспрессируются на покоящихся Т-клетках, но лишь слабо экспрессируются на покоящихся В-клеток и антиген-презентирующих клетках (АРС), таких как дендритные клетки (DC).
[000104] Клеточная активации увеличивает поверхностную экспрессию SEMA4D, а также генерации растворимого SEMA4D (sSEMA4D). Паттерн экспрессии SEMA4D позволяет предположить, что он играет важную физиологическую, а также патологическую роль в иммунной системе. Было показано, что SEMA4D способствует активации, агрегации и выживанию В-клеток; повышению CD40-индуцированной пролиферации и выработки антител; повышению ответа антител на зависимые Т-клеточные антигены; увеличению пролиферации Т-клеток; повышению созреванию дендритных клеток и способности стимулировать Т-клетки; и непосредственно участвует в демиелинизации и дегенерации аксонов (Shi et al., Immunity 13:633-642 (2000); Kumanogoh et al., J. Immunol. 169:1175-1181 (2002) и Watanabe et al., J. Immunol. 167:4321-4328 (2001)).
Антитело против SEMA4D человека
[000105] В данном изобретении предложена связывающая молекула против SEMA4D, например, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное с вариабельной областью тяжелой цепи (VH) и вариабельной областью легкой цепи (VL) связанными с, или идентичными аминокислотным последовательностям, содержащим VH и VL SEQ ID NO: 1 и SEQ ID NO: 5, соответственно. В определенных аспектах предложенная связывающая молекула, например, антитело или его антигенсвязывающий фрагмент, вариант, или его производное, является полностью человеческим.
[000106] В определенных аспектах, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или его производное, представленная в данном документе, имеет область VH и VL, содержащую аминокислотные последовательности, которые имеют по меньшей мере около 80%, около 85%, около 88%, около 89%, около 90%, около 91%, около 92%, около 93%, около 94%, около 95%, около 96%, около 97%, около 98%, около 99% или 100% идентичности областям VH и VL эталонной молекулы антитела против SEMA4D с областями VH и VL, содержащими аминокислотные последовательности SEQ ID NO: 1 и SEQ ID NO: 5, соответственно.
[000107] В определенных аспектах связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное может ингибировать взаимодействие SEMA4D с его рецептором, например, плексином-В1, плексином-В2 или CD72. В определенных аспектах связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное может ингибировать SEMA4D-опосредованную трансдукцию сигнала плексина-В1.
[000108] В определенных аспектах, связывающие молекулы против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант или производное, конкурентно ингибирует эталонное антитело, содержащее вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO: 1 и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO: 5 от связывания с SEMA4D. В некоторых аспектах, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант или производное связывается с тем же эпитопом SEMA4D, что и эталонное антитело, содержащее VH, содержащую аминокислотную последовательность SEQ ID NO: 1 и VL, содержащую аминокислотную последовательность SEQ ID NO: 5. В определенных аспектах VH связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта или производного содержит три области, определяющие комплементарность (CDR) HCDR1, HCDR2 и HCDR3, a VL содержит три CDR, LCDR1, LCDR2, LCDR3, причем CDR, содержат аминокислотные последовательности SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно, за исключением, по меньшей мере, одной, двух, трех, четырех, пяти или шести одиночных консервативных аминокислотных замен в одном или более CDR. В определенных аспектах CDR содержат аминокислотные последовательности SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно.
[000109] В определенных аспектах VH связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта или производного содержит аминокислотную последовательность на по меньшей мере 70%, 75%, 80%, 85%, 90%, 95% или 100% идентичную SEQ ID NO: 1, a VL связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта или производного содержит аминокислотную последовательность на по меньшей мере 70%, 75%, 80%, 85%, 90%, 95% или 100% идентичную SEQ ID NO: 5. В определенных аспектах VH содержит аминокислотную последовательность SEQ ID NO: 1, a VL содержит аминокислотную последовательность SEQ ID NO: 5.
[000110] Также в данном документе предложены полипептиды, кодирующие антитела против SEMA4D или антигенсвязывающие фрагменты, варианты или производные, описанные в данном документе, полинуклеотиды, кодирующие такие полипептиды, векторы, содержащие такие полинуклеотиды, и клетки-хозяева, содержащие такие векторы или полинуклеотиды, для применения, например, в получении связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе,.
[000111] Подходящие биологически активные варианты связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта или производного предусмотрены данным раскрытием, и могут быть получены и использованы в соответствии со способами, представленных в данном документе, или в соответствии со способами, хорошо известными специалистам в данной области техники. Такие варианты сохраняют определенные желательные свойства связывания эталонного антитела против SEMA4D, представленного в данном описании. Способы получения вариантов антител, как правило, доступны в данной области техники.
[000112] Способы мутагенеза и изменений нуклеотидной последовательности хорошо известны в данной области техники. См., например, Walker and Gaastra, eds. (1983) Techniques in Molecular Biology (MacMillan Publishing Company, New York); Kunkel, Proc. Natl. Acad. Sci. USA 82:488-492 (1985); Kunkel et al., Methods Enzymol. 154:367-382 (1987); Sambrook et al. (1989) Molecular Cloning: A Laboratory Manual (Cold Spring Harbor, N.Y.); патент США №4873192; и приведенные там ссылки; включенные в данный документ в качестве ссылки. Руководство в отношении соответствующих замен аминокислот, которые не влияют на биологическую активность полипептида, представляющего интерес, можно найти в модели Dayhoff et al. (1978) в Atlas of Protein Sequence and Structure (Natl. Biomed. Res. Found., Washington, D.C.), pp. 345-352, включенной в данный документ в качестве ссылки в полном объеме. Модель Dayhoff et al. использует матрицу подобия аминокислот с точковой принятой мутацией (РАМ) (матрица РАМ 250), чтобы определить подходящие консервативные аминокислотные замены. В определенных аспектах, используются консервативные замены, такие как замена одной аминокислоты другой, имеющие аналогичные свойства. Примеры консервативных замен аминокислот описанные в модели матрицы РАМ 250 Dayhoff et al. включают, без ограничения, Gly↔Ala, Val↔Ile↔Leu, Asp↔Glu, Lys↔Arg, Asn↔Gln и Phe↔Trp↔Tyr.
[000113] При построении вариантов связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, интересующего полипептида, модификации сделанные таким образом, что варианты по-прежнему обладают требуемыми свойствами, например, способностью специфически связываться с SEMA4D, например, SEMA4D человека, SEMA4D примата, отличного от человека (например, макака, мармозетки, и/или макака резуса SEMA4D) и/или SEMA4D грызуна (например, SEMA4D мыши и/или крысы), например, экспрессируемых на поверхности или секретируемых клеткой, причем связывающие молекулы, например, антитело или его фрагмент, вариант или производное обладает связыванием с SEMA4D, блокированием рецептора или нейтрализующей активностью описанными в данном документе. В определенных аспектах, мутации сделанные в ДНК, кодирующей вариант полипептида сохраняют рамку считывания и не создают комплементарные участки, которые могут производить вторичную структуру мРНК. См публикацию заявки на европейский патент №75444.
[000114] Методы измерения специфичности связывания и/или активности связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта или производного, включают, но не ограничиваются ими, стандартные анализы связывания, включая анализы конкурентного связывания, анализы для контроля секреции иммуноглобулина с помощью Т-клеток или В-клеток, анализы пролиферации Т-клеток, анализы апоптоза, анализы ИФА, и тому подобные. См., например, такие анализы, описанные в WO 93/14125; Shi et al., Immunity 13:633-642 (2000); Kumanogoh et al., J. Immunol. 169:1175-1181 (2002); Watanabe et al., J. Immunol. 167:4321-4328 (2001); Wang et al., Blood 97:3498-3504 (2001) и Giraudon et al., J. Immunol 172:1246-1255 (2004), все из которых включены в данное описание в качестве ссылки.
[000115] При обсуждении в данном документе, является ли, по меньшей мере какой-либо конкретный полипептид, в том числе и константные области, CDR, области VH или области VL, раскрытый в данном описании, на по меньшей мере около 65%, около 70%, около 75%, около 80%, около 85%, около 90%, около 91%, около 92%, около 93%, около 94%, около 95%, около 96%, около 97%, около 98%, около 99% или даже около 100% идентичным другому полипептиду, причем % идентичности может быть определен с использованием методов и компьютерных программ/программного обеспечения, известных в данной области техники. Оптимальное выравнивание последовательностей для сравнения может быть проведено, например, с помощью алгоритма локальной гомологии (Smith & Waterman, Adv. Appl. Math. 2:482-489 (1981), с помощью алгоритма глобального выравнивания (Needleman & Wunsch, J. Mol. Biol. 48:443 (1970), с помощью методов поиска подобия (Pearson & Lipman, Proc. Natl. Acad. Sci. U.S.A. 85:2444 (1988); Altschul et al., Nucl. Acids Res. 25:3389-402 (1997), с помощью компьютерных реализаций этих алгоритмов (например, GAP, BESTFIT, FASTA и BLAST в Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Dr., Madison, Wis.), как правило, с использованием параметров по умолчанию, или выравнивания вручную и визуального контроля (см., например, Current Protocols in Molecular Biology, Ausubel et al. (eds.), 1994).
[000116] Для целей данного изобретения, процент идентичности последовательности может быть определен с использованием алгоритм поиска гомологии Смита-Уотермана с использованием штрафа за открытие гэпа, равным 12 и штрафа за продление гэпа, равным 2, матрицей BLOSUM, равной 62. Вариант может, например, отличается от эталонного антитела против SEMA4D (например, MAb 2517, предложенное в данном документе) с помощью всего лишь от 1 до 15 аминокислотных остатков, всего лишь 1 до 10 аминокислотных остатков, таких как 6-10, всего лишь 5, всего лишь 4, 3, 2 или даже 1 аминокислотного остатка.
[000117] В определенных аспектах в данном изобретении предложено антитело или его антигенсвязывающий фрагмент, вариант или производное, которое специфически связывается с SEMA4D, причем указанное антитело или его фрагмент содержит VH и VL. В определенных аспектах VH содержит области, определяющие комплементарность (HCDR) HCDR1, HCDR2 и HCDR3, содержащие аминокислотные последовательности, идентичные или идентичные, за исключением одной, двух, трех, четырех, пяти или шести аминокислотных замен кислоты в одном, двух или всех трех из HCDR в SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 4, соответственно. В определенных аспектах HCDR1, HCDR2 и HCDR3 содержат аминокислотные последовательности, идентичные SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 4, соответственно. В определенных аспектах VL содержит области, определяющие комплементарность (LCDR) LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности, идентичные или идентичные, за исключением одной, двух, трех, четырех, пяти или шести аминокислотных замен кислоты в одном, двух или всех трех из LCDR в SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно. В определенных аспектах LCDR1, LCDR2 и LCDR3 содержат аминокислотные последовательности, идентичные SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно. В определенных аспектах VH дополнительно содержит каркасные области (HFW) HFW1, HFW2, HFW3 и HFW4, a VL дополнительно содержит каркасные области (LFW) LFW1, LFW2, LFW3 и LFW4. В определенных аспектах, каркасные области получены из антитела человека. В определенных аспектах, например, в которых антитело представляет собой антитело для применения в модельной системе, не являющейся моделью человека, каркасные области получают из антитела, не являющегося антителом человека например, антитела мыши. В определенных аспектах VH содержит аминокислотную последовательность SEQ ID NO: 1. В определенных аспектах VL содержит аминокислотную последовательность SEQ ID NO: 5.
[000118] В определенных аспектах в данном изобретении предложено антитело, например, полностью человеческое антитело или его антигенсвязывающий фрагмент, вариант или производное, которое специфически связывается с семафорином-4D (SEMA4D), содержащее VH и VL. В определенных аспектах VH содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичную SEQ ID NO: 1. В определенных аспектах VL содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичную SEQ ID NO: 5. В определенных аспектах VH содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичную SEQ ID NO: 1; a VL содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичную SEQ ID NO: 5. В определенных аспектах VH содержит аминокислотную последовательность SEQ ID NO: 1, a VL содержит аминокислотную последовательность SEQ ID NO: 5. В определенных аспектах VH и VL являются полностью человеческими.
[000119] В определенных аспектах, антитело против SEMA4D, или его антигенсвязывающий фрагмент, вариант или производное, представленные в данном документе, может специфически связываться с SEMA4D человека, SEMA4D грызуна, например, SEMA4D мыши и/или SEMA4D крысы, и/или SEMA4D примата, не являющегося человеком, например, SEMA4D макака и/или SEMA4D мармозетки.
[000120] В определенных аспектах антитело или его фрагмент, вариант или производное дополнительно содержит константную область тяжелой цепи, или ее фрагмент, вариант, или производное, слитую с С-концом VH. Константная область тяжелой цепи или ее фрагмент может быть получена из любых видов, но в определенных аспектах константная область тяжелой цепи или ее фрагмент, вариант или производное представляет собой, или является полученной от константной области тяжелой цепи человека, например, константной области IgG1, IgG2, IgG3, IgG4, IgA, IgE или IgM человека. В определенных аспектах константная область тяжелой цепи представляет собой константную область IgG4 человека или ее фрагмент, вариант или производное. В некоторых аспектах, например, когда предложенное антитело против SEMA4D или его фрагмент должно быть применено в модельной системе, не являющейся модельной системой человека, константная область тяжелой цепи или ее фрагмент может представлять собой константную область тяжелой цепи не являющейся тяжелой цепью человека, например, константную область тяжелой цепи мыши, такую как константная область IgG1 мыши.
[000121] В определенных аспектах антитело или его фрагмент, вариант или производное дополнительно содержит константную область легкой цепи, или ее фрагмент, вариант, или производное, слитую с С-концом VL. Константная область легкой цепи или ее фрагмент может быть получена из любых видов, но в определенных аспектах константная область легкой цепи или ее фрагмент является полученной от константной области легкой цепи человека, например, константной области каппа или лямбда человека. В определенных аспектах константная области легкой цепи или ее фрагмент, вариант или производное, представляет собой или является производным от константной области легкой цепи лямбда человека. В определенных аспектах константная область легкой цепи представляет собой константную область лямбда человека. В некоторых аспектах, например, когда предложенное антитело против SEMA4D или его фрагмент должно быть применено в модельной системе, не являющейся модельной системой человека, константная область легкой цепи или ее фрагмент может представлять собой константную область легкой цепи не являющейся легкой цепью человека, например, константную область легкой цепи мыши, такую как константная область лямбда мыши.
[000122] В определенных аспектах в данном изобретении предложен фрагмент антитела против SEMA4D, содержащий области VH и VL, описанные выше. В определенных аспектах фрагмент может представлять собой, например, фрагмент Fab, фрагмент Fab', фрагмент F(ab')2, фрагмент Fd, одноцепочечный фрагмент Fv (scFv) или дисульфид-связанный фрагмент Fv (sdFv).
[000123] В определенных аспектах, антитело против SEMA4D или его фрагмент, вариант или производное, предложенное в данном документе, может быть мультиспецифическим, например, биспецифическим. В дополнении к связывающим свойствам антитела против SEMA4D, приведенным в данном документе, мультиспецифическое антитело или его фрагмент, предложенные в данном документе может связываться с дополнительным эпитопом SEMA4D или могут связываться с другими несвязанными эпитопами.
[000124] В определенных аспектах антитело против SEMA4D, или его фрагмент, предложенное в данном документе, может специфически связываться с SEMA4D, например, SEMA4D человека, SEMA4D мыши, SEMA4D крысы и/или SEMA4D примата, отличного от человека, например, SEMA4D яванского макака и/или SEMA4D мармозетки или любой их комбинацией с аффинностью связывания, характеризующейся константой диссоциации KD не более чем 500 нМ, 100 нМ, 50,0 нМ, 40,0 нМ, 30,0 нМ, 20,0 нМ, 10,0 нМ, 9,0 нМ, 8,0 нМ, 7,0 нМ, 6,0 нМ, 5,0 нМ, 4,0 нМ, 3,0 нМ, 2,0 нМ, 1,0 нМ, 0,50 нМ, 0,10 нМ, 0,050 нМ, 0,01 нМ, 0,005 нМ или 0,001 нМ. Методы и приборы для измерения KD антитела или его фрагмента к SEMA 4D, такие как BIACORE, хорошо известны специалистам в данной области техники.
[000125] В определенных аспектах, антитело против SEMA4D или его фрагмент, предложенное в данном документе, может ингибировать связывание SEMA4D с рецептором SEMA4D, например, плексином-В1, плексином-В2 и/или CD72.
[000126] В определенных аспектах, антитело против SEMA4D или его антигенсвязывающий фрагмент, вариант или производное предложенные в данном документе является полностью человеческим, и вызывает минимальный ответ или отсутствие иммунного ответа против антитела при введении субъекту-человеку. Методы измерения иммунного ответа против антитела у субъекта, хорошо известны в данной области техники. См., например, Darwish, IA, Int. J. Biomed. Sci. 2:217-235 (2006).
[000127] Константная область антитела против SEMA4D может быть подвергнута мутации для изменения эффекторной функции в ряде способов. Например, см. патент США №6737056 В1 и публикацию заявки на патент США №2004/0132101 А1, которые раскрывают мутации Fc, которые оптимизируют связывание с рецепторами Fc антитела.
[000128] В определенных аспектах связывающие молекулы против SEMA4D, например, антитела или их фрагменты, варианты или производные, предложенные в данном документе, часть Fc может быть мутирована для модуляции, например, увеличения или уменьшения, эффекторной функции с использованием методов, известных в данной области техники. Например, удаление или инактивацию (через точечные мутации или другие средства) домена константной области может уменьшить связывание Fc-рецептора циркулирующего модифицированного антитела, тем самым увеличивая локализацию опухоли. В других случаях, модификации константной области, согласующиеся с данным раскрытием, модулирует связывание комплемента и, таким образом, может увеличить или уменьшить время полужизни в сыворотке. Другие модификации константной области могут быть использованы для модификации дисульфидных мостиков или олигосахаридных фрагментов, которые позволяют расширить локализацию за счет увеличения специфичности антигена или гибкости антитела. В результате физиологические профили, биодоступность и другие биохимических эффекты модификаций, такие как локализация опухоли, биораспределение и полужизнь в сыворотке, легко могут быть измерены и подсчитаны с использованием хорошо известных иммунологических методов без излишнего экспериментирования.
[000129] Связывающие молекулы против SEMA4D, например, антитела или их фрагменты, предложенные в данном документе, включают производные, которые модифицированы, например, путем ковалентного присоединения молекулы любого типа к антителу таким образом, чтобы ковалентное присоединение не препятствовало специфическому связыванию антитела с родственным эпитопом. Так, например, но не в качестве ограничения, производные антител включают антитела, которые были модифицированы, например, путем гликозилирования, ацетилирования, пэгилирования, фосфорилирования, амидирования, дериватизации известными защитными/блокирующими группами, протеолитического расщепления, связывания с клеточным лигандом или другим белком и т.д. Любая из многочисленных химических модификаций может быть осуществлена известными способами, в том числе, но не ограничиваясь ими, путем специфического химическое расщепление, ацетилирования, формилирования и т.д. Кроме того, производное может содержать одну или более неклассических аминокислот.
[000130] «Консервативная аминокислотная замена» является той, в которой аминокислотный остаток заменен на аминокислотный остаток, имеющий боковую цепь с подобным зарядом. Семейства аминокислотных остатков, имеющих боковые цепи с аналогичными зарядами были определены в данной области техники. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислотными боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, аспарагин, глутамин, серии, треонин, тирозин, цистеин), неполярными боковыми цепями (например, глицин, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Альтернативно, мутации могут быть введены случайным образом вдоль всей или части кодирующей последовательности, например, путем насыщающего мутагенеза, а полученные мутанты могут быть подвергнуты скринингу на биологическую активность для идентификации мутантов, которые сохраняют активность (например, способность связывать полипептид против SEMA4D, чтобы блокировать взаимодействие SEMA4D с его рецептором или ингибировать, задерживать или уменьшать метастазы у субъекта, например, больного раком).
[000131] Например, можно ввести мутации только в каркасные области или только в области CDR молекулы антитела. Введенные мутации могут представлять собой нейтральные или молчащие миссенс-мутации, т.е. нет иметь эффекта, или иметь малый эффект в отношении способности антитела связываться с антигеном. Эти типы мутаций могут быть полезны для оптимизации кодонов или улучшения продуцирования антител гибридомой. В качестве альтернативы, не-нейтральные миссенс мутации могут изменять способность антитела связывать антиген. Специалист в данной области техники будет в состоянии спроектировать и протестировать мутантные молекулы с требуемыми свойствами, такими как отсутствие изменений в активности связывания антигена или изменениях в активности связывания (например, улучшение активности связывания антигена или изменениях специфичности антител). После мутагенеза, кодируемый белок обычно может быть экспрессирован и функциональная и/или биологическая активность кодируемого белка, (например, способность иммуноспецифично связывать по меньшей мере один эпитоп полипептида SEMA4D) может быть определена с использованием методик, описанные в данном описание, или постоянно модифицируя методики, известные в данной области техники.
[000132] В некоторых аспектах, связывающая молекула против SEMA4D, например, антитело или его фрагмент, предложенная в данном документе, может содержать по меньшей мере одну оптимизированную область, определяющую комплементарность (CDR). Под «оптимизированной CDR» подразумеваются, что CDR, была изменена и оптимизирована для улучшения аффинности связывания и/или активности против SEMA4D, которая передается связывающей молекуле против SEMA4D, содержащей оптимизированную CDR. «Активность против SEMA4D» или «блокирующая активность SEMA4D» может включать активность, которая модулирует, например, уменьшает, устраняет, снижает или предотвращает одну или более активности SEMA4D. Неограничивающие активности SEMA4D включают: активацию В-клеток, агрегирование и выживание; CD40-индуцированную пролиферацию и продуцирование антител; реакцию антител на зависимый Т-клеточные антигены; пролиферацию Т-клеток или других иммунных клеток; созревание дендритных клеток; демиелинизацию и дегенерацию аксонов; апоптоз плюрипотентных нейронных предшественников и/или олигодендроцитов; индукцию миграции эндотелиальных клеток; ингибирование спонтанной миграции моноцитов; стимулирование роста опухолевых клеток или метастазов, связывание с плексином-В1 или другим рецептором клеточной поверхности, или любую другую активность ассоциации с растворимым SEMA4D или SEMA4D, который экспрессируется на поверхности SEMA4D+ клеток. В конкретном варианте осуществления, активность против SEMA4D включает способность ингибировать, задерживать или уменьшать метастазирование опухолей, либо в сочетании с ингибированием, задержкой или уменьшением роста клеток первичной опухоли и опухолевых метастазов, или независимо от роста первичной опухолевых клеток и опухолевых метастазов. Активность против SEMA4D также может быть связана с уменьшением частоты или серьезности заболеваний, связанных с экспрессией SEMA4D, в том числе, но не ограничиваясь этим, некоторые виды рака, включая солидные опухоли и лимфы, аутоиммунные заболевания, воспалительные заболевания, включая воспалительные заболевания центральной нервной системы (ЦНС) и периферической нервной системы (ПНС), нейродегенеративные заболевания, отторжения трансплантата, и инвазивный ангиогенез.
Полинуклеотиды, кодирующие антитела против SEMA4D
[000133] В данном изобретении предложен также выделенный полинуклеотид, или два или более полинуклеотидов, содержащих одну или более последовательностей нуклеиновых кислот, кодирующих связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант или производное, предложенную в данном документе.
[000134] В одном аспекте в данном изобретении предложен выделенный полинуклеотид или комбинация полинуклеотидов, содержащий одну или более последовательностей нуклеиновых кислот, кодирующих связывающую молекулу против SEMA4D, например, антитело или его фрагмент, вариант или производное, предложенное в данном документе, или его субъединицу, например, субъединицу тяжелой цепи или ее фрагмент, или субъединицу легкой цепи или ее фрагмент.
[000135] В определенных аспектах, полинуклеотид или комбинация полинуклеотидов, предложенный в данном документе, содержит последовательность нуклеиновой кислоты, которая кодирует VH связывающей молекулы против SEMA4D, например, антитела или его фрагмента, варианта или производного. В определенных аспектах, полинуклеотид или комбинация полинуклеотидов, предложенный в данном документе, содержит последовательность нуклеиновой кислоты, которая кодирует VL связывающей молекулы против SEMA4D, например, антитела или его фрагмента, варианта или производного. В определенных аспектах, полинуклеотид или комбинация полинуклеотидов, предложенный в данном документе, содержит последовательность нуклеиновой кислоты, которая кодирует VH, и последовательность нуклеиновой кислоты, которая кодирует VL связывающей молекулы против SEMA4D, например, антитела или его фрагмента, варианта или производного. В определенных аспектах последовательность нуклеиновой кислоты, кодирующая VH и последовательность нуклеиновой кислоты, кодирующая VL расположены в одном векторе. Такой вектор предложен в данном описании. В определенных аспектах последовательность нуклеиновой кислоты, кодирующая VH и последовательность нуклеиновой кислоты, кодирующая VL расположены в отдельных векторах. Такие векторы также предложены в данном описании. Векторы, предложенные в данном изобретении, могут дополнительно содержать генетические элементы, обеспечивающие экспрессию антитела или его фрагмента. Такие генетические элементы, такие как промоторы, последовательности поли-аденилирования и энхансеры, описаны в данном документе в других местах. В данном изобретении также предложена клетка-хозяин, содержащая полинуклеотид или комбинацию полинуклеотидов, предложенных в данном документе, и/или вектор или векторы, предложенные в данном документе.
[000136] Также предложен способ получения антитела против SEMA4D или его фрагмента, варианта или производного, предложенного в данном документе, причем способ включает культивирование клетки-хозяина, предложенной в данном документе, и выделение антитела или его фрагмента.
[000137] В некоторых аспектах в данном изобретении предложен выделенный полинуклеотид или два или более полинуклеотида, содержащий одну или более последовательностей нуклеиновых кислот, кодирующих антитело против SEMA4D или его антигенсвязывающий фрагмент, вариант или производное, или субъединицу, причем антитело содержит VH или VL, при этом VH содержит области, определяющие комплементарность (HCDR) HCDR1, HCDR2 и HCDR3, содержащие аминокислотные последовательности, идентичные или идентичные за исключением одной, двух, трех или четырех аминокислотных замен в одной, двух или трех HCDR SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 4, соответственно; a VL содержит области, определяющие комплементарность (LCDR) LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности, идентичные или идентичные за исключением одной, двух, трех или четырех аминокислотных замен в одной, двух или трех LCDR SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно.
[000138] В определенных аспектах в данном изобретении предложен выделенный полинуклеотид или два или более полинуклеотидов, содержащих одну или более последовательностей нуклеиновых кислот, кодирующих антитело против SEMA4D или его антигенсвязывающий фрагмент, вариант или производное, или субъединицу, причем антитело содержит VH и VL, при этом VH, содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичную SEQ ID NO: 1, a VL содержит аминокислотную последовательность на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичную SEQ ID NO: 5.
[000139] Любой из полинуклеотидов, описанных выше, может дополнительно содержать дополнительные последовательности нуклеиновых кислот, кодирующие, например, константные области тяжелой или легкой цепи или их фрагменты, описанные в данном документе в другом месте, сигнальный пептид для прямой секреции кодируемого полипептида, или других гетерологичные полипептиды, описанные в данном документе. Кроме того, как более подробно описано в данном документе в другом месте, данное описание включает композицию, содержащую один или более из полинуклеотидов, описанных выше.
[000140] В одном варианте осуществления данное описание включает композицию, содержащую первый полинуклеотид и второй полинуклеотид, причем первый полинуклеотид, содержит последовательность нуклеиновой кислоты, кодирующую VH, как описано в данном документе, и второй полинуклеотид, кодирующий VL, как описано в данном документе.
[000141] Данное изобретение также включает фрагменты полинуклеотидов указанные в данном документе, как описано в другом месте. Кроме того, в данном изобретении предложены полинуклеотиды, которые кодируют слитые полипептиды, фрагменты Fab и другие производные, как описано в данном документе.
[000142] Полинуклеотиды, предложенные в данном описании, могут быть получены или изготовлены любым способом, известным в данной области техники. Например, если нуклеотидная последовательность антитела известна, полинуклеотид, кодирующий антитело, может быть собран из химически синтезированных олигонуклеотидов (например, как описано в Kutmeier et al., Bio Techniques 17:242 (1994)), который, кратко, включает синтез перекрывающихся олигонуклеотидов, содержащих части последовательности, кодирующей антитело, отжиг и лигирование этих олигонуклеотидов, а затем амплификацию лигированных олигонуклеотидов с помощью ПЦР.
[000143] Альтернативно, полинуклеотид, кодирующий связывающие молекулы против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант или производное, предложенный в данном документе может быть получен из последовательностей нуклеиновых кислот, полученных из подходящего источника. Если клон, содержащий полинуклеотид, кодирующий антитело конкретного не доступен, но последовательность молекулы антитела, как известно, нуклеиновая кислота, кодирующая антитело, может быть химически синтезирована или получена из подходящего источника (например, библиотеки кДНК антител или библиотеки кДНКа, полученной от, или нуклеиновой кислоты, например, поли А+ РНК, выделенной из, любой ткани или клетки, экспрессирующей антитело или другого антитела против SEMA4D, таких, как клетки гибридом выбранные как, экспрессирующие антитела) с помощью ПНР-амплификации с использованием синтетических праймеров, гибридизующихся с 3' и 5' концами последовательности или путем клонирования с использованием олигонуклеотидного зонда, специфичного для конкретного последовательность гена, чтобы определить, например, кДНК клона из библиотеки кДНК, которая кодирует антитело или другого антитела против SEMA4D. Амплифицированные нуклеиновые кислоты, созданные с помощью ПЦР могут быть затем клонированы в реплицируемые векторы клонирования с использованием любого способа, хорошо известного в данной области техники.
[000144] После определения нуклеотидной последовательности и соответствующей аминокислотной последовательности антитела против SEMA4D или его антигенсвязывающего фрагмента, варианта или производного, его нуклеотидной последовательностью можно манипулировать с помощью методов, хорошо известных в данной области техники для манипулирования нуклеотидной последовательностью, например, при помощи методов рекомбинантных ДНК, сайт-направленного мутагенеза, ПЦР и т.д. (см, например, методы, описанные в Sambrook et al. (1990) Molecular Cloning, A Laboratory Manual (2nd ed.; Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.) и Ausubel et al., eds. (1998) Current Protocols in Molecular Biology (John Wiley & Sons, NY), которые оба включены в данное описание в качестве ссылки в полном объеме), для получения антител, имеющих различную аминокислотную последовательность, например, для создания аминокислотных замен, делеций и/или инсерций.
[000145] Полинуклеотид или комбинацию полинуклеотидов, кодирующих связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант или производное, может состоять из любого полирибонуклеотида или полидезоксирибонуклеотида, который может представлять собой немодифицированную РНК или ДНК или модифицированную РНК или ДНК. Например, полинуклеотид или комбинация полинуклеотидов, кодирующий антитело против SEMA4D или его антигенсвязывающий фрагмент, вариант или производное может состоять из одно- и двухцепочечной ДНК, ДНК, которая представляет собой смесь одно- и двухцепочечных областей, одно- и двухцепочечной РНК и РНК, которая представляет собой смесь одно- и двухцепочечных областей, гибридной молекулы, содержащие ДНК и РНК, которые могут быть одноцепочечными или, более типично, двухцепочечными или смесью одного - и двухцепочечных областей. Кроме того, полинуклеотид или комбинация полинуклеотидов, кодирующий антитело против SEMA4D или его антигенсвязывающий фрагмент, вариант или производное может состоять из трехцепочечных областей, содержащей РНК или ДНК или как РНК, так и ДНК. Полинуклеотид или комбинация полинуклеотидов, кодирующий антитело против SEMA4D или его антигенсвязывающий фрагмент, вариант или производное может также содержать одно или более модифицированных оснований или каркасов ДНК или РНК, модифицированных для обеспечения стабильности или по другим причинам. «Модифицированные» основания включают, например, тритилированные основания и необычные основания, такие как инозин. Различные модификации могут быть сделаны в ДНК и РНК; таким образом, «полинуклеотид» охватывает химически, ферментативно или метаболически модифицированные формы.
[000146] Выделенный полинуклеотид или комбинация полинуклеотидов, кодирующих неприродный вариант полипептида, полученный из иммуноглобулина (например, часть тяжелой цепи иммуноглобулина или часть легкой цепи) может быть создана путем введения одной или более нуклеотидных замен, добавлений или делеций в нуклеотидную последовательность иммуноглобулина таким образом, что одна или более аминокислотных замен, добавлений или делеций вводятся в кодируемый белок. Мутации могут быть введены с помощью стандартных методик, таких как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. В некоторых аспектах, консервативные аминокислотные замены могут быть сделаны в одном или более несущественных аминокислотных остатков.
Слитые белки и конъюгаты антител
[000147] Как обсуждено более подробно в данном документе в другом месте, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант или производное, предложенная в данном документе, может дополнительно быть рекомбинантно слита с гетерологичным полипептидом на N- или С-конце или химически конъюгированна (включая ковалентную и нековалентную конъюгацию) с полипептидами или другими гетерологичными фрагментами. Например, антитело против SEMA4D может быть рекомбинантно слито или конъюгировано с молекулами, используемыми в качестве меток в анализах обнаружения и эффекторными молекулами, такими как гетерологичные полипептиды, лекарственные средства, радионуклиды или токсины. См, например, публикации РСТ WO 92/08495; WO 91/14438; WO 89/12624; патент США №5314995 и ЕР 396387. В некоторых аспектах гетерологичный фрагмент может представлять собой полипептид, цитотоксический агент, терапевтический агент, пролекарство, липид, углевод, нуклеиновую кислоту, детектируемую метку, полимер или любую их комбинацию. Иллюстративные гетерологические полипептиды включают, без ограничения, связывающую молекулу, фермент, цитокин, лимфокин, гормональный пептид или любую их комбинацию. Иллюстративные цитотоксические агенты включают, без ограничения, радионуклид, биологический токсин, ферментативно активный токсин или любую их комбинацию. Иллюстративные детектируемые метки включают, без ограничения, фермент, флуоресцентную метку, хемилюминесцентную метку, биолюминесцентную метку, радиоактивную метку или любую их комбинацию.
[000148] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, предложенная в данном документе, может включать производные, которые модифицированы, например, путем ковалентного присоединения любого типа фрагмента к антителу, таким образом, что ковалентное присоединение не мешает связывающей молекуле связываться с SEMA4D. Так, например, но не в качестве ограничения, производные антител могут быть модифицированы, например, путем гликозилирования, ацетилирования, пэгилирования, фосфорилирования, амидирования, дериватизации известными защитными/блокирующими группами, протеолитического расщепления, связывания с клеточным лигандом или другим белком и т.д. Любая из многочисленных химических модификаций может быть осуществлена известными способами, в том числе, но не ограничиваясь ими, путем специфического химическое расщепление, ацетилирования, формилирования и т.д. Кроме того, производное может содержать одну или более неклассических аминокислот.
[000149] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант или производное, как предложено в данном документе, может быть составлена из аминокислот, соединенных друг с другом пептидными связями или модифицированными пептидными связями, например, пептидные изостеры, и может содержать аминокислоты, отличные от 20 ген-кодирующих аминокислот. Например, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть модифицирована путем естественных процессов, таких как посттрансляционный процессинг или с помощью химических методов модификации, которые хорошо известны в данной области техники. Такие модификации хорошо описаны в основных текстах и в более детальных монографиях, а также в множестве научной литературы. Модификации могут происходить в любом месте в связывающей молекуле против SEMA4D, включая пептидные каркасы, аминокислотные боковые цепи и амино- или карбоксильные концы, или на фрагментах, таких как углеводы. Кроме того, данная связывающая молекула против SEMA4D может содержать много типов модификаций. Связывающие молекулы против SEMA4D могут быть разветвленными, например, в результате убиквитинирования, и они могут быть циклическими, с ветвлением или без него. Циклическая, разветвленная и разветвленная циклическая связывающая молекула против SEMA4D может быть результатом посттрансляционных природных процессов или может быть получена синтетическими методами. Модификации включают ацетилирование, ацилирование, АДФ-рибозилирование, амидирование, ковалентное присоединение флавина, ковалентное присоединение остатка гема, ковалентное присоединение нуклеотида или нуклеотидного производного, ковалентное присоединение липида или производного липида, ковалентное присоединение фосфотидилинозитола, перекрестное сшивание, циклизацию, образование дисульфидных связей, деметилирование, образование ковалентных поперечных связей, образование цистеина, образование пироглутамата, формилирование, гамма-карбоксилирование, гликозилирование, формирование GPI якоря, гидроксилирование, йодирование, метилирование, миристоилирование, окисление, пэгилирование, протеолитический процессинг, фосфорилирование, пренилирование, рацемизацию, селеноилирование, сульфатацию, опосредуемое транспортной РНК присоединение аминокислот к белка, таким как аргинилирование и убиквитинирование. (См., например, Proteins-Structure and Molecular Properties, Т.E. Creighton, W.H. Freeman and Company, NY; 2nd ed. (1993); Johnson, ed. (1983) Posttranslational Covalent Modification of Proteins (Academic Press, NY), pgs. 1-12; Seifter et al., Meth. Enzymol. 182:626-646 (1990); Rattan et al., Ann. NY Acad. Sci. 663:48-62 (1992)).
[000150] В данном изобретение также предложены слитые белки, содержащие связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как представлено в данном документе, и гетерологичный полипептид. Гетерологичный полипептид, с которым слито антитело, может быть полезным для функционирования или полезным для нацеливания клеток, экспрессирующих полипептид против SEMA4D. Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть слита или конъюгирована с одним или более гетерологичными полипептидами или другими фрагментами для увеличения полужизни полипептидов in vivo или для применения в иммунологических анализах с использованием способов, известных в данной области техники. Например, в одном варианте осуществления, ПЭГ или альбумин сыворотки человека может быть конденсированным или конъюгированным со связывающей молекулой против SEMA4D, как представлено в данном документе, чтобы увеличить ее полужизнь in vivo. См. Leong et al., Cytokine 16:106 (2001); Adv. in Drug Deliv. Rev. 54:531 (2002) или Weir et al., Biochem. Soc. Transactions 30:512 (2002).
[000151] Более того, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как представлено в данном документе, может быть слита с одним или более маркерными последовательностями, такими как пептид, для облегчения их очистки или обнаружения. В некоторых вариантах осуществление маркерная аминокислотная последовательность представляет собой гекс-гистидиновый пептид, такой как метка, представленная в векторе pQE (QIAGEN Inc.), среди прочих, многие из которых являются коммерчески доступными. As described in Gentz et al., Proc. Natl. Acad. Sci. USA 86:821-824 (1989), например, гекса-гистидин обеспечивает удобную очистку слитого белка. Другие пептидные метки, пригодные для очистки включают, но не ограничиваются ими, метку «НА», что соответствует эпитопу, полученному из белка гемагглютинина вируса гриппа (Wilson et al., Cell 37:767 (1984)) и метку «flag».
[000152] Слитые белки могут быть получены с использованием методов, которые хорошо известны в данной области техники (см., например, патент США №5116964 и 5225538). Точный сайт, на котором происходит слияние может быть выбран опытным путем, чтобы оптимизировать секрецию или связывающие характеристики гибридного белка. ДНК, кодирующую слитый белок затем трансфицируют в клетку-хозяина для экспрессии.
[000153] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть использована в неконъюгированной форме или может быть конъюгирована с по меньшей мере одной из множества молекул, например, для улучшения терапевтических свойств молекулы, для облегчения обнаружения мишени, или для визуализации или лечения пациента. Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть использована в неконъюгированной форме или может быть помечена или конъюгирована, или до, или после очистки, или при выполнении очистки.
[000154] В частности, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть конъюгирована с терапевтическими агентами, пролекарствами, цитотоксическими агентами, пептидами, белками, ферментами, вирусами, липидами, модификаторами биологического ответа, фармацевтическими агентами или ПЭГ.
[000155] Специалисты в данной области техники будет понятно, что конъюгаты также могут быть собраны с использованием различных методов, в зависимости от выбранного агента, с которым произведено сопряжение. Например, конъюгаты с биотином получает, например, путем реакции связывания полипептида с активированным сложным эфиром биотина, таким как N-гидроксисукцинимид эфир биотина. Аналогично, конъюгаты с флуоресцентным маркером, могут быть получены в присутствии агента сочетания, например, те, которые перечислены в данном описании, или путем реакции с изотиоцианатом, например, флуоресцеин-изотиоцианатом. Конъюгаты связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, могут быть получены аналогичным образом.
[000156] Данное изобретение дополнительно включает связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, конъюгированную с диагностическим или терапевтическим агентом. Такие связывающие молекулы против SEMA4D могут быть использованы диагностически, например, контролировать развитие или прогрессирование заболевания в качестве части клинической процедуры тестирования, чтобы, например, определить эффективность данной схемы лечения и/или профилактики. Например, обнаружение может быть облегчено путем связывания связывающей молекулы против SEMA4D с детектируемым веществом. Примеры детектируемых веществ включают различные ферменты, простетические группы, флуоресцентные материалы, люминесцентные материалы, биолюминесцентные материалы, радиоактивные материалы, испускающие позитроны металлы с использованием различной позитронно-эмиссионной томографии, а также ионы нерадиоактивных парамагнитных металлов. См., например, патент США №4741900 для ионов металлов, которые могут быть конъюгированы с антителами, для применения в качестве диагностики в соответствии с данным изобретением. Примеры подходящих ферментов включают пероксидазу хрена, щелочную фосфатазу, β-галактозидазу или ацетилхолинэстеразу; примеры подходящих простетических групп включают стрептавидин/биотин и авидин/биотин; примеры подходящих флуоресцентных материалов включают умбеллиферон, флуоресцеин, флуоресцеинизотиоцианат, родамин, дихлортриазиниламин флуоресцеина, дансилхлорид или фикоэритрин; пример люминесцентного материала включает люминол; примеры биолюминесцентных материалов включают люциферазу, люциферин и экворин; а примеры подходящего радиоактивного материала включают 125I, 131I, 111In, 90Y или 99Тс.
[000157] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть конъюгирована с терапевтической молекулой, такой как цитотоксин, терапевтическим агент или ион радиоактивного металла. Цитотоксин или цитотоксический агент включает любой агент, который является вредным для клеток.
[000158] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может также быть помечена детектируемой меткой путем ее связывания с хемилюминесцентным соединением. Присутствие хемилюминесцентного-меченой связывающей молекулы против SEMA4D затем определяют путем обнаружения присутствия люминесценции, которая возникает в ходе химической реакции. Примеры особенно полезных хемилюминесцентных соединений для мечения представляют собой люминол, изолюминол, ароматический эфир акридиния, имидазол, соль акридина и эфир щавелевой кислоты.
[000159] Один из способов, в котором связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как представлено в данном документе, можно детектируемо пометить путем ее объединения с ферментом и с использованием связанного продукта в иммуноферментном анализе (ИФА) (Voller, A., "The Enzyme Linked Immunosorbent Assay (ELISA)" Microbiological Associates Quarterly Publication, Walkersville, Md.; Diagnostic Horizons 2:1-7 (1978); Voller et al., J. Clin. Pathol. 31:507-520 (1978); Butler, Meth. Enzymol. 73:482-523 (1981); Maggio, ed. (1980) Enzyme Immunoassay, CRC Press, Boca Raton, Fla.; Ishikawa et al., eds. (1981) Enzyme Immunoassay (Kgaku Shoin, Tokyo). Фермент, который связан со связывающей молекулой против SEMA4D будет вступать в реакцию с соответствующим субстратом, например, хромогенным субстратом, таким образом, чтобы производить химический радикал, который может быть обнаружен, например, спектрофотометрически, флуориметрически или путем визуальных средств. Ферменты, которые могут быть использованы для детектируемого мечения антител включают, но не ограничиваются ими, малатдегидрогеназу, нуклеазу стафилококка, дельта-5-стероидоизомеразу, дрожжевую алкогольдегидрогеназу, альфа-глицерофосфат дегидрогеназу, триозофосфатизомеразу, пероксидазу хрена, щелочную фосфатазу, аспарагиназу, глюкозооксидазу, бета-галактозидазу, рибонуклеазу, уреазу, каталазу, глюкозо-6-фосфат-дегидрогеназу, глюкоамилазу и ацетилхолинэстеразу. Кроме того, обнаружение может быть осуществлено с помощью колориметрических методов, которые используют хромогенный субстрат для фермента. Обнаружение также может быть достигнуто путем визуального сравнения степени ферментативной реакции субстрата по сравнению с аналогично подготовленными стандартами.
[000160] Обнаружение также может быть осуществлено с использованием любого из множества других иммуноанализов. Например, с помощью радиоактивно маркирования связывающей молекулы против SEMA4D можно обнаружить связывающую молекулу посредством использования радиоиммуноанализа (РИА). Радиоактивный изотоп может быть обнаружен с помощью средств, включая, но не ограничиваясь этим, гамма-счетчик, сцинтилляционный счетчик или авторадиограф.
[000161] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может также быть помечена с помощью металлов, излучающих флуоресценцию, таких как 152Eu или других из серии лантанидов. Эти металлы могут быть присоединены к связывающей молекуле с использованием таких хелатирующих металл групп, как диэтилентпиаминпептауксусная кислота (ДТПА) или этилендиаминтетрауксусная кислота (ЭДТА).
[000162] Способы конъюгации различных фрагментов со связывающей молекулой против SEMA4D, как предложено в данном описании, хорошо известны обычным специалистам в данной области техники.
Экспрессия полипептидов антител
[000163] Последовательности ДНК, которые кодируют легкие и тяжелые цепи связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающий фрагментов, вариантов или производных, как предложено в данном документе, могут быть созданы, либо одновременно, либо по отдельности, с использованием обратной транскриптазы и ДНК полимеразы в соответствии с хорошо известными методами. ПЦР может быть инициирован праймерами консенсусных константных областей или более специфическими праймерами, основанными на опубликованных последовательностях ДНК и аминокислот тяжелых и легких цепей. Как обсуждалось выше, ПЦР также могут быть использованы для выделения клонов ДНК, кодирующие легкие и тяжелые цепи антитела. В этом случае библиотеки могут быть подвергнуты скринингу при помощи консенсусных праймеров или более крупных гомологичных зондов, таких зонды константной области мыши.
[000164] ДНК, как правило, плазмидная ДНК, может быть выделена из клеток с использованием методик, известных в данной области техники, помещена на карту рестрикции и секвенирована в соответствии со стандартными, хорошо известными методами, изложенными в деталях, например, в ссылках, связанных с методами рекомбинантной ДНК, предусмотренными в данном документе в другом месте.
[000165] После манипуляций с изолированной генетического материала, для обеспечения связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как представлено в данном документе, полинуклеотиды, кодирующие связывающую молекулу могут быть вставлены в вектор экспрессии для введения в одну или более клеток-хозяев, которые могут быть использованы для получения желаемого количества связывающей молекулы против SEMA4D.
[000166] Рекомбинантная экспрессия антитела против SEMA4D или его фрагмента, производного или аналога, например, тяжелой или легкой цепи антитела, требует построения одного или более экспрессирующих векторов, содержащих полинуклеотид или комбинацию полинуклеотидов, который кодирует антитело. После того как был получен полинуклеотид или комбинация полинуклеотидов, кодирующих молекулу антитела или тяжелую или легкую цепь антитела или его часть (например, содержащий вариабельную область тяжелой или легкой цепи), вектор или векторы для получения молекулы антитела может быть получен с помощью технологии рекомбинантной ДНК с использованием методик, хорошо известных в данной области техники. Таким образом в данном документе описаны способы получения белка путем экспрессии полинуклеотида или комбинации полинуклеотидов, содержащих антитела, кодирующие последовательности нуклеиновых кислот. Способы, которые хорошо известны специалистам в данной области техники, могут быть использованы для конструирования векторов экспрессии, содержащих последовательности, кодирующие антитела и соответствующие транскрипционные и трансляционные контрольные сигналы. Эти методы включают, например, методы рекомбинантной ДНК in vitro, синтетические методики, и генетическую рекомбинацию in vivo. В данном изобретении, таким образом, предложены воспроизводимые векторы, содержащие последовательности нуклеиновых кислот, кодирующие связывающие молекулы против SEMA4D, например, антитело, как предложено в данном документе, или его тяжелую или легкую цепь, или вариабельную область тяжелой или легкой цепи, функционально связанную с промотором. Такие векторы могут содержать нуклеотидную последовательность, кодирующую константную область тяжелой и/или легкой цепи антитела (см, например, публикацию РСТ WO 86/05807; публикацию РСТ WO 89/01036 и США патент США №5122464) и вариабельную область антитела может быть клонирована в вектор такой, как пригодный для экспрессии всей тяжелой или легкой цепи.
[000167] Термин «вектор» или «экспрессирующий вектор» используется в данном документе для обозначения векторов, используемых в соответствии с данным изобретением в качестве носителя для введения внутрь и экспрессии нужного гена в клетке-хозяине. Как известно специалистам в данной области техники, такие векторы легко могут быть выбраны из, например, плазмид, фагов и вирусов, например, ретровирусов. В общем случае, векторы совместимы с данным изобретением будет содержать селективный маркер, соответствующие сайты рестрикции для облегчения клонирования нужного гена и способность входить и/или реплицироваться в эукариотических или прокариотических клетках.
[000168] Могут быть использованы многочисленные векторные системы экспрессии. Например, один класс вектора использует элементы ДНК, которые являются производными от вирусов животных, таких как бычий вирус папилломы, вирус полиомы, аденовирус, вирус коровьей оспы, бакуловирус, ретровирусы (RSV, MMTV или MOMLV) или вирус SV40. Другие предполагают использование полицистронных систем с внутренними сайтами связывания рибосомы (IRES). Кроме того, клетки, в хромосомы которых интегрированы ДНК могут быть выбраны путем введения одного или более маркеров, которые обеспечивают отбор трансфицированных клеток-хозяев. Маркер может обеспечить прототрофию ауксотрофному хозяину, биоцидную устойчивость (например, антибиотическую) или устойчивость к тяжелым металлам, таким как медь. Ген селектируемых маркеры либо может быть непосредственно связаны с последовательностями ДНК, которые будет экспрессированы, или введены в ту же клетку путем котрансформации. Дополнительные элементы могут быть также необходимы для оптимального синтеза мРНК. Эти элементы могут включать в себя сигнальные последовательности, сигналы сплайсинга, а также транскрипционные промоторы, энхансеры и сигналы терминации.
[000169] В определенных аспектах клонированные вариабельные области молекулы нуклеиновых кислот могут быть вставлены в вектор экспрессии вместе с генами константной области тяжелой и легкой цепей, синтезированными, как описано выше. Конечно, может быть использован любой вектор экспрессии, который способен вызывать экспрессию в эукариотических клетках. Примеры подходящих векторов включают, но не ограничиваются ими плазмиды pcDNA3, pHCMV/Zeo, pCR3.1, pEF 1/His, pIND/GS, pRc/HCMV2, pSV40/Zeo2, pTRACER-HCMV, pUB6/V5-His, pVAX1 и pZeoSV2 (доступные от Invitrogen, Сан-Диего, штат Калифорния) и плазмиду pCI (доступную от Promega, Мэдиссон, штат Висконсин). В целом, скрининг большого числа трансформированных клеток на те, которые экспрессируют соответственно высокий уровень тяжелых и легких цепей иммуноглобулина, являются рутинным экспериментированием, что может быть осуществлено, например, с помощью роботизированных систем.
[000170] В целом, после подготовки вектор или последовательность ДНК, кодирующая мономерную субъединицу связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, вектор экспрессии могут быть введены в соответствующую клетку-хозяина. Введение плазмиды в клетку-хозяина может быть осуществлено различными методами, хорошо известными специалистам в данной области техники. Они включают, но не ограничиваются ими, трансфекцию (в том числе электрофорез и электропорацию), слияние протопластов, осаждение фосфатом кальция, слияния клеток с оборачивающей ДНК, микроинъекцию и инфицирование интактным вирусом. См., Ridgway (1988) "Mammalian Expression Vectors" in Vectors, ed. Rodriguez and Denhardt (Butterworths, Boston, Mass.), Chapter 24.2, pp. 470-472. Как правило, введение плазмиды в хозяина происходит через электропорацию. Клетки-хозяева, несущие экспрессионную конструкцию можно выращивать в условиях, подходящих для продуцирования легких цепей и тяжелых цепей и могут быть анализированы на синтез белка и сборку тяжелой и/или легкой цепи. Типичные методы анализа включают твердофазный иммуноферментный анализ (ИФА), радиоиммуноанализ (РИА) или сортировку клеток, активированных флуоресценцией (FACS), иммуногистохимию и тому подобное.
[000171] Вектор экспрессии могут быть трансфицированы в клетку-хозяин с помощью обычных методов, а трансфицированные клетки затем можно культивировать обычными способами для получения связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе,. Таким образом, данное изобретение включает летки-хозяева, содержащие полинуклеотид или комбинацию полинуклеотидов, кодирующих антитела, как предложено в данном документе, или его тяжелую или легкую цепи, функционально связанный с промотором, например, гетерологичным промотором. В некоторых вариантах осуществления для экспрессии двухцепочечных антител, векторы, кодирующие как тяжелые, так и легкие цепи могут быть коэкспрессированы в клетку-хозяина для экспрессии и сборки всей связывающей молекулы, как подробно описано ниже.
[000172] Используемый в данном описании термин «клетка-хозяин» относится к клеткам, которые несут векторы, сконструированные с использованием методов рекомбинантных ДНК, и кодирующие по меньшей мере один гетерологичный полинуклеотид. В описаниях процессов для выделения антител из рекомбинантных хозяев, термины «клетка» и «культура клеток» используются взаимозаменяемо для обозначения источника антитела, если только явно не указано иное. Другими словами, восстановление полипептида из «клеток» может означать либо из центрифугированных осажденных целых клеток, либо из клеточной культуры, содержащей как среду, так и суспендированные клетки.
[000173] Разнообразные векторные экспрессионные системы-хозяева могут быть использованы для экспрессии связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе,. Такие экспрессионные системы-хозяева представляют собой носители, с помощью которых интересующие кодирующие последовательности могут быть получены и затем очищены, но и представляют собой клетки, которые могут, когда трансформированы или трансфицированы соответствующими кодирующими последовательностями нуклеотидов, экспрессируют молекулу антитела, предложенную в данном документе in situ. Они включают, но не ограничиваются ими, микроорганизмы, такие как бактерии (например, Е. coli, В. subtilis), трансформированные рекомбинантной ДНК бактериофага, векторы экспрессии на основе плазмидной ДНК или космидной ДНК, содержащие кодирующие последовательности антител, дрожжи (например, Saccharomyces, Pichia), трансформированные рекомбинантными векторами экспрессии дрожжей, содержащими кодирующие последовательности антитела; системы клеток насекомых, инфицированные рекомбинантными вирусными векторами экспрессии (например, бакуловирусы), содержащие последовательности, кодирующие антитела; системы клеток растений, инфицированные рекомбинантными вирусными векторами экспрессии (например, вирус мозаики цветной капусты, CaMV; вирус табачной мозаики, TMV) или трансформированные рекомбинантными плазмидными векторами экспрессии (например, плазмида Ti), содержащие последовательности, кодирующие антитела; или системы клеток млекопитающих (например, клетки COS, СНО, BLK, 293, 3Т3), несущие рекомбинантные экспрессионные конструкции, содержащие промоторы, полученные из генома клеток млекопитающих (например, промотор металлотионеина) или от вирусов млекопитающих (например, поздний промотор аденовируса; 7,5K промотор вируса коровьей оспы или немедленно ранний промотор цитомегаловируса человека). В определенных аспектах, бактериальные клетки, такие как Escherichia coli, или эукариотические клетки, особенно для экспрессии рекомбинантных целых молекул антител, могут быть использованы для экспрессии рекомбинантной молекулы антитела. Так, например, клетки млекопитающих, такие как клетка яичника китайского хомячка (СНО), в сочетании с вектором являются эффективной системой экспрессии антител (Foecking et al., Gene 45:101 (1986); Cockett et al., Bio/Technology 8:2 (1990)).
[000174] Линия клетки-хозяина используется для экспрессии белка может быть получена от млекопитающего. Примеры линии клетки-хозяина включает, без ограничения, СНО (яичника китайского хомяка), DG44 и DUXB11 (линии яичника китайского хомяка, минус DHFR), HeLa (рак шейки матки человека), CVI (линия почек обезьяны), COS (производное от CVI с антигеном SV40 Т), VERY, BHK (почка новорожденного хомячка), MDCK, 293, WI38, R1610 (фибробласты китайского хомяка) BALBC/3T3 (фибробласт мыши), HAK (линия почек хомяка), SP2/O (миелома мыши), P3X63-Ag3.653 (миелома мыши), BFA-1c1BPT (бычьи эндотелиальные клетки), RAJI (лимфоциты человека) и 293 (почка человека). Линии клетки-хозяина, как правило, доступны от коммерческих поставщиков, Американская коллекции культур клеток или из опубликованной литературы.
[000175] Кроме того, может быть выбран, штамм клетки-хозяин, который модулирует экспрессию вставленных последовательностей или модифицирует и обрабатывает генный продукт конкретным желаемым образом. Такие модификации (например, гликозилирование) и обработка (например, расщепление) белковых продуктов могут быть важными для функции белка. Различные клетки-хозяева имеют характерные и специфические механизмы для пост-трансляционной обработки и модификации белков и генных продуктов. Соответствующие клеточные линии или системы хозяев могут быть выбраны для обеспечения правильной модификации и обработки экспрессированного чужеродного белка. С этой целью могут быть использованы эукариотические клетки-хозяева, которые обладают клеточным механизмом для правильного процессинга первичного транскрипта, гликозилирования и фосфорилирования генного продукта.
[000176] Для длительного продуцирования с высоким выходом рекомбинантных белков может быть использована стабильная экспрессия. Так, например, могут быть сконструированы клеточные линии, которые стабильно экспрессируют молекулы антитела. Вместо того чтобы использовать векторы экспрессии, которые содержат вирусные сайты инициации репликации, клетки-хозяева могут быть трансформированы ДНК под контролем соответствующих контрольных элементов экспрессии (например, промотора, энхансера, последовательности терминации транскрипции, сайта полиаденилированя и т.д.) и селективного маркера. После введения чужеродной ДНК сконструированные клетки могут расти в течение 1-2 суток в обогащенной среде, а затем переключается на селективные среды. Селектируемый маркер в рекомбинантной плазмиде придает устойчивость к селекции и позволяет клеткам стабильно интегрировать плазмиду в свои хромосомы и расти с образованием очагов, которые, в свою очередь, могут быть клонированы и размножены в клеточные линии. Этот метод с успехом может быть использован для конструирования клеточных линий, которые стабильно экспрессируют молекулу антитела.
[000177] Уровни экспрессии молекулы антитела могут быть увеличены путем усиления вектора (для обзора см. Bebbington and Hentschel (1987) "The Use of Vectors Based on Gene Amplification for the Expression of Cloned Genes in Mammalian Cells in DNA Cloning" (Academic Press, NY) Vol. 3. Когда маркер в векторной системе, экспрессирующей антитело является амплифицируемым, увеличение уровня ингибитора, присутствующего в культуре клетки-хозяина, приведет к увеличению числа копий гена-маркера. Поскольку усиленная область связана с геном антитела, продуцирование антител также будет увеличиваться (Crouse et al., Mol. Cell. Biol. 3:257 (1983)).
[000178] Продуцирование in vitro позволяет расширение масштабы с получением большого количества нужных полипептидов. Методики для культивирования клеток млекопитающих в условиях культуры ткани известны в данной области техники и включают однородную суспензионную культуру, например в реакторе с эрлифтом или в перемешивающем реакторе непрерывного действия или иммобилизованные или захваченные культуры клеток, например, в полых волокнах, микрокапсулах, на микрогранулах агарозы или керамических картриджах. При необходимости и/или при желании, растворы полипептидов, могут быть очищены обычными методами хроматографии, например, гель-фильтрацией, ионообменной хроматографией, хроматографией на DEAE-целлюлозе или (иммуно-)аффинной хроматографии, например, после биосинтеза синтетической шарнирной область полипептида или до или после стадии хроматографии HIC, описанной в данном документе.
[000179] Молекулы нуклеиновых кислот, кодирующие связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, также может быть экспрессирована в клетках, не являющихся клетками млекопитающих, таких как клетки насекомых, бактерий или дрожжей, или растений. Бактерии, которые легко принимают нуклеиновые кислоты включают члены энтеробактерий, такие как штаммы Escherichia coli или Salmonella; и Bacillaceae, такие как Bacillus subtilis; Pneumococcus; Streptococcus и Haemophilus influenzae. Следует также иметь в виду, что при экспрессии в бактериях, гетерологичные полипептиды, как правило, становятся частью телец включения. Тельца включения могут быть выделены, очищены и затем собраны в функциональные молекулы. Там, где тетравалентные формы антител желательны, субъединицы могут затем самособраны в четырехвалентные антитела (WO 02/096948 А2).
[000180] В бактериальных системах, ряд векторов экспрессии может быть преимущественно выбран в зависимости от предполагаемого использования для экспрессируемой молекулы антитела. Так, например, когда должно быть получено большое количество такого белка для создания фармацевтических композиций молекулы антитела, могут быть желательны векторы, которые направляют экспрессию высоких уровней слитых белковых продуктов, которые легко очищаются.
[000181] В дополнение к прокариотам, могут быть также использованы эукариотические микроорганизмы. Saccharomyces cerevisiae или обычные пекарские дрожжи, является наиболее часто используемым среди эукариотических микроорганизмов, хотя ряд других штаммов обычно также доступны, например, Pichia pastoris.
[000182] В системе насекомого, Autographa californica вирус ядерного полиэдроза (AcNPV), как правило, используются в качестве вектора для экспрессии чужеродных генов. Вирус растет в клетках Spodoptera frugiperda. Кодирующая последовательность антитела может быть клонирована индивидуально в несущественные области (например, ген полиэдрина) вируса и помещена под контроль промотора AcNPV (например, промотор полиэдрина).
[000183] После того, как связывающая молекула SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, были рекомбинантно экспрессированы, он может быть очищен любым способом, известным в данной области техники для очистки молекулы иммуноглобулина, например, с помощью хроматографии (например, ионообменной, аффинной, в частности, по сродству к белку А, и колоночной хроматографии по размеру), центрифугирования, дифференциальной растворимости или любым другим стандартным методом для очистки белков. В качестве альтернативы, способы увеличения аффинности антител, как предложено в данном документе, раскрыт в публикации заявки на патент США №20020123057 А1.
Методы лечения с использованием терапевтических антител против SEMA4D
[000184] Данное изобретение относится к способам применения связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, для лечения субъектов, имеющих заболевание или расстройство, связанное с патологией SEMA4D.
[000185] Следующее обсуждение относится к методам диагностики и лечения различных заболеваний и расстройств с помощью связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, например, способной специфически связывать SEMA4D, например, SEMA4D человека, мыши или человека и мыши, и имеющей нейтрализующую активность SEMA4D.
[000186] В одном аспекте в данном изобретении предложен способ нейтрализации SEMA4D у человека, включающий введение субъекту-человеку связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе,. В определенных аспектах субъект-человек, нуждающийся в лечении аутоиммунного заболевания или расстройства, воспалительного заболевания или расстройства, рака, нейровоспалительного заболевания или расстройства, нейродегенеративного заболевания или расстройства, или любой их комбинации. В определенных аспектах нейровоспалительное заболевание или расстройство представляет собой рассеянный склероз. В определенных аспектах нейродегенеративное заболевание или расстройство представляет собой инсульт, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, синдром Дауна, атаксию, боковой амиотрофический склероз (ALS), лобно-височную деменцию (FTD), связанное с ВИЧ когнитивное нарушение, волчанку ЦНС, умеренное когнитивное нарушение или их комбинацию. В определенных аспектах, аутоиммунное заболевание или воспалительное заболевание представляет собой артрит, например, ревматоидный артрит, атеросклероз (см., например, публикацию РСТ № WO 2015/054628, которая включена в данное описание в качестве ссылки в полном объеме), или остеодегенеративное заболевание, такое как остеопороз (см., например, патент США №9447191, который включен в данное описание в качестве ссылки в полном объеме).
[000187] В одном аспекте, лечение включает применение или введение связывающей молекулы против SEMA4D, например, антитела, или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, субъекту, или применение или введение в выделенную ткань или линию клеток от субъекта, причем субъект имеет заболевание, симптом заболевания или предрасположенность к заболеванию. В другом аспекте, лечение также включает применение или введение фармацевтической композиции, содержащей связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, субъекту, или в выделенную ткань или линию клеток от субъекта, имеющего заболевание, симптом заболевания или предрасположенность к заболеванию.
[000188] В одном аспекте, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть полезна для лечения рака, например, для лечения различных злокачественных и доброкачественных опухолей. Под «противоопухолевой активностью» подразумевают уменьшение скорости пролиферации злокачественных клеток или накопления, и, следовательно, снижения скорости роста существующей опухоли или опухоли, которая возникает во время терапии и/или разрушение существующих неопластических клеток (опухоли) или вновь образованных опухолевых клеток, и, следовательно, уменьшение общего размера опухоли во время терапии. Так, например, терапия со связывающей молекулой против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, может вызвать физиологическую реакцию, например, сокращение кровеносных сосудов или миграцию CTL к микросреде опухоли. Способы лечения рака со связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, можно найти, например, в публикации РСТ № WO 2014/209802 [комбинированная иммунотерапия], которая включена в данное описание в качестве ссылки в полном объеме.
[000189] В одном аспекте в данном изобретении предложена связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, для применения в качестве лекарственного средства, в частности, для применения в лечении или профилактике рака или для применения в предраковом состоянии или поражении.
[000190] В одном аспекте связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть полезна для лечения аутоиммунного заболевания или воспалительного заболевания. В одном аспекте связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, могут быть полезны для лечения нейровоспалительного или нейродегенеративного заболевания. Способы лечения нейровоспалительного или нейродегенеративного заболевания, могут быть найдены, например, в публикации РСТ № WO 2013/055922 [ВВВ], публикации РСТ № WO 2015/061330 [HD] и публикации РСТ № WO 2013/170221 [нейрогенез/инсульт], содержание которых включено в качестве ссылки в полном объеме.
[000191] В соответствии с методами, предусмотренными в данном документе, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть применена для содействия положительного терапевтического ответа по отношению к злокачественной клетке человека. Под термином «положительный терапевтический ответ» по отношению к лечению рака понимают положительный эффект в заболевании в сочетании с противоопухолевой активностью этих связывающих молекул, например, антитела или его фрагмента и/или улучшение симптомов, связанных с заболеванием. То есть, может наблюдаться антипролиферативное действие, предотвращение дальнейшего роста опухоли, уменьшение размера опухоли, уменьшение сосудистой сети опухоли, уменьшение количества раковых клеток, и/или уменьшение одного или более симптомов, связанных с заболеванием. Так, например, улучшение заболевания можно охарактеризовать как полный ответ. Под термином «полный ответ» подразумевают отсутствие клинически обнаруживаемых заболеваний с нормализации каких-либо аномальных ранее рентгенологических исследований, костного мозга и спинномозговой жидкости (CSF). В качестве альтернативы, улучшение заболевания может быть классифицировано как частичный ответ. Под «частичным ответом» понимают снижение по меньшей мере на 50% всех измеримых опухолевых нагрузок (то есть, числа опухолевых клеток, присутствующих у субъекта) в отсутствие новых поражений и сохраняющиеся в течение по меньшей мере, одного месяца. Такой ответ применим только к измеримым опухолям.
[000192] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, также может найти применение при лечении воспалительных заболеваний и недостатков или нарушений иммунной системы. Воспалительные заболевания характеризуются воспалением и разрушением тканей, или их комбинацией. Под «противовоспалительной активностью» подразумевают уменьшение или предотвращение воспаления. «Воспалительное заболевание» включает любой воспалительный иммунный опосредованный процесс, в котором инициирующее событии или мишень иммунного ответа включает не-самоантиген(ы), в том числе, например, аллоантигены, ксеноантигены, вирусные антигены, бактериальные антигены, неизвестные антигены или аллергены. В одном варианте осуществления воспалительное заболевание представляет собой воспалительное заболевание периферической или центральной нервной системы. В другом варианте осуществления воспалительное заболевание представляет собой воспалительное заболевание суставов.
[000193] Кроме того, термин «воспалительное заболевание(я)» включает «аутоиммунное заболевание(я)». Используемый в данном описании термин «аутоиммунный» обычно понимаются, как охватывающий иммунно-опосредованные воспалительные процессы, связанные с «собственными» антигенами. При аутоиммунных заболеваниях, собственные антиген(ы) выступают причиной иммунные реакции хозяина. Аутоиммунное заболевание может быть результатом несоответствующего иммунного ответа, направленного против собственного антигена (аутоантигена), который представляет собой отклонение от нормального состояния аутотолерантности. В общем, антитело (в частности, но не исключительно, антитело IgG, действуя в качестве цитотоксической молекулы или в виде иммунных комплексов, являются главными медиатором различных аутоиммунных заболеваний, многие из которых могут быть изнурительными или опасны для жизни.
[000194] В одном варианте осуществления связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть использована для лечения рассеянного склероза (PC). PC, также известный как рассеянный склероз или encephalomyelitis disseminata, представляет собой аутоиммунное заболевание, при котором иммунная система атакует центральную нервную систему, что приводит к демиелинизации. Название рассеянный склероз относится к шрамам (склерозы, также упоминается как бляшки или повреждение), которые образуются в нервной системе. Поражения PC обычно включают области белого вещества, близкие к желудочкам мозжечка, ствол мозга, базальные ганглии и спинной мозг, а также зрительный нерв. PC приводит к разрушению олигодендроцитов, клеток, ответственных за создание и поддержание миелиновой оболочки. PC приводит к истончению или полной потере миелина и, при развитии заболевания к перерезке аксонов.
[000195] Неврологические симптомы могут варьировать в зависимости от PC, и болезнь часто прогрессирует до физической и умственной инвалидности. PC принимает различные формы, с новыми симптомами происходит либо в дискретных приступах (рецидивирующей формы) или медленно накапливающихся с течением времени (прогрессивные формы). Между приступами, симптомы могут уйти полностью, но часто возникают постоянные неврологические повреждения, особенно по мере развития болезни.
[000196] Нейтрализация SEMA4D с использованием связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, может быть использовано для уменьшения тяжести PC через несколько различных механизмов, например, моноклональные антитела против SEMA4D могут блокировать иммунное созревание и активацию SEMA4D чтобы уменьшить скорость рецидива за счет уменьшения вторичных иммунных ответов на антигены ЦНС, а моноклональные антитела против SEMA4D могут блокировать действие растворимого SEMA4D в опосредовании апоптоза олигодендроцитов в ЦНС, что может снизить тяжесть заболевания за счет снижения демиелинизации.
[000197] В одном аспекте связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть использована для лечения артрита. Артрит представляет собой воспалительное заболевание суставов, которое может быть вызвано аутоиммунным состоянием, при котором иммунная система атакует суставы. В определенных вариантах осуществления артрит выбирают из группы, состоящей из остеоартрита, подагрического артрита, анкилозирующего спондилоартрита, псориатического артрита, реактивного артрита, ревматоидного артрита, юношеского ревматоидного артрита, инфекционного артрита, воспалительного артрита, септического артрита, дегенеративного артрита, arthritis mutilans и артрита Лайма. В одном варианте осуществления, артрит представляет собой ревматоидный артрит (РА).
[000198] Данное изобретение относится к способам лечения или профилактики артрита, путем введения субъекту связывающей молекулы против SEMA4D, представленной в данном документе. Способы, представленные в данном документе, могут уменьшить боль, отек или жесткость, связанные с артритом, например, ревматоидным артритом. В данном изобретении также предложены способы улучшения совместной производительности, функции и здоровья. В определенных вариантах осуществления данного раскрытия, лечение приводит к снижению оценки тяжести артрита, снижению тяжести/площади под кривой артрита, снижению параметров гистопатологии связанных с артритом (воспалению, паннусу, повреждению хряща и повреждению кости), уменьшению в сыворотке крови уровней арахидоновой кислоты или уменьшению антител против коллагена. В определенных вариантах осуществления, полезные или желаемые клинические результаты включают, но не ограничиваются ими, облегчение симптомов, связанных с артритом; профилактику артрита; задержку начала артрита; снижение заболеваемости артритом в популяции; уменьшение степени от состояний, связанных с артритом; стабилизацию (например, неухудшение) статуса патологического состояния, расстройства или заболевания, связанного с артритом; задержку начала или замедления состояния, расстройства или заболевания, связанного с прогрессированием артрита; улучшение состояния, расстройства или патологического состояния, ремиссию (частичную или полную) состояния, расстройства или заболевания, связанного с артритом, будь то в обнаружении или невозможности обнаружить; или увеличения или улучшения состояния, расстройства или заболевания, связанного с артритом.
[000199] Предлагаемые в данном документе способы могут быть использованы для лечения людей, которые имеют артрит или лиц, которые подвержены риску развития артрита. Таким образом, в некоторых вариантах осуществления в данном изобретении предложен способ лечения субъекта, имеющего нормальные суставы, пограничный артроз суставов, или сильно артрозные суставы, причем способ включает введение связывающей молекулы против SEMA4D, как предложено в данном документе, субъекту, описанному в данном документе. В некоторых вариантах осуществления способы, предложенные в данном документе, могут быть использованы для лечения хронического артрита в течение оставшейся части жизни субъекта.
[000200] В соответствии с методами, предусмотренными в данном документе, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть применена для способствования формированию положительного терапевтического ответа по отношению к лечению или профилактике аутоиммунного заболевания и/или воспалительного заболевания. Под термином «положительный терапевтический ответ» по отношению к аутоиммунному заболеванию и/или воспалительному заболеванию понимают облегчение заболевания в сочетании с противовоспалительной активностью, противоангиогенной активностью, противоапоптотической активностью, или тому подобному данных антител, и/или облегчению симптомов, связанных с заболеванием. То есть можно наблюдать, антипролиферативное действие, предотвращение дальнейшего распространения SEMA4D-экспрессирующих клеток, снижение воспалительной реакции, включая, без ограничения, пониженную секрецию провоспалительных цитокинов, молекул адгезии, протеаз, иммуноглобулинов (в тех случаях, когда клетка, несущая SEMA4D, представляет собой В-клетку), их комбинации и тому подобное, увеличение производства противовоспалительных белков, снижение числа аутореактивных клеток, повышение иммунной толерантности, ингибирование выживания аутореактивных клеток, уменьшение апоптоза, уменьшение эндотелиальной миграция клеток, увеличение спонтанной миграции моноцитов, уменьшение и/или облегчение одного или более симптомов, опосредованных стимуляцией sSEMA4D или SEMA4D-экспрессирующих клеток. Такие положительные терапевтические ответы не ограничиваются путями введения и могут включать введение донору, в ткань донора (такую как, например перфузия органа), хозяину, любую их комбинацию, и тому подобные.
[000201] Клинический ответ может быть оценен с использованием методов скрининга, таких как магнитно-резонансная томография (МРТ), Х-рентгенографических изображений, компьютерное томографическое (КТ), анализ проточной цитометрит или флуоресценцентно активированная сортировка клеток (FACS), гистологию, макропатологию и химический анализ крови, включая, без ограничения изменения обнаруживаемые с помощью ИФА, РИА, хроматографии и тому подобного. В дополнении к этим положительным терапевтическим реакциям, субъект проходит лечение с помощью связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, может испытывать благотворное влияние на улучшении симптомов, связанных с этим заболеванием.
[000202] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть использована в комбинации с по меньшей мере одной другой терапией против рака, включая, без ограничения, хирургическое вмешательство или хирургическая процедура; иммуномодулирующая терапия, лучевая терапия; химиотерапия, необязательно в сочетании с аутогенной трансплантацией костного мозга, или другой терапией против рака; причем дополнительная терапию против рака применяют до, во время или после терапии связывающей молекулой против SEMA4D, например, антителом или его антигенсвязывающим фрагментом. Таким образом, когда объединенные методы лечения включают введение связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, как предложено в данном документе, в сочетании с введением другого терапевтического средства, как и при химиотерапии, лучевой терапии, других противораковых терапиях антителами, терапии рака на основе малой молекулы, или терапии рака на основе вакцины/иммунотерапии, способы, представленные в данном документе, включают совместное введение с использованием отдельных препаратов или одного фармацевтического препарата, или и последовательное введение в любом порядке.
[000203] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть использована в сочетании с любыми известными терапиями для лечения аутоиммунных и воспалительных заболеваний, в том числе любого агента или комбинации агентов, которые, как известно, полезны, или которые были использованы или используются в данное время, для лечения аутоиммунных и воспалительных заболеваний. Таким образом, когда объединенные методы лечения включают введение связывающей молекулы против SEMA4D в сочетании с введением другого терапевтического средства, способы, представленные в данном документе, включают совместное введение с использованием отдельных препаратов или одного фармацевтического препарата, или и последовательное введение в любом порядке. В некоторых вариантах осуществления антитела против SEMA4D, описанные в данном документе, вводят в сочетании с иммунодепрессантами или противовоспалительными лекарственными средствами, причем антитело и терапевтический агент(ы) могут быть введены последовательно, в любом порядке или одновременно (т.е. параллельно или в один период времени).
[000204] В определенных аспектах, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть применена отдельно или в сочетании с иммунодепрессантами для лечения и/или профилактики ревматоидного артрита. Как обсуждалось выше, эффективность лечения может быть оценена с использованием любых средств и включает, но не ограничивается ими, эффективность, измеренную с помощью клинических реакций, определенных Американским колледжем критериев ревматологии, Европейской лигой критериев ревматизма, или каким-либо другим критерием. См., например, Felson et al., Arthritis. Rheum. 38:727-35 (1995) и van Gestel et al., Arthritis Rheum. 39:34-40 (1996).
[000205] В других аспектах, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть применена отдельно или в сочетании с иммунодепрессантами для лечения и/или профилактики рассеянного склероза.
[000206] Еще одним аспектом данного изобретения является применение связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, для диагностического мониторинга уровней белка в ткани, как части процедуры клинических испытаний, например, для определения эффективности данного режима лечения. Например, обнаружение может быть облегчено путем связывания антитела с детектируемым веществом. Примеры детектируемых веществ включают различные ферменты, простетические группы, флуоресцентные материалы, люминесцентные материалы, биолюминесцентные материалы и радиоактивные материалы. Примеры подходящих ферментов включают пероксидазу хрена, щелочную фосфатазу, β-галактозидазу или ацетилхолинэстеразу; примеры подходящих простетических групп включают стрептавидин/биотин и авидин/биотин; примеры подходящих флуоресцентных материалов включают умбеллиферон, флуоресцеин, флуоресцеинизотиоцианат, родамин, дихлортриазиниламин флуоресцеина, дансилхлорид или фикоэритрин; пример люминесцентного материала включает люминол; примеры биолюминесцентных материалов включают люциферазу, люциферин и экворин; а примеры подходящего радиоактивного материала включают 125I, 131I, 35S или 3Н.
VIII. Фармацевтические композиции и способы введения
[000207] Способы получения и введения связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, субъекту, нуждающемуся в этом, хорошо известны или могут быть легко определены специалистами в данной области техники. Путь введения связывающей молекулы против SEMA4D может представлять собой, например, пероральный, парентеральный, ингаляционный или местный. Термин парентеральный, используемый в данном документе, включает, например, внутривенное, внутриартериальное, внутрибрюшинное, внутримышечное, подкожное, ректальное или вагинальное введение. Хотя все эти формы введения, рассматриваются как находящиеся в пределах объема данного описания, пример формы для введения будет представлять собой раствор для инъекций, в частности, для внутривенной или внутриартериальной инъекции или капельного внутривенного вливания. Обычно подходящая фармацевтическая композиция для инъекций может содержать буфер (например, ацетатный, фосфатный или цитратный буфер), поверхностно-активное вещество (например, полисорбат), необязательно стабилизирующий агент (например, альбумин человека) и т.д. Тем не менее, в других способах, совместимых с излагаемыми в данном документе, связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть доставлена непосредственно в место неблагоприятного условия, например, в солидную опухоль, тем самым увеличивая воздействие на пораженную ткань терапевтического агента.
[000208] Связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, можно вводить в фармацевтически эффективном количестве in vivo для лечения SEMA4D-опосредованных заболеваний, таких как рак, аутоиммунные заболевания, воспалительные заболевания, включая воспалительные заболевания центральной нервной системы (ЦНС) и периферической нервной системы (ПНС), нейродегенеративных заболеваний и инвазивного ангиогенеза. В связи с этим следует понимать, что раскрытые связывающие молекулы, могут быть приготовлены таким образом, чтобы облегчить введение и способствовать стабильности активного агента. В определенных аспектах, фармацевтические композиции, предложенные в данном документе, могут включать фармацевтически приемлемый, нетоксичный, стерильный носитель, такой как физиологический раствор, нетоксичные буферы, консерванты и тому подобное. Для целей данной заявки, фармацевтически эффективного количества связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как представлено в данном документе, конъюгированной или неконъюгированной, означает количество, достаточное для достижения эффективного связывания с мишенью и для достижения эффекта, например, для облегчения симптомов заболевания или расстройства, или обнаружения вещества, или клетки.
[000209] Фармацевтические композиции, используемые в данном описании, включают фармацевтически приемлемые носители, включая, например, ионообменные вещества, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как сульфат протамина, вторичный кислый фосфат натрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, карбоксиметилцеллюлозу натрия, полиакрилаты, воски, полиэтилен-полиоксипропилен блок-сополимеры, полиэтиленгликоль и ланолин.
[000210] Препараты для парентерального введения включают, без ограничения, стерильные водные или неводные растворы, суспензии и эмульсии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и инъецируемые органические сложные эфиры, такие как этилолеат. Водные носители включают, например, воду, спиртовые/водные растворы, эмульсии или суспензии, в том числе солевые и буферные среды. Фармацевтически приемлемые носители включают, но не ограничиваются ими, 0,01-0,1 М, например, 0,05 М фосфатный буфер или 0,8% физиологический раствор. Другие общие парентеральные носители включают растворы фосфата натрия, декстрозу Рингера, декстрозу и хлорид натрия, лактат Рингера или нелетучие масла. Внутривенные носители включают жидкие и питательные добавки, добавки электролитов, такие как на основе декстрозы Рингера, и тому подобное. Также могут присутствовать консерванты и другие добавки такие, как, например, противомикробные средства, антиоксиданты, хелатирующие агенты и инертные газы и тому подобное.
[000211] В некоторых аспектах, фармацевтические композиции, подходящие для применения в виде инъекций, включают стерильные водные растворы (где водорастворимые) или дисперсии и стерильные порошки для незапланированного приготовления стерильных инъекционных растворов или дисперсий. В таких случаях композиция должна быть стерильной и должна быть жидкой до такой степени, чтобы свободно помещаться в шприц. Она должна быть стабильной в условиях производства и хранения и может быть защищена от загрязняющего действия микроорганизмов, таких как бактерии и грибы. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.) и их подходящие смеси. Текучесть может поддерживаться, например, за счет использования покрытия, такого как лецитин, путем поддержания требуемого размера частиц в случае дисперсии и использованием поверхностно-активных веществ. Подходящие композиции для применения в терапевтических способах, раскрытые в данном описании, описаны в Remington Pharmaceutical Sciences (Mack Publishing Co.) 16th ed. (1980).
[000212] Предотвращение действия микроорганизмов может быть достигнуто с помощью различных антибактериальных и противогрибных агентов, например, парабенов, хлорбутанола, фенола, аскорбиновой кислоты, тимерозала и тому подобных. В некоторых аспектах изотонические агенты, например сахара, многоатомные спирты, такие как маннит, сорбит или хлорид натрия, могут быть включены в композицию. Пролонгированное всасывание инъекционных композиций может быть осуществлено путем включения в композиции агента, который задерживает абсорбцию, например, моностеарата алюминия и желатина.
[000213] В любом случае, стерильные инъекционные растворы могут быть получены путем включения активного соединения (например, связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, самой по себе или в сочетании с другими активными агентами) в требуемом количестве в соответствующий растворитель с одним или комбинацией ингредиентов, перечисленных в данном описании, в случае необходимости, с последующей стерилизацией путем фильтрования. Как правило, дисперсии получают путем введения активного соединения в стерильный носитель, который содержит основную дисперсионную среду и требуемые другие ингредиенты из тех, которые перечислены выше. В случае стерильных порошков для приготовления стерильных инъекционных растворов, способы получения могут включать вакуумную сушку и сушку вымораживанием, что обеспечивает порошок активного ингредиента плюс любого дополнительного желательного ингредиента из предварительно стерильно отфильтрованного раствора. Препараты для инъекций обрабатывают, разливают в контейнеры, такие как ампулы, мешки, бутылки, шприцы или флаконы, и запечатывают в асептических условиях в соответствии со способами, известными в данной области техники. Кроме того, препараты могут быть упакованы и проданы в форме набора, такого как тот, что описан в заявке на патент США №09/259337. Такие изделия могут иметь этикетки или вкладыши, указывающие, что связанные с ними композиции полезны для лечения пациента, страдающего от или предрасположенного к заболеванию или расстройству.
[000214] Парентеральные композиции могут представлять собой разовую болюсную дозу, инфузию или загрузочную болюсную доза с последующей поддерживающей дозой. Эти композиции могут быть введены в определенные фиксированные или переменные интервалы, например, один раз в сутки или «по требованию».
[000215] Некоторые фармацевтические композиции, предложенные в данном описании могут быть введены перорально в приемлемой лекарственной форме, включая, например, капсулы, таблетки, водные суспензии или растворы. Некоторые фармацевтические композиции также могут быть введены с помощью назального аэрозоля или ингаляции. Такие композиции могут быть приготовлены в виде растворов в физиологическом растворе с использованием бензилового спирта или других подходящих консервантов, стимуляторов абсорбции для повышения биологической доступности и/или других обычных солюбилизирующих или диспергирующих агентов.
[000216] Количество связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, как предложено в данном документе, которая может быть объединена с материалами-носителями для получения разовой лекарственной формы, будет изменяться в зависимости от подвергаемого лечения пациента и конкретного способа введения. Композицию можно вводить в виде разовой дозы, множественных доз или в течение установленного периода времени в инфузии. Схема дозировки также могут быть скорректированы, чтобы обеспечить оптимальный желаемый ответ (например, терапевтический или профилактический ответ).
[000217] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, можно вводить человеку или другому животному в соответствии с вышеупомянутыми способами лечения в количестве, достаточном для получения терапевтического эффекта. Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, можно вводить человеку или другому животному в обычной лекарственной форме, полученной путем комбинирования антитела с обычным фармацевтически приемлемым носителем или разбавителем в соответствии с известными методиками. Специалистом в данной области техники будет понятно, что форма и характер фармацевтически приемлемого носителя или разбавителя диктуется количеством активного ингредиента, с которым он должен быть объединен, путь введения и другими хорошо известными переменными.
[000218] Под «терапевтически эффективной дозой или количеством» или «эффективным количеством» понимают количество связывающей молекулы против SEMA4D, например, варианта антитела или его антигенсвязывающего фрагмента, или производного, как предложено в данном документе, которое при введении приводит к положительному терапевтическому ответу в отношении лечения пациента с заболеванием, подлежащим лечению.
[000219] Терапевтически эффективные дозы композиций, как через предусмотренные в данном описание для лечения SEMA4D-опосредованных заболеваний, таких как рак; аутоиммунные заболевания, например, артрит, рассеянный склероз, воспалительные заболевания, включая воспалительные заболевания центральной нервной системы (ЦНС) и периферической нервной системы (ПНС); нейродегенеративные заболевания и инвазивный ангиогенез, варьируется в зависимости от многих различных факторов, в том числе посредством введения, целевого сайта, физиологического состояния пациента, является ли пациент человеком или животным, другие лекарственные препараты вводят, и является ли лечение профилактическим или терапевтическим. Как правило, пациент является человеком, но млекопитающие, не являющиеся человеком, в том числе трансгенные млекопитающие, могут также быть подвергнуты лечению. Дозы лечения могут быть титрованы с использованием обычных методов, известных специалистам в данной области техники с целью оптимизации безопасности и эффективности.
[000220] Количество связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или его производного, как предложено в данном документе, для введения легко определяется обычным специалистом в данной области техники без излишнего экспериментирования. Факторы, влияющие на способ введения и соответствующее количество связывающей молекулы против SEMA4D включают, но не ограничиваются ими, тяжести заболевания, истории заболевания и возраст, рост, массу, здоровье и физическое состояние индивидуума, который проходит курс лечения. Аналогичным образом, количество связывающей молекулы против SEMA4D для введения, будет зависеть от способа введения, и будет ли субъект получать одну дозу или несколько доз этого агента.
[000221] В данном изобретении также предложено применение связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, в производстве лекарственного средства для лечения аутоиммунного заболевания и/или воспалительного заболевания, в том числе, например, артрита, рассеянного склероза, воспалительных заболеваний ЦНС и ПНС, нейродегенеративных заболеваний или рака.
[000222] В данном изобретении также предложено применение связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, варианта, или производного, в производстве лекарственного средства для лечения аутоиммунного заболевания и/или воспалительного заболевания, в том числе, например, артрита, рассеянного склероза, воспалительных заболеваний ЦНС и ПНС, нейродегенеративных заболеваний или рака, причем, лекарственное средство применяют к субъекту, который был предварительно лечен, по меньшей мере, одной другой терапией. Под «предварительно леченым» или «предварительным лечением» понимают, что субъект получал одну или более других видов терапии (например, были лечены по меньшей мере одной другой терапией против рака) до приема лекарственного средства, содержащего связывающую молекулу против SEMA4D. «Предварительно леченый» или «предварительное лечение» понимают, что субъекты, которые были лечены по меньшей мере одной другой терапией в течение 2 лет, в течение 18 месяцев, в течение 1 года, в течение 6 месяцев, в течение 2 месяцев, в течение 6 недель, в течение 1 месяца, в течение 4 недель, в течение 3 недель, в течение 2 недель, в течение 1 недели, в течение 6 суток, в течение 5 суток, в течение 4 суток, в течение 3 суток, в течение 2 суток или даже в течение 1 суток до начала лечения лекарственным средством, содержащего связывающие молекулы против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как представлено в данном документе. Это не обязательно, чтобы субъект был респондером по предварительному лечению предварительной терапией или терапией. Таким образом, субъект, который принимает лекарственное средство, содержащее связывающую молекулу против SEMA4D мог бы быть респондером, или мог не реагировать (например, рак был невосприимчив) на предварительное лечение предварительной терапией, или к одному или более из предварительных терапии где предварительных лечений, включающих несколько терапий. Примеры других терапий лечения рака, для которых субъект может получать предварительное лечение до приема лекарственного средства, содержащего связывающую молекулу против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, включают, без ограничения, операции; радиационную терапию; химиотерапию, необязательно в сочетании с аутогенной трансплантации костного мозга; другие противораковые терапии моноклональным антителом, терапии рака на основе малой молекулы, или терапии рака на основе вакцины/иммунотерапии, стероидные терапии; другие терапии рака; или любую их комбинацию.
IX. Диагностика
[000223] В данном изобретении дополнительно предложен способ диагностики, полезный в ходе диагностики SEMA4D-опосредованного заболевания, такого как некоторые виды рака, аутоиммунные заболевания, воспалительные заболевания, в том числе, например, артрит, рассеянный склероз, воспалительные заболевания центральной нервной системы (ЦНС) и периферической нервной системы (ПНС), нейродегенеративные заболевания, и инвазивный ангиогенез, который включает измерение уровня экспрессии белка SEMA4D или транскрипта в ткани или других клетках или жидкости организма от индивидуума и сравнение измеренного уровня экспрессии со стандартным уровнем экспрессии SEMA4D в нормальной ткани или жидкости организма, в результате чего увеличение уровня экспрессии по сравнению со стандартом является показателем расстройства.
[000224] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе могут быть использованы для анализа уровни белка SEMA4D в биологическом образце с использованием классических иммуногистологических методов, известных специалистам в данной области техники (например, см Jalkanen, et al., J. Cell. Biol. 101:976-985 (1985); Jalkanen et al., J. Cell Biol. 105:3087-3096 (1987)). Другие методы на основе антител, используемые для обнаружения экспрессии белка SEMA4D включают иммунологические, такие как твердофазный иммуноферментный анализ (ИФА), иммунопреципитация или Вестерн-блоттинг. Подходящие анализы описаны более подробно в данном документе в другом месте.
[000225] Под «оценкой уровня экспрессии полипептида SEMA4D» понимают качественное или количественное измерение или оценку уровня полипептида SEMA4D в первом биологическом образце, либо непосредственно (например, путем определения или оценки абсолютного уровня белка) или относительно (например, путем сравнения со связанным с заболеванием уровнем полипептида во втором биологическом образце). В некоторых аспектах, уровень экспрессии полипептида SEMA4D в первом биологическом образце может быть измерен или оценен, и сопоставлен со стандартным уровнем полипептида SEMA4D, за стандарт принимают второй биологический образец, полученный у индивидуума, не имеющее расстройства, или он определяется путем усреднения уровней от популяции индивидуумов, не имеющих расстройства. Как будет понятно в данной области техники, после того, как «стандартный» уровень полипептида SEMA4D станет известен, он может быть использован повторно в качестве стандарта для сравнения.
[000226] Под термином «биологический образец» подразумевают любой биологический образец, полученный от индивидуума, клеточной линии, культуры ткани или другого источника клеток, потенциально экспрессирующих SEMA4D. Способы получения биопсии ткани и жидкости организма от млекопитающих хорошо известны в данной области техники.
X. Иммунологические анализы
[000227] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, может быть проанализирована на иммуноспецифическое связывание любым способом, известным в данной области техники. Иммунологические анализы, которые могут быть использованы, включают, но не ограничиваются ими, конкурентные и неконкурентные тест-системы с использованием методов, таких как Вестерн-блоттинг, радиоиммуноанализы, ИФА (твердофазный иммуноферментный анализ), «сэндвич» иммуноанализ, иммунопреципитацию, реакции преципитации, реакции диффузной гель преципитации, иммунодиффузные анализы, агглютинации, анализы связывания комплемента, иммунорадиометрические анализы, флуоресцентные иммунологические анализы, иммунологические анализы с белком А, однако не ограничиваются ними. Такие анализы являются обычными и хорошо известны в данной области техники (см, например, Ausubel et al., eds, (1994) Current Protocols in Molecular Biology (John Wiley & Sons, Inc., NY) Vol. 1, которая включена в данное описание посредством ссылки в полном объеме). Типичные иммунологические анализы кратко описаны ниже (но не предназначены для ограничения).
[000228] Связывающая молекула против SEMA4D, например, антитело или его антигенсвязывающий фрагмент, вариант, или производное, как предложено в данном документе, кроме того, могут быть использованы гистологически, как и в иммунофлуоресценции, иммуноэлектронной микроскопии или не-иммунологических анализах, для обнаружения SEMA4D белка in situ или их консервированных вариантов, или пептидных фрагментов. Выявление in situ может быть осуществлено путем отбора гистологического образца у пациента, и применения к нему меченого антитела против SEMA4D или его антигенсвязывающего фрагмента, например, путем наложения меченого антитела (или фрагмента) на биологический образец. Благодаря использованию такой процедуры, можно определить не только присутствие белка SEMA4D, или консервативных вариантов или пептидных фрагментов, но и его распределение в исследуемой ткани. С помощью данного изобретения, обычному специалисту будет легко воспринять, что любой из широкого спектра гистологических методов (таких, как процедуры окрашивания) можно модифицировать для того, чтобы достичь такого обнаружения in situ.
[000229] Связывающая активность данной партии связывающей молекулы против SEMA4D, например, антитела или его антигенсвязывающего фрагмента, вариант, или производного, как предложено в данном документе, могут быть определены в соответствии с хорошо известными способами. Специалисты в данной области техники будут способны определить рабочие и оптимальные условия анализа для каждого определения с использованием рутинного экспериментирования.
[000230] Есть множество способов, доступных для измерения аффинности взаимодействия антиген-антитело, но относительно мало для определения констант скорости. Большинство методов полагается на любое мечение антитела или антигена, что неизбежно усложняет рутинные измерения и вводит неопределенности в измеряемых величинах.
[000231] Поверхностный плазмонный резонанс (SPR), выполненный на BIACORE® предлагает ряд преимуществ по сравнению с традиционными методами измерения аффинности взаимодействий антиген-антител: (i) отсутствие необходимости метить ни антитело, ни антиген; (ii) антитела не должны быть очищены заранее, может быть использован непосредственно супернатант клеточной культуры; (iii) измерения в реальном времени, позволяют быстро в полу-количественном виде сравнить различные взаимодействия моноклональных антител, которые включены и являются достаточными для многих целей оценки; (iv) биоспецифическая поверхность может быть восстановлена таким образом, чтобы ряд различных моноклональных антител легко можно было сравнить в одинаковых условиях; (v) аналитические процедуры полностью автоматизированы, и обширные серии измерений могут быть выполнены без вмешательства пользователя. BIAapplications Handbook, version АВ (reprinted 1998), BIACORE® code No. BR-1001-86; BIAtechnology Handbook, version AB (reprinted 1998), BIACORE® code No. BR-1001-84. Исследования связывания на основе ППР требуют, чтобы один член связывающей пары быть иммобилизован на поверхности датчика. Иммобилизованный связывающий партнер упоминается в качестве лиганда. Связывающий партнер в растворе называется аналит. В некоторых случаях, лиганд присоединен опосредованно к поверхности через связывание с другой иммобилизованной молекулой, которая называется молекулой захвата. Ответ ППР отражает изменение массовой концентрации на поверхности детектора, когда аналиты связываются или диссоциируют.
[000232] На основе ППР, в режиме реального времени измерения BIACORE® позволяют осуществлять мониторинг взаимодействий непосредственно, как они происходят. Метод хорошо подходит для определения кинетических параметров. Ранжирование сравнительной аффинности легко осуществить, и обе константы - кинетики и аффинности могут быть получены из данных сенсограммы.
[000233] Когда аналит пропускают дискретно через поверхность лиганда, полученную сенсограмму можно разделить на три основных этапа: (i) ассоциация аналита с лигандом во время инъекции образца; (ii) равновесие или стационарное состояние во время инъекции пробы, при котором уровень связывания аналита уравновешивается диссоциациями комплекса; (iii) диссоциация анализируемого вещества с поверхности во время пропускания потока буфера.
[000234] Фазы ассоциации и диссоциации предоставляют информацию о кинетике взаимодействия аналит-лиганд (ka и kd, скорости образования и диссоциации комплекса, kd/ka=KD). Равновесная фаза содержит информацию об аффинности взаимодействия аналит-лиганд (KD).
[000235] Программное обеспечение BIAevaluation предоставляет комплексные средства для аппроксимации кривой, используя как численное интегрирование так и глобальные подходящие алгоритмы. При соответствующем анализе данных, отдельные скорости и константа аффинности для взаимодействия могут быть получены из простого исследования BIACORE®. Диапазон измеримой аффинности по этой технологии очень широк, начиная от мМ и до пМ.
[000236] Специфичность эпитопа является важной характеристикой моноклонального антитела. Картирование эпитопа с BIACORE®, в отличие от обычных методов с использованием радиоиммуноанализа, ИФА или других методов адсорбции на поверхности, не требует маркировки или очищенные антитела, а также позволяет проводить тесты специфичности нескольких сайтов с использованием последовательности из нескольких моноклональных антител. Кроме того, большое количество анализов могут быть обработаны автоматически.
[000237] Попарные эксперименты по связыванию позволяют проверить способность двух MAb одновременно связываться с одним антигеном. MAb, направленные против отдельных эпитопов будут связываться независимо друг от друга, в то время как MAb, направленные против идентичных или близкородственных эпитопов будут мешать друг другу связываться. Эти эксперименты BIACORE® по связыванию просты в осуществлении.
[000238] Например, можно использовать молекулу захвата, чтобы связать первое Mab с последующим добавлением антигена и второго MAb последовательно. В сенсограммах будет отображено: (1) сколько антигенов связывается с первым Mab, (2) до какой степени второе MAb связывается с поверхностно-соединенным антигеном, (3) если второе MAb не связывается, изменит ли порядок попарного теста результаты.
[000239] Ингибирование пептида еще один метод, используемый для картирования эпитопов. Этот метод может дополнять попарные исследования антител и может объединять функциональные эпитопы по структурным признакам, когда первичная последовательность антигена известна. Пептиды или фрагменты антигена тестировали на ингибирование связывания различных MAb с иммобилизованным антигеном. Пептиды, которые препятствуют связыванию данного MAb считаются структурно связанными с эпитопом, определенным данным MAb.
[000240] В данном изобретении используют, если не указано иное, обычные методы клеточной биологии, клеточной культуры, молекулярной биологии, трансгенной биологии, микробиологии, рекомбинантной ДНК и иммунологии, которые известны специалистам в данной области техники. Такие методы подробно описаны в литературе. См, например, Sambrook et al., ed. (1989) Molecular Cloning A Laboratory Manual (2nd ed.; Cold Spring Harbor Laboratory Press); Sambrook et al., ed. (1992) Molecular Cloning: A Laboratory Manual, (Cold Springs Harbor Laboratory, NY); D.N. Glover ed., (1985) DNA Cloning, Volumes I and II; Gait, ed. (1984) Oligonucleotide Synthesis; Mullis et al. патент США №4683195; Hames and Higgins, eds. (1984) Nucleic Acid Hybridization; Hames and Higgins, eds. (1984) Transcription And Translation; Freshney (1987) Culture Of Animal Cells (Alan R. Liss, Inc.); Immobilized Cells And Enzymes (IRL Press) (1986); Perbal (1984) A Practical Guide To Molecular Cloning; the treatise, Methods In Enzymology (Academic Press, Inc., N.Y.); Miller and Calos eds. (1987) Gene Transfer Vectors For Mammalian Cells, (Cold Spring Harbor Laboratory); Wu et al., eds., Methods In Enzymology, Vols. 154 and 155; Mayer and Walker, eds. (1987) Immunochemical Methods In Cell And Molecular Biology (Academic Press, London); Weir and Blackwell, eds., (1986) Handbook Of Experimental Immunology, Volumes I-IV; Manipulating the Mouse Embryo, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., (1986); and in Ausubel et al. (1989) Current Protocols in Molecular Biology (John Wiley and Sons, Baltimore, Md.).
[000241] Общие принципы проектирования антител изложены в Borrebaeck, ed. (1995) Antibody Engineering (2nd ed.; Oxford Univ. Press). Общие принципы белковой инженерии изложены в Rickwood et al., eds. (1995) Protein Engineering, A Practical Approach (IRL Press at Oxford Univ. Press, Oxford, Eng.). Общие принципы антител и связывания антитело-гаптен изложены в: Nisonoff (1984) Molecular Immunology (2nd ed.; Sinauer Associates, Sunderland, Mass.) и Steward (1984) Antibodies, Their Structure and Function (Chapman and Hall, New York, N.Y.). Кроме того, стандартные методы в области иммунологии, известные в данной области техники и конкретно не описанные могут быть теми, что раскрыты в Current Protocols in Immunology, John Wiley & Sons, New York; Stites et al., eds. (1994) Basic and Clinical Immunology (8th ed; Appleton & Lange, Norwalk, Conn.) и Mishell and Shiigi (eds) (1980) Selected Methods in Cellular Immunology (W.H. Freeman and Co., NY).
[000242] Стандартные работы, устанавливающие общие принципы иммунологии, включают Current Protocols in Immunology, John Wiley & Sons, New York; Klein J., Immunology: The Science of Self-Nonself Discrimination (John Wiley & Sons, NY (1982)); Kennett et al., eds. (1980) Monoclonal Antibodies, Hybridoma: A New Dimension in Biological Analyses (Plenum Press, NY); Campbell (1984) "Monoclonal Antibody Technology" in Laboratory Techniques in Biochemistry and Molecular Biology, ed. Burden et al., (Elsevier, Amsterdam); Goldsby et al., eds. (2000) Kuby Immunology (4th ed.; W.H. Freeman and Co., NY); Roitt et al. (2001) Immunology (6th ed.; London: Mosby); Abbas et al. (2005) Cellular and Molecular Immunology (5th ed.; Elsevier Health Sciences Division); Kontermann and Dubel (2001) Antibody Engineering (Springer Verlag); Sambrook and Russell (2001) Molecular Cloning: A Laboratory Manual (Cold Spring Harbor Press); Lewin (2003) Genes VIII (Prentice Hall, 2003); Harlow and Lane (1988) Antibodies: A Laboratory Manual (Cold Spring Harbor Press); Dieffenbach and Dveksler (2003) PCR Primer (Cold Spring Harbor Press).
[000243] Все ссылки, приведенные выше, а также все ссылки, приведенных в данном описании, включены в данное описание посредством ссылок в полном объеме.
[000244] Следующие примеры предлагаются в качестве иллюстрации, а не в качестве ограничения.
Примеры
Пример 1. Создание полностью человеческого моноклонального антитела MAb D2517 против SEMA4D
[000245] Полностью человеческое моноклональное антитело D2517 против SEMA4D было создано с помощью следующего способа. Библиотеки полностью человеческих антител создавали в вирусе коровьей оспы, и подвергали скринингу на связывание с SEMA4D в соответствии со способами, описанными в публикации заявки на патент США №2013-0288927-А1, которая включена в данное описание в качестве ссылки в полном объеме. В общей сложности 96 антител были сгруппированы в шесть различных групп эпитопов посредством испытания с помощью ИФА. Конкурентное связывание антител человека с нативной формой SEMA4D человека на клетках Jurkat оценивали с использованием антител мыши - mAb76 и mAb67 и контрольного IgG мыши. mAb76 и mAb67 связываются с известными эпитопов SEMA4D человека, и конкуренция с любым из них указывает на функциональность. Клетки Jurkat предварительно инкубировали в течение 30 минут на льду с mAb76, mAb67 или контрольным IgG мыши при 5 мкг/мл в 100 мкл и 200000 клеток в буфере FACS (1X PBS + 0,05% БСА + 2 мМ ЭДТА). Это обеспечило насыщению связывания антител мыши блокировать связывание эпитопов. Тестируемые антитела и контрольные антитела человека предварительно инкубировали при 1 мкг/мл на льду в течение 30 минут с реагентом вторичного козьего антитела-Dylight 649 против Fc человека (Jackson Immunoresearch 496-170). После инкубации клеток Jurkat с антителами IgG мыши, клетки промывали и инкубировали с тестовыми антителами/смесью вторичного комплекса в течение 30 минут на льду. Затем клетки промывали два раза 200 мкл буфера FACS и ресуспендировали в фиксирующем растворе 250 мкл PBS/1% БСА и 0,5% параформальдегида с PI. После ресуспендирования клетки анализировали с помощью проточной цитометрии на FACS CANTO II. Популяцию негативного PI гейтировали, а сдвиг Dylight649 фиксировали и оценивали. Процент ингибирование связывания было рассчитано по сравнению со связыванием антител человека с клетка Jurkat, предварительно инкубированными с нерелевантным IgG мыши.
[000246] MAb С2305 был выбран для дальнейшей характеристики из-за его способности к перекрестному блокированию ранее охарактеризованных мышиных антител D67-2 и 76-1 против SEMA4D. См, например, патент США №8496938, описание которой включено в данное описание в качестве ссылки в полном объеме.
[000247] Полинуклеотид, кодирующий VH MAb С2305 клонировали в вектор экспрессии млекопитающих, который содержал кодирующую последовательность константной области тяжелой цепи человека гамма-4, создавая полноразмерную тяжелую цепь. Полинуклеотид, кодирующий VL MAb С2305 клонировали в вектор экспрессии млекопитающих, который содержал кодирующую последовательность константной области лямбда, создавая полноразмерную легкую цепь. Векторы экспрессии, содержащие тяжелую цепь и легкую цепь, были совместно трансфицированы в клетки CHO-S. Моноклональное антитело, которое было получено, секретировали из клеток и собирали после 3-6-суточного периода экспрессии. Полученный MAb очищали с помощью белок А хроматографии и характеризовали. С помощью проточной цитометрии и ИФА было продемонстрировано, что полученное полностью человеческое MAb (MAb С2305) является специфичным в отношении SEMA4D, и имеет возможность конкурировать с мышиным MAb 67-2 за связывание с SEMA4D. Функциональную активность MAb С2305 далее оценивали в анализе блокирования рецептора в соответствии со способом, описанным в примере 3, ниже. Блокирование рецептора наблюдалось, но на более низком уровне, чем у гуманизированного MAb 2503 (патент США №8496938, также упоминаемый как VX15/2503), который был использован в качестве компаратора.
[000248] MAb С2305 было полностью секвенировано, а затем было модифицировано для улучшения аффинности. Область, определяющую комплементарность тяжелой цепи 3 (HCDR3) подвергали стандартными методикам сайта-направленного мутагенеза, и новую полностью человеческую вариабельную область легкой цепи (VL) идентифицировали из библиотеки легкой цепи в соответствии со способами, описанных в публикации заяви на патент США №2013-0288927-А1. Из этих изменений Mab с улучшенной аффинностью, MAb D2517, выбирали в качестве ведущего антитела. MAb D2517 клонировали, собирали, и экспрессировали в виде полностью человеческого антитела IgG4 с легкой цепью лямбда. Последовательности VH, VL и CDR MAb D2517 представлены в Таблице 2.
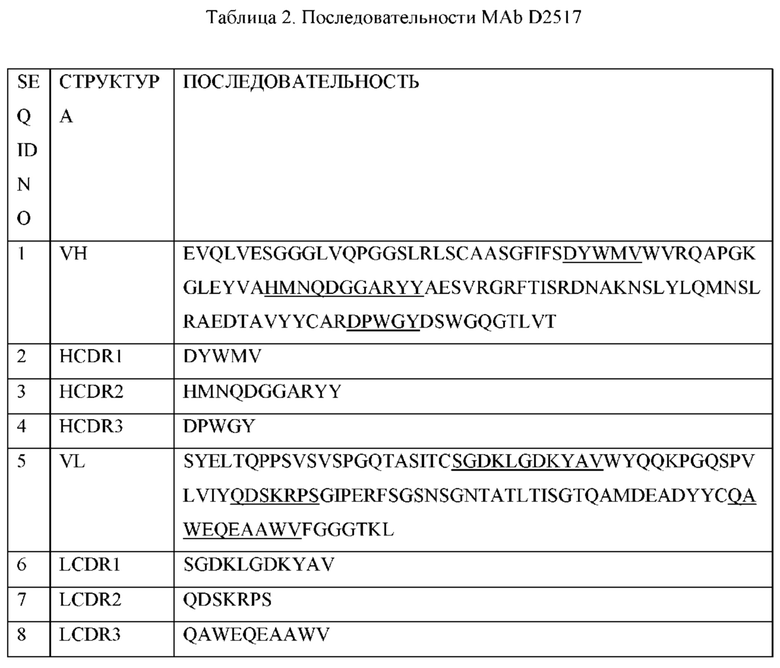
Пример 2. Характеристика связывания MAb D2517
[000249] Характеристики связывания MAb D2517 определяли с помощью анализа BIACORE, следующим образом. Антитела, а также компараторное антитело VX15/2503, оба разводили в PBS, захватывали на датчике с козьими антителами против IgGFc человека при низкой плотности, а затем SEMA4D-His мармозетки пропускали через захваченное антитело в диапазоне концентраций антигена, равном 0-25 нм. Полученные результаты приведены в Таблице 3. Аффинность MAb D2517 в отношении SEMA4D была подобной аффинности VX15/2503.
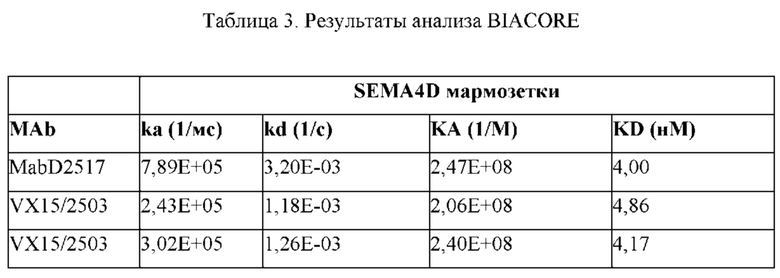
[000250] Способность MAb D2517 связывается с SEMA4D человека, мыши, мармозетки и макака определяли методом ИФА с использованием следующего способа. С-лунковые планшеты ИФА Nunc MaxiSorp покрывали в течение ночи 100 мкл/лунку CD100-His, растворенным в 1X PBS. После инкубации в течение ночи, планшеты промывали и затем блокировали 200 мкл/лунка PBS + 0,5% БСА + 0,025% Tween 20 в течение по меньшей мере 1 часа при комнатной температуре. После дополнительной промывки, 100 мкл/лунка, разбавленные MAb (100 нг/мл) добавляли в каждую лунку планшета для ИФА, который инкубировали при комнатной температуре в течение 2 часов, а затем промывали. Далее, добавляли 100 мкл/лунка 1:10000 антитела козы против Fc человека (Jackson, кат. №109-035-098 партия 118460) в каждую лунку, и планшет ИФА инкубировали при комнатной температуре в течение 1 часа. Затем планшет промывали и анализировали с 100 мкл/лунка субстратом ТМВ в течение 15 минут. Реакцию обнаружения останавливали с помощью 100 мкл/лунка 2N серной кислоты, и планшет считывали с использованием ридера планшетов при длине волны, равной 450-570 нм.
[000251]. Результаты представлены на Фиг. 1А (SEMA4D человека), Фиг. 1B (SEMA4D мармозетки), Фиг. 1С (SEMA4D макака) и Фиг. 1D (SEMA4D мыши).
Пример 3. MAb D2517 блокирует связывание SEMA4D с его рецептором
[000252] Способность MAbD2517 блокировать SEMA4D, полученный от различных видов для связывания с его рецептором - плексин В1, оценивали следующим образом.
[000253] MAbD2517 и MAbVX15/2503 разбавляли в ацетатном буфере. Антитела были сравнивали в серии трехкратных разведений на их способность блокировать комплексы SEMA4D-His (SEMA4D человека, макака, мыши или крысы) от связывания с клетками 293PLXNB1. Все антитела, разбавленные от 1,5 мкг/мл до 88 нг/мл в 96-луночном планшете и комбинированные 1:1 с 0,8 мкг/мл соответствующего SEMA4D-His, инкубировали в течение ночи при 4°С.
[000254] На следующий день комплексы антитело/SEMA4D-His или контроли были добавляли к 2,5×105 клеток 293PLXNB1 в 96-луночном планшете и связывание осуществляли в течение 30 мин при 4°С. После промывания клетки окрашивали анти-6xHis-APC (30 мин, 4°С), промывали и анализировали с помощью проточной цитометрии на FACS Canto II. Результаты представлены на Фиг. 2A-2D. Значения ЕС50 были рассчитаны из кривых и приведены в Таблице 4.
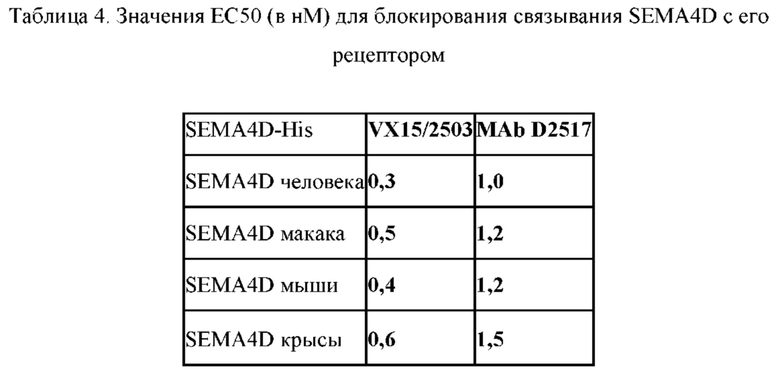
Пример 4. Тестирование мышиного химерного эвивалента MAbD2517 в модели опухоли
[000255] Аминокислотные последовательности VH и VL (SEQ ID NO: 1 и SEQ ID NO: 5) MAb D2517 встраивали в векторы, экспрессирующие константные области IgG1 и лямбда мыши для получения химерного антитела MAb D2585. Антитела экспрессировали в клетках CHO-S и очищали, как описано в примере 1.
[000256] Самкам мышей Balb/C 6-8 недельного возраста (n=12) прививали клетки опухоли молочной железы 30000 Tubo.A5 подкожно в жировую ткань молочной железы. Лечение с помощью контрольного антитела IgG1/2B8.1E7 мыши или химерного антитела MAbD2585 против SEMA4D начинали через 7 суток после инокуляции (10 мг/кг, ИП (интраперитонеально), еженедельно Х5). Опухоли были измеряли с помощью циркуля 2х/неделя, начиная на 11 сутки после имплантации. Животных умерщвляли, когда объем опухоли достигал 800 мм3.
[000257] Рост опухоли измеряли с помощью циркуля, а измерения были использованы для расчета объема опухоли с использованием формулы (w2×l)/2, где у опухоли w = ширина, меньшая величина, а l = длина в мм. Средний объем опухоли и кривые выживаемости Каплана-Мейера, определяемые как время до конечной точки, в которой объем опухоли = 800 мм3, представлены на Фиг. 3А и 3В, соответственно. Статистический анализ проводили с использованием двухфакторного дисперсионного анализа (ANOVA) для среднего объема опухоли (р<0,05), и анализ журнала Rank для выживания (р<,0.1), соответственно, которые были статистически значимыми.
[000258] Частоту опухолевых регрессий в модели опухоли Тубо была также измерена и показана на Фиг. 3С. Регрессия представляет собой отсутствие ощутимой опухоли, определяемое как измерение опухоли <50 мм3 в течение по меньшей мере двух последовательных измерений. Лечение с помощью химерного антитела MAbD2585 увеличило количество регрессий у мышей, несущих Тубо. Количество регрессий у группы мышей, которых лечили химерным антителом MAbD2585 было статистически значимо по сравнению с контрольным Ig (р=0,01), как определено точным критерием Фишера.
[000259] Суть и объем данного изобретения не должны быть ограничены ни одним из описанных выше иллюстративных вариантов осуществления, но должны быть определены только в соответствии с нижеследующей формулой изобретения и ее эквивалентами.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАННЕЕ ОБНАРУЖЕНИЕ АКТИВАЦИИ ГЛИАЛЬНЫХ КЛЕТОК ПРИ НЕЙРОДЕГЕНЕРАТИВНЫХ ИЛИ НЕЙРОВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЯХ | 2018 |
|
RU2766341C2 |
| ЛЕЧЕНИЕ РАКА С ПОМОЩЬЮ АНТИТЕЛА К СЕМАФОРИНУ 4D В КОМБИНАЦИИ С ЭПИГЕНЕТИЧЕСКИМ МОДУЛИРУЮЩИМ АГЕНТОМ | 2018 |
|
RU2783535C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СПЕЦИФИЧНЫЕ К ИЛ-21, И ОБЛАСТИ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2708336C2 |
| АНТИТЕЛА ПРОТИВ KIT И ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2681730C2 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕСЯ С PSL PSEUDOMONAS, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2708977C2 |
| АНТИТЕЛА ПРОТИВ CD40 И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2796413C2 |
| АНТИТЕЛА ПРОТИВ CD19 ЧЕЛОВЕКА, ОБЛАДАЮЩИЕ ВЫСОКОЙ АФФИННОСТЬЮ | 2016 |
|
RU2761077C1 |
| АНТИТЕЛА ПРОТИВ PD-1 И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2788616C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СПЕЦИФИЧНЫЕ К ИЛ-21, И ОБЛАСТИ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2804456C1 |
| АНТИТЕЛА ПРОТИВ CTLA4 И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2779312C2 |




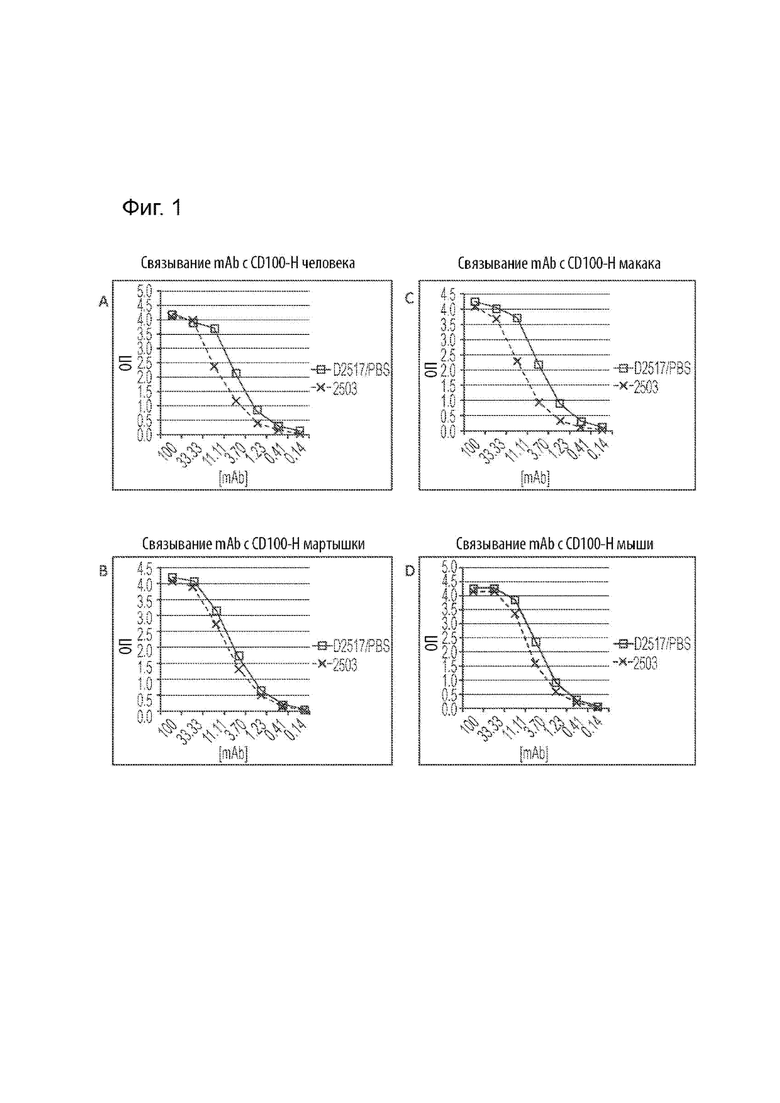
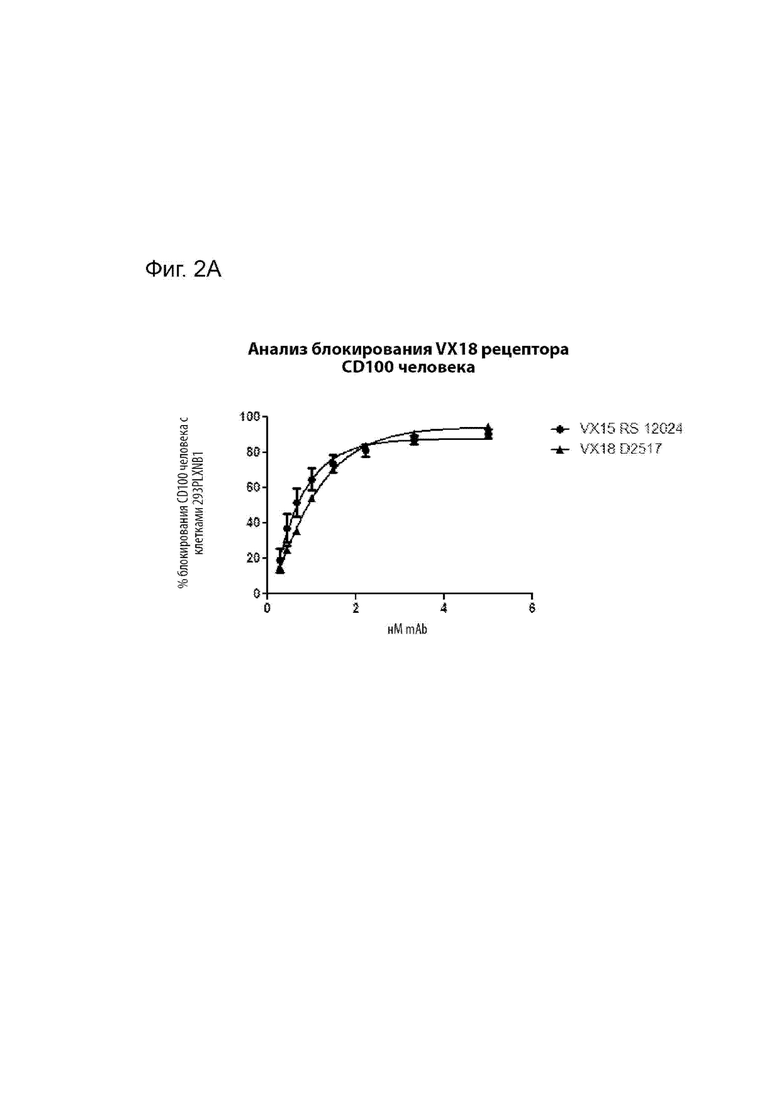
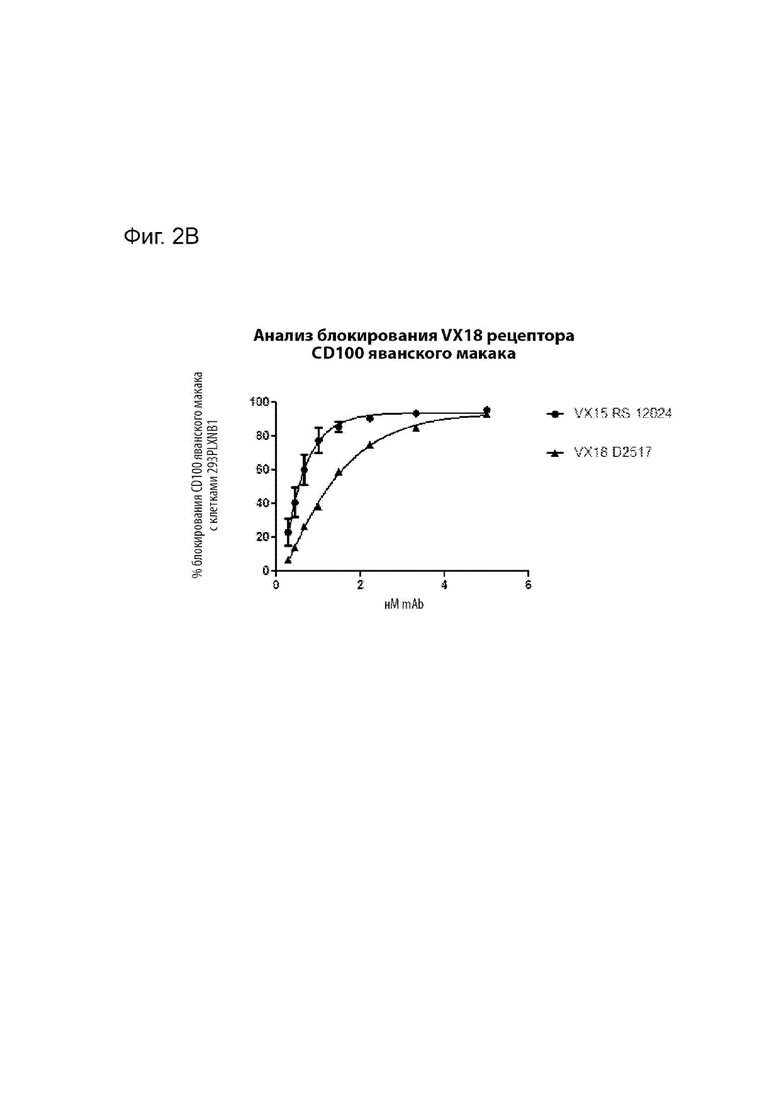
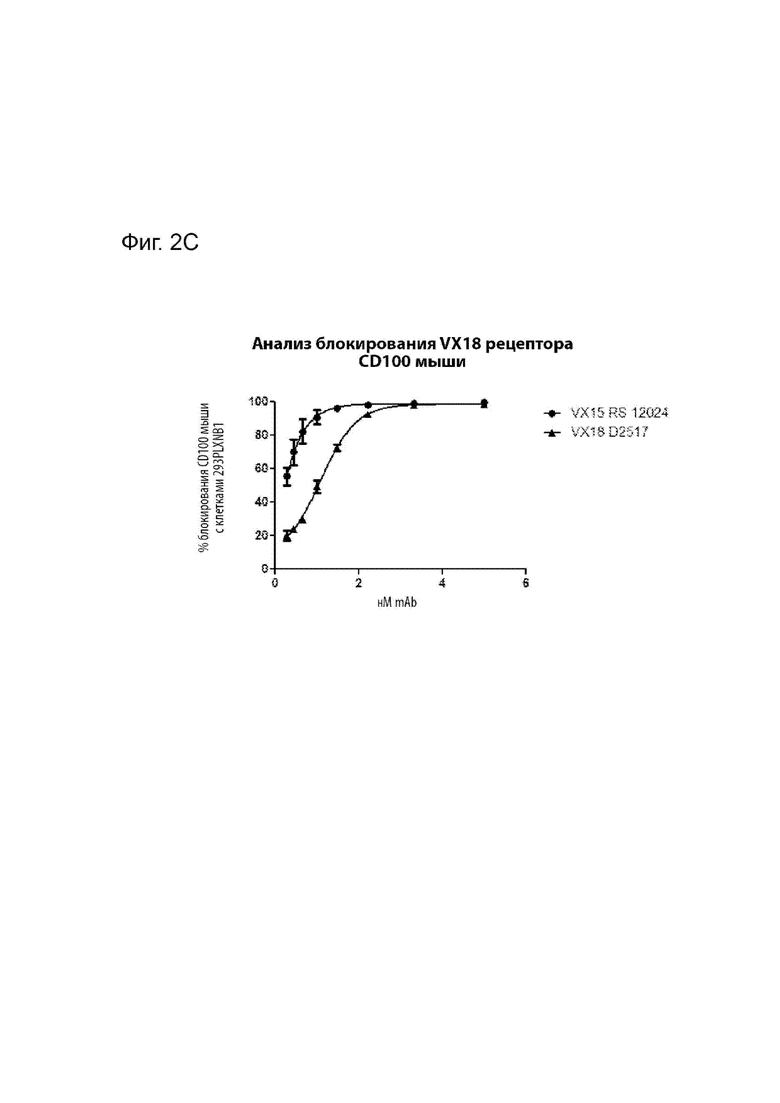
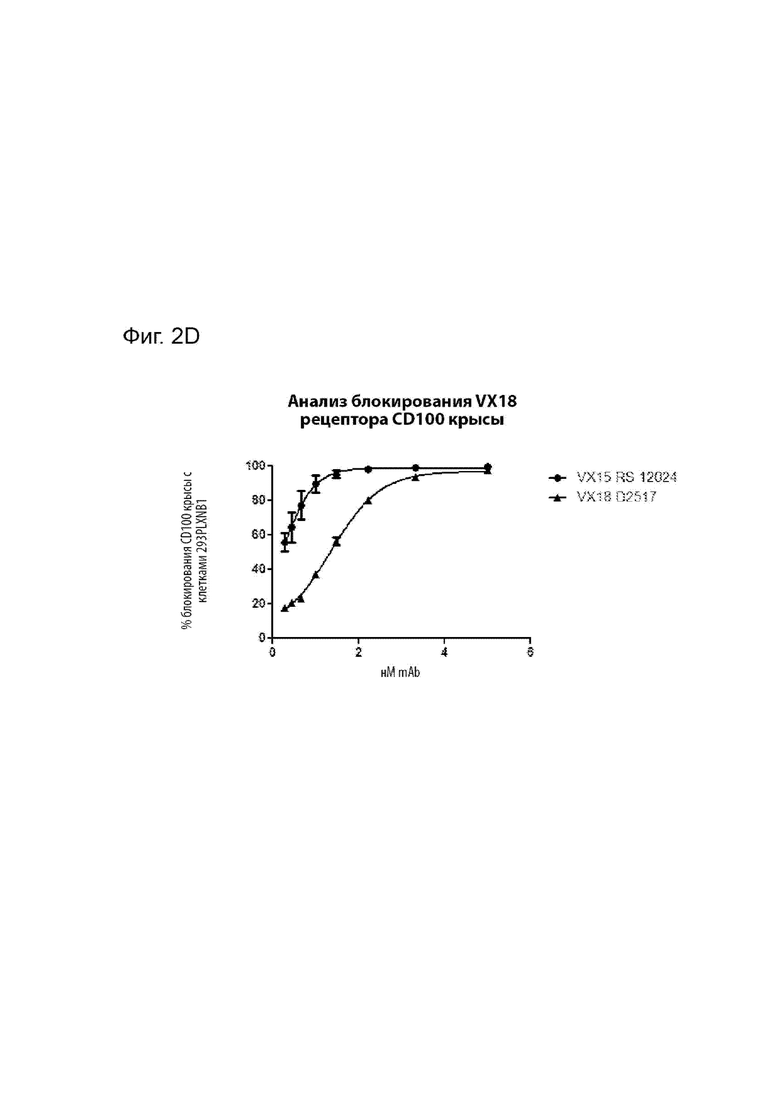
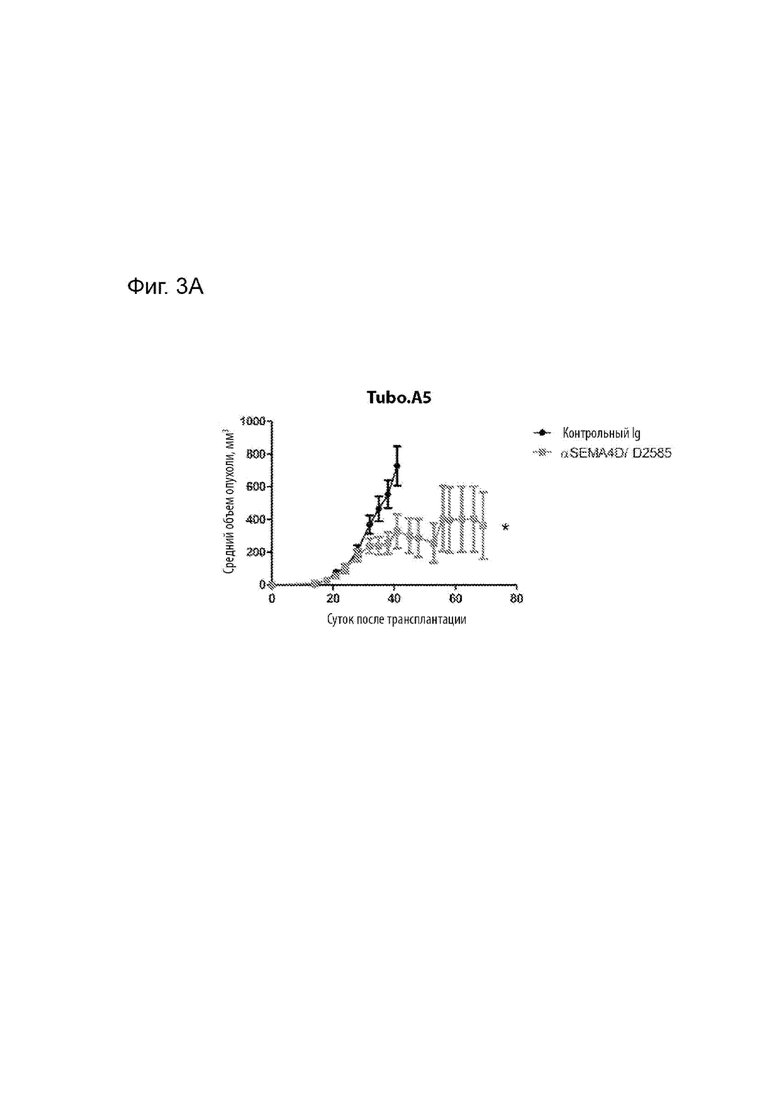
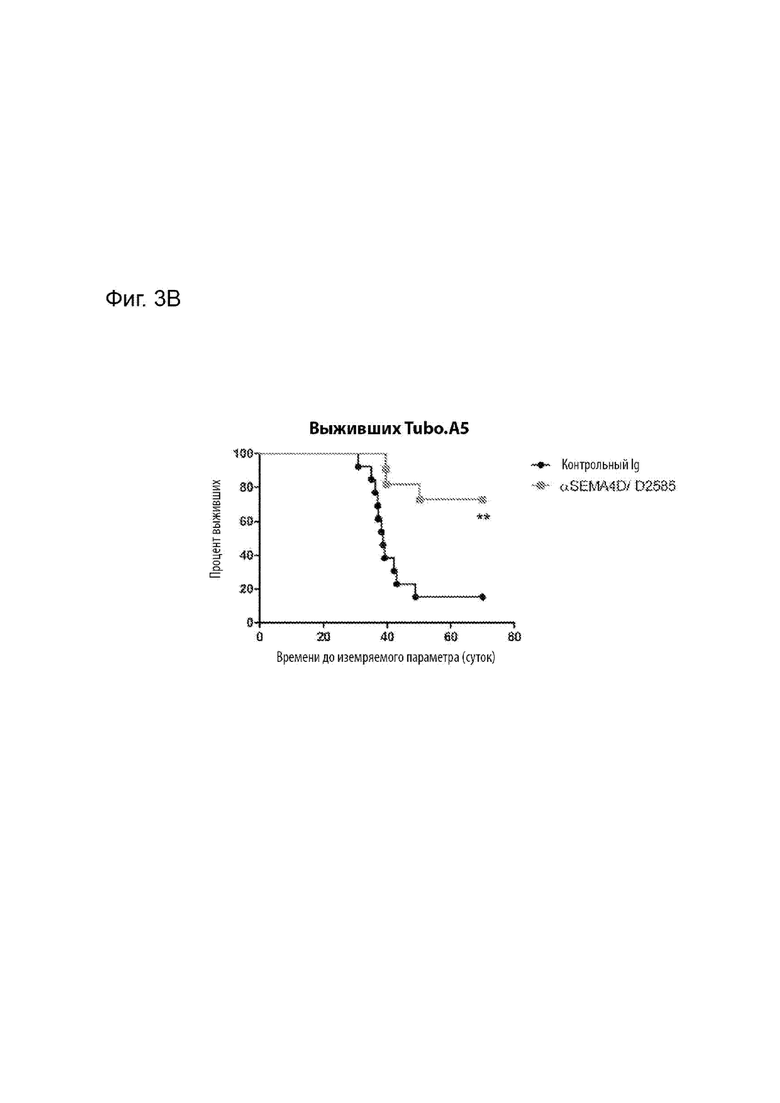
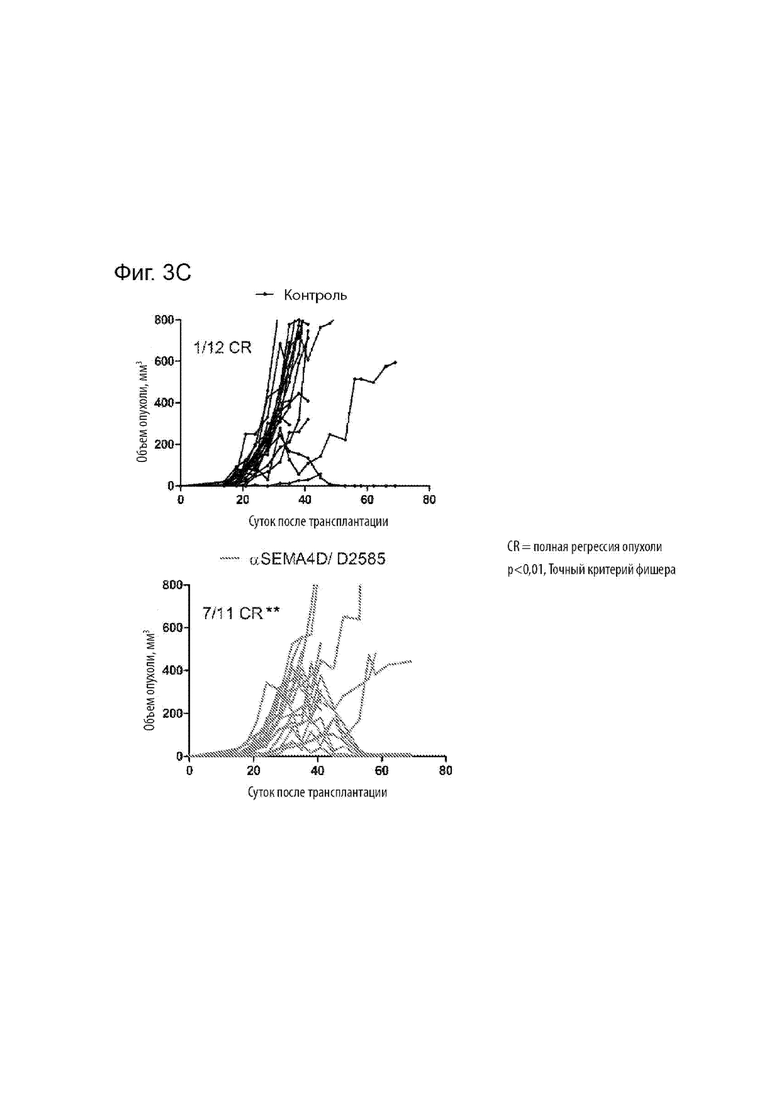
Изобретение относится к области биотехнологии. Предложено антитело, специфично связывающееся с семафорином-4D (SEMA4D). Также предложены включающий указанное антитело конъюгат, композиция и способ для лечения заболеваний, связанных с патологией SEMA4D, включая аутоиммунные заболевания, воспалительные заболевания, рак, нейровоспалительные расстройства и нейродегенеративные заболевания. Кроме того, изобретение относится к кодирующим указанное антитело полинуклеотидам, векторам экспрессии и клеткам-хозяевам для получения антител и конъюгатов. Группа изобретений обеспечивает расширение арсенала средств для лечения заболеваний, связанных с патологиями SEMA4D. 11 н. и 35 з.п. ф-лы, 8 ил., 4 табл., 4 пр.
1. Антитело или его антигенсвязывающий фрагмент, которые специфично связываются с семафорином-4D (SEMA4D), содержащие вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL); причем VH содержит области, определяющие комплементарность (HCDR) HCDR1, HCDR2 и HCDR3, содержащие аминокислотные последовательности, идентичные SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 4, соответственно; и при этом VL содержит области, определяющие комплементарность (LCDR) LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности, идентичные SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8, соответственно.
2. Антитело или его фрагмент по п. 1, отличающиеся тем, что VH дополнительно содержит каркасные области (HFW) HFW1, HFW2, HFW3 и HFW4, и при этом VL дополнительно содержит каркасные области (LFW) LFW1, LFW2, LFW3 и LFW4.
3. Антитело или его фрагмент по п. 2, отличающиеся тем, что указанные каркасные области происходят из антитела человека.
4. Антитело или его фрагмент по п. 2, отличающиеся тем, что указанные каркасные области происходят из антитела, не являющегося антителом человека.
5. Антитело или его фрагмент по любому из пп. 1–3, отличающиеся тем, что VH содержит аминокислотную последовательность SEQ ID NO: 1.
6. Антитело или его фрагмент по любому из пп. 1–3, отличающиеся тем, что VL содержит аминокислотную последовательность SEQ ID NO: 5.
7. Антитело или его фрагмент по любому из пп. 1–3, отличающиеся тем, что VH содержит аминокислотную последовательность SEQ ID NO: 1, и VL содержит аминокислотную последовательность SEQ ID NO: 5.
8. Антитело или его фрагмент по любому из пп. 1–7, дополнительно содержащие константную область тяжелой цепи или ее фрагмент, слитые с C-концом VH.
9. Антитело или его фрагмент по п. 8, отличающиеся тем, что указанная константная область тяжелой цепи или ее фрагмент представляют собой константную область тяжелой цепи антитела человека.
10. Антитело или его фрагмент по п. 9, отличающиеся тем, что указанная константная область тяжелой цепи или ее фрагмент представляют собой константную область IgG4 человека.
11. Антитело или его фрагмент по п. 8, отличающиеся тем, что указанная константная область тяжелой цепи или ее фрагмент представляют собой константную область тяжелой цепи, не являющейся тяжелой цепью антитела человека.
12. Антитело или его фрагмент по п. 11, отличающиеся тем, что указанная константная область тяжелой цепи или ее фрагмент представляют собой константную область IgG1 мыши.
13. Антитело или его фрагмент по любому из пп. 1–12, дополнительно содержащие константную область легкой цепи или ее фрагмент, слитые с C-концом VL.
14. Антитело или его фрагмент по п.13, отличающиеся тем, что указанная константная область легкой цепи или ее фрагмент представляют собой константную область легкой цепи антитела человека.
15. Антитело или его фрагмент по п. 14, отличающиеся тем, что указанная константная область легкой цепи или ее фрагмент представляют собой константную область легкой цепи лямбда антитела человека.
16. Антитело или его фрагмент по п. 13, отличающиеся тем, что указанная константная область легкой цепи или ее фрагмент представляют собой константную область легкой цепи, не являющейся легкой цепью антитела человека.
17. Антитело или его фрагмент по п. 16, отличающиеся тем, что указанная константная область легкой цепи или ее фрагмент представляют собой константную область легкой цепи лямбда антитела мыши.
18. Антитело или его фрагмент по любому из пп. 1–17, отличающиеся тем, что указанный фрагмент представляет собой фрагмент Fab, фрагмент Fab', фрагмент F(ab')2, фрагмент Fd, одноцепочечный фрагмент Fv (scFv) или дисульфид-связанный фрагмент Fv (sdFv).
19. Антитело или его фрагмент по любому из пп. 1–18, отличающиеся тем, что указанное антитело или его фрагмент способны специфично связываться с двумя или более различными эпитопами.
20. Антитело или его фрагмент по любому из пп. 1–19, которые могут специфично связываться с SEMA4D человека, SEMA4D мыши, SEMA4D крысы или SEMA4D отличного от человека примата.
21. Антитело или его фрагмент по п. 20, отличающиеся тем, что указанный SEMA4D отличного от человека примата представляет собой SEMA4D яванского макака или SEMA4D мармозетки.
22. Антитело или его фрагмент по п. 20 или 21, которые специфично связываются с SEMA4D с аффинностью, характеризующейся константой диссоциации KD не более чем 500 нМ, 100 нМ, 50,0 нМ, 40,0 нМ, 30,0 нМ, 20,0 нМ, 10,0 нМ, 9,0 нМ, 8,0 нМ, 7,0 нМ, 6,0 нМ, 5,0 нМ, 4,0 нМ, 3,0 нМ, 2,0 нМ, 1,0 нМ, 0,50 нМ, 0,10 нМ, 0,050 нМ, 0,01 нМ, 0,005 нМ или 0,001 нМ; и при этом SEMA4D представляет собой SEMA4D человека, SEMA4D мыши, SEMA4D яванского макака, SEMA4D мармозетки или любую их комбинацию.
23. Антитело или его фрагмент по любому из пп. 1–22, которые могут ингибировать связывание SEMA4D с рецептором SEMA4D.
24. Антитело или его фрагмент по п. 23, отличающиеся тем, что указанный рецептор SEMA4D представляет собой плексин-B1, плексин-B2, CD72 или их комбинацию.
25. Антитело или его фрагмент по любому из пп. 1–24, которые вызывают минимальный ответ или отсутствие иммунного ответа на антитело при введении субъекту, представляющему собой человека.
26. Конъюгат, способный специфично связываться с семафорином-4D (SEMA4D), состоящий из антитела или его фрагмента по любому из пп. 1–25 и гетерологичного фрагмента.
27. Конъюгат по п. 26, отличающийся тем, что указанный гетерологичный фрагмент включает полипептид, цитотоксический агент, терапевтический агент, пролекарство, липид, углевод, нуклеиновую кислоту, детектируемую метку, полимер или любую их комбинацию.
28. Конъюгат по п. 27, отличающийся тем, что указанный полипептид включает связывающую молекулу, фермент, цитокин, лимфокин, гормональный пептид или любую их комбинацию.
29. Конъюгат по п. 27, отличающийся тем, что указанный цитотоксический агент включает радионуклид, биологический токсин, ферментативно активный токсин или любую их комбинацию.
30. Конъюгат по п. 27, отличающийся тем, что указанная детектируемая метка включает фермент, флуоресцентную метку, хемилюминесцентную метку, биолюминесцентную метку, радиоактивную метку или любую их комбинацию.
31. Композиция, содержащая антитело или его фрагмент по любому из пп. 1–25 или конъюгат по любому из пп. 26–30 и носитель, для нейтрализации SEMA4D у субъекта.
32. Полинуклеотид, содержащий одну или более последовательностей нуклеиновых кислот, кодирующих антитело или его фрагмент по любому из пп. 1–25.
33. Полинуклеотид по п. 32, содержащий последовательность нуклеиновой кислоты, кодирующую VH антитела или его фрагмента.
34. Полинуклеотид по п. 32, содержащий последовательность нуклеиновой кислоты, кодирующую VL антитела или его фрагмента.
35. Комбинация полинуклеотидов для получения антитела или его фрагмента по любому из пп. 1–25, содержащая полинуклеотид, который имеет последовательность нуклеиновой кислоты, кодирующую тяжелую цепь антитела или его фрагмента по любому из пп. 1–25, и полинуклеотид, который имеет последовательность нуклеиновой кислоты, кодирующую легкую цепь антитела или его фрагмента по любому из пп. 1–25.
36. Вектор экспрессии, содержащий полинуклеотид по п. 32 или комбинацию полинуклеотидов по п. 35.
37. Комбинация векторов экспрессии, содержащая полинуклеотиды комбинации по п. 35.
38. Клетка-хозяин для получения антитела или его фрагмента по любому из пп. 1–25, содержащая полинуклеотид по п. 32, или комбинацию полинуклеотидов по п. 35, или вектор по п. 36, или комбинацию векторов по п. 37.
39. Клетка-хозяин для получения конъюгата по любому из пп. 26–30, содержащая полинуклеотид по п. 32, или комбинацию полинуклеотидов по п. 35, или вектор по п. 36, или комбинацию векторов по п. 37.
40. Способ получения антитела или его фрагмента по любому из пп. 1–25, включающий культивирование клетки-хозяина по п. 38 и выделение указанного антитела или его фрагмента.
41. Способ нейтрализации SEMA4D у субъекта, представляющего собой человека, включающий введение указанному субъекту, представляющему собой человека, антитела или его фрагмента по любому из пп. 1–25, конъюгата по любому из пп. 26–30, или композиции по п. 31.
42. Способ по п. 41, отличающийся тем, что указанный субъект, представляющий собой человека, нуждается в лечении аутоиммунного заболевания или расстройства, воспалительного заболевания или расстройства, рака, нейровоспалительного заболевания или расстройства, нейродегенеративного заболевания или расстройства или любой их комбинации.
43. Способ по п. 42, отличающийся тем, что указанное нейровоспалительное заболевание или расстройство представляет собой рассеянный склероз.
44. Способ по п. 42, отличающийся тем, что указанное нейродегенеративное заболевание или расстройство представляет собой инсульт, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, синдром Дауна, атаксию, боковой амиотрофический склероз (ALS), лобно-височную деменцию (FTD), связанное с ВИЧ когнитивное нарушение, волчанку ЦНС, умеренное когнитивное нарушение или их комбинацию.
45. Способ по п. 42, отличающийся тем, что указанное аутоиммунное заболевание или воспалительное заболевание представляет собой артрит.
46. Способ по п. 45, отличающийся тем, что указанное аутоиммунное заболевание или воспалительное заболевание представляет собой ревматоидный артрит.
| US 2014099334 A1, 10.04.2014 | |||
| FISHER TERRENCE L | |||
| et al., Generation and preclinical characterization of an antibody specific for SEMA4D, MABS, 2016, vol | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| PATNAIK A | |||
| et al., Safety, Pharmacokinetics, and Pharmacodynamics of a Humanized Anti-Semaphorin 4D Antibody, in a First-In-Human Study of Patients with Advanced Solid | |||
Авторы
Даты
2022-07-20—Публикация
2018-05-04—Подача