Изобретение относится к получению хиральных γ-кетосульфонилпроизводных пинановой структуры, в частности тиолсульфонатов (RSO2SR), сульфонов (RSO2R) и сульфокислот (RSO3H), включая их сольваты.
Из сульфопроизводных терпеноидов с кето-группой в углеродном скелете известна сульфокамфорная кислота (наиболее близкий аналог), которая используется в производстве лекарственных препаратов, обладающих коронарорасширяющей способностью, антибактериальной активностью, болеутоляющим свойством (сульфокамфокаин, полусинтетические пенициллины и цефалоспорины). Сульфонамиды на основе камфоры обладают ингибирующей активностью в отношении вирусов Эбола и Марбург [А.С. Соколова, Д.В. Баранова, О.И. Яровая, Д.С. Баев, О.А. Полежаева и др. Изв. АН, Сер. Хим., 2019, 5, 1041].
Прямых аналогов γ-кетосульфонильных производных пинановой структуры в литературе не известно.
Наиболее близким аналогом получения γ-кетосульфонильных производных пинановой структуры является способ, описанный в работе [Лезина О.М., Гребенкина О.Н., Судариков Д.В., Крымская Ю.В., Рубцова С.А., Кучин А.В. ЖОрХ. 2015, 51 (10), 1391], который заключается в окислении гидрокситиолов пинановой структуры диоксидом хлора. Однако работ по окислению γ-кетотиолов диоксидом хлора (прямых аналогов способа) в литературе не выявлено.
Задачей настоящего изобретения является синтез хиральных γ-кетосульфонильных производных пинановой структуры и разработка эффективных способов их получения.
Технический результат заключается в расширении арсенала монотерпеновых сульфопроизводных заданной структуры, востребованных в органическом синтезе биологически активных соединений, полученных эффективным способом с высоким выходом.
Технический результат достигается получением хиральных γ-кетосульфонильных производных пинановой структуры формулы (I), в частности, тиолсульфонатов (RSO2SR), сульфонов (RSO2R) и сульфокислот (RSO3H), включая их сольваты:
 ,
,
где звездочкой обозначена связь, к которой присоединяется сульфогруппа (-SO2-).
Технический результат способа достигается тем, что способ получения сульфопроизводных, заключающийся в окислении тиолов пинановой структуры диоксидом хлора (ClO2) путем смешивания раствора тиола в органическом растворителе с водным или органическим раствором диоксида хлора, согласно изобретения, в качестве исходных соединений используют γ-кетотиолы пинановой структуры, для получения сульфокислоты в качестве растворителя используют пиридин или диметилформамид, для получения сульфона в качестве растворителя используют ацетонитрил, гексан или хлороформ, для получения тиолсульфоната - ацетонитрил и катализатор VO(acac)2.
Синтез сульфопроизводных структурной формулы (I) осуществляется согласно схеме 1. Раствор тиолов (3R)-1, (2S)-2 или дисульфидов (3R)-3, (2S)-4 в органическом растворителе смешивают с водным или органическим раствором диоксида хлора при мольном соотношении тиол : ClO2, равном 1:1÷3, при комнатной температуре. Продуктами реакции являются тиолсульфонаты (3R)-5, (2S)-6, сульфоны (3R)-7, (2S)-8, (2R)-8 и сульфокислоты (3R)-9, (2S)-10, (2R)-10.
Схема 1. Окисление кетотиолов диоксидом хлора.
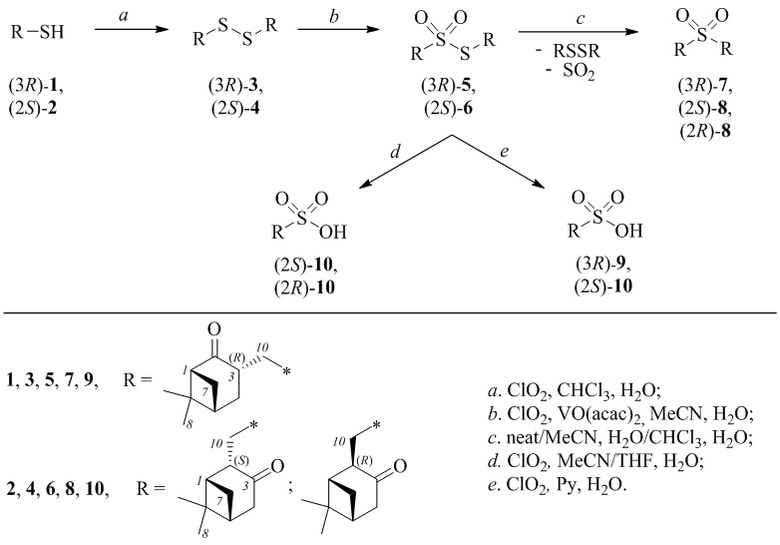
Исходные тиолы 1, 2 были получены многостадийным синтезом из (-)-β-пинена  через 2-норпинанон и пинокарвон соответственно. Последние присоединением тиоуксусной кислоты были превращены в соответствующие тиоацетаты по методике [F. Martínez-Ramos, M. E. Vargas-Díaz, L. Chacón-García, J. Tamariz, P. Joseph-Nathan, L. G. Zepeda, Tetrahedron: Asymmetry, 2001, 12, 3095], а затем деацилированы гидразингидратом (NH2NH2·H2O) в тиолы 1, 2.
через 2-норпинанон и пинокарвон соответственно. Последние присоединением тиоуксусной кислоты были превращены в соответствующие тиоацетаты по методике [F. Martínez-Ramos, M. E. Vargas-Díaz, L. Chacón-García, J. Tamariz, P. Joseph-Nathan, L. G. Zepeda, Tetrahedron: Asymmetry, 2001, 12, 3095], а затем деацилированы гидразингидратом (NH2NH2·H2O) в тиолы 1, 2.
(-)-β-Пинен - коммерческий продукт производства Sigma Aldrich, чистота 99%,  . Гидразин гидрат - коммерческий продукт производства Alfa Aesar, чистота 98%. Водный раствор диоксида хлора (ClO2) - промышленный продукт, концентрацию которого определяли титрованием по методике [Н.Ф. Петренко, A.В. Мокиенко, Диоксид хлора: применение в технологиях водоподготовки, Одесса, Оптимум. 2005, 371].
. Гидразин гидрат - коммерческий продукт производства Alfa Aesar, чистота 98%. Водный раствор диоксида хлора (ClO2) - промышленный продукт, концентрацию которого определяли титрованием по методике [Н.Ф. Петренко, A.В. Мокиенко, Диоксид хлора: применение в технологиях водоподготовки, Одесса, Оптимум. 2005, 371].
Способ позволяет получить целевые продукты в одну стадию с сохранением структуры терпенового фрагмента исходного тиола с высоким выходом. Для подбора оптимальных условий синтеза соединений 5-10 варьировались такие параметры, как растворитель, соотношение тиол : диоксид хлора, наличие катализатора VO(acac)2 и время реакции. Нами были опробованы в качестве растворителей пиридин, тетрагидрофуран, ацетонитрил, диметилформамид, хлороформ, дихлорметан, гексан. Соотношение тиол : ClO2 изменялось от 1 : 1÷3, соответственно, время реакции - от 0.5÷3.0 ч.
Было выявлено, что оптимальный растворитель для получения сульфокислот (3R)-9, (2S)-10 - пиридин или диметилформамид, для сульфона - ацетонитрил или хлороформ, для тиолсульфонатов (3R)-5, (2S)-6 - ацетонитрил и наличие катализатора VO(acac)2 в количестве 5-10 мол. %. Оптимальное соотношение тиол : ClO2 для получения сульфокислот и сульфонов составляет 1 : 2, для получения тиолсульфонатов - дисульфид : ClO2, равное 1 : 1÷2. Использование данных условий приводит к повышению выхода сульфокислот до 98% (от теоретического) с диастереоселективностью (de) до 98%, тиолсульфонатов - 74-81%, сульфонов - 58%.
ИК спектры регистрировали на ИК-Фурье-спектрометре Shimadzu IR Prestige 21 в тонком слое. Спектры ЯМР 1H и 13C регистрировали на спектрометре Bruker Avance-300 (300.17 МГц для 1Н и 75.48 МГц для 13С) в растворах CDCl3 (внутренний стандарт - сигнал хлороформа) и ДМСО-d6. Полное отнесение сигналов 1Н и 13С выполняли с помощью двумерных гомо- (1H-1H COSY, 1H-1H NOESY) и гетероядерных экспериментов (1H-13C HSQC). Масс-спектры регистрировали на высокоэффективном жидкостном хроматографе с масс-селективным детектором Thermo finnigan LCQ Fleet (растворитель - CH3OH). Детектирование проводили по отрицательным и положительным ионам. Колоночную хроматографию выполняли на силикагеле Alfa Aesar (0.06-0.2 мм).
Примеры синтеза и характеристики полученных соединений.

S-(((1R,3R,5R)-6,6-Диметил-2-оксобицикло[3.1.1]гептан-3-ил)метил) ((1R,3R,5R)-6,6-диметил-2-оксобицикло[3.1.1]гептан-3-ил)метансульфонотиоат (5). К раствору 0.366 г (1 ммоль) дисульфида 3 в 40 мл ацетонитрила при перемешивании добавляли 0.027 г (0.1 ммоль) VO(acac)2, затем водный раствор 0.0675 г (1 ммоль) ClO2. Время синтеза 1 ч. Реакционную смесь частично упаривали до появления осадка (целевой продукт). Осадок отфильтровывали. Выход 0.295 г (74%). Светло-желтый воскообразный порошок. 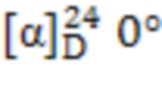 (с 0.26, CHCl3). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.74, 0.76 (2с, 6H, H8, H8'), 1.37 (с, 6H, H9', H9), 1.73-1.88 (m, 4H, H4a, H4'a, H7а, H7'а), 2.27-2.36 (m, 2H, H5, H5'), 2.53-2.77 (м, 6H, H1, H1', H4b, H4'b, H7b, H7'b), 3.05-3.29 (m, 4H, H3, H3', H10а, H10'а), 3.58-3.70 (м, 1Н, H10'b), 4.32 (d, 1H, H10b, J=11.9). Спектр ЯМР 13С (CDCl3, δ, м.д.): 22.0, 22.1 (C8, C8'), 25.1, 25.2 (C7, C7'), 26.1, 26.3 (C9', C9), 28.4 (C4'), 29.9 (C4), 35.6 (C10'), 38.6 (C3), 40.6, 40.7 (C5, C5'), 43.4 (C3'), 43.8 (C6, C6'), 57.2, 57.4 (C1, C1'), 62.4 (C10), 211.1, 213.4 (C2, C2'). ИК спектр (KBr, ν, cm–1): 472, 489, 534, 611, 1024, 1130 st (SO2), 1321 st (SO2), 1460, 1708 st (С=O), 2872 st, 2945 st. Вычислено (%) для С20Н30O4S2: C 60.27, H 7.59, S 16.09; Найдено: С 60.25, Н 7.66, S 16.20.
(с 0.26, CHCl3). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.74, 0.76 (2с, 6H, H8, H8'), 1.37 (с, 6H, H9', H9), 1.73-1.88 (m, 4H, H4a, H4'a, H7а, H7'а), 2.27-2.36 (m, 2H, H5, H5'), 2.53-2.77 (м, 6H, H1, H1', H4b, H4'b, H7b, H7'b), 3.05-3.29 (m, 4H, H3, H3', H10а, H10'а), 3.58-3.70 (м, 1Н, H10'b), 4.32 (d, 1H, H10b, J=11.9). Спектр ЯМР 13С (CDCl3, δ, м.д.): 22.0, 22.1 (C8, C8'), 25.1, 25.2 (C7, C7'), 26.1, 26.3 (C9', C9), 28.4 (C4'), 29.9 (C4), 35.6 (C10'), 38.6 (C3), 40.6, 40.7 (C5, C5'), 43.4 (C3'), 43.8 (C6, C6'), 57.2, 57.4 (C1, C1'), 62.4 (C10), 211.1, 213.4 (C2, C2'). ИК спектр (KBr, ν, cm–1): 472, 489, 534, 611, 1024, 1130 st (SO2), 1321 st (SO2), 1460, 1708 st (С=O), 2872 st, 2945 st. Вычислено (%) для С20Н30O4S2: C 60.27, H 7.59, S 16.09; Найдено: С 60.25, Н 7.66, S 16.20.

S-(((1S,2S,5R)-6,6-Диметил-3-оксобицикло[3.1.1]гептан-2-ил)метил) ((1S,2S,5R)-6,6-диметил-3-оксобицикло[3.1.1]гептан-2-ил)метансульфонотиоат ((2S)-6). Получали аналогично тиолсульфонату 5 из дисульфида (2S)-4. Соотношение (2S)-4 : ClO2 = 1 : 2. Время синтеза 1 ч. Выход 81%. Светло-желтый воскообразный порошок.  (с 0.24, CHCl3). Т. пл. 134-137 °С. Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.88, 0.90 (2с, 6H, H8, H8'), 1.26-1.32 (m, 1H, H7а, H7'а), 1.35 (с, 6H, H9', H9), 2.13-2.21 (m, 2H, H5, H5'), 2.41 (t, 1H, H1', J=6.3), 2.51-2.79 (м, 7H, H1, H4, H4', H7b, H7'b), 2.82–2.91 (м, 1Н, H2'), 2.98 (m, 2H, H2, H10'а), 3.13–3.23 (m, 1H, H10а), 3.80 (dd, 1H, H10'b, J=13.6, 5.6), 4.10 (д, 1H, H10b, J=13.9). Спектр ЯМР 13С (CDCl3, δ, м.д.): 21.8, 21.9 (C8, C8'), 26.4, 26.6 (C9', C9), 33.7, 34.1 (C7, C7'), 37.2 (C10'), 38.4, 38.7 (C5, C5'), 38.8, 39.2 (C6, C6'), 42.3, 42.7 (C1, C1'), 44.5, 44.6 (C4, C4'), 51.4 (C2), 56.4 (C2'), 62.5 (C10), 209.5, 212.3 (C3, C3'). ИК спектр (KBr, ν, cm–1): 474, 545, 1045, 1128 st (SO2), 1321 st (SO2), 1409, 1467, 1712 st (С=O), 2872 st, 2924 st, 2933 st. Вычислено (%) для С20Н30O4S2: C 60.27, H 7.59, S 16.09; Найдено: С 60.55, Н 7.66, S 16.10.
(с 0.24, CHCl3). Т. пл. 134-137 °С. Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.88, 0.90 (2с, 6H, H8, H8'), 1.26-1.32 (m, 1H, H7а, H7'а), 1.35 (с, 6H, H9', H9), 2.13-2.21 (m, 2H, H5, H5'), 2.41 (t, 1H, H1', J=6.3), 2.51-2.79 (м, 7H, H1, H4, H4', H7b, H7'b), 2.82–2.91 (м, 1Н, H2'), 2.98 (m, 2H, H2, H10'а), 3.13–3.23 (m, 1H, H10а), 3.80 (dd, 1H, H10'b, J=13.6, 5.6), 4.10 (д, 1H, H10b, J=13.9). Спектр ЯМР 13С (CDCl3, δ, м.д.): 21.8, 21.9 (C8, C8'), 26.4, 26.6 (C9', C9), 33.7, 34.1 (C7, C7'), 37.2 (C10'), 38.4, 38.7 (C5, C5'), 38.8, 39.2 (C6, C6'), 42.3, 42.7 (C1, C1'), 44.5, 44.6 (C4, C4'), 51.4 (C2), 56.4 (C2'), 62.5 (C10), 209.5, 212.3 (C3, C3'). ИК спектр (KBr, ν, cm–1): 474, 545, 1045, 1128 st (SO2), 1321 st (SO2), 1409, 1467, 1712 st (С=O), 2872 st, 2924 st, 2933 st. Вычислено (%) для С20Н30O4S2: C 60.27, H 7.59, S 16.09; Найдено: С 60.55, Н 7.66, S 16.10.

(1R,1'R,3R,3'R,5R,5'R)-3,3'-(Сульфонилбис(метилен))бис(6,6-диметилбицикло[3.1.1]гептан-2-он) (7). а) К раствору 0.184 г (1 ммоль) тиола 1 в 20 мл ацетонитрила при перемешивании добавляли водный раствор, содержащий 0.135 г (2 ммоль) ClO2. Время синтеза 0.5 ч. Экстрагировали хлороформом, органическую фракцию упаривали. б) Образуется при стоянии (S)-тиолсульфоната 5 в течение 1-3 недель. Выделяли методом колоночной хроматографии (петролейный эфир : Et2O = 7:1). Выход 0.099 г (54%). Белый порошок (перекристаллизован из EtOH). Т. пл. 148–150°С.  (с 0.1, CHCl3). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.73 (с, 3H, H8), 1.36 (с, 3H, H9), 1.75-1.85 (m, 2H, H4a, H7a), 2.23-2.34 (m, 1H, H5), 2.55 (ddd, 1H, H7b, J=10.9, 5.9, 5.6), 2.68–2.77 (m, 2H, H1, H4b), 2.96 (dd, 1H, H10a, J=13.8, 9.7), 3.28-3.40 (m, 1H, H3), 4.01 (dd, 1H, H10b, J=13.5, 2.9). Спектр ЯМР 13С (CDCl3, δ, м.д.): 22.1 (C8), 25.1 (C7), 26.1 (C9), 30.0 (C4), 37.1 (C3), 40.7 (C5), 43.3 (C6), 54.8 (C10), 57.3 (C1), 211.6 (C2). ИК спектр (KBr, ν, cm–1): 468, 503, 1024, 1136 m (SO2), 1201, 1282 m (SO2), 1303, 1319, 1462, 1708 st (С=O), 2873 m, 2926 st, 2953 st. Вычислено (%) для С20Н30O4S: C 65.54, H 8.25, S 8.75; Найдено: С 65.65, Н 8.30, S 8.80.
(с 0.1, CHCl3). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.73 (с, 3H, H8), 1.36 (с, 3H, H9), 1.75-1.85 (m, 2H, H4a, H7a), 2.23-2.34 (m, 1H, H5), 2.55 (ddd, 1H, H7b, J=10.9, 5.9, 5.6), 2.68–2.77 (m, 2H, H1, H4b), 2.96 (dd, 1H, H10a, J=13.8, 9.7), 3.28-3.40 (m, 1H, H3), 4.01 (dd, 1H, H10b, J=13.5, 2.9). Спектр ЯМР 13С (CDCl3, δ, м.д.): 22.1 (C8), 25.1 (C7), 26.1 (C9), 30.0 (C4), 37.1 (C3), 40.7 (C5), 43.3 (C6), 54.8 (C10), 57.3 (C1), 211.6 (C2). ИК спектр (KBr, ν, cm–1): 468, 503, 1024, 1136 m (SO2), 1201, 1282 m (SO2), 1303, 1319, 1462, 1708 st (С=O), 2873 m, 2926 st, 2953 st. Вычислено (%) для С20Н30O4S: C 65.54, H 8.25, S 8.75; Найдено: С 65.65, Н 8.30, S 8.80.

(1S,1'S,2S,2'S,5R,5'R)-2,2'-(Сульфонилбис(метилен))бис(6,6-диметилбицикло[3.1.1]гептан-3-он) ((2S)-8). К раствору 0.184 г (1 ммоль) тиола (2S)-2 в 20 мл ацетонитрила при перемешивании добавляли водный раствор, содержащий 0.135 г (2 ммоль) ClO2. Время синтеза 0.5 ч. Экстрагировали хлороформом, органическую фракцию упаривали. Продукт очищали методом колоночной хроматографии (элюент - петролейный эфир : Et2O = 3:1). Получен в смеси (2S)-8:(2R)-8=1:5 (de 67%). Спектры ЯМР получены вычитанием сигналов из спектра смеси сульфонов (2S)-8, (2R)-8. Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.84 (с, 3H, H8), 1.32–1.36 (m, 4H, H7а, H9), 2.12–2.19 (m, 1H, H5), 2.42–2.59 (м, 4H, H1, H4а, Н4b, H7b), 2.85–2.92 (m, 1H, H10a), 3.01–3.13 (m, 1H, H2), 3.77–3.86 (m, 1H, H10b). Спектр ЯМР 13С (CDCl3, δ, м.д.): 21.9 (C8), 26.5 (C9), 33.8 (C7), 38.5 (C5), 38.8 (C6), 43.4 (C1), 44.5 (C4), 50.1 (C2), 55.8 (C10), 210.1 (C3). ИК спектр (KBr, ν, cm–1): 459, 481, 763, 1049, 1138 st (SO2), 1201, 1292 st (SO2), 1321, 1411, 1467, 1714 st (С=O), 2877 st, 2926 st, 2981 st; MS (ESI, 5 kV): m/z (%): 389.47 (100) [M+23]+, 367.29 (83) [M+1]+. Вычислено (%) для С20Н30O4S: C 65.54, H 8.25, S 8.75; Найдено: С 65.65, Н 8.30, S 8.69.

(1S,1'S,2R,2'R,5R,5'R)-2,2'-(Сульфонилбис(метилен))бис(6,6-диметилбицикло[3.1.1]гептан-3-он) ((2R)-8). Получали аналогично сульфону (2S)-8 или при стоянии (S)-тиолсульфоната (2S)-6 в течение 1-3 недель. Выход 58%. Белый порошок (перекристаллизован из EtOH). Т. пл. 168-171°С.  (с 0.2, CHCl3). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 1.01 (с, 3H, H8), 1.14 (д, 1H, H7а, J=11.2), 1.40 (с, 3H, H9), 2.15–2.24 (m, 1H, H5), 2.47–2.66 (м, 3H, H1, H4а, H7b), 2.71–2.84 (m, 1H, Н4b), 3.01 (dd, 1H, H10a, J=14.1, 9.9), 3.29 (d, 1H, H2, J=9.9), 3.63 (dd, 1H, H10b, J=14.1, 2.4). Спектр ЯМР 13С (CDCl3, δ, м.д.): 19.8 (C8), 26.2 (C9), 29.0 (C7), 37.8 (C5), 39.3 (C6), 41.1 (C1), 44.2 (C4), 46.7 (C2), 53.9 (C10), 210.3 (C3). ИК спектр (KBr, ν, cm–1): 459, 481, 763, 1049, 1138 st (SO2), 1201, 1292 st (SO2), 1321, 1411, 1467, 1714 st (С=O), 2877 st, 2926 st, 2981 st; MS (ESI, 5 kV): m/z (%): 389.47 (100) [M+23]+, 367.29 (83) [M+1]+. Вычислено (%) для С20Н30O4S: C 65.54, H 8.25, S 8.75; Найдено: С 65.65, Н 8.30, S 8.79.
(с 0.2, CHCl3). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 1.01 (с, 3H, H8), 1.14 (д, 1H, H7а, J=11.2), 1.40 (с, 3H, H9), 2.15–2.24 (m, 1H, H5), 2.47–2.66 (м, 3H, H1, H4а, H7b), 2.71–2.84 (m, 1H, Н4b), 3.01 (dd, 1H, H10a, J=14.1, 9.9), 3.29 (d, 1H, H2, J=9.9), 3.63 (dd, 1H, H10b, J=14.1, 2.4). Спектр ЯМР 13С (CDCl3, δ, м.д.): 19.8 (C8), 26.2 (C9), 29.0 (C7), 37.8 (C5), 39.3 (C6), 41.1 (C1), 44.2 (C4), 46.7 (C2), 53.9 (C10), 210.3 (C3). ИК спектр (KBr, ν, cm–1): 459, 481, 763, 1049, 1138 st (SO2), 1201, 1292 st (SO2), 1321, 1411, 1467, 1714 st (С=O), 2877 st, 2926 st, 2981 st; MS (ESI, 5 kV): m/z (%): 389.47 (100) [M+23]+, 367.29 (83) [M+1]+. Вычислено (%) для С20Н30O4S: C 65.54, H 8.25, S 8.75; Найдено: С 65.65, Н 8.30, S 8.79.

((1R,3R,5R)-6,6-Диметил-2-оксобицикло[3.1.1]гептан-3-ил)метансульфоновая кислота (9). К раствору 0.184 г (1 ммоль) тиола 1 в 20 мл пиридина при перемешивании добавляли водный раствор, содержащий 0.135 г (2 ммоль) ClO2. Время синтеза 1 ч. Реакционную смесь упаривали. Растворяли в Et2O. Осадок, содержащий С5H5N·НCl, удаляли. Раствор содержит сольват кислоты 9 с пиридином. Выход 96%. Вязкая жидкость. Спектр ЯМР 1Н (СDСl3, δ, м.д., J/Hz): 0.44 (с, 3H, H8), 1.06 (с, 3H, H9), 1.49-1.62 (m, 2H, H4a, H7a), 1.95-2.06 (m, 1H, H5), 2.15-2.27 (m, 1H, H7b), 2.33 (t, 1H, H1, J=5.2), 2.43-2.51 (m, 1H, H4b), 2.55 (dd, 1H, H10a, J=14.2, 9.6), 2.90-3.04 (m, 1H, H3), 3.50 (d, 1H, H10b, J=13.9). Спектр ЯМР 13С (СDСl3, δ, м.д.): 21.4 (C8), 24.6 (C7), 25.6 (C9), 29.4 (C4), 39.9 (C3), 40.2 (C5), 42.3 (C6), 51.4 (C10), 56.8 (C1), 127.1, 141.0, 146.1 (CPy), 213.2 (C2). ИК спектр (KBr, ν, cm–1): 528, 609, 682, 756, 999, 1039 (SO2), 1178 (SO2), 1195 (SO2), 1242 (SO2), 1388, 1462, 1705 (С=O), 2873, 2949, 3435 (OH); MS (ESI, 5 kV): m/z (%): 231.14 (100) [M-1]-. Вычислено (%) для С10Н16O4S·4С5H5N: C 65.66, H 6.61, N 10.21, S 5.84; Найдено: С 65.85, Н 6.70, N 10.11, S 5.64.

((1S,2S,5R)-6,6-Диметил-3-оксобицикло[3.1.1]гептан-2-ил)метансульфоновая кислота ((2S)-10) (сольват с пиридином). К раствору 0.184 г (1 ммоль) тиола 2 в 20 мл пиридина при перемешивании добавляли водный раствор, содержащий 0.135 г (2 ммоль) ClO2. Время синтеза 1 ч. Реакционную смесь упаривали. Растворяли в Et2O. Осадок, содержащий С5H5N·НCl, удаляли. Раствор содержит сольват кислоты (2S)-10 с пиридином. Выход 0.60 г (95%). Вязкая жидкость. Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Hz): 0.80 (с, 3H, H8), 1.23 (д, 1H, H7а, J=10.6), 1.29 (с, 3H, H9), 2.05-2.13 (m, 1H, H5), 2.55–2.75 (м, 4H, H1, H4, H7b), 2.82 (dd, 1H, H10b, J=14.1, 8.8), 3.05 (d, 1H, H2, J=8.8), 3.62 (dd, 1H, H10b, J=13.3, 3.6). Спектр ЯМР 13С (CDCl3, δ, м.д.): 21.8 (C8), 26.5 (C9), 33.7 (C7), 38.5 (C5), 38.7 (C6), 42.5 (C1), 44.5 (C4), 52.9 (C10), 53.0 (C2), 212.1 (C3). ИК спектр (KBr, ν, cm–1): 478, 520, 603, 682, 754, 968, 997, 1035 st (SO2), 1163 st, 1999 st, 1226 st (SO2), 1386, 1485, 1714 st (С=O), 2883 st, 2924 st, 2972 st, 3439 st (OH); MS (ESI, 5 kV): m/z (%): 231.14 (100) [M–H]¯. Вычислено (%) для С10Н16O4S·5С5H5N: C 66.96, H 6.58, N 11.16, S 5.11; Найдено: С 66.85, Н 6.66, N 11.08, S 5.20.
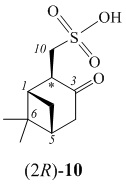
((1S,2R,5R)-6,6-Диметил-3-оксобицикло[3.1.1]гептан-2-ил)метансульфоновая кислота ((2R)-10). К раствору 0.184 г (1 ммоль) тиола (2S)-2 в 20 мл ацетонитрила при перемешивании добавляли водный раствор, содержащий 0.135 г (2 ммоль) ClO2. Время синтеза 1.5 ч. Экстрагировали хлороформом, водную фракцию упаривали. Сухой остаток водной фракции содержит смесь кислот (2S)-18:(2R)-18 в соотношении 1:2. Выход смеси кислот (2S)-10, (2R)-10 0.223 г (90%). Спектры ЯМР получены вычитанием сигналов из спектра смеси кислот (2S)-10, (2R)-10. Спектр ЯМР 1Н (D2O, δ, м.д., J/Hz): 0.90 (с, 3H, H8), 1.18 (д, 1H, H7а, J=11.3), 1.34 (с, 3H, H9), 2.09-2.19 (m, 1H, H5), 2.39-2.47 (м, 1H, H1), 2.47-2.60 (m, 3H, H4, H7b), 2.87–3.01 (m, 1H, H10a), 3.01-3.10 (m, 1H, H2), 3.28 (d, 1H, H10b, J=13.9). Спектр ЯМР 13С (D2O, δ, м.д.): 19.1 (C8), 25.5 (C9), 28.4 (C7), 37.3 (C5), 38.4 (C6), 41.2 (C1), 44.2 (C4), 49.2 (C2), 50.7 (C10), 218.0 (C3). ИК спектр (KBr, ν, cm–1): 478, 590, 607, 756, 918, 1039 st (SO2), 1161 st, 1205 st, 1234 st (SO2), 1369, 1408, 1467, 1714 st (С=O), 2877 st, 2924 st, 2964 st, 3327 st (OH); MS (ESI, 5 kV): m/z (%): 231.17 (100) [M-H]-. Вычислено (%) для С10Н16O4S: C 51.71, H 6.94, S 13.80; Найдено: С 51.65, Н 7.16, S 13.40.
Обоснование применения.
Сульфокислоты и тиолсульфонаты используются в качестве полупродуктов в органическом синтезе, в производстве некоторых химико-фармацевтических препаратов. Тиолсульфонаты и сульфоны обладают бактерицидной и фунгицидной активностями [D.R. Hogg. In Comprehensive Organic Chemistry, Vol. 3, Sulphur Compounds. (Eds. D. Barton, W.D. Ollis). Pergamon Press: Oxford (1979)].
Монотерпеноиды являются доступным растительным сырьем, обладающим природной хиральностью и биологической активностью [Paduch R., Kandefer-Szerszen M., Trytek M., Fiedurek J. Arch. Immun. Ther. Exp., 2007, 55, 315-327. DOI: 10.1007/s00005-007-0039-1]. Химическая модификация нативных терпеноидов зачастую усиливает биологическую активность или расширяет ее спектр [Никитина Л.Е., Артемова Н.П., Старцева В.А. Природные и тиомодифицированные производные. Germany: Lap Lambert, 2012, 168]. Известно, что пинановые гидрокситиолсульфонаты проявляют антимикробную активность в отношении Candida albicans, Staphylococcus aureus и Cryptococcus neoformans [O.N. Grebyonkina, O.M. Lezina, E.S. Izmest'ev, D.V. Sudarikov, S.V. Pestova, S.A. Rubtsova, A.V. Kutchin, Russ. J. Org. Chem. 2017, 53(6), 860].
В работе [L.E. Nikitina, N.P. Artemova, V.A. Startseva, I.V. Fedyunina, V.V. Klochkov, Chem. Nat. Comp. 2017, 53(5), 811] выявлено, что сульфон камфеновой структуры подавляет рецепторную активность тромбоцитов сильнее, чем ацетилсалициловая кислота и клопидогрель; практически полностью подавляет агрегацию тромбоцитов, индуцированную адреналином, АДФ и коллагеном.
Сульфокамфорная кислота используется в производстве лекарственных препаратов, обладающих коронарорасширяющей способностью, антибактериальной активностью, болеутоляющим свойством (сульфокамфокаин, полусинтетические пенициллины и цефалоспорины). Сульфонамиды на основе камфоры обладают ингибирующей активностью в отношении вирусов Эбола и Марбург [А.С. Соколова, Д.В. Баранова, О.И. Яровая, Д.С. Баев, О.А. Полежаева и др. Изв. АН, Сер. Хим., 2019, 5, 1041].
| название | год | авторы | номер документа |
|---|---|---|---|
| Хиральные γ-кетосульфанильные производные пинановой структуры и способ их получения | 2021 |
|
RU2783164C1 |
| Сульфопроизводные на основе бета-пинена и способ их получения | 2019 |
|
RU2708617C1 |
| ХИРАЛЬНЫЕ МИРТАНИЛСУЛЬФОНАМИДЫ | 2019 |
|
RU2725878C1 |
| Способ получения монотерпеновых сульфокислот | 2016 |
|
RU2651791C2 |
| Трифторметилированные монотерпеновые аминоспирты на основе нопинона, камфорохинона или вербанона | 2022 |
|
RU2802954C1 |
| Сульфопроизводные α-пинена | 2017 |
|
RU2657730C1 |
| Хиральные трифторметилированные монотерпеновые тиоацетаты и тиолы на основе миртеналя | 2020 |
|
RU2743302C1 |
| Сульфанильные и ацетилсульфанильные производные абиетанового типа | 2018 |
|
RU2689131C1 |
| Хиральные монотерпеновые сульфинамиды | 2017 |
|
RU2646959C1 |
| Хиральные 18-сульфопроизводные дегидроабиетана и способ их получения | 2020 |
|
RU2726793C1 |
Настоящее изобретение относится к способу получения хирального γ-кетосульфонильного производного пинановой структуры формулы (I) - тиолсульфонат (RSO2SR), сульфон (RSO2R), сульфокислота (RSO3H), включая его сольват:

где звездочкой обозначена связь, к которой присоединяется сульфогруппа (-SO2-). Способ заключается в окислении тиола пинановой структуры диоксидом хлора (ClO2) путем смешивания раствора тиола в органическом растворителе с водным или органическим раствором диоксида хлора. При этом в качестве исходного соединения используют γ-кетотиол пинановой структуры, для получения сульфокислоты в качестве растворителя используют пиридин или диметилформамид, для получения сульфона в качестве растворителя используют ацетонитрил, гексан или хлороформ, а для получения тиолсульфоната - ацетонитрил и катализатор VO(acac)2. Технический результат – получение хирального γ-кетосульфонильного производного пинановой структуры эффективным способом с высоким выходом.
Способ получения хирального γ-кетосульфонильного производного пинановой структуры формулы (I) - тиолсульфонат (RSO2SR), сульфон (RSO2R), сульфокислота (RSO3H), включая его сольват:

где звездочкой обозначена связь, к которой присоединяется сульфогруппа (-SO2-), заключающийся в окислении тиола пинановой структуры диоксидом хлора (ClO2) путем смешивания раствора тиола в органическом растворителе с водным или органическим раствором диоксида хлора, при этом в качестве исходного соединения используют γ-кетотиол пинановой структуры, для получения сульфокислоты в качестве растворителя используют пиридин или диметилформамид, для получения сульфона в качестве растворителя используют ацетонитрил, гексан или хлороформ, для получения тиолсульфоната - ацетонитрил и катализатор VO(acac)2.
| Лезина О.М | |||
| и др | |||
| Взаимодействие монотерпеновых гидрокситиолов с диоксидом хлора | |||
| ЖОрХ, 2015, т.51, Вып | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Сульфопроизводные на основе бета-пинена и способ их получения | 2019 |
|
RU2708617C1 |
| Agami, C | |||
| et al | |||
| A Convenient Access to Chiral Sulfonic Acids | |||
| Synthetic Communications, 1990, 20(21), 3289-3294 | |||
| Sokolova, A | |||
| S | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2022-09-23—Публикация
2021-06-28—Подача