Изобретение относится к области физических исследований вещества методами оптической спектроскопии с целью дискриминации различных энантиомеров хиральных соединений методами спектроскопии гигантского комбинационного рассеяния (ГКР) света. Изобретение позволяет проводить высокочувствительное и специфичное определение различных энантиомеров, что актуально для процессов производства энантиомерно чистых соединений, а также для исследования различных биологических образцов.
Известен способ детекции хиральных соединений описанный в патенте [1]. Этот способ позволяет детектировать хиральные аналиты, содержащие ароматические группы с помощью предложенного ахирального супрамолекулярного комплекса (СК) и индикаторного красителя (ИК). ИК связывается с СК только в том случае, если СК связал исследуемый аналит, в результате чего можно детектировать сигнал кругового дихроизма от полученного комплекса, причем сигал кругового дихроизма более интенсивен чем от аналита в отдельности, а также спектр кругового дихроизма от тройного комплекса смещается в видимый или ближний ультрафиолетовый диапазон, что облегчает его детектирование. К недостаткам известного способа стоит отнести то, что он подходит для детекции только ароматических соединений, а точнее соединений, которые могут связываться с СК. Во-вторых, в силу того, что уровень сигнала кругового дихроизма для биологических молекул составляет порядка 10-6 от величины абсорбции, то даже увеличение сигнала в несколько раз не дает значительного усиления чувствительности. Кроме того, известный способ позволяет определять хиральность аналитов только косвенным путем, по детекции сигнала от тройного комплекса, что менее предпочтительно чем определение хиральности непосредственно исследуемого аналита.
Известен способ получения спектров ГКР биологических молекул с высокой чувствительностью и устройство для его осуществления, описанные в заявке [2]. Известный способ позволяет увеличить сигнал ГКР за счет применения как ГКР-активного субстрата, так и помещения исследуемого аналита в резонатор-подобную структуру. К недостаткам известного способа стоит отнести то, что он не подходит для детекции различных энантиомеров, так как резонаторные структуры не позволяют сохранять информацию о направлении поляризации света. Кроме того, ГКР-активный субстрат не обладает возможностью приобретать или изменять свою хиральность при связывании хирального аналита, что также не позволяет применять известный способ для детекции хиральности органических молекул.
В результате поиска прототипа для предлагаемого решения обнаружено не было.
Техническим результатом предлагаемого изобретения является возможность специфичной и высокочувствительной дискриминации различных энантиомеров органических молекул методами поверхностно усиленной спектроскопии гигантского комбинационного рассеяния света, с помощью ГКР-активного субстрата с индуцируемой хиральностью в резонатор-подобных структурах.
Технический результат достигается тем, что предложен способ детекции энантиомеров хиральных органических молекул, включающий модификацию ахиральных нанопроволок молекулами исследуемого аналита и молекулами стандарта с известной хиральностью, иммобилизацию полученных модифицированных нанопроволок на нижней отражающей поверхности, нанесение на иммобилизованные модифицированные нанопроволоки верхней отражающей поверхности на заданном расстоянии, обеспечивающем увеличение амплитуды спектров гигантского комбинационного рассеяния, снятие спектров гигантского комбинационного рассеяния молекул исследуемого аналита.
Возможен частный случай, когда в качестве молекул стандарта с известной хиральностью используют D- или L-цистеин.
Возможен второй частный случай, в котором только нижняя отражающая поверхность, только верхняя отражающая поверхность или обе отражающие поверхности выполнены из материала, специфически отражающего и/или поглощающего излучение с заданным направлением поляризации.
Возможен третий частный случай, когда в качестве материалов нижней и верхней отражающих поверхностей используют металлы, диэлектрики, оптические мета-поверхности с упорядоченной периодической структурой.
Возможен четвертый частный случай, в котором для иммобилизации модифицированных нанопроволок применяют полимеры.
Возможен пятый частный случай, в котором заданное расстояние между нижней и верхней отражающей поверхностью варьируют путем нанесения различного количества полимера.
Возможен шестой частный случай, когда используют ахиральные нанопроволоки состоящие из золота и серебра, причем соотношение золота к серебру составляет от 0,1% до 99,9%.
Возможен седьмой частный случай, в котором используют ахиральные нанопроволоки диаметром от 1 до 20 нм, длиной не менее 50 нм.
Возможен восьмой частный случай, когда на поверхности ахиральных нанопроволок иммобилизуют лиганды, для обеспечения селективного связывания аналитов.
Детекция различных энантиомеров хиральных биологических молекул является важной задачей, так как энантиомеры используются в химическом синтезе сложных молекул и обладают различной биологической активностью. Традиционные подходы по измерению кругового дихроизма или дисперсии оптического вращения плохо подходят для дискриминации биологических молекул, так как абсорбция света, связанная с хиральностью может составлять всего 10-4-10-6 от общей абсорбции образца. Кроме того, для многих органических молекул диапазон длин волн, к котором проявляется максимальное различие энантиомеров находится в ультрафиолетовом диапазоне длин волн, где активно поглощают биологические молекулы, что также затрудняет детекцию. Улучшить чувствительность обнаружения хиральных биомолекул можно с помощью методов спектроскопии гигантского комбинационного рассеяния света, в частности поверхностно усиленной спектроскопии ГКР. Поверхностно усиленная ГКР наблюдается при помещении исследуемого образца вблизи ГКР-активного субстрата, например, металлических наноструктур, вблизи которых образуются сильные локальные поля, и эффект комбинационного рассеяния увеличивается на порядки (104-1010). Основные параметры эффекта ГКР связаны с морфологией плазмонных наночастиц и их относительным распределением в субстрате. В связи с этим было решено использовать ГКР-активный субстрат, содержащий плазмонные наночастицы в частности металлические наночастицы из золота и серебра, так как варьируя состав металлических наночастиц их размер и форму можно управлять длинами волн плазмонного резонанса в широком диапазоне длин волн, добиваясь тем самым усиления сигнала ГКР в определенном диапазоне длин волн. Применение металлических наноструктур в форме нанопроволок обусловлено тем, что наночастицы с данной геометрией, обладающие диаметром менее 20 нм, могут приобретать ту или иную хиральность в зависимости от хиральности связанных с ними молекул. При этом их размер и соотношение золота и серебра в составе можно подобрать так, чтобы сместить оптический сигнал от индуцированной хиральности в ту область спектра где сигнал можно будет детектировать с более низким фоном, а соответственно большей чувствительностью и достоверностью. Было обнаружено, что тонкие (менее 20 нм) металлические нанопроволоки, обладающие индуцированной L-хиральностью, сильнее усиливают спектры ГКР L-хиральных аналитов, а нанопроволоки, обладающие индуцированной D-хиральностью, сильнее усиливают спектры ГКР D-хиральных аналитов. При использовании распознающих молекул для дискриминации различных энантиомеров специфичность ограничена специфичностью связывания распознающих молекул и аналита, которая в случае детекции двух различных энантиомеров может быть снижена, а при непосредственном снятии спектров, исследуемых аналитов, неточностей и погрешностей, связанных с селективностью распознающих молекул, быть не может.Кроме того, чувствительность детекции также увеличена за счет применения резонатор-подобной структуры ГКР-активного субстрата, отражающие поверхности которой выполнены так, чтобы не изменять направление поляризации отраженного излучения и селективно отражать или поглощать свет различной поляризации. При этом диапазон длин волн в котором проходит усиление сигнала может быть изменен путем подбора расстояния между двумя отражающими структурами, что обеспечивает дополнительное усиление сигнала.
Реализация способа детекции энантиомеров хиральных органических молекул раскрывается на следующем примере.
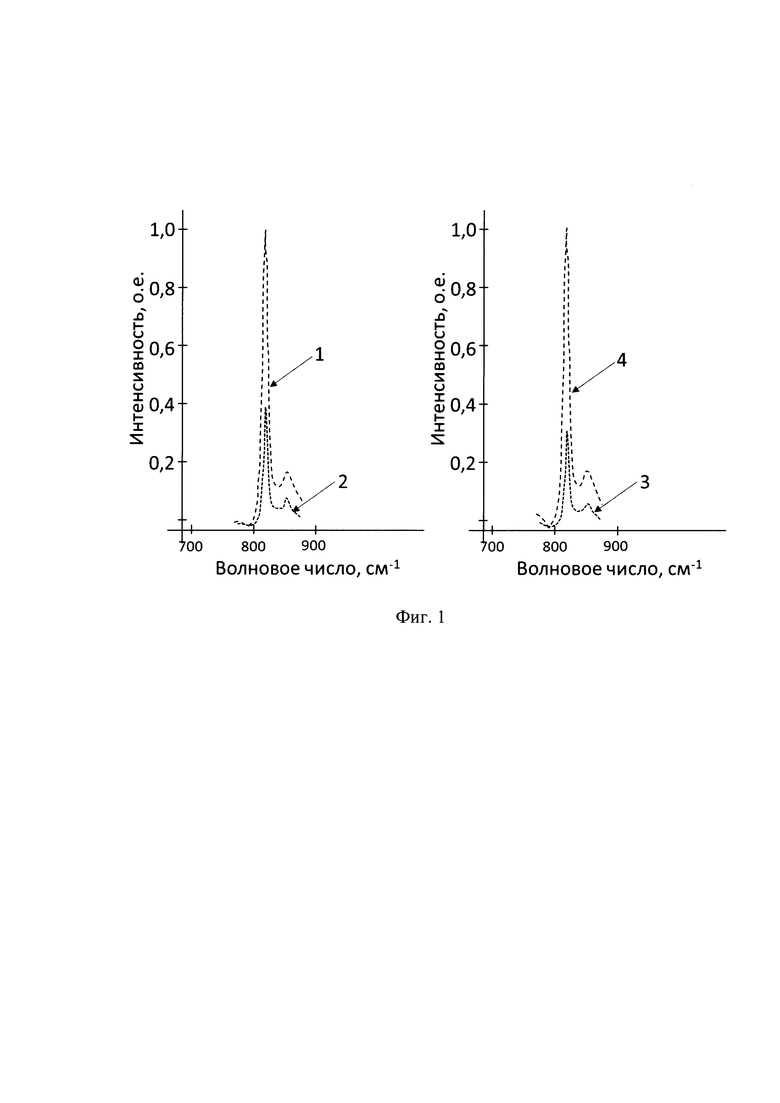
Для регистрации спектров применен спектрометр комбинационного рассеяния WITec 500 Alpha. В качестве исследуемых аналитов выбраны энантиомеры L- и D-цистеин. Металлические нанопроволоки получены путем инкубации смеси нитрата серебра, тетрахлорзолотоводородной кислоты и аскорбиновой кислоты в 50 мМ растворе поливинил пиррол идона в N,N-диметилформамиде при температуре 20°С в течение 18 ч. После завершения роста нанопроволок реакционную смесь центрифугировали и осадок перерастворяли в воде для получения ахиральных металлических нанопроволок. В результате были получены нанопроволоки со средним диаметром около 9 нм и длиной не менее 150 нм (оценено по результатам просвечивающей электронной микроскопии). Соотношение серебра к золоту в реакционной смеси составляло 1:1. Затем было приготовлено четыре раствора: стандарт L - 0,01 мМ раствор L-цистеина, стандарт D - 0,01 мМ раствор D-цистеина, аналит L - 0,1 мМ раствор L-тирозина, аналит D - 0,1 мМ раствор D-тирозина. Путем добавления к водному раствору металлических нанопроволок стандартов и аналитов были получены четыре образца для исследования: образец 1 - нанопроволоки + стандарт L + аналит L; образец 2 - нанопроволоки + стандарт L + аналит D; образец 3 - нанопроволоки + стандарт D + аналит L; образец 4 - нанопроволоки + стандарт D + аналит D. После этого исследуемые образцы были нанесены из раствора путем высушивания капли между нижней и верхней отражающими поверхностями, представляющими собой металлизированные подложки. Спектры поверхностно-усиленной спектроскопии гигантского комбинационного рассеяния описанных образов приведены на фиг.1 и обозначены цифрами от 1 до 4 в соответствии с номерами образцов (амплитуда спектров нормирована по образцу 1 (левый график) и образцу 4 (правый график)). Из анализа спектров видно, что максимально усиление сигнала происходит в образцах, в которых хиральности стандарта и исследуемого аналита совпадают, а само усиление интенсивности спектров ГКР происходит в 2,5-3 раза.
Предложенный способ детекции энантиомеров хиральных органических молекул позволяет с высокой чувствительностью определять хиральность органических молекул методом поверхностно-усиленной спектроскопии гигантского комбинационного рассеяния света при усилении интенсивности сигнала в резонатор-подобных структурах. При этом за счет использования нанопроволок, в качестве ГКР-активного субстрата с индуцированной хиральностью, можно определять хиральность исследуемого аналита путем добавления стандартов с известной хиральностью. Предлагаемый способ может быть эффективно использован как в научных исследованиях, так и в процессах синтеза и характеризации хиральных билдинг-блоков и готовых соединений.
Источники информации
1. Werner Nau, Frank Biedermann. Method for detecting a chiral analytes. Европейский патент ЕР 2899531 A2.
2. Соколов П., Мочалов К., Крюкова И. Способ регистрации спектров гигантского комбинационного рассеяния света и проточная ячейка для его реализации. Заявка на патент РФ RU 2021114719 А.
| название | год | авторы | номер документа |
|---|---|---|---|
| СУБСТРАТ ДЛЯ УСИЛЕННОЙ ПОВЕРХНОСТЬЮ СПЕКТРОСКОПИИ КОМБИНАЦИОННОГО РАССЕЯНИЯ СВЕТА | 2021 |
|
RU2763861C1 |
| СПОСОБ РЕГИСТРАЦИИ СПЕКТРОВ ГИГАНТСКОГО КОМБИНАЦИОННОГО РАССЕЯНИЯ СВЕТА И ПРОТОЧНАЯ ЯЧЕЙКА ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2021 |
|
RU2765617C1 |
| Способ получения усиленного сигнала комбинационного рассеяния света от молекул сывороточного альбумина человека в капле жидкости | 2019 |
|
RU2708546C1 |
| Оптический сенсор с плазмонной структурой для определения химических веществ низких концентраций и способ его получения | 2019 |
|
RU2720075C1 |
| Планарный наноструктурированный сенсор на основе поверхностного плазмонного резонанса для усиления комбинационного рассеяния света тромбоцитов человека и способ его получения | 2022 |
|
RU2788479C1 |
| Способ определения белков с помощью гигантского комбинационного рассеяния с использованием криозолей плазмонных наночастиц | 2019 |
|
RU2717160C1 |
| ПЛАНАРНЫЙ ТВЕРДОФАЗНЫЙ ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ОПРЕДЕЛЕНИЯ БЕЛКОВЫХ СОЕДИНЕНИЙ МЕТОДОМ СПЕКТРОСКОПИИ ГИГАНТСКОГО КОМБИНАЦИОННОГО РАССЕЯНИЯ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ДЕТЕКТИРОВАНИЯ БЕЛКОВЫХ СОЕДИНЕНИЙ | 2016 |
|
RU2659987C2 |
| Способ качественного и количественного определения биологически активного действующего вещества в водорастворимых лекарственных препаратах | 2021 |
|
RU2774817C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИОНОВ МЕТАЛЛА В РАСТВОРЕ | 2011 |
|
RU2460060C1 |
| КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ГКР-АКТИВНОСТЬЮ ДЛЯ ОПРЕДЕЛЕНИЯ ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ В УГЛЕВОДОРОДНЫХ ПРОДУКТАХ, СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ, ПЛАНАРНЫЙ ТВЕРДОФАЗНЫЙ ОПТИЧЕСКИЙ СЕНСОР НА ЕЕ ОСНОВЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ СЕНСОРА ДЛЯ АНАЛИЗА ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2016 |
|
RU2627980C1 |
Изобретение относится к области физических исследований вещества методами оптической спектроскопии и касается способа детекции энантиомеров хиральных органических молекул. Способ включает в себя модификацию ахиральных нанопроволок молекулами исследуемого аналита и молекулами стандарта с известной хиральностью, иммобилизацию полученных модифицированных нанопроволок на нижней отражающей поверхности, нанесение на иммобилизованные модифицированные нанопроволоки верхней отражающей поверхности на расстоянии, обеспечивающем увеличение амплитуды спектров гигантского комбинационного рассеяния, и снятие спектров гигантского комбинационного рассеяния молекул исследуемого аналита. Технический результат заключается в обеспечении возможности специфичной и высокочувствительной дискриминации различных энантиомеров органических молекул. 8 з.п. ф-лы, 1 ил.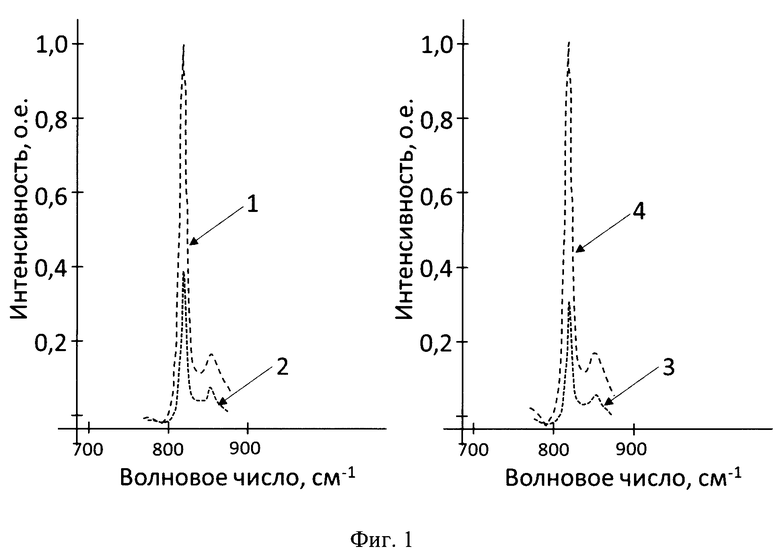
1. Способ детекции энантиомеров хиральных органических молекул, включающий модификацию ахиральных нанопроволок молекулами исследуемого аналита и молекулами стандарта с известной хиральностью, иммобилизацию полученных модифицированных нанопроволок на нижней отражающей поверхности, нанесение на иммобилизованные модифицированные нанопроволоки верхней отражающей поверхности на заданном расстоянии, обеспечивающем увеличение амплитуды спектров гигантского комбинационного рассеяния, снятие спектров гигантского комбинационного рассеяния молекул исследуемого аналита.
2. Способ по п. 1, отличающийся тем, что в качестве молекул стандарта с известной хиральностью используют D- или L-цистеин.
3. Способ по п. 1, отличающийся тем, что только нижняя отражающая поверхность, только верхняя отражающая поверхность или обе отражающие поверхности выполнены из материала, специфически отражающего и/или поглощающего излучение с заданным направлением поляризации.
4. Способ по пп. 1, 3, отличающийся тем, что в качестве материалов нижней и верхней отражающих поверхностей используют металлы, диэлектрики, оптические мета-поверхности с упорядоченной периодической структурой.
5. Способ по п. 1, отличающийся тем, что для иммобилизации модифицированных нанопроволок применяют полимеры.
6. Способ по п. 1, отличающийся тем, что заданное расстояние между нижней и верхней отражающей поверхностью варьируют путем нанесения различного количества полимера.
7. Способ по п. 1, отличающийся тем, что используют ахиральные нанопроволоки, состоящие из золота и серебра, причем соотношение золота к серебру составляет от 0,1% до 99,9%.
8. Способ по пп. 1, 7, отличающийся тем, что используют ахиральные нанопроволоки диаметром от 1 до 20 нм, длиной не менее 50 нм.
9. Способ по пп. 1, 7, 8, отличающийся тем, что на поверхности ахиральных нанопроволок иммобилизуют лиганды для обеспечения селективного связывания аналитов.
| EP 2899531 B1, 14.06.2017 | |||
| CN 111272728 A, 12.06.2020 | |||
| US 8638434 B2, 28.01.2014 | |||
| СПОСОБ АНАЛИЗА ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ | 1991 |
|
RU2014588C1 |
Авторы
Даты
2022-10-04—Публикация
2021-12-29—Подача