Настоящее изобретение относится к области технологий материалов, материаловедческих и аналитических исследований, и может быть использовано в нефтехимической промышленности для качественного и количественного обнаружения полиароматических гетероциклических серосодержащих соединений в нефтепродуктах с высокими чувствительностью, селективностью и экспрессностью.
Из уровня техники известны решения, направленные на создание оптических сенсорных устройств на основе наночастиц благородных металлов. Данные сенсорные устройства позволяют разрабатывать новые подходы к высокочувствительному, селективному и экспрессному определению набора химических соединений в различных диагностических целях. Создаваемые планарные оптические сенсоры - многослойные структуры на специальном субстрате-подложке, способные модулировать сигнал (усиливать интенсивность, изменять частоту и т.д.) - однозначно необходимы для перехода на современные технологии «lab-on-chip» («лаборатории на чипе»), что позволяет совершенствовать современные аналитические методы, применяемые как в, так и вне лаборатории. Известные решения находят применение в широком круге таких приложений, как диагностика здоровья, мониторинг экологического состояния окружающей среды, детектирование наркотических и взрывоопасных веществ. К особому классу оптических сенсоров относятся устройства, действие которых основано на принципах спектроскопии гигантского комбинационного рассеяния (ГКР, от англ. SERS - Surface Enhanced Raman Scattering). Известно, что наночастицы благородных металлов и нанокомпозиционные материалы на их основе способны усиливать сигнал комбинационного рассеяния в 106-1014 раз за счет их способности генерировать локальное электромагнитное поле, взаимодействующее с колебательными состояниями анализируемых органических молекул. Явление ГКР открывает новые возможности в понижении предела обнаружения по сравнению с известными методами и создании сверхчувствительных диагностических методов анализа. Как правило, эффективное использование спектроскопии ГКР однозначно накладывает требование на наличие полосы поглощения целевых анализируемых веществ в видимой области длин волн (350-750 нм). При этом введение в состав структуры сенсорного устройства дополнительных реагентов или изменение химического состава слоев, то есть химическое модифицирование, призвано усилить чувствительность и селективность подобных датчиков.
Из уровня техники известно решение, представленное в статье «Graphene oxide and shape-controlled silver nanoparticle hybrids for ultrasensitive single-particle surface-enhanced Raman scattering (SERS) sensing» (W. Fan, Y.H. Lee, S. Pedireddy, Q. Zhang, T. Liu and X. Y. Ling, Nanoscale, 2014, 6, 4843-4851, DOI: 10.1039/c3nr06316j). В данном гибридном материале оксид графена совмещен с наночастицами серебра контролируемой формы: октаэдрической (336±18 нм), сферической (151±25 нм) или кубической (121±7 нм). Оксид графена согласно данной работе синтезируется на основе порошка графена, модифицированного по методу Хаммерса (N.I. Kovtyukhova, P.J. Ollivier, В.R. Martin, Т.Е. Mallouk, S.A. Chizhik, Е.V. Buzaneva and A.D. Gorchinskiy, Chem. Mater., 1999, 11, 771-778; DOI: 10.1021/cm981085u), в несколько последовательных стадий, первая из которых состоит в добавлении к порошку концентрированного раствора серной кислоты, пероксодисульфата калия и пентаоксида фосфора при нагревании. Затем следует промывка водой и сушка полученного недоокисленного порошка под вакуумом. Далее следует стадия окисления порошка перманганатом калия в присутствии концентрированной серной кислоты, а также пероксидом водорода. После этого осуществляют промывку порошка раствором соляной кислоты. При этом в качестве источника серебра служат наночастицы в форме нанокубов, октаэдров (А. Тао, Р. Sinsermsuksakul and P.D. Yang, Angew. Chem., Int. Ed., 2006, 45, 4597-4601. DOI: 10.1002/anie.200601277) и сфер (P.С. Lee, D. Meisel, J. Phys. Chem., 1982, 86 (17), 3391-3395: DOI: 10.1021/j100214a025). Полученный нанокомпозит серебро-углерод, нанесенный на модифицированный кремниевый субстрат, способен усиливать сигнал комбинационного рассеяния, что позволяет детектировать ароматические соединения на уровне 10-9 М.
Однако известное решение предполагает осуществление большого количества трудоемких и длительных стадий синтеза, что приводит к неполной воспроизводимости свойств получаемых материалов. Кроме того, из-за использования дополнительных реагентов - стабилизаторов и ПАВ необходимым этапом получения геля являются многократные промывки. Неполнота отмывки наночастиц серебра от ПАВ и стабилизаторов приводит к появлению мешающих сигналов в спектрах ГКР (гигантского комбинационного рассеяния). Также описанный способ получения геля невозможно адаптировать под массовое производство, он требует использования труднодоступных, дорогостоящих реактивов. Более того, указанное решение не ориентировано на определение полиароматических гетероциклических серосодержащих соединений (ПАГС) поскольку максимум поглощения ПАГС находится в более коротковолновой области, чем возбуждающее лазерное излучение и полоса плазмонного резонанса наночастиц серебра.
Из уровня техники также известен метод получения нанокомпозита оксида графена с наночастицами серебра, описанный в работе «Surface-enhanced Raman spectroscopy for DNA detection by the self-assembly of Ag nanoparticles onto Ag nanoparticle-graphene oxide nanocomposites» (T. Lin, H. Wu, T. Tasi, Y. Lai and H. Shen, Phys. Chem. Chem. Phys., 2015, 17, 18443-18448, DOI: 10.1039/C5CP02805A). Данный способ получения нанокопозитного материала не требует дополнительных стадий и реагентов и состоит в нагревании водной суспензии оксида графена (N.I. Kovtyukhova, P.J. Ollivier, В.R. Martin, Т.Е. Mallouk, S.А. Chizhik, Е.V. Buzaneva and A.D. Gorchinskiy, Chem. Mater., 1999, 11, 771-778; DOI: 10.1021/cm981085u) с раствором нитрата серебра, сопровождающееся прикапыванием цитрата натрия. Получаемый гибридный материал следующего состава: наночастицы серебра (ок. 15.6 нм) - наночастицы серебра (ок. 57.5 нм) - оксид графена - позволяет мультиплексно детектировать различные аналиты на уровне концентраций 10-6-10-12 М.
Однако известный способ характеризуется невозможностью контроля процессов зародышеобразования и получения наночастиц серебра с узким распределением частиц по размерам, что не позволяет использовать получаемый нанокомпозитный материал в качестве активного слоя в сенсорном устройстве для количественного определения актуальных аналитов.
Из уровня техники известен химически модифицированный планарный оптический сенсор, содержащий последовательно расположенные: 1) подложку-субстрат на основе диэлектрического химически инертного материала; 2) наноструктурированное покрытие на основе наночастиц благородных металлов (М. Piliarik, J. Homola, Surface plasmon resonance (SPR) sensors: approaching their limits? OPTICS EXPRESS, 2009, Vol. 17, №19, 16505-16517). Принцип работы данного сенсора основан на изменении показателя преломления на границе раздела между анализируемой средой и сенсорным устройством. В целях улучшения селективности сенсорного устройства его химически модифицируют путем нанесения мономолекулярных слоев дополнительных реагентов непосредственно на наноструктурированную металлическую поверхность.
Однако известное сенсорное устройство не применимо в анализе ПАГС из-за его недостаточной селективности, поскольку регистрируемый сигнал не содержит структурной информации об анализируемых молекулах и не может использоваться в анализе многокомпонентных смесей целевых аналитов. Кроме того, нанесение любого дополнительного слоя на поверхность наноструктурированного металла приводит к нарушению функциональности сенсора.
Из уровня техники известно решение, представленное в заявке на изобретение US 2005/017981, МПК G01N 21/65 (2006.01), опуб.19.05.2005 - «Оптический датчик с многослойной плазмонной структурой для усовершенствованного обнаружения химических групп посредством SERS», описывающее оптический сенсор, действие которого основано на использовании спектроскопии комбинационного рассеяния, способ его получения и способ анализа с его использованием. Способ получения и способ анализа, описанный в этом литературном источнике, включает нанесение на химически модифицированный планарный оптический сенсор пробы с исследуемым соединением с образованием привитых к поверхности сенсора соединений и их детектирование с помощью спектроскопии (ГКР) с последующей расшифровкой спектров ГКР по характеристическим колебаниям анализируемых соединений с использованием стандартного программного обеспечения. Известное сенсорное устройство состоит из: 1) подложки, на основе диэлектрического химически инертного материала; 2) «плазмон-резонансного зеркала» из благородных металлов, сформированное на чувствительной поверхности подложки; 3) слоя плазмон-резонансных частиц, размещенного поверх зеркала; 4) слоя оптически прозрачного диэлектрика толщиной около 2-40 нм, разделяющего зеркало и слой частиц. С использованием описанного сенсорного устройство возможно детектировать аналит с коэффициентом усиления до 1012, т.е. обнаруживать единичные молекулы аналита. В качестве технического результата известного решения повышается чувствительность анализа.
Однако известная группа изобретений не позволяет проводить высокочувствительный анализ ПАГС, поскольку данные соединения, содержащиеся в нефти, поглощают излучение в УФ-области 270-280 нм, что намного выше по энергии по сравнению с плазмонной полосой поглощения Ag (420 нм) и Au (520 нм), что делает их практически не детектируемыми для спектроскопии ГКР.
Наиболее близким к заявляемому является группа изобретений, представленная в патенте на изобретение RU2572801 «Химически модифицированный планарный оптический сенсор, способ его изготовления и способ анализа полиароматических гетероциклических серосодержащих соединений с его помощью», раскрывающая планарный оптический сенсор, содержащий последовательно расположенные подложку на основе диэлектрического химически инертного материала, наноструктурированное покрытие толщиной 1-10 мкм на основе наночастиц благородных металлов, размеры которых составляют 20-90 нм, и прозрачную микропористую пленку хитозана, химически модифицированную π-акцепторным соединением, способным распознавать анализируемое вещество и химически связываться с ним путем формирования комплекса с переносом заряда, способ получения указанного оптического сенсора и способ анализа полиароматических гетероциклических серосодержащих соединений с использованием данного сенсора. Преимуществом заявляемой группы изобретений является способность предконцентрировать и селективно связывать анализируемое вещество, контролируемо смещать область полосы поглощения анализируемого вещества в составе комплекса с переносом заряда, обнаруживать аналит с коэффициентом усиления до 1012, в том числе за счет резонансных оптических явлений, при этом также стоит отметить сокращение расхода благородного металла, а значит, уменьшение стоимости сенсора, а также потенциальную миниатюризацию устройства за счет минимизации рабочей площади элемента сенсора до менее, чем 4×4 мм2.
Недостатком известного технического решения является невозможность использования гибких и пористых подложек, поскольку при получении сенсора используются достаточно высокие температуры. Более того, данное техническое решение не предполагает получения сенсорного устройства с равномерным распределением наночастиц благородных металлов по поверхности, что не позволяет регистрировать воспроизводимый на всей сенсорной поверхности усиленный сигнал ГКР. Также в связи с трудоемкостью процедуры аэрозольного пиролиза наночастиц серебра на предварительно травленное предметное стекло, данное техническое решение не масштабируемо. Кроме того, согласно известному техническому решению затруднительным является процесс нарезания полученной пластинки (5 см × 5 см) с сенсибилизированной поверхностью на небольшие сенсоры (4 см × 4 см) со строго заданной площадью.
Задачей настоящей группы изобретений является получение планарных оптических сенсоров, позволяющих использовать метод спектроскопии гигантского комбинационного рассеяния (ГКР) с высоким коэффициентом чувствительности (низким пределом обнаружения), высокой селективностью, широким диапазоном определяемых концентраций, высокими воспроизводимостью и прецизионностью.
Поставленная задача решается композицией, обладающей ГКР-активностью для определения полиароматических гетероциклических серосодержащих соединений в углеводородных продуктах, представляющей собой хемотропный гель, характеризующийся параметрами динамической вязкости 0.1-1 сП, содержащий полимерную матрицу с наночастицами серебра анизотропной формы с размерами 10-90 нм и частицами оксида графена с размерами 1-2 мкм, при этом количество каждого компонента - наночастиц серебра и частиц оксида графена, в полимерной матрице составляет от 0.5 до 5 масс. %.
При этом не менее 90% наночастиц серебра и частиц оксида графена присутствуют в полимерной матрице в виде композиционных частиц, при этом на 0.1 мкм2 площади поверхности частицы оксида графена приходится от 10 до 40 наночастиц серебра.
Предпочтительно, что в качестве полимерной матрицы использованы вещества, устойчивые к воздействию неполярных растворителей.
Предпочтительно в качестве полимерных веществ, устойчивых к воздействию неполярных растворителей использовать альгинат натрия, или хитозан, или гидроксиэтилцеллюлоза.
Предлагаемая композиция характеризуется полосой плазмонного резонанса 400-450 нм, при этом композиционные частицы в геле распределены равномерно, а наночастицы серебра равномерно распределены по поверхности частицы оксида графена.
Поставленная задача также решается способом получения заявляемой композиции, обладающей ГКР-активностью, включающим синтез оксида серебра из 0.01-0.05 М раствора нитрата серебра, после чего полученную суспензию растворяют в водном растворе аммиака, взятого в двух-четырехкратном молярном избытке по отношению к нитрату серебра, полученный раствор, содержащий аммиачный комплекс серебра, смешивают с оксидом графена с размерами частиц 1-2 мкм, взятых в количестве 1-10 ммоль на 10 мл раствора, после чего в полученную суспензию последовательно вводят нитрат серебра и восстанавливающий агент для получения наночастиц серебра в суспензии размерами 10-90 нм, в которую затем вводят полимерный порошок для перевода суспензии в хемотропный гель.
Предпочтительно, использовать 10-20 мас.% водный раствор аммиака с концентрацией.
Предпочтительно, частицы оксида графена получать по модифицированному методу Хаммерса.
Предпочтительно, для получения наночастиц серебра с размерами 10-90 нм вводить нитрат серебра в количестве 10-30 ммоль в расчете на 10 мл полученной суспензии нанокомпозита серебро-углерод.
Предпочтительно, в качестве восстанавливающего агента использовать аскорбиновую кислоту, или боргидрид натрия, или гидроксиламинхлорид.
Предпочтительно, что восстанавливающий агент вводят в количестве 5-100 ммоль в расчете на 10 мл суспензии нанокомпозита серебро-углерод.
Предпочтительно, в качестве полимерного порошка использовать гидроксиэтилцеллюлозу, или хитозан, или альгинат натрия, в количестве из расчета 1 г порошка на 10-30 мл суспензии.
Также поставленная задача решается планарным твердофазным оптическим сенсором для определения полиароматических гетероциклических серосодержащих соединений в углеводородных продуктах, включающим размещенную на основе пленку толщиной до 5 мкм, полученную из заявляемой композиции и содержащую на поверхности π-акцепторное соединение.
Предпочтительно, в качестве основы для сенсора использовать стекло или гибкие и пористые материалы, например, хроматографическая бумага, фольга.
Поставленная задача также решается способом получения планарного твердофазного оптического сенсора для определения полиароматических гетероциклических серосодержащих соединений в углеводородных продуктах, включающим нанесение на основу заявляемой композиции толщиной от 1 до 100 мкм, с последующим высушиванием до образования пленки на поверхности основы, и модифицированием поверхности полученной пленки раствором π-акцепторного соединения концентрацией 0.1-10 ммоль/л, при этом раствор π-акцепторного соединения наносят на поверхность геля в количестве 0.2-1 мкл на 1 мм2.
Предпочтительно, в качестве π-акцепторного соединения использовать соединение из ряда: 1,4-бензохинон (БХ); 2,5-дихлор-3,6-диокси-1,4-бензохинон, или хлораниловая кислота (ХЛК); 2,3-дихлор-5,6-дициано-1,4-бензохинон (ДДХ); 7,7,8,8-тетрацианохинондиметан (ТЦХМ); тетрацианоэтилен (ТЦНЭ); 9,10-антрацендион (АД); 2,4,5,7-тетранитро-9-флуоренон (ТНФ); 2,7-динитро-9-флуоренон (ДНФ). При этом раствор π-акцепторного соединения представляет собой раствор соединения в органических растворителях, выбранных из ряда: хлороформ, изопропанол, диэтиловый эфир.
Предпочтительно, наносить хемотропный гель на основу методом пропитки или трафаретной печати.
Предпочтительно, в качестве основы использовать стекло или такие гибкие и пористые материалы, как хроматографическая бумага и фольга.
Также поставленная задача решается способом анализа полиароматических гетероциклических серосодержащих соединений, включающим нанесение на предлагаемый планарный твердофазный оптический сенсор жидкой пробы с исследуемым соединением с образованием окрашенного межмолекулярного комплекса π-акцепторного соединения с полиароматическими гетероциклическими серосодержащими соединениями, и о качественном и количественном содержании гетероциклических соединений судят по результатам анализа, проведенного методом спектроскопии гигантского комбинационного рассеяния. При этом на поверхность сенсора предпочтительно накапывать жидкие пробы объемом 10-50 мкл для качественного и количественного определения анализируемых веществ с концентрациями 10-6-10-3 М.
Предпочтительно при проведении анализа использовать лазерное излучение с длиной волны 514 или 532, или 633, или 785 нм и мощностью, не превышающей 10% от номинальной величины, при облучении сенсора с нанесенной пробой не более 10 секунд.
Техническим результатом предлагаемого изобретения является то, что получено универсальное сенсорное устройство для определения ПАГС в агрессивных безводных средах анализируемых нефтепродуктов. Данный технический результат достигается за счет устойчивости хемотропного геля, наносимого на основу к воздействию неполярных растворителей и обладающего химическим сродством к полиароматическим гетероциклических серосодержащим соединениям. Кроме того, за счет равномерного распределения наночастиц серебра и частицы оксида графена в геле что позволяет регистрировать воспроизводимый на всей сенсорной поверхности усиленный сигнал ГКР. Усиление сигнала комбинационного рассеяния в 103-106 раз достигается за счет полосы плазмонного резонанса хемотропного геля 400-450 нм. Еще одним преимуществом предлагаемого изобретения является использование гибких и пористых подложек, что позволяет масштабировать данное техническое решение.
Предлагаемый оптический сенсор имеет незначительный фоновый сигнал на спектрах гигантского комбинационного рассеяния, что позволяет определять ПАГС в углеводородах на уровне 10-5 М или порог обнаружения ПАГС на уровне 10-6 М.
Заявляемая группа изобретений позволяет эффективно предконцентрировать и селективно связывать анализируемое вещество, контролируемо смещать область полосы поглощения анализируемого вещества в составе комплекса с переносом заряда, обнаруживать аналит с коэффициентом усиления до 1012, в том числе за счет резонансных оптических явлений. При этом также стоит отметить потенциальную миниатюризацию устройства за счет минимизации рабочей площади элемента сенсора до менее, чем 4×4 мм2, сокращение расхода благородного металла, а значит, уменьшение стоимости сенсора.
Таким образом, использование предлагаемого сенсора позволяет детектировать сигнал ГКР с высоким коэффициентом чувствительности, высокой селективностью, широким диапазоном определяемых концентраций, высокой воспроизводимостью и прецизионностью.
На первой стадии для получения наноструктурированных планарных оптических сенсоров синтезируют нанокомпозит серебро-углерод. Синтез проводят следующим образом: 0.1 М водный раствор гидроксида натрия добавляют по каплям в свежеприготовленный 0.02 М водный раствор нитрата серебра взятых в объемном соотношении 1:1±3:1 до полного осаждения коричневого осадка - оксида серебра (I). Полученный осадок тщательно промывают денонсированной водой высокой чистоты для этого надосадочный раствор отделяют декантацией 3-5 раз. После промывки к полученному осадку приливают деионизированную воду высокой чистоты объемом, равным первоначальному раствору нитрата серебра. Полученную смесь интенсивно взбалтывают и отставляют до оседания взвеси на 1-10 мин. Раствор, образовавшийся над осадком, сливают, а полученный осадок растворяют в двукратном по отношению к нитрату серебра молярном избытке 10-20% водного раствора аммиака. Затем прозрачный раствор аммиачного комплекса серебра фильтруют через мембранный фильтр с размером пор 450±100 нм. Параллельно водную суспензию 1.667 М оксида графена, полученного согласно общеизвестному модифицированному методу Хаммерса и характеризующегося соотношением ID-моды/IG-моды=1.935, D-мода при 1351 см-1 и G-мода при 1598 см-1, обрабатывают ультразвуковым излучением для повышения гомогенности суспензии в течение 10-30 мин. Далее полученную суспензию оксида графена разбавляют деионизированной водой до исходного объема раствора нитрата серебра и полностью вносят в полученный раствор аммиачного комплекса серебра. Смесь нагревают до кипения на плитке с магнитной мешалкой при интенсивном перемешивании в течение 30-40 мин. После этого раствор охлаждают до комнатной температуры (22-23°С), центрифугируют при 8000±1000 об/мин в течение 15±5 мин и отмывают нанокомпозит серебро-углерод деионизированной водой высокой чистоты 5-10 раз с последующим контролем структуры полученной суспензии методом электронной микроскопии. Избыток раствора аммиака в реакционной смеси приводит к частичному аминированию поверхности композита, при этом происходит модификация функциональных групп на поверхности оксида графена. Ниже представлена возможная модификация функциональных групп поверхности оксида серебра при кипячении в избытке раствора аммиака. На этой стадии наночастицы серебра в нанокомпозите имеют сферическую форму со средним размером наночастиц (13±5) нм.
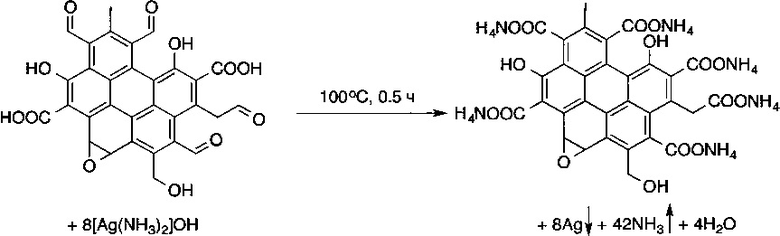
На второй стадии проводят процесс химического доращивания наночастиц серебра в нанокомпозите, с приданием им анизотропной ограненной формы. Для этого к полученной на первой стадии суспензии нанокомпозита серебро-углерод при перемешивании добавляют 0.001 М раствор свежеприготовленного нитрата серебра в объемном соотношении 1:1-1:3 и выдерживают полученную смесь в течение 10-30 минут при постоянном перемешивании. Затем к полученному раствору добавляют свежеприготовленный 0.001-0.005 М водный раствор восстанавливающего агента: или аскорбиновой кислоты, или тетрабората натрия, или гидроксиламинхлорида, объемом, равным исходному объему раствора с суспензией нанокомпозита. Полученную смесь выдерживают при комнатной температуре и перемешивании в течение 1-2 ч с использованием магнитной мешалки для более полного восстановления ионов серебра. Реакция полученного нанокомпозита со смесью водных растворов нитрата серебра и аскорбиновой кислоты приводит к тому, что исходные наночастицы серебра выступают в виде затравок, центров кристаллизации, приводящих к росту более крупных, физически контактирующих друг с другом наночастиц, образующих при подобном контакте «горячие точки», которые способствуют последующему максимальному усилению сигнала комбинационного рассеяния. После этого раствор центрифугируют при 8000±1000 об/мин в течение 15±5 мин, полученный доращенный нанокомпозит серебро-углерод отмывают деионизированной водой высокой чистоты 5-10 раз с последующим контролем структуры полученной суспензии методом электронной микроскопии. Наночастицы серебра в полученном на этом этапе нанокомпозите имеют анизотропную форму со средним распределением по размерам 10-70 нм, что является оптимальным для реализации эффекта ГКР, а размер частиц самого нанокомпозита лежит в пределах 1-15 мкм. Полученный нанокомпозит тем самым концентрирует наночастицы серебра, при этом имеет достаточно большую площадь поверхности и может быть эффективно отделен от маточного раствора центрифугированием и даже седиментацией.
На третьей стадии получают хемотропный гель. Для этого к суспензии нанокомпозита с дорощенными наночастицами серебра, полученную на второй стадии разбавляют деионизированной водой до объема, в соотношении 1:1-2:1 с исходным объемам нитрата серебра, далее в полученный раствор вносят сухой полимерный порошок из ряда гидроксиэтилцеллюлоза, хитозан, альгинат натрия 1-2 г на 30 мл, выдерживают полученную смесь при комнатной температуре и постоянном перемешивании на средней мощности магнитной мешалки до полного растворения полимерного порошка, затем проводят процесс гомогенизации полученного геля в планетарной мельнице в течение 15-30 мин. Из полученного геля, удаляют водную фазу путем высушивания при комнатной температуре (22-23°С) в течение 5-15 ч (до полного затвердевания слоя геля и формирования пористой пленки на поверхности основы) или с использованием лиофильной сушки при температуре - 40±10°С и давлении 1.000 мбар. На этой стадии формируется высокопористый нанокомпозит в виде объемного материала или пористой пленки площадью поверхности до 400 м2/г, полосой плазмонного резонанса в видимой области спектра 400-450 нм и динамической вязкостью 0.1-1 сП.
Процесс гомогенизации геля можно проводить в планетарной мельнице или с применением лабораторной мешалки с верхним приводом для перемешивания вязких сред. Использование на этой стадии процесса гомогенизации приводит не только к более равномерному распределению компонентов, что важно с точки зрения большей воспроизводимости оптического анализа, в частности регистрации сигнала ГКР, но и формированию достаточно стабильной системы жидкость - воздух (пену), высушивание которой на воздухе приводит к образованию покрытия с увеличенной площадью поверхности.
Преимуществом предлагаемого способа получения хемотропного геля на основе нанокомпозита наночастиц серебро-углерод, состоит в том, что:
- осуществляется контроль процессов зародышеобразования,
- не требуется использование ПАВ и стабилизаторов как в синтезе нанокомпозита серебро-углерод, так и при последующем доращивании наночастиц серебра,
- наночастицам серебра придается анизотропная форма с достаточно узким распределением частиц по размерам,
- полученный нанокомпозита серебро-углерод смешивается с полимерным материалом из следующего ряда: гидроксиэтилцеллюлоза, хитозан, альгинат натрия,
- смесь нанокомпозита серебро-углерод с полимером гомогенизируется в планетарной мельнице.
На четвертой стадии проводят процедуру нанесения гомогенизированного геля на основу (подложку). В качестве основы для нанесения используют целлюлозу или другие гибкие и пористые материалы (хроматографическая бумага, фольга, стекло) методом пропитки, трафаретной печати (воспроизведение поверхности планарного оптического сенсора при помощи трафаретной печатной формы, сквозь которую нанокомпозиционный ксерогель проникает на запечатываемый материал - субстрат) наносят хемотропный гель на основе нанокомпозита серебро-углерод до толщины 1-100 мкм. При этом подложка представляет собой гибкий, пористый, длинномерный субстрат, выполняющий функции предконцентрирования и/или пространственного разделения смеси аналитов. При этом наночастицы благородных металлов имеют размеры 10-90 нм, удельная площадь поверхности нанокомпозита составляет от 50 до 400 м2/г, а толщина сухого покрытия из хемотропного геля составляет слой менее 5 мкм.
На пятой стадии полученную сенсорную поверхность нарезают канцелярским ножом на небольшие пластинки площадью 10-20 мм2. Затем поверхность планарного оптического сенсора дополнительно химически модифицируют π-акцепторным соединением, способным распознавать анализируемое вещество и химически связываться с ним путем формирования комплекса с переносом заряда (КПЗ). При этом образование КПЗ состава ПАГС: π-акцептор на поверхности сенсора обеспечивает высокую скорость анализа при высоком значении соотношения сигнал/шум и отсутствии ложной спектральной информации.
При этом в качестве π-акцепторного соединения наиболее технологично использовать соединение из ряда: 1,4-бензохинон (БХ); 2,5-дихлор-3,6-диокси-1,4-бензохинон или хлораниловая кислота (ХЛК); 2,3-дихлор-5,6-дициано-1,4-бензохинон (ДДХ); 7,7,8,8-тетрацианохинондиметан (ТЦХМ); тетрацианоэтилен (ТЦНЭ); 9,10-антрацендион (АД); 2,4,5,7-тетранитро-9-флуоренон (ТНФ); 2,7-динитро-9-флуоренон (ДНФ). Наиболее технологично наносить раствор π-акцепторного соединения в органических растворителях, выбранных из ряда: хлороформ, изопропанол, диэтиловый эфир, обеспечивающих концентрацию π-акцепторного соединения 1-10 мМ.
После высушивания в лиофилизаторе (вакуумном сублиматоре) при температуре -40±10°С и давлении 1.000 мбар или высушивали на воздухе при комнатной температуре (22-23°С) в течение 5-15 ч полученные структуры могут быть использованы в качестве планарных оптических сенсоров. Полученные спектральные данные свидетельствуют о том, что использование лиофильной сушки не является необходимой процедурой и достаточно получение ксерогелей путем высушивания при комнатной температуре на воздухе. При этом наличие пиков D- и G- мод графена не мешает определению аналита, более того, эти пики могут в дальнейшем использоваться как внутренний эталон для получения количественных данных о концентрации аналита.
При проведении анализа на поверхности химически модифицированного планарного оптического сенсора формируется окрашенный комплекс с переносом заряда (КПЗ), в котором ПАГС выступают в роли эффективных донорами электронной плотности за счет неподеленной пары электронов атома серы и делокализованных электронов ароматических колец. Образование КПЗ, содержащего химически связанное целевое анализируемое вещество, повышает селективность анализа. Также смещение полосы поглощения КПЗ в видимую область (400-800 нм), близкую по энергии как к энергии возбуждающего лазера, так и к полосе плазмонного резонанса наночастиц серебра, приводит к резкому (в 103 и более раз) увеличению чувствительности анализа за счет резонансных эффектов, что позволяет определять целевые вещества при низких концентрациях.
Для детектирования анализируемых веществ с концентрациями 10-6-10-3 М предпочтительно использовать жидкие пробы объемом 10-50 мкл путем их накалывания на поверхность сенсора для более эффективного предконцентрирования целевого аналита на рабочей поверхности оптического сенсора.
Для обеспечения высокой эксперессности анализа при высоком отношении сигнал / шум и отсутствии появления ложной спектральной информации, мощность лазерного излучения не должна превышать 10% от номинальной величины при продолжительности набора спектров аналитов в составе КПЗ не более 10 секунд. При этом для проведения анализа используют лазерное излучение с длиной волны 514, или 532, или 633, или 785 нм, или 1064 нм.
Для проведения анализа помимо стационарных КР-спектрометров возможно использование портативных приборов с вышеперечисленными длинами волн для регистрации спектров ГКР. Таким образом, предлагаемое техническое решение эффективно для использования в целях мобильного высокочувствительного и высокоточного входного контроля и идентификации полиароматических гетероциклических серосодержащих компонентов нефтепродуктов, ускоренного контроля образцов в процессе нефтепереработки, для окончательного контроля и установления качества нефтепродуктов как в лабораторных, так и в «полевых» условиях.
Анализ общеизвестных источников информации показал, что получение нанокомпозита наночастицы серебро-углерод и создание химически модифицированного планарного оптического сенсора на его основе путем нанесения хемотропного геля с функцией предконцентрирования и/или пространственного разделения смеси аналитов, дополнительно химически модифицированную π-акцепторным соединением, способным распознавать анализируемое вещество и химически связываться с ним путем формирования комплекса с переносом заряда на гибкую, пористую, длинномерную подложку на основе целлюлозы или других гибких и пористых материалов, не известно. Таким образом, заявляемая структура сенсора, сообщает всей группе изобретений соответствие как критерию «новизна», так и критерию «изобретательский уровень».
В настоящем изобретении приняты следующие обозначения и термины:
ГКР - гигантское комбинационное рассеяние,
композиция, обладающая ГКР-активностью - состав, наносимый на инертную основу для проведения анализа пробы на ее поверхности путем регистрации спектра ГКР - спектра комбинационного рассеяния с сигналами, усиленными по интенсивности в 103-106 раз,
композиционные частицы - представляют собой гибридные частицы, состоящие из частиц оксида графена чешуйчатой формы с расположенными на поверхности наночастицами серебра,
ПАГС - полиароматические гетероциклические серосодержащие соединения,
ПЭМ - просвечивающая электронная микроскопия,
УЗ-излучение - ультразвуковое излучение,
КПЗ - комплексы с переносом заряда,
БХ - 1,4-бензохинон,
ХЛК - 2,5-дихлор-3,6-диокси-1,4-бензохинон или хлораниловая кислота,
ДДХ - 2,3-дихлор-5,6-дициано-1,4-бензохинон,
ТЦХМ - 7,7,8,8-тетрацианохинондиметан,
ТЦНЭ - тетрацианоэтилен,
АД - 9,10-антрацендион,
ТНФ -2,4,5,7-тетранитро-9-флуоренон,
ДНФ - 2,7-динитро-9-флуоренон.
Химические символы/ сокращения имеют свои обычные значения: °С (градус (градусы) Цельсия), сП (сантипауз (сантипаузы)), мбар (миллибар (миллибары)), об/мин (обороты в минуту), нм (нанометр (нанометры)), мкм (микрометр (микрометры)), см (сантиметр (сантиметр)), мкл (микролитр (микролитры)), мкг (микрограмм (микрограммы)), М (моль (моли) в литре), л (литр (литры)), мл (миллилитр (миллилитры)), мкл (микролитр (микролитры)), г(грамм (граммы)), мг (миллиграмм (миллиграммы)), моль (моли), ммоль (миллимоль (миллимоли)), мас.% (массовый процент (массовые проценты)).
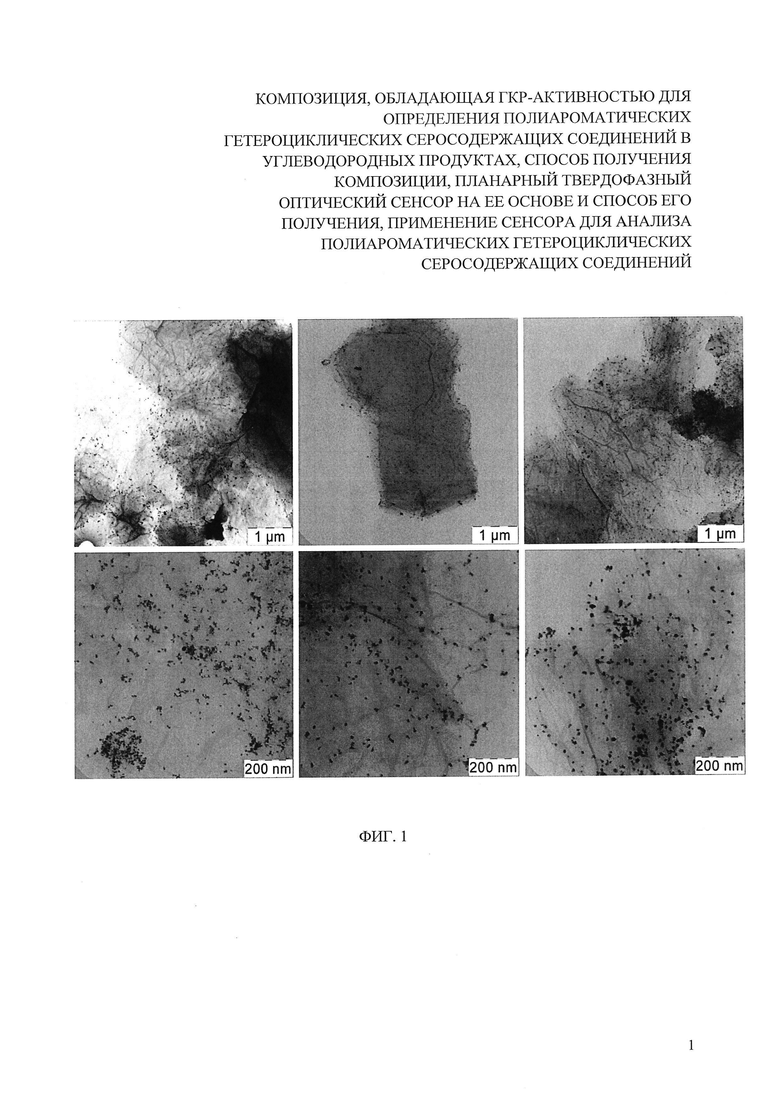
На фиг. 1 представлены микрофотографии ПЭМ образцов нанокомпозита оксид графена - серебро до доращивания наночастиц серебра. Концентрационное соотношение оксид графена: серебро: а) 1:1, б) 1:1.5, в) 1:2, соответственно.
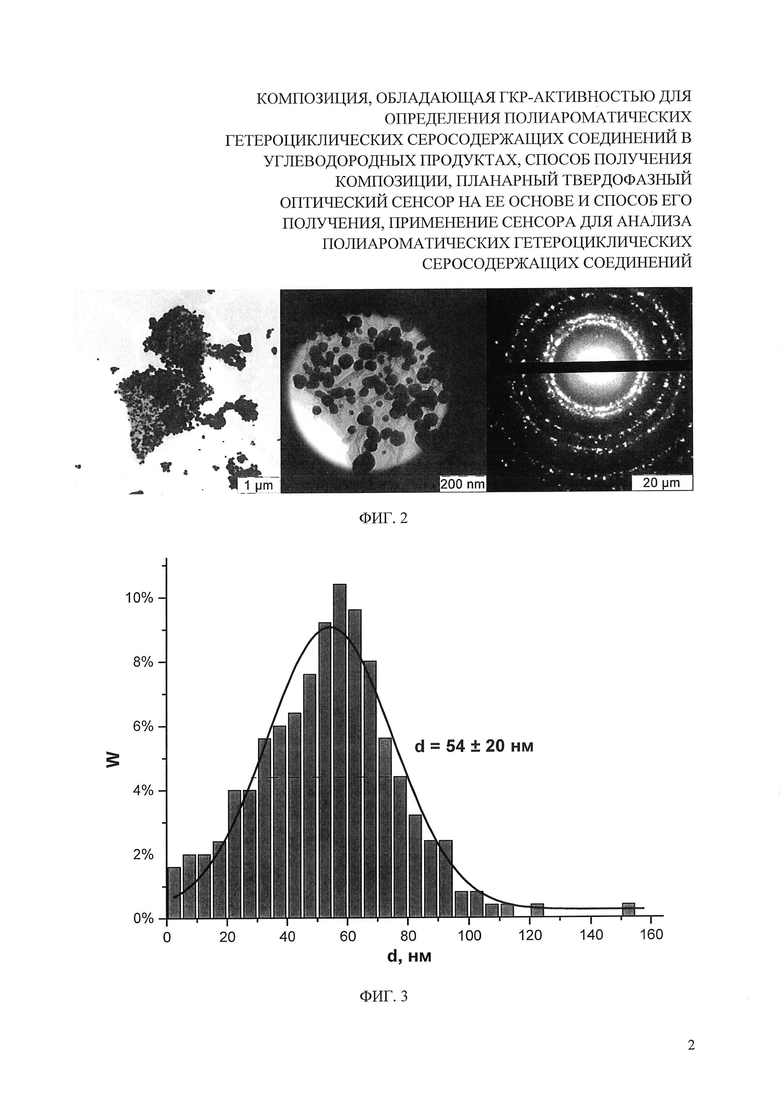
На фиг. 2 представлены микрофотографии ПЭМ образцов нанокомпозита серебро-углерод после процедуры доращивания. Концентрационное соотношение оксид графена: серебро на исходном композите 1:2 и картина электронной дифракции нанокомпозита.
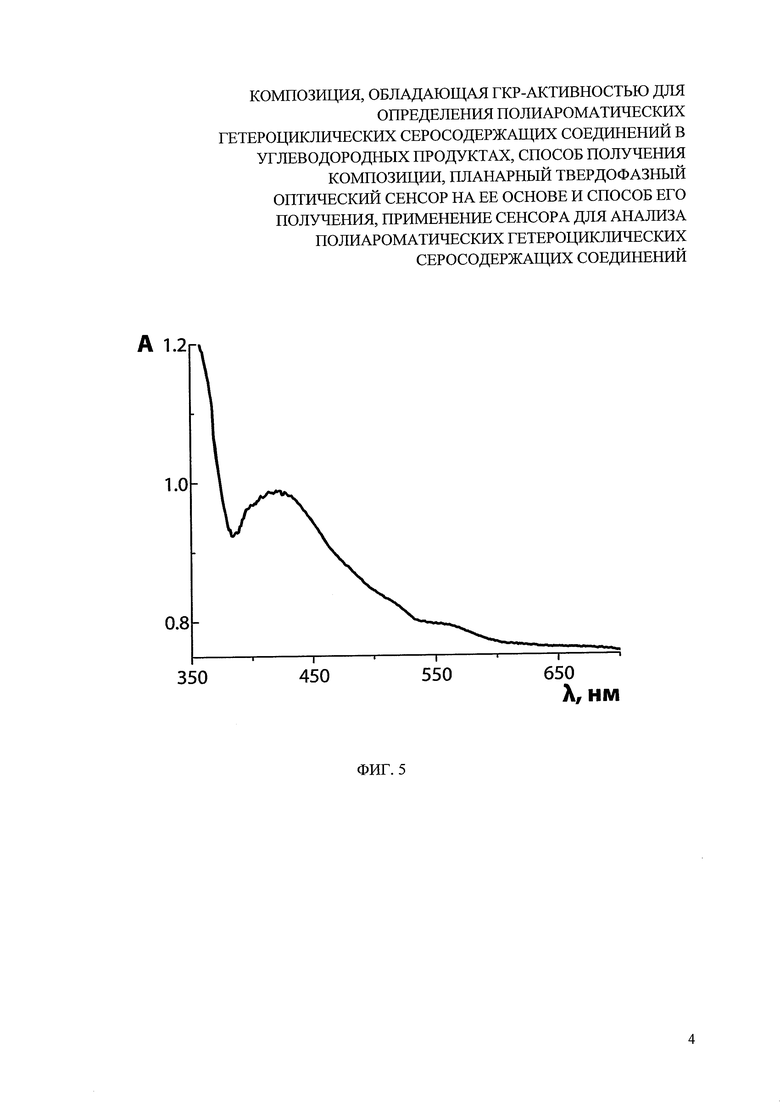
На фиг. 3 представлено распределение размера наночастиц серебра в составе нанокомпозита серебро-углерод после процедуры доращивания.
На фиг.4 представлены иллюстрации процесса получения ГКР - активных слоев, содержащих нанокомпозит оксид графена и серебра в хемотропных гелях с альгинатом натрия. Позициями на фигурах обозначены: 1 - электронно-микроскопическая фотография нанокомпозита, образец после литья в ячейки на отражающей алюминиевой основе, а также ячейки после формирования слоя геля (оптическая фотография), 2 - пористая структура геля после лиофильной сушки, 3 - планшет из 16 ячеек в чашке Петри диаметром 10 см, 4 - пористая целлюлозная основа после пропитки хемотропным гелем и высушивания.
На фиг. 5 представлены спектры диффузного отражения полученной на основе высушенного хемотропного геля пористой пленки.
На фиг. 6 представлена оптическая фотография основы: гель, нанесенный и высушенный на поверхности стекла, увеличение 20 х.
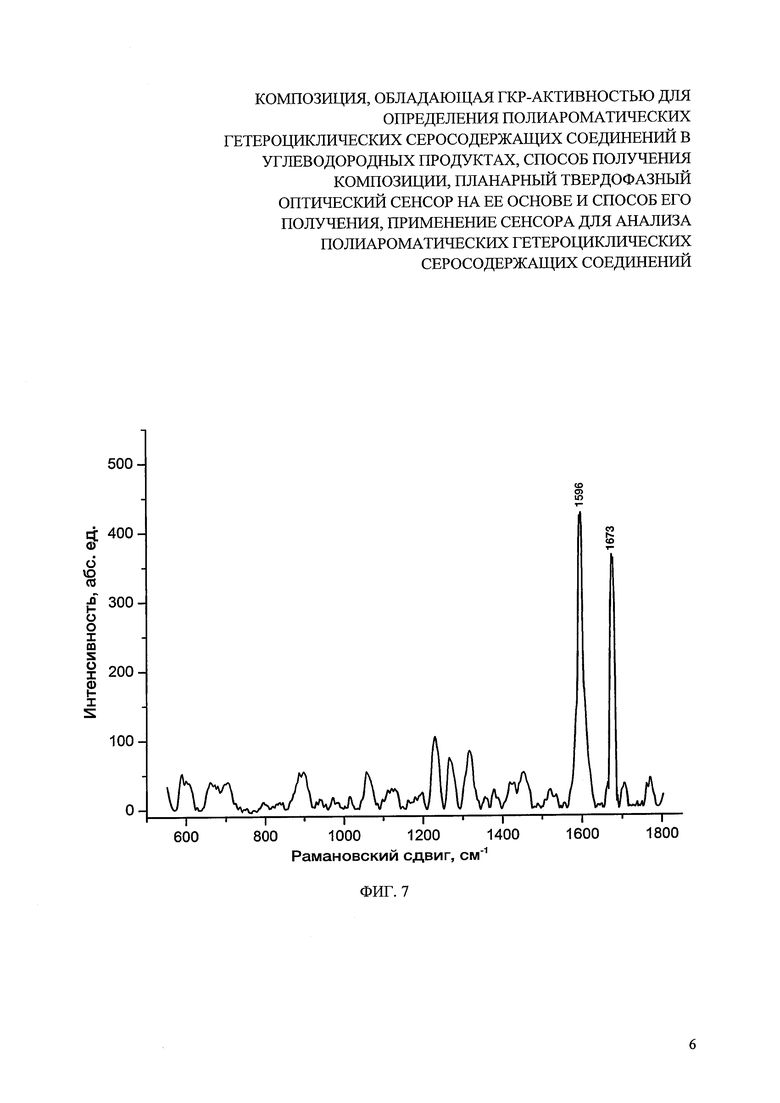
На фиг. 7 представлен спектр ГКР на поверхности сенсора (гель, нанесенный и высушенный на поверхности стекла). Аналит - комплекс с переносом заряда ДДХ (10 мкл, 5×10-3 М) - ДБТ (10 мкл, 1×10-4 М). Длина волны лазера 632.8 нм.
На фиг. 8 представлена оптическая фотография сенсора (гель, нанесенный и высушенный на поверхности хроматографической бумаги), увеличение 20×.
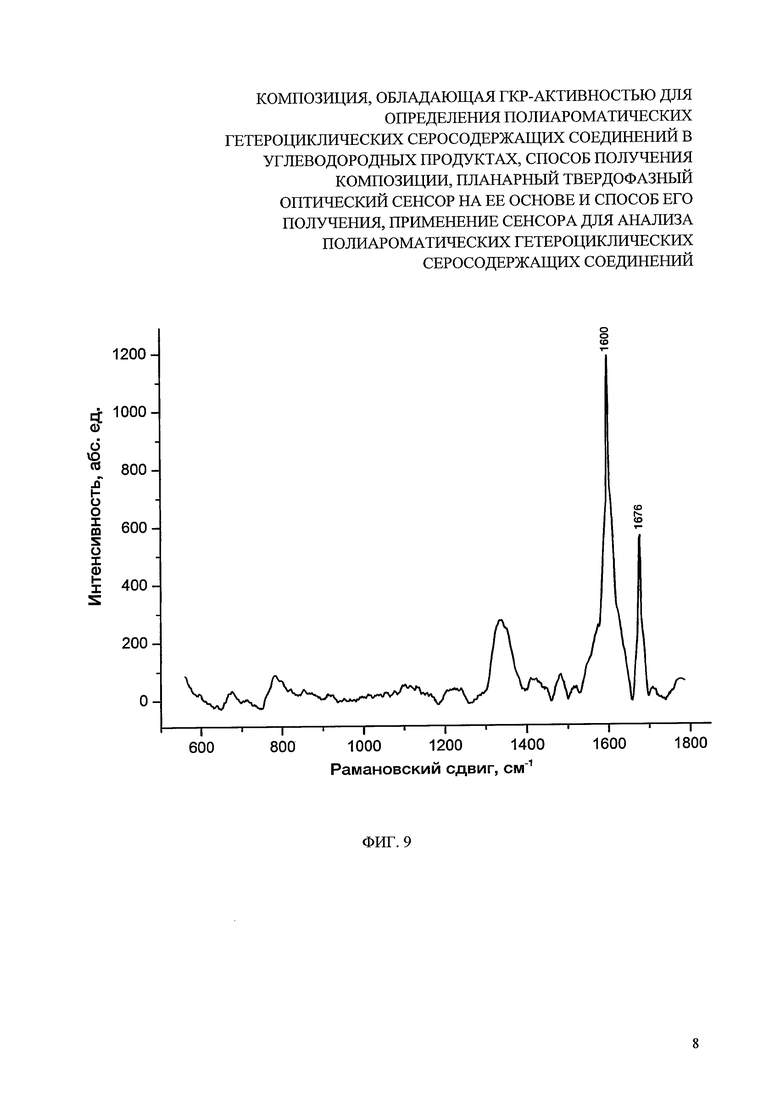
На фиг. 9 представлен спектр ГКР сенсора (гель, нанесенный и высушенный на поверхности хроматографической бумаги). Аналит - комплекс с переносом заряда ДДХ (10 мкл, 5×10-3 М) - ДБТ (10 мкл, 1×10-4 М). Длина волны лазера 632.8 нм.
На фиг. 10 представлена оптическая фотография сенсора (гель, нанесенный и высушенный на поверхности хроматографической бумаги), увеличение 20×.
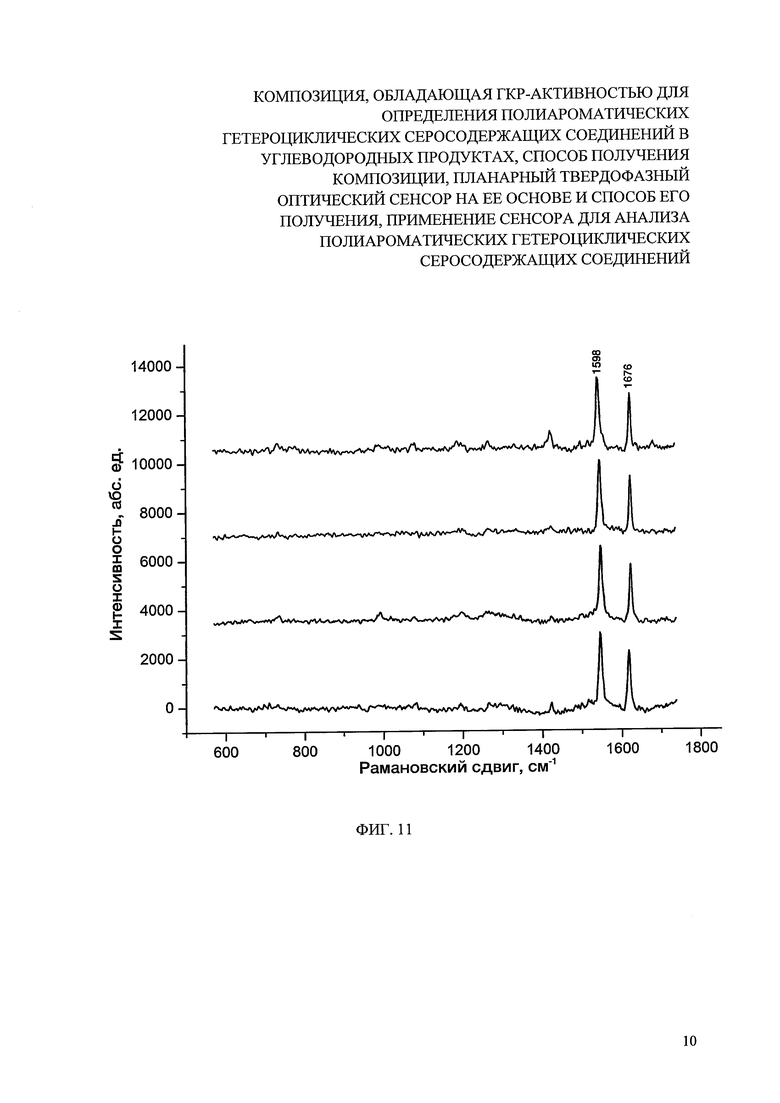
На фиг. 11 представлены спектры ГКР, зарегистрированных в различных точках на поверхности сенсора (гель, нанесенный и высушенный на поверхности хроматографической бумаги). Аналит - комплекс с переносом заряда ДДХ (10 мкл, 5×10-2 М)-ДБТ (10 мкл, 1×10-4 М).
На фиг. 12 представлена оптическая фотография сенсора (гель на основе гидроксиэтилцеллюлозы, нанесенный и высушенный на поверхности хроматографической бумаги), увеличение 20×.
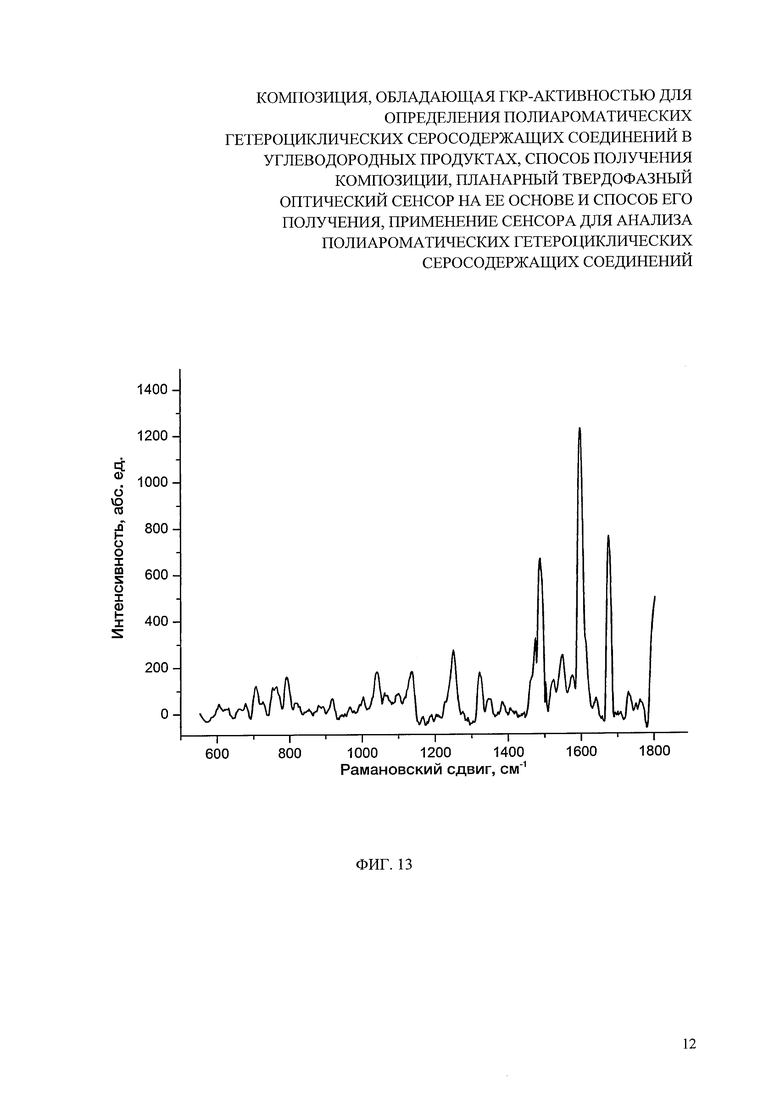
На фиг. 13 представлены спектры ГКР, зарегистрированных в различных точках на поверхности сенсора (гель, нанесенный и высушенный на поверхности хроматографической бумаги).
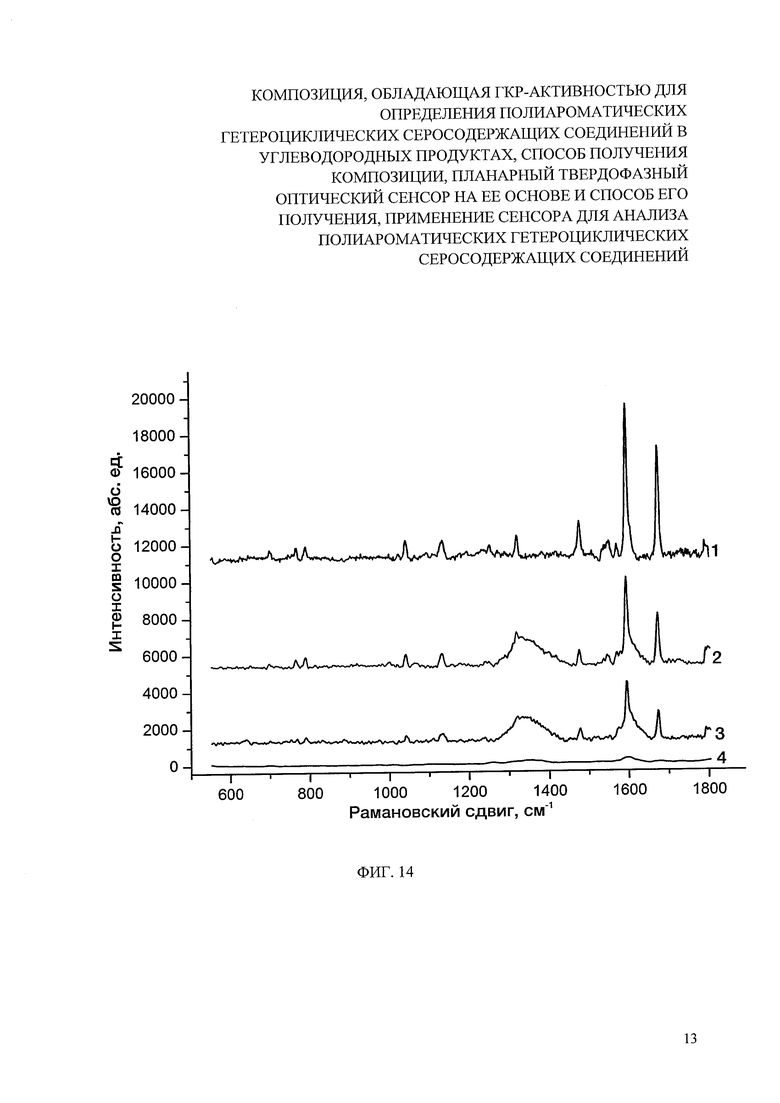
На фиг. 14 представлены спектры ГКР на сенсоре (гель, нанесенный и высушенный на поверхности хроматографической бумаги), от комплекса с переносом заряда ДДХ (10 мкл, 5×10-3 М). Длина волны лазера 632.8 нм. Позициями на фигурах обозначены: 1 - ДБТ (10 мкл, 5×10-3 М), 2 - ДБТ (10 мкл, 1×10-3 M), 3 - ДБТ (10 мкл, 5×10-4 М), 4 - ДБТ (10 мкл, 5×10-3 М).
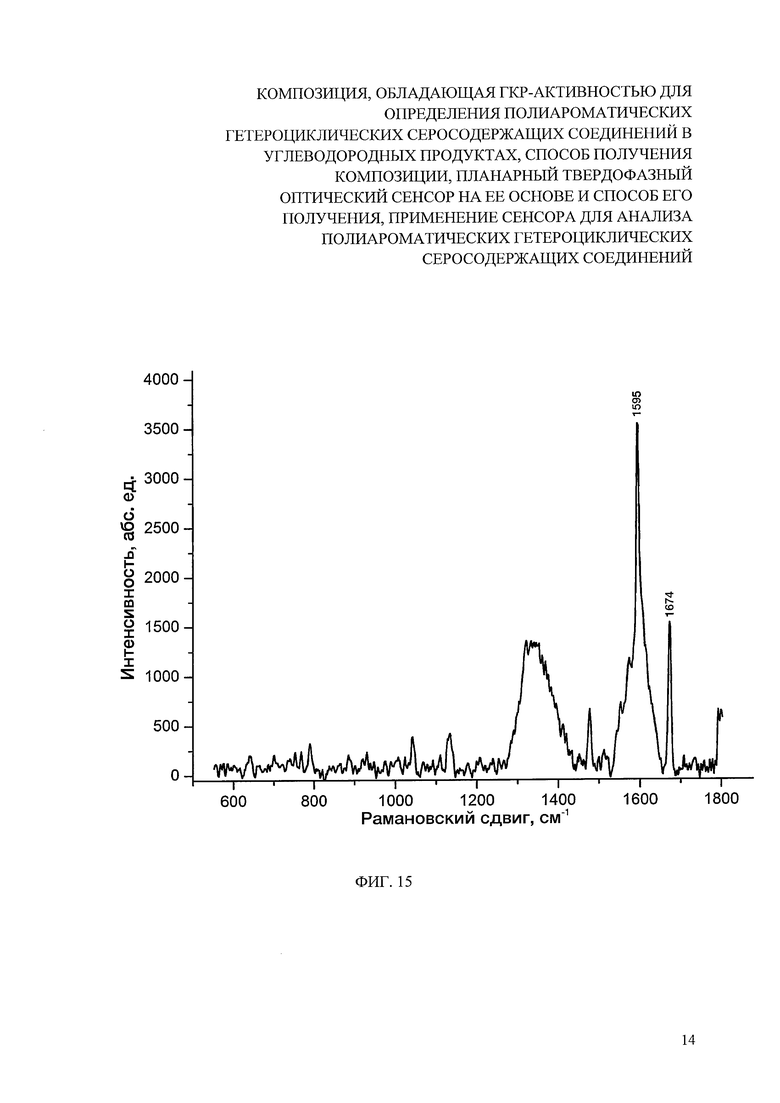
На фиг. 15 представлен спектр ГКР на сенсоре (гель, нанесенный и высушенный на поверхности хроматографической бумаги). Аналит - комплекс с переносом заряда ДДХ (10 мкл, 5×10-3 М) - ДБТ (10 мкл, 5×10-5 М). Длина волны лазера 632.8 нм.
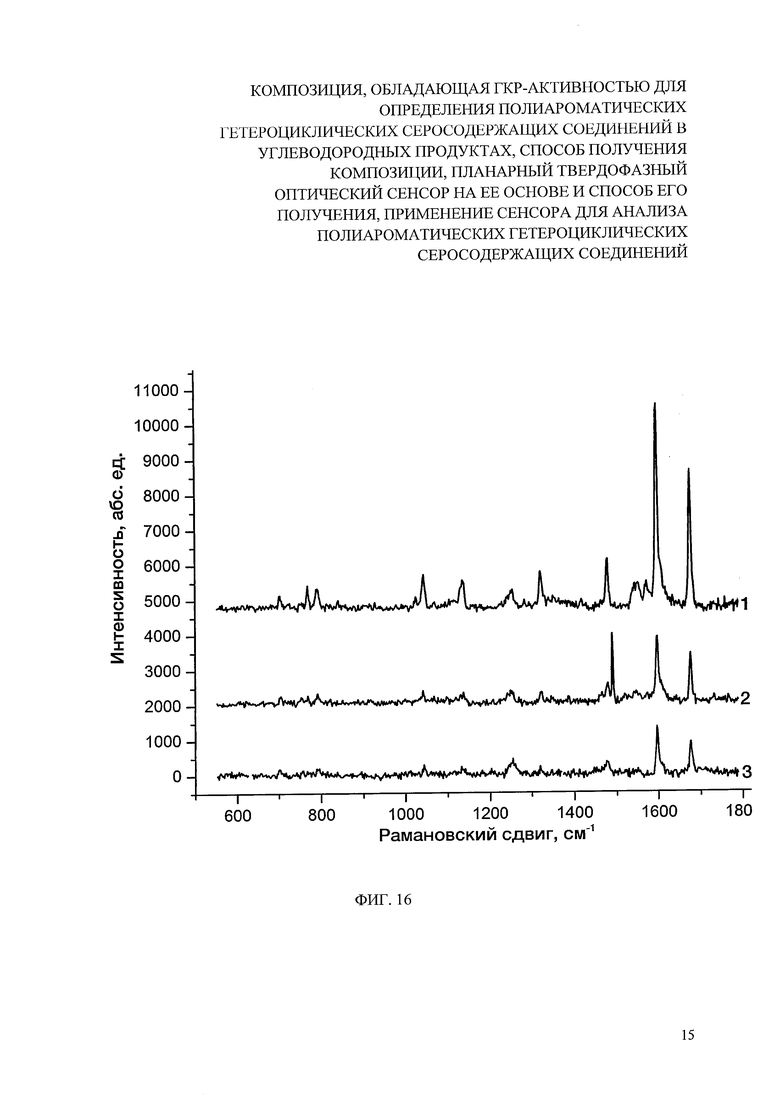
На фиг. 16 представлены спектры ГКР на поверхности сенсора (гомогенизированный гель, нанесенный и высушенный на поверхности хроматографической бумаги), комплекса с переносом заряда ДДХ (10 мкл, 5×10-3 М). Длина волны лазера 632.8 нм.
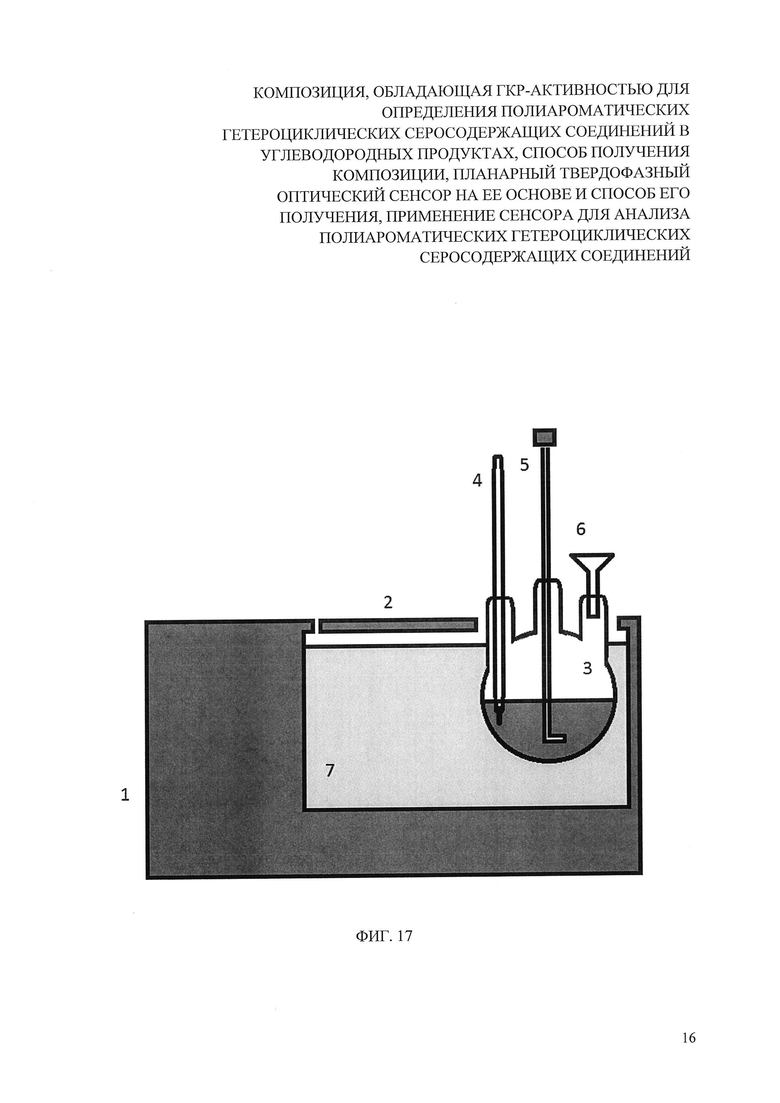
На фиг. 17 представлена схема установки для синтеза оксида графена по модифицированному методу Хаммерса. Позициями на фигурах обозначены: 1 - программируемый термостат; 2 - крышка термостата; 3 - трехгорлая колба, 4 - термометр; 5 - механическая мешалка; 6 - стеклянная воронка, 7 - емкость с антифризом.
Представленные ниже примеры конкретного осуществления изобретения приведены для предоставления специалистам в данной области техники полного описания проведения и применения анализа по изобретению, но не ограничивают предполагаемый авторами изобретения объем изобретения.
Все приведенные ниже реагенты являются коммерчески доступными. Все процедуры, если не оговорено особо, осуществляли при комнатной температуре или температуре окружающей среды, то есть в диапазоне от 18 до 25°С; в ходе всех экспериментов для приготовления водных растворов и промывки суспензий использовали деионизированную воду высокой чистоты, очищенную с использованием установки «Milli-Q», «Millipore»; использовали хроматографическую бумагу «Whatman» с толщинами от 0.18 до 0.52 мм; криохимическое высушивание образцов проводили в лиофильной сушке (вакуумном сублиматоре) «FreeZone 1», «Labconco»; спектры ГКР зарегистрированы на КР-спектрометр «Renishaw in Via Reflex» с фокусным расстоянием 250 мм, размером пятна лазера 1-300 мкм, при этом все спектры ГКР сняты с использованием 20×-ного объектива и с временем экстинкции 10 с, юстировку прибора проводили с использованием монокристаллических пластин кремния в качестве стандарта; оптические фотографии снимались на конфокальном микроскопе «Leica DMLM» с разрешением до 2.5 мкм; изображения ПЭМ снимались на просвечивающем электронном микроскопе «JEM-1011», «JEOL» с цифровой камерой бокового расположения «Gatan Erlangshen ES500W»; спектры диффузного рассеяния света от полученных образцов исследовали с помощью спектрографа «LS-55 Perkin Elmer» в спектральном диапазоне 200-900 нм со спектральной шириной щелей от 2.5 до 20 нм; разделение неоднородных систем проводилось с помощью центрифуги «Centrifuge 5804», «Eppendorf»; для фильтрования использовали насосный фильтр «MillexLCR» («Millipore», с порами 450 мкм); взвешивание препаратов проводили с точностью ±0.02 мг на аналитических весах «Discovery», «OHAUS»; точные объемы жидкостей отбирали с использованием автоматических дозаторов «Eppendorf» с диапазонами объемов: 2-20, 10-100, 20-200, 100-1000 и 500-5000 мкл; гомогенизацию неоднородных систем ультразвуковым облучением проводили в УЗ-ванне «Elmasonic Р», «Elma», механическую гомогенизацию неоднородных систем проводили с использованием или мини-ротатора «Bio RS-24», «BioSan», или планетарной мельницы «PULVERISETTE», «FRITSCH», или магнитной мешалки «RCT basic», «IKA» с возможностью подогрева.
Пример 1. Способ получения химически модифицированного планарного оптического сенсора для анализа производных дибензотиофена.
На первой стадии синтезировали нанокомпозит серебро-углерод следующим образом: 30 мл 0.1 М водного раствора гидроксида натрия («Aldrich», NaOH) добавили по каплям в 30 мл свежеприготовленного 0.02 М водного раствора нитрата серебра («Sigma Aldrich», AgNO3) до полного осаждения коричневого осадка - оксида серебра (I). Полученный осадок трижды тщательно промыли водой. Далее надосадочный раствор отделили декантацией, к полученному осадку добавили 30 мл воды, механически гомогенизировали посредством многократных интенсивных встряхиваний, дали осесть. Раствор над осадком слили и полученный осадок растворили в 3 мл 10% водного раствора аммиака (полученного из 30% водного раствора гидроксида аммония, «Aldrich»). Затем прозрачный раствор аммиачного комплекса серебра фильтровали через сменный мембранный фильтр «Millex-LCR» («Millipore», размер пор 450 нм). Далее 1.763 мл суспензии оксида графена разбавили водой до 20 мл и внесли в полученный раствор аммиачного комплекса серебра. Полученную смесь нагревали до кипения на плитке с магнитной мешалкой и кипятили при интенсивном перемешивании в течение 30 мин. После этого раствор охладили до комнатной температуры (22-23°С), центрифугировали при 8000 об/мин в течение 10 мин. Нанокомпозит серебро-углерод пятикратно отмывали водой порциями по 30 мл. Полученные структуры имеют вид, представленный на фотографиях ПЭМ (фиг.1 ), свидетельствующих о равномерности распределения наночастиц серебра по поверхности оксида графена. Наночастицы серебра, полученных описанным способом, характеризуются узким распределением частиц по размеру (табл. 1).
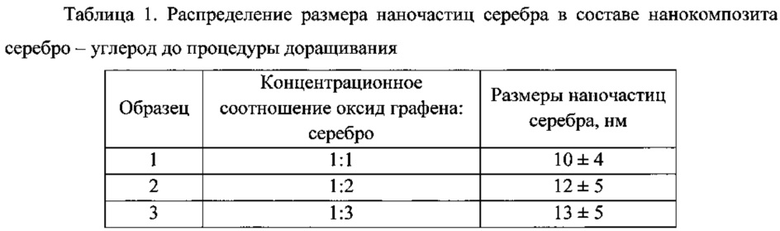
На второй стадии проводили доращивание наночастиц серебра. Для этого к 30 мл полученной на первой стадии суспензии при перемешивании добавили 30 мл свежеприготовленного 0.001 М раствора нитрата серебра. Полученную смесь выдерживали в течение 20 минут. Затем к полученному раствору добавили 30 мл свежеприготовленного 0.001 М водного раствора аскорбиновой кислоты, смесь выдерживали при комнатной температуре (22-23°С) и перемешивании при помощи магнитной мешалки в течение 1 часа. После этого раствор центрифугировали при 8000 об/мин в течение 10 мин. Полученный осадок пятикратно отмывали водой порциями по 20 мл. Полученная композиция представляет собой частицы оксида графена в виде пластинок (размерами 1-2 мкм) с равномерно размещенными на их поверхности наночастицами серебра (фиг. 2). Равномерность распределения наночастиц серебра на поверхности частиц оксида графена в среднем составляет 25 наночастиц серебра и варьируется в интервале 10-40 наночастиц серебра на 0.1 мкм2 площади поверхности частицы оксида графена. При этом не менее 90% наночастиц серебра и частиц оксида графена присутствуют в суспензии в виде композиционных частиц. Таким образом был получен нанокомпозит с наночастицами серебра размером (54±20) нм. Распределение размера наночастиц серебра в составе нанокомпозита серебро-углерод после процедуры доращивания представлен на фиг. 3.
На третьей стадии в 30 мл суспензии, полученной на второй стадии, внесли 1.5 г твердого порошка альгината натрия («Sigma-Aldrich»), выдерживали при комнатной температуре (22-23°С) и постоянном перемешивании на средней мощности магнитной мешалки до его полного растворения, затем гомогенизировали в планетарной мельнице в течение 20 мин. Получили гель из которого удалили водную фазу путем лиофильной (вакуум-сублимационной) сушки при температуре -30°С и давлении 1.000 мбар. На этой стадии получили нанокомпозит в виде объемного материала - пористой пленки, оптическая фотография которой представлена на фиг. 4, с площадью поверхности 350 м2/г, полосой плазмонного резонанса в видимой области спектра 400-450 нм (фиг. 5) и динамической вязкостью 0.7 сП.
На четвертой стадии 5 мл полученного гомогенизированного геля наносили автоматизированным дозирующим устройством на предметное стекло площадью 5×5 см2, выступающее в роли подложки-субстрата. Полученную подложку с нанесенным на нее гелем криохимически высушили в лиофильной сушке (вакуумном сублиматоре) при температуре - 30°С и давлении 1.000 мбар в течение 3 ч (фиг. 6). Ключевые параметры и общая схема синтеза геля с использованием в качестве полимерного гелеобразователя раствора альгината натрия представлены в табл. 2.
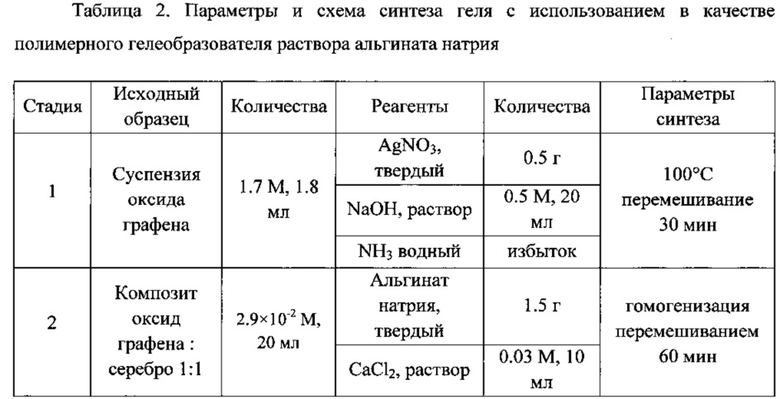
На пятой стадии полученную сенсорную поверхность 5×5 см2 нарезали канцелярским ножом на небольшие пластинки 4×4 мм2. Затем на полученную сенсорную пластинку в целях модификации поверхности π-акцепторным соединением на нее нанесли 10 мкл раствора 5×10-3 М ДДХ в хлороформе.
На поверхность полученного сенсора нанесли жидкую пробу объемом 10 мкл путем накалывания для более эффективного предконцентрирования целевого аналита на рабочей поверхности оптического сенсора.
Анализ жидких проб, нанесенных на сенсор, проводили с использованием КР-спектрометра «Renishaw in Via Reflex» в конфокальном режиме на красном лазере (Не/Ne, длина волны - 632.8 нм, 20 мВт) при мощности фильтра нейтральной плотности 10% и времени накопления сигнала - 10 с.
Полученный планарный оптический сенсор обладает повышенной пористостью (удельная площадь поверхности ок. 350 м2/г) и при его использовании в спектроскопии ГКР предел обнаружения ДБТ составил 5×10-7 М (фиг. 7). Селективность определения ПАГС достигалась за счет регистрации спектров ГКР в «области молекулярных отпечатков пальцев» и соотнесению получаемых частот колебаний комбинационного рассеяния на примере ДБТ: 1596±3 см-1 и 1671±3 см-1.
Пример 2. Проведен аналогично примеру 1, но на четвертой стадии 2 мл геля нанесли на хроматографическую бумагу «Whatman» с толщиной 0.18 мм («Grade 2Chr») и площадью 2×5 см2, затем высушили в лиофилизаторе (вакуумном сублиматоре) при температуре - 30°С и давлении 1.000 мбар. Полученный таким образом планарный оптический сенсор, оптическая фотография которого представлена на фиг. 8, использовали для определения ДБТ в изооктане. С использованием полученного таким образом планарного оптического сенсора достигались высокие коэффициенты усиления в спектрах ГКР (фиг. 9).
Пример 3. Проведен аналогично примеру 2, но на четвертой стадии подложку с нанесенным гелем высушили на воздухе при комнатной температуре (фиг. 10). Полученные спектральные данные свидетельствуют о том, что использование лиофильной сушки не является необходимой процедурой и достаточно получение ксерогелей путем высушивания при комнатной температуре на воздухе. При этом наличие пиков D- и G-мод графена не мешает определению аналита, более того, эти пики могут в дальнейшем использоваться как внутренний эталон для получения количественных данных о концентрации аналита. На фиг. 11 представлены спектры ГКР, зарегистрированные в различных точках поверхности: в центре и на границах полученного планарного оптического сенсора, демонстрирующие воспроизводимое усиление аналитического сигнала от точки к точке. Данный эффект достигается за счет равномерности распределения аналита по поверхности сенсора.
Пример 4. Проведен аналогично примеру 1 (табл. 3), но в качестве полимерного связующего использовали 0.3% раствора гидроксиэтилцеллюлозы с последующим нанесением 2 мл полученного геля на хроматографическую бумагу «Whatman» с толщиной 0.18 мм («Grade 2Chr») и площадью 2×5 см2, высушиванием при комнатной температуре (22-23°С).
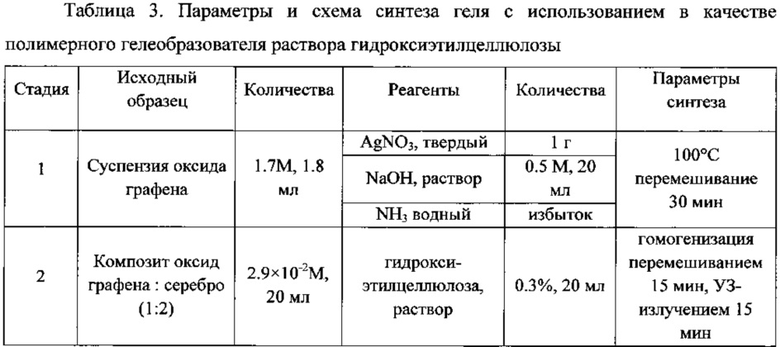
Полученный планарный оптический сенсор очевидно достаточно негомогенное распределение активных центров по поверхности подложки (фиг. 12), что технически связано с агломерацией нанокомпозита в растворе гидроксиэтилцеллюлозы по сравнению со случаем использования альгината натрия, способствующего формированию хемотропного геля и, в конечном итоге, более равномерному распределению компонентов. Однако спектры ГКР, зарегистрированные на полученном планарном сенсоре, также демонстрируют хорошую чувствительность определения ПАГС с меньшей воспроизводимостью по поверхности (фиг. 13).
Пример 5. Проведен аналогично примеру 1, ключевые параметры и схема синтеза геля, представлены в табл.4.
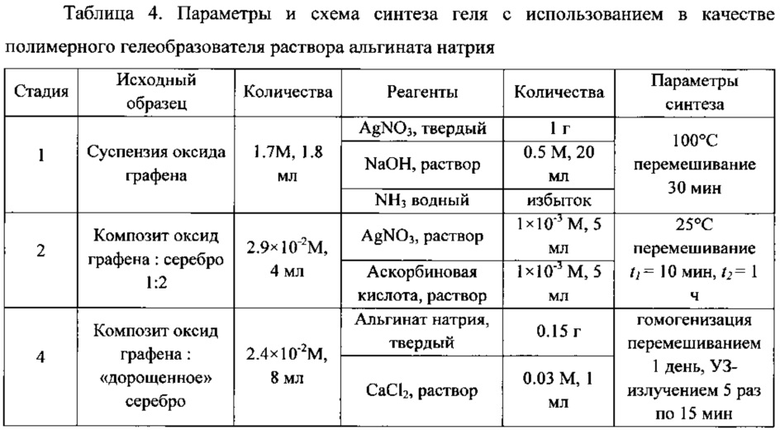
Планарный сенсор получали нанесением 2 мл геля на хроматографическую бумагу «Whatman» с толщиной 0.52 мм и площадью 2×5 см2 и последующем высушиванием при комнатной температуре (22-23°С) на воздухе. Полученный образец демонстрирует большую чувствительность по отношению к компонентам нефтепродуктов. Данный оптический сенсор позволял детектировать ПАГС на уровне 10-5 М (фиг. 14). Полученные спектры ГКР свидетельствуют о том, что искусственное увеличение степени покрытия поверхности оксида графена наночастицами серебра при введении дополнительной стадии доращивания исходно осажденных центров кристаллизации приводило к существенному, в 5-10 раз, увеличению коэффициента усиления сигнала и большей воспроизводимости полученных результатов.
Пример 6. Проведен аналогично примеру 5, планарный сенсор получали нанесением 5 мл геля на универсальную алюминиевую фольгу толщиной 11 мкм площадью 5×5 см2 и последующим высушиванием при комнатной температуре (22-23°С) на воздухе. Данный оптический сенсор позволял детектировать ПАГС на уровне 10-5 М (фиг. 15).
Пример 7. Проведен аналогично примеру 1, ключевые параметры и схема синтеза представлены в табл.5.
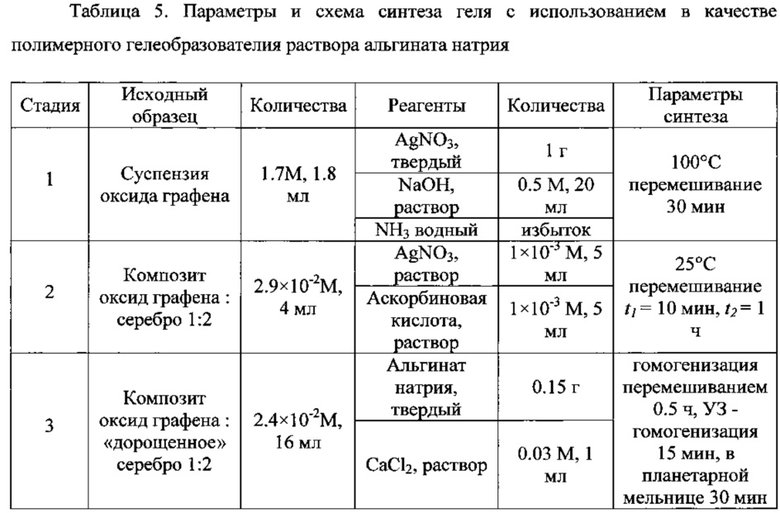
Полученный гель, дополнительно гомогенизированный в планетарной мельнице при частоте 550 об/мин, нанесли на хроматографическую бумагу «Whatman» с толщиной 0.18 мм («Grade 2Chr») и площадью 2×5 см2. Носитель с нанесенным гелем высушили при комнатной температуре (22-23°С) на воздухе. Полученный оптический сенсор позволил регистрировать спектры ГКР в диапазоне концентраций ДБТ: 5×10-3-5×10-5 М с пределом обнаружения ДБТ 6×10-7 М (фиг. 16).
Пример 8. Проведен аналогично примеру 1 с варьированием концентрации раствора нитрата серебра на первой стадии получения хемотропного геля, количеств оксида графена, добавляемого для доращивания наночастиц серебра нитрата серебра и восстанавливающего агента в расчете на 10 мл раствора или суспензии, полученной на предыдущей стадии (табл. 6).
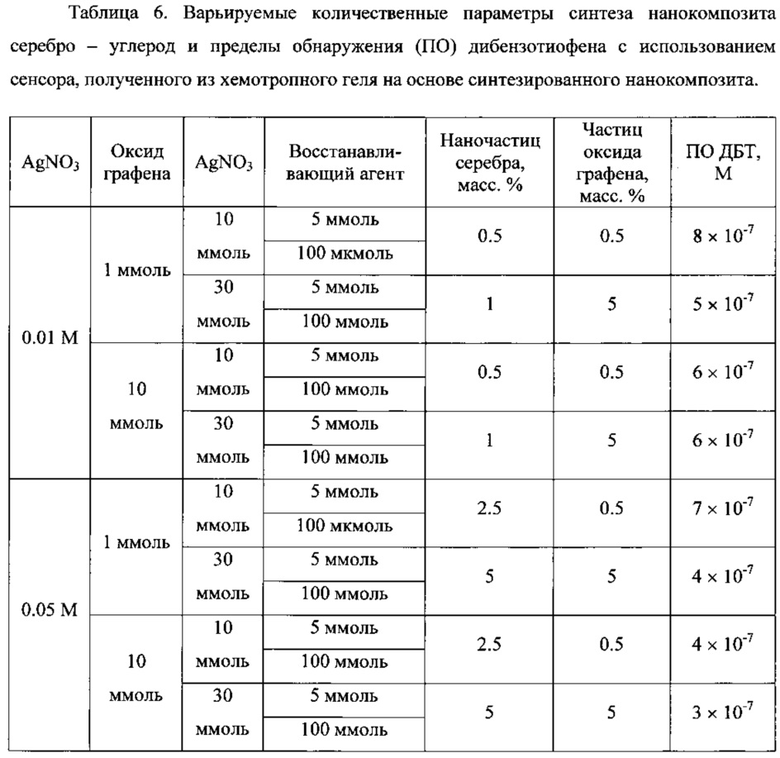
Количественное варьирование состава нанокомпозита серебро-углерод (табл. 6) позволяет качественно и количественно определять ДБТ с пределами обнаружения 3×10-7-8×10-7 М.
Пример 9. Проведен аналогично примеру 1 с варьированием природы используемого полимера, массы порошка полимера в расчете на 10 мл суспензии нанокомпозита серебро-углерод, субстрата для получения оптического планарного сенсора, толщины слоя наносимого хемотропного геля (табл. 7).
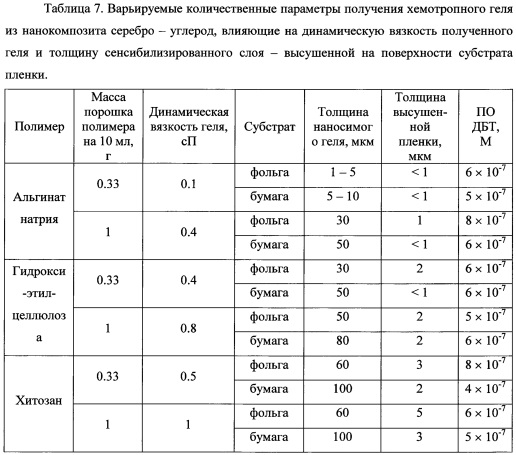
Изменение содержания полимера в полученном хемотропном геле от 0.33 до 1 г на 10 мл суспензии нанокомпозита серебро-углерод позволяет качественно и количественно определять ДБТ с пределами обнаружения 4×10-7-8×10-7 М.
Стандартная методика синтеза оксида графена (модифицированный метод Хамерса).
В трехгорлую колбу, оснащенную термометром и механической мешалкой, помещают 3 г графита, 1.5 г NaNO3 и 69 мл концентрированной серной кислоты H2SO4. Затем колбу погружают в термостат при t≈4°С (фиг. 7). При интенсивном перемешивании в течение нескольких часов добавляют 9 г KMnO4, контролируя температуру реакционной смеси, которая не должна подниматься выше 20°С. Затем реакционную смесь нагревают до 35°С и в течение 30 мин медленно смешивают с 140 мл воды, не допуская нагрева смеси выше 70°С. Горячую суспензию выдерживают при этой температуре еще 15 мин, затем разбавляют до 480 мл дистиллированной водой. Далее колбу вынимают из термостата. Избыток KMnO4 и MnO2 восстанавливают 200 мл Н2О2 (3%). Полученную суспензию желто-коричневого цвета оставляют на 8-12 часов. Затем разделяют на пробирки по 50 мл, центрифугируют (6000 об/мин) в течение 5 мин, промывают дистиллированной водой. Описанную процедуру разделения повторяют 3-5 раз. Полученную суспензию оксида графена коричневого цвета хранят в закрытой посуде без доступа воздуха и света.
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМИЧЕСКИ МОДИФИЦИРОВАННЫЙ ПЛАНАРНЫЙ ОПТИЧЕСКИЙ СЕНСОР, СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И СПОСОБ АНАЛИЗА ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ С ЕГО ПОМОЩЬЮ | 2015 |
|
RU2572801C1 |
| ПЛАНАРНЫЙ ТВЕРДОФАЗНЫЙ ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ОПРЕДЕЛЕНИЯ БЕЛКОВЫХ СОЕДИНЕНИЙ МЕТОДОМ СПЕКТРОСКОПИИ ГИГАНТСКОГО КОМБИНАЦИОННОГО РАССЕЯНИЯ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ДЕТЕКТИРОВАНИЯ БЕЛКОВЫХ СОЕДИНЕНИЙ | 2016 |
|
RU2659987C2 |
| СПОСОБ ОБНАРУЖЕНИЯ И ОПРЕДЕЛЕНИЯ ДНК С ЗАДАННОЙ ПОСЛЕДОВАТЕЛЬНОСТЬЮ МЕТОДОМ СПЕКТРОСКОПИИ ГИГАНТСКОГО КОМБИНАЦИОННОГО РАССЕЯНИЯ | 2019 |
|
RU2723160C1 |
| ГАЗОАНАЛИТИЧЕСКИЙ МУЛЬТИСЕНСОРНЫЙ ЧИП НА ОСНОВЕ АМИНИРОВАННОГО ГРАФЕНА, МОДИФИЦИРОВАННОГО НАНОЧАСТИЦАМИ ГИДРОКСИДОВ И ОКСИДОВ НИКЕЛЯ, И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2023 |
|
RU2814613C1 |
| НАБОР ДЛЯ ДИАГНОСТИКИ РАКА МОЧЕВОГО ПУЗЫРЯ С ПОМОЩЬЮ МУТАЦИЙ С228Т И C250T В ПРОМОТОРЕ ГЕНА hTERT И СПОСОБ ЕЕ ОСУЩЕСТВЛЕНИЯ | 2020 |
|
RU2764807C1 |
| Планарный наноструктурированный сенсор на основе поверхностного плазмонного резонанса для усиления комбинационного рассеяния света тромбоцитов человека и способ его получения | 2022 |
|
RU2788479C1 |
| Оптический сенсор с плазмонной структурой для определения химических веществ низких концентраций и способ его получения | 2019 |
|
RU2720075C1 |
| СЕНСОР ДЛЯ ПОЛУЧЕНИЯ СПЕКТРОВ ГИГАНТСКОГО КОМБИНАЦИОННОГО РАССЕЯНИЯ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2012 |
|
RU2537301C2 |
| Нанокомпозитный магнитный материал на основе поли-3-амино-7-метиламино-2-метилфеназина и наночастиц FeO, закрепленных на одностенных углеродных нанотрубках, и способ его получения | 2016 |
|
RU2635254C2 |
| ГАЗОАНАЛИТИЧЕСКИЙ МУЛЬТИСЕНСОРНЫЙ ЧИП НА ОСНОВЕ ГРАФЕНА, МОДИФИЦИРОВАННОГО НАНОЧАСТИЦАМИ БЛАГОРОДНЫХ МЕТАЛЛОВ, И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2023 |
|
RU2814586C1 |





Настоящее изобретение относится к области технологий материалов и материаловедческих и аналитических исследований. Композиция, обладающая ГКР-активностью, для определения полиароматических гетероциклических серосодержащих соединений (ПАГС) в углеводородных продуктах представляет собой хемотропный гель, содержащий полимерную матрицу с наночастицами серебра анизотропной формы с размерами 10-90 нм и частицами оксида графена с размерами 1-2 мкм. Способ получения этой композиции включает синтез оксида серебра, растворение полученной суспензии в водном растворе аммиака, смешивание полученного раствора с оксидом графена, последовательное введение в полученную суспензию нитрата серебра и восстанавливающего агента для получения наночастиц серебра в суспензии размерами 10-90 нм и введение полимерного порошка для перевода суспензии в хемотропный гель. Планарный твердофазный оптический сенсор включает размещенную на основе пленку толщиной до 5 мкм, полученную из композиции, обладающей ГКР-активностью, и содержащую на поверхности π-акцепторное соединение. Способ анализа ПАГС включает нанесение на планарный твердофазный оптический сенсор жидкой пробы с исследуемым соединением. Технический результат заключается в создании планарных оптических сенсоров, позволяющих использовать метод спектроскопии гигантского комбинационного рассеяния (ГКР) с высоким коэффициентом чувствительности, высокой селективностью, широким диапазоном определяемых концентраций и высокими воспроизводимостью и прецизионностью. 5 н. и 19 з.п. ф-лы, 6 табл., 17 ил.
1. Композиция, обладающая ГКР-активностью для определения полиароматических гетероциклических серосодержащих соединений в углеводородных продуктах, представляющая собой хемотропный гель, характеризующийся параметрами динамической вязкости 0.1-1 сП, содержащий полимерную матрицу с наночастицами серебра анизотропной формы с размерами 10-90 нм и частицами оксида графена с размерами 1-2 мкм, при этом количество каждого компонента - наночастиц серебра и частиц оксида графена - в полимерной матрице составляет от 0.5 до 5 мас.%.
2. Композиция по п. 1, характеризующаяся тем, что не менее 90% наночастиц серебра и частиц оксида графена присутствуют в полимерной матрице в виде композиционных частиц, при этом на 0.1 мкм2 площади поверхности частицы оксида графена приходится от 10 до 40 наночастиц серебра.
3. Композиция по п. 1, характеризующаяся тем, что в качестве полимерной матрицы использованы вещества, устойчивые к воздействию неполярных растворителей.
4. Композиция по п. 3, характеризующаяся тем, что в качестве полимерных веществ, устойчивых к воздействию неполярных растворителей, использованы альгинат натрия, или хитозан, или гидроксиэтилцеллюлоза.
5. Композиция по п. 1, характеризующаяся тем, что она обладает полосой плазмонного резонанса 400-450 нм.
6. Композиция по п. 2, характеризующаяся тем, что композиционные частицы в геле распределены равномерно.
7. Композиция по п. 2, характеризующаяся тем, что наночастицы серебра равномерно распределены по поверхности частицы оксида графена.
8. Способ получения композиции, обладающей ГКР-активностью по п. 1, включающий синтез оксида серебра из 0.01-0.05 М раствора нитрата серебра, после чего полученную суспензию растворяют в водном растворе аммиака, взятого в двух-четырехкратном молярном избытке по отношению к нитрату серебра, полученный раствор, содержащий аммиачный комплекс серебра, смешивают с оксидом графена с размерами частиц 1-2 мкм, взятых в количестве 1-10 ммоль на 10 мл раствора, после чего в полученную суспензию последовательно вводят нитрат серебра и восстанавливающий агент для получения наночастиц серебра в суспензии размерами 10-90 нм, в которую затем вводят полимерный порошок для перевода суспензии в хемотропный гель.
9. Способ по п. 8, характеризующийся тем, что используют водный раствор аммиака с концентрацией 10-20 мас.%.
10. Способ по п. 8, характеризующийся тем, что частицы оксида графена получают по модифицированному методу Хаммерса.
11. Способ по п. 8, характеризующийся тем, что нитрата серебра для получения наночастиц размерами 10-90 нм вводят в количестве 10-30 ммоль в расчете на 10 мл полученной суспензии нанокомпозита серебро-углерод.
12. Способ по п. 8, характеризующийся тем, что в качестве восстанавливающего агента используют аскорбиновую кислоту, или боргидрид натрия, или гидроксиламинхлорид.
13. Способ по п. 8, характеризующийся тем, что восстанавливающего агента вводят в количестве 5-100 ммоль в расчете на 10 мл суспензии нанокомпозита серебро-углерод.
14. Способ по п. 8, характеризующийся тем, что в качестве полимерного порошка используют гидроксиэтилцеллюлозу, или хитозан, или альгинат натрия, в количестве из расчета 1 г порошка на 10-30 мл суспензии.
15. Планарный твердофазный оптический сенсор для определения полиароматических гетероциклических серосодержащих соединений в углеводородных продуктах, включающий размещенную на основе пленку толщиной до 5 мкм, полученную из композиции по п. 1 и содержащую на поверхности π-акцепторное соединение.
16. Сенсор по п. 15, характеризующийся тем, что в качестве основы использованы стекло или гибкие и пористые материалы, например хроматографическая бумага, фольга.
17. Способ получения планарного твердофазного оптического сенсора для определения полиароматических гетероциклических серосодержащих соединений в углеводородных продуктах, включающий нанесение на основу композиции по п. 1 толщиной от 1 до 100 мкм, с последующим высушиванием до образования пленки на поверхности основы, и модифицированием поверхности полученной пленки раствором π-акцепторного соединения концентрацией 0.1-10 ммоль/л, при этом раствор π-акцепторного соединения наносят на поверхность геля в количестве 0.2-1 мкл на 1 мм2.
18. Способ по п. 17, характеризующийся тем, что в качестве π-акцепторного соединения используют соединение из ряда: 1,4-бензохинон (БХ); 2,5-дихлор-3,6-диокси-1,4-бензохинон, или хлораниловая кислота (ХЛК); 2,3-дихлор-5,6-дициано-1,4-бензохинон (ДДХ); 7,7,8,8-тетрацианохинондиметан (ТЦХМ); тетрацианоэтилен (ТЦНЭ); 9,10-антрацендион (АД); 2,4,5,7-тетранитро-9-флуоренон (ТНФ); 2,7-динитро-9-флуоренон (ДНФ).
19. Способ по п. 18, характеризующийся тем, что раствор π-акцепторного соединения представляет собой раствор соединения в органических растворителях, выбранных из ряда: хлороформ, изопропанол, диэтиловый эфир.
20. Способ по п. 17, характеризующийся тем, что нанесение на основу хемотропного геля осуществляют методом пропитки или трафаретной печати.
21. Способ по п. 17, характеризующийся тем, что в качестве основы используют стекло или такие гибкие и пористые материалы, как хроматографическая бумага и фольга.
22. Способ анализа полиароматических гетероциклических серосодержащих соединений, включающий нанесение на планарный твердофазный оптический сенсор по п. 15 жидкой пробы с исследуемым соединением с образованием окрашенного межмолекулярного комплекса π-акцепторного соединения с полиароматическими гетероциклическими серосодержащими соединениями, и о качественном и количественном содержании гетероциклических соединений судят по результатам анализа, проведенного методом спектроскопии гигантского комбинационного рассеяния.
23. Способ по п. 22, отличающийся тем, что для качественного и количественного определения анализируемых веществ с концентрациями 10-6-10-3 М используют жидкие пробы объемом 10-50 мкл путем их накапывания на поверхность сенсора.
24. Способ по п. 22, отличающийся тем, что при проведении анализа используют лазерное излучение с длиной волны 514, или 532, или 633, или 785 нм и мощностью, не превышающей 10% от номинальной величины, при облучении сенсора с нанесенной пробой не более 10 с.
| СЕНСОР ДЛЯ ПОЛУЧЕНИЯ СПЕКТРОВ ГИГАНТСКОГО КОМБИНАЦИОННОГО РАССЕЯНИЯ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2012 |
|
RU2537301C2 |
| ХИМИЧЕСКИ МОДИФИЦИРОВАННЫЙ ПЛАНАРНЫЙ ОПТИЧЕСКИЙ СЕНСОР, СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И СПОСОБ АНАЛИЗА ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ С ЕГО ПОМОЩЬЮ | 2015 |
|
RU2572801C1 |
| US 8383416 B2, 26.02.2013 | |||
| US 20160077090 A1, 17.03.2016. | |||
Авторы
Даты
2017-08-14—Публикация
2016-09-16—Подача