Настоящее изобретение относится производным 1,7-диарил-1,6-гептадиен-3,5-диона к из получению и их применению.
Появление все большего количества бактериальных изолятов, обладающих множественной резистентностью, привело к тому, что лечить бактериальные заболевания стало сложнее. Повышение жесткости гигиенических стандартов и всемирный рост нозокомиальных инфекций вызвали интерес в новым препаратам, способам и применениям, позволяющим ингибировать пролиферацию штаммов, обладающих множественной резистентностью.
Поиск альтернатив антибиотическим терапевтическим средствам имеет жизненно важное значение для лечения инфекций, вызываемых бактериями, например, в частности, из-за роста встречаемости ванкомицин-резистентных бактериальных штаммов (VRSA), в 2002 г. в Японии и в США. В Европе первый изолят VRSA от пациента был зарегистрирован в Португалии в 2013 г.
Рост устойчивости грибковых инфекций к противогрибковым препаратам дополнительно усиливает сложность с лечением поверхностных инфекций. Клинические последствия устойчивости к противогрибковым препаратом проявляются в провалах лечения, особенно у пациентов с иммуносупрессией.
Соответственно, новые подходы к контролю болезнетворных патогенов, обладающих устойчивостью или множественной устойчивостью, заключаются, с одной стороны в поиске новых антидотов, например, антибиотиков или антимикотиков, а с другой стороны, в поиске альтернативных вариантов инактивации.
Было показано, что одним из альтернативных способов является фотодинамическая инактивация микроорганизмов. Фотоокислительный процесс играет решающую роль в фотодинамической инактивации микроорганизмов.
Фотосенсибилизатор возбуждается светом с определенной длиной волны. Возбужденный сенсибилизатор может запустить образование активных форм кислорода (ROS, АФК), после чего могут образовываться, с одной стороны, радикалы, например, супероксид-анионы, радикалы перекиси водорода и гидроксильные радикалы, и/или, с другой стороны, возбужденный молекулярный кислород, например, синглетный кислород.
В обеих реакция преобладает фотоокисление определенных биомолекул, которые находятся в непосредственной близости от активных форм (АФК). Соответственно, окисляются, в частности, липиды и белки, например, являются компонентами клеточной мембраны микроорганизмов. Разрушение клеточной мембраны, в свою очередь, приводит к инактивации микроорганизмов, которые она затрагивает. Аналогичные процесс уничтожения иммет место у вирусов и бактерий.
В качестве примера, синглетный кислород атакует предпочтительно чувствительные к окислению молекулы. Примерами чувствительных к окислению молекул являются молекулы, которые содержат двойные связи или чувствительные к окислению группы, такие как фенолы, сульфиды или тиолы. Ненасыщенные жирные кислоты с мембранах бактерий особенно подвержены повреждению.
Из уровня техники известно много сенсибилизаторов, которые, например, происходят группы порфиринов и их производных, или фталоцианинов и их производных, или фуллеренов и их производных, или являются производными со структурой фенолтиазиниевой структурой, такими как метиленовый сисний или толуидиновый синий, например, или представителями ряда феноксазиния, как нильский синий. Фотодинамика метиленового синего или толуидинового синего в отношении бактерий уже используется в стоматологии.
Большинство фотосенсибилизаторов, известных в уровне техники, представляют собой вещества с относительно сложной молекулярной структурой, которая обуславливает сложность их получения.
Куркумин (1,7-бис-(4-гидрокси-3-метоксифенил)-1,6-гептадиен-3,5-дион) является одним из наиболее важных куркуминоидов турмерика. Турмерик (Curcuma longa) представляет собой растение семейства имбирных. Желтую окраску обуславливают в основном куркумин, деметоксикуркумин и бисдеметоксикуркумин.
Природный куркумин характеризуется низкой фотостабильностью. Например, при дневном свете раствор куркумин осветляется в течение 30 мин.
Природный куркумин также характеризуется низкой стабильностью в воде. Во многих случаях для обеспечения возможности его применение в водной среде требуется применение солюбилизаторов, таких как ДМСО или другие не биосовместимые вещества. Кроме того, его активность в отношении грамотрицательных бактерий ограничена, поскольку структура клеточной стенки таких микроорганизмов препятствует поглощению куркумина.
Соответственно, одной из задач настоящего изобретения является обеспечение новых фотосенсибилизаторов, которые более эффективно инактивируют микроорганизмы.
Еще одной задачей настоящего изобретения является обеспечение новых фотосенсибилизаторов, позволяющих проводить фотодинамическую дезинфекцию объектов и/или жидкостей и/или пациентов во время терапии и/или профилактики.
Задача настоящего изобретения решена за счет предложенного способа инактивации микроорганизмов, которые предпочтительно включают вирусы, археи, бактерии, споры бактерий, грибы, споры грибов, простейшие, паразиты, передающиеся через кровь, и их комбинации, включающий следующие этапы:
(А) приведение микроорганизмов в контакт с по меньшей мере одним фотосенсибилизатором, причем указанный сенсибилизатор представляет собой по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100):
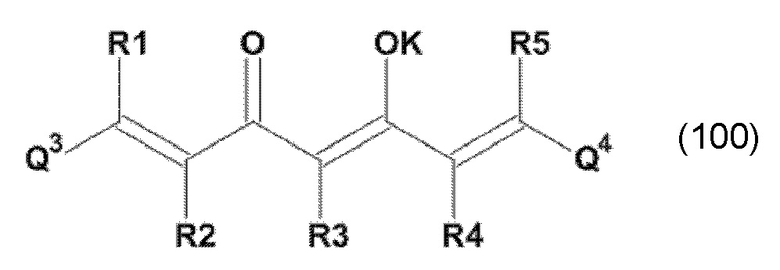
и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (101):
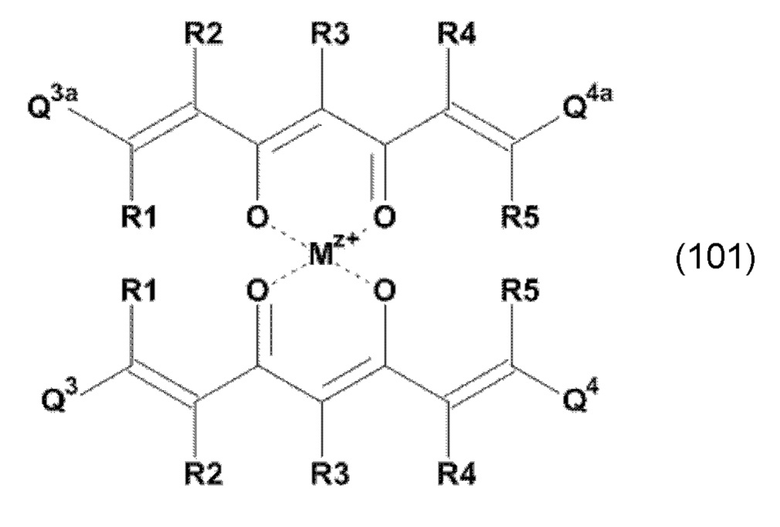
или фармацевтически приемлемую соль, и/или сложный эфир, и/или комплекс указанного соединения,
где Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток,
где K представляет водород или катион, и
где Mz+ представляет катион металла, где z представляет собой формальную степень окисления (окислительное число) указанного металла М, и z представляет целое число от 1 до 7, предпочтительно, от 2 до 5, и где
(а1) по меньшей мере один из остатков Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, представляет собой незамещенный, моноциклический или полициклический гетероароматический остаток, который содержит по меньшей мере 5 атомов кольца, где указанные атомы кольца включают по меньшей мере один атом углерода и по меньшей мере один атом азота, который в предпочтительном варианте может быть протонирован, или
(а2) по меньшей мере один из остатков Q3, Q3a, Q4 и Q4a, причем предпочтительно каждый из остатков Q3 и Q4, предпочтительно каждый из остатков Q3 и Q3a, предпочтительно каждый из остатков Q3, Q3a и Q4, предпочтительно каждый из остатков Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1 с общей формулой (4), (5), (6), (7), (8) или (9), предпочтительно (5), (7) или (9):
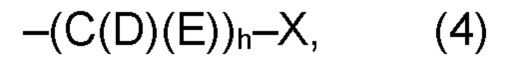
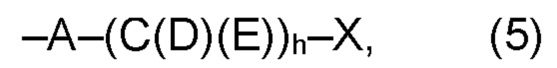
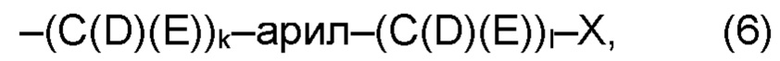
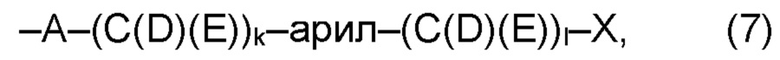
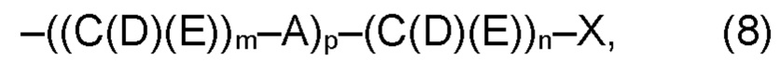
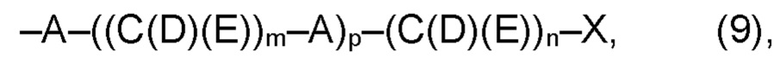
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, где фенил и бензил может быть незамещенным или замещенным,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где X, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
или где
(b) остаток R3 представляет собой органический остаток W2, имеющий общую формулу (4), (5), (6), (7), (8), (9) или (10), предпочтительно (4):
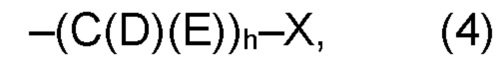
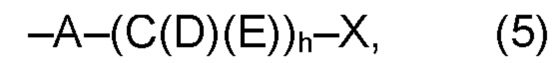
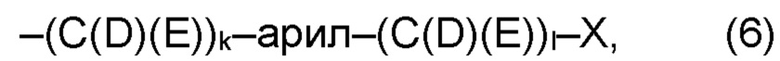
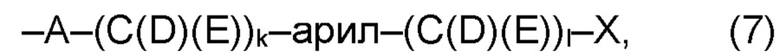
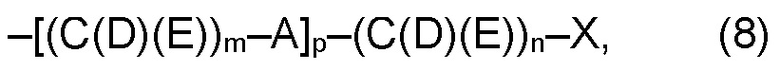
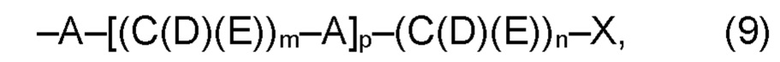
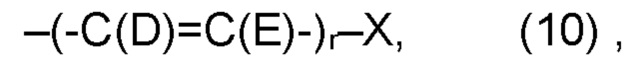
и
где, необязательно, по меньшей мере один из остатков Q3, Q3a, Q4 и Q4a, предпочтительно каждый из остатков Q3 и Q4, предпочтительно каждый из остатков Q3 и Q3a, предпочтительно каждый из остатков Q3, Q3a и Q4, предпочтительно каждый из остатков Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3, органических растворителей W1, имеющих общую формулу (4), (5), (6), (7), (8) или (9), предпочтительно (5), (7) или (9),
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n, p и r, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где X, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С, и (В) облучение указанных микроорганизмов и по меньшей мере одного фотосенсибилизатора электромагнитным излучением при подходящей длине волны и плотности энергии.
В предпочтительном варианте способ в соответствии с настоящим изобретением осуществляют для инактивации микроорганизмов посредством фотодинамической терапии пациента или посредством фотодинамической дезинфекции (обеззараживания) поверхности изделия или жидкости, предпочтительно посредством фотодинамической дезинфекции (обеззараживания) поверхности изделия или жидкости.
Задача настоящего изобретения решается также за счет обеспечения по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100)
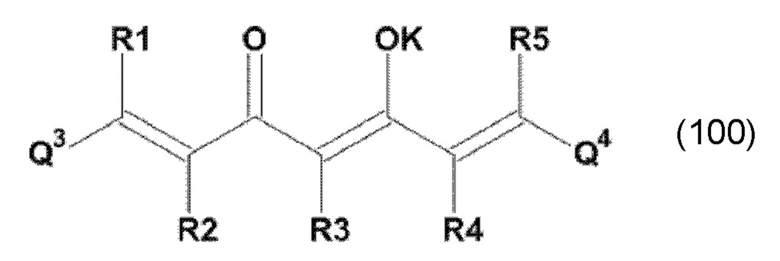
и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (101):
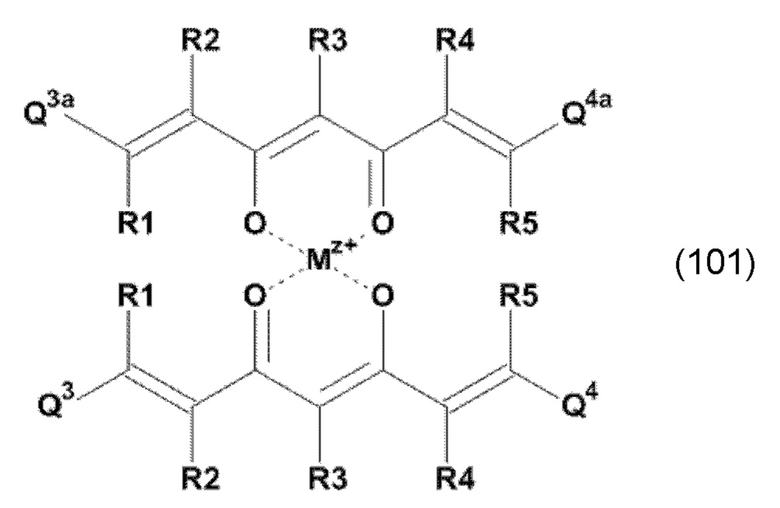
или фармацевтически приемлемой соли, и/или сложного эфира, и/или комплекса указанного соединения, для применения в качестве фотосенсибилизатора в медицинском лечении для инактивации микроорганизмов, которые предпочтительно выбраны из группы, состоящей из вирусов, археев, бактерий, спор бактерий, грибов, спор грибов, простейших, водорослей и передающихся с кровью паразитов,
где Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток,
где K представляет водород или катион, и
где Mz+ представляет катион металла, где z представляет собой формальную степень окисления указанного металла М, и z представляет целое число от 1 до 7, предпочтительно, от 2 до 5, и где
(а1) по меньшей мере один из остатков Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, представляет собой незамещенный, моноциклический или полициклический гетероароматический остаток, который содержит по меньшей мере 5 атомов кольца, где указанные атомы кольца включают по меньшей мере один атом углерода и по меньшей мере один атом азота, который в предпочтительном варианте может быть протонирован, или
(а2) по меньшей мере один из остатков Q3, Q3a, Q4 и Q4a, предпочтительно каждый из остатков Q3 и Q4, предпочтительно каждый из остатков Q3 и Q3a, предпочтительно каждый из остатков Q3, Q3a и Q4, предпочтительно каждый из остатков Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3, органических заместителей W1 с общей формулой (4), (5), (6), (7), (8) или (9); предпочтительно (5), (7) или (9):
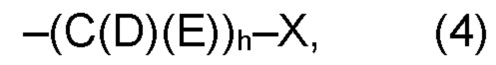
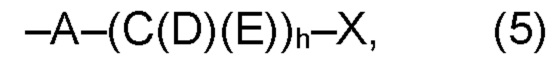
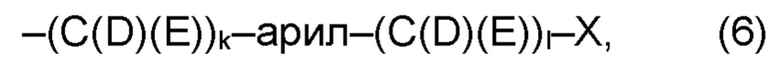
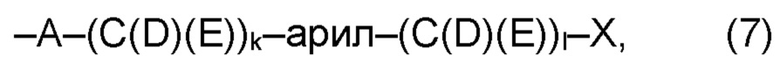
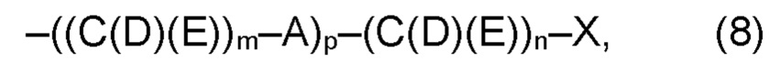
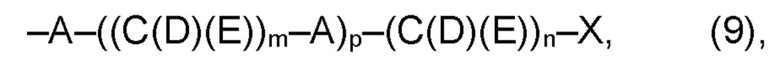
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где X, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
или где
(b) остаток R3 представляет собой органический остаток W2, где органический остаток W2 имеет общую формулу (4), (5), (6), (7), (8), (9) или (10), предпочтительно (4):
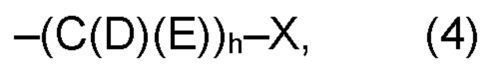
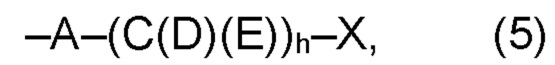
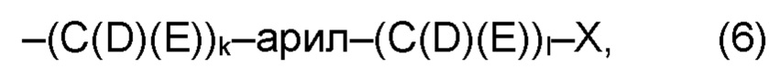
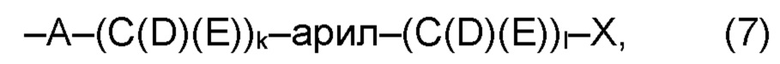
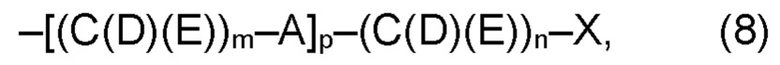
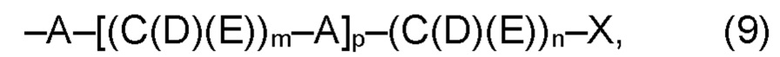
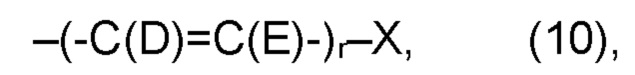
и
где, необязательно, по меньшей мере один из остатков Q3, Q3a, Q4 и Q4a, предпочтительно каждый из остатков Q3 и Q4, предпочтительно каждый из остатков Q3 и Q3a, предпочтительно каждый из остатков Q3, Q3a и Q4, предпочтительно каждый из остатков Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3, органических заместителей W1 с общей формулой (4), (5), (6), (7), (8) или (9), предпочтительно (5), (7) или (9),
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n, p и r, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где X, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
В предпочтительном варианте указанные микроорганизмы и по меньшей мере один фотосенсибилизатор облучают электромагнитным излучением при подходящей длине волны и плотности энергии.
В одном из предпочтительных вариантов реализации изобретения, в соединении формулы (100), K представляет собой катион Mz+ металла М, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 3, и где указанное соединение имеет формулу (102):
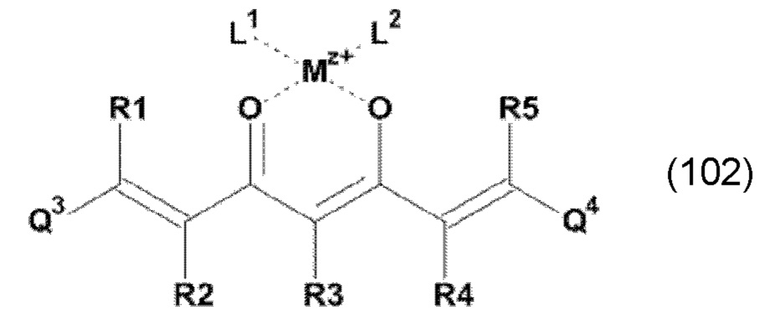
где L1 и L2, соответственно, независимо от других, представляют воду, фтор, хлорид, бромид, йодид, фосфат, гидрофосфат, дигидрофосфат, сульфат, гидросульфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода и/или их смеси. В предпочтительном варианте карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода, представляет собой формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат, цитрат и/или их смеси.
Подходящие производные 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) и их получение описаны, например, в документе СА 2 888 140 А1, содержание которого включено в настоящий текст посредством ссылки.
В предпочтительном варианте подходящее производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) представляет собой по меньшей мере одно соединение формулы (111), (112), (114), (115), (122)-(125) или (137)-(138), предпочтительно, по меньшей мере одно соединение формулы (114) или (115):
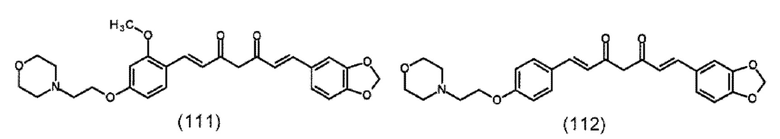
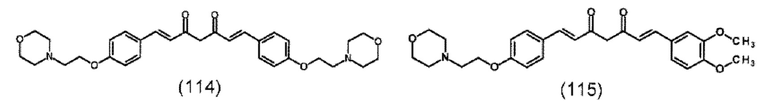
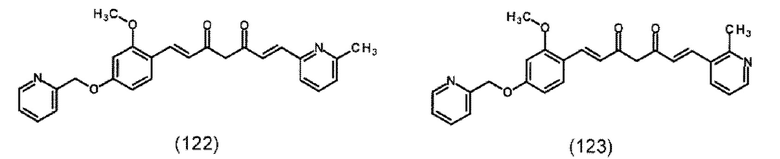
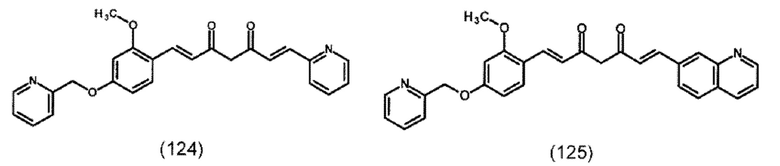
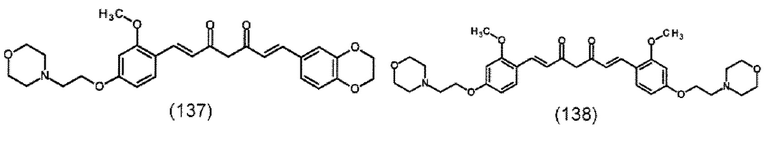
Подходящие производные 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) и их получение описано в документе ЕР 2 698 368 А1, содержание которого включено в настоящий текст посредством ссылки.
В предпочтительном варианте подходящее производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) представляет собой по меньшей мере одно соединение формулы (150), (177), (178), (202), (205) или (209), предпочтительно, по меньшей мере одно соединение формулы (150) или (177):
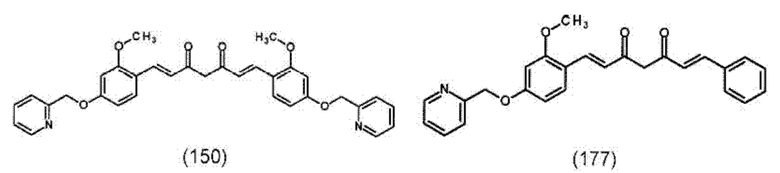
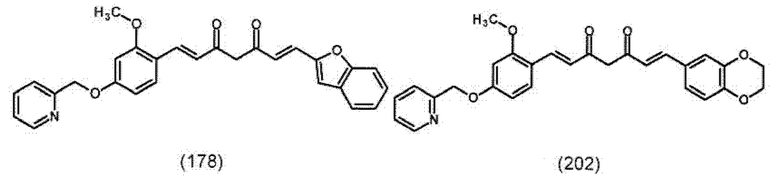
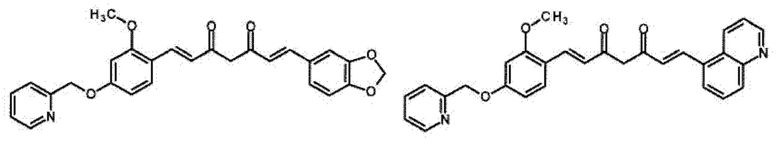
Подходящее производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) и его получение описано также в источнике Taka et al. (Bioorg. Med. Chem. Lett. 24, 2014, стр. 5242 - 5246), содержание которого включено в настоящий текст посредством ссылки. В предпочтительном варианте подходящее производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) представляет собой соединение формулы (228):
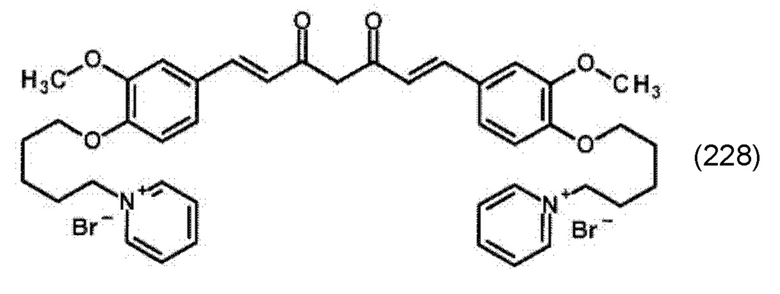
Подходящее производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) и его получение описаны в документе CN 103952008 А1, содержание которого включено в настоящий текст посредством ссылки.
В предпочтительном варианте подходящее производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) представляет собой соединение формулы (229):
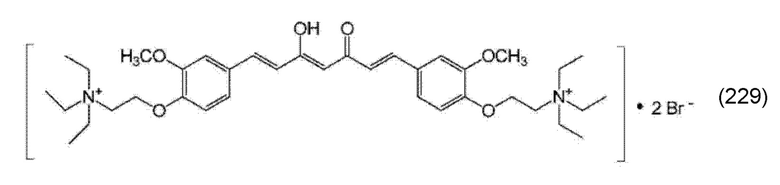
Задача настоящего изобретения решается также за счет обеспечения производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1):
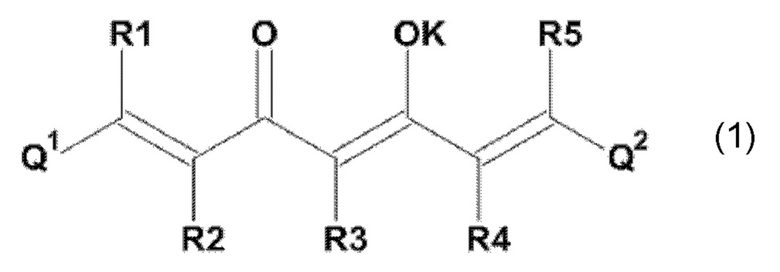
где остатки Q1 и Q2, соответственно, независимо от других, представляют (один, число = 1) замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
где K представляет водород или катион, и
где указанное производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1) не содержит группу ОН, которая напрямую связана с органическим остатком Q1 или Q2, и где
(а) по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1a с общей формулой (5а), (6а), (7а), (8а) или (9а), предпочтительно (5а), (7а) или (9а):
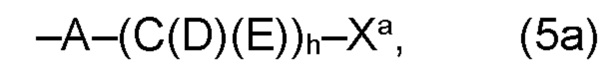
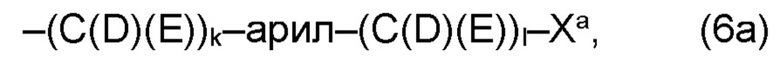
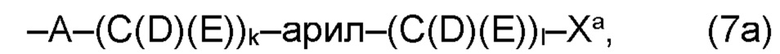
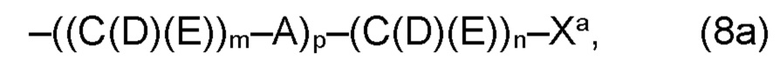
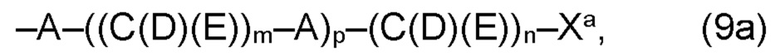
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
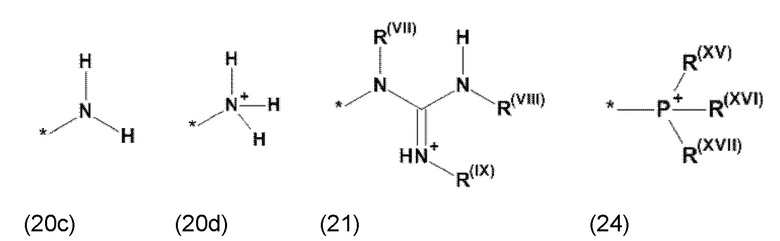
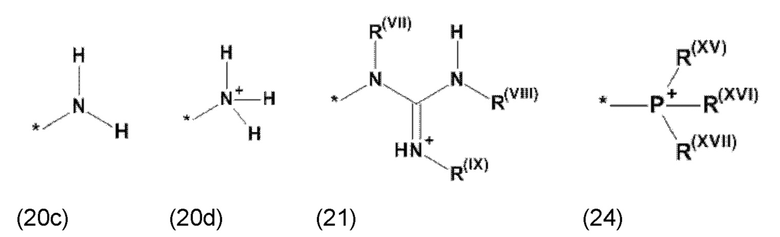
где Xa, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
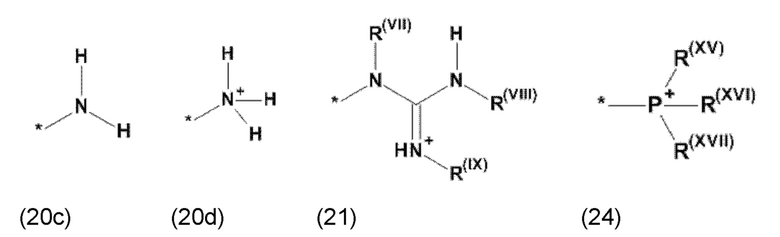
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
или где
(b) остаток R3 представляет собой органический остаток W2a, где указанный органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (4b):
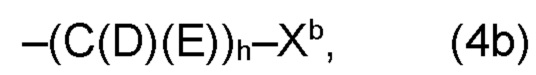
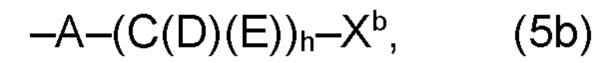
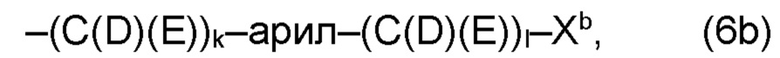
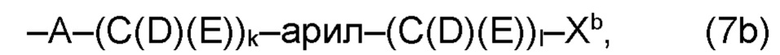
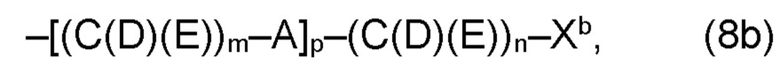
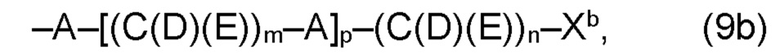
и
где, необязательно, по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1b с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (5b), (7b) или (9b),
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, где предпочтительно Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
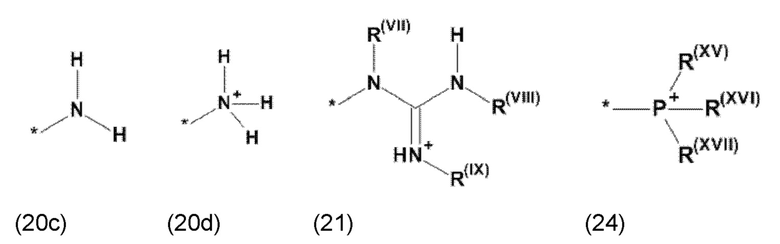
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
В одном из предпочтительных вариантов реализации изобретения, в соединении формулы (1), K представляет собой катион Mz+ металла М, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 3, и где указанное соединение имеет формулу (2):
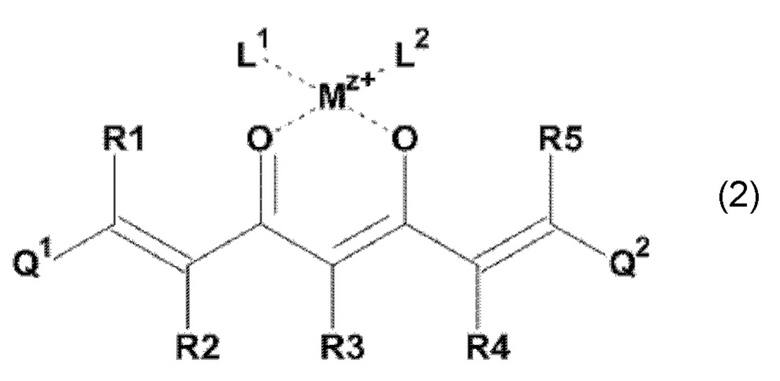
где L1 и L2, соответственно, независимо от других, представляют воду, фтор, хлорид, бромид, йодид, фосфат, гидрофосфат, дигидрофосфат, сульфат, гидросульфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода и/или их смеси. В предпочтительном варианте карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода, представляет собой формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат, цитрат и/или их смеси.
Задача настоящего изобретения решается также за счет обеспечения соединения формулы (3):
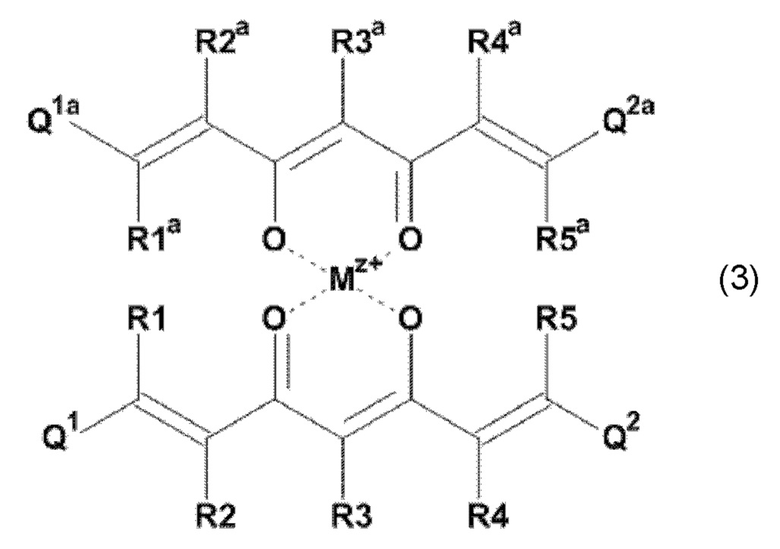
где Mz+ представляет катион металла, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 5, и
где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остатки Q1a и Q2a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток, предпочтительно один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
и где
(а) по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1a с общей формулой (5а), (6а), (7а), (8а) или (9а), предпочтительно (5а), (7а) или (9а):
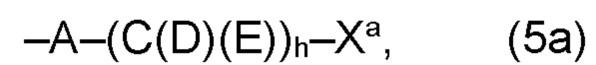
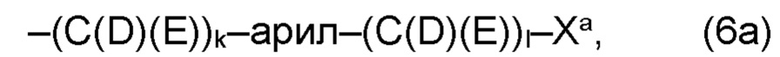
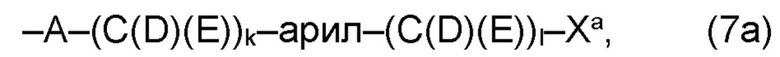
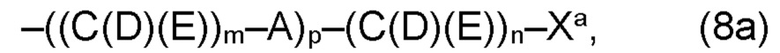
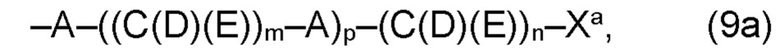
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xa, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
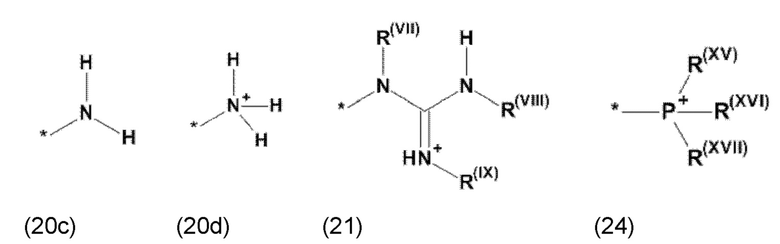
где каждый из остатков R(VII), R(VIII), и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где по меньшей мере один из остатков Q1a и Q2a, предпочтительно каждый из остатков Q1a и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1c с общей формулой (4с), (5с), (6с), (7с), (8с) или (9с), предпочтительно (5с), (7с) или (9с):
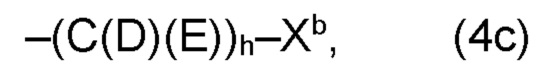
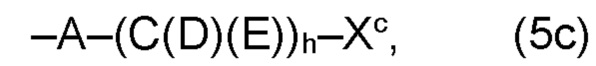
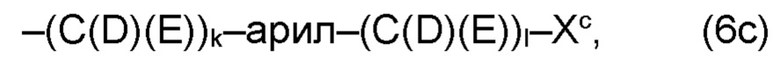
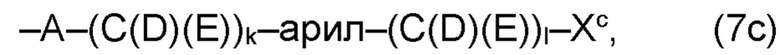
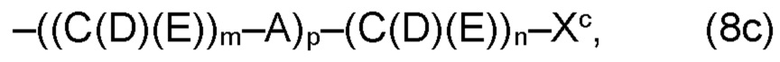
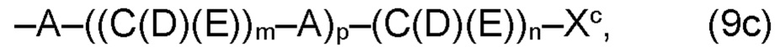
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) и G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xc, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xc, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
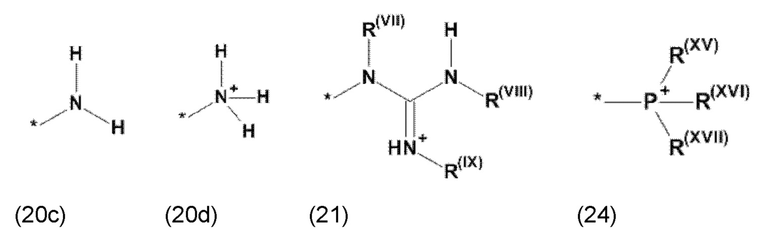
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С,
где остатки R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С, или где
(b) остаток R3 или R3a, соответственно, независимо от других, представляет собой органический остаток W2a, где указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (4b):
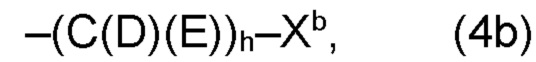
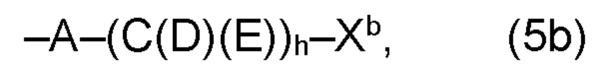
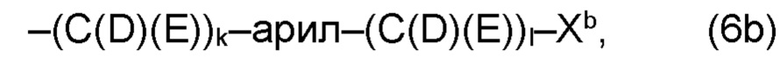
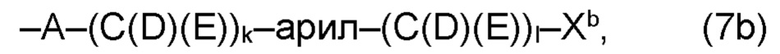
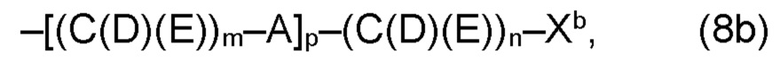
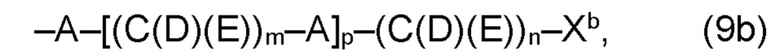
и
где, необязательно, по меньшей мере один из остатков Q1, Q1a, Q2 и Q2a, предпочтительно каждый из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q1a, предпочтительно каждый из остатков Q1, Q13 и Q2, предпочтительно каждый из остатков Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1b с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (5b), (7b) или (9b),
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R1a, R2, R2a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
В предпочтительном варианте в соединении формулы (3) остатки Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
(а) по меньшей мере один из остатков Q1, Q1a, Q2 и Q2a, предпочтительно каждый из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q1a, предпочтительно каждый из остатков Q1, Q1a и Q2, предпочтительно каждый из остатков Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1a с общей формулой (5а), (6а), (7а), (8а) или (9а), предпочтительно (5а), (7а) или (9а):
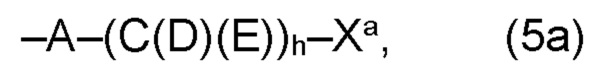
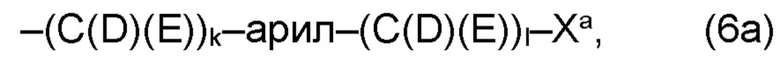
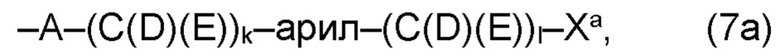
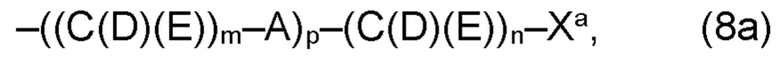
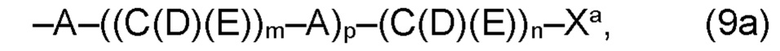
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xa, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
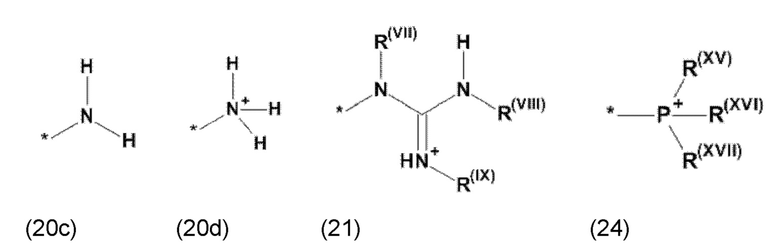
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
или где
(b) остаток R3 или R3a, соответственно, независимо от других, представляет собой органический остаток W2a, где указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (4b):
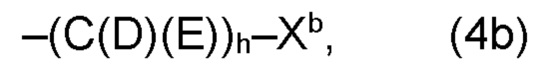
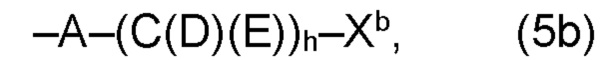
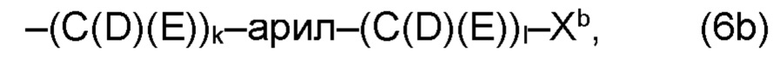
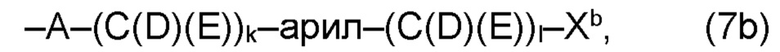
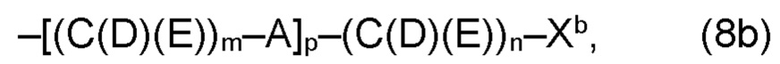
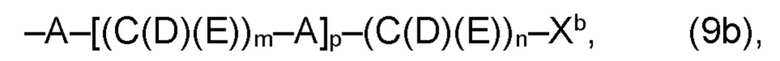
и
где, необязательно, по меньшей мере один из остатков Q1, Q1a, Q2 и Q2a, предпочтительно каждый из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q1a, предпочтительно каждый из остатков Q1, Q1a и Q3, предпочтительно каждый из остатков Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1b с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (5b), (7b) или (9b),
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
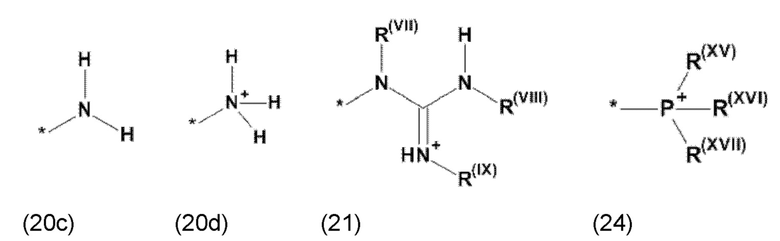
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R1a, R2, R2a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
Соединения согласно настоящему изобретению формулы (1), формулы (2) и формулы (3), соответственно, являются производным 1,7-диарил-1,6-гептадиен-3,5-диона, которое описывается следующим образом.
Любой подходящий анион может применяться в качестве противоиона для положительно заряженного атома азота, например, протонированного атома азота или четвертичного атома азота или положительно заряженного атома фосфора, например, четвертичного атома фосфора. В предпочтительном варианте анионы, применяемые в качестве противоионов для положительно заряженного атома азота или атома фосфора, представляют собой атомы, которые позволяют получить фармакологически приемлемые соли.
В одном из предпочтительных вариантов реализации настоящего изобретения X, Xa, Xb и/или Xc в производном 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), формулы (2) и/или формулы (3), а также производном 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100), формулы (101) и/или формулы (102) для применения в соответствии с настоящим изобретением представляет собой органический остаток, содержащий по меньшей мере один протонированный атом азота или по меньшей мере один четвертичный остаток фосфора, предпочтительно органический остаток с общей формулой (20b), (20d), (21) или (24), который содержит фторид, хлорид, бромид, йодид, сульфат, гидросульфат, фосфат, гидрофосфат, дигидрофосфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода и/или их смеси в качестве противоиона. В предпочтительном варианте карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода, представляет собой формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат, цитрат и/или их смеси.
Дополнительные предпочтительные варианты реализации настоящего изобретения описаны в зависимых пунктах формулы изобретения.
В более предпочтительном варианте реализации производное 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), формулы (2) и/или формулы (3), а также производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100), формулы (101) и/или формулы (102) для применения в соответствии с настоящим изобретением не содержит нейтральный атом азота, который может быть протонирован, например, как в случае амино-остатка, метиламино-остатка или диметиламино-остатка и не содержит положительно заряженного, предпочтительно четвертичного атома азота, как в случае остатка пиридин-1-ий-1-ила остатка триметиламмониево, а также не содержит положительно заряженного, предпочтительно четвертичного, атома фосфора, который связан с органическим остатком Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a.
Термин "прямой" («напрямую», «прямо», «непосредственно») следует понимать в том смысле, что атом азота и/атом фосфора напрямую связан с ароматическим остатком Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a.
Авторы изобретения неожиданно обнаружили, что размещение атома азота и/или атома фосфора прямо на ароматической системе колец остатков Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4 приводит к существенному снижению выхода активных форм кислорода, например.
Для противомикробной эффективности фотодинамической терапии или фотодинамической очистки поверхностей или жидкости требуется максимально возможный выход активных форм кислорода. Когда атом азота и/или атом фосфора расположен прямо на ароматической системе колец остатка Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a, поглощаемая энергия рассеивается в основном за счет флуоресцентных эффектов. Это приводит к значительному снижению эффективности фотодинамического действия, т.е., к уменьшению количества активных форм кислорода (АФК, ROS), образующегося за счет фотодинамических процессов, и/или возбужденного молекулярного кислорода, образующегося в фотодинамических процессах.
Кроме того, авторы изобретения неожиданно обнаружили, размещение по меньшей мере одного нейтрального атома азота, который может быть протонирован и/или по меньшей мере одного положительно заряженного, предпочтительно, четвертичного атома азота и/или по меньшей мере одного положительно заряженного, предпочтительно четвертичного атома фосфора на по меньшей мере одном атоме углерода, например, в форме метиленовой группы, который, таким образом отделен от ароматического остатка Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a, не оказывает негативного влияния на фотодинамические свойства соединения формулы (1), и/или соединения формулы (2), и/или соединения формулы (3), и/или соединения формулы (100),и/или соединения формулы (101), и/или соединения формулы (102).
Положительный заряд на атоме азота и/или атома фосфора также обеспечивает эффективное присоединение соединения в соответствии с настоящим изобретением формулы (1), формулы (2), и/или формулы (3), и/или соединения для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102) к отрицательно заряженным компонентам клеточной стенки микроорганизмов. Соответственно, по меньшей мере один атом углерода, например, в форме метиленовой группы, также действует как спейсер, что позволяет эффективно расположить громоздкую структуру соединения формулы (1), и/или соединения формулы (2), и/или соединения формулы (3), и/или соединения формулы (100), и/или соединения формулы (101), и/или соединения формулы (102) на клеточной стенки микроорганизмов.
Далее, авторы изобретения неожиданно обнаружили, что за счет расположения по меньшей мере одного нейтрального атома азота, который может быть протонирован, и/или по меньшей мере одного положительно заряженного, предпочтительно четвертичного атом азота и/или по меньшей мере одного положительно заряженного, предпочтительно четвертичного атома фосфора, может быть улучшена растворимость соединения в соответствии с настоящим изобретением формулы (1), формулы (2), и/или формулы (3), и/или соединения для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102), в полярных растворителях, например, воде.
В более предпочтительном варианте реализации производное 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), формулы (2) и/или формулы (3), а также производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102) не содержит группу ОН, которая напрямую связана с органическим остатком Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a.
Термин "прямой" («напрямую», «прямо», «непосредственно») следует понимать в том смысле, что группа ОН напрямую связана с ароматическим остатком Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a.
Авторы изобретения неожиданно обнаружили, что прямое расположение группы ОН on на ароматической системе колец остатков Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a приводит к значительному нарушению фотостабильности фотосенсибилизатора. Нарушение фотостабильности приводит к более быстрому обесцвечиванию и, соответственно, к более быстрой инактивации фотосенсибилизатора при облучении электромагнитным излучением с соответствующей длиной волны.
В предпочтительном варианте указанный по меньшей мере один нейтральный атом азота, который может быть протонирован, и указанный по меньшей мере один положительно заряженный, предпочтительно, четвертичный атом азота не является амидом карбоновой кислоты.
В более предпочтительном варианте реализации производное 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), формулы (2) и/или формулы (3), а также производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102) не является карбаматным остатком, который предпочтительно связан напрямую с органическим остатком Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a.
Авторы настоящего изобретения обнаружили, что расположение карбаматного остатка прямо на ароматической системе колец остатков Q1, Q1a, Q2, Q2a, Q3, Q3a, Q4 или Q4a приводит к значительному нарушению фотостабильности фотосенсибилизатора. Нарушение фотостабильности приводит к более быстрому обесцвечиванию и, соответственно, к более быстрой инактивации фотосенсибилизатора при облучении электромагнитным излучением с соответствующей длиной волны.
Термин "фотосенсибилизатор" в контексте настоящего изобретения следует понимать как обозначающий соединения, которые поглощают электромагнитное излучение, предпочтительно видимый свет, УФ-свет и/или инфракрасный свет, и за счет этого образуют активные формы кислорода (АФК, ROS), предпочтительно свободнее радикалы и/или синглетный кислород из триплетного кислорода.
Термин "фотодинамическая терапия" в контексте настоящего изобретения следует понимать как обозначающий индуцируемую светом инактивацию клеток микроорганизмов, предпочтительно, включая вирусы, археи, бактерии, споры бактерий, грибы, споры грибов, простейшие, водоросли, передающиеся с кровью паразиты, или их комбинации, на и/или в теле пациента.
Термин "фотодинамическая дезинфекция (очистка)" в контексте настоящего изобретения следует понимать как обозначающий индуцируемую светом инактивацию микроорганизмов, предпочтительно включая вирусы, археи, бактерии, споры бактерий, грибы, споры грибов, простейшие, водоросли, передающиеся с кровью паразиты, или их комбинации, на поверхностях изделий и/или пищевых продуктов и/или в жидкостях.
Термин "инактивация" в контексте настоящего изобретения следует понимать как обозначающий снижение жизнеспособности или разрушение микроорганизма, предпочтительно, его разрушение. Индуцируемую светом инактивацию можно, например, определить по уменьшению числа микроорганизмов после инактивации по cpof a predefined starting quantity of said microorganisms в присутствии по меньшей мере одного соединения в соответствии с настоящим изобретением формулы (1), формулы (2) и/или формулы (3) и/или соединения для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102).
В соответствии с настоящим изобретением термин "снижение жизнеспособности" следует понимать как означающий, что количество микроорганизмов снижается по меньшей мере на 80.0%, предпочтительно, по меньшей мере 99.0%, предпочтительно, по меньшей мере 99.9%, более предпочтительно по меньшей мере на 99.99%, более предпочтительно на по меньшей мере 99.999%, еще более предпочтительно по меньшей мере на 99.9999%. В наиболее предпочтительном варианте число микроорганизмов снижается более, чем на 99.9% - 100%, предпочтительно более, чем на 99.99% 100%.
В предпочтительном варианте снижение количества микроорганизмов проводят в соответствии с руководством Boyce, J. M., Pittet, D. ("Guidelines for hand hygiene in healthcare settings. Recommendations of the Healthcare Infection Control Practices Advisory Committee and the HIPAC/SHEA/APIC/IDSA Hand Hygiene Task Force", Am. J. Infect. Control 30 (8), 2002, стр. 1-46) в виде log10 - коэффициента ослабления (уменьшения).
В соответствии с настоящим изобретением термин "log10- коэффициент ослабления" следует понимать как обозначающий разницу между логарифмом по основанию 10 числа микроорганизмов до и логарифмом по основанию 10 числа микроорганизмов после облучения указанных микроорганизмов электромагнитным излучением в присутствии по меньшей мере одного соединения в соответствии с настоящим изобретением формулы (1), формулы (2) и/или формулы (3) и/или соединения для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102).
Примеры подходящих методов определения log10 фактора ослабления описаны в стандарте DIN EN 14885:2007-01 "Chemical disinfectants and antiseptics. Application of European standard for chemical disinfectants and antiseptics" или в документе Rabenau, H. F., Schwebke, I. ("Leitlinie der Deutschen Vereinigung zur  der Viruskrankheiten (DVV) e. V. und der Robert Koch-lnstituts (RKI) zur
der Viruskrankheiten (DVV) e. V. und der Robert Koch-lnstituts (RKI) zur  von chemischen Desinfektionsmittein auf Wirksamkeit gegen Viren in der Humanmedizin" Bundesgesundheitsblatt, Gesundheitsforschung, Gesundheitsschutz 51(8), (2008), стр. 937-945).
von chemischen Desinfektionsmittein auf Wirksamkeit gegen Viren in der Humanmedizin" Bundesgesundheitsblatt, Gesundheitsforschung, Gesundheitsschutz 51(8), (2008), стр. 937-945).
В предпочтительном варианте log10 коэффициент ослабления после облучения микроорганизмов электромагнитным излучением в присутствии по меньшей мере одного соединения в соответствии с настоящим изобретением формулы (1), формулы (2) и/или формулы (3) и/или соединения для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102) составляет по меньшей мере 2 log10, предпочтительно, по меньшей мере 3 log10, более предпочтительно, по меньшей мере 4 log10, более предпочтительно, по меньшей мере 4.5 log10, более предпочтительно, по меньшей мере 5 log10, более предпочтительно, по меньшей мере 6 log10, еще более предпочтительно, по меньшей мере 7 log10, еще более предпочтительно, по меньшей мере 7.5 log10.
В качестве примера "снижение количества микроорганизмов после облучения микроорганизмов электромагнитным излучением в присутствии по меньшей мере одного соединения в соответствии с настоящим изобретением формулы (1), формулы (2) и/или формулы (3), и/или соединения для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102) на 2 процентных пункта относительно исходного количества этих микроорганизмов " обозначает log10 коэффициент ослабления, составляющий 2 log10.
В более предпочтительном варианте количество микроорганизмов после облучения микроорганизмов электромагнитным излучением в присутствии по меньшей мере одного соединения в соответствии с настоящим изобретением формулы (1), формулы (2) и/или формулы (3) и/или соединения для применения в соответствии с настоящим изобретением формулы (100), формулы (101) и/или формулы (102) снижается на по меньшей мере 1 процентный пункт, более предпочтительно по меньшей мере на 2 процентных пункта, предпочтительно по меньшей мере на 4 процентных пункта, более предпочтительно по меньшей мере на 5 процентных пунктов, более предпочтительно по меньшей мере на 6 процентных пунктов, еще более предпочтительно по меньшей мере на 7 процентных пунктов, относительно исходного количества указанных микроорганизмов.
Термин "микроорганизмы" в контексте настоящего изобретения следует понимать как относящийся, в частности, как вирусам, археям, прокариотическим микроорганизмам, таким как грибы, простейшим, спорам грибов, одноклеточным водорослям. Микроорганизмы могут быть одноклеточными или многоклеточными, например, мицелий грибов.
Производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением имеет формулу (1):
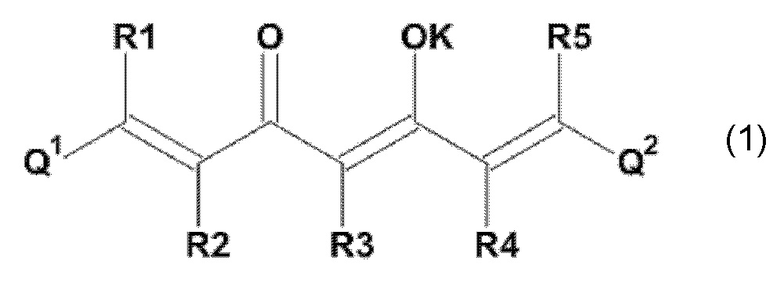
где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
причем указанное производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1) не содержит группу ОН, которая напрямую связана с органическим остатком Q1 или Q2, и
при этом K представляет водород или катион.
В варианте (а) производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, K представляет водород или катион, и по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1a с общей формулой (5а), (6а), (7а), (8а) или (9а), предпочтительно (5а), (7а) или (9а):
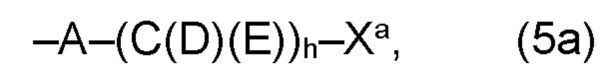
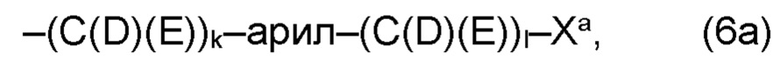
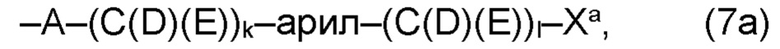
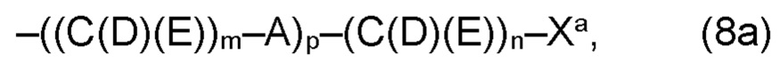
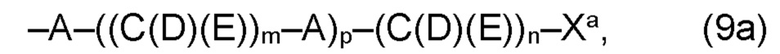
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xa, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
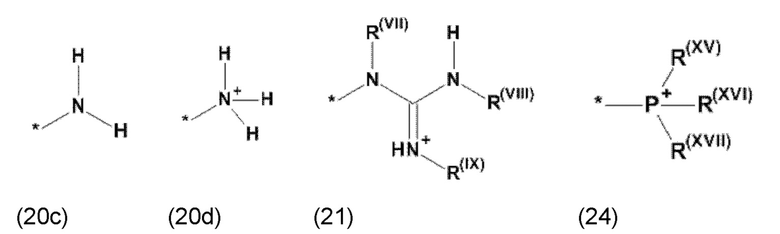
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
В варианте (b) производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, K представляет водород или катион, и остаток R3 представляет собой органический остаток W2a имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (4b):
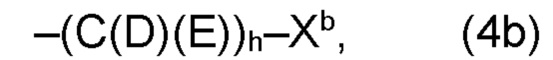
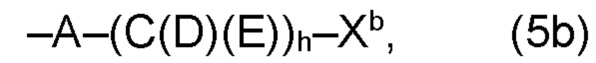
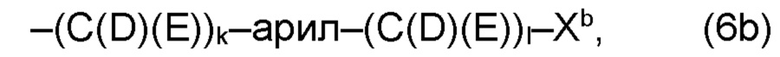
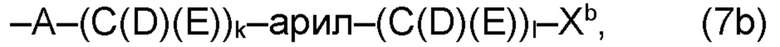
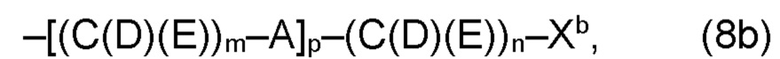
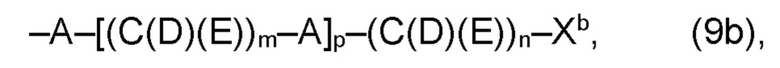
и
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, где, более предпочтительно, Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
Необязательно, в варианте (b) производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1b с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (5b), (7b) или (9b):
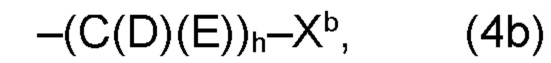
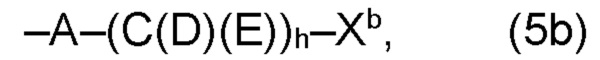
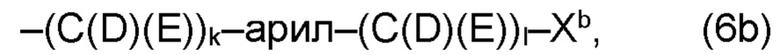
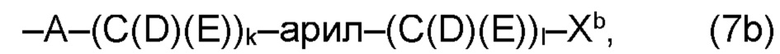
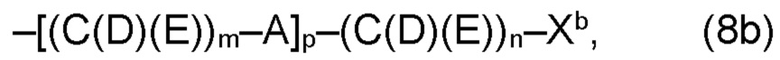
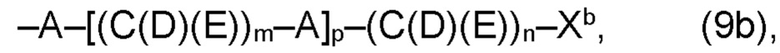
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, где, более предпочтительно, Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
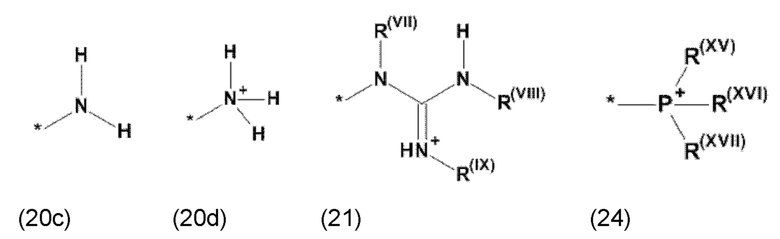
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С.
В одном из предпочтительных вариантов реализации соединения формулы (1), K представляет собой катион Mz+ металла М, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 5, более предпочтительно, от 2 до 3, и где указанное соединение имеет формулу (2):
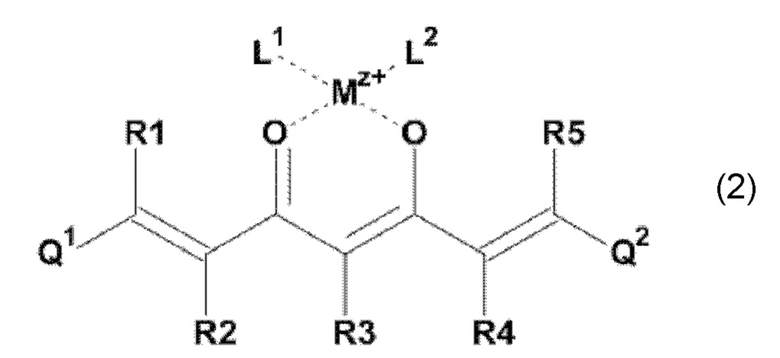
где L1 и L2, соответственно, независимо от других, представляют воду, фтор, хлорид, бромид, йодид, цианид, карбонил, тиоцианат, фосфат, гидрофосфат, дигидрофосфат, сульфат, гидросульфат, ацетилацетонат, эфир уксусной кислоты, ацетонитрил, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода, и/или их комбинации. В предпочтительном варианте карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода, представляет собой формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат, цитрат и/или их комбинации.
В более предпочтительном варианте L1 и L2 идентичны, например, представляют собой полидентантный лиганд. Подходящие полидентантные лиганды содержат два или более координационных центров, которые могут связываться с катионом М2+. Примерами подходящих полидентантных лигандов являются этилендиамин, нитрилотриуксусная кислота (NTA), этилендиаминтетраацетатные соли (ЭДТА), ацетилацетонат, сложные эфиры уксусной кислоты, цитрат, бис(2-метоксиэтил)эфир (диглим), 8-гидроксихинолинил, 2,2'-бипиридин, 1,10-фенантролин (фен), димеркаптоянтарная кислота, тартрат или оксалат.
Производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением также имеет формулу (3):
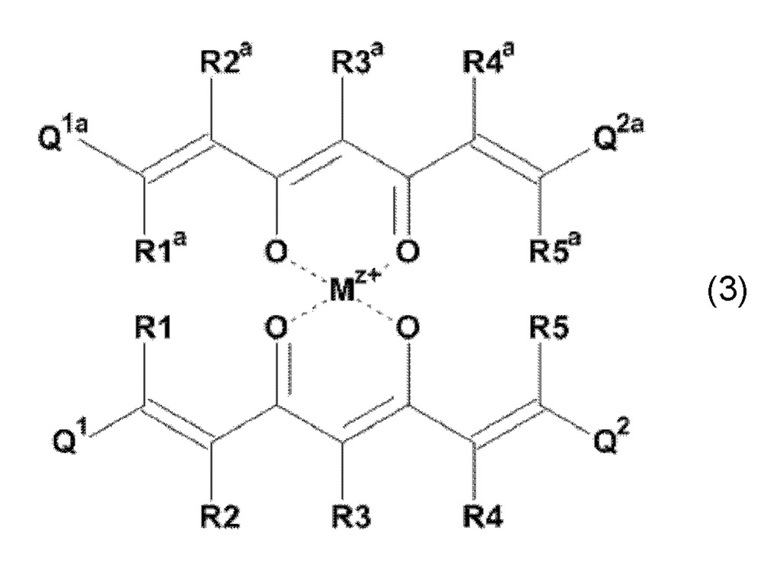
В варианте (а) производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (3), Mz+ представляет катион металла М, где z представляет собой формальную степень окисления указанного металла М и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 3, и
где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
где остатки Q1a и Q2a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток, предпочтительно один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
и где по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1a с общей формулой (5а), (6а), (7а), (8а) или (9а), предпочтительно (5b), (7b) или (9b):
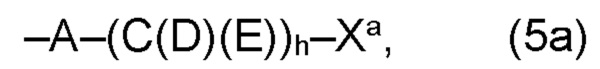
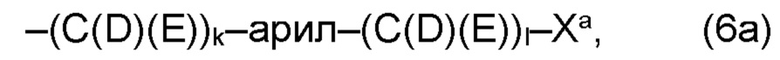
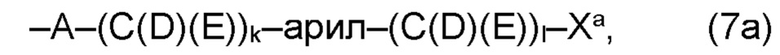
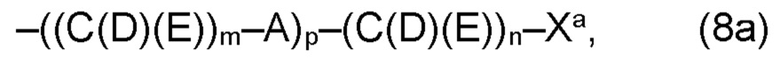
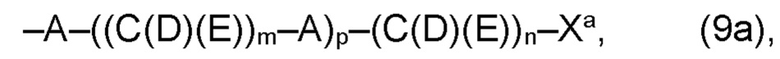
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xa, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
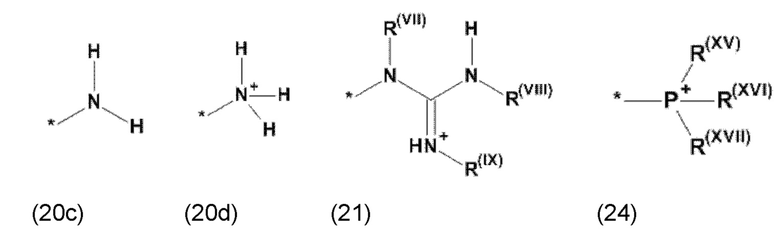
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где по меньшей мере один из остатков Q1a и Q2a, предпочтительно каждый из остатков Q1a и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1c с общей формулой (4с), (5с), (6с), (7с), (8с) или (9с), предпочтительно (5с), (7с) или (9с):
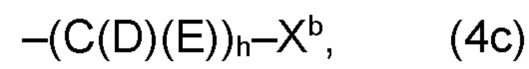
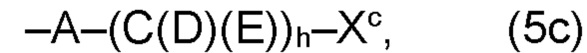
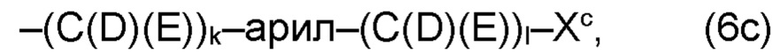
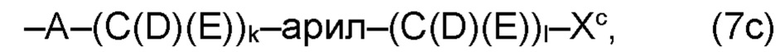
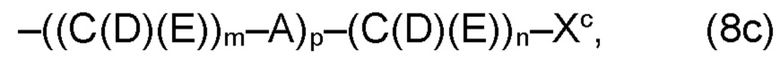
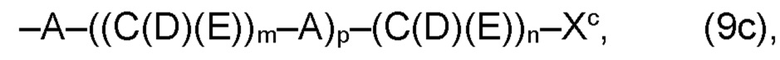
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xc, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xc, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
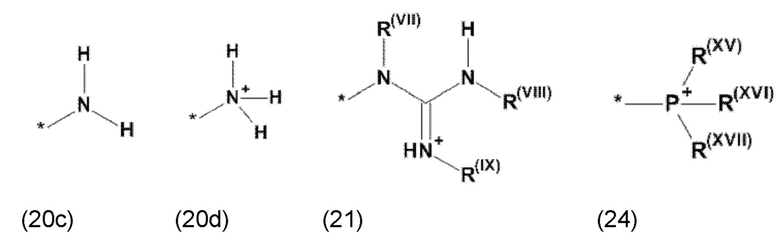
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С,
где остатки R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
В варианте (b) производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (3), Mz+ представляет катион металла М, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 5, и
где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
где остатки Q1a и Q2a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток, предпочтительно один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
и где остаток R3 или R3a, предпочтительно остатки R3 и R3a, соответственно, независимо от других, представляют an органический остаток W2a с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (4b):
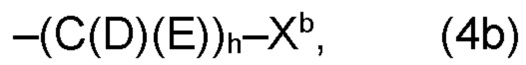
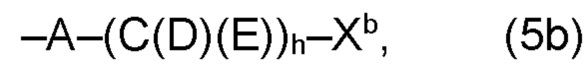
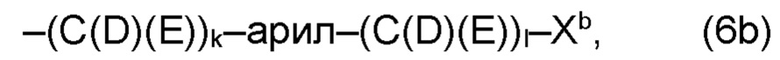
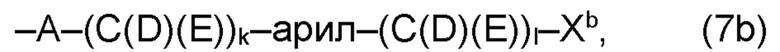
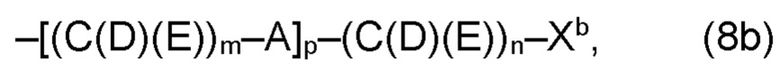
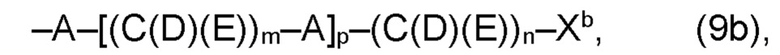
и
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, где, более предпочтительно, Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
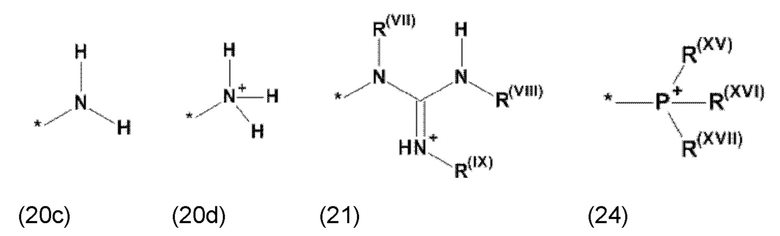
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R1a, R2, R2a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
Необязательно, в варианте (b) производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (3), по меньшей мере один из остатков Q1, Q1a, Q2 и Q2a, предпочтительно каждый из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q1a, предпочтительно каждый из остатков Q1, Q1a и Q2, предпочтительно каждый из остатков Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1b с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (5b), (7b) или (9b):
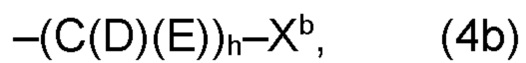
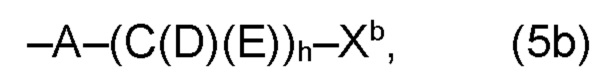
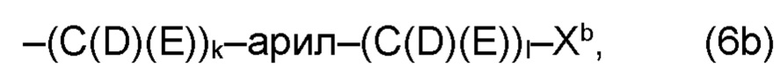
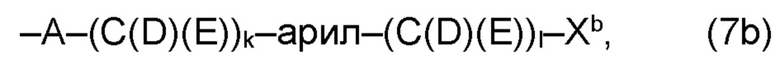
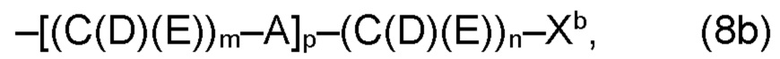
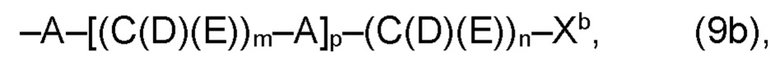
и
где h представляет целое число от 1 до 20, предпочтительно, от 1 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 1 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, где, более предпочтительно, Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
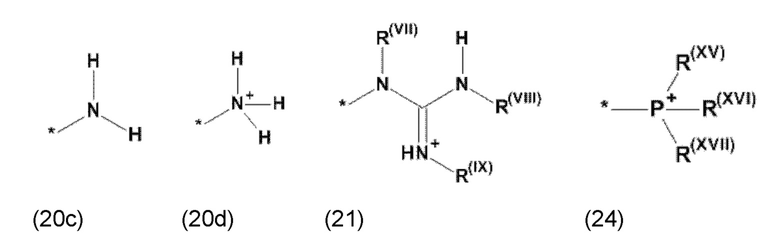
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С.
В одном из предпочтительных вариантов реализации соединения формулы (3), указанное соединение имеет формулу (3а):
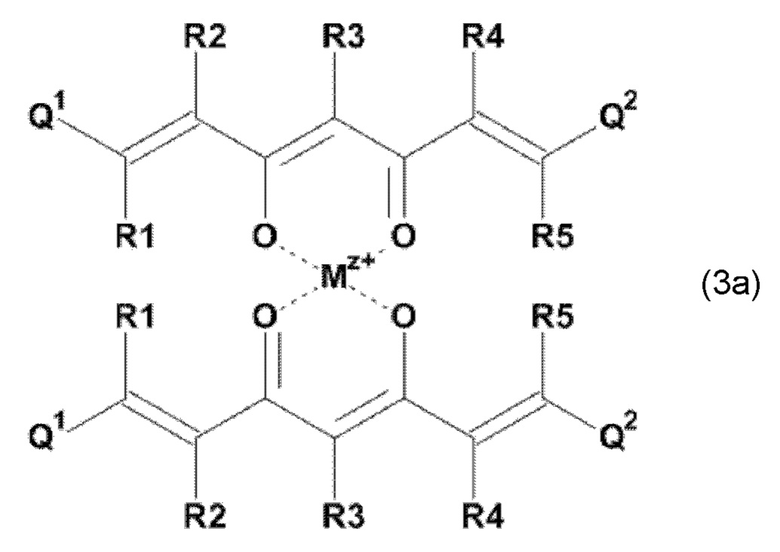
В варианте (а) производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (3а), Mz+ представляет катион металла М, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 3, и где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1a с общей формулой (5а), (6а), (7а), (8а) или (9а), предпочтительно (5а), (7а) или (9а):
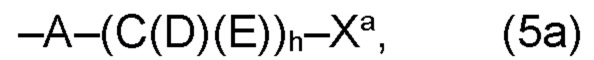
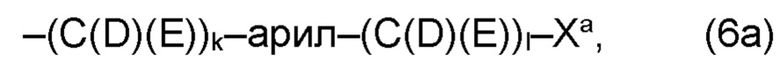
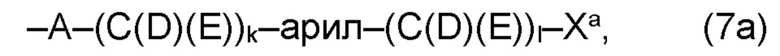
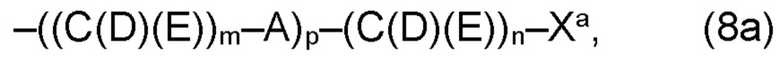
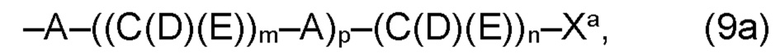
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xa, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
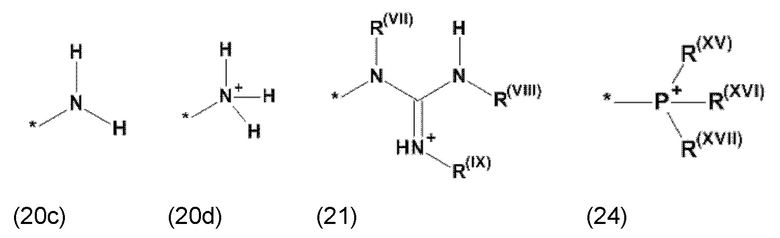
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
В варианте (b) производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (3а), Mz+ представляет катион металла М, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 5, и
где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
и где остаток R3, соответственно представляет собой органический остаток W2a, где органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (4b):
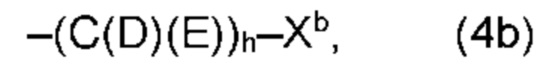
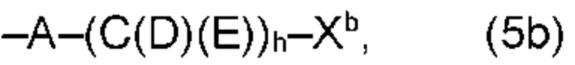
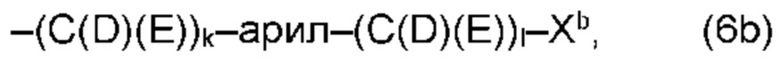
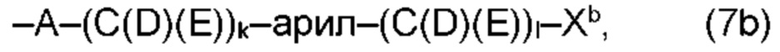
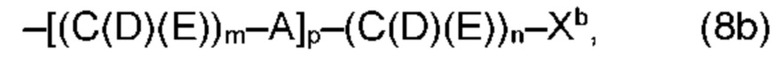
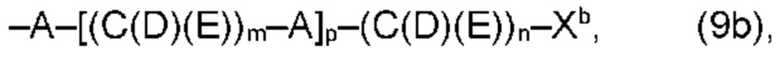
и
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, где, более предпочтительно, Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
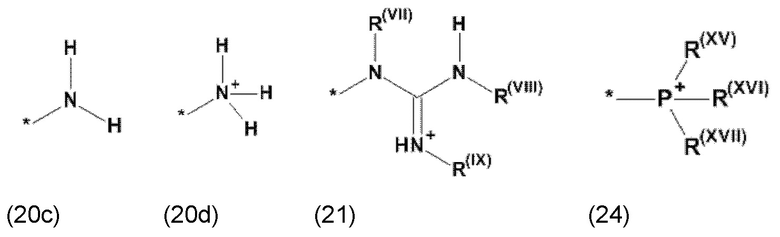
где каждый из остатков R(VII), R(VII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII)), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
Необязательно, в варианте (b) производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (3а) по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1b с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно (5b), (7b) или (9b):
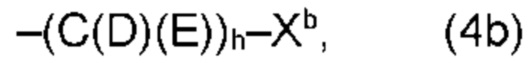
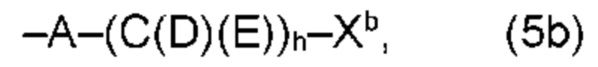
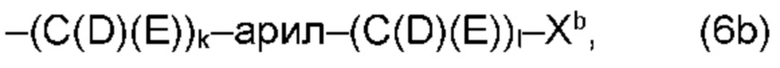
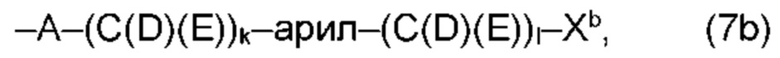
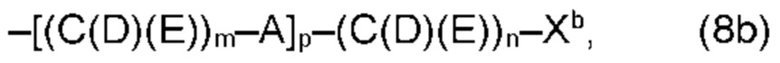
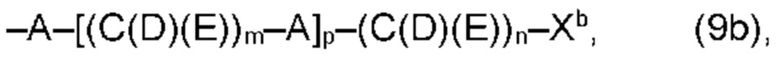
и
где h представляет целое число от 1 до 20, предпочтительно, от 1 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 1 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, где, более предпочтительно, Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
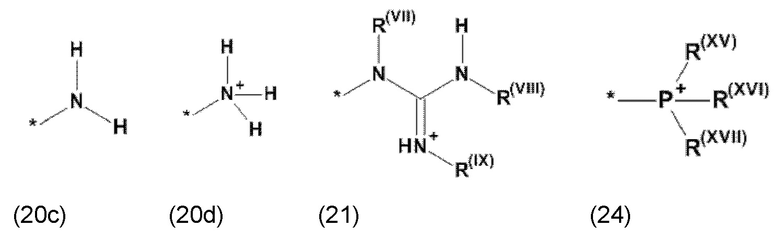
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII)), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С.
В одном из предпочтительных вариантов реализации соединения формулы (2), и/или соединения формулы (3), и/или соединения формулы (3а), и/или соединения формулы (101), и/или соединения формулы (102), металл М выбран из группы, которая состоит из щелочных металлов, щелочноземельных металлов, переходных металлов, металлов и металлоидов из третьей, четвертой, пятой и шестой основных групп периодической таблицы элементов и их комбинаций; в предпочтительном варианте металл М выбран из группы, которая состоит из Be, Mg, Са, Sr, Ва, Ti, Zr, Hf, V, Nb, Та, Cr, Mo, W, Mn, Tc, Rh, Fe, Ru, Os, Co, Rh, Ir, Ni, Pd, Pt, Cu, Ag, Au, Zn, B, Al, Ga, In, Si, Ge, Sn, Bi, Se, Те и их комбинаций.
В более предпочтительном варианте металл М выбран из группы, которая состоит из В, Al, Zn, Cu, Mg, Са, Fe, Si, Ga, Sn, Rh, Co, Ti, Zr, V, Cr, Mo, Mn, Ru, Pd, Ir, Ni и их комбинаций. В более предпочтительном варианте Mz+ представляет Mg2+, Са2+, Fe2+, Fe3+, Zn2+, Cu2+, B3+ или Si4+.
В соответствии с настоящим изобретением в соединении формулы (1), или соединении формулы (2), или соединении формулы (3а) остатки Q1 и Q2, или в соединении формулы (3) остатки Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, который предпочтительно, соответственно, независимо от других, представляет собой фенильный остаток, нафтильный остаток, азуленовый остаток, феналеновый остаток, аценафтильный остаток, флуореновый остаток, фенантреновый остаток, антраценовый остаток, флуорантеновый остаток, пиреновый остаток, бензо[a]антраценовый остаток, хризеновый остаток, а бензо[b]флуорантеновый остаток, бензо[h]флуорантеновый остаток, а бензо[а]пиреновый остаток, дибен-зо[а,h]антраценовый остаток, тетраценовый остаток, трифениленовый остаток, пентаценовый остаток или гексаценовый остаток, более предпочтительно фенильный остаток, нафтильный остаток, феналеновый остаток или антраценовый остаток.
В соответствии с настоящим изобретением в соединении формулы (100) или соединении формулы (102), остатки Q3 и Q4, или в соединении формулы (101), остатки Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, которые предпочтительно, соответственно, независимо от других, представляют фенильный остаток, нафтильный остаток, азуленовый остаток, феналеновый остаток, аценафтильный остаток, флуореновый остаток, фенантреновый остаток, антраценовый остаток, флуорантеновый остаток, пиреновый остаток, бензо[а]антраценовый остаток, хризено-вый остаток, бензо[b]флуорантеновый остаток, бензо[h]флуорантеновый остаток, бензо[а]пиреновый остаток, дибензо[а,h]антраценовый остаток, тетраценовый остаток, трифениленовый остаток, пентаценовый остаток или гексаценовый остаток, более предпочтительно, фенильный остаток, нафтильный остаток, феналеновый остаток или антраценовый остаток, или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток, который предпочтительно содержит по меньшей мере 5 атомов кольца, где указанные атомы кольца включают по меньшей мере один атом углерода и по меньшей мере один атом азота, который в предпочтительном варианте может быть протонирован, где, более предпочтительно, указанный один замещенный или незамещенный моноциклический или полициклический гетероатомный остаток, соответственно, независимо от других, представляет собой пиррольный остаток, пиридиновый остаток, хинолиниловый остаток, изохинолиновый остаток, индоловый остаток, изоиндоловый остаток, пиримидиновый остаток, пиразиновый остаток, имидазоловый остаток или актидиновый остаток, более предпочтительно пиридиновый остаток, хинолиниловый остаток, изохинолиновый остаток или индоловый остаток.
В предпочтительном варианте указанный один замещенный или незамещенный, моноциклический или полициклический, гетероатомный остаток содержит от 5 до 14, более предпочтительно, от 6 до 10 атомов в кольце, где указанные атомы кольца включают по меньшей мере 1 атом углерода или по меньшей мере 1 атом азота, который предпочтительно может быть протонирован. В более предпочтительном варианте атомы кольца включают от 1 до 3 атомов азота, которые предпочтительно могут быть протонированы, и, которые, в еще более предпочтительном варианте, не расположены рядом друг с другом.
В варианте (а1) соединения формулы (100), соединения формулы (101) и/или соединения формулы (102) по меньшей мере один из остатков Q3, Q3a, Q4 и Q4a, соответственно, независимо от других, представляет собой ненасыщенный моноциклический или полициклический гетероароматический остаток, который содержит по меньшей мере 5, предпочтительно от 5 до 14, более предпочтительно, от 6 до 10 атомов кольца, где указанные атомы кольца включают по меньшей мере один атом углерода и по меньшей мере один атом азота, который в предпочтительном варианте может быть протонирован. В более предпочтительном варианте указанные атомы кольца включают от 1 до 3, предпочтительно 1 или 2, атомов азота, которые предпочтительно могут быть протонированы. В еще более предпочтительном варианте указанные атомы азота не расположены в соседних положениях.
В предпочтительном варианте указанные замещенные моноциклические или полициклические ароматические остатки или замещенные моноциклические или полициклические, гетероатомные остатки, с по меньшей мере одним органическим остатком W1, или одним органическим остатком W1a или одним органическим остатком W1b, или одним органическим остатком W1c, и/или с галогеном, нитро, карбоксилатом, альдегидом, содержащим от 1 до 8 атомов С, кетоном, содержащим от 2 до 8 атомов С, О-алкилом, содержащим от 1 до 12 атомов С, О-алкенилом, содержащим от 2 до 12 атомов С, О-арилом, содержащий от 5 до 20 атомов С, эфиром, содержащим от 2 до 12 атомов С, эфиром карбоновой кислоты, содержащим от 1 до 12 атомов С, амидом карбоновой кислоты, содержащим от 1 до 12 атомов С, где предпочтительно атом С карбоксамидной группы связан с указанными замещенными моноциклическими или полициклическими ароматическими остатками или замещенными моноциклическими или полициклическими, гетеро-атомными остатками, алкилом, содержащим от 1 до 12 атомов С, алкенилом, содержащим от 2 до 12 атомов С, циклоалкилом, содержащим от 3 до 12 атомов С, циклоалкенилом, содержащим от 3 до 12 атомов С, алкиларилом, содержащим от 1 до 12 атомов С, арилом, содержащим от 5 до 20 атомов С, или гетероарилом, который не содержит атом азота, содержат в составе заместителей от 4 до 40 атомов С.
В более предпочтительном варианте указанные замещенные моноциклические или полициклические ароматические остатки или замещенные моноциклические или полициклические, гетероатомные остатки, содержащие по меньшей мере один органический остаток W1, или один органический остаток W1a, или один органический остаток W1b, или один органический остаток W1c, и/или содержащие галоген, нитро, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, алкил, содержащий от 1 до 12 атомов С, алкенил,
содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, цикло-алкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, или гетероарил, который не содержит атом азота, содержат в составе заместителей от 4 до 40 атомов С.
В предпочтительном варианте указанный один замещенный или незамещенный моноциклический или полициклический ароматический остаток содержит по меньшей мере 5 атомов кольца, предпочтительно от 5 до 16, более предпочтительно, от 6 до 14, более предпочтительно, от 6 до 10, которые, соответственно, содержат по меньшей мере 1 атом углерода и по меньшей мере один, предпочтительно, от 1 до 2, атомов кислорода, которые более предпочтительно не находятся в соседних положениях.
В предпочтительном варианте в соединении формулы (1) и/или соединении формулы (2), и/или соединении формулы (3а), остаток Q1, или в соединении формулы (100) и/или соединении формулы (102), остаток Q3 представляет собой ароматический остаток с общей формулой (11а), (12а), (13а), (14а), (15а), (16а), (17а), (18а) или (19а):
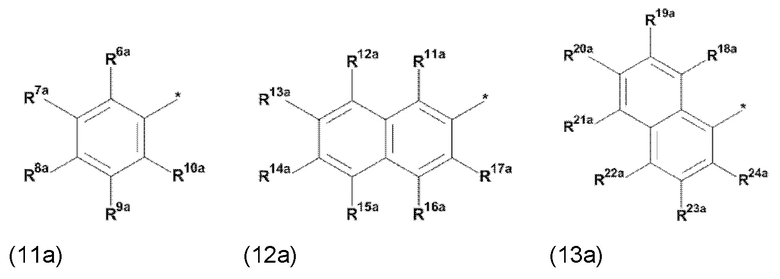
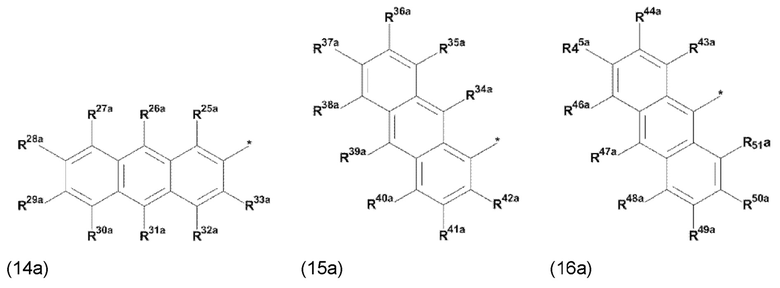
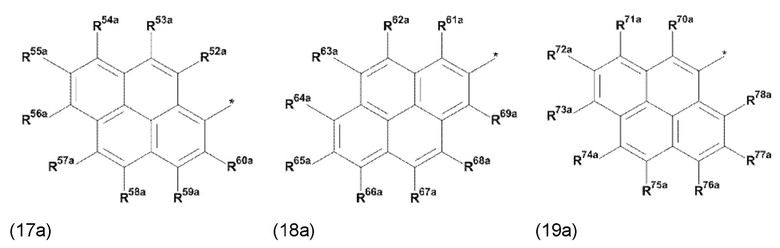
где в соединении формулы (1), и/или соединении формулы (2), и/или соединении формулы (3а), остаток Q2 или в соединении формулы (100) и/или в соединении формулы (102), остаток Q4 представляет ароматический остаток с общей формулой (11b), (12b), (13b), (14b), (15b), (16b), (17b), (18b) или (19b):
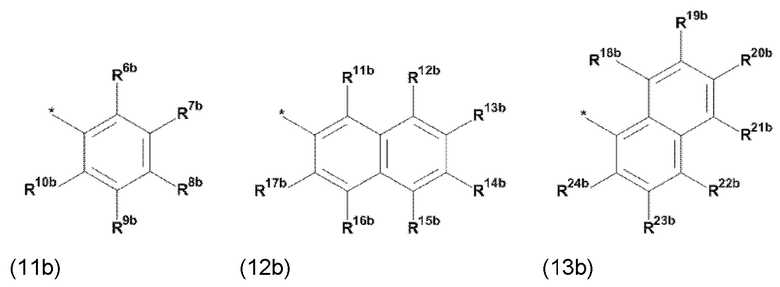
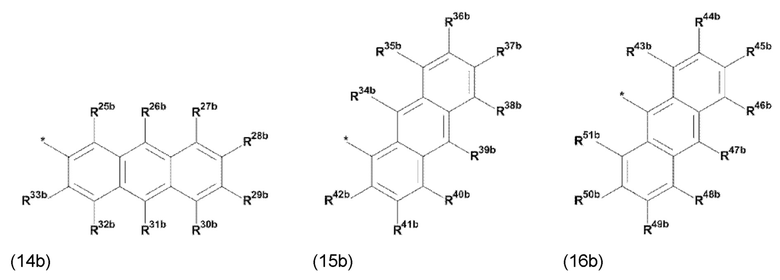
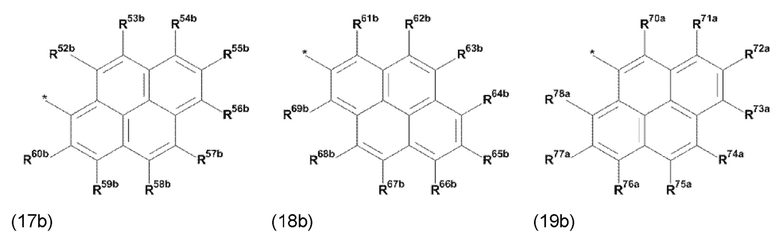
где соответственно по меньшей мере 1, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 остатков R6a - R10a, R11a - R17a, R18a - R24a, R25a - R33a , R34a - R42a, R43a - R51a R52a - R60a, R61a - R69a, R70a - R78a, R6b - R10b, R11b - R17b, R18b - R24b, R25b - R33b, R34b - R42b, R43b - R51b, R52b - R60b, R61b - R69b или R70b - R78b, соответственно, независимо от других представляют собой собой органический остаток W1 или органический остаток W1 а, органический остаток W1b, или органический остаток W1c, и
где остатки R6a - R10a, R11a - R17a, R18a - R24a, R25a - R33a, R34a - R42a, R43a - R51a, R52a -R60a R61a - R69a, R70a - R78a, R6b - R10b, R11b - R17b R18b - R24b, R25b - R33b R34b - R42b, R43b - R51b, R52b - R60b, R61b - R69b или R70b - R78b, которые не являются органическим остатком W1, оили органическим остатком W1a, или органическим остатком W1b, или органическим остатком W1c, соответственно, независимо от других, являются идентичными или разными и представляют водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, амид карбоновой кислоты, содержащий от 1 до 12 атомов С, где, предпочтительно, соответственно атом С карбоксамидной группы связан с одним из остатков Q1 - Q4, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С, предпочтительно, водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С.
В более предпочтительном варианте остаток Q1 или остаток Q3 представляет собой ароматический остаток с общей формулой (11а), (12а) или (13а)
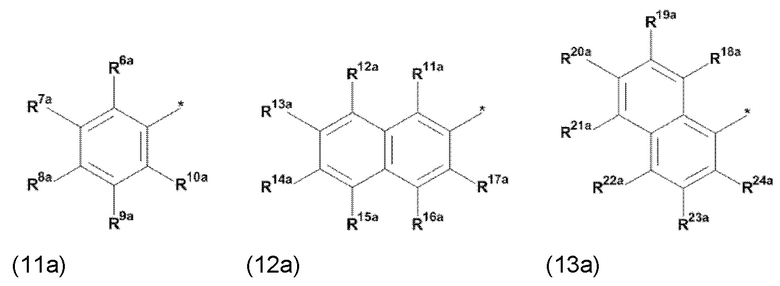
и остаток Q2 или остаток Q4 представляет собой ароматический остаток с общей формулой (11b), (12b) или (13b),
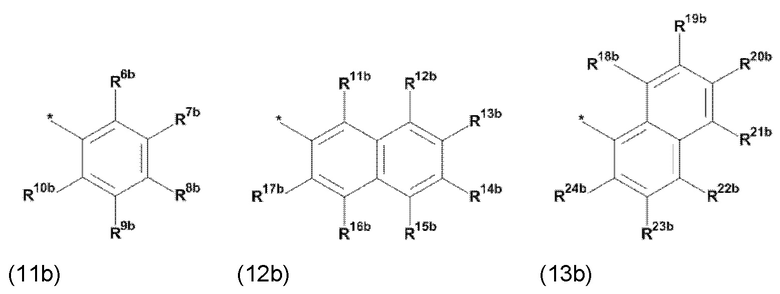
где, соответственно, по меньшей мере 1, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 остатков R6a - R10a, R11a - R17a, R18a - R24a, R6b - R10b, R11b - R17b или R18b - R24b, соответственно, независимо от других, представляет собой органический остаток W1, или органический остаток W1a, или органический остаток W1b, или органический остаток W1c, аиnd где остатки R10a, R11a - R17a, R18a - R24a, R6b - R10b, R11b - R17b и R18b - R24b, которые не являются органическим остатком W1, или органическим остатком W1a, или органическим остатком W1b, или органическим остатком W1c, соответственно, независимо от других, являются идентичными или разными и представляют водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, амид карбоновой кислоты, содержащий от 1 до 12 атомов С, где, предпочтительно, соответственно, атом С карбоксамидной группы связан с одним из остатков Q1 - Q4, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С, предпочтительно, водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С.
В предпочтительном варианте в соединении формулы (3), остатки Q1 и Q1a, или в соединении формулы (101), остатки Q3 и Q3a, соответственно, независимо от других, представляют собой ароматический остаток с общей формулой (11а), (12а), (13а), (14а), (15а), (16а), (17а), (18а) или (19а):
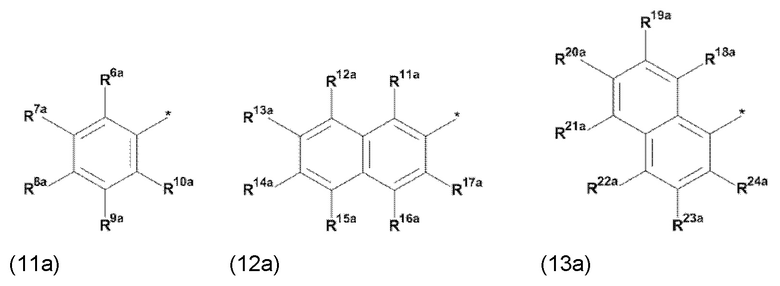
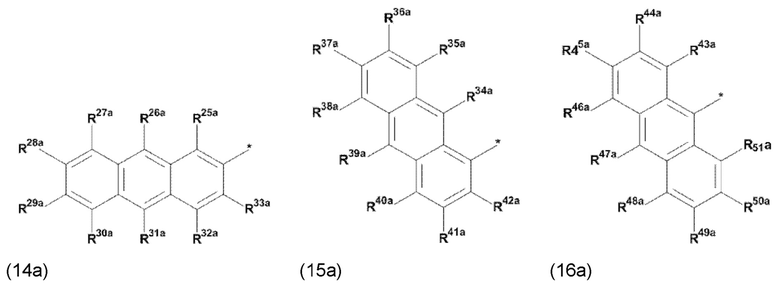
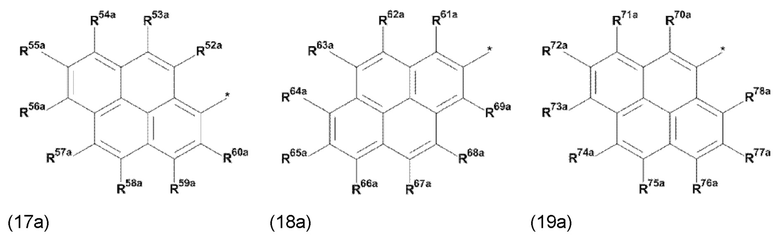
и где в соединении формулы (3) остатки Q2 и Q2a, или в соединении формулы (101) остатки Q4 и Q4a, соответственно, независимо от других, представляют ароматический остаток с общей формулой (11b), (12b), (13b), (14b), (15b), (16b), (17b), (18b) или (19b):
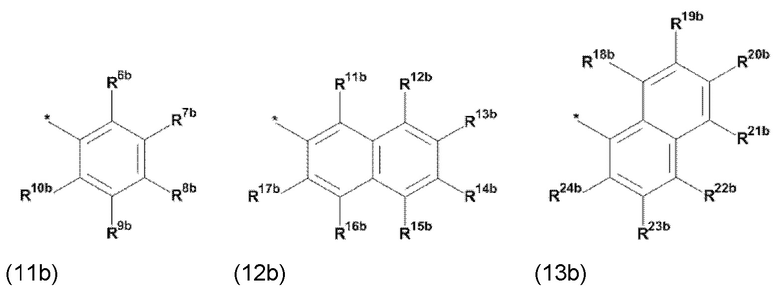
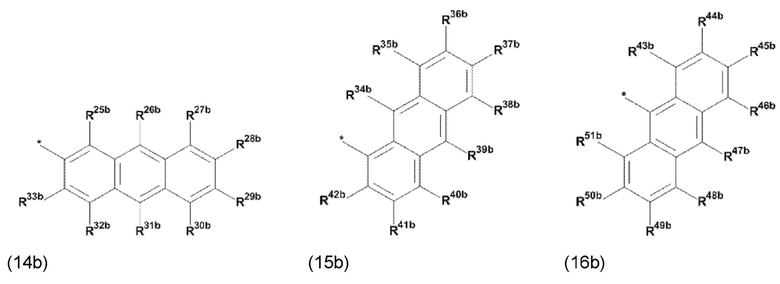
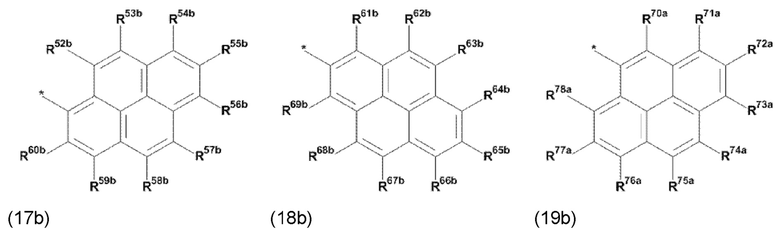
где, соответственно, по меньшей мере 1, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 остатков R6a - R10a, R11a - R17a, R18a - R24a, R25a - R33a, R34a - R42a, R43a - R51a, R52a - R60a, R61a - R69a R70a - R78a R6b - R10b, R11b - R17b, R18b - R24b, R25b - R33b, R34b - R42b, R43b - R51b, R52b - R60b, R61b - R69b или R70b - R78b, соответственно, независимо от других, представляет собой органический остаток W1, или органический остаток W1 а, или органический остаток W1b, или органический остаток W1c, и
где остатки R6a - R10a, R11a - R17a, R18a - R24a, R25a - R33a, R34a - R42a, R43a - R51a, R52a - R60a R61a - R69a, R70a - R78a, R6b - R10b R11b - R17b, R18b - R24b, R25b - R33b, R34b - R42b, R43b - R51b, R52b - R60b, R61b - R69b или R70b - R78b, которые не являются органическим остатком W1, или органическим остатком W1a, или органическим остатком W1b, или органическим остатком W1c, соответственно, независимо от других являются идентичными или разными и представляют водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, амид карбоновой кислоты, содержащий от 1 до 12 атомов С, где предпочтительно, соответственно, атом С карбоксамидной группы связан с одним из остатков Q1 - Q4a, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С, предпочтительно водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С.
В более предпочтительном варианте в соединении формулы (3), остатки Q1 и Q1a, или, в соединении формулы (101), остатки Q3 и Q3a, соответственно, независимо от других, представляют собой ароматический остаток с общей формулой (11а), (12а) или (13а):
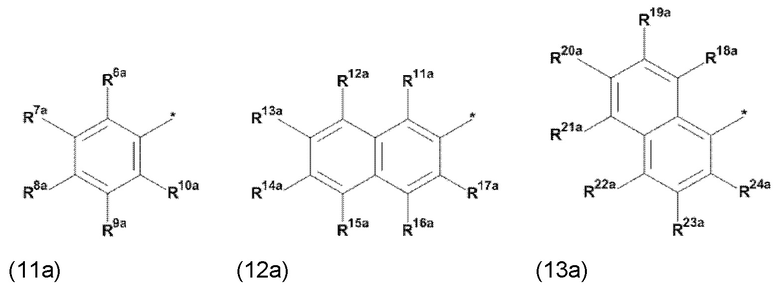
и где в соединении формулы (3), остатки Q2 и Q2a, или, в соединении формулы (101), остатки Q4 и Q4a, соответственно, независимо от других, представляют собой ароматический остаток с общей формулой (11b), (12b) или (13b):
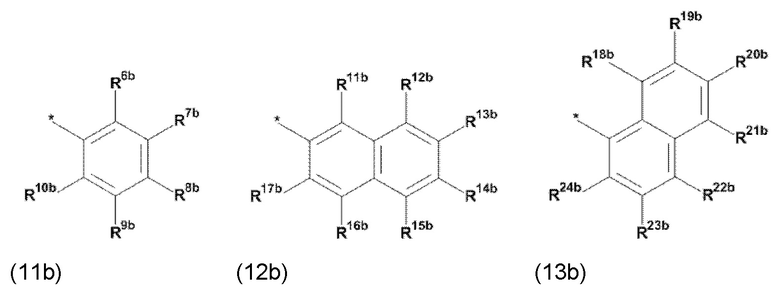
где, соответственно, по меньшей мере 1, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 остатков R6a - R10a, R11a - R17a, R18a - R24a, R6b - R10b, R11b - R17b или R18b - R24b, соответственно, независимо от других, представляет собой органический остаток W1, или органический остаток W1a, или органический остаток W1b, или органический остаток W1c, где
остатки R10a, R11a - R17a, R18a - R24a, R6b - R10b, R11b - R17b и R18b - R24b, которые не являются органическим остатком W1, или органическим остатком W1a, или органическим остатком W1b, или органическим остатком W1c, соответственно, независимо от других, являются идентичными или разными и представляют водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, амид карбоновой кислоты, содержащий от 1 до 12 атомов С, где предпочтительно, соответственно, атом С карбоксамидной группы связан с одним из остатков Q1 - Q4a, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С, предпочтительно водород, галоген, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов С, кетон, содержащий от 2 до 8 атомов С, О-алкил, содержащий от 1 до 12 атомов С, О-алкенил, содержащий от 2 до 12 атомов С, О-арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, эфир карбоновой кислоты, содержащий от 1 до 12 атомов С, алкил, содержащий от 1 до 12 атомов С, алкенил, содержащий от 2 до 12 атомов С, циклоалкил, содержащий от 3 до 12 атомов С, циклоалкенил, содержащий от 3 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов С.
В альтернативном варианте реализации варианта (b) соединения формулы (1), и/или соединения формулы (2), и/или соединения формулы (3), и/или соединения формулы (3а), по меньшей мере один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно, общую формулу (5b), (7b) или (9b):
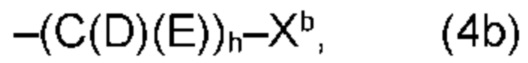
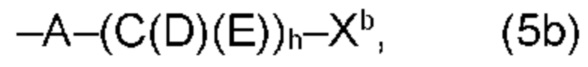
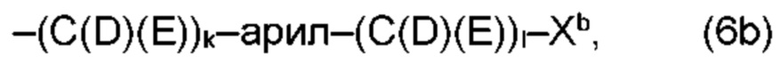
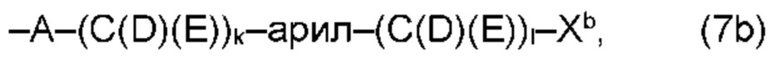
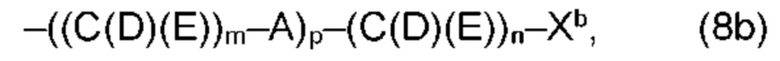
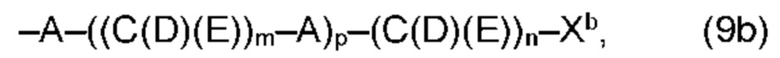
где, необязательно, по меньшей мере один из остатков Q1 и Q2, предпочтительно каждый из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один, предпочтительно, от 1 до 9, более предпочтительно, от 1 до 7, более предпочтительно, от 1 до 5, более предпочтительно, от 1 до 4, более предпочтительно, от 2 до 3 органических остатков W1b с общей формулой (4b), (5b), (6b), (7b), (8b) или (9b), предпочтительно с общей формулой (5b), (7b) или (9b),
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, предпочтительно, кислород, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, предпочтительно (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, где указанный по меньшей мере один нейтральный атом азота, который может быть протонирован, не является амино-остатком (-NH2), и где указанный по меньшей мере один положительно заряженный атом азота не является протонированным амино-остатком (-NH3+) и не является гуанилатным остатком.
В предпочтительном варианте В альтернативном варианте реализации варианта (b) соединения формулы (1), и/или соединения формулы (2), и/или соединения формулы (3), и/или соединения формулы (3а), органический остаток Xb, соответственно, независимо от других, представляет собой остаток формулы (20а), (20b), (21), (22а), (22b), (23а), (23b) или (24), предпочтительно, остаток формулы (20а), (20b), (21) или (24), предпочтительно, остаток формулы (20а), (20b) или (21):
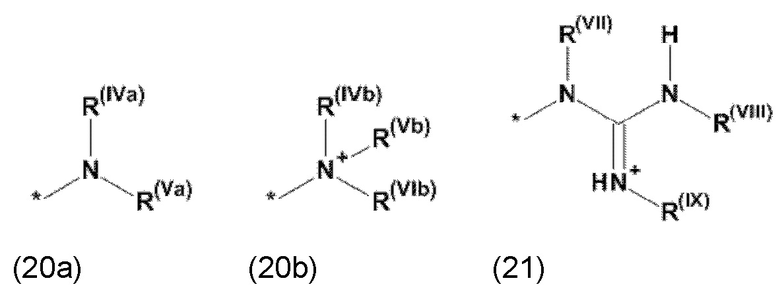
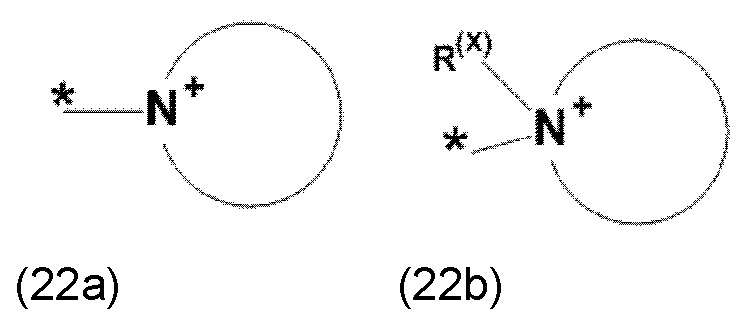
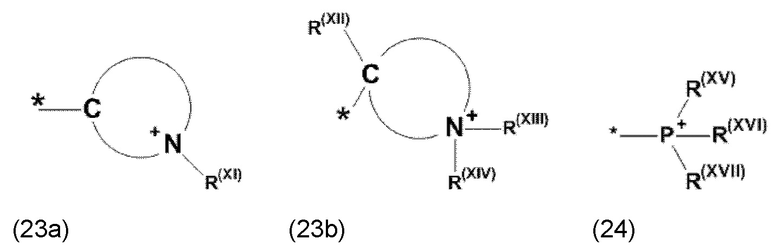
где каждый из остатков R(IVa), R(IVb), R(X), R(XI), R(XII), R(XIII), и R(XIV), предпочтительно каждый из остатков R(iva) и r(ivb), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где каждый из остатков R(Va), R(Vb), R(VIb), R(VII), R(VIII), R(XV), и R(XVII) предпочтительно каждый из R(IVa), R(Vb), R(VIb),R(XV), R(XVI), R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остаток формулы (22а) и остаток формулы (23а):
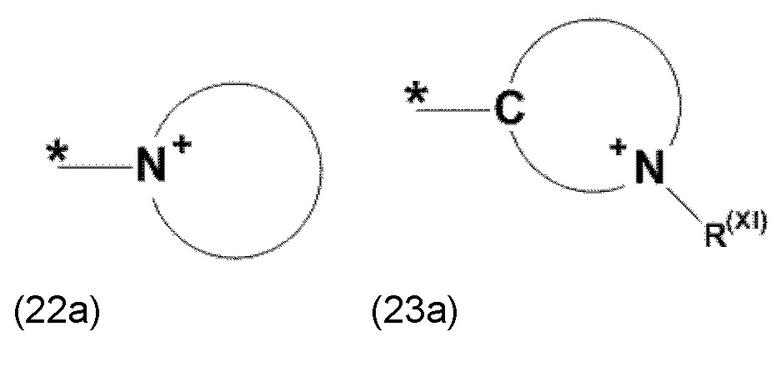
представляет замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует двойную связь, и
где остаток формулы (22b) и остаток формулы (23b):
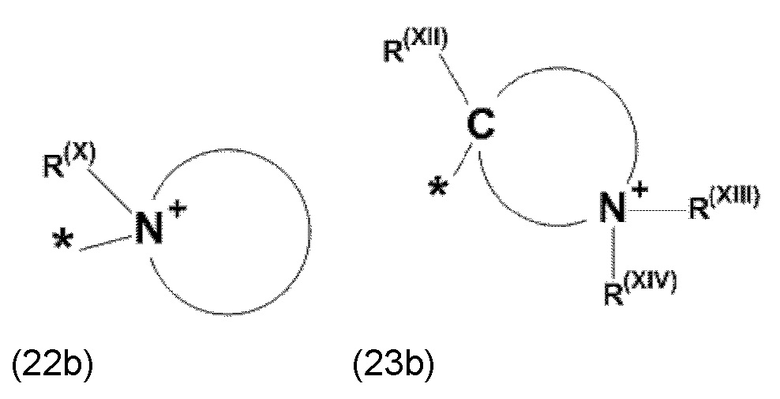
представляют замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует одинарную связь.
В одном из предпочтительных вариантов реализации соединения формулы (100), соединения формулы (101), и/или соединения формулы (103), органический остаток X, соответственно, независимо от других, представляет собой остаток формулы (20а), (20b), (21), (22а), (22b), (23а), (23b) или (24), предпочтительно, остаток формулы (20а), (20b) или (21):
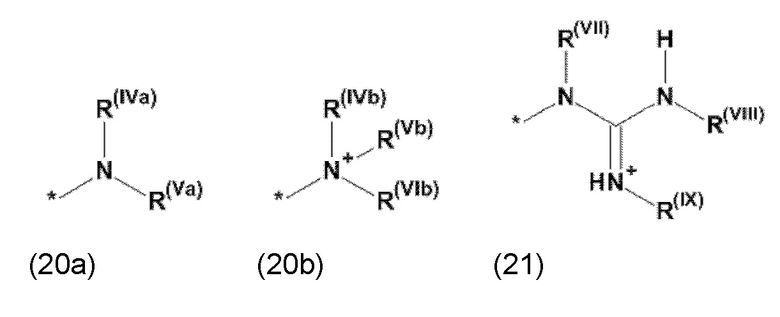
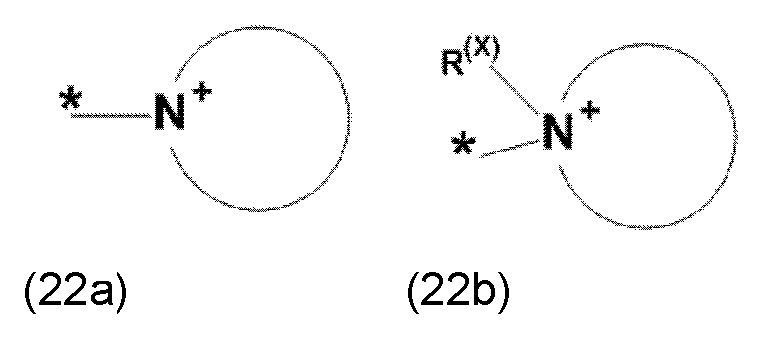
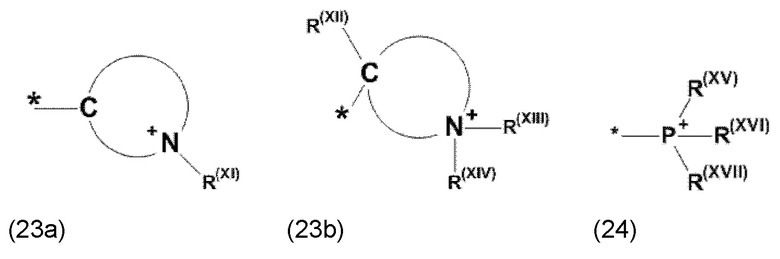
где каждый из остатков R(IVa), R(Va), R(IVb), R(Vb), R(VIb), R(VII), R(VIII), R(IX), R(X), R(XI), R(XII), R(XIII), и R(XIV) соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остаток формулы (22а) и остаток формулы (23а):
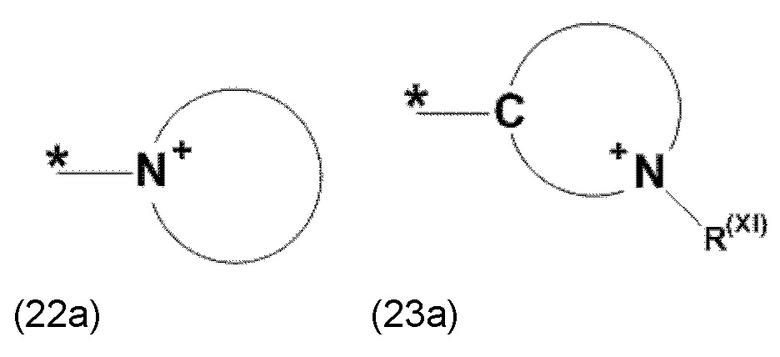
представляет замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует двойную связь, и
где остаток формулы (22b) и остаток формулы (23b):
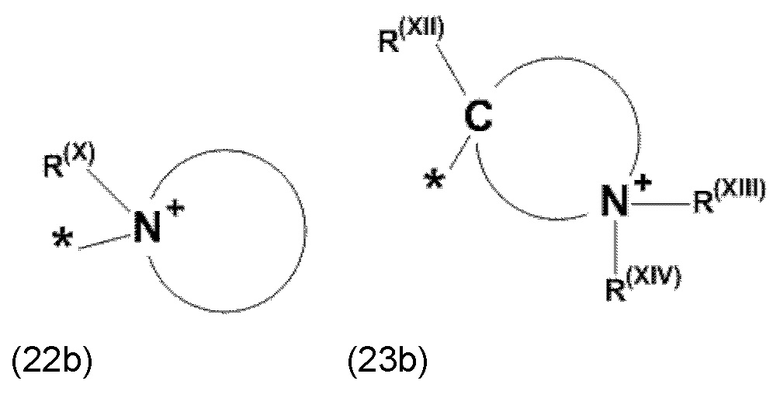
представляет замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует одинарную связь.
В одном из предпочтительных вариантов реализации соединения формулы (1), соединения формулы (2), и/или соединения формулы (3), органический остаток Xb и/или Xc, соответственно, независимо от других, представляет собой остаток формулы (20а), (20b), (21), (22а), (22b), (23а), (23b) или (24):
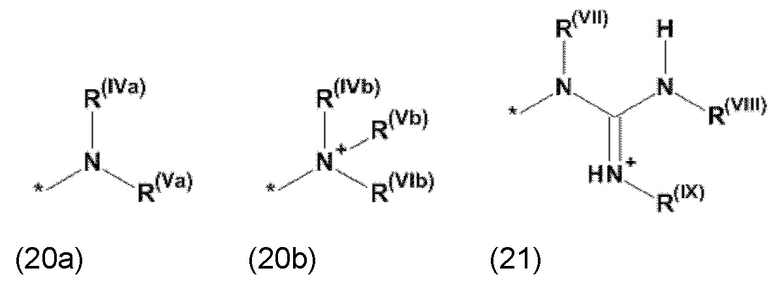
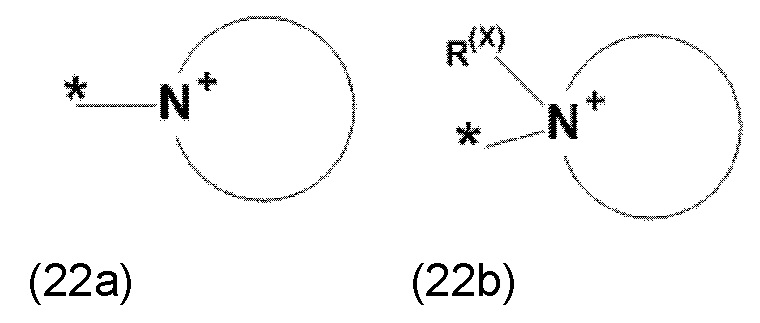
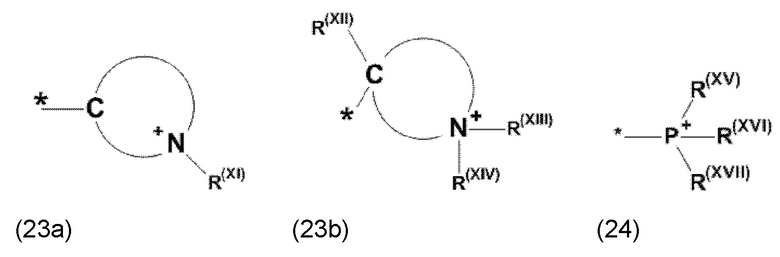
где каждый из остатков R(IVa), R(Va), R(IVb), R(Vb), R(VIb), R(VII), R(VIII), R(IX), R(X), R(XI), R(XII), R(XIII), и R(XIV) соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остаток формулы (22а) и остаток формулы (23а):
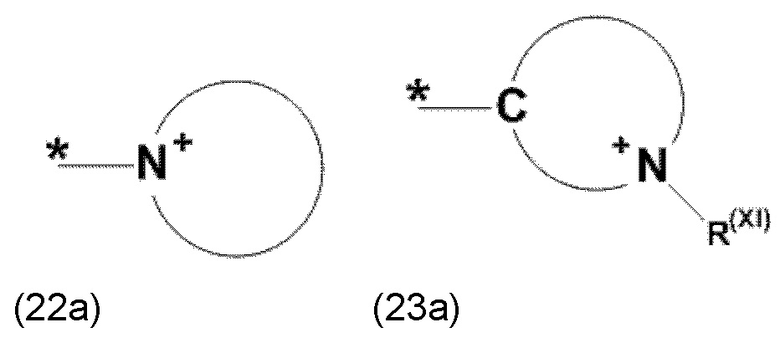
представляет замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует двойную связь, и
где остаток формулы (22b) и остаток формулы (23b):
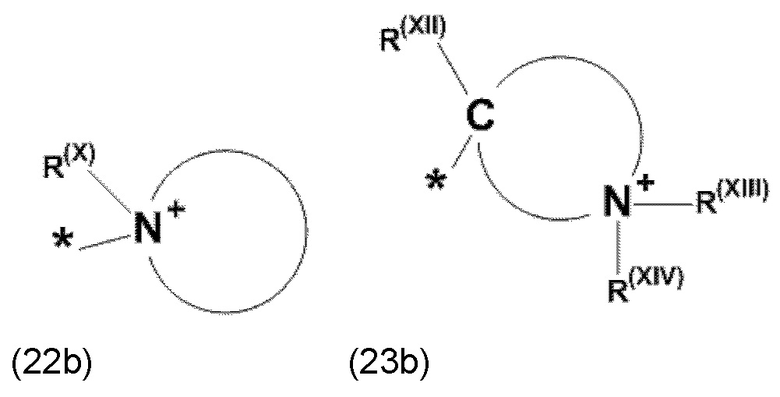
представляет замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует одинарную связь.
В более предпочтительном варианте каждый остаток формулы (23а) выбран из группы, состоящей из остатков с формулами (25а), (25b) и (25с):
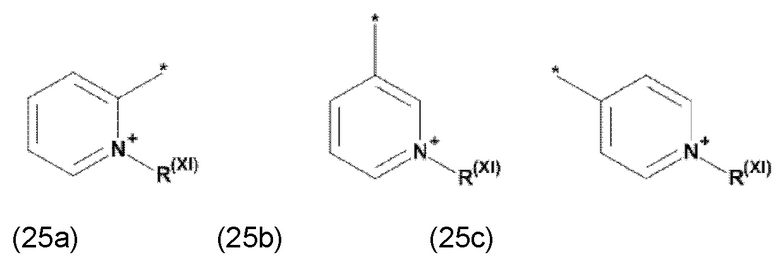
где R(XI) могут, соответственно, представлять собой арильный остаток, содержащий от 5 до 20 атомов С, например, фенил или бензил, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 20 атомов С, например, метил, этил, н-пропил, изо-пропил, н-бутил или трет-бутил, алкенильный остаток, который может быть линейным или разветвленным, содержащим от 2 до 20 атомов С, гидроксиалкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 20 атомов С, например, гидроксиметил, 2-гидроксиэтил, 3-гидроксипропил или 1-гидрокси-1-метилэтил, или этиловый остаток, который может быть линейным или разветвленным, содержащим от 2 до 20 атомов С, например, метоксиметил, метоксиэтил, метоксипропил, этоксиметил, этоксиэтил, этоксипропил, пропоксиметил, пропоксиэтил или пропоксипропил.
В более предпочтительном варианте реализации каждый остаток формулы (22а) выбран из группы, состоящей из остатков формулы (26):
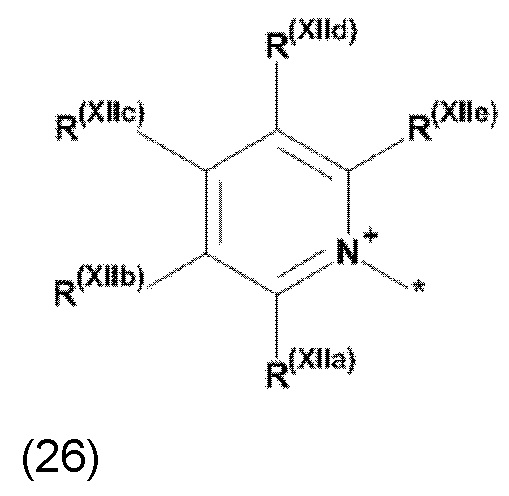
где остатки R(XIIa) - R(XIIe) соответственно, независимо от других, могут представлять собой водород, арильный остаток, содержащий от 5 до 20 атомов С, например, фенил или бензил, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 20 атомов С, например, метил, этил, н-пропил, изо-пропил, н-бутил или трет-бутил, алкенильный остаток, который может быть линейным или разветвленным, содержащим от 2 до 20 атомов С, гидроксиалкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 20 атомов С, например, гидроксиметил, 2-гидроксиэтил, 3-гидроксипропил или 1-гидрокси-1-метил-этил, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 2 до 20 атомов С, например, метоксиметил, метоксиэтил, метоксипропил, этоксиметил, этоксиэтил, этоксипропил, пропоксиметил, пропоксиэтил или пропоксипропил. В предпочтительном варианте остатки R(XIIa) - R(XIIe) соответственно, независимо от других, представляют собой водород, метил, этил, проп-1-ил, бут-1-ил, пент-1-ил, гекс-1-ил, гепт-1- или окт-1-ил.
В более предпочтительном варианте реализации остаток формулы (21b) представляет собой 1-метилпирролидин-1-ий-1-ил, 1-метилпиперазин-1-ий-1-ил или 4-метилморфолин-4-ий-4-ил.
В более предпочтительном варианте реализации соединения формулы (100), соединения формулы (101), и/или соединения формулы (103) органический остаток X, соответственно, независимо от других, представляет собой остаток формулы (20с), (20d), (21) или (24), предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
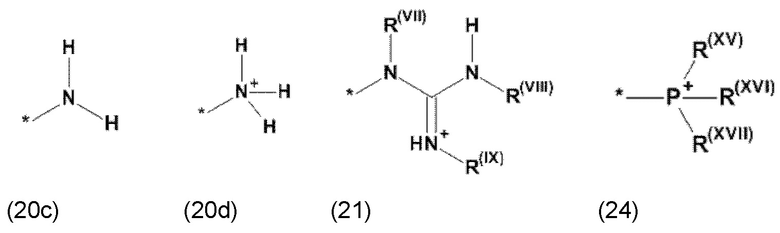
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно водород, и где каждый из остатков R(XV), R(XVI) и R(XVII)), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, предпочтительно арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, или алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С.
В более предпочтительном варианте реализации в соединении формулы (100), соединении формулы (101) и/или соединении формулы (103), остатки R(IVa), R(Va), R(IVb), R(Vb), R(VIb), R(VII), R(VIII), R(IX), R(X), R(XI), R(XII), R(XIII), R(XIV), R(XV), R(XVI) и R(XVII) независимо от других выбраны из водорода и алкильных групп с общей формулой -(СН2)n-СН3, где n представляет собой целое число от 0 до 19, предпочтительно, от 1 до 17.
В более предпочтительном варианте реализации в соединении формулы (1), и/или соединении формулы (2), и/или соединении формулы (3), и/или соединении формулы (3а), и/или соединении формулы (100), и/или соединении формулы (101), и/или соединении формулы (102) остатки R(IVa), R(Va), R(IVb), R(Vb), R(VIb), R(VII), R(VIII), R(IX), R(X), R(XI), R(XII), R(XIII) и R(XIV) независимо от других выбраны из группы, которая состоит из водорода, метила, этила, проп-1-ила, проп-2-ила, бут-1-ила, бут-2-ила, 2-метилпроп-1-ила, 2-метилпроп-2-ила, пент-1-ила, пент-2-ила, пент-3-ила, 2-метилбут-1-ила, 2-метилбут-2-ила, 2-метилбут-3-ила, 2-метилбут-4-ила, 2,2-диметилпроп-1-ила, гекс-1-ила, гекс-2-ила, гекс-3-ила, гепт-1-ила, окт-1-ила, 2-метилпент-1-ила, 2-метилпент-2-ила, 2-метилпент-3-ила, 2-метилпент-4-ила, 2-метилпент-5-ила, 3-метилпент-1-ила, 3-метилпент-2-ила, 3-метилпент-3-ила, 2,2-диметилбут-1-ила, 2,2-диметилбут-3-ила, 2,2-диметилбут-4-ила, 2,3-диметилбут-1-ила, 2,3-диметилбут-2-ила, фенила и бензила.
В особенно предпочтительном варианте реализации производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), формулы (2), формулы (3) и/или формулы (3а), а также производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100), формулы (101) и/или формулы (102) для применения в соответствии с настоящим изобретением, остатки R(XV), R(XVI) и R(XVII)) соатвтка формулы (24),
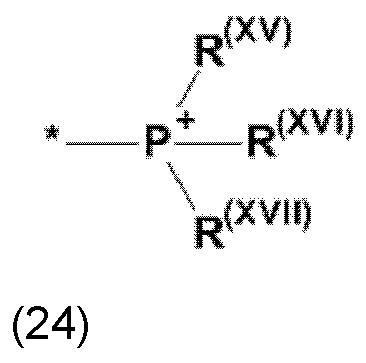
независимо от других выбраны из метила, этила, проп-1-ила, проп-2-ила, бут-1-ила, бут-2-ила, 2-метилпроп-1-ила, 2-метилпроп-2-ила, пент-1-ила, пент-2-ила, пент-3-ила, 2-метилбут-1-ила, 2-метилбут-2-ила, 2-метилбут-3-ила, 2-метилбут-4-ила, 2,2-диметилпроп-1-ила, гекс-1-ила, гекс-2-ила, гекс-3-ила, гепт-1-ила, окт-1-ила, 2-метилпент-1-ила, 2-метилпент-2-ила, 2-метилпент-3-ила, 2-метилпент-4-ила, 2-метилпент-5-ила, 3-метилпент-1-ила, 3-метилпент-2-ила, 3-метилпент-3-ила, 2,2-диметилбут-1-ила, 2,2-диметилбут-3-ила, 2,2-диметилбут-4-ила, 2,3-диметилбут-1-ила и 2,3-диметилбут-2-ила, фенила и бензила.
В более предпочтительном варианте реализации соединения формулы (100), соединения формулы (101) и/или соединения формулы (103) остатки R(IVa), R(Va), R(IVb), R(Vb), R(VIb), R(VII), R(VIII), R(IX), R(X), R(XI), R(XII), R(XIII), R(XIV), R(XV), R(XVI) и R(XVII)) независимо от других выбраны из водорода или остатка формулы (10):
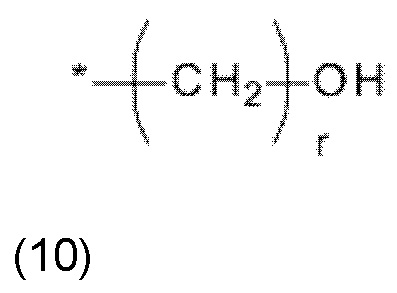
где, соответственно, r представляет целое число от 1 до 20, предпочтительно, от 1 до 8, более предпочтительно, от 1 до 4.
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гепта-диен-3,5-диона формулы (100), и/или формулы (101), и/или формулы (102) органический органический остаток W2 и/или W1, соответственно, независимо от других, представляют органический остаток с общей формулой (30а), (30b), (30с), (30d), (30е), (30f), (30g), (30h), (30i), (30k), (30m), (30n), (30p), (31а), (31b), (32), (33), (34), (35), (36), (37а) или (37b), предпочтительно органический остаток с общей формулой (30а), (30b), (30с), (30d), (30е), (30f), (30g), (30h), (30i), (30k), (30m), (30n), (30p), (31а), (31b), (32), (33), (34), (35) или (36), предпочтительно органический остаток с общей формулой (37а):
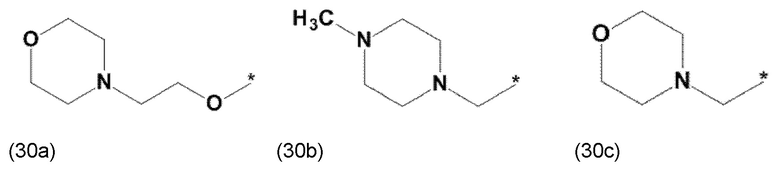
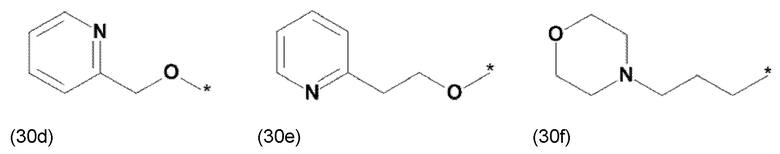
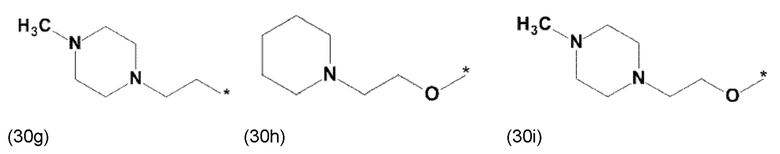
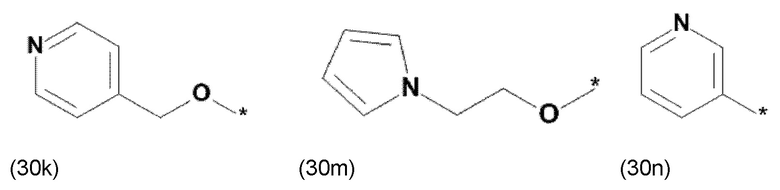
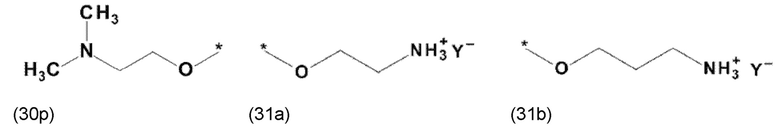
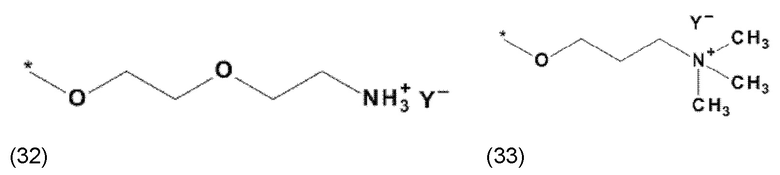
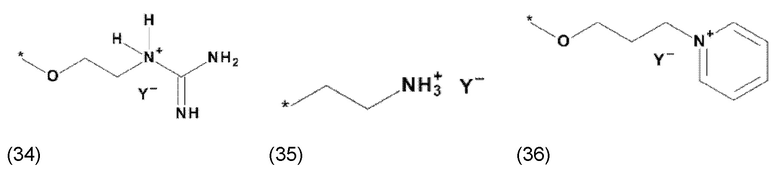
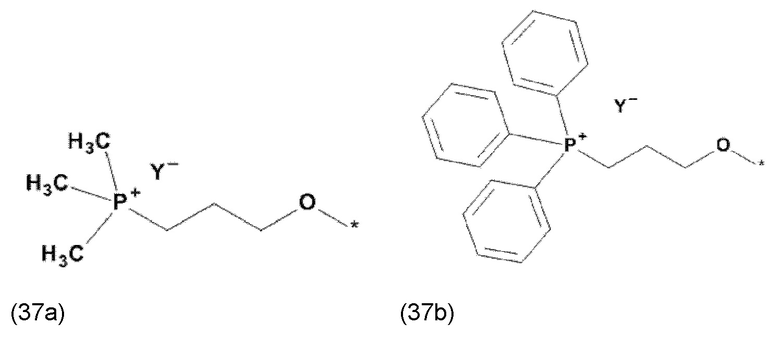
где Y- представляет собой анион, который, соответственно, независимо от других, представляет фторид, хлорид, бромид, йодид, сульфат, гидросульфат, фосфат, гидрофосфат, дигидрофосфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода. В предпочтительном варианте карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода независимо от других представляет собой формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат или цитрат.
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гепта-диен-3,5-диона согласно настоящему изобретению формулы (1), и/или формулы (2) и/или формулы (3), и/или формулы (3а) органический остаток W1a, соответственно, независимо от других, представляет органический остаток с общей формулой (31а), (31b), (32), (34), (37а) или (37b), предпочтительно органический остаток с общей формулой (31а), (31b), (32) или (34), предпочтительно органический остаток с общей формулой (37а):
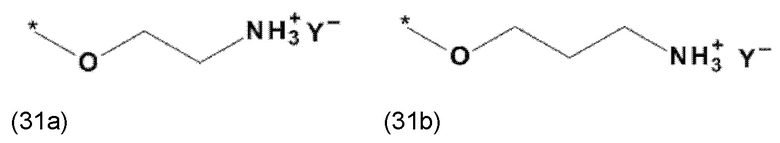
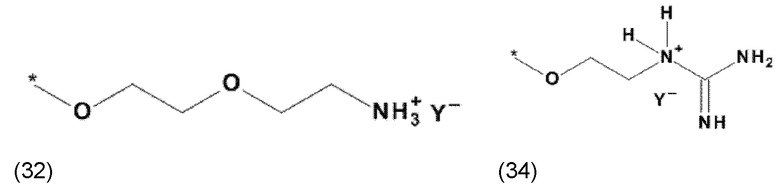
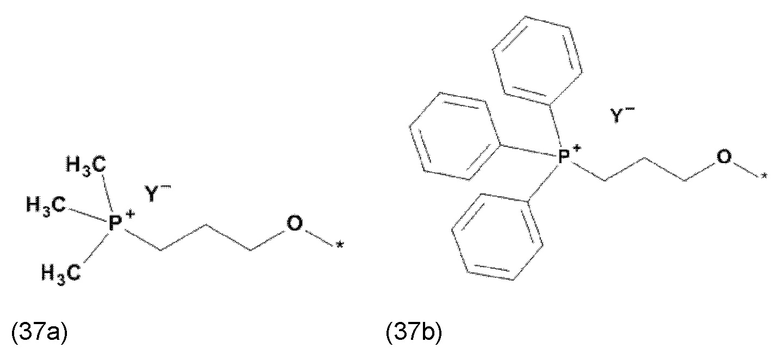
где Y- представляет собой анион, который, соответственно, независимо от других, представляет фторид, хлорид, бромид, йодид, сульфат, гидросульфат, фосфат, гидрофосфат, дигидрофосфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода. В предпочтительном варианте карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода, представляет собой, Независимо от других, формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат или цитрат.
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гепта-диен-3,5-диона согласно настоящему изобретению формулы (1), и/или формулы (2,) и/или формулы (3), и/или формулы (3а) органический остаток W2a, и/или W1b, и/или W1c, соответственно, независимо от других, представляют органический остаток с общей формулой (31а), (31b), (32), (34), (35), (37а) или (37b), предпочтительно, органический остаток с общей формулой (31а), (31b), (32), (34) или (35), предпочтительно органический остаток с общей формулой (37а):
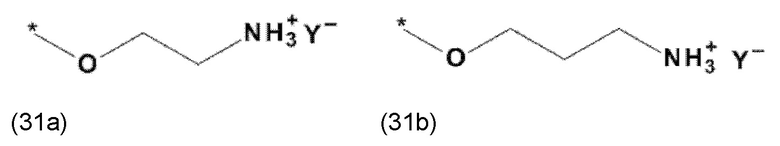
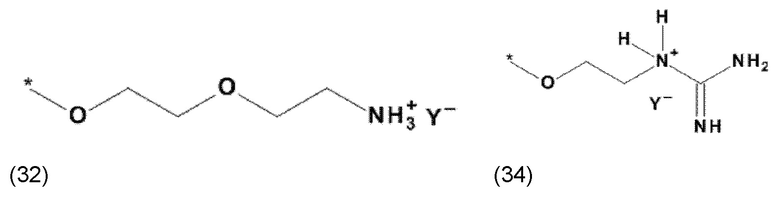
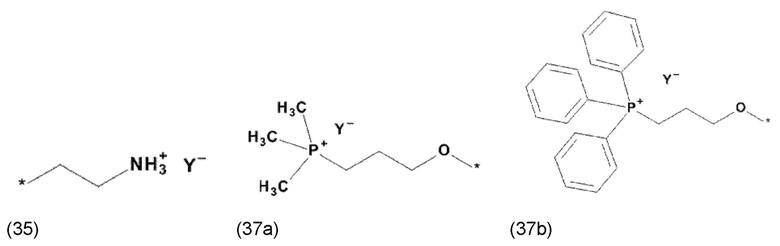
где Y- представляет собой анион, который, соответственно, независимо от других, представляет фторид, хлорид, бромид, йодид, сульфат, гидросульфат, фосфат, гидрофосфат, дигидрофосфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода. В предпочтительном варианте карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода, представляет собой, и независимо от других, формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат или цитрат.
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) для применения в соответствии с настоящим изобретением, указанное соединение представляет собой по меньшей мере одно соединение формулы (40)-(67), предпочтительно, по меньшей мере одно соединение формулы (40)-(63), (66) или (67), предпочтительно, соединение формулы (64):
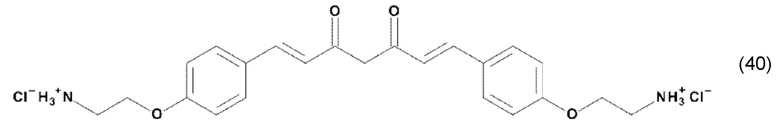
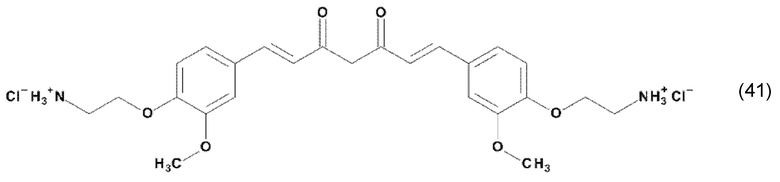
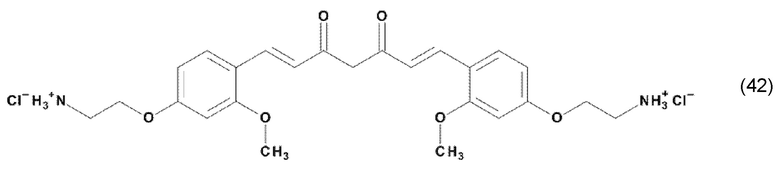
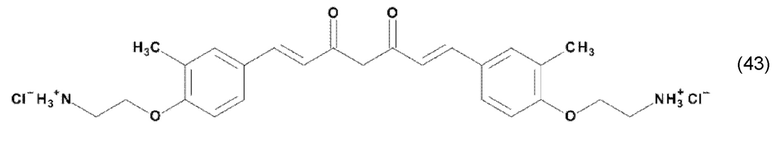
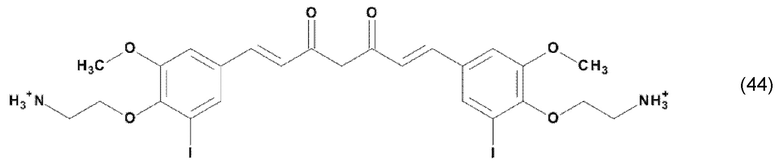
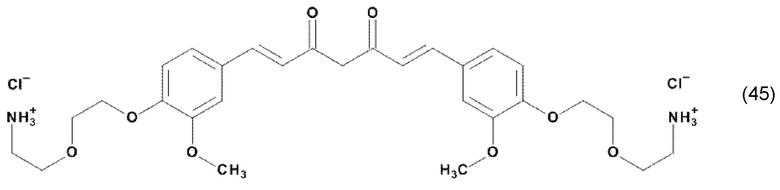
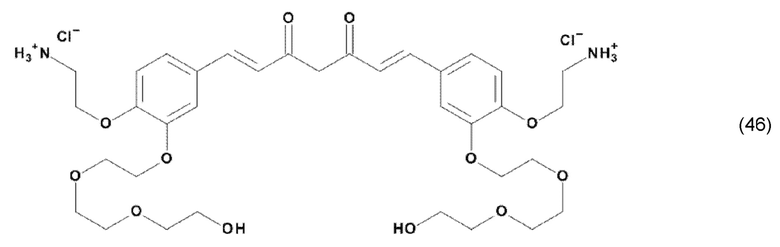
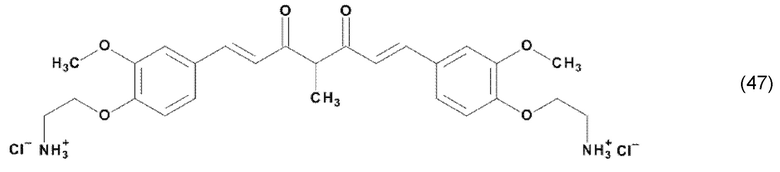
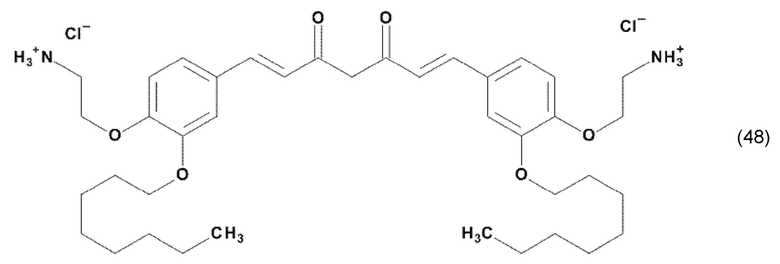
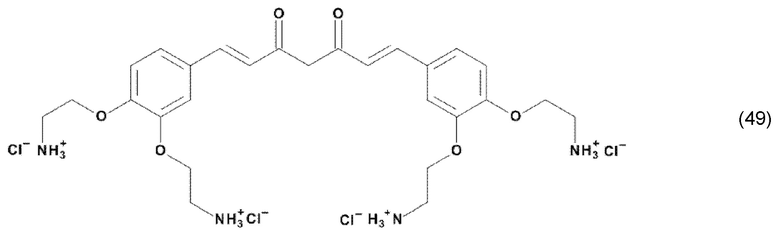
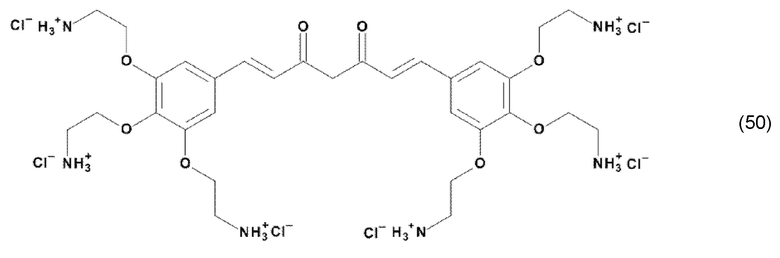
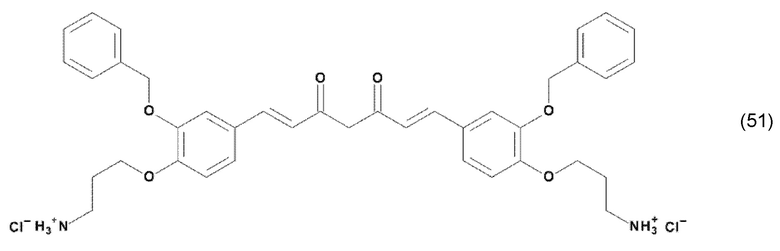
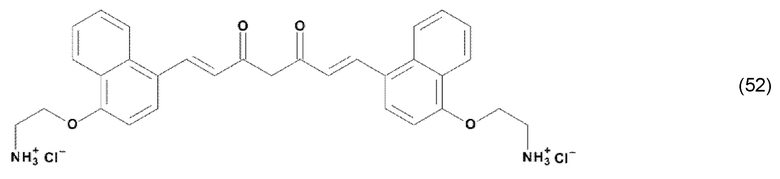
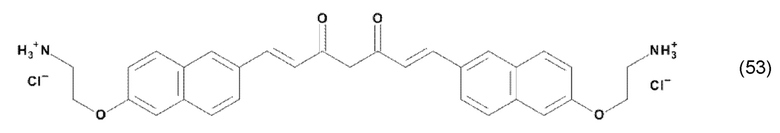
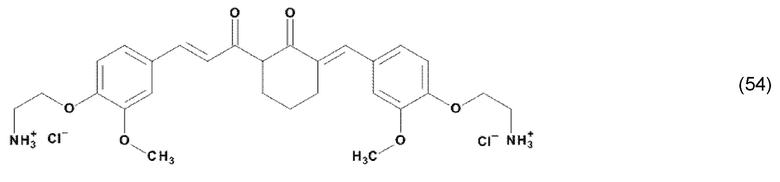
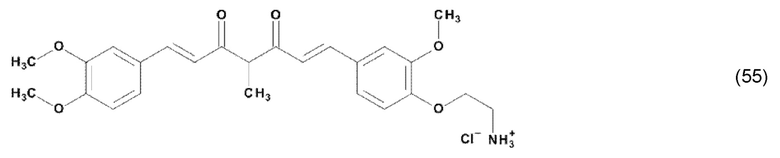
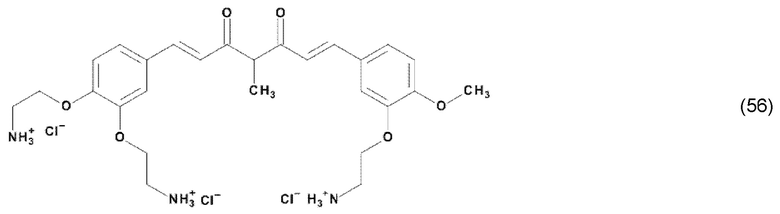
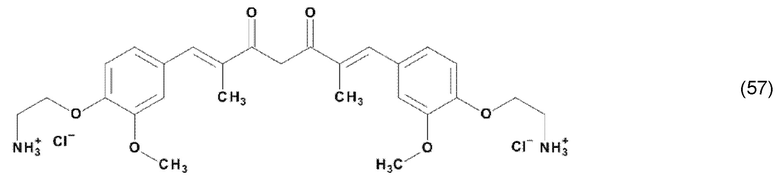
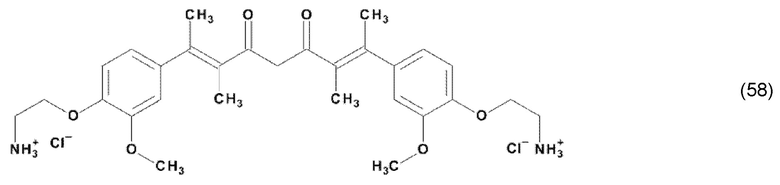
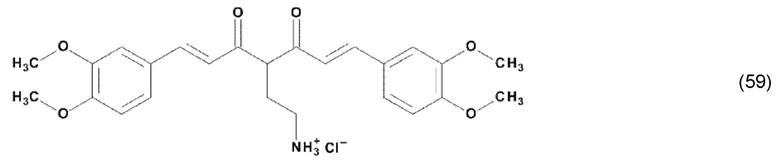
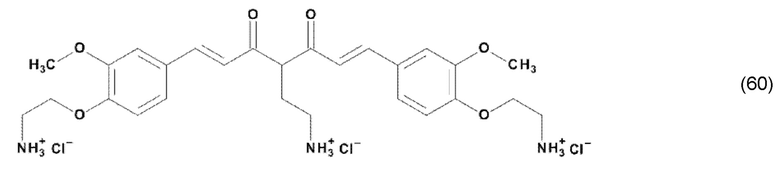
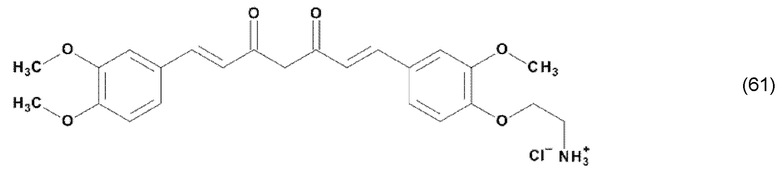
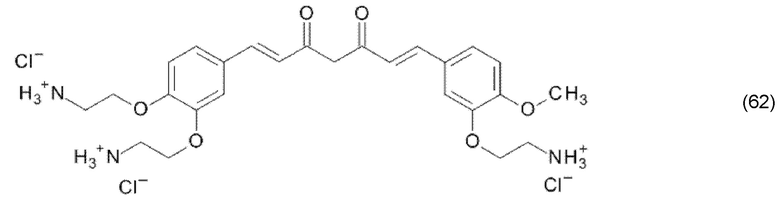
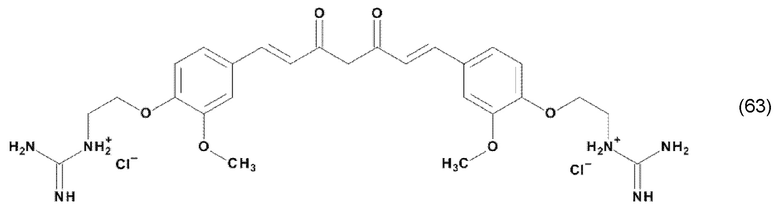
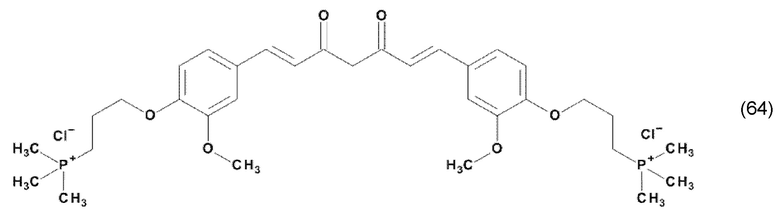
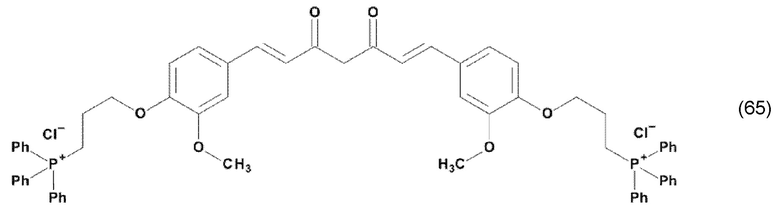
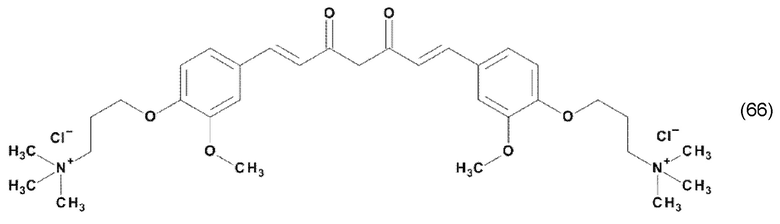
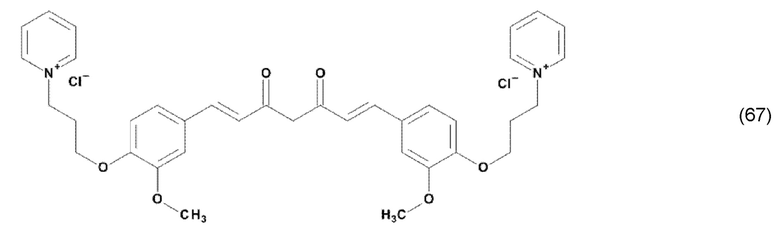
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100) для применения в соответствии с настоящим изобретением, указанное соединение представляет собой по меньшей мере одно соединение формулы (40)-(67) и (110)-(229).
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (1), указанное соединение представляет собой по меньшей мере одно соединение формулы (40)-(65), предпочтительно, по меньшей мере одно соединение формулы (40)-(62), предпочтительно, по меньшей мере одно соединение формулы (40)-(58), (60), (61), (62) или (63), предпочтительно, по меньшей мере одно соединение формулы (64):
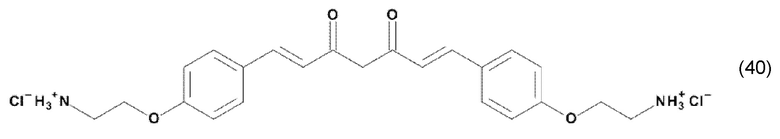
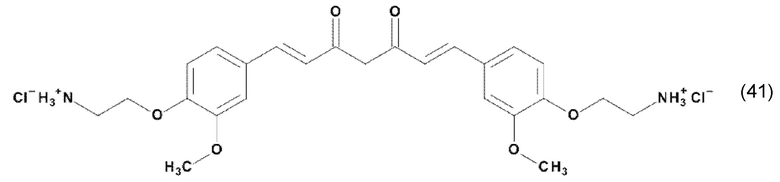
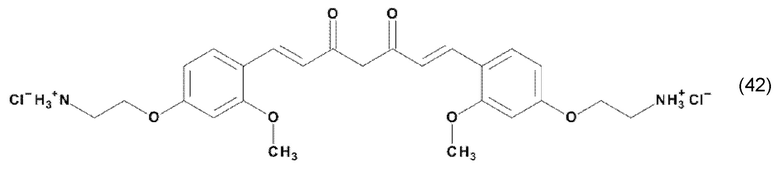
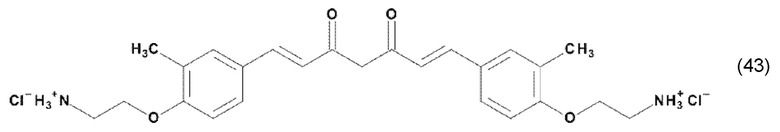
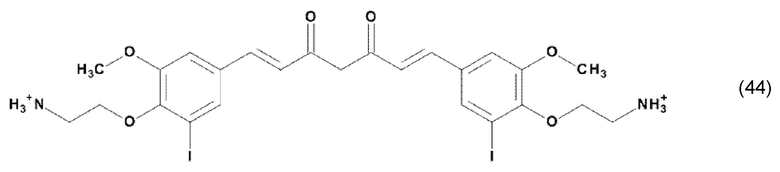
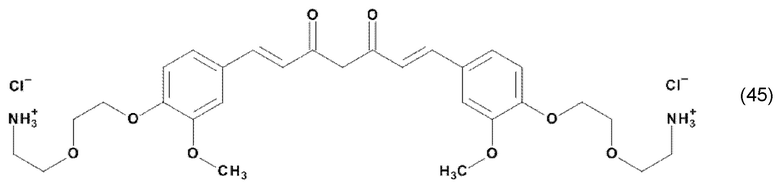
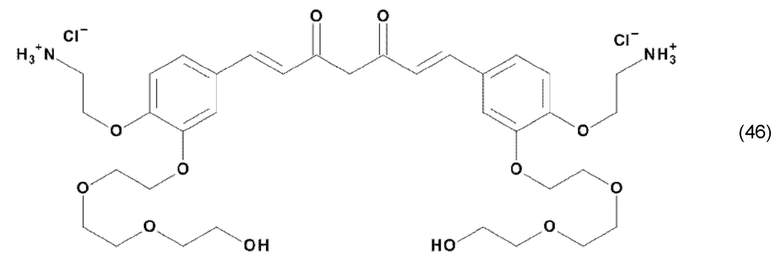
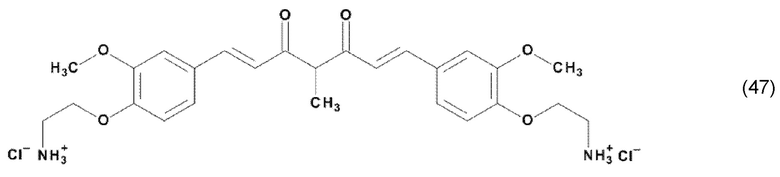
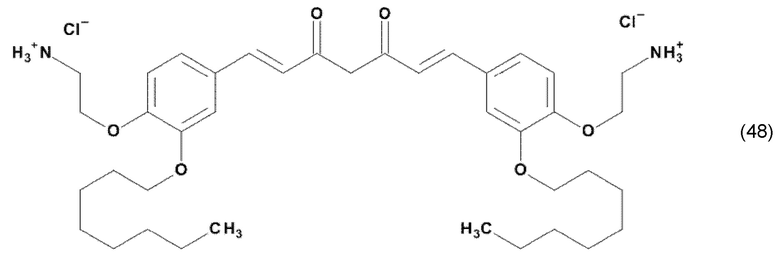
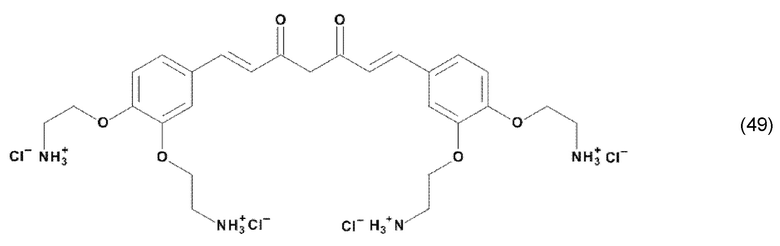
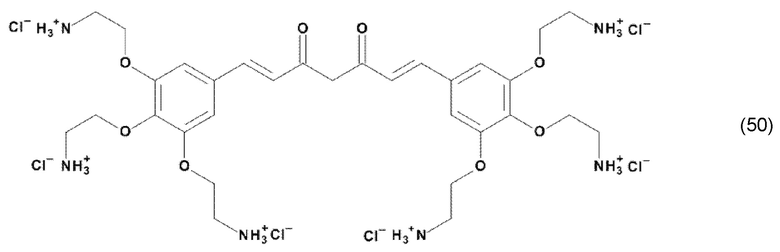
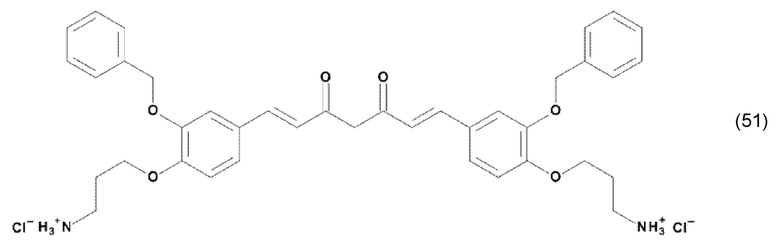
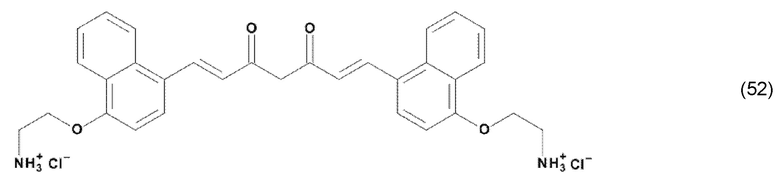
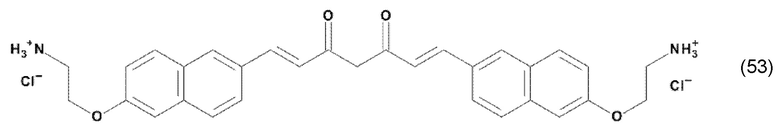
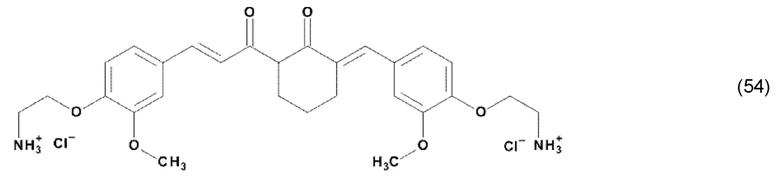
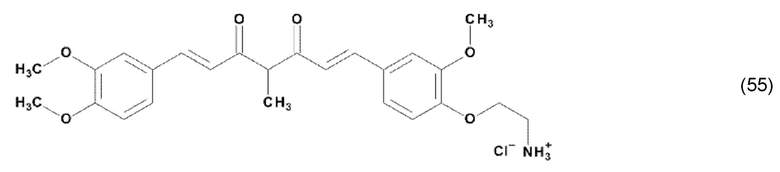
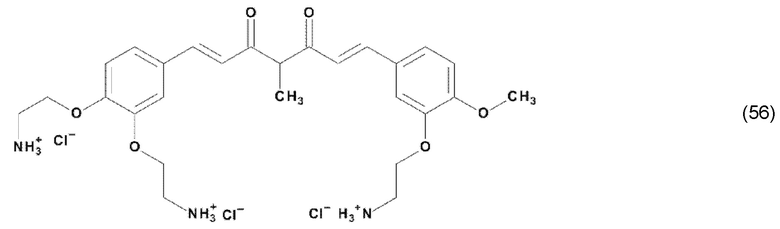
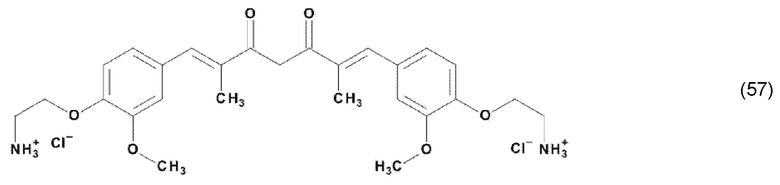
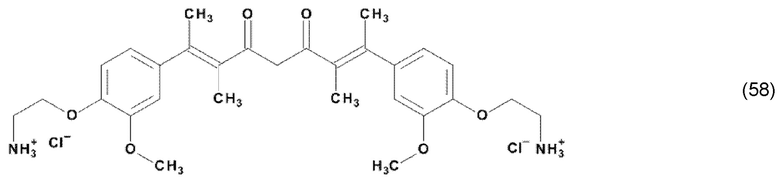
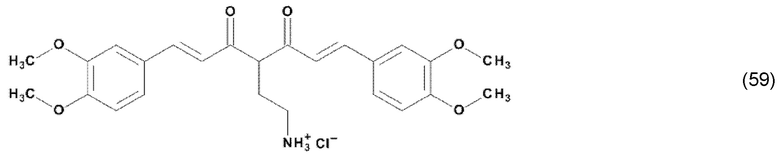
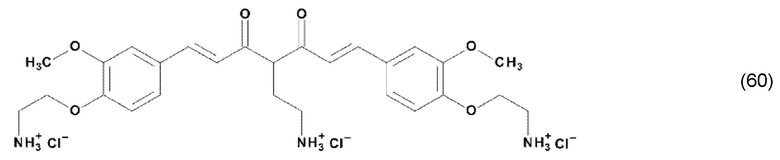
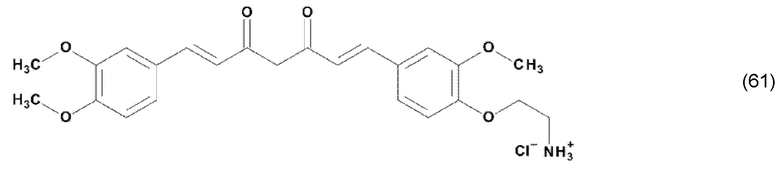
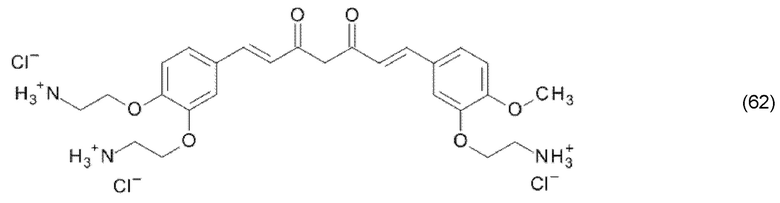
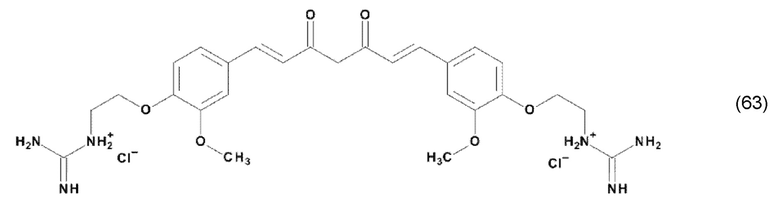
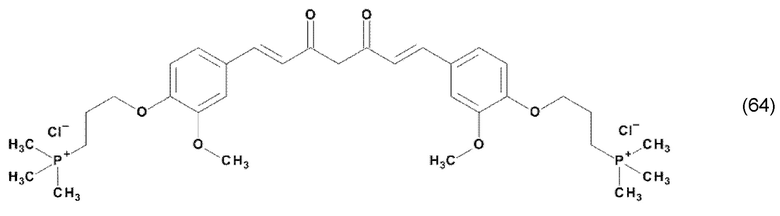
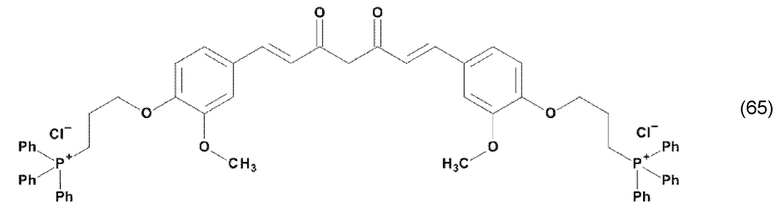
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (2) или производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (102) для применения в соответствии с настоящим изобретением, указанное соединение представляет собой по меньшей мере одно соединение формулы (68), (69а) или (69b):
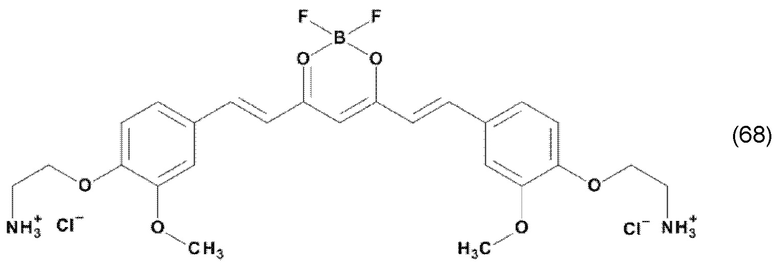
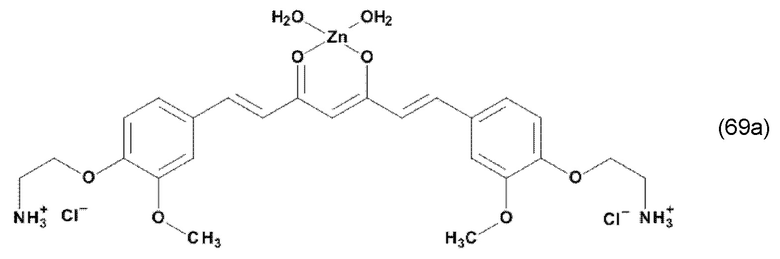
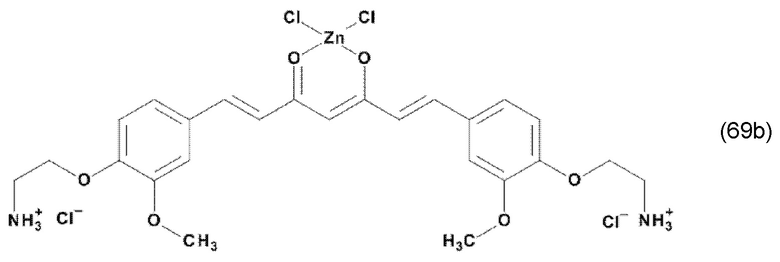
В более предпочтительном варианте реализации производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно настоящему изобретению формулы (3) или производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (101) для применения в соответствии с настоящим изобретением, указанное соединение представляет собой по меньшей мере одно соединение формулы (70):
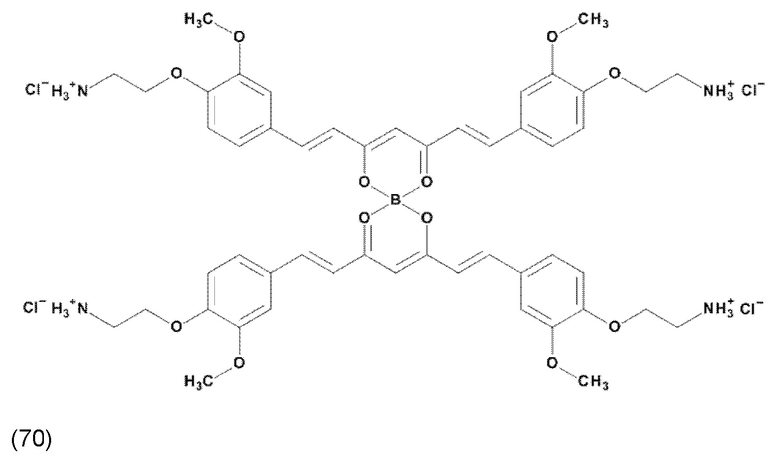
В производном 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) в соответствии с настоящим изобретением, а также в производном 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100), и/или формулы (101), и/или формулы (102), и/или формулы (3а) для применения в соответствии с настоящим изобретением, указанные остатки кетона, остатки карбоновой кислоты, остатки амида карбоновой кислоты, циклоалкильные остатки, циклоалкенильные остатки, алкильные остатки и алкенильные остатки могут быть линейными или разветвленными, предпочтительно линейными, а также могут быть незамещенными или могут содержать в качестве заместителей по меньшей мере один остаток, который представляет собой галоген, предпочтительно хлор, бром, йод или фтор, нитро, гидрокси, алкилокси, предпочтительно метокси, этокси, н-пропилокси, изо-пропилокси, н-бутилокси или н-пентилокси, или алканоилокси, предпочтительно формилокси, ацетокси или н-пропаноилокси.
В более предпочтительном варианте реализации или алкильные остатки, соответственно, независимо от других, выбраны из группы, состоящей из метила, этила, н-пропила, изо-пропила, н-бутила, изо-бутила, трет-бутила, н-пентила, 3-метилбутила, 2,2-диметилпропила, н-гексила, н-гептила и н-октила.
В более предпочтительном варианте реализации указанные алкильные могут быть выбраны из нециклических полиольных остатков с общей формулой -СН2(СН(ОН))gCH2OH, где G представляет собой целое число от 1 до 10, предпочтительно, от 1 до 4. В более предпочтительном варианте нециклические полиольные остатки выбраны из группы, состоящей из арабитила, рибитила, ксилитила, эритритила, треитила, лактитила, маннитила и сорбитила, более предпочтительно, D-рибитила и D-арабитил.
В более предпочтительном варианте реализации указанные циклоалкильные остатки и циклоалкенильные остатки могут содержать атомы кислорода в качестве атомов кольца и могут быть незамещенными, либо могут содержать в качестве заместителей по меньшей мере остаток, выбранный из гидроксила, алкилокси, предпочтительно метокси, этокси, н-пропилокси, изо-пропилокси, н-бутилокси или н-пентилокси, оилиг алканоилокси, предпочтительно формилокси, ацетокси или н-пропаноилокси.
В более предпочтительном варианте реализации указанные циклоалкильные остатки и циклоалкенильные остатки, которые содержат атомы кислорода в качестве атомов кольца, соответственно, независимо от других, выбраны из группы, которая состоит из тетрагидрофуранила, тетрагидропиранила, диоксоланила и диоксанила.
В более предпочтительном варианте реализации указанные арильные остатки, соответственно содержат максимум 4, более предпочтительно, максимум 3, более предпочтительно, максимум 2, конденсированных колец. В еще более предпочтительном варианте каждый из арильных остатков содержат 1 кольцо.
В предпочтительном варианте указанные арильные остатки, соответственно, независимо от других, выбраны из группы, которая состоит из фенила, бензила, нафтила, антраценила, фенантренила и пиренила.
В одном из предпочтительных вариантов реализации указанные алкенильные остатки, соответственно, независимо от других, содержат от 2 до 17 атомов С, более предпочтительно, от 2 до 13 атомов С, более предпочтительно, от 2 до 9 атомов С, более предпочтительно, от 2 до 5 атомов С. В более предпочтительном варианте реализации указанные алкенильные остатки, соответственно, независимо от других, выбраны из группы, которая состоит из этенила, н-пропенила и н-бутенила.
В более предпочтительном варианте реализации указанные альдегиды, соответственно, независимо от других, содержат от 1 до 17 атомов С, более предпочтительно, от 1 до 13 атомов С, более предпочтительно, от 1 до 9 атомов С, более предпочтительно, от 1 до 5 С атомов. В более предпочтительном варианте реализации указанные альдегиды, соответственно, независимо от других, выбраны из группы, которая состоит из метаналь-1-ил (формил), этаналь-1-ил (2-оксоэтил), н-пропаналь-1-ил (3-оксопропил) и н-бутаналь-1-ил (4-оксобутил).
В более предпочтительном варианте реализации указанные кетоны, соответственно, независимо от других, содержат от 2 до 17 атомов С, более предпочтительно, от 3 до 14 атомов С, более предпочтительно от 3 до 9 атомов С. В более предпочтительном варианте реализации указанные кетоны, соответственно, независимо от других, выбраны из группы, которая состоит из диметил-кетил, метилэтил-кетил, этилметил-кетил, диэтилке-тил, метилпропил-кетил, этилпропил-кетил, пропилметил-кетил, пропилэтил-кетил и ди-пропил-кетил, которые могут быть линейными или разветвленными.
В более предпочтительном варианте реализации указанные альдегидные остатки и/или кетоновые остатки могут представлять собой остатки моносахаридов, предпочтительно, остатки пентозы или кетозы.
В предпочтительном варианте подходящие остатки моносахаридов, соответственно, независимо от других, содержат от 3 до 7 атомов углерода, предпочтительно, от 5 до 6 атомов углерода, и содержат карбонильную группу, предпочтительно, альдегидную группу или кето-группу, а также по меньшей мере гидроксильную группу, и могут быть незамкнутыми или циклическими, предпочтительно, как фураноза или пираноза.
В предпочтительном варианте подходящие моносахаридные остатки являются производными моносахаридных остатков, которые, соответственно, независимо от других, выбраны из группы, которая состоит из D-глицеринового альдегид, L-глицеринового альдегида, D-эритрозы, L-эритрозы, D-треозы, L-треозы, D-рибозы, L-рибозы, D-арабинозы, L-арабинозы, D-ксилозы, L-ксилозы, D-ликсозы, L-ликсозы, D-аллозы, L-аллозы, D-альтрозы, L-альтрозы, D-глюкозы, L-глюкозы, D-маннозы, L-маннозы, D-гулозы, L-гулозы, D-идозы, L-идозы, D-галактозы, L-галактозы, D-талозы, L-талозы, дигидроксиацетона, D-эритрулозы, L-эритрулозы, D-рибулозы, L-рибулозы, D-ксилулозы, L-ксилулозы, D-псикозы, L-псикозы, D-фруктозы, L-фруктозы, D-сорбозы, L-сорбозы, D-тагатозы и L-тагатозы. В более предпочтительном варианте подходящие моносахариды выбраны из группы, которая состоит из D-рибозы, L-рибозы, D-арабинозы, L-арабинозы, D-ксилозы, L-ксилозы, D-ликсозы, L-ликсозы, D-аллозы, L-аллозы, D-альтрозы, L-альтрозы, D-глюкозы, L-глюкозы, D-маннозы, L-маннозы, D-гулозы, L-гулозы, D-идозы, L-идозы, D-галактоза, L-галактоза, D-талозы, L-талозы, D-рибулозы, L-рибулозы, D-ксилулозы, L-ксилулозы, D-псикозы, L-псикозы, D-фруктоза, L-фруктоза, D-сорбозы, L-сорбозы, D-тагатозы и L-тагатозы.
В более предпочтительном варианте реализации указанные сложные эфиры карбоновых кислот, соответственно, независимо от других, содержат от 1 до 17 атомов С, более предпочтительно, от 1 до 15 атомов С, более предпочтительно, от 1 до 12 атомов С, причем предпочтительно атом С карбоксилатной группы связан с одним из остатков Q1 - Q4a. В более предпочтительном варианте реализации указанные сложные эфиры карбоновых кислот, соответственно, независимо от других, выбраны из группы, которая состоит из этилового эфира, н-пропилового эфира, изо-пропилового эфира, н-бутилового эфира, сек-бутилового эфира, трет-бутилового эфира и бензилового эфира. В более предпочтительном варианте указанные сложные эфиры карбоновых кислот выбраны из группы, которая состоит из метоксикарбоила, 2-метокси-2-оксо-эт-1-ила, 3-метокси-3-оксо-проп-1-ила, 4-метокси-4-оксо-бут-1-ила, этоксикарбоила, 2-этокси-2-оксо-эт-1-ила, 3-этокси-3-оксо-проп-1-ила, 4-этокси-4-оксо-бут-1-ила, пропоксикарбоила, 2-окси-2-пропокси-эт-1-ила, 3-оксо-3-пропокси-проп-1-ила, 4-оксо-4-пропокси-бут-1-ила, изопропоксикарбонила, 2-изопропокси-2-оксо-эт-1-ила, 3-изопропокси-3-оксо-проп-1-ила, 4-изопропокси-4-оксо-бут-1-ила, бутоксикарбонила, 2-бутокси-2-оксо-эт-1-ила, 3-бутокси-3-оксо-проп-1-ила, 4-бутокси-4-оксо-бут-1-ила, изобутоксикарбонила, 2-изобутокси-2-оксо-эт-1-ила, 3-изобутокси-3-оксо-проп-1-ила, 4-изобутокси-4-оксо-бут-1-ила, трет-бутоксикарбонила, 2-трет-бутокси-2-оксо-эт-1-ила, 3-трет-бутокси-3-оксо-проп-1-ила, 4-трет-бутокси-4-оксо-бут-1-ила, феноксикарбонила, 2-окси-2-фенокси-эт-1-ила, 3-оксо-3-фенокси-проп-1-ила, 4-оксо-4-фенокси-бут-1-ила, бензилоксикарбонила, 2-бензилокси-2-оксо-эт-1-ила, 3-бензилокси-3-оксо-проп-1-ила и 4-бензилокси-4-оксо-бут-1-ила.
В более предпочтительном варианте реализации указанные амиды карбоновых кислот, соответственно, независимо от других, содержат от 1 до 17 атомов С, более предпочтительно, от 1 до 15 атомов С, более предпочтительно, от 1 до 12 атомов С, причем предпочтительно атом С карбоксамидной группы, соответственно, связан с одним из остатков Q1 - Q4a.
Указанные амиды карбоновых кислот предпочтительно не являются карбамидами.
В более предпочтительном варианте реализации указанные амиды карбоновых кислот, соответственно, независимо от других, выбраны из группы, которая состоит из карбамоила, 2-амино-2-оксо-эт-1-ила, 3-амино-3-оксо-проп-1-ила, 4-амино-4-оксо-бут-1-ила, метилкарбамоила, 2-(метиламино)-2-оксо-эт-1-ила, 3-(метиламино)-3-оксо-проп-1-ила, 4-(метиламино)-4-оксо-бут-1-ила, диметилкарбамоила, 2-(диметиламино)-2-оксо-эт-1-ила, 3-(диметиламино)-3-оксо-проп-1-ила, 4-(диметиламино)-4-оксо-бут-1-ила, этилкарбамоила, 2-(этиламино)-2-оксо-эт-1-ила, 3-(этиламино)-3-оксо-проп-1-ила, 4-(этиламино)-4-оксо-бут-1-ила, этил(метил)карбамоила, 2-[этил(метил)амино]-2-оксо-эт-1-ила, 3-[этил(метил)амино]-3-оксо-проп-1-ила, 4-[этил(метил)амино]-4-оксо-бут-1-ила, диметилкарбамоила, 2-(диметиламино)-2-оксо-эт-1-ила, 3-(диметиламино)-3-оксо-проп-1-ила, 4-(диметиламино)-4-оксо-бут-1-ила, дипропилкарбамоила, 2-(дипропиламино)-2-оксо-эт-1-ила, 3-(дипропиламино)-3-оксо-проп-1-ила, 4-(дипропиламино)-4-оксо-бут-1-ила, диизопропилкарбамоила, 2-(диизопропиламино)-2-оксо-эт-1-ила, 3-(диизопропиламино)-3-оксо-проп-1-ила, 4-(диизопропиламино)-4-оксо-бут-1-ила, дибутилкарбамоила, 2-(дибутиламино)-2-оксо-эт-1-ила, 3-(дибутиламино)-3-оксо-пропила, 4-(дибутиламино)-4-оксо-бут-1-ила, ди-трет-бутилкарбамоила, 2-(ди-трет-бутиламино)-2-оксо-эт-1-ила, 3-(ди-трет-бутиламино)-3-оксо-пропила и 4-(ди-трет-бутиламино)-4-оксо-бут-1-ила.
В более предпочтительном варианте реализации указанный гетероарильный остаток, который не содержит атом азота и содержит 4 от 20 до С, выбран из группы, состоящей из фуранила и бензофуранила.
В более предпочтительном варианте реализации указанные эфирные остатки, соответственно, независимо от других, содержат от 2 до 17 атомов С, более предпочтительно, от 2 до 13 атомов С, более предпочтительно, от 2 до 9 атомов С. В более предпочтительном варианте реализации указанные эфирные остатки, например, выбраны из группы, которая состоит из метоксиметила, метоксиэтила, метокси-н-пропила, этоксиметила, н-пропоксиметила, 2-этоксиэтоксиметила, 2-(2-этоксиэтокси)этила, изо-пропоксиметила, трет-бутилоксиметила, диокса-3,6-гептила и бензилоксиметила. В более предпочтительном варианте реализации указанные эфирные остатки могут представлять собой отдельные эфирные остатки, олигоэфирные остатки, полиэфирные остатки или их смеси.
В соответствии с настоящим изобретением термин "галоген", соответственно, независимо от других следует понимать как обозначающий фтор, хлор, бром или йод. В соответствии с настоящим изобретением термин "галид", соответственно, независимо от других, следует понимать как опознающий фторид, хлорид, бромид или йодид.
Если не указано иное, хиральные центры могут быть в R- или S-конфигурации. Настоящее изобретение охватывает как оптически чистые объемы, таки и стереоизомерные смеси, такие как энантиомерные смеси и диастереоизмерные смеси, в любом соотношении.
Настоящее изобретение, предпочтительно, также предусматривает мезомеры и/или таутомеры соединения формулы (1), и/или соединения формулы (2), и/или соединения формулы (3), и/или соединения формулы (100), и/или соединения формулы (101), и/или соединения формулы (102), а также чистые соединения и смеси изомеров, в любых соотношениях.
В качестве примера, соединение формулы (1) может быть в кено-форме (1а) или в енольной форме (1b):
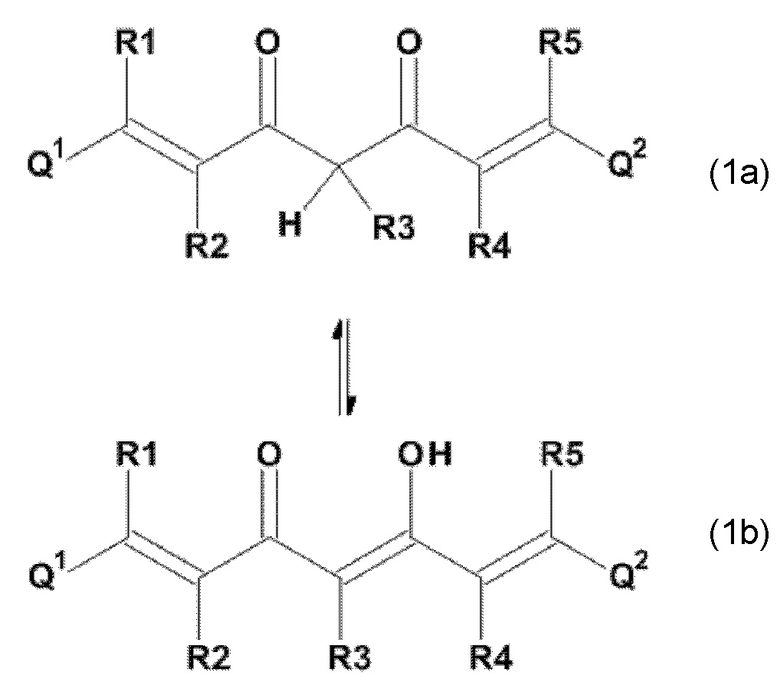
Вариант способа получения производного 1,7-диарил-1,6-гептадион-3,6-диона формулы (1) включает следующие этапы:
(А) осуществление реакции замещенного арилкетона формулы (80) с замещенным ацетилацетоном формулы (81) в присутствии растворителя, предпочтительно этилаце-тата, диметилсульфоксида (ДМСО), диметилформиата (ДМФА) или их смесей, в присутствии дегидрирующего агента, предпочтительно трибутилбората, В2О3 или их смесей, и первичного или и/или вторичного амина, предпочтительно н-бутиламина, морфолина, пиперидина или их смесей с получением соединения формулы (82):
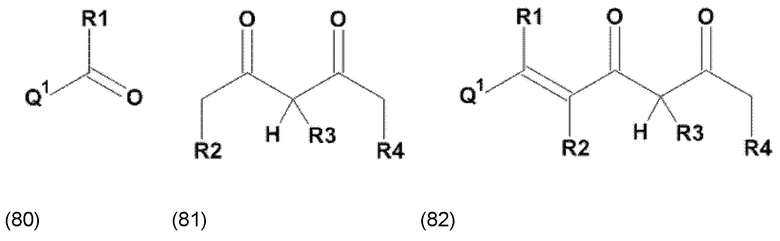
где Q1 представляет замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остаток Q1 содержит в качестве заместителей по меньшей мере один органический остаток W1a имеющий общую формулу (5а), (6а), (7а), (8а) или (9а):
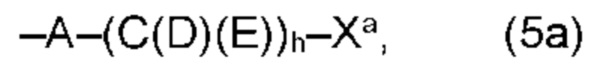
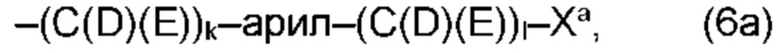
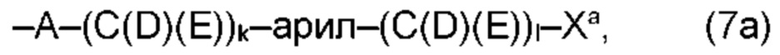
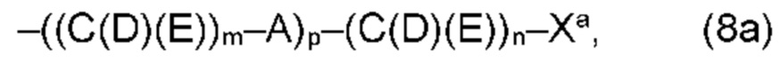
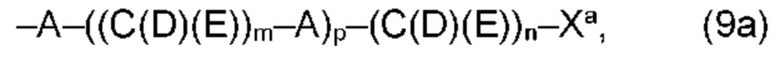
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где k представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р соответственно независимо от других представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А соответственно независимо от других, представляет кислород или серу,
где D и Е соответственно независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Ха соответственно независимо от других, представляет остаток формулы (20е), (21) или (24), предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
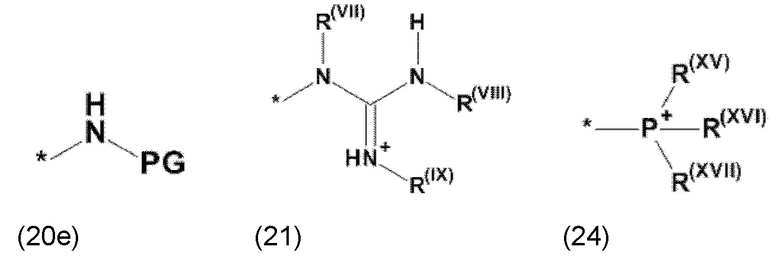
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют а защитную группу PG, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R3 и R4, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
(В) осуществление реакции соединения формулы (82) с замещенным арилкетоном формулы (83) в присутствии растворителя, предпочтительно этилацетата, диметилсульфоксида (DMSO, ДМСО), диметилформиата (ДМФА) или их смесей, в присутствии дегидрирующего агента, предпочтительно трибутилбората, В2О3 или их смесей, и первичного и/или вторичного амина, предпочтительно н-бутиламина, морфолина, пиперидина или их смесей, в результате чего получали производное 1,7-диарил-1,6-гептадион-3,6-дион формулы (1а):
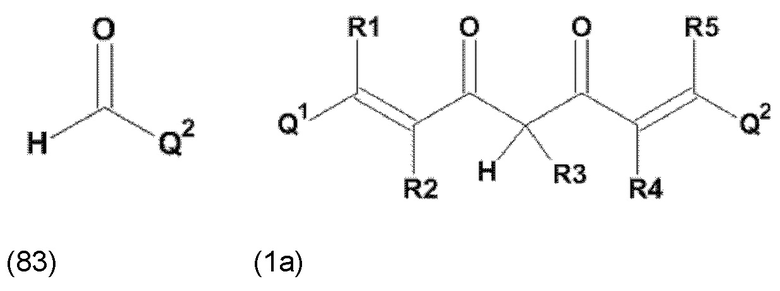
где Q2 представляет замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остаток Q2 необязательно содержит по меньшей мере один органический остаток W1a, имеющий общую формулу (5а), (6а), (7а), (8а) или (8а), и
где остаток R5 представляет водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
(С) необязательно, удаление любых присутствующих защитных групп PG.
В альтернативном варианте производное 1,7-диарил-1,6-гептадион-3,6-диона формулы (1) в соответствии с настоящим изобретением может быть получено путем:
(А1) осуществления реакции куркумин с соединением с общей формулой Xa-(C(D)(E))h-OH в присутствии диэтилазодикарбоксилата (DEAD) и трифенилфосфина (PPh3), а также растворителя, предпочтительно этилацетата, диметилсульфоксида (DMSO, ДМСО), диметилформиата (ДМФА) или их смесей, или
(А2) осуществления реакции куркумина с соединением с общей формулой Xa-(C(D)(E))h-Z в присутствии K2CO3 и KI, а также растворителя, предпочтительно этилацетата, диметилсульфоксида (DMSO, ДМСО), диметилформиата (ДМФА) или их смесей,
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где остаток Z, независимо от других, представляет Cl, Br, I, тозилат (OTs) или мезилат (OMs), и где Ха, соответственно, независимо от других, представляет остаток формулы (20е), (21) или (24), предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
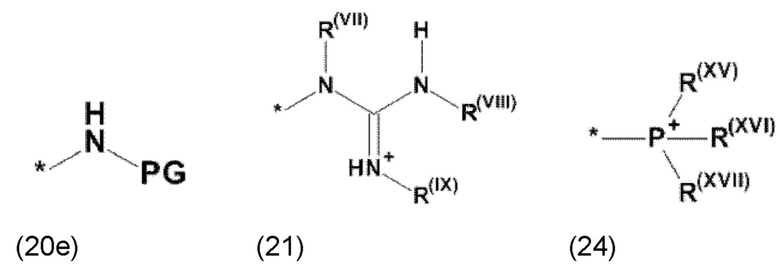
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют защитную группу PG, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
(В) удаления присутствующих защитных групп PG.
Дополнительный вариант способа получения производного 1,7-диарил-1,6-гептадион-3,6-диона формулы (1) включает этапы:
(А) осуществления реакции замещенного или незамещенного арилкетона формулы (80а) с замещенным ацетилацетоном формулы (81а) в присутствии растворителя, предпочтительно этилацетата, диметилсульфоксида (DMSO, ДМСО), диметилформиата (ДМФА) или их смесей, в присутствии дегидрирующего агента, предпочтительно трибутилбората, В2О3 или их смесей, и первичного и/или вторичного амина, предпочтительно н-бутиламина, морфолина, пиперидина или их смесей с получением соединения формулы (82а),
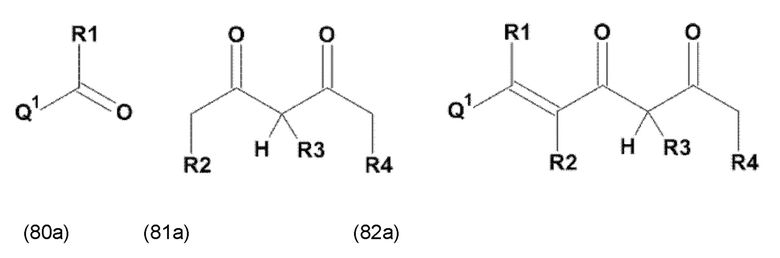
где остаток R3 представляет собой органический остаток W2a, имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
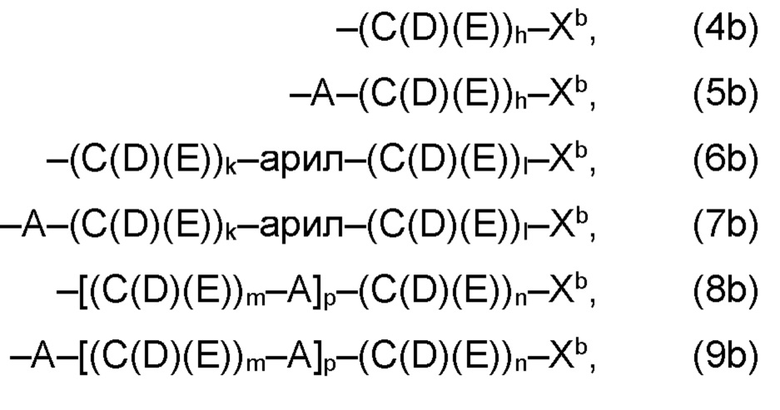
где Q1 представляет замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остаток Q1 необязательно содержит в качестве заместителей по меньшей мере один органический остаток W1b имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), и
где h представляет целое число от 1 до 20, предпочтительно, от 2 до 8, где к представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, где I представляет целое число от 0 до 10, предпочтительно, от 1 до 8, предпочтительно, от 2 до 6, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, предпочтительно, от 2 до 4, и
где А, соответственно, независимо от других, представляет кислород или серу,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(l) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xb, соответственно, независимо от других, представляет остаток формулы (20е), (21) или (24), предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
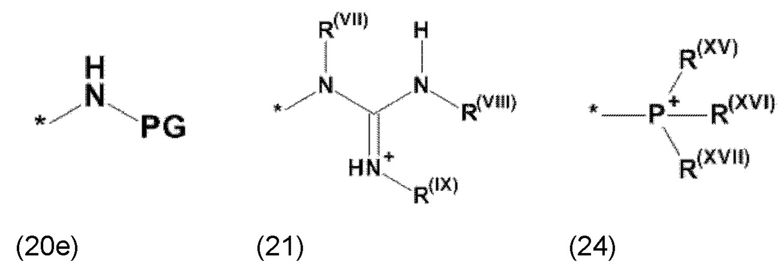
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют защитную группу PG, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2 и R4, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
(В) осуществления реакции соединения формулы (82а) с замещенным арилкетоном формулы (83а) в присутствии растворителя, предпочтительно этилацетата, диметилсульфоксида (DMSO, ДМСО), диметилформиата (ДМФА) или их смесей, в присутствии дегидрирующего агента, предпочтительно трибутилбората, В2О3 или их смесей, и первичного и/или вторичного амина, предпочтительно н-бутиламина, морфолина, пиперидина или их смесей, с получением производного 1,7-диарил-1,6-гептадион-3,6-диона формулы (1а):
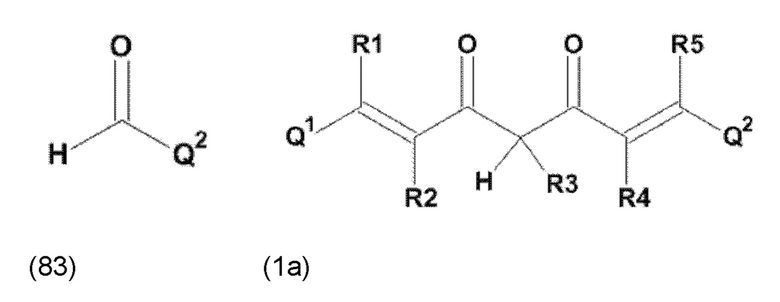
где Q2 представляет замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остаток Q2 необязательно содержит в качестве заместителей по меньшей мере один органический остаток W1a, имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b), и
где остаток R5 представляет водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
(С) необязательно, удаление присутствующих защитных групп PG.
Один из способов получения производного 1,7-диарил-1,6-гептадион-3,6-диона формулы (2) включает следующие:
(А) осуществление реакции соединения формулы (1) с солью металла М(L1)(L2)
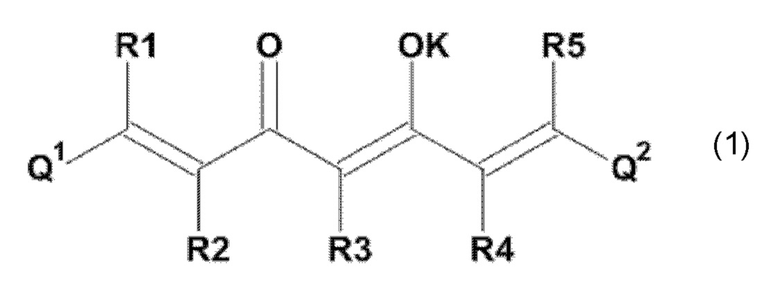
с получением производного 1,7-диарил-1,6-гептадион-3,6-диона формулы (2):
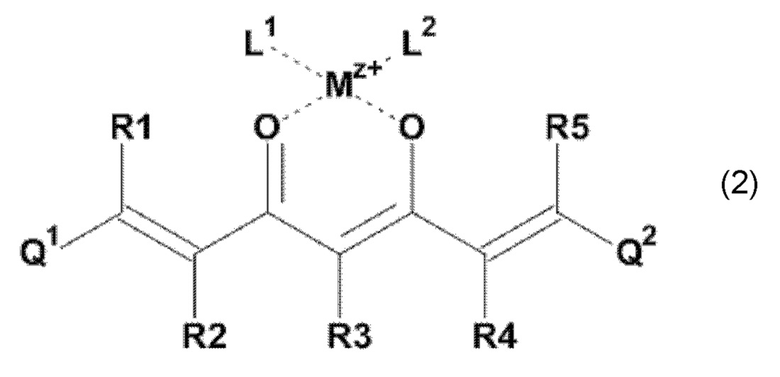
где L1 и L2, соответственно, независимо от других, представляют воду, галид, цианид, тиоцианат, фосфат, гидрофосфат или карбоксилирование карбоновой кислотой, содержащей от 1 до 10 утомов углерода, предпочтительно формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат или цитрат, и где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и где
(а) по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1a имеющий общую формулу (5а), (6а), (7а), (8а) или (9а):

где h представляет целое число от 1 до 20, где к представляет целое число от 0 до 10, где I представляет целое число от 0 до 10, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, и
где А, соответственно, независимо от других, представляет кислород или серу,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Ха, соответственно, независимо от других, представляет остаток формулы (20е), (21) или (24), предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
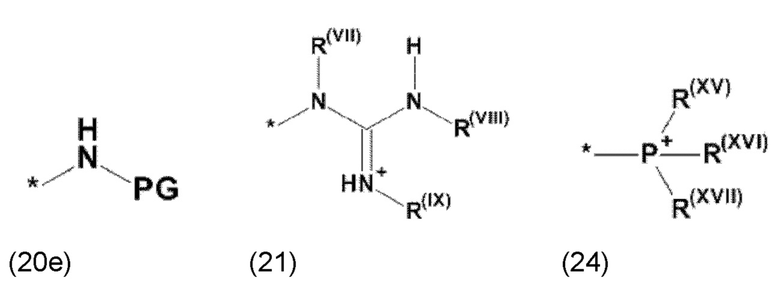
где каждый из остатков R(VII), R(VIII) т R(IX), соответственно, независимо от других, представляют защитную группу PG, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С,
или где
(b) остаток R3 представляет собой органический остаток W2a имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
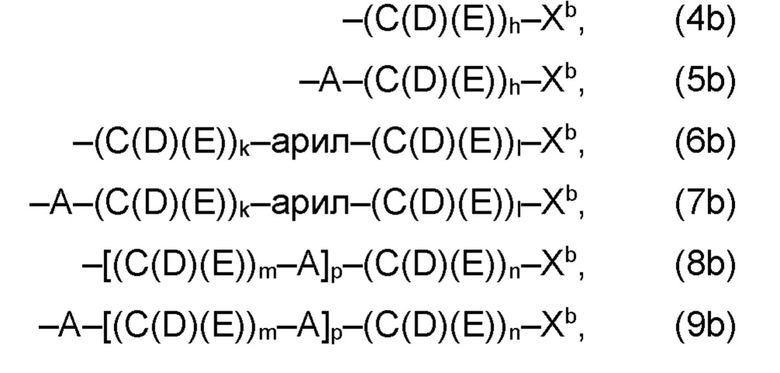
и
где, необязательно, по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1b имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b),
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где I представляет целое число от 0 до 10, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, и
где А, соответственно, независимо от других, представляет кислород или серу,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xb, соответственно, независимо от других, представляет остаток формулы (20е), (21) или (24), предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
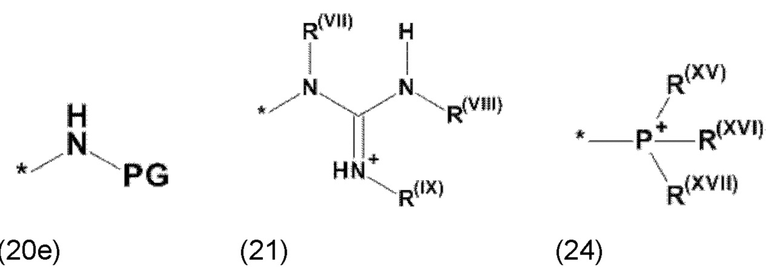
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют защитную группу PG, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
Один из способов получения производного 1,7-диарил-1,6-гептадион-3,6-диона формулы (3) включает следующие этапы:
(А) осуществление реакции соединения формулы (2):
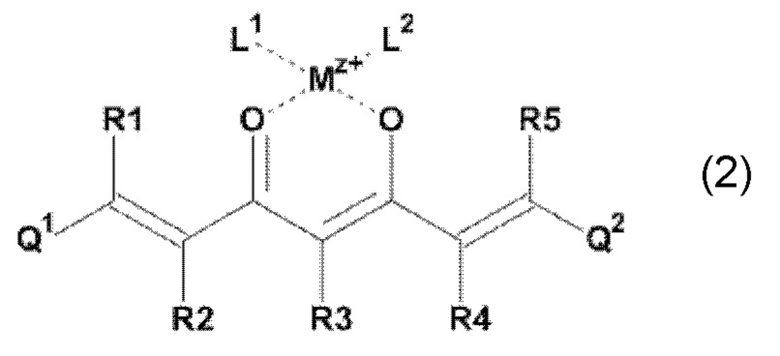
с соединением формулы (1е):
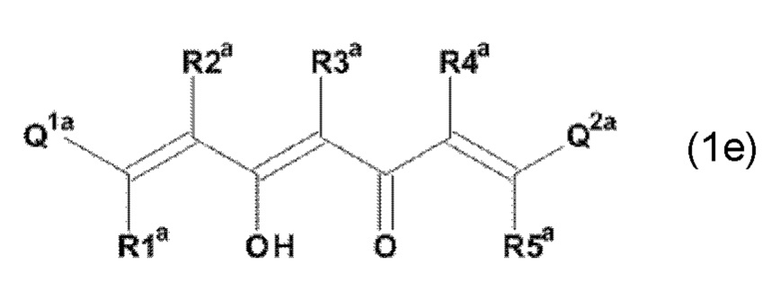
с получением производного 1,7-диарил-1,6-гептадион-3,6-диона формулы (3):
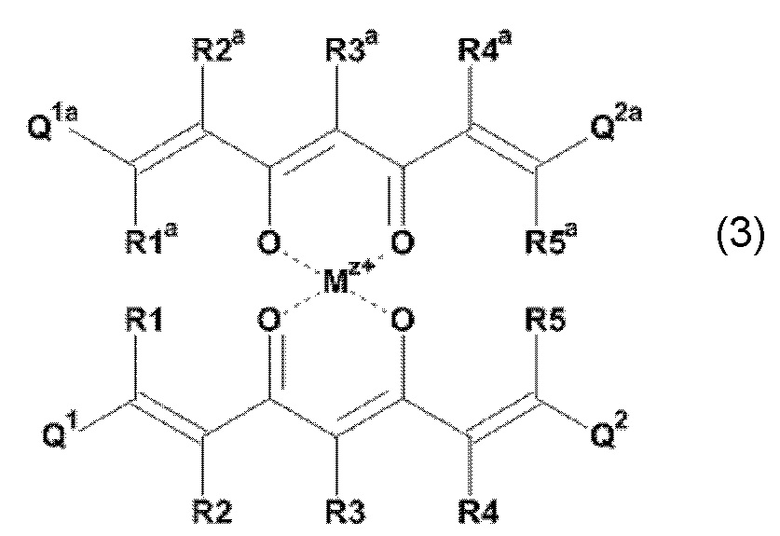
где L1 и L2, соответственно, независимо от других, представляют воду, фтор, хлорид, бромид, йодид, фосфат, гидрофосфат, дигидрофосфат, сульфат, гидросульфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода и/или их смеси,
где Mz+ представляет катион металла, где z представляет собой формальную степень окисления указанного металла М, и где z представляет целое число от 1 до 7, предпочтительно, от 2 до 5, и
где остатки Q1 и Q2, соответственно, независимо от других, представляют 1 замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остатки Q1a и Q2a, соответственно, независимо от других, представляют 1 замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток,
и где
(а) по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1a, где указанный по меньшей мере один органический остаток W1a имеет общую формулу (5а), (6а), (7а), (8а) или (9а):
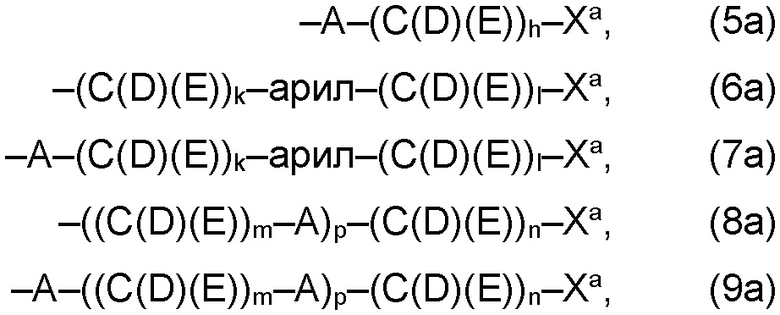
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где I представляет целое число от 0 до 10, и где m, n и р, соответственно, независимо от других, представляют целое число от 1 до 6, и
где А, соответственно, независимо от других, представляет кислород или серу, где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Ха, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
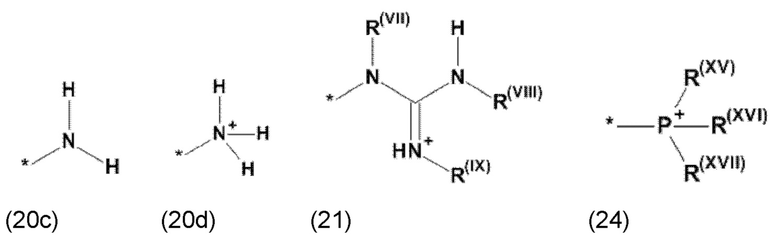
где каждый из остатков R(VII), R(VIII) т R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и
где по меньшей мере один из остатков Q1a и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1c, где указанный по меньшей мере один органический остаток W1c имеет общую формулу (5с), (6с), (7с), (8с) или (9с):

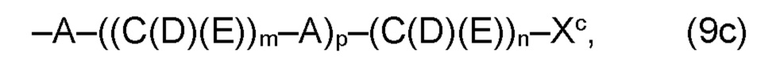
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где I представляет целое число от 0 до 10, и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где А, соответственно, независимо от других, представляет кислород или серу,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xc, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xc, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
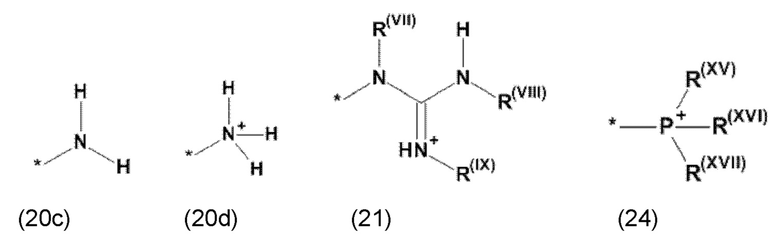
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С,
где остатки R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, 5 циклоалкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С, или где
(b) остаток R3 или R3a, соответственно, независимо от других, представляет собой органический остаток W2a, где указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
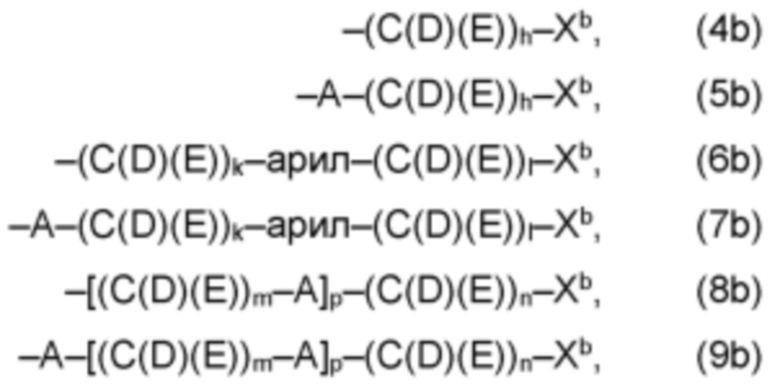
и
где, необязательно, по меньшей мере один из остатков Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере 20 один органический остаток W1b имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b),
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где I представляет целое число от 0 до 10, и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и 25 где А, соответственно, независимо от других, представляет кислород или серу,
предпочтительно, кислород,
где D и Е, соответственно, независимо от других, представляют водород, галоген, G-R(I) или G-C(=G)-R(II), где G, соответственно, независимо от других, представляет кислород или серу, и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом азота, или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно, четвертичный, атом фосфора, причем предпочтительно Xb, соответственно, независимо от других, представляет остаток формулы (20с), (20d), (21) или (24), более предпочтительно, остаток формулы (20с), (20d) или (21), более предпочтительно, остаток формулы (24):
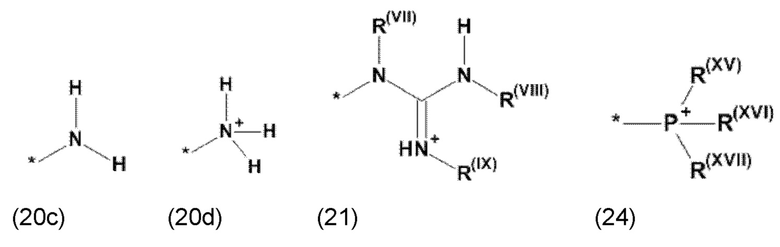
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, и где каждый из остатков R(XV), R(XVI) т R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов С, алкиларильный остаток, содержащий от 5 до 12 атомов С, алкильный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, или эфирный остаток, который может быть линейным или разветвленным, содержащим от 1 до 8 атомов С, т
где остатки R1, R1a, R2, R2a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов С, алкиларил, содержащий от 1 до 12 атомов С, арил, содержащий от 5 до 20 атомов С, эфир, содержащий от 2 до 12 атомов С, или гликоль, содержащий от 2 до 12 атомов С.
При использовании различных аминозащитных групп PG в синтезе можно использовать ортогональную стратегию защитных групп, где различные аминофункциональные группы молекулы могут направленно освобождаться одна за другой для участия в реакции.
Подходящие методы удаления аминозащитных групп PG известны в предшествующем уровне техники. В качестве примера можно привести бензилоксикарбонил (Cbz), который может быть удален путем обработки кислотами Льюиса, например, ZnBr2, в уксусной кислоте. Ди-трет-бутилоксикарбонил (boc) может быть удален, например, путем кислотного гидролиза. Аллилоксикарбонил (alloc) может, например, быть отщеплен под действием тетракис(трифенилфосфин)палладий(0) и нуклеофила.
Активное или пассивное введение, адгезия и распространение патогенов в организме хозяина называется инфекцией. Источники инфекционных частиц встречаются повсеместно. Соответственно, например, организм человека колонизируется большим количеством микроорганизмов, которые обычно находятся под контролем нормального метаболизма и неповрежденной иммунной системы. Однако при ослаблении иммунной системы, например, может произойти сильная пролиферация патогенных микроорганизмов и, в зависимости от типа возбудителя, могут проявиться различные симптомы заболевания. Медицина располагает специальными средствами, предназначенными для лечения многих заболеваний, вызванных патогенными микроорганизмами, например, антибиотиками против бактерий или антимикотическими средствами препаратами против грибов или противовирусными препаратами против вирусов. Однако при использовании этих средств наблюдается рост числа резистентных (устойчивых) патогенов, которые иногда также обладают резистентностью к нескольким лекарственным средствам. В связи с появлением этих патогенов, обладающих устойчивостью и множественной устойчивостью, лечение инфекционных заболеваний становится все более трудным. Клиническими последствиями резистентности (устойчивости) являются провалы лечения, особенно у пациентов с иммуносупрессией
Одноклеточные или многоклеточные микроорганизмы могут вызывать инфекционные заболевания. Применение по меньшей мере одного патоген-специфического лекарственного средства, например, антибиотика, антимикотического средства или противовирусного терапевтического средства, может уменьшить количество патогенных микроорганизмов и/или привести к инактивации патогена. Применение патоген-специфического средства может быть системным и/или топическим (местным).
При системном применении патоген-специфическое средство переносится в кровеносную и лимфатическую системы организма, который лечат, и, таким образом, распределяется по всему организму. При системном применении патоген-специфического препарата могут иметь место деградация препарата и/или побочные эффекты, например, в результате биохимической трансформации (метаболизма) препарата.
При местном применении патоген-специфического средства, средство наносят туда, где оно должно проявлять свое терапевтическое действие, например, на инфицированную часть кожи, а здоровую кожу не задействуют. Это позволяет в основном избежать системных побочных эффектов.
Поверхностные инфекции кожи или мягких тканей не обязательно должны лечиться системным применением патоген-специфического средства, поскольку средство может быть наносить непосредственно на инфицированные участки кожи.
Известные патогенно-специфические средства проявляют побочные эффекты и взаимодействия, некоторые из которых могут быть тяжелыми, как при системном, так и при местном применении. Кроме того, в случае местного применения, неправильный прием лекарственных средств (комплаентность) пациента, в частности, при применении антибиотиков, может привести к возникновению устойчивости.
Альтернативой здесь является фотодинамическая инактивация микроорганизмов, поскольку устойчивость к фотодинамической инактивации неизвестна. Независимо от типа микроорганизмов, с которыми необходимо бороться, и связанных с ними инфекционных заболеваний, количество патогенных микроорганизмов уменьшается и/или патогенные микроорганизмы уничтожаются. В качестве примера, можно контролировать смеси различных микроорганизмов, например, грибков и бактерий или различные штаммы бактерий.
Задача настоящего изобретения решается за счет обеспечения способа инактивации микроорганизмов, которые предпочтительно включают вирусы, археи, бактерии, споры бактерий, грибы, споры грибов, простейшие, водоросли, передающиеся с кровью паразиты, или их комбинации, где способ включает следующие этапы:
(A) приведение микроорганизмов в контакт с по меньшей мере одним фотосенсибилизатором, причем указанный сенсибилизатор представляет собой по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (101), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (2), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона формулы (3) или фармацевтически приемлемую соль, и/или сложный эфир, и/или комплекс указанного соединения, и
(B) облучение указанных микроорганизмов и по меньшей мере одного фотосенсибилизатора электромагнитным излучением при подходящей длине волны и плотности энергии.
В предпочтительном варианте способ в соответствии с настоящим изобретением осуществляют для инактивации микроорганизмов для (в рамках) фотодинамической терапии пациента и/или фотодинамической дезинфекции (очистки, обеззараживания) по меньшей мере одной поверхности изделия и/или по меньшей мере одной поверхности участка.
В одном из предпочтительных вариантов реализации способа согласно настоящему изобретению, облучение указанных микроорганизмов и по меньшей мере одного фотосенсибилизатора электромагнитным излучением при подходящей длине волны и плотности энергии осуществляют в присутствии по меньшей одного соединения, являющегося донором кислорода, предпочтительно пероксида, и/или по меньшей мере одного кислород-содержащего газа, предпочтительно, кислорода.
Указанное по меньшей одно соединение, являющееся донором кислорода и/или указанный по меньшей мере один кислород-содержащий газ можно предпочтительно наносить перед или во время этапа (В) способа согласно настоящему изобретению.
При добавлении дополнительного кислорода в форме по меньшей мере одного кислород-содержащего соединения и/или по меньшей мере одного кислород-содержащего газа перед или в ходе облучения микроорганизмов и по меньшей мере одного фотосенсибилизатора электромагнитным излучением при подходящей длине волны и плотности энергии, повышается выход образования активных форм кислорода (АФК, ROS), предпочтительно, кислородных радикалов и/или синглетного кислорода.
В предпочтительном варианте фотосенсибилизатор представляет собой по меньшей мере одно соединение формулы (100), по меньшей мере одно соединение формулы (101), по меньшей мере одно соединение формулы (102), по меньшей мере одно соединение формулы (1), по меньшей мере одно соединение формулы (2), по меньшей мере одно соединение формулы (3) или их комбинацию, или фармацевтически приемлемую соль, и/или сложный эфир, и/или комплекс указанного соединения.
В более предпочтительном варианте фотосенсибилизатор представляет собой производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (2), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3),и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3а), или фармацевтически приемлемую соль, и/или сложный эфир, и/или комплекс указанного соединения.
Задача настоящего изобретения решается также за счет применения по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (100), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (101), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (102) или фармацевтически приемлемой соли, и/или сложного эфира, и/или комплекса указанного соединения, в качестве фотосенсибилизатора для инактивации микроорганизмов, которые предпочтительно включают вирусы, археи, бактерии, споры бактерий, грибы, споры грибов, простейшие, водоросли, передающиеся с кровью паразиты, или их комбинации.
В более предпочтительном варианте производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (2), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3а) или фармацевтически приемлемую соль, и/или сложный эфир, и/или комплекс указанного соединения применяют в качестве фотосенсибилизатора для инактивации микроорганизмов, которые предпочтительно включают вирусы, археи, бактерии, споры бактерий, грибы, споры грибов, простейшие, водоросли, передающиеся с кровью паразиты, или их комбинации.
Производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101) и/или формулы (102), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (2), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3а) характеризуется высоким выходом синглетного кислорода после облучения электромагнитным излучением при подходящей длине волны и плотности энергии.
В способе в соответствии с настоящим изобретением и/или применении в соответствии с настоящим изобретением электромагнитное излучение предпочтительно находится в видимом, ультрафиолетовом и/или инфракрасном спектральном диапазоне. В более предпочтительном варианте длина волны электромагнитного излучения находится в диапазоне от 280 до 1000 нм, более предпочтительно от 380 до 1000 нм.
В более предпочтительном варианте плотность энергии электромагнитного излучения лежит в диапазоне от 1 мкВт/см2 до 1 кВт/см2, более предпочтительно от 1 мВт/см2 до 100 Вт/см2, более предпочтительно от 2 мВт/см2 до 50 Вт/см2, более предпочтительно от 6 мВт/см2 до 30 Вт/см2, более предпочтительно от 7 мВт/см2 до 25 Вт/см2.
Продолжительность облучения может варьировать в зависимости от типа микроорганизмов и/или тяжести инфекции. В предпочтительном варианте продолжительность облучения лежит в диапазоне от 1 мкс до 1 ч, более предпочтительно от 1 мс до 1000 с.
В качестве примере, процедуру облучения можно проводить как описано в одном из документов: WO 96/29943 А1, ЕР 0437183 В1 или WO 2013/172977 А1.
В предпочтительном варианте устройство для облучения также включает устройства для выделения по меньшей мере одного кислород-содержащего соединения, предпочтительно, пероксида, и/или по меньшей мере одного кислород-содержащего газа, предпочтительно, кислорода.
В предпочтительном варианте электромагнитное излучение вырабатывается источником излучения, выбранным из группы, состоящей из искусственных источников излучения, например, УФ-ламп, ИК-ламп, люминесцентных ламп, светоизлучающих диодов, лазеров или химического света.
Кроме того, авторы изобретения неожиданно обнаружили, что производное 1,7-диарил- 1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (2), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3), и/или производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (3а) и/или соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы указанных соединению, предпочтительно демонстрируют высокую аффинность по отношению к микроорганизмам.
За счет аффинности указанные по меньшей мере одно производное 1,7-диарил-1,6- гептадиен-3,5-диона для применения в соответствии с настоящим изобретением фор- мулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы эффективно связываются с микроорганизмами и образуют достаточно местного синглетного кислорода для инактивации микроорганизмов, предпочтительно, их уничтожения.
В предпочтительном варианте применения в качестве фотосенсибилизатора по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100,) и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, связываются микроорганизмами. После облучения электромагнитным излучением при подходящей длине волны и плотности энергии, происходит инактивация микроорганизмов, предпочтительно их уничтожение под действием образующихся активных форм кислорода (АФЕ, ROS), предпочтительно, радикалов кислорода и/или синглетного кислорода.
В предпочтительном варианте связывание по меньшей мере одного производного 1,7- диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующих фармацевтически приемлемых солей и/или сложных-эфиров и/или комплексов с микроорганизмами приводит к окрашиванию или определению положения микроорганизмов. Это позволяет мониторировать процесс инактивации или деколонизации микроорганизмов.
В контексте настоящего изобретения термин "деколонизация" следует понимать как обозначающий удаление, предпочтительно, полное удаление микроорганизмов.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют в инактивации одноклеточных или многоклеточных микроорганизмов, которые предпочтительно выбраны из группы, состоящей из вирусов, археев, бактерий, спор бактерий, грибов, например, мицелиальных грибов и дрожжей, спор бактерий, простейших, водорослей и переносимых кровью паразитов.
В предпочтительном варианте можно обрабатывать поверхности тела, например, коду или слизистые оболочки, человека или животных, предпочтительно млекопитающих В этом предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3) и/или формулы (3а,) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, предпочтительно в фармацевтическом препарате, применяют для дезинфекции и/или деколонизации поверхности кожи или мягких тканей, причем в предпочтительном варианте сохраняется целостность кожи.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102),и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют в фармацевтическом препарате для местного и/или топического, предпочтительно назального, орального, анального, вагинального или кожного применения (нанесения).
Термин "топическое применение" также следует понимать как обозначающий нанесение на ухо или в ухо, предпочтительно, наружное ухо. Наружное ухо состоит из ушного хряща, ушной раковины, мочки уха, наружного слухового или ушного канала и наружной части барабанной перепонки.
Термин "топическое применение" также следует понимать как обозначающий нанесение на или в нос и/или околоносовые пазухи, такие как, например, гайморова пазуха, лобная пазуха и/или клиновидная пазуха.
Термин "топическое применение" также следует понимать как обозначающий нанесение на поверхность глаза, предпочтительно, наружную, апикальную сторону эпителиального слоя роговицы и/или наружную поверхность глазного аппарата, предпочтительно слезные протоки, конъюнктиву и/или веки.
Термин "топическое применение" также следует понимать как обозначающий нанесение на наружную, апикальную сторону эпителия полых органов, например, пищевода, желудочно-кишечного тракта, желчного пузыря, желчных протоков, гортани, дыхательных путей, бронхов, яичников, матки, влагалища, уретры, мочевого пузыря или уретры.
Термин "топическое применение" также следует понимать как обозначающий нанесение на зубы или в зубы, например, в корневом канале и/или в корневой полости и/или в фиссуре зуба, или в десневых карманах и/или при фенестрации кости.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяются для получения фармацевтического препарата для профилактики и/или лечения инфекционной, предпочтительно вирусной, бактериальной и/или микотической кожной болезни, предпочтительно выбранной из группы, которая состоит из стафилококкового ожогоподобного кожного синдрома, импетиго, кожных абсцессов, фурункуловы, карбункулов, флегмона, целлюлита, острого лимфаденита, пилионидальной болезни, пиодермы, гнойного дерматита, септических дерматитов, гнойного дерматита, эритразмы, рожи, обыкновенных угрей или грибковых инфекций.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяются для получения фармацевтического препарата для заживления ран, например, в случае нарушений заживления после хирургических вмешательств.
В предпочтительном варианте по меньшей мере одно производное 1,7-диарил-1,6- гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, или фармацевтический препарат, содержащий по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, применяют для дезинфекции и/или снижения численности бактерий в инфицированных ранах.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяются для получения фармацевтического препарата для профилактики и/или лечения инфекционных, предпочтительно вирусных, бактериальных и/или грибковых заболеваний, болезней уха, верхних дыхательных путей, полости рта, горла, гортани, нижних дыхательных путей и/или пищевода.
Преобладание патогенных микроорганизмов является, например, основной причиной инфекции в полости рта. В связи с этим возникает проблема, заключающаяся в том, что микроорганизмы организованы синергетически в чрезвычайно сложные биопленки. Эти биопленки, например, бляшки или зубной камень, состоят из множества комплексных слоев и содержащихся в них белков, углеводов, фосфатов и микроорганизмов. Зубной камень встречается, в частности, когда поверхность зуба не освобождается от отложений при естественной или искусственной чистке. Соответственно, такая ситуация затрудняет доступ к микроорганизмам, связанным в биопленку.
Обычные терапевтические средства, такие как антибиотики и ополаскиватели для полости рта или механическая чистка зубов могут применяться только в ограниченном объеме, поскольку либо они не могут влиять на бактерии непосредственно, например, во время чистки зубов трудно дозировать и применять, например, антибиотики и ополаскиватели для полости рта, либо их применение в целом не оправдано из-за негативных побочных эффектов.
Например, в Соединенных Штатах ежегодно проводится 20 миллионов операций по обработке корневых каналов, в рамках которых осуществляется более 2 миллионов повторных эндодонтических вмешательств, которых можно было бы избежать за счет улучшенной дезинфекции корневых каналов.
В предпочтительном варианте способ в соответствии с настоящим изобретением применение в соответствии с настоящим изобретением подходят для эффективного уничтожения микроорганизмов в системе корневых каналов человеческого зуба, включая корневой канал и зубные канальцы.
В одном из предпочтительных вариантов реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют в качестве фотосенсибилизатора в фотодинамическое инактивации микроорганизмов в ротовой полости.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяются для получения фармацевтического препарата для лечения и/или профилактики инфекционного, предпочтительно вирусного, бактериального и/или микотического поражения ткани зуба, предпочтительно, налета, кариеса или пульпита, и/или инфекционного, предпочтительно вирусного, бактериального и/или микотического поражения периодонта, предпочтительно, гингивита, парадонтита, пульпита или периимплантита.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101) и/или формулы (102) и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2),, и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, или фармацевтический препарат, содержащий по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют для чистки зубов, зубных протезов и/или скоб.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, или фрамацевтический препарат, содержащий по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют в назальной деколонизации микроорганизмов.
В качестве примера, метициллин-резистентные штаммы золотистого стафилакокка (MRSA) персистируют при оральной и назальной колонизации, а также обладают высокой устойчивостью к внешним условиям. Соответственно, назальная деколонизация, т.е., удаление микроорганизмов, также уменьшает колонизацию в других участках тела.
Кроме того, настоящее изобретение относится к фармацевтическое композиции, содержащей по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6- гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы и одно или более физиологически приемлемых вспомогательных веществ.
В предпочтительном варианте фармацевтическая композиция содержит по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, и одно или более физиологически приемлемых вспомогательных веществ.
В предпочтительном варианте фармацевтическую композицию получают путем по меньшей мере одного соединения формулы (100) и/или формулы (101) и/или формулы (102) и/или формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) или их соответствующих фармацевтически приемлемых солей, и/или сложных эфиров, и/или комплексов с одним или более физиологически приемлемых вспомогательных веществ и придания ей подходящей для введения формы.
Подходящая форма введения для фармацевтической композиции в соответствии с настоящим изобретением предпочтительно выбрана из группы, которая состоит из мазей, кремов, гелей, лосьонов, перемешиваемых смесей, растворов, например, в форме капель или спреев, порошков, микрокапсул и паст.
Фармацевтическую композицию в соответствии с настоящим изобретением можно вводить (применять) местно или топически, предпочтительно назально, перорально, анально, вагинально или кожно.
Примерами физиологически приемлемых вспомогательных веществ являются обычно применяемые в фармацевтике жидкие или твердые наполнители и вещества для создания объема, растворители, эмульгаторы, смазывающие вещества, корректоры вкуса, красители и/или буферные вещества.
В предпочтительном варианте физиологически приемлемое вспомогательное вещество представляет собой поливинилпирролидон (PVP, ПВП), циклодекстрин, полиэтиленгликоль (PEG, ПЭГ) или их смеси.
В более предпочтительном варианте фармацевтически приемлемая композиция содержит липосомы.
В более предпочтительном варианте реализации фармацевтически приемлемая композиция содержит эффективное количество по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемых солей, и/или сложных эфиров, и/или комплексов, где эффективное количество составляет, соответственно, от 0.01 мкг до 1000 мкг на грамм композиции, предпочтительно, соответственно, от 0.1 мкг до 500 мкг на грамм композиции.
В одном из предпочтительных вариантов реализации изобретения, фармацевтическая композиция содержит по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, и по меньшей мере один дополнительный фармацевтически активный компонент.
В предпочтительном варианте указанный по меньшей мере по меньшей мере один дополнительный фармацевтически активный компонент выбран из группы, которая состоит из антибиотиков, антимикотических средств, противовирусных средств, антигистаминовых препаратов, симпатомиметиков, антигеморрагических препаратов, смягчающих и защитных средств для кожи, анальгетиков, дезинфицирующих средств, иммуноферментов и иммуноглобулинов, антипаразитарных веществ, инсектицидов, репеллентов и кортикостероидов.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, или фрамацевтический препарат, содержащий по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы наносятся самостоятельно потребителем, необязательно, с последующим облучением подходящим источником излучения, который генерирует электромагнитное излучение при подходящей длине волны и плотности энергии.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, или препарат, содержащий по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, применяют в инактивации микроорганизмов в биологических жидкостях, предпочтительно, в медицинских препаратах крови.
Подходящее оборудование для облучения биологических жидкостей известно специалистам и описано, например, в WO 99/43790 А1, US 2009/0010806 А1 или WO 2010/141564 А2.
Примерами подходящих биологических жидкостей являются кровь и препараты крови, в том числе, замороженная свежая плазма, концентрат эритроцитов, концентрат тромбоцитов, концентрат гранулоцитов, богатая тромбоцитами плазма, препараты стволовых клеток, концентраты отдельных факторов свертывания, человеческий альбумин, иммуноглобулины, фибриновый клей, антитромбин, белок С, белок S, фибринолитики или их комбинации.
В одном из предпочтительных вариантов реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют для фотодинамической дезинфекции поверхностей всех типов. Фотодинамическая дезинфекция (очистка, обеззараживание) поверхности приводит к фотодинамической инактивации микроорганизмов на обрабатываемой поверхности.
Примерами подходящих поверхностей, являются поверхности из пластика, металла, стекла, текстиля, дерева, камня или их комбинаций.
В более предпочтительном варианте указанное производное 1,7-диарил-1,6-гептадиен- 3,5-диона в соответствии с настоящим изобретением формулы (1) и/или формулы (3) и/или формулы (3а) или фармацевтически приемлемую соль, и/или сложный эфир, и/или комплекс указанного соединения применяют в фотодинамической дезинфекции, очистке поверхностей и/или покрытия оболочкой (нанесения покрытий на), предпочтительно медицинские продуктов, электронных устройств, гигиенических изделий, пищевой упаковки, пищевых продуктов, мебели, строительных материалов или участков.
В более предпочтительном варианте по меньшей мере одно производное 1,7-диарил-1,6- гептадиен-3,5-диона для применения в соответствии с настоящим изобретением фор- мулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, наносят на и/или вводят в поверхность, необязательно, затем облучают подходящим источником излучения, который дает электромагнитное излучение при подходящей длине волны и плотности энергии. В предпочтительном варианте указанное по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы обеспечивают "самодезинфекцию" поверхности в ходе облучения.
Соответственно, облучение можно осуществлять сразу после обработки поверхности по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-дион согласно настоящему изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами, предпочтительно после нанесения (применения) по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующих фармацевтически приемлемы солей, и/или сложных эфиров, и/или комплексов на поверхность и/или введения по меньшей мере одного производного 1,7- диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-дион согласно настоящему изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующих фармацевтически приемлемых солей, и/или сложных эфиров, и/или комплексов в поверхность и/или в более поздний момент времени.
В более предпочтительном варианте обрабатывают изделия, которые имеют ограниченный срок годности в связи с температурным режимом, например, изделия, выполненные из термопластичных пластиков, или изделия, которые подвергаются воздействию дезинфицирующих веществ.
Изделия, которые имеют ограниченный срок годности в связи с температурным режимом, не удается достаточно стерилизовать, например, из-за того, что при более высоких температурах они теряют форму или становятся хрупкими.
Кроме того, неправильное и/или избыточное применение дезинфицирующих средств может привести к повышению устойчивости в результате отбора более устойчивых микроорганизмов, если, например, концентрация вещества и время экспозиции и, следовательно, патогенное редукционное действие слишком малы.
В более предпочтительном варианте реализации способ в соответствии с настоящим изобретением применяют для предотвращения бактериальной инфекции, например, перед имплантацией или после успешной деколонизации, например, для предотвращения новой колонизации болезнетворными микроорганизмами, такими как, например, патогенными для парадонта организмами.
Для предотвращения инфицирования микроорганизмами способ в соответствии с настоящим изобретением можно также применять для деколонизации поверхностей.
В качестве примера, контакт пациентов с иммуносупрессией с зараженными изделиями часто приводит к развитию инфекции, поскольку пациенты с иммунодепрессией, как правило, чувствительны инфекциям, например, даже при низком количестве бактерий. В частности, поверхности медицинских изделий, предпочтительно медицинских принадлежностей или стоматологических принадлежностей, более предпочтительно медицинских принадлежностей для инвазивного применения, таких как катетеры, полые зонды, трубки или иглы, необходимо дезинфицировать перед их введением в тело человека.
Соответственно, в более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют для инактивации микроорганизмов на поверхностях медицинских изделий, предпочтительно медицинских изделий для инвазивного применения, таких как, например, контактные линзы, хирургические инструменты, стоматологические боры, стоматологические зеркала, кюретки, стоматологические файлы, катетеры, полые зонды, трубки или иглы.
В предпочтительном варианте медицинские изделия выбирают из раневых покрытий, перевязочных материалов, хирургических инструментов, катетеров, полых зондов, трубок или игл.
В более предпочтительном варианте термин "медицинские изделия" следует также понимать как включающий зубные мосты, ложки для оттисков, окклюзионные капы (шины) или искусственные зубные изделия, например, протезы, коронки или импланты.
В предпочтительном варианте обработка поверхности изделий всех типов по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-дион согласно настоящему изобретения формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами, и/или покрытие и/или иммобилизация по меньшей мере одно производного 1,7-диарил-1,6-гептадиен-3,5-диона, применяемого в соответствии с настоящим изобретением, формулы (100) и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производным 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами на поверхности медицинский изделий и последующее облучение электромагнитным излучением при подходящей длине волны и плотности энергии, обеспечивает снижение, предпочтительно, предотвращение колонизации микроорганизмами обрабатываемых поверхностей.
В предпочтительном варианте обработку поверхности осуществляют путем атомизации, нанесения кистью, впрыскивания (инъекции), распыления, погружения или их комбинаций.
Облучение можно осуществлять непосредственно после обработки поверхности по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен- 3,5-дион согласно настоящему изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами, предпочтительно после нанесения по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производного 1,7- диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или соответствующей фармакологически приемлемой соли, и/или сложного эфира, и/или комплекса указанного соединения на поверхность и/или введения по меньшей мере одного производного 1,7- диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или соответствующей фармакологически приемлемой соли, и/или сложного эфира, и/или комплекса указанного соединения в поверхность одновременно с с и/или в более поздний момент времени, до или во время применения обработанного изделия, например, медицинского изделия.
В более предпочтительном варианте применения по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или соответствующей фармакологически приемлемой соли, и/или сложного эфира, и/или комплекса указанного соединения в раневых покрытиях и/или перевязочных материалах, например, хлопчатобумажной марли, в ходе или после применения раневого покрытия и/или перевязочного материала, которое содержит по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, можно осуществить облучение электромагнитным излучением при подходящей длине волны и плотности энергии, после чего происходит снижение количества микроорганизмов в области раны или обработанных частей кожи, предпочтительно, инактивация.
В более предпочтительном варианте реализации в дополнение к по меньшей мере одному производному 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одному производному 1,7-диарил-1,6-гептадиен-3,5-диона согласно изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующим фармацевтически приемлемым солям, и/или сложным эфирам, и/или комплексами, раневое покрытие и/или перевязочный материал содержит дополнительные компоненты, предпочтительно адсорбенты, например, альгинат кальция или вспененный полиуретан или другие фармацевтически приемлемые вещества.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют для инактивации микроорганизмов на поверхностях пищевой упаковки.
Примеры подходящей пищевой упаковки включает контейнеры, выполненные из стекла, металла, пластика, бумаги, картона или их комбинаций.
Перед запылением пищевым продуктом или напитком, подходящие контейнеры можно, например, обработать по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-дион согласно изобретения формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами затем облучить подходящим источником излучения, который дает электромагнитное излучение при подходящей длине волны и плотности энергии. Затем в продезинфицированный контейнера можно поместить подходящий пищевой продукт или напиток и запечатать контейнер.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют для инактивации микроорганизмов на поверхности пищевых продуктов.
Куркумин представляет собой одобренную пищевую добавку, имеющую номер Е100. Соответственно, модифицированные куркумины, например, производное 1,7-диарил-1,6- гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или производное 1,7- диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, в предпочтительном варианте также являются приемлемыми пищевыми добавками.
Примерами подходящих продуктов питания являются такие продукты питания, как мясо, рыба, яйца, семена, зерно, орехи, ягоды, специи, фрукты или овощи, которые могут вступать в контакт с патогенными видами бактерий, такими как Salmonella, Clostridium, Escherichia coli - или Camphylobacter. Преимуществом является то, что также можно осуществлять дезинфекцию инкубационных яиц.
Термин "желудочно-кишечная инфекция" используется для описания группы заболеваний, которые в первую очередь отличаются симптомами в верхней части желудочно-кишечного тракта, такими как рвота, понос и боли в животе. Желудочно-кишечные инфекции вызываются вирусами, бактериями или паразитами. Заражение патогенными микроорганизмами обычно происходит через зараженную воду и/или зараженную пищу.
Наиболее известными источниками желудочно-кишечных инфекций являются, например, Salmonella, Campylobacter или Escherichia coli, такие как, например, энтерогеморрагическая Escherichia coli (ЕНЕС). Диарея и рвота, обусловленные пищевым отравлением, в основном вызываются стафилококками.
Чаще всего патогены желудочно-кишечных инфекций, такие как сальмонелла, например, попадают в пищеварительный тракт человека через продукты питания. Авторы настоящего изобретения обнаружили, что применение способа в соответствии с настоящим изобретением позволяет эффективно удалять микроорганизмы с поверхности пищевых продуктов.
Сальмонелла, например, это бактерии, которые встречаются во всем мире. Вызываемое сальмонеллой заболевание представляет собой типичную инфекцию пищевых продуктов, которая вызывает диарею. Патогены размножаются в желудочно-кишечном тракте человека и животных. На неохлажденных пищевых продуктах сальмонелла может быстро размножаться. При определенных условиях бактерии попадают в пищу из-за плохой гигиены на кухне, например, через грязные разделочные доски и/или ножи.
Примерами продуктов питания, которые часто несут сальмонеллу, являются сырые, т.е. не полностью приготовленные яйца и яичные продукты, такие как майонез, кремы или салаты на основе яиц или сырого теста. Другими примерами продуктов питания, которые часто несут сальмонеллу, являются мороженое, сырое мясо, например, сырой фарш или тартар, сырые колбаски, например, копченая колбаса или салями. Овощные продукты питания также могут быть колонизированы сальмонеллой.
Кампилобактерии - это встречающиеся во всем мире бактерии, вызывающие инфекционную диарею. Виды кампилобактерии живут в основном в желудочно-кишечном тракте животных, которые, как правило, сами не болеют. Кампилобактерии является наиболее распространенной бактериальной причиной диареи в Германии.
Основным источником инфекции для кампилобактерии является потребление продуктов питания, которые заражены бактериями. Часто она передается через мясо птицы. Кампилобактерии не могут размножаться в продуктах питания, но камплобактерии могут выживать в течение некоторого времени в окружающей среде. Опять же, неправильная гигиена на кухне может привести к инфекции, например, через разделочные доски и/или ножу, которые не очищаются должным образом после приготовления сырого мяса.
Примерами пищевых продуктов, которые часто загрязнены кампилобактериями, являются недоготовленное мясо птицы и продукты из птицы, непастеризованное молоко или непастеризованные молочные продукты, фарш, который не был тщательно приготовлен, или свежие сырые колбасы, такие как копченая колбаса, а также загрязненная питьевая вода, например, из колодезной системы.
Энтерогеморрагическая кишечная палочка (ЕНЕС) присутствует в кишечнике таких жвачных животных, как крупный рогатый скот, овцы, козы или олени. Бактерии выводятся с фекалиями инфицированных животных. Поскольку кишечная палочка ЕНЕС имеет относительно слабую чувствительности, она может выживать в окружающей среде в течение нескольких недель. Они сохраняют инфеекционную способность и даже небольшого количества болезнетворных микроорганизмов достаточно для передачи инфекции. Шкура крупного рогатого скота и других жвачных животных может быть заражена следами фекалий. Если трогать и гладить животных, бактерии могут попасть на рука, а оттуда - в рот. Даже игры на лугах, где содержались жвачные животные, могут привести к заражению детей.
Применение способа в соответствии с настоящим изобретением позволяет осуществить фотодинамическую дезинфекцию поверхности обуви, например, подошвы.
Кроме того, авторы изобретения обнаружили, что способ в соответствии с настоящим изобретением также подходит для фотодинамической дезинфекции поверхностей животного происхождения, таких как шкура, кожа, мех, волокна или шерсть.
В качестве примера, из-за плохой гигиены рук бактерии ЕНЕС могут сохраняться на изделиях, до которых дотрагиваются, и оттуда может происходить их распространение.
Переход к человеку может происходить также с помощью продуктов питания, которые употребляются в пищу сырыми или недостаточно нагретыми. Примеры продуктов питания, которые часто загрязнены ЕНЕС - это непастеризованное молоко и непастеризованные молочные продукты, сырые или недостаточно приготовленные мясные продукты, такие как, например, говяжий фарш (например, гамбургеры) и разбросанные сырые колбасные изделия, например, чайные колбасы. Овощные продукты питания также часто загрязнены ЕНЕС, например, овощи, которые загрязнены патогенными микроорганизмами в результате оплодотворения или загрязненной воды, непастеризованные фруктовые соки, которые производятся из загрязненных фруктов, семена, которые используются для выращивания побегов, и все продукты питания, на которые патогенные микроорганизмы из загрязненных продуктов питания могут переноситься прямо или косвенно грязными руками или посудой для приготовления пищи.
Например, Clostridium difficile - это бактерия, которая встречается во всем мире. У здоровых людей Clostridium difficile представляет собой безвредную кишечную бактерию. Если конкурирующие виды нормальной микрофлоры кишечника подавляются антибиотиками, Clostridium difficile может размножаться и вырабатывать токсины, которые при некоторых обстоятельствах могут привести к угрожающей жизни диарее, например, антибиотикозависимому колиту, в частности, если диарея, вызванная антибиотиками, уже присутствует.
Clostridium difficile является одним из наиболее распространенных больничных патогенов (нозокомиальных патогенов). Кроме того, Clostridium difficile может образовывать устойчивые постоянные формы, так называемые споры, с помощью которых в определенных обстоятельствах бактерии могут выживать в течение многих лет вне желудочно-кишечного тракта. Соответственно, они могут также передаваться через такие предметы и поверхности, как, например, туалеты, дверные ручки, ручки и/или поручни, к которым прилипают болезнетворные микроорганизмы.
Описанных выше проблем можно избежать благодаря способу в соответствии с настоящим изобретением, поскольку применение способа в соответствии с настоящим изобретением эффективно удаляет болезнетворные патогены на зараженных поверхностях.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы применяют для инактивации микроорганизмов в области, например, чистой комнате или операционной. После введения в эту область, например, путем нанесения миста, распыления, впрыскивания или испарения, область можно облучить подходящим источником излучения, который генерирует электромагнитное излучение при подходящей длине волны и плотности энергии, после чего присутствующие микроорганизмы инактивируются.
В более предпочтительном варианте реализации по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, применяют для инактивации микроорганизмов в жидкости или жидком препарате. Примеры подходящие жидкости или жидкие препараты представляют собой эмульсионные краски, охлаждающие жидкости, охлаждающие смазывающие вещества, смазывающие вещества, тормозные жидкости, краски, клеи или масла. В предпочтительном варианте жидкий препарат представляет собой водный препарат.
В предпочтительном варианте жидкость представляет собой воду.
Соответственно, по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы можно применять для подготовки воды в производстве напитков и пищевых продуктов, фармацевтических препаратов, химической и косметической промышенности, и электрической промышленности. Кроме того, по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы можно применять для подготовки питьевой воды и дождевой воды, для обработки сточных вод или для подготовки воды для применения в технологиях кондиционирования воздуха.
В предпочтительном варианте применения по меньшей мере одно производное 1,7- диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-дион согласно изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, жидкости или жидкие препараты можно затем облучать подходящим источником излучения, который генерирует электромагнитное излучение при подходящей длине волны и плотности энергии. В предпочтительном варианте по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы обеспечивают самодезинфекцию жидкости или жидкого препарата в ходе облучения.
В дополнительно предпочтительном варианте применения по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или по меньшей одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемых солей, и/или сложных эфиров, и/или комплексов, указанное производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или указанное производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы могут быть фиксированы на твердой подложке и, соответственно, могут применяться в составе твердой матрицы.
В особенно предпочтительном варианте по меньшей мере одно производное 1,7-диарил- 1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), фиксированное на твердой подложке, и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-дион согласно изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), фиксированное на твердой подложке, и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы вводят в обрабатываемую жидкость, предпочтительно, воду или кровь.
В особенно предпочтительном варианте подложка представляет собой полимер, который несет по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, которые ковалентно присоединены. Эта композиция, содержащая подложку по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, проявляет противомикробную активность сразу после воздействия электромагнитного излучения при подходящей длине волны и плотности энергии.
Далее, настоящее изобретение относится к изделиям с покрытием или оболочкой, которые содержат или покрыты по меньшей мере одним производным 1,7-диарил-1,6- гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами. В предпочтительном варианте изделие содержит по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, и/или покрыто ими.
В предпочтительном варианте поверхность изделия с покрытием снабжена по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами.
В более предпочтительном варианте поверхность изделия с покрытием снабжена по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами.
Изделие с покрытием можно затем облучить подходящим источником излучения, которое генерирует электромагнитное излучение при подходящей длине волны и плотности энергии. В предпочтительном варианте указанное производное 1,7-диарил-1,6- гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или указанное производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы обеспечивают "самодезинфекцию" поверхности изделия с покрытием в ходе дезинфекции.
Соответственно облучение можно осуществлять непосредственно после обработки изделия с покрытием по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-дион согласно изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующими фармацевтически приемлемыми солями, и/или сложными эфирами, и/или комплексами, предпочтительно после нанесения указанного по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующих фармацевтически приемлемых солей, и/или сложных эфиров, и/или комплексов на поверхность изделия с покрытие и/или введения по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100) и/или формулы (101) и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующих фармацевтически приемлемых солей, и/или сложных эфиров, и/или комплексы на поверхность изделия с покрытием, и/или в более поздний момент времени, предпочтительно перед или во время применения изделия с покрытием.
Примерами подходящих изделий являются медицинские товары, упаковка пищевых продуктов, гигиенические изделия (предметы гигиены), текстиль, ручки, поручни, контактные линзы, строительные материалы, банкноты, монеты, игровые фишки, карточки, спортивное оборудование, текстиль, посуда, столовые приборы или электронные устройства.
Другими подходящими изделиями являются устройства или установки линий передачи воды и/или содержащие воду контейнеры, в которых, например, в ходе работы установки или блока, образуется конденсат.
Примерами подходящих изделий являются уплотнения, мембраны, экраны, фильтры, контейнеры и/или трубы для установок по производству горячей воды, распределители горячей воды, теплообменники, кондиционеры, увлажнители воздуха, холодильники, охлаждающие устройства, холодильники, диспенсеры для напитков, стиральные машины или сушильные аппараты.
Например, небольшие количества микроорганизмов, несмотря на фильтрацию поступающего извне воздуха, могут проникать в кондиционер и существовать там короткое время. Продукты метаболизма этих микроорганизмов могут вызывать затхлый и плесневый запах.
Далее, для работы кондиционера необходимо удалять из воздуха влагу и удерживать ее. Большая часть конденсата удаляется и, например, проходит через контур конденсата. Однако остаточная влага остается на поверхности испарителя кондиционера, в частности, это имеет место в пассажирском автомобиле, где кондиционер выключается только при выключении двигателя, после чего невозможно обеспечить выравнивание температур.
Микроорганизмы, которые попадают в испаритель из воздуха, например, споры грибов и/или бактерий, оказываются в идеальном теплом, влажном климате и могут бесконтрольно размножаться.
Некоторые плесени, например, несут риск для здоровья, поэтому следует регулярно дезинфицировать установки для кондиционирования воздуха и удалять присутствующие в них организмы путем осуществления способа в соответствии с настоящим изобретением.
При замене фильтра кондиционера, например, пылевого и/или пыльцевого фильтра, корпус фильтра и окружающие воздуховоды кондиционера можно очистить с помощью способа в соответствии с настоящим изобретением. Очистка испарителя установки кондиционирования воздуха с применением настоящего изобретения позволяет также удалить запахи, возникающие на воздухе установки кондиционирования воздуха.
Например, бактерии легионеллы - это бактерии, которые вызывают у человека различные симптомы, например, гриппоподобные симптомы или тяжелые легочные инфекции. Бактерии легионеллы предпочтительно размножаются при температуре от 25°С до 45°С. В частности, в искусственных водопроводных системах, таких как водопроводные трубы в зданиях, патогенные микроорганизмы находят хорошие условия для размножения из-за преобладающих там температур. Кроме того, бактерии легионеллы могут хорошо размножаться в отложениях и футеровках трубопроводов. В этом случае можно применять способ в соответствии с настоящим изобретением, например, в комбинации с методом удаления отложений и/или футеровки.
Бактерии легионеллы (Legionella) передаются распыленной водой, туманом. Капли, содержащие болезнетворные микроорганизмы, могут распространяться на воздухе и вдыхаться. Примеры возможных источников инфекции - горячее водоснабжение, в частности, душевые, увлажнители воздуха или водопроводные краны, а также градирни, кондиционеры или другие агрегаты, которые распыляют воду в капли воды, например, мистеры, туманные фонтаны, водяные объекты и т.п. Передача воды также возможна в плавательных бассейнах через водопады, горки, гидромассажные ванны и/или фонтаны. Заражение легионеллами можно предотвращать путем применения способа в соответствии с настоящим изобретением на поверхностях зараженных изделий.
Способ в соответствии с настоящим изобретением можно, например, применять в оборудовании или установках линий водоснабжения и/или емкостей для водоснабжения, например, в оборудовании или установках, которые используются в рыбоводстве.
Эпидемические заболевания рыбы являются примером огромной экономической угрозы для всех интенсивно работающих рыбных хозяйств, где выращиваемая рыба содержится в замкнутом пространстве. Для борьбы с болезнями рыб добавляют, например, антибиотики и/или химические добавки. Примерами используемых химических добавок являются гидроксид кальция, перекись водорода, препараты перуксусной кислоты, сульфат меди, хлорамины, карбонат натрия, хлорид натрия или формальдегид.
Для снижения применения вышеупомянутых антибиотиков и/или химических добавок по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы можно применять для фотодинамической дезинфекции оборудования или установок в рыбном хозяйстве, например, рыбных прудах, бассейнах, насосах, фильтрах, трубах, сетях, крючках или подложках. Аналогичным образом, рыбу и/или икру рыбы можно подвергать фотодинамической дезактивации.
Аналогично, террариумы, аквариумы, песок, гравий и/или зеленые растения можно подвергать фотодинамической дезинфекции дор и/или в процессе их применения.
Примеры подходящего электронного оборудования включают горячие пластины, пульты дистанционного управления, наушники, модули громкой связи, гарнитуры, мобильные телефоны или элементы управления, такие как кнопки, переключатели, сенсорные экраны или клавиши.
Примеры подходящих строительных материалов включают бетон, стекло, песок, гравий, облицовку стен, штукатурку, стяжку и т.п.
Примеры подходящих облицовок стен включают деревянные панели, плиты, массивные деревянные панели, древесноволокнистые плиты средней плотности, фанерные плиты, мультиплексные плиты, армированные волокнами бетонные плиты, гипсокартонные плиты, гипсокартонные плиты, а также пластиковые, пенопластовые или целлюлозные обои.
В качестве примере, по меньшей мере одно производное 1,7-диарил-1,6-гептадиен- 3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или, соответственно, его фармацевтически приемлемую соль, и/или эфир, и/или комплекс можно применять для удаления плесени.
В предпочтительном варианте поверхность, покрытую плесенью, обрабатывают по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемой солью, и/или сложным эфиром, и/или комплексами, а затем облучают подходящим источником излучения, который дает электромагнитное излучение при подходящей длине волны и плотности энергии, после чего происходит снижение количества, предпочтительно, инактивации, плесени на обработанных поверхностях.
В более предпочтительном варианте реализации частицы, покрытые по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одним производным 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы, например, неорганические или органические частицы, образуют изделие с покрытием.
В более предпочтительном варианте частицы включают по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или, соответственно, их фармацевтически приемлемые соли, и/или эфиры, и/или комплексы, которые ковалентно связаны с указанными частицами.
В указанно предпочтительном варианте применения в соответствии с настоящим изобретением или способа в соответствии с настоящим изобретением, облучение микроорганизмов и по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6- гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), и/или, соответственно, их фармацевтически приемлемых солей, и/или эфиров, и/или комплексов электромагнитным излучением при подходящей длине волны и плотности энергии осуществляют в присутствии по меньшей одного соединения, являющегося донором кислорода, предпочтительно пероксида, и/или по меньшей мере одного кислород-содержащего газа, предпочтительно, кислорода.
По меньшей одно соединение, являющееся донором кислорода, и/или по меньшей мере один кислород-содержащий газ можно предпочтительно наносить (применять) до или во время облучения электромагнитным излучением при подходящей длине волны и плотности энергии.
За счет дополнительного обеспечения кислорода в форме по меньшей мере одного кислородсодержащего соединения и/или по меньшей мере одного кислородсодержащего газа до или в ходе облучения указанных микроорганизмов и по меньшей мере одного фотосенсибилизатора электромагнитным излучением при подходящей длине волны и плотности энергии, повышается выход активных форм кислорода (АФЕ, ROS), предпочтительно, радикалов кислорода и/или синглетного кислорода.
В соответствии с настоящим изобретением по меньшей мере одно производное 1,7-диарил-1,6-гептадиен-3,5-диона в соответствии с настоящим изобретением формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а) и/или их соответствующие фармацевтически приемлемые соли, и/или сложные эфиры, и/или комплексы можно применять в качестве медицинского средства.
Указанные фармакологически приемлемые комплексы предпочтительно представляют собой комплексы включения указанного по меньшей мере одного производного 1,7- диарил-1,6-гептадиен-3,5-диона для применения в соответствии с настоящим изобретением формулы (100), и/или формулы (101), и/или формулы (102), и/или по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), предпочтительно по меньшей мере одного производного 1,7-диарил-1,6-гептадиен-3,5-диона согласно изобретению формулы (1), и/или формулы (2), и/или формулы (3), и/или формулы (3а), с поливинилпирролидоном (PVP, ПВП), циклодекстринами или их смесями.
Подходящий способ получения комплексов включения соответствующих производных 1,7-диарил-1,6-гептадиен-3,5-дионв описан, например, в источнике:
S. Winter, N. Tortik, A. Kubin, В. Krammer, K. Plaetzer, Back to the roots: photodynamic inactivation of bacteria based on water-soluble curcumin bound to polyvinylpyrrolidone as a photosensitizer, Photochem. Photobiol. Sci., 2013,12, 1795-1802. DOI: 10.1039/C3PP50095K.
Настоящее изобретение проиллюстрировано приведенными ниже неограничивающими фигурами чертежей и примерами.
Фигура 1 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-0 гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 2 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием
SACUR-01a гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 3 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-01b гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 4 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-01c гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 5 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-01e гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 6 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-02 гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигуры 7а и 7b демонстрируют фотодинамическую инактивацию (PDI) E.coli под действием SACUR-03 гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 8 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-04 гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 9 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-05 гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 10 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-08 гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 11 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-09b гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 12 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-10а хлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 13 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-10b гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 14 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-10с хлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 15 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-11b гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 16 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-12a гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 17 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-13b гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 18 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием Zn-SACUR-1a гидрохлорида против E.coli в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 19 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием RO-SACUR-1a гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 20 демонстрирует фотодинамическую инактивацию (PDI) E.coli под действием SACUR-14b
гидрохлорида в сравнении с контролями (без света, без фотосенсибилизатора). Фигура 21 демонстрирует результаты анализа фототоксичности с применением SACUR-01a против Е. coli, АТСС 25922 (слева) и против S. aureus, АТСС 25923 (справа). Фигура 22 демонстрирует результаты анализа фототоксичности с применением SACUR-03 против Е. coli, АТСС 25922 (слева) и против S. aureus, АТСС 25923 (справа). Фигура 23 демонстрирует результаты анализа фототоксичности с применением SACUR-07 против Е. coli, АТСС 25922 (слева) и против S. aureus, АТСС 25923 (справа). Фигура 24 демонстрирует результаты анализа фототоксичности с применением SACUR-01a BF2 против S. aureus, АТСС 25923. Фигура 25 демонстрирует результаты анализа фототоксичности с применением SACUR-09a против S. aureus, АТСС 25923. Фигура 26 демонстрирует результаты анализа фототоксичности с применением SACUR-11a against S. aureus АТСС 25923. Фигура 27 демонстрирует результаты анализа фототоксичности с применением SACUR-11C против S. aureus, АТСС 25923. Фигура 28 демонстрирует результаты анализа фототоксичности с применением SACUR-12b against S. aureus, АТСС 25923. Фигура 29 демонстрирует результаты анализа фототоксичности с применением SACUR-13a против S. aureus, АТСС 25923. Фигура 30 демонстрирует результаты анализа фототоксичности с применением SACUR-13C против S. aureus, АТСС 25923. Фигура 31 демонстрирует результаты анализа фототоксичности с применением SACUR-14a против S. aureus, АТСС 25923. Фигура 32 демонстрирует результаты анализа фототоксичности с применением SACUR-15a против S. aureus, АТСС 25923. Фигура 33 демонстрирует результаты анализа фототоксичности с применением SACUR-15b против S. aureus, АТСС 25923.
Пример 1) Получения различных производных 1,7-диарил-1,6-гептадиен-3,5-диона.
Общая схема синтеза
Все химикаты были закуплены у традиционных поставщиков (TCI, ABCR, Acros, Merck и Fluka) и использовались без дальнейшей очистки. Растворители дистиллировали перед использованием и при необходимости сушили обычным способом. Сухой ДМФА приобретали в компании Fluka (Тауфкирхен, Германия).
Тонкослойную хроматографию проводили на тонкопленочных алюминиевых фольгах, покрытых силикагелем 60 F254 фирмы Merck (Дармштадт, Германия). Препаративную тонкослойную хроматографию проводили на имеющихся в продаже стеклянных пластинах, покрытых силикагелем 60 (20 см × 20 см, Carl Roth GmbH & Со. кг, Карлсруэ, Германия). Соединения детектировали с использованием ультрафиолетового света (=254 нм, 333 нм), а некоторые из них определяли невооруженным глазом или окрашивали нингидрином. Хроматографию проводили с помощью силикагеля (0.060-0.200) от компании Acros (Waltham, США).
ЯМР-спектры регистрировали на спектрометре Bruker Avance 300 (300 МГц [1Н-ЯМР], 75 МГц [13С-ЯМР]) (Bruker Corporation, Беллерика, США).
Все химические сдвиги приведены в δ [ppm] относительно внешнего стандарта (третра-метилсилан, TMS). Константы связи, соответственно, приведены в Гц; характеристика сигналов: s = синглет, d = дублет, t = триплет, m = мультиплет, dd = дублет дублетов, br = широкий. Относительное число атомов опрелеляли интеграцией. Окончательная идентификация сигналов в углеродных спектрах осуществлялась методом DEPT (угол импульса: 135°). Пределы погрешности: 0.01 ppm в течение 1Н-ЯМР, 0.1 ppm в течение 13С-ЯМР и 0.1 Гц для констант связи. Используемый Растворитель представляет собой указанный для каждого спектра.
Инфракрасные спектры регистрировали на спектрометре Biorad Excalibur FTS 3000 spectrometer (Bio-Rad Laboratories GmbH, Мюнхен, Германия).
ЭР-МС измеряли на спектрометре ThermoQuest Finnigan TSQ 7000, все МСВР определяли на спектрометре ThermoQuest Finnigan MAT 95 (соответственно, Thermo Fisher Scientific Inc, Уолтхэм, США); в качестве ионизирующего газа для бомбардировки ускоренными атомами применяли аргон.
Точки плавления определяли с помощью специального инструмента 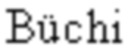 SMP-20 (Bűchi Labortechnik GmbH, Эссен, Германия) с использованием стеклянного капилляра.
SMP-20 (Bűchi Labortechnik GmbH, Эссен, Германия) с использованием стеклянного капилляра.
Все УФ/ВИД спектры регистрировали с использованием спектрометра Varian Cary 50 Bio UV/VIS; флуоресцентные спектры регистрировали с использованием спектрометра Varian Cary Eclipse.
Растворители для проведения специального класса спектроскопической чистоты измерений поглощения и испускания были приобретены в специальном у компаний Acros или Baker, или Uvasol у компании Merck. Для всех измерений использовалась миллипористая вода (18 MΩ, Milli QPIus).
1. Синтез альдегидных компонентов
Реагенты и алкилирующие реагенты, перечисленные в Таблице 1, приобретали из коммерческих источников.
В качестве алкилирующих реагентов использовали соответствующие алкилбромиды или алкилтозилаты.
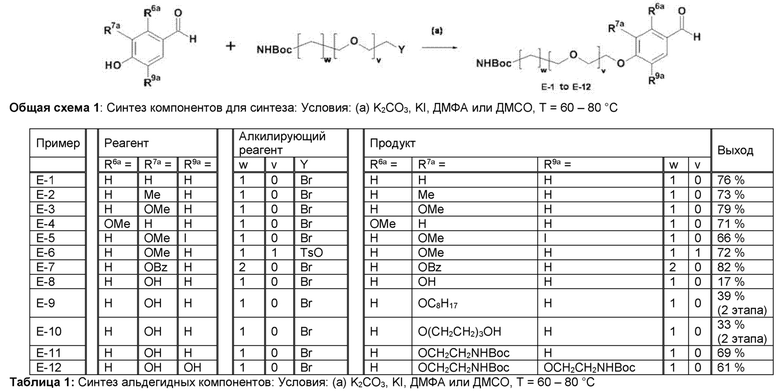
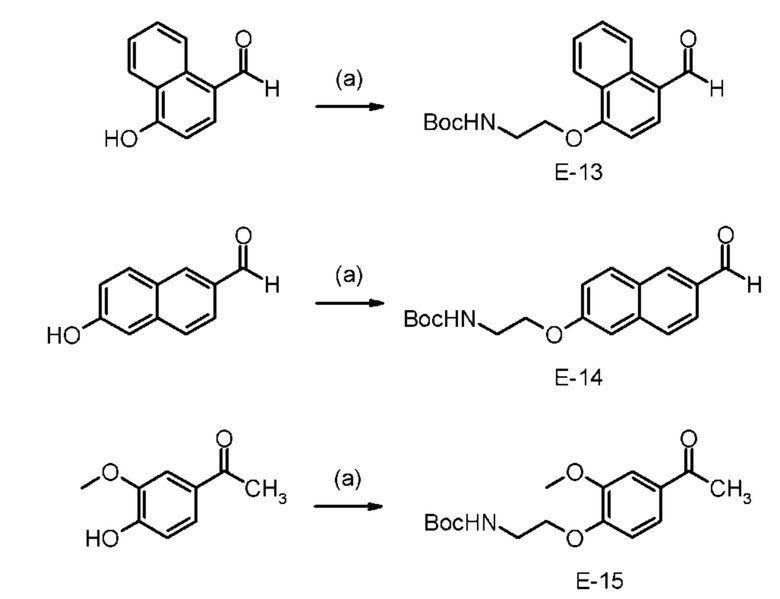
Общая схема 2: Синтез дополнительных альдегидных компонентов: Условия: (а) К2СО3, KI, ДМФА или ДМСО, Т=60-80°С
1.1 Замещенные ванилины
1.1.1 Общая процедура:
10 ммоль соответствующего реагента помещали в атмосфере азота в 20 мл диметил-формамида:
(I) 4-гидроксибензальдегид (1.22 г, 10 ммоль)
(II) ванилин (1.52 г, 10 ммоль)
(III) бензилоксиванилин (2.28 г, 10 ммоль)
(IV) 6-гидрокси-2-нафтальдегид (1.72 г, 10 ммоль)
(V) 4-гидрокси-3-метокси-ацетофенон (1.66 г, 10 ммоль)
Последовательно добавляли соответствующий алкилирующий реагент (12-15 ммоль, 1.2-1.5 экв.) в ДМФА (10 мл) и К2СО3 (2.76 г, 20 ммоль). Смесь перемешивали в атмосфере азота в течение 24 ч при 80°С. После охлаждения до комнатной температуры Реакционную смесь разбавляли 60 миллилитрами этилацетата и перемешивали органическую фазу трижды, каждый раз с 40 миллилитрами насыщенного водного раствора хлорида натрия, и один раз с 50 миллилитрами воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе.
Для очистки продукта осуществляли колоночную хроматографию на силикагеле.
Е-1: 4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
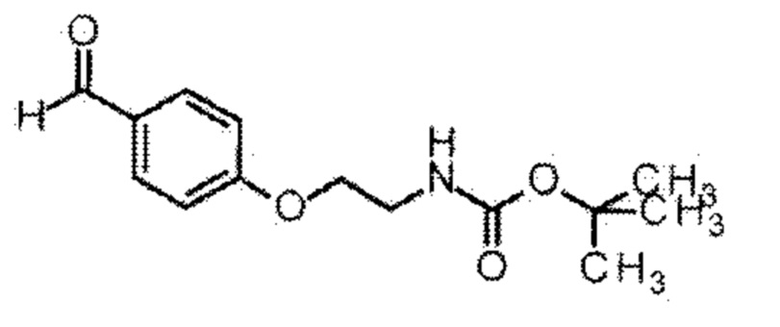
Реагент: 4-гидроксибензальдегид.
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этилбромид (3.34 г, 15 ммоль).
Выход: 76% теоретического, 2.5 г бледно-желтого твердого вещества
Молекулярная масса = 265.30 г/моль; Эмпирическая формула = C14H19NO4
1Н-ЯМР (300 МГц, CDCl3), δ=9.87 (s, 1Н), 7.82 (d, J=8.8 Гц, 2Н), 6.98 (d, J=8.7 Гц, 2Н), 5.05 (s, 1Н), 4.09 (t, J=5.2 Гц, 2Н), 3.55 (dd, J=10.4, 5.1 Гц, 2Н), 1.44 (s, 9Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 288.1 (17%, MNa+), 265.1 (1%, МН+), 210.1 (100%, МН+-С4Н9), 166.1 (19%, МН+-boc).
Е-3: 3-метокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
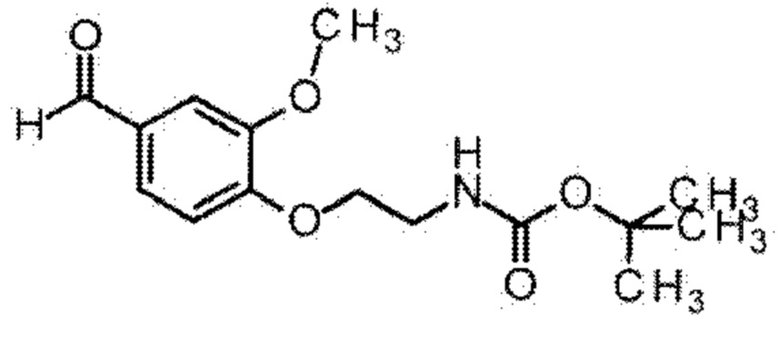
Реагент: ванилин (4-гидрокси-3-метоксибензальдегид).
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этилбромид (3.34 г, 15 ммоль).
Выход: 79% теоретического, 2.54 г бледно-желтого твердого вещества
Молекулярная масса = 295.34 г/моль; Эмпирическая формула = C15H21NO5
1Н-ЯМР: (300 МГц, CDCl3), δ=9.85 (s, 1Н), 7.43 (d, J=1.8 Гц, 1Н), 7.42 (m, 1Н), 6.98 (d, J=8.0 Гц, 1Н), 5.10 (s, 1Н), 4.15 (t, J=5.1 Гц, 2Н), 3.92 (s, 3Н), 3.60 (dd, J=10.6, 5.3 Гц, 2Н), 1.44 (s, 9H). MC: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 318.1 (13%, MNa+), 296.1 (100%, МН+), 240.1 (45%, МН+-С4Н9), 196.1 (9%, МН+-boc).
Е-15: 3-метокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)ацетофенон
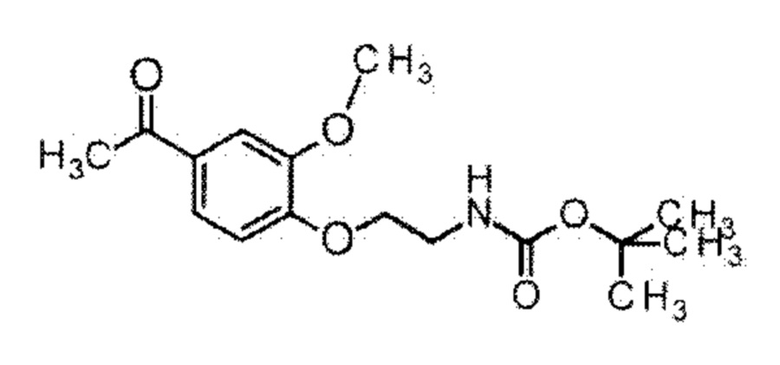
Получение в соответствии с А.1).
Реагент: 4-гидрокси-3-метоксиацетофенон (ацетованилон).
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этил бромид (3.34 г, 15 ммоль).
Выход: 77% теоретического, 2.75 г бледно-желтого твердого вещества
Молекулярная масса = 309.36 г/моль; Эмпирическая формула = C16H23NO5
1Н-ЯМР: (300 МГц, CDCl3), δ=7.51 (d, J=1.9 Гц, 1Н), 7.49 (s, 1Н), 6.94 (d, J=7.9 Гц, 1Н), 5.19 (s, 1Н), 4.12 (t, J=5.1 Гц, 2Н), 3.89 (s, 3Н), 3.58 (q, 5.3 Гц, 2Н), 2.52 (s, 3Н), 1.43 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 332.1 (29%, MNa+), 309.1 (2%, МН+), 254.1 (33%, МН+-С4Н9), 210.1 (100%, МН+-boc).
Е-14: 6-(2-N-трет-бутилоксикарбонил-аминоэтокси)нафталин-2-карбальдегид
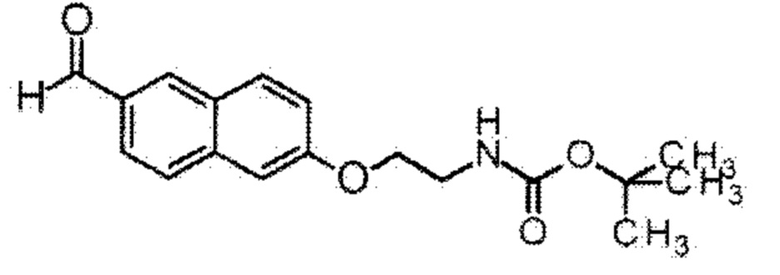
Реагент: 6-гидрокси-2-нафтальдегид.
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этилбромид (3.34 г, 15 ммоль).
Выход: 71% теоретического, 2.30 г бледно-желтого твердого вещества
Молекулярная масса = 315.37 г/моль; Эмпирическая формула = C18H21NO4
1Н-ЯМР: (300 МГц, CDCl3), δ=10.09 (s, 1Н), 8.25 (s, 1Н), 7.94-7.85 (m, 2Н), 7.79 (d, J=8.5 Гц, 1Н), 7.23 (dd, J=8.9, 2.5 Гц, 1Н), 7.17 (d, J=2.3 Гц, 1Н), 5.05 (s, 1Н), 4.18 (t, J=5.1 Гц, 2Н), 3.62 (dd, J=10.5, 5.3 Гц, 2Н), 1.46 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 338.2 (11%, MNa+), 316.2 (12%, МН+), 260.1 (100%, МН+-С4Н9), 216.1 (14%, МН+-boc).
Е-7: 3-бензилокси-4-(2-N-трет-бутилоксикарбонил-аминопропилокси)бензальдегид
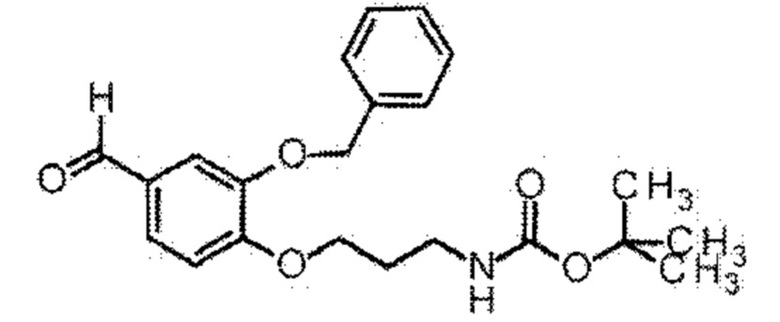
Реагент: бензилоксиванилин (4-бензилокси-3-метоксибензальдегид).
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)пропилбромид (3.34 г, 15 ммоль).
Выход: 82% теоретического, 2.64 г бледно-желтого твердого вещества
Молекулярная масса = 385.45 г/моль; Эмпирическая формула = C22H27NO5
1Н-ЯМР: (300 МГц, CDCl3), δ=9.74 (s, 1Н), 7.44-7.16 (m, 7Н), 6.91 (dd, J=8.1, 1.4 Гц, 1Н), 5.47 (s, 1Н), 5.21 (m, 2Н), 4.08 (td, J=5.6, 2.2 Гц, 2Н), 3.33 (d, J=5.2 Гц, 2Н), 2.03-1.92 (m, 2Н), 1.36 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 408.2 (37%, MNa+), 386.1 (2%, МН+), 330.1 (63%, МН+-С4Н9), 286.1 (100%, МН+-boc).
Е-6: 3-метокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси-этокси)бензальдегид
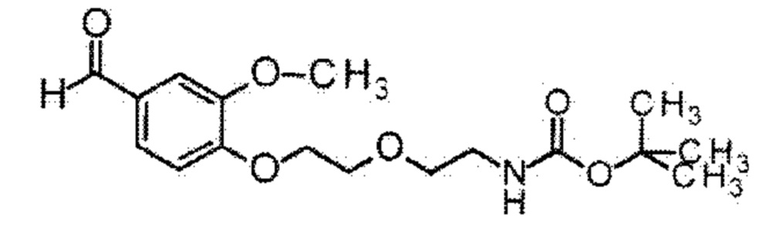
Реагент: ванилин (4-гидрокси-3-метоксибензальдегид).
В качестве алкилирующего реагента использовали 2-[2-(трет-бутоксикарбониламино)этокси]этил-4-метил бензолсульфонат (4.26 г, 12 ммоль).
Выход: 72% теоретического; 2.78 г бледно-желтого твердого вещества
Молекулярная масса = 339.39 г/моль; Эмпирическая формула = C17H25NO6
1Н-ЯМР: (300 МГц, CDCl3), δ=9.76 (s, 1Н), 7.42-7.26 (m, 2Н), 6.92 (d, J=8.1 Гц, 1Н), 5.08 (s, 1Н), 4.21-4.12 (m, 2Н), 3.86-3.78 (m, 2Н), 3.84 (s, 3Н), 3.54 (dd, J=7.4, 2.6 Гц, 2Н), 3.26 (m, 2H), 1.35 (s, 9H). MC: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 356.9 (100%, MNH4+), 339.9 (41%, МН+), 239.9 (6%, MH+-boc).
1.1.2 Общая процедура:
15 ммоль соответствующего реагента помещали в атмосфере азота в 10 мл диметил-формамида:
(VI) 4-гидрокси-3-метил-бензальдегид (2.04 г, 15 ммоль)
(VII) 4-гидрокси-2-метокси-бензальдегид (2.28 г, 15 ммоль)
Последовательно добавляли соответствующий алкилирующий реагент (12-15 ммоль, 1.2-1.5 экв.) в ДМФА (20 мл) и К2СО3 (4.14 г, 30 ммоль). Смесь перемешивали в атмосфере азота в течение 24 ч при 80°С. После охлаждения до комнатной температуры реакционную смесь разбавляли 120 миллилитрами этилацетат ии перемешивали органическую фазу трижды, каждый раз с 40 миллилитрами насыщенного водного раствора хлорида натрия, и один раз с 40 миллилитрами воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Для очистки продукта осуществляли колоночную хроматографию на силикагеле.
Е-2: 3-метил-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
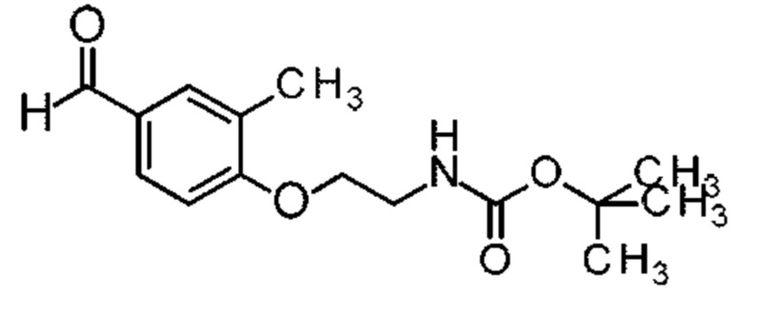
Реагент: 4-гидрокси-3-метил-бензальдегид.
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этил бромид (5.02 г, 22.5 ммоль).
Выход: 73% теоретического, 3.44 г желтоватого твердого вещества
Молекулярная масса = 279.34 г/моль; Эмпирическая формула = C15H21NO4
1Н-ЯМР: (300 МГц, CDCl3), δ=9.85 (s, 1Н), 7.75-7.66 (m, 2Н), 6.90 (d, J=8.9 Гц, 1Н), 4.95 (s, 1Н), 4.11 (t, J=5.2 Гц, 2Н), 3.59 (m, 2Н), 2.27 (s, 3Н), 1.45 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 302.1 (11%, MNa+), 280.1 (9%, МН+), 224.1 (100%, МН+-С4Н9), 180.1 (4%, МН+-boc).
Е-4: 2-метокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
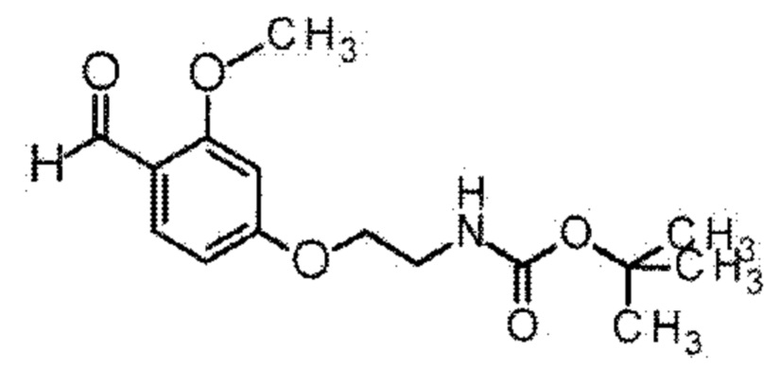
Реагент: 4-гидрокси-2-метокси-бензальдегид.
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этил бромид (5.02 г, 22.5 ммоль).
Выход: 71% теоретического, 3.94 г бледно-желтого твердого вещества
Молекулярная масса = 295.34 г/моль; Эмпирическая формула = C15H21NO5
1Н-ЯМР: (300 МГц, CDCl3), δ=10.25 (d, J=1.2 Гц, 1Н), 7.76 (dd, J=8.6, 1.5 Гц, 1Н), 6.58-6.46 (m, 1Н), 6.44 (s, 1Н), 5.06 (s, 1Н), 4.07 (t, J=5.0 Гц, 2Н), 3.87 (s, 3Н), 3.53 (m, 2Н), 1.43 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН+10 ммоль NH4OAc): 318.1 (8%, MNa+), 296.1 (100%, МН+), 240.1 (87%, МН+-С4Н9), 196.1 (3%, МН+-boc).
Е-5: 3-метокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)-5-йодо-бензальдегид
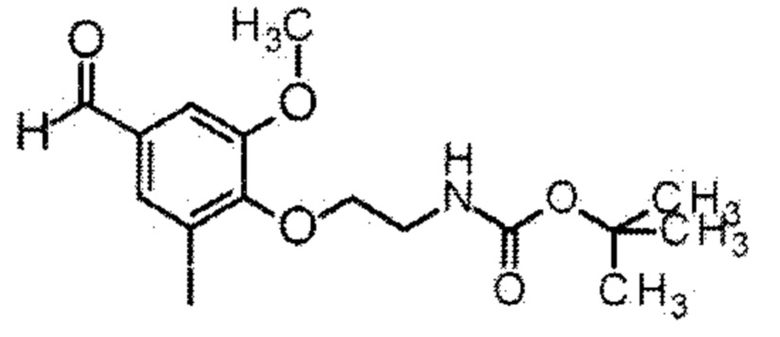
5-йодованилин (4.17 г, 15 ммоль) помещали в атмосфере азота в 10 мл диметилформамида.
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этил бромид (5.02 г, 22.5 ммоль), растворенный в 20 мл диметилформамида. Последовательно добавляли алкилирующий реагент и К2СО3 (4.14 г, 30 ммоль). Смесь перемешивали в атмосфере азота в течение 24 ч при 80°С. После охлаждения до комнатной температуры Реакционную смесь разбавляли 120 миллилитрами этилацетата и перемешивали органическую фазу трижды, каждый раз с 40 миллилитрами насыщенного водного раствора хлорида натрия, и один раз с 40 миллилитрами воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Для очистки продукта осуществляли колоночную хроматографию на силикагеле.
Выход: 66% теоретического, 3.07 г желтого твердого вещества
Молекулярная масса = 421.23 г/моль; Эмпирическая формула = C15H20INO5
1Н-ЯМР: (300 МГц, CDCl2), δ=9.82 (s, 1Н), 7.84 (d, J=1.7 Гц, 1H), 7.39 (d, J=1.8 Гц, 1H), 5.40 (s, 1Н), 4.17 (t, J=4.9 Гц, 2H), 3.91 (s, 3Н), 3.52 (dd, J=10.3, 5.3 Гц, 2H), 1.45 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 444.1 (6%, MNa+), 422.1 (3%, МН+), 366.0 (63%, МН+-С4Н9), 322.0 (100%, МН+-bос).
1.2 Полизамещенные альдегиды
Соответствующий реагент помещали в атмосфере азота в 10 мл диметилформамида:
(VIII) 3,4-дигидроксибензальдегид (3.45 г, 25 ммоль)
(IX) 3,4,5-тригидроксибензальдегид (2.31 г, 15 ммоль)
В качестве алкилирующего реагента использовали 2-(трет-бутоксикарбониламино)этилбромид (11.2 г, 50 ммоль, 2 экв.), растворенный в 30 мл диметилформамида. Последовательно добавляли алкилирующий реагент К2СО3 (13.8 г, 100 ммоль) добавляли. Смесь перемешивали в атмосфере азота в течение 16 ч при 80°С. Добавляли вторую порцию алкилирующего реагента (50 ммоль, 2 экв.) в 20 мл диметилформамида и перемешивали смесь в течение еще 24 ч при 80°С. После охлаждения до комнатной температуры реакционную смесь разбавляли 250 миллилитрами этилацетата и перемешивали органическую фазу трижды, каждый раз с 150 миллилитрами насыщенного водного раствора хлорида натрия, и один раз со 100 миллилитрами воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Для очистки продукта осуществляли колоночную хроматографию на силикагеле (Реагент: сначала петролейный эфир: этилацетат = 3:1, затем, петролейный эфир: этилацетат = 3:2).
Е-11: 3,4-бис-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
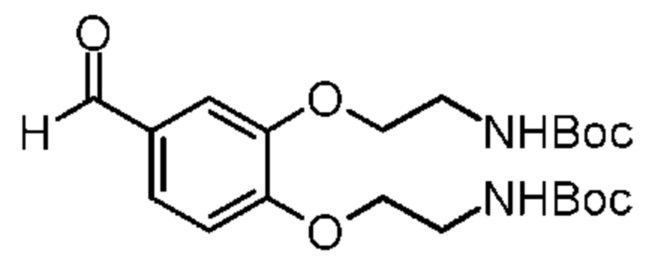
Реагент: 3,4-дигидроксибензальдегид
Выход: 8.1 г бледно-желтого стеклоподобного вещества, 69% теоретического
Молекулярная масса = 424.50 г/моль; Эмпирическая формула = C21H32N2O7
1Н-ЯМР: (300 МГц, CDCl3), δ=9.83 (s, 1Н), 7.52-7.37 (m, 2Н), 6.99 (d, J=8.2 Гц, 1Н), 5.20 (s, 2Н), 4.17-4.06 (m, 4Н), 3.56 (m, 4Н), 1.44 (s, 9Н), 1.43 (s, 9Н). МС: (ионизацияэлектрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 447.2 (100%, MNa+), 425.2 (70%, МН+), 369.2 (49%, МН+-С4Н9), 269.1 (78%, МН+-boc).
Е-12: 3,4,5-трис-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
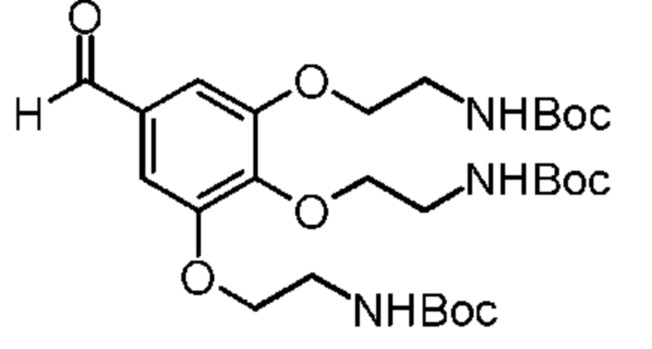
Реагент: 3,4,5-триидроксибензальдегид
Выход: 6.22 г бледно-желтого стеклообразного вещества, 61% теоретического
Молекулярная масса = 583.68 г/моль; Эмпирическая формула = C28H45N3O10
1Н-ЯМР: (300 МГц, CDCl3), δ=9.82 (s, 1Н), 7.11 (s, 2Н), 5.71 (s, 1Н), 5.21 (s, 2Н), 4.12 (t, J=4.6 Гц, 6Н), 3.62-3.51 (m, 4Н), 3.42 (d, J=4.9 Гц, 2Н), 1.44 (d, J=8.7 Гц, 27Н). МС: (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 606.3 (47%, MNa+), 584.3 (100%, МН+), 528.3 (4%, МН+-С4Н9), 484.3 (23%, МН+-boc).
1.3 Смешанный замещенный бензальдегиды
Этап 1:
3,4-дигидроксибензальдегид (3.45 г, 25 ммоль) помещали в атмосфере азота в 20 мл ди-метилформамида. Последовательно добавляли 2-(трет-бутоксикарбониламино)этилбромид (6.72 г, 30 ммоль) в 30 мл диметилформамида и К2СО3 (4.6 г, 33 ммоль) добавляли. Смесь перемешивали в атмосфере азота в течение 24 ч при 80°С. После охлаждения до комнатной температуры реакционную смесь разбавляли 150 миллилитрами этилацетат и перемешивали органическую фазу трижды, каждый раз со 100 миллилитрами насыщенного водного раствора хлорида натрия, и один раз со 100 миллилитрами воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Для очистки продуктов осуществляли колоночную хроматографию на силикагеле.
Е-8: 3-гидрокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
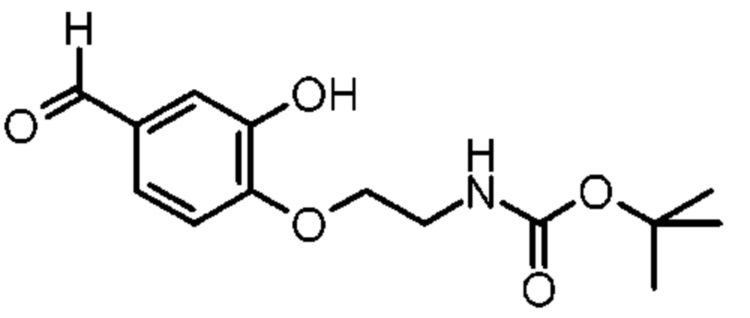
Выход: 1.48 г бледно-желтого стеклоподобного вещества, 17% теоретического Молекулярная масса = 281.31 г/моль; Эмпирическая формула = C14H19NO5
1Н-ЯМР: (300 МГц, CDCl3), δ=9.78 (s, 1Н), 7.42 (d, J=1.9 Гц, 1Н), 7.36 (dd, J=8.2, 1.9 Гц, 1Н), 7.14 (s, 1Н), 6.89 (d, J=8.2 Гц, 1Н), 5.53 (s, 1Н), 4.13 (t, J=4.9 Гц, 2Н), 3.58 (dd, J=10.6, 5.2 Гц, 2Н), 1.42 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 304.1 (19%, MNa+), 282.1 (2%, МН+), 226.1 (100%, МН+-С4Н9), 182.1 (42%, MH+-boc).
Е-8а: 4-гидрокси-3-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
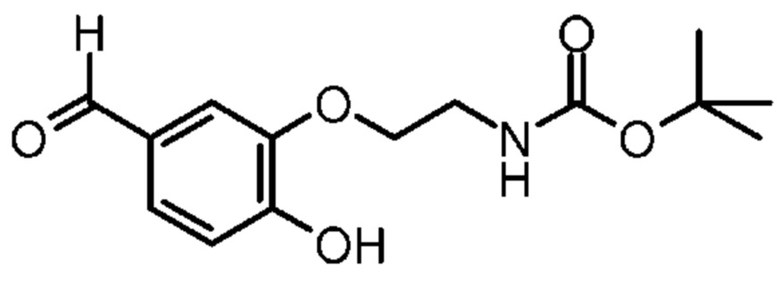
Выход: 2.60 г бледно-желтого стеклоподобного вещества, 37% теоретического
Молекулярная масса = 281.31 г/моль; - Эмпирическая формула = C14H19NO5
Е-11: 3,4-бис-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
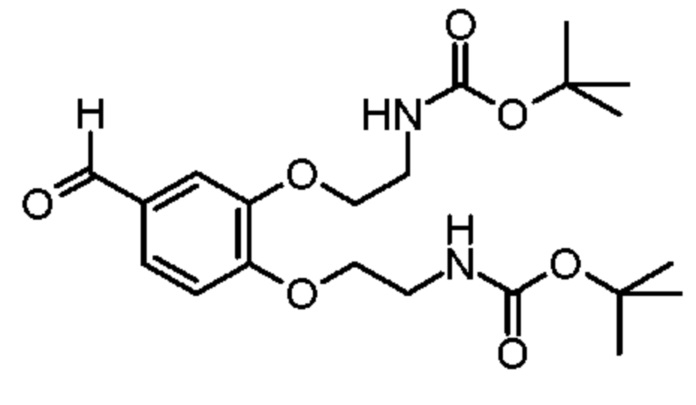
Выход: 1.38 г бледно-желтого стеклоподобного вещества, 13% теоретического
Молекулярная масса = 424.50 г/моль; Эмпирическая формула = C21H32N2O7
1Н-ЯМР и МС как описано выше.
Этап 2:
1.41 г (5 ммоль) 3-гидрокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегида (Е-8) помещали в атмосфере азота в 10 мл диметилформамида. Последовательно добавляли алкилирующий реагент, а именно триэтиленгликоль монотозилат или 1-бромоктанол, а также К2СО3 (2.07 г, 15 ммоль), растворяя каждый в 10 мл диметилформамида. Смесь перемешивали в атмосфере азота в течение 24 ч при 80°С. После охлаждения до комнатной температуры реакционную смесь разбавляли 80 миллилитрами этилацетат и перемешивали органическую фазу три раза, каждый раз 50 мл насыщенного водного раствора хлорида натрия, и один раз с 50 мл воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Для очистки продукта осуществляли колоночную хроматографию на силикагеле.
Е-10: 3-(2-(2-(2-гидрокси-этокси)этокси)этокси)-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
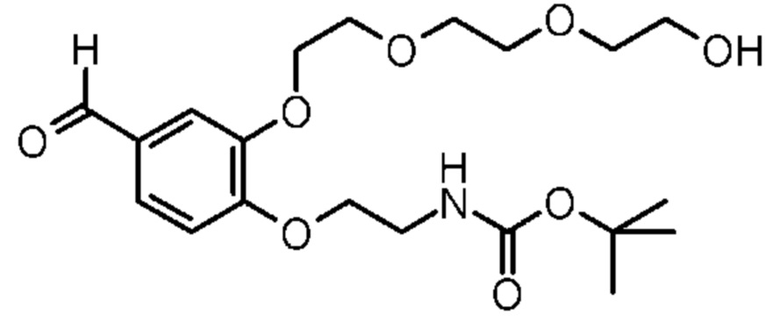
В качестве реагента для алкилирования использовали триэтиленгликоль монотозилат (3.04 г, 10 ммоль). Колоночная хроматография этиловым эфиром ЕЕ/EtOH = 3:1
Выход: 1.53 г бледно-желтого стеклообразного вещества, 74% теоретического
Молекулярная масса = 413.47 г/моль; Эмпирическая формула = C20H31NO8
1Н-ЯМР: (300 МГц, CDCl3), δ=9.83 (s, 1Н), 7.48-7.38 (m, 2Н), 6.96 (d, J=8.1 Гц, 1Н), 4.24 (dd, J=5.3, 3.4 Гц, 2Н), 4.12 (t, J=4.8 Гц, 2Н), 3.92 (dd, J=5.3, 3.4 Гц, 2Н), 3.74 (t, J=4.6 Гц, 6Н), 3.66-3.61 (m, 2Н), 3.58 (t, J=4.7 Гц, 2Н), 1.43 (s, 9Н). МС: (ионизация электро-распылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 436.2 (35%, MNa+), 414.2 (33%, МН+), 370.2 (5%, МН+-С4Н9), 314.2 (100%, МН+-boc).
Е-9: 3-октилокси-4-(2-N-трет-бутилоксикарбонил-аминоэтокси)бензальдегид
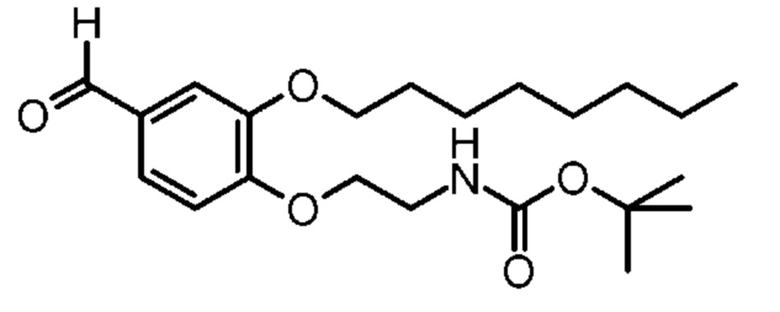
В качестве агента для алкилирования использовали 1-бромоктанол (1.93 г, 10 ммоль). Колоночная хроматография со смесью петролейный эфир: этилацетат = 3:1
Выход: 1.53 г бледно-желтого стеклообразного вещества, 78% теоретического
Молекулярная масса = 393.53 г/моль; Эмпирическая формула = C22H35NO5
1Н-ЯМР: (300 МГц, CDCl3), δ=9.81 (s, 1Н), 7.43-7.32 (m, 2Н), 6.96 (d, J=8.4 Гц, 1H), 4.11 (t, J=5.3 Гц, 2H), 4.02 (t, J=6.7 Гц, 2H), 3.55 (dd, J=10.2, 5.0 Гц, 2H), 1.91-1.76 (m, 2Н), 1.47-1.39 (m, 2Н), 1.42 (s, 9Н), 1.36-1.16 (m, 8Н), 0.90-0.80 (m, 3Н). МС: (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 416.2 (51%, MNa+), 396.2 (4%, МН+), 338.2 (7%, МН+-С4Н9), 294.2 (100%, МН+-boc).
1.4 Замещенный нафтальдегид
Е-13: 4-(2-N-трет-бутилоксикарбонил-аминоэтокси)нафталин-1-карбальдегид
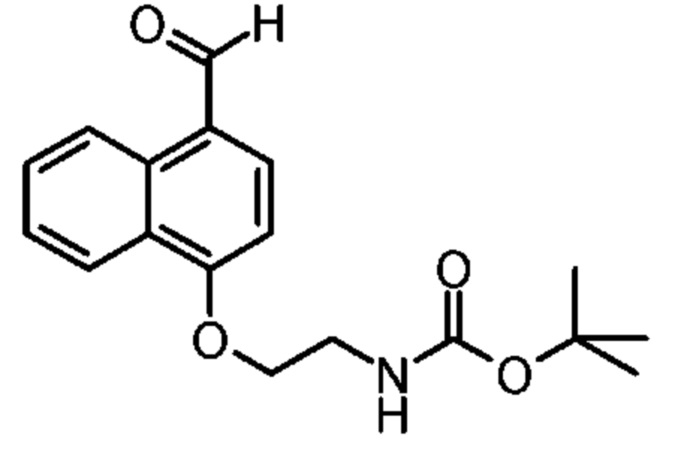
4-гидроксинафт-1-альдегид (1.74 г, 10 ммоль) помещали в атмосфере азота в 10 мл ди-метилформамида. Последовательно добавляли 2-(трет-бутоксикарбониламино)этилбромид (4.4 г, 20 ммоль) в 10 мл диметилформамида, йод ид калия (10 ммоль, 1.66 г) и Cs2CO3 (6.5 г,20 ммоль). Смесь перемешивали в атмосфере азота в течение 24 ч при 80°С. После охлаждения до комнатной температуры реакционную смесь разбавляли 80 миллилитрами этилацетат и встряхивали органическую фазу три раза, каждый раз с 50 мл насыщенного водного раствора хлорид натрия, и один раз со 100 миллилитрами воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Неочищенный продукт промывали смесью этиловый эфир/петролейный эфир 1:19 для удаления избытка реагента. Затем оранжевое твердое вещество экстрагировали смесь этиловый эфир/петролейный эфир 1:2 (3х, каждый раз использовали по 100 мл) и отфильтровывали преципитат. Раствор выпаривали на роторном испарителе, а остаток растворяли в 250 мл диэтилового эфира. Органическую фазу дважды встряхивали, каждый раз с 50 миллилитрами 3 М NaOH, и один раз со 100 миллилитрами воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Для дальнейшей очистки продукта осуществляли колоночную хроматографию на силикагеле. Выход: 2.08 г бледно-желтого твердого вещества, 47% теоретического
Молекулярная масса = 315.37 г/моль; Эмпирическая формула = C18H21NO4
1Н-ЯМР: (300 МГц, CDCl3),δ=10.19 (s, 1Н), 9.30 (d, J=8.5 Гц, 1H), 8.33 (d, J=8.4 Гц, 1H), 7.94-7.86 (m, 1Н), 7.76-7.64 (m, 1Н), 7.62-7.51 (m, 1Н), 6.94-6.82 (m, 1Н), 5.07 (s, 1Н), 4.29 (dd, J=6.9, 3.2 Гц, 2H), 3.73 (m, 2Н), 1.46 (s, 9Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 338.2 (16%, MNa+), 316.2 (19%, МН+), 260.1 (100%, МН+-С4Н9), 216.1 (4%, МН+-boc).
2. Синтез замещенных куркуминов
Соответствующие куркумины синтезировали с применением предварительных этапов, описанных выше, как куркумины, защищенные трет-бутилоксикарбонилом (boc). После этого защитную группу "Ьос" удаляли.
2.1 Синтез симметрично замещенных куркуминов
Общая схема 3: Синтез различных симметрично замещенных куркуминов: Условия: (а) ацетилацетон, В2О3, В(OBu)3, н-бутиламин, этилацетат, 80°С, 6 ч, затем гидролиз с использованием НОАс 40% в течение ночи, КТ; (b) ацетилацетон, В2О3, В(OBu)3, н-бутиламин, ДМФА, 80°С, 6 ч, затем гидролиз с использованием НОАс 40% в течение ночи, КТ; (с) 3,5-гептандион, В2О3, В(OBu)3, н-бутиламин, ДМФА, 80°С, 6 ч, затем гидролиз с использованием НОАс 40% в течение ночи, КТ; (d) ДХМ, ТФУК, КТ, 5 ч; затем ионообменная смола Amberlite IRA-958, вода.
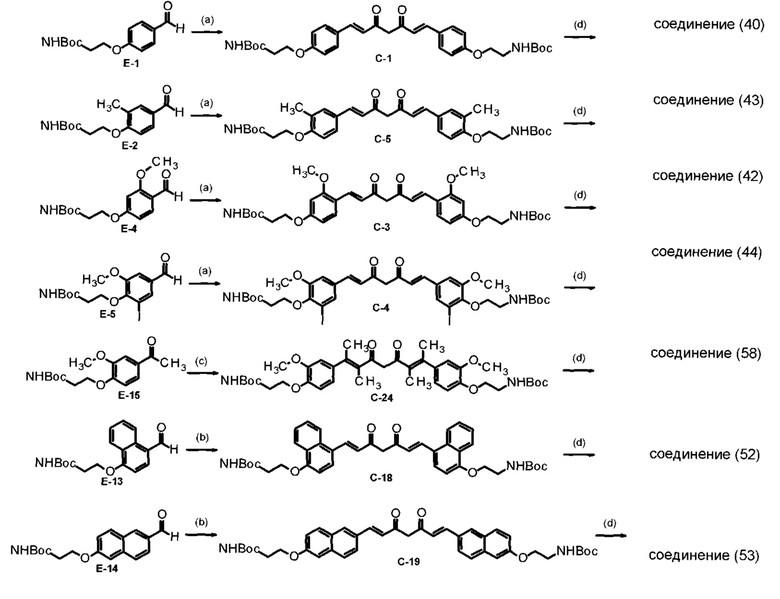
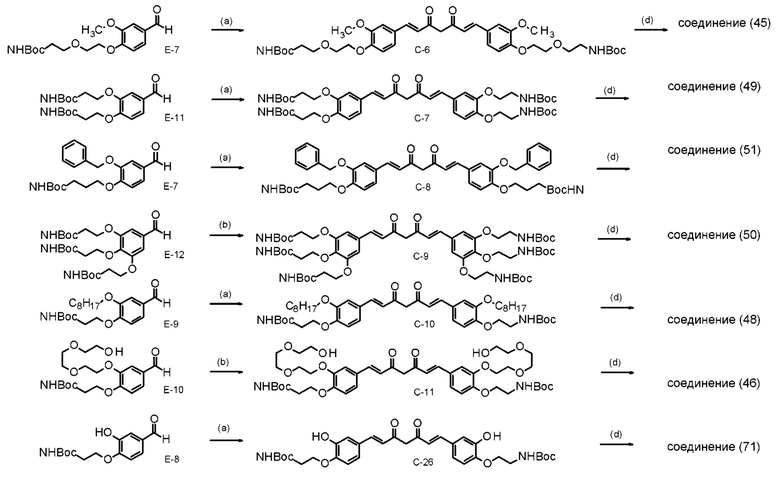
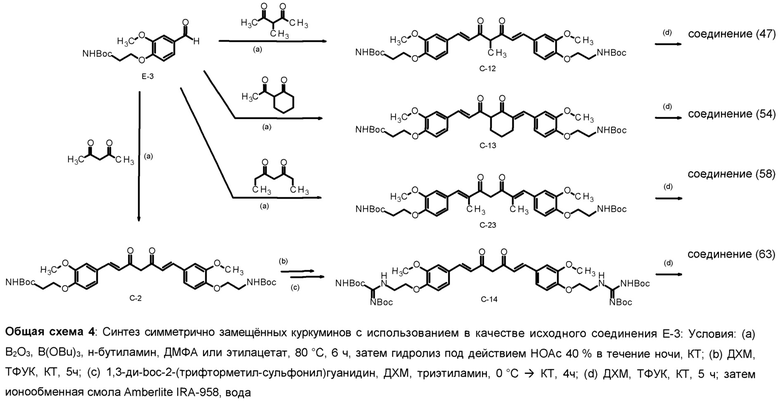
2.1.1 Общая процедура:
Ацетилацетон (0.1 г, 1 ммоль) и оксид бора В2О3 (0.07 г, 1 ммоль) растворяли в этилацетате (2 мл) и перемешивали в течение 30 минут при 50°С. Замещенный бензальдегид (20 ммоль) в этилацетате (3 мл) вместе с трибутилборатом (0.7 г, 3 ммоль) добавляли последовательно и перемешивали смесь в течение еще получаса. Затем добавляли по каплям н-бутиламин (0.1 мл в 1 мл этилового эфира) в течение 5 минут. После перемешивания в течение еще пяти ч при 50°С реакционную смесь оставляли выстояться в течение ночи. Раствор выпаривали на роторном испарителе, а остаток быстро высушивали в высоком вакууме. Добавляли 10 мл этилацетата на 1 г неочищенного продукта и растворяли неочищенный продукт. Для последующего гидролиза комплекса бора добавляли двойной объем 50% уксусной кислоты (20 мл на 1 г неочищенного продукта). После перемешивания в течение 24 ч при комнатной температуре при защите от света, смесь растворителей удаляли при пониженном давлении. Остаток экстрагировали три раза этиловым эфиром (3х 20 мл) и отфильтровывали нерастворимую соль. Объединенные органические фазы промывали водой (30 мл), сушили при помощи MgSO4 и наконец, удаляли растворитель при пониженном давлении. Очистку осуществляли при помощи колоночной хроматографии на силикагеле с использованием комбинации ацетон/петролейный эфир. Затем полученную очищенную фракцию куркумина растворяли в минимально возможном количестве этилацетата. Добавление по каплям этого раствора в избыток петролейного эфира приводило к осаждению продукта в виде тонкого желто-оранжевого порошка.
1,7-бис(3,4-диметоксифенил)гепта-1,6-диен-3,5-дион (третраметоксикуркумин)
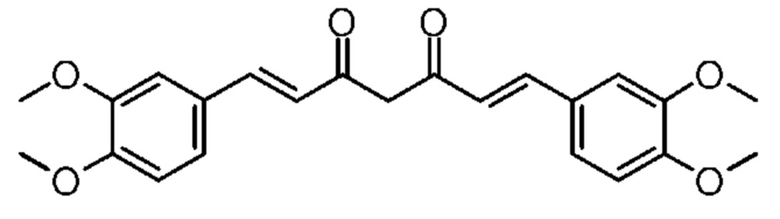
Количество соответствующего используемого альдегида: 334 мг = 2 ммоль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 2:5 → 1:2
Выход: 289 мг, 73% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок. Молекулярная масса = 396.44 г/моль; Эмпирическая формула = С23Н24О6
С-1: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-фенил]-3,5-диоксо-гепта-1,6-диенил}-фенокси)-этил1-карбаминовой кислоты трет-бутиловый эфир
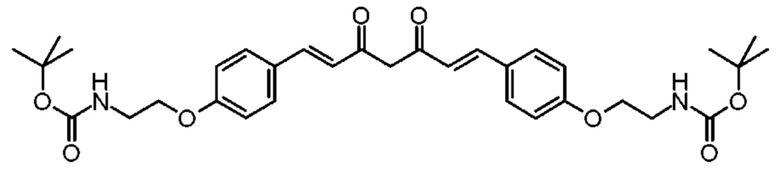
Количество соответствующего используемого альдегида Е-1: 530 мг =2 ммоль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 2:3
Выход: 363 мг, 67% теоретического, желтое твердое вещество или желтый порошок
Молекулярная масса = 594.71 г/моль; Эмпирическая формула = C33H42N2O8
1Н-ЯМР: (300 МГц, CDCl3), δ=7.61 (d, J=15.8 Гц, 2Н), 7.50 (d, J=8.8 Гц, 4Н), 6.89 (d, J=8.7 Гц, 4Н), 6.50 (d, J=15.8 Гц, 2Н), 5.02 (s, 2Н), 4.05 (t, J=5.1 Гц, 4Н), 3.60-3.48 (m, 4Н), 1.45 (s, 18Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAC): 595.3 (100%, МН+), 539.2 (18%, МН+-С4Н9).
С-5: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-метил-фенил]-3,5-диоксо-гепта-1,6-диенил}-2-метил-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
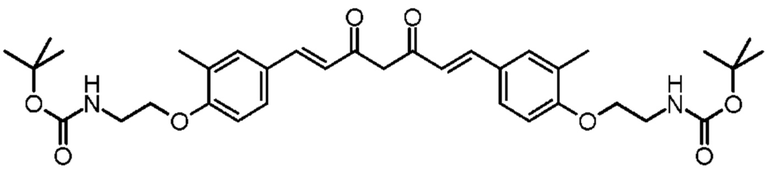
Количество соответствующего используемого альдегида Е-2: 559 мг = 2 ммоль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 2:3
Выход: 442 мг, 59% теоретического, оранжево-желтое твердое вещество или оранжево-желтый порошок. Молекулярная масса = 622.77 г/моль; Эмпирическая формула = C35H46N2O8
1Н-ЯМР: (300 МГц, CDCl3), δ=7.59 (d, J=15.8 Гц, 2Н), 7.36 (d, J=10.8 Гц, 4Н), 6.80 (d, J=8.3 Гц, 2Н), 6.49 (d, J=15.8 Гц, 2Н), 4.94 (s, 2Н), 4.06 (t, J=5.0 Гц, 4Н), 3.58 (m, 4Н), 2.25 (s, 6Н), 1.46 (s, 18Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 623.3 (100%, МН+), 567.3 (21%, МН+-С4Н9).
С-3: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-2-октилокси-фенил]-3,5-диоксо-гепта-1,6-диенил}-3-октилокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
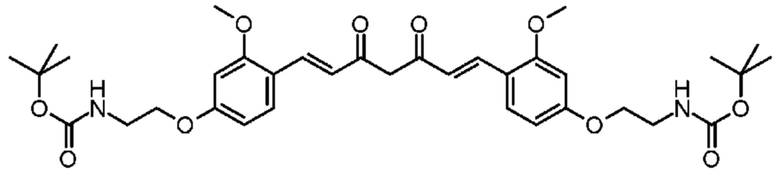
Количество соответствующего используемого альдегида Е-4: 591 мг = 2 ммоль Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 2:3
Выход: 393 мг, 58% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок. Молекулярная масса = 654.76 г/моль; Эмпирическая формула = C35H46N2O10
1Н-ЯМР: (300 МГц, CDCl3), δ=7.89 (d, J=16.0 Гц, 2Н), 7.47 (d, J=8.5 Гц, 2Н), 6.62 (d, J=16.0 Гц, 2Н), 6.52-6.39 (m, 4Н), 4.99 (s, 2Н), 4.06 (t, J=5.1 Гц, 4Н), 3.88 (s, 6Н), 3.55 (m, 4Н), 1.45 (s, 18Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 655.3 (100%, МН+).
С-4: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-метокси-5-йодофенил]-3,5-диоксо-гепта-1,6-диенил}-2-октилокси-6-йодофенокси)-этил1-карбаминовой кислоты трет-бутиловый эфир
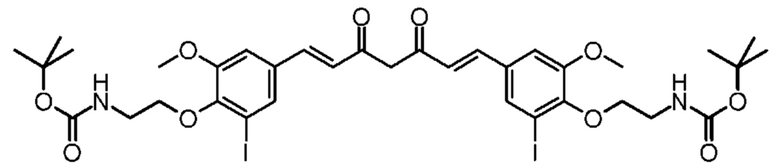
Количество соответствующего используемого альдегида Е-5: 842 мг = 2 ммоль Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:4 → 1:2
Выход: 580 мг, 64% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок. Молекулярная масса = 906.56 г/моль; Эмпирическая формула = C35H44I2N2O10
1Н-ЯМР: (300 МГц, CDCl3), δ=7.57 (d, J=1.5 Гц, 2Н), 7.50 (d, J=15.8 Гц, 2Н), 7.02 (d, J=1.5 Гц, 2Н), 6.51 (d, J=15.8 Гц, 2Н), 5.47 (s, 2Н), 4.11 (t, J=4.7 Гц, 4Н), 3.90 (s, 6Н), 3.52 (m, 4H), 1.46 (s, 18H). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 929.1 (100%, MNa+), 907.1 (100%, MH+), 807.1 (42%, MH+-boc).
C-2: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-метокси-фенил]-3,5-диоксо-гепта-1,6-диенил}-2-метокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
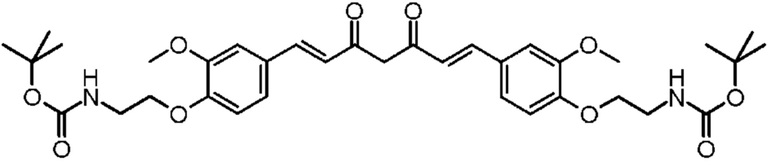
Количество соответствующего используемого альдегида Е-15: 590 мг = 2 ммоль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 2:3
Выход: 354 мг, 54% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок. Молекулярная масса = 654.76 г/моль, Эмпирическая формула = C35H46N2O10
1Н-ЯМР: (300 МГц, CDCl3), δ=7.58 (d, J=15.7 Гц, 2Н), 7.14-6.99 (m, 4Н), 6.87 (d, J=8.3 Гц, 2Н), 6.48 (d, J=15.8 Гц, 2Н), 5.16 (s, 2Н), 4.09 (t, J=4.9 Гц, 4Н), 3.90 (s, 6Н), 3.56 (m, 4Н), 1.44 (s, 18Н). МС: (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 655.3 (100%, МН+), 555.3 (26%, МН+-boc).
С-6: (2-{2-[4-(7-{4-[2-(2-трет-бутоксикарбониламино-этокси)-этокси]-3-метокси-фенил}-3,5-диоксо-гепта-1,6-диенил)-2-метокси-фенокси1-этокси}-этил)-карбаминовой кислоты трет-бутиловый эфир
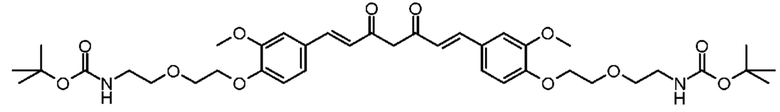
Количество соответствующего используемого альдегида Е-7: 679 мг = 2 ммоль Выход: 349 мг, 47% теоретического, оранжевое вязкое твердое вещество или оранжевый порошок
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:2 → 1:1
Молекулярная масса = 742.87 г/моль; Эмпирическая формула = C39H54N2O12
1Н-ЯМР: (300 МГц, CDCl3), δ=7.59 (d, J=15.8 Гц, 2H), 7.18 - 7.03 (m, 4Н), 6.90 (d, J=8.3 Гц, 2H), 6.49 (d, J=15.8 Гц, 2H), 5.07 (s, 2Н), 4.24-4.15 (m, 4Н), 3.91 (s, 6Н), 3.88-3.83 (m, 4Н), 3.61 (t, J=5.1 Гц, 4H), 3.33 (m, 4Н), 1.43 (s, 18Н). МС: (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 671.3 (51%, MNa+), 655.3 (86%, МН+), 555.3 (100%, MH+-boc).
С-7: {2-[4-{7-[3,4-бис-(2-трет-бутоксикарбониламино-этокси)-фенил]-3,5-диоксо-гепта-1,6-диенил}-2-(2-трет-бутоксикарбониламино-этокси)-фенокси]-этил}-карбаминовой кислоты трет-бутиловый эфир
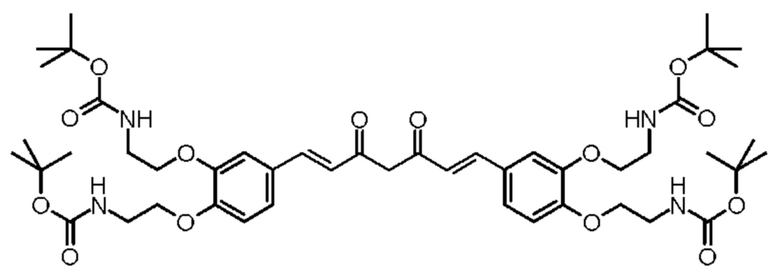
Количество соответствующего используемого альдегида Е-11: 850 мг = 2 ммоль
Выход: 374 мг, 41% теоретического, оранжевое очень вязкое твердое вещество или оранжевато-красный порошок
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 1:2
Молекулярная масса = 913.08 г/моль; Эмпирическая формула = C47H68N4O14
1Н-ЯМР (300 МГц, CDCl3), δ=7.57 (d, J=15.8 Гц, 2Н), 7.19-7.12 (m, 4Н), 6.98-6.86 (m, 2Н), 6.50 (d, J=15.8 Гц, 2Н), 5.28 (s, 4Н), 4.10 (t, J=4.4 Гц, 8Н), 3.55 (m, 8Н), 1.46 (s, 18Н), 1.45 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 913.5 (100%, МН+), 457.3 (7%, (М+2Н+)2+):
С-8: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-бензилокси-фенил1-3,5-диоксо-гепта-1,6-диенил}-2-бензилокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
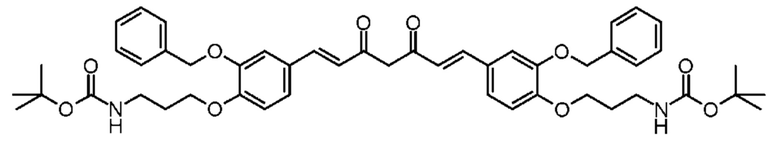
Количество соответствующего используемого альдегида Е-7: 738 мг = 2 ммоль
Выход: 518 мг, 62% теоретического, оранжевое твердое вещество или оранжевый порошок
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 2:3
Молекулярная масса = 835.02 г/моль; Эмпирическая формула = C49H58N2O10
1Н-ЯМР (300 МГц, CDCl3), δ=7.55 (d, J=15.8 Гц, 2Н), 7.45-7.31 (m, 10Н), 7.14-7.04 (m, 4Н), 6.86 (d, J=8.3 Гц, 2Н), 6.46 (d, J=15.8 Гц, 2Н), 5.39 (s, 2Н), 5.22 (s, 4Н), 4.14 (t, J=5.9 Гц, 4Н), 3.39 (m, 4Н), 2.09-2.00 (m, 4Н), 1.41 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 857.4 (100%, MNa+), 835.4 (76%, МН+), 735.4 (53%, MH+-boc).
С-9: {2-[4-{7-[3,4,5-трис-(2-трет-бутоксикарбониламино-этокси)-фенил1-3,5-диоксо-гепта-1,6-диенил}-2,6-бис-(2-трет-бутоксикарбониламино-этокси)-фенокси1-этил}-карбаминовой кислоты трет-бутиловый эфир
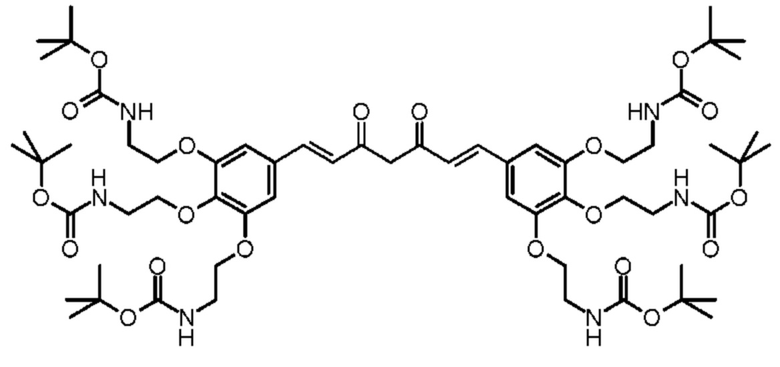
Количество соответствующего используемого альдегида Е-11: 1166 мг = 2 ммоль
Выход: 554 мг, 45% теоретического, оранжевое очень вязкое твердое вещество или оранжевато-красный порошок. Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:4 → 1:2. Молекулярная масса = 1231.46 г/моль; Эмпирическая формула = C61H94N6O20
1Н-ЯМР (300 МГц, CDCl3), δ=7.52 (d, J=15.1 Гц, 2Н), 6.79 (s, 4Н), 6.51 (d, J=15.1 Гц, 2Н), 5.75 (s, 2Н), 5.25 (s, 3Н), 4.10 (m, 12Н), 3.57 (m, 8Н), 3.41 (m, 4Н), 1.47 (s, 18Н), 1.47 (s, 36Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 1253.6 (100%, MNa+), 1231.6 (49%, МН+), 1131.3 (51%, MH+-boc).
С-10: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-октилокси-фенил]-3,5-диоксо-гепта-1,6-диенил}-2-октилокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
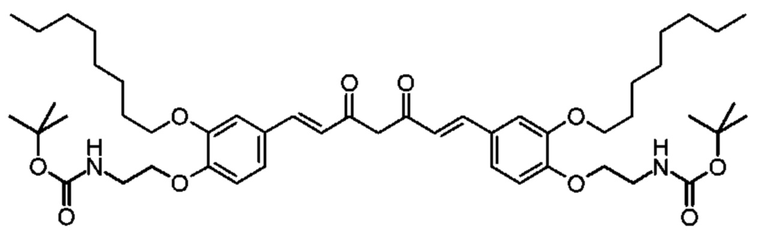
Количество соответствующего используемого альдегида Е-10: 787 мг = 2 ммоль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:4 → 1:2
Выход: 400 мг, 47% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок. Молекулярная масса = 851.14 г/моль; Эмпирическая формула = C49H74N2O10
1Н-ЯМР (300 МГц, CDCl3), δ=7.58 (d, J=15.7 Гц, 2Н), 7.15-7.05 (m, 4Н), 6.89 (d, J=8.2 Гц, 2Н), 6.48 (d, J=15.8 Гц, 2Н), 5.17 (s, 2Н), 4.09 (t, J=5.0 Гц, 4Н), 4.03 (t, J=6.7 Гц, 4Н), 3.54 (m, 4Н), 1.91-1.80 (m, 4Н), 1.41 (s, 18Н), 1.51-1.26 (m, 20Н), 0.89 (t, 4.5 Гц, 6Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 873.5 (100%, MNa+), 851.4 (13%, МН+), 751.5 (38%, MH+-boc).
2.1.2 Общая процедура:
Реакцию проводили в атмосфере азота с защитой от света. В качестве бета-дикетона использовали:
(X) ацетилацетон (0.1 г, 1 ммоль)
(XI) 3-метил-2,4-пентандион (0.12 г, 1 ммоль)
(XII) 3,5-гептандион (0.13 г, 0.137 мл, 1 ммоль) или
(XIII) 2-ацетилциклогексанон (0.14 г, 1 ммоль).
Соответствующий бета-дикетон и оксид бора В2О3 (0.05 г, 0.7 ммоль) растворяли в сухом ДМФА (2 мл) и перемешивали в течение 30 минут при 70°С. Соответствующий замещенный альдегид (2 ммоль) вместе с трибутилборатом (0.46 г, 2 ммоль) растворяли в сухом ДМФА (5 мл). Этот раствор добавляли в состав и перемешивали его в течение еще получаса ч при 85°С. Затем по каплям добавляли н-бутиламин (0.1 мл в 1 мл диметилфор-мамида) добавляли и перемешивали состав при 70°С в течение 4 ч. После охлаждения до комнатной температуры удаляли все летучие компоненты потоком азота в течение ночи (выход, трубка за перегородкой).
Добавляли 10 мл этилацетата добавляли на 1 г неочищенного продукта и растворяли неочищенный продукт. Для последующего гидролиза комплексов бора добавляли двойной объем 50% уксусной кислоты добавляли (20 мл на 1 г неочищенного продукта). После перемешивания в течение 24 ч при комнатной температуре при защите от света смесь растворителей удаляли при пониженном давлении (максимальная температура водяной бани 50°С). Остаток экстрагировали три раза этиловым эфиром (3х 50 мл) и отфильтровывали нерастворимую соль. Объединенные органические фазы промывали водой (50 мл), сушили при помощи MgSO4 и наконец удаляли растворитель при пониженном давлении. Очистку осуществляли при помощи колоночной хроматографии на силикагеле с использованием комбинации ацетон/петролейный эфир. Затем чистую фракцию куркумина растворяли в минимальном возможном количестве этилацетата. Добавляя по каплям этот раствор в избыток петролейного эфира осаждали продукт в виде желто-оранжевого порошка.
С-26: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-гидрокси-фенил]-3,5-диоксо-гепта-1,6-диенил}-2-гидрокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
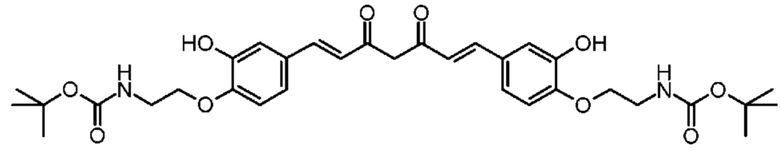
Бета-дикетон: ацетилацетон
Количество соответствующего используемого альдегида Е-10: 560 мг = 2 ммоль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир=1:2 → 2:3
Выход: 28% теоретического, оранжевое вязкое твердое вещество (180 мг). Молекулярная масса = 626.71 г/моль; Эмпирическая формула = C33H42N2O10
1Н-ЯМР (300 МГц, CDCl3), δ=7.57 (d, J=15.8 Гц, 2Н), 7.34 (m, Н), 7.19-7.08 (m, 2Н), 6.85 (d, J=8.4 Гц, 2Н), 6.64 (d, J=15.8 Гц, 2Н), 5.17 (s, 2Н), 4.07 (t, J=5.0 Гц, 4Н), 3.58-3.44 (m, 4Н), 1.43 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 627.2 (100%, МН+), 527.2 (37%, МН+-boc).
С-18: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-нафтил]-3,5-диоксо-гепта-1,6-диенил}-нафтокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
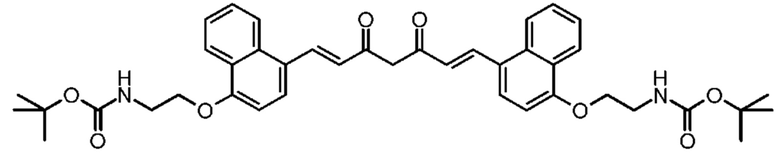
Бета-дикетон: ацетилацетон
Количество соответствующего используемого альдегида Е-13: 630 мг = 2 ммоль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 2:7 → 1:2
Выход: 62% теоретического, оранжевое вязкое твердое вещество (430 мг).
Молекулярная масса = 694.83 г/моль; Эмпирическая формула = C41H46N2O8
1Н-ЯМР (300 МГц, CDCl3), δ=8.48 (d, J=15.5 Гц, 2Н), 8.33 (d, J=8.1 Гц, 2Н), 8.25 (d, J=8.0 Гц, 2Н), 7.80 (d, J=8.1 Гц, 2Н), 7.63 (t, J=6.9 Гц, 2Н), 7.55 (t, J=6.8 Гц, 2Н), 6.86 (d, J=8.2 Гц, 2Н), 6.68 (d, J=15.5 Гц, 2Н), 5.04 (s, 2Н), 4.26 (t, J=5.0 Гц, 4Н), 3.72 (q, J=5.0 Гц, 5Н), 1.47 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 717.3 (100%, MNa+), 695.3 (56%, МН+), 639.3 (73%, МН+-С4Н9).
С-19: [2-(6-{7-[6-(2-трет-бутоксикарбониламино-этокси)-нафтил]-3,5-диоксо-гепта-1,6-диенил}-нафтокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
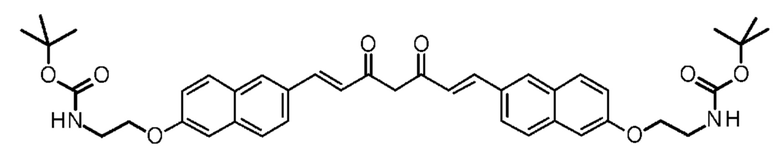
Бета-дикетон: ацетилацетон
Количество соответствующего используемого альдегида Е-19: 1.26 г=4 ммоль
Выход: 820 мг, 59% теоретического, красноватое вязкое твердое вещество или оранжевый порошок.
Молекулярная масса = 694.83 г/моль; Эмпирическая формула = C41H46N2O8
1Н-ЯМР (300 МГц, CDCl3), δ=7.85 (d, J=15.8 Гц, 2Н), 7.79-7.63 (m, 8Н), 7.20-7.08 (m, 4Н), 6.71 (d, J=15.8 Гц, 2Н), 5.06 (s, 2Н), 4.15 (t, J=5.0 Гц, 4Н), 3.61 (m, 4Н), 1.46 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 717.3 (58%, MNa+), 695.3 (100%, МН+), 639.3 (97%, МН+-С4Н9).
С-13: трет-бутил-N-[2-[4-[(Е)-3-[(3Е)-3-[[4-[2-(трет-бутоксикарбониламино)этокси]-3-метокси-фенил]метилен]-2-оксо-циклогексил]-3-оксо-проп-1-енил]-2-метокси-фенокси]этил]карбамат
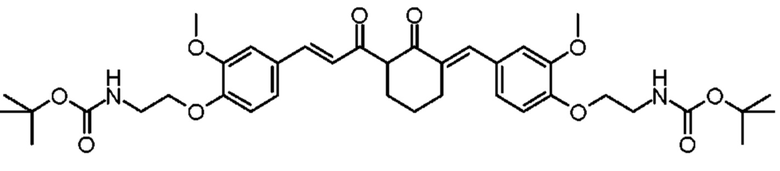
Бета-дикетон: 2-ацетилциклогексанон
Количество соответствующего используемого альдегида: 580 мг = 2 ммоль
Флэш-хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 2:5 → 1:2
Содержащие продукт фракции выпаривали на роторном испарителе и перекристаллизовывали неочищенный продукт из смеси ацетон/петролейный эфир 1:3. После медленного охлаждения до КТ, его сначала медленно охлаждали в течение ночи в холодильнике, затем охлаждали в течение 3 ч в морозилке. Твердое вещество несколько раз экстрагировали небольшим количеством смеси ацетон/петролейный эфир 1:3, а в конце промывали петролейным эфиром. Продукт сушили на воздухе. Затем получали небольшую кристаллическую фракцию путем кристаллизации исходной жидкости.
Выход: 68% теоретического, оранжевые матовые кристаллические иглы (472 мг).
Молекулярная масса = 694.83 г/моль; Эмпирическая формула = C38H50N2O10
1Н-ЯМР (300 МГц, CDCl3), δ=7.76-7.62 (m, 2Н), 7.17 (dd, J=8.3, 1.5 Гц, 1Н), 7.09 (d, J=1.7 Гц, 1Н), 7.06-6.85 (m, 5Н), 5.22-5.08 (m, 2Н), 4.11 (t, J=4.5 Гц, 4Н), 3.92 (s, 3Н), 3.89 (s, 3Н), 3.57 (m, 4Н), 2.83-2.73 (m, 2Н), 2.71-2.64 (m, 2Н), 1.86-1.77 (m, 2Н), 1.45 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAC): 717.4 (24%, MNa+), 695.4 (100%, МН+), 595.3 (30%, МН+-boc).
С-9: {2-[4-{7-[3,4,5-трис-(2-трет-бутоксикарбониламино-этокси)-фенил]-3,5-диоксо-гепта-1,6-диенил}-2,6-бис-(2-трет-бутоксикарбониламино-этокси)-фенокси]-этил}-карбаминовой кислоты трет-бутиловый эфир
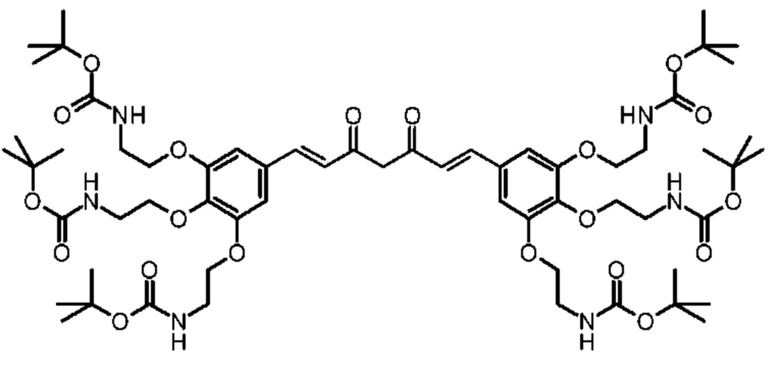
Бета-дикетон: ацетилацетон
Количество соответствующего используемого альдегида Е-12: 1160 мг = 2 ммоль
Выход: 66% теоретического, оранжевое вязкое твердое вещество или оранжевато-красный порошок (810 мг).
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:4 → 2:3.
Молекулярная масса = 1231.46 г/моль; Эмпирическая формула = C61H94N6O20
1Н-ЯМР и МС как описано выше.
С-11: трет-бутил-N-[2-[4-[(1Е,6Е)-7-[4-[2-(трет-бутоксикарбониламино)этокси]-3-[2-[2-(2-гидроксиэтокси)этокси]этокси]фенил]-3,5-диоксо-гепта-1,6-диенил1-2-[2-[2-(2-гидроксиэтокси)этокси]этокси]фенокси]этил]карбамат
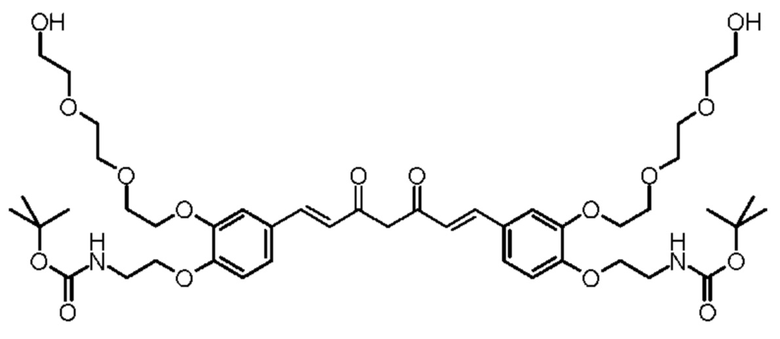
Бета-дикетон: ацетилацетон
Количество соответствующего используемого альдегида Е-10: 830 мг = 2 ммоль
Выход: 37% теоретического, оранжевое очень вязкое твердое вещество (330 мг) Колоночная хроматография на силикагеле, ацетон/петролейный эфир = 1:2 → 1:1; преп. ТСХ, ацетон/петролейный эфир (ПЭ)=1:1. Молекулярная масса = 891.03 г/моль; Эмпирическая формула = C45H66N2O16
1Н-ЯМР (600 МГц, CDCl3), δ=7.58 (d, J=15.7 Гц, 2Н), 7.20-7.06 (m, 4Н), 6.88 (d, J=8.1 Гц, 2Н), 6.48 (d, J=15.8 Гц, 2Н), 5.91 (s, 2Н), 4.25-4.17 (m, 4Н), 4.12-4.04 (m, 4Н), 3.93-3.86 (m, 4Н), 3.83-3.46 (m, 20Н), 1.44 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 891.7 (92%, МН+), 446.3 (100%, (М+2Н+)2+).
С-23: трет-бутил-N-[2-[4-[(1Е,6Е)-7-[4-[2-(трет-бутоксикарбониламино)этокси]-3-метокси-фенил]-2,6-диметил-3,5-диоксо-гепта-1,6-диенил]-2-метокси-фенокси]этил]карбамат
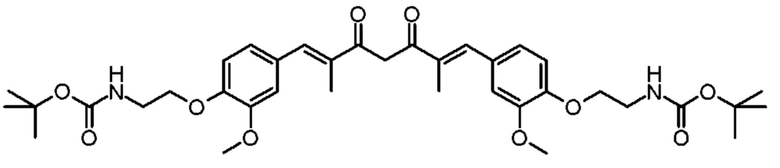
Бета-дикетон: 3,5-гептандион.
Количество соответствующего используемого ацетофенона Е-3: 608 мг = 2 ммоль
Выход: 72% теоретического, оранжевое твердое вещество (490 мг).
Колоночная хроматография на силикагеле, ацетон/петролейный эфир = 2:5 → 1:2; преп. ТСХ, ацетон/петролейный эфир = 1:2. Молекулярная масса = 682.82 г/моль; Эмпирическая формула = C37H50N2O10
1Н-ЯМР (300 МГц, CDCl3), δ=7.55 (s, 2Н), 7.07-6.88 (m, 6Н), 6.31 (s, 1Н), 5.16 (s, 2Н), 4.12 (t, J=5.0 Гц, 4Н), 3.89 (s, 6Н), 3.57 (q, J=5.1 Гц, 4Н), 2.18 (s, 6Н), 1.45 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 705.2 (MNa+, 67%), 683.4 (МН+, 100%), 627.3 (MH+ - С4Н9, 4%), 583.3 (MH+-boc, 63%), 527.2 (MH+ - boc -C4H9, 27%).
C-24: трет-бутил-N-[2-[4-[(1E,6Е)-7-[4-[2-(трет-бутоксикарбониламино)этокси]-3-метокси-фенил]-1,2,6-триметил-3,5-диоксо-octa-1,6-диенил]-2-метокси-фенокси]этил]карбамат
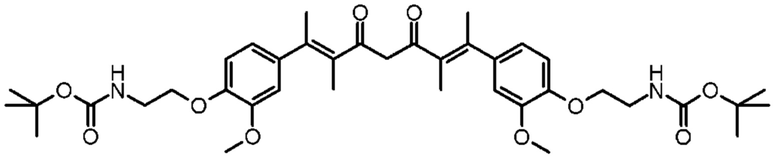
Бета-дикетон: 3,5-гептандион
Количество соответствующего используемого ацетофенона Е-15: 608 мг = 2 ммоль
Выход: 19% теоретического, оранжевое очень вязкое твердое вещество (137 мг)
Колоночная хроматография на силикагеле, ацетон/петролейный эфир = 2:5 → 1:2; преп. ТСХ, ацетон/петролейный эфир = 1:2. Молекулярная масса = 710.87 г/моль; Эмпирическая формула = C39H54N2O10
1Н-ЯМР (300 МГц, CDCl3), δ=7.12-6.91 (m, 6Н), 6.26 (s, 1Н), 5.14 (s, 2Н), 4.13 (t, J=5.3 Гц, 4Н), 3.91 (s, 6Н), 3.56 (q, J=5.2 Гц, 4Н), 2.17 (s, 6Н), 2.12 (s, 6Н), 1.44 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 732.4 (MNa+, 88%), 710.4 (МН+, 100%), 654.4 (8%, МН+-С4Н9), 610.4 (53%, MH+-boc).
С-12: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-метокси-фенил]-3,5-диоксо-гепта-4-метил-1,6-диенил}-2-метокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
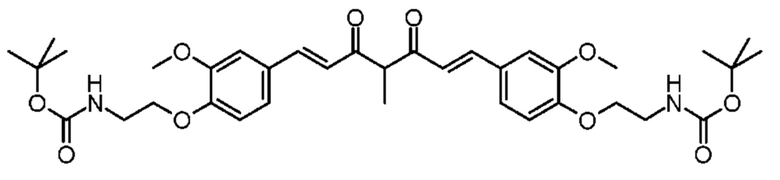
Бета-дикетон: 3-метил-2,4-пентандион
Количество соответствующего используемого альдегида Е-3: 2.94 г = 0.01 моль
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 2:3
Выход: 59% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок (403 мг).
Молекулярная масса = 682.82 г/моль; Эмпирическая формула = C36H48N2O10
1Н-ЯМР (300 МГц, CDCl3), δ=7.74-7.56 (m, 2Н), 7.20-6.82 (m, 7Н), 6.70 (d, J=15.9 Гц, 1Н), 5.13 (s, 2Н), 4.10 (dd, J=10.7, 5.3 Гц, 4Н), 3.92 (s, 3Н), 3.88 (s, 3Н), 3.56 (m, 4Н), 2.17 (m, 3Н), 1.44 (s, 9Н), 1.43 (s, 9Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 691.3 (43%, MNa+), 669.3 (100%, МН+), 569.3 (17%, MH+-boc).
2.2 Модификация гуанидином
С-14: трет-бутил-(2,2'-(4,4'-((1Е,6Е)-3,5-диоксогепта-1,6-диен-1,7-диил)бис(2-метокси-4,1-фенилен))бис(окси)бис(этан-2,1-диил))бис(азанедиил)бис((трет-бутоксикарбониламино)метан-1-ил-1-илиден)дикарбамат
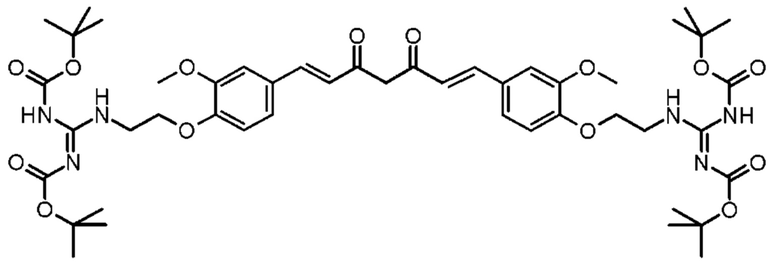
N,N'-ди-boc-N''-трифлилгуанидин получали способом, аналогичным описанному в Organic Syntheses, Coll. Т. 10, стр. .266 (2004); Т. 78, стр. .91 (2002).
Куркумин С-2 осаждали в дихлорметане (ДХМ) при комнатной температуре (КТ) в течение 5 ч трифторуксусной кислотой (ТФУК). Полученную соль трифторацетат отделяли центрифугированием. Триэтиламин (0.51 г, 0.66 мл, 5 ммоль) медленно добавляли по каплям при помощи шприца к N,N'-ди-boc-N''-трифлилгуанидину (0.82 г, 2 ммоль) в дихлорметане (10 мл) с и 2-5°С. Добавляли трифторацетат куркумина С-2 (550 мг, 0.8 ммоль). После перемешивания в течение 5 ч при комнатной температуре, его разбавляли дихлорметаном (30 мл) и промывали органическую фазу водным раствором гидросульфата калия (3%, 20 мл) и водой (20 мл). После сушки при помощи MgSO4 раствор фильтровали и выпаривали на роторном испарителе. Неочищенный материал очищали при помощи колоночной хроматографии на силикагеле с использованием комбинации ацетон/петролейный эфир (ПЭ) (ацетон/петролейный эфир = 1:3 → 1:2). Выход: 47% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок (437 мг).
Молекулярная масса = 930.08 г/моль; Эмпирическая формула = C47H66N6O14
1Н-ЯМР (300 МГц, CDCl3), δ=11.47 (s, 2Н), 8.79 (s, 2Н), 7.59 (d, J=15.8 Гц, 2Н), 7.16-7.05 (m, 4Н), 7.01 (d, J=8.3 Гц, 2Н), 6.50 (d, J=15.8 Гц, 2Н), 4.20 (t, J=5.3 Гц, 4Н), 3.92 (s, 6Н), 3.89-3.81 (m, 4Н), 1.51 (s, 18Н), 1.49 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 939.6 (9%, МН+), 470.4 (100%, (М+2Н+)2+).
2.3 Синтез замещенных куркуминов с использованием реакции Мицунобу
Синтез осуществляли способом, аналогичным способам, описанным в работе Lepore, S.D. и Не, Y.: ("Применение of Sonication for the Coupling of Sterically Hindered Substrates in the Phenolic Mitsunobu Reaction"; J. Org. Chem. 68, 2003, страницы 8261-8263).
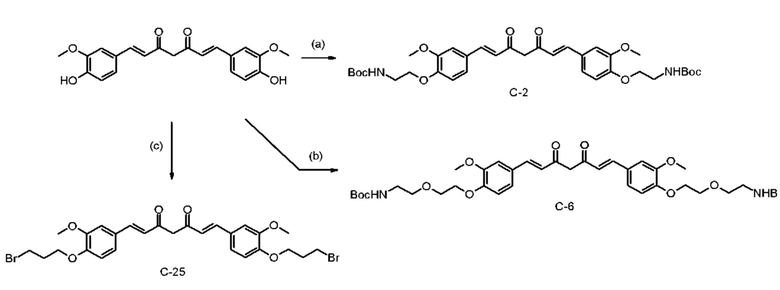
Общая схема 5: Синтез замещенных куркуминов посредством реакции Мицунобу с использованием куркумина в качестве исходного материала: Условия: (а) 2-N-трет-бутилоксикарбонил-аминоэтанол, DEAD, PPh3, ДМФА, или ТГФ, или ДХМ, 0°С → КТ; (b) 2-(2-N-трет-бутоксикарбонил-аминоэтокси)этанол, DEAD, PPh3, ДМФА, или ТГФ, или ДХМ, 0°С → КТ; (с) 3-бром-пропан-1-ол, DEAD, PPh3, ТГФ или ДХМ, 0°С → КТ;
2.3.1 Общая процедура:
Брали куркумин (0.36 г, 1 ммоль) вместе с трифенилфосфином (1.04 г, 4 ммоль) и соответствующим boc-защищенным аминоспиртом (1 ммоль или 3 ммоль) в сухом ТГФ (4 мл). Диэтилазодикарбоксилат (DEAD) (0.7 г, 4 ммоль, 40% в толуоле) в сухом ТГФ (6 мл) добавляли по каплям в течение 20 минут при приблизительно от 2°С до 5°С, и затем перемешивали смесь в течение 4 ч при к.т. в темноте. Смесь разбавляли 40 миллилитрами уксусной кислоты в этиловом эфире (ЕЕ) и встряхивали органический раствор три раза, каждый раз с 20 мл воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Остаток очищали колоночной хроматографией на силикагеле с применением комбинации ацетон/петролейный эфир (Dry Load). Для дополнительной очистки продукт растворяли в минимально возможном количестве этилового эфира и осаждали путем добавления 10-кратного количества петролейного эфира.
[2-(4-{7-[4-гидрокси-3-метокси-фенил]-3,5-диоксо-гепта-1,6-диенил}-2-метокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
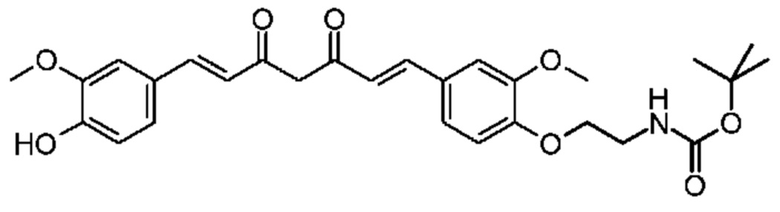
Количество соответствующего используемого трет-бутил-N-(2-гидроксиэтил)карбамата boc-замещенного аминоспирта: 161 мг = 1 ммоль.
Колоночная хроматография на силикагеле с комбинацией ацетон/петролейный эфир (ПЭ)=1:2;
Препаративная тонкослойная хроматография с комбинацией ацетон/петролейный эфир (ПЭ)=2:3.
Выход: 41% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок (210 мг).
Молекулярная масса = 511.58 г/моль; Эмпирическая формула = C28H33NO8
С-2: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-метокси-фенил]-3,5-диоксо-гепта-1,6-диенил}-2-метокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
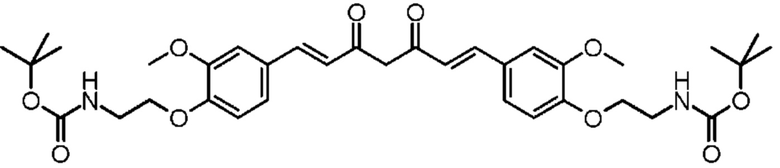
Количество соответствующего используемого трет-бутил-N-(2-гидроксиэтил)карбамата boc-защищенного аминоспирта: 483 мг = 3 ммоль.
Колоночная хроматография на силикагеле с комбинацией ацетон/петролейный эфир (ПЭ)=1:3 → 1:2.
Выход: 71% теоретического, оранжевое вязкое твердое вещество (465 мг).
Молекулярная масса = 654.76 г/моль; Эмпирическая формула = C35H46N2O10
1Н-ЯМР и МС как описано выше.
С-6: (2-{2-[4-(7-{4-[2-(2-трет-бутоксикарбониламино-этокси)-этокси]-3-метокси-фенил}-3,5-диоксо-гепта-1,6-диенил)-2-метокси-фенокси]-этокси}-этил)-карбаминовой кислоты трет-бутиловый эфир
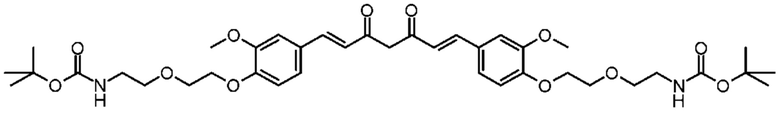
Количество соответствующего используемого boc-замещеного аминоспирта 2-(2-N-трет-бутоксикарбонил-аминоэтокси)этанола: 715 мг = 3 ммоль.
Выход: 52% теоретического, оранжевое вязкое твердое вещество или оранжевый порошок (386 мг)
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:2 → 2:3
Молекулярная масса = 742.87 г/моль; Эмпирическая формула = C39H54N2O12
1Н-ЯМР и МС как описано выше.
С-25: (1Е,6Е)-1,7-бис[4-(3-бромпропокси)-3-метокси-фенил]гепта-1,6-диен-3,5-дион
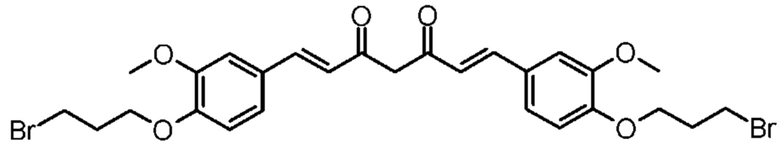
Куркумин (2.00 г, 5.4 ммоль) вместе с трифенилфосфином (5.26 г, 20 ммоль) и 3-бром-пропан-1-олом (2.25 г, 1.51 мл, 16.2 ммоль) в сухой ТГФ (40 мл) и дегазировали при 0°С. По каплям на протяженгии 20 минут добавляли диэтилазодикарбоксилат (DEAD) (7 мл, 40% в толуоле, 20 ммоль) и перемешивали смесь в течение ночи в ванне с тающим льдом в темноте, исключая влагу. Смесь вливали в трехкратное количество диэтилового эфира. После выпадения осадка надосадочный раствор аккуратно декантировали.
Остаток дважды экстрагировали, используя каждый раз 50 мл диэтилового эфира. Объединенные органические растворы встряхивали с 100 мл воды. Органическую фазу отделяли, сушили при помощи MgSO4 и выпаривали на роторном испарителе. Остаток суспендировали в смеси ацетоне/петролейный эфир 1:2 и отфильтровывали желто-оранжевый раствор от бесцветных кристаллов. Остаток на фильтре промывали несколько раз маленькими порциями холодной смеси растворителей и выпаривали фильтрат на роторном испарителе. Предварительную очистку остатка осуществляли плунжерной фильтрацией на силикагеле с использованием комбинации ацетон/петролейный эфир 1:2. После удаления смеси растворителей твердый остаток суспендировали в этаноле в ультразвуковой ванне (30 мл), центрифугировали и сливали надосадочный раствор. Этот этап промывки повторяли в целом три раза, после чего продукт сушили на воздухе. Выход: 2.08 г оранжевого порошка, 63% теоретического. Молекулярная масса = 610.34 г/моль; Эмпирическая формула = C27H30Br2O6
1Н-ЯМР (300 МГц, CDCl3), δ=7.61 (d, J=15.8 Гц, 2Н), 7.16-7.04 (m, 4Н), 6.92 (d, J=8.3 Гц, 2Н), 6.50 (d, J=15.8 Гц, 2Н), 4.20 (t, J=6.0 Гц, 4Н), 3.91 (s, 6Н), 3.64 (t, J=6.4 Гц, 4Н), 2.39 (р, J=6.1 Гц, 4Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 609.1 (57%, MH+), 611.0 (100%, MH+).
Куркумины С-27 - С-30 получали из бис-(3-бром-пропокси)куркумина С-25:
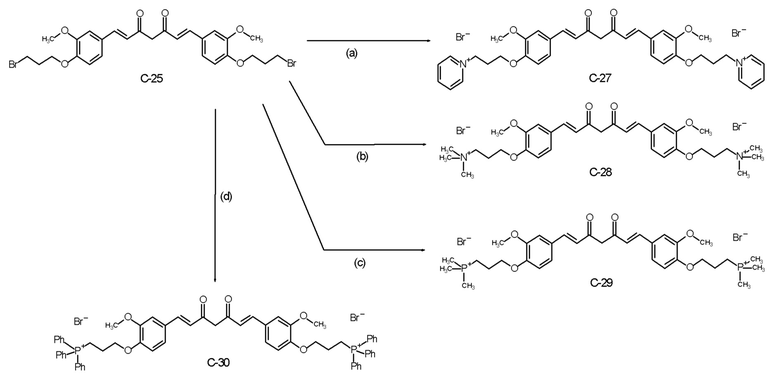
Общая схема 6: Синтез симметрично замещенных куркуминов из С-25: Условия: (а) пиридин, ДМФА, 50°С, в течение ночи; (b) триметиламин в этаноле, ДМФА, 50°С, в течение ночи; (с) триметилфосфин в толуоле, ДМФА, аргон, 50°С, в течение ночи; (d) трифенилфосфин, ДМФА, 50°С, в течение ночи;
2.4 Куркумины с четвертичными зарядами
Бис-(3-бром-пропокси)куркумин (61 мг, 0.1 ммоль) С-25 помещали в сухой ДМФА (3 мл). По каплям через перегородку при помощи шприца на протяжении 5 минут добавляли триметиламин (2 мл, 5.6 М в этаноле, 11 ммоль) или пиридин (790 мг, 0.8 мл, 10 ммоль) в ДМФА (2 мл) и перемешивали смесь в течение ночи в темноте при 50°С, исключая воздействие влаги.
Смесь вливали в пятикратное количество диэтилового эфира. Осадку давали осесть и осторожно декантировали раствор. Остаток промывали несколько раз диэтиловым эфиром, а затем суспендировали в 15 мл смеси хлороформ/диэтиловый эфир 1:1. Суспензии давали полностью отстояться, надосадочный раствор выливали, а сушили при помощи вакуумной помпы. Продукт очищали путем ВЭЖХ.
Ионообменная хроматография
Колонку загружали смолой Amberlite 954 и кондиционировали ионообменную смолу 0.1М раствором HCl. После промывки водой ее повторно кондиционировали смесь вода/MeOH/MeCN 3:1:1. Затем соль ТФУК в небольшом количестве смеси растворителей медленно выливали на смолу и споласкивали небольшим количеством растворителя. После удаления растворителя при пониженном давлении оставшийся раствор высушивали замораживанием.
С-28: 3,3'-(4,4'-((1Е,6Е)-3,5-диоксогепта-1,6-диен-1,7-диил)бис(2-метокси-4,1-фенилен))бис(окси)бис(N,N,N-триметилпропан-1-aminium) хлорид
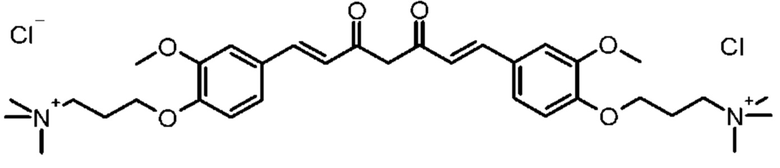
Выход: 30 мг оранжевого твердого вещества, 45% теоретического
Молекулярная масса: 568.76 +2х 35.45 = 639.66 г/моль; Эмпирическая формула: C33H48N2O6Cl2
1Н-ЯМР и МС: см. ниже (SA-CUR-10a).
С-27: 1,1'-(3,3'-(4,4'-((1Е,6Е)-3,5-диоксогепта-1,6-диен-1,7-диил)бис(2-метокси-4,1-фенилен))бис(окси)бис(пропан-3,1-диил))дипиридинит хлорид
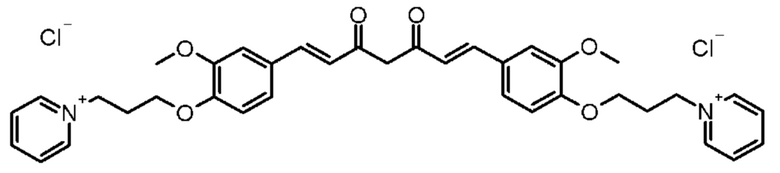
Выход: 36 мг оранжевого твердого вещества, 78% теоретического выхода
Молекулярная масса: 608.74+2х 35.45=679.64 г/моль; Эмпирическая формула: C37H40N2O6Cl2
1Н-ЯМР и МС: см. ниже (SA-CUR-10c).
2.5 Куркумин с группами фосфония
Бис-(3-бром-пропокси)куркумин С-25 (122 мг, 0.2 ммоль) помещали в сухой дихлорметан (ДХМ) (10 мл) и перемешивали в атмосфере азота. Используемый фосфин в толуоле (2 мл, 1 М, 2 ммоль) добавляли по каплям на протяжении 5 минут через перегородку при помощи шприца. Смесь перемешивали в течение ночи в пробирке Шленка при 50°С, исключая воздействие влаги, в темноте и в атмосфере защитного газа. Все летучие компоненты удаляли при пониженном давлении, а остаток суспендировали в 30 мл диэтилового эфира при помощи ультразвуковой ванны. Давали осесть осадку и осторожно сливали надосадочный раствор. Остаток промывали несколько раз диэтиловым эфиром. После осаждения преципитата сливали надосадочный раствор и сушили остаток при помощи вакуумной помпы.
Ионообменная хроматография
В короткую колонку загружали смолу Amberlite 954 и кондиционировали ионообменную смолу 0.1М раствором HCl. После промывки водой ее повторно кондиционировали смесью вода/MeOH/MeCN 3:1:1. Затем соль ТФУК в небольшом количестве смеси растворителей медленно элюировали через смолу, а затем споласкивали небольшим количеством растворителя. После удаления растворителя при пониженном давлении оставшийся раствор высушивали замораживанием. Количественный выход.
С-29: 3,3'-(4,4'-(1Е,6Е)-3,5-диоксогепта-1,6-диен-1,7-диил)бис(2-метокси-4,1-фенилен))бис(окси)бис(триметилпропан-1-фосфоний) хлорид
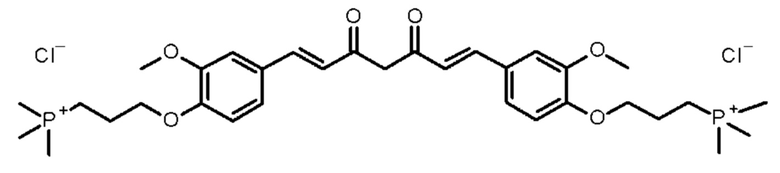
Фосфин: триметилфосфин
Выход: 58 мг оранжевого твердого вещества, 21% теоретического
Молекулярная масса: 602.69 +2х 35.45=673.59 г/моль; Эмпирическая формула: C33H48P2O6Cl2
1Н-ЯМР и МС: см. ниже SA-CUR-15a.
С-30: 3,3'-(4,4'-((1Е,6Е)-3,5-диоксогепта-1,6-диен-1,7-диил)бис(2-метокси-4,1-фенилен))бис(окси)бис(трифенилпропан-1-фосфоний) хлорид
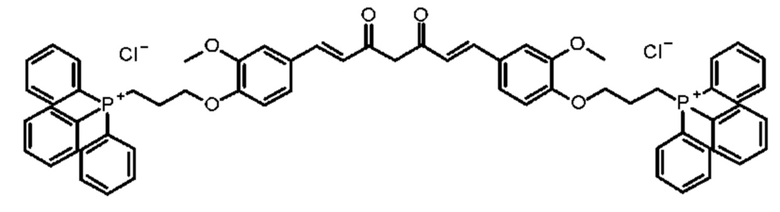
Фосфин: трифенилфосфин
Выход: 107 мг оранжевого твердого вещества, 56% теоретического
Молекулярная масса: 975.12 +2х 35.45=1046.02 г/моль; Эмпирическая формула: C63H60P2O6Cl2
1Н-ЯМР и МС: см. ниже SA-CUR-15b.
2.6 Синтез замещенных куркуминов путем алкилирования
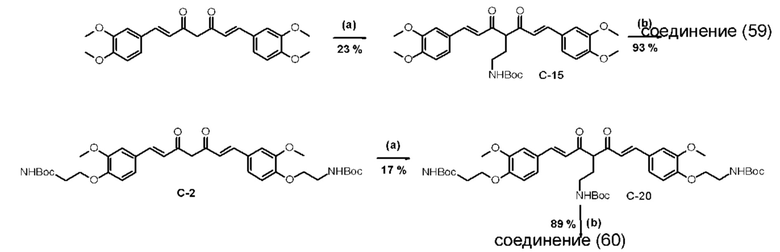
Общая схема 7: Синтез замещенных куркуминов путем алкилирования: Условия: (a) 2-N-трет-бутилоксикарбонил-аминобромид, DBU, толуол, или ДХМ, или ТГФ, 0°С → КТ → 60°С; (b) ДХМ, ТФУК, КТ, 5 ч; затем ионообменная смола Amberlite IRA-958, вода
Третраметоксикуркумин (0.4 г, 1 ммоль) или куркумин С-2 (0.6 г, 1 ммоль) и 2-N-трет-бутоксикарбониламиноэтила бромид (0.34 г, 1.5 ммоль) помещали в толуол (4 мл). Добавляли 1.8-диазабицикло[5.4.0]ундек-7-ен (DBU) (0.15 г, 1 ммоль) и перемешивали смесь в течение 15 ч при комнатной температуре. Раствор разбавляли этилацетатом (30 мл), и промывали раствором хлорида натрия (30 мл), раствором гидросульфата калия (5%, 30 мл) и водой (30 мл). После сушки при помощи MgSO4 его выпаривали на роторном испарителе, а остаток очищали колоночной хроматографией на силикагеле со смесью этилацетат/петролейный эфир, а затем препаративной тонкослойной хроматографией.
С-15: 1,7-бис-(3,4-диметоксифенил)-гепта-4-(2-трет-бутоксикарбониламиноэтил)-1,6-диен-3,5-дион
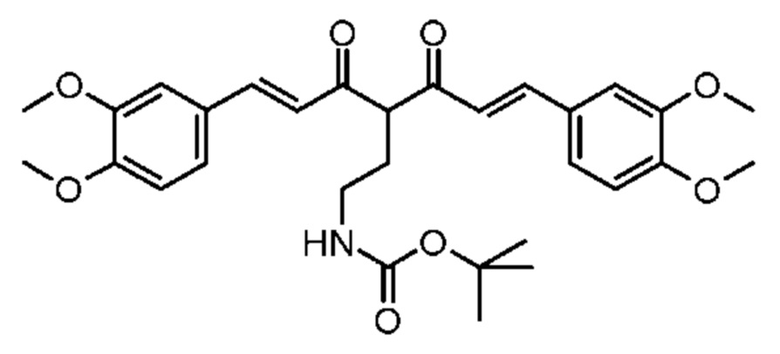
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:1
Выход: 14% теоретического, оранжевое твердое вещество или оранжево-желтый порошок (76 мг)
Молекулярная масса = 539.63 г/моль; Эмпирическая формула = C30H37NO8
1Н-ЯМР (300 МГц, CDCl3), δ=7.72-7.53 (m, 2Н), 7.22-7.04 (m, 4Н), 6.86 (d, J=8.1 Гц, 2Н), 6.54 (d, J=15.7 Гц, 2Н), 5.11 (s, 1Н), 3.88-3.72 (m, 2Н), 3.93 (s, 12Н), 2.81-2.70 (m, 2Н), 1.43 (s, 9Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 562.3 (MNa+, 13%), 540.3 (МН+, 100%), 484.2 (2%, МН+-С4Н9), 440.3 (61%, МН+-boc).
С-20: [2-(4-{7-[4-(2-трет-бутоксикарбониламино-этокси)-3-метокси-фенил]-3,5-диоксо-гепта-4-(2-трет-бутоксикарбониламино-этил)-1,6-диенил}-2-метокси-фенокси)-этил]-карбаминовой кислоты трет-бутиловый эфир
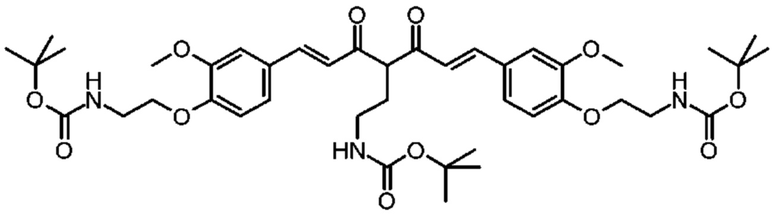
Колоночная хроматография на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 → 1:1
Выход: 12% теоретического, оранжевый, оранжево-желтый порошок (96 мг).
Молекулярная масса = 797.95 г/моль; Эмпирическая формула = C42H59N3O12
1Н-ЯМР (300 МГц, CDCl3), δ=7.64 (d, J=15.7 Гц, 2Н), 7.24-7.01 (m, 6Н), 6.78 (d, J=15.8 Гц, 2Н), 5.16 (s, 2Н), 4.12 (dd, J=10.6, 5.4 Гц, 4Н), 3.93 (s, 3Н), 3.90 (s, 3Н), 3.86-3.75 (m, 2Н), 3.54 (m, 4Н), 2.82-2.71 (m, 2Н), 1.45 (s, 9Н), 1.44 (s, 9Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 820.4 (MNa+, 69%), 798.4 (МН+, 100%), 742.4 (6%, МН+-С4Н9), 698.3 (36%, МН+-boc).
2.7 Синтез несимметрично замещенных куркуминов
Общая процедура:
Этап 1:
В качестве бета-дикетонов применяли ацетилацетон (1.5 г, 15 ммоль) или 3-метил-2,4-пентандион (3.42 г, 30 ммоль). Соответствующий бета-дикетон и оксид бора В2О3 (1.5 г, 21 ммоль) суспендировали в этилацетате (20 мл) и перемешивали в течение 60 минут при 70°С. Добавляли замещенный бензальдегид Е-3 (1.02 г, 3.5 ммоль) в этилацетате (5 мл) и трибутилборат (1.68 г, 7 ммоль) и перемешивали смесь в течение получаса при 85°С. Затем добавляли по каплям н-бутиламин (0.5 мл в 3 мл этилацетата) в течение 10 минут. После перемешивания в течение еще часов при 80°С, его охлаждали до 50°С и добавляли 100 мл 50% уксусной кислоты для гидролиза комплекса бора. После перемешивания в течение ночи при комнатной температуре удаляли смесь растворителей, при защите от света, а остаток экстрагировали три раза этиловым эфиром (используя каждый раз по 30 мл). Объединенные органические фазы промывали дважды водой (50 мл каждый pax), сушили при помощи MgSO4 и наконец, удаляли растворитель при пониженном давлении.
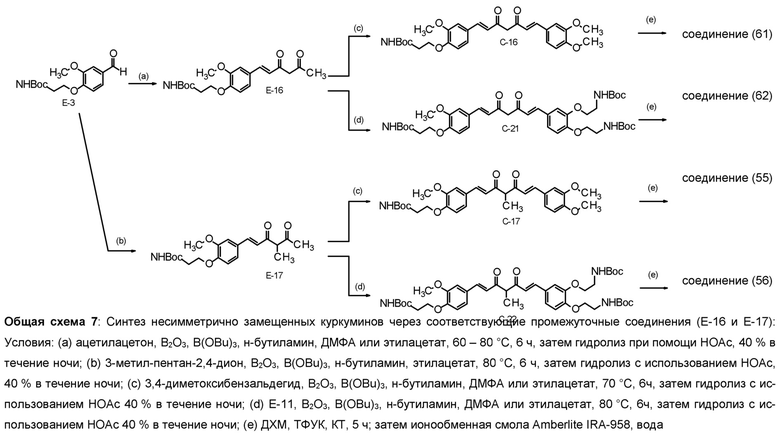
Е-16: трет-бутил-2-(4-(3,5-диоксогекс-1-енил)-2-метоксифенокси)этилкарбамат
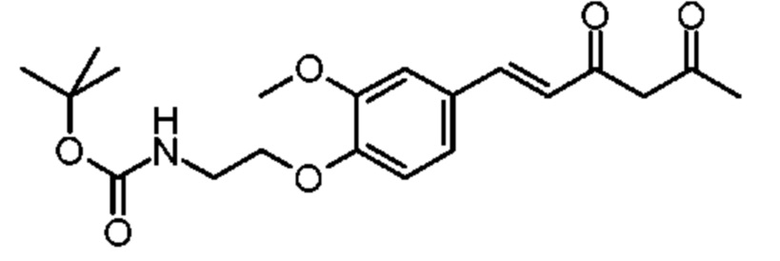
В качестве бета-дикетона использовали ацетилацетон. Очистку осуществляли при помощи колоночной хроматографии на силикагеле с применением комбинации ацетон/петролейный эфир = 2:5 → 1:2. Соответствующий симметрично замещенный куркумин обладает более низкой растворимостью в EtOH, чем указанный продукт.
Выход: 687 мг, 52% теоретического, желтое твердое вещество.
Молекулярная масса = 377.44 г/моль; Эмпирическая формула = C20H27NO6
1Н-ЯМР (300 МГц, CDCl3), δ=7.53 (d, J=15.8 Гц, 1Н), 7.12-7.00 (m, 2Н), 6.88 (d, J=8.3 Гц, 1Н), 6.34 (d, J=15.8 Гц, 1Н), 5.16 (s, 1Н), 4.10 (t, J=5.1 Гц, 2Н), 3.90 (s, 3Н), 3.56 (d, J=5.3 Гц, 2Н), 2.16 (s, 3Н), 1.44 (s, 9Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 777.4 (46%, 2MNa+), 400.2 (38%, MNa+), 378.2 (12%, МН+), 322.1 (100%, МН+-С4Н9), 278.1 (47%, МН+ - boc).
Е-17: трет-бутил-2-(4-(3,5-диоксо-4-метил-гекс-1-енил)-2-метоксифенокси)-этилкарбамат
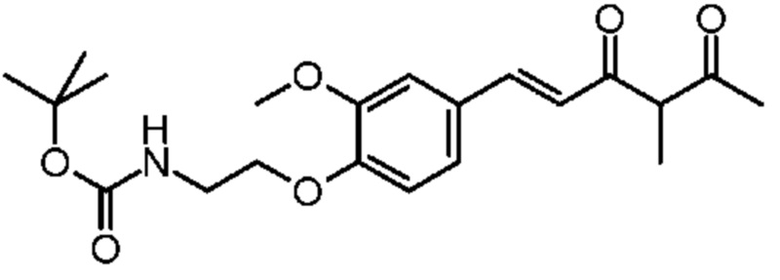
В качестве бета-дикетона использовали 3-метил-2,4-пентандион. Очистку осуществляли при помощи колоночной хроматографии на силикагеле с применением комбинации ацетон/петролейный эфир = 1:3 и препаративной ТСХ с использованием комбинации ацетон/петролейный эфир = 1:2.
Выход: 644 мг, 47% теоретического, желтое твердое вещество.
Молекулярная масса = 391.47 г/моль; Эмпирическая формула = C21H29NO6
1Н-ЯМР (300 МГц, CDCl3), δ=7.58 (dd, J=15.7, 6.5 Гц, 1Н), 7.13 (d, J=8.3 Гц, 1Н), 7.05 (dd, J=4.9, 1.8 Гц, 1Н), 6.89 (d, J=8.3 Гц, 1Н), 6.74 (dd, J=37.9, 15.7 Гц, 1Н), 5.11 (s, 1Н), 4.10 (t, J=5.1 Гц, 2Н), 3.91 (s, 3Н), 3.56 (m, 2Н), 2.25+2.18 (s, 3Н), 2.02 (s, 3Н), 1.44 (s, 10Н). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAC): 805.5 (24%, 2MNa+), 414.3 (53%, MNa+), 392.3 (19%, MH+), 336.2 (100%, MH+-C4H9), 292.2 (34%, MH+ - boc).
Этап 2:
Трет-бутил-2-(4-(3,5-диоксогекс-1-енил)-2-метоксифенокси)этилкарбамат (185 мг, 0.5 ммоль) или трет-бутил-2-(4-(3,5-диоксо-4-метил-гекс-1-енил)-2-метоксифенокси)этилкарбамат (191 мг, 0.5 ммоль) и оксид бора В2О3 (0.07 г, 1 ммоль) суспендировали в этилацетате (3 мл) и перемешивали в течение 60 минут при 80°С. Последовательно добавляли замещенный бензальдегид (0.6 ммоль) в этилацетате (3 мл) и трибутилборат (0.24 г, 1 ммоль) добавляли и перемешивали смесь в течение получаса при 80°С. Затем добавляли по каплям н-бутиламин (0.1 мл in 1 мл этилового эфира) на протяжении 5 минут. После перемешивания в течение еще трех ч при 80°С слегка охлажденный раствор при температуре около 50°С вливали в 40 мл 50% уксусной кислоты. После перемешивания в течение ночи при комнатной температуре при защите от света, смесь растворителей удаляли при пониженном давлении, а остаток экстрагировали три раза этиловым эфиром (используя каждый раз 20 мл). Объединенные органические фазы промывали дважды водой (используя каждый раз 20 мл), сушили при помощи MgSO4 и наконец удаляли растворитель при пониженном давлении. Очистку осуществляли при помощи колоночной хроматографии на силикагеле.
С-16: трет-бутил-2-(4-((1Е,6Е)-7-(3,4-диметоксифенил)-3,5-диоксогепта-1,6-диенил)-2-метоксифенокси)этил карбамат
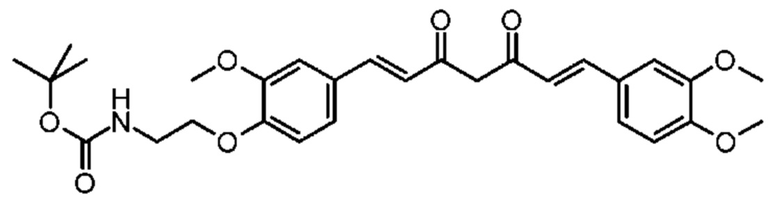
Количество соответствующего используемого альдегида Е-16: 100 мг = 0.6 ммоль
Колоночная хроматография с использованием комбинации ацетон/петролейный эфир = 1:2 → 2:3
Выход: 121 мг, 46% теоретического, оранжевое вязкое твердое вещество или оранжево-желтый порошок.
Молекулярная масса = 525.60 г/моль; Эмпирическая формула = C29H35NO8
1Н-ЯМР (300 МГц, CDCl3), δ=7.60 (dd, J=15.7, 4.5 Гц, 2Н), 7.15-7.06 (m, 4Н), 6.89 (dd, J=8.3, 3.3 Гц, 2Н), 6.50 (d, J=15.8 Гц, 2Н), 5.13 (s, 1Н), 4.11 (t, J=5.0 Гц, 2Н), 3.94 (s, 3Н), 3.93 (s, 3Н), 3.92 (s, 3Н), 3.62-3.52 (m, 2Н), 1.45 (s, 9Н).
МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 1073.5 (19%, 2M+Na+), 526.2 (100%, МН+), 470.2 (21%, МН+-С4Н9).
С-21: 2-(4-((1Е,6Е)-7-(3А-бис(2-(трет-бутоксикарбониламино)этокси)фенил)-3,5-диоксогепта-1,6-диенил)-2-метоксифенокси)этилкарбамат
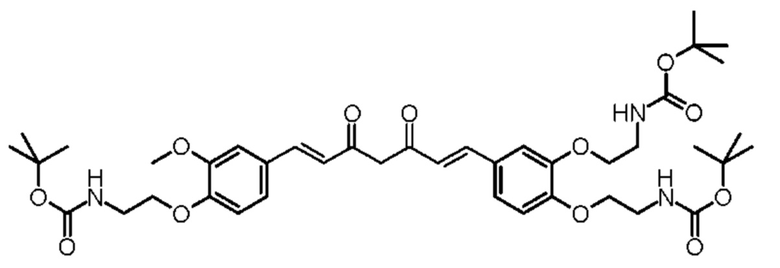
Количество соответствующего используемого альдегида Е-16: 255 мг = 0.6 ммоль
Колоночная хроматография с использованием комбинации ацетон/петролейный эфир = 2:5 → 1:2
Выход: 172 мг, 44% теоретического, оранжевое, очень вязкое твердое вещество.
Молекулярная масса = 783.92 г/моль; Эмпирическая формула = C41H57N3O12
1Н-ЯМР (300 МГц, CDCl3), δ=7.57 (dd, J=15.7, 9.3 Гц, 2Н), 7.17-7.05 (m, 4Н), 6.90 (dd, J=8.2, 6.6 Гц, 2Н), 6.49 (d, J=15.7 Гц, 2Н), 5.27 (s, 2Н), 5.14 (s, 1Н), 4.10 (m, 6Н), 3.91 (s, 3Н), 3.55 (m, 6Н), 1.46 (s, 9Н), 1.44 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 804.6 (73%, MNa+), 784.4 (100%, МН+), 684.3 (71%, MH+-boc).
С-17: трет-бутил-2-(4-((1Е,6Е)-7-(3А-диметоксифенил)-3,5-диоксо-4-метил-гепта-1,6-диенил)-2-метоксифенокси)этил карбамат
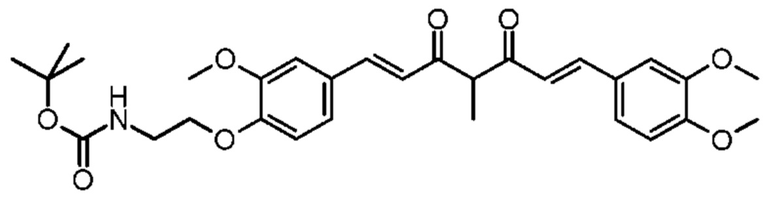
Количество соответствующего используемого альдегида Е-17: 100 мг = 0.6 ммоль
Колоночная хроматография с использованием комбинации ацетон/петролейный эфир = 1:2 → 2:3
Выход: 113 мг, 42% теоретического, оранжевое, вязкое твердое вещество
Молекулярная масса = 539.63 г/моль; Эмпирическая формула = C30H37NO8
1Н-ЯМР (300 МГц, CDCl3), δ=7.75-7.56 (m, 2Н), 7.20-6.82 (m, 7Н), 6.70 (d, J=15.9 Гц, 1Н), 5.15 (s, 1Н), 4.15-4.06 (m, 2Н), 3.95 (s, 3Н), 3.91 (s, 3Н), 3.89 (s, 3Н), 3.57 (m, 2Н), 2.18 (s, 3Н), 1.44 (s, 9H). МС (ионизация электрораспылением, CH2Cl2/МеОН + 10 ммоль NH4OAc): 562.2 (MNa+, 41%), 540.3 (МН+, 100%), 484.2 (МН+-С4Н9, 46%), 440.3 (МН+-boc, 3%).
С-22: 2-(4-((1Е,6Е)-7-(3,4-бис(2-(трет-бутоксикарбониламино)этокси)фенил)-3,5-диоксо-4-метил-гепта-1,6-диенил)-2-метоксифенокси)этилкарбаминовая кислота
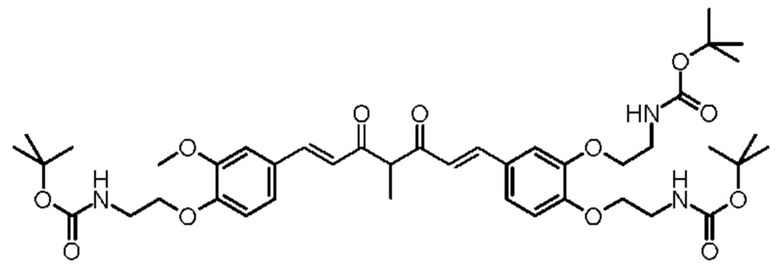
Количество соответствующего используемого альдегида Е-17: 255 мг = 0.6 ммоль
Колоночная хроматография с использованием комбинации ацетон/петролейный эфир = 2:5 → 1:2
Выход: 160 мг, 40% теоретического, оранжевое, очень вязкое твердое вещество. Молекулярная масса = 797.95 г/моль; Эмпирическая формула = C42H59N3O12
1Н-ЯМР (300 МГц, CDCl3), δ=7.74-7.52 (m, 2Н), 7.21-6.88 (m, 7Н), 6.70 (d, J=15.9 Гц, 1Н), 5.29 (s, 2Н), 5.16 (s, 1Н), 4.10 (t, J=4.8 Гц, 6Н), 3.90 (m, 3Н), 3.56 (m, 6Н), 2.17 (m, 3Н), 1.46 (s, 9Н), 1.45 (s, 18Н). МС (ионизация электрораспылением, CH2Cl2/MeOH + 10 ммоль NH4OAc): 820.4 (100%, MNa+), 798.3 (43%, МН+), 698.4 (67%, МН+-boc).
3. Удаление защитной группы Boc из куркуминов и ионообменная хроматография
Соответствующий boc-защищенный куркумин (0.2 ммоль, 120-160 мг) растворяли в ДХМ (6 мл). Медленно при перемешивании по каплям добавляли 4 мл 10% раствора ТФУК в ДХМ (содержащем 6% TIS). После перемешивания в течение 5 ч при к.т. при защите от света, осаждали продукт путем добавления диэтилового эфира (10 мл). Осадок удаляли центрифугированием, а затем удаляли супернатант. Твердое вещество суспендировали в диэтиловом эфире (30 мл) и снова удаляли центрифугированием. Супернатант также удаляли. Повторяли этап промывки еще раз и сушили продукт на воздухе в темноте.
Ионообменная хроматография
Колонку загружали смолой Amberlite 954 и кондиционировали ионообменную смолу с использованием 0.1М HCl. После промывки водой до очень слабой кислотной реакции при необходимости осуществляли повторное кондиционирование с использованием смеси вода/MeOH/MeCN. Затем через смолу медленно элюировали соль ТФУК в минимально возможном количеств смеси растворителей и несколько раз споласкивали небольшим количеством растворителя. После удаления растворителя при пониженном давлении оставшийся раствор высушивали замораживанием. Количественный выход.
Элюент:

4. Комплексы куркуминов
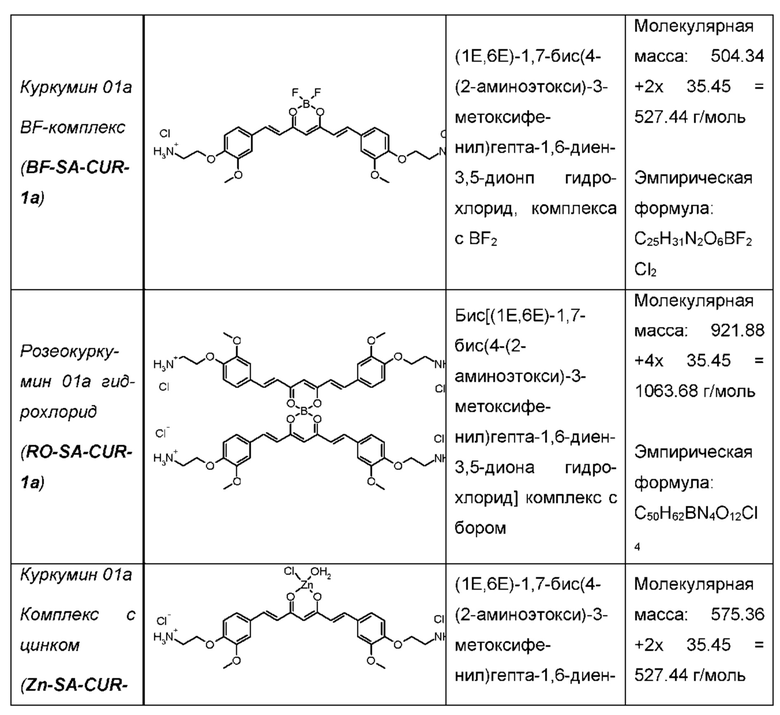

4.а) Соль ТФУК соединения SA-CUR-01a (68 мг, 0.1 ммоль) помещали в сухой ДХМ (10 мл). Добавляли по каплям трифторид этерата бора (20 мкл, 0.12 ммоль) и перемешивали смесь в течение ночи. Раствор разбавляли диэтиловым эфиром (20 мл), разделяли по двум пробиркам Blue Caps и центрифугировали. Сгусток промывали несколько раз диэтиловым эфиром и сушили на воздухе. Красный порошок (соль ТФУК), количественный выход.
Ионообменная хроматография
В короткую колонку загружали смолу Amberlite 954 и кондиционировали ионообменную смолу с использованием 0.1М HCl. После промывки водой до очень слабой кислой реакции соль ТФУК промывали минимальным количеством воды, медленно элюировали через смолу и несколько раз споласкивали небольшим количеством растворителя. Водный раствор лиофилизировали. Количественный выход.
4.b) SA-CUR-01a хлорид (108 мг, 0.2 ммоль) и триоксид бора (0.05 ммоль) перемешивали в течение ночи в водном растворе HCl (1 М, 2 мл) при комнатной температуре. Растворитель удаляли в потоке азота, а остаток сушили. Красный порошок, количественный выход.
4.с) SA-CUR-01a хлорид (54 мг, 0.1 ммоль) и дигидрат ацетата цинка (0.05 ммоль) нагревали с обратным холодильником в смеси этанол/уксусная кислота/вода 3:2:1 (3 мл) в течение 2 дней. Растворитель удаляли в потоке азота, а остаток сушили. Оранжевый порошок, количественный выход.
Сводные данные о полученных соединениях приведены в Общей схеме 8.
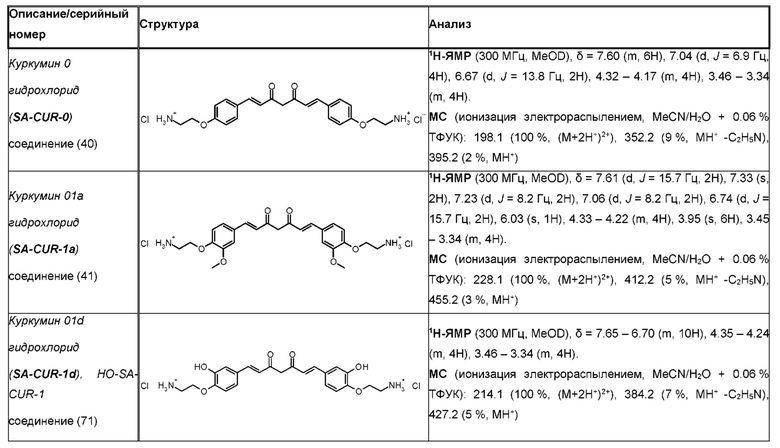
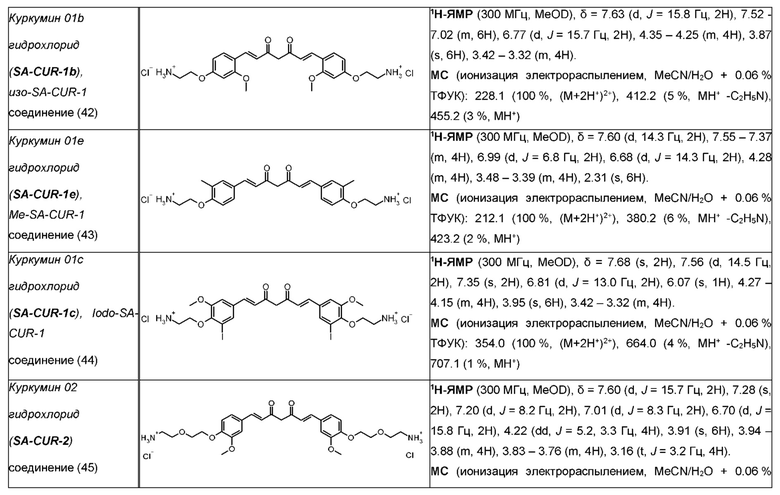
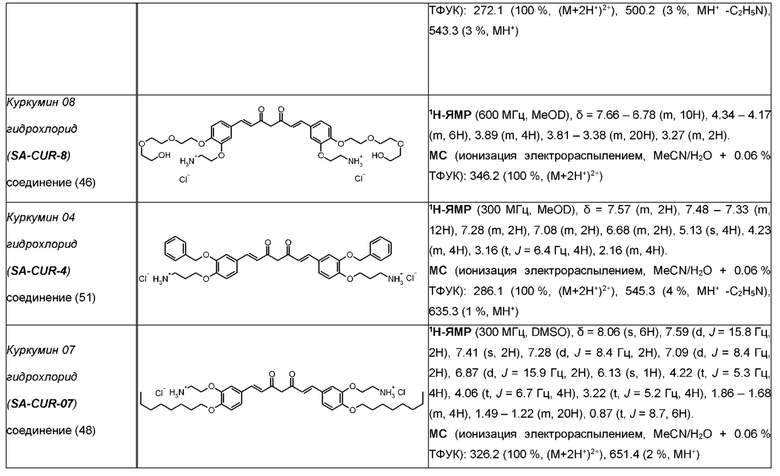
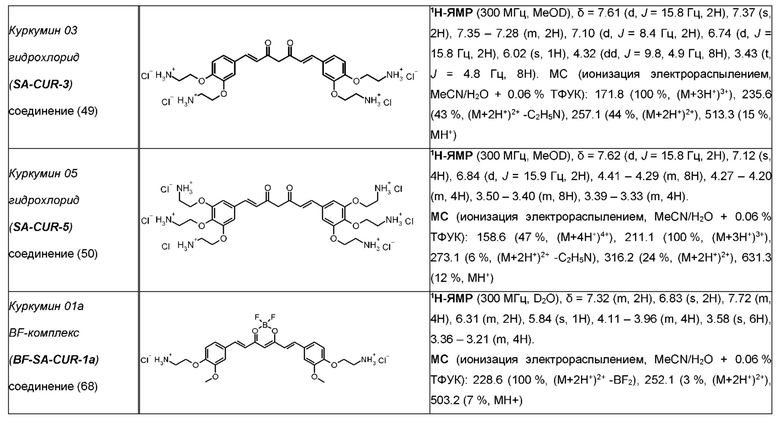
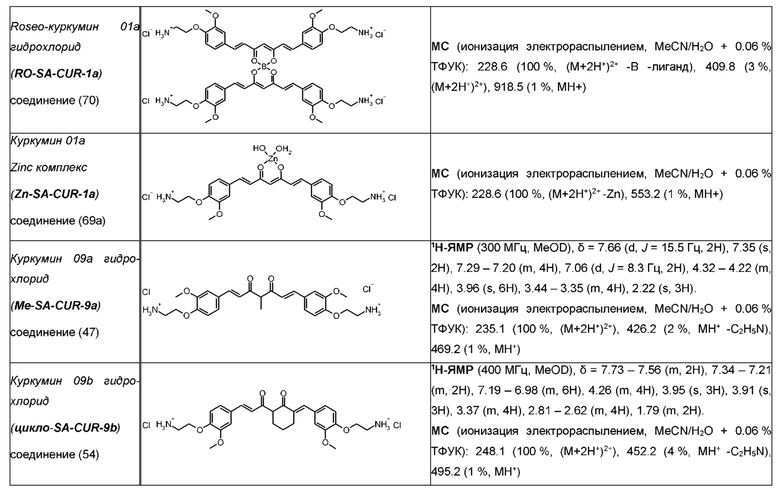
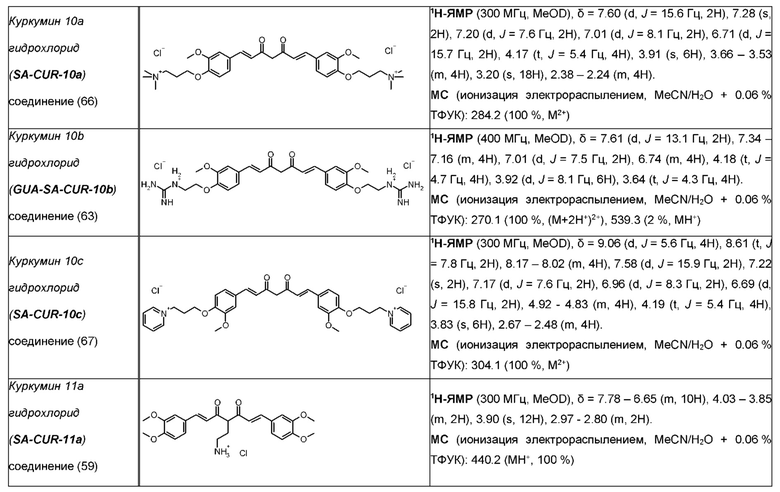
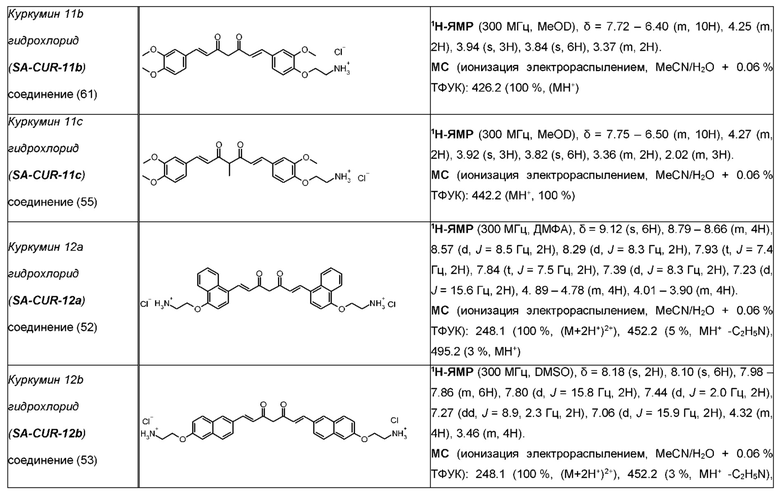
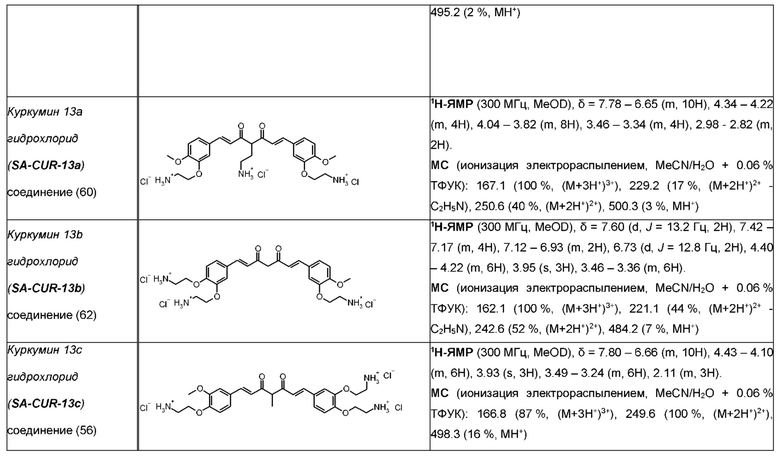
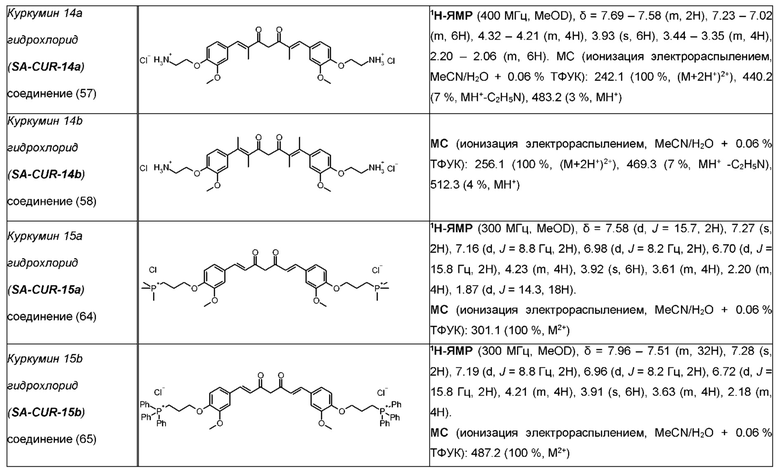
Пример 2) Эксперименты по фототоксичности
а) Получение растущих культур штаммов бактерий
Все указанные эксперименты проводили в стерильных условиях в стерильном боксе (Biosafe 4-130, Ehret, Эммендинген, Германия). После добавления фотоактивных соединений все работы осуществляли в полной темноте.
Образец клеток бактерий Staphylococcus aureus (номер АТСС: 25923) или Escherichia coli (номер АТСС: 25922) отбирали из криозамороженной культуры и выращивали в аэробных условиях при 37°С и 175 об/мин в течение ночи в орбитальной качалке (MAXQ4000, Thermo Scientific, Дубьюк, Айова, США). Выращивание осуществляли в 20 мл бульоне Тодда-Хьюитта (Carl Roth, Карлсруэ, Германия), содержащей 0,3% дрожжевого экстракта (AppliChem, Дармштадт, Германия).
В альтернативном варианте для выращивания использовали среду Мюллера-Хинтона:
Жидкая среда Мюллера-Хинтона (Merck KGaA, Дармштадт, Германия) 2,0 г/л мясного экстракта, 17,5 г/л гидролизата казеина, 1,5 г/л крахмал, рН: 7,4+0,2.
Агар Мюллера-Хинтона (Merck KGaA, Дармштадт, Германия)
2,0 г/л мясного экстракта, 17,5 г/л гидролизата казеина, 1,5 г/л крахмал, 15 г/л агара, рН: 7,4+0,2.
б) Получение культуры в экспоненциальной фазе роста
Затем делали разведения (0, 5, 10, 25 и 20% об./об. ночной культуры) и измеряли их поглощения при 600 нм в трех повторах в 100 мкл (Infinite 200 М Pro, Tecan, Меннедорф, Швейцария). С помощью калибровочной кривой (Microsoft Excel) рассчитывали объем, требующийся для получения 20 мл культуры с величиной поглощения 0,05 при 600 нм. Указанный рассчитанный объем ночной культуры добавляли к 20 мл бульона Тодда-Ньюита (состав указан выше) и выращивали в течение двух часов при 37°С при постоянном перемешивании (175 об/мин, MAXQ4000). Указанные культуры находились в экспоненциальной фазе роста; поглощение при 600 нм было между 0,3 и 0,45.
Последующую инкубацию с фотоактивными веществами, а также облучение электромагнитным излучением и определение фототоксичности осуществляли двумя различными методами.
в.1) Инкубация, облучение и определение фототоксичности
2-х часовые культуры разделяли на аликвоты объемом 1800 мкл. После центрифугирования при 20°С, 830 g, 5 мин (центрифуга 5417R, Eppendorf, Гамбург, Германия), осадки ресуспендировали в фосфатном буфере (фосфатно-солевой буфер, модифицированный по Дульбекко, DPBS, Sigma-Aldrich) либо с 10 или с 50 мкМ раствором соответствующего фотосенсибилизатора, при этом конечный объем составлял 1800 мкл.
Полученные растворы сразу же выращивали в орбитальной мешалке (параметры смотри выше) в течение 5 или 25 минут.
Для каждого фотосенсибилизатора использовали по три контроля одновременно. Контроль "только свет" содержал DPBS без фотосенсибилизатора. Контроль "только фотосенсибилизатор" ("только PS") выращивали также, как образцы PDI, но не облучали и держали строго в темноте. Следующий контроль (двойной отрицательный, "Со-/-") не получал ни света, ни фотосенсибилизатора.
После инкубации дубликаты образцов (по 500 мкл каждый) переносили в 24-луночный планшет для микротитрования (Cellstar, Greiner Bio-он, Фриккенхаузен, Германия). Образцы "только PS" и "Со -/-" помещали в их собственный планшет для микротитрования, который заворачивали в алюминиевую фольгу, чтобы обеспечить полную светонепроницаемость.
Выращивание осуществляли при постоянном перемешивании (MTS4, IKA, Штауфен, Германия, ~ 175 об/мин) снизу на светодиодной матрице с максимальной однородностью освещающей поверхности. Все указанные контроли перемешивали одинаково. Технические данные для источника света приведены в Таблице 2; общая доза света составила 33,8 Дж/см2.

Определение количества колониеобразующих единиц (КОЕ) осуществляли в соответствии с методом, опубликованным Miles и Misra (Miles, АА; Misra, SS, Irwin, JO (1938 Nov), "The estimation of the bactericidal power of the blood" The Journal of hygiene 38 (6): 732-49). В связи с этим серийные разведения (1:10) соответствующей бактериальной суспензии были получены в DPBS. Затем 5×10 мкл каждого бактериального разведения капали на чашки Тодда-Хьюитта (с бульоном, содержащим 1,5% агара (агар-агар, Kobe I, Roth, Карлсруэ, Германия) и выращивали при 37°С в течение 24 ч. Затем определяли количество выживших колониеобразующих единиц. Все тесты проводили четыре раза.
в.2) Инкубация, облучение и определение фототоксичности
Во втором эксперименте использованные фотосенсибилизаторы (PS) растворяли в воде Millipore и доводили до различных концентраций. 25 мкл бактериальной суспензии, выращенной в течение ночи (~ 108/мл), выращивали с 25 мкл раствора фотосенсибилизатора различных концентраций при комнатной температуре в течение 10 секунд в темноте в 96-луночном планшете.
Затем суспензию облучали в течение 5-20 минут. Для облучения использовали источник света BlueV от Waldmann (Филлинген-Швеннинген, Германия), который излучает свет от 380 до 480 нм (максимум излучения примерно при 420 нм). Плотность приложенной энергии составляла 17,5 мВт/см2.
Каждый эксперимент сопровождался тремя контролями, чтобы исключить побочный эффект облучения / фотосенсибилизатора (PS) на выживаемость бактерий: (i) без PS, только свет (= контроль со светом), (ii) без света, только PS (= контроль в темноте) и (iii) без света, без PS (= базовый контроль). Определение количества колониеобразующих единиц (КОЕ) на мл также осуществляли в соответствии с методом, опубликованным Miles, Misra и Irwin, описанным выше в разделе в.1). Все тесты осуществляли четыре раза.
г) Результаты экспериментов по фототоксичности
Результаты экспериментов по фототоксичности, описанные выше в разделе в.1), показаны на Фигурах 1-20. Фотосенсибилизаторы тестировали на бактериальном штамме Е. coli АТСС 25922. На Фигурах 1-20 показаны измеренные количества колониеобразующих единиц (КОЕ).
Результаты экспериментов по фототоксичности, описанные в разделе в.2), показаны на Фигурах с 21 по 33. Фотосенсибилизаторы (PS) SACUR-01a, SACUR-03 и SACUR-07 тестировали на бактериальных штаммах S. aureus АТСС 25923 и Е. coli АТСС 25922 (Фиг. 21-23). Все остальные PS протестировали на штамме S. aureus АТСС 25923 (Фиг. 24-33). На Фиг. 21-33 показано логарифмическое уменьшение после освещения относительно контрольного контроля.
На Фиг. 21 показаны результаты эксперимента по фототоксичности с использованием SACUR-01a на штамме Е. coli АТСС 25922 (слева) и на штамме S. aureus АТСС 25923 (справа). Время облучения для Е. coli составляло 15 минут; для S. aureus - 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) составлял 3,6×108/мл для Е. coli и 3,9×108/мл для S. aureus.
На Фиг. 22 показаны результаты эксперимента по фототоксичности с использованием SACUR-03 на штамме Е. coli АТСС 25922 (слева) и на штамме S. aureus АТСС 25923 (справа). Время облучения для Е. coli составляло 15 минут; для S. aureus - 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) составлял 3,3×108/мл для Е. coli и 4,3×108/мл для S. aureus.
На Фиг. 23 показаны результаты эксперимента по фототоксичности с использованием SACUR-07 на штамме Е. coli АТСС 25922 (слева) и на штамме S. aureus АТСС 25923 (справа). Время облучения для Е. coli составляло 45 минут; для S. aureus - 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) составлял 2,6×108/мл для Е. coli и 3,6×108/мл для S. aureus.
На Фиг. 24 показаны результаты эксперимента по фототоксичности с использованием SACUR-01a BF2 на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 3,6×108 бактерий на мл.
На Фиг. 25 показаны результаты эксперимента по фототоксичности с использованием SACUR-09a на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 3,3×108 бактерий на мл.
На Фиг. 26 показаны результаты эксперимента по фототоксичности с использованием SACUR-11a на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 6,3×108 бактерий на мл.
На Фиг. 27 показаны результаты эксперимента по фототоксичности с использованием SACUR-11с на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 5,1×108 бактерий на мл.
На Фиг. 28 показаны результаты эксперимента по фототоксичности с использованием SACUR-12b на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 30 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 6,2×108 бактерий на мл.
На Фиг. 29 показаны результаты эксперимента по фототоксичности с использованием SACUR-13a на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 7,5×108 бактерий на мл.
На Фиг. 30 показаны результаты эксперимента по фототоксичности с использованием SACUR-13C на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 5,5×108 бактерий на мл.
На Фиг. 31 показаны результаты эксперимента по фототоксичности с использованием SACUR-14a на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 10 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 4,2×108 бактерий на мл.
На Фиг. 32 показаны результаты эксперимента по фототоксичности с использованием SACUR-15a на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 3,6×108 бактерий на мл.
На Фиг. 33 показаны результаты эксперимента по фототоксичности с использованием SACUR-15b на штамме S. aureus АТСС 25923. Время облучения для S. aureus составляло 5 минут. Средний базовый контроль (среднее арифметическое со стандартным отклонением) (без света, без PS) соответствовал ~ 6,3×108 бактерий на мл.
Как видно из Фиг. 1-33, облучение использованных микроорганизмов, Staphylococcus aureus (S. aureus) и Escherichia coli (E. coli), описанной световой дозой синего света (390-500 нм) в отсутствие фотосенсибилизатора (0 мкМ соответствующего куркумина) не влияло на количество выживших микроорганизмов по сравнению с неосвещенным контролем.
В Таблице 3 показано влияние испытуемых веществ на штамм Е. coli АТСС 25922 с приложенной световой дозой 33,8 Дж/см2 для максимума излучения приблизительно при 435 нм (60 минут освещения с интенсивностью 9,4 мВт/см2). Значение для среднего базового контроля (среднее арифметическое со стандартным отклонением) (без света, без PS) составляло 3,6×108/мл. Логарифмическое уменьшение после освещения показано относительно базового контроля. Соответствующее верхнее значение, обозначенное *, относится к инкубационному периоду в 5 мин и соответственно нижнее значение, обозначенное #, относится к инкубационному периоду в 25 мин.
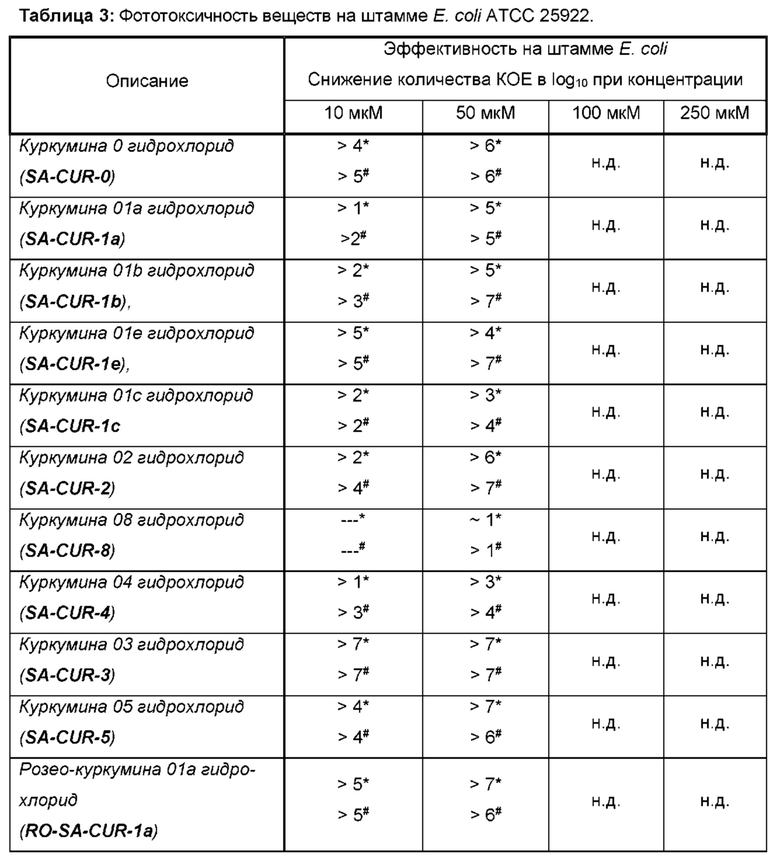
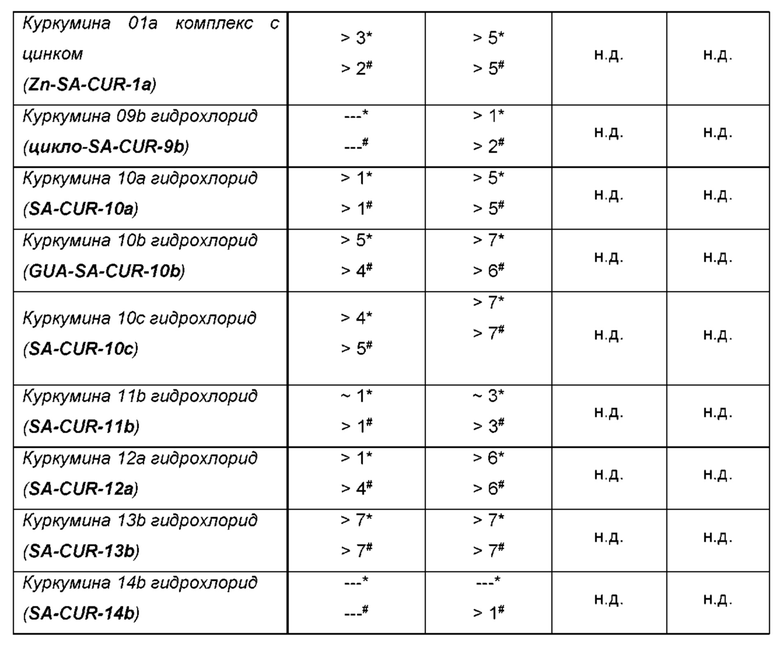
В Таблице 4 показано действие испытуемых веществ на штамм Е. coli АТСС 25922 для приложенной световой дозы 15,7 Дж/см2 с максимумом излучения примерно при 420 нм (15 мин освещения при интенсивности 17,5 мВт/см2). Значение для среднего базового контроля (среднее арифметическое со стандартным отклонением) (без света, без PS) составляло 3,6×108/мл для кишечной палочки. Логарифмическое уменьшение после освещения показано относительно базового контроля.
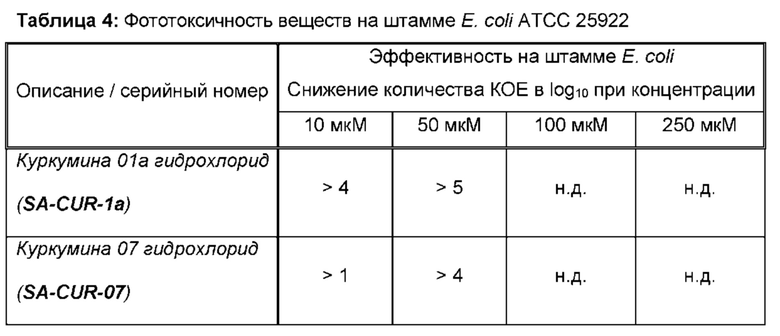
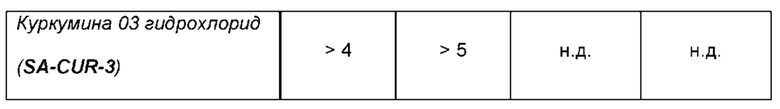
В Таблице 5 показано действие испытуемых веществ на штамм S. aureus АТСС 25923. Время облучения составляло 5 минут (максимум излучения примерно при 420 нм) для приложенной интенсивности 17,5 мВт/см2, т.е. приложенной световой энергии (дозировка) 5,3 Дж/см2. Значение для среднего базового контроля (среднее арифметическое со стандартным отклонением) (без света, без PS) составляло 3,9×108/мл. Логарифмическое уменьшение после освещения показано относительно базового контроля.
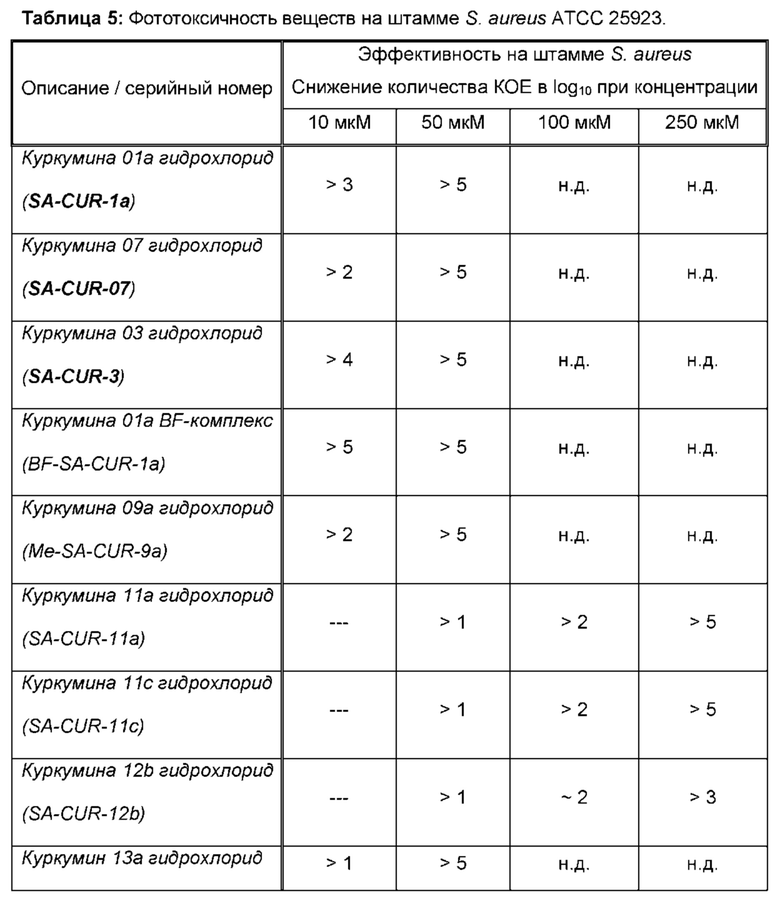
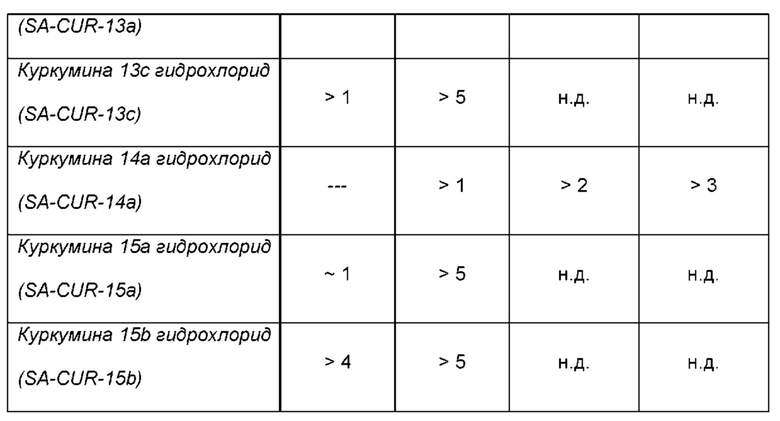
Как ясно видно из Фиг. 1-33, после инкубации микроорганизмов в соответствии с используемыми концентрациями соответствующих фотосенсибилизаторов и последующего облучения с приведенной выше дозировкой света происходит снижение КОЕ/мл и, таким образом, инактивация Е. coli и S. aureus.
Сравнительный Пример 3
В дальнейшем испытывали стабильность и фототоксичность следующих соединений.
Соединение CRANAD-2 представляет собой хороший флуорофор, который имеет квантовый выход флуоресценции, сравнимый с родаминовыми красителями или красителями Су5.
Инкубацию CRANAD-2 с бактериальными штаммами S. aureus АТСС 25923 и Е. coli АТСС 25922, а также облучение электромагнитным излучением и определение фототоксичности проводили, как описано в разделах в.1) и в.2) выше. Инактивация тестируемых бактериальных штаммов S. aureus АТСС 25923 и Е. coli АТСС 25922 при освещении в присутствии CRANAD-2 не обнаруживалась ни одним из методов.
Из-за наличия аминных заместителей непосредственно в ароматическом кольце, которые могут выступать в качестве доноров электронных пар, фотофизика смещается в синглетный процесс, и для триплетных процессов доступно значительно меньше энергии. Хорошая передача энергии на триплетный уровень должна быть предпосылкой для фотодинамического эффекта, который, однако, не наблюдался для соединения CRANAD-2.
Инкубацию соединения (71) (SACUR-01d) с бактериальными штаммами S. aureus АТСС 25923 и Е. coli АТСС 25922, а также облучение электромагнитным излучением и определение фототоксичности проводили, как описано в разделах в.1) и в.2) выше. Какая-либо инактивация тестируемых бактериальных штаммов S. aureus АТСС 25923 и Е. coli АТСС 25922 не наблюдалась ни в одном из способов при освещении в присутствии соединения (71) (SACUR-01d), поскольку разложение соединения в измеряемом растворе означало, что не были получены надежные значения. Соединение (71) (SACUR-01d) проявляло низкую стабильность в водном растворе, которая была сравнимой с природным основным веществом куркумин. Свободные ОН-группы вносят большой вклад в эту фотонестабильность, потому что благодаря им соединение может легко превращаться в хиноидный мезомер, и таким образом облегчается отщепление одной половины молекулы с образованием феруловых кислот или замещенных ванилинов.
Молярный коэффициент экстинкции для соединения (71) (SACUR-01d) при 420 нм в водных растворах А-С, приведенных ниже, варьировался между 8000 и 16000 М-1 см-1 и, таким образом, был значительно меньше, чем известное значение для куркумина (ε420, H2O=23800 М-1 см-1) (см. Arnaut LG, Formosinho SJ. J. Photochem. Photobiol. A: Chem. 75, 1993, страницы 1-20). Эти результаты показывают, что соединение (71) не обладает достаточной стабильностью в водном растворе для установления фотодинамического эффекта после облучения. Водный раствор А: дистиллированная вода.
Водный раствор В: изотонический раствор хлорида натрия (0,9 мас. % NaCl). Водный раствор С: буфер PBS, рН 7,4 (состав см. в Sambrook, J.; Maniatis, Т.; Russel, D.W.: Molecular cloning: a laboratory manual. Cold Spring Harbor Laboratory Press; 3-я редакция (2001)).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ ПАЛЛАДИЙ (0) | 2003 |
|
RU2334754C2 |
| ИЗМЕНЕНИЕ ЦВЕТА ВОЛОС С ЗАЩИТОЙ КОЖИ | 2007 |
|
RU2462228C2 |
| ОЛИГОМЕРНЫЕ СОЕДИНЕНИЯ, КОМПОЗИЦИЯ, СПОСОБ СТАБИЛИЗАЦИИ И ОЛИГОМЕРНЫЕ ПРОДУКТЫ | 1993 |
|
RU2130461C1 |
| ЗАМЕЩЕННЫЕ ИНДОЛЫ | 2000 |
|
RU2255087C2 |
| ЗАМЕЩЕННЫЕ БЕНЗИМИДАЗОЛЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2000 |
|
RU2261248C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 2-ПИРИДИНЦИКЛОГЕКСАН-1, 4-ДИАМИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2002 |
|
RU2287523C2 |
| СИЛАНЫ И ОТВЕРЖДАЕМЫЕ КОМПОЗИЦИИ, КОТОРЫЕ СОДЕРЖАТ ЭТИ СИЛАНЫ В КАЧЕСТВЕ СШИВАЮЩИХ АГЕНТОВ | 2016 |
|
RU2711919C2 |
| ЖИДКИЕ ПРЕПАРАТИВНЫЕ ФОРМЫ | 2001 |
|
RU2324350C9 |
| N-ГУАНИДИНОАЛКИЛАМИДЫ, ИХ ПОЛУЧЕНИЕ, ИХ ПРИМЕНЕНИЕ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ | 2000 |
|
RU2253651C2 |
| ПРОИЗВОДНЫЕ ОКСАЗОЛИДИНА, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ИЛИ СЛОЖНЫЕ ЭФИРЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2090564C1 |
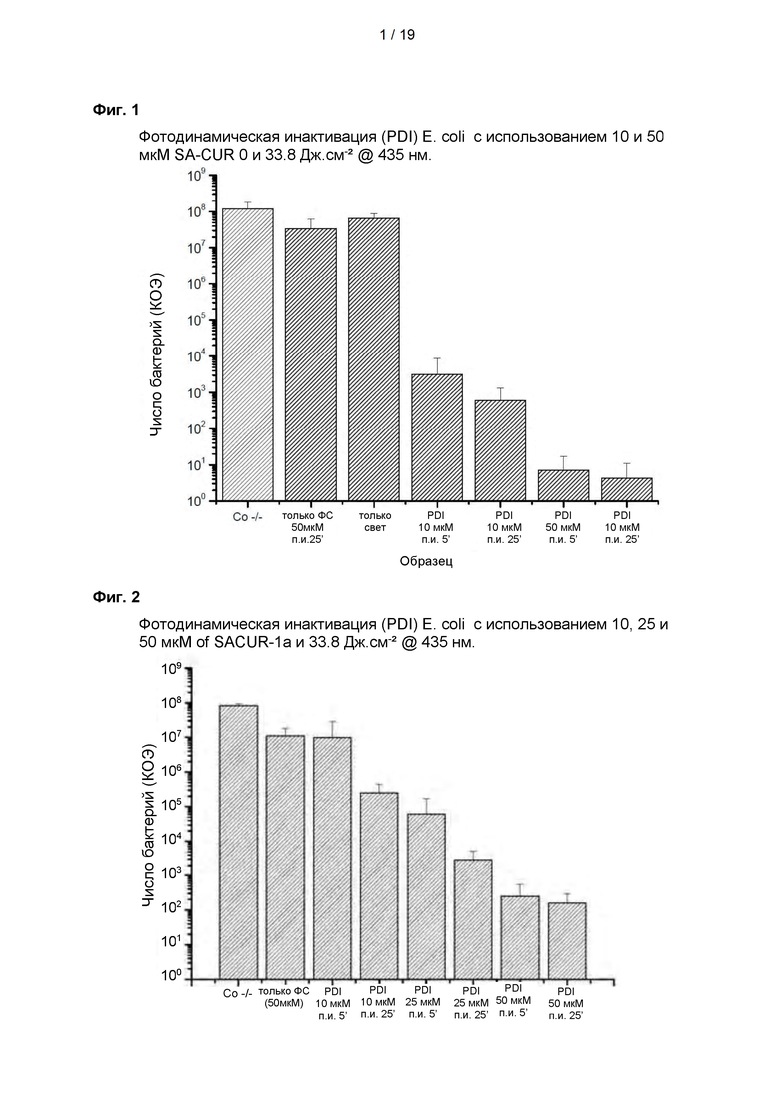
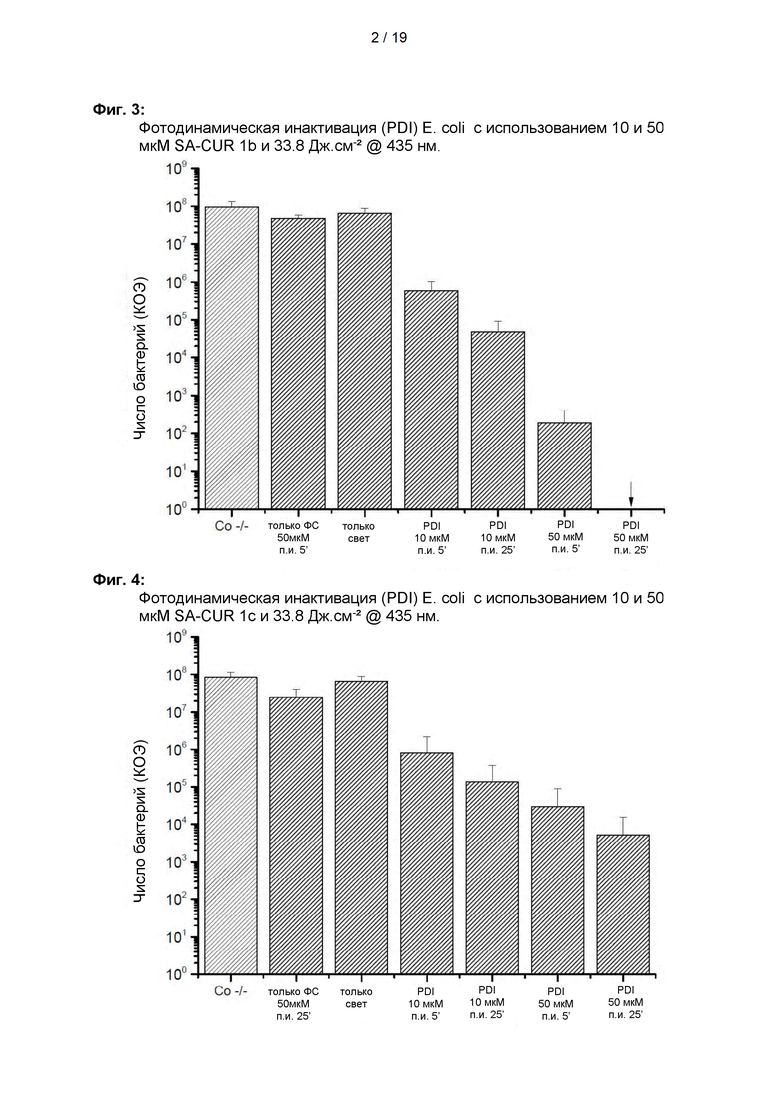
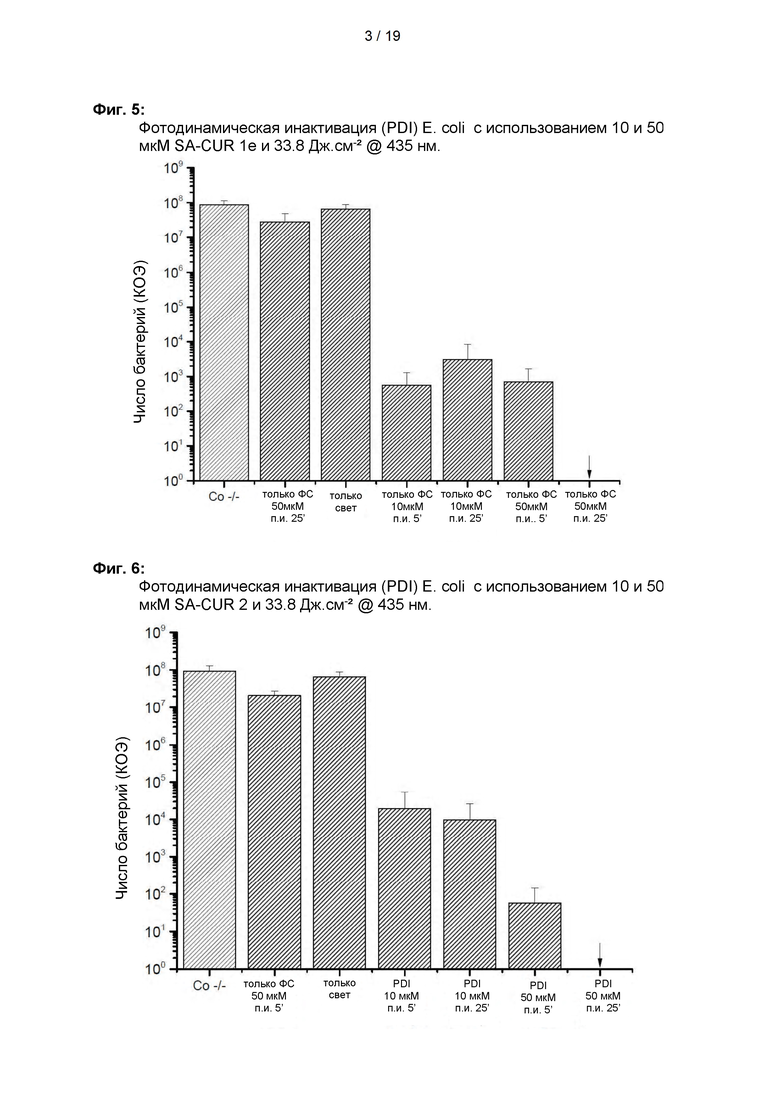
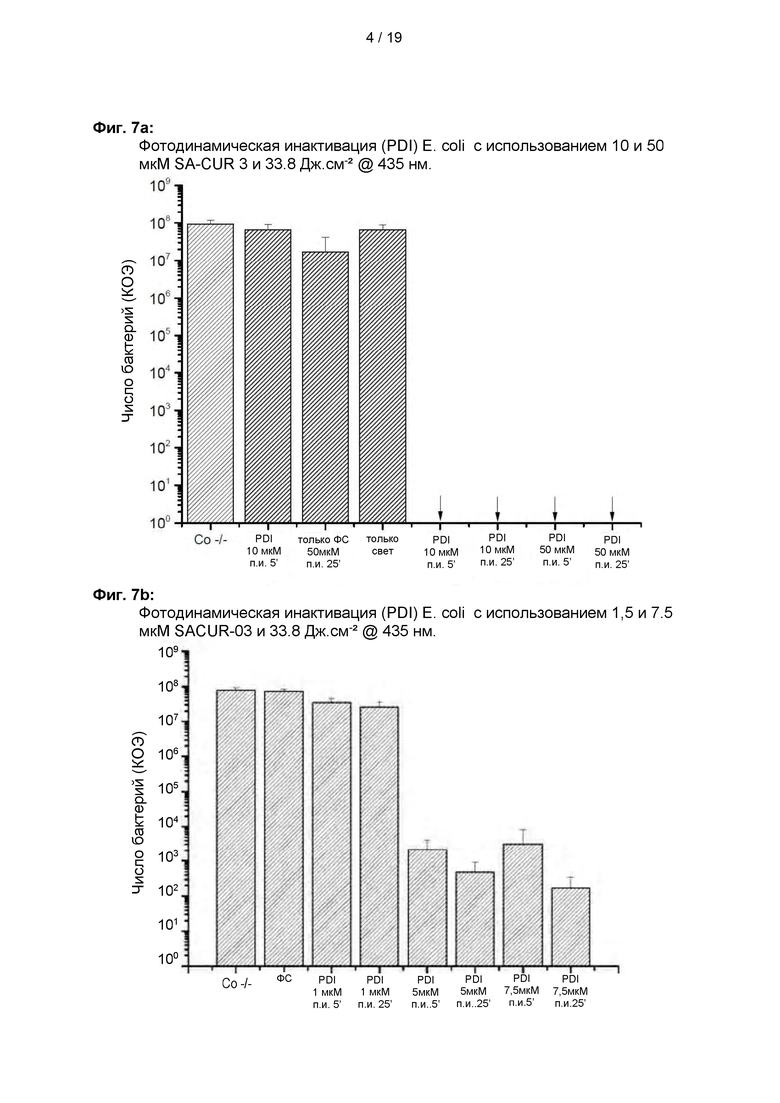
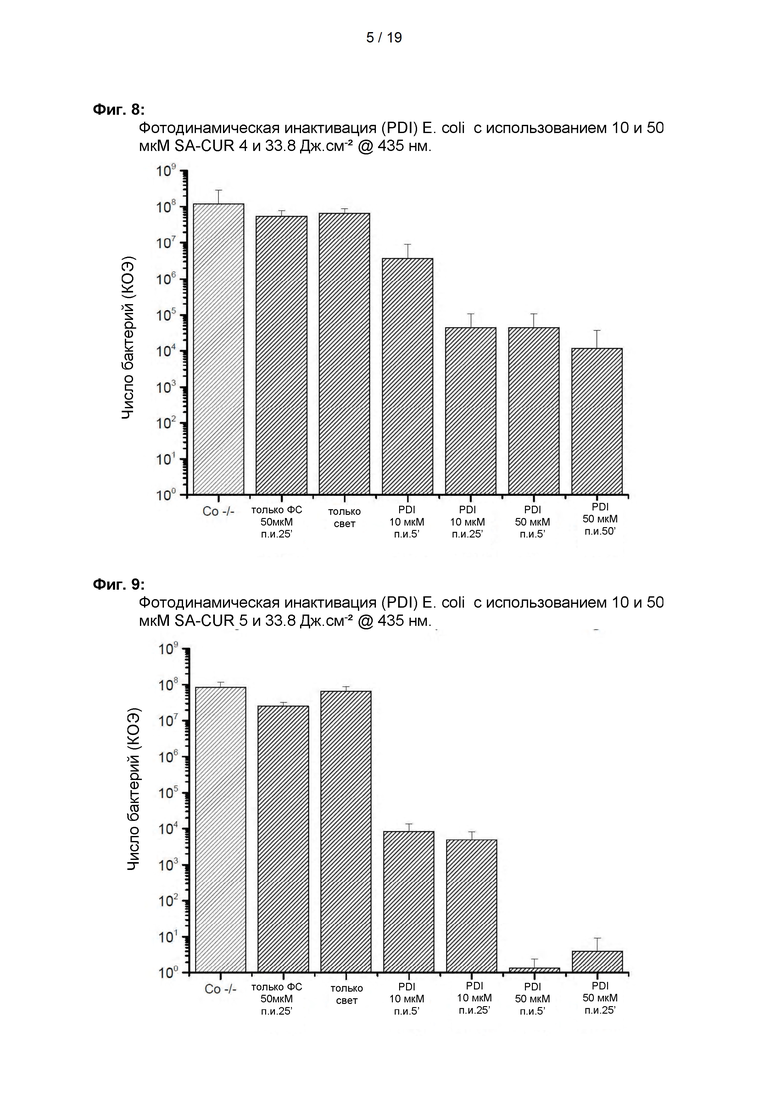
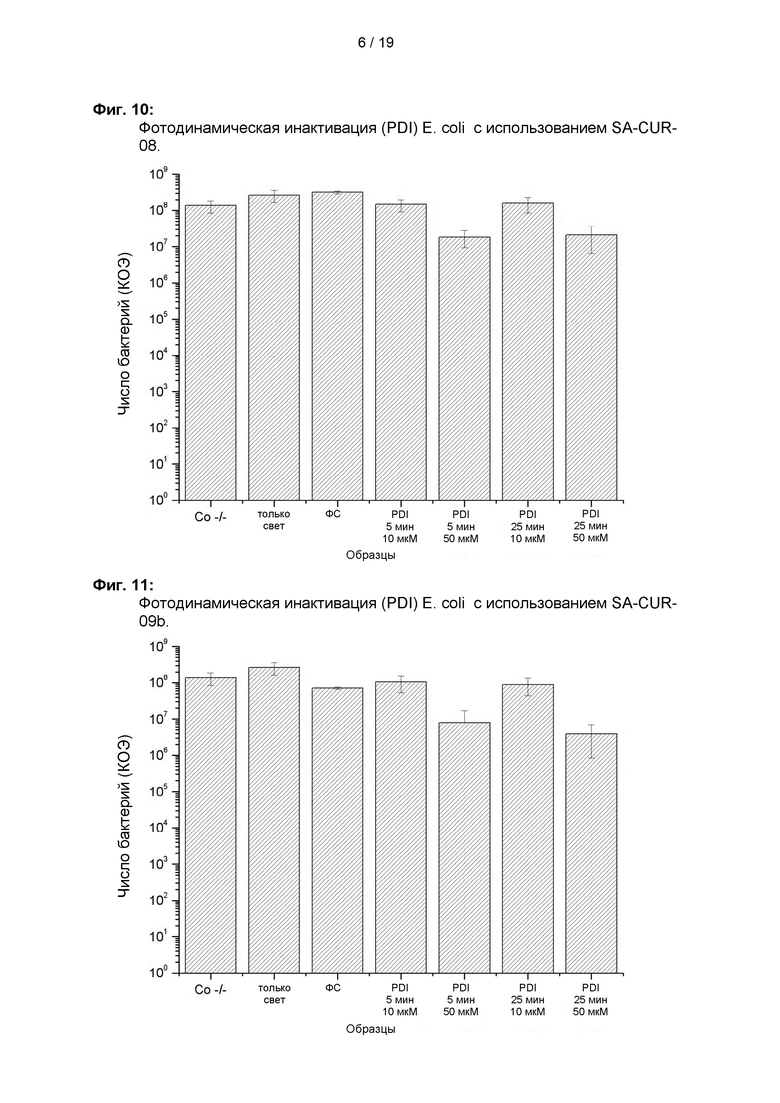
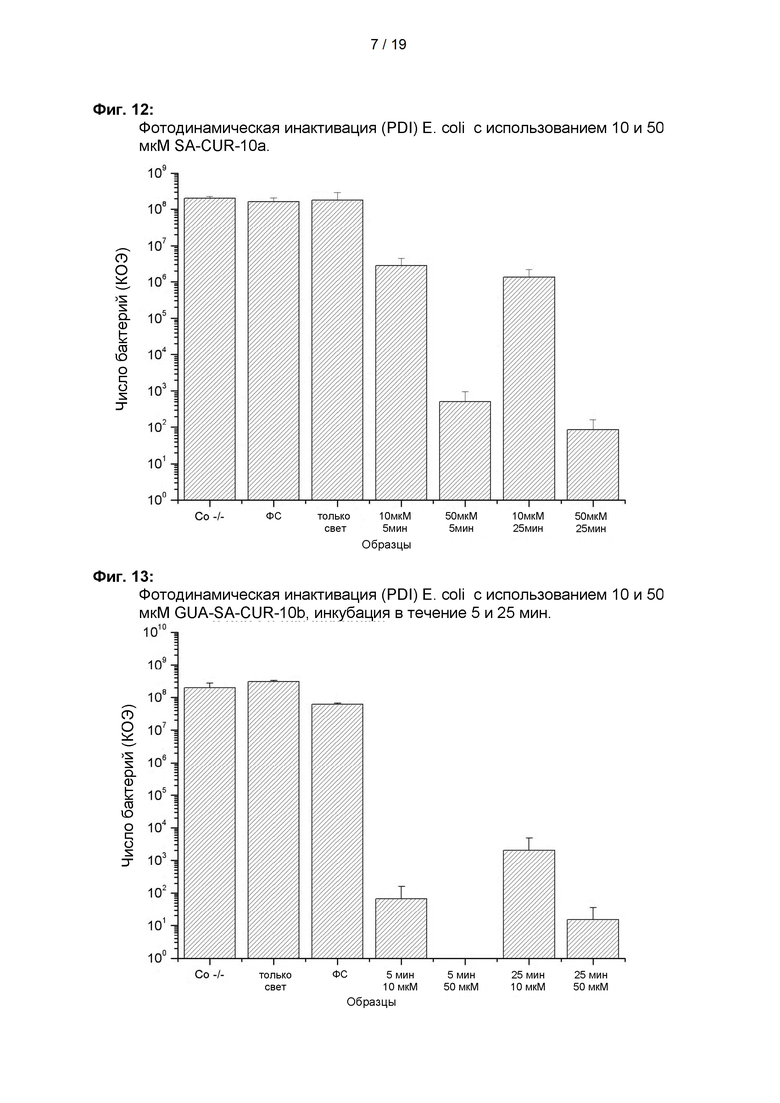
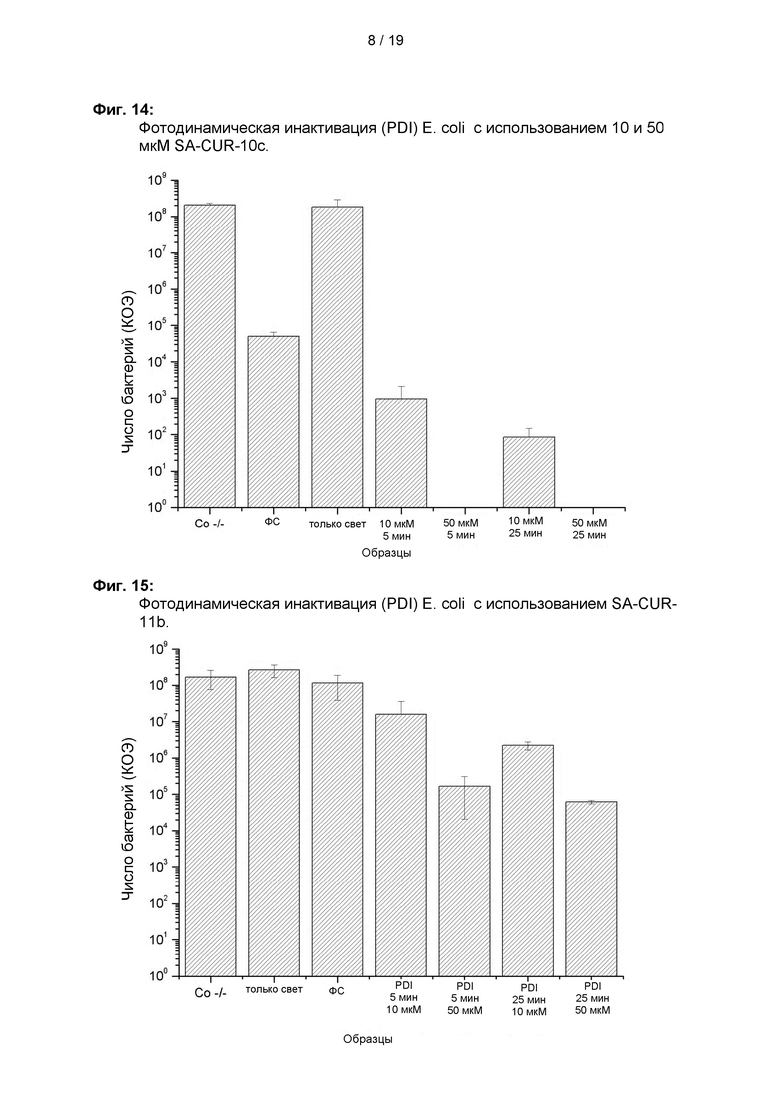
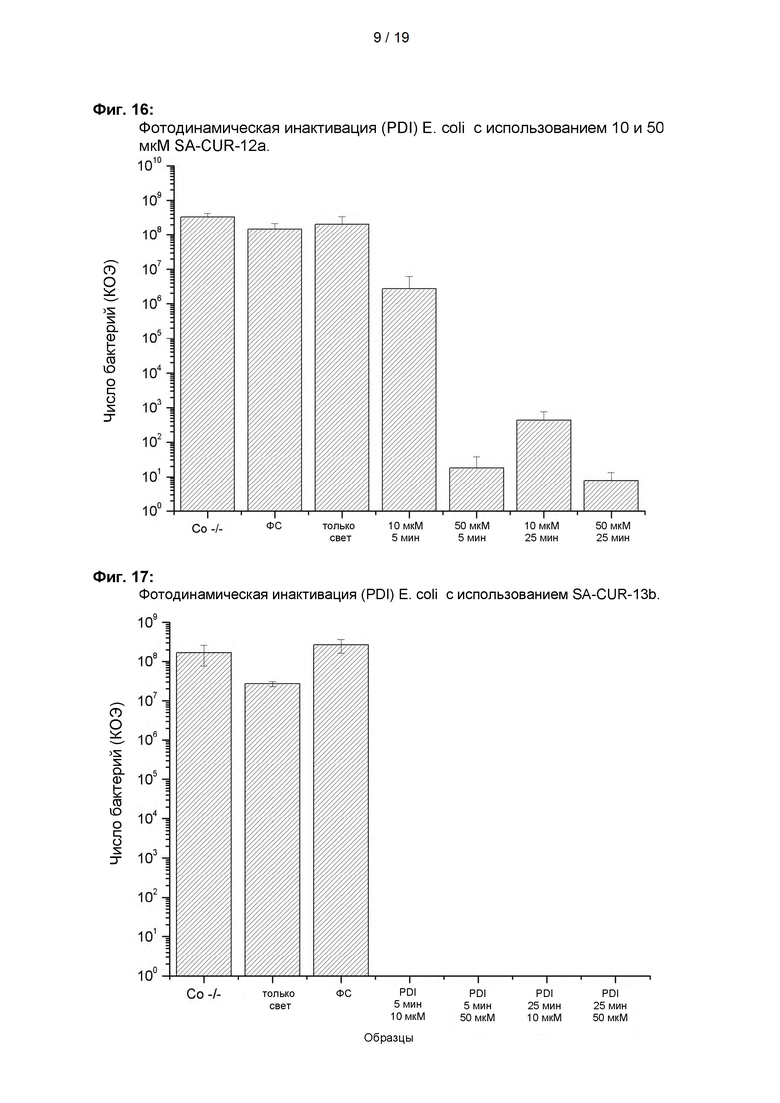
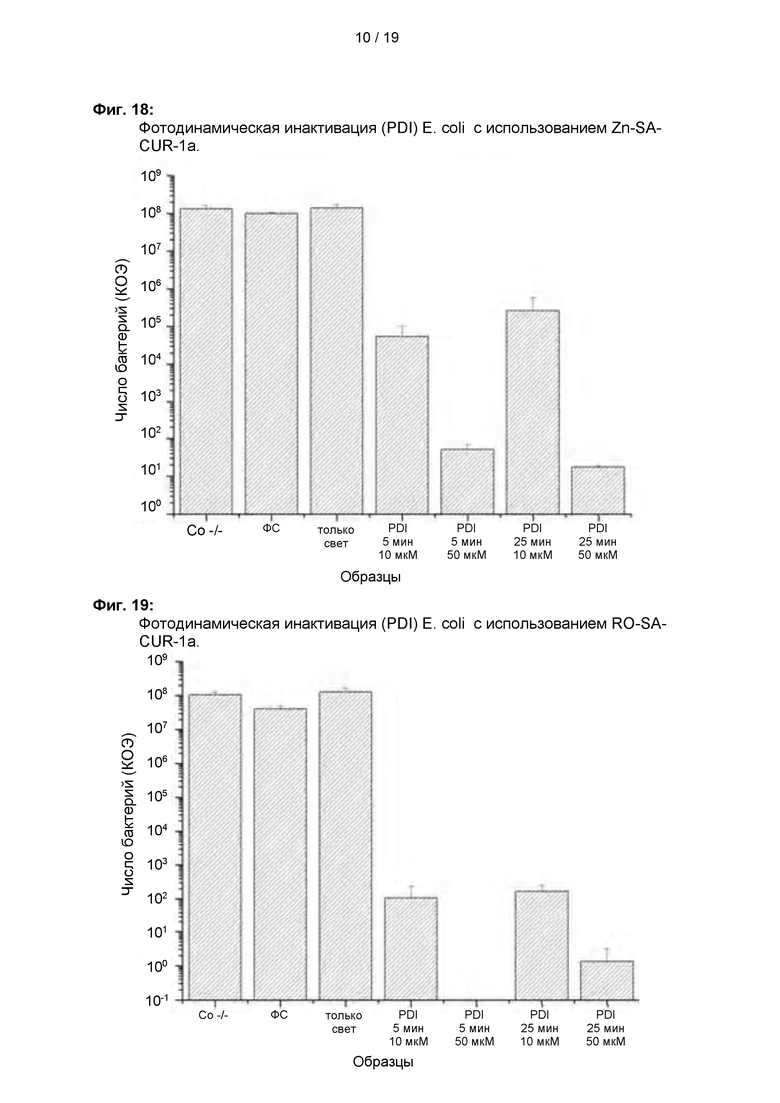
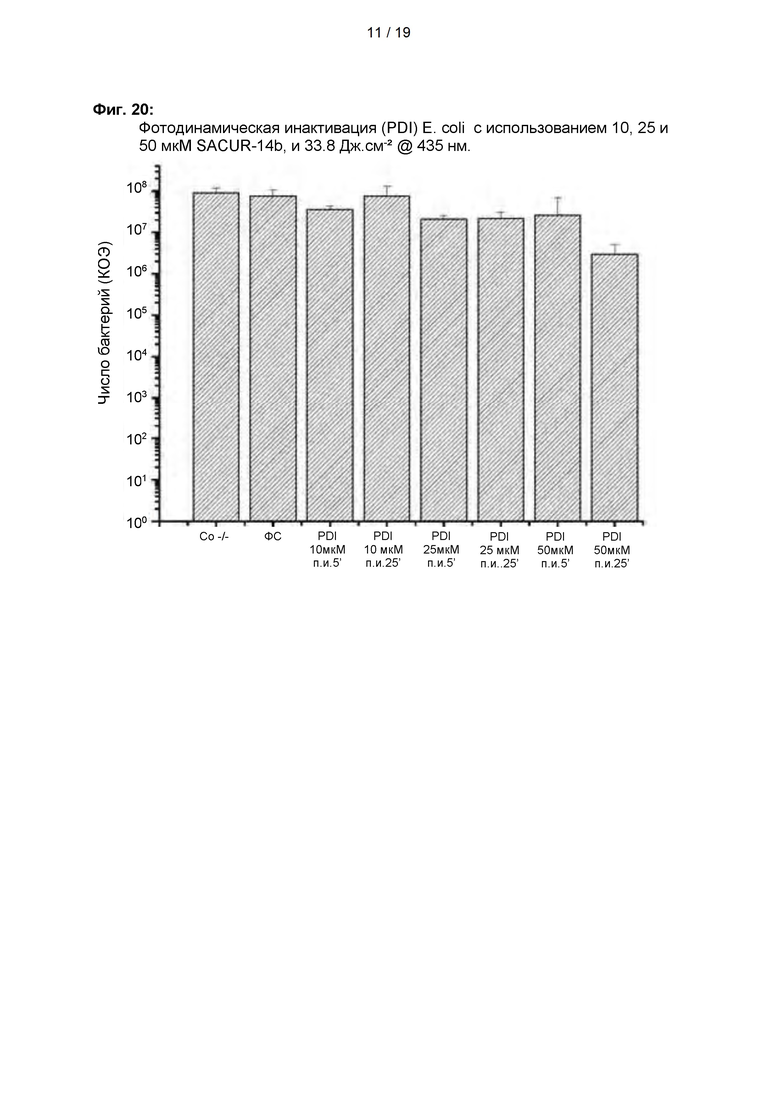
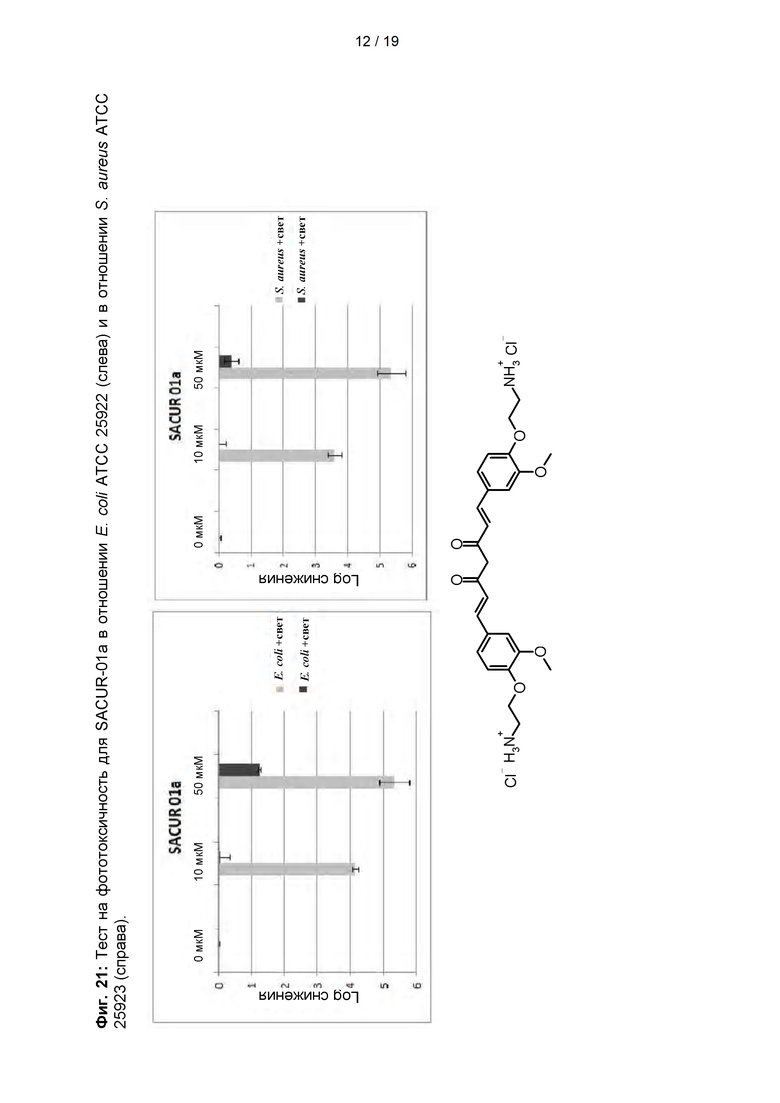
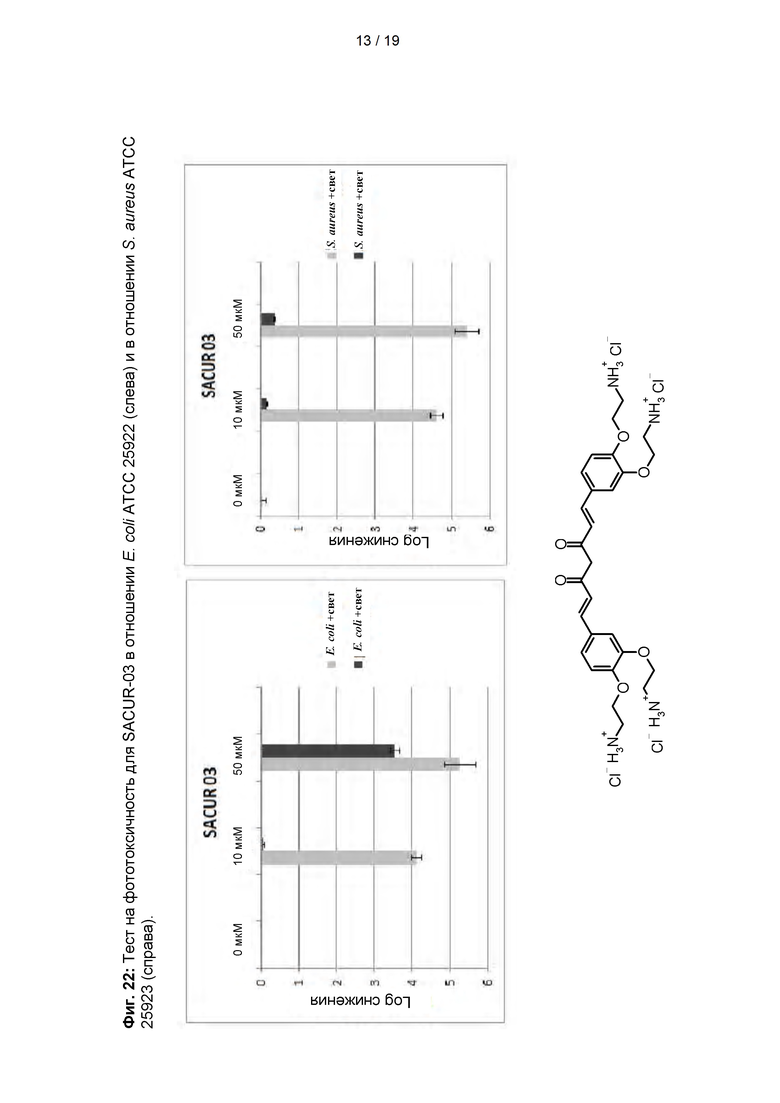

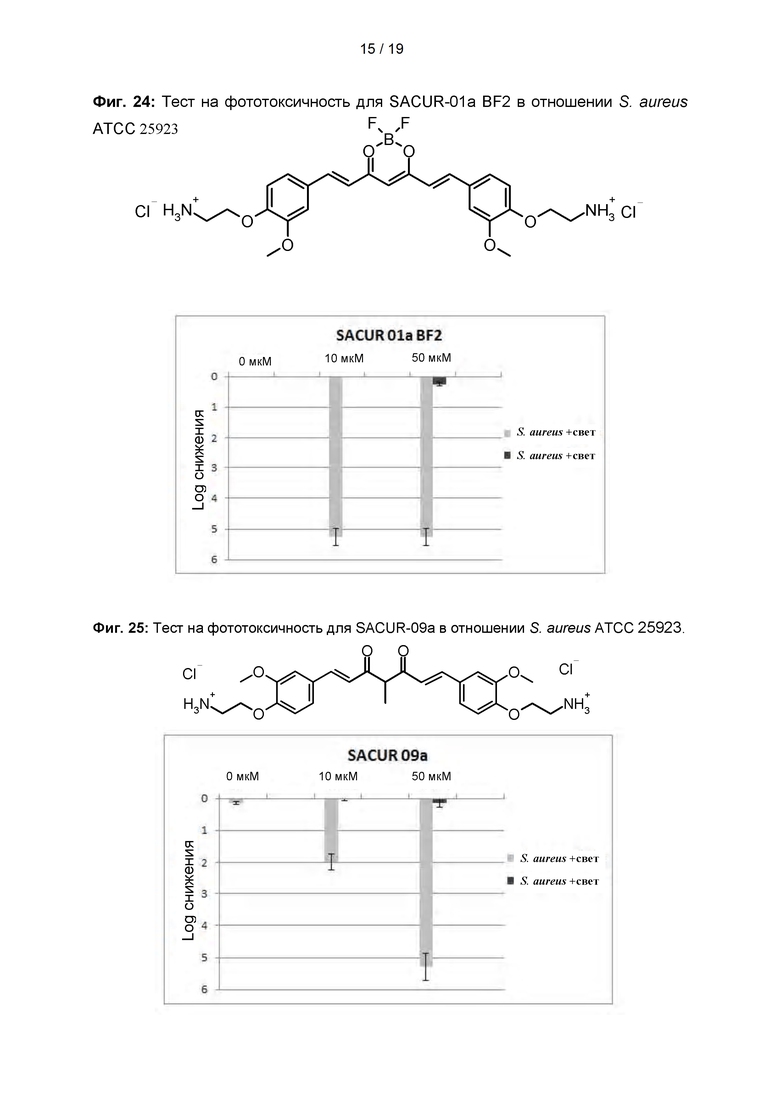

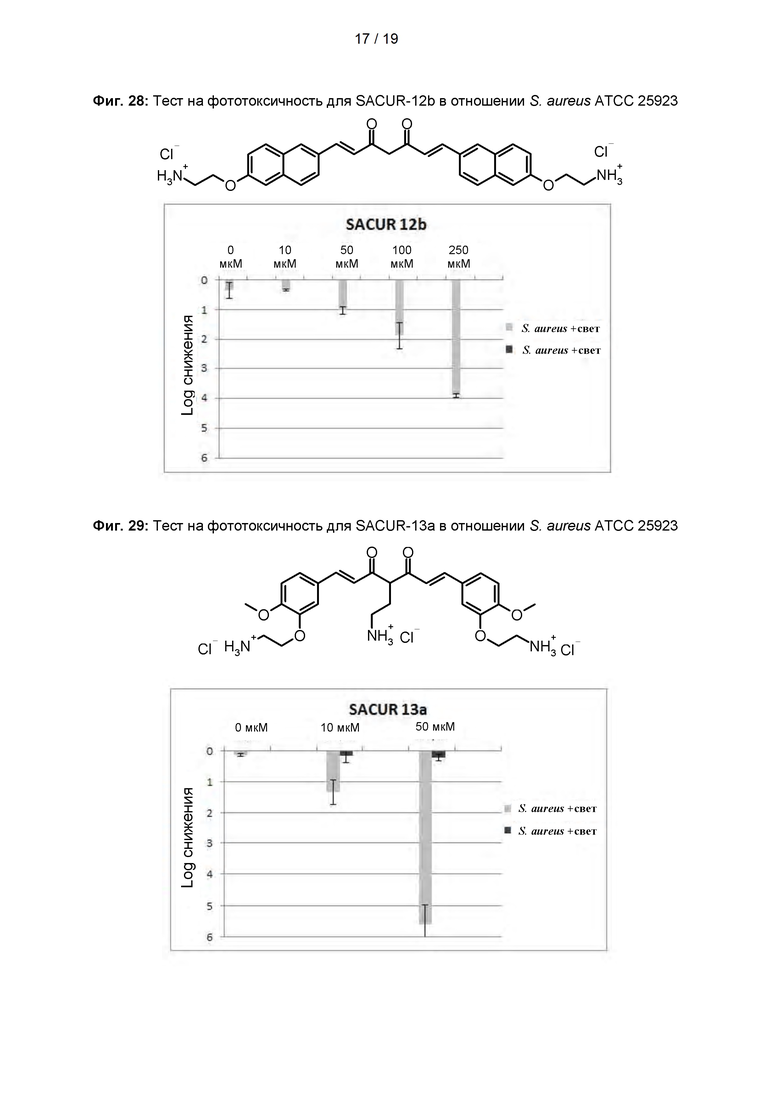
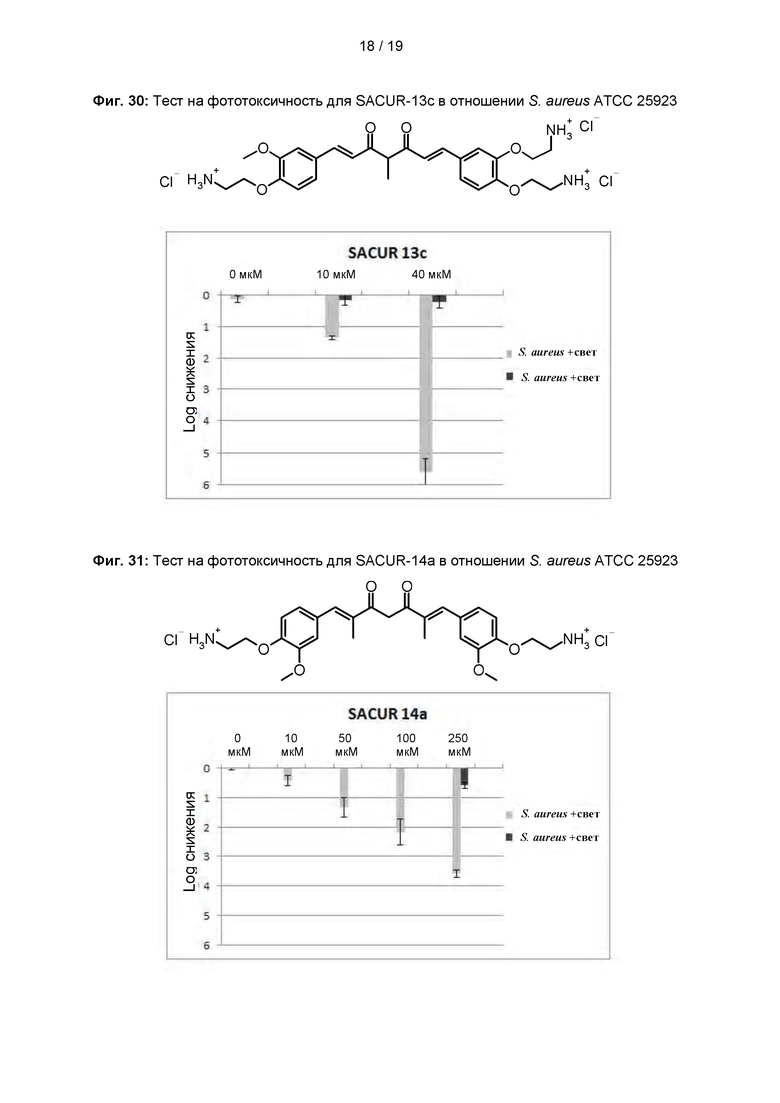
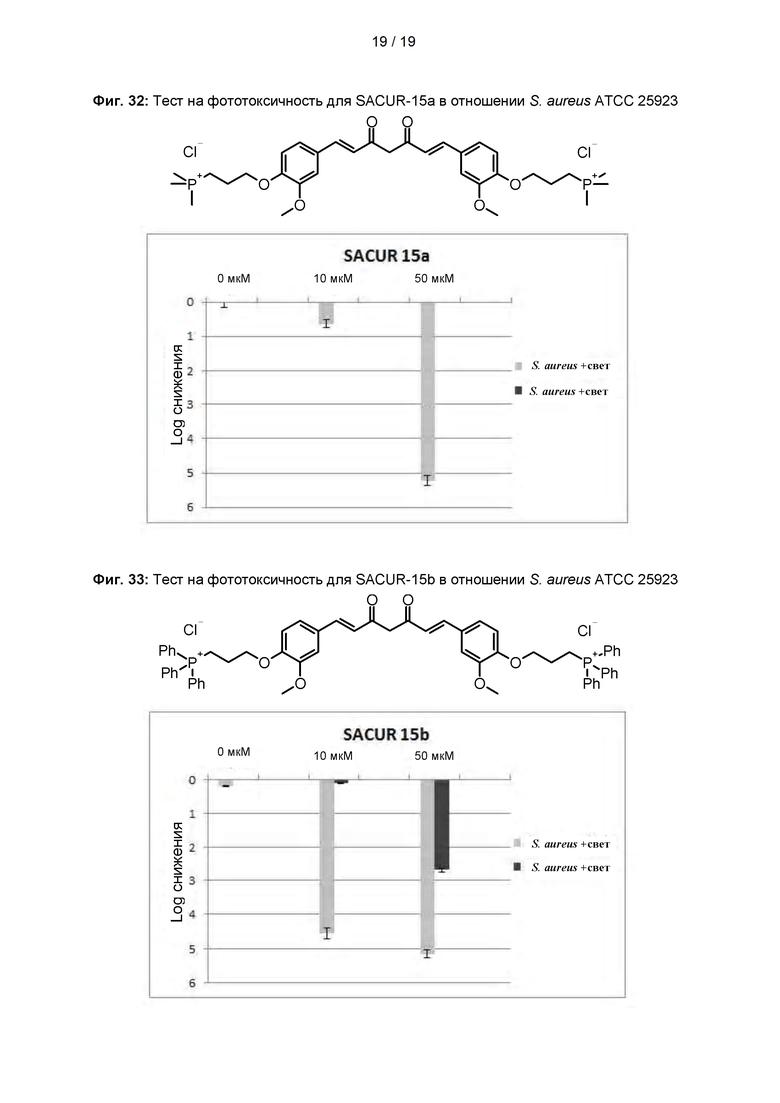
Изобретение относится к фотосенсибилизаторам для инактивации микроорганизмов. Предложены соединения (производные) 1,7-диарил-1,6-гептадиен-3,5-диона, используемые в качестве фотосенсибилизатора в медицинском лечении для инактивации микроорганизмов, а также для очистки поверхности, покрытия изделий, дезинфекции жидкостей и пищевых продуктов. Способ инактивации микроорганизмов предусматривает приведение в контакт микроорганизмов с по меньшей мере одним фотосенсибилизатором и облучение указанных микроорганизмов электромагнитным излучением. Изобретение позволяет повысить эффективность инактивации микроорганизмов. 6 н. и 18 з.п. ф-лы, 33 ил., 5 табл., 2 пр.
1. Соединение 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1)
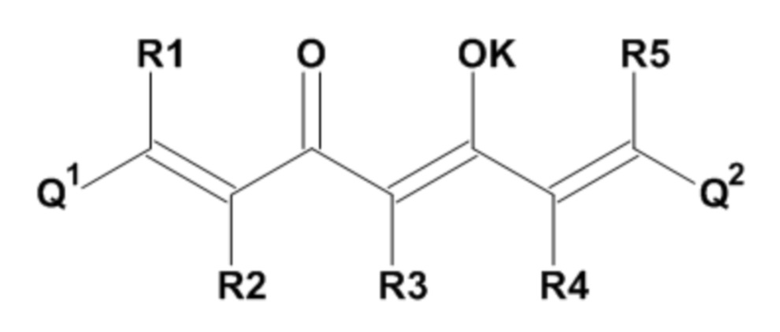 , (1)
, (1)
где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
где соединение 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1) не содержит группу OH, которая напрямую связана с органическим остатком Q1 или Q2, и
где K представляет водород или катион, и где
(a) по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1a, где
указанный по меньшей мере один органический остаток W1a имеет общую формулу (5a), (6a), (7a), (8a) или (9a):
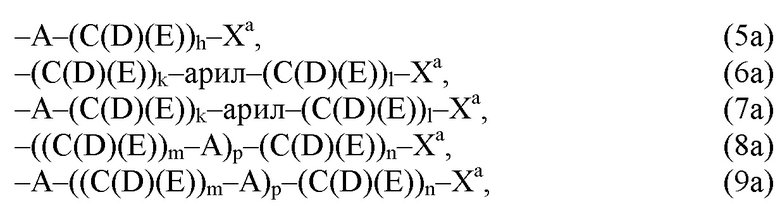
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xa, соответственно, независимо от других, представляет остаток формулы (20c), (20d) или (21):
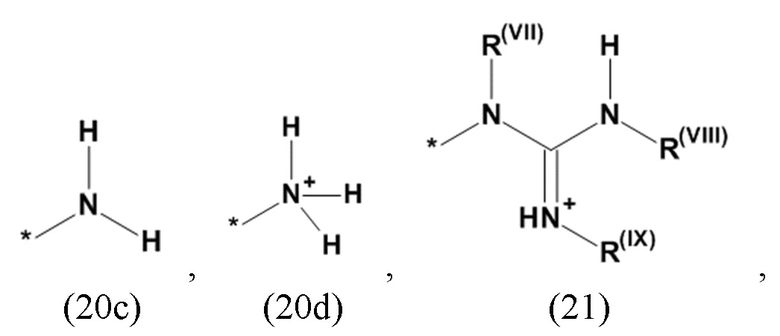
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, циклоалкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C,
или где
(b) остаток R3 представляет собой органический остаток W2a, который содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, и/или по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота и/или по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, где
указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
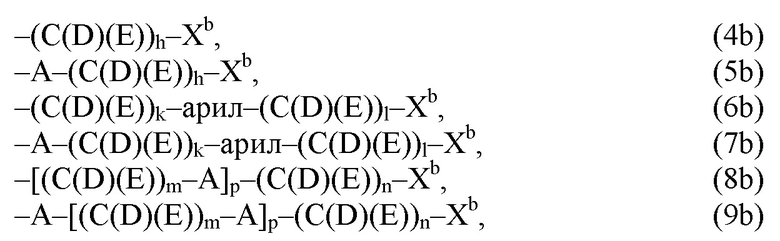
и
где, необязательно, по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1b, имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b),
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C.
2. Соединение по п. 1,
где K представляет катион Mz+ металла M, где z представляет собой формальную степень окисления указанного металла M и представляет собой целое число от 1 до 7, предпочтительно от 2 до 5, и
где указанное соединение имеет формулу (2)
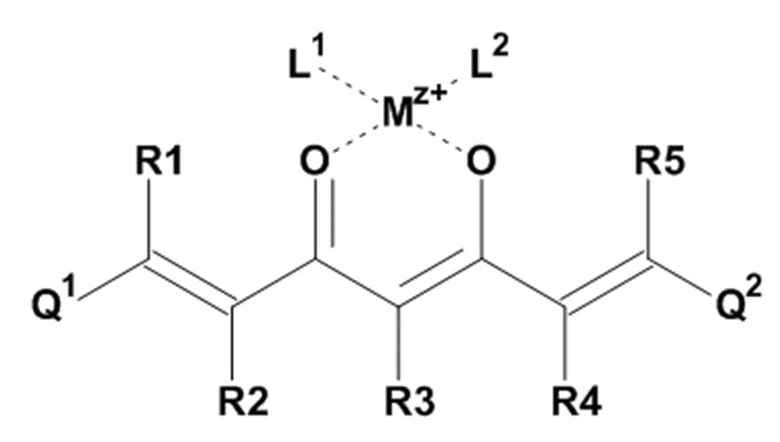 , (2)
, (2)
где L1 и L2, соответственно, независимо от других, представляют воду, галид, цианид, тиоцианат, фосфат, гидрофосфат или карбоксилат-ион карбоновой кислоты, содержащей от 1 до 10 атомов углерода, предпочтительно формиат, ацетат, н-пропионат, лактат, оксалат, фумарат, малеинат, тартрат, сукцинилат, бензоат, салицилат или цитрат.
3. Соединение 1,7-диарил-1,6-гептадиен-3,5-диона формулы (3)
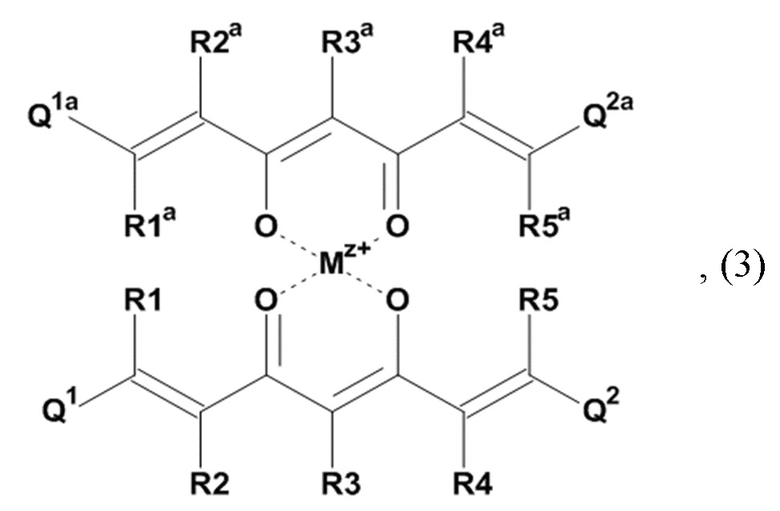
где Mz+ представляет катион металла, где z представляет собой формальную степень окисления указанного металла M и представляет собой целое число от 1 до 7, предпочтительно от 2 до 5, и
где Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остатки Q1a и Q2a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток,
и где
(a) по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1a, имеющий общую формулу (5a), (6a), (7a), (8a) или (9a):
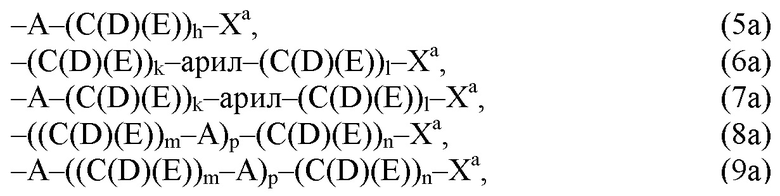
где по меньшей мере один из остатков Q1a и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1c, имеющий общую формулу (5c), (6c), (7c), (8c) или (9c):
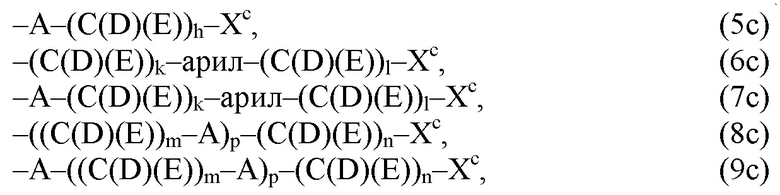
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота, и
где Xa, соответственно, независимо от других, представляет остаток формулы (20c), (20d), (21) или (24):
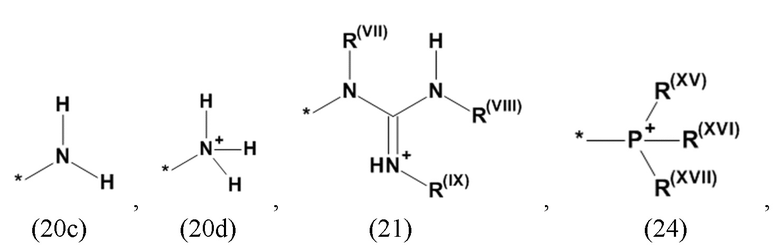
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляет водород, арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и
где Xc, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, и
где остатки R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, циклоалкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C,
или где
(b) остаток R3 или R3a, соответственно, независимо от других, представляет собой органический остаток W2a, где
указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
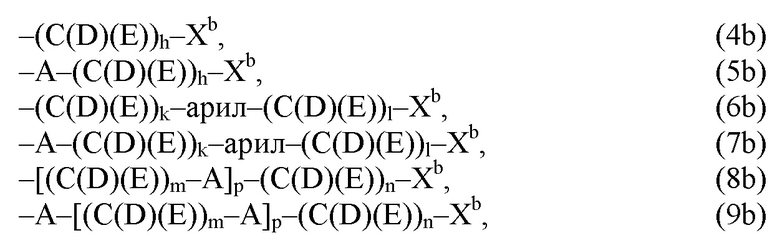
и
где, необязательно, по меньшей мере один из остатков Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1b, имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b),
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n, p и r, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, и
где остатки R1, R1a, R2, R2a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C.
4. Соединение по п. 3, характеризующееся тем, что соединение формулы (3) имеет формулу (3a)
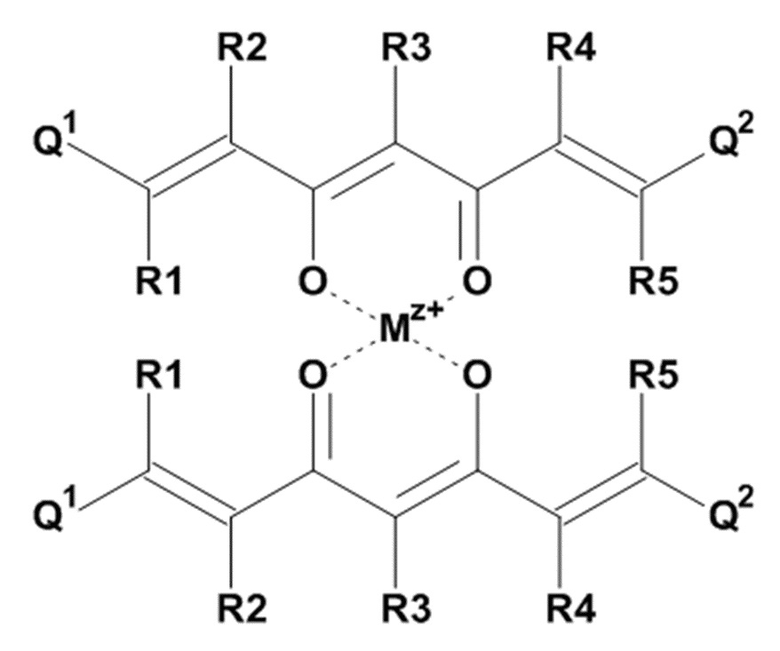 , (3a)
, (3a)
где Mz+ представляет катион металла, где z представляет собой формальную степень окисления указанного металла M и представляет целое число от 1 до 7, предпочтительно от 2 до 5, и
где Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и где
(a) по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1a, имеющий общую формулу (5a), (6a), (7a), (8a) или (9a):
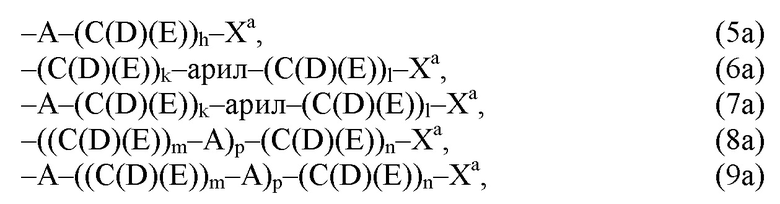
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота, и
где Xa, соответственно, независимо от других, представляет остаток формулы (20c), (20d), (21) или (24):
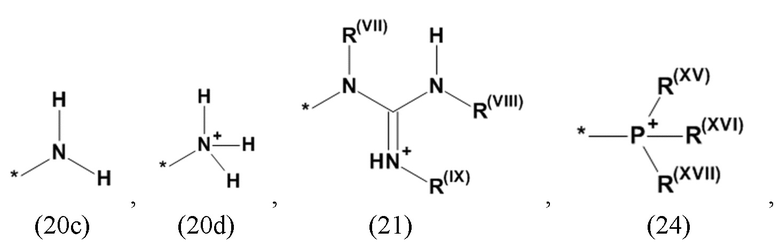
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, циклоалкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C,
или где
(b) остаток R3, соответственно, независимо от других, представляет собой органический остаток W2a, где указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
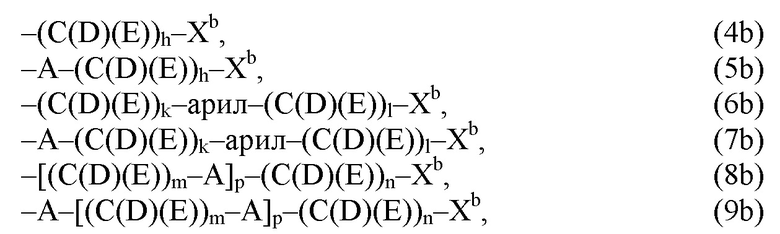
и
где, необязательно, по меньшей мере один из остатков Q1, и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1b, имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b),
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n, p и r, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C.
5. Соединение по любому из пп. 2, 3 или 4,
где M выбран из группы, которая состоит из B, Al, Zn, Cu, Mg, Ca, Fe, Si, Ga, Sn, Rh, Co, Ti, Zr, V, Cr, Mo, Mn, Ru, Pd, Ir, Ni и их комбинаций.
6. Соединение по любому из пп. 1 - 5,
где остатки Q1, Q1a, Q3 и Q3a, соответственно, независимо от других, представляют собой ароматический остаток с общей формулой (11a), (12a), (13a), (14a), (15a), (16a), (17a), (18a) или (19a):
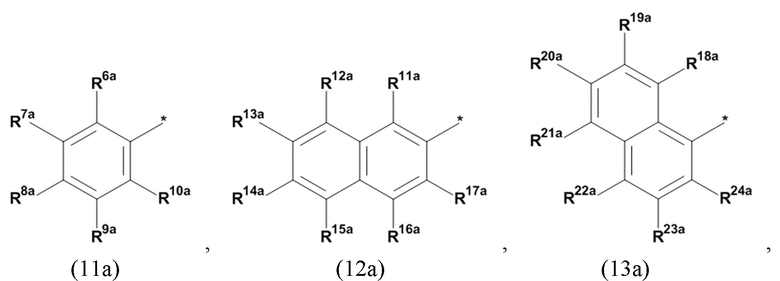
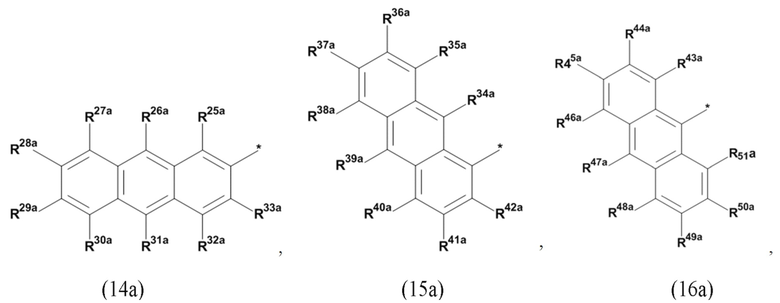
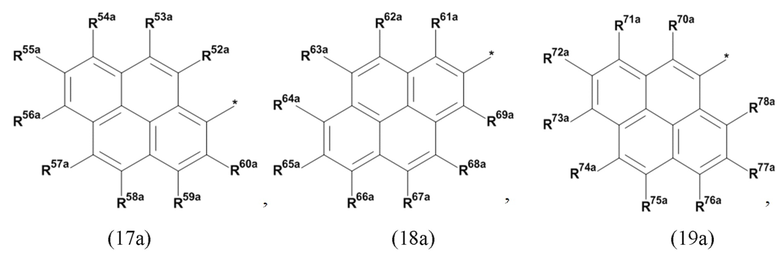
и
где остатки Q2, Q2a, Q4 и Q4a, соответственно, независимо от других, представляют ароматический остаток с общей формулой (11b), (12b), (13b), (14b), (15b), (16b), (17b), (18b) или (19b):
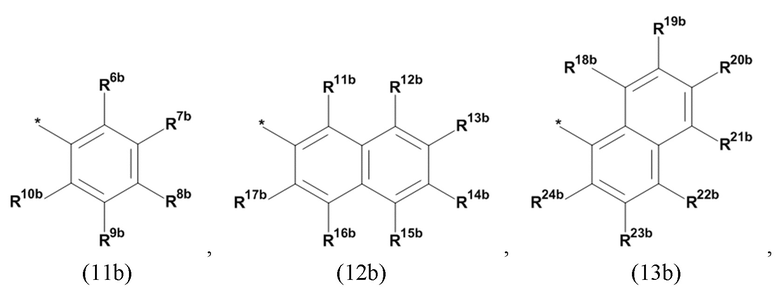
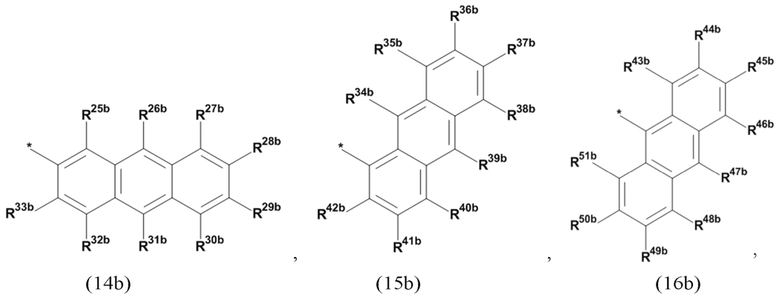
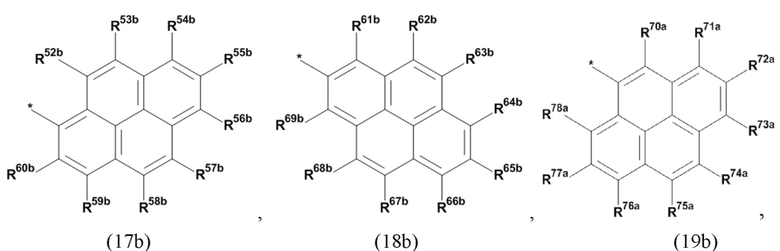
и
где, соответственно, по меньшей мере 1 остаток R6a - R10a, R11a - R17a, R18a - R24a, R25a - R33a, R34a - R42a, R43a - R51a, R52a - R60a, R61a - R69a, R70a - R78a, R6b - R10b, R11b - R17b, R18b - R24b, R25b - R33b, R34b - R42b, R43b - R51b, R52b - R60b, R61b - R69b или R70b - R78b, соответственно, независимо от других, представляет собой органический остаток W1a, или органический остаток W1b, или органический остаток W1c, и
где остатки R6a - R10a, R11a - R17a, R18a - R24a, R25a - R33a, R34a - R42a, R43a - R51a, R52a - R60a, R61a - R69a, R70a - R78a, R6b - R10b, R11b - R17b, R18b - R24b, R25b - R33b, R34b - R42b, R43b - R51b, R52b - R60b, R61b - R69b или R70b - R78b, которые не являются органическим остатком W1a, или органическим остатком W1b, или органическим остатком W1c, соответственно, независимо от других, являются идентичными или разными и представляют водород, галоген, гидроксил, тиол, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов C, кетон, содержащий от 2 до 8 атомов C, O–алкил, содержащий от 1 до 12 атомов C, S–алкил, содержащий от 1 до 12 атомов C, O–алкенил, содержащий от 2 до 12 атомов C, S–алкенил, содержащий от 2 до 12 атомов C, O–арил, содержащий от 5 до 20 атомов C, S–арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, тиоэфир, содержащий от 2 до 12 атомов C, эфир карбоновой кислоты, содержащий от 1 до 12 атомов C, амид карбоновой кислоты, содержащий от 1 до 12 атомов C, сложный тиоэфир, содержащий от 1 до 12 атомов C, алкил, содержащий от 1 до 12 атомов C, алкенил, содержащий от 2 до 12 атомов C, циклоалкил, содержащий от 3 до 12 атомов C, циклоалкенил, содержащий от 3 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов C.
7. Соединение по п. 6,
где остатки Q1, Q1a, Q3 и Q3a, соответственно, независимо от других, представляют собой ароматический остаток с общей формулой (11a), (12a) или (13a) и где остатки Q2, Q2a, Q4 и Q4a, соответственно, независимо от других, представляют собой ароматический остаток с общей формулой (11b), (12b) или (13b), и
где, соответственно, по меньшей мере 1 остаток R6a - R10a, R11a - R17a, R18a - R24a, R6b - R10b, R11b - R17b или R18b - R24b, соответственно, независимо от других, представляет собой органический остаток W1a, или органический остаток W1b, или органический остаток W1c,
где остатки R10a, R11a - R17a, R18a - R24a, R6b - R10b, R11b - R17b и R18b - R24b, которые не являются органическим остатком W1a, или органическим остатком W1b, или органическим остатком W1c, соответственно, независимо от других, являются идентичными или разными и представляют водород, галоген, гидроксил, тиол, нитро, карбоксилат, альдегид, содержащий от 1 до 8 атомов C, кетон, содержащий от 2 до 8 атомов C, O–алкил, содержащий от 1 до 12 атомов C, S–алкил, содержащий от 1 до 12 атомов C, O–алкенил, содержащий от 2 до 12 атомов C, S–алкенил, содержащий от 2 до 12 атомов C, O–арил, содержащий от 5 до 20 атомов C, S–арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, тиоэфир, содержащий от 2 до 12 атомов C, эфир карбоновой кислоты, содержащий от 1 до 12 атомов C, амид карбоновой кислоты, содержащий от 1 до 12 атомов C, сложный тиоэфир, содержащий от 1 до 12 атомов C, алкил, содержащий от 1 до 12 атомов C, алкенил, содержащий от 2 до 12 атомов C, циклоалкил, содержащий от 3 до 12 атомов C, циклоалкенил, содержащий от 3 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, или гетероарил, который не содержит атом азота, содержащий от 4 до 20 атомов C.
8. Соединение по любому из пп. 1 - 7,
где органический остаток Xb и/или Xc, соответственно, независимо от других, представляет остаток формулы (20a), (20b), (21), (22a), (22b), (23a), (24b) или (24):
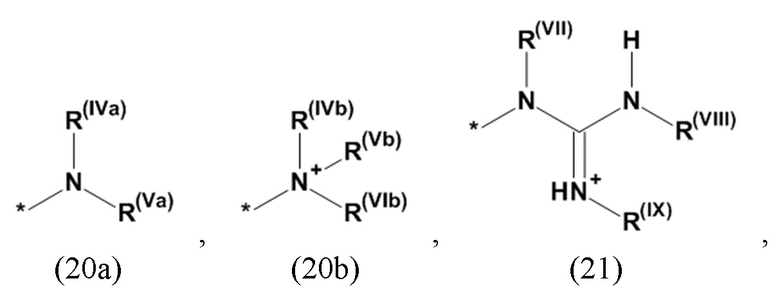
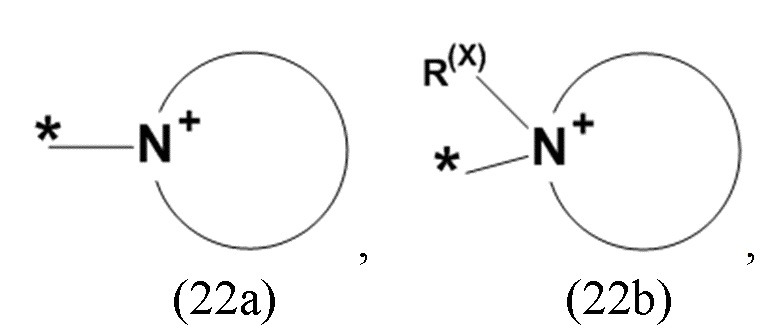
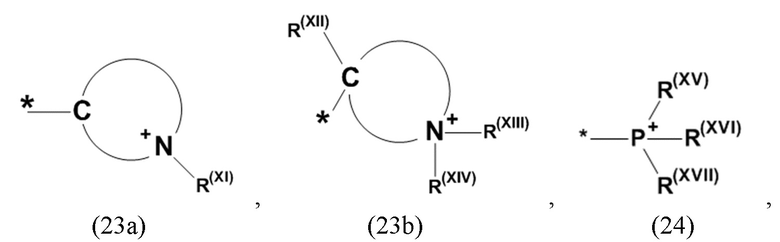
где каждый из остатков R(IVa), R(Va), R(IVb), R(Vb), R(VIb), R(VII), R(VIII), R(X), R(XI), R(XII), R(XIII), R(XIV), R(XV), R(XVI),и R(XVII), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и
где остаток формулы (22a) и остаток формулы (23a): 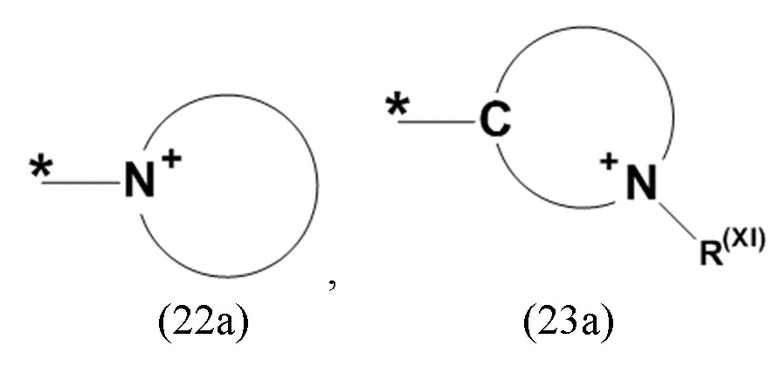
представляют замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует двойную связь, и
где остаток формулы (22b) и остаток формулы (23b):
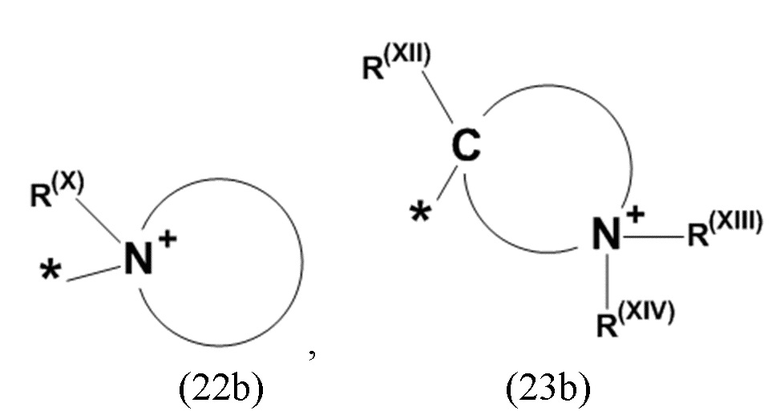
представляют замещенный или незамещенный гетероциклический остаток, содержащий от 5 до 7 атомов кольца, которые включают по меньшей мере 1 атом углерода и по меньшей мере 1 атом азота, а также, необязательно, 1 или 2 атома кислорода, где 1 атом азота образует одинарную связь.
9. Соединение по любому из пп. 1 - 8,
где органический остаток W2a, и/или W1b, и/или W1c, соответственно, независимо от других, представляют органический остаток с общей формулой (31a), (31b), (32), (34), (35), (37a) или (37b):
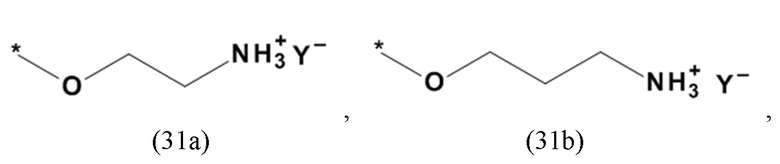
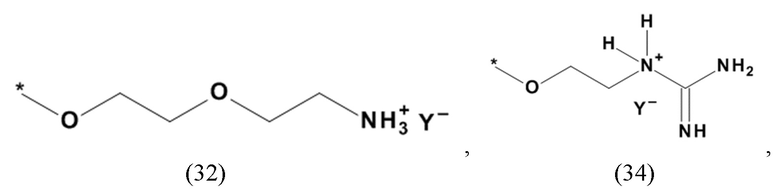
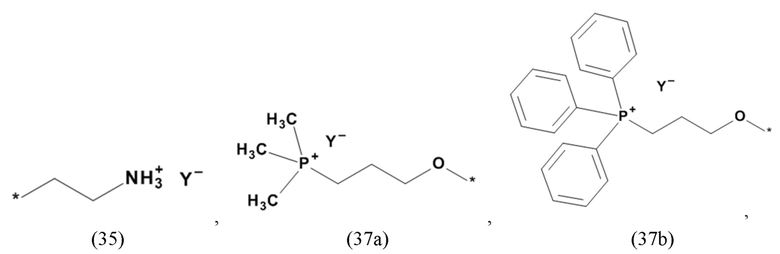
где Y- представляет собой анион, который, соответственно, независимо от других, представляет фторид, хлорид, бромид, йодид, сульфат, гидросульфат, фосфат, гидрофосфат, дигидрофосфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода.
10. Соединение по любому из пп. 1 - 9,
где органический остаток W1a, соответственно, независимо от других, представляет органический остаток с общей формулой (31a), (31b), (32) или (34):
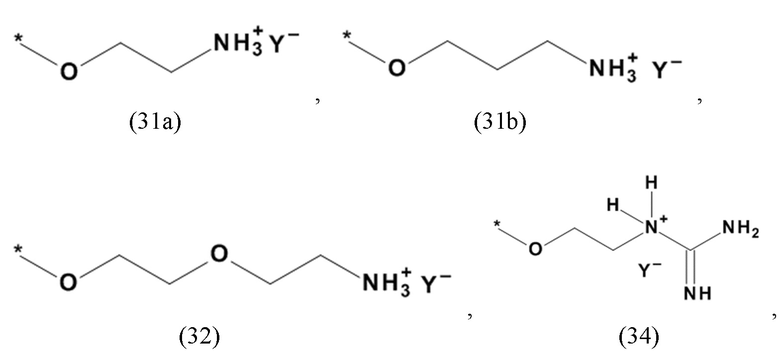
и
где Y- представляет собой анион, который, соответственно, независимо от других, представляет фторид, хлорид, бромид, йодид, сульфат, гидросульфат, фосфат, гидрофосфат, дигидрофосфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода.
11. Соединение по любому из пп. 1 - 10,
где указанное соединение представляет собой по меньшей мере одно соединение формулы (40) - (63), (68), (69a), (69b) или (70):
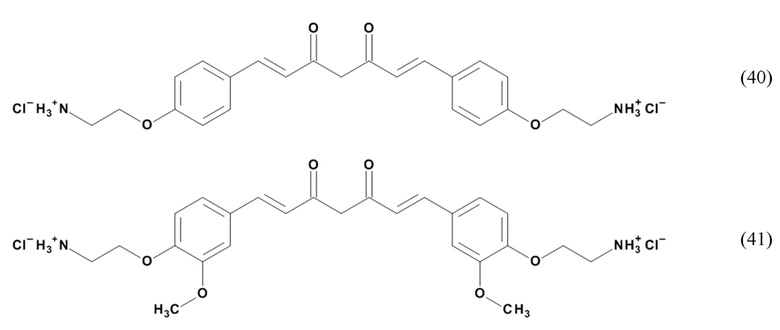
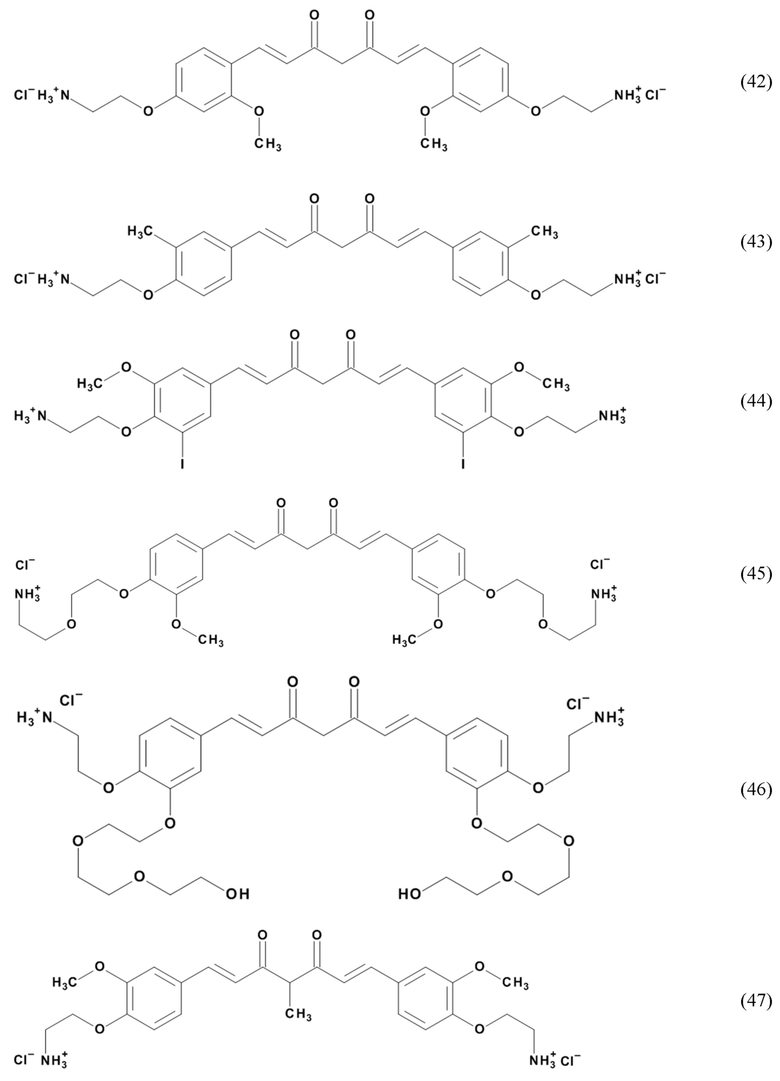
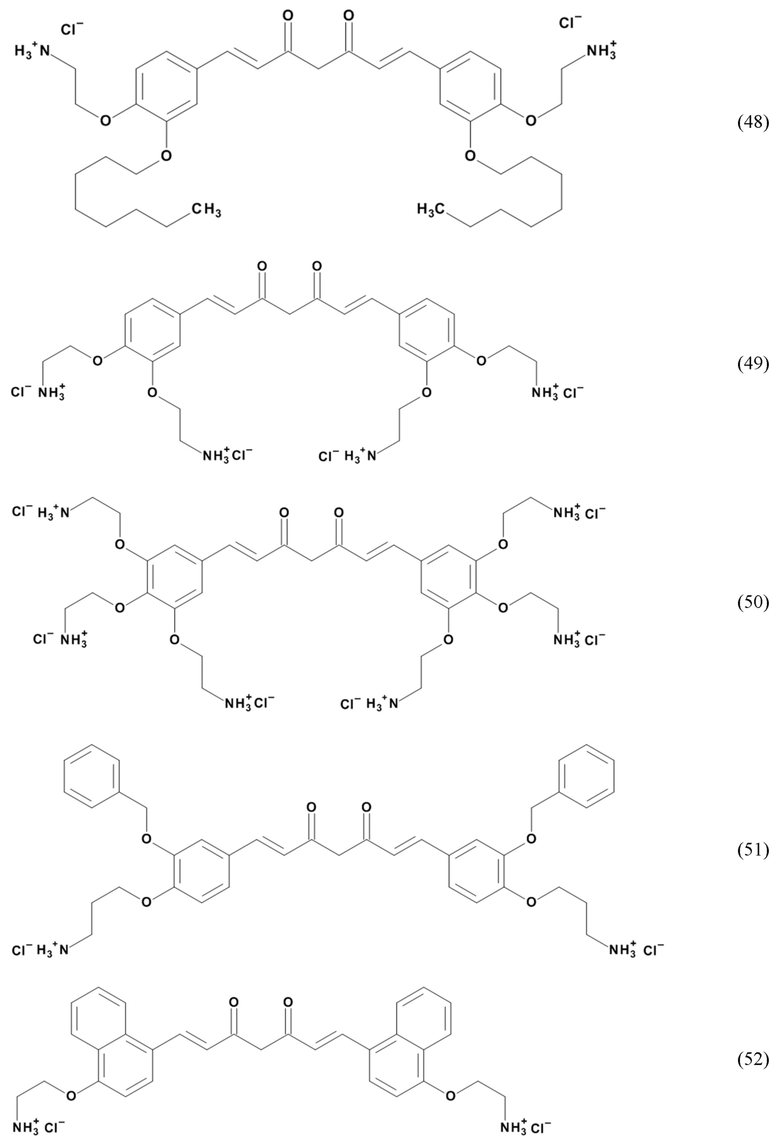
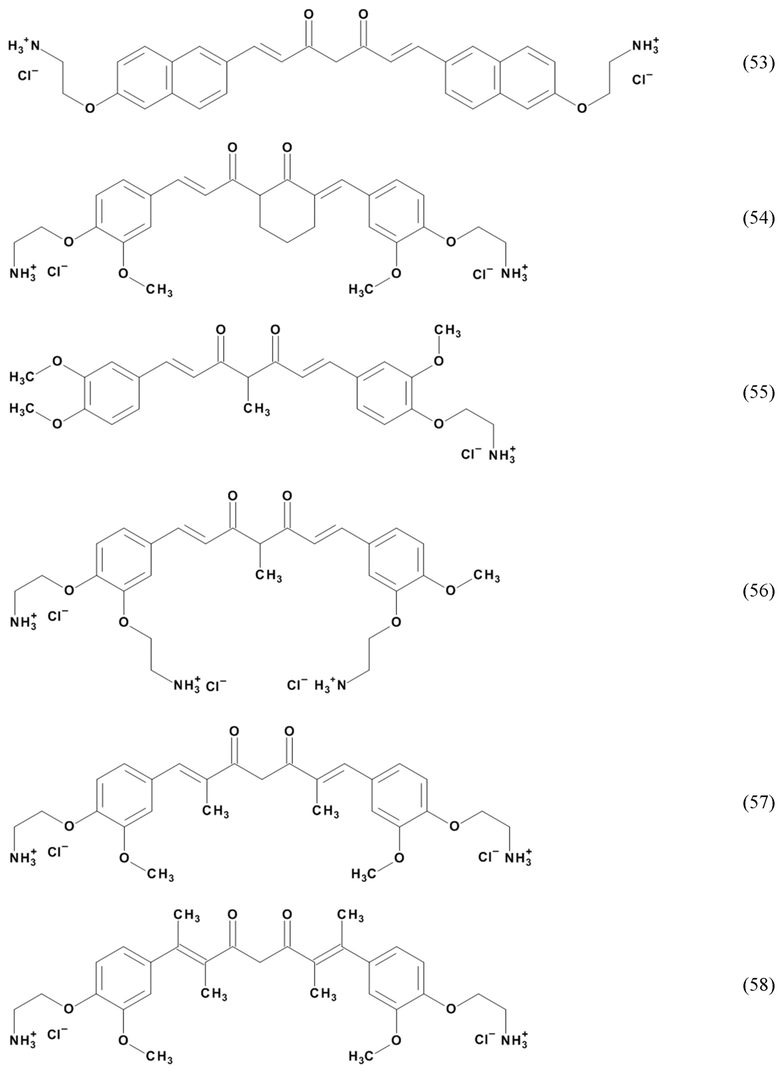
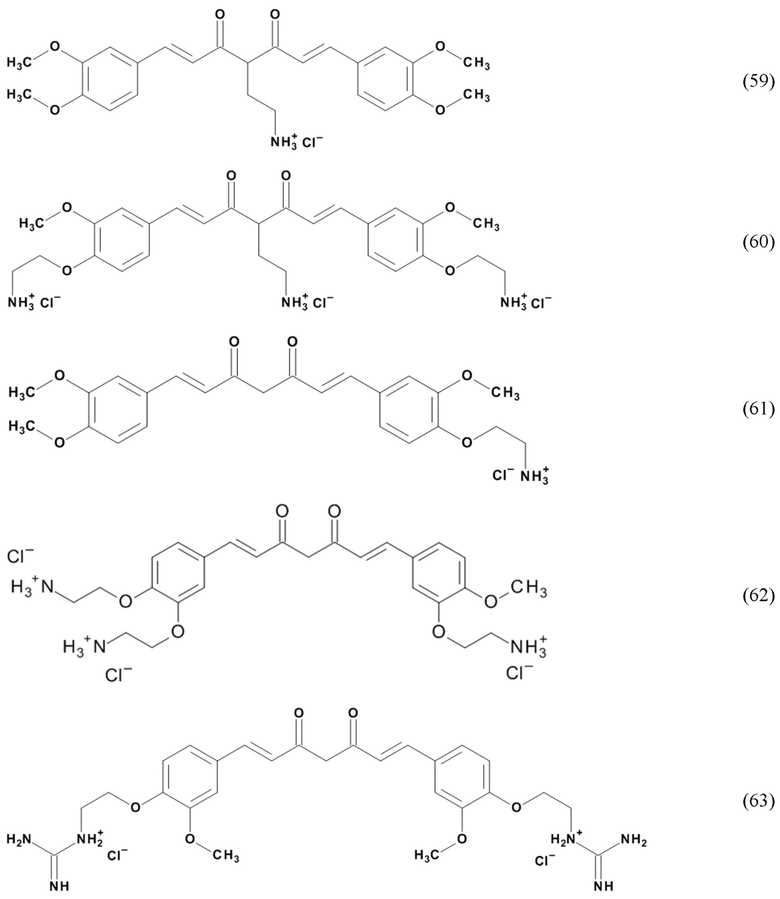
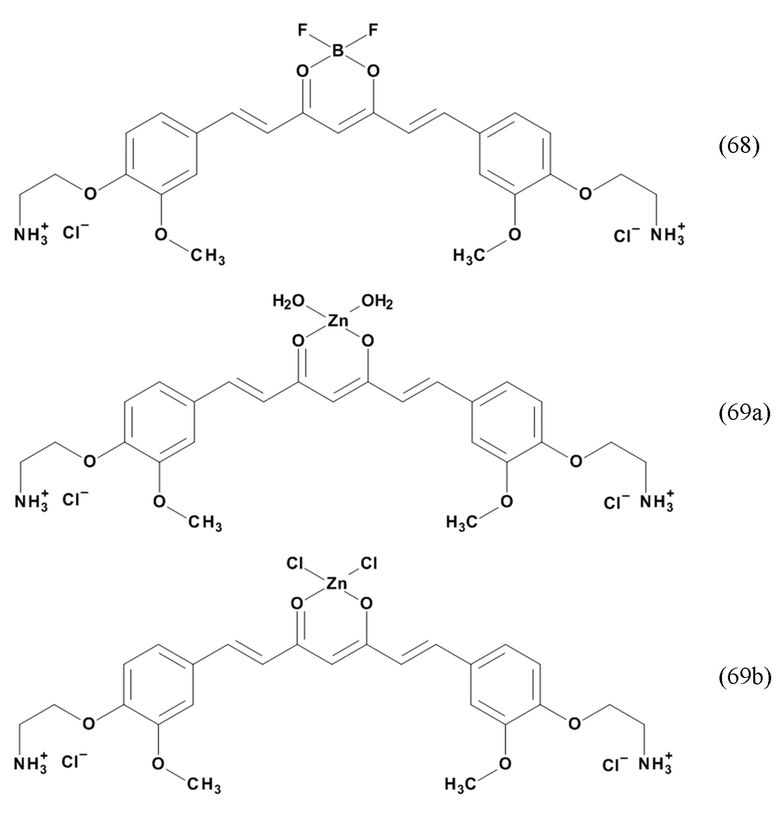
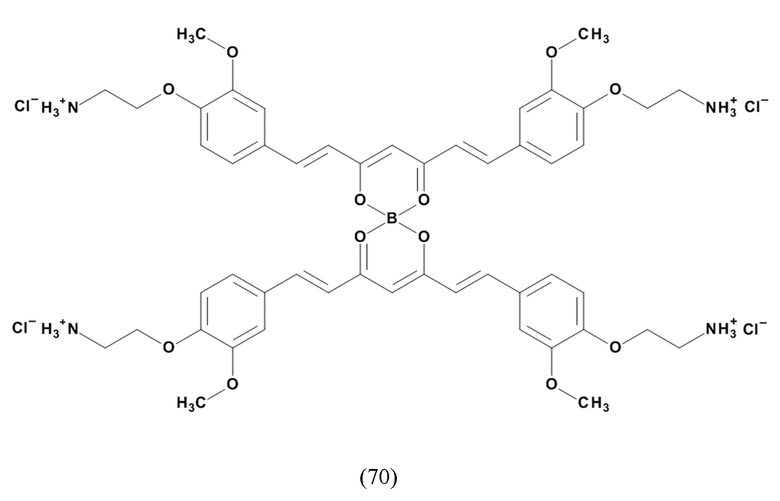 .
.
12. Применение соединения 1,7-диарил-1,6-гептадиен-3,5-диона формулы (1) и/или (3) или, соответственно, его фармакологически приемлемой соли и/или сложного эфира в качестве фотосенсибилизатора в медицинском лечении для инактивации микроорганизмов, причем указанное соединение представляет собой по меньшей мере одно соединение по любому из пп. 1-11,
где формула (1) представляет собой
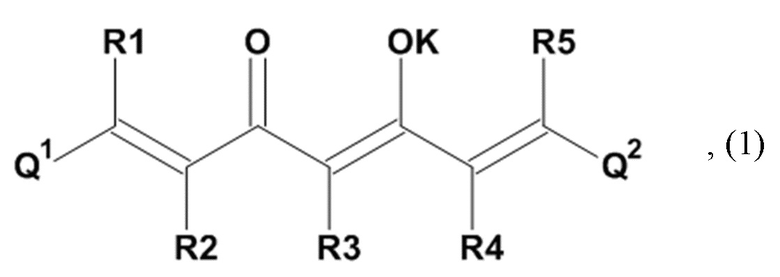
где остатки Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток,
где соединение формулы (1) не содержит группу OH, которая напрямую связана с органическим остатком Q1 или Q2, и
где K представляет водород или катион, и где
(a) по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1a, где
указанный по меньшей мере один органический остаток W1a имеет общую формулу (5a), (6a), (7a), (8a) или (9a):
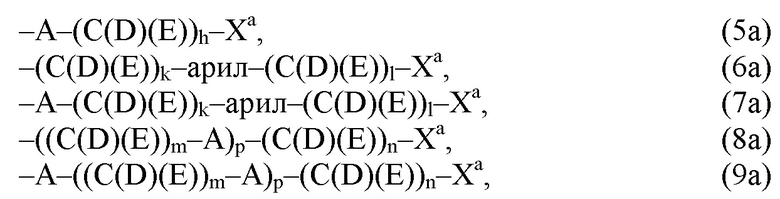
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xa, соответственно, независимо от других, представляет остаток формулы (20c), (20d) или (21):
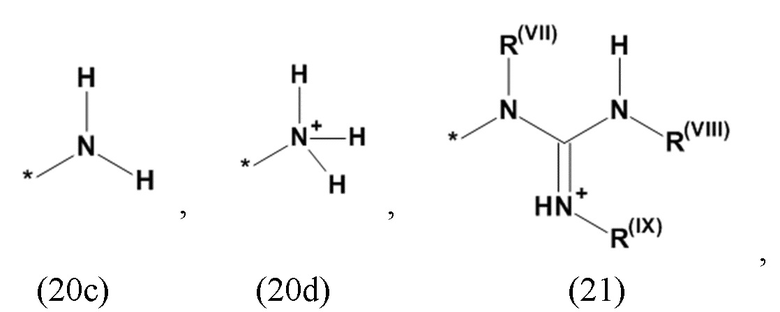
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляют водород, арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и
где остатки R1, R2, R3, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, циклоалкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C,
или где
(b) остаток R3 представляет собой органический остаток W2a, который содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, и/или по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота и/или по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, где
указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
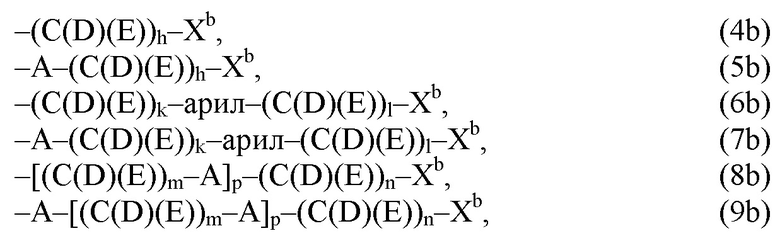
и
где, необязательно, по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1b, имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b),
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, и
где остатки R1, R2, R4 и R5, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C; и где
формула (3) представляет собой:

где Mz+ представляет катион металла, где z представляет собой формальную степень окисления указанного металла M и представляет собой целое число от 1 до 7, предпочтительно от 2 до 5, и
где Q1 и Q2, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток, и
где остатки Q1a и Q2a, соответственно, независимо от других, представляют один замещенный или незамещенный, моноциклический или полициклический ароматический остаток или один замещенный или незамещенный, моноциклический или полициклический гетероароматический остаток,
и где
(a) по меньшей мере один из остатков Q1 и Q2, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1a, имеющий общую формулу (5a), (6a), (7a), (8a) или (9a):
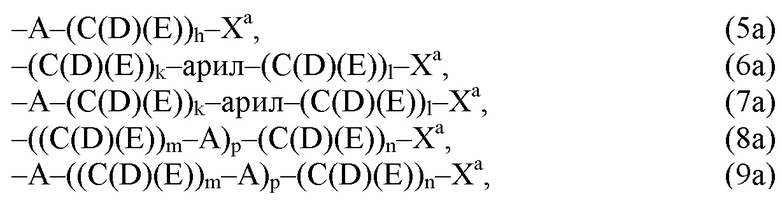
где по меньшей мере один из остатков Q1a и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1c, имеющий общую формулу (5c), (6c), (7c), (8c) или (9c):
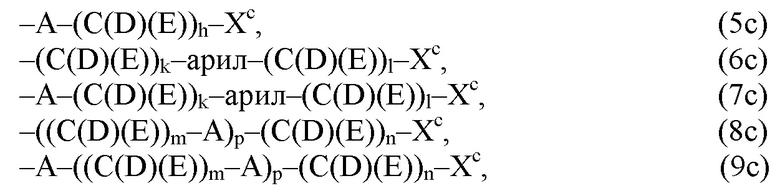
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n и p, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота, и
где Xa, соответственно, независимо от других, представляет остаток формулы (20c), (20d), (21) или (24):
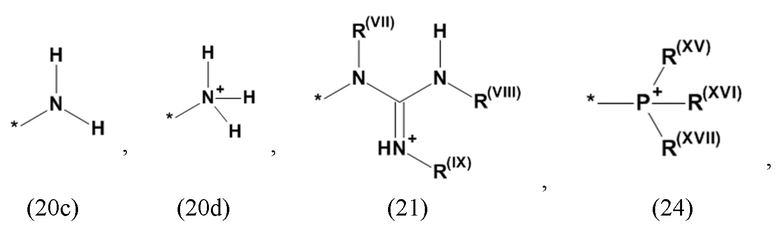
где каждый из остатков R(VII), R(VIII) и R(IX), соответственно, независимо от других, представляет водород, арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и где каждый из остатков R(XV), R(XVI) и R(XVII), соответственно, независимо от других, представляют арильный остаток, содержащий от 5 до 12 атомов C, алкиларильный остаток, содержащий от 5 до 12 атомов C, алкильный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, или эфирный остаток, который может быть линейным или разветвленным, содержащий от 1 до 8 атомов C, и
где Xc, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, или (ii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, и
где остатки R1, R1a, R2, R2a, R3, R3a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, циклоалкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C,
или где
(b) остаток R3 или R3a, соответственно, независимо от других, представляет собой органический остаток W2a, где
указанный один органический остаток W2a имеет общую формулу (4b), (5b), (6b), (7b), (8b) или (9b):
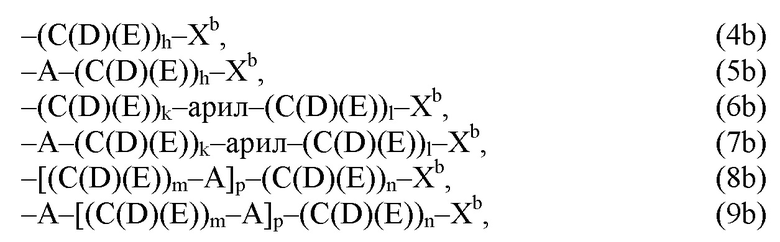
и
где, необязательно, по меньшей мере один из остатков Q1, Q1a, Q2 и Q2a, соответственно, независимо от других, содержит в качестве заместителей по меньшей мере один органический остаток W1b, имеющий общую формулу (4b), (5b), (6b), (7b), (8b) или (9b),
где h представляет целое число от 1 до 20, где k представляет целое число от 0 до 10, где l представляет целое число от 0 до 10 и где m, n, p и r, соответственно, независимо от других, представляют целое число от 1 до 6, и
где A, соответственно, независимо от других, представляет кислород или серу,
где D и E, соответственно, независимо от других, представляют водород, галоген, G–R(I) или G–C(=G)–R(II), где G, соответственно, независимо от других, представляет кислород или серу и где остатки R(I) и R(II), соответственно, независимо от других, представляют водород, метил, этил, н-пропил, н-бутил, н-пентил, фенил или бензил, причем фенил и бензил могут быть незамещенными или замещенными,
где арил представляет замещенную или незамещенную ароматическую группу или замещенную или незамещенную гетероароматическую группу, которая не содержит атом азота,
где Xb, соответственно, независимо от других, представляет собой органический остаток, который (i) содержит по меньшей мере один нейтральный атом азота, который может быть протонирован, (ii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом азота или (iii) содержит по меньшей мере один положительно заряженный, предпочтительно четвертичный, атом фосфора, и
где остатки R1, R1a, R2, R2a, R4, R4a, R5 и R5a, соответственно, независимо от других, представляют водород, галоген, алкил, содержащий от 1 до 12 атомов C, алкиларил, содержащий от 1 до 12 атомов C, арил, содержащий от 5 до 20 атомов C, эфир, содержащий от 2 до 12 атомов C, или гликоль, содержащий от 2 до 12 атомов C.
13. Способ инактивации микроорганизмов, включающий следующие этапы:
(A) приведение микроорганизмов в контакт с по меньшей мере одним фотосенсибилизатором, причем указанный фотосенсибилизатор представляет собой по меньшей мере одно соединение по любому из пп. 1-11, и
(B) облучение указанных микроорганизмов и по меньшей мере одного фотосенсибилизатора электромагнитным излучением.
14. Способ по п. 13, где K в соединении представляет собой катион Mz+ металла M, где z представляет собой формальную степень окисления указанного металла M, и где z представляет целое число от 1 до 7, предпочтительно от 2 до 3, и где указанное соединение имеет формулу (102):
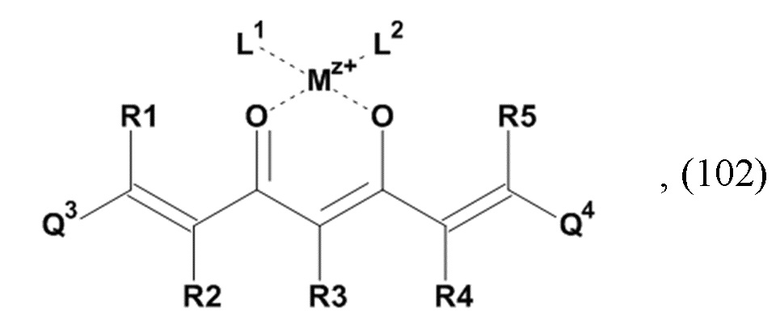
где L1 и L2, соответственно, независимо от других, представляют воду, фторид, хлорид, бромид, йодид, фосфат, гидрофосфат, дигидрофосфат, сульфат, гидросульфат, тозилат, мезилат или по меньшей мере одно карбоксилирование карбоновой кислотой, содержащей от 1 до 15 атомов углерода и/или их смеси.
15. Способ по п. 13 или 14, где облучение указанных микроорганизмов и по меньшей мере одного фотосенсибилизатора электромагнитным излучением осуществляют в присутствии по меньшей одного соединения, являющегося донором кислорода, предпочтительно пероксида и/или по меньшей мере одного кислородсодержащего газа, предпочтительно кислорода.
16. Способ по п. 13 или 15, где длина волны электромагнитного излучения находится в диапазоне от 280 до 1000 нм, более предпочтительно от 380 до 1000 нм.
17. Способ по п. 13 или 15, где плотность энергии электромагнитного излучения лежит в диапазоне от 1 мкВт/см2 до 1 кВт/см2, более предпочтительно от 1 мВт/см2 до 100 Вт/см2, более предпочтительно от 2 мВт/см2 до 50 Вт/см2, более предпочтительно от 6 мВт/см2 до 30 Вт/см2, более предпочтительно от 7 мВт/см2 до 25 Вт/см2.
18. Способ по любому из пп. 13 - 17, где указанный по меньшей мере фотосенсибилизатор представляет собой по меньшей мере одно соединение по любому из пп. 4-11 и/или его фармацевтически приемлемую соль и/или эфир.
19. Немедицинское применение соединения по любому из пп. 1 - 11 и/или его фармацевтически приемлемой соли и/или эфира в качестве фотосенсибилизатора для инактивации микроорганизмов, которые предпочтительно выбраны из группы, состоящей из вирусов, археев, бактерий, спор бактерий, грибов, спор грибов, простейших, водорослей и передающихся с кровью паразитов.
20. Применение по п. 19 для очистки поверхности и/или покрытия изделия.
21. Применение по п. 19 или 20 для очистки поверхности и/или покрытия медицинских продуктов, пищевой упаковки, текстиля; строительных материалов, электронных устройств, мебели или гигиенических изделий.
22. Применение по п. 19 или 20 для дезинфекции жидкостей.
23. Применение по п. 19 или 20 для дезинфекции пищевых продуктов.
24. Изделие с покрытием, характеризующееся тем, что на поверхность изделия нанесено по меньшей мере одно соединение по любому из пп. 1-11.
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ИНАКТИВАЦИИ БАКТЕРИЙ Enterococcus faecalis (ВАРИАНТЫ) | 2013 |
|
RU2550132C1 |
| CN 101570496 B, 15.08.2012 | |||
| BALTAZAR L | |||
| M | |||
| et al.: "Antimicrobial photodynamic therapy: an effective alternative approach to control fungal infections" | |||
| FRONTIRES IN MICROBIOLOGY, Bd | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2022-10-11—Публикация
2016-08-26—Подача