Изобретение относится к химической промышленности, а именно к получению соединения, которое может быть использовано в медицине в качестве активной основы лекарственного препарата, препятствующего слиянию мембран вируса SARS-CoV-2 и клетки хозяина, т.е. обладающего ингибирующей способностью по отношению к спайковому белку SARS-CoV-2.
За последние десятилетия возникновение эпидемий и пандемий, вызванных вирусами атипичной пневмонии (SARS-CoV, 2002-2003), свиного гриппа (H1N1, 2009-2010), птичьего гриппа (H7N9, 2013), ближневосточным вирусом (MERS-CoV 2013-2015), вирусом Эбола (2014-2015) коронавирусом SARS-CoV-2 (2019 - н.вр) обострило проблему поиска антивирусных препаратов. Перспективными соединениями, способными препятствовать распространению вирусной инфекции считаются порфириновые соединения, так как они способны связываться с различными белками вирусов и проявлять ингибирование различных стадий жизненного цикла вируса, особенно на стадиях прикрепления вириона к клетке хозяина и слияния их мембран. SARS-CoV содержит структурный S-белок, состоящий из двух субьединиц S1 и S2. S1-субьединица выполняет функцию стыковки с ангиотензинпревращающим ферментом клетки хозяина, S2-субьединица отвечает за слияние мембран. В связи с этим S-белок коронавирусов считается перспективной мишенью, так как стыковка вириона с клеточной мембраной и слияние мембран является ключевым этапом инфицирования.
Известно также в качестве противовирусного средство [Pat. 20190351049 A1 United States, Int. Cl. A61K 39/215, GOIN 33/569, C07K 14/165, А61K 45/06, А61K 39/12, С07K 16/10. Human Antibodies to Middle East Respiratory Syndrome - Coronavirus Spike Protein [Text] / Kyratsous C. (Irvington, NY, US), Stahl N. (Carmel, NY, US), Sivapalasingam S. (Brooklyn, NY, US); Assignee Regeneron Pharmaceuticals, Inc. (Tarrytown, NY, US). Appl. №16/530,140; Filed Aug. 2, 2019; Pub. Date Nov. 21, 2019. - 149 p.: pic], в котором в качестве терапевтического средства для предотвращения или лечения инфекции предложены антитела имуноглобулинов IgG1 или IgG4. Эффект терапевтического средства основан на специфическом связывании со спайковым белком коронавируса и ингибирования или нейтрализации его активности. Антитела представляют собой полностью человеческие моноклональные антитела либо их модифицированные антигенсвязывающие фрагменты.
Известно также средство [Pat. WO 2021180604 A1, Int. Cl. A61P 31/14, C07K 16/10. Sars-cov-2 (sars2, covid-19) antibodies [Text] / Grosveld F.G. (Rotterdam, NL), Drabek D. (Rotterdam, NL), Haperen R. van (Rotterdam, NL), Bosch B.J. (Utrecht, NL), Fedry J. (Utrecht, NL), Hurdiss D. L. (Utrecht, NL), Kuiken T. (Rotterdam, NL), Haagmans B. L. (Rotterdam, NL), Rockx В. H. G. (Rotterdam, NL). Assignee Harbour Antibodies Bv (Rotterdam, NL), Universiteit Utrecht Holding B.V. (Utrecht, NL). Appl. №PCT/EP2021/055693; Filed 03.04.2021; Pub. Date 16.09.2021. - 346 p.: pic], в котором предложено использование полностью человеческого моноклонального антитела IgG1 или его антигенсвязывающих фрагментов для распознавания спайкового белка SARS-Cov-2 (SARS2-S). В некоторых вариантах реализации антитела связываются с SARS2-S с высокой аффинностью и/или ингибируют инфекцию SARS-Cov-2. В некоторых вариантах реализации антитела обеспечивают предотвращение, лечение или облегчение течения заболевания COVID-19.
Известно также средство [Патент 2744274 С1 Российская Федерация, МПК C12N 1/00, С07K 14/165, С07K 16/10, C12N 15/13. Моноклональное антитело к RBD фрагменту в составе S белка вируса SARS-CoV-2 [Текст] / Шахпаронов М.И. (RU), Павлюков М. С.(RU), Антипова Н.В. (RU); заявитель Федеральное государственное бюджетное учреждение науки Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова Российской академии наук (ИБХ РАН), патентообладатель Федеральное государственное бюджетное учреждение науки Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова Российской академии наук (ИБХ РАН); заявл. 20.11.2020; опубл. 04.03.2021 г., Бюл. №7], связанное с получением мышиных моноклональных антител к RBD фрагменту в составе S белка вируса SARS-CoV-2. Специфичность моноклонального антитела к RBD фрагменту в составе S белка вируса SARS-CoV-2 подтверждена методами иммуноферментного анализа, иммуноблоттинга, иммуноцитохимического и иммуногистохимического окрашивания.
Существенным недостатком перечисленных изобретений является узкая направленность на S1-субьединицу SARS-CoV-2. Известно, что из всех генов коронавируса, ген, кодирующий S1-субьединицу S-белка, наиболее изменчив, поэтому эффективность антител, предложенных для определенных штаммов коронавируса SARS-CoV-2, не очевидна в отношении других штаммов SARS-CoV-2. Другим существенным недостатком используемого подхода к ингибированию функций S-белка коронавируса за счет связывания с антителами заключается в том, что природные поликлональные или моноклональные антитела имеют белковую природу и могут вызывать тяжелые аллергические реакции.
Известна фармацевтическая композиция, направленная на ингибирование консервативной части S-белка - S2-субьединицы [Pat. ЕР 1618127 B1, Int. Cl. С07K 14/165. Immunogenic composition comprising a spike protein of the SARS coronavirus [Text] / Rappuoli R. (Emeryville, US), Masignani V. (Emeryville, US), Stadler K. (Emeryville, US), Gregersen J.-P. (Emeryville, US), Chien D. (Emeryville, US), Han J. (Emeryville, US), Polo J. (Emeryville, US), Weiner A. (Emeryville, US), Houghton M. (Emeryville, US), Song H.C. (Emeryville, US), Seo M.Y. (Emeryville, US), Donnelly J.J. (Emeryville, US), Klenk H.D. (Emeryville, US), Valiante N. (Emeryville, US); Assignee Novartis Vaccines and Diagnostics, Inc. (Emeryville, US). Appl. №04750188.7; Filed 09.04.2004; Pub. Date 10.12.2014; Bulletin 2014/50. - 212 p.: pic.]. Композиция может использоваться в лечении или профилактике инфекции, вызванной вирусом тяжелого острого респираторного синдрома (ТОРС). В состав иммуногенной композиции входит полипептид, содержащий SEQ ID NO: 6042, или его фрагмент. SEQ ID NO: 6042, а также могут входить адьюванты, минеральные соли. Полипептидные молекулы могут быть физически получены из вируса SARS или получены рекомбинантным или синтетическим путем, например, на основе известных последовательностей. Полученные последовательности можно использовать для ингибирования проникновения вируса и слияния мембран с целевой клеткой-хозяином млекопитающего.
Известно в качестве противовирусного средство [Pat. 107022008 А China С07K 14/165, С12N 15/50, А61K 38/16, А61P 31/14. Suppress polypeptide and its application of human coronary virus's infection wide spectrum [Text] /  SHANXI JINBO BIOMEDICAL Co., Ltd. Appl. №CN 107022008 A; Filed: 2017.08.08; Pub. Date Nov. 2021.04.23. - 16 p.: pic], в котором предложены полипептиды HCoV-EK, способные к ингибированию слияния виромембраны вирусов SARS, таких как RsSHC014-CoV или RsW1V1-CoV и мембраны клетки-хозяина.
SHANXI JINBO BIOMEDICAL Co., Ltd. Appl. №CN 107022008 A; Filed: 2017.08.08; Pub. Date Nov. 2021.04.23. - 16 p.: pic], в котором предложены полипептиды HCoV-EK, способные к ингибированию слияния виромембраны вирусов SARS, таких как RsSHC014-CoV или RsW1V1-CoV и мембраны клетки-хозяина.
Известно также в качестве противовирусного средство [Zhu Y. et al. Design of potent membrane fusion inhibitors against SARS-CoV-2, an emerging coronavirus with high fusogenic activity //Journal of virology. - 2020. - Vol. 94. -№. 14. - P. e00635-20. - doi:10.1128/JVI.00635-20], которое может использоваться в способе лечения или профилактики коронавирусной инфекции, вызываемой коронавирусом SARS-CoV и SARS-CoV-2. Противовирусное средство представляет собой ингибитор слияния липопептидов на основе последовательности HR2, названный IPB02, который показал высокую активность в ингибировании опосредованного S-белком SARS-CoV-2 слияния клеток и псевдовирусной трансдукции.
Известно противовирусное средство [Pat. 8003332 В2 United States, Int. Cl. GOIN 33/53, A61K 39/12. Inhibition of membrane fusion proteins [Text] / Kielian M. (Pelham, NY, US), Liao M. (San Francisco, CA, US) Assignee: Albert Einstein College of Medicine of Yeshiva University (Bronx, NY, US). Appl. No.: 11/918,835; Filed: May 4, 2006; Pub. Date: Nov. 16, 2006.- 41p.: pic] гибридные белки, способные связываться с белками вирусов (вирус гриппа НА, ортомиксовирусы, парамиксовирусы, филовирусы, коронавирусы, вирус иммунодефицита человека-1, предотвращая рефолдинг до конечной конформации шпильки, необходимой для слияния мембран, тем самым ингибируют слияние и инфекцию.
Известно противовирусное средство [Pat. 9725487 В2 United States, Int. Cl. C07K 14/005, A61K 38/04, A61K 38/16, C07K 7/00, C07K 7/08, C12Q 1/18, C07K 7/06, G01N 33/569, C12N 7/00. Compositions and methods for measles virus inhibition [Text] / Robert F. Garry (New Orleans, LA, US); Russell B. Wilson (Mandeville, LA, US); Assignee; The Administrators of the Tulane Educational Fund (New Orleans, LA, US); Autoimmune Technologies, LLC (New Orleans, LA, US). Appl. №14/711,364; Filed: May 13, 2015; Pub. Date: Aug. 27, 2015. - 32p.: pic] пептид, имеющий аминокислотную последовательность области инициации слияния вирусов (FIR) или функционального сегмента FIR, или имеющий аминокислотную последовательность, которая аналогична последовательности FIR. Пептид связывается с белком вируса, что препятствует слиянию с клеточной мембраной млекопитающего.
Известно противовирусное средство [Pat. 7491489 В2 United States, Int. Cl. C12Q 1/00, C12Q 1/18, C12Q 1/70, G01N 33/53. Synthetic peptide targeting critical sites on the SARS-associated coronavirus spike protein responsible for viral infection and method of use thereof [Text] / Zheng B. (Hong Kong, CN); Guan Y. (Hong Kong, CN), Huang J. (Hong Kong, CN); He M.-L. (Hong Kong, CN); Assignee: The University of Hong Knog (Hong Kong, CN). Appl. № 11/262,044; Filed: Oct. 28, 2005; Pub. Date May 25, 2006. - 29 p.: pic], основанное на использовании пептидов, нацеленных на четыре области белка S, которые эффективно ингибируют инфекцию SARS CoV в клеточной линии почки обезьяны (FRhK-4). Синергические противовирусные эффекты наблюдались, когда клетки обрабатывали комбинациями двух или трех из этих пептидов до инфицирования.
Существенными недостатками перечисленных изобретений являются: сложность синтеза пептидов, жесткие требования к их хранению, не высокая биодоступность, а также тяжелые аллергические реакции на высокомолекулярное экзогенное соединение.
Низкомолекулярные соединения оценивались как вещества, препятствующие слиянию мембран. Известно [Park J. Е. et al. Proteolytic processing of Middle East respiratory syndrome coronavirus spikes expands virus tropism //Proceedings of the National Academy of Sciences. - 2016. - Vol. 113. - №. 43. - P. 12262-12267. - doi:10.1073/pnas.1608147113], что предварительная обработка S-белка трипсином перед связыванием с рецептором предотвращает инфекцию. Это происходит потому, что обработка трипсином вызывает необратимые конформационные изменения S-белка, так что он не может опосредовать слияние мембран. Недостатком предложенного вещества является условие предварительной обработки S-белка до контакта с рецептором клетки млекопитающего, так как обработка трипсином после связывания псевдовирусных частиц с их соответствующим рецепторами приводит к активации слияния плазматических мембран.
За прототип принят препарат ингибитор коронавирусов не белковой природы [Sisk, J.M. Coronavirus S protein-induced fusion is blocked prior to hemifusion by Abl kinase inhibitors / Sisk J. M., Frieman M.В., Machamer С.E. // J. Gen. Virol. - 2018. - Vol. 99. - N 5. - P. 619-630. - doi: 10.1099/jgv.0.001047] - противолейкозный цитостатический препарат иматиниб, в котором слияние мембран (как вирус-клетка, так и клетка-клетка) блокируется в присутствии имантиниба.
Основными недостатками прототипа являются множественное побочное действие, а также не доказанное ингибирующее действие в случае вируса SARS-CoV-2.
Задачей изобретения является получение водорастворимого порфирина с высоким выходом, который имел бы два периферийных протяженных, гидрофобных заместителя, связывающихся в S2 субъединицы S-белка SARS-CoV-2, тиразильные фрагменты которых обеспечат дополнительную устойчивость комплексу за счет образования нескольких водородных связей с аминокислотными остатками полипептидной цепи S2 единицы.
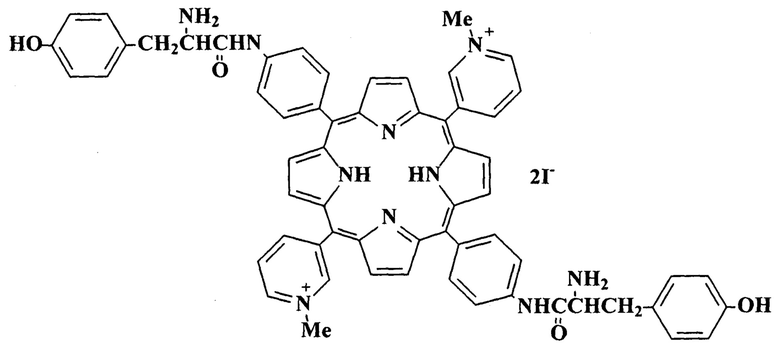
Задача решена 5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний-3'-ил)порфин дииодидом формулы:
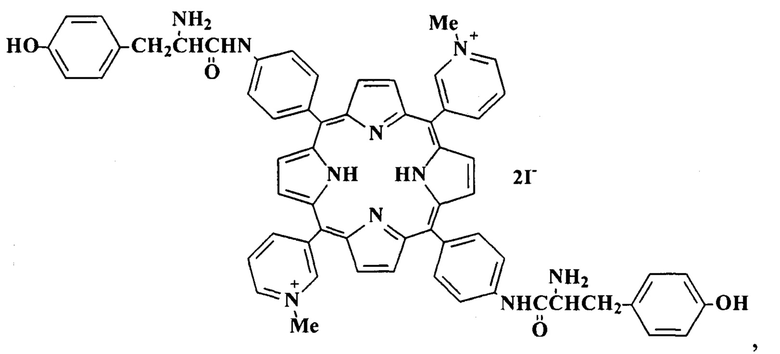
проявляющим свойство связывания с S2 субъединицей S-белка SARS-CoV-2.
Поставленная задача решена за счет того, что получено новое порфириновое соединение с остатками L-тирозина, структура которого подтверждена физико-химическими методами анализа. Выбор порфирина обусловлен следующими причинами: два катионных заместителя обеспечивают растворимость соединений в водных и физиологических средах, два других периферийных заместителя, как и макрогетероциклическое кольцо, являются гидрофобными, что обеспечивает связывание в S2-субьединице S-белка. Наличие 8-ми гетероатомов и 4-х ароматических фрагментов в дииодиде 5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний-3'-ил)порфина обеспечивает возможность образования Н-связей и пи-пи связей тиразиновых фрагментов с аминокислотными остатками S-белка. Протяженность молекулы позволяет связывать альфа-спирали HR1 или HR2 гептадного повтора. Проведенный молекулярный докинг дииодида 5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний-3'-ил)порфина с S-белком SARS-CoV-2 показал высокую аффинность связывания (-10,4 ккал/моль) в требуемой области S2-субьединицы SARS-CoV-2. Высокое сродство несимметричного дитиразинзамещенного порфирина к спайковому белку SARS-CoV-2 позволяет рассчитывать, что полученный порфирин будет активен и в отношении других вирусов или мембранных белков болезнетворных микроорганизмов, в том числе обладающих лекарственной резистентностью.
Для получения этого соединения используют следующие вещества:
- 3-пиридилкарбоксальдегид - коммерческий продукт TCI EUROPE N.V.;
- пиррол - ТУ 6-09-07-242-84;
- пропионовая кислота - ТУТ CP 1150Н-63, хч;
- пропионовый ангидрид - ТУ 6-09-08-1176-77;
- оксид алюминия - ТУ 6-09-426-75;
- хлороформ - ТУ 263-44493179-01 с изм. №1,2;
- 4-нитробензальдегид - коммерческий продукт «Merck» (Германия);
- соляная кислота конц.- ГОСТ 3885-73;;
- аммиак - ГОСТ 3760-79;
- хлорид олова дигидрат - ГОСТ 36-78;
- нитрометан - коммерческий продукт Русхим;
- трифторуксусная кислота - коммерческий продукт Acros Organics;
- калия гидроокись - ГОСТ 24363-80;
- N,N'-диметиламинопиридин - коммерческий продукт Acros Organics;
- N,N'-дициклогексилкарбимид - коммерческий продукт Acros Organics;
- L,-N,O-ди-Вос-тирозин - коммерческий продукт Acros Organics
- метанол - ГОСТ 2222-95;
- хлористый метилен - ТУ 2631-44493179-98 с изм. №1, 2, 3;
- гексан - ТУ 6-09-06-4521-77;
- метилиодид - ТУ: 6-09-3988-83.
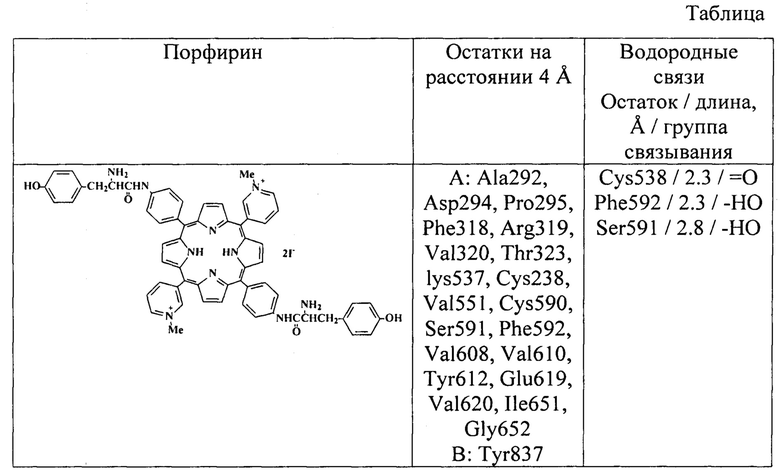
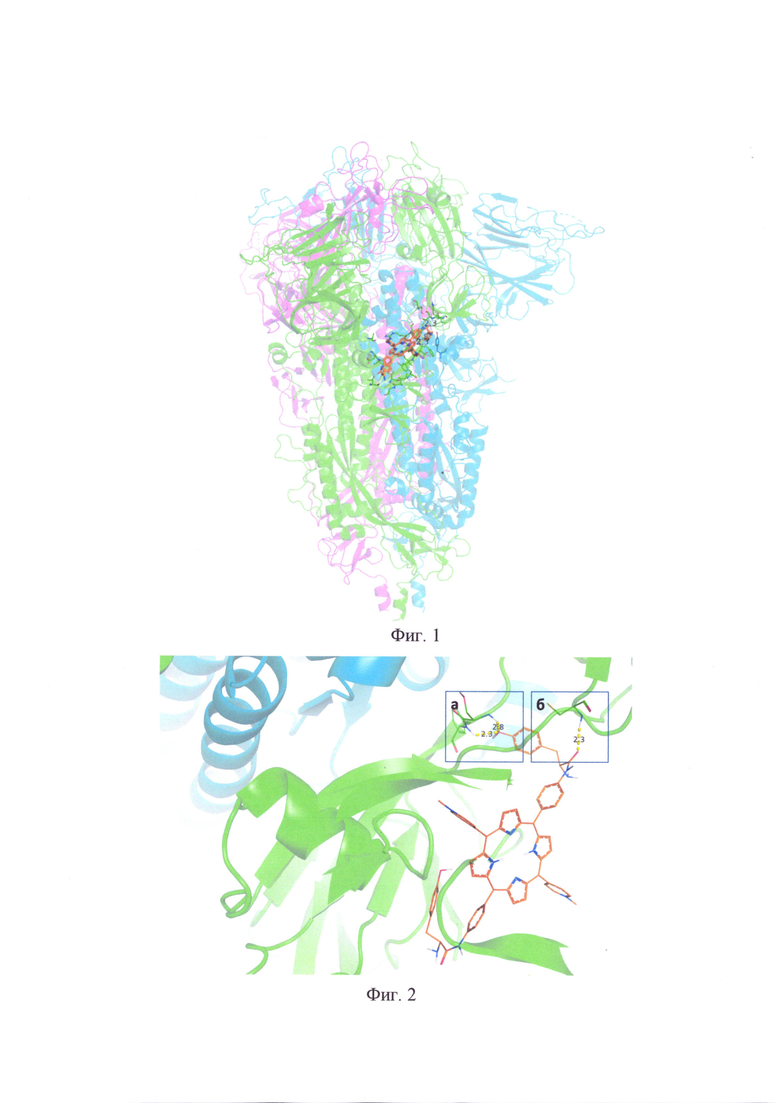
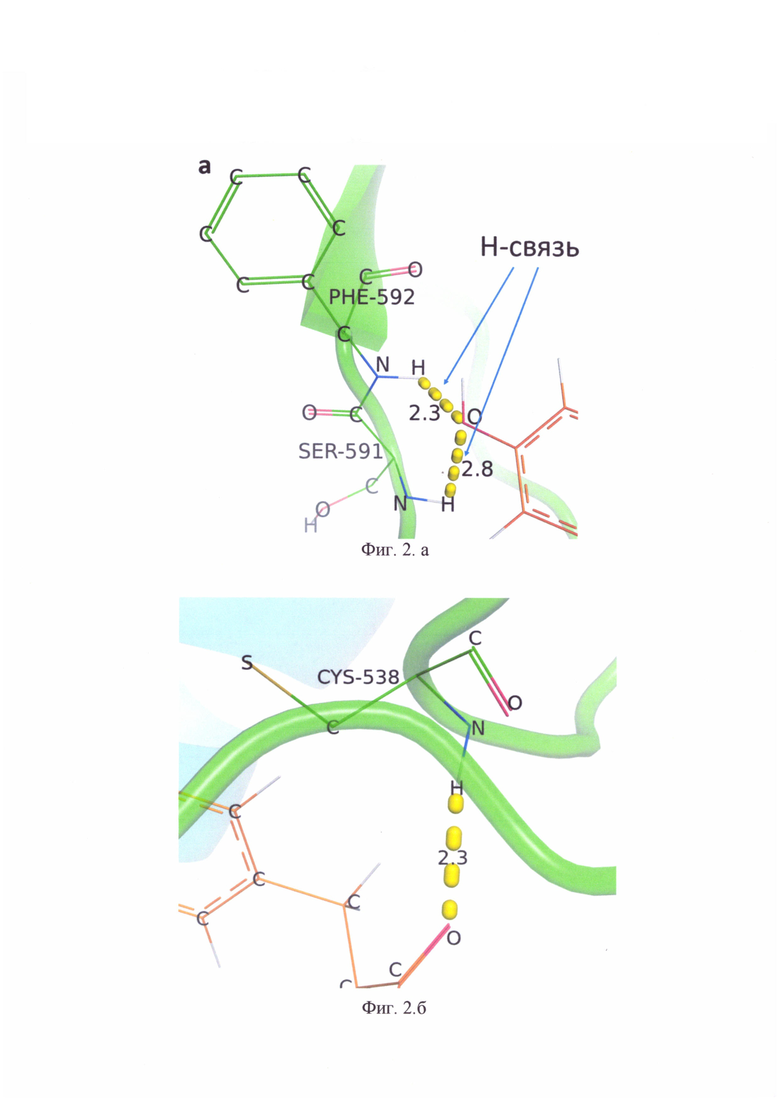
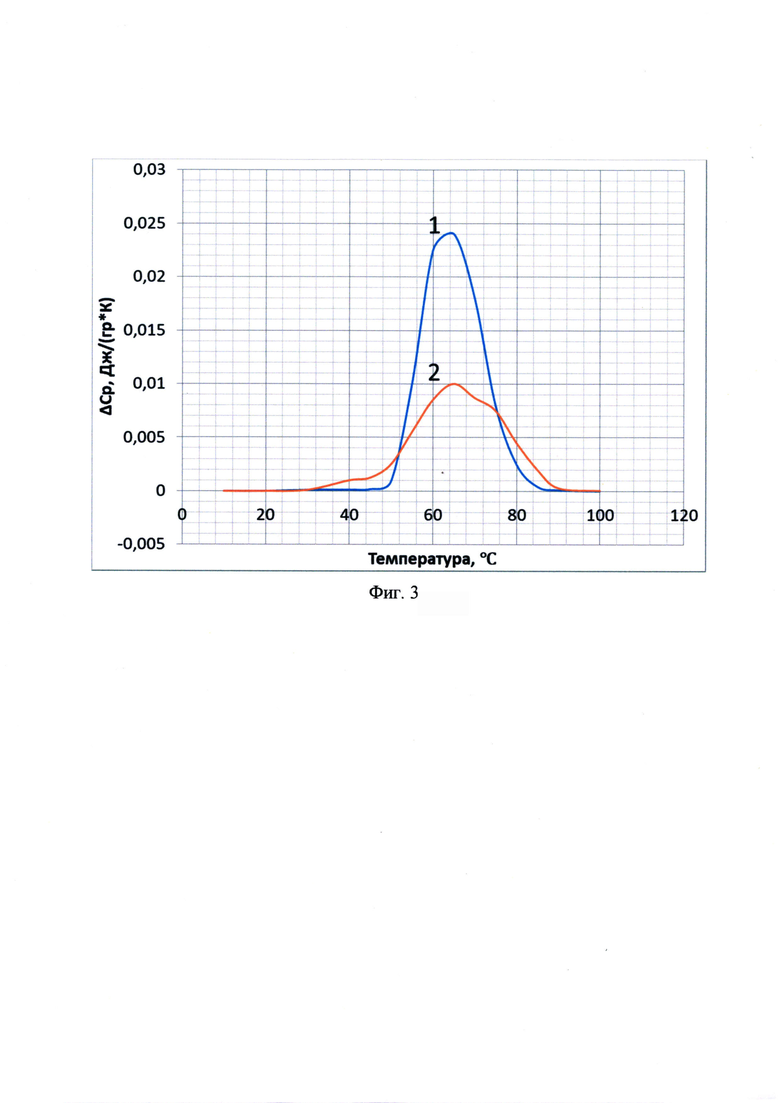
Изобретение поясняется чертежами, где на фиг.1 показан результат молекулярной стыковки S-белка SARS-CoV-2 в составе тримера (цепи «А» (зеленая), «В» (голубая), «С» (розовая)) с дитиразинзамещенным порфирином. Стыковка порфирина спайковым белком происходит в S-белке SARS-CoV-2, а именно в HR1 гептадном повторе цепи «А» и цепи «В», при этом порфирин дополнительно стабилизирован в белке за счет образования Н-связей между гетероатомами заместителя и аминокислотными остатками белка (таблица); на фиг. 2 представлен детализированный фрагмент комплекса, включающий гептадные повторы HR1D цепи «А» и цепи «В», взаимодействующие с дитиразинзамещенным порфирином; на фиг. 2а) представлены Н-связи, образующиеся между тиразиновым заместителем порфирина и аминокислотным остатками полипептидной цепи Phe592, Ser591, на фиг. 2б представлена Н-связь, образующаяся между тиразиновым заместителем порфирина и Cys538 аминокислотным остатком полипептидной цепи S-белка; на фиг. 3. представлены температурные зависимости избыточной удельной теплоемкости (ΔсP) растворов: S белка (линия 1), комплекса дититазинзамещенного порфирина с S-белком (линия 2).
Заявленное соединение получают следующим образом: Вначале получали мезо-(пиридиний-3-ил)дипирролилметан следующим образом:
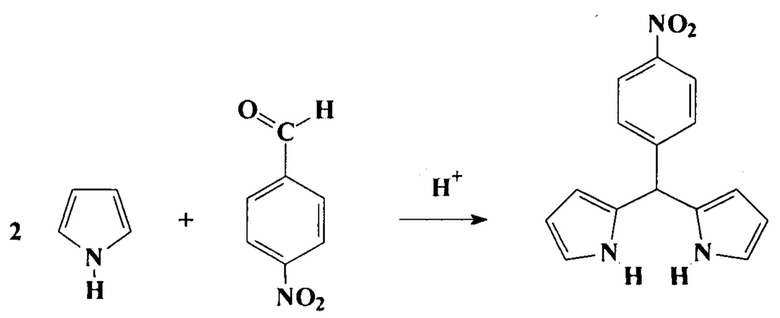 .
.
К раствору 5,0 мл концентрированной соляной кислоты в 200 мл воды при перемешивании постепенно добавляли 5,0 мл (72,22 ммоль) пиррола и 2,3 мл (24,37 ммоль) 3-пиридилкарбоксальдегида. Смесь перемешивали 2 ч, медленно нейтрализовали раствором 5,5 мл (73,47 ммоль) концентрированного раствора аммиака в 25 мл воды, осадок отфильтровывали, промывали водой, измельчали в ступке под слоем воды, отфильтровывали и высушивали при комнатной температуре на воздухе. Выход 4,5 г (68,8%).
1Н ЯМР (вн. ст.СНCl3) δ, м.д.: 8,49 dd (1Н, J=4,7 Hz; 1J=1,3 Hz; 6-Н-Ру); 8,45 d (1Н, 3J=1,9 Hz; 2-H-Py); 8,27 bs (2H, NH); 7,54 dt (1H, 4J=8,0 Hz; 3J=1,9 Hz; 5-H-Py); 7,27 dd (1H, 4J=8,0 Hz; J=4,7 Hz; 4-H-Py); 6,76 dd (2H, 5J=4,1 Hz; 6J=2,6 Hz; H-Pyr); 6,19 dd (2H,+7J=5,9 Hz; 8J=2,9 Hz; H-Pyr); 5,88-5,91 m (2H, H-Pyr); 5,49 s (1H, ms-H) (CDCl3)
Затем получали 5,15-бис(4'-нитрофенил)-10,20-бис(пиридиний-3'-ил)порфин
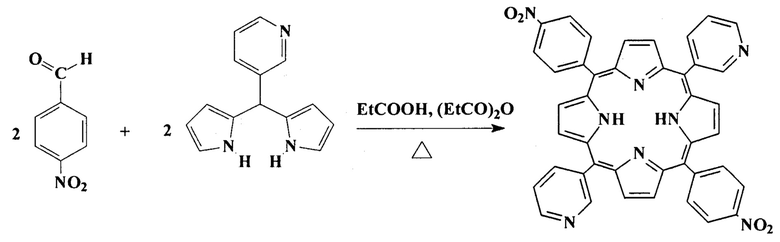 .
.
Кипятили 1,5 ч раствор 4,5 г (20,15 ммоль) мезо-(пиридиний-3'-ил)дипирролилметана и 3,2 г (21,17 ммоль) 4-нитробензальдегида в смеси 100 мл пропионовой к-ты и 10 мл (0,106 ммоль) уксусного ангидрида, затем отгоняли растворитель под вакуумом, остаток разбавляли водой, нейтрализовали раствором аммиака, осадок отфильтровывали, промывали водой и высушивали на воздухе при 70°С. Остаток экстрагировали в аппарате Сокслета хлористым метиленом с добавкой 2 мл триэтиламина до бесцветного вытека. Экстракт хроматографировали на калонке (2,5×50 см) с оксидом алюминия II степени активности, элюируя хлористым метиленом с добавкой 1% этанола. Элюат упаривали до 2 мл, порфирин осаждали 100 мл гексана, отфильтровывали, промывали гексаном и высушивали на воздухе при 70°С. Выход 1,45 г (20,4%).
Rf (алуфол): 0,88 (бензол-метанол, 20:1)
ЭСП λmax, нм (lg ε): 647 (3,83); 590 (3,94); 551 (4,06); 516 (4,33); 420 (5,51) (хлороформ)
MS (MALDI-TOF), т/z. 708,013 [М+Н]+, (вычислено 708,73)
1Н ЯМР (вн. ст.СНCl3) δ, м.д.: 9,48s (2Н, 2-Н-Ру); 9, 11dd (2Н, J=5,0Hz; 1J=1,6Hz, 4-Н-Ру); 8,89d (4Н, 2J=4,4Hz, 2,8,12,18-H); 8,85d (4H, 2J=4,4Hz, 3,7,13,17-H); 8,69d (4H, 3J=7,8Hz, 2,6-H-Ar); 8,55dt (2H, 4J=7,6Hz; 1J=1,6Hz, 6-H-Py); 8,43d (4H, 3J=7,8Hz, 3,5-H-Ar); 7,81dd (2H, 4J=7,6Hz; J=5,0Hz, 5-H-Py); -2,79bs (2H, NH) (CDCl3)
Далее получали 5,15-бис(4'-аминофенил)-10,20-бис(пиридиний-4'-ил)порфин
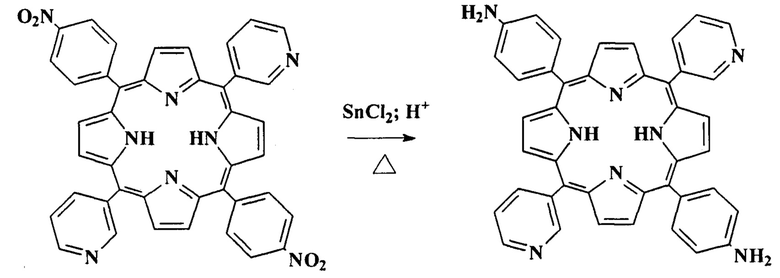 .
.
Кипятили 1 ч смесь 1,5 г (2,12 ммоль) 5,15-бис(4'-нитрофенил)-10,20-бис(пиридиний-3'-ил)порфина с 6,0 г (26,59 ммоль) хлорида олово дигидрата, 10 мл концентрированной соляной кислоты и 15 мл воды в 100 мл метанола. Раствор охлаждали, фильтровали, промывали водой с соляной кислотой осадок до бесцветного вытека, разбавляли пополам водой и нейтрализовали при перемешивании раствором 25,0 г (0,446 моль) гидроксида калия в 50 мл воды, осадок отфильтровывал, промывали водой и высушивали на воздухе при 70°С. Растворяли остаток кипячением в аппарате Сокслета в 200 мл хлористого метилена до бесцветного вытека, раствор охлаждали, и хроматографировали на колонке (2,5×50 см) с оксидом алюминия II степени активности, элюируя хлористым метиленом. Порфириновый элюат упаривали до 2 мл, и порфирин осаждали 100 мл гексана, фильтровали, промывали гексаном и высушивали на воздухе при 70°С. Выход 0,73 г (53,2%).
Rf (силуфол): 0,87 (бензол-метанол, 2:1)
ЭСП λmax, нм (lg ε): 653 (3,80); 596 (5,4); 560 (4,0); 521 (4,15); 426 (5,44) (хлороформ)
MS (MALDI-TOF), m/z: 647,676 [М+Н]+ (вычислено 647,76)
1Н ЯМР (вн. ст.DMSO) δ, м.д.: 9,38 s (2Н, 2-Ру); 9,06 d (2Н, J=4,9 Hz, 6-Ру); 9,00 d (4Н, J=3,3 Hz, β-Н); 8,79 d (4Н, J=3,3 Hz, β-H); 8,66 d (2H, J=8,7 Hz, 4-Py); 7,91 t (2H, J=6,4 Hz, 5-Py); 7,87 d (4H, J=7,8 Hz, 2,6-H-Ar); 7,02 d (4H, J=7,8 Hz, 2,6-H-Ar); 6,61 bs (4H, NH2); -2,80 bs (2H, NH) (DMSO-d6).
Затем получали 5,15-бис[4'-(N,O-бис-Вос-L-тирозинил)амидофенил]-10,20-бис(пиридиний-3'-ил)порфин
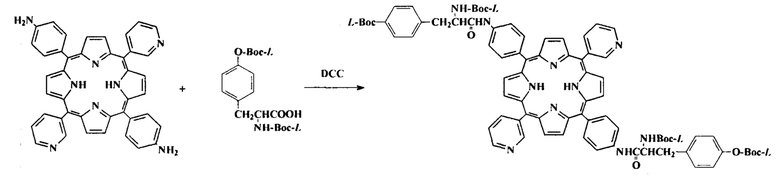 .
.
При перемешивании и охлаждении льдом к раствору 200 мг (0,52 ммоль) N,O-ди-Вос-L-тирозина и 60 мг (0,50 ммоль) 4-N,N-диметиламинопиридина в 10 мл осушенного хлористого метилена прибавляли 120 мг (0,58 ммоль) N,N'-дициклогексилкарбодиимида (ДЦК). Смесь перемешивали при охлаждении 2 ч, прибавляли 50 мг (0,0773 ммоль) 5,15-бис(4'-аминофенил)-10,20-бис(пиридиний-3'-ил)порфина и выдерживали при перемешивании 48 ч (контроль ТСХ), добавляли дополнительно 200 мг ДЦК и перемешивали еще 24 ч. Реакционную смесь фильтровали и хроматографировали на колонке (2,5×50 см) с оксидом алюминия II степени, элюируя хлористым метиленом с добавкой 1% метанола, элюат упаривали до 2 мл и продукт высаживали 100 мл гексана, отфильтровывали и высушивали на воздухе при 70°С. Выход 70 мг (56,6%).
Rf (силуфол): 0,58 (бензол-метанол, 10:1)
ЭСП Lmax, нм (lg ε): 652 (3,68); 594 (3,71); 553 (3,89); 619 (4,12); 422 (5,49) (хлороформ)
MS (MALDI TOF), m/z: 1375,588 [М+2Н]+ (вычислено 1375,60)
1Н ЯМР (вн. ст. СНCl3) δ, м.д.: 9,46 s (2Н); 9,07 d (2Н, J=4,2 Hz); 8,94 d (4Н, J=4,0 Hz); 8,81 d (4H, J=4,0 Hz); 8,25 m (4H); 8,17 d (4H, J=7,7 Hz); 7,43 d (4H, J=8,1 Hz, 2,6-H-Ar); 7,25 d (4H, J=8,1 Hz, 3,5-H-Ar); 7,16 d (4H, J=8,4 Hz, 3,5-H-Ar'); 7,12 d (4H, J=8,4 Hz, 2,6-H-Ar'); 6,52 d (4H, J=5,5 Hz); 5,29 bs (2H); 5,02 d (2H, J=8,3 Hz); 4,66 bs (2H); 4,56 q (2H, J=7,2 Hz); 4,18 q (4H, J=7,2 Hz); 3,33 m (4H); 3,10 dd (2H, J=6,2 Hz); 1,58 s, 1,57 s (36H, tBu); 1,55 s (20H, tBu); 1,45 s (16H, tBu); -2,82 bs (2H, NH) (CDCl3).
Затем получали 5,15-бис[4'-бис(N,O-бис-Вос-L-тирозинил)амидофенил]-10,20-бис(N-метилпиридиний-3'-ил)порфин дииодид
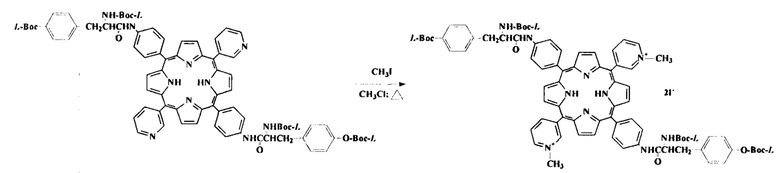
Кипятили 4 ч раствор 90 мг (0,066 ммоль) 5,15-бис[4'-бис(N,О-ди-Вос-L-тирозинил)-амидофенил]-10,20-бис(пиридиний-3'-ил)порфина в смеси 2 мл (32,11 ммоль) метилиодида 5 мл нитрометана (осуш.) и 10 мл осушенного хлористого метилена, затем смесь охлаждали, выливали на чашку Петри и высушивали на воздухе при 70°С. Выход 110 мг (100%)
ЭСП λmax, нм (lg ε): 659 (3,75); 595 (3,90); 563 (3,98); 525 (4,20); 431 (5,27) (хлороформ) MS (MALDI-TOF) m/z: 1405,25 (DHB) вычислено для C82H86N10O12 1403,64 1H ЯМР (вн. ст. CHCl3) δ, м.д.: 9,46 s (2H, 2-Py); 9,07 d (2H, J=4,2 Hz, 4-Py); 8,94 d (4H, J=4,0 Hz, 2,8,12,18-H); 8,81 d (4H, J=4,0 Hz, 3,7,13,17-H); 8,17 d (4H, J=7,7Hz); 7,43 d (4H, J=8,1 Hz, 2,6-H-Ar); 7,25 d (4H, J=8,1 Hz, 3,5-H-Ar); 7,16 d (4H, J=8,4 Hz, 3,5-H-Ar×); 7,12 d (4H, J=8,4 Hz, 2,6-H-Ar'); 5,29 bs (2H, CONH); 4,66 bs (2H, CONH); 4,56 dd (2H, J=13,4 Hz, 5,8 Hz, C*H); 3,08-3,16 m, 3,30-3,36 m (2xH, CH2); 1,57 s, 1,58 s (36H, tBu); -2,82 bs (2H, NH) (CDCl3)
Получение заявляемого соединения - 5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний-3'-ил)порфин дииодида
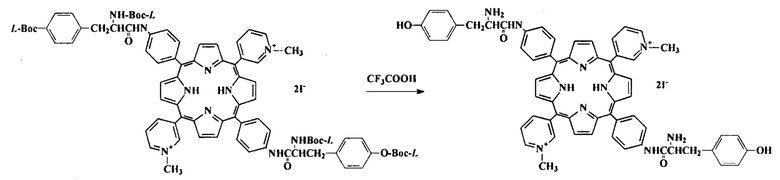
Перемешивали 4 ч раствор 110 мг (0,066 ммоль) 5,15-бис[4'-бис(N,O-ди-ВОС-L-тирозинил)амидофенил]-10,20-бис(N-метилпиридиний-3'-ил)порфин дииодида в 4 мл трифторуксусной к-ты. Реакционную смесь и выдерживали 12 ч, затем выливали на чашку Петри и высушивали на воздухе при 70°С. Выход 80 мг (80%)
Rf (силуфол): ~0,05 (метанол)
ЭСП λmax, нм (lg ε): 646 (3,69); 589 (3,84); 550 (3,90); 514 (4,22); 421 (5,41) (хлороформ) MS (MALDI-TOF) m/z: 1004,92 (DHB) вычислено для C62H54N10O4 1003,18
1Н ЯМР (вн. ст.CH3ОН) δ, м.д.: 9,87 s (2 Н, 2-Н-Ру); 9,35 d (4Н, J=6,1 Hz, 6-Н-Ру); 9,34 d (2Н, J=7,9 Hz, 4-Н-Ру); 9,04-8,86 m (8 Н, β-Н); 8,50 t (2 Н, J=6,6 Hz, 5-Py-H); 8,17 d (4 H, J=8,4 Hz, 2,6-H-Ar); 7,98 d (4 H, J=8,4 Hz, 3,5-H-Ar); 7,17 d (4 H, J=8,3 Hz, 2,6-H-Ar-Tyr); 8,78 d (4 H, J=8,3 Hz, 3,5-H-Ar-Tyr); 4,78 s (CH3ОН); 4,71 s (6 H, NCH3); 4,26 t(2H, J=6,7 Hz, C*H-Tyr); 3,24-3,30 m (2 H, NH); 3,22 bs (СН3OH); (метанол-d4)
Пример применения заявляемого соединения (связывание с S-белком SARS-CoV-2)
Коронавирусы проникают в клетки за счет S-белка на их оболочке. S-белок коронавируса представляет собой заякоренный в мембране тример и содержит две субъединицы: S1 субъединицу для связывания рецептора и S2 субъединицу, обеспечивающую слияние мембран вируса и клетки хозяина. S2 субъединица состоит из гибридного пептида (FP) (788-806 остатков), последовательности гептадного повтора 1 (HR1) (912-984 остатка), гептадного повтора 2 (HR2) (1163-1213 остатков), трансмембранного домена TMD (1213-1237 остатков) и домена цитоплазмы (1237-1237 остатков). Первый этап инфицирования, связан с прикреплением вириона к рецептору клетки хозяина, осуществляется за счет S1 -субьединицы белка SARS-CoV-2 с одной стороны и ангиотензинпревращающего фермента 2 или рецептор CD147, с другой стороны. Далее следует процесс слияния мембран вируса и клетки хозяина, в котором участвуют S2-субьединица S-белка SARS-CoV-2 и эндосомальная цистеинпротеаза, сериновая пептидаза и фурин, клеточная мембрана клетки хозяина. Из двух субьединиц S-белка S2-субьединица является консервативной, a S1- более подвержена мутациям, поэтому необходимо разработка и создание соединений, способных ингибировать слияние мембран. Для этого был синтезирован дитиразинзамещенный порфирин, который при внесении в растворы S-белка SARS-CoV-2 образует устойчивый комплекс с S2 субъединицей S-белка.
На фиг. 1 в качестве примера представлен результат молекулярной стыковки дитиразинзамещенного порфирина с S-белком. Стыковка порфирина спайковым белком происходит в S-белке SARS-CoV-2, а именно в HR1 гептадном повторе цепи «А» и цепи «В», при этом порфирин дополнительно стабилизирован в белке за счет образования Н-связей между гетероатомами заместителя и аминокислотными остатками белка (таблица).
Результат молекулярной стыковки S-белка в составе тримера (цепи «А» (зеленая), «В» (голубая), «С» (розовая)) с дитиразинзамещенным порфирином представлен на фиг. 1. На фиг. 2 представлен детализированный фрагмент комплекса. На фиг. 2а) представлены Н- связи, образующиеся между тиразиновым заместителем порфирина и аминокислотным остатком полипептидной цепи Phe592, Ser591, на фиг. 2б аналогичные Н-связи с Cys538. Высокая энергия связывания дитиразинзамещенного порфирина с S-белком SARS-CoV-2 обеспечивается множественными специфическими и вандервалльсовыми взаимодействиями и подтверждается образованием коротких (менее 3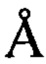 ) Н-связей (таблица).
) Н-связей (таблица).
Для получения комплекса дититазинзамещенного порфирина с S-белком SARS-CoV-2 навеску массой 0,0001 г 5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний-3'-ил)порфин дииодида растворяли в 28,2 г. бидистиллированной воды. Далее, отбираем 2 мл полученного раствора с концентрацией порфирина 3,5⋅10-6 моль/л. В порфириновый раствор вносится навеска 0,018 г NaCl для получения осмолярного раствора. S-белок концентрацией (1,3⋅10-5 моль/л) готовили в фосфатном буфере (PBS) с РН=7,4. Раствор PBS готовился путем растворения 1 таблетки (Merck, артикул S-P4417-100TAB) в 200 мл деионизованной воды для получения фосфатно-солевого буфера PBS (0,01 М фосфатный буфер, 0,0027 М хлорид калия, 0,137 М хлорид натрия, рН 7,4 при 25°С). Для получения комплекса 5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний'-3-ил)порфина в 2 мл раствора порфирина вносили 550 мкл раствора S-белка. Раствор выдерживали при 25°С не менее 15 минут при постоянном перемешивании.
ИК спектральным доказательством образования комплекса дититазинзамещенного порфирина с S-белком SARS-CoV-2 является следующее: спектр комплекса не аддитивен спектрам исходных реагентов, например, появляются новые полосы при 3493,15 см-1 и 846,5 см-1, отсутствующие в ИК спектрах исходных реагентов. При комплексообразовании часть полос поглощения S-белка претерпевают смещение в высокочастотную область (1241,26→1231,71; 1534,15→1538,92; 2118,38→2121,51; 2923,50→2926,16; 2955,55→2963,56; 3461,49→3493,15 см-1) в то время как часть полос поглощения белка смещается в коротковолновый диапазон (478.06→473.61; 626.69→621.11; 1241,26→1231,71; 1776,10→1774,51; 2847,36→2845,77; 3239,81→3236,64; 3392,30→3361,23 см-1). Перечисленные изменения в ИК спектрах служат подтверждением комплексообразования между S-белком и порфирином.
Термохимическим доказательством образования комплекса дититазинзамещенного порфирина с S-белком SARS-CoV-2 является уменьшение температуры денатурации комплекса по сравнению с S-белком на 10-11°С (Фиг. 3).
| название | год | авторы | номер документа |
|---|---|---|---|
| 5-[4-(1,3-БЕНЗОТИАЗОЛ-2-ИЛ)ФЕНИЛ]-10,15,20-ТРИС(1-МЕТИЛПИРИДИНИЙ-3-ИЛ)ПОРФИРИН ТРИИОДИД, ПРОЯВЛЯЮЩИЙ СВОЙСТВО СВЯЗЫВАНИЯ СПАЙКОВОГО БЕЛКА ВИРУСА SARS-CoV-2 | 2021 |
|
RU2773397C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ПРОИЗВОДНОЕ 1,3,5-ТРИАЗИН-2,4-ДИАМИНА, ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2827891C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ТРИЦИКЛИЧЕСКОЕ СЕРУСОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ 1,2-ДИГИДРОХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2814434C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИЦИКЛИЧЕСКОГО СЕРУСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 1,2-ДИГИДРОХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2 | 2021 |
|
RU2819783C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛОРОДСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 6-ГАЛОГЕНХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2 | 2021 |
|
RU2827892C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ КИСЛОРОДСОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ 6-ГАЛОГЕНХИНОЛИНА, ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2827893C1 |
| ПРИМЕНЕНИЕ ТРИЦИКЛИЧЕСКОГО СЕРУСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 1,2-ДИГИДРОХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-CoV-2 | 2021 |
|
RU2780247C1 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ SARS-COV-2 | 2021 |
|
RU2769828C1 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНОГО 1,3,5-ТРИАЗИН-2,4-ДИАМИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2 | 2021 |
|
RU2780249C1 |
| Способ выявления заражения людей и животных SARS CoV2 и диагностический набор для осуществления способа | 2021 |
|
RU2776295C1 |
Изобретение относится к органической химии, а именно к 5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний-3'-ил)порфин дииодиду. Технический результат: получен водорастворимый порфирин, имеющий два периферийных протяженных гидрофобных заместителя, связывающихся в S2 субъединицы S-белка SARS-CoV-2, тиразильные фрагменты которых обеспечат дополнительную устойчивость комплексу за счет образования нескольких водородных связей с аминокислотными остатками полипептидной цепи S2 единицы. 5 ил., 1 табл., 1 пр.
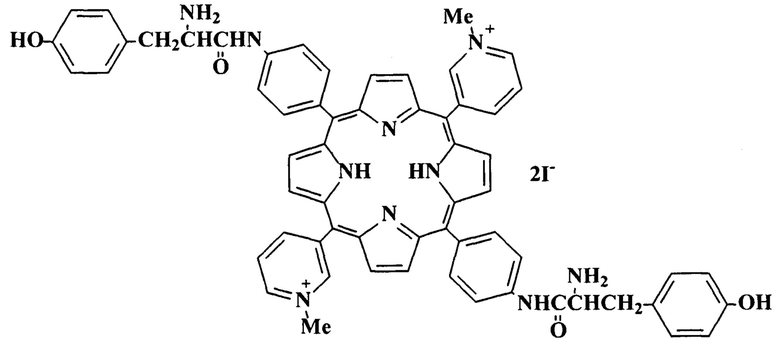
5,15-бис(4'-бис-L-тирозиниламидофенил)-10,20-бис(N-метилпиридиний-3'-ил)порфин дииодид, проявляющий свойство связывания S-белка вируса SARS-CoV-2:
| 5-[4-(1,3-БЕНЗОТИАЗОЛ-2-ИЛ)ФЕНИЛ]-10,15,20-ТРИС(1-МЕТИЛПИРИДИНИЙ-3-ИЛ)ПОРФИРИН ТРИИОДИД, ПРОЯВЛЯЮЩИЙ СВОЙСТВО СВЯЗЫВАНИЯ СПАЙКОВОГО БЕЛКА ВИРУСА SARS-CoV-2 | 2021 |
|
RU2773397C1 |
| Yury A | |||
| Gubarev et al, Possible therapeutic targets and promising drugs based on unsymmetrical hetaryl-substituted porphyrins to combat SARS-CoV-2, Journal of Pharmaceutical Analysis, 11(6), 2021, p.691-698 | |||
| Syrbu SA, et al, Synthesis of Hetaryl-Substituted Asymmetric Porphyrins and Their Affinity to SARS-CoV-2 | |||
Авторы
Даты
2022-12-01—Публикация
2022-08-03—Подача