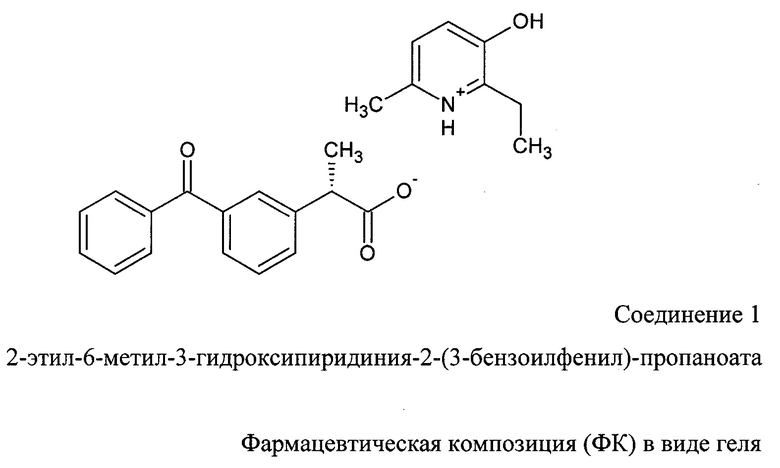
Изобретение относится к области медицины и фармации, конкретно, к синтезу 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата и фармацевтической композиции (ФК) на его основе в виде геля, обладающее способностью стимулировать репаративные процессы тканей пародонта, антиоксидантным, противовоспалительным, иммунокорригирующим, цитопротекторным, антиульцерогенным действием и пригодно для лечения воспалительных заболеваний пародонта:
Уровень техники
В настоящее время, несмотря на совершенствование и внедрение в практику новых методов лечения пародонтита, согласно статистике ВОЗ, воспалительным заболеваниям пародонта подвержена половина населения планеты. До 50% всей заболеваемости приходится на пародонтит: хроническое заболевание, характеризующееся волнообразным течением. Важной задачей при пародонтите является достижение и поддержание стойкой ремиссии. Непрерывно рецидивирующее течение заболевания приводит к интенсификации дегенеративно-деструктивных процессов пародонта с исходом в пародонтоз, который приводит к потере зубов и снижению качества жизни. Заболеваемость пародонтозом по данным ВОЗ составляет 5-8% в мировой популяции.
Согласно клиническим рекомендациям по лечению воспалительных заболеваний пародонта в составе комплексной терапии рекомендовано использование нестероидных противовоспалительных средств (http://pras59.ru/clinical-recomendation).
Существует способ местного лечения воспалительных заболеваний пародонта с использованием индометацина, иммобилизованного на 3% взвеси полисорба (Методические рекомендации «Комплексное лечение воспалительных заболеваний пародонта с использованием иммобилизованного индометацина», Ставрополь, 1992, с. 3-6). За счет неселективной ЦОГ-ингибирующей активности индометацин проявляет выраженное противовоспалительное, противоотечное, а также обезболивающее и жаропонижающее действие. Однако при применении данного лекарственного средства высок риск системных побочных эффектов, в том числе местных эрозивно-язвенных дефектов.
Известно применение холисала для лечения воспалительных заболеваний пародонта (Лютов Н.Г. Холисал в лечении пародонтоза и заболеваний слизистой оболочки рта. Русский медицинский журнал, том 9, 6, 2001). Основные действующие вещества препарата: холина салицилат, относящийся к производным салициловой кислоты и проявляющий противовоспалительную, анальгезирующую активность; и цеталкония хлорид, являющийся антисептическим средством. Составляющие препарата также представлены консервирующими и вкусовыми компонентами, гелевой основой. Недостатком данного состава является слабое противовоспалительное действие, отсутствие репаративного эффекта, высокий риск эрозивно-язвенных осложнений.
Известно использование для лечения стоматологических заболеваний неселективного НПВС - диклофенака в виде гелевой композиции, активные компоненты которой представлены хлоргексидина глюконатом и диклофенаком. Гелевая композиция предназначена для нанесения на слизистую полости рта. Обладает антисептическим, выраженным противовоспалительным эффектом (патент РФ №2288699, 2006 г.).
Известен способ лечения воспалительных заболеваний пародонта с поэтапным использованием сначала геля метрогил-дента, активные вещества которого представлены хлоргексидина глюконатом и метронидазолом, затем диклоран-желе, действующим веществом которого является диклофенак (патент РФ №2206311, 2003 г.).
Известно несколько способов лечения пародонтита путем аппликации биополимерных пленок, содержащих в составе гидрофильного слоя с диклофенаком. Так, в патенте РФ №158996, 2016 г. гидрофильный слой содержит диклофенак и винпоцетин, а в патенте РФ №2153319, 2000 г. - кавинтон и вольтарен. Данные способы лечения обладают противовоспалительным, нейропротекторным, антиагрегантным, сосудорасширяющим действием, что позволяет снизить активность воспаления, нормализовать микроциркуляцию и улучшить гемодинамику в пораженных тканях пародонта.
Также диклофенак может использоваться в качестве активного вещества в составе гелесодержащей фармацевтической композиции на основе сольватокомплексов глицератов кремния и титана (патент РФ №2417102, 2011 г.).
Известен состав для лечения генерализованного пародонтита, состоящий из мирамистина, энтеросгеля, мелоксикама (патент Украина №60035, 2010 г.).
Кроме того, имеются данные, свидетельствующие об удлинении периода ремиссии и снижении вероятности развития рецидива при применении иммобилизованного на сорбенте мелоксикама и иммуностимулирующего воздействия низкоэнергетического лазера в комплексной терапии хронического генерализованного пародонтита (Хубаев Т.С. Эффективность сочетания иммобилизованных противовоспалительных препаратов и иммуностимулирующего воздействия при лечении пациентов с хроническим пародонтитом / Диссертация на соискание ученой степени к.м.н., - 2021).
Кетопрофен относится к производным пропановой кислоты. Благодаря неселективной ЦОГ-ингибирующей активности, оказывает выраженный обезболивающий эффект, жаропонижающее, противовоспалительное, противоотечное действие, что снижает миграцию иммунокомпетентных клеток в очаг воспаления, нормализует микроциркуляцию.
Существует множество лекарственных форм кетопрофена, позволяющих применять его системно: парентерально (в виде 0,05% раствора для в/м, в/в инъекций, суппозитория), внутрь (в виде капсул, таблеток, гранул), а также местно (в виде 5% геля, 16% раствора для полоскания).
Известен способ местного лечения воспалительных заболеваний пародонта в виде аппликаций на слизистую оболочку с помощью геля Флексен®, содержащего в качестве действующего вещества 2,5% кетопрофена (Зорян А.В. Сравнительная оценка эффективности применения различных групп противовоспалительных препаратов при катаральном гингивите и пародонтите легкой степени / Диссертация на соискание ученой степени к.м.н., - М., 2004). А также раствор для полоскания ОКИ, содержащий кетопрофена лизиновую соль 16 мг/мл (Багдасарова И.В. Значение ПГ Е2 и ПГ F2α в патогенезе воспалительных заболеваний пародонта и обоснование использования ингибиторов ПГ в комплексной терапии гингивита и пародонтита / Диссертация на соискание ученой степени к.м.н., - М., 2004).
Известен способ применения кетопрофена в форме геля или раствора, наносимого на пораженный пародонт, в комбинации с адгезивной пленкой диплен-дента X, позволяющей локализовать препарат в месте нанесения, для поддержания терапевтической концентрации (патент РФ №2652349, 2018 г.). Изобретение РФ №2491061, 2013 г., представляет собой средство для местного лечения воспалительных заболеваний пародонта, применяемое в виде аппликаций, на основе кремнийорганического геля состава Si(C3H7O3)4⋅6С3Н8О3⋅24H2O, включающее лекарственные добавки: кетопрофен и метилурацил, при следующем соотношении компонентов, масс. %:
кетопрофен - 0,5-1,0
метилурацил - 1,0-1,5
кремнийорганический гель состава Si(C3H7O3)4⋅6C3H8O3⋅24H2O - остальное до 100,0.
Противовоспалительный и обезболивающий эффект кетопрофена сочетается с иммуномодулирующими и репаративными свойствами метилурацила.
Несмотря на выраженный противовоспалительный эффект, существенным недостатком представленных способов лечения пародонтита с применением НПВС, а в частности с применением кетопрофена, является его неспособность коррекции гомеостаза в пораженных тканях, вследствие отсутствия или слабо выраженного антиоксидантного, антигипоксантного, мембранстабилизирующего и регенерирующего действия. Кроме того, ЦОГ-ингибирующее действие НПВС при недостатке цитопротекторных свойств лекарственных композиций, может приводить к появлению эрозивно-язвенных дефектов слизистой полости рта НПВС гастропатии и энтеропатии и развитию системных побочных эффектов.
В последние годы в комплексном лечении пародонтита широко применяется антиоксидантная терапия.
Имеются данные, свидетельствующие о положительном эффекте дополнительного включения в терапию хронического генерализованного пародонтита антиоксидантных витаминных комплексов (никотиновой кислоты, аскорбиновой кислоты и др.), в частности, α-токоферола ацетата (Лемецкая Т.И. Клинико-экспериментальное обоснование классификации болезней пародонта и патогенетические принципы лечебно-профилактической помощи больным с патологией пародонта / Диссертация на соискание ученой степени д.м.н., - 1998.)
В работе Ордян Л.Л. описано применение препарата цитофлавин в комплексной терапии хронического генерализованного пародонтита (экспериментально-клиническое исследование / Диссертация на соискание ученой степени к.м.н., - 2013).
В патенте РФ №2420257, 2011 г., описан способ получения стоматологического геля с хлоргексидином и дибунолом для лечения воспалительных заболеваний пародонта и ротовой полости при следующем содержании компонентов, мас. %:
Антисептическое действие хлоргексидина сочетается с антиоксидантными, регенерирующими свойствами дибунола, что в совокупности придает гелю противовоспалительную активность. Однако длительное применение средства может привести к развитию дисбиоза ротовой полости, что в свою очередь станет причиной усугубления воспалительного процесса.
Известна паста диоцинкохим, наносимая в виде аппликаций на слизистую оболочку пораженного пародонта, рекомендованная больным сахарным диабетом (Назаренко З.Ю. Комплексная терапия микроциркуляторных нарушений в деснах больных хроническим генерализованным пародонтитом на фоне сахарного диабета / Диссертация на соискание ученой степени к.м.н., - 2008). Содержит следующие компоненты, мас. %:
Масляный 30% раствор витамина Е до 100 (патент РФ №2026062, 1995 г.). Паста оказывает антибактериальное, антиоксидантное, регенерирующее действие. Недостатками данной пасты являются ее многосоставность, труднодоступность составляющих компонентов. Диоксидин, являясь синтетическим антибактериальным средством, обладает мутагенными и тератогенными свойствами. Кроме того, широкий спектр и выраженное бактерицидное действие также могут приводить к дисбиозу ротовой полости.
Известны способы лечения воспалительных заболеваний пародонта с помощью дополнительного включения в комплексную терапию лекарственного препарата полиоксидоний, обладающего иммуномодулирующими, антиоксидантными и противовоспалительным свойствами. Доказана эффективность внутримышечного введения препарата по 6 мг 1 раз в день через день в количестве 5 инъекций в составе комплексной терапии пародонтита у лиц с сахарным диабетом 2 типа (Михайлова Ю.А. Клинико-лабораторное обоснование использования иммунокоррегирующих препаратов в комплексном лечении пародонтита у больных с осложненной формой диабета / Диссертация на соискание ученой степени к.м.н., - 2009). Для местного применения на слизистую оболочку пародонта используется коллагеновая губка в виде носителя, которая пропитывается раствором препарата полиоксидоний (1,5 мл), что позволяет локализовать и пролонгировать действие (Сашкина Т.И. Патогенетические основы неполной регенерации при хроническом генерализованном пародонтите / Диссертация на соискание ученой степени д.м.н., - 2017). Также, возможно включение полиоксидония в состав гидрофильного слоя адгезивных биопленок (патент РФ №2185807, 2002 г.). В патенте РФ №2470640, 2012 г., описано получение кремнийорганического геля для лечения воспалительных заболеваний пародонта и ротовой полости, в качестве активной лекарственной добавки в котором может быть использован полиоксидоний. Методика применения предполагает аппликации на слизистую оболочку или инстилляции в пародонтальные карманы один раз в день на 15 мин в течение 5-7 дней.
2-Этил-6-метил-3-гидроксипиридина сукцинат (лекарственный препарат мексидол) обладает выраженным антиоксидантным действием, проявляющимся за счет снижения липопероксидации, благодаря электронодонорной активности алкильных заместителей, а также повышения активности супероксиддисмутазы. Антигипоксический эффект реализуется благодаря содержанию сукцината и стабилизации стенок сосудов вследствие снижения образования циклических эндопероксидов - простагландинов Н2 и G2 (мембранопротекторный эффект). Таким образом, улучшается микроциркуляция и реологические свойства крови. Данные эффекты обеспечивают противовоспалительное, цитопротекторное действие, усиливают регенерирующий потенциал клеток (https://mexidol.ru/extra/File/Mexidol.pdf).
Доказаны ноотропное и транквилизирующее (патент РФ №2065299), противоишемическое и антиатеросклеротическое (патент РФ №2144822), антиангинальное (патент РФ №2168993), гепатопротекторное (патент РФ №2189817), антибактериальное (патент РФ №2157686) действие мексидола.
Для лечения воспалительных заболеваний пародонта препарат используют как местно (5% раствор мексидола в форме полоскания или пропитывания марлевых турунд), так и системно: перорально по 100-500 мг в форме таблеток или капсул 1-2 раза в день или в виде 5% раствора по 2 мл 1 раз в день внутримышечно (патент РФ №2223088, 2004 г.).
Также для профилактики и лечения заболеваний пародонта и слизистой ротовой полости рекомендуется использование зубной пасты Мексидол Дент актив, содержащей в качестве активного компонента мексидол (патент РФ №2239414, 2004 г.).
Имеются данные, свидетельствующие о высокой эффективности применения мексидола в комбинации с реамберином в лечении хронического генерализованного пародонтита (Корнилова Н.В. Клинико-лабораторное обоснование эффективности применения производных 3-оксипиридина и янтарной кислоты на этапе медикаментозного лечения хронического генерализованного пародонтита / Диссертация на соискание ученой степени к.м.н., - 2011).
Доказана эффективность включения в комплексное лечение хронического генерализованного пародонтита, особенно тяжелой степени заболевания, лекарственного препарата мексикор по 1 капсуле (100 мг) внутрь 3 раза в день и лазерной терапии в проекции кубитальной вены в течение 10 минут с 2-х сторон, а также местно в области альвеолярного отростка в течение 2-5 минут на протяжении 12 дней (Ташина Е.А. Гемостазкорригирующий компонент в оптимизации лечения хронического пародонтита / Диссертация на соискание ученой степени к.м.н., - 2021).
Однако, несмотря на оказываемое препаратами с антиоксидантными свойствами (в частности производными 2-этил-6-метил-3-гидроксипиридина) ингибирование процессов свободнорадикального окисления, улучшение микроциркуляции и регенераторного потенциала тканей, при их применении отмечается слабый противовоспалительный, противоотечный и анальгетический эффекты.
Таким образом, для создания лекарственного средства, обладающего свойствами стимулирования регенерации тканей пародонтального комплекса, ингибирующего воспалительные и деструктивные процессы, оказывающего антиоксидантное, цитопротекторное и антиульцерогенное действие целесообразны синтез и исследование нового соединения или фармацевтической композиции 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата.
Раскрытие изобретения
Целью изобретения является синтез соединения 1 и создание на его основе ФК в виде геля - лекарственного средства, обладающего способностью стимулировать репаративные процессы тканей пародонта, а также антиоксидантным, противовоспалительным, иммунокорригирующим, цитопротекторным и антиульцерогенным действием.
Поставленная цель достигается синтезом нового соединения 1 - 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата и фармацевтической композиции (ФК) на его основе.
Технический результат заключается в синтезировании нового соединения 1, получении фармацевтической композиции (ФК) на его основе в виде геля, а также исследовании их биологической активности.
ФК в виде мягкой лекарственной формы - гель, содержащий активное соединение 1, получали путем растворения соединения 1 в спиртах (этиловый, пропиленгликоль) и использования в качестве гидрофильной основы производных целлюлозы, в частности гидроксипропилцеллюлозы, которая обладает нейтральными свойствами, физиологична и не раздражает слизистых оболочек полости рта, разрешена к медицинскому применению. Количество целевых добавок к активному соединению 1 для получения стабильной ФК в виде геля выбрано экспериментально.
Синтез нового соединения 1 осуществляли путем взаимодействия эквимолярных количеств 2-этил-6-метил-3-гидроксипиридина и 2-(3-бензоилфенил)-пропановой кислоты.
Пример 1. Синтез 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата
В трехгорлую колбу, снабженную мешалкой, обратным холодильником и термометром, загружают 50 мл этилового спирта. Затем при перемешивании постепенно добавляют 6,75 г (0,026 гм) 2-(3-бензоилфенил)-пропановой кислоты, после растворения добавляют 3,64 г (0,026 гм) 2-этил-6-метил-3-гидроксипиридина. Полученный раствор нагревают до 30°С и перемешивают до полного растворения, фильтруют, от фильтрата отгоняют растворитель под вакуумом. Тщательно сушат. Получают 9,32 г (89,7%) белого со слегка желтоватым оттенком гигроскопичного порошка с Т плав. = 95-100°С.
Найдено, %: С 73,60; Н 6,54; N3,53; C24H25NO4м.м. 391,45
Вычислено, %: С 73,64; Н 6,43; N 3,58; О 16,35
ИК, ν, см-1: 3434 (ОН); 2976, 2937, 2835 (СН); 2366 (N+); 1656 (С=С), 1578 (C=N).
рН 0,1% раствора в воде: 6,5.
Пример 2. Синтез 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата
В трехгорлую колбу, снабженную мешалкой и термометром, загружают 6,75 г (0,026 гм) 2-(3-бензоилфенил)-пропановой кислоты и присыпают 3,64 г (0,026 гм) 2-этил-6-метил-3-гидроксипиридина, массу тщательно перемешивают. Через 15 минут отбирают пробу для определения температуры плавления. При плавлении полученного вещества 97-100°С массу выгружают. Получают 10,1 г (97,2%) белого кристаллического гигроскопичного порошка с Т плав. = 97-100°С.
Найдено, %: С 73,62; Н 6,46; N 3,57; C24H25NO4 м.м. 391,45
Вычислено, %:С 73,64; Н 6,43; N 3,58; О 16,35
ИК, ν, см-1: 3434 (ОН); 2976, 2937, 2835 (СН); 2366 (N+); 1656 (С=С), 1578 (C=N).
рН 0,1% раствора в воде: 6,5.
ТСХ: на пластинах Silicagel УФ 254 в системе растворителей бензол:ацетон - 1:1 (одно пятно)
Пример 3. Получение ФК в виде геля на основе 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата
В трехгорлую колбу, снабженную мешалкой, загружают 23,5 мл (18,8 г) этилового спирта и 5 мл (4 г) пропиленгликоля. При перемешивании к раствору добавляют 5 г соединения 1. Полученную массу тщательно перемешивают. К полученной массе добавляют 73 мл (80,7 г) 7% водного раствора гидроксипропилцеллюлозы*. Получают 100,0 мл (103,5 г) однородного, прозрачного со слегка желтоватым оттенком мягкой консистенции геля, содержащего 5% соединения 1 (1 мл геля содержит 50 мг соединения 1).
*Примечание: 7% раствор гидроксипропилцеллюлозы получают прибавлением 7,6 г гидроксипропилцеллюлозы к 100 мл нагретой до 55-60°С воды для инъекций, массу тщательно перемешивают, охлаждая до 20-25°С.
Полученный гель соответствует требованиям ГФ XIV по основным показателям качества, предусмотренным для мягких лекарственных форм (количественное определение, внешний вид, стабильность).
Биологические исследования соединения 1 и ФК на его основе.
Исследования выполнены в соответствии с этическими требованиями к работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР №755 от 12.08.1987 г.), Федеральный закон «О защите животных от жестокого обращения» от 01.01.1997 г., «Об утверждении Правил надлежащей лабораторной практики» (приказ МЗ РФ №199н от 01.04.2016 г.)) и одобрены локальным этическим комитетом.
Гистологические исследования проводились на микроскопе «HUMASCOPE ADVANCED LED», Германия. Микрофотографии выполнены с использованием цифровой фотокамеры Human GmbH (USB) 8,0 Мпикс, Германия.
Пример 4. Биологическая активность соединения 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата
Острая токсичность соединения 1, кетопрофена и мексидола.
Оценка острой токсичности соединения 1 произведена в опытах на белых беспородных мышах (195 особей обоего пола массой 19-23 г), полученных из биопитомника «СМК СТЕЗАР», при внутрижелудочном введении субстанции и препаратов сравнения в крахмальной слизи в объеме 0,3-0,5 мл.
Показатель ЛД50 рассчитывался методом Личфилда-Уилкоксона (кн. Е.В. Арзамасцев, И.В. Березовская, О.В. Верстакова и др. Методические рекомендации по изучению общетоксического действия лекарственных средств / Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - С. 25-35; Гуськова Т. А. Токсикология лекарственных средств. - М: Издательский дом "Русский врач". - 2003. - С. 20-24.).
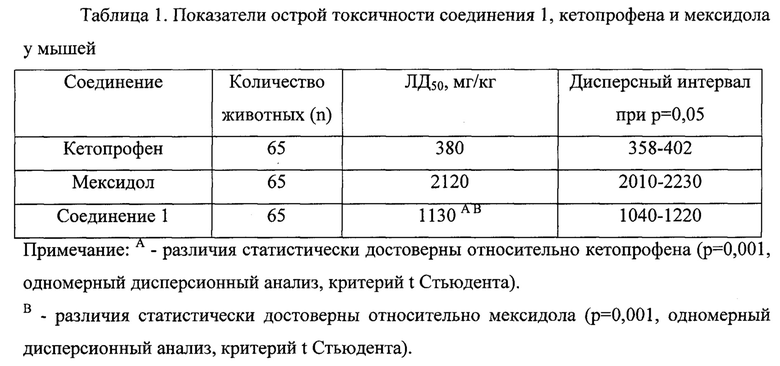
Результаты исследования острой токсичности соединения 1 и отдельных фрагментов заявляемой молекулы, приведены в таблице 1.
Представленные результаты демонстрируют, что соединение 1 в 2,97 раза менее токсично кетопрофена, но в 1,88 токсичнее мексидола при их внутрижелудочном введении.
Пример 5. Модель для изучения фармакологической активности соединения 1 Фармакологическая активность соединения 1 изучена на модели экспериментального пародонтита в опытах на белых нелинейных крысах (75 особей обоего пола массой 180-220 г, полученных из биопитомника «СМК СТЕЗАР». Экспериментальный пародонтит воспроизводился методом Школьной К.Д., Атрушкевич В.Г. (Способ экспериментального моделирования пародонтита, патент РФ №2625295 -2017 г).
Исследовано соединение 1 при введении его внутрижелудочно, а также при местном аппликативном применении ФК в виде геля на ткани пародонта.
Соединение 1 и отдельные фрагменты при внутрижелудочном введении предварительно растворяли в крахмальной слизи в объеме 1,5-2,0 мл, ФК применяли аппликативно в объеме 0,1 мл (5 мг) в сутки.
Пример 6. Антиоксидантная активность соединения 1 на модели экспериментального пародонтита
Результаты исследования влияния соединения 1 и препаратов сравнения на процессы свободно-радикального окисления у крыс с экспериментальным пародонтитом приведены в таблице 2.
При сравнении внутрижелудочного введения соединения 1 с сериями применения кетопрофена и мексидола значительно эффективнее ингибировались процессы липопероксидации: диеновые конъюгаты (ДК) - на 73,3% (p1<0,001) и 26,7% (р2<0,001) соответственно, малоновый диальдегид (МДА) плазмы - на 42,9% (p1<0,001) и 8,8% (р2<0,05), МДА эритроцитов - на 34% (p1<0,001) и 7,2% (р2>0,05), МДА при железоиндуцированном окислении (Fe-МДА) плазмы - на 55,6% (p1<0,001) и 22,7% (р2<0,001), Fe-МДА эритроцитов - на 40,4% (p1<0,001) и 16,8% (р2<0,01); а потенциал антиоксидантной системы восстанавливался быстрее: активность каталазы в плазме - на 23,9% (p1<0,001) и 10,3% (р2<0,05), в эритроцитах - на 16,8% (p1<0,01) и 7,9% (р2>0,05), активность супероксиддисмутазы (СОД) - на 39,7% (p1<0,001) и 22,1% (р2<0,001); максимальная интенсивность свечения (Imax) - на 31,9% (p1<0,001) и 6,0% (р2>0,05), светосумма хемилюминесценции (S) - на 35,5% (p1<0,001) и 10,2% (р2<0,05) соответственно.
ФК показала себя наиболее эффективно при сравнении с сериями введения кетопрофена и мексидола, приводя к ингибированию процессов липопероксидации: ДК - на 86,6% (p1<0,001) и 40% (р2<0,001) соответственно, МДА плазмы - на 54,6% (p1<0,001) и 20,5% (р2<0,01), МДА эритроцитов - на 40% (p1<0,001) и 13,2% (р2<0,05), Fe-МДА плазмы - на 68,3% (p1<0,001) и 35,4% (р2<0,001), Fe-МДА эритроцитов - на 55,4% (p1<0,001) и 31,8% (р2<0,001). Наблюдался рост активности антиоксидантной системы на фоне применения ФК. Так, активность каталазы в плазме возрастала относительно применения кетопрофена и мексидола на 34,2% (p1<0,001) и 21,4% (р2<0,01) соответственно, в эритроцитах - на 23% (p1<0,01) и 14,1% (р2<0,05), активность СОД - на 46,6% (p1<0,001) и 29% (p2<0,001); Imax - на 55,1% (p1<0,001) и 29,2% (p2<0,001), S - на 44% (p1<0,001) и 18,7% (р2<0,01).
Внутрижелудочное введение соединения 1 и аппликации ФК приводили к ингибированию процессов свободнорадикального окисления при сравнении с кетопрофеном, что подтверждалось снижением максимальной интенсивности свечения и светосуммы биохемилюминесценции, а также ингибированием синтеза продуктов перекисного окисления липидов и активацией антиоксидантного ферментного потенциала. Соединение 1 по уровню ингибирования процессов свободнорадикального окисления и стимулированию антиоксидантной активности при его системном применении было сопоставимо с мексидолом, но при сочетании с местным применением его гелевой композиции значительно его превосходило.
Пример 7. Противовоспалительная активность соединения 1 и ФК на модели экспериментального пародонтита
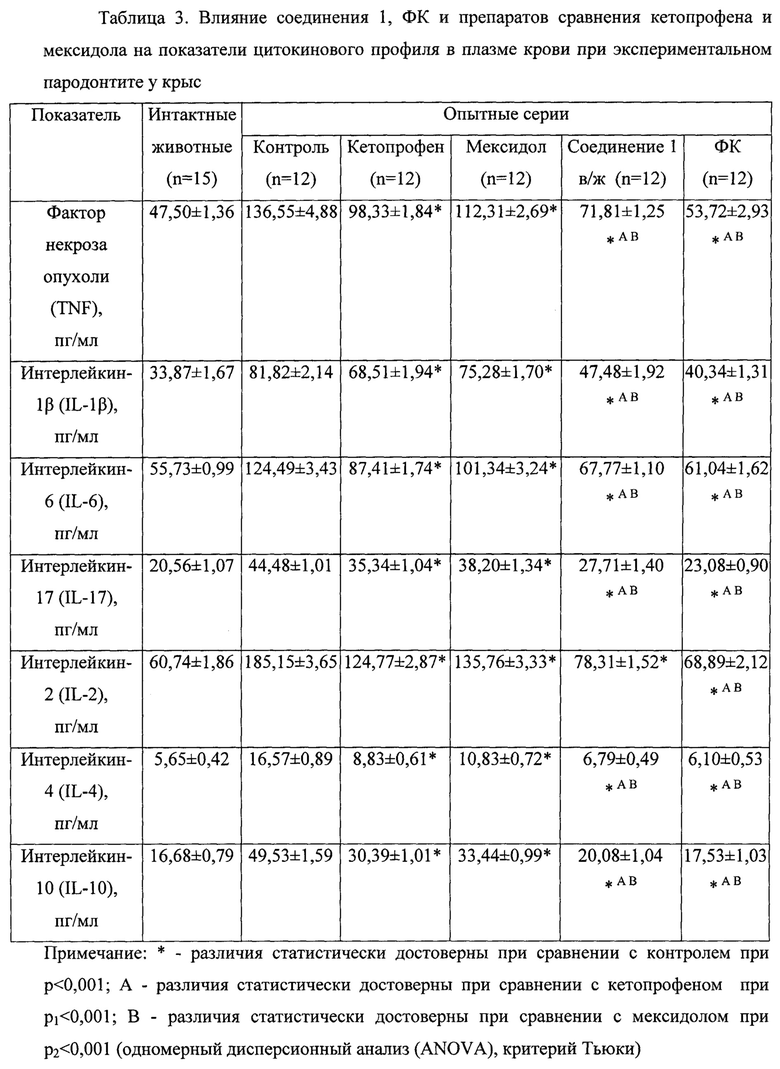
Исследование системного воспаления проводилось у белых нелинейных крыс по уровню про- и противовоспалительных цитокинов в плазме крови иммуноферментным методом с применением стандартного набора реактивов Bender Medsystems. Результаты исследования показателей цитокинового профиля у животных с экспериментальным пародонтитом при применении соединения 1 и ФК приведены в таблице 3.
При сравнении внутрижелудочного введения соединения 1 с сериями применения кетопрофена и мексидола значительно эффективнее нивелировался дисбаланс цитокинов, а именно: содержание фактора некроза опухоли (TNF) - на 55,8% (p1<0,001) и 85,2% (р2<0,001) соответственно, интерлейкина-1β (IL-1β) - на 62,1% (p1<0,001) и 82,1% (р2<0,001), интерлейкина-6 (IL-6) - на 35,2% (p1<0,001) и 60,2% (р2<0,001), интерлейкина-17 (IL-17) - на 37,1% (p1<0,001) и 51% (р2<0,001), интерлейкина-2 (IL-2) - на 76,5% (p1<0,001) и 94,6% (p2<0,001), интерлейкина-4 (IL-4) - на 36,1% (p1<0,001) и 71,5% (р2<0,001), интерлейкина-10 (IL-10) - на 61,8% (р1<0,001) и 80,1% (р2<0,001).
ФК показала себя наиболее эффективно и при сравнении с сериями введения кетопрофена и мексидола, показатели цитокинемии были снижены: TNF - на 93,9% (p1<0,001) и 123,3% (р2<0,001) соответственно, IL-1β - на 83,2% (p1<0,001) и 103,2% (р2<0,001), IL-6 - на 47,3% (p1<0,001) и 72,3% (р2<0,001), IL-17- на 59,6% (p1<0,001) и 73,5% (p2<0,001), IL-2 - на 92% (p1<0,001) и 110,1% (р2<0,001), IL-4 - на 48,3% (p1<0,001) и 83,7% (р2<0,001), IL-10 - на 77,1% (p1<0,001)5) и 95,4% (р2<0,001).
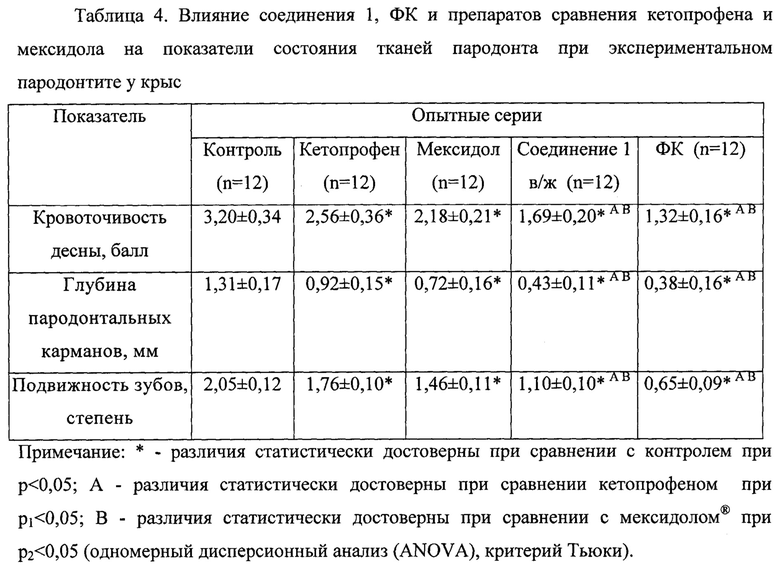
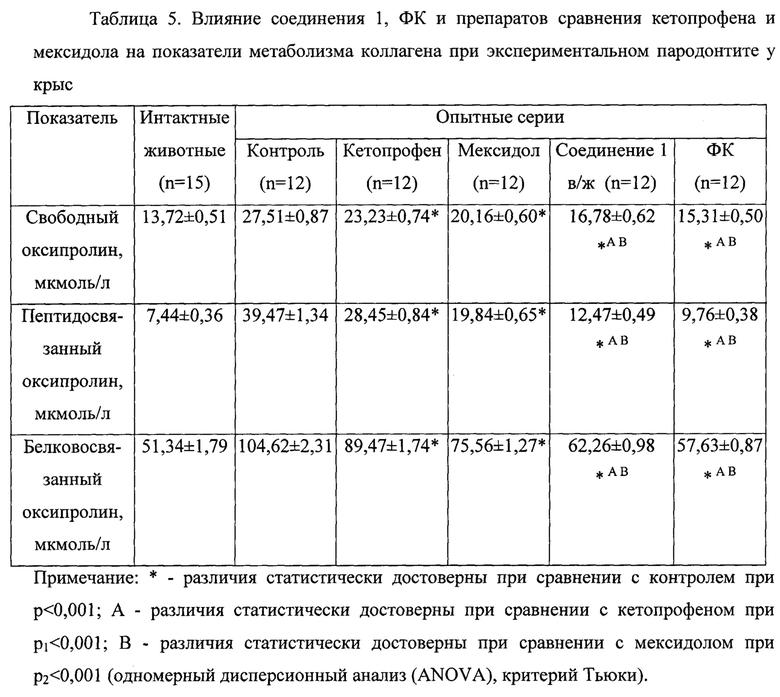
Курсовое внутрижелудочное введение соединения 1 и местное аппликативное применение ФК способствовали ингибированию местных признаков воспаления десны, что проявлялось купированием гнойной экссудации, уменьшением отека и гиперемии, кровоточивости десны, глубины пародонтальных карманов и подвижности зубов относительно серии животных контроля и получавших мексидол или кетопрофен. Результаты представлены в таблице 4 и на фиг. 1-4.
Таким образом, в отличие от кетопрофена и мексидола, соединение 1 и ФК на его основе отличаются большим противовоспалительным потенциалом, и позволяет ингибировать на модели экспериментального пародонтита воспалительную реакцию как на системном, так и на местном уровне.
Пример 8. Влияние соединения 1 и ФК на нарушение метаболизма коллагена, ингибирование деструктивных процессов и стимулирование пролиферативного потенциала тканей пародонта на модели экспериментального пародонтита.
Результаты исследования показателей метаболизма коллагена у животных с экспериментальным пародонтитом при применении соединения 1 и ФК приведены в таблице 5.
При сравнении серии внутрижелудочного введения соединения 1 с сериями применения кетопрофена и мексидола прослеживалось восстановление нарушений метаболизма коллагена, что подтверждалось ингибированием уровня маркера деструкции коллагена - свободного оксипролина (СО) на 47% (р1<0,001) и 24,6% (р2<0,001) соответственно. Наряду с этим происходило снижение белковосвязанного (БСО) и пептидносвязанного (ПСО) оксипролина: ПСО - на 214,8% (р1<0,001) и 99,1% (р2<0,001), БСО - на 53% (р1<0,001) и 25,9% (p2<0,001) соответственно.
ФК при местном аппликативном применении в сравнении с сериями введения кетопрофена и мексидола показала себя наиболее эффективно, что подтверждалось показателями: СО был снижен на 57,7% (p1<0,001) и 35,3% (р2<0,001) соответственно, ПСО - на 251,2% (p1<0,001) и 135,5% (р2<0,001), БСО - на 62% (p1<0,001) и 34,9% (p2<0,001) соответственно, превалируя над сериями с кетопрофеном и мексидолом. Снижение уровней показателей метаболизма коллагена указывает на ограничение избыточной пролиферации коллагеновых волокон грануляций в области десневых карманов и ингибировании процессов фиброзной дегенерации воспаленных тканей пародонта.
Пример 9. Морфологическая оценка состояния тканей пародонта на фоне применения соединения 1
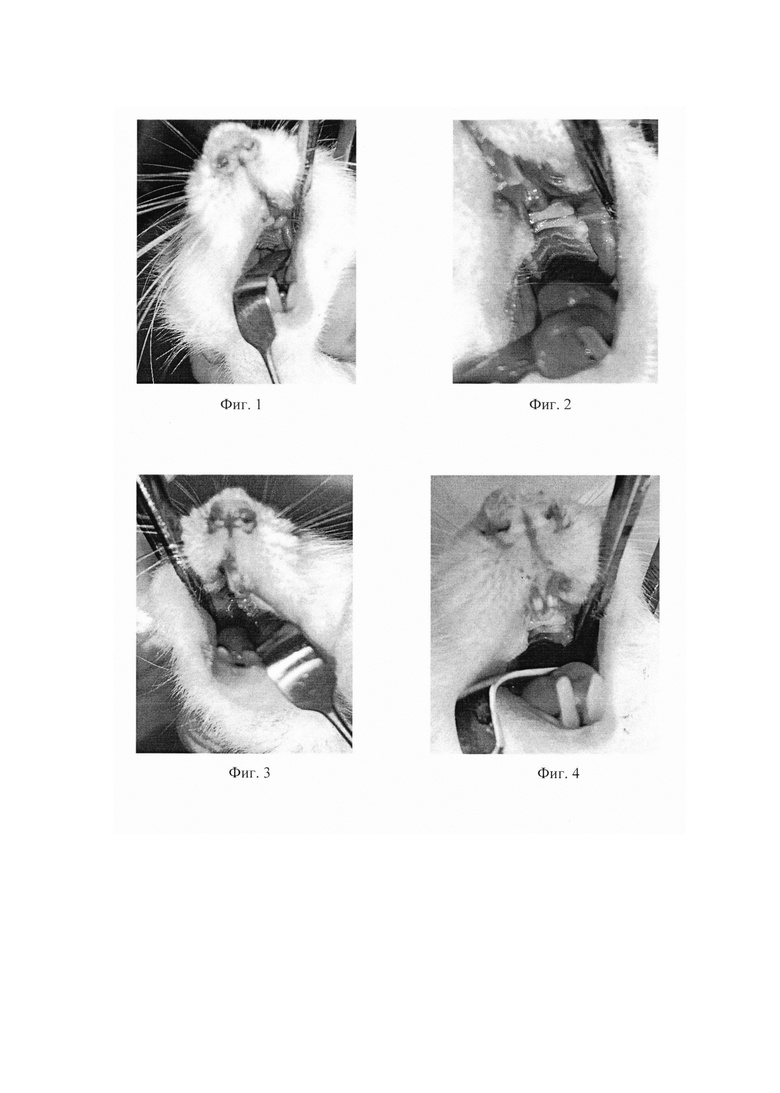
Гистологическое исследование тканей пародонта контрольной серии (фиг. 5, 6) выявило признаки хронического воспалительного процесса. В мягких тканях десны наблюдается замещение собственной пластинки слизистой оболочки незрелой грануляционной тканью, сопровождающееся обилием новообразованных мелких полнокровных сосудов с явлениями тромбоза. Определялась лейкоцитарная инфильтрация и нарушение линии базальной мембраны эпителия с внедрением коллагеновых волокон непосредственно в многослойный плоский неороговевающий эпителий. Периодонтальная щель расширена. Выявляется разволокнение периодонтальной связки с умеренной экссудацией и лейкоцитарной инфильтрацией, вследствие чего волокна выглядят «набухшими». Определяются зоны разволокнения с образованием разнонаправленных волокон с явлениями фиброзной дегенерацией пародонта. Об активной резорбции свидетельствует неровность альвеолярного края периодонтальной щели и наличие лакун резорбции цемента. В альвеолярной кости визуализируются множественные лакуны резорбции костной ткани с клеточной инфильтрацией преимущественно гистиоцитами и остеокластоподобными клетками.
На фоне терапии кетопрофеном при морфологическом исследовании тканей пародонта (фиг. 7, 8) определяются признаки хронического воспалительного процесса в виде умеренной клеточной инфильтрации из лейкоцитов и плазматических клеток. В собственной пластинке слизистой оболочки визуализировались явления склерозирования с внедрением коллагеновых волокон сквозь базальную мембрану многослойного плоского неороговевающего эпителия и формированием зон фиброзных разрастаний. Определялось умеренное расширение периодонтальной щели, участки разволокнения периодонтальной связки с явлениями лейкоцитарной инфильтрации. На фоне персистирующих ограниченных экссудативных очагов в тканях пародонта наблюдались очаги зрелой грануляционной ткани и неравномерного фиброза. Нарушения микроциркуляции характеризовались умеренной плотностью полнокровных сосудов, периваскулярной лимфоцитарной инфильтрацией, наличием явлений тромбоза отдельных сосудов. В альвеолярной кости наблюдались лакуны резорбции с инфильтрацией тканевыми макрофагами.
После курса внутрижелудочного введения соединения 1 и аппликативного применения ФК (фиг. 9, 10) на его основе слизистая оболочка десны выполнена многослойным плоским эпителием, покрывающим собственную пластинку, представленную правильно ориентированными пучками коллагеновых волокон и фиброцитами. В тканях пародонта регистрировались лишь единичные полнокровные сосуды. Экссудация была представлена в виде ограниченных очагов в области периодонта.
В неизмененной периодонтальной щели расположены коллагеновые волокна периодонтальной связки, с сосудами и клеточными элементами в виде гистиоцитов и фибробластов. Периодонтальная связка плотно прикреплена к альвеолярной кости, которая имеет нормальную структуру, без процессов резорбции. Однако у единичных особей выявлялись лакуны резорбции и увеличение внутрикостных каналов. Зубная пульпа имела правильную архитектонику, в отдельных наблюдениях отмечалось избыточное кровенаполнение сосудов, с явлениями стаза.
Пример 10. Оценка ульцерогенного действия соединения 1
На фоне курсового применения кетопрофена общее количество язв составило 14,75±2,07, их площадь достигала 23,38±2,75 мм2. Частота развития желудочных кровотечений составила 75%. Появляется летальность в данной подопытной группе, погибла 1 крыса - 8,3%. Количество глубоких язв достигало 11,63±1,84, а площадь - до 18,25±2,62 мм2.
Внутрижелудочное введение кетопрофена (фиг. 11) оказывало ульцерогенное действие на слизистую оболочку кишечника с формированием язвенных дефектов различной глубины. Преимущественно язвообразование происходило по всей длине тонкой кишки и в проксимальном отделе толстой кишки. Язвы имели воспалительный характер: розово-красного цвета, с приподнятыми подрытыми краями, на дне и по краям язвы определялись множественные инъецированные сосуды, детрит в дне язвенного дефекта буро-коричневого цвета легко удалялся шпателем. Обнаруживались также язвы линейной формы, располагающиеся циркулярно и приводящие к деформации стенки и сужению просвета кишки. Язвы имели размеры от 1×1 до 3×8 мм, количество язв от 2 до 8 на 1 см2. Площадь язвенной поверхности в тонкой кишке занимала 274,0±32,63 мм2, количество составило 72,25±6,77, в толстой кишке среднее число язв, приходящееся на 1 животное - 23,0±2,40, площадь - 58,13±5,03 мм2. У 12,5% животных в толстой кишке зарегистрированы циркулярно расположенные линейные язвы, приводящие к сужению просвета кишки.
Курс внутрижелудочного введения мексидола, а также внутрижелудочное введение соединения 1 и ФК (фиг. 13), не оказывало ульцерогенного действия на слизистую оболочку желудка и кишечника на всем его протяжении. Слизистая оболочка желудка при вскрытии его просвета бледно-розового цвета, блестящая, гладкая, с эластичными складками, присутствует прозрачная слизь.
Таким образом, предлагаемое соединение 1 и фармацевтическая композиция в виде геля на его основе обладают выраженными антиоксидантными, противовоспалительными и антиульцерогенными свойствами, стимулируют репаративные процессы тканей пародонта, ингибируют деструктивные процессы тканей пародонтального комплекса, что позволяет их применять в качестве эффективных патогенетических средств при воспалительных заболеваниях пародонта.


Краткое описание чертежей
Фиг. 1. Контрольная серия. Отек, гиперемия десны, обильный гнойный экссудат из пародонтального кармана.
Фиг. 2. Кетопрофен. Отек гиперемия десны, повышенная кровоточивость тканей пародонта после зондирования.
Фиг. 3. Мексидол. Незначительный отек, гиперемия, неглубокие пародонтальные карманы до 0,72, нет кровоточивости после зондирования.
Фиг. 4. ФК. Десна бледно-розового цвета, наличие десневой бороздки, кровоточивости после зондирования не определяется, экссудация отсутствует.
Фиг. 5. Контрольная серия животных. А - расширение периодонтальной щели; Б - множественные лакуны резорбции, подвергшиеся фиброзной дегенерацией; В - полнокровные сосуды. Окраска гематоксилином и эозином, × 100.
Фиг. 6. Контрольная серия животных. А - остеокласт в полости резорбции. Окраска гематоксилином и эозином, × 400.
Фиг. 7. Кетопрофен. А - очаговое разрастание фиброзной ткани; А - расширение периодонтальной щели; Б - множественные лакуны резорбции; В - полнокровные сосуды с явлениями тромбоза. Окраска гематоксилином и эозином, × 100.
Фиг. 8. Кетопрофен. А - очаговое разрастание фиброзной ткани сквозь базальную мембрану многослойного плоского неороговевающего эпителия. Окраска гематоксилином и эозином, × 400.
Фиг. 9. Соединение 1 внутрижелудочно+аппликация геля. А - периодонтальная щель; Б - альвеолярная костная ткань; В - цемент корня зуба. Окраска гематоксилином и эозином, × 100.
Фиг. 10. ФК. А - периодонтальная связка с упорядоченно расположенными коллагеновыми волокнами; Б - неизменная структура альвеолярной костной ткани. Окраска гематоксилином и эозином, × 400.
Фиг. 11. Кетопрофен. Желудок белой нелинейной крысы. Множественные язвы с кровотечением.
Фиг. 12. Тонкая кишка белой нелинейной крысы. Контрольная группа (индометацин 5 мг/кг внутрижелудочно 5 дней). Истончение и язвенные дефекты на слизистой оболочке кишки.
Фиг. 13. Соединение 1. Желудок белой нелинейной крысы. Нормальная слизистая оболочка желудка.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, обладающее противовоспалительным, антиоксидантным и антиульцерогенным действием, способностью ингибировать развитие дегенеративно-деструктивных процессов тканей, представляющее собой 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноат | 2023 |
|
RU2814495C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2750418C1 |
| СРЕДСТВО С ПАНКРЕО- И ГЕПАТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ ДЛЯ ПАРЕНТЕРАЛЬНОГО ВВЕДЕНИЯ | 2017 |
|
RU2662324C1 |
| Способ коррекции бактериального гнойного менингита с помощью 2-этил-6-метил-3-гидроксипиридиния 2,6-дихлорфенил(амино)фенилэтаноата в условиях эксперимента | 2019 |
|
RU2724883C1 |
| Новое производное 3-гидроксипиридина, обладающее липидрегулирующей активностью | 2020 |
|
RU2743923C1 |
| L-Энантиомер 2-этил-6-метил-3-гидроксипиридиния гидроксибутандиоата, обладающий церебропротекторной активностью | 2017 |
|
RU2663836C1 |
| Комплексные соли ацексамовой кислоты, стимулирующие регенерацию костной ткани, ускоряющие процессы репаративного остеогенеза, стимулирующие минерализацию костной ткани при остеопорозе | 2018 |
|
RU2668966C1 |
| НЕЙРОТРОПНОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ, АНТИАМНЕСТИЧЕСКОЙ И ВЕСТИБУЛОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2547728C1 |
| Производные 5-этил-2-амино-1, 3, 4-тиадиазола, обладающие обезболивающей, противовоспалительной, противоаллергической и анальгетической активностями | 2016 |
|
RU2651572C2 |
| Способ коррекции остеопороза и остеопоротических переломов 2-этил-6-метил-3-гидроксипиридинийгидроксибутандиоатом в эксперименте | 2021 |
|
RU2775439C1 |



Группа изобретений относится к новому лекарственному средству, пригодному для лечения воспалительных заболеваний пародонта, и фармацевтической композиции на его основе. Предлагаемое средство представляет собой 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноат. Предлагается также фармацевтическая композиция для лечения воспалительных заболеваний пародонта в виде геля, которая содержит указанное выше лекарственное средство, растворенное в спиртах - этиловом спирте и пропиленгликоле, и гидрофильную основу из производного целлюлозы и воды. Предлагаемые средство и композиция обладают выраженными антиоксидантными и противовоспалительными свойствами, стимулируют репаративные процессы тканей пародонта, ингибируют деструктивные процессы тканей пародонтального комплекса, что позволяет их применять в качестве эффективных патогенетических средств при воспалительных заболеваниях пародонта. 2 н. и 2 з.п. ф-лы, 13 ил., 5 табл., 10 пр.
1. Средство, обладающее стимулирующим репаративные процессы тканей пародонта, антиоксидантным и противовоспалительным действием, представляющее собой 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноат.
2. Фармацевтическая композиция для лечения воспалительных заболеваний пародонта в виде геля, содержащая лекарственное средство по п. 1, растворенное в спиртах - этиловом спирте и пропиленгликоле, и гидрофильную основу из производного целлюлозы и воды.
3. Фармацевтическая композиция по п. 2, содержащая в качестве производного целлюлозы гидроксипропилцеллюлозу.
4. Фармацевтическая композиция по п. 3, для получения которой использованы: 5 г 2-этил-6-метил-3-гидроксипиридиния-2-(3-бензоилфенил)-пропаноата, 18,8 г этилового спирта, 4 г пропиленгликоля, 80,7 г 7% водного раствора гидроксипропилцеллюлозы.
| ВНУТРИПОРШНЕВАЯ КАМЕРА СЖАТИЯ ДЛЯ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО ГОРЕНИЯ | 1936 |
|
SU52396A1 |
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО | 2003 |
|
RU2259816C1 |
| Способ лечения воспалительных заболеваний пародонта у женщин в мено- и постменопаузальном периодах | 2021 |
|
RU2763874C1 |
| US 5032384 A, 16.07.1991 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2023-04-04—Публикация
2022-03-31—Подача