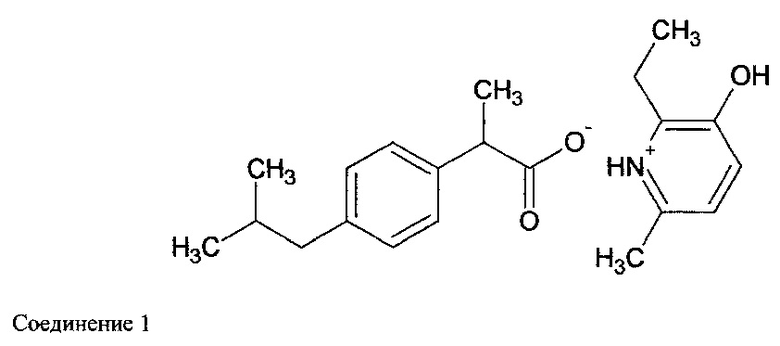
Изобретение относится к области медицины и фармации, конкретно к синтезу 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноата, обладающего противовоспалительным, антиоксидантным и антиульцерогенным действием, способностью ингибировать развитие дегенеративно-деструктивных процессов тканей, пригодного для лечения воспалительно-дегенеративных заболеваний суставов:
Уровень техники
В настоящее время, несмотря на многообразие применяемых способов лечения, остеоартрозом крупных суставов страдает от 42 до 71% населения России трудоспособного возраста, при этом от 65 до 81% случаев заболевание носит посттравматический характер, в связи с чем оно приобретает высокую социально-экономическую значимость. Ассоциация заболеваний суставов с поражением желудочно-кишечного тракта чрезвычайно распространена и обусловлена широким применением нестероидных противовоспалительных средств (НПВС). Данный побочный эффект способствует снижению качества жизни пациентов, а также обуславливает необходимость фармакологической коррекции возникшей патологии, что влечет за собой значительные финансовые потери.
Основными лекарственными средствами, входящими в стандарт лечения остеоартроза, являются НПВС, применяемые в режиме непрерывного использования (https://cr.minzdrav.gov.ru/schema/667_1).
Известен способ лечения остеоартроза с применением нимесулида 200 мг/сут (Сизова Л.В. Влияние различных методов лечения на показатели качества жизни больных остеоартрозом / Диссертация на соискание ученой степени к.м.н., - Оренбург, 2004). За счет селективного ингибирования циклооксигеназы-2 (ЦОГ-2) препарат оказывает противовоспалительное действие, а также характеризуется меньшей частотой возникновения эрозивно-язвенных повреждений ЖКТ. Однако при длительном применении способен оказывать гепатотоксическое действие, заключающееся в повышение аспартатаминотрансферазы крови, что послужило причиной отказа от его применения в ряде европейских стран.
Существует способ лечения остеоартроза, заключающийся в пероральном приеме комбинированного средства на основе диацереина, хондроитина и глюкозамина (патент RU 2742172 С2, 2021 г.). Препарат оказывает противовоспалительное действие за счет ингибирования синтеза интерлейкина-1 и обладает хондропротекторной активностью. Несмотря на низкую частоту возникновения НПВС-гастропатии, диацерин, входящий в состав препарата, нередко приводит к развитию диареи, а также в некоторых случаях способен индуцировать развитие гепатотоксических реакций.
Известен метод терапии остеоартроза, основанный на пероральном приеме пролонгированной формы диклофенака в дозе 100 мг/сут (Норина С.В. Диагностика и эффективность лечения остеоартроза коленного сустава на поликлиническом уровне / Диссертация на соискание ученой степени к.м.н., - Хабаровск, 2007). Отмечается выраженное противовоспалительное действие, проявляющееся уменьшением отечности и болевого синдрома.
Как известно, ибупрофен относится к группе производных пропионовой кислоты. Его терапевтический эффект реализуется за счет неселективного ингибирования продукции циклооксигеназы (ЦОГ) с последующим снижением синтеза провоспалительньгх простагландинов, что объясняет наличие у него анальгезирующего, жаропонижающего, противовоспалительного и противоотечного действий.
Известен способ патогенетического лечения остеоартроза, суть которого заключается в пероральном приеме ибупрофена (Дмитриев В.А. Сравнительная характеристика фармакокинетики, клинической эффективности и безопасности генерических препаратов Диклофенака и Ибупрофена / Диссертация на соискание ученой степени к.м.н., - М., 2008). Недостатком данной терапии является высокая частота формирования эрозивно-язвенных поражений слизистой оболочки желудочно-кишечного тракта при длительном приеме в средних терапевтических дозах, отсутствие репаративной стимуляции поврежденных тканей сустава.
Известен способ применения ибупрофена в составе фармацевтической композиции для перорального приема, которая включает в себя соль хондроитина сульфата и глюкозамина сульфата, ибупрофен и вспомогательные вещества: разрыхлители, глиданты, материал для капсул и красители в следующем соотношении компонентов (мас./мас. %):
(Патент ЕА №019542 В1,2014 г.)
Данная фармацевтическая композиция обладает противовоспалительным, обезболивающим и хондропротекторным действием. Недостатками данного препарата являются возможность развития побочных эффектов в виде эрозивно-язвенных повреждений слизистой оболочки желудочно-кишечного тракта, манифестирующих желудочно-кишечным кровотечением. Кроме того, для достижения хондропротекторного эффекта необходимо длительное применение препарата, что может способствовать снижению приверженности пациентов к лечению и реализации ульцерогенного эффекта ибупрофена.
В последние годы отмечается широкое включение в терапию остеоартроза лекарственных препаратов, обладающих антиоксидантной активностью.
Имеются данные, свидетельствующие о положительном эффекте включения в комбинированную терапию остеоартроза витамина С (Кцоева А.А. Влияние комплексного лечения с использованием витамина С на функцию хондроцитов при остеоартрозе коленного сустава / Диссертация на соискание ученой степени к.м.н., - Владикавказ, 2014).
Известно пероральное применение тиоктовой кислоты при заболеваниях суставов, оказывающей противовоспалительное и антиоксидантное действие (Иманаева А.Я. Изучение влияния тиоктовой кислоты на течение адъювантного артрита / Диссертация на соискание ученой степени к.м.н., - Казань, 2013).
Имеется способ комбинированного лечения остеоартроза со включением в комплекс терапии аевита - препарата, содержащего альфа-токоферола ацетат (витамин Е) и ретинола пальмитат (витамин А), которые обладают антиоксидантным действием (Комарова С.А. Эффективность комплексного лечения с применением системной энзимотерапии у женщин с первичным остеоартрозом / Диссертация на соискание ученой степени к.м.н., - Уфа, 2010).
Существует метод комплексной терапии остеоартроза с использованием милдроната (Стовичек О.А. Использование Милдроната в комплексной терапии остеоартроза и его комбинации с гипертонической болезнью / Диссертация на соискание ученой степени к.м.н., - Ярославль, 2007). Комбинированная терапия больных остеоартрозом с включением милдроната в сравнении с традиционным лечением НПВС оказывала более выраженное влияние на процессы свободнорадикального окисления липидов и деградации коллагена.
Известен способ профилактики посттравматического артроза коленного сустава, сущность которого заключается во внутрисуставном введении этоксидола в дозе 5 мг/кг в количестве 5 инъекций (патент РФ 2516951 С1, 2013 г.). Результатом применения данного метода является угнетение процессов липопероксидации, повышение активности антиоксидантной системы, стимуляция репаративных процессов поврежденных суставных тканей.
Недостаток вышеперечисленных методов выражается в отсутствии выраженного ингибирования активности ЦОГ и, как следствие, низком противовоспалительном и обезболивающем эффектах.
2-Этил-6-метил-3-гидроксипиридина сукцинат (лекарственный препарат мексидол) обладает выраженным антиоксидантным действием за счет ингибирования процессов перекисного окисления липидов (ПОЛ) путем активного реагирования с первичными и гидроксильными радикалами пептидов, а также способствует повышению активности ферментов антиоксидантной системы, в частности супероксиддисмутазы и глутатионпероксидазы, отвечающих за нейтрализацию образовавшихся активных форм кислорода. Антигипоксантный эффект реализуется за счет содержания сукцината и его специфического влияния на энергетический обмен путем активации энергосинтезирующих функций митохондрий, увеличения содержания АТФ и креатинфосфата в условиях гипоксии, а также стабилизации сосудистой стенки вследствие снижения образования эндогенных пероксидов и реализации его мембранопротективного действия (https://mexidol.ru/extra/File/Mexidol.pdf).
Обосновано гепатопротекторное (патент РФ №2189817), антибактериальное (патент РФ №2157686), ноотропное и анксиолитическое (патент РФ №2065299) действие мексидола.
Имеются данные, свидетельствующие о высокой эффективности применения мексидола в условиях травматического повреждения суставного хряща (Попова О.А. Особенности посттравматической регенерации суставного хряща при использовании водорастворимых антиоксидантов различных классов / Диссертация на соискание ученой степени к.м.н. - Саранск, 2013). Отмечалось достоверное снижение активности процессов ПОЛ, а также некоторое хондропротективное действие, реализующееся посредством стимуляции репаративных процессов.
Известен способ лечения остеоартроза, заключающийся во внутрисуставном введении мексидола в дозе 5 мг/кг (Шутова М.И. Некоторые аспекты патогенеза метаболических нарушений и возможности их коррекции при травматических повреждениях коленного сустава в эксперименте / Диссертация на соискание ученой степени к.м.н. - Саранск, 2014). Определялось угнетения образования первичных и вторичных продуктов ПОЛ с одновременным повышением нейтрализующей активности антиоксидантной системы.
Однако, у препаратов с антиоксидантным типом действия, несмотря на выраженное угнетение свободнорадикальных процессов, отмечается слабый противовоспалительный и обезболивающий эффекты.
Таким образом, для создания лекарственного препарата, обладающего способностью ингибировать воспалительные и дегенеративно-деструктивные процессы в хряще и синовиальной оболочке, стимулировать репаративные процессы в поврежденных тканях суставов, а также оказывающего антиоксдидантное, цитопротекторное и антиульцерогенное действие целесообразен синтез и оценка эффективности нового соединения 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноата.
Раскрытие изобретения
Целью изобретения является синтез соединения - обладающего противовоспалительным, антиоксидантным и антиульцерогенным действием, способностью ингибировать развитие дегенеративно-деструктивных процессов тканей, пригодного для лечения воспалительно-дегенеративных заболеваний суставов.
Достижение поставленной цели осуществляется путем синтеза нового соединения 1 -2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноата.
Технический результат заключается в синтезировании нового соединения, а также исследовании его биологической и фармакологической активности.
Синтез нового соединения 1 осуществляли путем взаимодействия эквимолярных количеств 2-этил-6-метил-3-гидроксипиридина и 4-изобутилфенилпропановой кислоты.
Пример 1. Синтез 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноата
В трехгорлую колбу, снабженную мешалкой, обратным холодильником и термометром, загружают 50 мл абсолютированного этилового спирта. При перемешивании постепенно добавляют 4,13 г (0,020 гм) 4-изобутилфенилпропановой кислоты, после растворения добавляют 2,74 г (0,020 гм) 2-этил-6-метил-3-гидроксипиридина. Полученный раствор нагревают до 40°С, перемешивают до полного растворения, фильтруют, от фильтрата отгоняют растворитель под вакуумом. Тщательно сушат. Получают 5,90 г белого со слегка желтоватым оттенком гигроскопичного порошка с Т плав.=103-105°С.
Найдено, %: С 73,41; Н 8,54; N 4,07; C21H29NO3 м.м. 343,46
Вычислено, %: С 73,44; Н 8,51; N 4,08; О 13,97
ИК, v, см-1: 3421 (ОН); 2981,2917,2810 (СН); 2358 (N+); 1640 (ОС), 1578 (ON). рН 0,5% раствора в воде: 6,7;
ТСХ: в системе бензол-ацетон (1:3) на Silicagel УФ 254 в зоне адсорбции одно пятно.
Пример 2. Синтез 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноата
В гомогенизатор загружают 4,13 г (0,020 гм) 4-изобутилфенилпропановой кислоты и 2,74 г (0,020 гм) 2-этил-6-метил-3-гидроксипиридина, массу тщательно перемешивают, и в течение 2 часов гомогенизируют с частотой вращения 300-400 об./мин. Массу выгружают, отбирают пробу для определения растворимости в воде и размера частиц (не более 50 мкм). Получают 6,13 г почти белого кристаллического гигроскопичного порошка с Т плав.=103-105°С.
Найдено, %: С 73,42; Н 8,53; N 4,06; C21H29NO3 м.м. 343,46
Вычислено, %: С 73,44; Н 8,51; N 4,08; О 13,97
Ж, v, см-1: 3421 (ОН); 2981,2917, 2810 (СН); 2358 (N+); 1640 (ОС), 1578 (ON). рН 0,5% раствора в воде: 6,7;
ТСХ: в системе бензол-ацетон (1:3) на Silicagel УФ 254 в зоне адсорбции одно пятно.
Биологические и фармакологические исследования соединения 1 Исследования проводились в соответствии с этическими нормами, применяемыми при работе с лабораторными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР №755 от 12.08.1987 г. ), Федеральный закон «О защите животных от жестокого обращения» от 01.01.1997 г., «Об утверждении Правил надлежащей лабораторной практики» (приказ МЗ РФ №199н от 01.04.2016 г. )) и были одобрены локальным этическим комитетом.
Гистологические исследования выполнялись с использованием биологического микроскопа «HUMASCOPE ADVANCED LED», Германия. Микрофотографии были сделаны с помощью цифровой фотокамеры Human GmbH (USB) 8,0 Мпикс, Германия.
Пример 3. Биологическая активность соединения 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноата
Острая токсичность соединения 1, ибупрофена и мексидола.
Оценка острой токсичности соединения 1 произведена в опытах на белых беспородных мышах (195 особей обоего пола массой 26-30 г), полученных из биопитомника «СМК СТЕЗАР», при внутрижелудочном введении соединения 1 и препаратов сравнения в крахмальной слизи в объеме 0,3-0,5 мл.
Расчет показателя ЛД50 проводился с использованием метода Личфилда-Уилкоксона (кн. Е.В. Арзамасцев, И.В. Березовская, О.В. Верстакова и др. Методические рекомендации по изучению общетоксического действия лекарственных средств / Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - С. 25-35; Гуськова Т.А. Токсикология лекарственных средств. - М: Издательский дом "Русский врач". - 2003. - С.20-24.).
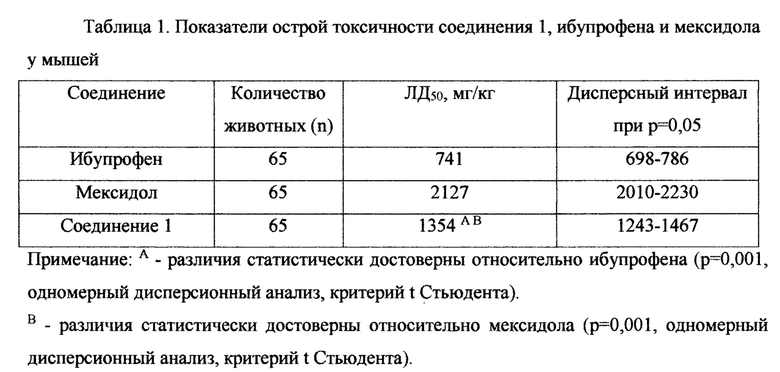
Результаты исследования острой токсичности соединения 1 и отдельных фрагментов заявляемой молекулы, приведены в таблице 1.
Полученные данные указывают, что соединение 1 в 1,83 раза менее токсично ибупрофена, но в 1,57 токсичнее мексидола при их внутрижелудочном введении.
Пример 4. Модель для изучения фармакологической активности соединения 1 Фармакологическая активность соединения 1 изучена в опытах при посттравматическом артрите после моделирования повреждения коленного сустава на белых нелинейных крысах (75 особей обоего пола массой 190-220 г, полученных из биопитомника «СМК СТЕЗАР»). Модель повреждения коленного сустава воспроизводилась механическим способом в модификации Г.М. Дубровина и соавторов (удостоверение на рационализаторское предложение №1628 от 21.09.2004 г. ).
Исследование фармакологической активности соединения 1 проводилось при его внутрижелудочном введении после предварительного растворения в 0,2-0,3 мл крахмальной слизи.
Продолжительность курса внутрижелудочного введения соединения 1 в дозе 11,65 мг/кг, как и препаратов сравнения - ибупрофена и мексидола в дозах 6,35 мг/кг и 45,58 мг/кг соответственно составила 15 суток с кратностью введения 1 раз в сутки.
Пример 5. Антиоксидантная активность соединения 1 при посттравматическом артрите коленного сустава в эксперименте
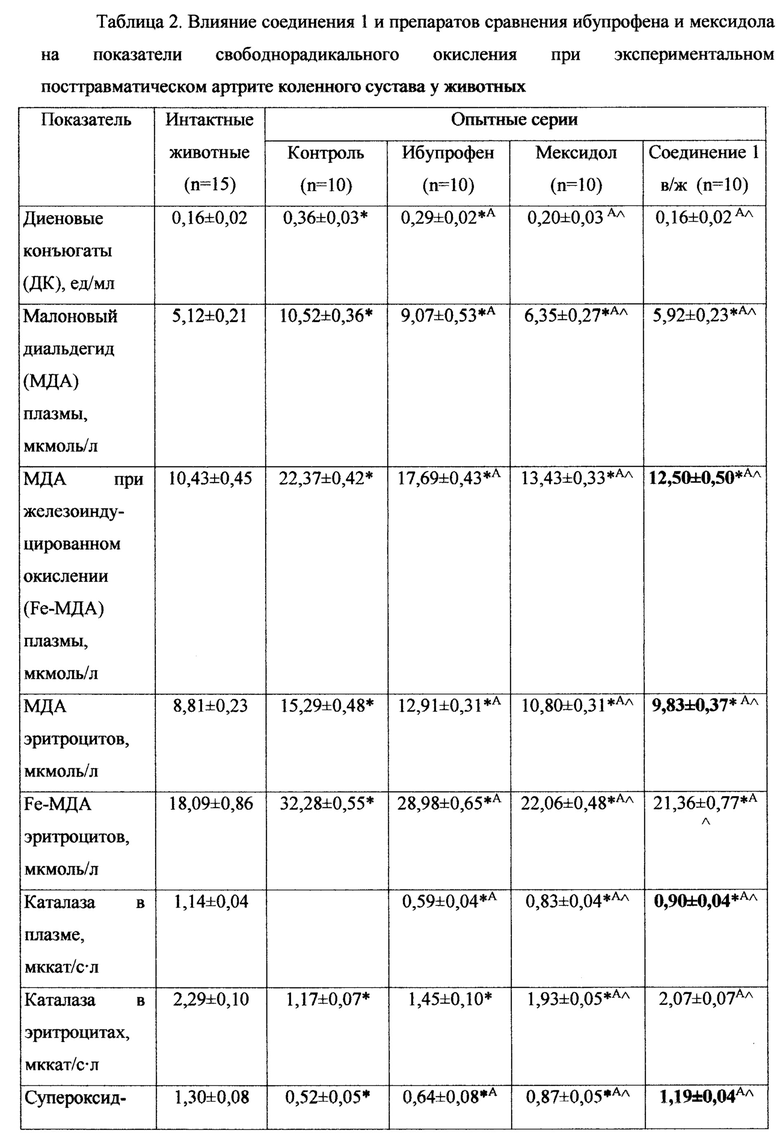
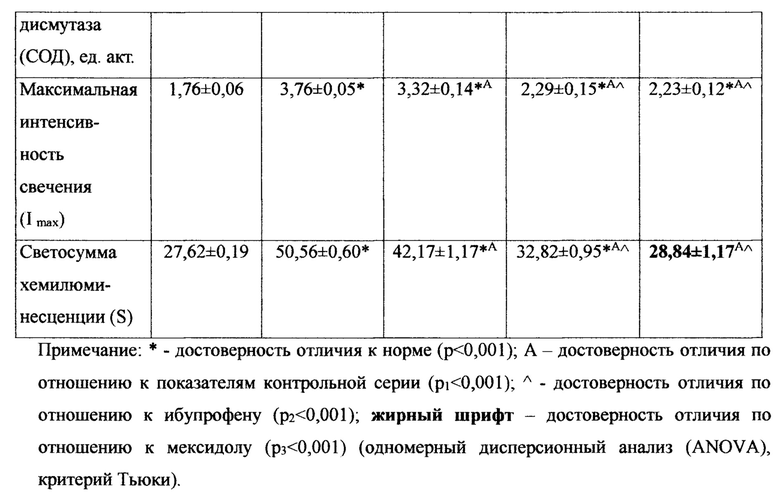
Результаты исследования влияния соединения 1 и препаратов сравнения на процессы свободнорадикального окисления у крыс при посттравматическом артрите коленного сустава приведены в таблице 2.
В ходе сравнения серии внутрижелудочного введения соединения 1 с сериями применения ибупрофена и мексидола определялось более эффективное угнетение процессов ПОЛ: диеновые конъюгаты (ДК) снижались на 36,3% (р2<0,001) и 11,2% (р3<0,001) соответственно, малоновый диальдегид (МДА) плазмы - на 29,9% (р2<0,001) и 4,1% (р3=0,030), МДА эритроцитов - на 20,1% (р2<0,001) и 6,3% (р3=0,041) соответственно, МДА при железоиндуцированном окислении (Fe-МДА) плазмы - на 23,2% (р2<0,001) и 4,1% (р3=0,031), Fe-МДА эритроцитов - на 23,6% (р2<0,001) и 2,2% (р3=0,164) соответственно. Отмечалось более быстрое восстановление ферментного антиоксидантного потенциала, что подтверждалось повышением активности каталазы в плазме в сравнении с сериями ибупрофена и мексидола на 64,6% (р2<0,001) и 14,6% (р3<0,001) соответственно, в эритроцитах - на 53% (р2<0,001) и 11,9% (р3=0,269), активность супероксидисумутазы (СОД) стимулировалась на 105,7% (р2<0,001) и 61,5% (р3<0,001) соответственно. При внутрижелудочном введении соединения 1 в сравнении с сериями ибупрофена и мексидола отмечалось более эффективное ингибирование процессов свободнорадикального окисления, что подтверждалось снижением максимальной интенсивности свечения (Imax) - на 29% (р2<0,001) и 1,6% (р3=0,816) и светосуммы хемилюминесценции (S) - на 26,4% (р2<0,001) и 7,9% (р3<0,001) соответственно.
Пример 6. Противовоспалительная активность соединения 1 при посттравматическом артрите коленного сустава в эксперименте
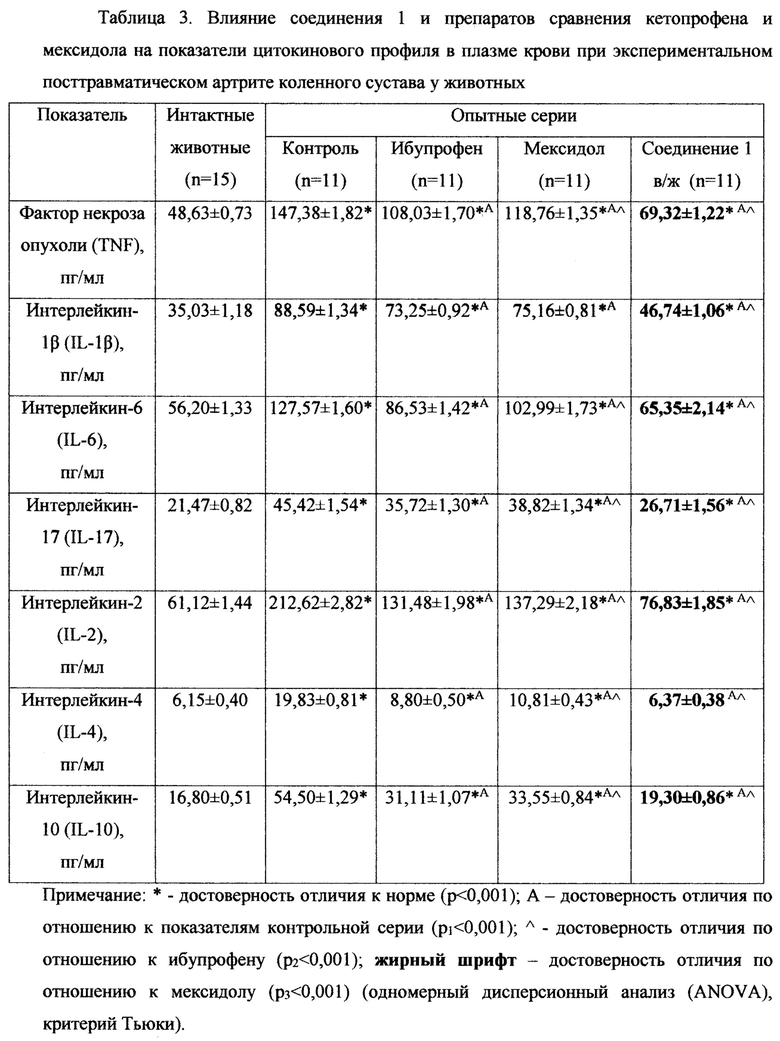
Результаты исследования противовоспалительной активности, проводимого по оценке динамики уровней провоспалительных и противовоспалительных цитокинов, при посттравматическом артрите коленного сустава у животных приведены в таблице 3.
Сравнительный анализ серии внутрижелудочного введения соединения 1 с сериями применения ибупрофена и мексидола показал более эффективное купирование воспалительного процесса, о чем свидетельствует достоверное снижение показателей цитокинового профиля: уровень фактора некроза опухоли (TNF) уменьшился на 26,3% (р2<0,001) и 33,6% (р3<0,001) соответственно, интерлейкина-1β (IL-1β) - на 29,9% (р2<0,001) и 32% (р3<0,001), интерлейкина-6 (IL-6) - на 16,6% (р2<0,001) и 29,5% (р3<0,001), интерлейкина-17 (1L-17) - на 19,8% (р2<0,001) и 26,7% (р3<0,001), интерлейкина-2 (IL-2) - на 25,7% (р2<0,001) и 28,5% (р3<0,001), интерлейкина-4 (IL-4) - на 12,4% (р2<0,001) и 22,4% (р3<0,001), интерлейкина-10 (IL-10) - на 21,7% (р2<0,001) и 26,2%(р3<0,001).
Пример 7. Влияние соединения 1 на обмен коллагена при посттравматическом артрите коленного сустава в эксперименте
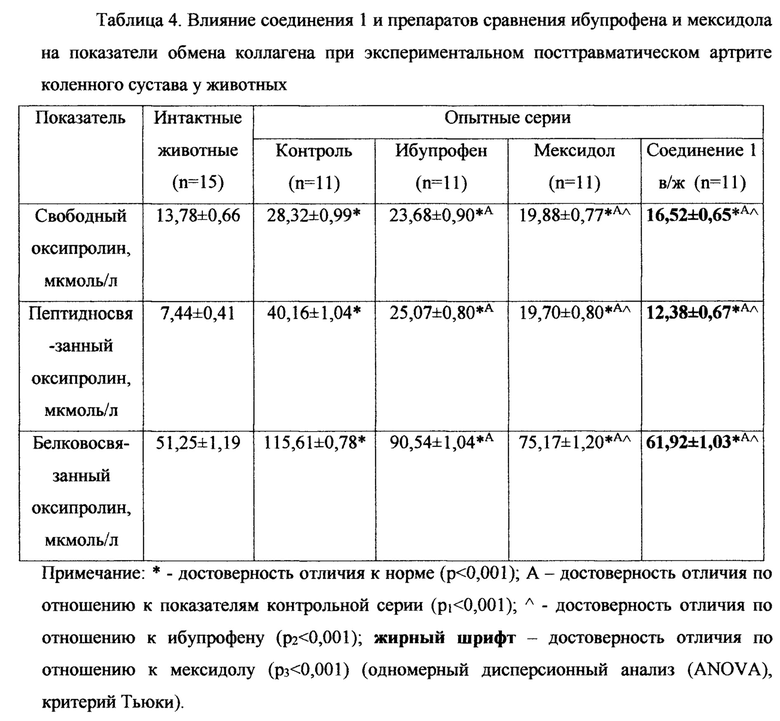
Результаты исследования динамики показателей обмена основного компонента внеклеточного матрикса суставного хряща коллагена у животных при посттравматическом артрите коленного сустава приведены в таблице 5.
В ходе проведения сравнительного анализа между сериями применения соединения 1 и внутрижелудочного введения ибупрофена и мексидола определялось нивелирование патологических изменений обмена коллагена, проявляющееся снижением уровня свободного оксипролина (СО) на 25,3% (р2<0,001) и 11,9% (р3<0,001) соответственно. Вместе с тем происходило уменьшение уровня пептидносвязанного (ПСО) оксипролина на 31,5% (р2<0,001) и 18,2% (р3<0,001) и белковосвязанного (БСО) оксипролина на 24,7% (р2<0,001) и 11,4% (р3<0,001) сравнительно с данными в сериях применения ибупрофена и мексидола соответственно.
Соединение 1 при его внутрижелудочном применении оказывало более эффективное корригирующее воздействие на метаболизм коллагена, что проявлялось уменьшением альтеративных изменений коллагеновых структур, а также нивелированием процессов фибриллогенеза и ограничением склерозирования поврежденных тканей сустава.
Пример 8. Влияние соединения 1 на клеточный состав синовии при посттравматическом артрите коленного сустава в эксперименте
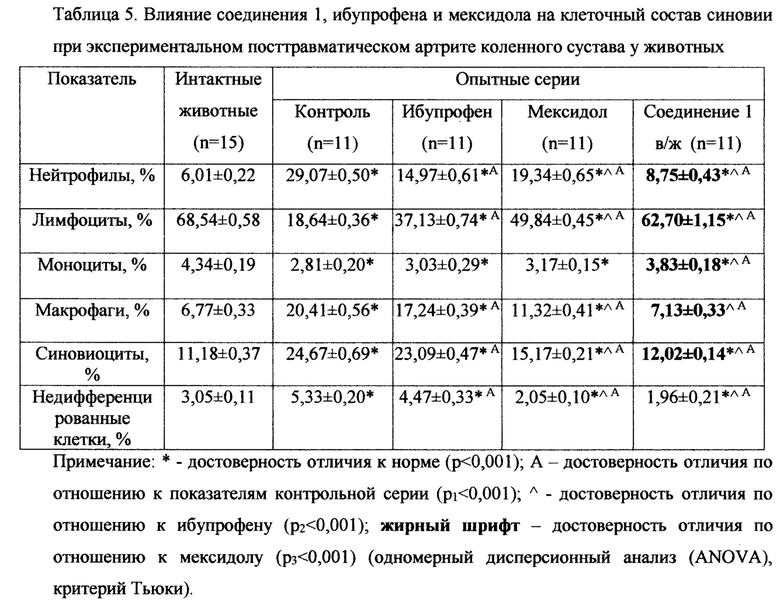
Результаты исследования клеточного состава синовии у животных при посттравматическом артрите коленного сустава приведены в таблице 5.
Внутрижелудочное введение соединения 1 оказалось наиболее эффективным в сравнении с сериями применения ибупрофена и мексидола, приводя к коррекции количественного распределения клеток синовиальной жидкости. Это подтверждалось изменением маркеров деструкции сустава - уровень нейтрофилов снижался на 21,5% (р2<0,001) и 36,5% (р3<0,001), макрофагов на 49,6% (р2<0,001) и 20,6% (р3<0,001), синовиоцитов на 44,9% (р2<0,001) и 12,8% (р3<0,001), а уровень лимфоцитов повышался на 137,2% (р2<0,001) и 69% (р3<0,001), моноцитов на 28,5% (р2<0,001) и 22,5% (р3<0,001) относительно показателей серий ибупрофена и мексидола. Данные изменения свидетельствуют о купировании воспалительного процесса и ограничении деструктивных процессов тканей сустава.
Пример 9. Морфологические изменения суставных тканей при применении соединения 1 у животных при посттравматическом артрите коленного сустава в эксперименте
При гистологическом исследовании сагиттального среза суставного хряща (фиг. 1) в перифокальной зоне выявлялось нарушение его нормальной цитоархитектоники в виде формирования глубоких узур, достигающих середины глубокой зоны. В поверхностной хрящевой зоне наблюдалось уменьшение толщины и последующее отслоение бесклеточной пластинки с прогрессированием расщепления коллагеновых структур. Превалирующая часть хондроцитов находилась в состоянии кариопикноза и апоптоза. Область травматического дефекта была представлена активно пролиферирующими элементами тканей мезенхимального происхождения, распространяющимися за его границы, с формированием большого количества соединительнотканных стриктур с окружающими структурными элементами сустава. В промежуточной зоне визуализировалось единичное расположение хондроцитов, находящихся на разных стадиях дегенеративных изменений, а также лакуны, лишенные клеточных элементов. Наблюдалось разволокнение базофильной линии с нарушением ее целостности и прорастанием сосудистых структур и костномозгового паннуса в хрящевую зону. В субхондральной кости определялись патологические изменения в системе микроциркуляторного русла в виде тромбоза и облитерации сосудов. Вследствие образования костных кист и деструктивных изменений костной ткани отмечалось формирование локальных зон остеосклероза с утолщением костных трабекул. При окраске метиленовым синим выявлялись множественные очаги метахромазии в виде неравномерного окрашивания, характеризующие участки разволокнения коллагеновых структур (фиг. 2). При визуализации синовиальной оболочки определялось увеличение ее толщины, что свидетельствовало о формировании хронического синовита.
После терапии ибупрофеном при визуальном осмотре коленного сустава отмечалось уменьшение отека с сохранением хромоты и выпадением двигательной активности. При вскрытии сустава выделялась мутная синовиальная жидкость, суставная поверхность была тусклая, хрящ имел желтоватый оттенок. Макроскопически в области травматического дефекта визуализировалась фиброзная ткань, распространяющаяся за его пределы. При микроскопическом исследовании суставного хряща (фиг. 3) определялась нечеткость его зональной структуры. В поверхностной зоне наблюдалось нарушение целостности бесклеточной пластинки с локальными зонами отслойки. Отмечалось сохранение узур с уменьшением их глубины, достигающей промежуточной зоны, деструктивные изменения которой характеризовались наличием беспорядочно расположенных хондроцитов, запустеванием лакун и формированием бесклеточных зон. В глубоком слое хрящевой ткани визуализировались хондроциты с признаками дегенеративных изменений. В области субхондральной кости наряду с участками остеолизиса отмечалось формирование зон очагового остеосклероза. После окраски метиленовым синим визуализировались очаги метахромазии, локализованные в поверхностной и промежуточной зонах хрящевого матрикса. В капсуле и синовиальной оболочке коленного сустава отмечалось формирование очагов клеточной инфильтрации с преобладанием клеток макрофагального типа, утолщение стенок и избыточная пролиферация сосудов. Синовиоциты покровного слоя характеризовались наличием дегенеративных изменений.
При применении мексидола отмечалось торможение процессов вторичных деструктивных изменений, ограничение разрастания соединительной ткани, восстановление конгруэнтности суставных поверхностей. При объективном исследовании отмечалось уменьшение отека с сохранением ограничения движений в поврежденном суставе, в области наносимой травмы определялась фиброзная ткань, а также отсутствие блеска суставного хряща. На остальных же участках суставная поверхность была блестящая, бледно-розового цвета. При микроскопическом исследовании отмечалось сохранение нарушенной зональности структуры хрящевого матрикса. В поверхностной зоне хряща визуализировались узуры с нарушением целостности бесклеточной пластинки, а промежуточная и глубокая зоны сохранили свою цитоархитектонику. В субхондральной кости отсутствовали очаги остеосклероза (фиг. 4). При обработке метиленовым синим визуализировались участки метохромазии, локализованные непосредственно в области, окружающей хондроциты. Отмечалось уменьшение общего числа разрушенных и дегенеративно-измененных хондроцитов. В промежуточной зоне на фоне применения мексидола определялись репаративные изменения, характеризующиеся увеличением количества хондроцитов и изогенных групп.
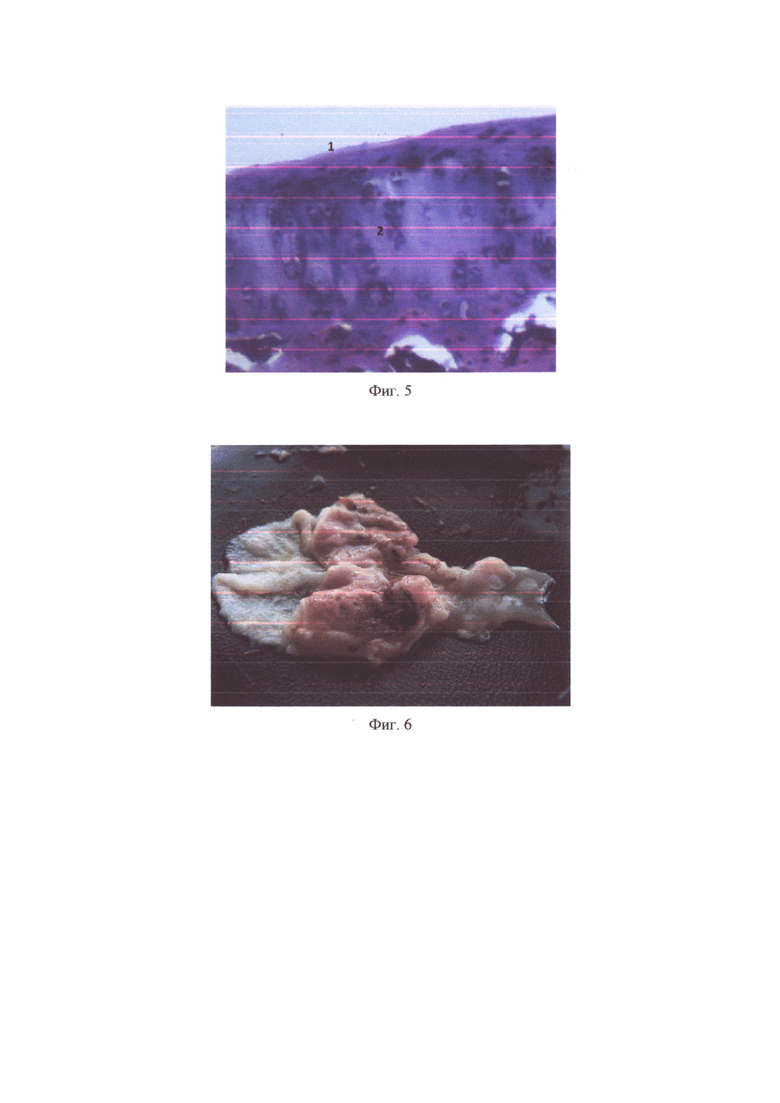
Внутрижелудочное введение соединения 1 оказало более выраженный лечебный эффект в сравнении с монотерапией ибупрофеном и мексидолом. Объективно поврежденные суставы были не деформированы с сохранением полного объема выполняемых функций. При вскрытии сустава выделилось 0,2 мл синовиальной жидкости желтого цвета, травматический дефект был заполнен регенерирующей тканью со сглаживанием суставной поверхности. На фоне применения соединения 1 при микроскопическом исследовании визуализировалась следующая гистологическая картина. Дефект в области наносимой травмы был заполнен регенератом, представленным хондроцитами и фиброзной тканью, края которого были ограничены размерами поврежденного участка. Вне зоны повреждения суставной хрящ был ровный, окрашен равномерно с сохранением нормальной цитоархитектоники и отсутствием очагов деструкции. Поверхностная бесклеточная пластинка сохранила свою равномерность и структуру без признаков истончения, и отслойки. Визуализировалось групповое расположение хондроцитов, из которых лишь единичные имели дистрофические изменения. В промежуточной зоне хряща наблюдались репаративные изменения, характеризующиеся увеличением количества изогенных групп, представленных скоплением хондроцитов с нормальными ядрами и функциональной активностью. При окрашивании метиленовым синим определялось отсутствие очагов метахромазии матрикса хрящевой ткани (фиг. 5).
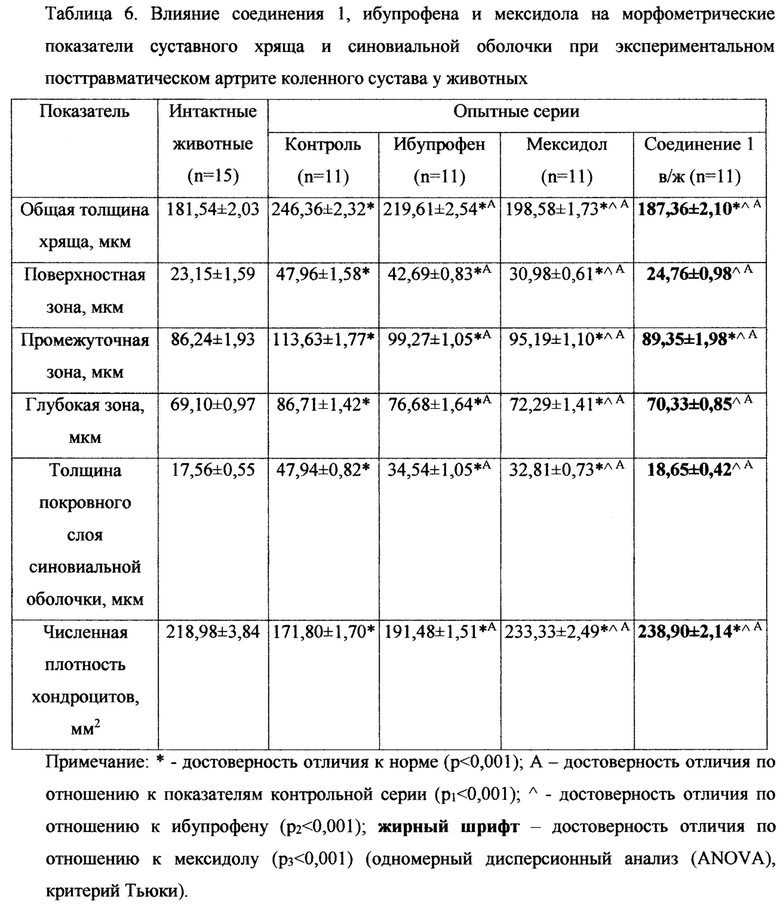
При оценке морфометрических показателей (таб. 6) при применении соединения 1 выявлялось достоверное снижение общей толщины хряща на 23,9% (p1<0,001) относительно показателей контрольной серии, что на 13% (р2<0,001) и 4,5% (р3<0,001) выше аналогичных значений серий применения ибупрофена и мексидола соответственно.
Пример 10. Исследование ульцерогенной активности соединения 1 В серии с зондовым пероральным применением ибупрофена наблюдалось язвообразование в желудке у 63,6% животных. У 51,4% животных обнаружены признаки желудочного кровотечения. Общая площадь язв в желудке составила 20,86±2,92 мм2, из которой площадь глубоких дефектов - 29,89±1,30%. По количеству глубокие язвы составили 10,36±0,70% от общего числа язв (фиг. 6). На слизистой тонкой кишки язвообразования не наблюдалось. Поражение толстой кишки определялось у 54,5% животных. Площадь язв составила 28,86±2,78 мм2, количество язв - 10,14±1,52.
Курс внутрижелудочного введения мексидола, а также внутрижелудочное введение соединения 1 (фиг. 7), не приводил к повреждающему действию слизистой оболочки желудка и кишечника во всех отделах. При вскрытии желудка слизистая оболочка была бледно-розового цвета, блестящая, гладкая, с эластичными складками, покрытая прозрачной слизью.
Таким образом, соединение 1 обладает выраженными антиоксидантными, противовоспалительными и антиульцерогенными свойствами, ингибирует деструктивно-дистрофические процессы в тканях сустава, что позволяет применять соединение 1 в качестве эффективного патогенетического средства при воспалительно-дегенеративных заболеваниях суставов.
Краткое описание чертежей
Фиг. 1. Суставной хрящ коленного сустава крысы. Серия контрольная. Окраска гематоксилином и эозином. Ув. × 100. 1 - разрушение бесклеточной пластинки с образованием узур; 2 - нарушение зональной структуры хряща, исчезновение колонковых структур; 3 - фибриллярные бесклеточные участки промежуточной зоны; 4 - очаги некроза, пустые клеточные лакуны.
Фиг. 2. Суставной хрящ коленного сустава крысы. Серия контрольная. Окраска метиленовым синим. Ув. × 100. 1 - очаги метахромазия внеклеточного матрикса; 2 -участки деструкции поверхностной и промежуточной зоны хряща.
Фиг. 3. Суставной хрящ коленного сустава крысы. Зондовое внутрижелудочное введение ибупрофена. Окраска гематоксилином и эозином. Ув. × 100. 1 - повреждение поверхностной зоны хряща; 2 - пустые лакуны в поверхностной и промежуточной зоны; 3 - разрастание фиброзной ткани.
Фиг. 4. Суставной хрящ коленного сустава крысы. Зондовое внутрижелудочное введение мексидола. Окраска гематоксилином и эозином. Ув. × 100. 1 - нарушение целостности поверхностной бесклеточной пластинки; 2 - участки остеосклероза субхондральной кости.
Фиг. 5. Суставной хрящ коленного сустава крысы. Зондовое внутрижелудочное введение соединения 1. Окраска гематоксилином и эозином. Ув. × 100. 1 - сохранная поверхностная бесклеточная пластинка; 2 - вертикальная столбчатость хондроцитов промежуточной зоны.
Фиг. 6. Макропрепарат желудка. Зондовое внутрижелудочное введение ибупрофена. Множественные язвы с кровотечением.
Фиг. 7. Макропрепарат желудка. Зондовое внутрижелудочное введение соединения 1. Нормальная слизистая оболочка желудка.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ПОСТТРАВМАТИЧЕСКОГО АРТРОЗА КОЛЕННОГО СУСТАВА | 2013 |
|
RU2516951C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ СПОСОБНОСТЬЮ СТИМУЛИРОВАТЬ РЕПАРАТИВНЫЕ ПРОЦЕССЫ ТКАНЕЙ ПАРОДОНТА, А ТАКЖЕ АНТИОКСИДАНТНЫМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНИЯ-2-(3-БЕНЗОИЛФЕНИЛ)-ПРОПАНОАТ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2022 |
|
RU2793537C1 |
| СПОСОБ ОЦЕНКИ ИНТЕНСИВНОСТИ ДЕСТРУКТИВНЫХ ПРОЦЕССОВ ПРИ ТРАВМАТИЧЕСКОМ ПОВРЕЖДЕНИИ КОЛЕННОГО СУСТАВА И ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПОСТТРАВМАТИЧЕСКОГО АРТРОЗА | 2011 |
|
RU2463000C1 |
| КОМБИНИРОВАННОЕ СРЕДСТВО ДЛЯ ВНУТРИСУСТАВНОГО ВВЕДЕНИЯ | 2017 |
|
RU2737380C2 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСТТРАВМАТИЧЕСКОГО ОСТЕОАРТРОЗА | 2004 |
|
RU2271816C1 |
| СРЕДСТВО ДЛЯ УХОДА ЗА ОБЛАСТЬЮ ПЕРИФЕРИЧЕСКИХ СУСТАВОВ И ПОЗВОНОЧНИКА | 2008 |
|
RU2376011C1 |
| КОМБИНАЦИЯ ХОНДРОПРОТЕКТОРНОГО СРЕДСТВА С НПВС | 2017 |
|
RU2742172C2 |
| СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА И ПОСТТРАВМАТИЧЕСКИХ БОЛЕВЫХ СИНДРОМОВ | 2004 |
|
RU2274472C1 |
| СПОСОБ ПОДГОТОВКИ К ЛЮБРИКАНТНОЙ ТЕРАПИИ | 2005 |
|
RU2293559C2 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ОСТЕОАРТРИТА, ОСТЕОПОРОЗА И&NBSP;ОСТЕОАРТРОЗА СУСТАВОВ | 2013 |
|
RU2521227C1 |



Группа изобретений относится к области фармацевтической химии и включает 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноат и его применение для лечения воспалительно-дегенеративных заболеваний суставов. Технический результат - 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноат, обладающий противовоспалительным, антиоксидантным и антиульцерогенным действием, пригодный для лечения воспалительно-дегенеративных заболеваний суставов. 2 н.п. ф-лы, 7 ил., 6 табл., 10 пр.
1. Средство, обладающее противовоспалительным, антиоксидантным и антиульцерогенным действием, представляющее собой 2-этил-6-метил-3-гидроксипиридиния-4-изобутилфенилпропаноат.
2. Применение вещества по п.1 в качестве средства для лечения воспалительно-дегенеративных заболеваний суставов.
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ, ОБУСЛОВЛЕННОГО НАРУШЕНИЕМ ОКИСЛИТЕЛЬНОГО СТРЕССА | 2018 |
|
RU2674286C1 |
| Комплексные соли ацексамовой кислоты, стимулирующие регенерацию костной ткани, ускоряющие процессы репаративного остеогенеза, стимулирующие минерализацию костной ткани при остеопорозе | 2018 |
|
RU2668966C1 |
| Салицилат 2-этил-6-метил-3-гидроксипиридина, его сольваты и гидраты и способы их получения | 2017 |
|
RU2652891C1 |
| WO 2019117820 A1, 20.06.2019 | |||
| Жигачева И.В | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| II ОБЪЕДИНЕННЫЙ НАУЧНЫЙ ФОРУМ | |||
| VI СЪЕЗД ФИЗИОЛОГОВ СНГ | |||
| VI СЪЕЗД БИОХИМИКОВ РОССИИ | |||
| IX РОССИЙСКИЙ СИМПОЗИУМ "БЕЛКИ И ПЕПТИДЫ" | |||
Авторы
Даты
2024-02-29—Публикация
2023-01-11—Подача