Область техники, к которой относится изобретение
Настоящее изобретение относится к композиции, призванной способствовать, поддерживать или оптимизировать первичную миелинизацию, и/или структуру головного мозга, и/или плотность нейронных связей, и/или одно или более из перечисленного: когнитивный потенциал, способность к обучению и интеллектуальный потенциал, и/или когнитивную функцию у субъекта.
Уровень техники
Грудное вскармливание рекомендовано всем младенцам. Вместе с тем в некоторых случаях грудное вскармливание является недостаточным или невозможным по медицинским причинам. В подобных ситуациях детские смеси могут использоваться в качестве альтернативы материнскому молоку. Вместе с тем проведенные исследования показали, что детская смесь не всегда оказывает такие же воздействия на организм, как и материнское молоко.
В недавнем исследовании было показано, что структура головного мозга и/или пространственно-временное распределение миелинизированного вещества в головном мозге младенцев, получавших исключительно грудное вскармливание, может отличаться от наблюдаемого у младенцев, получавших детскую смесь, и что такие отличия могут коррелировать с повышенным уровнем интеллекта, более эффективным обучением и/или когнитивной функцией у детей грудного возраста, в частности, в дальнейшей жизни, даже при условии учета сопутствующих факторов ("Breastfeeding and early white matter development: a cross sectional study", Deoni et al, NeuroImage 82, (2013), 77-86). Упомянутое исследование также четко демонстрирует наличие связи, в частности, временной связи между первичной миелинизацией и, в частности, между траекторией первичной миелинизации со структурой головного мозга.
В прошлом продолжительные структурные исследования головного мозга младенцев на грудном вскармливании и получающих детскую смесь не проводились, и выявленные различия когнитивной функции и способностей часто попросту относили к таким факторам, как социально-экономический статус и образовательный статус матери. Возможные различия в структуре головного мозга младенцев на грудном вскармливании и получающих детскую смесь не рассматривались и не поддавались измерениям в тех масштабах, которые доступны сегодня, с момента, когда МРТ головного мозга младенцев стала повсеместной практикой, см. работу Deoni et al.
Важное значение структуры головного мозга, в частности количество и/или пространственное распределение миелинизированного вещества внутри головного мозга для когнитивной функции и интеллекта, является надежно установленным фактом. Собственно, миелин в головном мозге создает изолирующую оболочку по длине нейрона, обеспечивающую гораздо более быструю передачу нервных импульсов. Вместе с тем именно структура головного мозга, в частности, количество и/или пространственное распределение миелина внутри головного мозга, которое влияет на плотность нейронных связей, например на то, каким путем и насколько быстро и эффективно сообщения в форме нервных импульсов передаются внутри головного мозга и, в частности, между различными областями головного мозга. Такой обмен информацией внутри мозга может играть определенную роль в когнитивной функции и обучении и может влиять или даже служить для физиологического ограничения интеллектуального, когнитивного потенциала и/или способности к обучению, а также регулировать когнитивную функцию.
Соответственно, существует потребность найти способы для стимулирования, поддержки или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, в частности количества и/или пространственного распределения миелинизированного вещества внутри головного мозга, и/или плотности нейронных связей у субъекта, в частности у субъекта, получающего детскую смесь.
Кроме того, существует потребность найти способы оптимизации интеллектуального потенциала и/или когнитивного потенциала, и/или способности к обучению, и/или когнитивной функции у субъекта, в частности у субъекта, получающего детскую смесь.
Авторы настоящего изобретения неожиданно обнаружили, что композиция, содержащая холин, может способствовать стимулированию, поддержке или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, в частности количества и/или пространственного распределения миелинизированного вещества внутри головного мозга, и/или плотности нейронных связей у субъекта, в частности у субъекта, получающего детскую смесь.
Более конкретно, авторы настоящего изобретения установили, что композиция, содержащая холин, может способствовать стимулированию, поддержке или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, в частности количества и/или пространственного распределения миелинизированного вещества внутри головного мозга у субъекта, получающего детскую смесь, и может привести одну или более из перечисленных выше характеристик в полное или более близкое соответствие с наблюдаемыми у субъекта на грудном вскармливании, в частности исключительно на грудном вскармливании.
Такой вывод является следствием анализа питательной ценности по результатам продолжительного исследования когнитивной функции и визуализации головного мозга, в ходе которого изучались и сопоставлялись первичная миелинизация, в частности траектория первичной миелинизации, и/или структура головного мозга, в частности количество и/или пространственное распределение миелинизированного вещества внутри головного мозга, в частности которые определялись первичной миелинизацией и траекторией первичной миелинизации у субъектов на грудном вскармливании и получающих детскую смесь. Дополнительные подробности настоящего исследования и результаты приведены в примерах, включенных в текст настоящего документа.
Раскрытие изобретения
Основные положения изобретения изложены в формуле изобретения и более подробно представлены в детальном описании, включенном в текст настоящего документа.
Настоящее изобретение относится к искусственной питательной композиции, содержащей холин, которая может использоваться для содействия, поддержки или оптимизации одного или более из следующего:
• первичной миелинизации, в частности траектории первичной миелинизации,
• структуры головного мозга, в частности количества и пространственного распределения миелинизированного вещества внутри головного мозга и/или определенных областей головного мозга,
• плотности нейронных связей,
• интеллектуального потенциала,
• когнитивного потенциала,
• способности к обучению,
• когнитивной функции
у субъекта, в частности у субъекта, получающего детскую смесь. Более конкретно, упомянутым субъектом может быть младенец или ребенок человека, а точнее, младенец или ребенок человека, получающий детскую смесь.
Упомянутая искусственная питательная композиция может представлять собой композицию, выбранную из группы, состоящей из; детской смеси, молочной смеси для детей от 1 до 3 лет, композиции для младенцев, которая предназначена для добавления или разбавления грудным молоком человека, и продукта питания, предназначенного для потребления младенцем и/или ребенком в чистом виде или в комбинации с грудным молоком человека.
Упомянутая композиция может оптимизировать траекторию первичной миелинизации у субъекта, в частности у субъекта, получающего детскую смесь, и на любую величину приблизить их к средней траектории первичной миелинизации, наблюдаемой у субъектов на грудном вскармливании, в частности у субъектов исключительно на грудном вскармливании, в головном мозге в целом или в одной или более областей головного мозга при сопоставлении с композицией, в которой все другие компоненты идентичны за исключением содержания холина.
Упомянутая композиция может дополнительно содержать любой один или более из следующих ингредиентов:
• фосфолипид, в частности фосфолипид с формулой (I) или смесь соединений формулы (I) в соответствии с описанием в настоящем документе, и, в частности, может быть фосфатидилхолином, фосфатидилинозитолом, фосфатидилсерином, фосфатидилэтаноламином, сфингомиелином или их смесью,
• витамин, в частности витамин B12 и/или фолиевую кислоту,
• минеральное вещество, в частности железо, цинк, медь, кальций, фосфор, магний и любую их комбинацию,
• производное жирной кислоты причем, упомянутое производное жирной кислоты представляет собой содержащую жирную кислоту соединение, отличное от фосфолипида, причем упомянутое производное жирной кислоты может быть выбрано из группы, состоящей из свободной жирной кислоты, моноацилглицерина, диацилглицерина, триацилглицерина, сложного эфира холестерина и их комбинации, и при этом упомянутая жирная кислота может представлять собой докозагексаеновую кислоту и/или арахидоновую кислоту, и/или стеариновую кислоту, и/или нервоновую кислоту.
Если композиция дополнительно содержит один или более из этих ингредиентов, она может быть более эффективной.
Значения особенно эффективной концентрации приведенных выше ингредиентов приведены в пунктах формулы изобретения и в представленном ниже подробном описании, включенном в текст настоящего документа.
Краткое описание фигур
На фиг. 1 приведены средние для всего головного мозга (все белое вещество) траектории миелинизации у младенцев и детей младшего возраста на грудном вскармливании по сравнению с получающими две коммерческие детские смеси с различными уровнями холина.
На фиг. 1а приведены средние траектории миелинизации по областям головного мозга у младенцев и детей младшего возраста на грудном вскармливании по сравнению с получающими две коммерческие детские смеси с различными уровнями холина.
На фиг. 1b приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные с холином.
На фиг. 1c приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные со сфингомиелином.
На фиг. 1d представлено изображение головного мозга, на котором видны миелинизированные области головного мозга, связанные с фосфатидилинозитолом.
На фиг. 1e приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные с фосфатидилхолином.
На фиг. 1f приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные с фолиевой кислотой.
На фиг. 1g представлено изображение головного мозга, на котором видны миелинизированные области головного мозга, связанные с витамином В12.
На фиг. 1h приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные с железом.
На фиг. 1i приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные с цинком.
На фиг. 1j представлено изображение головного мозга, на котором видны миелинизированные области головного мозга, связанные с кальцием.
На фиг. 1k приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные с фосфором.
На фиг. 1l представлено изображение головного мозга, на котором видны миелинизированные области головного мозга, связанные с магнием.
На фиг. 1m представлено изображение головного мозга, на котором видны миелинизированные области головного мозга, связанные с докозагексановой кислотой.
На фиг. 1n приведена томограмма головного мозга, отображающая миелинизированные области головного мозга, связанные с арахидоновой кислотой.
На фиг. 2 продемонстрировано влияние нервоновой кислоты на плотность нейронов и плотность астроцитов.
На фиг. 3 продемонстрировано влияние стеариновой кислоты на плотность нейронов и плотность астроцитов.
На фиг. 4 продемонстрировано влияние октановой кислоты на плотность нейронов и плотность астроцитов.
На фиг. 5 продемонстрировано влияние сфингомиелина на количество нейросфер и
пролиферацию нейронов.
На фиг. 6 приведена относительная численность основных видов сфингомиелина (SM) в ингредиенте, детской смеси, коровьем молоке и грудном молоке. (Планки погрешности отражают стандартное отклонение при n = 3).
На фиг. 7 приведено относительное содержание жирной кислоты (ЖК) во фракции SM в ингредиенте, детской смеси, коровьем молоке и грудном молоке. (Планки погрешности отражают стандартное отклонение при n = 3).
На фиг. 8 приведено воздействие докозагексаеновой кислоты (DHA) на основной миелиновый белок (MBP), нейрофиламенты (NF) и/или MBP/NF на день 18 и/или день 30.
На фиг. 9 приведено воздействие стеариновой кислоты (SA) на A2B5, MBP, моноацилглицерин (MAG), NF, MBP/NF и/или MAG/NF на день 12, день 18 и/или день 30.
На фиг. 10 приведено воздействие витамина В12 на A2B5, NF, MBP/NF и/или MAG на день 12, день 18 и/или день 30.
На фиг. 11 приведено воздействие фолиевой кислоты (FA) на A2B5, NF, MAG, MAG/NF и/или MBP/NF на день 12, день 18 и/или день 30.
На фиг. 12 приведено воздействие холина (Cho) на A2B5, MAG и/или MBP на день 12, день 18 или день 30.
На фиг. 13 приведено воздействие железа на A2B5, MBP, MAG, NF и/или MAG/NF на день 12, день 18 и/или день 30.
На фиг. 14 приведено воздействие цинка на MBP, NF и/или MBP/NF на день 12, день 18 и/или день 30.
На фиг. 15 приведено воздействие фосфора на MAG, NF и/или MAG/NF на день 12, день 18 и/или день 30.
На фиг. 16 приведено воздействие магния на A2B5, MBP, NF, MAG, MBP/NF и/или MAG/NF на день 12, день 18 и/или день 30.
На фиг. 17 приведено воздействие меди на A2BF, MAG, и/или MAG/NF на день 12 и/или день 18.
На фиг. 18: продемонстрировано влияние фосфатидилхолина на A2B5 на 12-й день и на МАГ на 18-й день.
На фиг. 19 приведено воздействие фосфатидилинозитола на A2B5, MBP, MAG, NF, MAG/NF на день 12, день 18 и/или день 30.
На фиг. 20 приведено воздействие фосфатидилсерина на A2B5, NF и/или MAG/NF на день 12 и/или день 18.
На фиг. 21 приведено воздействие сфингомиелина на A2B5, MAG и/или MBP на день 12, день 18 и/или день 30.
На фиг. 22 приведено воздействие церамида (Cer) на A2B5 на день 12 и на MAG на день 18.
На фиг. 23 приведено воздействие галактоцерамида (GalCer) на A2B5, MBP, NF и/или MBP/NF на день 12 и/или на день 30.
На фиг. 24 приведено воздействие глюкоцерамида (GluCer) на A2B5 на день 12 и на NF на день 12 и день 18.
На фиг. 25 приведено воздействие D-эритроцерамида (D-ery) на A2B5 на день 12 и на MAG на день 18.
На фиг. 26 приведено воздействие церамид-1-фосфата (C1P) на A2B5 на день 12 и на NF и MAG на день 18.
На фиг. 27 приведено воздействие моносиалоганглиозида-3 (GM3) на A2B5, MBP, MAG и/или MBP/NF на день 12, день 18 и/или день 30.
На фиг. 28 приведено воздействие дисиалоганглиозидов-3 (GD3) на A2B5, MBP, NF и/или MAG на день 12, день 18 и/или день 30.
На фиг. 29 приведен профиль жирных кислот для фосфатидилинозитола (PI), фосфатидилхолина, фосфатидила (PC), фосфатидилсерина (PS) и сфингомиелина, используемых в примере 6.
На фиг. 30 приведено воздействие витамина В12 на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 31 приведено воздействие арахидоновой кислоты (ARA) на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 32 приведено воздействие стеариновой кислоты на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 33 приведено воздействие цинка на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 34 приведено воздействие фосфатидилинозитола на экспрессию мРНК MAG и MBP.
На фиг. 35 приведено воздействие GD3 на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 36 приведено воздействие DHA на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 37 приведено воздействие нервоновой кислоты на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 38 приведено воздействие железа на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 39 приведено воздействие фосфатидилхолина на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 40 приведено воздействие фосфатидилсерина на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 41 приведено воздействие фолиевой кислоты на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 42 приведено воздействие холина на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 43 приведено воздействие церамида на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 44 приведено воздействие галактоцерамида на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 45 приведено воздействие глюкоцерамида на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 46 приведено воздействие церамид-1-фосфата на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 47 приведено воздействие D-эритроцерамида на экспрессию мРНК MAG и MBP и на совместную экспрессию MBP и BetaIII.
На фиг. 48 приведено воздействие сфингомиелина на совместную экспрессию MBP и BetaIII.
На фиг. 49 приведено воздействие GM3 на совместную экспрессию MBP и BetaIII.
Осуществление изобретения
В одном аспекте настоящего изобретения приводится искусственная композиция, содержащая холин, и такая композиция может использоваться, чтобы стимулировать поддержку или оптимизировать первичную миелинизацию, в частности траекторию первичной миелинизации, и/или структуру головного мозга, и/или плотность нейронных связей, и/или интеллектуальный потенциал, и/или когнитивный потенциал, и/или способность к обучению, и/или когнитивную функцию у субъекта, в частности у субъекта, получающего детскую смесь.
За счет стимулирования, поддержки или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, в частности количества и/или пространственного распределения миелинизированного вещества внутри головного мозга, в частности которые определялись первичной миелинизацией и траекторией первичной миелинизации, и/или интеллектуального потенциала, и/или когнитивного потенциала, и/или способности к обучению, и/или когнитивной функции у субъекта, в частности у субъекта, получающего детскую смесь, композиция настоящего изобретения может предупреждать, снижать риск и/или смягчать последствия недостаточной первичной миелинизации, в частности траектории недостаточной первичной миелинизации, и/или недостаточной структуры головного мозга, и/или недостаточной плотности нейронных связей, и/или недостаточного интеллектуального потенциала, и/или недостаточного когнитивного потенциала, и/или недостаточной способности к обучению, и/или недостаточной когнитивной функции у упомянутого субъекта. Она может быть нетерапевтической или терапевтической.
Термин «стимулировать» при использовании в настоящем документе относится к одному или нескольким факторам, приводящим к развитию определенного процесса.
Термин «поддерживать» при использовании в настоящем документе относится к одному или нескольким факторам, поддерживающим определенный процесс после начала развития такого процесса.
Термин «субъект» при использовании в настоящем документе относится к млекопитающему, в частности кошке, собаке или человеку, более конкретно, термин относится к человеку, еще более конкретно - к младенцу или ребенку человека, и еще более конкретно - к младенцу или ребенку человека, получающему детскую смесь и/или молочную смесь для детей от 1 до 3 лет.
Термин «младенец» при использовании в настоящем документе относится к младенцу человека в возрасте до 12 месяцев и включает недоношенных и глубоко недоношенных младенцев, младенцев с низким весом при рождении, т.е. новорожденных с весом тела ниже 2500 г (5,5 фунтов), как по причине преждевременных родов, так и из-за ограниченного роста плода, а также младенцев, родившихся маленькими для своего гестационного возраста (SGA), т.е. малышей с весом при рождении ниже 10-го процентиля для малышей того же гестационного возраста.
Термин «ребенок» при использовании в настоящем документе относится к человеку в возрасте от 1 до 18 лет, более конкретно - к человеку в возрасте от 1 до 10 лет, еще более конкретно - к человеку в возрасте от 1 до 5 лет, и еще более конкретно - к человеку в возрасте от 1 до 2 лет.
Термин «младенец или ребенок, получающий детскую смесь» при использовании в настоящем документе относится к младенцу или ребенку, получающему как детскую смесь, так и/или молочную смесь для детей от 1 до 3 лет.
Термин «субъект на грудном вскармливании» при использовании в настоящем документе относится к млекопитающему, в частности кошке, собаке или человеку, более конкретно, термин относится к человеку, еще более конкретно - к младенцу или ребенку человека, и еще более конкретно - к младенцу или ребенку человека, получающему грудное молоко, в частности от полноценно питающейся матери.
Термин «первичная миелинизация» при использовании в настоящем документе относится к развитию миелинизации и, в частности, к процессу, в ходе которого не имеющие оболочки аксоны в головном мозге субъекта миелинизируются в процессе роста и развития. Она представляет собой процесс, который начинается, в частности в конкретных областях головного мозга, в утробе матери и продолжается после родов и который отличается наибольшей активностью в человеческого субъекта, в частности в первые 2 или 3 года жизни человека, более конкретно - в первый год жизни человека.
Термин «траектория первичной миелинизации» при использовании в настоящем документе относится к степени первичной миелинизации или накоплению нового миелина (которое, например, оценивается по миелиновой водной фракции) в зависимости от времени, и, в частности, в период и в течение младенчества и детства, в частности раннего детства, и более конкретно - в первые 5 лет жизни субъекта-человека, более конкретно - в первые 2 или 3 года жизни человека, еще более конкретно - в первый год или в первые 6 месяцев жизни человека, когда детская смесь может быть единственной формой питания для некоторых младенцев.
Термин «структура головного мозга» при использовании в настоящем документе относится к структуре серого и белого вещества в головном мозге и конкретных областях головного мозга, в частности миелинизированному белому веществу в головном мозге конкретных областях головного мозга, что определяется первичной миелинизацией, в частности траекторией первичной миелинизации, т.е. первичным структурным отложением миелина. Более конкретно, термин относится к количеству и/или пространственному распределению миелинизированного вещества внутри головного мозга и/или в конкретных областях головного мозга и, еще более точно, к количеству и/или пространственно-временному распределению миелинизированного вещества внутри головного мозга и/или в конкретных областях головного мозга.
Термин «интеллектуальный потенциал» при использовании в настоящем документе относится к возможным интеллектуальным способностям или возможностям, достижимым для субъекта, что определяется физиологическими факторами. В частности, интеллектуальный потенциал может относиться к подвижному интеллекту.
Термин «подвижный интеллект» при использовании в настоящем документе относится к нейронному потенциалу субъекта и/или способностям субъекта решать новые или абстрактные задачи, что определяется физиологическими факторами. Он отличается от «кристаллизованного интеллекта», который по меньшей мере частично определяется приобретенными в процессе обучения или постепенно накапливаемыми знаниями.
Термин «когнитивный потенциал» при использовании в настоящем документе относится к возможным когнитивным и/или умственным способностям или возможностям, достижимым для субъекта, что определяется физиологическими факторами. В частности, термин может относиться к одному или более из следующего; потенциала обработки информации, потенциала восприятия, потенциала внимания, потенциала мышления, потенциала рассуждения, потенциала понимания и запоминания, психомоторного потенциала, в том числе потенциала крупной моторики и мелкой моторики, визуального потенциала, в том числе потенциала визуального восприятия, потенциала слухового восприятия, языкового потенциала, в том числе потенциала языковых навыков передачи и восприятия информации, потенциала запоминания и вспоминания, потенциала концентрации, потенциала исполнительной функции, в том числе потенциала решения проблем, принятия решений и торможения.
Термин «способность к обучению» при использовании в настоящем документе относится к возможной способности или возможности субъекта к обучению, например насколько легко и/или быстро субъект может быть в состоянии воспринимать знания или навыки посредством приобретения опыта, изучения или образования, что определяется физиологическими факторами. А также к возможной способности субъекта адаптироваться в ответ на внешние факторы, что определяется физиологическими факторами.
Термин «обучение» при использовании в настоящем документе относится к приобретению знаний или навыков посредством опыта, изучения или образования.
Термин «познание» при использовании в настоящем документе относится к интеллектуальным процессам, посредством которых то или иное лицо узнает, воспринимает или понимает идеи; т.е. к способности думать и понимать. Познание включает все аспекты обработки информации, восприятия, внимания, мышления, рассуждения, понимания и запоминания, а также психомоторную функцию, языковую функцию, функции памяти, концентрации, исполнительную функцию и способности решения проблем.
Термин «оптимизировать» при использовании в настоящем документе относится к улучшению или повышению.
Поскольку грудное молоко человека является идеальным стандартом, если речь идет о питании младенцев, оптимальной может считаться траектория первичной миелинизации, измеряемая или наблюдаемая у субъектов на грудном вскармливании, в частности у субъектов исключительно на грудном вскармливании, в частности полноценно питающимися матерями. Поэтому композиция настоящего изобретения может рассматриваться как оптимизирующая траекторию миелинизации у субъекта, если она приводит траекторию первичной миелинизации у субъекта, в частности у субъекта, получающего детскую смесь, в полное или более близкое соответствие с измеряемой или наблюдаемой у субъекта на грудном вскармливании, более конкретно - у субъекта исключительно на грудном вскармливании, в частности полноценно питающейся матерью.
Траекторию первичной миелинизации у субъекта можно считать приведенной в полное или более близкое соответствие с измеряемой или наблюдаемой у субъекта на грудном вскармливании, более конкретно - у субъекта исключительно на грудном вскармливании, в частности полноценно питающейся матерью, если расстояние между любыми эквивалентными/идентичными точками измерения на траектории субъекта и траектории упомянутого субъекта на грудном вскармливании составляет до 50%, в частности до 25%, более конкретно - до 20%. Не имеющие ограничительного характера примеры в диапазоне до 50% включают 50%, 40%, 30%, 25%, 20%, 10%, 5%, 1%, 0,5% и 0,01%. В частности, траектории будут считаться биоэквивалентными.
Траектория миелинизации может измеряться в рамках любой комбинации временных точек. В частности, временные точки находятся в пределах первых 5 лет жизни человека, более конкретно - первых 2 или 3 лет жизни человека, еще более конкретно - первого года или первых 6 месяцев жизни человека.
Траектория первичной миелинизации может определяться посредством повторных измерений любого маркера миелинизации у субъекта в динамике по времени. В частности, траектория первичной миелинизации может оцениваться по результатам измерения связанной с миелином водной фракции (миелиновой водной фракции) и/или связанного с миелином водного депо (миелинового водного депо) у субъекта в различные моменты времени, в частности в различные моменты времени в течение первых 5 лет жизни субъекта-человека, более конкретно - первых 2 или 3 лет жизни человека, еще более конкретно - 1-го года или первых 6 месяцев жизни человека. Связанная с миелином водная фракция и/или связанное с миелином водное депо у субъекта может оцениваться по измерениям метода многокомпонентной релаксации (MCR) магнитно-резонансной томографии (MRI) и, в частности, с использованием методики mcDESPOT (Deoni et al 2008). В частности, траектория первичной миелинизации может определяться посредством многократного измерения связанного с миелином водного депо с использованием методики mcDESPOT во времени (Magn.Reson.Med.2008 60:1372-1387, содержание которой включено в текст настоящего документа путем ссылки).
Композиция настоящего изобретения может рассматриваться как оптимизирующая когнитивную функцию и/или интеллект субъекта, если она приводит показатели у одного или более субъектов, в частности у субъекта, получающего детскую смесь, по стандартизованному когнитивному тесту, включая тест на интеллект, тест школьной успеваемости и/или тест на нервно-психическое развитие, например по шкалам раннего обучения Маллен, в полное или более близкое соответствие с измеряемыми или наблюдаемыми у субъекта на грудном вскармливании, более конкретно - у субъекта исключительно на грудном вскармливании, в частности полноценно питающейся матерью. Когнитивная и нервно-психическая функции у субъекта могут считаться приведенными в полное или более близкое соответствие с оцениваемыми у упомянутого субъекта на грудном вскармливании, если различие между показателями проводимых для упомянутого субъекта одного или более стандартизованных тестов нервно-психического развития, например Т-показателей Маллен, и таковыми показателями у упомянутого субъекта на грудном вскармливании составляет менее одного стандартного отклонения, в частности менее половины стандартного отклонения показателей стандартизованного теста, например менее 10 пунктов, более конкретно - менее 5 пунктов для Т-показателей Маллен, в частности менее 2 пунктов. Упомянутые показатели стандартизованного теста нервно-психического развития, например Т-показатели Маллен, измеряются в один и тот же момент времени у упомянутого субъекта и у упомянутого субъекта на грудном вскармливании.
Упомянутый показатель Маллен может измеряться в любой подходящий момент времени, в частности в течение первых 5 лет жизни человека, 3 лет жизни человека, более конкретно - первых 2 лет жизни человека, еще более конкретно - первого года или первых 6 месяцев жизни человека.
Стимулируя поддержку или оптимизацию когнитивного потенциала, способности к обучению и/или интеллектуального потенциала, композиции изобретения могут оказывать краткосрочное или долгосрочное воздействие на когнитивную функцию, включая развитие когнитивных функций и/или обучения, и на предупреждение или минимизацию любых нейрокогнитивных отклонений, нарушений или задержек в развитии.
Упомянутый краткосрочный эффект может проявляться только в течение дней, недель или месяцев.
Упомянутый долгосрочный эффект может проявляться в течение лет, например 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60. 70, 80, 90 лет.
Композиции, содержащие холин, могут быть особенно эффективны для поддержки, стимулирования или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга в следующих областях мозга; мозжечке, зрительной коре, таламусе, теменной коре и лобной доле. Перечисленные области головного мозга связаны с двигательной функцией (включая координацию и выполнение движений), зрением, краткосрочной памятью и/или исполнительной функцией, и/или социально-эмоциональным мышлением, и/или пространственным мышлением. Соответственно, композиция, содержащая холин, может быть особенно эффективной для стимулирования, поддержки или оптимизации потенциала двигательной функции (включая координацию и осуществление двигательного потенциала) и/или психомоторного потенциала, зрительного потенциала, потенциала краткосрочной памяти и/или потенциала исполнительной функции, и/или потенциала социально-эмоционального мышления, и/или потенциала пространственного мышления.
В одном варианте осуществления изобретения когнитивный потенциал выбирают из группы, состоящей из потенциала двигательной функции (включая координацию и осуществление двигательного потенциала), и/или психомоторного потенциала, зрительного потенциала, потенциала краткосрочной памяти, потенциала исполнительной функции, потенциала социально-эмоционального мышления и потенциала пространственного мышления.
При стимуляции, поддержании или оптимизации потенциала двигательной функции (включая координацию и осуществление двигательного потенциала), зрительного потенциала, потенциала краткосрочной памяти, и/или потенциала исполнительной функции, и/или потенциала социально-эмоционального мышления, и/или потенциала пространственного мышления композиции согласно настоящему изобретению могут иметь краткосрочный или долгосрочный эффект, например улучшающий эффект на двигательную и психомоторную функцию (включая координацию и осуществление движения), и/или зрение, и/или краткосрочную память, и/или исполнительную функцию, и/или социально-эмоциональное мышление, и/или пространственное мышление. Упомянутый краткосрочный эффект может проявляться только в течение дней, недель или месяцев.
Упомянутый долгосрочный эффект может проявляться в течение лет, например 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60. 70, 80, 90 лет.
Термин «холин» относится к четвертичным аммониевым солям, содержащим катион N,N,N-триметилэтаноламмония и имеющим приведенную ниже структуру:

Холин
Противоион X- может, в частности, быть хлоридом, гидроксидом, цитратом, битартратом и их смесями.
Если не указано иное, в контексте настоящего изобретения термин «холин» должен быть призван определять все холины, присутствующие в составе питательной композиции настоящего изобретения в свободной форме (или в форме своих солей).
Холин может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, холин может содержаться в композиции в количестве более 30 мг/100 г сухой композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит холин в количестве, выбранном из группы, состоящей из следующего; более 30 мг, более 50 мг, более 100 мг, более 111 мг, более 170 мг, в диапазоне от 30 до 1000 мг, в диапазоне от 30 до 700 мг, в диапазоне от 50 до 1000 мг, в диапазоне от 50 до 700 мг, в диапазоне от 50 до 500 мг, в диапазоне от 100 до 400 мг, в диапазоне от 111 до 180 мг, в диапазоне от 170 мг до 300 мг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такие уровни холина в свободной форме (или в форме его солей) или в форме производных из содержащих его структур, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 1 г.
Холин может быть включен в состав композиции настоящего изобретения в чистом виде или в форме одной из физиологически приемлемых солей, таких как, например: холин хлорид, холинцитрат, холинбитартрат или их смеси.
Может быть особенно целесообразным, если композиция согласно настоящему изобретению дополнительно содержит один или более из следующих ингредиентов: витамины, и/или минералы, и/или фосфолипиды, и/или производные жирной кислоты.
Если композиция изобретения содержит холин и один или более из упомянутых выше ингредиентов, она может улучшено стимулировать поддержку и/или оптимизацию первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, и/или плотности нейронных связей, и/или когнитивного потенциала, и/или интеллектуального потенциала, и/или способности к обучению, и/или когнитивной функции у субъекта, в частности у субъекта, получающего детскую смесь. Это может быть, например, связано с тем, что упомянутые ингредиенты воздействуют на первичную миелинизацию в одной и той же и/или разных взаимодополняющих областях мозга. Такой усиленный эффект может носить синергический характер.
В одном варианте осуществления композиция изобретения дополнительно содержит витамин и/или минеральное вещество, и/или фосфолипид, и/или производное жирной кислоты.
Термин «витамин» при использовании в настоящем документе относится к любому витамину. Не имеющие ограничительного характера примеры витаминов включают: витамин A, витамин B1, витамин B2, витамин B6, витамин K, витамин C, витамин D, ниацин, биотин, пантотеновую кислоту, фолиевую кислоту, витамин B12 и их комбинации.
Особенно эффективными витаминами могут быть фолиевая кислота, витамин B12 и витамин B6, в частности фолиевая кислота и витамин B12, в частности фолиевая кислота.
В одном варианте осуществления изобретения витамин представляет собой витамин B12, фолиевую кислоту и/или их комбинацию.
Витамин может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
Фолиевая кислота может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, фолиевая кислота может содержаться в количестве более 50 мкг/100 г сухой композиции, более конкретно - от 50 мкг до 500 мкг/100 г сухой композиции.
В одном варианте осуществления композиция изобретения содержит фолиевую кислоту в количестве, выбранном из группы, состоящей из следующего; более 50 мкг, более 65 мкг, более 70 мкг, более 100 мкг, более 110 мкг, более 160 мкг, в диапазоне от 50 до 500 мкг, в диапазоне от 50 до 400 мкг, в диапазоне от 70 до 170 мкг, в диапазоне от 110 до 500 мкг, в диапазоне от 110 до 400 мкг, в диапазоне от 110 до 400 мкг, в диапазоне от 110 до 350 мкг, при этом все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такое количество фолиевой кислоты, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 400 мкг.
Фолиевая кислота может быть включена в состав питательных композиций настоящего изобретения как таковая или в форме своей физиологически приемлемой соли (фолата) или их смесей.
Витамин В12 может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, витамин В12 может содержаться в композиции в количестве, выбранном из группы, состоящей из следующего; более 0,01 мкг, в частности более 0,04 мкг, в частности более 0,05 мкг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция изобретения содержит витамин В12 в количестве, выбранном из группы, состоящей из следующего; более 0,01 мкг, более 0,5 мкг, более 0,7, более 5 мкг, в диапазоне от 0,1 до 10 мкг, от 0,4 до 5 мкг, от 0,5 до 2 мкг, от 1 до 1,5 мкг, от 4 до 8,5 мкг, в диапазоне от 5 до 8 мкг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такое количество витамина В12, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 7,6 мкг/100 г сухой композиции (77,6 мкг/кг сухой композиции).
Витамин В12 может быть включен в состав питательных композиций изобретения как таковой или в форме своей физиологически приемлемой соли, или их смесей, или с использованием любого источника, содержащего витамин В12. В частности, витамин В12 может быть включен в состав композиции в своей чистой форме, как цианкобаламин, гидроксокобаламин и любая их комбинация.
Композиции, содержащие витамин, в частности фолиевую кислоту и/или витамин В12, могут быть особенно эффективны для поддержки, стимулирования или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга в одной или более из следующих областей головного мозга; мозжечке, зрительной коре, двигательной и соматосенсорной коре. Перечисленные области головного мозга связаны с двигательной функцией (включая координацию и выполнение движений), зрительной функцией и психомоторной функцией.
Термин «минеральное вещество» при использовании в настоящем документе относится к любому минеральному веществу. Не имеющие ограничительного характера примеры минеральных веществ включают: железо, цинк, кальций, фосфор, медь, магний, иод, марганец, хлорид, калий, натрий, селен, хром и их комбинации. Минеральные вещества обычно добавляют в форме соли.
Особенно эффективными минеральными веществами могут быть железо, цинк, кальций, фосфор, медь и магний, в частности железо.
В одном из вариантов осуществления композиция согласно настоящему изобретению содержит железо, и/или цинк, и/или кальций, и/или фосфор, и/или медь, и/или магний, в частности железо и цинк, конкретнее железо.
В одном варианте осуществления питательная композиция в соответствии с настоящим изобретением содержит железо. Железо может содержаться в композиции настоящего изобретения в количестве, составляющем до 99,999% композиции.
В частности, железо может содержаться в композиции в количестве более 5 мг/100 г сухой композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит железо в количестве, выбранном из группы, состоящей из следующего; более 4 мг, более 9 мг, в диапазоне от 5 до 40 мг, в диапазоне от 9 до 40 мг, в диапазоне от 5 до 20 мг, в диапазоне от 9 до 20 мг, в диапазоне от 5 до 15 мг, в диапазоне от 9 до 15 мг, в диапазоне от 3,5 до 7 мг, причем все веса приведены из расчета на 100 г сухого веса композиции.
Железо может быть включено в состав композиций изобретения в форме одной из физиологически приемлемых солей, таких как, например, цитрат железа III, фосфат железа III, пирофосфат железа III, аскорбат железа II, карбонат железа II, цитрат железа II, фумарат железа II, глюконат железа II, лактат железа II, сульфат железа II или их смеси.
Железо может быть включено в состав композиции настоящего изобретения в форме физиологически приемлемого комплекса железа (такого как, например, железо-натриевая соль EDTA) или их смесей.
Fe2+ является более биодоступным, и поэтому, возможно, более целесообразно добавлять железо в композицию в форме соли или комплекса железа II, например в форме перечисленных выше солей железа II.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такие уровни железа, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 40 мг.
В одном варианте осуществления питательная композиция в соответствии с настоящим изобретением содержит цинк. Цинк может содержаться в композиции настоящего изобретения в количестве, составляющем до 99,999% композиции.
В частности, цинк может содержаться в композиции в количестве более 0,08 мг, более 0,3 мг, более 0,5 мг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит цинк в количестве, выбранном из группы, состоящей из следующего; в диапазоне от 0,5 до 8 мг, от 2 до 5,5 мг, от 2,5 до 4,5 мг, от 3 до 4 мг, от 4 до 7,5 мг, от 6 до 7,5 мг, причем все веса приведены из расчета на 100 г сухой композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такие уровни цинка, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 302,4 мг/день или не будет превышать 245 мг/день, или не будет превышать 166 мг/день, или не будет превышать 98,9 мг/день, или не будет превышать 95,6 мг/день.
Цинк может входить в состав композиции изобретения в форме физиологически приемлемой соли, такой как, например, нитрат цинка, сульфат цинка, глюконат цинка, ацетат цинка или их смеси, или в форме физиологически приемлемого комплекса цинка (такого как, например, пиколинат цинка) или их смесей.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит медь. Медь может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, медь может содержаться в композиции в количестве более 10 мкг, более 40 мкг, более 60 мкг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит медь в количестве, выбранном из группы, состоящей из следующего; более 100 мкг, в диапазоне от 100 мкг до 850 мкг, от 180 до 650 мкг, от 200 до 400 мкг, от 210 до 300 мкг, от 210 до 240 мкг, от 450 до 850 мкг, от 800 до 840 мкг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такие уровни меди, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 1426 мкг в день или не будет превышать 488 мкг в день.
Медь может быть включена в состав композиции настоящего изобретения как таковая или в форме физиологически приемлемой соли и/или посредством любого источника, содержащего медь, в частности Cu2+. Например, медь может быть включена в композицию в форме: сульфата меди и/или глюконата меди, и/или карбоната меди, и/или цитрата меди, и/или комплекса медь-лизин.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит магний. Магний может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, магний может содержаться в композиции в количестве более 0,2 мг, более 0,35 мг, более 0,5 мг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит магний в количестве, выбранном из группы, состоящей из следующего; в диапазоне от 0,35 до 90 мг, в диапазоне от 25 до 70 мг, от 30 до 65 мг, от 35 до 60 мг, от 40 до 50 мг, от 35 до 55 мг, причем все веса приведены из расчета на 100 г сухой композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такие уровни магния, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 110 мг в день или не будет превышать 65 мг в день.
Магний может быть включен в состав композиции настоящего изобретения как таковой или в форме физиологически приемлемой соли и/или посредством любого источника, содержащего магний, в частности Mg2+. Например, карбонат магния, хлорид магния, оксид магния, сульфат магния, глюконат магния, гидроксид магния, соли магния лимонной кислоты, соли магния ортофосфорной кислоты.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит кальций. Кальций может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, кальций может содержаться в композиции в количестве более 0,84 мг, более 2,52 мг, более 4,62 мг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит кальций в количестве, выбранном из группы, состоящей из следующего; в диапазоне от 84 до 760 мг, в диапазоне от 200 до 550 мг, в диапазоне от 250 до 450 мг, в диапазоне от 280 до 520 мг, от 350 до 650 мг, причем все веса приведены из расчета на 100 г сухой композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такие уровни кальция, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 482 мг в день или не будет превышать 477 мг в день.
Кальций может быть включен в состав композиции настоящего изобретения как таковой или в форме физиологически приемлемой соли и/или посредством любого источника, содержащего кальций, в частности Ca2+. Например, карбонат кальция, хлорид кальция, кальциевые соли лимонной кислоты, глюконат кальция, глицерофосфат кальция, лактат кальция, гидроксид кальция, кальциевые соли ортофосфорной кислоты.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит фосфор. Фосфор может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, фосфор может содержаться в композиции в количестве более 1,7 мг, более 14,3 мг, более 27,3 мг на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит фосфор в количестве, выбранном из группы, состоящей из следующего; в диапазоне от 17 до 516 мг, в диапазоне от 129 до 400 мг, в диапазоне от 140 до 390 мг, в диапазоне от 150 до 370 мг, от 160 до 365 мг, в диапазоне от 270 до 350 мг, от 200 до 360 мг, причем все веса приведены из расчета на 100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит такие уровни фосфора, что суммарное дневное потребление, обеспечиваемое питательной композицией изобретения, не будет превышать 863 мг в день или не будет превышать 787 мг в день.
Фосфор может быть включен в состав композиции настоящего изобретения как таковой или в форме физиологически приемлемой соли и/или посредством любого источника, содержащего фосфор, например фосфата кальция, гидрофосфата кальция.
Композиция, содержащая минеральное вещество, например одно или более из железа, цинка, меди, кальция, магния и фосфора, может быть особенно эффективной для поддержки, стимулирования или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга в одной или более из следующих областей мозга; мозжечке, зрительной коре, двигательной и соматосенсорной коре, мозолистом теле, лобной коре, височном белом веществе, внутренней капсуле, префронтальной коре двигательной коре. Перечисленные области головного мозга связаны с моторной функцией (включая координацию и выполнение движений), зрительной функцией, полушарным взаимодействием, исполнительной функцией, кратковременной памятью, решением задач, социально-эмоциональным функционированием, языком, функцией слухового восприятия, решением задач и/или кратковременной памятью.
В одном варианте осуществления композиция изобретения содержит фосфолипид его метаболический предшественник или метаболит.
Термин «фосфолипид» при использовании в настоящем документе относится к любому фосфолипиду и, в частности, к соединению формулы (I)
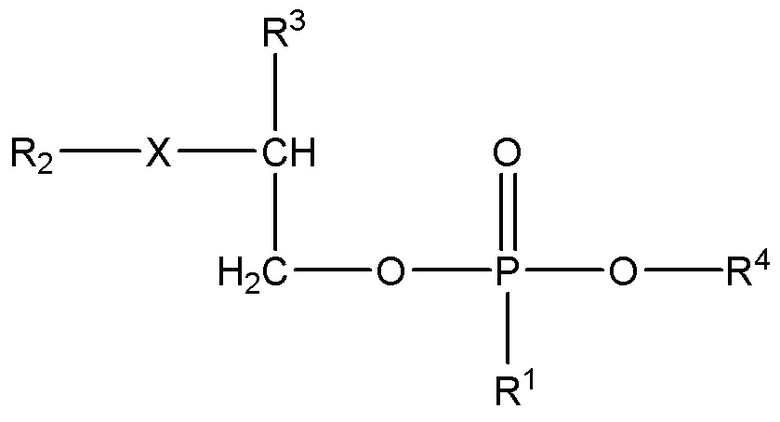
(I),
где
R1 представляет собой O,
X представляет собой NH или O
R2 представляет собой насыщенную или ненасыщенную линейную или разветвленную C2-C44 ацильную группу;
R3 представляет собой заместитель с формулой (II) или формулой (III)
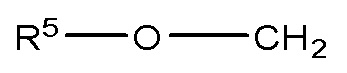
(II)
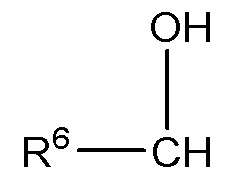
(III),
где R5 представляет собой насыщенную или ненасыщенную линейную или разветвленную C2-C44 ацильную группу, и
R6 представляет собой насыщенную C2-C44 алкильную или алкенильную группу; и
R4 выбирают из; C5 или C6 замещенной или незамещенной циклической алкильной или алкенильной группы, или
-(CH2)n-R7, где n представляет собой целое число в диапазоне от 1 до 4, в частности от 1 до 2, а R7 представляет собой -N(CH3), NH3 или заместитель с формулой (IV) и,

(IV),
в частности, R4 представляет собой C6 циклическую алкильную или алкенильную группу, замещенную одной или более гидроксигруппами, конкретнее R4 получена из инозитола (C6H12O6), и еще конкретнее миоинозитола, т.е. R4 представляет собой:
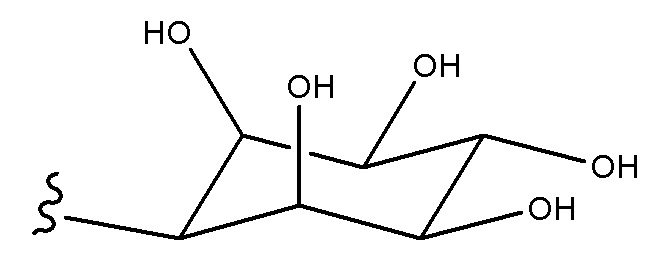
К не имеющим ограничительного характера примерам фосфолипидов относятся фосфатидилинозитол, фосфатидилсерин, фосфатидилэтаноламин, сфингомиелин и фосфатидилхолин.
В одном варианте осуществления настоящего изобретения фосфолипид выбирают из группы, состоящей из; фосфатидилхолина, фосфатидилинозитола, фосфатидилсерина, фосфатидилэтаноламина, сфингомиелина и/или их комбинации.
Фосфатидилинозитол представляет собой соединение формулы (V)
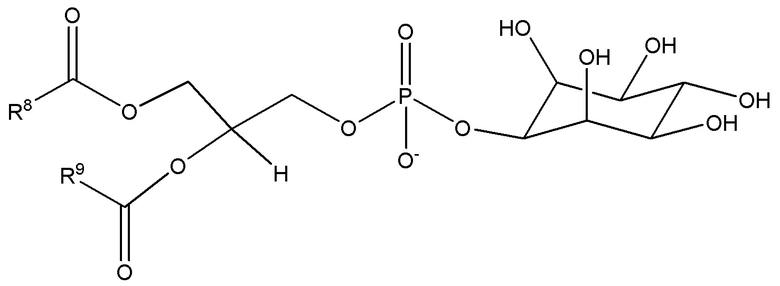
(V),
где R8 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43, и
R9 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R8 и R9 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C43, которые вместе со своими соседствующими карбонильными группами соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C44, и, еще более конкретно, R8 и R9 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C23, которые вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24.
Более конкретно, R8 и R9 представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C23, которые вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24, причем жирные кислоты, определяющие такие остатки жирных кислот, выбирают из группы, состоящей из; C14:0, C15:0, C16:0, C18:0, C20:0, C20:3, C20:4, C21:0, C22:0, C23:0, C24:0, C18:1n-9, C18:2n-6 и C24:1n-9. Еще более конкретно - C18:0, C18:1n-9, C18:2, C20:3 и C20:4.
Как будет очевидно специалисту в данной области. Термин «фосфатидилсерин» при использовании в настоящем документе относится к фосфатидил-L-серину.
Фосфатидилсерин представляет собой соединение формулы (VI)

(VI),
(VI),
где R10 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43, и
R11 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R10 и R11 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C43, которые вместе со своими соседствующими карбонильными группами соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C44, и, еще более конкретно, R10 и R11 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C23, которые вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24.
Более конкретно, R10 и R11 представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C23, которые вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24, причем жирные кислоты, определяющие такие остатки жирных кислот, выбирают из группы, состоящей из; C14:0, C15:0, C16:0, C18:0, C20:0, C20:3, C20:4, C21:0, C22:0, C23:0, C24:0, C18:1n-9, C18:2n-6 и C24:1n-9. Еще более конкретно - C18:0, C18:1n-9, C20:4 и C22:6.
Фосфатидилэтаноламин представляет собой соединение формулы (VII)
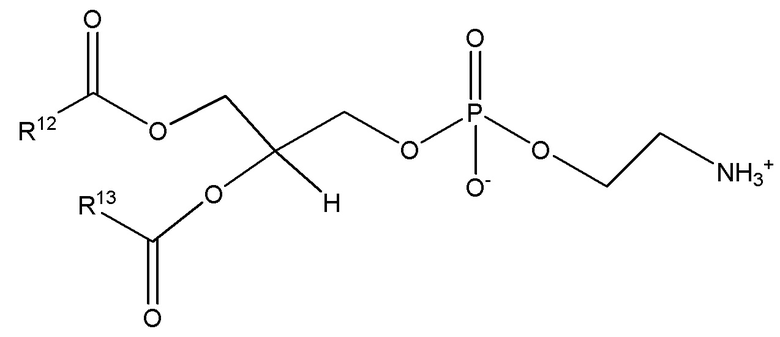
(VII),
где R12 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43, и
R13 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R12 и R13 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C43, которые вместе со своими соседствующими карбонильными группами соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C44, и, еще более конкретно, R12 и R13 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C23, которые вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24.
Термин «сфингомиелин» при использовании в настоящем документе относится к молекуле липида или смеси молекул липида, в которых сфингозиновый или сфинганиновый остов этерифицирован жирнокислотным остатком при аминогруппе (-NH2) посредством образования амидной связи и в которых гидроксильная группа в положении 1 сфингозинового остова связана с фосфорилхолиновой функциональной группой.
В частности, сфингомиелин представляет собой соединение формулы (VIII) или смесь соединений формулы (VIII)
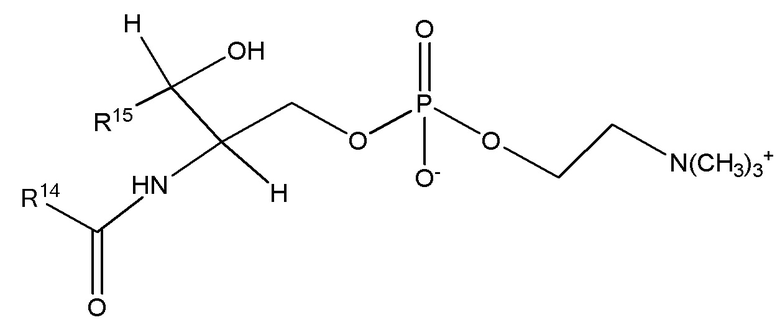
(VIII),
где
R14 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43,
R15 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R14 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C13 по C43, которая вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C44.
Не имеющие ограничительного характера примеры насыщенных или ненасыщенных жирных кислот с С14 по С44, которые могут определять такие остатки жирных кислот, включают; C14:0, C15:0, C16:0, C18:0, C20:0, C21:0, C22:0, C23:0, C24:1, C25:0, C28:1, C30:2, C30:1, C30:0, C32:3, C32:2, C32:1, C32:0, C33:1, C34:3, C34:2, C34:1, C34:0, C35:2, C35:0, C36:4, C36:3, C36:2, C36:1, C36:0, C37:1, C37:0, C38:4, C38:3, C38:1, C38:0, C39:1, C39:0, C40:2, C40:1, C40:0, C41:2, C41:1, C41:0, C42:47, C42:3, C42:2, C42:1, C42:0, C44:3, C44:1.
Более конкретно, R14 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C13 по C23, которая вместе со своей соседствующей карбонильной группой соответствует остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24, причем жирные кислоты, определяющие такие остатки жирных кислот, выбирают из группы, состоящей из; C14:0, C15:0, C16:0, C18:0, C20:0, C21:0, C22:0, C23:0, C24:0, C18:1n-9, C18:2n-6 и C24:1n-9.
Еще более конкретно, сфингомиелин представляет собой смесь соединений формулы (VIII), причем смесь составляют таким образом, что суммарное число жирнокислотных остатков (R14 вместе с прилегающей карбонильной группой), содержащихся в смеси, преобладающим образом представлено насыщенными жирными кислотами, и в наименьшей степени преобладают ненасыщенные жирные кислоты. Более конкретно, смесь составляют таким образом, что от 80% до 96% упомянутых жирнокислотных остатков в смеси являются насыщенными жирными кислотами, в частности насыщенными жирными кислотами C14, C15, C16, C18, C20, C22, C23, C24, более конкретно - C16, C18, C20, C22 и C24.
Фосфатидилхолин представляет собой соединение формулы (IX)

(IX),
где R16 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43, и
R17 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R16 и R17 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C43, которые вместе со своими соседствующими карбонильными группами соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C44, и, еще более конкретно, R16 и R17 независимо друг от друга представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C23, которые вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24.
Более конкретно, R16 и R17 представляют собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C13 по C23, которые вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24, причем жирные кислоты, определяющие такие остатки жирных кислот, выбирают из группы, состоящей из; C14:0, C15:0, C16:0, C16:1, C18:0, C20:0, C20:1, C20:3, C20:4, C21:0, C22:0, C22:6, C23:0, C24:0, C18:1n-9, C18:2n-6 и C24:1n-9. Еще более конкретно - C14:0, C16:0, C18:0, C18:1n-9, C18:2n-6, C20:1, C20:3, C20:4 и C22:6.
Фосфолипид, его метаболический предшественник и/или метаболит может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
В частности, сфингомиелин, его метаболический предшественник и/или метаболит может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
Более конкретно, композиция будет содержать сфингомиелин в количестве более 200 мг/кг сухого веса композиции, более конкретно - в диапазоне от 200 мг до 2,5 г/кг сухого веса композиции.
В одном варианте осуществления композиция содержит сфингомиелин в количестве, выбранном из группы, состоящей из; более 200 мг/кг, более 300 мг/кг, в диапазоне от 200 мг до 2,5 г/кг, в диапазоне от 200 мг до 2 г/кг, в количестве в диапазоне от 300 мг до 1,5 г/кг или от 400 мг до 1 г/кг, в диапазоне от 200 до 850 мг/кг, или от 300 до 820 мг/кг. Все веса приведены из расчета на сухой вес композиции.
В частности, фосфатидилхолин, его метаболический предшественник и/или метаболит может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
Более конкретно, композиция будет содержать фосфатидилхолин в количестве более 200 мг/кг сухого веса композиции, более конкретно - в диапазоне от 200 мг до 2,5 г/кг сухого веса композиции.
В одном варианте осуществления композиция содержит фосфатидилхолин в количестве, выбранном из группы, состоящей из; более 200 мг/кг, более 300 мг/кг, более 400 мг/кг, в диапазоне от 200 мг до 2,5 г/кг, в диапазоне от 200 мг до 2 г/кг, в количестве в диапазоне от 300 мг до 1,5 г/кг или от 400 мг до 1 г/кг, от 500 до 1,3 г/кг. Все веса приведены из расчета на сухой вес композиции.
В частности, фосфатидилинозитол, его метаболический предшественник и/или метаболит может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
Более конкретно, композиция будет содержать фосфатидилинозитол в количестве более 50 мг/кг сухого веса композиции, более конкретно - в диапазоне от 200 мг до 1,5 г/кг сухого веса композиции.
В одном варианте осуществления устройство содержит фосфатидилинозитол в количестве, выбранном из группы, состоящей из; более 200 мг/кг, более 300 мг/кг, в диапазоне от 200 мг до 2,5 г/кг, в диапазоне от 200 мг до 2 г/кг, в количестве в диапазоне от 250 мг до 800 мг/кг или от 400 мг до 1,5 г/кг, или от 400 мг до 800 мг/кг. Все веса приведены из расчета на сухой вес композиции.
В частности, фосфатидилсерин, его метаболический предшественник и/или метаболит может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
Более конкретно, композиция будет включать фосфатидилсерин в количестве более 50 мг/кг сухого веса композиции, более 200 мг/кг сухого веса композиции, более конкретно - в диапазоне от 150 мг до 1,5 г/кг сухого веса композиции, от 200 мг до 1 г/кг сухого веса композиции.
В одном варианте осуществления устройство содержит фосфатидилсерин в количестве, выбранном из группы, состоящей из; более 150, более 200 мг/кг, более 300 мг/кг, в диапазоне от 200 мг до 2,5 г/кг, в диапазоне от 200 мг до 2 г/кг, в количестве в диапазоне от 250 мг до 1000 мг/кг или от 400 мг до 1 г/кг. Все веса приведены из расчета на сухой вес композиции.
В частности, фосфатидилэтаноламин, его метаболический предшественник и/или метаболит может содержаться в композиции настоящего изобретения в количестве до 99,999% композиции.
Более конкретно, композиция будет содержать фосфатидилэтаноламин в количестве более 150 мг/кг сухого веса композиции, более 200 мг/кг сухого веса композиции, более конкретно - в диапазоне от 150 мг до 1,5 г/кг сухого веса композиции.
В одном варианте осуществления устройство содержит фосфатидилэтаноламин в количестве, выбранном из группы, состоящей из; более 170 мг/кг, более 180 мг/кг, более 200 мг/кг, в диапазоне от 200 мг до 2,5 г/кг, в диапазоне от 200 мг до 2 г/кг, в количестве в диапазоне от 250 мг до 800 мг/кг или от 200 мг до 1г/кг. Все веса приведены из расчета на сухой вес композиции.
В одном варианте осуществления композиция изобретения содержит фосфолипиды, включая фосфатидилинозитол, фосфатидилсерин, фосфатидилэтаноламин, сфингомиелин и фосфатидилхолин, так что суммарная концентрация не превышает 15,4 г/кг.
Если метаболический предшественник и/или метаболит одного или более фосфолипидов используется в композиции вместо фосфолипида или в комбинации ним, упомянутые соединения могут использоваться в таких количествах, что уровень фосфолипидов, физиологически доставляемых упомянутой композицией, находится в соответствии с заданным выше. Способность определять соответствующие количества входит в сферу компетенции специалиста в данной области.
Термин «метаболический предшественник» и/или «метаболит» одного или более фосфолипидов при использовании в настоящем документе не включает холин.
Не имеющими ограничительного характера примерами метаболических предшественников и/или метаболита фосфолипидов, в частности сфингомиелина, фосфатидилхолина, фосфатидилинозитола, фосфатидилсерина и/или фосфатидилэтаноламина, являются: галактоцерамиды, сфингозин, сфингозин-1-фосфат, церамид, D-эритродигидроцерамид и церамид-1-фосфат и ганглиозиды.
Особенно эффективными фосфолипидами могут быть фосфатидилхолин, фосфатидилсерин, фосфатидилинозитол и/или сфингомиелин, в частности сфингомиелин.
В одном варианте осуществления настоящего изобретения фосфолипид представляет собой фосфатидилхолин, фосфатидилсерин, фосфатидилинозитол, сфингомиелин и/или метаболический предшественник и/или метаболит любого из перечисленного, и/или комбинация любого из перечисленного. В частности, фосфолипид представляет собой сфингомиелин, его метаболический предшественник и/или метаболит.
Особенно эффективными метаболическими предшественниками и/или метаболитом фосфолипидов, в частности сфингомиелина, могут быть церамид и ганглиозиды, и церамид-1-фосфат, и d-эритродигидроцерамид.
Термином «церамид» обозначают молекулу липида, в которой остов сфингозина или сфинганина этерифицирован жирнокислотным остатком с образованием амидной связи. При использовании термина «церамид» в настоящем описании он может обозначать индивидуальное церамидное соединение, а также смесь индивидуальных церамидных соединений.
В частности, церамид представляет собой соединение формулы (IXa) или смесь соединений формулы (IXa)
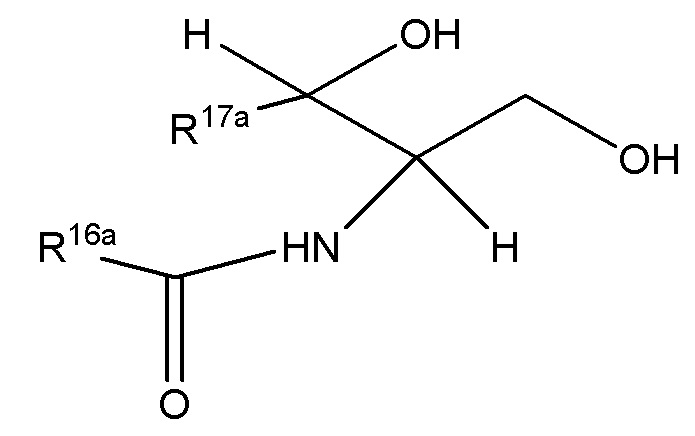
(IXa),
где
R16а представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43,
R17а представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R16а представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C13 по C43, которая вместе со своей соседствующей карбонильной группой соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C14 по C44.
Не имеющие ограничительного характера примеры насыщенных или ненасыщенных жирных кислот с С14 по С44, которые могут определять такие остатки жирных кислот, включают; C14:0, C15:0, C16:0, C18:0, C20:0, C21:0, C22:0, C23:0, C24:1, C25:0, C28:1, C30:2, C30:1, C30:0, C32:3, C32:2, C32:1, C32:0, C33:1, C34:3, C34:2, C34:1, C34:0, C35:2, C35:0, C36:4, C36:3, C36:2, C36:1, C36:0, C37:1, C37:0, C38:4, C38:3, C38:1, C38:0, C39:1, C39:0, C40:2, C40:1, C40:0, C41:2, C41:1, C41:0, C42:47, C42:3, C42:2, C42:1, C42:0, C44:3, C44:1.
Более конкретно, R16а представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C13 по C23, которая вместе со своей соседствующей карбонильной группой соответствует остаткам насыщенных или ненасыщенных жирных кислот с C14 по C24, причем жирные кислоты, определяющие такие остатки жирных кислот, выбирают из группы, состоящей из; C14:0, C15:0, C16:0, C18:0, C20:0, C21:0, C22:0, C23:0, C24:0, C18:1n-9, C18:2n-6, и C24:1n-9, и, в частности, группы, состоящей из: C16:0, C18:0, C20:0, C22:0 и C24:0.
Еще более конкретно, церамид представляет собой смесь соединений формулы (IXа), причем смесь составляют таким образом, что суммарное число жирнокислотных остатков (R16а вместе с прилегающей карбонильной группой), содержащихся в смеси, преобладающим образом представлено насыщенными жирными кислотами, и в наименьшей степени преобладают ненасыщенные жирные кислоты. Более конкретно, смесь составляют таким образом, что от 80% до 96% упомянутых жирнокислотных остатков в смеси являются насыщенными жирными кислотами, в частности насыщенными жирными кислотами C14, C15, C16, C18, C20, C22, C23, C24, более конкретно - C16, C18, C20, C22 и C24.
Термин «ганглиозид» при использовании в настоящем документе обозначает липидную молекулу олигогликозилцерамида, содержащую остаток церамида формулы IXa в соответствии с определением в настоящем документе. При использовании термина «ганглиозид» в настоящем описании он может обозначать индивидуальное ганглиозидное соединение, а также смесь индивидуальных ганглиозидных соединений, содержащих остаток церамида формулы IXa в соответствии с определением в настоящем документе.
Особенно эффективными ганглиозидами могут быть ганглиозиды из моносиалоганглиозидов-3 (GM3) и/или ганглиозиды из дисиалоганглиозидов-3 (GD3).
Церамид-1-фосфат и d-эритродигидроцерамид будут содержать остаток церамида формулы IXa в соответствии с определением в настоящем документе.
Ганглиозиды и/или церамиды, и/или церамид-1-фосфат, и/или d-эритродигидроцерамид могут входить в состав композиции в любых количествах.
Концентрации в диапазоне 2-11,5 мг/100 г для GD3 и/или GM3 могут быть особенно эффективными.
Сфингомиелин может быть синтезирован из церамида и фосфатидилхолина соответственно, может быть особенно целесообразно использовать церамид и/или один или более ганглиозидов в комбинации с фосфатидилхолином его метаболическим предшественником или метаболитом.
Фосфолипид, его метаболические предшественники и/или метаболит, содержащиеся в композиции настоящего изобретения могут быть природными, искусственными или представлять собой смесь вышеупомянутого. Упомянутые метаболические предшественники и/или метаболит могут использоваться в композиции изобретения в своем чистом виде или в по существу чистом виде. В альтернативном варианте осуществления их могут добавлять в форме содержащего их источника.
В настоящем изобретении может использоваться любой источник фосфолипида его метаболических предшественников и/или метаболита, пригодный для применения вовнутрь субъектом, для потребления которым предназначена данная композиция.
В частности, фосфолипид, его метаболический предшественник или метаболит будут получены из природных источников, к не имеющим ограничительного характера примерам которых относятся яйца, соя, коровьи мозги и/или молоко млекопитающих или его экстракты. Не имеющие ограничительного характера примеры источников сои включают пищевую добавку лецитин, не имеющие ограничительного характера примеры молока млекопитающих включают коровье, верблюжье, овечье, козье молоко, в том числе снятое молоко. Не имеющие ограничительного характера примеры экстрактов молока включают белковые экстракты, например сывороточный белок и казеин, мембраны жировых глобул молока (MFGM) и содержащие их экстракты.
Особенно полезным источником фосфолипидов, их метаболического предшественника или метаболита, в частности сфингомиелина, который может использоваться в настоящем изобретении, может быть концентрат сывороточного белка коровьего молока, обогащенный альфа-лактальбумином, и/или неочищенный альфа-лактальбумин, который был экстрагирован из сывороточного белка молока, в частности сывороточного белка коровьего молока.
Альфа-лактальбумин представляет собой высококачественный, легко перевариваемый, например, младенцами человека, сывороточный белок и является основным белком, присутствующим в ГМ. Альфа-лактальбумин и/или обогащенная альфа-лактальбумином молочная фракция идеально подходит для детских смесей с пониженным содержанием белка благодаря высокому содержанию незаменимых аминокислот, в частности триптофана. Несмотря на то, что альфа-лактальбумин сам по себе является белком, неочищенные источники могут содержать сфингомиелин.
В одном варианте осуществления фосфолипид, его метаболический предшественник или метаболит, в частности сфингомиелин, используется в форме концентрата сывороточного белка, обогащенного альфа-лактальбумином, или как альфа-лактальбумин.
В более конкретном варианте осуществления используется концентрат сывороточного белка коровьего молока, обогащенный альфа-лактальбумином, или альфа-лактальбумин с содержанием фосфолипида, в частности с содержанием сфингомиелина более 500 мг/100 г, 900 мг/100 г, 1000 мг/100 г сухого веса композиции.
Другим особенно полезным источником фосфолипидов, их метаболического предшественника или метаболита могут быть мембраны жировых глобул молока (в дальнейшем MFGM) или содержащие их экстракты, в частности MFGM или содержащие их экстракты из коровьего молока. Может быть особенно полезно, если MFGM или содержащие их экстракты содержат по меньшей мере 1%, 2%, 5%, 10%, 20%, 30%, 40% фосфолипидов и/или по меньшей мере 0,1%, 0,2%, от 0,5% до 5%, от 0,8% до 3%, от 1% до 2%, 1,6%, 1,9%, 1,8% фосфатидилхолина, фосфатидилинозитола, фосфатидилсерина, фосфатидилэтаноламина и/или сфингомиелина. MFGM могут также дополнительно содержать магний, фосфор и или кальций, в частности, в концентрациях в диапазоне от 0,05% до 2%, от 0,1% до 0,4%.
Композиция, содержащая фосфолипид и/или его метаболический предшественник и/или метаболит, в частности сфингомиелин, фосфатидилхолин и/или фосфатидилинозитол, может быть особенно эффективной для поддержки, стимулирования или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга в одной или более из следующих областей головного мозга; мозжечке, зрительной коре, мозолистом теле, внутренней капсуле, лобной доле, теменной доле, височной доле, двигательной коре, лобной коре. Такие области головного мозга связаны с одной или более из следующих функций: зрением, двигательной функцией (включая координацию и выполнение движений), полушарным взаимодействием, языковой функцией, функцией слухового восприятия (включая выслушивание и внимание), краткосрочной памятью, исполнительной функцией, включая решение задач, обработкой социальной информации и поведенческим взаимодействием, пространственным мышлением и языком.
В одном варианте осуществления композиция изобретения содержит производное жирной кислоты.
Производное жирной кислоты может содержаться в композиции настоящего изобретения в количестве, составляющем до 99,999% композиции.
Термин «производное жирной кислоты» при использовании в настоящем документе относится к содержащему жирную кислоту соединению, отличному от фосфолипида, и, в частности, к свободной жирной кислоте и/или к моноацилглицерину (в дальнейшем MAG) и/или диацилглицерину (в дальнейшем DAG), и/или трицацилглицерину (в дальнейшем TAG), и/или сложному эфиру холестерина. Более конкретно, данный термин относится к MAG, DAG, TAG или сложному эфиру холестерина. Еще более конкретно, данный термин относится к TAG.
Термин «MAG» при использовании в настоящем документе относится к молекуле глицерина, в которой одна из ОН-групп образовала сложноэфирную связь с жирной кислотой. В частности, термин «MAG» при использовании в настоящем документе относится к соединению формулы (X)
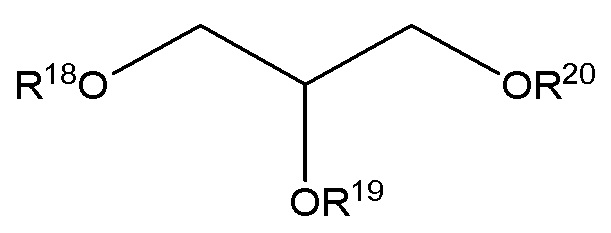
(X),
где
два из R18, R19 или R20 представляют собой H и где одно из R18, R19 или R20 представляет собой насыщенную или ненасыщенную ацильную группу с C4 по C44.
Более конкретно, два из R18, R19 или R20 представляют собой H, и одно из R18, R19 или R20 представляет собой насыщенную или ненасыщенную ацильную группу от C10 до C24, и еще более конкретно - насыщенную или ненасыщенную ацильную группу с C14 по C24.
Термин «DAG» при использовании в настоящем документе относится к молекуле глицерина, в которой две из ОН-групп образовали сложноэфирную связь с двумя жирными кислотами. В частности, термин «DAG» при использовании в настоящем документе относится к соединению формулы (X),
где
одно из R18, R19 или R20 представляет собой H, и где два из R18, R19 или R20 представляют собой насыщенную или ненасыщенную ацильную группу с C4 по C44. Более конкретно, насыщенную или ненасыщенную ацильную группу с C10 по C24, и еще более конкретно - насыщенные или ненасыщенные ацильные группы с C14 по C24. Две насыщенные или ненасыщенные ацильные группы с C4 по C44 из R18 R19 или R20 могут быть одинаковыми или различными.
Термин «TAG» при использовании в настоящем документе относится к молекуле глицерина, в которой три ОН-группы образовали сложноэфирную связь с тремя жирными кислотами. В частности, термин «TAG» при использовании в настоящем документе относится к соединению формулы (X),
где
где все из R18, R19 или R20 представляют собой насыщенные или ненасыщенные ацильные группы с C4 по C44, более конкретно - насыщенные или ненасыщенные ацильные группы с C10 по C24, и еще более конкретно - насыщенные или ненасыщенные ацильные группы с C14 по C24. Три насыщенные или ненасыщенные ацильные группы с C4 по C44 могут все быть одинаковыми, все различными, или же две группы могут быть одинаковыми, а одна отличаться от них.
Термин «сложный эфир холестерина» при использовании в настоящем документе относится к соединению формулы (XI)
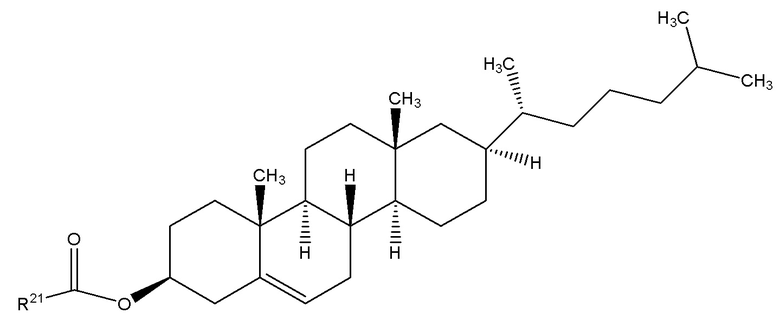
(XI),
где
R21 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R21 представляет собой разветвленные или неразветвленные ациклические алкильные или ациклические алкенильные группы с C9 по C43, которые вместе со своими соседствующими карбонильными группами соответствуют остаткам насыщенных или ненасыщенных жирных кислот с C10 по C44, и еще более конкретно - остаткам насыщенных или ненасыщенных жирных кислот с С14 по С24.
Термин «жирная кислота» при использовании в настоящем документе относится к соединению формулы (XII)
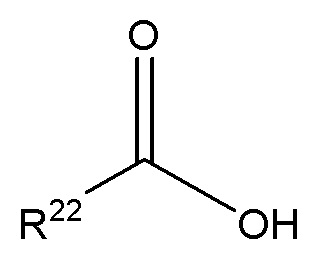
(XII),
где
R22 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C2 по C43.
Более конкретно, R22 представляет собой разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C9 по C43, еще более конкретно - разветвленную или неразветвленную ациклическую алкильную или ациклическую алкенильную группу с C13 по C23.
Не имеющие ограничительного характера примеры насыщенных или ненасыщенных жирных кислоты с С10 по С44, которые могут содержаться в производном жирной кислоты, т.е. могут представлять собой свободную жирную кислоту или жирную кислоту, которая определяет остаток (-ки) такой жирной кислоты в MAG, DAG, TAG и/или сложном эфире холестерина, включают; C10:0, C12:0, C14:0, C15:0, C16:0, C16:1n-7, C18:0, C18:1n-7, C18:1n-9, C18:2n-6, 18:3n-3, C20:0, C20:1n-9, C20:2n-6, C20:3n-6, C20:4n-6, 20:5n-3, C21:0, C22:0, C22:1n-9, C22:6n-3 C23:0, C24:1, в частности 24:1n-9, C25:0, C28:1, C30:2, C30:1, C30:0, C32:3, C32:2, C32:1, C32:0, C33:1, C34:3, C34:2, C34:1, C34:0, C35:2, C35:0, C36:4, C36:3, C36:2, C36:1, C36:0, C37:1, C37:0, C38:4, C38:3, C38:1, C38:0, C39:1, C39:0, C40:2, C40:1, C40:0, C41:2, C41:1, C41:0, C42:47, C42:3, C42:2, C42:1, C42:0, C44:3, C44:1. В частности, упомянутые жирные кислоты будут выбраны из группы, состоящей из: C10:0, C12:0, C14:0, C16:0, C16:1n-7, C18:0, C18:1n-7, C18:1n-9, C18:2n-6, 18:3n-3, C20:0, C20:1n-9, C20:2n-6, C20:3n-6, C20:4n-6, 20:5n-3, C22:0, C22:1n-9, C22:6n-3, C24:1, 24:1n-.
В настоящем изобретении может использоваться любое производное жирных кислот, пригодное для применения вовнутрь субъектом, для потребления которым предназначается данная композиция.
В частности, такое производное жирных кислот может поступать из природных источников, не имеющими ограничительного характера примерами которых являются яйца, водоросли, рыбий жир, плесневые грибы, дрожжи, семена, растения, например соя, и животные источники, например коровьи мозги и/или молоко млекопитающих или его экстракты. Не имеющие ограничительного характера примеры источников сои включают пищевую добавку лецитин, не имеющие ограничительного характера примеры молока млекопитающих включают коровье, верблюжье, овечье, козье молоко, в том числе снятое молоко. Не имеющие ограничительного характера примеры экстрактов молока включают белковые экстракты, мембраны жировых глобул молока (MFGM) и содержащие их экстракты. Источником производных жирных кислот могут также быть пальмовое масло, говяжий жир, свиное сало, хлопковое масло, арахисовое масло.
Может быть особенно полезно, если производное жирных кислот содержит насыщенную или ненасыщенную жирную кислоту, выбранную из группы, состоящей из: C20:4n-6, C22:6n-3, C24:1n-9, C16:0, C18:1n-9 и C18.0. В частности, C20:4n-6 и/или C22:6n-3, и/или C18:0. Более конкретно - 22:6n-3 и/или C18:0.
Композиция, содержащая фосфолипид, в частности сфингомиелин, фосфатидилхолин, фосфатидилсерин, фосфатидилинозитол, более конкретно - сфингомиелин, может быть особенно эффективной при использовании в комбинации с одной или более из перечисленных жирных кислот.
C20:4n-6 обозначает арахидоновую кислоту (в дальнейшем ARA или AA). C22:6n-3 обозначает докозагексаеновую кислоту (в дальнейшем DHA). 24:1n-9 обозначает нервоновую кислоту. C18.0 обозначает стеариновую кислоту. C16:0 обозначает пальмитиновую кислоту. C18:1n-9 обозначает олеиновую кислоту.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит производное жирной кислоты, содержащее DHA и/или ARA, и/или нервоновую кислоту, и/или стеариновую кислоту, в частности производное жирной кислоты, содержащее DHA и/или ARA, и/или стеариновую кислоту. Более конкретно - производное жирной кислоты, содержащее DHA и/или стеариновую кислоту.
Производное жирной кислоты, содержащее DHA и/или ARA, и/или нервоновую кислоту, и/или стеариновую кислоту, может содержаться в композиции настоящего изобретения в количестве, составляющем до 99,999% композиции.
В частности, производное жирной кислоты, содержащее DHA и/или ARA, и/или нервоновую кислоту, и/или стеариновую кислоту, может содержаться в композиции настоящего изобретения в количестве от 15 до 350 мг/100 г сухого веса композиции, более конкретно - от 30 мг до 300 мг/100 г сухого веса композиции.
В одном варианте осуществления композиция в соответствии с настоящим изобретением включает производное жирной кислоты, содержащее DHA и/или ARA, и/или нервоновую кислоту, и/или стеариновую кислоту, в количестве, выбранном из группы, состоящей из следующего; более 15 мг/100 г, более 30 мг/100 г, более 50 мг/100 г, более 55 мг/100 г, в диапазоне от 30 до 300 мг/100 г, в диапазоне от 30 до 200 мг/100 г или от 30 до 150 мг/100 г, в диапазоне от 50 до 300 мг/100 г, в диапазоне от 50 до 200 мг/100 г, в диапазоне от 50 до 150 мг/100 г, в диапазоне от 150 до 350, в диапазоне от 60 до 350 мг/100 г, в диапазоне от 60 до 120 мг/100 г, в диапазоне от 100 до 110 мг/100 г. Все концентрации приведены из расчета на сухой вес композиции.
Производные жирных кислот, содержащие стеариновую кислоту, присутствуют в природных источниках, например в пальмовом масле, говяжьем жире, свином сале, хлопковом масле, арахисовом масле.
Производные жирных кислот, содержащие нервоновую кислоту, присутствуют в природных источниках, например в маслах из семян Cardamine gracea, Heliphila longifola, Thlaspi perfoliatum, Tropaeolum speciosum, Lunaria biennis, Lunaria annua и Malania oleifera; в плесневых грибах Neocallismastix frontalis, Erysiphe graminis и Sphaerotheca humuli; в бактерии Pseudomonas atlantica; в дрожжах Saccharomyces cerevisiae и морской диатомовой водоросли Nitzschia cylindrus.
Производные жирных кислот, содержащие DHA и/или ARA, присутствуют в природных источниках, в таких как, например, яйца, водоросли, грибы, рыбий жир, и в растениях.
Масла, в состав которых входят производные жирных кислот, содержащие DHA и/или ARA и в общем случае другие полиненасыщенные жирные кислоты (ПНЖК), в частности EPA (эйкозапентаеновая кислота), могут иметь различное происхождение. Предпочтительно, производные жирных кислот, содержащие DHA, поставляются в форме рыбьего жира, в состав которого входят производные жирных кислот, содержащие DHA и/или ARA. Рыбий жир обычно содержит 5 мас. % или более, предпочтительно 10 мас. % или более производных жирных кислот, содержащих DHA и/или ARA. Также обычно доступны масла, в состав которых входят производные жирных кислот, содержащие DHA и/или ARA, извлекаемые из водорослей или микроорганизмов. Например, могут использоваться масла, получаемые из водорослей, содержащие 10 мас. % или более, например 20 мас. % или более производных жирных кислот.
Если питательная композиция в соответствии с настоящим изобретением содержит производные жирных кислот, содержащие ARA и DHA. Упомянутые ингредиенты, например, могут содержаться в композиции настоящего изобретения в количествах, которые приводят к весовому соотношению DHA : ARA в диапазоне от 4 : 1 до 1 : 4, например от 3 : 1 до 1 : 3, например от 2 : 1 до 1 : 2, например от 1,5 : 1 до 1 : 1,5, в частности от 1,1 : 1 до 1 : 1,1.
Также может быть полезно, если композиция настоящего изобретения содержит смесь производных жирных кислот причем, эта смесь формируется таким образом, что весовое соотношение ненасыщенных к насыщенным жирным кислотам и/или остаткам жирных кислот в композиции изобретения находится в диапазоне от 1 : 1 до 1 : 2; от 1 : 1,2 до 1 : 1,9, от 1 : 1,25 до 1 : 1,5; от 1 : 3 до 1 : 4.
Более того, если в композиции настоящего изобретения содержатся большие количества производных жирных кислот, содержащих DHA и/или ARA, может быть особенно полезно увеличить суммарное количество производных жирных кислот, содержащих насыщенные длинноцепочечные жирные кислоты, в частности C20/24. Такие насыщенные длинноцепочечные жирные кислоты могут быть важным компонентом миелина, способствуя его обертыванию и формированию его оболочки вокруг аксонов. Весовое соотношение DHA и/или AA к таким насыщенным длинноцепочечным жирным кислотам в композиции изобретения может, например, лежать в диапазоне от 1:1 до 1:10; от 1 : 2 до 1 : 9, от 1 : 3 до 1 : 4,5, от 1 : 3,5 до 1 : 4,5.
Композиция изобретения, содержащая производное жирной кислоты, например производное жирной кислоты, содержащее DHA и/или AA, может быть особенно эффективной для поддержки, стимулирования или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга в одной или более из следующих областей мозга: мозжечке, внутренней капсуле, теменной доле, двигательной и сенсорной коре (включая координацию и выполнение движений), визуальной коре, лобной коре. Перечисленные области головного мозга связаны со зрительной функцией, двигательной функцией и психомоторной функцией (включая координацию и выполнение движений) и/или исполнительной функцией и социально-эмоциональной функцией.
Специалист в области в состоянии определить соответствующие количества упомянутых выше питательных веществ, их метаболических предшественников или метаболитов, исходя из их природы, предназначения, целевого субъекта и дозы композиции, например сколько раз в день субъект будет употреблять композицию вовнутрь. Как правило, эффективная доза будет зависеть от возраста, размеров и состояния здоровья субъекта, от образа жизни субъекта, количества питательных веществ в композиции и, возможно, от пола субъекта.
Эффективной дозой может быть любая доза, которая способствует поддержке, стимулированию или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, и/или плотности нейронных связей, и/или интеллектуального потенциала, и/или когнитивного потенциала, и/или способности к обучению, и/или когнитивной функции у субъекта.
Для детской смеси или молочной смеси для детей от 1 до 3 лет специалист в области может определить исходные количества или соотношения соединений или питательных веществ, описанных в настоящем документе, например холина, относительно тех количеств, которые присутствуют в человеческом грудном молоке, вырабатываемом для младенца или ребенка того же возраста, в частности полноценно питающейся матерью.
Способность определять эффективную дозу на основании приведенной в настоящем документе информации и знаний в данной области входит в сферу компетенции специалиста в данной области.
В одном из вариантов осуществления композиция согласно настоящему изобретению содержит холин, витамин, в частности витамин B12 и/или фолиевую кислоту, фосфолипид, в частности фосфатидилхолин, и/или фосфатидилсерин, и/или фосфатидилинозитол, и/или сфингомиелин, и/или метаболический предшественник или метаболит любого из вышеперечисленных, минеральное вещество, в частности железо, и/или цинк, и/или кальций, и/или магний, и/или фосфор, и/или медь и производное жирной кислоты, в частности содержащее DHA и/или AA, и/или нервоновую кислоту, и/или стеариновую кислоту.
Особенно полезными концентрациями/количествами упомянутых ингредиентов в упомянутой композиции могут быть сфингомиелин в количестве по меньшей мере 300 или 420 мг/кг, в частности более 800 м/кг и более конкретно - более 900 мг/кг, фосфатидилхолин в количестве по меньшей мере 1000 мг/кг, фосфатидилсерин в количестве по меньшей мере 900 мг/кг, фосфатидилинозитол в количестве по меньшей мере 700 мг/кг, фолиевая кислота в количестве по меньшей мере 140 мг/кг, в частности по меньшей мере 160 мг/кг, витамин В12 в количестве по меньшей мере 2,34 мкг/100 г, в частности более 5 мкг/100 г, более конкретно - 7 мкг/100 г, железо в количестве по меньшей мере 6 мг/100 г или по меньшей мере 8,6 мг/100 г, более конкретно - 11,5 мг/100 г, еще более конкретно - более 16 мг/кг, холин в количестве по меньшей мере 124 мг/кг, более конкретно - 140 мг/кг, производное жирной кислоты, содержащее DHA, в количестве по меньшей мере 89 мг/100 г, производное жирной кислоты, содержащее AA, в количестве по меньшей мере 89 мг/100 г или по меньшей мере 175 мг/100 г, цинк в количестве по меньшей мере 4 или по меньшей мере 4,7 мг/100 г, более конкретно - 7 мг/100 г, кальций в количестве по меньшей мере 200 мг или по меньшей мере 500 мг/100 г, фосфор в количестве по меньшей мере 140 мг/100 г или по меньшей мере 350 мг/100 г, медь в количестве по меньшей мере 250 мкг/100 г или по меньшей мере 600 мкг/100 г, магний в количестве по меньшей мере 30 мг/100 г или по меньшей мере 50 мг/100 г. При этом все веса приведены из расчета на сухой вес композиции.
Концентрация, попадающая в пределы заданной ошибки для любой аналитической методики, используемой для измерения концентрации одного или более из перечисленных выше ингредиентов, должна рассматриваться как попадающая в диапазон концентраций, приводимых в настоящем документе.
В одном варианте осуществления композиция в соответствии с настоящим изобретением содержит холин, витамин B12 и/или фолиевую кислоту, сфингомиелин и/или его метаболический предшественник или метаболит, железо, цинк, а также производное жирной кислоты, содержащее DHA и/или AA.
В одном варианте осуществления композиция в соответствии с настоящим изобретением включает производное жирной кислоты, содержащее DHA и/или ARA, витамин В12 и/или фолиевую кислоту, сфингомиелин и железо.
В более конкретном варианте осуществления композиция в соответствии с настоящим изобретением включает производное жирной кислоты, содержащее DHA в концентрации 102 мг/100г, ARA в концентрации 102 мг/100 г, витамин В12 в концентрации 5,4 мкг/100 г, фолиевую кислоту в концентрации 169 мкг/100 г, сфингомиелин в концентрации 81,4 мг /100 г и железо в концентрации 6,7 мг/100 г.
Композицией настоящего изобретения может быть любого рода композиция, пригодная для непосредственного введения субъекту.
В частности, композиция будет представлять собой искусственную питательную композицию.
Используемый в настоящем документе термин «питательная композиция» относится к синтетической композиции, которая снабжает питанием субъекта. Такая питательная композиция может вводиться энтерально, парентерально или внутривенно. В частности, композиция будет приниматься энтерально и более конкретно - перорально.
В одном варианте осуществления настоящего изобретения упомянутая композиция будет представлять собой искусственную питательную композицию, выбранную из группы, состоящей из следующего; молочная смесь для детей от 1 до 3 лет, детская смесь или композиция для младенцев, которая предназначена для добавления или разбавления грудным молоком человека (в дальнейшем «ГМ»), например обогатитель ГМ, или продукт питания, предназначенный для потребления младенцем и/или ребенком как в чистом виде, так и в комбинации с ГМ, например прикорм.
Композиции настоящего изобретения также могут содержать любые другие ингредиенты или вспомогательные вещества, которые, как известно, можно использовать в этом типе композиции, например в детской смеси.
Не имеющие ограничительного характера примеры таких ингредиентов включают: белки, аминокислоты, углеводы, олигосахариды, липиды, пребиотики или пробиотики, нуклеотиды, нуклеозиды, другие витамины, минеральные вещества и другие микроэлементы.
В одном типичном варианте осуществления настоящего изобретения композиция содержит источник белков, источник липидов и источник углеводов.
Например, такая композиция может содержать белок в диапазоне от приблизительно 2 до 6 г/100 ккал, липиды в диапазоне от приблизительно 1,5 до 3 г/100 ккал и/или углеводы в диапазоне от приблизительно 1,7 до 12 г/100 ккал.
Если композиция представляет собой жидкость, ее энергетическая ценность может составлять от 60 до 75 ккал/100 мл.
Если композиция представляет собой твердое вещество, ее энергетическая ценность может составлять от 60 до 75 ккал/100 мл.
Предполагается, что тип белка не имеет большого значения для настоящего изобретения. Вместе с тем в случае искусственных композиций для младенцев и/или детей младшего возраста, например детской смеси или молочных смесей для детей от 1 до 3 лет, упомянутые белки должны поддерживать рост младенца и/или ребенка, так что упомянутый младенец и/или ребенок может соответствовать кривым роста, характерным для его генетического фона, веса при рождении и состояния здоровья.
Не имеющие ограничительного характера примеры белков включают: казеин, альфа-лактальбумин, молочную сыворотку, бета-лактоглобулин, белок сои, белок риса, белок кукурузы, белок овса, белок ячменя, белок пшеницы, белок ржи, белок гороха, яичный белок, белок семян подсолнечника, белок картофеля, белок рыбы, белок мяса, лактоферрин, сывороточный альбумин, иммуноглобины и их комбинации.
Не имеющие ограничительного характера примеры аминокислот включают лейцин, треонин, тирозин, изолейцин, аргинин, аланин, гистидин, изолейцин, пролин, валин, цистеин, глутамин, глутаминовую кислоту, глицин, серин, аргинин, лизин, метионин, фенилаланин, триптофан, аспарагин, аспарагиновую кислоту и их комбинации.
Не имеющие ограничительного характера примеры углеводов включают лактозу, сахарозу, мальтодекстрин, крахмал и их комбинации.
Не имеющие ограничительного характера примеры липидов включают: пальмовый олеин, подсолнечное масло с высоким содержанием олеиновой кислоты, сафлоровое масло с высоким содержанием олеиновой кислоты, масло канолы, рыбий жир, кокосовое масло, жир коровьего молока и их комбинации.
Может быть особенно полезно, если композиция включает жир в количестве от 25 до 30 г/100 г сухого веса композиции.
Не имеющие ограничительного характера примеры незаменимых жирных кислот включают: линолевую кислоту (LA), α-линоленовую кислоту (ALA). Композиции изобретения могут дополнительно содержать ганглиозиды моносиалоганглиозид-3 (GM3) и дисиалоганглиозиды-3 (GD3) и их комбинации.
Не имеющие ограничительного характера примеры пребиотиков включают: олигосахариды, необязательно содержащие фруктозу, галактозу, маннозу; пищевые волокна, в частности растворимые волокна, волокна сои; инулин; и их комбинации. Предпочтительные пребиотики представляют собой фруктоолигосахариды (FOS), галактоолигосахариды (GOS), изомальтоолигосахариды (IMO), ксилоолигосахариды (XOS), арабиноксилоолигосахариды (AXOS), маннанолигосахариды (MOS), соевые олигосахариды, гликозилсахарозу (GS), лактосахарозу (LS), лактулозу (LA), палатинозаолигосахариды (PAO), мальтоолигосахариды, смолы и/или их гидролизаты, пектины и/или их гидролизаты и комбинации вышеперечисленного.
Дополнительные примеры олигосахаридов описаны в публикации Wrodnigg, T. M.; Stutz, A.E. (1999) Angew. Chem. Int. Ed. 38:827-828, а также в WO 2012/069416, которые включены в настоящий документ путем ссылки.
Не имеющие ограничительного характера примеры пробиотиков включают: Bifidobacterium, Lactobacillus, Lactococcus, Enterococcus, Streptococcus, Kluyveromyces, Saccharoymces, Candida, в частности выбранные из группы, состоящей из Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus lactis, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus salivarius, Lactococcus lactis, Enterococcus faecium, Saccharomyces cerevisiae, Saccharomyces boulardii или их смесей, предпочтительно выбранные из группы, состоящей из Bifidobacterium longum NCC3001 (ATCC BAA-999), Bifidobacterium longum NCC2705 (CNCM I-2618), Bifidobacterium longum NCC490 (CNCM I-2170), Bifidobacterium lactis NCC2818 (CNCM I-3446), Bifidobacterium breve штамм A, Lactobacillus paracasei NCC2461 (CNCM I-2116), Lactobacillus johnsonii NCC533 (CNCM I-1225), Lactobacillus rhamnosus GG (ATCC53103), Lactobacillus rhamnosus NCC4007 (CGMCC 1.3724), Enterococcus faecium SF 68 (NCC2768; NCIMB10415) и их комбинаций.
Не имеющие ограничительного характера примеры нуклеотидов включают: цитидинмонофосфат (ЦМФ), уридинмонофосфат (УМФ), аденозинмонофосфат (АМФ), гуанозинмонофосфат (ГМФ) и их комбинации.
Другие подходящие и желательные ингредиенты питательных композиций, которые можно использовать в питательной композиции изобретения, могут быть описаны в руководящих указаниях Кодекса пищевых международных стандартов Codex Alimentarius в отношении рассматриваемого типа питательных композиций, например детской смеси, обогатителя ГМ, смеси для прикармливаемых детей, продуктов питания, предназначенных для употребления младенцами, например прикорма.
В еще более конкретном варианте осуществления композиция изобретения представляет собой детскую смесь, состав которой определен в примере 5 и, в частности, в таблице 11а.
Искусственную питательную композицию, например детскую смесь, используемую в изобретении, можно получать любым подходящим образом. Например, детскую смесь можно получать путем смешивания вместе источника белков, источника углеводов и источника жиров в соответствующих пропорциях. В случае использования в смесь можно включать эмульгаторы. На данном этапе можно добавлять холин, любые витамины и любые минеральные вещества, но обычно их добавляют позднее во избежание термического разложения. Перед смешиванием в источнике жиров можно растворять любые липофильные витамины, эмульгаторы и т.п. Затем можно примешивать воду, предпочтительно воду, очищенную обратным осмосом, с образованием жидкой смеси. Затем жидкую смесь можно подвергать термической обработке для снижения бактериальных нагрузок. Например, жидкую смесь можно быстро нагревать до температуры в диапазоне от приблизительно 80°C до приблизительно 110°C в течение от приблизительно 5 секунд до приблизительно 5 минут. Это можно осуществлять путем нагнетания пара или с помощью теплообменника; например пластинчатого теплообменника. Затем жидкую смесь можно охлаждать до температуры от приблизительно 60°C до приблизительно 85°C; например путем резкого охлаждения. После этого жидкую смесь можно гомогенизировать; например в две стадии: под давлением от приблизительно 7 МПа до приблизительно 40 МПа на первой стадии и от приблизительно 2 МПа до приблизительно 14 МПа на второй стадии. Затем гомогенизированную смесь можно дополнительно охлаждать для добавления любых термочувствительных компонентов; таких как витамины и минералы. На данном этапе для удобства стандартизируют рН и содержание твердых веществ в гомогенизированной смеси. Гомогенизированную смесь переносят в подходящий сушильный аппарат, такой как распылительная сушилка или сублимационная сушилка, и превращают в порошок. Влагосодержание порошка должно составлять менее приблизительно 5 мас. %. Если необходимо добавить пробиотик (-и), то его (их) можно культивировать в соответствии с любым подходящим способом и подготавливать для добавления в детскую смесь путем, например, сушки сублимацией или сушки распылением. Альтернативно бактериальные препараты можно приобретать у специализированных поставщиков, таких как Christian Hansen и Morinaga, уже в готовой подходящей форме для добавления в продукты питания, такие как детская смесь. Такие бактериальные препараты можно добавлять к порошковой детской смеси путем сухого смешивания.
Как явствует из приведенного выше описания, композиция настоящего изобретения может использоваться для стимулирования, поддержки или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, и/или плотности нейронных связей, и/или интеллектуального потенциала, и/или когнитивного потенциала, и/или способности к обучению, и/или когнитивной функции у субъекта, в частности у субъекта, получающего детскую смесь.
В другом аспекте настоящего изобретения предлагается способ стимулирования, поддержки или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, и/или плотности нейронных связей, и/или интеллектуального потенциала, и/или когнитивного потенциала, и/или способности к обучению, и/или когнитивной функции у субъекта, в частности у субъекта, получающего детскую смесь, причем упомянутый способ включает кормление упомянутого субъекта композицией, содержащей холин, как определено в настоящем документе.
В другом аспекте настоящего изобретения предлагается композиция, содержащая холин, как указано в настоящем документе, для применения в приготовлении композиции для стимулирования, поддержки или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, и/или плотности нейронных связей, и/или интеллектуального потенциала, и/или когнитивного потенциала, и/или способности к обучению, и/или когнитивной функции у субъекта, в частности у субъекта, получающего детскую смесь.
Может быть особенно целесообразно вводить композицию настоящего изобретения младенцу в возрасте 9 месяцев или менее, в частности в возрасте 6 месяцев или менее, более конкретно - в возрасте 3 месяца или менее.
Не имеющими ограничительного характера примерами возраста 3 месяцев или менее являются возраст до 2 недель, возраст до 1 месяца, возраст до 2 месяцев, возраст до 3 месяцев, возраст от 1 до 3 месяцев.
Воздействие композиции изобретения, описанной в настоящем документе, может иметь долгосрочный полезный для здоровья эффект. Деменция, например болезнь Альцгеймера, вызывает снижение способности субъекта думать и запоминать, а также приводит к эмоциональным и языковым проблемам. Риск того, что тот или иной субъект будет страдать деменцией, в частностью болезнью Альцгеймера, связывали с интеллектуальными способностями или интеллектом человека. Соответственно, за счет оптимизации интеллектуального, когнитивного потенциала и или способности к обучению можно снизить риск развития у субъекта деменции, в частности болезни Альцгеймера. Упомянутый долгосрочный эффект может проявляться в течение нескольких лет, например 40, 50, 60. 70, 80, 90 лет.
Кроме того, самые различные психиатрические и/или неврологические нарушения, например тревожные состояния, депрессию, аутизм и шизофрению, связывают со структурой головного мозга. За счет стимулирования, поддержки или оптимизации первичной миелинизации, в частности траектории первичной миелинизации, и/или структуры головного мозга, в частности определяемой первичной миелинизацией и траекторией первичной миелинизации, у субъекта появляется возможность предотвратить психиатрические и/или неврологические нарушения, например тревожные состояния, депрессию, аутизм и шизофрению, или снизить риск их развития, или сгладить остроту упомянутого (-ых) расстройства (расстройств). Упомянутый эффект может проявляться в течение нескольких лет, например 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60. 70, 80, 90 лет.
Если не указано иное, все приводимые в настоящем документе процентные соотношения представляют собой мас. %.
В контексте настоящего изобретения термины «содержащий» или «содержит» не исключают других возможных элементов. Композиция настоящего изобретения, включая многие варианты осуществления, описанные в настоящем документе, может содержать существенные элементы и ограничения изобретения, описанные в настоящем документе, а также любые дополнительные или необязательные ингредиенты, компоненты или ограничения, описанные в настоящем документе, или иные в зависимости от потребностей, состоять или по существу состоять из них.
Как будет очевидно специалисту в данной области, такую же пользу, которая раскрыта в настоящем документе, можно обеспечить, если принимать холин непосредственно, а не в форме композиции. Соответственно, холин может использоваться непосредственно вместо композиции настоящего изобретения в любом способе или варианте применения, приведенных в настоящем документе.
Как будет также очевидно специалисту в данной области, может быть особенно полезно, если холин вводят, т.е. потребляют отдельно, последовательно и/или одновременно с одним или более из следующих ингредиентов: витамином, в частности витамином В12 и/или фолиевой кислотой, и/или минеральным веществом, в частности железом и/или цинком, и/или кальцием, и/или фосфором, и/или магнием, и/или медью, и/или производным жирной кислоты, в частности производным жирной кислоты, содержащим докозагексаеновую кислоту и/или арахидоновую кислоту, и/или нервоновую кислоту, и/или стеариновую кислоту, и/или фосфолипидом, в частности фосфатидилхолином, фосфатидилсерином, фосфатидилинозитолом, и/или сфингомиелином.
Все детали настоящего изобретения в равной степени применимы к композиции, содержащей холин, а также к непосредственному применению холина.
Следует понимать, что все признаки настоящего изобретения, описанные в настоящем документе, можно свободно комбинировать и что изменения и модификации можно вносить без отступления от объема изобретения, определенного в формуле изобретения. Кроме того, если существуют известные эквиваленты конкретных признаков, такие эквиваленты включены так, как если бы они конкретно были упомянуты в данном описании.
Термины «в частности» или «более конкретно» при использовании в настоящем изобретении не должны рассматриваться как ограничивающие, но их следует интерпретировать как синонимы выражений «например» или «а именно».
Ниже представлен ряд не имеющих ограничительного характера примеров, которые иллюстрируют изобретение.
Экспериментальный раздел
Способы, определения и материалы
МРТ (магнитно-резонансная томография). Проводили МРТ-сканирование головного мозга младенцев и детей в возрасте от 0 до 5 лет с использованием методики визуализации белого вещества. Данная методика обеспечивает количественный показатель «миелиновая водная фракция» (MWF), который является суррогатным маркером содержания миелина в головном мозге. При построении как функции от времени за период раннего детства можно получить траектории миелинизации.
Композиция детской смеси. Шесть детских смесей, потребляемых младенцами, участвующими в исследовании, анализировали с точки зрения их состава/уровня связанных с миелином питательных веществ.
Питательные композиции тестировали в стандартных доступных в продаже детских смесях различных торговых марок/поставщиков и с различными уровнями содержащихся в них питательных веществ.
Когнитивные способности. Стандартизованные по возрасту (Т)-показатели крупной моторики, зрительного восприятия и языка (передача и восприятие) получены по шкалам раннего обучения Маллен - стандартизованного и утвержденного инструмента оценки раннего когнитивного развития младенцев и детей в возрасте 6 лет или младше.
Анализ питательных веществ
В таблице 1 приведены питательные вещества для каждой из 6 композиций детских смесей.
Таблица 1
Клиническое исследование
Участники-младенцы
Включенных в настоящее исследование младенцев отбирали из более масштабного продольного исследования нормального развития мозга и поведенческого развития: исследования Университета Брауна по оценке миелинизации и поведения в период развития (Brown University Assessment of Myelination and Behavior Across Maturation, BAMBAM). С тем чтобы сосредоточиться на нейротипическом развитии, дети с известными потенциальными факторами риска в отношении обучения, неврологических или психиатрических расстройств специально исключались в процессе подбора и включения в исследование. Поэтому исключались дети с внутриутробным воздействием алкоголя или запрещенных веществ, недоношенные (< 37 недель беременности) или множественными родовыми отклонениями, аномалиями развития плода по данным УЗИ, осложненной беременностью (например, преэклампсией), показателем APGAR < 8, пребыванием в ОИТН, неврологическими нарушениями (например, травмой головы, эпилепсией), психиатрическими отклонениями или нарушениями развития у младенца, родителей или родных братьев/сестер (включая депрессию у матери, для которой потребовалось медикаментозное лечение). Текущий скрининг, например MCAT на предмет аутизма или CBCL на предмет проблем поведения, дополнительно использовался, чтобы исключить уже отобранных детей с настораживающим с клинической точки зрения поведением или очевидными медицинскими отклонениями (например, расстройствами аутического спектра).
Собирали комбинацию ретроспективных и перспективных данных у родителей в рамках изучения подробного анамнеза и опроса родителей в отношении использованной детской смеси, процентного соотношения грудного вскармливания и питания смесью и продолжительности исключительно грудного вскармливания. Такую информацию обновляли при каждом визите исследования, который проводился примерно каждые 6 месяцев для детей в возрасте до 2 лет и ежегодно для детей более старшего возраста. На основе такой информации детей распределяли в одну из 2 групп: № 1. Получавшие исключительно детскую смесь; и № 2. Получавшие исключительно грудное вскармливание по меньшей мере в течение 90 дней (3 месяцев). Дети, получавшие комбинацию грудного молока и детской смеси в течение 3 месяцев были исключены из нашего анализа. Младенцы из группы, получавшей исключительно детскую смесь, были дополнительно подразделены на основании информации от родителей в отношении основной детской смеси, использовавшейся в течение первых 3 месяцев. Основной детской смесью считали такую, которая использовалась 90% времени или больше (например, в случае если во время отпуска родители использовали альтернативную торговую марку).
На основании таких критериев в группу № 1 отобрали 94 младенца и ребенка младшего возраста, получавших исключительно детскую смесь. Сюда входили 13 детей, которые получали смесь № 2; 28 получавших смесь № 5; 8 получавших смесь № 3; 39 получавших смесь № 4; 5 получавших смесь № 1 и 1 получавший смесь № 6. Выборку из 52 младенцев на исключительно грудном вскармливании также отбирали и приводили в соответствие с приведенной выше группой, получавшей детскую смесь, по следующим показателям: среднему возрасту, продолжительности беременности, весе при рождении, соотношении мальчики : девочки, этническому соотношению, образованию матери, размере семьи и числе языков, на которых говорят дома (в дополнение к английскому). В таблице 1а приведены данные по группированию для каждой смеси.
Таблица 1a. Разбивка данных для продольного анализа и анализа питательной ценности
Методы визуализации и анализа
Сканирование каждого младенца проводили с использованием методики mcDESPOT (многокомпонентное равновесное одноимпульсное определение T1 и T2) для визуализации белого вещества в соответствии с Deoni et al. (Magn. Reson. Med. 2008, 60:1372-1387), которая обеспечивает количественный показатель миелиновой водной фракции (MWF) - оценку содержания миелина - в каждой точке головного мозга. Сканирование всех младенцев проводили в течение естественного (то есть без применения седативных средств) сна с использованием протоколов визуализации mcDESPOT с акустическим подавлением. Суммарное время сканирования менялось в пределах от 19 минут для самых маленьких начинающих ходить детей до 24 минут в случае детей в возрасте старше 4 лет.
Все данные получали на сканере Siemens 3T Tim Trio с 12-канальной РЧ-катушкой для головы. Чтобы свести к минимуму движения в течение сканирования, детей пеленали с использованием педиатрического вакуумного иммобилизационного пакета MedVac (CFI Medical Solutions, США) и подушек из пеноматериала. Шум сканера снижали за счет уменьшения амплитуд пикового градиента и скоростей изменения градиента, а также за счет использования шумоизолирующих вкладышей для проема сканера (Quiet Barrier HD Composite, UltraBarrier, США). Также использовали педиатрические наушники MiniMuff и электродинамические головные телефоны (MR Confon, Германия). Состояние детей постоянно отслеживали с помощью педиатрическое системы пульсоксиметрии и инфракрасной камеры. Все дети продолжали спать в течение МРТ-сканирования, и в анализируемых данных отсутствуют какие-либо артефакты, связанные с движением.
После совмещения изображений, удаления сигнала, не связанного с головным мозгом, и коррекции неоднородности основного и прикладываемого магнитного поля (B0 и B1) использовали трехкомпонентную модель сигнала (включающую связанную с миелином воду; воду внутри и вне аксонов; и свободную воду, не участвующую в процессах обмена) для обработки данных mcDESPOT, чтобы получить воксельные карты MWF.
Затем карту для каждого ребенка нелинейно совмещали со специальным шаблоном исследования. Из общедоступных баз данных формировали маски белого вещества, соответствующие 5 билатеральным областям (лобное, височное, затылочное, теменное и мозжечковое белое вещество), а также для ствола, колена и валика мозолистого тела, регистрировали их в общем шаблоне и накладывали на карту MWF каждого ребенка. Затем для каждого ребенка определяли средние значения для каждой области и использовали их для последующего анализа развития и моделирования траектории.
Различия в развитии
Для анализа различий в развитии между младенцами на грудном вскармливании и получавшими детскую смесь, а также между младенцами, получавшими различные детские смеси, использовали метод моделирования нелинейных смешанных эффектов. Данные для групп № 1 и № 2 и каждой подгруппы для различных смесей независимо обрабатывали с использованием модифицированных моделей роста Гомпертца. Затем сопоставляли каждый из четырех параметров модели Гомпертца между группами грудного вскармливания и детских смесей с использованием двухвыборочного t-критерия, а также между подгруппами 4 смесей с использованием вариационного анализа с последующим применением апостериорного критерия Тьюки, чтобы выявить различающиеся группы детских смесей.
Оценка и анализ когнитивной функции
Наряду с МРТ-томографией у каждого ребенка в течение 7 дней после сканирования оценивали общие когнитивные способности и навыки с использованием шкалы раннего обучения Маллен, MSEL (Mullen EM, 1995). MSEL обеспечивает общую оценку поведенческого развития в областях контроля мелкой и крупной моторики, языковых навыков восприятия и передачи информации и зрительного восприятия. Нормализованные по возрасту Т-показатели по этим областям могут быть объединены в три композитных показателя: композитный показатель раннего обучения (ELC, включающий мелкую моторику, зрительное восприятие, языковые навыки восприятия и передачи информации); показатель невербального развития (NVDQ, включающий показатели мелкой моторики и зрительного восприятия); и показатель вербального развития (VDQ, включающий показатели языковых навыков передачи и восприятия информации).
Как и в случае данных MWF по результатам МРТ, анализировались потенциальные различия средних показателей по группам для ELC, VDQ и NVDQ между младенцами на грудном вскармливании и получавшими детскую смесь, а также между подгруппами, получавшими различные детские смеси. В дополнение к сопоставлениям средних исследовались продольные изменения по этим трем композитным значениям с использованием моделирования смешанных эффектов в предположении линейного тренда.
Пример 1
Определение факторов питания на основании перекрестного анализа
Из описанной выше когорты дети в возрасте до 5 лет, которые получали различные детские смеси в младенческий период, были включены в расширенный корреляционный анализ для выявления взаимосвязи между составом питательных веществ в детской смеси и миелинизацией головного мозга. Из этой когорты 6 наиболее часто используемых детских смесей анализировали с точки зрения их питательной композиции. Строили единую общую линейную модель (GLM), которая моделировала все количественно заданные питательные вещества и возраст ребенка.
Затем рассчитывали ранговую корреляцию Спирмана между содержанием питательного вещества и показателем содержания миелина (скорректированного с учетом возраста ребенка) для каждого вокселя изображения или точки в пределах головного мозга. Значимость определяли как p < 0,05, скорректированное с учетом ошибок 1-го типа с использованием метода кластерной коррекции. Связь или тренд определяли как p < 0,15. В ходе первоначального анализа учет всех 22 питательных веществ, перечисленных в таблице 1, приводил к недостоверной модели. Чтобы сократить число питательных компонентов в модели, мы проанализировали внутреннюю корреляцию между питательными веществами. Исходя из консервативного порогового значения 0,9, мы исключили питательные компоненты, для которых наблюдалась высокая корреляция друг с другом в составах различных детских смесей. В результате получили итоговую модель, которая включала железо, сфингомиелин, фолиевую кислоту, холин, DHA, цинк и фосфатидилхолин.
P < 0,05: железо, сфингомиелин, фолиевая кислота, холин, DHA.
P<0,15: цинк и фосфатидилхолин.
К питательным компонентам, для которых наблюдалась высокая корреляция друг с другом, относились:
фолиевая кислота и витамин B12.
DHA и AA.
Цинк, кальций, магний, медь и фосфор.
Фосфатидилхолин, фосфатидилсерин и фосфатидилинозитол.
В случае холина связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, таламусе, теменной коре и лобной доле. Результаты представлены на фиг. 1b.
В случае сфингомиелина связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, внутренней капсуле, лобной доле, теменной доле, височной доле. Результаты представлены на фиг. 1с.
В случае фосфатидилинозитола связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, двигательной коре, лобной коре. Результаты представлены на фиг. 1d.
В случае фосфатидилхолина связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, внутренней капсуле, лобной доле, теменной доле, височной доле. Результаты представлены на фиг. 1е.
В случае фолиевой кислоты связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, двигательной коре, зрительной коре. Результаты представлены на фиг. 1f.
В случае витамина В12 связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, двигательной и соматосенсорной коре. Результаты представлены на фиг. 1g.
В случае железа связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, внутренней капсуле, двигательной и соматосенсорной коре, мозолистом теле, лобной коре, височном белом веществе. Результаты представлены на фиг. 1h.
В случае цинка связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, внутренней капсуле, двигательной и соматосенсорной коре, мозолистом теле, лобной коре, височном белом веществе. Результаты представлены на фиг. 1i.
В случае кальция связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, двигательной и соматосенсорной коре, мозолистом теле, лобной коре, височном белом веществе. Результаты представлены на фиг. 1j.
В случае фосфора связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, двигательной и соматосенсорной коре, префронтальной коре. Результаты представлены на фиг. 1k.
В случае магния связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, зрительной коре, внутренней капсуле, мозолистом теле, лобной коре, двигательной коре. Результаты представлены на фиг. 1l.
В случае DHA связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, первичной и вторичной двигательной коре, внутренней капсуле, зрительной коре, лобной коре. Результаты представлены на фиг. 1m.
В случае АА связь с миелинизацией (миелиновую водную фракцию) наблюдали в головном мозге во времени, в частности в мозжечке, внутренней капсуле, теменной доле, двигательной и сенсорной коре, зрительной коре, лобной коре. Результаты представлены на фиг. 1n.
Пример 2
a) Траектория миелинизации всего головного мозга по результатам продольного исследования
На основании имеющихся данных рассчитывали траектории продольного развития миелина (первичную миелинизацию) с использованием многократно измеренных данных MWF у детей, детские смеси которых содержали различные количества холина (состав таких смесей приведен ниже в таблице 2). Траектории рассчитывали с использованием метода продольных нелинейных смешанных эффектов. Данные для детей из группы каждой из смесей обрабатывали с использованием модифицированных моделей роста Гомпертца. Результаты представлены на фиг. 1.
Таблица 2
b) Средняя траектория миелинизации по областям головного мозга по результатам продольного исследования
На основании имеющихся данных рассчитывали средние траектории продольного развития миелина по областям мозга (первичная миелинизация) с использованием многократно измеренных данных MWF у детей, детские смеси которых содержали различные количества холина (состав таких смесей приведен ниже в таблице 2а). Траектории рассчитывали с использованием метода продольных нелинейных смешанных эффектов, а данные для детей из группы каждой из смесей обрабатывали с использованием модифицированных моделей роста Гомпертца. Результаты представлены на фиг. 1a.
Таблица 2a
Результаты представлены на фиг. 1a.
Пример 3
Поставщики и маточные растворы
Несущие среды и дозы
Составы сред и способы культивирования
1) Нейробазальная полная среда
Нейробазальная среда (LIFE TECHNOLOGIES CORP, № 21103-049)
Добавка 50X B27 (LIFE TECHNOLOGIES CORP, № 12587-010)
2 мМ L-глутамин (LIFE TECHNOLOGIES CORP, № 25030-149)
1X раствор пенициллина-стрептомицина (Pen-Strep) (LIFE TECHNOLOGIES CORP, № 15140-122)
2) Нейробазальная полная среда с факторами роста (GF)
Приведенная выше рецептура с добавлением GF
1M Трис (Мол. вес 121,14, Fisher SCI BP152)
Гепарин (sigma H3149)
БСА (Sigma A7030)
Вода, не содержащая ДНКаз, РНКаз, протеаз (Fisher SCI AC327390010)
EGF (GIBCO PHG0311)
Флакон bFGF (GIBCO PHG0021)
3) Нейробазальная среда без холина (Life technologies, специальная формула, без L-глутамина, без фенолового красного)
Примечание: полная среда и полная среда с GF готовились так же, как указано выше.
Формирование библиотек нейронных клеток-предшественников (NPC):
диссоциация неокортекса мышей E14
Необходимые реагенты:
Фосфатно-солевой буфер Дульбекко (DPBS) (1X) + 10% Pen/Strep
Нейробазальная среда / 10% Pen/Strep / 10X HEPES
Процедура
Мозги детенышей E14 собирали и помещали в охлажденную на льду среду DPBS(1X) + 10% Pen/Strep, затем их препарировали с использованием препаровальной лупы. Для каждого детеныша одно полушарие мозга помещали в 2 мл нейробазальной среды / 10% P/S / 10X HEPES, а второе полушарие мозга помещали в другую пробирку.
Ткань из каждой пробирки в асептических условиях и вручную разделяли на единичные клетки, добавляли нейробазальную полную среду и центрифугировали при 130 G в течение 5 мин. Затем ткань ресуспендировали в нейробазальной полной среде с GF помещали в чашку Сorning для суспензионной культуры 100 мм X 20 мм (№ 430591). Клетки пересевали дважды в соотношении 1 : 3, после чего их центрифугировали (130 g 5 мин), ресуспендировали в среде для замораживания (10% DMSO и нейробазальная полная среда, без GF) и замораживали в жидком азоте (LN2).
Размораживание клеток для скрининга соединений
Флаконы извлекали из LN2, быстро размораживали, и клетки по каплям переносили в коническую колбу объемом 15 мл. Добавляли 10 мл нейробазальной полной среды. Клетки переносили в чашку для суспензионной культуры и помещали в инкубатор на 2 часа. Через 1,5 часа проверяли состояние клеток. На основании состояния и количества оценивали число необходимых планшетов и подогревали соответствующее количество полной нейробазальной среды. Через 2 часа клетки помещали в 15-мл коническую пробирку и вращали при 130 g в течение 5 минут. Затем клетки ресуспендировали в нейробазальной полной среде с GF (3 мкл GF на каждые 10 мл среды). Клетки затем выращивали в течение ночи, после чего использовали в экспериментах.
Посев клеток в 96-луночные планшеты только для подсчета нейросфер и диаметров
96-луночный планшет Corning Costar 3474 с поверхностью Ultra low attachment, предотвращающей прилипание клеток
Диссоциация и посев клеток
3-4 мл клеток отбирали из наклонного планшета и добавляли в конический объемом 15 мл. Часть остающейся среды использовали для споласкивания планшета. Всю оставшуюся среду отбирали и помещали в коническую пробирку объемом 15 мл и центрифугировали при 130 G в течение 5 мин. Удаляли всю среду. Клетки осторожно ресуспендировали в 5 мл теплого фосфатно-солевого буферного раствора (PBS) и вновь центрифугировали. Затем удаляли PBS и клетки осторожно ресуспендировали в 500 мкл раствора для отделения клеток Accutase (Corning™ Accutase™ Cell Detachment Solution, № 25058CI). Затем клетки осторожно взмучивали пипеткой с носиком объемом 1000 мкл, так чтобы ресуспендировать осадок, а затем помещали в водяную баню со встряхиванием на 5-10 минут, после чего периодически встряхивали вихревыми движениями вручную.
Среды готовили, как указано ниже, все среды содержали GF:
холина/несущая среда
Окт : дек
холина/несущая среда
холина/несущая среда
холина/несущая среда
Контрольную среду и среду с соединением готовили со средой № 2, и они содержали 29 мкМ холина,
среды с низким (5 мкМ) и средним (70 мкМ) содержанием холина готовили со средой № 3.
Среду ОСТОРОЖНО взмучивали пипеткой с носиком 1000 мкл, а затем с носиком 200 мкл для большей дисперсии клеток.
Сгустки содержали не более ~ 3-5 клеток. Для разбавления фермента добавляли 5-10 мл теплой среды (GF). Добавляли 2 мл среды. Ее отбирали пипеткой 1000 мкл, а затем 3 мл добавляли серологической пипеткой. Перед высеиванием клетки просеивали через утвержденное для клеточных культур сито 40 мкм.
1 мл отбирали для подсчета клеток. Клетки вновь центрифугировали. Удаляли среду над осадком клеток. Добавляли 1 мл подготовленной среды (без GF). Клетки отбирали пипеткой 1000 мкл. Проводили разбавление клеток (24 000 клеток/лунка) в 250 мкл соответствующей среды. Клетки ежедневно встряхивали и растили 2 дня.
Фиксирование и окрашивание
1. Фиксацию клеток проводили под тягой. Для фиксации и последующего иммуногистохимического анализа удаляли 100 мкл среды и добавляли 100 мкл 4%-го параформальдегида (PFA) в 1X PBS для фиксации клеток, одновременно вручную подсчитывая нейросферы, затем клетки дважды промывали 1X PBS в течение 5 мин и оставляли в 1X PBS, обернув фольгой и оставив в течение ночи при 4°C, или же проводили окрашивание с помощью Dapi. Отбирали 100 мкл PBS и добавляли 100 мкл раствора для окрашивания антителами (AB) (1% козьей сыворотки, 1xPBS и 0,1% Triton X) при комнатной температуре в течение 1 часа. Раствор для окрашивания антителами удаляли. Клетки затем окрашивали с помощью Dapi 1 : 5000 в растворе для окрашивания антителами, 100 мкл на лунку, затем клетки инкубировали при комнатной температуре в течение 15 мин в темноте. Клетки затем промывали 2 раза в растворе для окрашивания антителами в течение пяти минут. Изображения получали с использованием визуализатора GE Cytell или конфокального микроскопа LSM 710 Zeiss и анализировали диаметры нейросфер с помощью программного обеспечения ImageJ (Национальные институты здоровья).
Высеивание клеток в 24-луночные планшеты для монослойной дифференциации или анализа включения EdU
холина/несущая среда
холина/несущая среда
холина/несущая среда
холина/несущая среда
24-луночные планшеты со стеклянным дном (Mat Tek P24G-1.0-13-F Case, 24-луночные планшеты со стеклянным дном) покрывали поли-L-орнитином (Sigma P4957) и фибронектионом (Sigma F1141), прежде чем использовать в приведенном ниже анализе.
См. выше про диссоциацию и посев клеток.
Клетки высевали (10 000 клеток на лунку) в полной среде с GF в течение 24 часов (500 мкл на лунку). После фиксации клеток их переводили в среду без холина, среду с другим соединением или соответствующую среду.
Анализ на дифференциацию: количественное определение экспрессии нейронального, глиального и NPC маркера
Через 24 часа проверяли фиксацию клеток на планшете, затем осторожно удаляли среду.
Добавляли 500 мкл среды соединения, содержащей 2% Nu Serum (заменитель сыворотки) (Corning™ Nu-Serum Growth Medium Supplement, № CB55004), контроль, среду с низким или средним содержанием холина. Примечание: среда не содержала GF.
Контрольную среду и среду с соединением готовили со средой № 2, и они содержали 29 мкМ холина, среды с низким (5 мкМ) и средним (70 мкМ) содержанием холина готовили со средой № 3.
Клетки культивировали в течение 9 дней в среде с 2% Nu Serum, причем среду заменяли каждый 2-й день. Для фиксации и последующего иммуногистохимического анализа среду удаляли, клетки однократно промывали с использованием 1X PBS в течение 5 мин и фиксировали с использованием 4%-ного PFA в 1X PBS в течение 15 мин при 4°C. Клетки затем дважды промывали с использованием 1X PBS в течение 5 мин, оставляли в 1X PBS, обернув в фольгу и оставив на ночь при 4°C, или же с ними сразу же проводили окрашивание с первичным антителом.
Окрашивание для дифференциации
Удаляли PBS и добавляли достаточное количество раствора для окрашивания антителами (1% козьей сыворотки, 1x PBS и 0,1% Triton X), чтобы покрыть дно, блок выдерживали при комнатной температуре в течение 1 часа.
Разбавление первичного антитела проводили в соответствующем количестве раствора для окрашивания антителами, 250 мкл на лунку (антитела выдерживали лишь непродолжительное время на льду, мышиный анти-MAP2 или TUJ1 1 : 500 (нейронный маркер), анти-GFAP кролика (глиальный маркер) 1 : 1000, анти-Nestin CFP курицы (антитело EGFP (маркер клеток-предшественников)) 1 : 1000. Раствор для окрашивания антителами удаляли и в каждую лунку добавляли раствор первичного антитела. Клетки оборачивали в фольгу и выдерживали в течение ночи при 4°C. Клетки затем промывали 400 мкл раствора для окрашивания антителами в течение 5 мин однократно, чтобы удалить первичные антитела. Готовили растворы вторичного антитела (в объеме, достаточном для 250 мкл на каждую лунку) (козье анти-мышиное Аlexa 488 1 : 2000, анти-кролика Cy3 (1 : 500), анти-курицы Аlexa 647 1 : 500 и 1 : 5000 Dapi).
Клетки инкубировали при комнатной температуре в течение 1 часа в темноте и промывали 2 раза в растворе для окрашивания антителами в течение пяти минут. Их выдерживали при 4°C или получали изображение с использованием визуализатора GE Cytell или конфокального микроскопа LSM 710 Zeiss и анализировали с помощью программного обеспечения ImageJ (Национальные институты здоровья).
Ассоциированный с микротрубочками белок 2 (MAP2), нейрональный бета-тубулин III (TuJ1), глиофибриллярный кислый белок (GFAP) и Nestin CFP (антитело EGFP).
Экспрессию каждого маркера измеряли на полученных изображениях (показатель интегральной плотности в ImageJ) и нормализовали по флуоресценции DAPI с маркировкой всех ядер (показатель интегральной плотности).
Октановую кислоту метили нейрональным бета-тубулином III (TuJ1), использовавшиеся впоследствии соединения метили ассоциированным с микротрубочками белком 2 (MAP2).
Анализ пролиферации монослойной культуры NPC (включение EdU - маркера S-фазы)
Через 24 часа проверяли фиксацию клеток на планшете, затем осторожно удаляли среду. Добавляли. 500 мкл среды с соединением и GF. Клетки культивировали в течение 3 дней в соответствующей среде.
Контрольную среду и среду с соединением готовили со средой № 2, и они содержали 29 мкМ холина, среды с низким (5 мкМ) и средним (70 мкМ) содержанием холина готовили со средой № 3.
Включение EDU измеряли с использованием набора визуализации Click-iT® EdU Alexa Fluor® 555 (Life technologies, № c10338).
На конец 3 дня EdU добавляли в каждую лунку в концентрации 10 мкМ на 30 минут до фиксации.
Для фиксации и последующего иммуногистохимического анализа среду удаляли и клетки однократно промывали 1X PBS в течение 5 мин и фиксировали 4% PFA в 1X PBS в течение 15 мин при 4°C, затем клетки дважды промывали 1X PBS в течение 5 мин, оставляли в 1X PBS, обернув фольгой и оставив в течение ночи при 4°C, или же проводили окрашивание.
Удаляли PBS и добавляли достаточное количество раствора для окрашивания антителами (1% козьей сыворотки, 1x PBS и 0,1% Triton X), чтобы покрыть дно, блок выдерживали при комнатной температуре в течение 1 часа. Клетки окрашивали для EDU. Клетки инкубировали в течение 30 мин при комнатной температуре в темноте. Клетки промывали 1X PBS и окрашивали Dapi 1 : 5000 мкл в течение 15 мин. Клетки однократно промывали 1X PBS, затем оставляли в PBS при 4°C или сразу же получали изображение с использованием визуализатора GE Cytell (приложение для жизнеспособности клеток) или конфокального микроскопа LSM 710 Zeiss (с анализом с помощью программного обеспечения ImageJ (Национальные институты здоровья)).
Результаты приведены в таблицах 3-7 и на фиг. 2-5.
Таблица 3. Воздействие нервоновой кислоты (NA) на плотность нейронных клеток и плотность астроцитов
Таблица 4. Воздействие стеариновой кислоты (SA) на плотность нейронных клеток и плотность астроцитов
Таблица 5. Воздействие октановой кислоты (OA) на плотность нейронных клеток и плотность астроцитов
Таблица 6. Воздействие сфингомиелина на число нейросфер
Таблица 7. Воздействие сфингомиелина (SM) на пролиферацию нейронов
Пример 4
Экспериментальная часть
Образцы
Ингредиент C2, концентрат сывороточного белка, обогащенный альфа-лактальбумином (идентификатор системы контроля образцов: K2Q-00030); первое молоко для младенцев, содержащее концентрат сывороточного белка, обогащенный альфа-лактальбумином (идентификатор системы контроля образцов: K2Q-00032); коровье молоко (цельное молоко); человеческое грудное молоко (набор из 6 отдельных образцов для контроля качества, собранных через 4 недели после рождения ребенка; Lee Biosolutions, г. Сент-Луис, штат Миссури, США).
Экстракция фосфолипидов из молочных продуктов
Сухое молоко. Навеску 1 г гомогенизированного порошка отвешивали в стеклянную колбу объемом 50 мл и разбавляли в 20 мл чистой дистиллированной воды. Раствор нагревали при 40°C в течение 30 мин на водяной бане. Количество этого раствора объемом 500 мкл из переносили в стеклянную пробирку объемом 10 мл.
Коровье молоко и грудное молоко: Аликвоту 500 мкл гомогенизированной жидкости переносили в стеклянную пробирку объемом 10 мл.
Анализируемые соединения экстрагировали в соответствии с MP по количественному определению состава грудного молока с использованием СВЭЖХ-МС/МС (RDLS-MP-80138-Rev01) по результатам трех измерений с использованием 9,5 мл смеси хлороформ/метанол (2 + 1). Коротко говоря, пробирки встряхивали и помещали в ультразвуковую баню при 40°C на 15 мин с последующим центрифугированием в течение 10 мин при 2500 об/мин. К жидкой фазе добавляли 2 мл раствора хлорида калия (0,88%, моль/моль), затем встряхивали и центрифугировали в течение 10 мин при 2500 об/мин. Нижнюю органическую фазу переносили в стеклянный сосуд, выпаривали досуха в слабом потоке азота N2 и восстанавливали в 500 мкл хлороформа/метанола (9 + 1) до ввода в ЖХ-МС.
Анализ фосфолипидов методами жидкой хроматографии в сочетании с масс-спектрометрией (ЖХ-МС)
Анализы проводили на Q Exactive Plus Orbitrap (Thermo Fisher Scientific, г. Бремен, Германия), снабженном ЖХ-системой Thermo Scientific Dionex UltiMate 3000 Rapid Separation. Разделение проводили на колонке HILIC (100 x 2,1 (внутр. диам.) мм; 1,7 мкм) с подвижной фазой, состоящей из (A) ацетата аммония 10 мМ и (B) ацетонитрила. Объем ввода задавали равным 10 мкл и градиент начинали с 95% B до 70% B в течение 15 мин, поддерживали в течение 1 мин на уровне 70% B, в течение 3 мин возвращали к исходным условиям и уравновешивали в течение 6 мин.
Q Exactive Plus Orbitrap был снабжен датчиком химической ионизации при атмосферном давлении (APCI), который работал в режиме положительной ионизации. Параметры APCI и МС были следующими: ток коронного разряда 4,0 мкА, защитный газ и вспомогательный газ 24 и 5 условных единиц соответственно; температуры капилляра и испарителя составляли 320 и 390°C соответственно, расход продувочного газа составлял 0 условных единиц и РЧ-уровень s-линзы был равен 80. Целевое значение автоматического контроля усиления (AGC) задавали на уровне 1 × 106 зарядов, а максимальное время ввода - 100 мс с разрешением 35 000 и 1 микросканом на весь МС. AGC устанавливали равным 1 × 106 зарядов, а максимальное время ввода - 250 мс с разрешением 17 500 с 1 микросканом в режиме независимой от данных фрагментации. Перечень включения выборочных ионов-предшественников использовали при 30% нормализованной энергии соударения. Накопление данных проводилось в диапазоне масс 133-2000 Да в профильном режиме. Применяли внешнюю калибровку масс. Управление системой осуществляли с помощью Xcalibur 3.0 (Thermo Fisher Scientific).
Виды SM извлекали из полной ионной хроматограммы с использованием точной массы. Ионы-предшественники соответствовали распаду фосфатидилхолина на источнике до церамида. Перечень включения использовали для специфической фрагментации 57 региоизомеров SM, опираясь на ионы-предшественники, соответствующие m/z церамида с потерей молекулы воды [Cer-H2O + H+], на основе базы данных LipidView и научных литературных источников (Trenerry V.C., Akbaridoust G., Plozza T., Rochfort S., Wales W.J., Auldist M., Ajilouni S. Ultra-high-performance liquid chromatography-ion trap mass spectrometry characterisation of milk polar lipids from dairy cows fed different diets. Food Chemistry 2013, 141, 1451-1460; Godzien J., Ciborowski M., Martinez-Alcazar M.P., Samczuk P., Kretowski A., Barbas C. Rapid and reliable identification of phospholipids for untargeted metabolomics with LC-ESI-QTOF-MS/MS. Journal of Proteome Research 2015, 14, 3204-3216).
Анализ метилового эфира жирных кислот (FAME) методом газовой хроматографии с пламенно-ионизационным детектором (ГХ-ПИД)
Фракции SM собирали в течение от 8,5 до 10 мин в стеклянные пробирки по 5 раз для каждого образца. После испарения растворителя в потоке N2 проводили FAME-анализы по три раза для каждого образца в соответствии с MP для количественного определения жирной кислоты в грудном молоке методом газовой хроматографии (RDLS-MP-8980-00030-Rev01-FAME_Human milk fat 2012, версия 1.0).
Результаты и обсуждение
Для разделения классов PL (т.е. фосфатидилинозитола (PI), фосфатидилсерина (PS), фосфатидилэтаноламина (PE), фосфатидилхолина (PC) и SM) использовали жидкостную хроматографию на основе гидрофильного взаимодействия (HILIC). Отнесение числа углеродов и ненасыщенных фрагментов для отдельных видов SM проводили на основании точной массы псевдомолекулярного иона, регистрируемого масс-спектрометром Orbitrap. Относительную численность видов SM определяли для сравнения ингредиента, детской смеси, коровьего молока и грудного молока.
Виды SM в различных молочных продуктах
В анализируемых образцах регистрировали 45 видов SM (таблица 8).
Таблица 8. Регистрировали виды SM (обозначены x) в образцах ингредиента, детской смеси, коровьего молока и грудного молока. Виды SM, которые были зарегистрированы только в грудном молоке, выделены полужирным шрифтом.
Виды SM 24:1, SM 38:4, SM 38:3 и SM 42:4 были обнаружены в грудном молоке лишь в следовых количествах.
Относительная численность видов SM
Относительную численность (%) SM в различных молочных продуктах определяли по площади пика, разделенной на сумму площадей всех пиков, соответствующих видам SM в хроматограмме для каждого образца. На фиг. 6 приведена относительная численность основных видов SM в ингредиенте, детской смеси, коровьем молоке и грудном молоке.
Относительная численность видов SM, присутствующих в ингредиенте и детской смеси, было сопоставимым с показателем для коровьего молока и незначительно отличалось от доли в грудном молоке для некоторых видов (например, SM 32:1, SM 32:0, SM 33:1; SM 34:1, SM 38:0, SM 39:1, SM 39:0 и SM 41:1) были меньше в грудном молоке, чем в ингредиенте, детской смеси и коровьем молоке. При этом для SM 36:2, SM 36:1, SM 36:0, SM 37:1, SM 38:2, SM 38:1, SM 40:1, SM 42:2 и SM 42:1 наблюдали более высокую относительную численность в грудном молоке по сравнению с другими молочными продуктами.
Выборка грудного молока состояла из набора из 6 отдельных образцов для контроля качества, собранных на момент 4 недели или позже после рождения ребенка. С учетом того, что содержание SM в грудном молоке меняется в зависимости от диеты и времени лактации, это может частично объяснять наблюдаемые различия. Тем не менее, несмотря на колебания в относительно численности некоторых видов SM, > 85% видов SM, которые регистрировали в грудном молоке, также обнаруживали в детской смеси и коровьем молоке.
Следует отметить, что для заданного m/z, определяемого по МС-спектру, могут предлагаться различные комбинации LCB-ЖК (например, SM 34:1 может соответствовать SM d18:1/16:0, d18:0/16:1, d16:1/18:0 и пр.). Поэтому оценивали профиль ГХ ЖК, чтобы получить более подробную информацию о молекулярных структурах SM в различных молочных продуктах.
Профиль жирных кислот (ЖК) во фракции SM для различных молочных продуктов
Региоизомерную структуру SM исследовали вначале фракционированием SM, а затем анализируя ЖК, присутствующие во фракциях с помощью ГХ-ПИД. Фракционирование SM проводили, как описано выше для анализа ЖХ-МС, но в этом случае элюат направляли в стеклянную пробирку объемом 5 мл, а не на МС. Затем проводили метилирование каждой фракции до последующего ГХ-анализа. Относительная численность ЖК во фракции SM приведена на фиг. 7.
Как показано на фиг. 7, фракция SM содержала главным образом насыщенные ЖК (НЖК) (т.е. миристиновую кислоту 14:0, пентадекановую кислоту 15:0, пальмитиновую кислоту 16:0, стеариновую кислоту 18:0, арахидоновую кислоту 20:0, бегеновую кислоту 22:0, трикозановую кислоту 23:0 и лигноцериновую кислоту 24:0). Более высокую долю НЖК отмечали во фракции SM для всех молочных продуктов (таблица 9). Этот результат согласуется с научной литературой, указывая на более высокое распределение НЖК c углеродной цепью более 18 во фракции SM. Такое высокое количество НЖК отражает структурную роль SM, в частности снижают текучесть и поддерживают жесткость мембраны жировых глобул молока.
Таблица 9. Процентное содержание НЖК, мононенасыщенных жирных кислот (МНЖК) и ПНЖК, регистрируемые во фракции SM от различных молочных продуктов.
Мононенасыщенные ЖК (МНЖК) составляют примерно 4-11% ЖК во фракции SM. Олеиновая кислота 18:1n-9 и нервоновая кислота 24:1n-9 были зарегистрированными 2 МНЖК. Интересно, что 24:1n-9 обнаруживали в сравнительно высокой пропорции в грудном молоке по сравнению с другими молочными продуктами, и это наблюдение согласуется с данными в научной литературе. Единственную ПНЖК - линолевую кислоту 18:2n-6 - обнаруживали в сравнительно высокой концентрации в анализируемых детских смесях и грудном молоке по сравнению с другими продуктами. Наконец, омега-3 ПНЖК не обнаруживали во фракции SM. Это также находится в соответствии с данными, приведенными в научной литературе, которые показывают, что арахидоновая кислота (AA, 20:4n-6), эйкозапентаеновая кислота (EPA, 20:5n-3) и докозагексаеновая кислота (DHA, 22:6n-3) главным образом присутствуют в PE, PI и PS.
Пример 5
Примеры искусственных питательных композиций (детских смесей) в соответствии с настоящим изобретением приведены в таблице 10 и таблице 10а
Таблица 10
на 100 г
Композиция может также содержать любые дополнительные ингредиенты, обычно присутствующие в составах детских смесей.
Таблица 10a
Композиция может также содержать любые дополнительные ингредиенты, обычно присутствующие в составах детских смесей.
Пример 6
Совместное культивирование нейронов и олигодендроцитов
Нейроны / олигодендроциты (OL) культивировали как описано ранее в работе Charles et al., 2000.
Беременных самок крыс на 17 день беременности умерщвляли посредством смещения шейных позвонков (крысы Wistar) и плоды извлекали из матки. Передний мозг удаляли и помещали в охлаждаемую льдом среду Лейбовица (L15), содержащую 2% пенициллина-стрептомицина (PS) и 1% бычьего сывороточного альбумина (БСА). Передний мозг разделяли трипсинизацией в течение 20 мин при 37°C (трипсин EDTA 1X). Реакцию останавливали добавлением модифицированной по способу Дульбекко среды Игла (DMEM), содержащей ДНКазу I степени II (0,1 мг/мл) и 10% эмбриональной сыворотки телят (FCS). Затем клетки механически разделяли 3 пересевами через пипетку объемом 10 мл. После этого клетки центрифугировали при 180 x g в течение 10 мин при температуре 4°C на слой БСА (3,5%) в среде L15. Супернатант сливали и клетки в осадке ресуспендировали в DMEM, содержащей 10% FCS. Затем клетки центрифугировали при 515 x g в течение 10 мин при 4°C. Супернатант сливали и клетки в осадке ресуспендировали в культуральной среде, содержащей нейробазальную среду с добавками 2% B27, 2 мМ L-глутамина (L Glu), 2% раствора PS, 1% FCS и 10 нг/мл тромбоцитарного фактора роста (PDGF-AA). Жизнеспособные клетки подсчитывали с помощью цитометра Нойбауэра с использованием теста на вытеснение трипанового синего. Клетки высевали с плотностью 20 000 клеток/лунка в 96-луночные планшеты с предварительным покрытием поли-L-лизином и ламинином.
Через день после высеивания (день 1 культивирования) клетки инкубировали с тестируемым соединением (выбранным из перечисленных в таблице 11) или с эстрадиолом. Контрольные клетки не инкубировали с тестируемым соединением или эстрадиолом. В качестве положительного контроля использовали эстрадиол. Известно, что эстрадиол индуцирует пролиферацию клеток-предшественников олигодендроцитов (OPC). Был также продемонстрирован положительный эффект воздействия эстрадиола на дифференциацию OL, а также его влияние на процесс ранней миелинизации. Опубликованы также выводы о положительном влиянии эстрадиола на отрастание нейритов (см. обзор Alevaro et al., 2010).
Планшеты выдерживали при 37°C в увлажняемом инкубаторе в атмосфере воздуха (95%) - CO2 (5%). Половину среды заменяли через день свежей средой с тестируемым соединением или контрольным соединением. Тестируемое или контрольное соединения выдерживали при заданной концентрации в продолжение всех экспериментов. Соединения тестировали на 1 культуре (6 лунок на каждый набор условий). Клетки затем использовали в день 12, 18 или 30 культивирования для оценки одного из следующих показателей: пролиферация OPC, дифференциация OPC в OL и процесс ранней миелинизации (миелиновая оболочка), или созревание OL (миелиновое созревание) и процесс зрелой миелинизации (миелиновая оболочка).
Пролиферация OPC: измерение A2B5-положительных клеток и полной длины аксонов (NF)
На день 12 культивирования клетки фиксировали холодной смесью абсолютного этанола (95%) и чистой уксусной кислоты (5%) в течение 5 мин. Затем увеличивали проницаемость клеток и блокировали неспецифические сайты фосфатным буферным физиологическим раствором (PBS), содержащим 0,1% сапонина и 1% FCS, в течение 15 мин при комнатной температуре.
Клетки затем инкубировали с моноклональными анти-A2B5, конъюгированными с alexa fluor® 488, продуцированными в организме мышей, с разведением 1/200 в PBS, содержащем 1% FCS, 0,1% сапонина, в течение 2 ч при комнатной температуре и с анти-NF (фосфорилированный и нефосфорилированный нейрофиламент 200), продуцированными в организме кролика, с разведением 1/500 в PBS, содержащем 1% FCS, 0,1% сапонина в течение 2 ч при комнатной температуре. Наличие данного антитела обнаруживали с использованием козьего антикроличьего антитела с Alexa Fluor 568 при разбавлении 1/400 в PBS с 1% FCS, 0,1% сапонина в течение 1 ч при комнатной температуре.
Количественно определяли суммарное число OPC (число A2B5-положительных клеток) (чтобы оценить пролиферацию), измеряли аксонную сеть (полную длину аксонов (NF)), чтобы оценить влияние соединения на нейронную сеть (качество миелинизации напрямую связывают с качеством аксонной сети).
Дифференциация OPC в OL и процесс миелинизации (миелиновая оболочка): измерение числа и площади MAG-положительных клеток, перекрывания MAG/NF оболочки и полной длины аксонов (NF)
На день 18 культивирования клетки фиксировали холодной смесью абсолютного этанола (95%) и чистой уксусной кислоты (5%) в течение 5 мин. Затем увеличивали проницаемость клеток и блокировали неспецифические сайты фосфатным буферным физиологическим раствором (PBS), содержащим 0,1% сапонина и 1% FCS, в течение 15 мин при комнатной температуре.
Клетки затем инкубировали с моноклональными анти-MAG, продуцированными в организме мышей, с разведением 1/400 в PBS, содержащем 1% FCS, 0,1% сапонина, и с анти-NF (фосфорилированный и нефосфорилированный нейрофиламент 200), продуцированными в организме кролика, с разведением 1/500 в PBS, содержащем 1% FCS, 0,1% сапонина, в течение 2 ч при комнатной температуре. Наличие данного антитела обнаруживали с использованием козьего антимышиного антитела CF 488 A при разбавлении 1/800 в PBS с 1% FCS, 0,1% сапонина и козьего антикроличьего антитела с Alexa Fluor 568 при разбавлении 1/800 в PBS с 1% FCS, 0,1% сапонина в течение 1 ч при комнатной температуре.
Количественно определяли полное число OL (число и площадь MAG-положительных клеток) (чтобы оценить процесс дифференциации), а также оболочку из OPC вокруг аксонов (перекрывание MAG/NF оболочки) (процесс миелинизации). Проводили измерение аксонной сети (полной длины аксонов (NF)), чтобы оценить влияние соединений на нейронную сеть.
Созревание OL (созревание миелина): измерение числа и площади МВР-положительных клеток, перекрывания МВР/NF оболочки и полной длины аксонов (NF)
На день 30 культивирования клетки фиксировали холодной смесью абсолютного этанола (95%) и чистой уксусной кислоты (5%) в течение 5 мин. Затем увеличивали проницаемость клеток и блокировали неспецифические сайты фосфатным буферным физиологическим раствором (PBS), содержащим 0,1% сапонина и 1% FCS, в течение 15 мин при комнатной температуре.
Клетки затем инкубировали с моноклональными анти-MBP, продуцированными в организме мышей, с разведением 1/1000 в PBS, содержащем 1% FCS, 0,1% сапонина, и с анти-NF (фосфорилированный и нефосфорилированный нейрофиламент 200), продуцированными в организме кролика, с разведением 1/500 в PBS, содержащем 1% FCS, 0,1% сапонина, в течение 2 ч при комнатной температуре. Наличие данного антитела обнаруживали с использованием козьего антимышиного антитела CF 488 A при разбавлении 1/800 в PBS с 1% FCS, 0,1% сапонина и козьего антикроличьего антитела с Alexa Fluor 568 при разбавлении 1/400 в PBS с 1% FCS, 0,1% сапонина в течение 1 ч при комнатной температуре.
Количественно определяли полное число OL (число и площадь МВР-положительных клеток) (чтобы оценить процесс созревания OL), а также оболочку из миелина вокруг аксонов (перекрывание МВР/NF оболочки). Проводили измерение аксонной сети (полной длины аксонов (NF)), чтобы оценить влияние соединений на нейронную сеть.
Для всех измерений тестировали по одной культуре (6 лунок на каждый набор условий). Для каждого тестируемого набора условий получали 30 изображений (каждое изображение соответствовало тому или иному полю) на лунку и анализировали с использованием ImageXpress (Molecular devices) с 20x увеличением с СИД лампой (возбуждение 360/480/565 и испускание 460/535/620). 30 изображений получали автоматически, и они отображали 80% общей поверхности культуральной лунки.
Результаты выражали в виде совокупной средней длины в мкм нейритной сети или миелиновой оболочки с меткой для заданного маркера (MAG или MBP) на каждое поле. Для оценки формирования оболочки измеряли область перекрывания между NF и MAG или MBP.
Для оценки популяции OPC, популяции MAG-положительных клеток, популяции MBP-положительных клеток проводили автоматический подсчет числа положительных клеток на каждом изображении (= поле). Результаты выражали в виде средних значений положительных клеток на каждое поле.
Все изображения получали в одинаковых условиях.
Таблица 11
Результаты представлены на фиг. 8-28
Пример 7
Материалы и способы
1. Приготовление питательного слоя: диссоциация неонатальной коры и сохранение смешанных глиальных культур
Свежепрепарированные мозги помещали в водяную баню при 37°C на 3 мин, затем кору измельчали продавливанием через носик пипетки P1000, чтобы получить более мелкие фрагменты. Добавляли 75 мкл раствора ОРС папаина на каждый образец мозга, затем ткани инкубировали в водяной бане при 37°C в течение 20 мин. К суспензии тканей затем добавляли смешанную глиальную культуру, с тем чтобы обеспечить инактивацию раствора OPC папаина.
Ткани затем растирали с помощью стерильной оплавленной на огне пастеровской пипетки, после чего добавляли по 4 мл среды смешанной глиальной культуры на каждый образец мозга. Клетки центрифугировали при 1200 об/мин (~ 300 g) в течение 5 мин, затем клетки ресуспендировали в теплой среде смешанной глиальной культуры и высевали в колбу с PLL-покрытием.
Через 4 часа после высевания производили полную замену среды, с тем чтобы удалить большую часть остатков тканей, образовавшихся при растирании, и стимулировать жизнеспособность культуры. Через 3 дня культивирования проводили замену 2/3 среды, после чего среду больше не меняли. Затем клетки выдерживали в культуре до конфлюентности.
2. Приготовление гиппокампальных нейронов
Гиппокампальные нейроны выделяли из эмбрионов детенышей (E18) крыс линии Спрег-Доули. Коротко говоря, после умерщвления животных мозги изолировали,удаляли покрывающие оболочки из медиального аспекта мозговых полушарий, затем препарировали гиппокампы и хранили при 4°C до полного завершения процесса.
Затем ткань инкубировали с 2,5% трипсина в течение 15 мин на водяной бане при 37°C, после чего осторожно промывали и хранили в культуральной среде. Разделение гиппокампа проводили многократным пипетированием через функционализированную стерильную пастеровскую пипетку. После механической диссоциации клетки высевали с желаемой плотностью в нейрональной посевной среде, давали восстановиться в течение 4 часов, а затем переводили в полную нейрональную культуральную среду.
3. Очистка OPC от смешанных глиальных культур для формирования о-культур OL/гиппокампальных нейронов
На день 9 смешанной глиальной культуры колбы встряхивали при 50 об/мин в течение 45 мин на орбитальном встряхивателе в инкубаторе для тканевых культур в атмосфере 5% CO2. Цель такого встряхивания заключалась в том, чтобы удалить любые слабо связанные примесные клетки из монослоя.
Затем меняли среду и заменяли ее 4 мл свежей культуральной смешанной глиальной среды с добавлением 5 мкг/мл инсулина. Колбы снова устанавливали на встряхиватель, уравновешивали примерно в течение 3 часов, затем встряхивали примерно в течение 16 часов при 220 об/мин (в течение ночи).
На следующее утро собирали смешанную глиальную культуральную среду, содержащую микроглиальные и OPC клетки и предварительно высевали в чашки Петри P100 (необработанные для культивирования) в течение 30 мин для очистки клеток OPC; при этом микроглиальные клетки сразу же начинали фиксироваться на поверхности чашки Петри, тогда как клетки ОРС оставались в надосадочной среде.
Через 30 минут после предварительного высевания среду собирали и производили подсчет OL, после чего их высевали на гиппокампальные нейроны в конечном объеме 1 мл среды OL.
Проводили полную замену среды OL (без CNTF), затем клетки сохраняли в культуре до соответствующего момента проведения экспериментов.
Для экспериментов созревания использовали следующую процедуру:
a. Рост OPC на питательном слое астроцитов для 10 DIV (дней in vitro)
b. Выделение OPC (день 0)
c. Добавление соединений (день 3)
d. Количественная оценка созревания на день 4, 7 и 10.
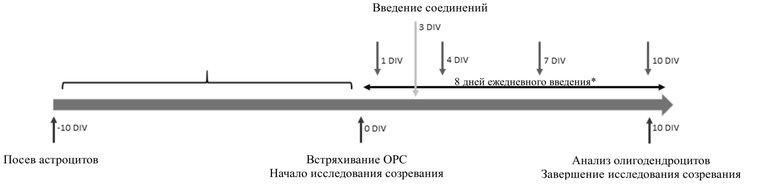
Для экспериментов миелинизации использовали следующую процедуру:
a. Рост гиппокампальных нейронов до полного созревания нейрональной сети (14 DIV)
b. Одновременный рост OPC на питательном слое астроцитов в течение 10 DIV
c. Выделение OPC и совместное культивирование с нейронами (день 14)
d. Добавление соединений (день 15)
e. Количественная оценка миелинизации на день 15 (через 1 день после высевания совместного культивирования до внесения соединения), 18, 21/23 и 28/29 совместного культивирования
4. Получение изображений
Все культуры в различные моменты времени эксперимента фиксировали в 4% параформальдегида и 4% сахарозы при комнатной температуре (КТ) в течение 10 мин. Первичные и вторичные антитела вносили в буфер GDB (30 мМ фосфатный буфер, pH 7.4, содержащий 0,2% желатина, 0,5% Triton X-100 и 0,8 M NaCl) в течение 2 ч при комнатной температуре. Клетки окрашивали соответствующим маркером (использованное первичное антитело: анти-A2B5 антитело (ABCAM кат. № ab53521), крысиное анти-MBP (BIO-RAD кат. № aa82-87), антитело маркера олигодендроцитов O4 (R&D Systems кат. № MAB1326), моноклональное антитело анти-βIII тубулин (Promega кат. № G7121); использованное вторичное антитело: Alexa анти-555 крысы (Life Tech A-21434), Alexa анти-488 мыши (Life Tech A-11009). После иммуноцитохимического окрашивания все изображения получали с помощью Array Scan XTI (ThermoScientific); объектив был 20x с группированием 2 x 2. Для каждого условия и воспроизводящей лунки (трехкратно) получали минимум 15 изображений.
Для анализа всех накопленных изображений использовали программное обеспечение HCS Studio Cell Analysis, в частности его приложение «Scan».
Папаиновый раствор OPC (составленный в MEM)
Раствор папаина 1,54 мг/мл
L-цистеин 360 мкг/мл
ДНКаза I 60 мкг/мл
Среда для смешанной культуры глиальных клеток (составленная в DMEM)
FBS 10%
Пенициллин/стрептомицин: (0,33% из маточного раствора) 33 единиц/мл пенициллина и 33 мкг/мл стрептомицина
GlutaMAX 1%
Среда OL
DMEM
100X OL-добавка
Бычий инсулин (из 1 мг/мл маточного раствора)
GlutaMAX
Холотрансферрин (из 33 мг/мл маточного раствора)
Добавка B27
FBS
CNTF (из 50 нг/мкл маточного раствора)
Результаты представлены на фиг. 30-49
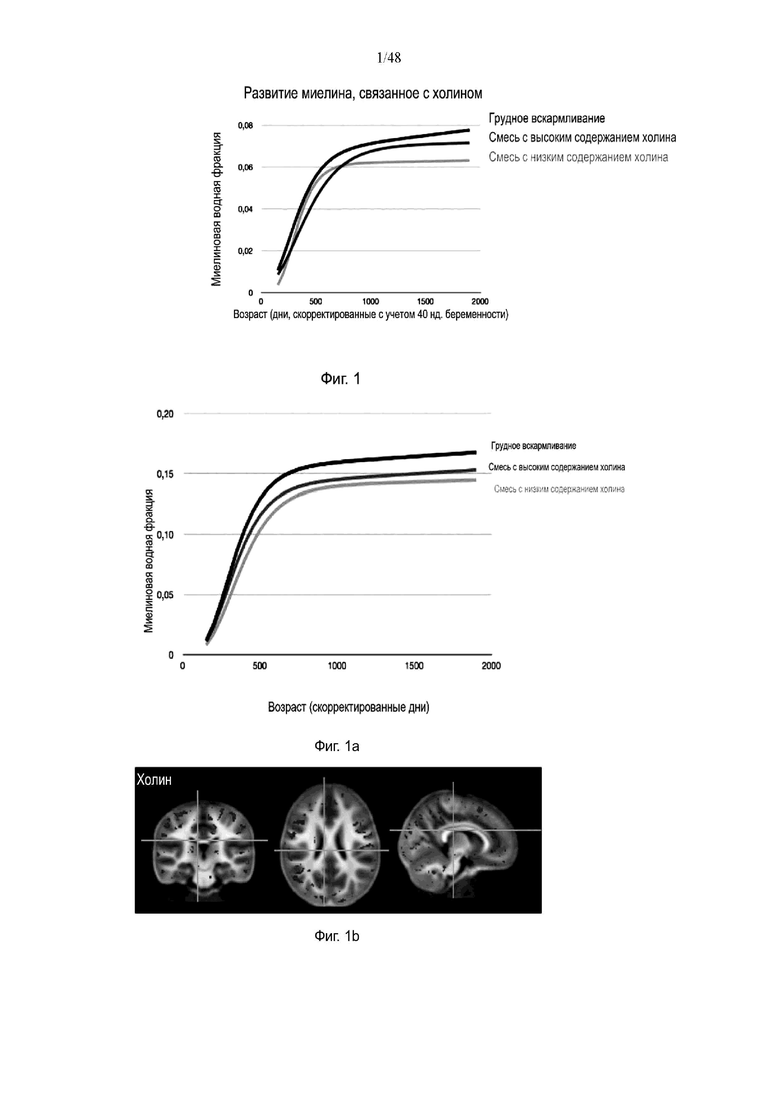
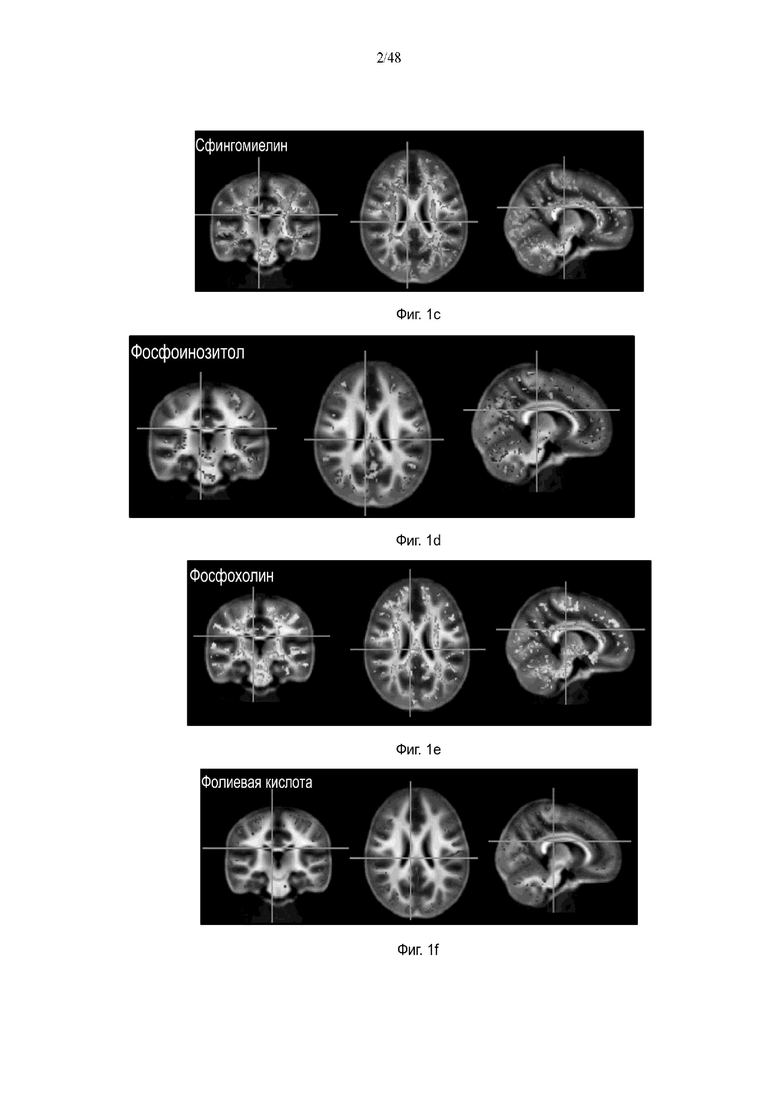
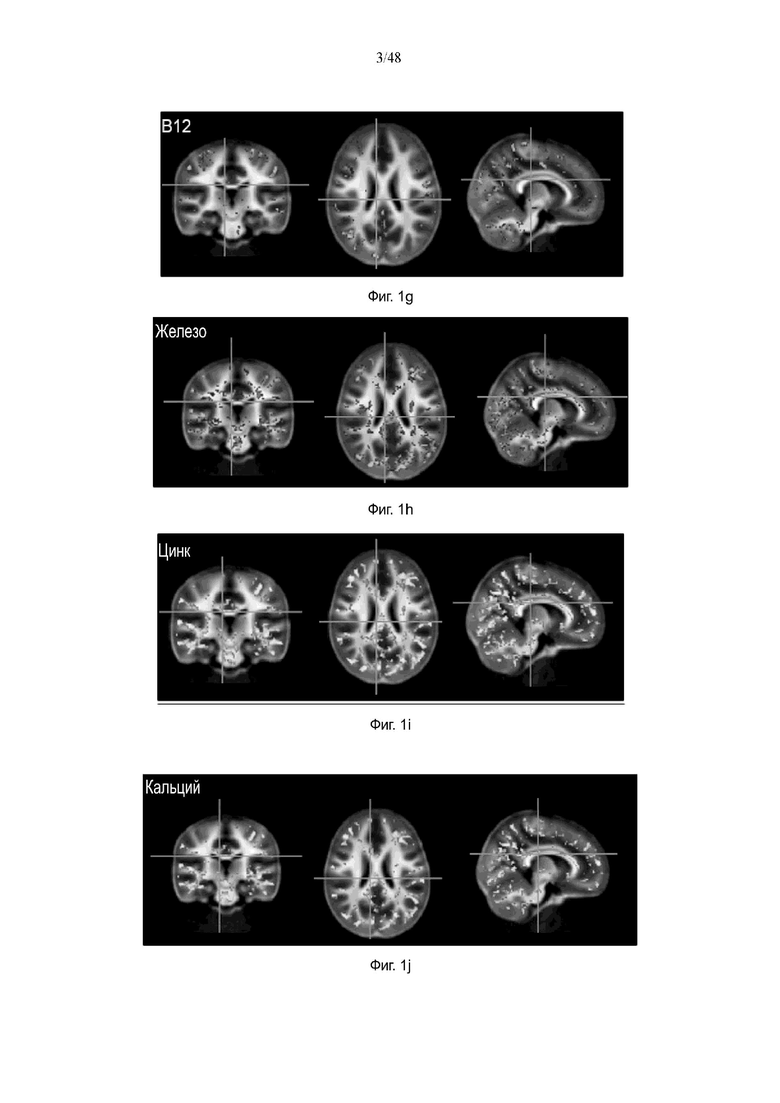
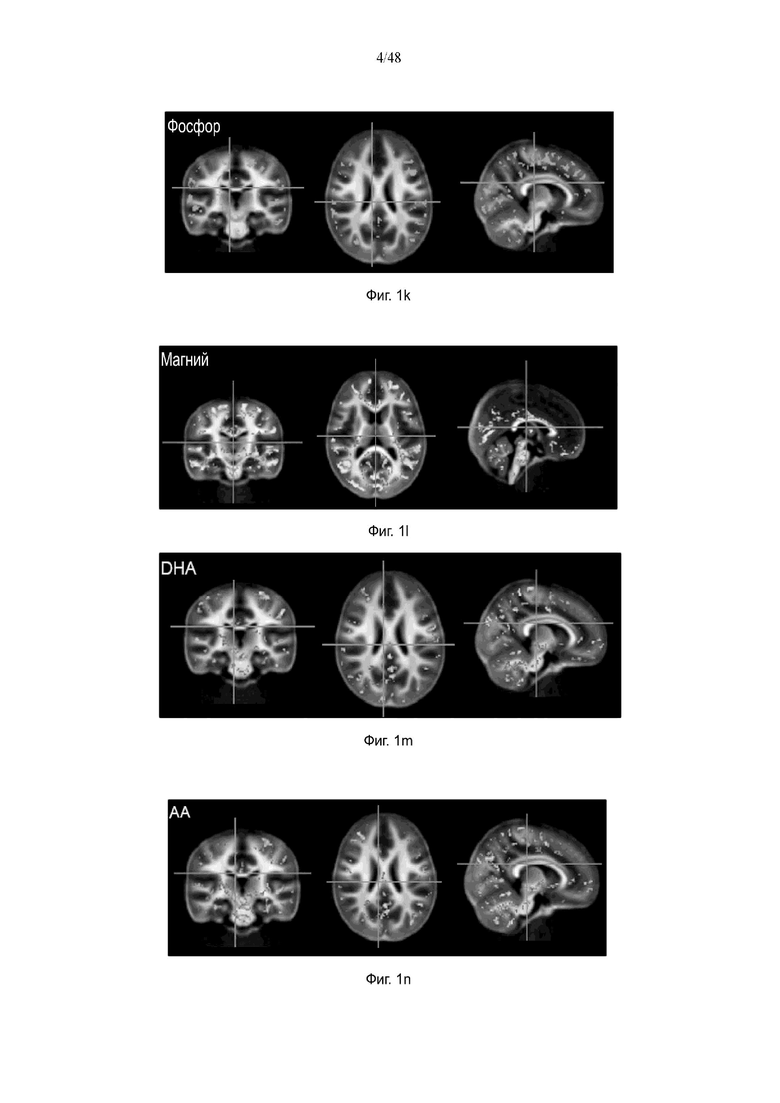
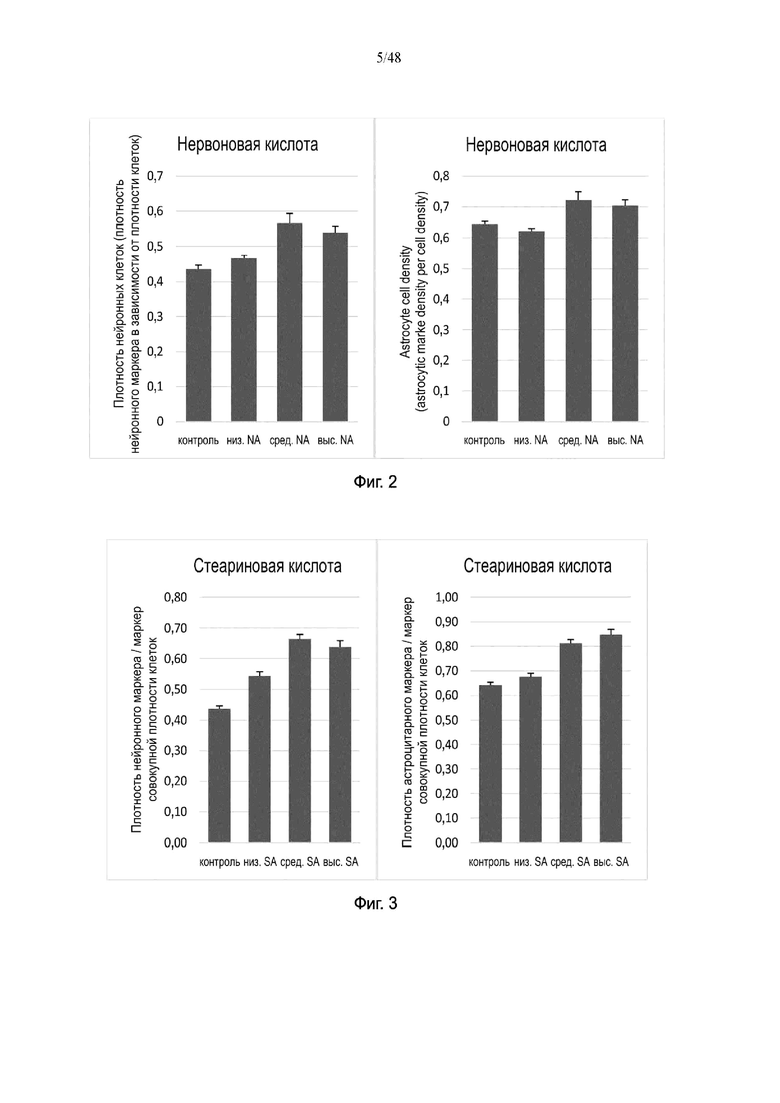
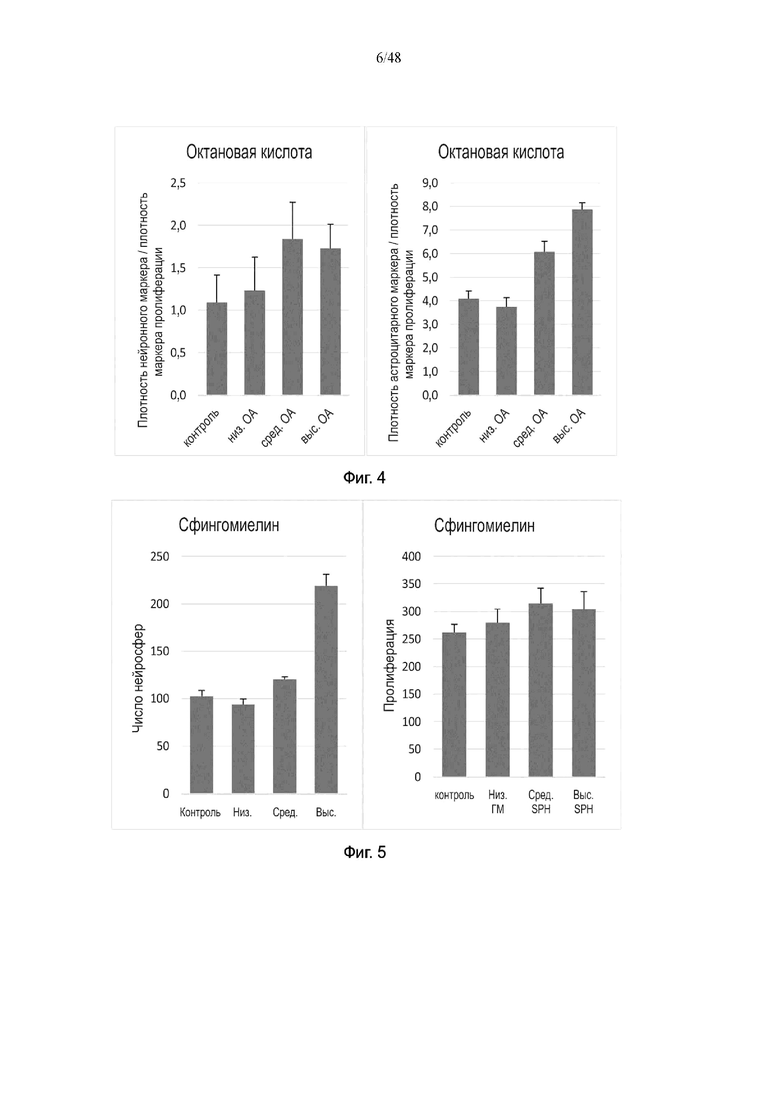
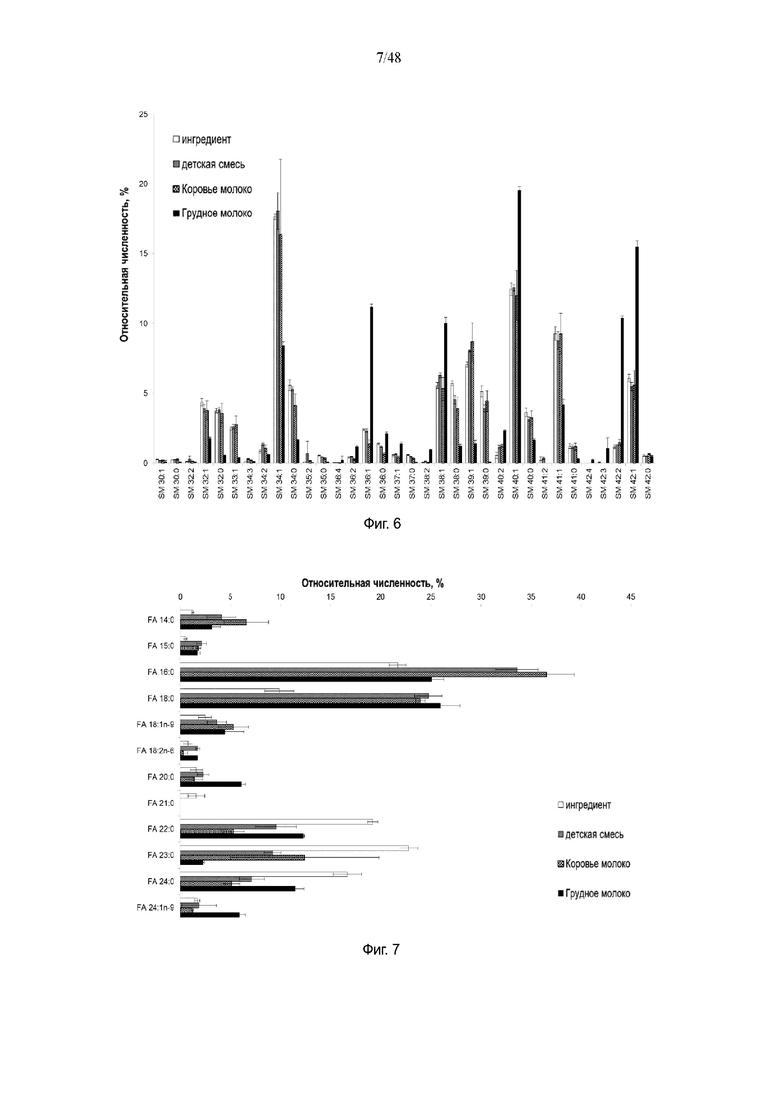
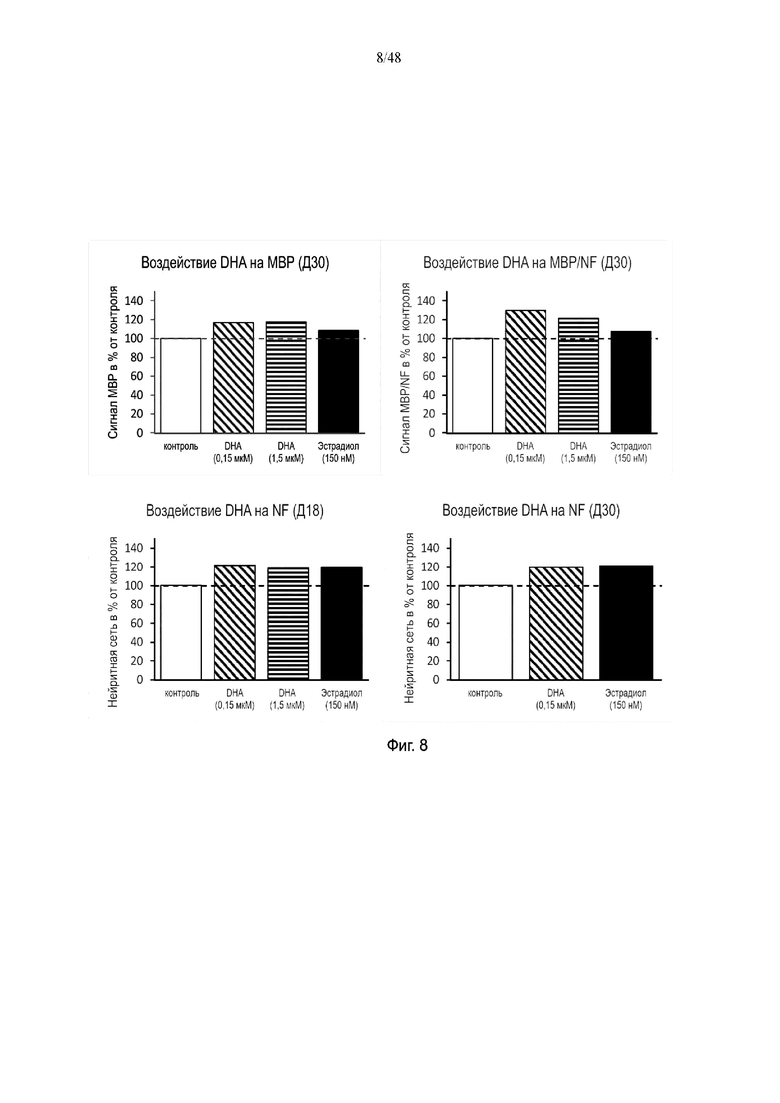
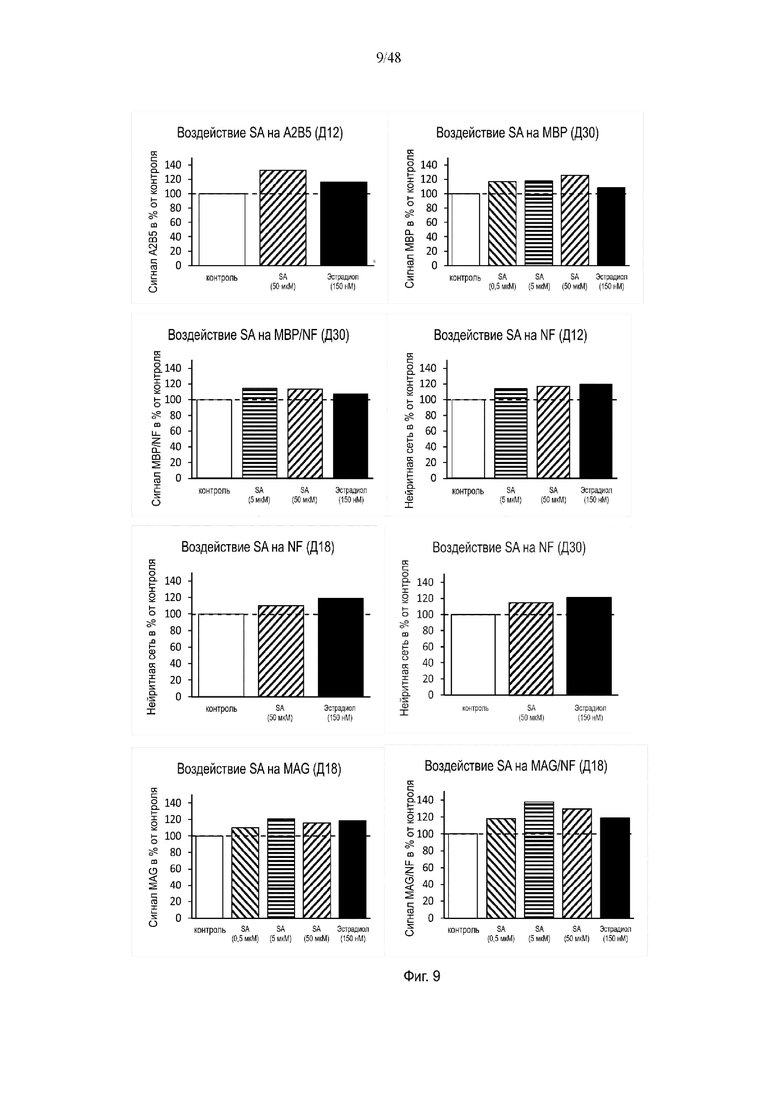
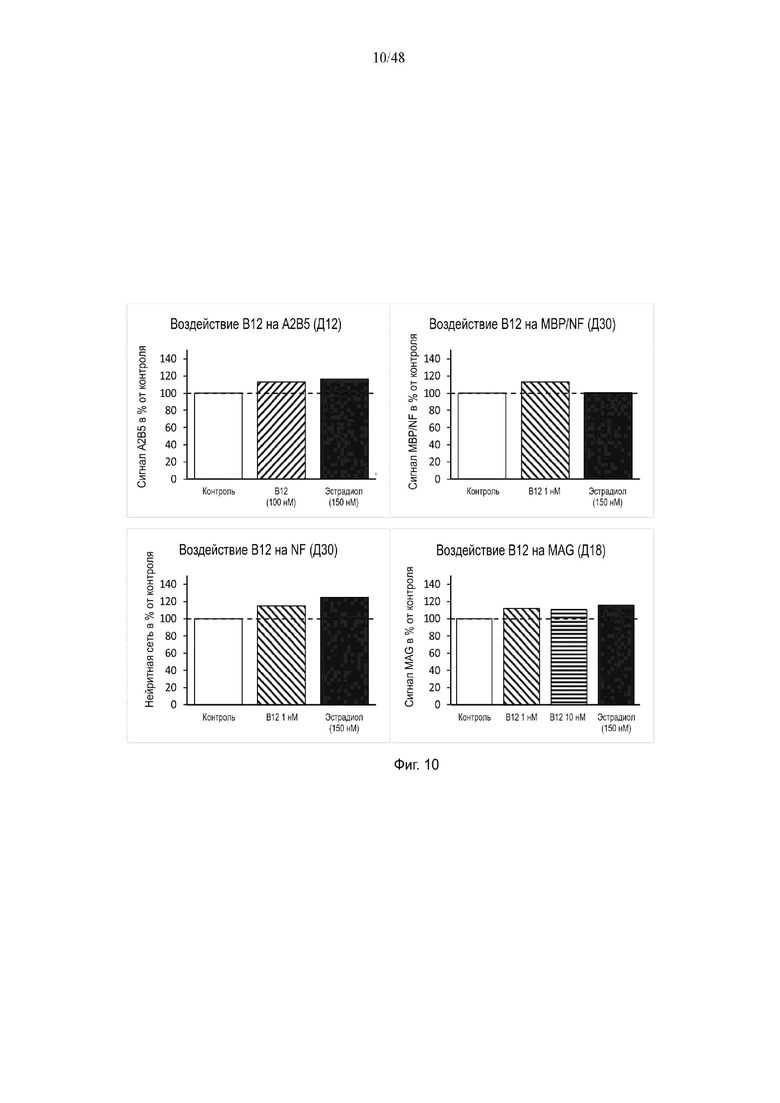

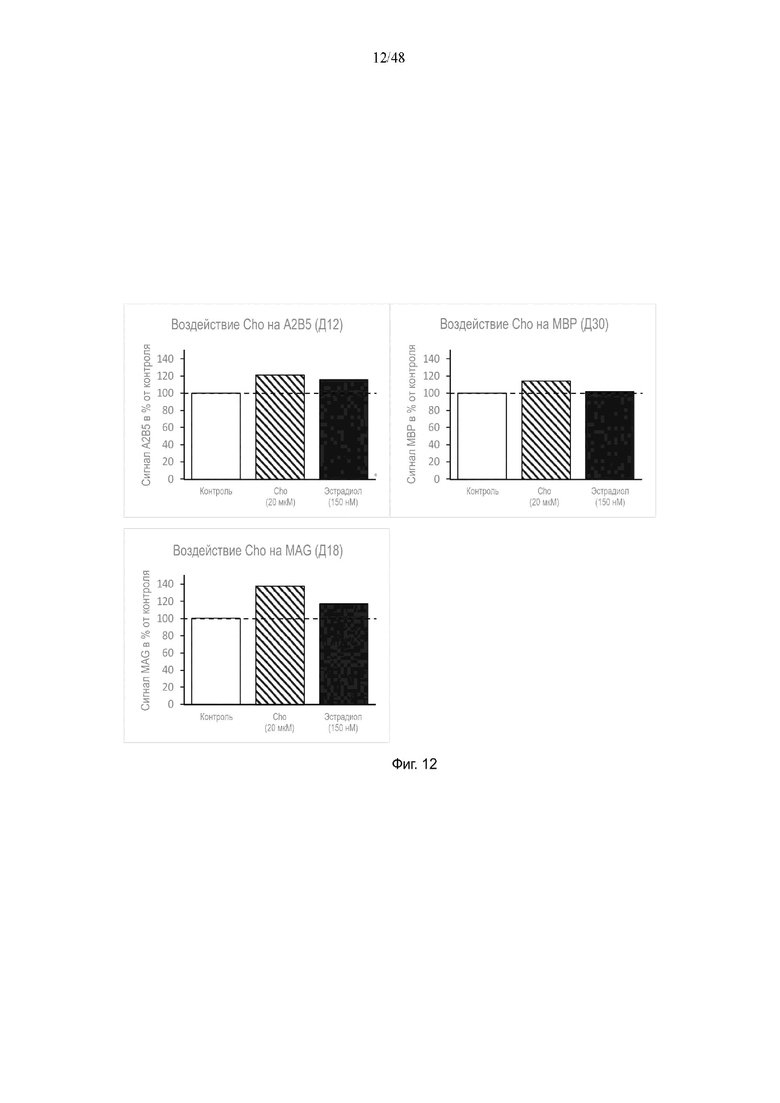
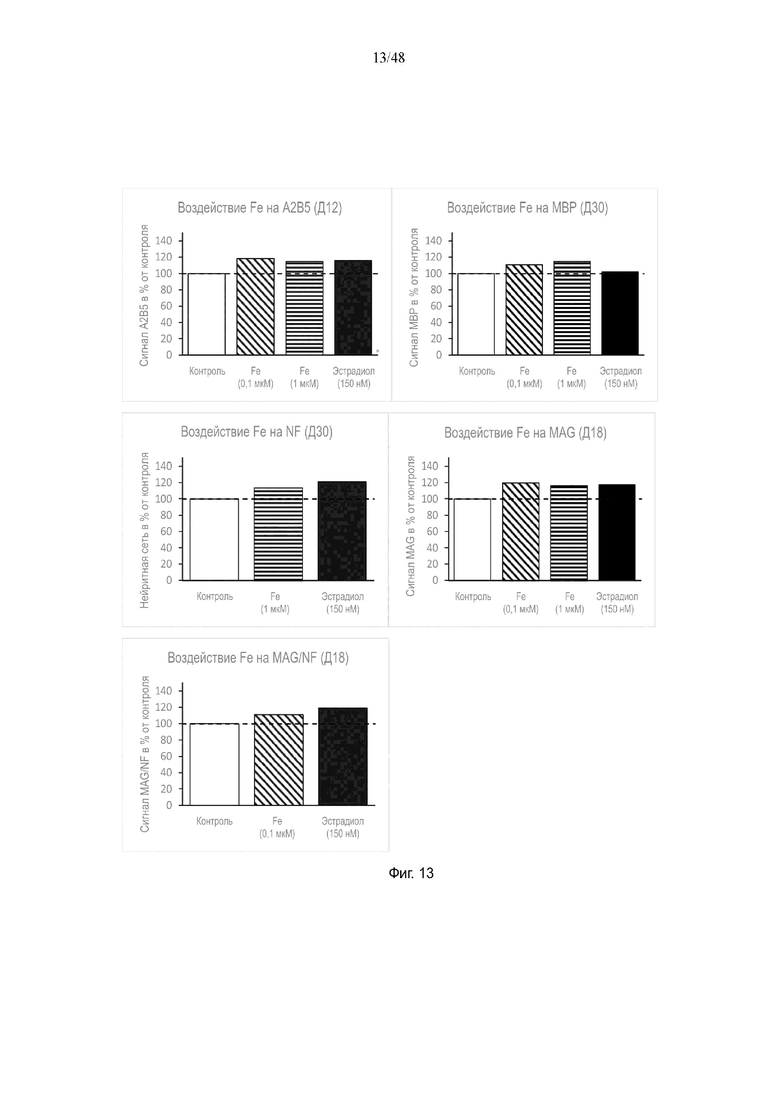

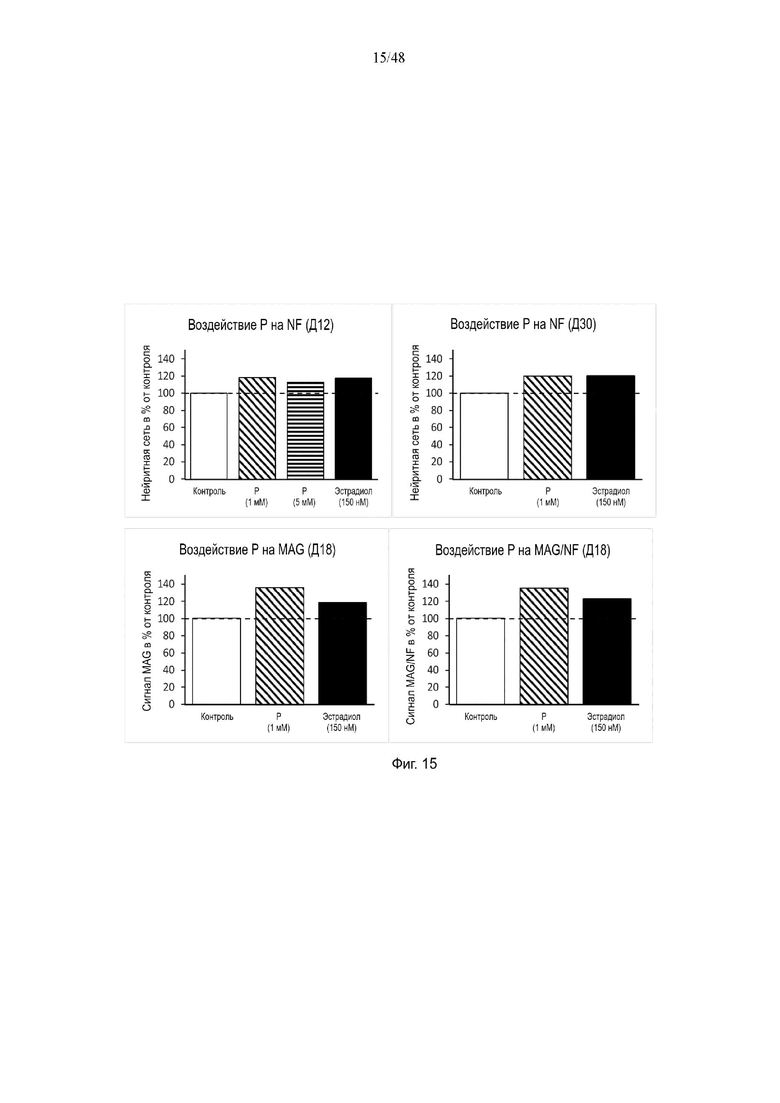

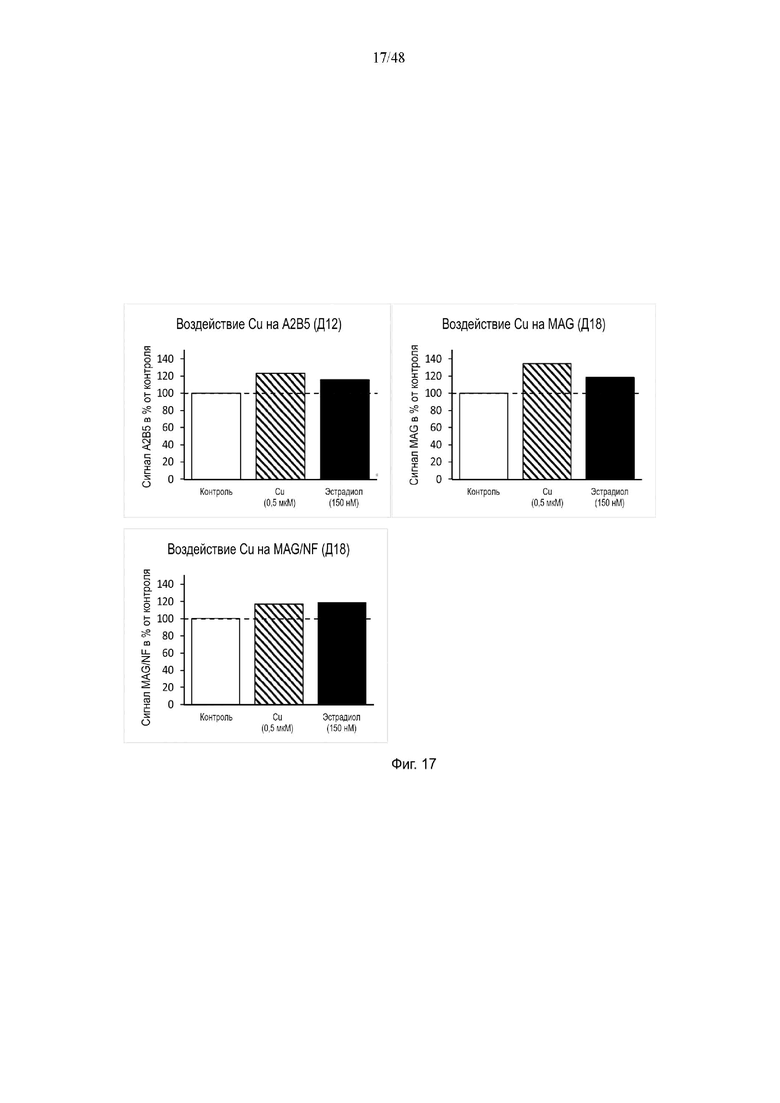
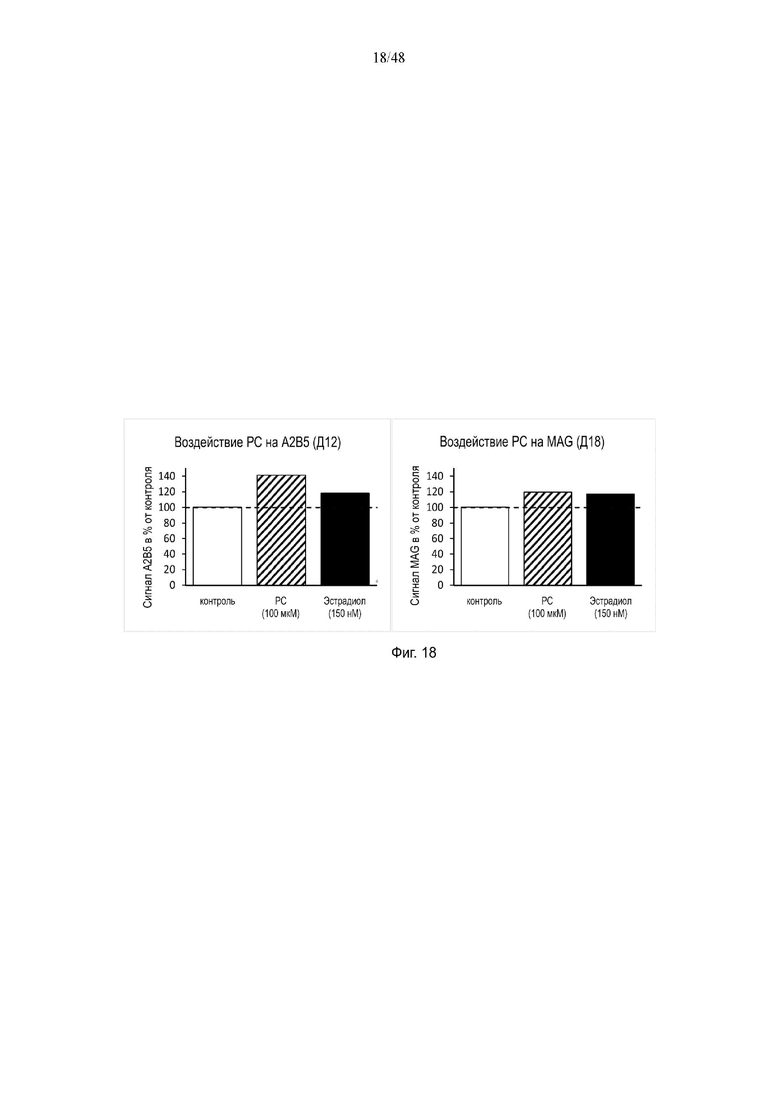
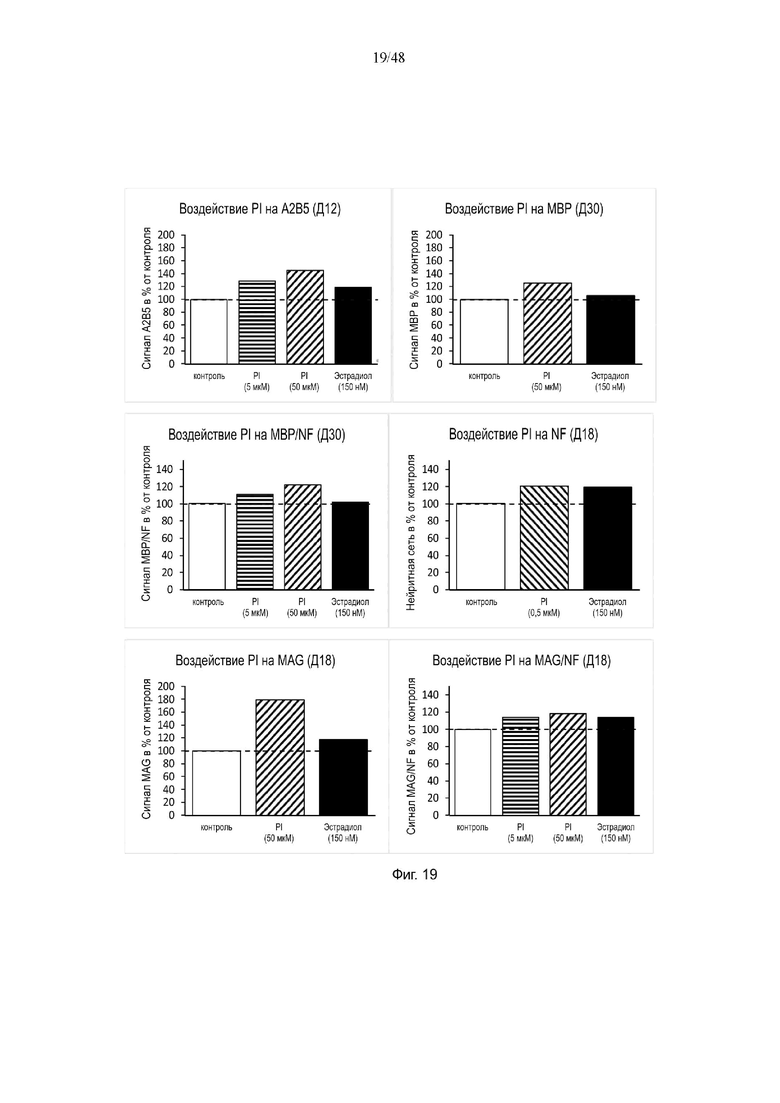
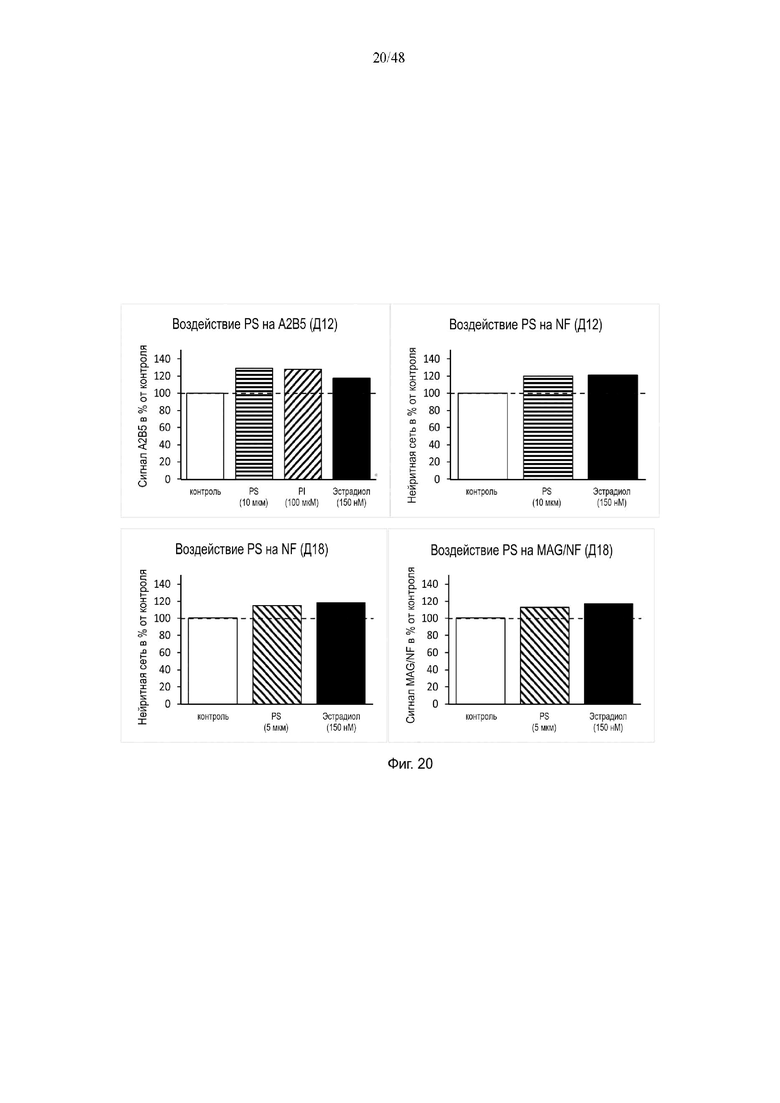
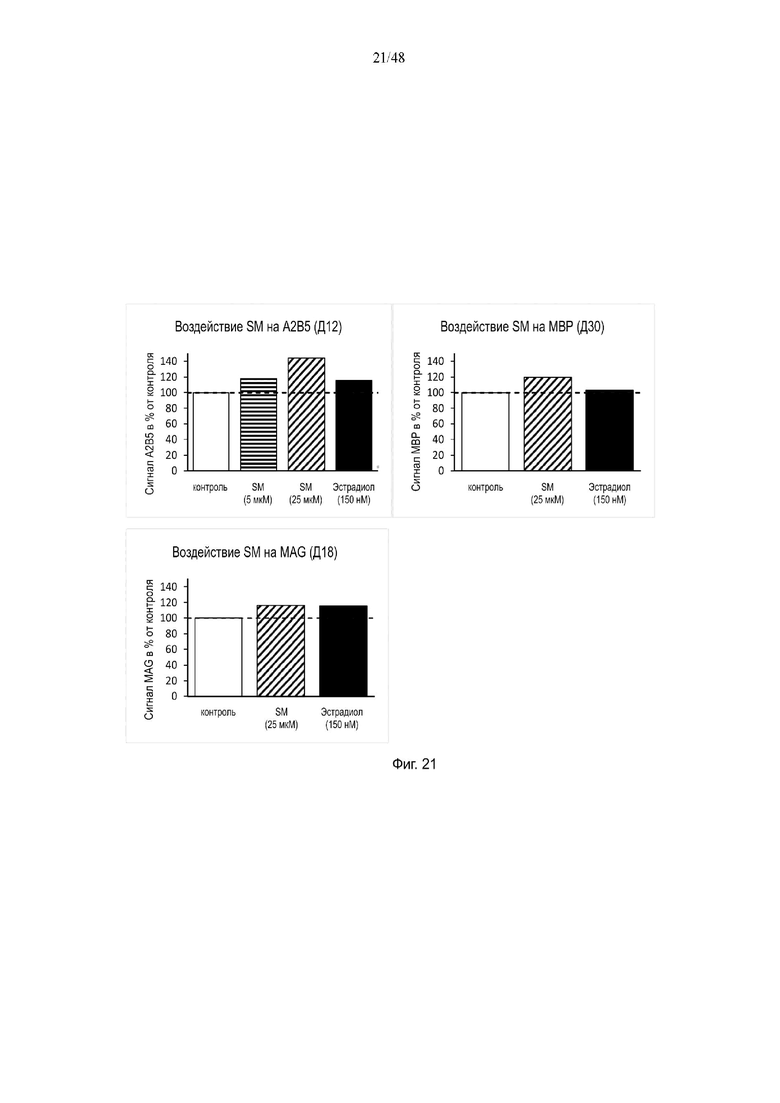
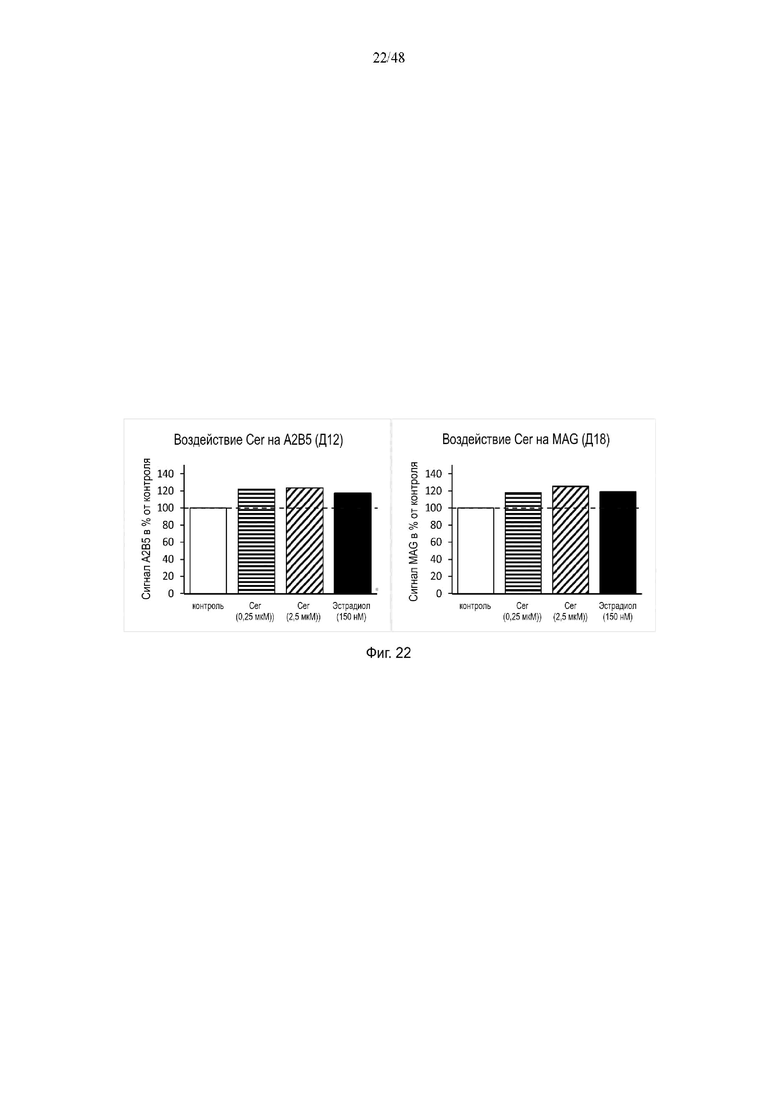
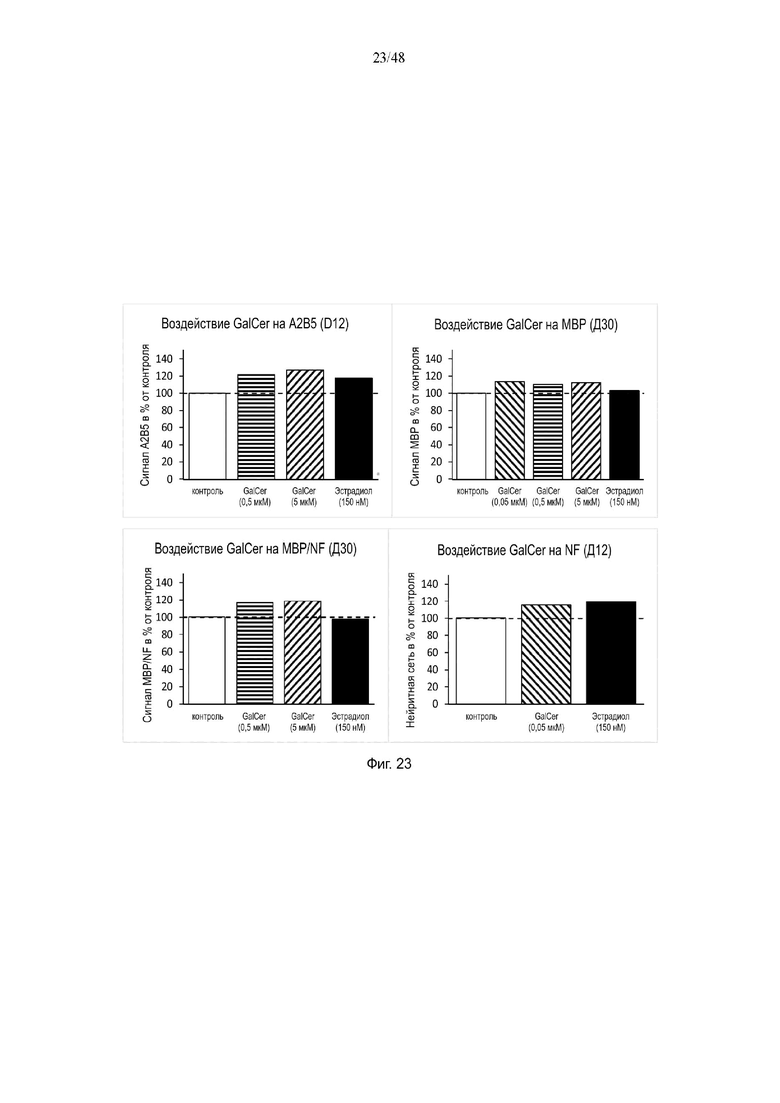
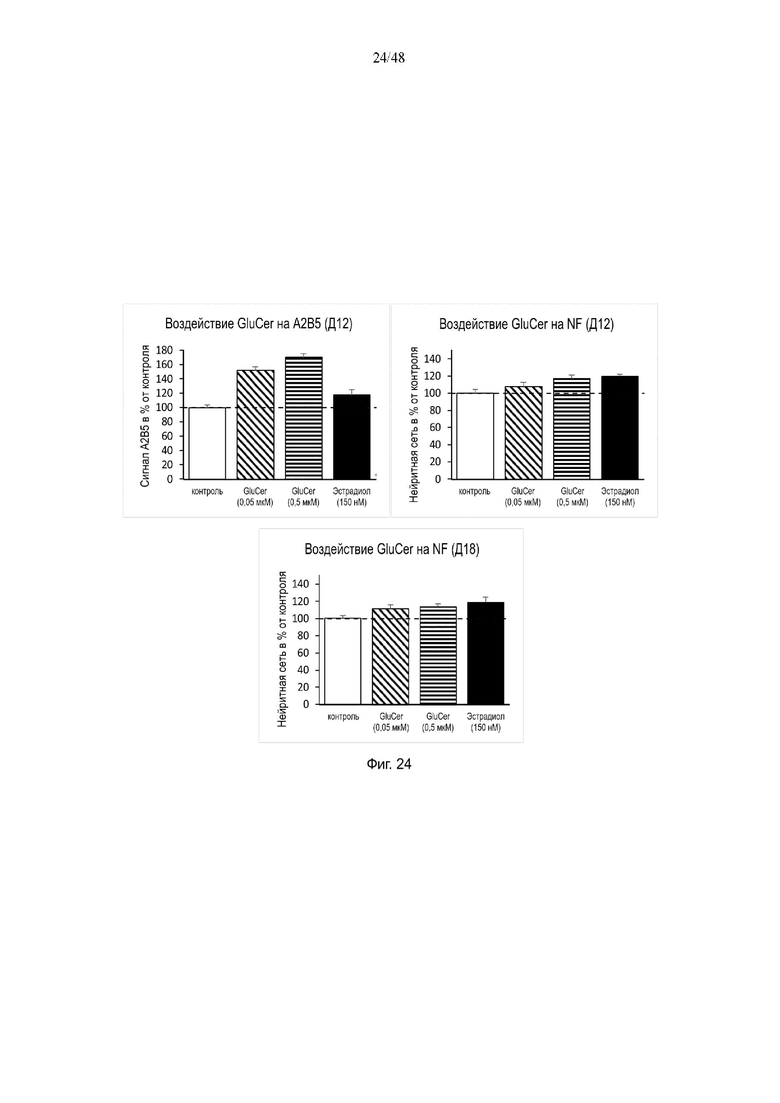

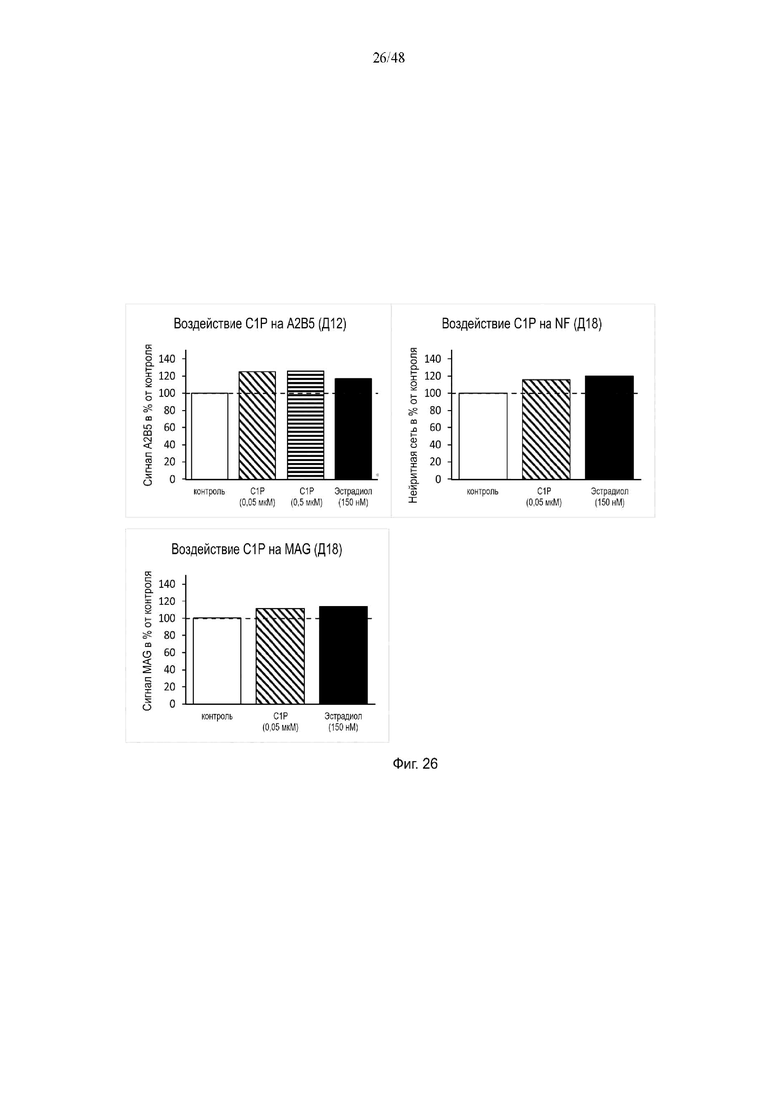
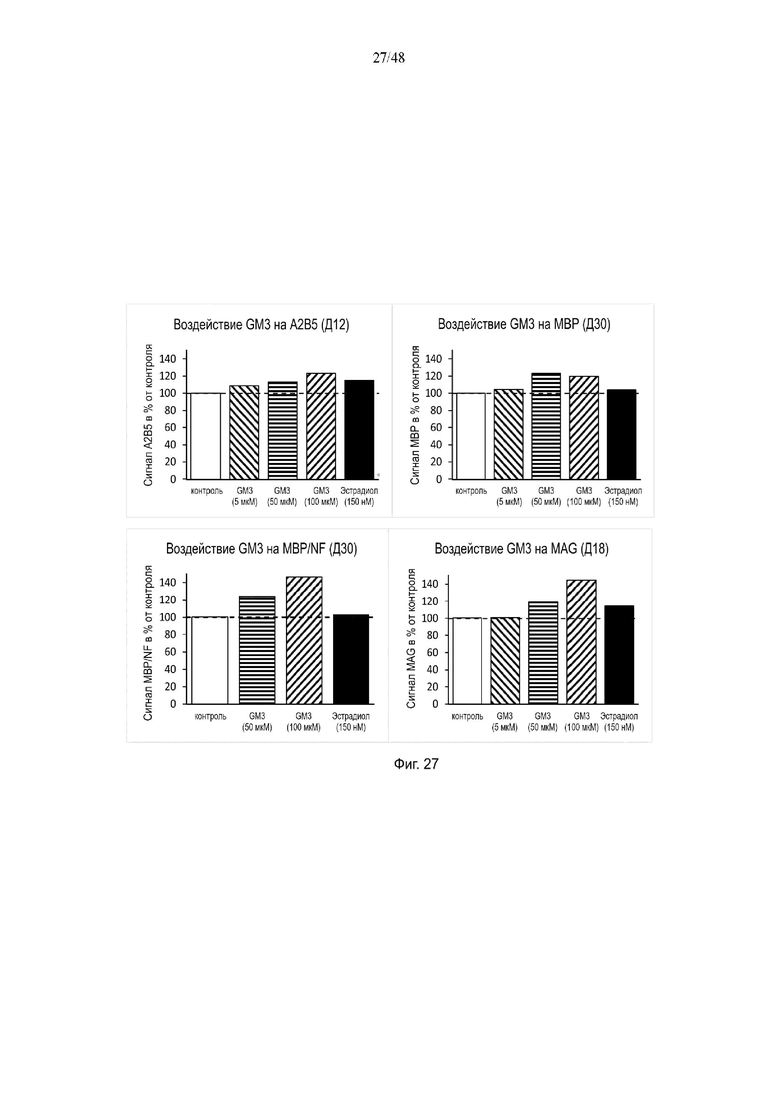
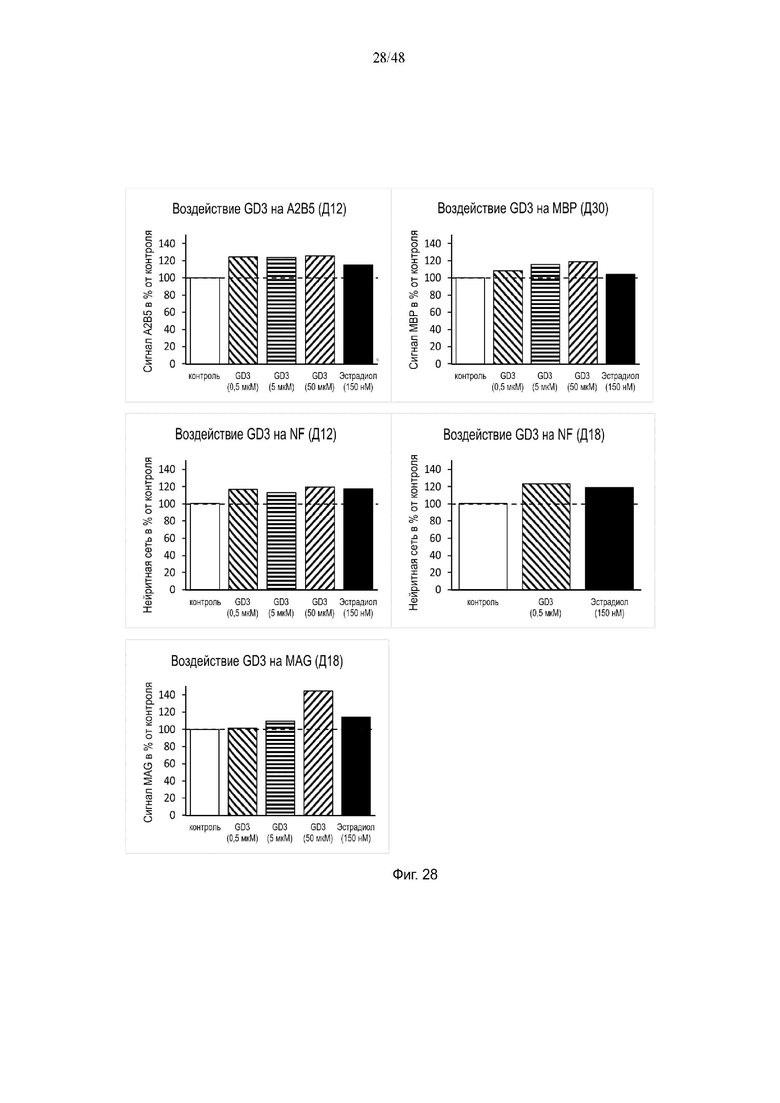

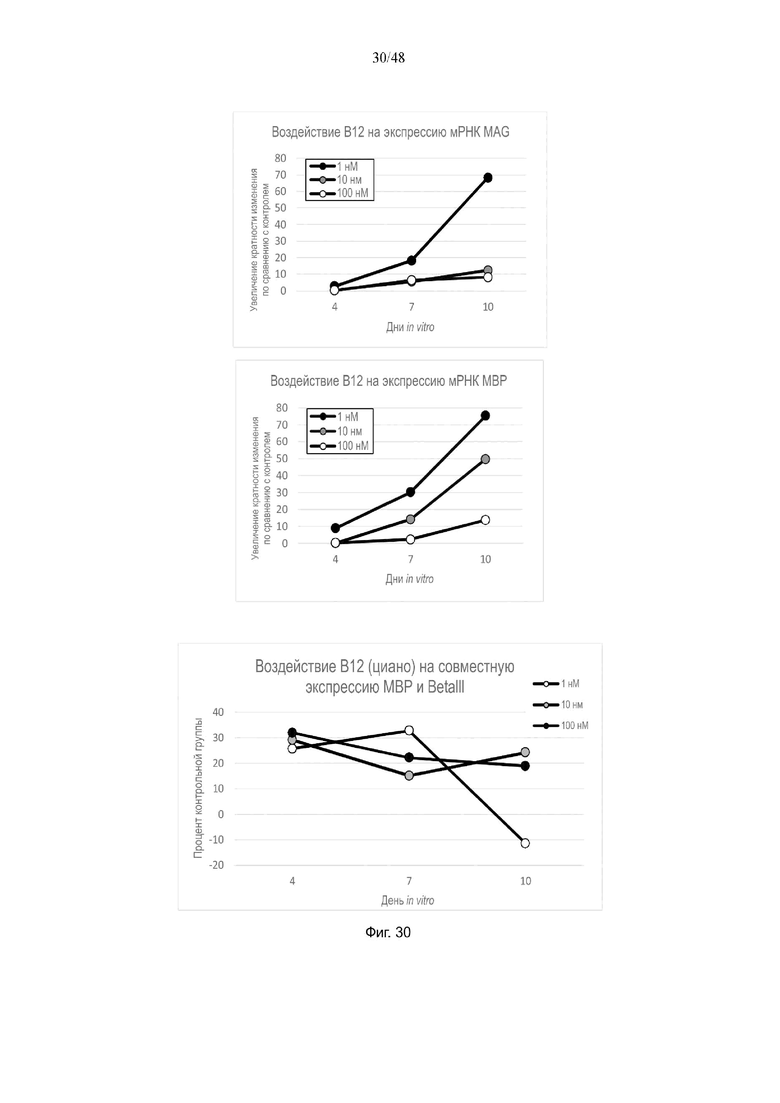
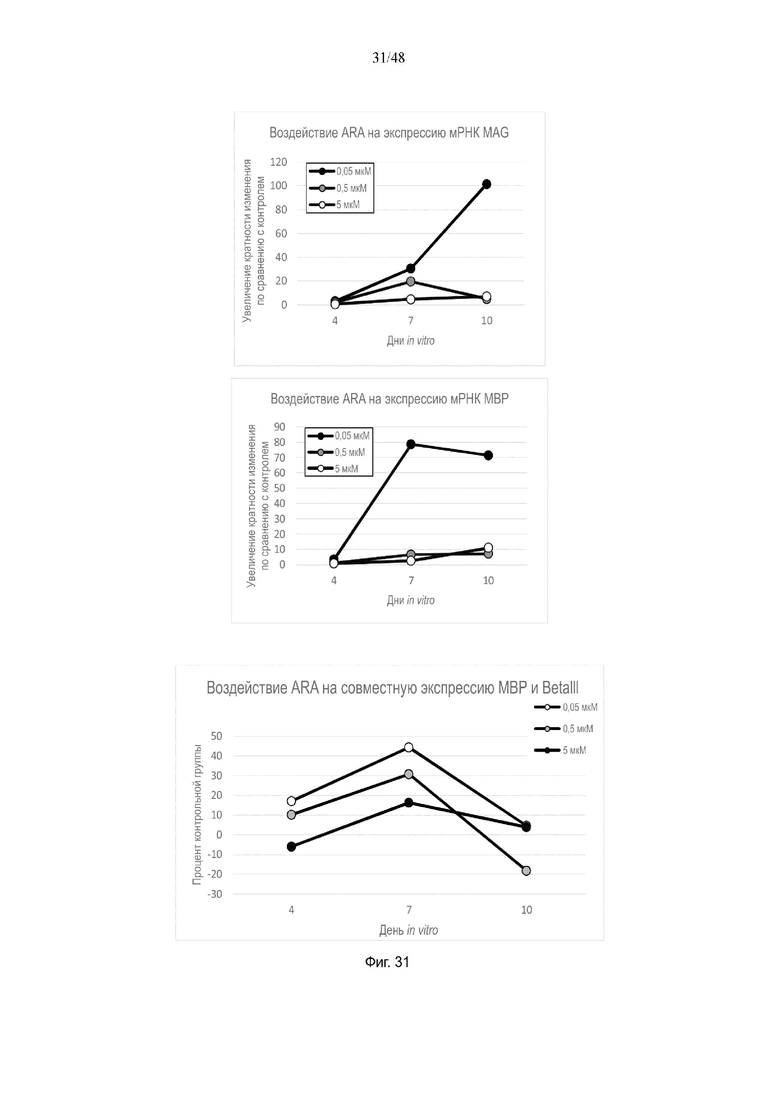

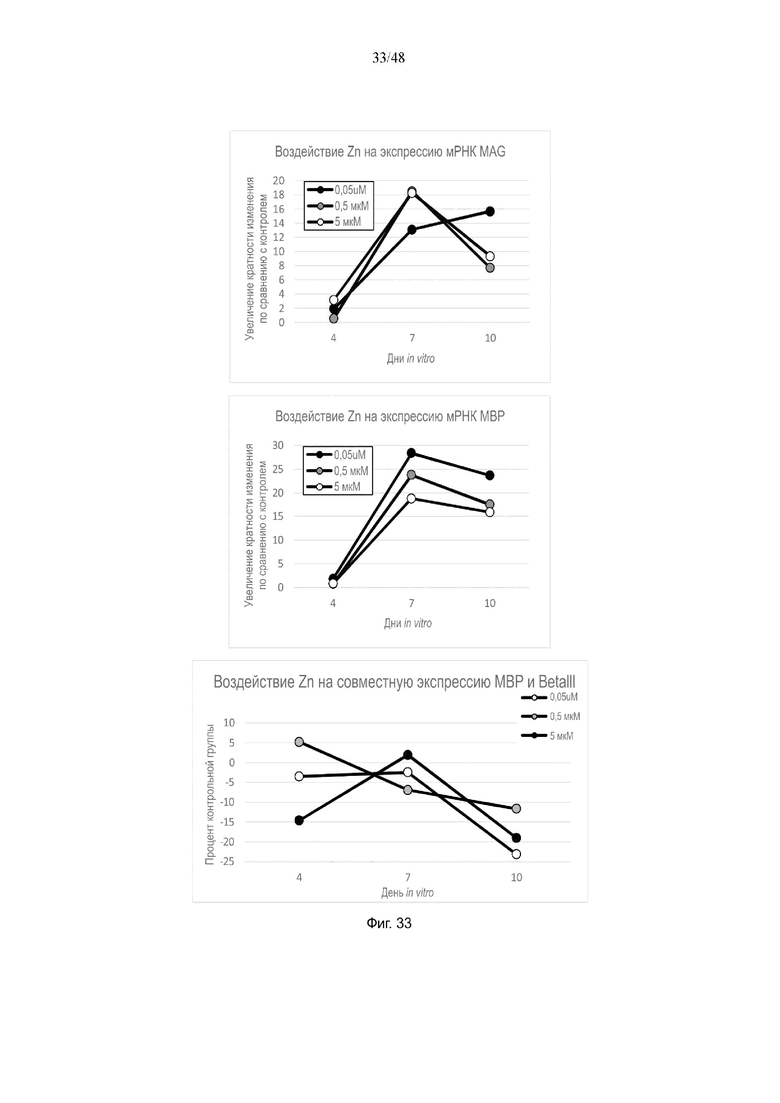



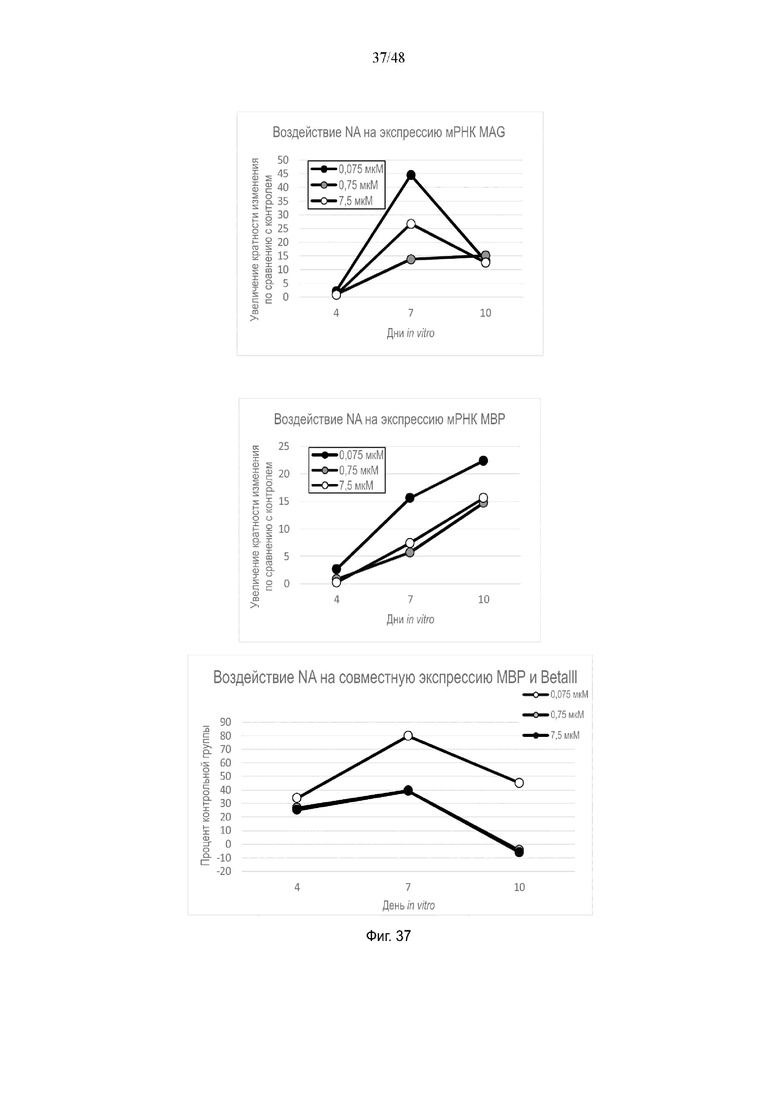
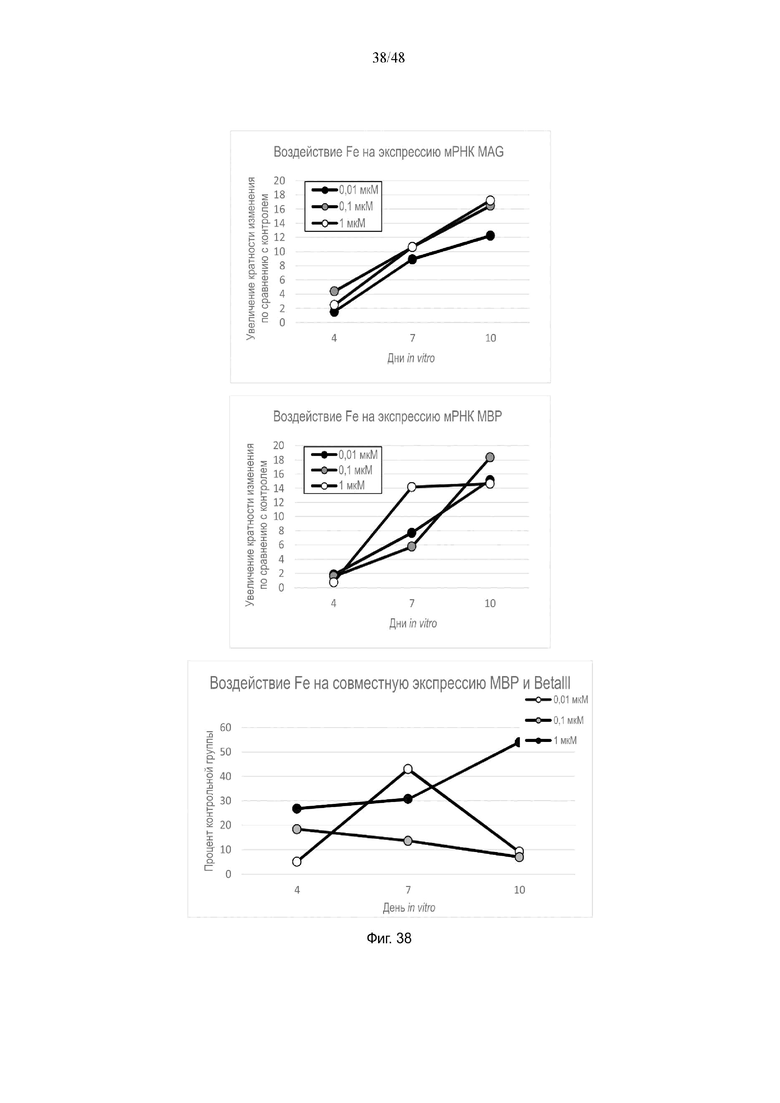
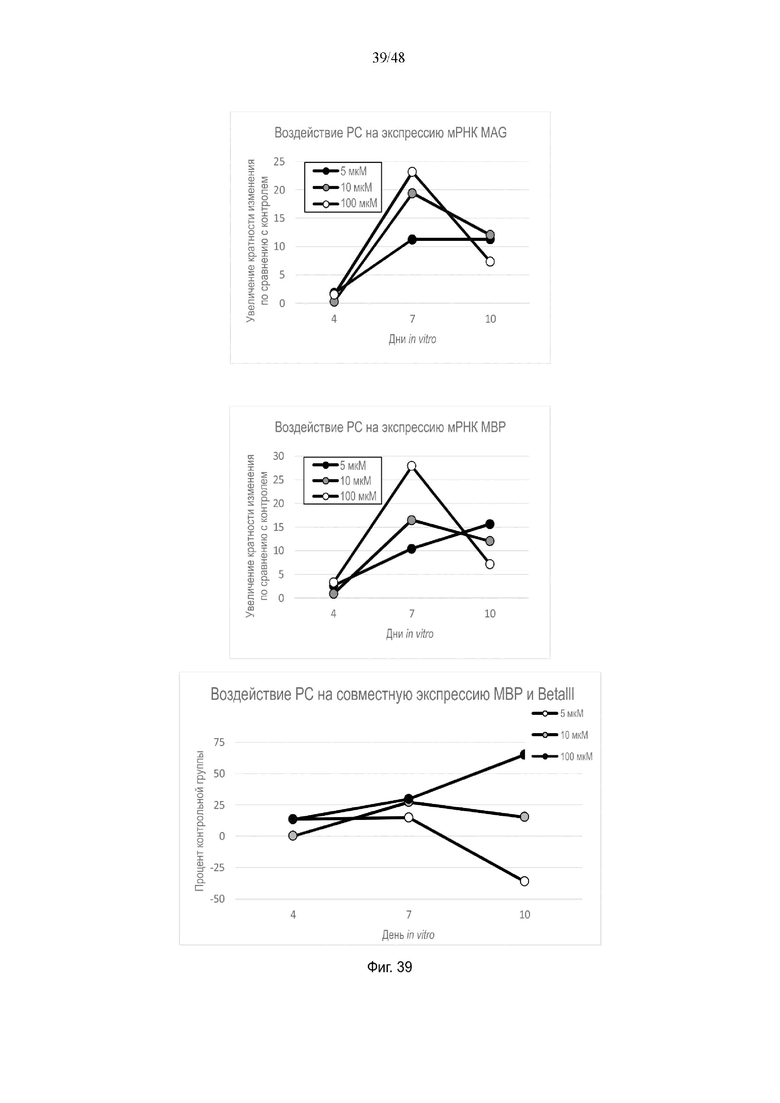
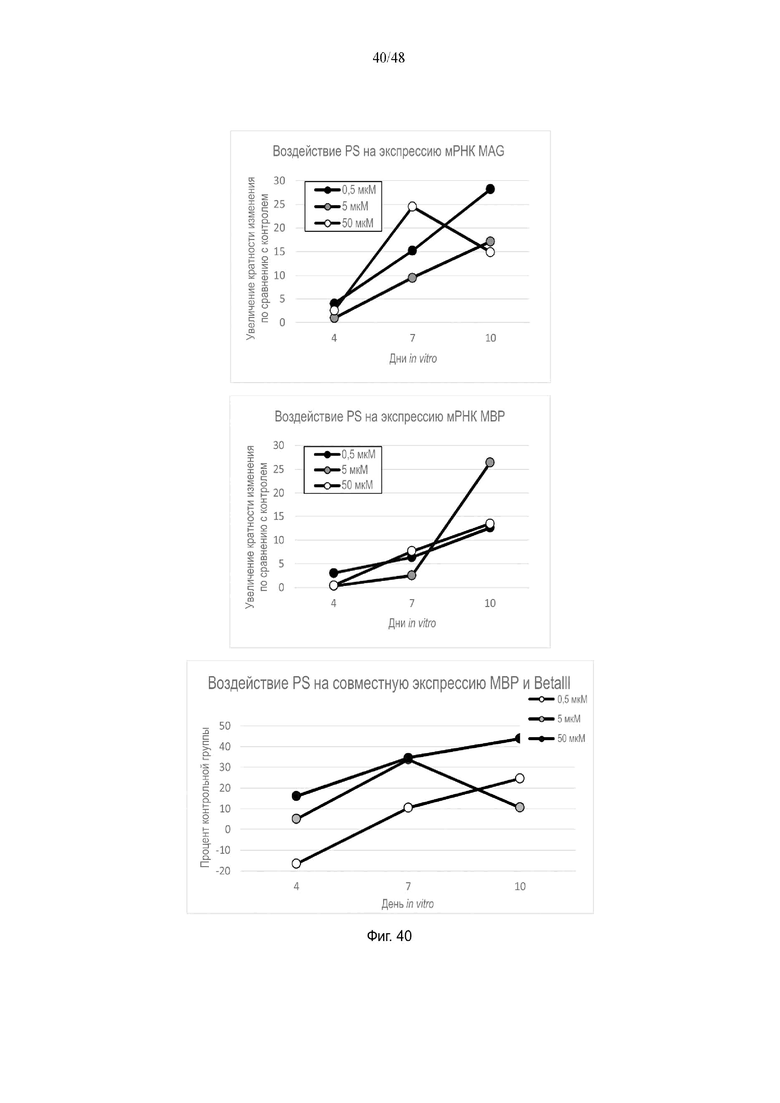
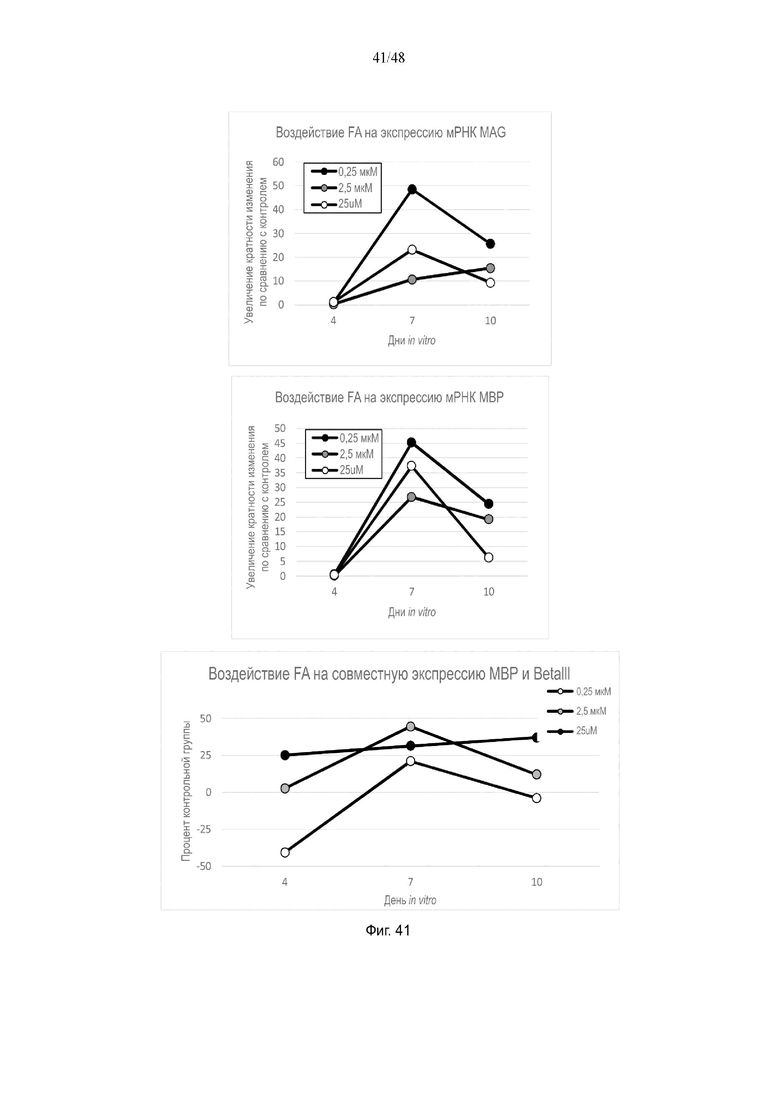
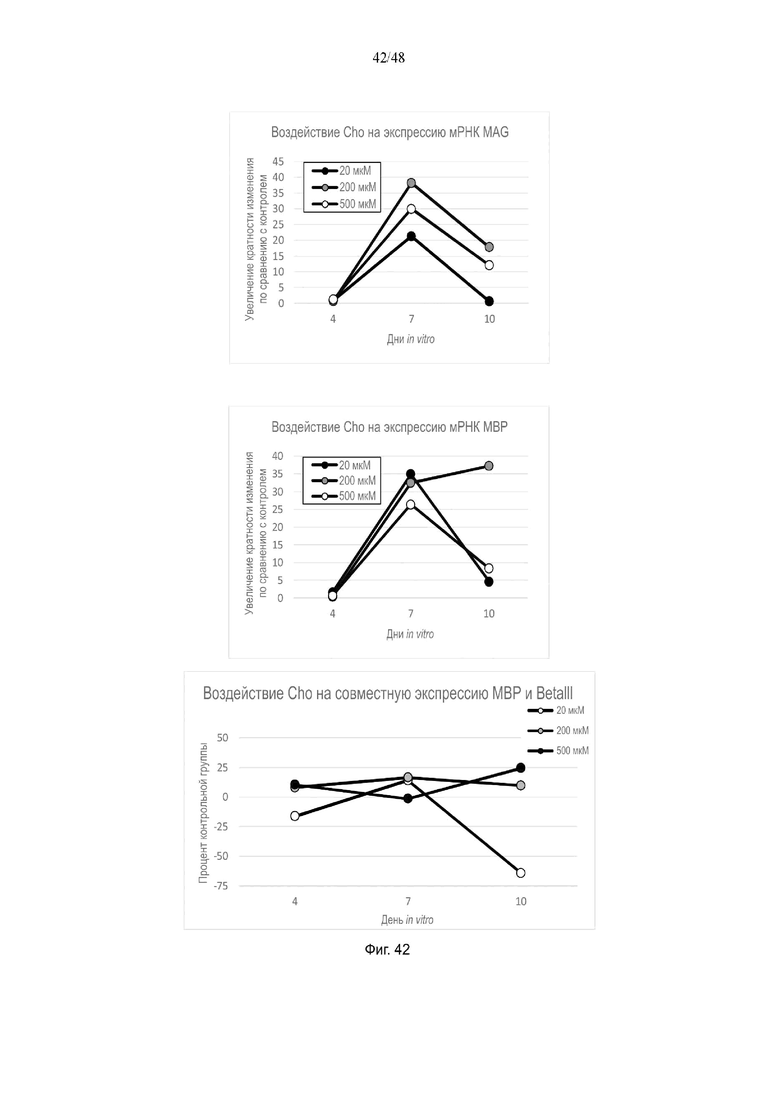
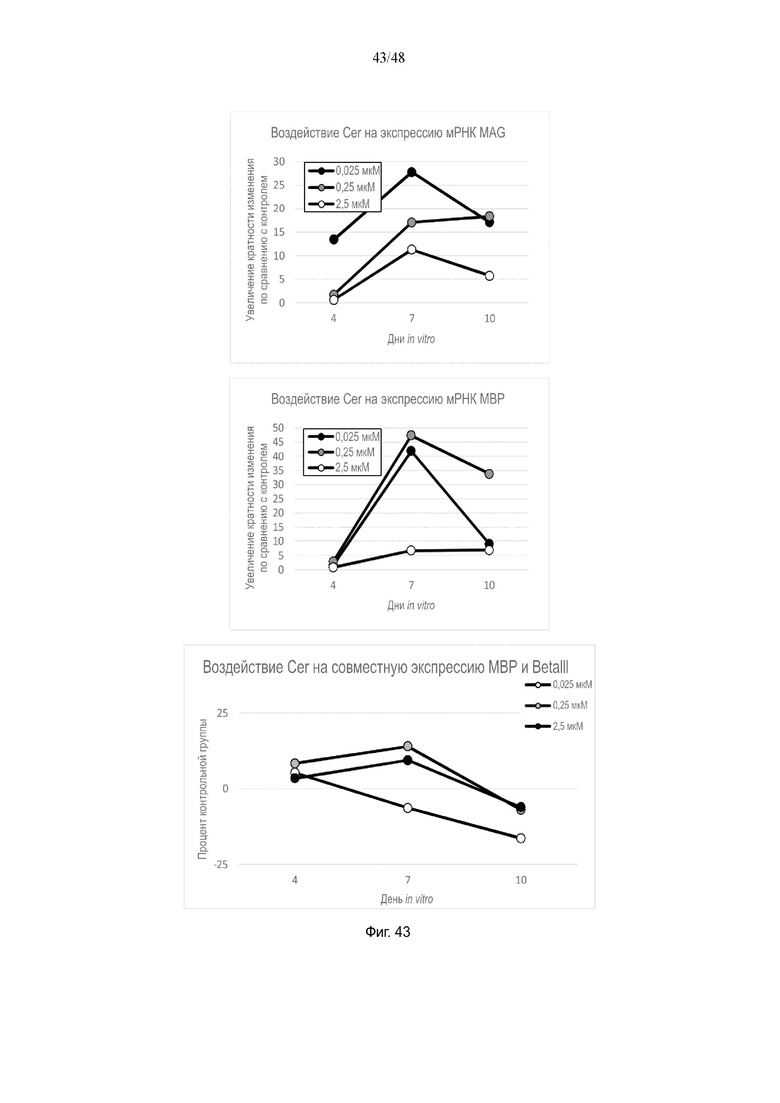
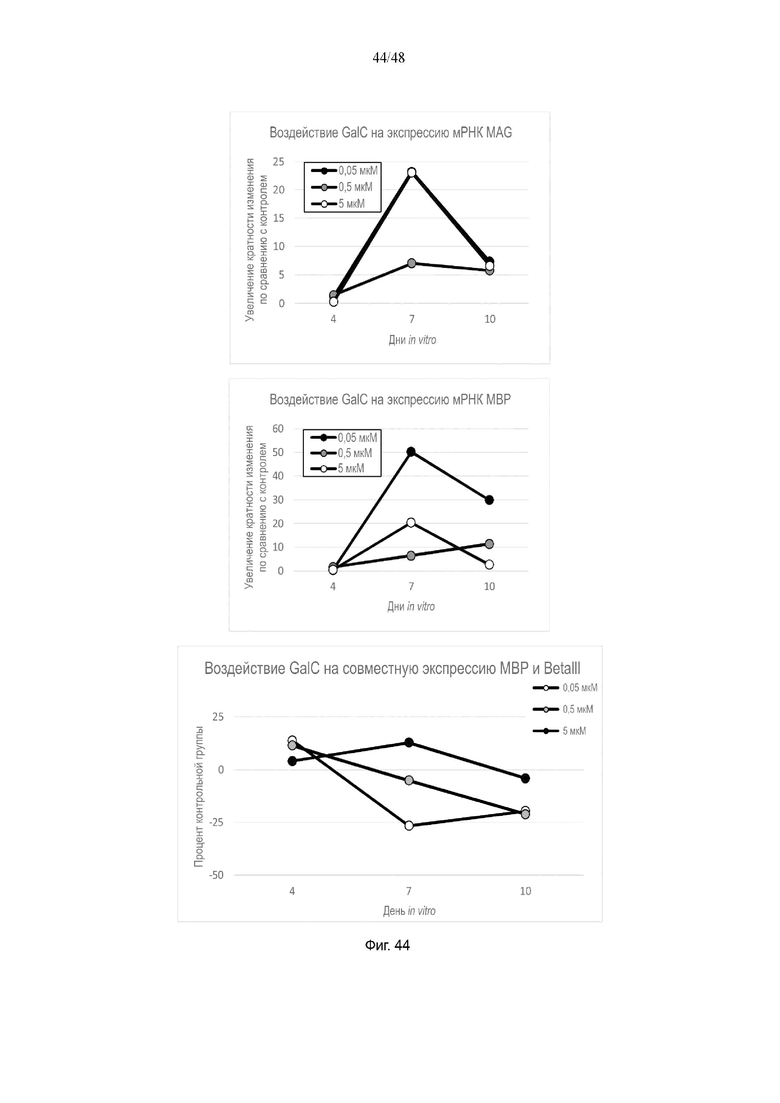
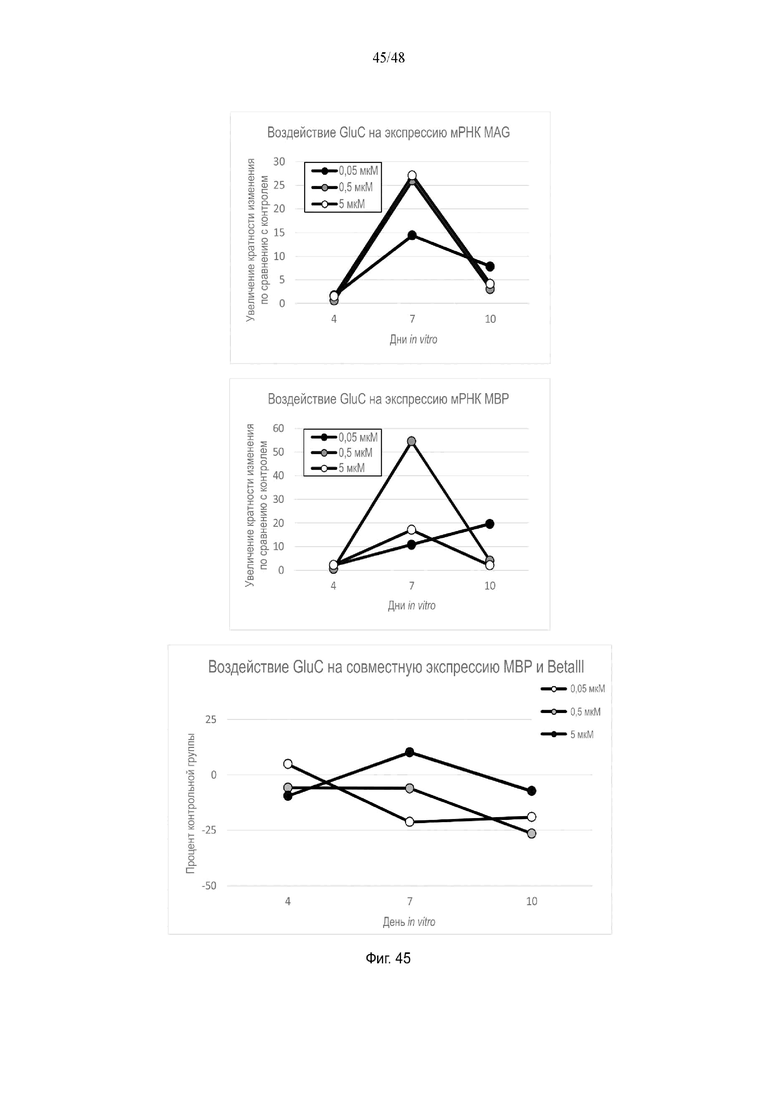
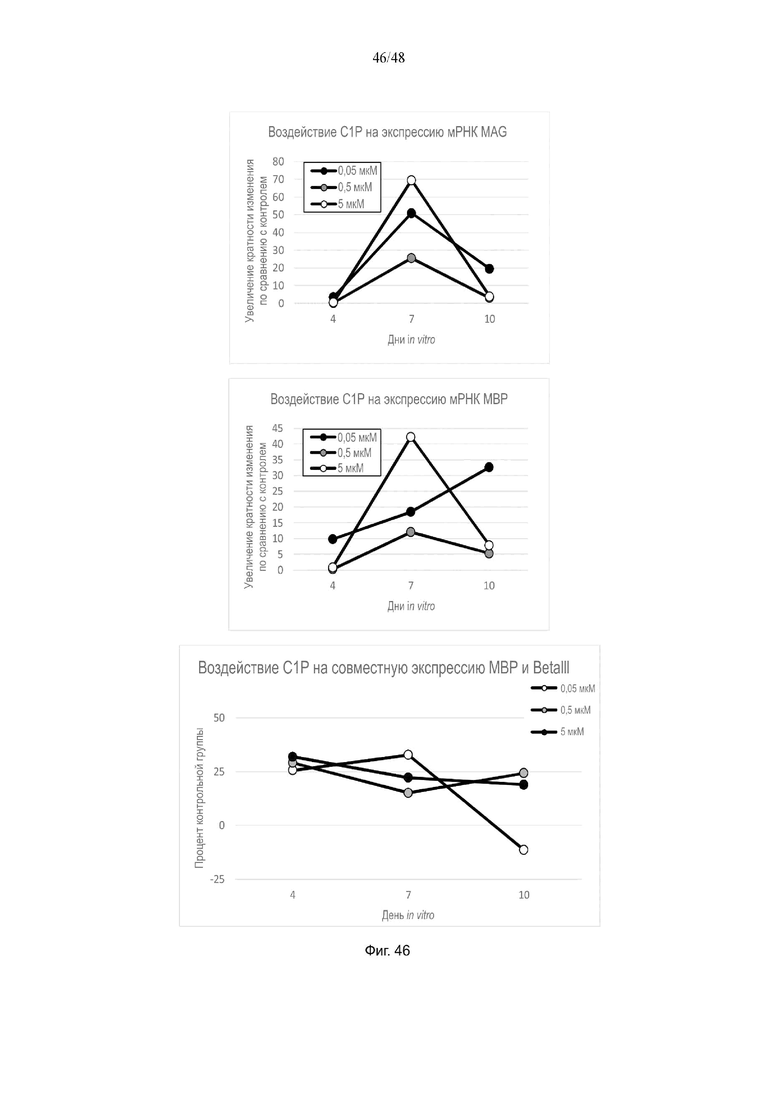

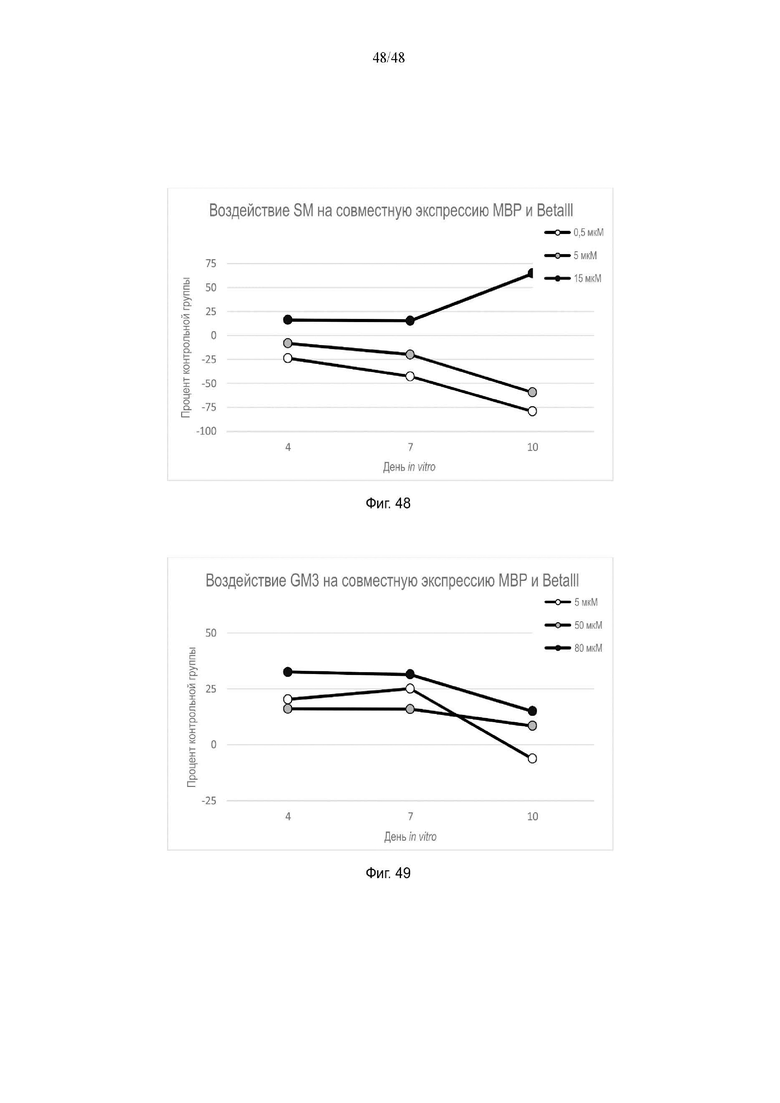
Изобретение относится к пищевой промышленности. Применение синтетической питательной композиции, содержащей холин в свободной форме или в виде его соли, для предупреждения, снижения риска или смягчения неоптимальной траектории миелинизации de novo у субъекта, вскармливаемого смесью, где субъектом является человеческий младенец или ребенок, такой как человеческий младенец или ребенок, вскармливаемый смесью, и где указанная композиция содержит холин в количестве от 50 до 1000 мг/100 г на сухую массу композиции, и где человеческий младенец - это младенец в возрасте до 12 месяцев, а ребенок - человек в возрасте от 1 до 18 лет, предпочтительно от 1 до 5 лет; и где траектория миелинизации de novo является неоптимальной, когда расстояние между любыми эквивалентными и/или одинаковыми точками измерения младенческой траектории и траекторией, достигнутой у младенцев, которые находятся исключительно на грудном вскармливании в течение их первых 3 месяцев жизни, превышает 50%. Синтетическая питательная композиция, содержащая холин в свободной форме или в виде его соли, для предупреждения, снижения риска или смягчения неоптимальной траектории миелинизации de novo у субъекта, вскармливаемого смесью, которая также содержит фолиевую кислоту, и витамин В12, и соединение жирной кислоты, отличное от фосфолипида, включающее докозагексаеновую кислоту и/или арахидоновую кислоту, и сфингомиелин, в которой холин присутствует в указанной композиции в количестве от 50 до 1000 мг/100 г, при этом сфингомиелин присутствует в указанной композиции в количестве от 300 мг/кг до 2,5 г/кг, при этом фолиевая кислота присутствует в указанной композиции в количестве от 110 до 500 мкг/100 г, а витамин В12 присутствует в указанной композиции в количестве от 5 до 10 мкг/100 г, а железо присутствует в указанной композиции в количестве от 5 до 40 мг/100 г, а соединение жирной кислоты, содержащее DHA, присутствует в композиции в количестве от 60 до 350 мг/100 г, а соединение жирной кислоты, содержащее арахидоновую кислоту (ARA), присутствует в композиции в количестве от 60 до 350 мг/100 г сухой массы композиции, в которой вся масса указана в расчете на сухую массу композиции. При этом указанное соединение жирной кислоты представляет собой моноацилглицерин, и/или диацилглицерин, и/или триацилглицерин и представляет собой композицию, выбранную из группы, состоящей из: детской смеси, молока для прикорма, композиции для младенцев, которая предназначена для добавления или разбавления грудным молоком человека, и пищевого продукта, предназначенного для потребления младенцем и/или ребенком либо отдельно, либо в сочетании с грудным молоком человека, где младенцем является младенец в возрасте до 12 месяцев, а ребенком является человек в возрасте от 1 до 18 лет и предпочтительно от 1 до 5 лет. Изобретение позволяет способствовать стимулированию, поддержке или оптимизации первичной миелинизации. 2 н. и 8 з.п. ф-лы, 49 ил., 18 табл., 7 пр.
1. Применение синтетической питательной композиции, содержащей холин в свободной форме или в виде его соли, для предупреждения, снижения риска или смягчения неоптимальной траектории миелинизации de novo у субъекта, вскармливаемого смесью, где субъектом является человеческий младенец или ребенок, такой как человеческий младенец или ребенок, вскармливаемый смесью, и где указанная композиция содержит холин в количестве от 50 до 1000 мг/100 г на сухую массу композиции, и где человеческий младенец - это младенец в возрасте до 12 месяцев, а ребенок - человек в возрасте от 1 до 18 лет, предпочтительно от 1 до 5 лет;
и где траектория миелинизации de novo является неоптимальной, когда расстояние между любыми эквивалентными и/или одинаковыми точками измерения младенческой траектории и траекторией, достигнутой у младенцев, которые находятся исключительно на грудном вскармливании в течение их первых (3) месяцев жизни, превышает 50%.
2. Применение по п. 1, где упомянутая композиция дополнительно содержит один или более из следующих ингредиентов: минеральное вещество, и/или витамин, и/или фосфолипид, и/или соединение жирной кислоты, причем упомянутое соединение жирной кислоты представляет собой содержащее жирную кислоту соединение, отличное от фосфолипида.
3. Применение по п. 2, где указанный витамин представляет собой фолиевую кислоту и/или витамин В12, где указанный минерал представляет собой железо и где указанное соединение жирной кислоты содержит докозагексаеновую кислоту (DHA) и/или арахидоновую кислоту и представляет собой моноацилглицерин, и/или диацилглицерин, и/или триацилглицерин.
4. Применение по п. 2 или 3, где упомянутый фосфолипид представляет собой соединение формулы (I) или смесь соединений формулы (I)
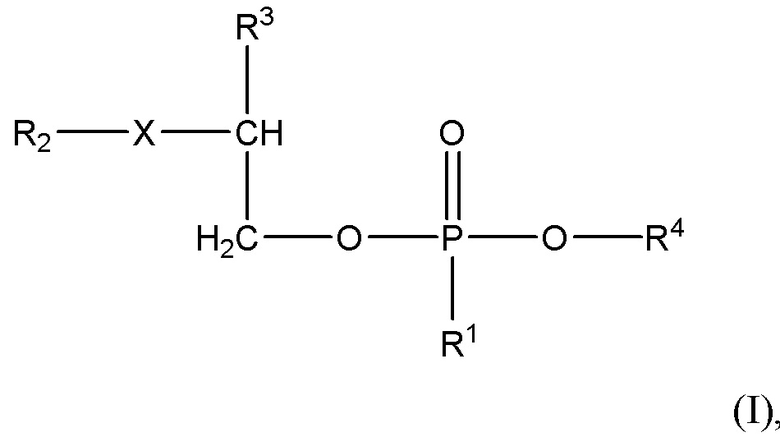
где R1 представляет собой O,
X представляет собой NH или O,
R2 представляет собой насыщенную или ненасыщенную линейную или разветвленную C2-C44 ацильную группу;
R3 представляет собой заместитель с формулой (II) или формулой (III)
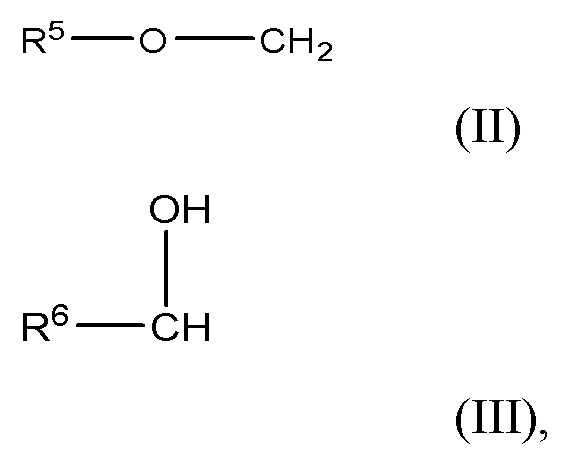
где R5 представляет собой насыщенную или ненасыщенную линейную или разветвленную C2-C44 ацильную группу, и
R6 представляет собой насыщенную C2-C44 алкильную или алкенильную группу; и
R4 выбирают из C5 или C6 замещенной или незамещенной циклической алкильной или алкенильной группы, или
-(CH2)n-R7, где n представляет собой целое число в диапазоне от 1 до 4, в частности от 1 до 2, а R7 представляет собой -N(CH3), NH3 или заместитель с формулой (IV)

в частности R4 представляет собой C6 циклическую алкильную или алкенильную группу, замещенную одной или более гидроксильными группами.
5. Применение по п. 2 или 4, где фосфолипид выбран из группы, состоящей из фосфатидилхолина, фосфатидилинозитола, фосфатидилсерина, фосфатидилэтаноламина и сфингомиелина и любой смеси из перечисленного выше.
6. Применение по любому из пп. 2, 3 или 5, где при наличии в композиции железа его содержание составляет более 5 мг/100 г сухой массы композиции, где при наличии в композиции фолиевой кислоты ее содержание составляет более 100 мкг/100 г сухой массы композиции, где при наличии в композиции витамина В12 его содержание составляет более 5 мкг/100 г сухой массы композиции, где при наличии в композиции сфингомиелина его содержание составляет более 300 мг/кг сухой массы композиции, где при наличии в композиции соединения жирной кислоты, содержащего DHA, его содержание в композиции составляет от 60 до 350 мг/100 г сухой массы композиции и где при наличии в композиции соединения жирной кислоты, содержащего арахидоновую кислоту, его содержание составляет от 60 до 350 мг/100 г сухой массы композиции.
7. Применение по любому из предшествующих пунктов, где упомянутая композиция представляет собой композицию, выбранную из группы, состоящей из детской смеси, молочной смеси для прикорма, композиции для младенцев, которая предназначена для добавления или разбавления грудным молоком человека, и продукта питания, предназначенного для потребления младенцем и/или ребенком в чистом виде или в комбинации с грудным молоком человека, где младенцу до 12 месяцев, а ребенку от 1 года до 18 лет, предпочтительно от 1 года до 5 лет.
8. Применение по любому предшествующему пункту, где человеческому младенцу до 12 месяцев.
9. Применение по любому предшествующему пункту, где траектория миелинизации de novo является неоптимальной, когда расстояние между любыми эквивалентными и/или одинаковыми точками измерения младенческой траектории и траекторией, достигнутой у младенцев, которые находятся исключительно на грудном вскармливании в течение их первых (3) месяцев жизни, превышает 20%.
10. Синтетическая питательная композиция, содержащая холин в свободной форме или в виде его соли, для предупреждения, снижения риска или смягчения неоптимальной траектории миелинизации de novo у субъекта, вскармливаемого смесью, которая также содержит фолиевую кислоту, и витамин В12, и соединение жирной кислоты, отличное от фосфолипида, включающее докозагексаеновую кислоту и/или арахидоновую кислоту, и сфингомиелин, в которой холин присутствует в указанной композиции в количестве от 50 до 1000 мг/100 г, при этом сфингомиелин присутствует в указанной композиции в количестве от 300 мг/кг до 2,5 г/кг, при этом фолиевая кислота присутствует в указанной композиции в количестве от 110 до 500 мкг/100 г, а витамин В12 присутствует в указанной композиции в количестве от 5 до 10 мкг/100 г, а железо присутствует в указанной композиции в количестве от 5 до 40 мг/100 г, а соединение жирной кислоты, содержащее DHA, присутствует в композиции в количестве от 60 до 350 мг/100 г, а соединение жирной кислоты, содержащее арахидоновую кислоту (ARA), присутствует в композиции в количестве от 60 до 350 мг/100 г сухой массы композиции,
в которой вся масса указана в расчете на сухую массу композиции,
при этом указанное соединение жирной кислоты представляет собой моноацилглицерин, и/или диацилглицерин, и/или триацилглицерин,
и при этом указанная композиция представляет собой композицию, выбранную из группы, состоящей из детской смеси, молока для прикорма, композиции для младенцев, которая предназначена для добавления или разбавления грудным молоком человека, и пищевого продукта, предназначенного для потребления младенцем и/или ребенком либо отдельно, либо в сочетании с грудным молоком человека, где младенцем является младенец в возрасте до 12 месяцев, а ребенком является человек в возрасте от 1 до 18 лет и предпочтительно от 1 до 5 лет.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| PRADO E.L., DEWEY K.G., Nutrition and brain development in early life // Nutrition Reviews, Vol.72(4), p.267-284 | |||
| NYARADI A | |||
| et al., The role of nutrition in children’s neurocognitive development, from pregnancy through childhood // Frontiers in Human Neuroscience, March 2013, Volume7, Article 97, p.1-16 | |||
Авторы
Даты
2023-05-03—Публикация
2016-12-13—Подача