Изобретение относится к медицине, а именно к терапии и пульмонологии, и может быть использовано для персонифицированной программы ведения пациентов с бронхиальной астмы (БА) с сопутствующей мультиморбидной патологией с учетом индивидуального риска обострений заболевания в течение ближайшего года наблюдения.
В последние годы неуклонно растет количество пациентов, имеющих коморбидные, полиморбидные или мультиморбидные заболевания (Кардиоваскулярная терапия и профилактика. 2019;18(1):5-66. http://dx.doi.org/10.15829/1728-8800-2019-1-5-66). Согласно последним публикациям, наиболее частыми мультиморбидными состояниями при БА являются заболевания верхних дыхательных путей, хронический синусит, гастроэзофагеальная рефлюксная болезнь (ГЭРБ), ожирение и депрессия. Эксперты GINA (Global Initiative for Asthma Глобальная инициатива по бронхиальной астме 2022) считают, что основными коморбидными заболеваниями БА, на которые следует обращать внимание это риносинусит, ожирение и ГЭРБ. Но, в тоже время, GINA указывает на то, что у пациентов с БА, особенно у пациентов с трудноконтролируемой или тяжелой БА, обычно присутствует несколько сопутствующих заболеваний и рекомендуется активное лечение сопутствующих заболеваний, поскольку они могут усугублять бремя симптомов, ухудшать качество жизни и приводить к взаимодействию лекарств, а некоторые сопутствующие заболевания также ухудшают контроль БА. Многие исследователи уделяют большое внимание коморбидным заболеваниям у пациентов с БА, анализируют их влияние на прогноз и процесс лечения БА (Урясьев О.М., Панфилов Ю.А. Влияние ожирения на клинико-функциональные показатели и эффективность противоастматической терапии у больных бронхиальной БА. Наука молодых (Eruditio Juvenium). 2013;4:79-88). Для выявления наиболее часто встречающихся при БА сопутствующих заболеваний Su X. et al. провели обширный мета-анализ имеющихся литературных данных, который показал, что у пациентов с БА по сравнению с лицами, не имеющими данного диагноза, были более распространены следующие заболевания: сердечно-сосудистая патология, в том числе артериальная гипертензия и заболевания сосудов головного мозга; ожирение, сахарный диабет и другие метаболические и эндокринные заболевания; а также психические и неврологические расстройства, заболевания кишечника и мочевыводящих путей, рак и другие бронхо-легочные заболевания (Su X., Ren Y., Li Μ., et al. Prevalence of Comorbidities in Asthma and Nonasthma Patients: A Meta-analysis // Medicine. 2016. Vol.95, №22. P. e3459. doi:10.1097/MD.0000000000003459). Немаловажен также тот факт, что коморбидные заболевания встречаются у пациентов с БА значительно чаще по сравнению с популяцией в целом (Karlstad 0., Nafstad P., Tverdal Α., et al. Comorbidities in an asthma population 8-29 years old: a study from the Norwegian Prescription Database // Pharmacoepidemiology and Drug Safety. 2012. Vol. 21, №10. P. 1045-1052. doi:10.1002/pds.2233). Популяционное исследование, проведенное в Шотландии, показало, что 62,6% пациентов с БА имели хотя бы 1 сопутствующее заболевание, а 16,3% 4 или более (Weatherburn С.J., Guthrie В., Mercer S.W., et al. Comorbidities in adults with asthma: Population based cross-sectional analysis of 1.4 million adults in Scotland // Clinical and Experimental Allergy. 2017. Vol. 47, №10. P. 1246-1252. doi:10.1111/cea. 12971). Американские авторы Ir. Mindlis et al. показали, что пожилые пациенты с БА, имеют 2 или более сопутствующих заболевания, среднее число которых составляет 5,3 (SD=2,3; диапазон 0-12) (Mindlis I, Wisnivesky JP, Wolf MS, et al. Comorbidities and depressive symptoms among older adults with asthma. J Asthma. 2022;59(5):910-916. doi: 10.1080/02770903.2021.1887890). В последних мета-анализах появились данные о распространенности остеоартроза у пациентов с БА, которая составляет 49,5% (95% ДИ, 36,4%-6,6%) (Althoff MD, Ghincea A, Wood LG, et al. Asthma and Three Colinear Comorbidities: Obesity, OS A, and GERD. J Allergy Clin Immunol Pract. 2021;9(11):3877-3884. doi: 10.1016/j.jaip.2021.09.003.). Корейские исследователи показали, что артрит, ринит, депрессия и ожирение были независимо связаны с БА у корейских пациентов старше 40 лет (Park J, Kim ТВ, Joo Η, Lee JS, Lee SD, Oh YM. Diseases Concomitant With Asthma in Middle-Aged and Elderly Subjects in Korea: A Population-Based Study. Allergy Asthma Immunol Res. 2013 Jan;5(l): 16-25. https://doi.org/10.4168/aair.2013.5.l.16).
При оценке влияния коморбидных заболеваний на контроль БА, показано, что у 92% пациентов с трудно контролируемой БА имелось хотя бы 1 коморбидное заболевание. Количество сопутствующих заболеваний обратно пропорционально уровню контроля БА, чем больше заболеваний, тем хуже контроль (Hekking РР, Amelink Μ, Wener RR, et al. Comorbidities in Difficult-to-Control Asthma. J Allergy Clin Immunol Pract. 2018;6(1): 108-113. doi: 10.1016/j.jaip.2017.06.008). D.A. Beuther et al. так же показали, что у пациентов с трудно или неконтролируемой БА отмечается высокий уровень распространенности коморбидных заболеваний и сопутствующего ожирения (Beuther D. Α., Sutherland Ε. R. Overweight, obesity, and incident asthma: a meta-analysis of prospective epidemiologic studies. Am. J. Respir. Crit. Care Med. 2007; 175:661-666). При сочетании БА с коморбидными заболеваниями и ожирением ухудшается достижение контроля над заболеванием, снижается ответ на стандартную терапию (Ермолова А.В., Будневский А.В., Малыш Е.Ю., и др. Клинико-функциональные особенности бронхиальной астмы у больных с метаболическим синдромом. Клин. мед. 2015; 93 (6):44-49). Таким образом, сопутствующая патология должна рассматриваться с большим вниманием в стратегиях борьбы с БА и должна быть важным компонентом ковариационного анализа в исследованиях с субъективными результатами для здоровья (Wijnhoven НА, Kriegsman DM, Hesselink АЕ, de Haan Μ, Schellevis FG. The influence of co-morbidity on health-related quality of life in asthma and COPD patients. Respir Med. 2003 May;97(5):468-75. doi: 10.1053/rmed.2002.1463. PMID: 12735662.).
Существующие методики прогнозирования обострения БА можно разделить на две группы.
1. Методики определения как такового прогноза обострения БА
Так, например, известен «Способ прогнозирования обострения бронхиальной астмы» (патент РФ №2563998 от 27.09.2015 г.), заключающийся в заборе и исследование периферической крови на стадии ремиссии БА. Полученную кровь делят на 2 пробы, при этом проводят ультрафиолетовое облучение одной из проб в течение 60 секунд, получают из них образцы сыворотки крови, которые исследуют методом краевой дегидратации в поляризованном свете, и при обнаружении агрегаций кристалла-сферолита и внедренного в него шаровидного скопления мелких слабо анизотропных гранул в пробе, облучению не подвергавшейся, и кристаллов-сферолитов, окруженных рыхло расположенными скоплениями слабо анизотропных гранул, в пробе, подвергшейся облучению, прогнозируют обострение бронхиальной астмы. Способ позволяет прогнозировать обострение БА на доклинической стадии, когда проведение профилактических мероприятий будет своевременным и не даст возможности перейти заболеванию в стадию обострения.
Недостатками способа является определение стадии ремиссии или обострения на текущий момент времени и невозможность спрогнозировать количество обострений БА в течение ближайшего года, метод сложно применять в рутинной клинической практике при оказании первичной медико-санитарной помощи, не учитывается коморбидная патология.
Так же известен «Способ прогноза количества обострений у больных бронхиальной БА» (патент РФ №2458347 от 10.08.2012 г.), который заключается в том, что на градиенте плотности фиколл-верографин путем центрифугирования выделяют лимфоциты из цельной крови пациента, взятой из кубитальной вены в утренние часы натощак, в моменты обострения БА и после его купирования. Взвесь лимфоцитов наносят на предметное стекло по типу «толстой капли», высушивают при комнатной температуре, в полученных образцах иммуноцитохимическим методом с использованием мышиных античеловеческих антител CD38, антимышиных FITC-меченных антител и люминесцентной микроскопии подсчитывают на 300 клеток в поле зрения CD38+ лимфоциты. При снижении их количества во втором образце относительно первого на 4 и более клетки прогнозируют отсутствие обострений БА в течение года, при повышении на 4 и более клетки - как минимум 2 обострения, отсутствие динамики изменения количества CD38+ лимфоцитов либо колебания в пределах 3 клеток предусматривает 1 обострение. Способ позволяет прогнозировать количество обострений БА в течение года после госпитализации.
Недостатком способа является сложность применения в рутинной клинической практике иммуноцитохимического исследования крови, не учитывается коморбидная патология.
2. Методики определения прогноза обострения БА с учетом коморбидного состояния пациента
Ранее нами был разработан «Способ прогнозирования обострений бронхиальной астмы в течение ближайшего года у пациентов с сопутствующим ожирением» (патент РФ №2655829 от 29.05.2018 г.), заключающийся в определение диагностических показателей: индекс массы тела (BMI), уровень лептина в венозной крови, уровень адипонектина в венозной крови, комплаенс пациентов с помощью «Шкалы комплаенса больных хроническими неспецифическими заболеваниями легких», уровень ситуативной тревожности по шкале тревоги Спилбергера, уровень депрессии по шкале самооценки депрессии Цунга. Способ позволяет вычислить по разработанной формуле индекс вероятности обострения БА в течение 1 года наблюдения. Недостатками способа является учет только ожирения, не берется во внимание другая коморбидная патология, которая может выступать в качестве триггерных факторов и повышать риск обострений БА в течение ближайшего года.
По данным Всемирной организации здравоохранения (ВОЗ), БА одно из основных распространенных хронических неинфекционных заболеваний (ХНИЗ), которым страдают не только взрослые, но и дети (https://www.who.int/news-room/fact-sheets/detail/noncommunicable-diseases).
Недостаточная физическая активность (ФА) сопряжена с риском развития ХНИЗ, в том числе избыточной массой тела, ожирения (Бобрик Ю.В., Мороз Г.Α., Пономарев В.А. Роль физической культуры в первичной профилактике хронических неинфекционных заболеваний и повышении качества жизни населения. Научный вестник Крыма. 2018;6(17): 19-23).
Для БА характерны вариабельность респираторных симптомов, проявляющаяся в различной интенсивности, продолжительности, периодичности, а также обратимость бронхиальной обструкции (2022 GINA Report, Global Strategy for Asthma Management and Prevention. https: //ginasthma. org/gina-reports/).
При таком вариабельном течении БА пациенты зачастую ограничивают свою активность, ведут малоподвижный образ жизни, не увеличивают интенсивность и продолжительность ФА, считая, что ФА провоцирует симптомы БА (Добрынина Е.А. Бронхиальная астма и физические нагрузки. Вестник науки и образования. 2017; 1(12(36)), 102-105). Действительно, ФА высокой интенсивности может быть одним из триггеров острого бронхоспазма (Царев С.В. Бронхоспазм, вызываемый физической нагрузкой. Астма и аллергия.2018;(4):3-6), но, по данным литературы, дозированные тренировки при оптимальных условиях (влажность воздуха, температура), напротив, способствуют снижению частоты и тяжести приступов (Трибунцева Л.В., Будневский А.В., Шкатова Я.С, Иванчук Ю.С., Токмачев Р.Е. Значение физической активности для клинического течения бронхиальной астмы: обзор литературы. Российский медико-биологический вестник имени академика И.П. Павлова. 2021;29(1): 161-170). У пациентов с БА бронхоспазм при физической нагрузке (ФН) часто связан с плохим контролем заболевания. Возникновение бронхоконстрикции, связанной с ФН, ограничивает в дальнейшем занятия физическими упражнениями, что в свою очередь негативно влияет на качество жизни (КЖ) пациентов. (Mancuso СА, Sayles W, Robbins L, Phillips EG, Ravenell K, Duffy C, et al. Barriers and facilitators to healthy physical activity in asthma patients. The Journal of asthma: official journal of the Association for the Care of Asthma. 2006;43(2): 137-43.). Кроме того, ограничение ΦΑ может приводить к избыточной массе тела, ожирению.
Влияние на БА мультиморбидных заболеваний таких как: сердечно-сосудистые, депрессия, сахарный диабет, дислипидемия, остеопороз, риносинусит, хроническая обструктивная болезнь легких, ожирение, артрит, рак, ГЭРБ, активно изучается (Park J, Kim ТВ, Joo Η, Lee JS, Lee SD, Oh YM. Diseases concomitant with asthma in middle-aged and elderly subjects in Korea: a population-based study. Allergy Asthma Immunol Res 2013;5:16-25). Избыточное отложение жировой ткани, даже в отсутствие БА приводит к физиологическим изменениям функции легких, например, снижение легочных объемов, увеличение ригидности грудной клетки, формированию диспноэ (Beuther DA, Sutherland ER. Obesity and pulmonary function testing. J Allergy Clin Immunol. 2005;115:1100-1101). Из-за отложения жира в грудной клетке развивается ее ригидность и, как следствие, затруднение вдоха. Отложение жира в брюшной полости приводит к ограничению подвижности диафрагмы из-за перерастяжения мышечных волокон (Перцева Т.А., Нудьга Н.П. Астма и ожирение: какова взаимосвязь. Украинский пульмонологический журнал. 2011;1:61-64).
Системное воспаление является общим патогенетическим механизмом, как для большинства фенотипов БА, так и для ожирения, сахарного диабета, депрессии и объясняет возможную связь между этими заболеваниями (Kapadia S.G., Wei С, Bartlett S.J., et al. Obesity and symptoms of depression contribute inde-pendently to the poor asthma control of obesity // Respiratory Medicine. 2014. Vol. 108, №8. P. 1100-1107. doi:10.1016/j.rmed.2014.05.012). Известно, ожирение увеличивает риск развития БА, атакже утяжеляет ее течение, снижая уровень контроля симптомов, повышая риск обострений (Соловьева И.Α., Собко Е.А., Демко И.В., Крапошина А.Ю., Гордеева Н.В., Локтионова М.М. Бронхиальная астма и ожирение. Терапевтический архив. 2017; 89 (3), 116-120). Ожирение напрямую связано с хроническим системным воспалением. Выполняя функции эндокринного органа, жировая ткань продуцирует различные биологически активные вещества, такие как лептин, адипонектин, а также провоспалительные медиаторы -интерлейкин-6 (IL-6), фактор некроза опухоли-альфа (ФНО-α). БА рассматривается как хроническое воспалительное заболевание дыхательных путей, которое приводит к гиперреактивности бронхов. Следовательно, ожирение, усиливая воспаление дыхательных путей, может влиять на БА. Доказано, высокий уровень IL-6, связанный с ожирением, способствует усилению, поддержанию воспаления в легких, и, как результат, усилению и поддержанию симптомов БА (Кытикова О.Ю., Гвозденко Т.Α., Антонюк М.В. Роль системного воспаления при бронхиальной астме и ожирении. Клиническая медицина. 2018;96(9):784-790).
Кроме того, при ожирении, в результате токсического воздействия промежуточных продуктов метаболизма жирных кислот, структурные элементы жировой ткани находятся в состоянии постоянного оксидантного стресса, что в свою очередь активирует внутриклеточные сигнальные системы в адипоцитах. Это приводит к повышению экспрессии промежуточных продуктов метаболизма жирных кислот, усилению воспалительных процессов во всей жировой ткани организма. Генерализация воспаления сопровождается повышенным синтезом провоспалительных цитокинов, в том числе IL-6, ФНО-α.
Общие молекулярно-клеточные патогенетические механизмы БА и ожирения определяют более выраженные клинические симптомы, частые обострения, и, как результат, низкий уровень контроля, резистентность к базисной терапии в сочетании с более частым использованием β-агонистов для купирования симптомов, тяжесть течения БА, частые госпитализации при обострении заболевания (Маркова Т.Н., Фомина Д.С., Костенко Α. Α., Бобрикова Е.Н. Ожирение и бронхиальная астма: два заболевания с общими аспектами патогенеза. Профилактическая медицина. 2020;23(4): 126-132).
Исследователи указывают определенные взаимосвязи между активностью иммунной системы и психологическим состоянием. Например, цитокины, такие как IL-1, -2 и -6, и ФНО-α, участвуют в регуляции аффективного поведения. Исследование на животных показало, что острая иммунная проблема имеет эффект, аналогичный эффекту серьезного депрессивного расстройства. Кроме того, хронический стресс может привести к нарушению регуляции оси гипоталамус-гипофиз-надпочечники, избыточной выработке уровня кортизола, устойчивости к глюкокортикостероидам и развитию системного воспаления. Системное воспаление характеризуется повышенным уровнем воспалительных маркеров, таких как С-реактивный белок (СРБ), IL-6, IL-1β, ФНО-α и лептина. Повышенный уровень IL-6, СРБ и CD 163 (маркера активации макрофагов) был связан со снижением функции легких (особенно при тяжелой БА) и нейтрофильным воспалением дыхательных путей (Zhang L., Zhang X., Zheng J., et al. Depressive symptom-associated IL-1β and TNF-α release correlates with impaired broncho dilator response and neutrophilic airway inflammation in asthma // Clinical and Experimental Allergy. 2019. Vol. 49, №6. P. 770-780. doi: 10.1111/cea. 13346). Старение также связано с хроническим провоспалительным состоянием, с повышенными концентрациями IL-1, IL-6 и ФНО-α. Известно, что различные медиаторы воспаления, включая IL-1, IL-6, IL-8, ФНО-α и другие цитокины, повышены у пациентов с остеоартрозом. Кроме того, известно, что пациенты с ожирением употребляют большее количество калорий, что приводит к перегрузке митохондрий, к перепроизводству активных форм кислорода, повреждению митохондриальных (и клеточных) компонентов и митохондриальной потере. Дисфункция митохондрий приводит к неполному окислению жирных кислот и увеличению циркулирующих липидов. Некоторые метаболически активные липиды подавляют передачу сигналов инсулина и могут способствовать развитию инсулинорезистентности. Ситуация усугубляется малоподвижностью, поскольку физическая активность это способ повышения митохондриальной активности (Aguilera-Aguirre L., Bacsi Α., Saavedra-Molina Α., et al. Mitochondrial dysfunction increases allergic airway inflammation // Journal of Immunology. 2009. Vol. 183, №8. P. 5379-5387. doi: 10.4049/jimmunol.0900228). Астма связана с оксидативным стрессом, который может быть частично вызван дисфункцией митохондрий, но также ускоряет митохондриальную дисфункцию (Sahiner U.M., Birben Ε., Erzurum S., et al. Oxidative stress in asthma: Part of the puzzle // Pediatric Allergy and Immunology. 2018. Vol.29, №8. P. 789-800. doi: 10.1111/pai. 12965).
Таким образом, пациенты с БА и сопутствующей мультиморбидной патологией требуют персонифицированной программы ведения, для своевременного предупреждения обострения.
Задачей, на решение которой направленно данное изобретение является возможность прогноза обострений БА в ближайший год у больных с сопутствующей мультиморбидной патологией.
Достигаемым техническим результатом является получение достоверного прогноза развития обострений БА у больных с сопутствующей мультиморбидной патологией.
Технический результат достигается за счет следующих приемов.
У пациента с бронхиальной астмой с сопутствующей мультиморбидной патологией определяют такие показатели, как уровень двигательной активности по опроснику ODA23+, объем форсированного выдоха за 1-ю секунду маневра форсированная жизненная емкость легких выдоха (-FEV1-), уровень перекисей сыворотки крови, уровень активности пациентов по шкале Лекена, уровень лептина венозной крови, индекс массы тела (BMI), уровень интерлейкина-6 (IL-6), кумулятивный индекс заболеваний CIRS.
Затем на основании полученных данных вычисляют индекс вероятности частоты обострения БА в течение ближайшего года у пациентов с сопутствующей мультиморбидной патологией (ЕхасВА) по формуле:
 где ODA23+ - результат по опроснику двигательной активности ODA23+, в баллах,
где ODA23+ - результат по опроснику двигательной активности ODA23+, в баллах,
FEV1 - объем форсированного выдоха за 1-ю секунду, в процентах,
PerOx - уровень перекисей сыворотки крови, мкмоль/л,
Leken результат оценки динамики активности пациентов по шкале Лекена, в баллах,
Leptin - уровень лептина венозной крови, нг/мл,
BMI - индекс массы тела, кг/м2,
IL6 - уровень IL-6, пг/мл,
CIRS - кумулятивный индекс заболеваний, в баллах.
При значении ЕхасВА менее 2 прогнозируют низкий риск развития обострений БА, с количеством обострений 1 раз в год. При значении ЕхасВА 2 и более прогнозируют высокий риск обострений, с количеством обострений в год 2 и более раз.
Нами была разработана прогностическая модель частоты обострений БА у больных с сопутствующей мультиморбидной патологией.
Для расчета параметров модели были проанализированы данные 237 больных БА в возрасте от 18 до 78 лет: мужчин - 51 (21,5%), женщин - 186 (78,5%), средний возраст 52,6±1,3 лет.Пациенты находились под наблюдением в течение 12 месяцев, комплексное обследование проводили на этапе включения в исследование и через 12 месяцев.
Диагноз БА установлен в соответствии с критериями GINA 2022.
Все пациенты прошли комплексное обследование, включавшее сбор жалоб и анамнеза, оценку объективного статуса, определение лабораторных показателей венозной крови.
BMI рассчитывали по формуле BMI=Macca/рост2 (кг/м2): BMI 18,5-25 кг/м2 - норма, BMI 25-30 кг/м2 - избыточная масса тела BMI > 30 кг/м2 - ожирение.
На основании данных анамнеза, данных амбулаторных карт, данных дополнительных методов исследования, проводимых пациентам, были проанализированы и оценены имеющиеся сопутствующие заболевания. Оценку мультиморбидной патологии проводили с использованием кумулятивной рейтинговой шкалы патологии CIRS (Cumulative Illness Rating Scale) (Miller MD, Paradis CF, Houck PR, et al. Rating chronic medical illness burden in geropsychiatric practice and research: application of the Cumulative Illness Rating Scale // Psychiatry Res. 1992;41(3):237-48) Среднее количество сопутствующих заболеваний составило 4,8±0,61. Средний балл индекса CIRS составил 7,44±0,95 балла, максимальный балл 19, минимальный 2. Значение индекса CIRS было значимо выше среди пациентов с ожирением составило 10,1±1,9 балла, в то время как у пациентов без ожирения было 4,68±0,31 балла. Были отмечены достоверные различия значений индекса CIRS в зависимости от наличия или отсутствия ожирения (р<0,0001).
Уровень двигательной активности оценивали с помощью опросника двигательной активности ODA23+, разработанного в ФГБУ «ГНИЦПМ» Минздрава России (Аронов Д.М., Красницкий В.Б., Бубнова М.Г., 2013 г.). Двигательная активность оценивалась как «Очень высокая» при ≥109 баллов, «Высокая» при 85-108 баллах, «Умеренная» при 62-84 баллах, «Низкая» при 39-61 баллах, «Очень низкая» при ≤38 баллов.
Оценку динамики активности пациентов в повседневной жизни проводили с помощью шкалы Лекена (Leken's functional index). При результате 0 баллов - ограничения жизнедеятельности не было, степень ограничения жизнедеятельности как «Легкая» оценивалась при 1-4 баллах, «Умеренная» при 5-7 баллах, «Выраженная» при 8-10 баллах, «Резко выраженная» при 11-13 баллах, «Крайне выраженная» при ≥14 баллов (Lequesne Μ. Indices of severity and disease activity for osteoarthritis. Semin Arthritis Rheum. 1991;20(6(2)):48-54).
Исследование показателей функции внешнего дыхания (ФВД) проводили на спирографе «Диамант-С» (Россия) с регистрацией петли «поток-объем». Анализировался показатель FEV1 - объем форсированного выдоха за 1-ю секунду маневра форсированная жизненная емкость легких (ФЖЕЛ) выдоха. Фиксировались должные значения спирометрического показателя, выраженные в процентах к нормативу для соответствующего возраста, роста и пола.
Уровень окислительного стресса определяли по уровню перекисей методом иммуноферментного анализа (ИФА) с помощью набора PerOx фирмы Immundiagnostik (Германия). Уровень окислительного стресса оценивался как «Низкий» при уровне перекиси водорода <180 мкмоль/л, «Средний» при 180-310 мкмоль/л, «Высокий» при >310 мкмоль/л.
Уровень показателя профиля адипоцитокинов лептина определяли с помощью ИФА набором реактивов «LEPTIN-Sensitive-ELISA» фирмы «Mediagnost GmbH» (Германия). Референсные значения для мужчин: 2,0-5,6 нг/мл, для женщин 3,7-11,1 нг/мл.
Уровень показателя провоспалительного профиля - интерлейкина (IL)-6 определяли с помощью «сэндвич»-варианта твердофазного ИФА набором реактивов «ИНТЕРЛЕЙКИН-6-ИФА-БЕСТ» фирмы ВЕКТОР-БЕСТ (Россия). Референсные значения <7,0 пг/мл.
Статистическая обработка данных проводилась с помощью пакета программ STATGRAPHICS 18 for Windows.
С использованием аппарата многофакторного регрессионного анализа была построена модель, описывающая зависимость частоты обострений БА в течении ближайшего года у пациентов с сопутствующей мультиморбидной патологией от исследуемых факторов.
Таким образом, в качестве прогнозируемой переменной был выбран индекс вероятности обострения БА в течение ближайшего года (ЕхасВА) в у.е., в качестве зависимых переменных:
- ODA23+результат по опроснику двигательной активности ODA23+ (баллы);
- FEV1 - объем форсированного выдоха за 1-ю секунду маневра ФЖЕЛ выдоха (% от должного);
- PerOx - уровень перекисей сыворотки крови (мкмоль/л);
- Leken - результат оценки активности пациентов по шкале Лекена (баллы);
- Leptin уровень лептина венозной крови (нг/мл);
- BMI - индекс массы тела (кг/см2);
- IL-6 - уровень провоспалительного профиля - ИЛ-6 (пг/мл);
- CIRS - кумулятивный индекс заболеваний CIRS (Cumulative Illness Rating Scale).
При построении модели учитывалось не только влияние отдельно каждого фактора на частоту обострений БА, но и их сочетанное (парное) воздействие. Оценка значимости коэффициентов уравнения регрессии оценивалась на основе критерия Стьюдента. При этом незначимые (р>0,05) коэффициенты (и соответствующие им показатели) последовательно (начиная с коэффициента, имеющего наихудшую оценку) исключались из модели и осуществлялся перерасчет оставшихся коэффициентов. Этот процесс повторялся до тех пор, пока в модели не остались только значимые коэффициенты (с соответствующими показателями и их парными взаимодействиями).
Построенная таким образом модель имеет следующий вид:

Шкала для оценки риска развития обострений БА:
ЕхасВА <2 - низкий риск развития обострений БА, с количеством обострений 1 раз в год,
ЕхасВА >2 - высокий риск развития обострений, с количеством обострений в год 2 и более раз.
В табл. 1 приведены оценки параметров полученной модели.
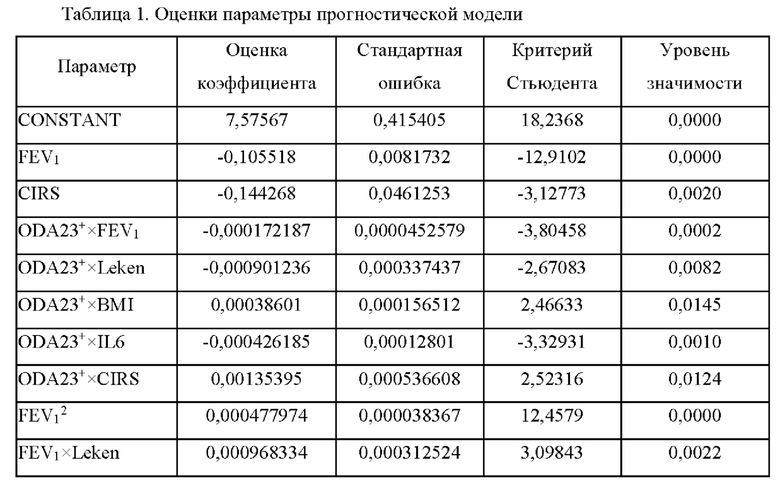
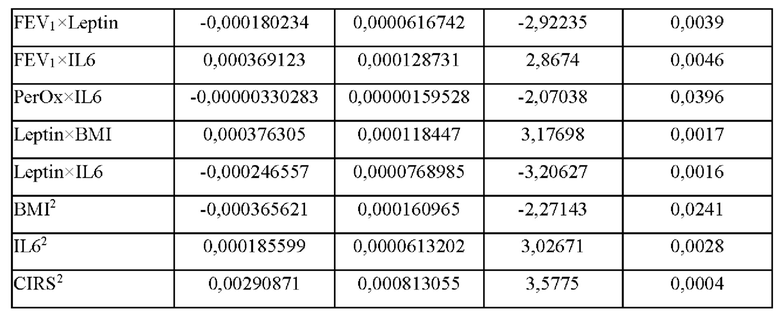
В таблице 2 представлены результаты оценки адекватности модели.
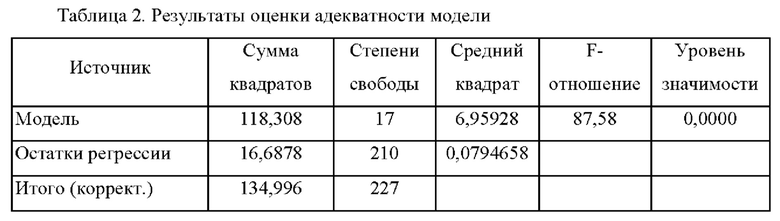
Как следует из таблицы 2, модель адекватно (F=83,96, p <0,0001) описывает имеющуюся зависимость между частотой обострений БА и исследуемыми показателями, включенными в модель в качестве независимых переменных.
Пример 1
Больная С, 48 лет, с Бронхиальная астма аллергическая, легкой степени тяжести, частично контролируемая ДН0. Гастроэзофагеальная рефлюксная болезнь, эндоскопически негативный вариант. Поллиноз. Сезонный аллергический риноконьюктивит.Фибромиома матки, субмикозная. Данные комплексного клинико-инструментального и лабораторного обследования: результат ODA23+ составил 79,7 баллов, FEV1 - 75% от должного, уровень PerOx - 406,02 мкмоль/л, результат активности пациентов по шкале Лекена - 3,5 баллов, уровень лептина венозной крови - 4,73 нг/мл, BMI - 24,01 кг/см2, уровень IL-6 - 9,42 пг/мл, кумулятивный индекс заболеваний CIRS 5 баллов.
Частота обострений БА, рассчитанная с помощью предлагаемой нами прогностической модели, в течение ближайшего года:

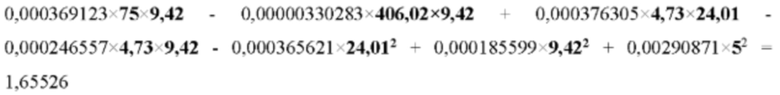
То есть, ЕхасВА <2 (низкий риск обострений).
Наблюдение пациента в течение года, выявило 1 обострение БА. Таким образом, сделанный нами прогноз реализовался.
Пример 2
Больная Р., 68 лет, с диагнозом Бронхиальная астма смешанного генеза, средней степени тяжести, не контролируемая ДНО. Ожирение 2 степени, экзогенно-конституционального генеза. Остеоартрит генерализованный: двусторонний остеоартрит коленных суставов 1 ст. справа и 2 ст. слева, коксартроз справа 2 ст. ФН 2. Гипертоническая болезнь 2 стадии, медикаментозно контролируемое течение, дислипидемия, риск ССЗ, 3 целевой уровень АД <130/80 мм. рт. ст.
Данные комплексного клинико-инструментального и лабораторного обследования: результат ODA23+ составил 87,5 баллов, FEV1 - 51,8% от должного, уровень PerOx - 2014,34 мкмоль/л, результат активности пациентов по шкале Лекена - 8,7 баллов, уровень лептина венозной крови - 28,97 нг/мл, BMI - 33,75 кг/см2, уровень ИЛ-6 - 37,33 пг/мл, кумулятивный индекс заболеваний CIRS 6 баллов.
Частота обострений БА, рассчитанная с помощью предлагаемой нами прогностической модели, в течение ближайшего года:

То есть, ЕхасВА ≥2 (высокий риск обострений).
Наблюдение пациента в течение года выявило 3 обострения БА. Таким образом, сделанный нами прогноз реализовался.
Разработанный способ прогнозирования частоты обострений БА позволяет прогнозировать частоту обострений заболевания (высокий риск, низкий риск) у пациентов с сопутствующей мультиморбидной патологией.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ У БОЛЬНЫХ БРОНХИАЛЬНОЙ АСТМОЙ И СОПУТСТВУЮЩИМ ОЖИРЕНИЕМ | 2019 |
|
RU2692229C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОБОСТРЕНИЙ БРОНХИАЛЬНОЙ АСТМЫ В ТЕЧЕНИЕ БЛИЖАЙШЕГО ГОДА У ПАЦИЕНТОВ С СОПУТСТВУЮЩИМ ОЖИРЕНИЕМ | 2018 |
|
RU2655829C1 |
| Способ определения степени бронхиальной обструкции у пациентов с бронхиальной астмой | 2023 |
|
RU2796385C1 |
| Способ прогнозирования обострений при бронхиальной астме лёгкой и средней степени тяжести | 2023 |
|
RU2835342C1 |
| Способ оценки тяжести обострения бронхиальной астмы с применением интегрального показателя | 2021 |
|
RU2765432C1 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ РИСКА РАЗВИТИЯ ДИСФУНКЦИИ МАЛЫХ ДЫХАТЕЛЬНЫХ ПУТЕЙ У ПАЦИЕНТОВ С БРОНХИАЛЬНОЙ АСТМОЙ НА РАННИХ СТАДИЯХ | 2020 |
|
RU2741858C1 |
| СПОСОБ ОЦЕНКИ И ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ДИСФУНКЦИИ МАЛЫХ ДЫХАТЕЛЬНЫХ ПУТЕЙ У ПАЦИЕНТОВ С БРОНХИАЛЬНОЙ АСТМОЙ, АССОЦИИРОВАННОЙ С ОЖИРЕНИЕМ | 2021 |
|
RU2778070C1 |
| Способ прогнозирования риска неконтролируемого течения бронхиальной астмы у детей с ожирением | 2022 |
|
RU2805825C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОБОСТРЕНИЙ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ У ПАЦИЕНТОВ С ОЖИРЕНИЕМ | 2017 |
|
RU2652550C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕКОНТРОЛИРУЕМОЙ БРОНХИАЛЬНОЙ АСТМЫ | 2014 |
|
RU2559905C1 |
Изобретение относится к медицине, а именно к терапии и пульмонологии, и может быть использовано для прогнозирования обострений бронхиальной астмы (БА) в течение ближайшего года у пациентов с сопутствующей мультиморбидной патологией. Осуществляют определение диагностических показателей, в качестве которых определяют: уровень двигательной активности по опроснику ODA23+, объем форсированного выдоха за 1-ю секунду маневра форсированная жизненная емкость легких выдоха (FEV1), уровень перекисей сыворотки крови, уровень активности пациентов по шкале Лекена, уровень лептина венозной крови, индекс массы тела (BMI), уровень интерлейкина-6 (ИЛ-6), кумулятивный индекс заболеваний CIRS. На основании полученных данных вычисляют индекс вероятности частоты обострения БА в течение ближайшего года у пациентов с сопутствующей мультиморбидной патологией (ExacBA) по формуле:
ExacBA = 7,57567 - 0,105518×FEV1 - 0,144268×CIRS - 0,000172187×ODA23+×FEV1 - 0,000901236×ODA23+×Leken + 0,00038601×ODA23+×BMI - 0,000426185×ODA23+×IL6 + 0,00135395×ODA23+×CIRS + 0,000477974×FEV12 + 0,000968334×FEV1×Leken - 0,000180234×FEV1×Leptin + 0,000369123×FEV1×IL6 - 0,00000330283×PerOx×IL6 + 0,000376305×Leptin×BMI - 0,000246557×Leptin×IL6 - 0,000365621×BMI2 + 0,000185599×IL62 + 0,00290871×CIRS2,
где ODA23+ – результат по опроснику двигательной активности ODA23+, в баллах, FEV1 – объем форсированного выдоха за 1-ю секунду, в процентах, PerOx – уровень перекисей сыворотки крови, мкмоль/л, Leken – результат оценки динамики активности пациентов по шкале Лекена, в баллах, Leptin - уровень лептина венозной крови, нг/мл, BMI - индекс массы тела, кг/м2, IL6 - уровень ИЛ-6, пг/мл, CIRS – кумулятивный индекс заболеваний, в баллах. При значении ExacBA менее 2 прогнозируют низкий риск развития обострений БА, с количеством обострений 1 раз в год. При значении ExacBA 2 и более прогнозируют высокий риск обострений, с количеством обострений в год 2 и более раз. Способ обеспечивает возможность получения достоверного прогноза развития обострений БА у больных с сопутствующей мультиморбидной патологией в течение ближайшего года за счет исследования комплекса факторов с применением математического аппарата многофакторного регрессионного анализа. 2 табл., 2 пр.
Способ прогнозирования обострений бронхиальной астмы (БА) в течение ближайшего года у пациентов с сопутствующей мультиморбидной патологией, включающий определение диагностических показателей, отличающийся тем, что в качестве показателей определяют: уровень двигательной активности по опроснику ODA23+, объем форсированного выдоха за 1-ю секунду маневра форсированная жизненная емкость легких выдоха (FEV1), уровень перекисей сыворотки крови, уровень активности пациентов по шкале Лекена, уровень лептина венозной крови, индекс массы тела (BMI), уровень интерлейкина-6 (ИЛ-6), кумулятивный индекс заболеваний CIRS, на основании полученных данных вычисляют индекс вероятности частоты обострения БА в течение ближайшего года у пациентов с сопутствующей мультиморбидной патологией (ExacBA) по формуле:
ExacBA = 7,57567 - 0,105518×FEV1 - 0,144268×CIRS - 0,000172187× ODA23+×FEV1 - 0,000901236×ODA23+×Leken + 0,00038601×ODA23+×BMI - 0,000426185×ODA23+×IL6 + 0,00135395×ODA23+×CIRS + 0,000477974×FEV12 + 0,000968334×FEV1×Leken - 0,000180234×FEV1×Leptin + 0,000369123×FEV1×IL6 - 0,00000330283×PerOx×IL6 + 0,000376305×Leptin×BMI - 0,000246557×Leptin×IL6 - 0,000365621×BMI2 + 0,000185599×IL62 + 0,00290871×CIRS2,
где ODA23+ – результат по опроснику двигательной активности ODA23+, в баллах,
FEV1 – объем форсированного выдоха за 1-ю секунду, в процентах,
PerOx – уровень перекисей сыворотки крови, мкмоль/л,
Leken – результат оценки динамики активности пациентов по шкале Лекена, в баллах,
Leptin - уровень лептина венозной крови, нг/мл,
BMI - индекс массы тела, кг/м2,
IL6 - уровень ИЛ-6, пг/мл,
CIRS – кумулятивный индекс заболеваний, в баллах,
и при значении ExacBA менее 2 прогнозируют низкий риск развития обострений БА, с количеством обострений 1 раз в год; а при значении ExacBA 2 и более прогнозируют высокий риск обострений, с количеством обострений в год 2 и более раз.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОБОСТРЕНИЙ БРОНХИАЛЬНОЙ АСТМЫ В ТЕЧЕНИЕ БЛИЖАЙШЕГО ГОДА У ПАЦИЕНТОВ С СОПУТСТВУЮЩИМ ОЖИРЕНИЕМ | 2018 |
|
RU2655829C1 |
| US 9726675 B2, 08.08.2017 | |||
| ТРИБУНЦЕВА Л.В | |||
| и др | |||
| Коморбидная патология у пациентов с бронхиальной астмой: обзор литературы | |||
| Наука молодых (Eruditio Juvenium) | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| ИГНАТОВА Г.Л | |||
| и др | |||
| Бронхиальная астма и ожирение: клинико-патогенетические аспекты выделения нового фенотипа заболевания | |||
| Современные | |||
Авторы
Даты
2023-05-22—Публикация
2023-02-18—Подача