Изобретение относится к профилактической, лечебной медицине, ветеринарии и касается профилактики и лечения населения и животных от радиоактивного поражения при воздействии на организм радиоактивных изотопов йода.
Йод представляет собой структурообразующий элемент тиреоидных гормонов. Эти гормоны отвечают за оптимальный рост и развитие организма, дифференцировку, развитие и функционирование всех тканей организма. Они контролируют поглощение кислорода клетками, стимулируют энергетические процессы, регулируют термопродукцию и уровень основного обмена влияют на сердечно-сосудистую и центральную нервную систему. Также йод участвует в разнообразных биохимических процессах негормонального характера. Йод активно поглощается организмом, входит в состав различных химических соединений, компонентов сложного йодного обмена.
В настоящее время известно 37 изотопов йода. Единственным стабильным изотопом является 127I. Радиоактивные изотопы йода отличаются разным периодом полураспада, энергией и характером распада. В химическом отношении эти искусственные радионуклиды являются фактически полными аналогами природного изотопа127I. В дополнение к радиоизотопам йода Теллур-132 также оказывает на организм аналогичное им воздействие.
При радиационной аварии атомных электростанций в начальный период, также называемый периодом йодной опасности, в окружающую среду попадает в огромном количестве 131I. Длительность периода составляет всего несколько месяцев ввиду короткого периода полураспада радионуклида. Так через 2 месяца после завершения выбросов радионуклидов на Чернобыльской АЭС количество131I уменьшилось в 250 раз.
Накопление радиоактивного йода повышает риск развития онкологических заболеваний и гипотиреоза, тиреоидной онкологии в частности, особенно у детей. Индивидуальные дозы, накопленные щитовидной железой вследствие поглощения 131I после Чернобыльской техногенной аварии, достигали 42 Гр и зависели от возраста человека, региональной экспозиции с этим радиоизотопом йода и от количества потребляемого коровьего молока. Средние популяционные дозы, накопленные щитовидной железой детей младшего возраста, достигли до 0,75 Гр на большей части зараженного участка. Накопленный 131I был основным фактором воздействия на щитовидную железу. Вклад этого изотопа в дозу, накопленную щитовидной железой в зараженных регионах, превышал 90% [1].
В случае техногенных аварий, например, на АЭС, выброс в окружающую среду радиоизотопов йода приводит к его поступлению в организм через органы дыхания, пищеварения, поврежденную кожу. Особую радиобиологическую опасность представляют йод-131. Радиоактивный йод избирательно накапливается в щитовидной железе, облучает ее, и тем самым может вызывать развитие заболеваний данного органа. Однако радиоактивный йод поражает не только щитовидную железу: нестабильные изотопы йода, включенные в состав тиреоидных гормонов, прежде всего Т3, связываясь с рецептором и чувствительным к гормону сайтом ДНК (элемент отклика гормона) при своем распаде в состоянии индуцировать мутагенез практически в любой ткани организма. В начальный период после аварии на АЭС накопление радиоизотопов йода происходит преимущественно ингаляционным путем, а в более поздний период радиоактивный йод накапливается при употреблении в пищу молока и молочных продуктов от животных, выпасаемых на загрязненных радиоактивным йодом пастбищах. Пищевым источником радиоактивного йода также могут быть овощи, ягоды и фрукты, выращенные на загрязненной территории. Следует учитывать тот факт, что преимущественной формой радиоактивного йода в пищевых продуктах становятся его разнообразные органические соединения.
Профилактики поражения радионуклидами йода предполагает введение внутрь препарата стабильного йода (обычно йодистого калия) в целях предотвращения или уменьшения поглощения радиоактивных изотопов йода щитовидной железой в случае загрязнения ими окружающей среды. Иными словами производится «блокирование щитовидной железы». Прием стабильного изотопа йода является срочной защитной мерой [2] и для периферийных органов и тканей, а не только щитовидной железы. Принимать препараты йода необходимо в ранние сроки после аварии. Прием препаратов йода через 1 час уменьшает дозу облучения щитовидной железы на 90%, через 3 часа – на 60%, через 6 часов – на 50%. Защитный эффект однократного приема йодистого калия длится 24 часа. Однократный прием для взрослого человека – 125 мг. Взрослым рекомендуется прием таблетированного или порошкового йодистого калия по 125 мг ежедневно в течение 7 дней (запивают 0,5 стакана воды или молока). Дети от 3 до 14 лет принимают препарат по 65 мг 1 раз в день (запивают 0,25–0,5 стакана воды или молока), также в течение 7 дней. Дети до 3 лет принимают по 65 мг йодистого калия 1 раз в день. Но им разрешается принимать препарат лишь в течение 2 дней, то есть двукратно, при суммарной дозе 130 мг. Беременные и кормящие женщины принимают йодистый калий по 125 мг 1 раз в день, в течение 2 дней (всего 250 мг). Также допускается применение 5%-ного спиртового раствора йода, но наружно путем нанесения на кожу. Этот способ особенно приемлем для детей младшего возраста. Для детей от 2 до 14 лет используют по 22 капли настойки 1 раз в день в течение 7 дней [3].
Прием 100 мг стабильного изотопа йода, в количестве эквивалентном 500 кратной суточной потребности в йоде взрослого человека, обеспечивает защиту организма на протяжении 24 часов. 100 мг йода, потребленных накануне заражения радиоактивным йодом, блокируют поглощение йода щитовидной железой на 95% [4]. Более мягкий вариант защиты предполагает дальнейший регулярный прием йода, но уже в количестве 15 мг в сутки, что обеспечивает защиту щитовидной железы на уровне 90%. Прием препарата стабильного изотопа йода должен происходить в течение всего периода подверженности организма угрозе радиоактивного заражения нестабильными изотопами йода.
Аналогичные мероприятия предусмотрены для защиты животных, но с учетом их суточной потребности в йоде. Необходимая профилактическая доза йодида составляет для лактирующей коровы 10 г на голову, а для козы - 1 г.
Однако высокие дозы неорганической формы йода при профилактике поражения радиоизотопами йода также отрицательно сказываются на щитовидной железе и йодном обмене в целом. Поэтому применяемый способ далек от критериев идеального средства защиты и порождает постпрофилактические проблемы для здоровья людей.
С другой стороны в мире накоплен огромный опыт профилактики йододефицитных заболеваний разовым приемом или инъекцией высоких доз йода, обычно в пределах 480-960 мг йода, в форме йодированного растительного масла на уровне годовой потребности человека в йоде. К 1995 году собрана статистика в объеме более чем 60 миллионов случаев применения липоидола в профилактических целях [5]. По мнению специалистов последствия подобной профилактики более удовлетворительные, чем после применения с этой целью йодированной соли с многократно более низким содержанием йода [6]. Механизм дейодирования йодсодержащих жирных кислот не установлен, но он отличается от дегалогенизации ароматических C-I соединений. Возможно, дегалогенизация йодированных жирных кислот происходит посредством ферментов семейства глутатион S трансфераз. Среди продуктов метаболизма йодированных жирных кислот выявляют преимущественно йодид, но в достаточных количествах присутствуют и органические йодсодержащие соединения.
Преобладающей формой йодсодержащих органических соединений в натуральных пищевых продуктах являются йодтирозины. В отличие от известных органических соединений амилойодина и йодинола, йодтирозины представляют собой ароматические химические соединения с ковалентно связанным йодом и в этом их существенное отличие от упомянутых выше соединений, которое и определяет характер всасывания, трансмембранного переноса, тканевого метаболизма этих соединений.
Таким образом, основным источником йода для организма в естественных условиях выступает его органические соединения с ковалентно связанным C-I –йодом. Прежде всего - йодтирозины, йодированные жирные кислоты. Особенностью обмена этих соединений является то, что они - компоненты периферийного йодного обмена. Белки, йодированные по тирозиновым аминокислотным остаткам, – обычная составная часть растительных и мясных пищевых продуктов, яиц, молока, морепродуктов. После внутриклеточного ферментативного дейодирования в органах и тканях тела, йодид выбрасывается в кровоток и становится доступным для щитовидной железы. Кроме того дийодтирозин служит эффектором синтеза и йодирования тиреоглобулина.
Наиболее близким по технической сущности к заявляемому изобретению является «Способ профилактики поражения радионуклидами йода и оптимизации йодного обмена в постпрофилактический период» (Патент RU 2 323 733 C2). Это техническое решение включает использование йодорганических соединений с ковалентно сязанным йодом в качестве эффективного источника стабильного изотопа йода. Накопленные знания за последовавшее время потребовали коррекции предложенного технического решения. В недостаточной степени были учтены отличия в поведении разных органических йодсодержащих соединений, обусловленных их химической природой. Вследствие этого не был выработан оптимальный режим профилактики. Не уделено должного внимания особенностям обмена органических соединений йода разной химической природы в периферийных тканях организма и реакция организма на них. В недостаточной степени раскрыта необходимость индивидуального подхода к йодной профилактике из-за физиолого-биохимических особенностей организма, особенно с учетом персонифицированного подхода к коррекции йодного обмена в постпрофилактический период. Наконец, недостаточно внимания уделено вопросу защиты периферийных тканей от воздействия радиоизотопов йода.
Цель изобретения состоит в разработке эффективного способа и препарата для профилактики поражения радиоизотопами йода, оптимизации и корректирования йодного обмена в постпрофилактический период. Настоящее изобретение направлено, как на решение проблемы эффективной защиты населения и животных от повреждающего воздействия радиоактивных изотопов йода, так и на ослабление потенциальных нарушений йодного обмена у человека и животных в результате профилактических мероприятий.
Предлагаемый способ профилактики поражения радионуклидами йода организма человека или животного основан на выборе органического источника стабильного изотопа йода в ковалентно связанной форме, соответствующей структуре йодного обмена, отличительной особенностью которого является его способность обеспечить эффективное йодное питание периферийных органов и тканей. Химическая структура этого вещества должна обеспечить его доступность периферийному негормональному йодному обмену. Йодное питание собственно щитовидной железы, которое находится в неразрывной связи с йодным обменом всего организма, должен обеспечить йодид, поступающий в кровоток в ходе периферийного ферментативного дейодирования соединений с ковалентно связанным йодом. Дийодтирозин (ДИТ), или его 4-гидрокси 3,5-дийодофенильное производное должен входить в состав йодсодержащего препарата для профилактики поражения радиоизотопами йода как обязательный компонент. ДИТ поступает в клетки периферийных тканей и подвергается внутриклеточной дегалогенизации. Дийодтирозин целесообразно применять в связанной форме как дийодтирозиновый аминокислотный остаток. Выбором связанной формы дийодтирозинового аминокислотного остатка в препарате решают проблему химической хиральной нестабильности L-дийодтирозина: исключают его оптическую рацемизацию. Динамика метаболизма дийодтирозина указывает на целесообразность двукратного введения содержащего его препарата в течение суток с интервалом 10-14 часов (предпочтительно через 12 часов). Техническое решение должно обеспечивать возможность проведения профилактических мероприятий по устранению йододефицита на популяционном, групповом и индивидуальном уровне, принимать во внимание текущий физиологический статус организма, Целесообразно предусмотреть возможность приема препарата, как самостоятельной субстанции, так и в составе пищевого продукта.
Таким образом, поставленные задачи решают пероральным введением йодсодержащего нутрицевтика в форме, биохимически адекватной структуре йодного обмена человека и животного, учитывая при этом не только качественные требования к источнику йода для организма, но и количественные аспекты, связанные с особенностями йодного метаболизма не только в щитовидной железе, но и в периферийных тканях. Дийодтирозиновый аминокислотный остаток, или его 4-гидрокси 3,5-дийодофенильный дериват должны быть обязательным компонентом органического йодсодержащего препарата. Вещества, содержащие его в своей структуре, могут быть выбраны из таких классов химических соединений, как аминокислота, пептид, полипептид, белок растительного, животного, микробиологического происхождения, их гидролизаты, другие биогенные соединения. Целесообразно использовать в качестве животных белков - казеины, яичный альбумин, молочные сывороточные белки, белки сыворотки крови, гемоглобин, в качестве растительных - соевый белок, глютен, зеин, их пептиды, а в качестве микробиологических белков, например, дрожжевые лизаты, лизаты молочнокислых бактерий. Биохимическая особенность этих соединений состоит в том, что в результате ферментативного протеолиза они высвобождают дийодтирозин в свободной форме. Дийодтирозин в отличие от йодида является субстратом периферийного йодного обмена. Это соединение прошло эволюционный отбор в качестве йодсодержащего нутрицевтика с соответствующей организацией йодного метаболизма у человека. Поэтому содержание йода в составе дийодтирозинового аминокислотного остатка, или его 4-гидрокси 3,5-дийодофенильного деривата должно составлять не менее 15% (предпочтительнее 90-100%) от общего количества ковалентно связанного йода в препарате. Пероральная монодоза йода в составе препарата для человека должна находиться в интервале 10 - 200 мг, при этом разовая доза препарата должна превышать физиологическую потребность в йоде в 100-1000 раз.
Выбор связанной формы дийодтирозина обеспечивает не только его химическую стабильность, но и удешевление производства йодосодержащего препарата из-за более низкой стоимости тирозинсодержащих пищевых белков сравнительно со свободной аминокислотой L-тирозин. Дополнительное снижение себестоимости от использования дийодтирозинового деривата сравнительно с монойодтрозиновым является следствием более высокой степени йодирования дийодтирозина: 58,7% против 41,4% у монойодтирозина. Дийодтирозин содержит двукратное количество йода по сравнению с монойодтирозином, а это позволит обходиться меньшим количеством йодсодержащего соединения.
В состав йодсодержащего препарата могут входить иные химические соединения с ковалентно связанным йодом – йодированные жирные кислоты, йодированные липиды, монойодтирозиновые производные. Однако дийодтирозиновому производному следует отдать предпочтение, как доминирующей алиментарной форме йода.
Следовательно, поставленная цель достигается тем, что:
- осуществляют защиту от йодных радионуклидов не только собственно щитовиной железы, но и периферийных тканей – участников йодного обмена;
- йодсодержащий препарат включает, как обязательный компонент, 4-гидрокси 3,5-дийодофенильное производное, что обусловлено характером его метаболизма и ролью в йодном питании и обмене;
- содержание йода в 4-гидрокси 3,5-дийодофенильном деривате должно составлять не менее 15 %, но предпочтительнее 90-100% от общей массы йода в композиции;
- йодсодержащий препарат производят в виде монодозы в твердой, или жидкой форме;
- йодсодержащий препарат получают включением в ее состав вспомогательных, разрешенных в пищевой и фармацевтической промышленности, веществ, в том числе сахаров и полиолов;
- йодсодержащий препарат получают в виде сыпучего порошка, или гранул, или сиропа, или водно-полиольного раствора;
- йодсодержащий препарат включают в состав таблетки, или капсулы, или драже;
- йодсодержащий препарат вводят в организм предпочтительно двукратно в течение суток с 10-14 часовым (в среднем 12 часовым) интервалом;
- разовая доза препарата должна превышать физиологическую потребность в йоде в 100-1000 раз;
- йодсодержащий препарат вводят в организм человека в виде пероральной монодозы в количестве 10 - 200 мг йода.
Препарат предназначен для непосредственного перорального приема, но может быть использован и для обогащения пищевого продукта, напитка.
Целесообразно вводить препарат в состав витаминно-минеральных комплексов.
Использование всех форм йодсодержащего препарата для животных с целью радиационной безопасности регулируется в соответствии с соответствующими установленными для йода ветеринарными, видовыми и профилактическими границами и нормами. Введение йодированных органических соединений в организм животного может осуществляться в составе биологически активных кормовых добавок, в различных формах витаминно-минеральных премиксов и различных кормовых продуктов. Обогащение кормов ведут с использованием твердой, или жидкой формы препарата.
Предпочтительно использовать связанную форму 4-гидрокси 3,5-дийодофенилсодержащих соединений, например, в составе белковых, или пептидных молекул во избежание оптической рацемизации и конверсии части хиральных соединения в энантиомер Д-ряда.
Также целесообразно производить композицию в форме батончика.
Предпочтительно присутствие в составе вспомогательных веществ из группы полиолов, например, сахарозы, глюкозы, фруктозы, ксилозы, лактозы как консервантов и стабилизаторов 4-гидрокси 3,5-дийодофенилсодержащих соединений.
Часть йода в препарате может быть присутствовать в виде 4-гидрокси 3-йодофенильного производного, йодированного липида, или йодированной жирной кислоты, или их комбинации. Эти соединения разнятся характером метаболизма в организме человека, но наряду с дийодтирозином подвержены периферийному тканевому метаболизму и эффективно блокируют поступление в клетки радиоактивных органических соединений йода.
Новизной и достоинствами изобретения является регламентирование приема йодсодержащего препарата, химической формы йодсодержащего препарата в соответствии со структурой йодного обмена, количественного содержания йода в препарате, регламентирование соотношения йодсодержащих органических соединений в препарате, способа приема препарата, формы выпуска и упаковки монодозы.
С целью обоснования эффективности ДИТ в качестве источника алиментарного йода и соединения способного оптимизировать йодный обмен, выполнена серия экспериментов на нелинейных крысах с использованием радиоактивных изотопов 125I и 131I.
В эксперименте I изучали динамику тканевого накопления меченого по 125I дийодтирозина, для чего использовали самцов белых нелинейных лабораторных крыс. Животных содержали в условиях вивария на полноценном рационе со свободным доступом к корму и воде. 125I-дийодтирозин в составе йодированного казеина коровьего молока вводили в желудок животных с помощью зонда в виде раствора (1 мл) в фосфатном буфере (11700 Бк на крысу). Через 30 мин, 1, 2, 4, 8, 16, 24, 48 и 96 часов после затравки 125I-йодтирозином проводили убой декапитацией обездвиженных эфиром крыс. На каждую временную точку использовали по 5 крыс. От каждого животного отбирали кровь, щитовидную железу, печень, почки, сердце, селезенку, скелетные мышцы. Также проводили 24-часовой сбор мочи и кала на 1 и 4 сутки эксперимента. Полученные образцы подвергли радиометрии на гамма-счетчике. Результаты эксперимента I приведены в таблице (Фиг. 1). Как следует из динамики накопления индикатора 125I, в ЖКТ происходит быстрый и эффективный гидролиз йодированного белка с высвобождением свободного дийодирозина, который после всасывания и поступления в кровоток накапливается с различной интенсивностью в тканях всех отобранных органов. Динамика накопления индикаторной метки в периферийных тканях и щитовидной железе принципиально отличается. В течение первых 2 - 4 часов метка поступает преимущественно в периферийные органы и ткани, достигает там максимума накопления в этом интервале, а в последующем демонстрирует неуклонное падение накопленной активности; щитовидная железа начинает заметно поглощать метку спустя 2-4 часа после затравки с достижением максимума поглощения через 8 часов.
Таким образом, длительность цикла периферийного негормонального йодного метаболизма йодсодержащего нутрицевтика укладывается приблизительно в 12 часов (10-14 часовой интервал). Та же картина наблюдается в щитовидной железе с поправкой на процесс синтеза тиреоглобулина и тиреоидных гормонов. Характер регистрируемой динамики тканевого поглощения метки свидетельствует о доминирующей роли периферийного тканевого йодного метаболизма органически связанной формы йода в снабжении алиментарным йодом щитовидной железы. Йодид - преимущественная форма йода в питании собственно щитовидной железы. В мышечную ткань поступил 47,8% введенной метки и именно мышцы играют ведущую роль в периферийном йодном обмене и снабжении щитовидной железы йодидом. В выведении 125I из организма участвовали и почки, и кишечник. За первые сутки с мочой экскретировано 54,2 %, а с фекалиями 12,5 % йода (Фиг.2).
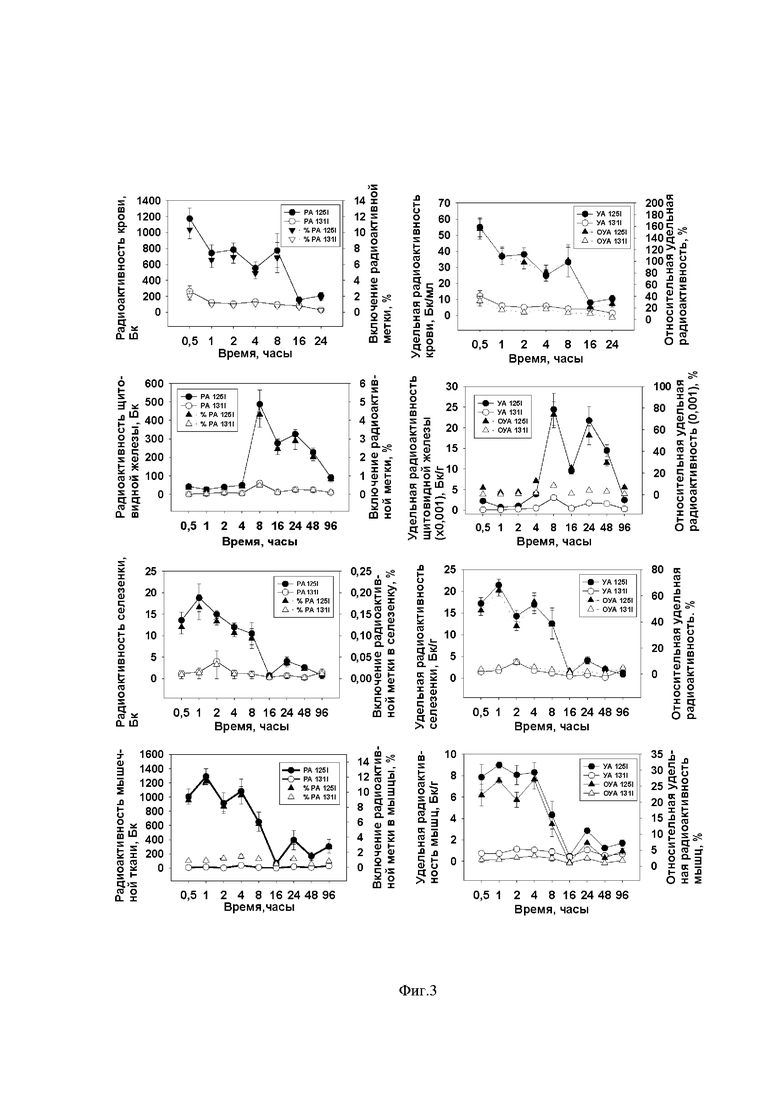
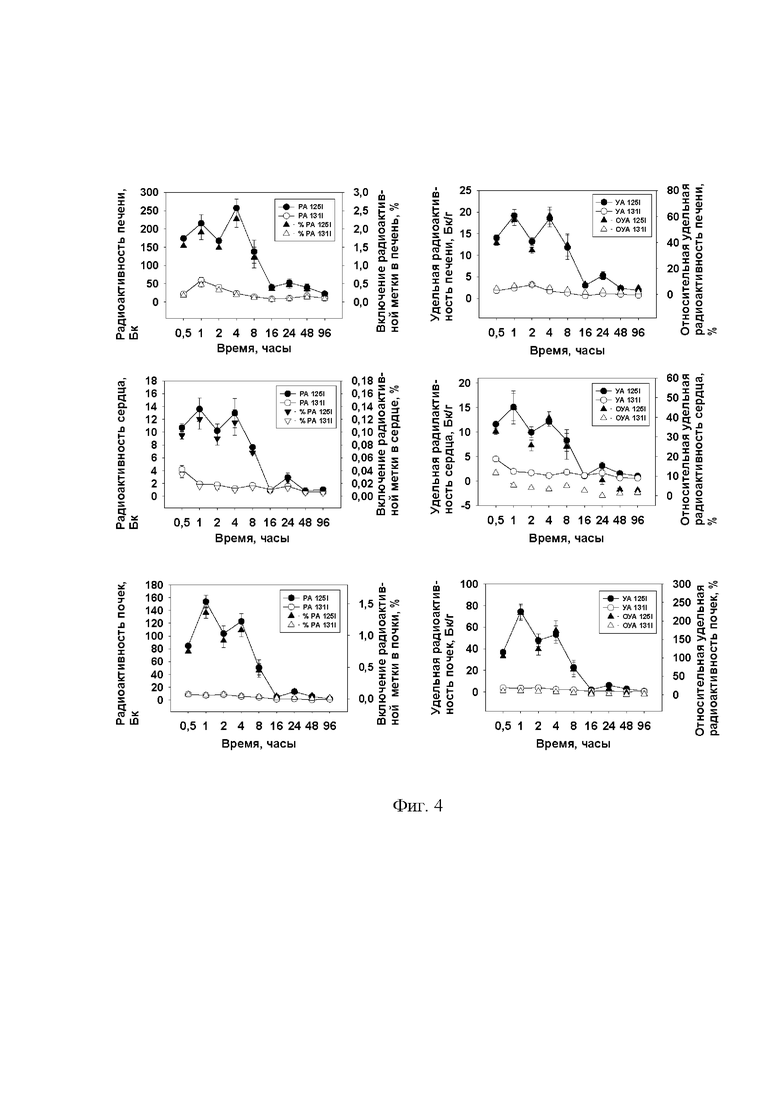
В сравнительном эксперименте II, цель которого состояла в изучении характера обмена йодсодержащего нутрицевтика неорганической и органической природы, исследовали поведение аниона йодида и йода из 4-гидрокси 3,5-дийодофенилпроизводного, а именно дийодтирозинового аминокислотного остатка (ДИТ) йодированного белка. Нелинейным крысам, получавшим корм с содержанием общего йода - 5 мг на 1000 г корма (50% этого йода составлял йодат калия, а остальные 50% - йодированный казеин, т.е. связанный ДИТ), одновременно перорально ввели в эквимолярных количествах 125I-дийодтирозин и 131I-йодид натрия. Далее исследовали динамику накопления введенных меток в тканях животных. Были выявлены принципиальные различия в динамике и структуре тканевого депонирования радиоактивных изотопов из неорганического и органического источников йода (Фиг. 3, 4). Эксперимент показал принципиальные различия в метаболизме йодида и дийодтирозинового аминокислотного остатка. Всасывание 125I (ДИТ) и 131I (йодид) происходит с различной эффективностью; ткани накапливают изотопы на различном уровне. Эксперимент зафиксировал ингибирование всасывания йодида на фоне питания ковалентно связанным йодом. Внетиреоидные ткани показали незначительное поглощение йодида, которое, скорее всего, связано с присутствием крови в исследуемых тканях. Пик включения изотопа из неорганического соединения йода в щитовидную железу приходился на 8 час (0,49% от введенного количества). Наивысший уровень 125I-ДИТ радиоактивности (РА) обнаружен в скелетных мышцах (1290 Бк через 1 час) и крови (1174 Бк через 0,5часа). Радиоактивность щитовидной железы в этот временной период в 2,65-2,41 раза ниже (487 Бк через 8 часов), но превышает радиоактивность других внетиреоидных тканей. Ткани крыс существенно разнятся и по удельной, и по относительной удельной (ОУА) 125I радиоактивности. Наивысшая удельная радиоактивность (УА) 24447,8 Бк/г зарегистрирована в щитовидной железе по истечении 8 часов после введения метки. Удельная радиоактивность периферийных тканей оказалась намного ниже. Спустя 16 часов после введения метки 125I, отслеживаемые параметры (процент включенной метки, уровень радиоактивности, удельная и относительная удельная радиоактивность) во внетироидных тканях достигли минимальных значений. Исключение составляла кровь, для которой минимальное значение зафиксировано спустя 24 часа. Динамика накопления 125I в щитовидной железе находилась в противофазе сравнительно с другими тканями. За первые 4 часа после затравки в периферийных тканях зафиксировано максимальное накопление метки, а уровень регистрируемого изотопа в щитовидной железе демонстрировал самые низкие значения. В период от 4 до 8 часов после введения метки в щитовидной железе наблюдался резкий подъем накопления радиоактивности и ее высокий уровень сохранился во временном диапазоне 8 - 16 часов после затравки. В тоже время в периферийных тканях происходило синхронное падение 125I радиоактивности в этот же временной период. За первые сутки организм крыс экскретировал (Рис. 2) 32,6 % и 15,26 % 125I метки с мочой и фекалиями.
Таким образом, получены экспериментальные доказательства способности организма животных к эффективному усвоению 4-гидрокси 3,5-дийодофенильных производных в качестве источника йода. Доказана способность организма гидролизовать такие 4-гидрокси 3,5-дийодофенилсодержащие соединения как йодированные белки, пептиды в желудочно-кишечном тракте, всасывать свободный дийодтирозин, или дийодтирозинсодержащий дипептид. Эксперимент продемонстрировал наличие механизма трансмембранного переноса дийодтирозина, его участие в периферийном йодном обмене. Эксперимент также выявил способность у множества тканей поглощать ДИТ, дейодировать его, что требует экспрессии внутриклеточной йодтирозин дейодиназы, выводить йодит из клетки в систему кровообращения посредством специфичной системы трансмембранного переноса. В ходе эксперимента получены доказательства доминирующей роли периферийного йодного обмена в снабжении йодом щитовидной железы. Наконец продемонстрировано эффективное поглощение йодида, высвобожденного в процессе периферийного йодного обмена, тканью щитовидной железы. Также подтверждена способность щитовидной железы поглощать экзогенный ДИТ. Метаболизм йодфенильных соединений в периферийных тканях укладывается в 12 часовой цикл. Таким образом, получены доказательства присутствия в тканях и клетках животного сложной системы метаболизма 4-гидрокси 3,5-дийодофенильных соединений и продемонстрирована целесообразность использовать их в качестве йодного нутрицевтика. Обнаружено, что йод в этой органической форме способен контролировать поглощение йодида в ЖКТ подавляя его. Следовательно, в естественных условиях неорганическая форма йода служит, скорее всего, лишь вспомогательным источником йода. Эксперимент раскрывает природу различий в обмене молекулярного йода и йодидного (йодатного) анионов. Эти различия обусловлены способностью элементного йода йодировать по крайней мере гидроксифенильные соединения, которые и определяют специфичный характер обмена молекулярного йода, что зафиксировано в многочисленных исследованиях [18, 19].
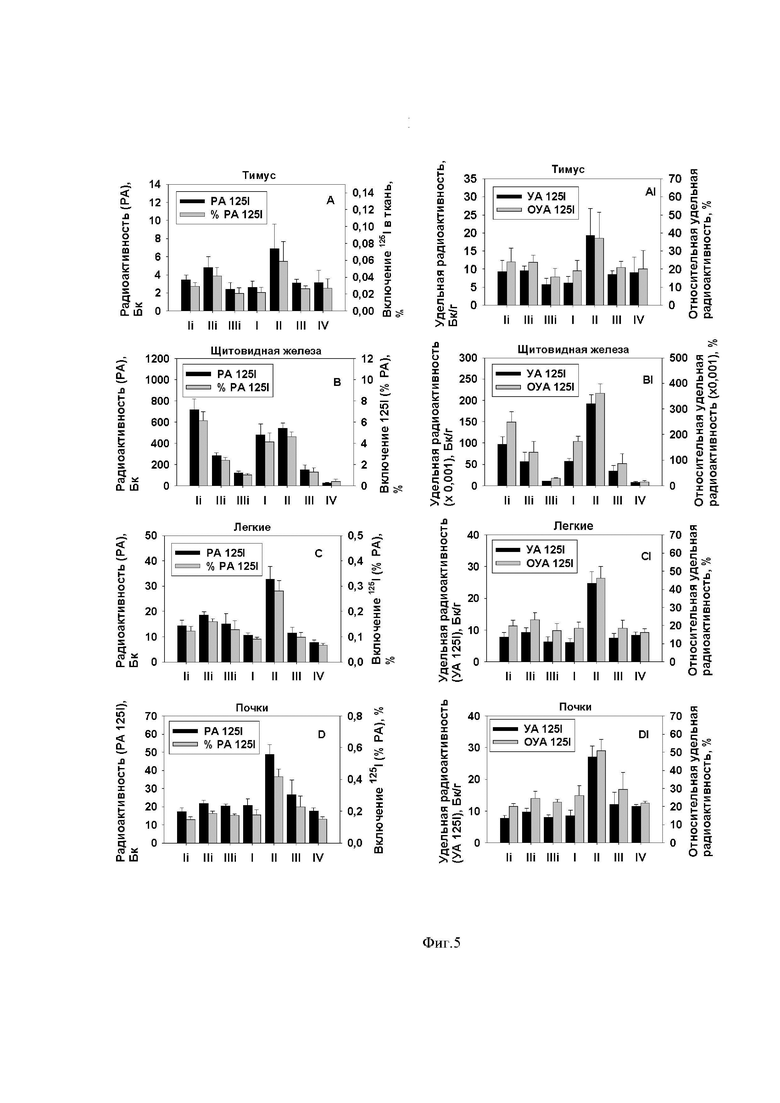
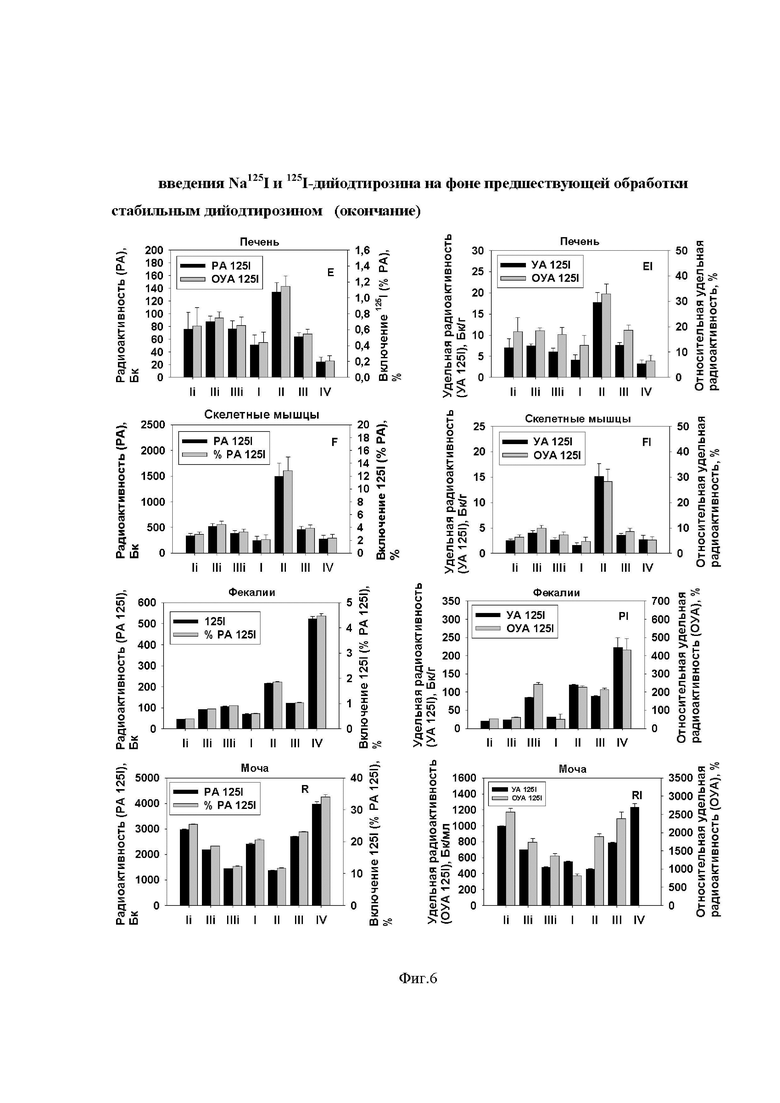
В следующем эксперименте (III) на нелинейных крысах изучен характер йодного обмена на фоне смодулированного статуса йодного питания в зависимости от химической природы йодсодержащего нутрицевтика. Было сформировано 7 групп животных по 5 крыс в каждой. Крысам перорально ввели около 10 кБк Na125I (неорганическая форма йода) через 2 часа после внутрижелудочной инъекции физраствора (контроль, Ii), 50 мкг (Iii) и 500 мкг (IIIi) органически связанного йода (белка с дийодтирозиновыми аминокислотными остатками), с одной стороны, и около 10 кБк в форме меченых 125I дийодтирозинов спустя 2 часа после пероральной нагрузки физраствором (контроль, I), 5 (II), 50 (III) и 500 мкг (IV) стабильного органически связанного йода (белка с дийодтирозиновыми аминокислотными остатками). Через 8 часов произвели убой животных и исследовали накопленную радиоактивность тканей. Полученные результаты отражены в Фиг. 5, 6. Выявлено достоверное падение всасывания, как неорганического йодида, так и ДИТ в обратно пропориональной зависимости от ранее введенной дозы нутрицевтика. Динамика экскреции йода с мочой отличалась для разных химических форм йодсодержащих нутрицевтиков, а именно: имело место уменьшение выделения в случае йодидной метки и нарастание выделения после ввода меченого, связанного ДИТ с ростом дозы ранее введенного алиментарного йода. Этот же эксперимент продемонстрировал влияние уровня йодного питания крыс на тканевое депонирование нутрицевтиков. На фоне роста йодного потребления (обеспеченного возрастающим приемом дийодтирозинов) тканевое поглощение йодтирозинов падало. В то же время аккумулирование йодида, пусть и не на высоком уровне, несколько возрастало.
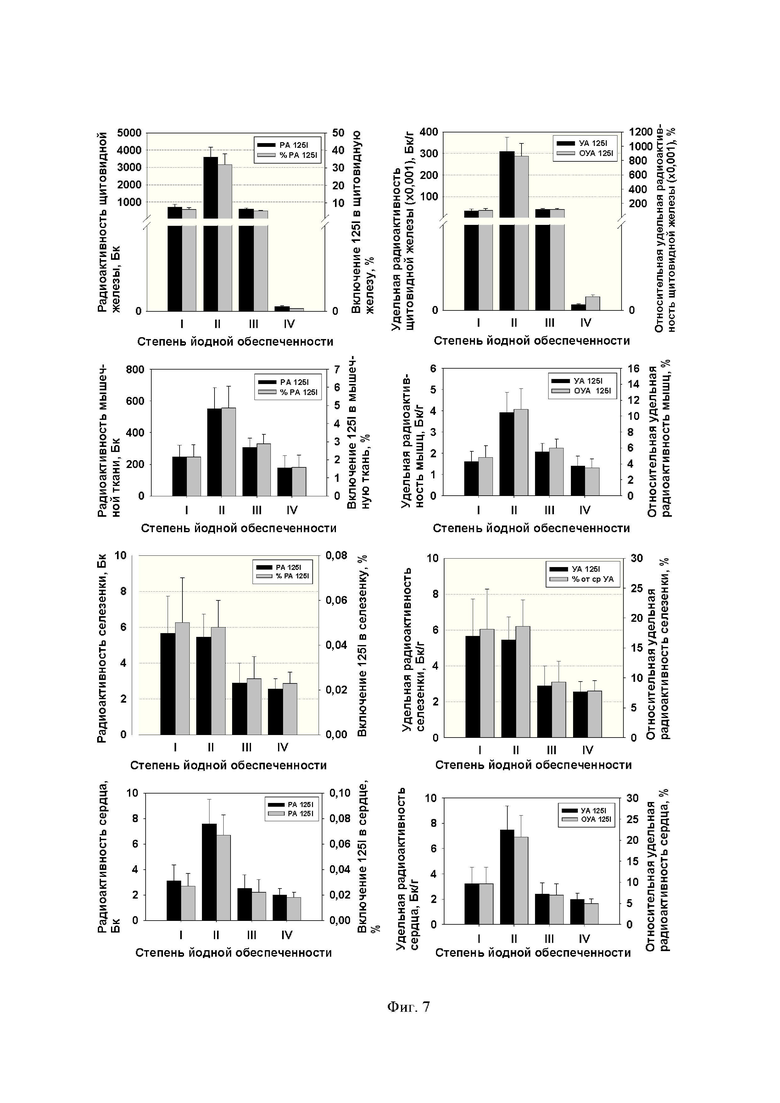
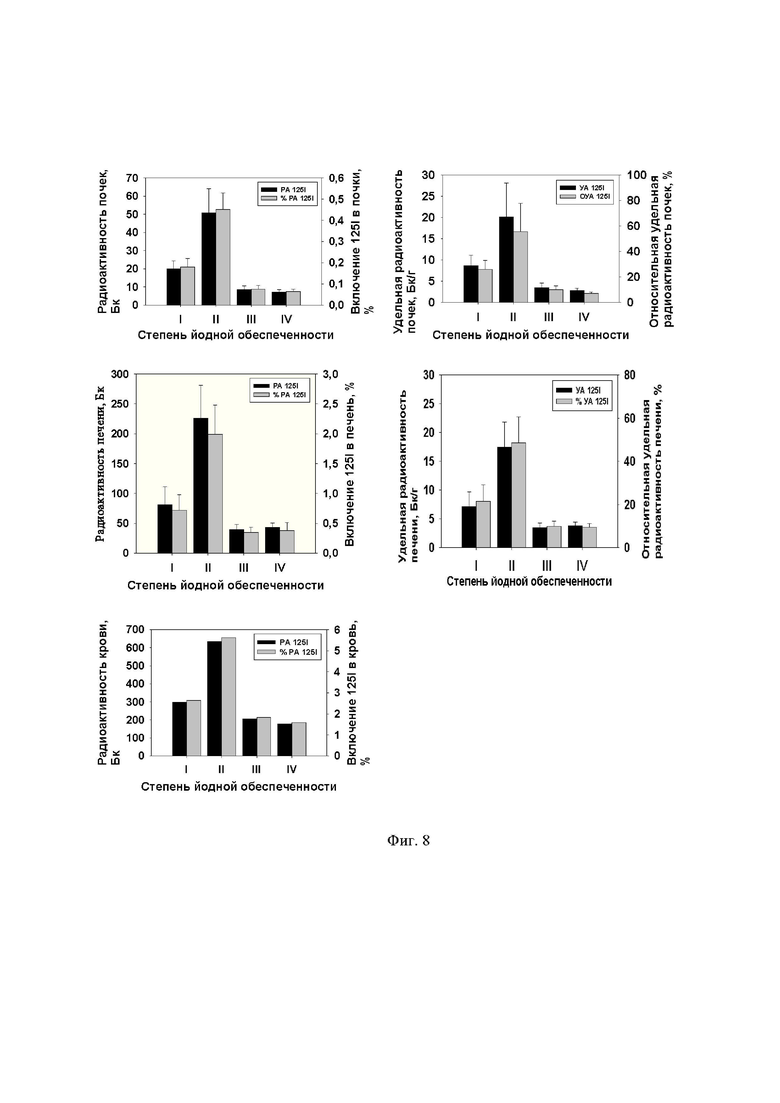
Еще один эксперимент (IV) проведен с целью изучения эффективности дийодтирозинового нутрицевтика (как компонента молочного белка) в профилактике йододефицитного состояния, связанного с недостаточным потреблением йода, и в оптимизации йодного обмена в зависимости от йодного статуса организма. Животных первой группы (I) содержали на искусственном, йододефицитном рационе, крысам второй группы (II) в течение 15 дневного срока скармливали йододефицитный корм с последующим переводом животных на корм, обеспечивающий адекватную, физиологическую норму потребления йода (15 суточный период питания перед убоем). Третью группу (III) использовали в качестве контроля с физиологической нормой потребления йода. Четвертая группа (IV) представляла статус избыточного (200 кратного по отношению к норме) йодного питания. Животным перорально ввели меченый по йоду казеин (125I-ДИТ) и спустя 24 часа регистрировали накопление метки в органах подопытных крыс (Фиг.7,8). Полученные результаты наглядно продемонстрировали способность ДИТ выполнить алиментарную функцию в йодном питании, эффективно решить проблему йодного дефицита.
Одновременно ДИТ проявил способность нормализовать йодный обмен в условиях текущего йодного статуса, обусловленного не только недостаточностью йодного потребления, но и избыточным потреблением этого элемента.
Результаты исследований с молочным йодированным белком, несущим дийодтирозиновые аминокислотные остатки, показали:
- эволюционно сложившуюся генетическую и биохимическую способность тканей организма животных к метаболизму экзогенного ДИТ;
- высокую эффективность связанной формы дийодтирозина в качестве йодосодержащего нутрицевтика;
- целесообразность использования ДИТ в качестве нутрицевтика, что позволяет организму реализовать адаптивные регуляторные механизмы поддержания йодного гомеостаза.
Таким образом, в отличие от неорганических соединений со стабильным изотопом йода, негормональные органические соединения с ковалентно связанным йодом имеют очевидные преимущества перед первыми, что обусловлено спецификой их обмена, и эти преимущества, что особенно важно, положительно сказываются на постпрофилактическом состоянии организма после применения супрафизиологических количеств йода. Дийодтирозиновые дериваты наиболее эффективный источник стабильного изотопа йода. Поглощение дийодтирозина чувствительно к текущему йодному статусу организма.
Техническим результатом изобретения является повышение эффективности профилактики радиационной йодной безопасности, расширение ассортимента профилактических средств, применяемых при угрозе радиационного заражения, снижение уровня патологий йодного обмена как результат применения высоких доз йода, что обеспечивается особенностями метаболизма йодсодержащих соединений в организме человека и животного. Препарат отличается высокой химической стабильностью при хранении.
Примеры осуществления изобретения
Изобретение иллюстрируется следующими примерами, которые, однако, не охватывают, а тем более не ограничивают весь объем притязаний данного изобретения.
Пример 1.
В условиях угрозы поражения радиоактивными изотопами принимают препарат, содержащий дийодтирозиновое производное йода. Целесообразно в начальное время угрозы накопления йодных радионуклидов использовать максимальную дозу стабильного изотопа йода, например, 200-400 мг в сутки. Целесообразен двукратный прием стабильного йода, например, утром, во время завтрака, и вечером, во время ужина с интервалом в 12 часов между приемами. И первый, и второй раз вводят по 100-200 мг стабильного изотопа йода. 12 часовой цикл приема соответствует характеру метаболизма экзогенного дийодтирозина.
Пример 2.
Получение гранулированной формы препарата следующего состава:
Готовят смесь для гранулирования следующего состава:
В скоростном смесителе тщательно смешивают крахмал (11,1 кг), сахарозу (45,0 кг) и йодированный казеин (135,9 кг). Тщательно перемешивают. Добавляют распылением 8 кг воды при постоянном перемешивании. Увлажненную смесь протирают с получением гранулята, который затем подвергают сушке в псевдоожиженном слое до конечно влажности гранул – 4%. Полученные гранулы фасуют в стик-пакеты по 4 г. Один пакетик содержит 200 мг йода.
Пример 3.
Получение таблетированной формы композиции следующего состава (масса таблетки 1,5 г):
В скоростном смесителе тщательно смешивают крахмал (6,667 кг), лактозу (20,194 кг) и 22,64 кг йодированного казеина. Подают через форсунку 5 л воды при постоянном перемешивании. Протирают с получением гранулята, который далее подвергают сушке в псевдоожиженном слое до конечно влажности гранул – 4%. Добавляют стеарат кальция и опудривают гранулы в потоке воздуха. Затем гранулы прессуют на таблеточном прессе, полученные таблетки обеспыливают и фасуют. Выход таблеток – 50 кг. Таблетка содержит 50 мг йода.
Пример 4.
Получение жидкой йодсодержащей композиции.
К 100,0 кг 50% водно-глицеринового раствора добавляют 13,583 кг йодированного по 3 и 5 положениях 4-гидрокси фенильных групп белка. Тщательно перемешивают и фасуют в стик-пакеты из материала с барьерными свойствами по 5,0 мл. Стик-пакет содержит порционное количество (50 мг) связанного йода. Монодоза йода предназначена как для перорального приема, так и обогащения кулинарного продукта, или напитка.
Пример 5.
Получение гранулированной формы композиции следующего состава:
Состав смеси для получения 50 кг гранул с конечной влажностью 4%:
В скоростном смесителе тщательно смешивают йодированный соевый белок (14,325), крахмал (6,175 кг), сорбит (13,75 кг), фруктозу (13,75 кг). Добавляют распылением при перемешивании смеси 5 л очищенной обратным способом воды. Протирают с получением гранул, которые затем подвергают сушке в псевдоожиженном слое до конечно влажности гранул – 4%. Полученные гранулы фасуют в стик-пакеты по 4 г. Один пакетик содержит 50 мг йода.
Пример 6.
Получение биологически активной кормовой добавки (БАКД) в виде порошка следующего состава:
В смесителе тщательно смешивают крахмал (48,15 кг), йодированный казеин (48,15 кг), предварительно измельченную сахарозу(3,7 кг). Полученный порошок фасуют в стик-пакеты. Для предотвращения поражения радиоизотопами йода лактирующей корове скармливают 7,65 г связанного йода, т.е. 200 г смеси в сутки.
Использованная литература:
1. Drozdovitch Vladimir, Radiation Exposure to the Thyroid After the Chernobyl Accident. Frontiers in Endocrinology 2021; Volume 11; Article 569041 Front Endocrinol (Lausanne).
2. Глоссарий МАГАТЭ по вопросам безопасности, Международное Агентство по Атомной Энергии, Вена, 2007 г.
3. Приложение к постановлению Министерства по чрезвычайным ситуациям Республики Беларусь и Министерства здравоохранения Республики Беларусь от 31.08.2006 N 41/67.
4. Verger P. et. al. Iodine kinetics and effectiveness of stable iodine prophylaxis after intake of radioactive iodine: a review, 2001, Thyroid, V.11; N. 4, P.353-360.
5. Sankar R. et al. Review of Experiences with Iodized Oil in National Programmes for Control of Iodine Deficiency Disorders. Indian J Pediatr 1995; Vol. 62; P. 381-393.
6. Wolff J. Physiology and Pharmacology of Iodized Oil in Goiter Prophylaxis. Medicine (Baltimore). Vol. 80, No. 1; P. 20-36, 2001.

Изобретение относится к медицине, ветеринарии, а именно к способу профилактики радиационного поражения. Цель изобретения состоит в разработке эффективного способа профилактики поражения радиоизотопами йода, оптимизации и корректирования йодного обмена в постпрофилактический период. Настоящее изобретение направлено, как на решение проблемы эффективной защиты населения и животных от повреждающего воздействия радиоактивных изотопов йода, так и на ослабление потенциальных нарушений йодного обмена у человека и животных в результате профилактических мероприятий. Поставленная цель достигается тем, что осуществляют защиту от йодных радионуклидов не только собственно щитовидной железы, но и периферийных тканей - участников йодного обмена. Связанную форму 4-гидрокси 3,5-дийодофенилсодержащих соединений, например, в составе белковых или пептидных молекул вводят в организм предпочтительно двукратно в течение суток с 10-14-часовым интервалом; разовая доза препарата должна превышать физиологическую потребность в йоде в 100-1000 раз; йодсодержащий препарат вводят в организм человека в виде пероральной монодозы в количестве 10-200 мг йода. Введение йодированных органических соединений в организм животного может осуществляться в составе пищевого продукта, напитка, биологически активных кормовых добавок, в различных формах витаминно-минеральных премиксов и различных кормовых продуктов. Обогащение кормов ведут с использованием твердой или жидкой формы препарата. 15 з.п. ф-лы, 8 ил., 6 пр.
1. Способ профилактики поражения радионуклидами йода человека или животного, обеспечивающий защиту от радиоактивных изотопов йода периферийных тканей организма и щитовидной железы, включающий прием препарата, содержащего йодорганическое вещество негормональной природы с ковалентно связанным стабильным изотопом йода, представляющее собой l-дийодтирозин, или 4-гидрокси 3,5-дийодфенильное соединение дийодтирозина как аминокислотного остатка белковой, или пептидной молекулы, перорально со 100-1000 кратным превышением физиологической потребности в йоде, двукратно в сутки с 10-14-часовым интервалом, при этом профилактику поражения радионуклидами йода осуществляют на популяционном, групповом и индивидуальном уровнях в период непосредственной угрозы поражения радионуклидами йода самостоятельно или в составе пищевого продукта.
2. Способ профилактики поражения радионуклидами йода человека или животного по п.1, отличающийся тем, что дийодтирозиновые аминокислотные остатки входят в состав белков животного происхождения.
3. Способ профилактики поражения радионуклидами йода человека или животного по п.1, отличающийся тем, что дийодтирозиновые аминокислотные остатки входят в состав белков растительного происхождения.
4. Способ профилактики поражения радионуклидами йода человека или животного по п.1, отличающийся тем, что дийодтирозиновые аминокислотные остатки входят в состав белков микробиологического происхождения.
5. Способ профилактики поражения радионуклидами йода человека или животного по п.1, отличающийся тем, что дийодтирозиновые аминокислотные остатки входят в состав пептидов.
6. Способ профилактики поражения радионуклидами йода человека или животного по п.1, отличающийся тем, что препарат дополнительно содержит йодированные жирные кислоты, йодированные липиды.
7. Способ профилактики поражения радионуклидами йода человека или животного по п.1, отличающийся тем, что препарат дополнительно содержит монойодтирозин, монойодтирозиновые аминокислотные остатки в составе белков, пептидов.
8. Способ профилактики поражения радионуклидами йода человека или животного по любому из пп.1-7, отличающийся тем, что препарат включают в витаминно-минеральный комплекс.
9. Способ профилактики поражения радионуклидами йода человека или животного по любому из пп.1-7, отличающийся тем, что йодсодержащий препарат применяют в твердом или жидком виде.
10. Способ профилактики поражения радионуклидами йода человека или животного по п.9, отличающийся тем, что препарат представляет собой порошок или гранулы.
11. Способ профилактики поражения радионуклидами йода человека или животного по п.9, отличающийся тем, что препарат имеет формат стик-пакета, саше, таблетки, капсулы, жевательной конфеты.
12. Способ профилактики поражения радионуклидами йода человека или животного по п.9, отличающийся тем, что препарат представляет собой сироп или водно-глицериновый раствор.
13. Способ профилактики поражения радионуклидами йода человека или животного по любому из пп.1-7, отличающийся тем, что препарат включают в пищевой продукт.
14. Способ профилактики поражения радионуклидами йода человека или животного по любому из пп.1-7, отличающийся тем, что препарат представляет собой биологически активную кормовую добавку.
15. Способ профилактики поражения радионуклидами йода человека или животного по любому из пп.1-7, отличающийся тем, что препарат входит в состав премикса.
16. Способ профилактики поражения радионуклидами йода человека или животного по любому из пп.1-7, отличающийся тем, что препарат входит в состав корма.
| WO 2004026322 A1, 2004.04.01 | |||
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ ДЛЯ ПРОФИЛАКТИКИ ЙОДНОЙ НЕДОСТАТОЧНОСТИ И ОПТИМИЗАЦИИ ЙОДНОГО ОБМЕНА И ПИЩЕВОЙ ПРОДУКТ, ЕЕ СОДЕРЖАЩИЙ | 2001 |
|
RU2192150C1 |
| Применение йодказеина для предупреждения йоддефицитных заболеваний в качестве средства популяционной, групповой и индивидуальной профилактики йодной недостаточности | |||
| Методические рекомендации | |||
| - М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004, стр | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Кинематографический аппарат | 1926 |
|
SU7301A1 |
Авторы
Даты
2023-05-29—Публикация
2022-06-01—Подача