Изобретение относится к поверхностной модификации металлов и сплавов медицинского назначения и может быть использовано при изготовлении медицинских имплантируемых устройств для травматологии, ортопедии и челюстно-лицевой хирургии.
Нарушение костной ткани вследствие травм является одной из наиболее значимых проблем и для лечения таких нарушений каждый год проводят около 2,5 миллионов по вживлению в тело человека различных медицинских изделий. В настоящее время проводится активное изучение материалов природного и искусственного происхождения для медицинских применений. Продолжительное время основное место материала для замены костной ткани занимает титан и его сплавы. Данные материалы демонстрируют высокую прочность, биоинертность и не склонны к коррозионным разрушениям. Особое внимание привлекают титановые сплавы, обладающие эффектом сверхупругости, которые демонстрируют механическое поведение, схожее с поведением костной ткани. Однако, существует проблема возникновения бактериальной инфекции на границе имплантат-кость. Такого рода инфекции и их дальнейшее распространение по организму опасно и может привести к развитию хронического воспаления, и, как следствие, необходимости удаления установленной конструкции. Постоянная замена имплантатов наносит серьезный ущерб здоровью человека, экономически не выгодна и вызывает большие трудности с медицинской точки зрения.
Исходя из этого актуальной задачей становится создание способа модификации поверхности имплантата для обеспечения антибактериального эффекта и предотвращения появления и распространения бактериальной инфекции.
Известен способ нанесения биоактивного покрытия титанового имплантата, вводимого в костную ткань человека (RU 2566060 С1, опубл. 20.10.2015). Способ заключается в получении многослойного покрытия методом атомно-слоевого осаждения. Покрытие состоит из слоев оксидов переходных металлов, таких как оксид титана TiO2 с кристаллической модификацией - анатаз, оксид циркония ZrO2, оксид гафния HfO2, оксид тантала Ta2O5 с аморфной структурой, оксид ниобия Nb2O5 с аморфной структурой, многокомпонентный оксид (TiO2)xTa2O5)1-х, где x равен 0,8-0,95 со структурой твердого раствора на основе тетрагональной кристаллической решетки.
Недостатком данного способа является то, что оксидные покрытия препятствуют только формированию нежелательных отложений на металлических поверхностях, помещенных в биологическую среду, но не являются носителями антибактериальных средств, а также негативным фактором является высокая стоимость необходимых для нанесения покрытия материалов.
Известен способ нанесения кальцитных, апатитовых и композиционных покрытий на титановые имплантаты (RU 2453630 С1, опубл. 20.06.2012). Для нанесения покрытия используют растворы нитрата или хлорида кальция и гидрокарбоната натрия при стехиометрическом соотношении реагентов 2:1. После начала выделения углекислого газа имплантаты помещают в реакционную смесь и выдерживают как минимум 10 минут при 20°С, далее промывают и оставляют как минимум на сутки в контакте с 0,6 M раствором (NH)2HPO4, затем выдерживают как минимум сутки в 1 M растворе Са(NO3)2, затем выдерживают как минимум сутки в 0,6 M растворе (NH4)2HPO4, промывают и помещают в раствор желатина или хондроитинсульфата.
Недостатком данного способа является то, что он в большей мере эффективен для повышения коррозионной стойкости и остеоинтеграции имплантатов, но не обеспечивает антибактериальный эффект поверхности.
Известен способ получения биоактивного покрытия с бактерицидными свойствами на имплантате (RU 2774836 С1, опубл. 23.06.2022). Способ заключается в активации поверхности раствором соляной кислоты или смесью соляной и азотной кислот, последующей обработке в растворе гидроксида натрия с дальнейшем нанесением покрытия на поверхность методом электрофоретического осаждения из раствора электролита, содержащего минимум один антибиотик на полимерном носителе, представляющем собой хондроитин сульфат и воду, с дополнительным введение кальция в электролит.
Недостатком данного покрытия является выбор антибиотика в качестве действующего антибактериального вещества. При применении антибиотиков существует риск потери способности организма самостоятельно противостоять различным видам инфекций. Также, ввиду их широкого применения, существуют штаммы бактерий полностью устойчивые к воздействию антибиотика, поэтому такое покрытие не может всецело обеспечить антибактериальный эффект.
Наиболее близким к предложенному методу прототипом является способ получения адгезивного покрытия для ортопедических имплантатов из титана и нержавеющей стали (RU 2632702 С1, опубл. 09.10.2017). На поверхность имплантатов из титана и нержавеющей стали, предварительно очищенную методом травления ионами аргона, плазменным напылением наносят антибактериальное биосовместимое покрытие, которое состоит из наночастиц высокочистого серебра (чистота 99,9%) размером 4,5-9,5 нм с нанесенным на их поверхность сплошным защитным углеродным нанопокрытием из тетраэдрического алмаза типа ta-C толщиной 0,4-1,2 нм.
Недостатком данного способа является ограниченность его применения. При нанесении покрытия имплантат будет подвержен значительному нагреву, что в случае сверхупругих титановых сплавов негативно повлияет на его механические характеристики.
Задача изобретения заключается в разработке способа модификации поверхности сплавов на основе титана медицинского назначения, обеспечивающего антибактериальный эффект поверхности за счет формирования наночастиц серебра, которые способны подавить воспаление и препятствовать образованию бактериальной пленки.
Техническим результатом, на который направленно данное изобретение, является создание покрытия, обеспечивающего устойчивый антибактериальный эффект поверхности после установки имплантата и предотвращающий возникновение и распространение бактериальных инфекций.
Технический результат достигается следующим образом.
Способ получения антибактериального покрытия, содержащего наночастицы серебра, на поверхности имплантата из титана или титанового сплава, включающий предварительную обработку поверхности указанного имплантата, отличающийся тем, что предварительную обработку поверхности указанного имплантата проводят в растворе из серной кислоты 98%-ой и перекиси водорода 30%-ой в соотношении 1:3, при температуре 18-22 °С в течение 90 мин, а антибактериальное покрытие получают путем модифицирования поверхности указанного имплантата с формированием на ней наночастиц серебра методом полиольного синтеза, который проводят в среде полиэтиленгликоля-400 с содержанием химически чистого нитрата серебра (AgNO3) в концентрации 2 мг/мл, при температуре 18-22 °С и при постоянном перемешивании в течение 18 мин, причем в течение 8 мин указанное перемешивание проводят под воздействием ультрафиолетового излучения, а в течение последующих 10 мин - без воздействия ультрафиолетового излучения, затем осуществляют промывание имплантата в дистиллированной воде и сушку на воздухе в течение 10-20 ч.
Поверхность имплантата из титана или его сплавов предварительно обрабатывают в 100 мл раствора серной кислоты (98%) и концентрированной перекиси водорода (30%) в соотношении 1:3 при комнатной температуре в течение 90 минут. Благодаря такой обработке на поверхности имплантата образуется однородная развитая пористая структура, которая благоприятствует интеграции имплантата с костной тканью, а также способствует увеличению площади поверхности для формирования наночастиц серебра. При большем времени предварительной обработки поверхность становится разнородна, а поры не равномерны, при меньшем времени обработки пористая структура до конца не формируется.
Модификация поверхности имплантата реализуется методом полиольного синтеза, химически чистый нитрат серебра (AgNO3) в количестве 2 мг/мл восстанавливают в растворе полиэтиленгликоля-400. Синтез проходит при температуре 18-22°С в течение 8 минут при постоянном перемешивании, с использованием магнитной мешалки со скоростью 600 оборотов/минуту под воздействием ультрафиолетового излучения мощностью 20 Вт и последующим перемешиванием в течении 10 минут без воздействия ультрафиолетового излучения. При меньших концентрациях нитрата серебра в среде синтеза распределение наночастиц по материалу может быть неравномерным, при больших количествах нитрата серебра в среде наночастицы на поверхности имплантата могут сформироваться в избытке, образуя крупные агломераты.
После модификации поверхности изделие промывают в дистиллированной воде в течение 15 минут под воздействием ультразвукового излучения, сушат на воздухе в течение 10-20 часов в зависимости от геометрических параметров имплантата. При меньшем времени не реализуется полное высыхание покрытия, большее время сушки является нерациональным и не влияет на свойства покрытия.
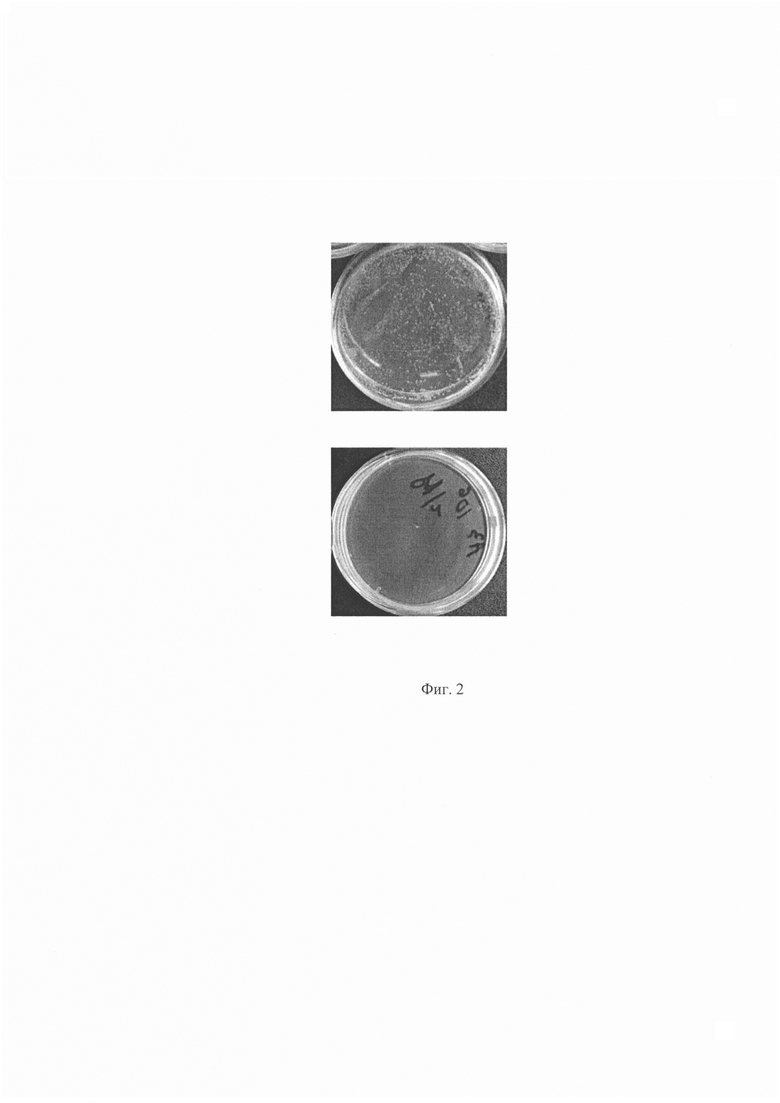
Изобретение поясняется чертежом, где на фиг. 1 показаны СЭМ изображения поверхности сплавов Ti-18Zr-15Nb, Ti и Ti-6Al-4V после формирования антибактериального покрытия; на фиг 2 приведены изображение чашек Петри после антибактериальных тестов на образце без покрытия и на образце с покрытием.
Пример 1
Образец сплава Ti-18Zr-15Nb (в ат. %) с площадью поверхности 100 мм2 был предварительно обработан в растворе серной кислоты (98%) и концентрированной перекиси водорода (30%) в соотношении 1:3 при температуре 18-22°С в течение 90 минут, после чего промыт в дистиллированной воде и погружен в 50 мл раствора полиэтиленгликоля-400. AgNO3 в количестве 2 мг/мл добавлен в среду при постоянном перемешивании. Покрытие наносили в течение 8 минут под воздействие ультрафиолетового излучения и далее в течение 10 минут без воздействия ультрафиолетового излучения. Далее образец был промыт в течение 15 минут в дистиллированной воде под воздействием ультразвукового излучения и высушен на воздухе в течение 10 часов.
Пример 2.
Образец сплава чистого титана с площадью поверхности 200 мм2 был предварительно обработан в растворе серной кислоты (98%) и концентрированной перекиси водорода (30%) в соотношении 1:3 при температуре 18-22°С в течение 90 минут, после чего промыт в дистиллированной воде и погружен в 100 мл раствора полиэтиленгликоля-400. AgNO3 в количестве 2 мг/мл добавлен в среду при постоянном перемешивании на магнитной мешалке. Покрытие наносили в течение 8 минут под воздействием ультрафиолетового излучения и далее в течение 10 минут без воздействия ультрафиолетового излучения. Далее образец был промыт в течение 15 минут в дистиллированной воде под воздействием ультразвукового излучения и высушен на воздухе в течение 15 часов.
Пример 3.
Образец сплава Ti-6Al-4V (в ат. %) с площадью поверхности 100 мм2 был предварительно обработан в растворе серной кислоты (98%) и концентрированной перекиси водорода (30%) в соотношении 1:3 при температуре 18-22°С в течение 90 минут, после чего промыт в дистиллированной воде и погружен в 50 мл раствора полиэтиленгликоля-400. AgNO3 в количестве 2 мг/мл добавлен в среду при постоянном. Покрытие наносили в течение 8 минут под воздействие ультрафиолетового излучения и далее в течение 10 минут без воздействия ультрафиолетового излучения. Далее образец был промыт в течение 15 минут в дистиллированной воде под воздействием ультразвукового излучения и высушен на воздухе в течение 12 часов.
Исследование поверхности
В результате исследований полученных покрытий методом электронной сканирующей микроскопии установлено, что поверхность всех материалов характеризуется равномерным распределением частиц серебра (Фиг. 1). Был установлен средний размер частиц, который составил 12-14 нм.
Антибактериальные испытания
Антибактериальные свойства покрытий оценивали с помощью анализа ингибирования роста клеток в отношении грамотрицательных бактерий E.coli, среду, содержащую бактерии в концентрации 400 клеток/мл, наносили на тестируемые образцы и затем инкубировали при 37°С в течение 24 часов. Аликвоту среды с клетками разбавляли, распределяли по чашкам с агаром и инкубировали при 37°С в течение 24 ч и подсчитывали число колониеобразующих единиц (Фиг. 2).
Анализ полученных результатов показал, что все испытуемые образцы, с нанесенным покрытием обладают сильным антибактериальным действием по отношению к бактериальной тест-культуре.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОКРЫТИЯ ИЗ НАНОМАТЕРИАЛОВ ДЛЯ ОСТЕОИНТЕГРИРУЕМЫХ БИОМЕДИЦИНСКИХ ПРОТЕЗОВ | 2006 |
|
RU2401129C2 |
| СПОСОБ НАНЕСЕНИЯ БИОАКТИВНОГО ПОКРЫТИЯ НА ТИТАНОВЫЕ ИМПЛАНТАТЫ | 2018 |
|
RU2684617C1 |
| Способ получения модифицированного биопокрытия на имплантате из титана (варианты) | 2019 |
|
RU2693468C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТОВ | 2013 |
|
RU2529262C1 |
| СПОСОБ ФОРМИРОВАНИЯ ГИБРИДНОГО ПОКРЫТИЯ НА АЛЮМИНИИ | 2023 |
|
RU2796602C1 |
| Способ получения модифицированного биопокрытия с наночастицами Fe-Cu на имплантате из титана | 2021 |
|
RU2771813C1 |
| СПОСОБ ФОТОКАТАЛИТИЧЕСКОЙ ОЧИСТКИ И СТЕРИЛИЗАЦИИ ВОЗДУХА | 2020 |
|
RU2743705C1 |
| ФУНКЦИОНАЛЬНЫЕ НАНОМАТЕРИАЛЫ С АНТИБАКТЕРИАЛЬНОЙ И АНТИВИРУСНОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2404988C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ СЕРЕБРА С ПОМОЩЬЮ МОДИФИЦИРОВАННОГО ХИТОЗАНА | 2019 |
|
RU2701914C1 |
| ЗОЛЬ ФОТОКАТАЛИТИЧЕСКИ АКТИВНОГО ОКСИДА ТИТАНА, КОМПОЗИЦИЯ ПОКРЫТИЯ И ДЕТАЛЬ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2007 |
|
RU2404852C1 |

Изобретение относится к способу получения антибактериального покрытия, содержащего наночастицы серебра на поверхности имплантата из титана или титанового сплава. Проводят предварительную обработку поверхности указанного имплантата в растворе из серной кислоты 98%-ой и перекиси водорода 30%-ой в соотношении 1:3, при температуре 18-22 °С в течение 90 мин. Затем получают антибактериальное покрытие путем модифицирования поверхности указанного имплантата с формированием на ней наночастиц серебра методом полиольного синтеза. Полиольный синтез проводят в среде полиэтиленгликоля-400 с содержанием химически чистого нитрата серебра (AgNO3) в концентрации 2 мг/мл, при температуре 18-22 °С и при постоянном перемешивании в течение 18 мин. В течение 8 мин указанное перемешивание проводят под воздействием ультрафиолетового излучения, а в течение последующих 10 мин - без воздействия ультрафиолетового излучения. Затем осуществляют промывание имплантата в дистиллированной воде и сушку на воздухе в течение 10-20 ч. Обеспечивается создание покрытия с устойчивым антибактериальным эффектом поверхности после установки имплантата. 2 ил., 3 пр.
Способ получения антибактериального покрытия, содержащего наночастицы серебра, на поверхности имплантата из титана или титанового сплава, включающий предварительную обработку поверхности указанного имплантата, отличающийся тем, что предварительную обработку поверхности указанного имплантата проводят в растворе из серной кислоты 98%-ой и перекиси водорода 30%-ой в соотношении 1:3, при температуре 18-22 °С в течение 90 мин, а антибактериальное покрытие получают путем модифицирования поверхности указанного имплантата с формированием на ней наночастиц серебра методом полиольного синтеза, который проводят в среде полиэтиленгликоля-400 с содержанием химически чистого нитрата серебра (AgNO3) в концентрации 2 мг/мл, при температуре 18-22 °С и при постоянном перемешивании в течение 18 мин, причем в течение 8 мин указанное перемешивание проводят под воздействием ультрафиолетового излучения, а в течение последующих 10 мин - без воздействия ультрафиолетового излучения, затем осуществляют промывание имплантата в дистиллированной воде и сушку на воздухе в течение 10-20 ч.
| Антиадгезивное антибактериальное покрытие для ортопедических имплантатов из титана и нержавеющей стали | 2016 |
|
RU2632702C1 |
| СПОСОБ ФОРМИРОВАНИЯ АНТИМИКРОБНОГО ПОКРЫТИЯ | 2012 |
|
RU2504349C1 |
| RU 2774836 C1, 23.06.2022 | |||
| СПОСОБ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТОВ | 2013 |
|
RU2529262C1 |
| WO 03099346 A2, 04.12.2003 | |||
| JP 6055623 B2, 27.12.2016. | |||
Авторы
Даты
2023-07-05—Публикация
2022-12-05—Подача