Область техники, к которой относится изобретение
Изобретение относится к области медицины, а именно к хирургии и травматологии-ортопедии и может быть использовано для лечения пациентов с острой хирургической инфекцией в области эндопротезов крупных суставов конечностей, например, коленного сустава.
Уровень техники
При хирургическом лечении параэндопротезной инфекции крупных суставов конечностей используют различные методы лечения: 1 - вскрытие и санация перипротезной гнойной полости с радикальной хирургической обработкой раны, извлечение съемных элементов конструкции эндопротеза с последующей их заменой, дренирование раны с ушиванием при произведенной санации с пролонгированной антибиотикотерапией; 2 - удаление инфицированного эндопротеза, с последующей его одно- или многоэтапной заменой; 3 - удаление эндопротеза с выполнением артродеза, 4 - выполнение высокой ампутации конечности.
Известно устройство для реализации метода лечения параэндопротезной инфекции, состоящее из компонентов аппарата Илизарова, со следующей компоновкой, для описания компоновки использован метод МУОЧО, Методические рекомендации МЗ РФ №2002/134, 2002 г. (1). При этом проксимальный модуль расположен на уровне V бедра, представлен одним полукольцом соответствующего объему мягких тканей размера, в кольце фиксированы следующие элементы: стержень-шуруп вне плоскости кольца на уровне IV в положении 10 часов под углом 120 градусов, стержень-шуруп вне плоскости кольца на уровне VI в положении 12 часов под углом 60 градусов. Дистальный модуль расположен на уровне IV голени, представлен одним полукольцом соответствующего объему мягких тканей размера, в кольце фиксированы следующие элементы: стержень-шуруп вне плоскости кольца на уровне III в положении 10 часов под углом 120 градусов, стержень-шуруп вне плоскости кольца на уровне V в положении 2 часа под углом 60 градусов. Модули аппарата соединены резьбовыми стержнями, при необходимости с шарнирами. Указанная компоновка содержит минимальное количество чрескостных элементов (четыре), не имеет замкнутых кольцевых опор, в тоже время позволяет жестко фиксировать коленный сустав на время лечения.
Известен метод хирургического лечения параэндопротезной инфекции без удаления эндопротеза, заключающийся в выполнении радикальной хирургической обработки раны, обильном промывании раны растворами антисептиков, замены съемных элементов эндопротеза, дренировании раны и наложение первичных швов с последующей пролонгированной антибактериальной терапией (2). Операция выполняется путем вскрытия очага параимплантной инфекции. Выполняют бактериологическое исследование раневого экссудата В процессе хирургической обработки иссекают все визуально измененные и некротизированные мягкие ткани. Затем производят извлечение съемных элементов конструкции эндопротеза (полиэтиленовые вкладыши). Производят оценку признаков нестабильности эндопротеза. Рану обильно промывают растворами антисептиков, устанавливают дренирующие силиконовые трубки. Заменяют съемные элементы эндопротеза (полиэтиленовые вкладыши) на новые. Выполняют ушиванием раны. В послеоперационном периоде проводят пролонгированную антибактериальную терапию с коррекцией схемы лечения в зависимости от состава и чувствительности выделенной раневой микрофлоры.
Недостатками данной методики являются:
1. Невозможность объективно оценить интраоперационно необходимый объем хирургической обработки, что обусловливает высокий риск ранних послеоперационных гнойных осложнений. При этом в связи со сложной конфигурацией раны и наличием труднодоступных участков послеоперационная рана может содержать некротизированные и нежизнеспособные ткани, что приводит к неудаче попытки купирования гнойного процесса без удаления эндопротеза
2. Невозможность достоверной оценки степени перипротезной резорбции костной ткани во время операции вскрытия гнойного очага, что влечет за собой опасность септической резорбции и нестабильности эндопротеза.
3. Отсутствие информации о видовом составе раневой микрофлоры и ее антибиотикорезистентности на момент начала антибактериальной терапии, что снижает ее эффективность.
Известен способ лечения больных с парапротезной инфекцией тазобедренного сустава (патент RU 2526956, 01.03.2013 г.), который предусматривает проведение декремента гнойно-воспалительного очага и стабилизацию тазобедренного сочленения с помощью аппарата внешней фиксации. Однако, данный способ предложен для лечения параэндопротезной инфекции тазобедренного сустава. Кроме того, открытое ведение раны при данном способе увеличивает риск вторичного инфицирования эндопротеза поли резистентными штаммами госпитальной микрофлоры и, снижает эффективность лечения, повышая вероятность рецидива инфекции и, таким образом, увеличивая риск ампутации конечности. Кроме того, применение вышеописанного способа увеличивает сроки госпитализации, компрометирует стабильность элементов эндопротеза. Суммарно вышеприведенные недостатки снижают вероятность сохранения эндопротеза и повышают риск ампутации конечности.
Таким образом анализ известных способов позволил выявить следующие проблемы, возникающих при обычном хирургическом лечении острой парапротезной инфекции после протезирования крупных суставов.
Первая проблема: при попытке купирования инфекции без удаления эндопротеза путем радикальной хирургической обработки гнойного очага, дренирования перипротезной полости и пролонгированной антибактериальной терапией, является сложность интраоперационной оценки состояния перипротезной костной ткани, а именно отсутствия ее септической резорбции.
Вторая проблема: необходимость радикальной хирургической обработки с удалением всех некротизированных, а также воспаленных перипротезных мягких тканей.
Третья проблема - опасность вторичного инфицирования эндопротеза госпитальной микрофлорой при открытом ведении раны, что заставляет при традиционном подходе накладывать на рану первичные швы.
Четвертая проблема - отсутствие при традиционном подходе данных о характере и антибиотикорезистентности раневой микрофлоры на момент закрытия раны и стартовой антибактериальной терапии.
Предлагаемое решение направлено на устранение вышеприведенных проблем.
Технический результат - расширение арсенала технических средств при использовании способа лечения параэндопротезной инфекции коленного сустава за счет снижение риска вторичного инфицирования раны госпитальной инфекцией и повышение вероятности успешного купирования инфекции без удаления эндопротеза.
Технический результат достигается за счет того, способ лечения параэндопротезной инфекции коленного сустава включает ревизию пораженного сустава, радикальную хирургическую обработку очага инфекции, после выполнения которой производят извлечение съемных элементов эндопротеза, наложение аппарата наружной фиксации, дистракцию оставшихся компонентов эндопротеза, заполнение перипротезной полости дренирующей губкой и лечение раны локальным отрицательным давлением в пределах 80-150 мм рт.ст., с отсроченным наложением швов на рану после купирования явлений воспаления и получения результатов бактериологического исследования.
Способ позволяет за счет открытого ведения раны и динамического наблюдения за состоянием перипротезных тканей достоверно оценить наличие септической резорбции, что дает возможность принять обоснованное решение о возможности сохранения эндопротеза.
Кроме того, способ позволяет выполнить щадящую хирургическую обработку, за счет этого удаляются только необратимо измененные ткани, а явления воспаления купируются в процессе послеоперационного лечения раны с использованием вакуум-ассистированной повязки. Диапазон отрицательного давления, в пределах 80-150 мм рт.ст., выявлен авторами изобретения в процессе проведенных ими исследований и в процессе практического применения. Причем использование в предлагаемом способе вакуум-ассистированной повязки позволяет существенно снизить риск вторичного инфицирования.
При этом способ лечения параэндопротезной инфекции коленного сустава позволяет отсрочить наложение швов на рану до получения результатов бактериологического исследования и подбора оптимальной схемы антибактериальной терапии. За счет этого, не требуется смена схемы антибиотикотерапии, что увеличивает ее эффективность и снижает риск рецидива инфекции.
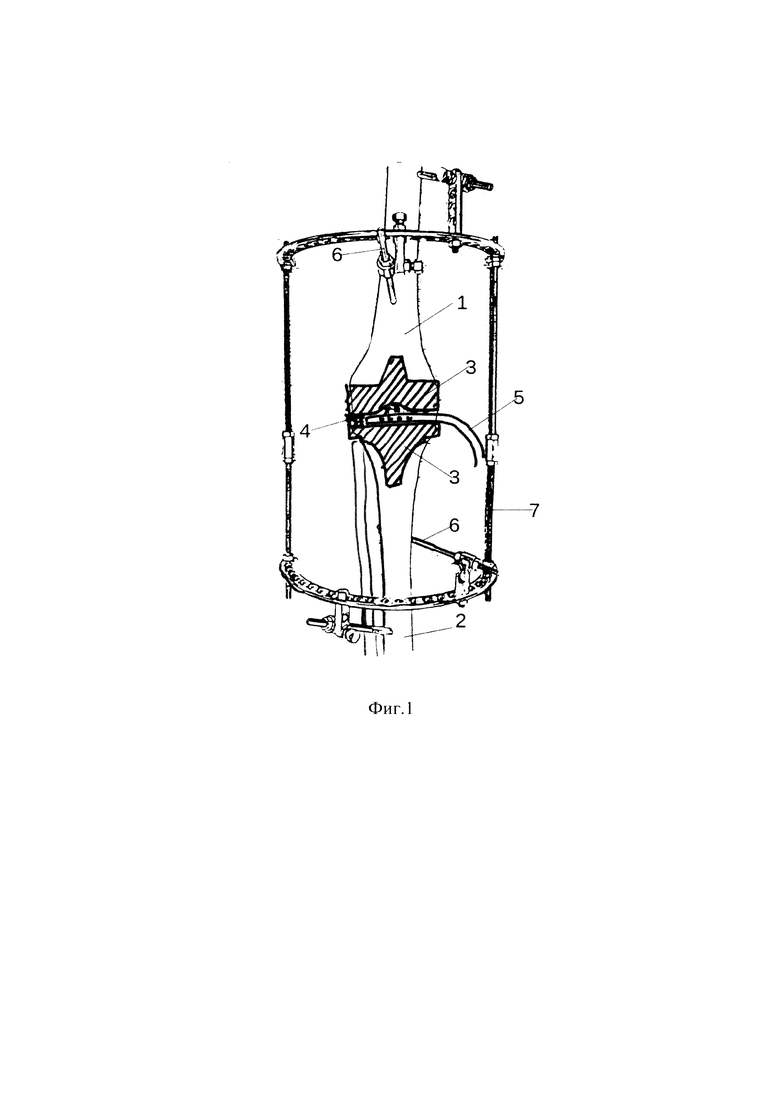
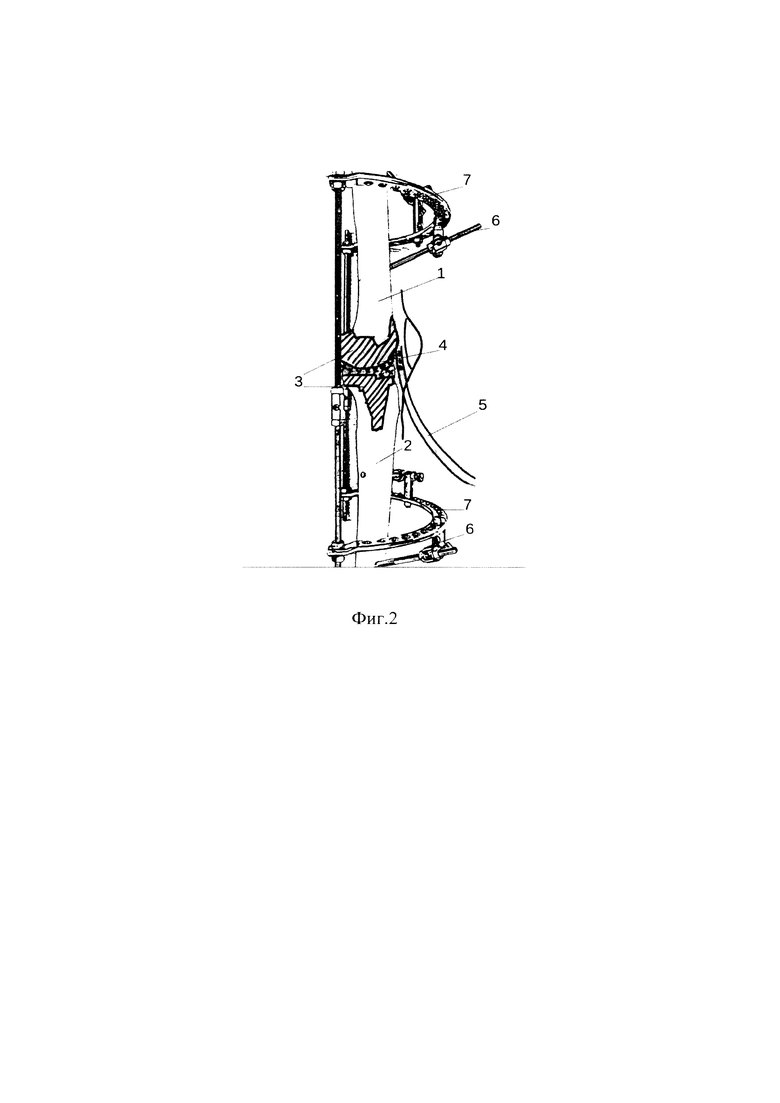
Изобретение поясняется чертежом, где на фиг. 1 - схема способа лечения параэндопротезной инфекции коленного сустава в прямой проекции, на фиг. - 2 схема способа лечения параэндопротезной инфекции коленного сустава в боковой проекции.
На чертеже приняты следующие обозначения: 1 - бедренная кость, 2 - большеберцовая кость, 3 - эндопротез, 4 - дренирующая губка, 5 - трубка к источнику отрицательного давления, 6 - стержень-шуруп, 7 - полукольца аппарата наружной фиксации
Осуществление изобретения.
Ниже представлено подробное описание способа: хирургическая обработка перипротезного гнойного очага, извлечение съемных элементов эндопротеза, некрэктомия, наложение аппарата наружной фиксации, дистракция компонентов эндопротеза, наложение вакуум-ассистированной повязки.
При осуществлении способа положение пациента на операционном столе лежа на спине. Операцию выполняют под эндотрахеальным наркозом или под комбинированной анестезией (+проводниковая анестезия глубокая или поверхностная). Оперируемую конечность обрабатывают от верхней границы мезогастрия до стопы 3-х кратно раствором антисептика. Нижняя конечность согнута в коленном суставе под углом 120 градусов, не ротирована. Под коленом для фиксации конечности в данном положении укладывают поперечный валик. Асептические условия операционного поля достигаются путем обкладывания операционного поля комплектом стерильного операционного белья от средней 1/3 бедра до лодыжки. Позиция и высота операционного стола установлена в соответствии с оптимальным фокусным расстоянием для хирурга.
Полностью иссекают послеоперационный рубец передней поверхности коленного сустава, отступя 0,5 см от его края в пределах кожи и подкожной клетчатки. Длина операционного разреза определяется длиной послеоперационного рубца и, при необходимости дополнительной ревизии раны, может быть увеличена в проксимальном или дистальном направлении. Тупым и острым путем с удалением наложенных при протезировании сустава лигатур осуществляют широкий доступ к инфицированному эндопротезу. Края раны разводятся с помощью четырехзубых крючков, либо в рану устанавливается ранорасширитель. С помощью операционного отсоса эвакуируют экссудат из перипротезной полости. Выполнят забор материала (мазок из раны или биопсия) для бактериологического исследования. Производят первичную оценку состояния эндопротеза путем определения патологической подвижности его компонентов, наличия отделяемого и грануляционной ткани между элементами эндопротеза и прилегающей к ним костной тканью. При отсутствии признаков нестабильности эндопротеза и/или септической резорбции костной ткани принимают решение о возможности сохранения эндопротеза.
Извлечение съемных частей эндопротеза производят в зависмости от конструкции эндопротеза в соответствии с сопроводительной документацией, при необходимости используя специальные приспособления, входящие в комплектацию эндопротеза.
После извлечения съемных частей производят тщательную ревизию перипротезных мягких тканей, поступательно удаляя все некротизированные, нежизнеспособные и пропитанные гнойным экссудатом ткани. Возможно использование дополнительных физических методов хирургической обработки раны, таких как обработка низкочастотная ультразвуковая обработка раны через раствор антисептика, либо гидропрессивная обработка с использованием доступной аппаратуры. После выполнения радикальной некрэктомии, тщательного гемостаза с использованием электрокоагуляции и обильного (до 5 литров) промывания раневой полости растворами антисептиков, выполняют наложение аппарата внеочаговой фиксации в положении разгибания коленного сустава.
При монтаже аппарата применяют способ унифицированного обозначения чрескостного остеосинтеза (1). Это способ предполагает разделение каждого сегмента (в нашем случае бедро и голень) на 8 равных по длине частей - уровней, обозначаемых цифрами от I до VIII от проксимального к дистальному. Длина одного уровня равна 1/8 длине сегмента конечности. На каждом уровне расположение чрескостных элементов уточняют с помощью разделения поперечного сечения на 12 секторов по аналогии с циферблатом часов. Центр сечения соответствует центру поперечного сечения кости. Каждому сектору присвоен номер в соответствии с указанием часов таким образом, что сектор 12 часов всегда располагается кпереди, а сектор 3 часа всегда изнутри. На левой и правой конечности обозначения сечений зеркальны. Также дополнительно указывают угол установки чрескостного элемента по отношению к оси сегмента, а именно ее проксимальной части. Как правило, ограничиваются тремя вариантами: 90, 120 и 60 градусов.
Сначала монтируют модуль на голень. Полукольцо на уровне IV голени ориентируют перпендикулярно к оси голени. В соответствии с предполагаемым расположением одного из стержней-шурупов монтирую кронштейн с 3-4 отверстиями, к кронштейну монтируется муфта в направлении предполагаемой установки стержня шурупа. Сверлом 4.2 мм через муфту через проекционный разрез кожи 0,5 см формируют канал в кости, в который затем устанавливают стержень-шуруп диаметром 6 мм. Последний посредством ранее установленных кронштейна и муфты фиксируют к кольцу. Второй стержень-шуруп устанавливают аналогично. Всего на голени устанавливают два стержня-шурупа: на уровне III в положении 10 часов под углом 120 градусов и на уровне V в положении 2 часа под углом 60 градусов.
Затем монтируют модуль на бедро. Полукольцо на уровне V бедра ориентируют перпендикулярно к механической оси нижней конечности, а не к анатомической оси бедренной кости. Таким образом, полукольца модулей ориентируют параллельно друг к другу. В соответствии с предполагаемым расположением одного из стержней-шурупов монтируют кронштейн с 3-4 отверстиями, к кронштейну монтируют муфту в направлении предполагаемой установки стержня шурупа. Сверлом 4.2 мм через муфту через проекционный разрез кожи 0,5 см формируют канал в кости, в который затем устанавливают стержень-шуруп диаметром 6 мм. Для проведения этих манипуляций на бедре используют протекторы мягких тканей соответствующих размеров. Стержень шуруп посредством ранее установленных кронштейна и муфты фиксируют к кольцу. Второй стержень-шуруп устанавливают аналогично. Всего на бедре устанавливают два стержня-шурупа: на уровне IV в положении 10 часов под углом 120 градусов и на уровне VI в положении 12 часов под углом 60 градусов вне плоскости кольца. Модули аппарата соединяют резьбовыми стержнями, при необходимости с шарнирами.
После наложения аппарата производят дистракцию бедренной и большеберцовой костей для увеличения диастаза между деталями эндопротеза. Этот диастаз рыхло заполняется специальной полиуретановой губкой, используемой для проведения терапии раны локальным отрицательным давлением и, как правило, входящей в комплекты расходных материалов для проведения данного вида лечения. К дренирующей губке подводят перфорированную трубку из силиконовой резины и заклеивают специальной клеящей пленкой с захватом 3-4 см кожи от краев раны для создания герметичности. Трубку присоединяют к контейнеру для сбора экссудата, который, в свою очередь, присоединен к источнику дозированного отрицательного давления. Далее проводится лечение ран локальным отрицательным давлением с использованием постоянного или переменного режимов вакуум-терапии (возможно дополнительное использование инсталляционных методик терапии) с индивидуальным подбором параметров разрежения в соответствии с рекомендациями производителей оборудования.
Контроль за состоянием раны и элементов эндопротеза производят на 2-4 день при смене дренирующей полиуретановой губки. Срок до смены повязки зависит от динамики лабораторных показателей системного воспаления, количества и характера экссудата из раны.
После получения результатов бактериологического исследования и купирования клинических и лабораторных признаков хирургической инфекции в условиях операционной производят удаление дренирующей губки. После этого тщательно повторно оценивают состояние эндопротеза с целью обнаружения признаков нестабильности элементов эндопротеза, а также минимального гнойного отделяемого между элементами протеза и костной тканью. В этом случае сохранение протеза признается невозможным, производится его полное удаление с имплантацией антибактериального спейсера, либо выполняется компрессия бедренной и большеберцовой костей в аппарате наружной фиксации для формирования артродеза.
В случае отсутствия признаков септической нестабильности эндопротеза и купирования проявлений инфекции выполняют имплантацию новых съемных элементов эндопротеза (полиэтиленовых вкладышей), через контрапертуры в перипротезном пространстве устанавливают перфорированную дренажную трубку. Рану послойно ушивают с использованием биодеградируемого шовного материала толщиной 1-0 для восстановления целостности капсулы сустава, после чего демонтируют аппарат наружной фиксации, извлекают стержни-шурупы и накладывают асептические повязки на рану. В до и послеоперационном периоде проводят направленную антибиотикотерапию с учетом чувствительности выделенного штамма раневой микрофлоры. Дренажную трубку удаляют на 2-5 день в зависимости от количества и характера экссудата.
Пример реализации изобретения
Пациентка ФГС, 53 лет. Госпитализирована в ГКБ им. В.В. Виноградова с жалобами на боль в области коленных суставов, повышение температуры тела до 38,5 С в течение 3 суток. В анамнезе: по поводу двустороннего гонартроза выполнено тотальное эндопротезирование коленных суставов по R.Watson-Jones в сентябре 2014 справа, в апреле 2016 - слева. При осмотре: напряженный отек, гиперемия и флюктуация в области коленных суставов, боль при движениях. При обследовании: лейкоцитоз 14×109/л, палочкоядерный сдвиг формулы крови. Установлен диагноз: Поздняя параэндопротезная инфекция, перипротезные абсцессы коленных суставов. В экстренном порядке произведено вскрытие перипротезных абсцессов (100 мл гнойного экссудата справа, 130 мл слева). При ревизии признаков септической нестабильности эндопротезов не выявлено. Произведена хирургическая обработка, удаление полиэтиленовых вкладышей, наложены аппараты внешней фиксации для дистракции и иммобилизации фрагментов, наложены вакуум-ассистированные повязки с обеих сторон с переменными параметрами отрицательного давления, разрежения, 80-130 мм рт ст.(с учетом индивидуальных медицинских показателей пациентки (объема и характера раневого экссудата) с интервалом в 3 минуты.
При бактериологическом исследовании материала с поверхности протезов выявлен рост MRSA с обеих сторон. Проводилось лечение ран с использованием вакуум-ассистированных повязок. После получения результатов бактериологического исследования произведена смена стартовой схемы антибактерильной терапии (цефазолин 1,0×2 в/м) на ванкомицин 1,0×2 р в/в с учетом чувствительности выделенной микрофлоры. После купирования клинических и лабораторных признаков воспаления 31.10.2016 произведена реимплантация вкладыша справа, демонтаж аппарата наружной фиксации, наложение вторичных швов. Послеоперационный период протекал без осложнений. Слева сохранялось гнойное отделяемое, при очередной смене повязки выявлены признаки септической нестабильности эндопротеза. 23.11.2016 выполнено удаление эндопротеза, имплантация спейсера с ванкомицином. Рана зажила, однако 09.12.2016 отмечено нарастание признаков воспаления. При пункции получено гнойное отделяемое. Инфицированный спейсер удален, по требованию больной от дальнейших попыток репротезирования решено воздержаться. Выполнен артродез в аппарате наружной фиксации. Достигнута консолидация с формированием стабильного артродеза.
Отдаленный результат прослежен в течение 2 лет. Рецидива параэндопротезной инфекции справа не отмечено, функция эндопротеза полностью восстановлена. Слева: артродез сформирован, опороспособность конечности восстановлена.
Таким образом, предложенный способ лечения параэндопротезной инфекции коленного сустава позволяет расширить арсенал средств лечения, повысить эффективность лечения за счет снижения риска вторичного инфицирования раны госпитальной инфекцией и повышения вероятности успешного купирования инфекции без удаления эндопротеза.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ хирургического лечения перипротезной инфекции крупных суставов с использованием препарата с бактериофагами "Фагодент" и вакуумного дренирования продуктов воспаления | 2017 |
|
RU2676401C2 |
| Способ хирургического лечения перипротезной инфекции крупных суставов с использованием поливалентного бактериофага фагодерм и вакуумного дренирования продуктов воспаления | 2016 |
|
RU2631052C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ ПОСЛЕ ЭНДОПРОТЕЗИРОВАНИЯ СУСТАВА | 2019 |
|
RU2712806C1 |
| Способ подготовки инфицированной периартикулярной раны для имплантации постоянного или временного стабилизирующего устройства | 2018 |
|
RU2712013C1 |
| Способ органосохраняющего лечения акушерского перитонита после абдоминальных родов с использованием вакуум-ассистированной лапаростомии | 2023 |
|
RU2816058C1 |
| Способ изготовления спейсера тазобедренного сустава при неопороспособной вертлужной впадине | 2017 |
|
RU2675551C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ИНФЕКЦИОННОЙ КОНТАМИНАЦИИ СУСТАВА У БОЛЬНЫХ С СЕПТИЧЕСКИМ АРТРИТОМ И ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ | 2018 |
|
RU2695818C1 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННОГО СТЕРНОМЕДИАСТИНИТА У КАРДИОХИРУРГИЧЕСКИХ БОЛЬНЫХ С ИСПОЛЬЗОВАНИЕМ АППАРАТНЫХ ВАКУУМ-АССИСТИРОВАННЫХ ПОВЯЗОК В СОЧЕТАНИИ С ПАРАВУЛЬНАРНЫМ И ПЕРОРАЛЬНЫМ ВВЕДЕНИЕМ БАКТЕРИОФАГОВ | 2020 |
|
RU2746975C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЛЕЧЕНИЯ БОЛЬНЫХ С ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ | 2016 |
|
RU2640391C1 |
| Способ лечения пациентов с хронической рецидивирующей перипротезной инфекцией тазобедренного сустава, обусловленной резистентными к антибиотикам микрорганизмами | 2020 |
|
RU2735651C1 |
Изобретение относится к области медицины, а именно к гнойной хирургии и травматологии-ортопедии, и может быть использовано для лечения параэндопротезной инфекции коленного сустава. Проводят ревизию пораженного сустава, радикальную хирургическую обработку очага инфекции, после выполнения которой производят извлечение съемных элементов эндопротеза. Выполняют наложение аппарата наружной фиксации, дистракцию оставшихся компонентов эндопротеза. Проводят заполнение перипротезной полости дренирующей губкой и лечение раны локальным отрицательным давлением в пределах 80-150 мм рт.ст. с отсроченным наложением швов на рану после купирования явлений воспаления и получения результатов бактериологического исследования. Способ обеспечивает повышение снижения риска вторичного инфицирования раны госпитальной инфекцией и повышение вероятности успешного купирования инфекции без удаления эндопротеза за счет особенностей выполнения при воздействии отрицательным давлением. 2 ил., 1 пр.
Способ лечения параэндопротезной инфекции коленного сустава, включающий ревизию пораженного сустава, радикальную хирургическую обработку очага инфекции, после выполнения которой производят извлечение съемных элементов эндопротеза, наложение аппарата наружной фиксации, дистракцию оставшихся компонентов эндопротеза, заполнение перипротезной полости дренирующей губкой и лечение раны локальным отрицательным давлением в пределах 80-150 мм рт.ст. с отсроченным наложением швов на рану после купирования явлений воспаления и получения результатов бактериологического исследования.
| Способ лечения перипротезной инфекции при эндопротезировании коленного сустава | 2020 |
|
RU2725272C1 |
| Способ хирургического лечения перипротезной инфекции крупных суставов с использованием препарата с бактериофагами "Фагодент" и вакуумного дренирования продуктов воспаления | 2017 |
|
RU2676401C2 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С ПАРАПРОТЕЗНОЙ ИНФЕКЦИЕЙ ТАЗОБЕДРЕННОГО СУСТАВА | 2013 |
|
RU2526956C1 |
| РАНЕВАЯ ПОВЯЗКА | 2011 |
|
RU2573816C2 |
| Способ хирургического лечения перипротезной инфекции крупных суставов с использованием поливалентного бактериофага фагодерм и вакуумного дренирования продуктов воспаления | 2016 |
|
RU2631052C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ РАН | 2021 |
|
RU2760088C1 |
| Цветков В.О | |||
| и др | |||
| Сохранение функционирующих медицинских имплантатов при параэндопротезной инфекции: взвешенный подход и современные возможости | |||
| В кн.: ИННОВАЦИОННЫЕ ТЕХНОЛОГИИ В | |||
Авторы
Даты
2023-07-14—Публикация
2022-04-25—Подача