Изобретение относится к области фармацевтики и может быть использовано для терапии патологий печени у животных.
Из проведенного информационного поиска известен силимарин, являющийся действующим компонентом многих препаратов, используемых для лечения и профилактики заболеваний печени, например, таких как Карсил (синонимы: Левасил, Гепарсил, Легалон, Силибор, Силимарин Гексал) - см.. Лекарственные средства. - М., издание пятнадцатое, Новая волна, 2005, т. 1. с. 526-527 - или Дарсил - см. Дарсил инструкция по применению - Каталог лекарств - адрес в: http://vapteke.com.ua/drugs/darsil.darnitsa.php.
Однако известные лекарственные препараты выпускаются в виде таблеток, гранул, драже или капсул, предназначены для перорального введения, обладают низкой терапевтической активностью, а также наличием различного рода побочных эффектов. Так, Карсил содержит лактозу и поэтому надлежит соблюдать осторожность при назначении его пациентам с глюкозы-галактозы, глюкозо-изомальтозным дефицитом. Входящий в состав продукта сорбитол может вызывать расстройство стула и гастропатию (см. Григорьев П.Я. и др. Диагностика и лечение и. - Советская медицина, 1985, №12, с. 61-67 или Блинков И.Л. и др.).
Ближайшими аналогами разрабатываемых форм являются наночастицы селена, несущие силимарин, приготовленные с использованием цистеина (Патент RU 2504347, МПК A61D 7/00, опубл. 20.01.14, Бюл. №2), содержащая силимарин, органический растворитель, солюбилизатор, консервант и сорастворитель при следующем соотношении компонентов, мас. %:
Кроме того, в качестве органического растворителя содержит диметилацетамид или 1-метил-2-пирролидон, или солюфор Р, или транскутол, или пропиленгликоль, или этиленгликоль, или глицероформаль, или диметилсульфоксид, в качестве солюбилизатора содержит кремофор EL или кремофор ELP, или кремофор RH40, или твин 80, или солютол HS15, в качестве консерванта содержит бензиловый спирт или парабены, в качестве сорастворителя содержит дистиллированную воду или раствор смеси водорастворимых витаминов, в качестве раствора смеси водорастворимых витаминов содержит витамины В1 тиамин, В2 рибофлавин, В3 (РР) никатинамид, В4 холин, В5 пантатеновую кислоту, В6 пиридоксин, В7(Н) биотин, В8 инозит, В9 фолиевую кислоту, В10-n-аминобензойную кислоту, В11 левокарнитин, В12 цианкобаламин, В13 оротовую кислоту, В15 пангамовую кислоту, В17 амигдалин, С аскорбиновую кислоту, взятые в равных соотношениях, дополнительно содержит жирорастворимые витамины А или Д, или Е, или F в количестве 1-10 мас. %, дополнительно содержит эссенциальные фосфолипиды в количестве 0,1-10 мас. %, дополнительно содержит метионин в количестве 0,1-10 мас. %.
Задачей изобретения является разработка стабильной инъекционной формы лекарственного средства, содержащего силимарин и коньюгат селена с соком алоэ, которая позволит повысить его биодоступность, усилить противовоспалительное действие, поддержать метаболические функции печени и снизить побочные эффекты.
Поставленная задача решается тем, что инъекционная лекарственная форма для лечения и профилактики заболеваний печени у животных содержит силимарин, коньюгат селена с соком алоэ, что усиливает противовоспалительное действие и нормализует метаболические функции.
Техническим результатом заявленного изобретения является получение стабильной инъекционной формы силимарина с коньюгатом селена с соком алоэ с достаточно низкой вязкостью, что позволяет снизить болезненность инъекции.
Инъекционная форма стабильна, нетоксична, не обладает местным раздражающим и аллергизирующим свойствами, позволит повысить биодоступность силимарина, усилить противовоспалительное действие и снизить побочные эффекты.
В качестве исходного метода приготовления селеновых наночастиц с компонентами сока алоэ был избран метод восстановления селенистой кислоты аскорбиновой кислотой.
Изобретение характеризуется следующим примером:
Пример 1. Получение инъекционной лекарственной формы для лечения и профилактики заболеваний печени у животных. Лекарственное средство получают путем смешивания расчетных количеств входящих в его состав компонентов в условиях постоянного термостатирования при температуре 45°С.
Для приготовления конъюгатов селена была использована одна аликвота сока, хранившаяся при -20 град С. рН сока был доведен до 9,0 с помощью 1М гидроксида натрия.
К 100 мл сока на магнитной мешалке добавляли 1 мл 0,1M селенистой кислоты, через минуту перемешивания внесено 33 мл 57 мМ L-цистеина. Практически сразу (в течение 1-2 минут) происходила смена цвета реакционной смеси с желтой до светло-красной, далее не менявшейся при перемешивании. Реакционную смесь ставили на мешалку на 10 минут, далее разливали по пузырькам и хранили при 4 град С.
Пример 2.
Инъекционная лекарственная форма для лечения и профилактики заболеваний печени у животных, отличающаяся тем, что содержит силимарин, стабилизатор силимарина - янтарную, или фумаровую, или яблочную, или лимонную, или щавелевую кислоты, селенистую кислоту, L-цистеин, коньюгаты коллоидов селена с соком листьев алоэ, стабилизатор рН - аскорбиновая кислота, при следующем соотношении компонентов, масс. %:
Силимарин - 0,5-3
Селенистая кислота - 0,01-0,1
Аскорбиновая кислота - 0,4
L-цистеин - 0,3-3,3
Депротеинизированный сок алоэ - 0,4-4
Стабилизатор для силимарина - 0,4-2,0
Дистиллированная вода - до 100.
Пример 3.
Инъекционная лекарственная форма для лечения и профилактики заболеваний печени у животных, отличающаяся тем, что содержит силимарин, стабилизатор силимарина - янтарную, или фумаровую, или яблочную, или лимонную, или щавелевую кислоты, селенистую кислоту, L-цистеин, коньюгаты коллоидов селена с соком листьев алоэ, стабилизатор рН - аскорбиновая кислота, при следующем соотношении компонентов, масс. %:
Силимарин - 0,5-3
Селенистая кислота - 0,01-0,1
Аскорбиновая кислота - 4
L-цистеин - 0,3-3,3
Депротеинизированный сок алоэ - 2
Стабилизатор для силимарина - 0,4-2,0
Дистиллированная вода - до 100.
Увеличение содержания аскорбиновой кислоты приводило к уменьшению устойчивости препарата и его расслаиванию.
Пример 4.
Инъекционная лекарственная форма для лечения и профилактики заболеваний печени у животных, отличающаяся тем, что содержит силимарин, стабилизатор силимарина - янтарную, или фумаровую, или яблочную, или лимонную, или щавелевую кислоты, селенистую кислоту, L-цистеин, коньюгаты коллоидов селена с соком листьев алоэ, стабилизатор рН - аскорбиновая кислота, при следующем соотношении компонентов, масс. %:
Силимарин - 0,5-3
Селенистая кислота - 0,01-0,1
Аскорбиновая кислота - 0,4-4
L-цистеин - 0,3-3,3
Депротеинизированный сок алоэ - 4
Стабилизатор для силимарина - 0,4-2,0
Дистиллированная вода - до 100.
Увеличение содержания в препарате сока алоэ приводило к ухудшению физико-химических характеристик препарата, его неоднородности и расслаивания.
1) Полученный раствор характеризуется следующими показателями:
1. ρ=1,035 г/мл (плотность при 28°С).
2. η=2,038 (относительная вязкость).
3. абсолютная вязкость 1,706 мПа*с, при 28°С.
4. рН 5,13.
2) Изучение аллергического действия препарата. Для изучения аллергического действия препарата двум кроликам массой тела ~5 кг, ввели внутримышечно по 0,1 мл (1 мг/кг по ДВ) препарата, полученного по примеру 1 - концентрация силимарина в препарате 50 г/л.
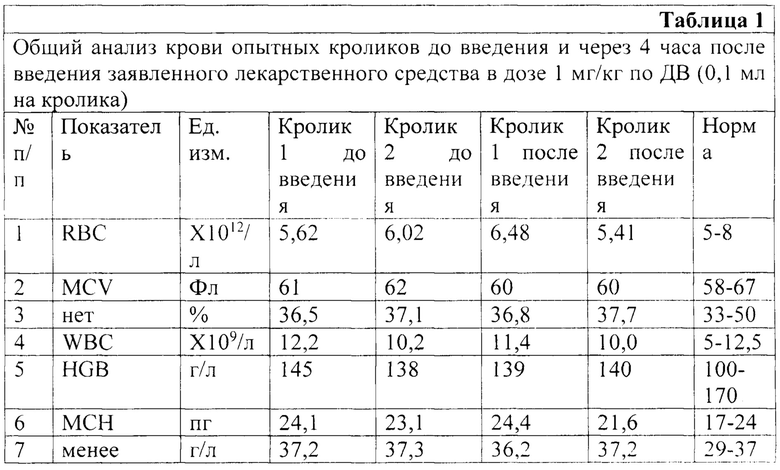
До введения препарата произвели забор крови для (OAK) - с антикоагулянтом и для биохимического анализа крови (БАК). На месте введения препарата - область бедра левой задней конечности - выстригли. Через 4 часа повторно взяли кровь для OAK и БАК. На месте инъекции в первые 4 часа после введения препарата кожных реакций не отмечалось, уплотнения, припухания и другие изменения отсутствовали. В таблице 1 представлен общий анализ крови опытных кроликов до введения и через 4 часа после введения заявленного лекарственного средства в дозе 1 мг/кг по ДВ (0,1 мл на кролика).
Из приведенных данных видно, что после инъекции препарата резких изменений показателей крови не наблюдалось, они колебались в пределах физиологической нормы.
3) Изучение местного раздражающего действия заявленного лекарственного средства.
Для изучения местного раздражающего действия препарата проводили конъюнктивальную пробу.
Опыт по определению раздражающего действия препарата на слизистые оболочки ставили на кроликах. В коньюнктивальный мешок левого глаза закапывали по 2 капли полученного препарата, в коньюнктивальный мешок правого глаза аналогично закапывали по 2 капли физиологического раствора. После инсталляции препарата в коньюнктивальный мешок - кроликам через 5 мин, через 24 и 48 ч покраснение конъюнктивы и истечение экссудата у всех кроликов не наблюдалось. Роговица глаза прозрачная, гладкая, без изъязвлений и помутнения.
Контрольное введение также было отрицательным (2 капли физиологического раствора натрия хлорида в коньюнктивальный мешок правого глаза).
Вывод: препарат не обладает местным раздражающим и аллергизирующим свойствами.
4) Определение острой токсичности полученного препарата.
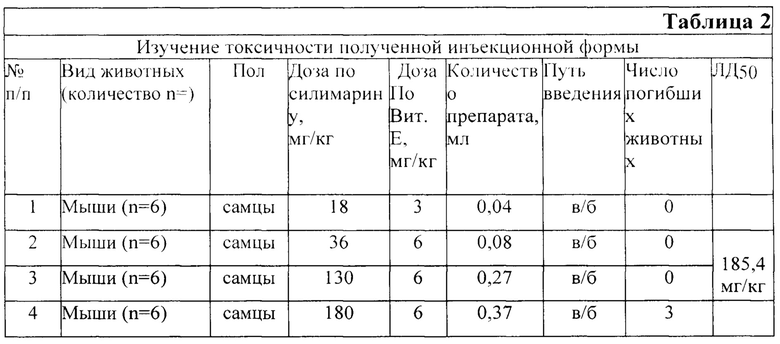
Для определения острой токсичности был использован препарат, полученный по примеру 1. Данные токсичности полученной инъекционной формы приведены в таблице 2.
Все мыши после введения препарата в дозах по силимарину с селеном и соком алоэ соответственно 18 и 36 мг/кг живой массы остались живы. Токсических явлений не отмечалось.
Таким образом, получена стабильная инъекционная форма лекарственного средства, содержащего силимарин. Инъекционная форма нетоксична, не обладает местным раздражающим и аллергизирующим свойствами, позволит усилить противовоспалительное действие, биодоступность силимарина и снизить побочные эффекты.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ПЕЧЕНИ У ЖИВОТНЫХ | 2012 |
|
RU2504347C1 |
| Гепатопротекторная инъекционная фармацевтическая композиция на основе силимарина и наночастиц селена | 2017 |
|
RU2645092C1 |
| ЗУБНОЙ ТРАНСДЕРМАЛЬНЫЙ ЭЛИКСИР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2327445C1 |
| ФАРМАЦЕВТИЧЕСКАЯ ГЕПАТОПРОТЕКТОРНАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2391989C2 |
| ГЕПАТОПРОТЕКТОРНАЯ И АНТИГЕПАТОТОКСИЧЕСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПЕЧЕНИ, ВКЛЮЧАЮЩИЙ ВВЕДЕНИЕ УКАЗАННОЙ КОМПОЗИЦИИ | 2008 |
|
RU2381800C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СУЛЬФОРАФАН ИЛИ ПРЕДШЕСТВЕННИК СУЛЬФОРАФАНА И ЭКСТРАКТ ИЛИ ПОРОШОК МОЛОЧНОГО ЧЕРТОПОЛОХА | 2013 |
|
RU2785683C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СУЛЬФОРАФАН ИЛИ ПРЕДШЕСТВЕННИК СУЛЬФОРАФАНА И ЭКСТРАКТ ИЛИ ПОРОШОК МОЛОЧНОГО ЧЕРТОПОЛОХА | 2013 |
|
RU2666953C2 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ У ЖИВОТНЫХ | 2010 |
|
RU2455999C2 |
| Композиция для инъекционного применения на основе фосфотидилхолина, метионина, витамина Е и селенита натрия - "Гепарс", обладающая гепатопротекторными свойствами, и способ ее получения | 2020 |
|
RU2760685C1 |
| Способ приготовления комплексного гелеобразного препарата для лечения и профилактики мастита у коров и комплексный гелеобразный препарат на его основе | 2015 |
|
RU2624868C2 |
Настоящее изобретение относится к области фармацевтики, а именно к ветеринарии, и раскрывает инъекционную лекарственную форму для лечения и профилактики заболеваний печени у животных, содержащую силимарин, стабилизатор силимарина - янтарную, или фумаровую, или яблочную, или лимонную, или щавелевую кислоты, селенистую кислоту, L-цистеин, коньюгаты коллоидов селена с соком листьев алоэ, стабилизатор рН - аскорбиновую кислоту, при следующем соотношении компонентов, мас.%: Силимарин - 0,5-3; Селенистая кислота - 0,01-0,1; Аскорбиновая кислота - 0,4-4; L-цистеин - 0,3-3,3; Сок алоэ - 0,4-4; Стабилизатор для силимарина - 0,4-2,0; Дистиллированная вода - до 100. Техническим результатом изобретения является стабильность получаемой инъекционной формы, которая нетоксична, не обладает местным раздражающим и аллергизирующим свойствами, позволяет повысить биодоступность силимарина, усилить противовоспалительное действие и снизить побочные эффекты. 2 табл., 4 пр.
Инъекционная лекарственная форма для лечения и профилактики заболеваний печени у животных, содержащая силимарин, стабилизатор силимарина - янтарную, или фумаровую, или яблочную, или лимонную, или щавелевую кислоты, селенистую кислоту, L-цистеин, коньюгаты коллоидов селена с соком листьев алоэ, стабилизатор рН - аскорбиновую кислоту, при следующем соотношении компонентов, мас.%:
Силимарин - 0,5-3
Селенистая кислота - 0,01-0,1
Аскорбиновая кислота - 0,4-4
L-цистеин - 0,3-3,3
Сок алоэ - 0,4-4
Стабилизатор для силимарина - 0,4-2,0
Дистиллированная вода - до 100.
| Гепатопротекторная инъекционная фармацевтическая композиция на основе силимарина и наночастиц селена | 2017 |
|
RU2645092C1 |
| VARLAMOVA EG et al | |||
| Therapeutic Potential and Main Methods of Obtaining Selenium Nanoparticles, Int J Mol Sci, 22 (19): 10808, 2021, Published online: 6 Oct 2021, doi: 10.3390/ijms221910808, pp.1-25 | |||
| B | |||
| FARDSADEGH et al | |||
| Aloe vera leaf extract mediated green synthesis of selenium nanoparticles and assessment of their In | |||
Авторы
Даты
2023-07-19—Публикация
2021-12-16—Подача