Настоящее изобретение относится к области фармации, а именно к созданию новых форм лекарственных препаратов, в частности касается лекарственной формы эхинохрома А в виде микро-/нановолокон, полученных из разрешенных в фармацевтике полимеров, содержащих эхинохром А. Изобретение может найти применение в медицине и обеспечит контролируемое и пролонгированное высвобождение эхинохрома А, его адресную доставку к очагу патологического процесса.
Сотрудниками Тихоокеанского института биоорганической химии имени Г. Б. Елякова Дальневосточного отделения Российской академии наук разработан антиоксидантный лекарственный препарат Гистохром, применяемый в кардиологии для лечения ишемической болезни сердца и ограничения зоны некроза при инфаркте миокарда (номер государственной регистрации Р N002363/01) и в офтальмологии для лечения дистрофических заболеваний сетчатки и роговицы, первичной открытоугольной глаукомы, диабетической ретинопатии сетчатки, кровоизлияний в стекловидное тело, сетчатку (номер государственной регистрации Р N002363/02). Уникальность гистохрома заключается в том, что он одновременно блокирует ряд звеньев свободнорадикальных реакций: нейтрализует активные формы кислорода (АФК), оксид азота и пероксидные радикалы, хелатирует ионы металлов, ингибирует перекисное окисление липидов, регулирует уровни антиоксидантных ферментов.
Активной субстанцией препарата гистохром является пигмент морских ежей эхинохром А (7-этил-2,3,5,6,8-пентагидрокси-1,4-нафтохинон), МНН: пентагидроксиэтилнафтохинон, номер государственной регистрации Р N002362/01.
В последнее десятилетие исследование свойств эхинохрома А привлекло внимание ученых многих стран, о чем свидетельствует рост количества публикаций о механизмах действия эхинохрома А [Kim H. K. et al. Multifaceted Clinical Effects of Echinochrome // Mar. Drugs 2021, 19 (8), 412]. В частности, были детально исследованы механизмы его антиоксидантного и кардиопротекторного действия [Jeong S.H. et al. Echinochrome A protects mitochondrial function in cardiomyocytes against cardiotoxic drugs // Mar. Drugs. - 2014. - Vol. 12, N 5. - P. 2922-2936.], обнаружен положительный эффект его применения при ишемическом и геморрагическом инсульте [Kim R. et al. Echinochrome A attenuates cerebral ischemic injury through regulation of cell survival after middle cerebral artery occlusion in rat // Mar. Drugs. - 2019. - Vol. 17, N 9. - P. 501], при болезни Альцгеймера [Lee S.R. et a. Acetylcholinesterase inhibitory activity of pigment echinochrome A from sea urchin Scaphechinus mirabilis // Mar. Drugs. - 2014. - Vol. 12, N 6. - P. 3560-3573.] и диабете [Soliman A.M. et al. Comparative study between the hypoglycemic and antioxidant effects of echinochrome on type 1 and type 2 diabetes mellitus // Research & Reviews: Research Journal of Biology. - 2016. - Vol. 4, N 3. - P. 1-9.]; обнаружены противовирусные [Fedoreyev S.A. et al. Antiviral and Antioxidant Properties of Echinochrome A // Mar. Drugs. - 2018. - Vol. 16 (12). - P. 509.] и противовоспалительные свойства [Lennikov A. et al. Amelioration of endotoxin-induced uveitis treated with the sea urchin pigment echinochrome in rats //Mol. Vis. - 2014. - Vol. 20. - P. 171-177.].
Показано, что применение эхинохрома А в комплексной терапии эрозивного гастродуоденита у подростков способствует ускорению процессов заживления эрозивных дефектов за счет активации локальной эндогенной антиоксидантной защиты [Ануфриева А.В. и др. Влияние эхинохрома А на биогенез свободных радикалов в слизистой оболочке желудка у подростков с эрозивным гастродуоденитом // Дальневосточный медицинский журнал, 2012, №1, 78-81.].
Показан терапевтический потенциал эхинохрома А при воспалительных заболеваниях кишечника с использованием модели экспериментального колита у мышей [Oh S. J. et al. Echinochrome A Reduces Colitis in Mice and Induces In Vitro Generation of Regulatory Immune Cells // Mar. Drugs. - 2019. - Vol. 17, N 11. - P. 622]. Внутривенное введение эхинорома А значительно предотвращает потерю массы тела и последующую летальность у мышей, вызванную колитом, способствует уменьшению воспаления и инициирует восстановление тканей.
В связи с большим разнообразием проявляемых эхинохромом А активностей с установленным механизмом действия, разработка новых лекарственных форм на его основе представляется перспективной задачей. Так как гистохром Однако, являясь зарегистрированным и успешно применяемым препаратом без выявленных негативных побочных эффектов, гистохром выпускается только в форме раствора для инъекций. Поэтому создание таблеток, капсул, глазных капель, ожого- и ранозаживляющих плёнок позволит значительно расширить границы применения препаратов эхинохрома А для лечения и комплексной терапии целого ряда социально-значимых заболеваний, таких как сердечно-сосудистые, офтальмологические и нейродегенеративные заболевания, диабет 1 и 2 типов, воспалительные заболевания легких, желудка и кишечника, и других болезней, связанных с развитием окислительного стресса в организме.
Большинство неудач в разработке новых лекарств обычно связаны с плохой растворимостью активного ингредиента в воде и низкой стабильностью его растворов. Плохая растворимость может привести к низкой биодоступности, и, как следствие, к неоптимальной доставке лекарств и их низкой эффективности. Около 40% существующих на рынке лекарств и почти 90% молекул-кандидатов в лекарственные средства плохо растворимы в воде [Kalepu S. et al. Insoluble drug delivery strategies: review of recent advances and business prospects // Acta Pharmaceutica Sinica B. - 2015. - Vol. 5, N 5. - P. 442-453.].
Поскольку эхинохром А практически нерастворим в воде, были предприняты попытки увеличить его растворимость и эффективность.
Известно кардиопротекторное средство на основе эхинохрома А, представляющее собой водный раствор эхинохрома А в молекулярно капсулированной форме в виде водорастворимого ассоциата с дифильным поверхностно-активным веществом, имеющим значение гидрофильно-липофильного баланса в диапазоне 12-18, и способ его получения. Показано, что молекулярные ассоциаты, полученные по такому способу, легко растворимы в воде с образованием стабильных растворов. Это делает возможным создание кардиопротекторных водных препаратов на основе эхинохрома А в виде концентрированных растворов или водорастворимых мазевых и таблетированных готовых форм, а также комплексных препаратов за счет обогащения дополнительно введенными компонентами через гидрофобную и/или водную фазу, увеличивая их биодоступность и биоэффективность [RU2500396 C2, 10.12.2013].
Создан водорастворимый комплекс включения бета-циклодекстрин-гистохром при молярном соотношении компонентов от 1:1 до 3:1 [RU2530886 C1, 20.10.2014]. Формирование комплекса и его структура подтверждены с помощью метода ЯМР и молекулярного моделирования. Комплекс бета-циклодекстрин-гистохром 1:2 обладал пролонгированной антиоксидантной активностью на модели перекисного окисления липидов.
Известна композиция антиоксидантов, пригодная для перорального применения в терапии воспалительного процесса в легких, содержащая эхинохром А, аскорбиновую кислоту, α-токоферола ацетат, микрокристаллическую целлюлозу, кремния диоксид коллоидный (Аэросил) и магния стеарат, причем компоненты в композиции находятся в определенном соотношении, в мас. % [RU2684783 C1, 15.04.2019]. Изобретение обеспечивает получение биодоступной, полностью растворимой в желудке антиоксидантной композиции, пригодной для приготовления пероральных лекарственных препаратов в таблетированной или капсулированной форме. Экспериментально показано, что активные компоненты композиции полностью переходят в течение 20 минут в раствор соляной кислоты, имитирующей желудочный сок (рН 1,2). Подтверждена стабильность заявляемой композиции, а именно определено, что активные компоненты сохраняются без изменения в течение 12 месяцев.
В качестве прототипа выбрана лекарственная форма гистохрома для перорального введения и пролонгированного действия, представляющая собой водорастворимый комплекс каррагинан-гистохром, характеризующийся весовым соотношением указанных компонентов 5:1 [RU2651042 С1, 18.04.2018]. Заявляемый комплекс предотвращает окисление гистохрома кислородом воздуха, сохраняет его антиоксидантные, кардиопротекторные свойства и проявляет пролонгированное гастропротекторное действие. Для получения указанного комплекса к водному раствору каррагинана прибавляют расчетное количество стокового спиртового раствора гистохрома, полученный раствор перемешивают при температуре 37°C в течение 60 мин. Включение эхинохрома А в каррагинановые матрицы повышало его стабильность и растворимость в водной среде. Показано, что гистохром на 10-20 % медленнее высвобождается из комплексов, чем из водного раствора, что обеспечивает его пролонгированное действие.
Недостатками известной лекарственной формы гистохрома является её непродолжительная стабильность (60 часов), незначительное пролонгированное действие и отсутствие возможности направленной доставки.
Задача изобретения - расширение арсенала лекарственных форм эхинохрома А, применение которой обеспечит адресную доставку действующего вещества, его контролируемое и пролонгированное высвобождение.
Задача решена созданием новой лекарственной формы эхинохрома А, которая, согласно изобретению, представляет собой микро-/нановолокна одного или более биосовместимых полимеров, обладающих разной гидрофильностью и чувствительностью к рН биологических сред, содержащих эхинохром А от 5 до 30 мас. %, изготовленная путем электроспиннинга совместного раствора одного или более биосовместимых полимеров и эхинохрома А.
Технический результат, обеспечиваемый изобретением, заключается в повышении стабильности эхинохрома А в заявляемой лекарственной форме. Препарат остается стабильным в полимерных матрицах не менее двух лет, что значительно дольше, чем в известных лекарственных формах (например, стабильность прототипа - водорастворимого комплекса каррагинан-гистохром составляет 60 часов). В отличие от прототипа изобретение обеспечивает контролируемое и более длительное пролонгированное высвобождение эхинохрома А и возможность его адресной доставки.
Изобретение позволяет формировать пленки из нановолокон различной природы и химического состава.
Заявляемая лекарственная форма эхинохрома А содержит разрешенные в фармацевтике биосовместимые полимеры, которые выбирают из группы синтетических, таких как поливинилпирролидон, поликапролактон, полиэтиленоксид, ацетилцеллюлоза, метилоксипропилцеллюлоза, полиэтиленгликоль, и/или из группы природных, таких как ульван, альгинат, желатин, гиалуроновая кислота, фиброин шелка, гликозаминогликан, хитозан.
Выбор полимеров, используемых в качестве носителей эхинохрома А, может влиять на архитектуру микро-/нановолоконных матриц и, в свою очередь, на эффективность инкапсуляции и профиль высвобождения, что позволяет изготавливать микро-/нановолоконные матрицы в соответствии с желаемыми спецификациями/свойствами для различных путей введения и различных терапевтических мишеней с возможностью адресной доставки эхинохрома А.
Например, когда эхинохром А должен высвобождаться в желудке (рН < 2,0), следует выбирать полимеры, растворимые в кислой среде, и смешивать их с полимерами с переменной растворимостью для достижения различных профилей высвобождения. Напротив, когда эхинохром А должен высвобождаться в двенадцатиперстной кишке (pH 5,6-8,0) или в тонком кишечнике (pH 7,2-7,5), следует выбирать полимеры, не растворимые при кислых pH, но растворимые при нейтральном или щелочном pH, и смешивать их с полимерами переменной растворимости для достижения пролонгированного профиля высвобождения.
Таким образом, используемые биосовместимые полимеры обладают разной гидрофильностью и чувствительностью к рН биологических сред, так что заявляемая лекарственная форма обеспечивает контролируемое высвобождение и/или адресную доставку эхинохрома А в биологических средах с различным рН.
Способ получения заявляемой лекарственной формы эхинохрома А заключается в том, что растворяют один или более биосовместимых полимеров в органических растворителях при комнатной температуре при перемешивании в течение 24 ч с получением прядильных растворов, затем добавляют к раствору полимера эхинохром А в таком количестве, чтобы получить общую концентрацию эхинохрома А в матрице, равную 5-30 мас. % (к массе матрицы) с последующим проведением электроспиннинга совместного раствора одного или более биосовместимых полимеров и эхинохрома А с получением на поверхности коллектора микро-/нановолокон в сухом состоянии.
Обнаружено, что при изготовлении микро-/нановолокон путем электроспиннинга совместного раствора эхинохрома А и указанных полимеров, содержание эхинохрома А должно составлять от 5 до 30 мас. % (к массе матрицы). Приготовление микро-/нановолокон с меньшим содержанием эхинохрома А (менее 5%) нецелесообразно с точки зрения дозировки лекарственной формы, а с большим (более 30%) - невозможно, поскольку при этом не формируются однородные матрицы при электроспиннинге.
Указанную лекарственную форму для терапевтического применения готовят в твердой форме или жидкой суспензии в фармацевтически приемлемом разбавителе. Универсальность материалов, полученных электроспиннингом, позволяет использовать их для приготовления таблеток или капсул, глазных капель, пленок и перевязывающих материалов. Эти препараты можно вводить любым подходящим способом введения. В предпочтительном варианте осуществления путь введения заявляемой лекарственной формы является пероральным, однако также может быть местным, трансдермальным, трансбуккальным, назальным, ректальным или парентеральным (включая подкожный, внутрибрюшинный, внутрикожный, внутримышечный, внутривенный) или их комбинацией.
Изобретение иллюстрируется следующими примерами.
Обозначения:
ЭхА - эхинохром А
ПКЛ - поликапролактон
ПВП - поливинилпирролидон
ГПМЦ - гидроксипропилметилцеллюлоза
АЦ - ацетилцеллюлоза
ПЭО - полиэтиленоксид
Пример 1
Способ получения полимерных микро-/нановолокон с включением эхинохрома А
ПКЛ растворяют в концентрации 12% мас./об. в смеси дихлорметан:диметилформамид (8:2 об./об.) (например, 1,2 г ПКЛ в 10 мл растворителя) при комнатной температуре при перемешивании в течение 24 ч для обеспечения гомогенности раствора. Затем к раствору полимера добавляют ЭхА в концентрации 1,333% мас./об. (например, 0,133 г ЭхА на 10 мл 12% мас./об. раствора ПКЛ). Раствор ПКЛ с ЭхА загружают в одноразовый шприц объемом 10 мл, оснащенный тупой иглой из нержавеющей стали (23G), шприц устанавливают на горизонтально расположенный программируемый шприцевой насос (Harvard PHD 2000, Harvard Apparatus). Проводят электроспиннинг полученного прядильного раствора ПКЛ-ЭхА с использованием генератора постоянного тока aγ-High Voltage Research (Gamma High Voltage Research) с приложенным напряжением 25 кВ, с фиксированной скоростью подачи раствора 3 мл/ч, и расстоянием от наконечника иглы до коллектора 15 см. Образующиеся волокна собирают на алюминиевую фольгу, обернутую на вращающийся барабанный коллектор RC-6000 (NaBondTechnologies) со скоростью вращения 500 об/мин. После формирования микро-/нановолокна удаляют с поверхности коллектора в сухом состоянии.
Пример 1.1
Способ осуществляют, как описано в примере 1, но в качестве полимера используют синтетический полимер ПВП, который растворяют в этаноле.
Пример 1.2
Способ осуществляют, как описано в примере 1, но в качестве полимера используют синтетический полимер АЦ, который растворяют в ацетоне. Электроспиннинг осуществляют при напряжении 20 кВ, скорости подачи раствора - 1 мл/ч, расстоянии от иглы до коллектора - 10 см.
Пример 1.3
Способ осуществляют, как описано в примере 1, но в качестве полимера используют полимер ПЭО, который растворяют в концентрации 8 % мас./об. в воде, скоростью подачи раствора устанавливают 0,1 мл/ч.
Пример 1.4
Способ осуществляют, как описано в примере 1, но в качестве полимера используют синтетический полимер ГПМЦ, который растворяют в смеси этанол:дихлорметан 1:1. Электроспиннинг осуществляют при напряжении 20 кВ, скорости подачи раствора - 0,5 мл/ч, расстоянии от иглы до коллектора - 20 см.
Пример 1.5
Способ осуществляют, как описано в примере 1, но в качестве полимера используют природный полимер ульван, который растворяют в концентрации 2,5 % мас./об. в смеси 15 мМ H3BO3 и 7 мМ CaCl2 в соотношении 60:40. Электроспиннинг осуществляют при напряжении 25 кВ, скорости подачи раствора - 0,1 мл/ч, расстоянии от иглы до коллектора - 12 см.
Пример 1.6
Способ осуществляют, как описано в примере 1, но в качестве полимера используют природный полимер альгинат, который растворяют в воде. Электроспиннинг осуществляют при напряжении 15 кВ, скорости подачи раствора - 0,5 мл/ч, расстоянии от иглы до коллектора - 15 см.
Пример 1.7
Приготовление смешанных микро-/нановолокон ПКЛ и ПВП в соотношении 1:1 с включением ЭхА (ПКЛ-ЭхА/ПВП-ЭхА (1:1)).
Растворы ПКЛ и ПВП готовят отдельно, как описано в примерах 1 и 1.1. К каждому раствору полимера добавляют ЭхА в концентрации 1,333% мас./об. Проводят совместный электроспиннинг растворов ПКЛ-ЭхА и ПВП-ЭхА на антипараллельной установке для обеспечения гомогенного смешивания полимерных волокон ПКЛ и ПВП. Электроспиннинг выполняют с приложенным напряжением и расстоянием от наконечника до коллектора, фиксированными на уровне 25 кВ и 15 см, соответственно, со шприцами, установленными на двух горизонтально противоположных программируемых шприцевых насосах. Скорость подачи прядильных растворов 3 мл/ч.
Пример 1.8
Способ осуществляют, как описано в примере 1.7, но полимеры ПКЛ и ПВП берут в соотношении 1:3.
Пример 1.9
Способ осуществляют, как описано в примере 1.7, но полимеры ПКЛ и ПВП берут в соотношении 3:1.
Пример 1.10
Для получения гибридных микро-/нановолокон [ПКЛ-ПВП(1:3)]-ЭхА, ПКЛ в концентрации 3% мас./об. и ПВП в концентрации 9% мас./об. растворяют в смеси дихлорметан:этанол (7:3 об./об.). Затем к раствору полимеров добавляют ЭхА в концентрации 1,333% мас./об. (например, 0,133 г ЭхА на 10 мл растворителя). Раствор ПКЛ/ПВП с ЭхА загружают в одноразовый шприц и проводят электроспиннинг с фиксированной скоростью подачи раствора 3 мл/ч, приложенным напряжением 25 кВ и расстоянием от наконечника до коллектора 15 см.
Пример 1.11
Для получения гибридных микро-/нановолокон ульвана и ПЭО готовят отдельно 2% масс./об. раствор ульвана и 4% масс./об. раствор ПЭО в деионизированной воде. Затем растворы ульвана и ПЭО смешивают в соотношении 2:1, добавляют ЭхА в концентрации 1,333% мас./об. Электроспиннинг осуществляют при напряжении 9 кВ, скорости подачи раствора - 0,1 мл/ч, расстоянии от иглы до коллектора - 10 см.
Пример 2
Исследование физико-химических свойств полимерных микро-/нановолокон с включением ЭхА
Химическая целостность ЭхА после электроспиннинга была подтверждена с помощью 1H ЯМР и УФ/видимой спектроскопии полученного после экстракции ЭхА из изготовленных матриц. ЭхА остается стабильным при электроспиннинге и полностью встраивается в микро-/нановолокна (более 95% загрузки).
На фиг. 1 (А, Б, В, Г, Д, Е, Ж, З, И) представлена морфологическая характеристика полученных микро-/нановолокон, выполненная с использованием настольного сканирующего электронного микроскопа (СЭМ) PhenomWorld (ThermoFischer Scientific) с вольфрамовой нитью (10 кВ) и держателем образца для снижения заряда. Показано, что из всех прядильных растворов успешно образуются микро-/нановолокна. Диапазон диаметров и средние диаметры получаемых микро-/нановолокон приведены в таблице.
Диапазон диаметров и средний диаметр получаемых микро-/нановолокон
Методом рентгеноструктурного анализа показано, что ЭхА находится в микро/нановолокнах в аморфном состоянии, что важно для кристаллических лекарственных субстанций, так как аморфизация способствует значительному повышению скорости растворения и биодоступности вещества. Такой эффект достигается именно в процессе электроспиннинга, так как процесс удаления растворителя происходит мгновенно и эхинохром А не успевает сформировать кристаллическую структуру.
На фиг. 2 приведены ИК-спектры волокон, изготовленных из ПВП, ПКЛ и их смесей, записанные на спектрометре FTIR Bruker Alpha II, в которых присутствуют характерные сигналы их ингредиентов. Из-за преобладания в волокнах большого количества ПКЛ и ПВП все матрицы демонстрировали в основном характерные полосы поглощения полимерных компонентов. О включении ЭхА в полимерные волокна свидетельствует полоса поглощения при 1560 см-1, относящаяся к валентным колебаниям карбонилов -С=О, поскольку другие его характеристические сигналы перекрываются с сигналами ПКЛ и/или ПВП.
Пример 3
Исследование стабильности ЭхА в полимерных микро/нановолокнах
Полимерные микро-/нановолокона в количестве 100 мг с включением ЭхА помещают в 10 мл подкисленного этилацетата, спустя два часа экстракт фильтруют, упаривают досуха при пониженном давлении. Сухой остаток растворяют в 10 мл подкисленного этанола, отбирают 300 мкл раствора, помещают в кварцевую кювету, содержащую 2,7 мл этанола и измеряютоптическую плотность. Содержание ЭхА рассчитываютпо калибровочной кривой. Установлено, что ЭхА остается стабильным в полимерных матрицах не менее двух лет, что значительно дольше, чем в известных лекарственных формах (60 часов, 1 год).
Пример 4
Исследование высвобождения ЭхА из полимерных микро-/нановолокон в биологические среды с различным рН.
Испытания на растворение приготовленных микро-/нановолокон и чистого ЭхА проводили в различных средах с использованием аппарата для растворения Vankel 750D с лопастным методом. Эксперименты проводились в общем объеме буфера 500 мл при 37°С и 50 об/мин. Волокона в количестве 20 мг (содержащих 2 мг ЭхА) и чистый ЭхА помещали в капсулы из целлюлозы, чтобы избежать всплывания материала во время эксперимента, диспергировали в 500 мл 0,1 М соляной кислоты и 0,1 М фосфатного буфера при рН 1,2, 4,5 и 6,8 соответственно. Через определенные промежутки времени (5, 10, 15, 20, 30, 45, 60, 120 и 180 мин для исследования растворения при рН 1,2 и 5; 10, 15, 20, 30, 45, 60, 120, 180, 240, 300 и 360 мин для исследований растворения при рН 6,8). Образец в количестве 3 мл отбирали из среды растворения каждой колбы и заменяли равным объемом свежей среды растворения. Отобранные пробы фильтровали через фильтры из регенерированной целлюлозы (шприцевые фильтры Whatman, Spartan, 0,45 мкм), используя для насыщения фильтров 1 мл. Отфильтрованный объем переносили в прозрачную для УФ-излучения 96-луночную плоскую прозрачную пластину и измеряли УФ-поглощение ЭхА при 470 нм с использованием планшет-ридера Infinite M200 PRO TECAN.
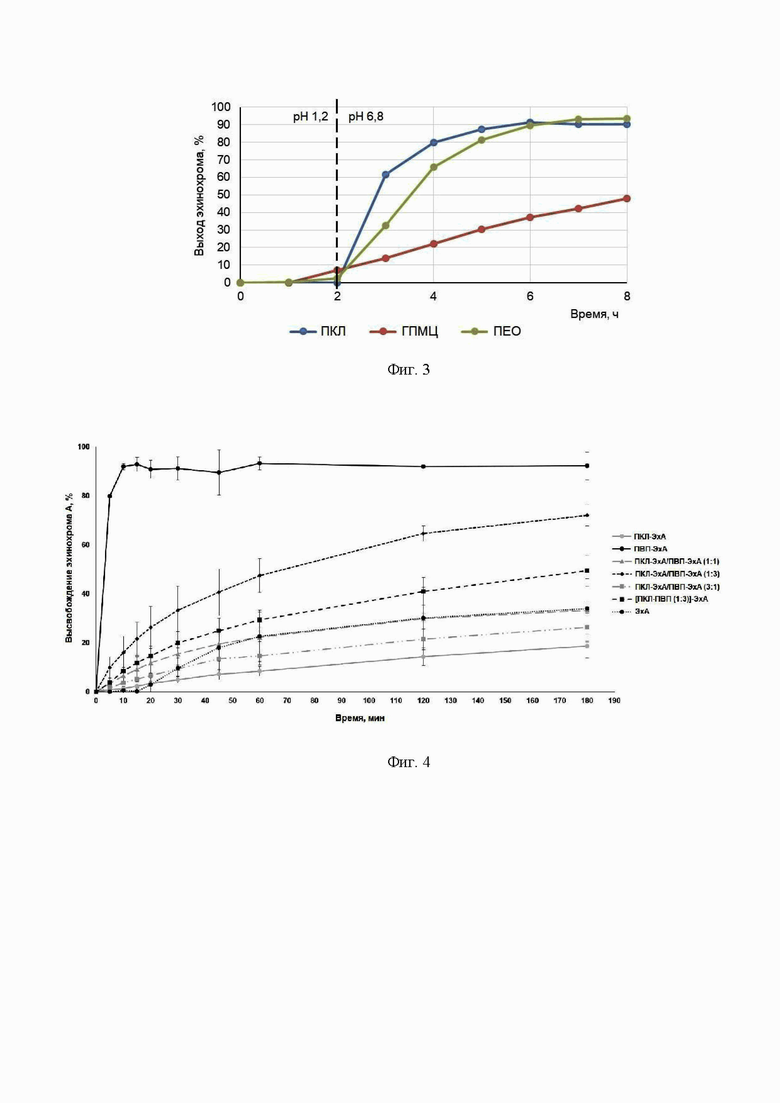
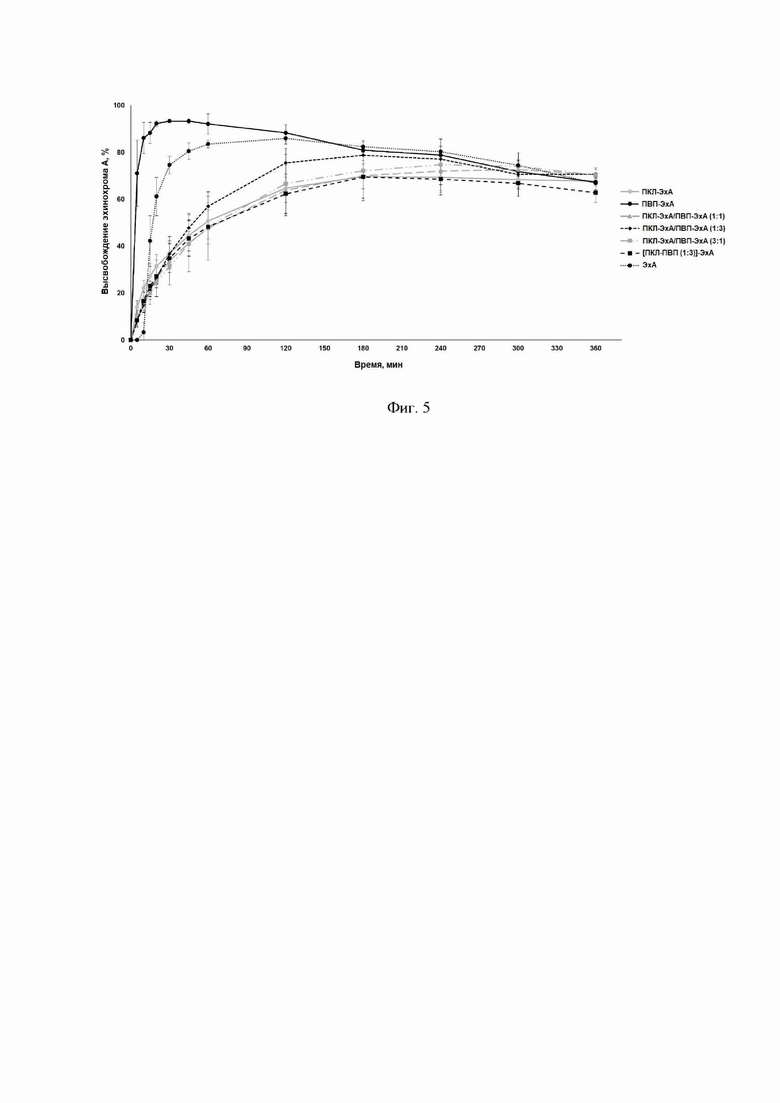
Результаты, демонстрирующие кинетику высвобождения ЭхА из полученных микро-/нановлокон, представлены на фиг. 3-5.
Из волокон АЦ высвобождения ЭхА не происходило за всё время эксперимента. Вероятно, нужно использовать АЦ в сочетании с гидрофильным полимером для обеспечения контролируемого выхода ЭхА из микро-/нановолокон, содержащих АЦ. Волокна ПВП растворялись полностью при рН 1,2, высвобождая все количество включенного ЭхА. ПКЛ и ПЭО градуировано высвобождали ЭхА только в среде, имитирующей тонкий кишечник, при рН 6,8, ГПМЦ постепенно высвобождала ЭхА в обеих средах (фиг. 3).
Исследования растворения смешанных и гибридных волокон из ПВП и ПКЛ с включением ЭхА показали, что комбинация двух полимеров, одного с высокой гидрофильностью и одного с высокой гидрофобностью, приводит к получению микро-/нановолокон, демонстрирующих различные профили высвобождения ЭхА (фиг. 4-5). Например, при рН 1,2 в течение 60 мин около 45% ЭхА было высвобождено из микро-/нановолокон ПКЛ-ЭхА/ПВП-ЭхА (1:3), тогда как из микро-/нановолокон ПКЛ-ЭхА/ПВП-ЭхА (3:1) было высвобождено лишь 10% ЭхА.
Таким образом, микро-/нановолокна ПВП являются перспективным носителем ЭхА для приготовления лекарственных форм с мгновенным высвобождением ЭхА. Микро-/нановолокна ПКЛ, ПЭО и ГПМЦ представляют интерес для направленной доставки ЭхА, так как обеспечивают постепенное высвобождение ЭхА.
Все микро-/нановолокна, полученные из смеси ПКЛ и ПВП, так же, как и гибридные, обеспечивают пролонгированный выход ЭхА при рН 1,2 и 6,8. Для высвобождения ЭхА в биологических средах с низким значением рН более перспективными являются волокна из смеси ПКЛ-ПВП 1:3. Все смеси полимеров могут быть использованы для направленной доставки ЭхА в биологических средах с нейтральным значением рН, так как обеспечивают постепенное высвобождение ЭхА в течение 5 часов при рН 6,8.
| название | год | авторы | номер документа |
|---|---|---|---|
| Лекарственная форма гистохрома для перорального введения и пролонгированного действия | 2017 |
|
RU2651042C1 |
| Средство, обладающее противовирусным действием в отношении вируса простого герпеса 1 типа | 2022 |
|
RU2782935C1 |
| Средство для защиты кожи от фотостарения | 2022 |
|
RU2790820C1 |
| ПРЕПАРАТ "ГИСТОХРОМ" ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ СЕТЧАТКИ И РОГОВИЦЫ ГЛАЗ | 1998 |
|
RU2134107C1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ "ГИСТОХРОМ" ДЛЯ ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА И ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 1998 |
|
RU2137472C1 |
| Способ изготовления функционально активной полимерной заплаты для артериальной реконструкции, устойчивой к аневризмообразованию | 2024 |
|
RU2835436C1 |
| Композиция антиоксидантов, пригодная для перорального применения в терапии воспалительного процесса в легких | 2018 |
|
RU2684783C1 |
| СРЕДСТВО ДЛЯ КОРРЕКЦИИ НАРУШЕНИЙ В ЛЕГОЧНОЙ ТКАНИ ПРИ ЦИТОСТАТИЧЕСКОМ ВОЗДЕЙСТВИИ | 2013 |
|
RU2554776C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАГИДРОКСИЭТИЛНАФТОХИНОНА (ЭХИНОХРОМА А) | 2015 |
|
RU2581055C1 |
| ВОДОРАСТВОРИМЫЙ КОМПЛЕКС ВКЛЮЧЕНИЯ БЕТА-ЦИКЛОДЕКСТРИН-ГИСТОХРОМ, ОБЛАДАЮЩИЙ ПРОЛОНГИРОВАННЫМ АНТИОКСИДАНТНЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2530886C1 |


Группа изобретений относится к области фармацевтики, а именно к созданию новой лекарственной формы эхинохрома А в виде микро-/нановолокон одного или более биосовместимых полимеров, обладающих разной гидрофильностью и чувствительностью к рН биологических сред, содержащих эхинохром А в количестве от 5 до 30 мас. %. Группа изобретений также касается способа получения указанной лекарственной формы эхинохрома А путем электроспиннинга совместного раствора одного или более биосовместимых полимеров и эхинохрома А, и ее применения для контролируемого и пролонгированного высвобождения и направленной доставки действующего вещества к очагу патологического процесса. Группа изобретений обеспечивает повышение стабильности эхинохрома А в заявляемой лекарственной форме, а именно препарат остается стабильным в полимерных матрицах не менее двух лет. Также изобретение обеспечивает контролируемое и более длительное пролонгированное высвобождение эхинохрома А и возможность его адресной доставки. 3 н. и 1 з.п. ф-лы, 5 ил., 4 пр., 1 табл.
1. Лекарственная форма эхинохрома А, представляющая собой микро-/нановолокна одного или более биосовместимых полимеров, обладающих разной гидрофильностью и чувствительностью к рН биологических сред, содержащих эхинохром А от 5 до 30 мас. %, изготовленная путем электроспиннинга совместного раствора одного или более биосовместимых полимеров и эхинохрома А.
2. Лекарственная форма эхинохрома А по п. 1, в которой биосовместимые полимеры являются синтетическими, выбранными из ряда: поливинилпирролидон, поликапролактон, полиэтиленоксид, ацетилцеллюлоза, метилоксипропилцеллюлоза, полиэтиленгликоль, и/или природными, выбранными из ряда: ульван, альгинат, желатин, гиалуроновая кислота, фиброин шелка, гликозаминогликан, хитозан.
3. Способ получения лекарственной формы эхинохрома А, заключающийся в том, что растворяют один или более биосовместимых полимеров в органических растворителях при комнатной температуре при перемешивании в течение 24 ч с получением прядильных растворов, затем добавляют к раствору полимера эхинохром А в таком количестве, чтобы получить общую концентрацию эхинохрома А в матрице, равную 5-30 мас. % (к массе матрицы) с последующим проведением электроспиннинга совместного раствора одного или более биосовместимых полимеров и эхинохрома А с получением на поверхности коллектора микро-/нановолокон в сухом состоянии.
4. Применение лекарственной формы эхинохрома А по п.1 для контролируемого и пролонгированного высвобождения действующего вещества в биологических средах с различным рН и его направленной доставки к очагу патологического процесса.
| E.A | |||
| VASILEVA et al | |||
| Development of new drug forms based on echinochrome a using electrospun micro/nanofibers | |||
| Vestnik FEB RAS, 2018, N6(202) Supplement, с.169-170 DOI: 10.25808/08697698.2018.202.6S.080 | |||
| ВОДОРАСТВОРИМЫЙ КОМПЛЕКС ВКЛЮЧЕНИЯ БЕТА-ЦИКЛОДЕКСТРИН-ГИСТОХРОМ, ОБЛАДАЮЩИЙ ПРОЛОНГИРОВАННЫМ АНТИОКСИДАНТНЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2530886C1 |
| Лекарственная форма гистохрома для перорального введения и пролонгированного действия | 2017 |
|
RU2651042C1 |
| КОМПОЗИЦИЯ ДЛЯ КОРРЕКЦИИ ПАТОЛОГИЧЕСКИХ НАРУШЕНИЙ УГЛЕВОДНОГО, ЛИПИДНОГО ОБМЕНА И АНТИОКСИДАНТНОГО СТАТУСА ОРГАНИЗМА | 2008 |
|
RU2360683C1 |
| E.A | |||
| VASILEVA et al | |||
| Development of new drug forms based on | |||
Авторы
Даты
2023-07-20—Публикация
2022-12-07—Подача