Изобретение относится к области фармакологии и касается средства, обладающего противовирусным действием в отношении вируса простого герпеса 1 типа (ВПГ-1).
Bill-1 относится к нейротропным вирусам, способным пожизненно персистировать в сенсорных нейронах организма человека, и представляет один из самых распространенных вирусных патогенов человека, вызывающих заболевания с многообразными клиническими проявлениями, от лабиального герпеса до менингита и энцефалита [Heldwein Е. Е., Krummenacher С.Entry of herpes viruses into mammalian cells. Cell Mol. Life Sci. 2008; 65: 1653-1668]. По данным ВОЗ от 60 до 95% людей во всем мире инфицировано одним или даже несколькими представителями группы герпесвирусов. Периодическая реактивация на фоне пожизненной персистенции ВПГ-1 приводит к необходимости постоянного применения антигерпетических препаратов.
Большинство современных лекарств, применяемых для лечения герпесвирусных инфекций, основаны на использовании модифицированных нуклеозидов, действие которых, направлено на подавление активности основного фермента репликации вируса - ДНК-полимеразы. «Золотым стандартом» лечения герпетической инфекции является ацикловир (2-амино-9-[(2-гидроксиэтокси)метил]-1,9-дигидро-6H-пурин-6-он) - аналог пуринового нуклеозида дезоксигуанозина, нормального компонента ДНК. В культуре клеток ацикловир обладает наиболее выраженной противовирусной активностью в отношении вирусов ВПГ-1, а также ВПГ-2, Varicellazoster, Эпштейна-Барр и цитомегаловируса [KresgeN., SimoniR. Developing the Purine Nucleoside Analogue Acyclovir: the Work of Gertrude B. Elion. Journal of Biological Chemistry 2008. Vol.283. N 19. P. 11-12].
Модифицированной формой ацикловира является менее токсичный препарат валацикловир [Неверов В.А. и др. Герпесвирусные инфекции, вызываемые нейротегментальнотропными вирусами (ВПГ-1, 2). Лекции. Russian Family Doctor. 2017; 21 (1): 29-28]. Эти препараты могут снижать тяжесть течения болезни и частоту появления ее симптомов, однако не обладают способностью излечивать инфекцию [World Health Organization. Herpes simplex virus. Newsbulletin: https://www.who.int/ru/news-roorn/factsheets/detail/herpes-simplex-viru4]. Более того, у пациентов с выраженным иммунодефицитом длительные или повторные курсы терапии ацикловиром могут приводить к появлению резистентных штаммов, поэтому дальнейшее лечение ацикловиром может быть неэффективным.
Эффективное клиническое действие может быть достигнуто при использовании рациональной комплексной терапии с применением лекарственных средств, обладающих различными механизмами действия. В связи с этим поиск противовирусных средств, отличающихся от ацикловира и его аналогов механизмом действия, избирательно подавляющих процессы адсорбции и репродукции вируса, не наносящих при этом вред организму хозяина и сочетающих противовирусное, противовоспалительное и иммуномодулирующее свойства, является одной из приоритетных задач современной вирусологии.
Морские гидробионты обладают значительным потенциалом для разработки таких препаратов. Литературные данные свидетельствуют о высокой противовирусной активности сульфатированных полисахаридов, предотвращающих проникновение ДНК- и РНК-содержащих вирусов в клетку, что является ключевой стадией распространения вирусной инфекции. Противовирусный эффект обусловлен взаимодействием сульфатированных полисахаридов с положительно заряженными гликопротеинами оболочки вирусов, участвующих в прикреплении вируса к гепарин сульфатам на поверхности клеток [Damonte Е.В. et al., Sulfated seaweed polysaccharides as antiviral agents. CurrMed Chem. 2004; 11:2399-2419].
Среди сульфатированных полисахаридов особое место занимают каррагинаны красных водорослей, поскольку они являются наиболее изученными среди полисахаридов водорослей с точки зрения токсичности, пирогенности и аллергенности, и безопасность их использования в пищевых и медицинских целях подтверждена многочисленными исследованиями в экспериментах in vivo [Report of the thirty-eighth session of the Codex Committee on Food Additives and Contaminants (CCFAC), The Hague, The Netherlands; 2006].
Каррагинаны представляют собой семейство сульфатированных галактанов, полимерная цепь которых построена из повторяющихся дисахаридных звеньев, состоящих из остатков D-галактозы и ее производных, соединенных регулярно чередующимися β-(1→4) и α-(1→3) связями [Yermak, I.; Khotimchenko, Y. Chemical properties, biological activities and applications of carrageenan from red algae; Recent advances in marine biotechnology, 2003]. Три широко используемых в промышленности типа каррагинанов, обозначаемые как каппа- и йота-, (желирующие типы), и лямбда- (не желирующий тип), содержат соответственно одну, две или три сульфатные группы на одно повторяющееся дисахаридное звено.
Наиболее значимыми среди фармакологических свойств каррагинанов является их иммуномодулирующая и антивирусная активности. Нами показано, что каррагинаны, выделенные из красных водорослей дальневосточных морей, обладают иммуномодулирующей активностью [Yermak I.M. et al., Effects of structural peculiarities of carrageenans on immunomodulation and anti-coagulant activities // Carbohydrate Polymers 2012, V. 87, P. 713-720] и повышают неспецифическую сопротивляемость (резистентность) организма к действию эндотоксинов грамотрицательных бактерий, инициирующих развитие эндотоксинемии [RU 2351351 С1, 10.04.2009].
Нами проведено сравнительное изучение противовирусной активности различных структурных типов каррагинанов против вируса простого герпеса 1-го типа по оценке профилактического, вирулицидного и вирусингибирующего действия полисахаридов и их влияния на прикрепление и проникновение вирусов в клетку [N. Krylova, А. Kravchenkoetal. Influence of the Structural Features of Carrageenans from Red Algae of the Far Eastern Seas on Their Antiviral Properties. Marine Drugs 2022, 20, 60. https://doi.org/10.3390/md20010060]. Показано что каррагинаны значительно повышают устойчивость клеток Vero к вирусной инфекции (профилактическое действие). Обработка каррагинанами клеток Vero перед их инфицированием выявила высокую противовирусную активность полисахаридов.
В тоже время каррагинаны проявляют недостаточно эффективное вирулицидное действие (прямая инактивация вирусных частиц). С целью усиления вирулицидного действия каррагинанов и применения их с профилактической целью в отношении ВПГ-1, заявителем создана предлагаемая антигерпетическая композиция, представляющая собой комплексы двух типов (каппа и каппа/лямбда) каррагинанов и эхинохрома А.
Эхинохром А (2,3,5,6,8-пентагидрокси-7-этил-1,4-нафтохинон) - хиноидный пигмент, выделенный из морского ежа Scaphechinus mirabilis, на основе которого разработан препарат Гистохром, используемый в кардиологии и офтальмологии. Недавно показана активность гистохрома и эхинохромаА в отношении ВПГ-1 [RU 2697887 С1, 21.08.2019; О.В. Иунихина, Н.В. Крылова и др. Сравнительное изучение in vitro антигерпетической активности эхинохрома А и продукта его окисления. Бюллетень экспериментальной биологии и медицины, 2021, Том 171, №4 С. 477-480].
Установлено, что основным механизмом противовирусного действия эхинохрома А в отношении ВПГ-1, ВПГ-2 и ВКЭ является прямая инактивация вирусных частиц - вирулицидное действие [FedoreyevS.A. et al., Antiviral and Antioxidant Properties of Echinochrome A // Mar.Drugs. 2018. Vol. 16, N 12. ID 509. doi: 10.3390/md16120509].
Также было отмечено умеренное ингибирующее действие эхинохрома А на ранней стадии вирусной инфекции, когда исследуемым соединением одновременно воздействуют и на ВПГ-1 и на клетки Vero. В то же время эхинохром А не подавлял репликацию ВПГ-1 при обработке им инфицированных клеток (вирусингибирующее действие) и при предварительной обработке неинфицированных клеток (профилактическое действие).
Известна композиция антиоксидантов, проявляющая противовирусную активность в отношении вирусов клещевого энцефалита и простого герпеса 1 типа, представляющая собой смесь эхинохрома А, аскорбиновой кислоты и α-токоферола при массовом соотношении компонентов 5:5:1 [RU 2697886 С1, 21.08.2019].
Основным недостатком известных технических решений является высокая цитотоксичность эхинохрома А и его композиции с антиоксидантами, поэтому создание композиций на основе эхинохрома А, позволяющих уменьшить его токсичность, но сохранить или увеличить его антивирусную активность является актуальной задачей.
Известна лекарственная форма гистохрома для перорального введения и пролонгированного действия, представляющая собой водорастворимый комплекс каррагинан-гистохром, характеризующийся весовым соотношением указанных компонентов 5:1, обладающая гастропротекторным, кардиопротекторным и антиоксидантным действием [RU2651042 С1, 18.04.2018].
Данные о противовирусных свойствах известной композиции не обнаружены.
Одной из основных проблем широкого применения эхинохрома А является его окисление и плохая растворимость. Мы показали, что включение эхинохрома А в гранулы каррагинана защищает его от окислительного разрушения [Yermak, I. Et al. Carrageenan gel beads for Echinochrome inclusion: Influence of structural features of carrageenan // Carbohydrate Polymers. Volume 272, 15 November 2021, 118479].
Однако сведения о противогерпетических свойствах в отношении ВПГ-1 комплекса каррагинан: эхинохром А в данной работе заявителя отсутствуют.
Задача изобретения - расширение арсенала средств, обладающих противовирусной активностью в отношении вируса простого герпеса 1 типа.
Задача решена применением комплекса каррагинан: эхинохром А при весовом соотношении компонентов 10:1 в качестве средства, обладающего противовирусным действием в отношении вируса простого герпеса 1 типа.
Для получения комплекса каррагинан: эхинохром А (Карр:ЭхА) при весовом соотношении компонентов 10:1 готовят стоковый спиртовый раствор эхинохрома А (ЭхА) 10 мг/мл (10 мг ЭхА в 1 мл 96% этилового спирта) и водный раствор каррагинана (Карр) 10 мг/мл (к 2 мл воды добавляют 20 мг Карр), который перемешивают на мешалке при температуре 37°С до полного растворения Карр в течение 120 мин. Затем к 1 мл водного раствора Карр (10 мг/мл) прибавляют 0,1 мл стокового спиртового раствора ЭхА (10 мг/мл), смесь перемешивают на мешалке в темноте при температуре 37°С в течение 60 мин и получают раствор комплекса Карр:ЭхА (10:1 в/в).
Для изучения возможного связывания ЭхА с к-каррагинаном были получены дифференциальные спектры ЭхА в растворах каррагинана и водно-спиртовом растворе. Две, характерных для ЭхА, полосы поглощения при 339.5 нм и 472 нм наблюдались в спектре поглощения ЭхА. В дифференциальных спектрах Эх в растворе Карр появление двух полос при 376 и 580 nm указывало на связывание ЭхА с Карр. Подобные дифференциальные спектры были получены и для других типов каррагинанов.
С целью доказательства взаимодействия каррагинана с эхинохромом А мы использовали ИК Фурье-спектроскопию.
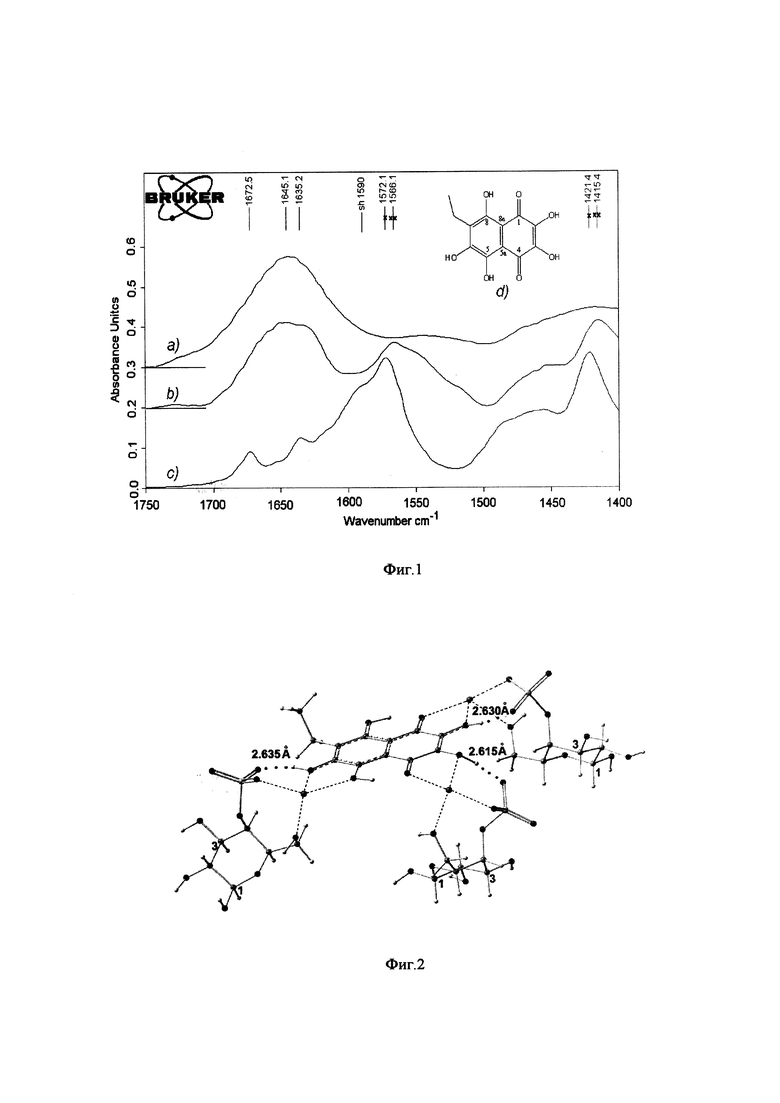
На фиг. 1 представлен ИК - спектр: а - κ-Карр.; b - κ-Карр/ЭхА; с - ЭхА; d - структура ЭхА.
В ИК-Фурье спектре чистого ЭхА полоса поглощения наблюдалась в области 1572 см-1, тогда как в ИК-спектре ЭхА в растворе Карр полоса поглощения сдвигается в более низкую область 1566 см-1. Сдвиг полосы поглощения в сторону более низких частот на 6 см-1, связан с образованием комплекса между Карр и ЭхА. Более того, при переходе в область более низких частот в комплексе Карр:ЭхА наблюдается полоса поглощения при 1415 см-1, тогда как в спектре чистого ЭхА она находится в области 1422 см-1. Таким образом, анализ ИК-Фурье-спектроскопии подтверждает взаимодействие ЭхА с Карр с образованием комплекса. Отсутствие каких-либо кластеров или заметного рассеяния в спектре Карр:ЭхА по сравнению со спектром Карр предполагает, что ЭхА гомогенно распределяется в полимерном матриксе полисахарида.
На фиг. 2 представлена пространственная структура комплекса Карр:ЭхА (10:1 в/в). На основании квантово-химических расчетов методом PCM-B3LYP/6-31+(d,p) H2O показано, что одна молекула ЭхА может связываться с тремя дисахаридными звеньями Карр.
Оценка антигерпетической активности
Исследования проводились на культуре эпителиальных клеток почки африканской зеленой мартышки Vero с использованием штамма L2 ВПГ-1 (получен из Государственной коллекции вирусов ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. Н.Ф. Гамалеи», Минздрав России).
Для исследований нами взяты два типа каррагинанов: каппа - каррагинан (κ-Карр) и не фракционированный (суммарный) каппа/лямбда каррагинан (κ/λ-Карр), а также композиции этих каррагинанов с эхинохромом А в соотношении 10:1 (κ-Карр:ЭхА 10:1 и κ/λ-Кар:ЭхА 10:1). В качестве референсного препарата использовали Ацикловир®(Sigma-Aldrich).
Антигерпетическую активность исследуемых соединений оценивали in vitro по воздействию каррагинанов и их композиций с эхинохромом А на разные стадии вирусной инфекции: непосредственно на вирус (вирулицидное действие), на защиту клеток от цитопатогенного действия вируса (профилактическое действие), на раннюю стадию инфекции (одновременное действие) и после проникновения вируса в клетки (вирусингибирующее «лечебное» действие).
Определение цитотоксичности
Цитотоксичность исследуемых соединений определяли с помощью МТТ-теста [Berridge M.V. et al. Tetrazolium dyes as tools in cell biology: new insights into their cellular reduction // Biotechnol. Annu. Rev. 2005. Vol. 11. P. 127-152. doi: 10.1016/S1387-2656(05)11004-7]. Для этого монослой клеток, выращенных в 96-луночных планшетах, инкубировали с исследуемыми соединениями в концентрациях 1-4000 мкг/мл в течение 72 ч при 37°С, 5% СО2. Затем добавляли раствор МТТ (Sigma-Aldrich) в концентрации 5 мг/мл и инкубировали 2 ч при 37°С, осадок растворяли изопропанолом. Оптическую плотность измеряли при λ=540 нм на планшетном ридере (LabSystems). В качестве 50% цитотоксической концентрации (СС50) принимали концентрацию соединения (мкг/мл), снижающую жизнеспособность клеточной культуры на 50% по сравнению с контролем.
Оценка противовирусной активности
Противовирусную активность тестируемых соединений оценивали с помощью метода ингибирования бляшкообразования [Руководство по вирусологии: вирусы и вирусные инфекции человека и животных / под ред. Д.К. Львова. Москва, 2013]. Монослой клеток Vero, выращенный в 24-луночных планшетах (1×105 клеток/лунку), инфицировали 100 БОЕ (бляшкообразующих единиц)/мл ВПГ-1, а тестируемые соединения добавляли в концентрациях 1-500 мкг/мл по нескольким схемам, представленным в таблице 1.

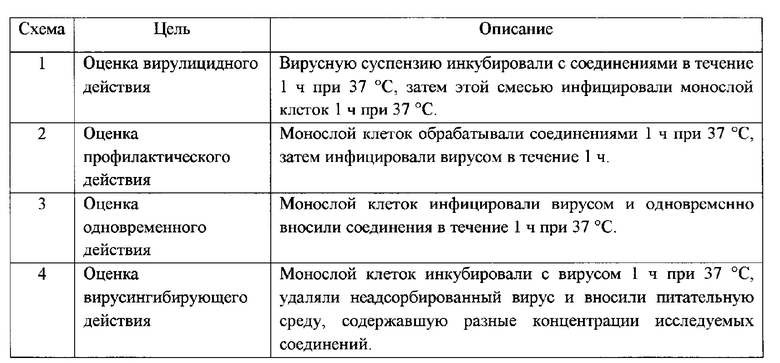
Во всех опытах монослой клеток после инкубации с ВПГ-1 промывали фосфатно-солевым буфером (рН 7,4), вносили поддерживающую среду, содержавшую 1% карбоксиметилцеллюлозы (Sigma-Aldrich), и культивировали в течение 72 ч при 37°С, 5% СО2. Затем клетки фиксировали 96% этанолом и окрашивали 0,5% спиртовым раствором кристаллического фиолетового (Sigma-Aldrich) для подсчета образовавшихся бляшек и вычисления коэффициента ингибирования бляшкообразования (PIC): Р1С=(1-PT/Рс)×100%, где PT и PC - количество вирусиндуцированных бляшек в обработанных соединением клетках и в контроле соответственно. IC50 каждого соединения определяли как концентрацию соединения (мкг/мл), которая на 50% подавляла образование вирусных бляшек по сравнению с контролем. Индекс селективности (SI) рассчитывали как отношение СС50 к IC50 для каждого соединения. Опыты повторяли трижды.
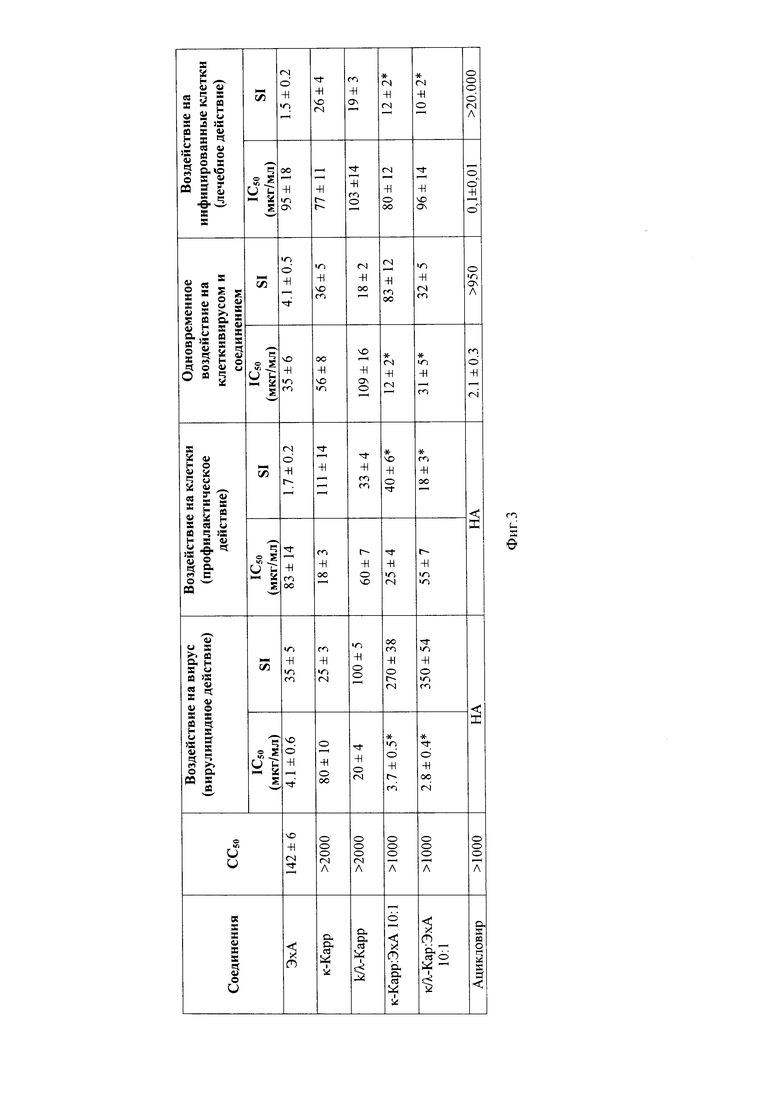
На фиг. 3 представлены результаты изучения влияния исследуемых соединений на разные стадии ВПГ-1 - инфекции.
Примечание: значения представляют собой среднее ± стандартное отклонение трех или более независимых экспериментов; κ-Карр и κ/λ-Карр - различные структурные типы каррагинанов; κ-Карр:ЭхА и κ/λ-Кар:ЭхА - комплексы различных типов каррагинанов с эхинохромом А. В качестве референсного соединения использовали ацикловир. * Достоверность различий между показателями каррагинана (κ-Карр и κ/λ-Карр) по сравнению с соответствующими показателями комплексов каррагинана с эхинохромом А (κ-Карр:ЭхА 10:1 и κ/λ-Кар:ЭхА 10:1) (р<0,05). «НА» - нет активности.
Обнаружено, что κ-Карр и κ/λ-Карр нетоксичны по отношению к клеткам Vero: СС50 выше 2000 мкг/мл, в отличие от ЭхА, СС50 которого составила 142±6 мкг/мл. Цитотоксическая активность комплексов Карр:ЭхА (10:1 в/в) в 2 раза больше (СС50>1000 мкг/мл) по сравнению с СС50 самих каррагинанов, и более чем в 6 раз меньше в сравнении с токсичностью эхинохрома А.
Изучение влияния исследуемых соединений на разные стадии ВПГ-1-инфекции, выявило то, что наиболее высокую противовирусную активность исследуемые композиции каррагинанов с эхинохромом А в соотношении 10:1 в/в проявляют при предварительной обработке вируса (прямое вирулицидное действие). Как видно, комплексы проявляют свое противовирусное действие на том же уровне IC50 (3,7±0,5 и 2,8±0,4 мкг/мл), что и ЭхА (4,1±0,6 мкг/мл). Однако, важно то, что в композиции Карр:ЭхА (10:1 в/в) концентрация ЭхА была на порядок меньше. Достигнутый эффект можно объяснить синергетическим действием каррагинана и эхинохрома А в заявляемом средстве. Рассчитанные значения индексов селективности (SI) κ-Карр:ЭхА (10:1 в/в) и κ/λ-Кар:ЭхА (10:1 в/в) равны 270±38 и 350±54 соответственно, что свидетельствует о расширении химиотерапевтического действия предлагаемых композиций. В этом эксперименте ацикловир не проявляет активности.
Предварительная обработка клеток Vero соединениями (профилактическое действие) демонстрирует, что IC50 разных типов каррагинанов и их композиций с эхинохромом А значимо не различаются (р>0,05): так IC50 κ-Карр составляла 18±3 мкг/мл, a IC50 κ-Карр:ЭхА (10:1 в/в) - 25±4 мкг/мл. Однако индексы селективности (SI=CC50/IC50), свидетельствующие об эффективности и безопасности соединений, у композиций каррагинанов с эхинохромом А были в 10 и 23 раза больше, чем у эхинохрома А, но меньше чем у самих каррагинановв 1,8-2,8 раза. Очевидно, что наблюдаемый профилактический эффект исследуемых комплексов обусловлен действием каррагинанов, тогда как снижение способности композиций каррагинанов с ЭхА к защите клеток от цитопатогенного действия ВПГ-1 можно объяснить токсичностью ЭхА (его SI=1,7). Ацикловир не обладает профилактическим действием.
При изучении влияния исследуемых соединений на раннюю стадию ВПГ-1 - инфекции (одновременное воздействие на клетки вирусом и соединением) установлено, что ингибирующая концентрация (IC50) композиции κ-Карр:ЭхА меньше по сравнению с κ-Карр в 4,7 раза и в 3 раза по сравнению с ЭхА. Подобная картина наблюдалась и с другой композицией каррагинанов - κ/λ-Кар с ЭхА: IC50 этой композиции меньше в 3,5 раза, чем у самого каррагинана, и схожа с ингибирующей концентрацией ЭхА. Необходимо отметить, что при данном способе применения соединений селективный индекс ЭхА на порядок меньше, чем у Карр и их композиций. Наблюдаемый эффект синергизма компонентов в композициях способствует более эффективному связыванию компонентов с оболочечными белками ВПГ-1, тем самым препятствуя прикреплению и проникновению вируса в клетки-мишени.
Применение каррагинанов и их композиций с эхинохромом А после прикрепления и проникновения вируса в клетки (через 1 ч после инфицирования - «лечебное действие») не выявило значимых различий (р>0,05) в их вирусингибирующих концентрациях (в среднем IC50 составляла 90 мкг/мл). В то же время индексы селективности исследуемых соединений различались (р≤0,05): у самих каррагинанов SI (в среднем ~20) были выше, чем у их композиций с ЭхА (SI-10), а у ЭхА - SI=1,5. Следовательно, исследуемые каррагинаны и их композиции с ЭхА на ранней стадии репликации вируса (через 60 мин после заражения) демонстрировали умеренную вирусингибирующую активность.
Таким образом, анализ влияния заявляемого комплекса Карр:ЭхА (10:1 в/в) на жизненный цикл ВПГ-1 выявил его способность повышать устойчивость клеток к заражению (профилактическое действие); оказывать непосредственное влияние на вирусные частицы, снижая их способность заражать клетки (вирулицидное действие); подавлять ранние стадии репликации вируса (вирусингибирующее действие). Установлено, что комплекс Карр:ЭхА (10:1 в/в) наиболее эффективно ингибируют репликацию ВПГ-1 при непосредственном воздействии на вирус, что обусловлено присутствием в композиции ЭхА. Выявленная значительная ингибирующая активность комплекса при воздействии на ранние этапы герпесвирусной инфекции обусловлена его способностью препятствовать прикреплению и проникновению вируса в клетки, а также, возможно, их активность связана с модуляцией внутриклеточных сигнальных путей.
| название | год | авторы | номер документа |
|---|---|---|---|
| Противовирусная композиция | 2018 |
|
RU2697886C1 |
| Средство, обладающее противовирусным действием в отношении вирусов клещевого энцефалита и герпеса простого I типа | 2018 |
|
RU2697887C1 |
| Средство, обладающее противовирусным действием в отношении герпесвируса человека I типа и энтеровируса В | 2022 |
|
RU2798659C1 |
| Средство, обладающее противовирусным действием в отношении коронавируса SARS-CoV-2 | 2022 |
|
RU2788762C1 |
| Средство для создания фармакологических препаратов для лечения клещевого энцефалита | 2016 |
|
RU2651777C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ СУММЫ ФЛАВОНОИДОВ ИЗ Alchemilla vulgaris L. | 2015 |
|
RU2580304C1 |
| 2-Амино-5,6-дифтор-1-(бета-D-рибофуранозил)-бензимидазол, способ получения и противовирусная активность его в отношении вируса герпеса простого 1-го типа | 2016 |
|
RU2629670C2 |
| 2-[6-МЕТИЛ-3-(ТИЕН-2-ИЛ)-5-ФЕНИЛ-5,6-ДИГИДРО-4Н-[1,2,4,5]ТЕТРАЗИН-1-ИЛ]-БЕНЗОТИАЗОЛ С ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСОВ КОКСАКИ В3 | 2023 |
|
RU2836398C1 |
| 6,8-Дифтор-2-(4-(трифторметил)фенил)хроман-4-он в качестве ингибитора репродукции вирусов гриппа А и В и способ его получения | 2023 |
|
RU2826250C1 |
| (3S)-4-[6-(Пурин-6-иламино)гексаноил]-3,4-дигидро-3-метил-7,8-дифтор-2Н-[1,4]бензоксазин и (3R)-4-[6-(Пурин-6-иламино)гексаноил]-3,4-дигидро-3-метил-7,8-дифтор-2Н-[1,4]бензоксазин, обладающие противовирусной активностью | 2016 |
|
RU2644351C1 |
Изобретение относится к области фармакологии, а именно к применению комплекса каррагинан:эхинохром А при весовом соотношении компонентов 10:1 в качестве средства, обладающего противовирусным действием в отношении вируса простого герпеса 1 типа. Изобретение обеспечивает расширение арсенала средств, обладающих противовирусным действием в отношении вируса простого герпеса 1 типа. Применение комплекса повышает устойчивость клеток к заражению, оказывает непосредственное влияние на вирусные частицы, снижая их способность заражать клетки, подавляет ранние стадии репликации вируса, т.е. обеспечивает профилактическое действие, вирулицидное действие и вирусингибирующее действие. Рассчитанное значение индекса селективности комплекса свидетельствует о большей безопасности его практического применения. 1 табл., 3 ил.
Применение комплекса каррагинан : эхинохром А при весовом соотношении компонентов 10:1 в качестве средства, обладающего противовирусным действием в отношении вируса простого герпеса 1 типа.
| Средство, обладающее противовирусным действием в отношении вирусов клещевого энцефалита и герпеса простого I типа | 2018 |
|
RU2697887C1 |
| Счетная линейка для расценки зерна по качеству | 1929 |
|
SU15930A1 |
| Модификатор | 1974 |
|
SU497341A1 |
| JP 08301772 A, 19.11.1996 | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| BRUNA G | |||
| MALAGOLI et al., Chemical characterization and antiherpes activity of sulfated polysaccharides from Lithothamnion muelleri | |||
| International Journal of Biological Macromolecules, 2014, V | |||
| Приспособление для соединения пучка кисти с трубкою или втулкою, служащей для прикрепления ручки | 1915 |
|
SU66A1 |
| Приспособление, обнаруживающее покушение открыть замок | 1910 |
|
SU332A1 |
Авторы
Даты
2022-11-07—Публикация
2022-06-01—Подача