[Область техники]
Настоящее изобретение относится к конструкции системы, выполненной с возможностью выполнения обнаружения в реальном времени реакций выделения и амплификации нуклеиновых кислот и амплифицированных результатов в устройстве для реализации полимеразной цепной реакции.
[Предпосылки создания изобретения]
Технология диагностики на месте оказания медицинской помощи (РОС), которая точно и быстро диагностирует заболевание пациента независимо от времени и места, привлекает внимание как чрезвычайно важная технология точной медицины на основе фактических данных. Диагностика на месте на основе симптомов сразу быстро проверяет наличие всех инфекционных патогенов, которые вызывают симптомы заболевания, на основе таких симптомов заболевания как кашель, диарея, высокая температура и отклонения в развитии гениталий, идентифицирует вызывающий их патоген и предписывает наилучшие антибиотики и средства для лечения. Диагностика на месте на основе симптомов представляет собой базовую технологию для точной медицины в будущем, и для развития диагностики на месте на основе симптомов добавляется множество исследований. Технология диагностики на месте имеет то преимущество, что она обеспечивает возможность быстрой и точной диагностики даже при помощи неспециалистов в этой области, например, с использованием тест-системы для определения беременности с целью подтверждения беременности и глюкометра, который может определять сахар, содержащийся в крови. К настоящему времени разработано множество способов определения для технологии молекулярной диагностики, при помощи которых можно одновременно определять различные патогены, и с использованием этих технологий возможно выяснить точную причину инфекционного заболевания и сделать оптимальное назначение лекарства, таким образом сокращая период восстановления пациента за счет лечения заболевания на ранней стадии. Соответственно, технология молекулярной диагностики привлекает внимание как базовая технология медицины будущего, которая улучшает качество медицинской помощи и сокращает стоимость медицинского обслуживания.
Однако в современной системе молекулярной диагностики подтверждение результата занимает более трех часов, и ее должны использовать опытные специалисты. Соответственно, для требуемой в данной области молекулярной диагностики на месте оказания медицинской помощи (РОС) важно разработать автоматизированное устройство небольшого размера, которое может выполнять сложный процесс выделения нуклеиновых кислот и исследование амплификации гена в реальном времени полностью автоматически, и оно должно быть простым в эксплуатации даже в отсутствие профессионального персонала.
В качестве представительного способа молекулярной диагностики существует способ, в котором используется полимеразная цепная реакция (PCR) (в дальнейшем называемая «PCR»). С момента открытия PCR Kary Mullis в 1985 г. PCR может быстро и просто амплифицировать конкретную ДНК, и, таким образом, PCR широко используется в молекулярной биологии и молекулярной диагностике. Используя PCR/PCR с обратной транскрипцией (PCR/RT-PCR), возможно проверить присутствует ли конкретная ДНК/РНК в биологическом образце, и, таким образом, ее широко используют для диагностики инфекций, вызванных патогенными микроорганизмами, такими как вирусы. Данная технология PCR/RT-PCR развилась в количественную PCR в реальном времени, и, таким образом, результат можно узнать одновременно с завершением PCR. Поэтому технологию PCR/RT-PCR используют в качестве стандартного способа диагностики с целью отслеживания эффектов лечения вируса иммунодефицита человека (HIV), вируса гепатита С (HCV), вируса гепатита В (HBV) или т.п., так как она не только значительно сокращает время исследования за счет упрощения процесса исследования, но также может точно определить количество патогенов. Дополнительно, технологию PCR/RT-PCR используют как наиболее важную технологию для диагностики заболеваний, так как она может исследовать наборы экспрессирующихся генов или генетические мутации, связанные с конкретными заболеваниями.
Для выполнения PCR требуется этап выделения нуклеиновой кислоты для удаления из биологического образца веществ, ингибирующих реакцию PCR, и выделения чистых нуклеиновых кислот. Процесс выделения нуклеиновой кислоты включает несколько этапов, требует квалифицированных методик для обработки биологических образцов и выделения нуклеиновой кислоты, и при выполнении процесса выделения нуклеиновой кислоты вручную существует проблема загрязнения вследствие ошибки оператора. Поэтому в большинстве процессов выделения нуклеиновых кислот с целью молекулярной диагностики используют автоматизированное оборудование для выделения нуклеиновых кислот.
Так как для реакции PCR и обнаружения продуктов реакции требуется устройство для количественной PCR в реальном времени, молекулярную диагностику обычно в основном осуществляют в больших больницах или специализированных учреждениях с клиническими лабораториями.
В ходе недавних научно-исследовательских работ были разработаны различные автоматизированные системы и устройства, в которых используются эти системы, которые автоматизируют все процессы выделения нуклеиновых кислот, реакцию PCR и обнаружение продуктов реакции так, что PCR можно легко применять даже в отсутствие специальных навыков.
Однако существуют проблемы того, что существующие устройства являются слишком дорогими или требуют большого количества времени на обработку, и различные исследования трудно выполнять немедленно.
Для разъяснения основного принципа PCR, когда двойную спираль ДНК нагревают до 95° для разделения на одиночные цепи, а затем реакционный раствор охлаждают до температуры отжига с целью селективной гибридизации праймеров, комплементарных обоим концам участка, который подлежит амплификации в реакционном растворе для PCR, повторно выполняют реакцию, в которой ДНК-полимераза создает двойную спираль путем последовательного связывания четырех типов комплементарных A, G, Т и С нуклеотидтрифосфатов с каждой одиночной цепью. Реакция PCR представляет собой реакцию, в которой конкретная двойная спираль ДНК амплифицируется в геометрической прогрессии по принципу 2n путем многократного выполнения 30-45 циклов (n) экспериментального нагрева и охлаждения реакционного раствора PCR. Реакция RT-PCR была расширена как способ обнаружения РНК путем синтеза кДНК при помощи реакции обратной транскрипции, а затем амплификации синтезированной кДНК при помощи PCR.
Для разъяснения принципа вновь разработанной количественной PCR в реальном времени с целью полномасштабного применения PCR для молекулярной диагностики, количественная PCR в реальном времени представляет собой способ количественного анализа амплифицированной ДНК с использованием реакции PCR, в которой в реакционный раствор для PCR добавляют вещество, излучающее флуоресценцию пропорционально количеству ДНК, а затем флуоресценцию измеряют на каждом цикле с целью нахождения цикла, в котором обнаруживается критическое значение флуоресценции, и на его основе количественно измеряют концентрацию исходной нуклеиновой кислоты-мишени.
В то время как с момента открытия PCR были разработаны различные прикладные технологии, многочисленные патогены и связанные с заболеваниями последовательности генов известны из Геномного проекта, и была быстро разработана молекулярная диагностика, в которой эти связанные с заболеваниями последовательности ДНК/РНК амплифицируются с целью качественной и количественной диагностики. Так как в традиционной PCR циклические изменения температуры занимают приблизительно 2 часа, непрерывно разрабатывались способы более быстрого и точного выполнения PCR для диагностики на месте. (Lab Chip, 2016, 16, 3866-3884)
Для выполнения реакции PCR за короткое время необходимо быстро изменять температуру реакционного раствора. Дополнительно, для амплификации только требуемой мишени за счет точной реакции PCR, праймеры должны быть рассчитаны на специфичное присоединение к требуемой мишени, и следует точно управлять температурой отжига в температурном цикле реакции PCR.
С этой целью были разработаны реакционные сосуды для микро PCR, которые имеют меньшую теплоемкость и лучший теплоперенос, чем реактор объемом 0,5 мл или 0,2 мл, обычно используемый в лабораториях. Так как в этих микрореакторах используется небольшое количество реакционного раствора, и они имеют большую площадь поверхности, тепло предается быстро, обеспечивая возможность быстрого нагрева и охлаждения. 10 мкл раствора для PCR вводят в тонкую реакционную канавку глубиной 40-80 мкм с размером 17×15 мм на кремниевой пластине и накрывают стеклянной пластиной для сохранения большой площади поверхности (>100 мм2/10 мкл). Однако при использовании традиционного термоблока типа Пельтье не удалось показать сокращение времени одного цикла до приблизительно 3 минут (Clin. Chem. 40/9, 1815 1818 (1994)).
Для быстрого нагрева реактора для PCR, в качестве начального устройства для реакции PCR был разработан способ многократного погружения реактора для PCR в водяную баню с высокой температурой и водяную баню с низкой температурой. (Turbo Thermalcycler. Bioneer Corp. Daejeon). В оборудовании для PCR, которое выполняет циклическое перемещение реакторов в зонах с разной температурой с использованием способа перемещения в пространстве, можно обеспечить возможность быстрого и точного осуществления реакции PCR путем погружения реактора в водяную баню с постоянной температурой, в которой температура заранее точно поддерживается. Однако в оборудовании для PCR требуется несколько бань с постоянной температурой, и оборудование характеризуется большим размером, а его техническое обслуживание является трудоемким. Соответственно, преобладающим является оборудование для PCR, в котором применяют способ циклического изменения температуры с разностью по времени, где температура изменяется в соответствии с временем с применением элемента Пельтье в неподвижном блоке.
Также был в качестве способа циклического изменения температуры при перемещении в пространстве и способа циклического изменения температуры с разностью по времени разработан способ PCR с использованием микроканалов. Способ циклического изменения температуры при перемещении в пространстве можно в широком смысле разделить на открытый реакторный способ, в котором непрерывное протекание выполняется способом в порядке поступления (FIFO), и замкнутый способ, в котором выполняются повторяющиеся перемещения в секциях с разной температурой. Открытый способ был разработан в 1994 г. Nakano и др. путем наматывания капиллярной трубки вокруг цилиндрического блока, имеющего отсеки с разной температурой, и обеспечения возможности непрерывного протекания раствора для PCR по капиллярной трубке. (Biosci. Biotech. Biochem., 58(2), 349 352, 1994). В 1998 г. Kopp и др. подтвердили осуществление PCR путем пропускания 10 мкл раствора через 20 циклов с длительностью цикла 4,5 секунд при использовании микроканального оборудования для PCR, в котором протекание повторяющимся образом происходит через секции с высокой и низкой температурой. (Science 280 1046-1048, 1998)
[Литература уровня техники]
Публикация патента Кореи №10-2016-0067872.
[Описание]
[Техническая задача]
Настоящее изобретение направлено на предоставление устройства, выполненного с возможностью выполнения полностью автоматического обнаружения нуклеиновых кислот-мишеней путем выделения нуклеиновых кислот из биологического образца, полимеразной цепной реакции (PCR) и сканирования компонент возбуждающего света в различных диапазонах длин волн и флуоресценции, соответствующей возбуждающему свету, проверки множества мишеней за одну операцию, простоты применения и получения точных результатов за короткое время.
Дополнительно, настоящее изобретение направлено на предоставление устройства, выполненного с возможностью быстрого и повторяющегося применения температуры, требуемой для процесса денатурации, и точной температуры, требуемой для отжига, в отношении мишени реакции в процессе управления температурой, необходимом для процесса PCR с целью выполнения быстрой и правильной PCR и максимального повышения надежности реакции. [Техническое решение]
Согласно аспекту настоящего изобретения предоставляется система для полимеразной цепной реакции (PCR), содержащая картридж (100) для выделения нуклеиновой кислоты, выполненный с возможностью выделения нуклеиновой кислоты из биологического образца при помощи хранящегося в нем реагента для выделения нуклеиновой кислоты, планшет (200) для PCR, содержащий канал, соединенный с картриджем для выделения нуклеиновой кислоты, и по меньшей мере одну реакционную лунку (W), которая вмещает сухую смесь для PCR, содержащую праймер, праймер/зонд или зонд праймера, и принимает раствор нуклеиновой кислоты, извлеченный из картриджа (100) для выделения нуклеиновой кислоты; и модуль (300) управления температурой, расположенный над планшетом (200) для PCR смежно с реакционной лункой (W) для применения разных температур и имеющий пару нагревательных блоков (310, 320), которые выполнены с возможностью перемещения в горизонтальном и вертикальном направлениях.
[Полезные эффекты]
Согласно вариантам осуществления настоящего изобретения возможно предоставить устройство, выполненное с возможностью автоматического выполнения обнаружения продуктов реакции путем выделения нуклеиновых кислот из биологического образца, полимеразной цепной реакции (PCR) и сканирования компонент возбуждающего света в различных диапазонах длин волн и флуоресценции, соответствующей возбуждающему свету, проверки множества мишеней за одну операцию, простоты применения и получения точных результатов за короткое время.
Дополнительно, согласно вариантам осуществления настоящего изобретения управление температурой, необходимое для процесса PCR, и точную температуру, требуемую для этапа денатурации и связывания, можно быстро применять в реальном времени к мишени реакции немедленно, вследствие чего возможна точная PCR, и возможно максимально повысить надежность реакции.
То есть в случае традиционного способа управления температурой, состоящего в перемещении реакционного раствора и повышении температуры, применение равномерного повышения температуры является невозможным, что неблагоприятно для реакции PCR. То есть в соответствии со способом перемещения реакционного раствора и последовательного повышения температуры невозможно добиться равномерности температуры во всем реагирующем веществе одновременно, и, таким образом, высока вероятность прохождения других реакций. Однако в варианте осуществления настоящего изобретения возможно устранить вышеописанные проблемы, поддерживать диапазон температур, установленный в нагревательном блоке, при постоянной температуре и более эффективно повышать температуру, требуемую для реакции PCR, путем непосредственного приложения давления ко всему реакционному раствору с целью повышения температуры.
Кроме того, для сведения к минимуму временной задержки в процессе изменения температуры от высокой температуры к низкой температуре конструкции нагревательных блоков в форме блоков расположены так, что они находятся рядом на расстоянии.
Поэтому при приложении давления к планшету для PCR положения нагревательных блоков изменяются так, что к нагревательным блокам, по отдельности имеющим разные температуры, прикладывают давление в реальном времени, и, таким образом, можно нестандартно решить проблемы, вызванные задержкой во времени, необходимой в процессе изменения температуры.
Кроме того, планшет для PCR реализован с возможностью вставки в картридж для выделения нуклеиновой кислоты, при этом картридж для выделения нуклеиновой кислоты является часто используемым, а планшет для PCR, используемый в разных тест-системах, хранится в небольшом объеме, и планшет для PCR, подходящий для исследования, можно вставлять и использовать по необходимости. В одной реакционной лунке, предусмотренной в планшете для PCR, можно анализировать не более шести значений флуоресценции, и количество реакционных лунок в планшете для PCR можно при необходимости увеличить до восьми. Таким образом, возможно амплифицировать и обнаруживать все патогены, которые могут содержаться в биологическом образце пациента, связанном с симптомами, и выполнять многомолекулярное диагностическое исследование на основе симптомов.
Дополнительно, согласно одному варианту осуществления настоящего изобретения, пластина постоянной температуры разделена на области, характеризующиеся градиентом первой температуры и второй температуры. Соответственно, когда к нагревательному блоку прикладывают давление при помощи модуля привода, область, имеющая установленную температуру (первую температуру или вторую температуру), соответствующую температуре нагревательного блока, перемещается соответственно, приложение контактного давления выполняется одновременно в отношении верхней и нижней поверхностей планшета для PCR, и, таким образом, возможно получить удвоенную эффективность по сравнению со способом, в котором пластина постоянной температуры поддерживается при одной температуре.
Дополнительно, при реализации подвижной конструкции пластины постоянной температуры для обеспечения надежности конфигурации и перемещения продукта в качестве конфигурации для выполнения операции приведения в движение используется лента для скольжения. Кроме того, нагрев планшета, содержащегося в мишени, реализуется одновременно на верхней и нижней поверхностях планшета, и, таким образом, время проверки можно уменьшить наполовину.
[Описание графических материалов]
На фиг.1 показана блок-схема, иллюстрирующая основные компоненты, которые составляют систему для полимеразной цепной реакции (PCR) согласно одному варианту осуществления настоящего изобретения.
На фиг.2-7 показаны виды для описания конструкции модуля (300) управления температурой в настоящем изобретении.
На фиг.8а проиллюстрирован один вариант осуществления планшета (200) для PCR в применении к настоящему изобретению, имеющего восемь реакционных лунок.
На фиг.8b проиллюстрирован один вариант осуществления планшета (200) для PCR в применении к настоящему изобретению, имеющего десять реакционных лунок.
На фиг.9-12 показаны концептуальные виды для описания конструкций и операций пластины постоянной температуры и модуля привода горизонтального перемещения в применении к настоящему изобретению.
На фиг.13 показан вид в перспективе картриджа для выделения нуклеиновой кислоты согласно настоящему изобретению и проиллюстрирована конструкция, в которую вставляется и с которой соединяется вышеописанный планшет для PCR.
На фиг.14 показан покомпонентный вид в перспективе изображения на фиг.13.
На фиг.15 проиллюстрирована внутренняя конструкция части (R1) в виде крышки картриджа в конструкции, изображенной на фиг.14.
На фиг.16 показан вид в перспективе, иллюстрирующий состояние соединения конструкции, изображенной на фиг.14.
На фиг.17-19 проиллюстрированы рабочие состояния нижней части конструкции картриджа согласно настоящему изобретению.
На фиг.20 проиллюстрирована общая конструкция и схема устройства, составляющего вышеописанную систему для PCR согласно настоящему изобретению.
На фиг.21 показан увеличенный вид компоновки соединения основных частей согласно настоящему изобретению, изображенной на фиг.20, и на фиг.22 показан концептуальный вид вертикального разреза частей, изображенных на фиг.21, для описания компоновки основных компонентов.
На фиг.23 показан концептуальный боковой вид в перспективе и в разрезе по фиг. 22.
[Варианты осуществления изобретения]
Преимущества и признаки настоящего изобретения, и способы для их достижения станут очевидны при обращении к вариантам осуществления, подробно описанным ниже в сочетании с сопроводительными графическими материалами. Однако настоящее изобретение не ограничено вариантами осуществления, описанными в настоящем документе, и может быть воплощено в других формах. Скорее, представленные в настоящем документе варианты осуществления предоставлены для того, чтобы раскрытие предмета изобретения могло быть всесторонним и полным, и чтобы сущность настоящего изобретения могла быть в достаточной мере передана специалистам в данной области техники.
Термины, используемые в настоящей заявке, используются только для описания конкретных вариантов осуществления и не предназначены для ограничения настоящего изобретения. Форма единственного числа включает множественное число, если из контекста явно не следует иное. В настоящей заявке такие термины, как «содержать» или «иметь», предназначены для обозначения присутствия признака, количества, этапа, операции, компонента, части или их комбинации, описанных в описании. То есть следует понимать, что такие термины, как «содержать» или «иметь» не препятствуют возможности добавления или существования одного или нескольких других признаков или количеств, этапов, операций, компонентов, частей или их комбинаций.
На фиг.1 показана блок-схема, иллюстрирующая основные компоненты, составляющие систему для полимеразной цепной реакции (PCR) (в дальнейшем называемую «настоящим изобретением») согласно одному варианту осуществления настоящего изобретения.
Со ссылкой на фиг.1, система для PCR (в дальнейшем называемая «настоящим изобретением») согласно одному варианту осуществления настоящего изобретения содержит модуль управления температурой, реализованный в виде конструкции нагревательных блоков, которая находится в контакте с планшетом для реакции PCR с целью применения конкретной температуры. Модуль управления температурой может быстро и повторяющимся образом применять температуру, требуемую для процесса денатурации, и точную температуру, требуемую для отжига, к мишени реакции немедленно в реальном времени без разности по времени в процессе управления температурой, необходимом для процесса PCR, чтобы быстро и правильно выполнять PCR, и максимального повышения надежности реакции.
В модуле управления температурой согласно настоящему изобретению с целью сведения к минимуму задержки во времени, необходимой для изменения температуры от первой температуры к относительно низкой второй температуре или от второй температуры к относительно высокой первой температуре в обратном процессе, путем изменения положений нагревательных блоков, установленных на первую температуру и вторую температуру, к планшету для реакции PCR в реальном времени прикладывается давление, и, таким образом, возможно нестандартно решить проблему, вызываемую временной задержкой, необходимой в процессе изменения температуры.
Кроме того, настоящее изобретение может дополнительно содержать конструкцию пластины постоянной температуры, которая расположена под планшетом для PCR и действует скользящим образом как подвижная в горизонтальном направлении конструкция. В этом случае конструкция пластины постоянной температуры, которая поддерживает температуру планшета для PCR при первой температуре или второй температуре, сводит к минимуму время необходимое для применения условия изменения температуры с целью максимального повышения скорости реакции.
В частности настоящее изобретение может содержать картридж 100 для выделения нуклеиновой кислоты, выполненный с возможностью выделения нуклеиновой кислоты из биологического образца при помощи хранящегося в нем реагента для выделения нуклеиновой кислоты и образования предварительной смеси или матрицы для PCR, планшет 200 для PCR, вставляемый в картридж для выделения нуклеиновой кислоты, имеющий канал, соединенный с картриджем для выделения нуклеиновой кислоты и размещенный в по меньшей мере одной реакционной лунке, которая принимает предварительную смесь или матрицу для PCR, извлеченную из картриджа 100 для выделения нуклеиновой кислоты, и вмещает сухой продукт для PCR, содержащий праймер, праймер/зонд или зонд праймера, и модуль 300 управления температурой, расположенный над планшетом 200 для PCR и содержащий пару нагревательных блоков 310 и 320 смежно с реакционной лункой W с целью применения разных температур.
Согласно вышеописанной конфигурации настоящего изобретения даже непрофессионалы способны легко вставить требуемый образец в картридж для выделения нуклеиновой кислоты так, чтобы можно было свободно выполнить выделение нуклеиновой кислоты. Кроме того, за счет использования конструкции нагревательных блоков, которая непосредственно применяет целевую температуру к реакционному раствору в планшете для PCR через тонкую пленку и путем приложения давления, можно выполнять быстрое и точное управление температурой температурного цикла, требуемое для возможности выполнения амплификации, применяемой к планшету 200 для PCR.
Кроме того, возможно предоставление устройства для PCR, реализованного в виде единой системы, которая может обнаруживать реагирующие вещества путем сканирования компонент возбуждающего света в различных диапазонах длин волн и флуоресценции, соответствующей возбуждающему свету, под планшетом для PCR в реальном времени при помощи модуля сканирования.
На фиг.2-7 показаны виды для описания конструкции модуля 300 управления температурой в настоящем изобретении.
На фиг.2 и 3 показаны виды в перспективе, иллюстрирующие модуль управления температурой согласно настоящему изобретению.
Со ссылкой на фиг.2 и 3, модуль 300 управления температурой выполняет постоянное управление температурой в отношении планшета 200 для PCR, при котором выполняется выделение нуклеиновой кислоты из биологического образца, смешивание нуклеиновой кислоты с полимеразой и прием предварительной смеси для PCR или выделенной нуклеиновой кислоты из картриджа для выделения нуклеиновой кислоты.
В частности модуль 300 управления температурой содержит первый нагревательный блок 310, который содержит первую прижимную поверхность G1, соответствующую поверхности реакционной лунки W, реализованной в планшете 200 для PCR, и при помощи нагревательного элемента поддерживается при установленной температуре в пределах диапазона температуры (в дальнейшем называемой «первой температурой»), требуемой для денатурации. Кроме того, модуль 300 управления температурой содержит второй нагревательный блок 320, который расположен в положении, соответствующем первому нагревательному блоку 310, и на расстоянии от первого нагревательного блока 310, содержит вторую прижимную поверхность G2, соответствующую поверхности реакционной лунки, и при помощи нагревательного элемента поддерживается при температуре, установленной в пределах диапазона температуры (в дальнейшем называемой «второй температурой»), требуемой для отжига. В частности конструкции первого нагревательного блока 310 и второго нагревательного блока 320 могут быть реализованы для обеспечения возможности горизонтального перемещения и вертикального перемещения.
В иллюстративном варианте осуществления каждый из первого нагревательного блока 310 и второго нагревательного блока 320 может иметь трехмерную конструкцию и содержать на его нижней поверхности плоскую прижимную поверхность. Кроме того, первый нагревательный блок 310 и второй нагревательный блок 320 могут быть расположены так, что они находятся на расстоянии друг от друга и имеют температуру в разных диапазонах температур.
В частности, как проиллюстрировано на фиг.2 и 3, первый нагревательный блок 310 и второй нагревательный блок 320 могут иметь конструкцию с расположением обращенными друг к другу. Кроме того, верхняя поверхность каждого из первого нагревательного блока 310 и второго нагревательного блока 320 может быть реализована как имеющая плоскую конструкцию, выполненную с возможностью выполнения функции приложения давления, и над верхней поверхностью может быть предусмотрена трехмерная конструкция, такая как прямоугольный параллелепипед. Трехмерная конструкция, такая как прямоугольный параллелепипед, представляет один вариант осуществления, и в сущность настоящего изобретения может быть включена любая трехмерная форма до тех пор, пока конструкция имеет плоскую поверхность для приложения давления.
Дополнительно, первый нагревательный блок 310 и второй нагревательный блок 320 могут быть расположены бок о бок, их смежные поверхности могут находиться на расстоянии одна от другой, и первый нагревательный блок 310 и второй нагревательный блок 320 могут поддерживаться при разных установленных температурах.
Например, первая температура первого нагревательного блока 310 представляет собой температуру, применяемую для денатурации, при которой разделяется двухцепочечная ДНК (содержащая ДНК, выделенную из биологического образца), и может быть установлена в диапазоне 94-96°С. В иллюстративном варианте осуществления настоящего изобретения первая температура может поддерживаться при 95°С.
Кроме того, вторая температура второго нагревательного блока 320 представляет собой температуру, требуемую для отжига праймера, чтобы соединить праймер с выделенной матричной ДНК, и может быть установлена в диапазоне 50-65°С. В иллюстративном варианте осуществления настоящего изобретения вторая температура может поддерживаться при 55°С.
Первый нагревательный блок 310 и второй нагревательный блок 320 не содержат в себе воду или переносящую тепло текучую среду, но реализованы в конструкции, имеющей металлический корпус, характеризующийся высокой теплоемкостью и высокой эффективностью теплопереноса. Следовательно, первый нагревательный блок 310 и второй нагревательный блок 320 могут всегда поддерживаться при установленной температуре при помощи предусмотренного в них нагревательного элемента. Для этого нагревательным элементом нужно управлять путем управления температурой так, чтобы при помощи установки в них датчика температуры можно было поддерживать постоянную температуру.
То есть в случае, если предварительная смесь для PCR вводится в планшет 200 для PCR, когда требуется применение первой температуры, первый нагревательный блок 310 перемещается в горизонтальном направлении так, чтобы находиться смежно с поверхностью планшета 200 для PCR. То есть, поскольку первая прижимная поверхность G1 имеет конструкцию плоской пластины, можно одновременно нагревать всю поверхность планшета 200 для PCR до одной и той же температуры и с одинаковым прижимающим усилием, и, таким образом, возможен равномерный перенос температуры ко всему образцу.
Дополнительно, когда необходимо применить вторую температуру, требуемую для этапа соединения, второй нагревательный блок 320 перемещается в горизонтальном направлении и располагается над планшетом для PCR, и, таким образом, возможно одновременно нагревать всю поверхность планшета 200 для PCR до одной и той же температуры и с одинаковым прижимающем усилием.
То есть дополнительное время для подготовки реакции при установленной температуре не требуется, и нагревательный блок приводится в действие таким образом, что вся поверхность планшета 200 для PCR может быть одновременно нагрета до одной и той же температуры и с одинаковым прижимающим усилием за счет простой горизонтальной операции. Соответственно, по сравнению с существующим способом управления установленной температурой возможно получить более быструю и точную реакцию PCR.
Дополнительно, в пространстве, находящемся между первым нагревательным блоком 310 и вторым нагревательным блоком 320, может быть предусмотрен элемент 340 в виде вентилятора охлаждения, выполненный с возможностью реализации эффекта охлаждения так, что первый нагревательный блок 310 и второй нагревательный блок 320 установлены на разные температуры, и второй нагревательный блок может постоянно нагреваться первым нагревательным блоком за счет лучистого тепла и проводимого тепла.
Важно, что второй нагревательный блок 320 относительно поддерживается при второй температуре, например температуре отжига 55°С. Для этого на верхней части может быть предусмотрена структура рассеивающего охлаждения, выполненная с возможностью сведения к минимуму теплового взаимодействия с первым нагревательным блоком 310 и простого рассеивания избыточного тепла с использованием элемента в виде вентилятора охлаждения. В качестве примера, в настоящем изобретении второй нагревательный блок 320 может дополнительно содержать часть 321 в виде структуры для управления температурой, реализованную на боковой части второй прижимной поверхности G2. Часть 321 в виде структуры для управления температурой имеет конструкцию, в которой на верхней части реализовано множество выступающих структур, и, таким образом, возможно повысить эффективность рассеивания тепла путем увеличения площади поверхности контакта с воздухом, что является преимущественным для поддержания постоянной низкой температуры.
В отличие от способа перемещения реакционного образца для реализации реакции PCR или перемещения реакционного образца в другую зону нагрева путем установки времени согласно настоящему изобретению, описанному выше, конструкцию нагревательных блоков применяют так, что температуру можно равномерно увеличивать одновременно в верхней части в состоянии, в котором реакционный образец неподвижен, и, таким образом, можно реализовать точную передачу первой температуры и второй температуры.
Дополнительно, в настоящем изобретении первый нагревательный блок 310 или второй нагревательный блок 320 предпочтительно соединен с модулем 330 привода, который реализует горизонтальное перемещение или вертикальное перемещение. Модуль 330 привода содержит направляющие элементы 331 и 332, проходящие через первый нагревательный блок 310 и второй нагревательный блок 320, и первый нагревательный блок 310 и второй нагревательный блок 320 могут перемещаться в вертикальном направлении по направляющим элементам 331 и 332.
То есть в настоящем изобретении первый нагревательный блок 310 и второй нагревательный блок 320 расположены на расстоянии друг от друга и сходятся друг с другом в соответствии с работой модуля 330 привода для реализации вертикального перемещения. Кроме того, предпочтительно под направляющими элементами 331 и 332 дополнительно предусмотрены упругие элементы S1 и S2, и, таким образом, когда нагревательный блок прикладывает давление к планшету для PCR, обеспечивается соответствующее упругое усилие для реализации демпфирования (см. фиг.5).
Дополнительно, в одном варианте осуществления настоящего изобретения может быть дополнительно предусмотрена пластина 350 постоянной температуры, соединенная с вышеописанным модулем управления температурой.
Дополнительно, в одном варианте осуществления настоящего изобретения может быть дополнительно предусмотрена пластина 350 постоянной температуры, соединенная с вышеописанным модулем управления температурой.
Как проиллюстрировано на фиг.2 и 3, пластина 350 постоянной температуры расположена под конструкциями нагревательных блоков 310 и 320, составляющих модуль 300 управления температурой, и после вхождения планшета 200 для PCR, в случае, когда первый нагревательный блок 310 или второй нагревательный блок 320 модуля 300 управления температурой перемещается в горизонтальном направлении и вертикальном направлении для приложения давления к планшету для PCR в верхней части, пластина 350 постоянной температуры может иметь такую же температуру, как у первого нагревательного блока 310 или второго нагревательного блока 320.
Для этого пластина 350 постоянной температуры может дополнительно содержать модуль 400 привода, горизонтального перемещения, который перемещается в горизонтальном направлении к нижней части планшета 200 для PCR.
Для этого пластина 350 постоянной температуры может дополнительно содержать модуль 400 привода, горизонтального перемещения, который перемещается в горизонтальном направлении к нижней части планшета 200 для PCR.
Как проиллюстрировано на фиг.2 и 3, модуль 400 привода горизонтального перемещения может содержать движущий стержень 420 и блок 410приводного двигателя, соединенный с одним концом пластины 350 постоянной температуры, и преобразующую пластину 430, которая преобразует вращательное усилие блока 410 приводного двигателя в усилие горизонтального перемещения движущего стержня 420.
Модуль 400 привода горизонтального перемещения обеспечивает возможность горизонтального перемещения пластины 350 постоянной температуры в направлении вниз описанного выше модуля 300 управления температурой. В частности пластина 350 постоянной температуры согласно варианту осуществления настоящего изобретения может быть разделена на первую область, нагретую до первой температуры, и вторую область, которая расположена на расстоянии от первой области и нагрета до второй температуры (см. описания фиг.21-23).
В частности в иллюстративном варианте осуществления настоящего изобретения модуль 300 управления температурой и пластина 350 постоянной температуры могут быть объединены друг с другом при помощи направляющих элементов 331 и 332.
То есть при приведении в действие модуля 400 привода горизонтального перемещения модуль 300 управления температурой и содержащиеся в нем пластина 350 постоянной температуры и нагревательные блоки 310 и 320 могут перемещаться совместно.
В этом случае пластина 350 постоянной температуры содержит первую область, нагретую до первой температуры, и вторую область, которая расположена на расстоянии от первой области и нагрета до второй температуры, первая прижимная поверхность G1 первого нагревательного блока 310 расположена так, чтобы соответствовать верхней части первой области, и планшет 200 для PCR расположен между пластиной 350 постоянной температуры и нагревательными блоками 310 и 320 сверху вниз, вследствие чего приложение давления может быть достигнуто одновременно и при одной и той же температуре.
То есть в варианте осуществления настоящего изобретения пластина 350 постоянной температуры разделена на области, характеризующиеся градиентом первой температуры и второй температуры. Соответственно, когда нагревательный блок прикладывает давление при помощи модуля 400 привода горизонтального перемещения, область, имеющая установленную температуру (первую температуру или вторую температуру), соответствующую температуре нагревательного блока, перемещается в горизонтальном направлении для соответствующего скольжения, одновременно выполняется приложение контактного давления в отношении верхней и нижней поверхностей планшета для PCR, и, таким образом, возможно получить удвоенную эффективность по сравнению со способом, в котором пластина постоянной температуры поддерживается при одной температуре.
На фиг.4 показан вид в поперечном разрезе модуля управления температурой, изображенного на фиг.3, при рассмотрении сзади, и на фиг.5 показан вид в поперечном разрезе модуля управления температурой при рассмотрении спереди.
Как описано выше, модуль 300 управления температурой согласно настоящему изобретению содержит модуль 330 привода, который реализует горизонтальное перемещение или вертикальное перемещение первого нагревательного блока 310 и второго нагревательного блока 320 так, что работу модуля нагрева можно автоматизировать.
Со ссылкой на фиг.2 5, модуль 330 привода выполняет операцию вертикального перемещения первого нагревательного блока 310 и второго нагревательного блока 320, и в то же время модуль 400 привода горизонтального перемещения перемещает первый нагревательный блок 310 и второй нагревательный блок 320 в горизонтальном направлении так, что часть, находящаяся в контакте с поверхностью реакционной лунки на планшете 200 для PCR, может быть заменена первой прижимной поверхностью G1 или второй прижимной поверхностью G2.
Первый нагревательный блок 310 и второй нагревательный блок 320 расположены рядом в состоянии нахождения на расстоянии друг от друга, при этом направляющие канавки 312 и 322 (см. фиг.2) предусмотрены для прохождения через первый нагревательный блок 310 и второй нагревательный блок 320, и первый нагревательный блок 310 и второй нагревательный блок 320 закреплены на направляющих элементах 331 и 332, проходящих через направляющую канавку. Соответственно, первый нагревательный блок 310 и второй нагревательный блок 320 выполняют вертикальное перемещение по направляющим элементам 331 и 332, и к планшету для PCR может прикладываться давление сверху.
Разумеется, в этом случае пластина 350 постоянной температуры расположена под первым нагревательным блоком 310 и вторым нагревательным блоком 320, при этом нагревательные блоки, содержащие области, имеющие одинаковые температуры, такие как первая температура и вторая температура, соответствуют пластине 350 постоянной температуры, и, таким образом, к планшету для PCR давление может прикладываться сверху и снизу.
Как описано выше, в соответствии с модулем 300 управления температурой согласно настоящему изобретению во всей PCR-мишени в планшете 200 для PCR первую температуру и вторую температуру можно применять непосредственно ко всей поверхности планшета для PCR, и, таким образом, возможно реализовать превосходные эффекты в том, что касается скорости применения и эффективности реакции.
Дополнительно, конструкция нагревательного блока модуля 300 управления температурой расположена в верхней части, где горизонтальное перемещение возможно в любое время, и опускается только при создании давления совместно с планшетом для PCR.
С целью реализации такой конструкции может быть предусмотрен первый упругий элемент S1, который вставляется в приводную рамку и характеризуется возвращающим усилием, чтобы всегда приподниматься, когда к нему не прикладывается давление. В настоящем изобретении при реализации прижатия в контакте с планшетом 200 для PCR предусмотрен второй упругий элемент 335, который переносит прижимающее усилие для предотвращения избыточного приложения прижимающего усилия (см. фиг.5). Второй упругий элемент 335 в проиллюстрированном варианте осуществления реализован в виде конструкции пластинчатой пружины, которая оказывает постоянное демпфирующее усилие, когда первый и второй нагревательные блоки прижимаются в направлении вниз, вследствие чего к поверхности планшета для PCR не прикладывается избыточное прижимающее усилие.
Дополнительно, в конструкции системы согласно настоящему изобретению планшет 200 для PCR имеет конструкцию в форме пластины, в которой реакционная лунка реализована на верхней поверхности. В этом случае планшет 200 для PCR выполнен так, что он дополнительно содержит конструкцию пластины 350 постоянной температуры в нижней части для поддержания постоянной температуры, например диапазона второй температуры (например, 55°С).
Причиной этого является то, что при повышении температуры за счет прижатия модуля 300 управления температурой согласно настоящему изобретению к первому нагревательному блоку с первой температурой (например, 95°С) или при повышении температуры за счет прижатия модуля 300 управления температурой согласно настоящему изобретению ко второму нагревательному блоку со второй температурой (например, 55°С) внутренняя эффективность амплификации является намного большей только тогда, когда планшет 200 для PCR быстро достигает целевой температуры.
Поэтому в одном варианте осуществления настоящего изобретения, предпочтительно дополнительно предусмотрена пластина 350 постоянной температуры, которая расположена под планшетом 200 для PCR и поддерживает температуру планшета 200 для PCR при второй температуре.
В частности конструкция пластины 350 постоянной температуры предпочтительно установлена неподвижно и реализована так, что применяется постоянная установленная температура. Однако, как описано выше, пластина 350 постоянной температуры более предпочтительно разделена на области, в которых применена первая температура и вторая температура, и пластина постоянной температуры может перемещаться в горизонтальном направлении.
На фиг.6 показан вид, иллюстрирующий состояние, в котором пластина 350 постоянной температуры перемещается в горизонтальном направлении к нижней части модуля управления температурой при помощи модуля 400 привода горизонтального перемещения в конструкции, изображенной на фиг.2, и входит в контакт, и на фиг.7 проиллюстрировано состояние, в котором пластина постоянной температуры в ходе эксплуатации, как изображено на фиг.6, перемещается в горизонтальном направлении наружу для изменения области температуры.
То есть в конструкции, изображенной на фиг.6, когда первый нагревательный блок 310 расположен с возможностью применения первой температуры, первая область в пластине 350 постоянной температуры перемещается в горизонтальном направлении к нижней части планшета для PCR вместе с первым нагревательным блоком, и первый нагревательный блок 310 соответствует обращению к верхней поверхности планшета для PCR. Согласно этому, как проиллюстрировано на фиг.7, когда вторая область перемещается в горизонтальном направлении к нижней части планшета для PCR вместе со вторым нагревательным блоком, второй нагревательный блок перемещается в горизонтальном направлении и работает так, что он обращен к верхней поверхности планшета для PCR.
Операция горизонтального перемещения пластины 350 постоянной температуры может быть выполнена скользящим образом, и пластина 350 постоянной температуры может быть реализована с возможностью перемещения в контакте с лентой для скольжения, находящейся в контакте с частью боковой поверхности пластины 350 постоянной температуры.
Кроме того, со ссылкой на фиг.6 и 7, на фиг.6 и 7 показаны концептуальные виды, иллюстрирующие нижнюю часть модуля управления температурой согласно настоящему изобретению. Как проиллюстрировано на фиг.6 и 7, пластина 350 постоянной температуры может содержать множество сквозных светопропускающих частей h, которые расположены между планшетом 200 для PCR и нижним модулем сканирования (не проиллюстрирован, ссылочная позиция 500 на фиг.1), и облучается возбуждающим светом, излучаемым из модуля сканирования, для пропускания света к планшету 200 для PCR и направления света модуля 500 сканирования, чтобы обнаружить люминесценцию.
Поэтому в настоящем изобретении выделение нуклеиновой кислоты, процесс PCR и процесс обнаружения можно реализовать при помощи одной системы, при этом объединенная система оборудована вышеописанным сканером, а отдельная конструкция планшета для PCR может быть реализована так, что ее можно применять для диагностики различных заболеваний.
На фиг.8а проиллюстрирован один вариант осуществления планшета (200) для PCR в применении к настоящему изобретению, имеющего восемь реакционных лунок. На фиг.8b проиллюстрирован один вариант осуществления планшета (200) для PCR в применении к настоящему изобретению, имеющего десять реакционных лунок.
Со ссылкой на фиг.8а и вышеописанные концептуальные виды на фиг.2 и 3, планшет 200 для PCR согласно настоящему изобретению содержит часть 210 в виде корпуса, имеющую по меньшей мере одну реакционную лунку W1, …, Wn, в которой на поверхности в форме пластины размещен сухой продукт с праймером, и конструкцию, проходящую от одного конца части 210 в виде корпуса и вставленную в картридж 100 для выделения нуклеиновой кислоты.
В частности может быть реализована конструкция, в которой реализована вставная часть 220, имеющая отверстие h1 для введения, в которое предварительная смесь для PCR вводится для введения из картриджа 100 для выделения нуклеиновой кислоты. Дополнительно, планшет 200 для PCR может быть реализован так, чтобы иметь соединительную часть, которая соединена с отверстием h1 для введения, и может иметь часть 231 в виде канала, предусмотренную на части в виде корпуса, подлежащей соединению с множеством реакционных лунок.
В частности планшет 200 для PCR содержит часть 210 в виде корпуса, в которой реализовано множество реакционных лунок W1, …, Wn, как проиллюстрировано на фиг.8а. В этом случае, в случае реакционной лунки в проиллюстрированной конструкции, конструкция реализована с наличием восьми реакционных лунок, но настоящее изобретение этим не ограничено. То есть может быть реализована конструкция, имеющая по меньшей мере одну реакционную лунку, а конструкция реакционной лунки также может быть реализована как конструкция с вогнутой структурой путем обработки поверхности части 210 в виде корпуса.
В частности в иллюстративном варианте осуществления настоящего изобретения, как проиллюстрировано на фиг.8а, предусмотрена разделительная структура 215, которая разделяет область реакционной лунки, чтобы выступать из области поверхности части 210 в виде корпуса, и в реакционной лунке диспергируются и смешиваются праймер, подготовленный в сухом состоянии в реакционной лунке, и предварительная смесь для PCR, введенная из картриджа для выделения нуклеиновой кислоты.
Дополнительно, планшет 200 для PCR содержит элемент в виде крышки (не проиллюстрирован), который герметизирует верхние части множества реакционных лунок, и элемент в виде крышки может быть изготовлен из прозрачного пленочного материала, характеризующегося светопропусканием.
При прижатии элемента в виде крышки к поверхности реакционной лунки для реализации внутренней части реакционной лунки в виде полости предварительная смесь для PCR, введенная из картриджа для выделения нуклеиновой кислоты, впоследствии толкает слой воздуха, присутствующий в полости, и вводится внутрь реакционной лунки.
В частности в настоящем изобретении, как проиллюстрировано в конструкции на фиг.8а, в части 210 в виде корпуса может быть предусмотрена часть 231 в виде канала, соединенная с реакционной лункой. Часть в виде канала может быть реализована так, чтобы проходить к дистальному концу 232 части в виде корпуса через часть 210 в виде корпуса от начальной точки части 231 в виде канала, соединенной с отверстием h1 для введения, и может быть реализована с возможностью соединения с оконечными частями множества реакционных отверстий в направлении противоположном вставной части на дистальном конце 232.
То есть, как на фиг.2, когда картридж для выделения нуклеиновой кислоты вставляется через отверстие h1 для введения, предусмотренное под вставной частью, канал реализован в направлении x1, пересекающем часть в виде корпуса от начальной точки части 231 в виде канала, и канал разветвляется влево и вправо в конечной точке части в виде корпуса с возможностью соединения с впускным отверстием в каждую реакционную лунку. Причиной для образования канала таким образом является то, что внутри области реакционной лунки, герметизированной элементом в виде крышки, присутствует небольшое количество воздуха, при этом заполнение вводимой предварительной смесью для PCR происходит от нижней области Cb относительно средней линии сх части в виде корпуса, как проиллюстрировано в конструкции на фиг.8а, и слой воздуха выталкивается в верхнюю область Са части в виде корпуса.
Поэтому смесь, в которой должна выполняться реакция PCR, относительно расположена в нижней области Cb реакционной лунки, и, таким образом, область, в которой нагревательный блок согласно настоящему изобретению выполняет приложение давления, и, вследствие характеристик устройства, область, в которой выполняется обнаружение модулем сканера, реализованы в нижней области Cb, как проиллюстрировано на фиг.8а. Соответственно, возможно повысить все из точности обнаружения, эффективности реакции PCR и эффективности управления температурой.
Дополнительно, в настоящем изобретении планшет 200 для PCR предпочтительно реализован из материала на основе синтетической смолы, имеющего высокое светопропускание. Это предназначено для повышения эффективности обнаружения за счет выполнения модуля сканера из материала, имеющего высокое светопропускание, в соответствии с функцией вышеописанного модуля сканера.
Такие материалы могут включать различные материалы на основе синтетических смол, такие как полипропилен (РР), полиэтилен (РЕ), полифталамид (РРА), полиметилметакрилат (РММА) и поликарбонат (PC), но они необязательно ограничены этими материалами, и можно использовать любой материал до тех пор, пока материал может обеспечивать определенное светопропускание.
Однако планшет 200 для PCR может сохранять постоянную температуру вследствие наличия источника тепла, применяемого от пластины постоянной температуры в нижней части, и для эффективного поддержания температуры, которую модуль управления температурой непосредственно применяет к предварительной смеси для PCR, раствору нуклеиновой кислоты, сухому праймеру/зонду или реагирующему веществу для PCR, содержащему эти компоненты, которые заполняют внутреннюю часть реакционной лунки, при этом толщина части 210 в виде корпуса может быть реализована в диапазоне от 1,0 мм до 3,0 мм. Когда толщина составляет менее 1,0 мм, высокотемпературное тепло, устанавливающее первую температуру, легко переносится к нижней части корпуса, что вызывает тепловое взаимодействие с пластиной постоянной температуры. Соответственно, управление температурой является непростым. Когда толщина превышает 3,0 мм, проще управлять температурой материала, размещенного в реакционной лунке. Однако непросто управлять температурой пластины постоянной температуры в нижней части, и, таким образом, трудно поддерживать постоянную температуру.
То есть в настоящем изобретении, как описано выше со ссылкой на фиг.4 и 5, первый нагревательный блок 310 и второй нагревательный блок 320 перемещаются в горизонтальном направлении, первая прижимная поверхность G1 или вторая прижимная поверхность G2, находящаяся в контакте с поверхностью реакционной лунки, входит в контакт с верхней поверхностью разделительной структуры 215, и элемент в виде крышки накрывает разделительную структуру и выполняет приложение давления, и установленная температура становится первой температурой или второй температурой для управления температурой реагирующего вещества.
Дополнительно, в случае циклического изменения температуры для планшета 200 для PCR в модуле управления температурой согласно конструкции, изображенной на фиг. 2 и 3, для повышения температуры до первой температуры первый нагревательный блок перемещается в горизонтальном направлении, чтобы быть обращенным к верхней поверхности планшета для PCR, и после горизонтального перемещения первой области пластины постоянной температуры вместе с первым нагревательным блоком первый нагревательный блок перемещается под нижнюю поверхность планшета для PCR и входит в прижимной контакт с нижней поверхностью планшета для PCR. Кроме того, с целью снижения температуры до второй температуры верхняя поверхность планшета 200 для PCR перемещается в горизонтальном направлении, чтобы быть обращенной ко второму нагревательному блоку, и после горизонтального перемещения второй области пластины постоянной температуры вместе со вторым нагревательным блоком второй нагревательный блок перемещается под нижнюю поверхность планшета 200 для PCR и входит в прижимной контакт с нижней поверхностью. Соответственно, верхнюю поверхность и нижнюю поверхность планшета 200 для PCR возможно нагревать и охлаждать одновременно. В настоящем изобретении пластина 350 постоянной температуры и первый и второй нагревательные блоки 310 и 320 реализованы с возможностью совместного горизонтального перемещения, и, таким образом, приложение давления к верхней части и нижней части планшета 200 для PCR выполняется одновременно и при одной температуре.
Вследствие этих действий за счет одновременного выполнения приложения контактного давления в отношении верхней и нижней поверхностей планшета для PCR возможно реализовать удвоенную эффективность по сравнению со способом, в котором пластина постоянной температуры поддерживается при одной температуре. Соответственно, нагрев планшета, содержащегося в мишени, реализуется одновременно на верхней и нижней поверхностях, и, таким образом, время проверки можно уменьшить наполовину.
На фиг.9-12 показаны схемы для подробного разъяснения конструкции и способа работы пластины постоянной температуры и модуля привода горизонтального перемещения.
На фиг.9 проиллюстрирована конструкция, в которой пластина 350 постоянной температуры закреплена, как изображено на фиг.2 и 3, и на фиг. 10 проиллюстрирована конструкция, в которой только пластина постоянной температуры является отдельной.
Со ссылкой на фиг.9 и 10, пластина 350 постоянной температуры согласно варианту осуществления настоящего изобретения расположена под конструкцией нагревательных блоков, составляющей модуль управления температурой, проиллюстрированный на фиг.2 и 3, и после расположения планшета 200 для PCR, когда первый нагревательный блок 310 или второй нагревательный блок 320 модуля 300 управления температурой прикладывает давление к планшету для PCR от верхней стороны путем горизонтального перемещения и вертикального перемещения, пластина 350 постоянной температуры может иметь такую же температуру, как у первого нагревательного блока 310 или второго нагревательного блока 320.
Как проиллюстрировано на фиг.9, пластина 350 постоянной температуры содержит разделительную часть SS, которая разделяет пластину 350 постоянной температуры на первую область a1, поддерживающую первую температуру, и вторую область а2, поддерживающую вторую температуру, и первая область a1 и вторая область а2 соединены одна с другой на основе обоих концов а3 и а4 разделительной части SS.
Для подачи питания или передачи управляющего сигнала, на одном конце пластины 350 постоянной температуры установлены соединительные конструкции Са и Cb.
В частности операция горизонтального перемещения пластины 350 постоянной температуры реализована скользящим образом и реализована для перемещения в контакте с лентой для скольжения, находящейся в контакте с боковой частью пластины 350 постоянной температуры. Соответственно, возможно реализовать упрощение конструкции, а также улучшить подвижность.
В этом случае во второй области а2 предусмотрено сквозное отверстие Н, для обеспечения возможности сканирования через него концентрации амплифицированного реагирующего вещества посредством обнаруживаемого света модуля 500 сканирования.
Для измерения температуры и управления температурой соответствующей области, в первой области a1 и второй области а2 могут быть предусмотрены датчики Sa и Sb температуры.
На фиг.11 показан вид, иллюстрирующий нижнюю поверхность, изображенную на фиг.10, в которой предусмотрена соединительная часть Сс и Cd для соединения для применения управляющего сигнала и подачи питания, предусмотрены датчики Sa и Sb температуры и, таким образом, возможна реализация поддержания постоянной температуры при первой температуре и второй температуре.
Для поддержания температур первой области или второй области пластины постоянной температуры можно использовать различные нагревательные элементы и способы установки различных элементов, таких как нагревательная проволока или нагреватель сопротивления, внутри пластины. Однако в иллюстративном варианте осуществления настоящего изобретения для достижения этого эффекта после реализации цепи электрода и датчика температуры на эпоксидной печатной плате и нанесения нагревательной краски между электродами металлические пластины, соответствующие первой и второй областям, приклеивают с возможностью прижатия к каждому датчику температуры и нагревательной краске.
На фиг.12 показан концептуальный вид сверху в плане для описания способа работы, более подробно описанного выше со ссылкой на фиг.6 и 7.
В настоящем изобретении может быть дополнительно предусмотрен модуль 400 привода горизонтального перемещения, который перемещает пластину 350 постоянной температуры в горизонтальном направлении к нижней части планшета 200 для PCR.
Как проиллюстрировано на фиг.2 и 3, как описано выше, модуль 400 привода горизонтального перемещения может содержать движущий стержень 420 и блок 410 приводного двигателя, которые соединены с одним концом пластины 350 постоянной температуры, и преобразующую пластину 430, которая преобразует вращательное усилие блока 410 приводного двигателя в усилие горизонтального перемещения движущего стержня 420.
Как проиллюстрировано на фиг.12, планшет 200 для PCR вставляют в картридж для выделения нуклеиновой кислоты, и он имеет соединенный с картриджем канал, при этом раствор нуклеиновой кислоты, извлеченный из картриджа 100 для выделения нуклеиновой кислоты, вводится в отверстие h1 для введения, и извлеченный раствор нуклеиновой кислоты перемещается в планшет 200 для PCR, в котором извлеченный раствор нуклеиновой кислоты вмещается с возможностью введения в по меньшей мере одну реакционную лунку, вмещающую сухую смесь для PCR, содержащую праймер, праймер/зонд или зонд праймера.
Затем первый нагревательный блок 310 или второй нагревательный блок 320 модуля 300 управления температурой согласно настоящему изобретению опускается к части в виде реакционной лунки планшета 200 для PCR с целью создания первой температуры или второй температуры.
В этом случае модуль 400 привода горизонтального перемещения перемещает в горизонтальном направлении вместе пластину 350 постоянной температуры и модуль 300 управления температурой, и планшет для PCR располагается с возможностью вставки между пластиной 350 постоянной температуры и модулем 300 управления температурой.
Когда нагревательный блок, перемещенный в горизонтальном направлении при помощи модуля 400 привода горизонтального перемещения, прикладывает давление к планшету для PCR, первая область или вторая область пластины постоянной температуры, имеющая установленную температуру (первую температуру или вторую температуру), соответствующую температуре нагревательного блока, естественным образом расположена в соответствии ему.
То есть, когда первая область a1 пластины 350 постоянной температуры перемещается в горизонтальном направлении к нижней части планшета 200 для PCR, первый нагревательный блок (310 на фиг.2) одновременно перемещается в горизонтальном направлении и соответствует обращению к верхней поверхности планшета для PCR, а затем нагревательный блок опускается для вхождения в контакт с верхней поверхностью планшета для PCR.
Дополнительно, когда вторая область а2 перемещается в горизонтальном направлении к нижней части планшета для PCR и располагается у нее, второй нагревательный блок (320 на фиг.2) одновременно перемещается в горизонтальном направлении и работает так, чтобы быть обращенным к верхней поверхности планшета для PCR, а затем нагревательный блок опускается для вхождения в контакт с верхней поверхностью планшета для PCR.
Иначе говоря, в случае циклического изменения температуры для планшета 200 для PCR, с целью повышения температуры до первой температуры первый нагревательный блок перемещается в горизонтальном направлении, чтобы быть обращенным к верхней поверхности планшета для PCR, и после горизонтального перемещения первой области пластины постоянной температуры первый нагревательный блок перемещается под нижнюю поверхность планшета для PCR и приводится в движение для вхождения в прижимной контакт с нижней поверхностью планшета для PCR.
Дополнительно, для снижения температуры вновь до второй температуры верхняя поверхность планшета 200 для PCR перемещается в горизонтальном направлении, чтобы быть обращенной ко второму нагревательному блоку, и после горизонтального перемещения второй области пластины постоянной температуры второй нагревательный блок перемещается под нижнюю поверхность планшета 200 для PCR и входит в прижимной контакт с этой нижней поверхностью. Соответственно, верхнюю поверхность и нижнюю поверхность планшета 200 для PCR возможно нагревать и охлаждать одновременно.
Таким образом, за счет одновременного выполнения приложения контактного давления в отношении верхней и нижней поверхностей планшета для PCR возможно реализовать удвоенную эффективность по сравнению со способом, в котором пластина постоянной температуры поддерживается при одной температуре.
В дальнейшем картридж 100 для выделения нуклеиновой кислоты, реализующий предварительную смесь для PCR, содержащую выделенную нуклеиновую кислоту, на планшете для PCR в настоящем изобретении будет описан со ссылкой на фиг.13-19.
На фиг.13 показан вид в перспективе картриджа для выделения нуклеиновой кислоты согласно настоящему изобретению и проиллюстрирована конструкция, в которую вставляют описанный выше планшет для PCR. На фиг.10 показан покомпонентный вид в перспективе изображения на фиг.9, и на фиг.11 проиллюстрирована внутренняя конструкция части R1 в виде крышки картриджа в конструкции, изображенной на фиг.10 (в настоящем варианте осуществления будет описана конструкция, в которой планшет для амплификации генов имеет две реакционные лунки).
Со ссылкой на фиг.13-15, картридж 100 для выделения нуклеиновой кислоты согласно настоящему изобретению может содержать часть R1 в виде крышки картриджа, имеющую множество вмещающих частей 22, 23, 24, 25 и 26, которые разделены на части для хранения растворов, необходимых для выделения ДНК, и часть R2 в виде корпуса картриджа, которая соединена с частью R1 в виде крышки картриджа способом вставки и содержит часть 11 для проведения реакции для проведения реакции раствора, введенного из вмещающих частей, с образцом или очистки раствора.
В этом случае может быть предусмотрен поршень 18, который вводит предварительную смесь для PCR, очищенную в части 11 для проведения реакции, в отверстие hi для введения планшета 200 для PCR, который соединен для вставки в часть R2 в виде корпуса картриджа.
Работа картриджа для выделения нуклеиновой кислоты согласно настоящему изобретению будет описана со ссылкой на фиг.14, 15 и 17. На фиг.16 показан вид в перспективе изображения на фиг.13, иллюстрирующий внутреннюю конструкцию после соединения.
В картридже для выделения нуклеиновой кислоты согласно настоящему изобретению на нижней поверхности части R2 в виде корпуса картриджа установлен поворотный клапан 19, имеющий образованный внутри него канал 19-1, и при повороте поворотного клапана вмещающие части 11, 12, 13, 14, 15, 16 и 17 части R2 в виде корпуса картриджа могут соединяться с каналом поворотного клапана 19. После соединения канала с конкретной вмещающей частью поршень 18 приводится в действие для забора раствора, содержащегося во вмещающей части, и, таким образом, раствор переносится в другую вмещающую часть или планшет 200 для PCR.
Со ссылкой на фиг.14 и 15, вмещающие части 22, 23, 24, 25 и 26, содержащие каждый раствор, необходимый для выделения ДНК, образованы внутри части R1 в виде крышки картриджа, и нижняя поверхность каждой из вмещающих частей герметизирована пленкой или т.п. и выполнена с возможностью легкого проникновения проникающей иглы (10-1 на фиг.12) вмещающей части основного корпуса. Дополнительно образованы пять отверстий 21-1, 21-2, 27, 28 и 29.
В первой вмещающей части 22 части R1 в виде крышки картриджа размещен буфер для связывания, во второй вмещающей части 23 размещен первый очищающий буфер, в третей вмещающей части 24 размещен второй очищающий буфер, в четвертой вмещающей части 25 размещен третий очищающий буфер, и в пятой вмещающей части 26 размещен элюирующий буфер.
Планшет 200 для PCR накрыт пленкой, образованной из прозрачного пластмассового материала (полиэтилена, полипропилена, PET или т.п.), и сухой праймер/зонд для PCR или смесь для PCR, содержащая эти компоненты, содержится внутри реакционной лунки, которая является такой же, как конструкция, изображенная на фиг.8а, описанной выше.
Эксплуатация картриджа для выделения нуклеиновой кислоты согласно настоящему изобретению может происходить в следующем порядке.
1. Ввод биологического образца
Часть R2 в виде корпуса картриджа, часть R1 в виде крышки картриджа и планшет 200 для PCR установлены в автоматизированном оборудовании, которое будет писано далее в объединенном состоянии, и биологический образец (кровь) вводится в первое отверстие 21-1, проиллюстрированное на фиг.14.
2. Выделение нуклеиновой кислоты из клетки и связывание с микроносителем
Как проиллюстрировано на фиг.17, буфер для связывания из первой вмещающей
части 22 вводится в часть 11 для проведения реакции путем поворота поворотного клапана 19 и приведения в действие поршня 18, расположенного в нижней части части R2 в виде корпуса картриджа, и смешивается с биологическим образцом и микроносителем (магнитным микроносителем, покрытым кремнеземом) из магнитной таблетки (МТ).
МТ, используемая в настоящем изобретении, установлена на дистальном конце сквозной трубки, проходящей внутрь части 11 для проведения реакции части R2 в виде корпуса картриджа, и нуклеиновая кислота, выделенная из клеток, содержащихся в биологическом образце, предназначена для связывания нуклеиновой кислоты с поверхностью магнитного микроносителя, диспергированного путем растворения магнитной таблетки.
В этом случае вместо магнитной таблетки магнитные микроносители можно диспергировать в буфере для связывания и использовать.
После этого, когда в герметизированное второе отверстие 21-2 части R2 в виде корпуса картриджа вводится ультразвуковая насадка и применяются ультразвуковые волны, ультразвуковые волны передаются через пластмассу, биологический образец, таблетка и буфер для связывания смешиваются с целью гомогенизации реакционного раствора, в этот момент времени биологические ткани, содержащиеся в биологическом образце, также разрушаются для высвобождения нуклеиновой кислоты, и высвобождающаяся нуклеиновая кислота связывается с поверхностью микроносителя.
При введении магнитного стержня в третье отверстие 27 части R2 в виде корпуса картриджа микроносители прикрепляются к стенке части для проведения реакции, а остальной реакционный раствор переносится в первую вмещающую часть путем поворота поворотного клапана и приведения в действие поршня.
3. Первая очистка
Первый очищающий буфер из второй вмещающей части 23 вводится в часть 11 для проведения реакции путем поворота поворотного клапана части R2 в виде корпуса картриджа и приведения в действие поршня, проиллюстрированного на фиг.16, и смешивается с микроносителями, связанными с нуклеиновой кислотой.
Затем, после извлечения магнитного стержня из третьего отверстия 27, изображенного на фиг.14, и применения ультразвуковых волн к ультразвуковой насадке во втором отверстии 21-2 выполняется первая очистка. В результате первой очистки удаляются неспецифично связанные с микроносителями вещества, отличные от нуклеиновых кислот.
Магнитный стержень вводится в третье отверстие 27 так, что микроносители прикрепляются к поверхности стенки части для проведения реакции, и первичная очищающая жидкость переносится во вторую вмещающую часть 23 путем поворота поворотного клапана и приведения в действие поршня.
4. Вторая очистка
Второй очищающий буфер из третьей вмещающей части 24 вводится в часть 11 для проведения реакции путем поворота поворотного клапана части R2 в виде корпуса картриджа, проиллюстрированной на фиг.16, и приведения в действие поршня, и смешивается с микроносителями, связанными с нуклеиновой кислотой.
Затем, после извлечения магнитного стержня из третьего отверстия 27, изображенного на фиг.14, и применения ультразвуковых волн к ультразвуковой насадке второго отверстия 21-2 выполняется вторичная очистка. В результате этой второй очистки удаляются неспецифично связанные с микроносителями вещества, отличные от нуклеиновых кислот.
Магнитный стержень вводится в третье отверстие 27 так, что микроносители прикрепляются к стенке части для проведения реакции, и вторичная очищающая жидкость переносится в третью вмещающую часть 24 путем поворота поворотного клапана и приведения в действие поршня.
5. Третья очистка
Третий очищающий буфер из четвертой вмещающей части 25 вводится в часть 11 для проведения реакции путем поворота поворотного клапана части R2 в виде корпуса картриджа, проиллюстрированной на фиг.16, и приведения в действие поршня, и смешивается с микроносителями, связанными с нуклеиновой кислотой.
Затем, после извлечения магнитного стержня из третьего отверстия 27, изображенного на фиг.14, и применения ультразвуковых волн к ультразвуковой насадке во втором отверстии 21-2 выполняется третья очистка. В результате третьей очистки удаляются неспецифично связанные с микроносителями вещества, отличные от нуклеиновых кислот.
Магнитный стержень вводится в третье отверстие 27 так, что микроносители прикрепляются к стенке части для проведения реакции, и третичная очищающая жидкость переносится в четвертую вмещающую часть 25 путем поворота поворотного клапана и приведения в действие поршня.
6. Элюирование нуклеиновой кислоты
Элюирующий буфер из пятой вмещающей части 26 вводится в часть 11 для проведения реакции путем поворота поворотного клапана части R2 в виде корпуса картриджа, проиллюстрированной на фиг.16, и приведения в действие поршня, и смешивается с микроносителями, связанными с нуклеиновой кислотой.
Затем, после извлечения магнитного стержня из третьего отверстия 27, изображенного на фиг.14, ультразвуковая насадка вводится во второе отверстие 21-2, и применяются ультразвуковые волны, при этом нуклеиновая кислота, связанная с поверхностью микроносителя, растворяется в элюирующем буфере.
7. Получение предварительной смеси для PCR
Магнитный стержень вводится в третье отверстие 27 так, что микроносители прикрепляются к стенке части для проведения реакции, выбирается поворот поворотного клапана и малого поршня, при этом элюирующий буфер с растворенной в нем нуклеиновой кислотой вводится в шестую вмещающую часть 17 с использованием малого поршня и смешивается с материалом для PCR (смесь полимеразы, дезоксирибонуклеозидтрифосфата (dNTP) или т.п.), размещенным в шестой вмещающей части, и, таким образом, получается предварительная смесь для PCR. Термин «предварительная смесь для PCR», используемый в настоящем изобретении, определяется и используется так, как воплощено в вышеописанных материалах. Вышеописанный процесс пропускается, когда реакция PCR предусматривает сухой праймер/зонд в каждой лунке планшета для PCR, и элюат нуклеиновой кислоты вводится непосредственно в планшет для PCR, как проиллюстрировано ниже.
8. Перенос в планшет для PCR
Предварительная смесь для PCR, полученная в шестой вмещающей части, вводится в планшет 200 для PCR путем поворота поворотного клапана части R2 в виде корпуса картриджа и приведения в действие поршня, проиллюстрированного на фиг.16, и смешивается с праймером/зондом, содержащимся в планшете 200 для PCR. В данном процессе введения, как проиллюстрировано на фиг.19, предварительная смесь для PCR перемещается по каналу Y поворотного клапана под давлением поршня 18 и вводится в отверстие hi для введения.
Затем в четвертое отверстие 29 вводится нагревательный стержень для нагрева покровной пленки части в виде впускного отверстия планшета для реакции PCR под давлением, и таким образом планшет для реакции PCR герметизируется.
9. Реакция PCR
Наконец, планшет 200 для PCR содержит выделенную нуклеиновую кислоту, полимеразу, dNTP, праймер/зонд и другие буферы из биологического образца.
Таким образом, реакция PCR выполняется путем приложения давления и применения тепла к планшету 200 для PCR при помощи описанного выше модуля управления температурой согласно настоящему изобретению.
На фиг.20-23 проиллюстрирована общая конструкция и схема устройства, составляющего описанную выше систему для PCR согласно настоящему изобретению.
Как проиллюстрировано на фиг.20, когда картридж 100 для выделения нуклеиновой кислоты установлен внутри системы для PCR согласно настоящему изобретению, описанный выше планшет 200 для PCR закреплен на боковой поверхности. Часть, в которой присутствует реакционная лунка, соответствующая части в виде корпуса планшета 200 для PCR, открыта наружу, и на ней расположен вышеописанный модуль 300 управления температурой.
На фиг.21 показан увеличенный вид компоновки соединения основной части согласно настоящему изобретению, изображенной на фиг.20, и на фиг.22 показан концептуальный вид вертикального разреза части, изображенной на фиг.21, для описания компоновки основных компонентов. На фиг.23 показан концептуальный боковой вид в перспективе и в разрезе по фиг.22.
Как проиллюстрировано на фиг.21-23, предварительная смесь для PCR, содержащая нуклеиновую кислоту, извлеченную из внутренней части картриджа 100 для выделения нуклеиновой кислоты согласно настоящему изобретению, вводится в планшет 200 для PCR, в котором реализована реакционная лунка. Первая прижимная поверхность G1, соответствующая поверхности реакционной лунки, реализована на верхней части планшета 200 для PCR, расположен первый нагревательный блок 310, поддерживаемый при помощи нагревательного элемента при температуре, требуемой для денатурации, и смежно расположен второй нагревательный блок 320, в котором с возможностью изменения реализована область, которая перемещается в горизонтальном направлении и прижимается. Соответственно, предварительная смесь для PCR, введенная в реакционную лунку, непосредственно нагревается нагревательным блоком для соответствия первой температуре 95°С, требуемой для денатурации, или второй температуре 55°С, требуемой для отжига.
Дополнительно, как проиллюстрировано на фиг.22 и 23, пластина 350 постоянной температуры расположена под планшетом 200 для PCR для поддержания температуры планшета 200 для PCR на постоянном уровне температуры.
Модуль 500 сканирования расположен под пластиной 350 постоянной температуры так, что свет L, излучаемый светоизлучающим элементом Е1, достигает планшета 200 для PCR через светопропускающий элемент Н пластины 350 постоянной температуры, и, таким образом, выполняется обнаружение флуоресценции.
В варианте осуществления настоящего изобретения, как описано выше, в случае повышения температуры путем прижатия к первому нагревательному блоку с первой температурой (например, 95°С) при помощи модуля управления температуры, или в случае прижатия ко второму нагревательному блоку со второй температурой (например, 55°С), становится намного проще управлять температурой внутренней реакции амплификации, когда планшет 200 для PCR поддерживается в постоянном диапазоне температур. Соответственно, постоянное поддержание температуры вышеописанной пластины постоянной температуры при второй температуре является очень важным фактором повышения надежности реакции. При повышении температуры планшета для PCR до 95°С, температура планшета для PCR может быстро достигать 95°С в течение 2-3 секунд путем повышения скорости теплопереноса за счет прижатия друг к другу блока с первой температурой и первой зоны постоянной температуры.
При выполнении RTPCR для обнаружения РНК-мишеней используется предварительная смесь для PCR или планшет для PCR, содержащий сухое вещество для реакции RT-PCR. После регулировки блока с низкой температурой до температуры реакции RT для прижатия к планшету для реакции PCR и поддержания прижатия в течение времени реакции RT, реакцию PCR можно выполнить после выполнения реакции обратной транскрипции.
Присутствие или отсутствие амплифицированной нуклеиновой кислоты или концентрацию амплифицированной нуклеиновой кислоты определяют при помощи реакции PCR, эту информацию можно использовать для диагностики, и в этом случае определения присутствия или отсутствия, или концентрации амплифицированной нуклеиновой кислоты можно достигнуть с использованием традиционного способа обнаружения нуклеиновой кислоты.
Например, можно использовать способ использования малой бороздки ДНК, который предполагает использование интеркалирующего красителя для ДНК, и SYBR Green, который представляет собой вводимый флуоресцентный краситель, способ сканирования компонент возбуждающего света в разных диапазонах длин волн и флуоресценции, соответствующей возбуждающему свету, с использованием зондов с разной флуоресценцией и присоединенных гасителей или т.п., но настоящее изобретение этим не ограничивается.
Выше настоящее изобретение описано на основе иллюстративного варианта осуществления, но техническая сущность настоящего изобретения им не ограничивается. То есть специалистам средней квалификации в данной области техники, к которой принадлежит настоящее изобретение, ясно, что в рамках объема, описанного в формуле изобретения, можно осуществить модификации или изменения, и модификации и изменения должны находиться в рамках объема приложенной формулы изобретения.
[Перечень ссылочных позиций]
100: картридж для выделения нуклеиновой кислоты
200: планшет для PCR
210: часть в виде корпуса
220: вставная часть
300: модуль управления температурой
310: первый нагревательный блок
320: второй нагревательный блок
330: модуль привода
340: элемент в виде вентилятора охлаждения
350: пластина постоянной температуры
400: модуль привода горизонтального перемещения
500: модуль сканирования
W: реакционная лунка.
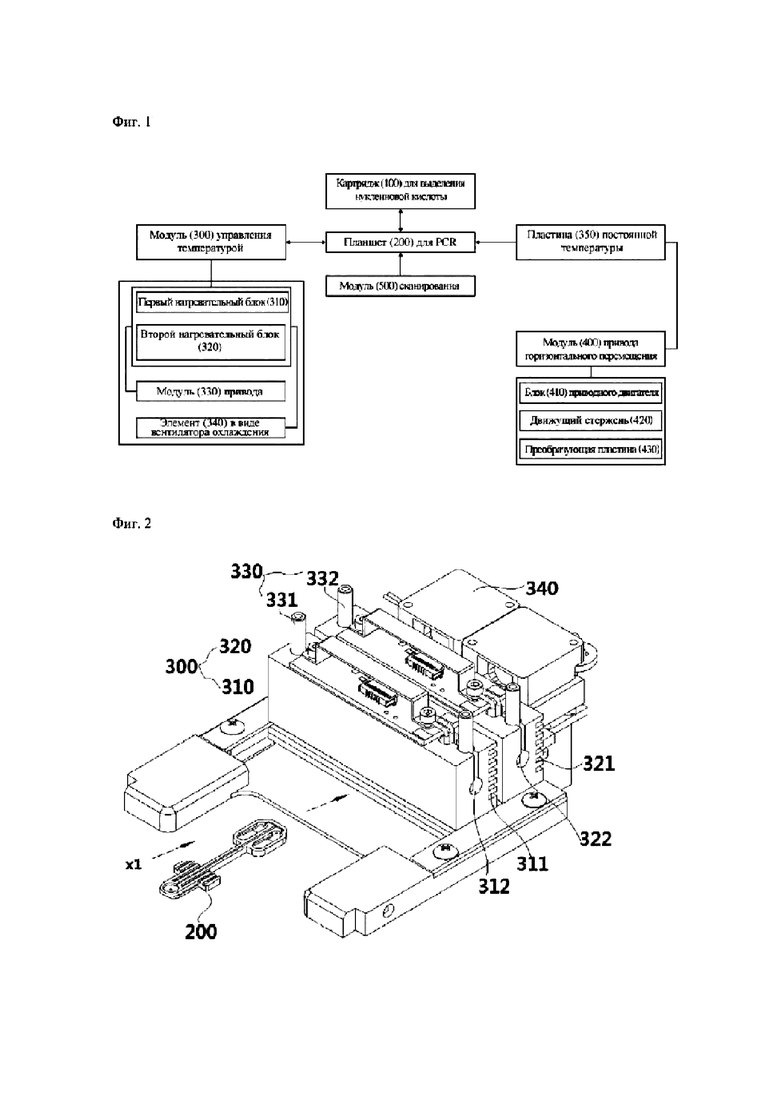
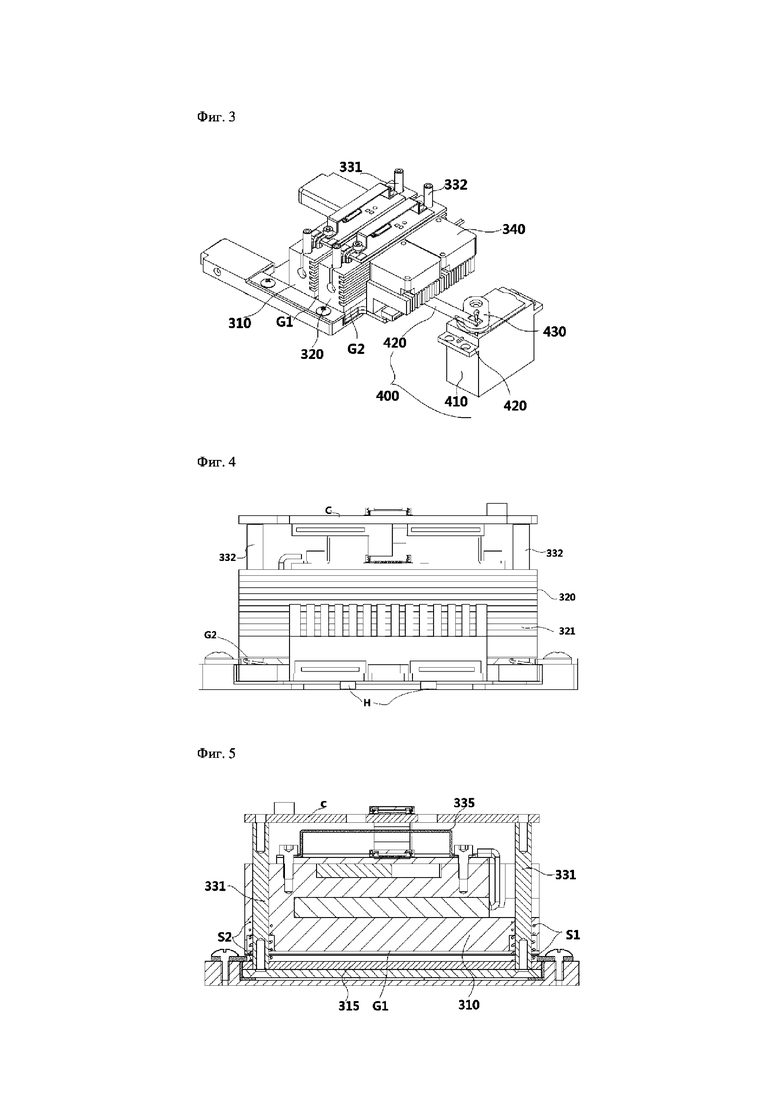
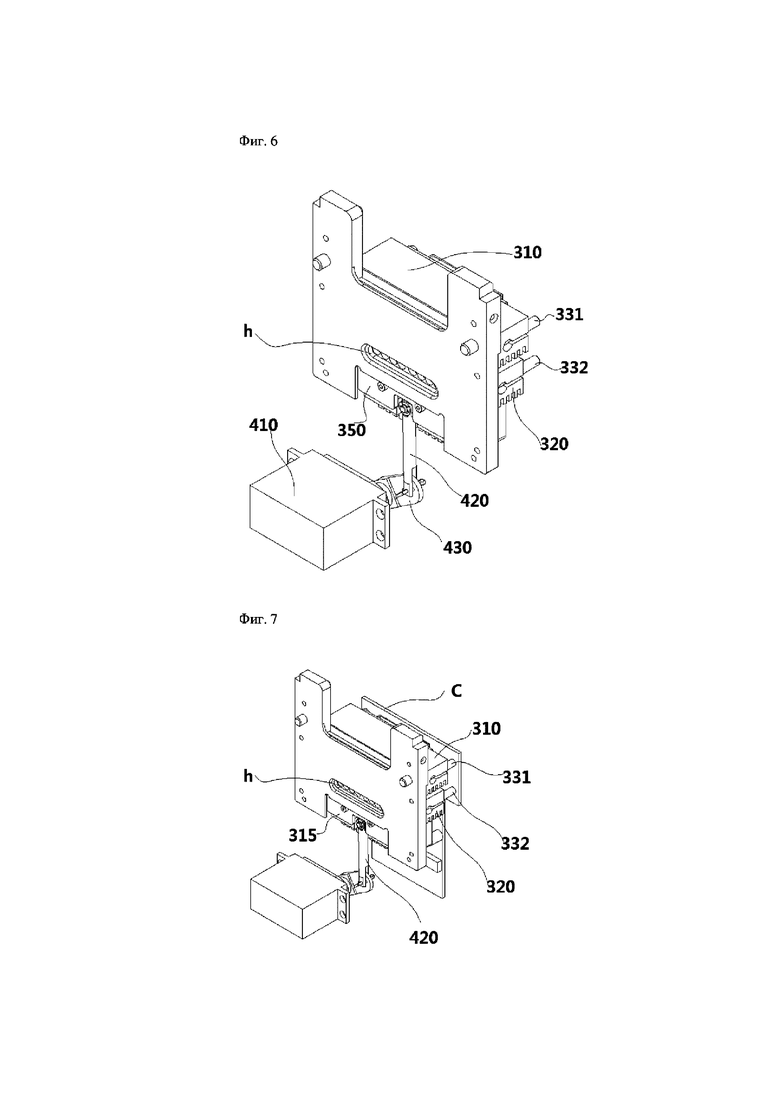
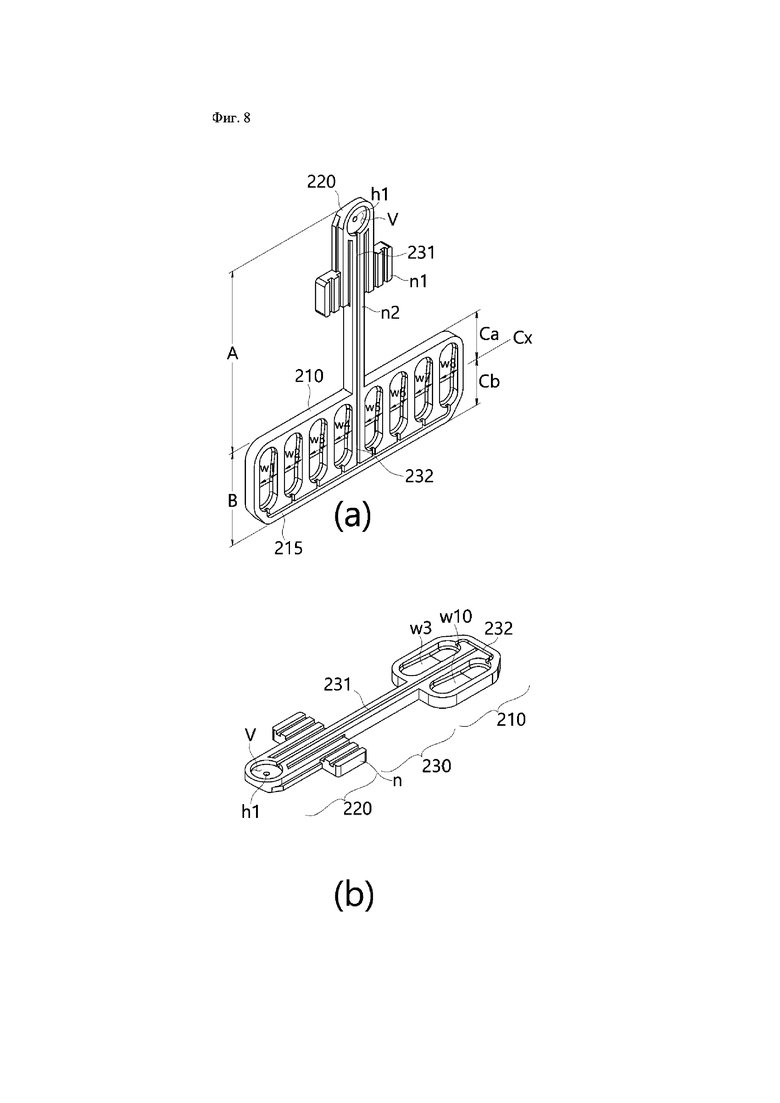
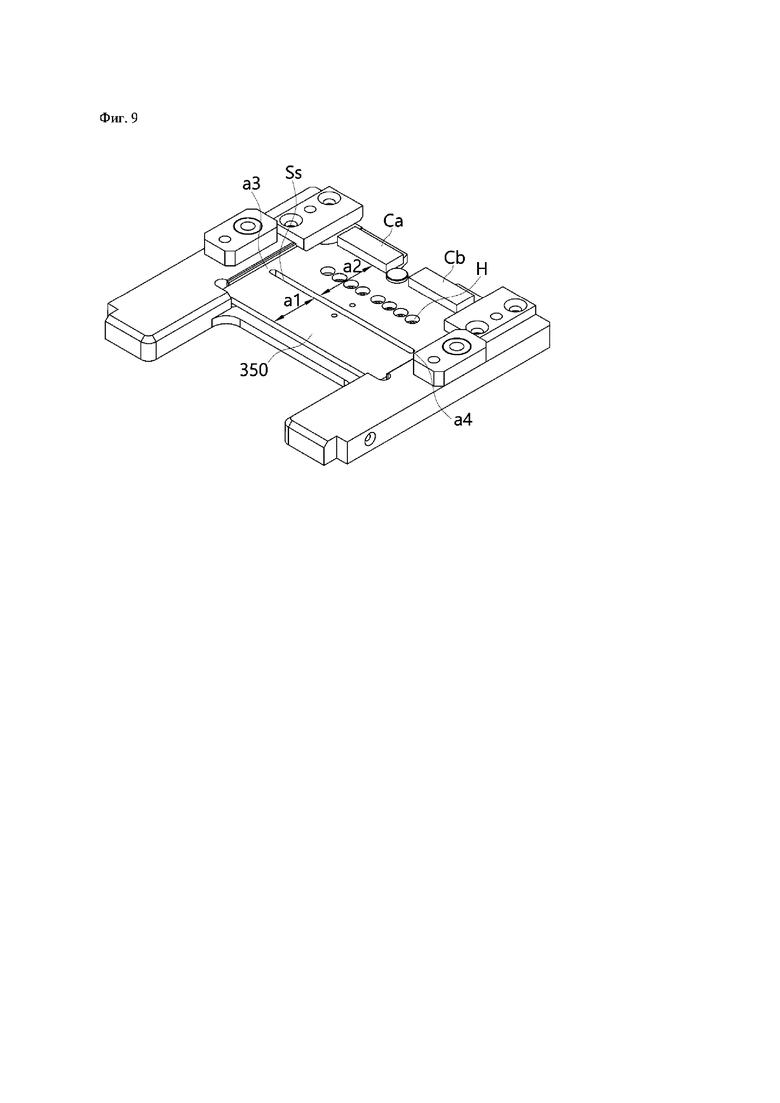
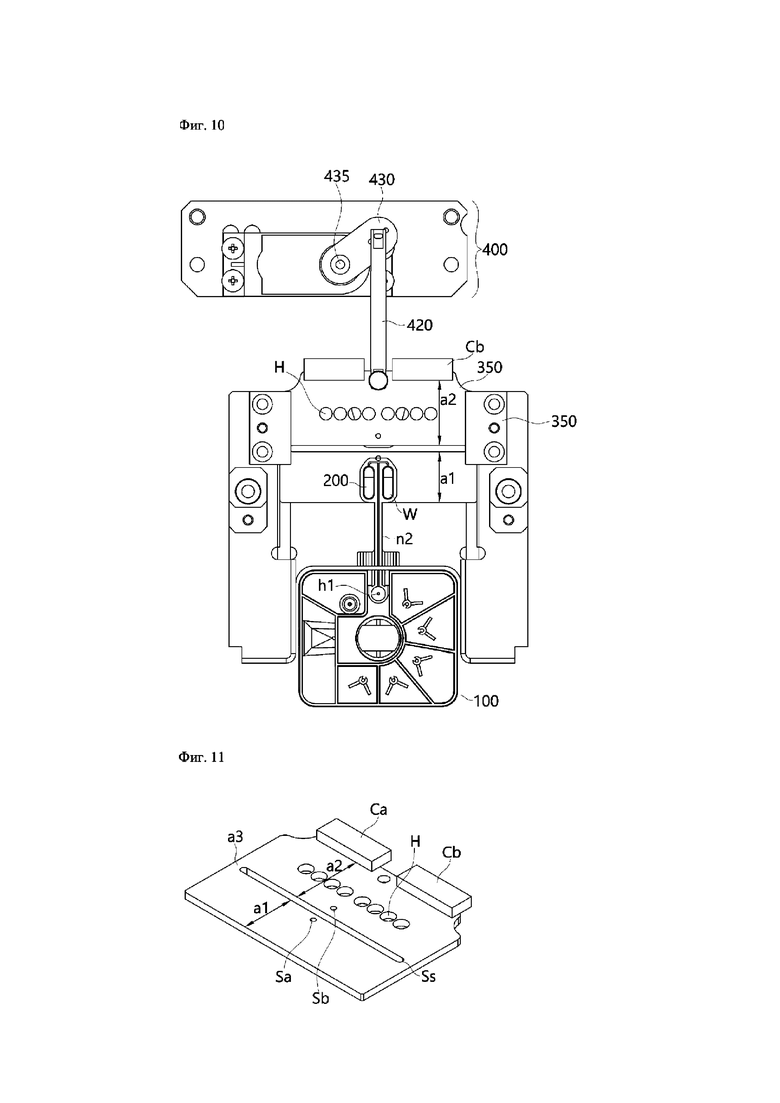
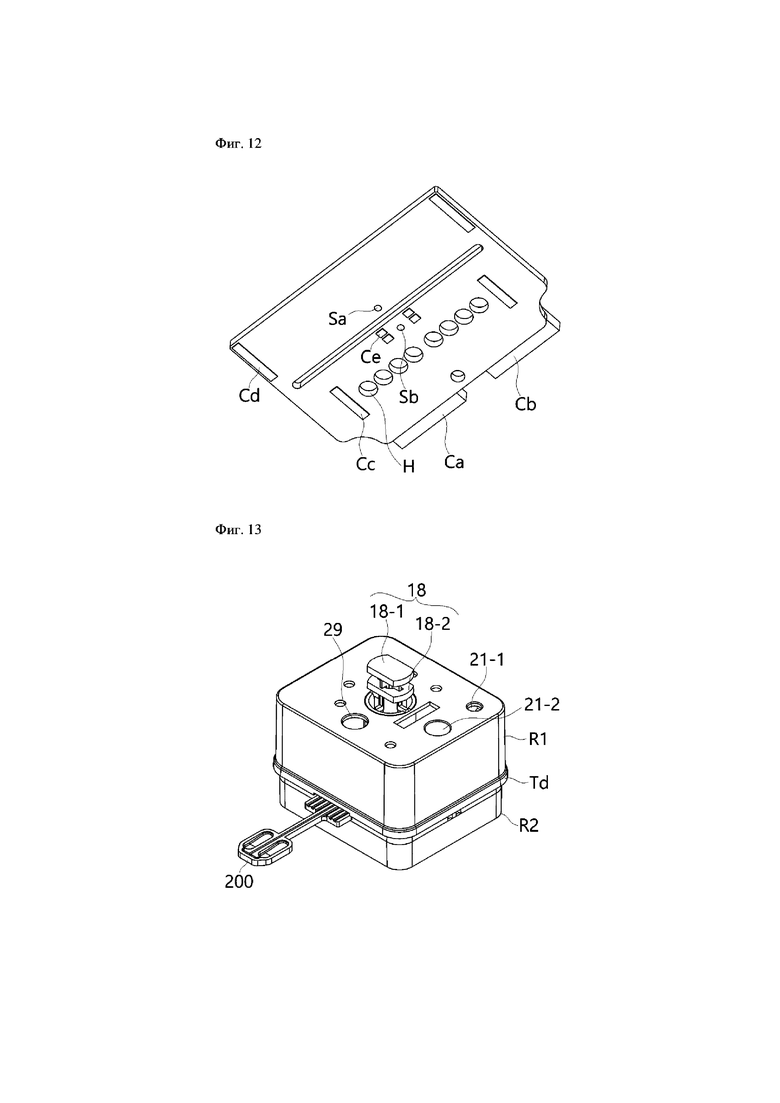
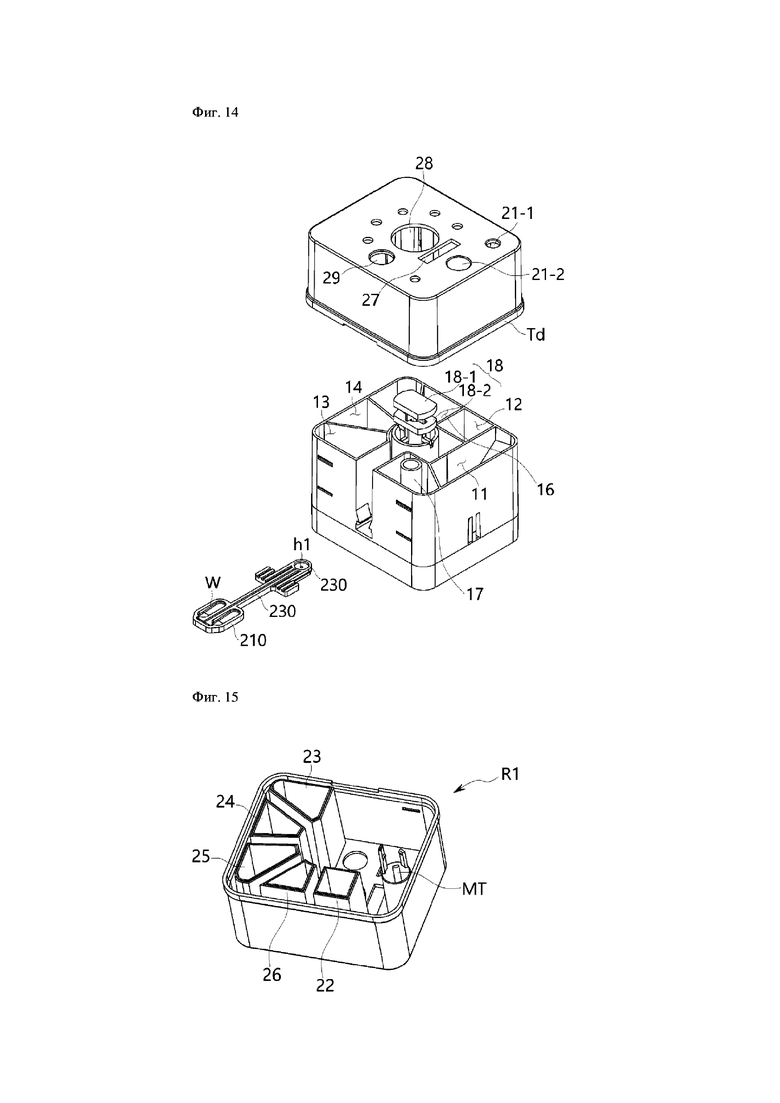
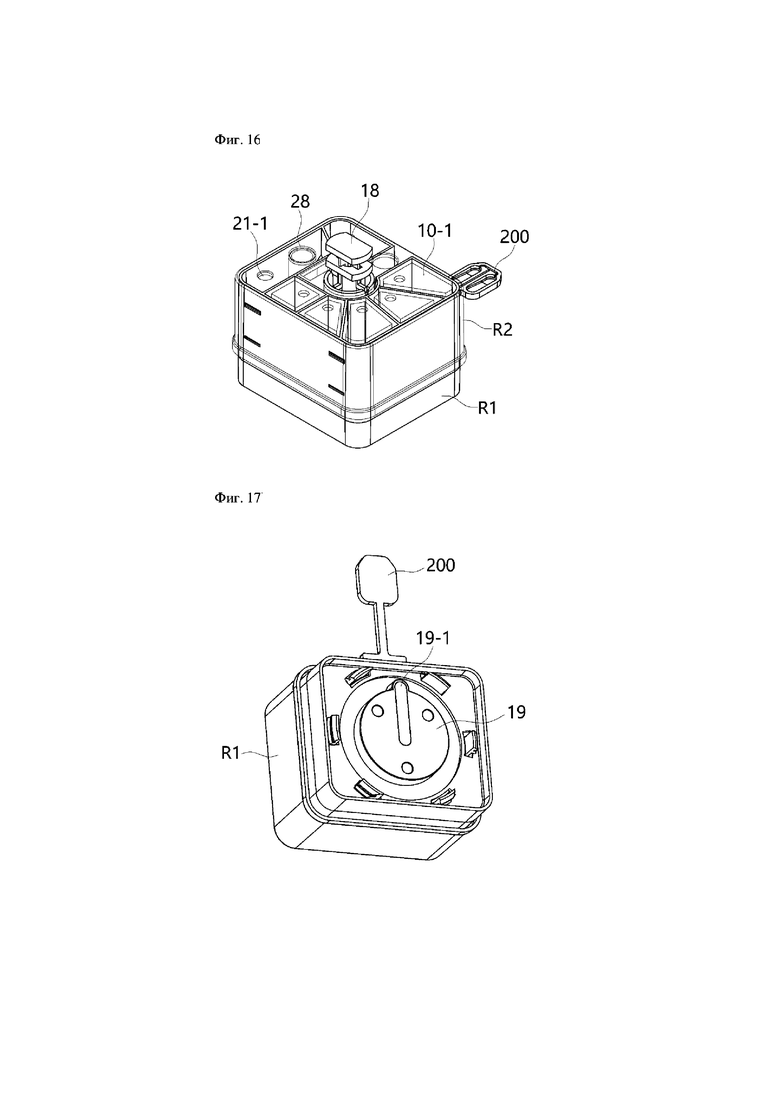
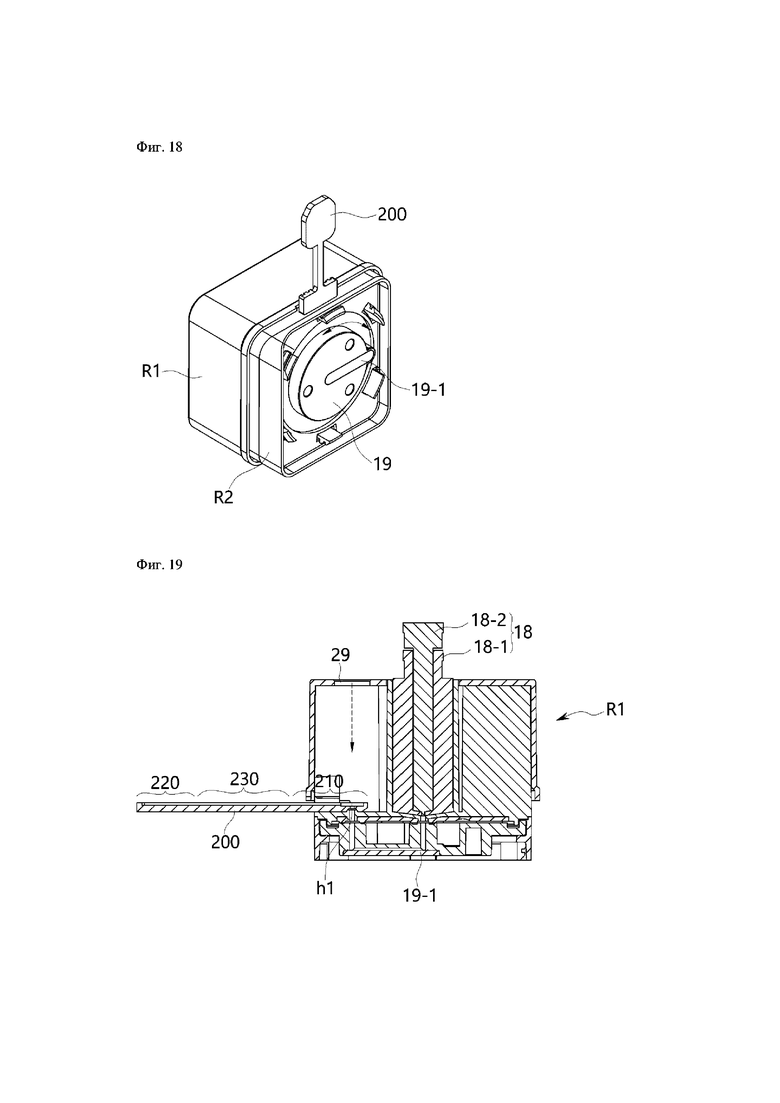

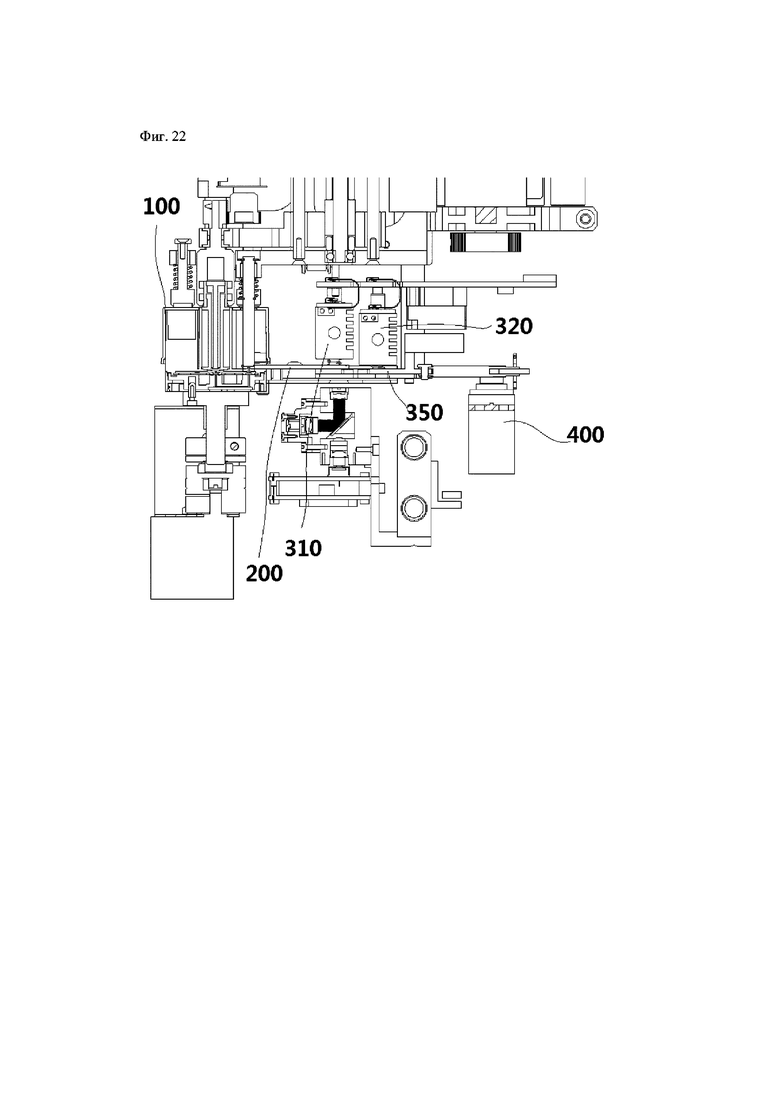
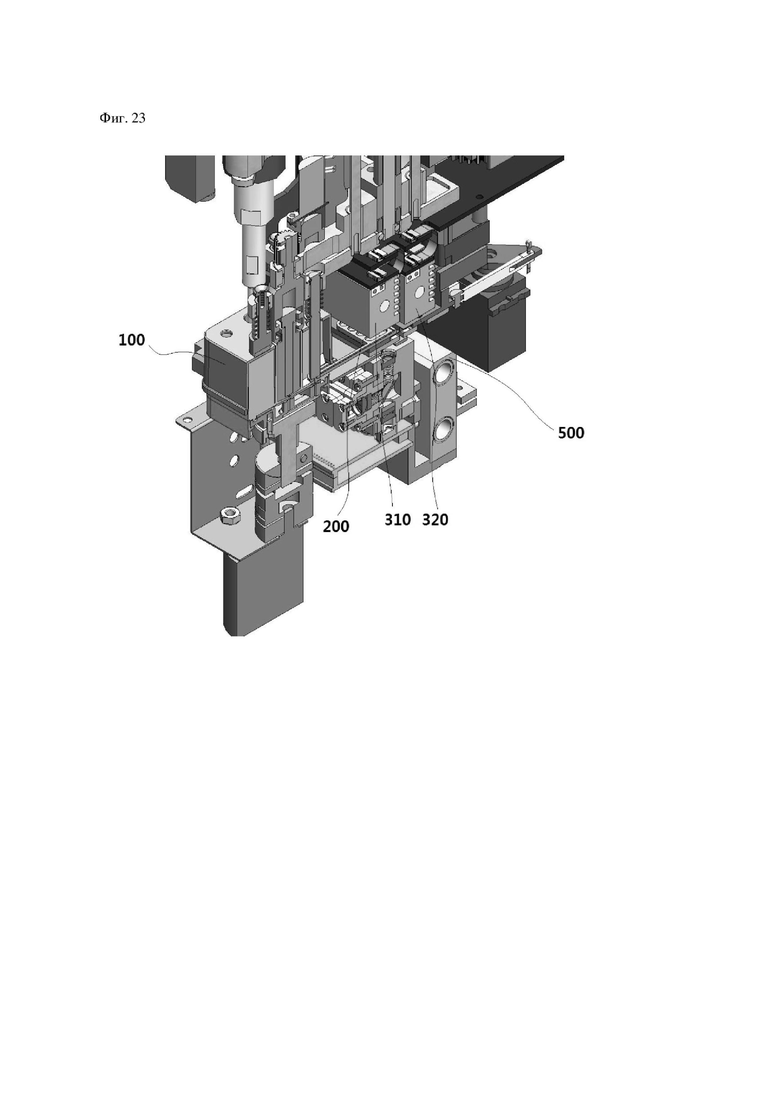
Изобретение относится к конструкции системы, выполненной с возможностью выполнения обнаружения в реальном времени реакций выделения и амплификации нуклеиновых кислот и амплифицированных результатов в устройстве для реализации полимеразной цепной реакции. Система для полимеразной цепной реакции (PCR) содержит: картридж для выделения нуклеиновой кислоты из биологического образца; планшет для PCR, имеющий канал, соединенный с картриджем для выделения нуклеиновой кислоты, и по меньшей мере одну реакционную лунку, которая вмещает сухую смесь для PCR, содержащую праймер, праймер/зонд или зонд-праймер, и принимает раствор нуклеиновой кислоты, извлеченный из картриджа; и модуль управления температурой, расположенный над планшетом для PCR смежно с реакционной лункой, имеющий пару нагревательных блоков, выполненных с возможностью перемещения в горизонтальном и вертикальном направлениях. Первый нагревательный блок содержит первую прижимную поверхность (G1), соответствующую поверхности реакционной лунки, и поддерживаемую при температуре, требуемой для денатурации. Второй нагревательный блок расположен в положении, соответствующем первому нагревательному блоку на расстоянии от него, содержит вторую прижимную поверхность (G2), соответствующую поверхности реакционной лунки и поддерживаемую при температуре, требуемой для отжига. Горизонтальные и вертикальные перемещения первого и второго нагревательных блоков обеспечивает модуль привода, расположенный в модуле управления температурой. Работа системы обеспечивает возможность быстрого и повторяющегося применения температуры, требуемой для процесса денатурации, и точной температуры, требуемой для отжига, в отношении мишени реакции в процессе управления температурой, необходимом для процесса PCR с целью выполнения быстрой и правильной PCR и максимального повышения надежности реакции. 2 н. и 17 з.п. ф-лы, 23 ил.
1. Система для полимеразной цепной реакции (PCR), содержащая:
картридж (100) для выделения нуклеиновой кислоты, выполненный с возможностью выделения нуклеиновой кислоты из биологического образца при помощи хранящегося в нем реагента для выделения нуклеиновой кислоты;
планшет (200) для PCR, имеющий канал, соединенный с картриджем для выделения нуклеиновой кислоты, и по меньшей мере одну реакционную лунку (W), которая вмещает сухую смесь для PCR, содержащую праймер, праймер/зонд или зонд-праймер, и принимает раствор нуклеиновой кислоты, извлеченный из картриджа (100) для выделения нуклеиновой кислоты; и
и модуль (300) управления температурой, расположенный над планшетом (200) для PCR смежно с реакционной лункой (W), для применения разных температур и имеющий пару нагревательных блоков (310, 320), которые выполнены с возможностью перемещения в горизонтальном и вертикальном направлениях, отличающаяся тем, что модуль (300) управления температурой содержит:
первый нагревательный блок (310), содержащий первую прижимную поверхность (G1), соответствующую поверхности реакционной лунки, и поддерживаемую при температуре (в дальнейшем называемой «первой температурой»), требуемой для денатурации;
второй нагревательный блок (320), расположенный в положении, соответствующем первому нагревательному блоку (310), и на расстоянии от первого нагревательного блока (310), содержащий вторую прижимную поверхность (G2), соответствующую поверхности реакционной лунки и поддерживаемую при температуре (в дальнейшем называемой «второй температурой»), требуемой для отжига; и
модуль (330) привода, выполненный с возможностью выполнения горизонтальных перемещений и вертикальных перемещений первого нагревательного блока (310) и второго нагревательного блока (320).
2. Система для PCR по п. 1, отличающаяся тем, что дополнительно содержит элемент (340) в виде вентилятора охлаждения, выполненный с возможностью управления проводимостью теплового излучения между первым нагревательным блоком (310) и вторым нагревательным блоком (320).
3. Система для PCR по п. 2, отличающаяся тем, что первый нагревательный блок (310) и второй нагревательный блок (320) расположены на расстоянии друг от друга и сходятся друг с другом в соответствии с работой модуля (330) привода для выполнения вертикального перемещения.
4. Система для PCR по п. 2, отличающаяся тем, что первый нагревательный блок (310) или второй нагревательный блок (320) дополнительно содержит часть (311, 321) в виде структуры охлаждения, образованную на одной его боковой поверхности.
5. Система для PCR по п. 2, отличающаяся тем, что первый нагревательный блок (310) и второй нагревательный блок (320) поддерживают установленную температуру на уровне первой температуры или второй температуры при помощи датчика температуры и нагревательного элемента.
6. Система для PCR по п. 2, отличающаяся тем, что модуль (330) привода содержит направляющий элемент (331, 332), проходящий через первый нагревательный блок (310) и второй нагревательный блок (320), и первый нагревательный блок (310) и второй нагревательный блок (320) выполняют вертикальное перемещение по направляющему элементу (331, 332).
7. Система для PCR по п. 5, отличающаяся тем, что дополнительно содержит упругий элемент (S1, S2), расположенный под направляющим элементом (331, 332).
8. Система для полимеразной цепной реакции (PCR), содержащая:
картридж (100) для выделения нуклеиновой кислоты, выполненный с возможностью выделения нуклеиновой кислоты из биологического образца при помощи хранящегося в нем реагента для выделения нуклеиновой кислоты;
планшет (200) для PCR, имеющий канал, соединенный с картриджем для выделения нуклеиновой кислоты, и по меньшей мере одну реакционную лунку (W), которая вмещает сухую смесь для PCR, содержащую праймер, праймер/зонд или зонд-праймер, и принимает раствор нуклеиновой кислоты, извлеченный из картриджа (100) для выделения нуклеиновой кислоты;
модуль (300) управления температурой, содержащий пару нагревательных блоков (310, 320), выполненных с возможностью горизонтального и вертикального перемещения для применения первой температуры и второй температуры, которые отличаются одна от другой, к верхней части планшета (200) для PCR, которая принимает раствор нуклеиновой кислоты и вмещает сухую смесь для PCR, содержащую праймер, праймер/зонд или зонд- праймер; и
пластину (350) постоянной температуры, расположенную под планшетом (200) для PCR для поддержания температуры планшета (200) для PCR на уровне первой температуры или второй температуры,
отличающаяся тем, что модуль (300) управления температурой содержит:
первый нагревательный блок (310), содержащий первую прижимную поверхность (G1), соответствующую поверхности реакционной лунки, и поддерживаемую при температуре (в дальнейшем называемой «первой температурой»), требуемой для денатурации;
второй нагревательный блок (320), расположенный в положении, соответствующем первому нагревательному блоку (310), и на расстоянии от первого нагревательного блока (310), содержащий вторую прижимную поверхность (G2), соответствующую поверхности реакционной лунки и поддерживаемую при температуре (в дальнейшем называемой «второй температурой»), требуемой для отжига; и
модуль (330) привода, выполненный с возможностью вертикальных перемещений первого нагревательного блока (310) и второго нагревательного блока (320).
9. Система для PCR по п. 8, отличающаяся тем, что пластина (350) постоянной температуры содержит первую область, нагретую до первой температуры, и вторую область, расположенную на расстоянии от первой области и нагретую до второй температуры, первая прижимная поверхность (G1) первого нагревательного блока (310) расположена так, чтобы соответствовать верхней части первой области, и вторая прижимная поверхность (G2) второго нагревательного блока (320) расположена так, чтобы соответствовать верхней части второй области.
10. Система для PCR по п. 9, отличающаяся тем, что модуль (300) управления температурой и пластина (350) постоянной температуры объединены друг с другом при помощи направляющего элемента (331, 332).
11. Система для PCR по п. 10, отличающаяся тем, что дополнительно содержит модуль (400) привода горизонтального перемещения, который перемещает в горизонтальном направлении пластину (350) постоянной температуры и модуль (300) управления температурой к нижней части планшета (200) для PCR.
12. Система для PCR по п. 9, отличающаяся тем, что пластина (350) постоянной температуры содержит разделительную часть (SS), разделяющую пластину (350) постоянной температуры на первую область и вторую область, и первая область и вторая область соединены на основе обоих концов разделительной части (SS).
13. Система для PCR по п. 9, отличающаяся тем, что пластина (350) постоянной температуры, датчик температуры и цепь нагревателя выполнены на печатной плате (РСВ), и металлические пластины, соответствующие одной из первой области и второй области, связаны так, что нагреватель и датчик температуры прижаты друг к другу.
14. Система для PCR по п. 9, отличающаяся тем, что пластина (350) постоянной температуры выполнена с возможностью горизонтального перемещения скользящим образом, и пластина (350) постоянной температуры выполнена с возможностью перемещения для вхождения в контакт с лентой для скольжения, находящейся в контакте с частью боковой поверхности пластины (350) постоянной температуры.
15. Система для PCR по п. 9, отличающаяся тем, что при перемещении первой области в горизонтальном направлении и расположении у нижней части планшета для PCR, первый нагревательный блок выполнен с возможностью перемещения от верхней стороны к нижней стороне, обращения к верхней поверхности планшета для PCR и прижатия, и при перемещении второй области в горизонтальном направлении и расположении у нижней части планшета для PCR, второй нагревательный блок выполнен с возможностью перемещения от верхней стороны к нижней стороне, обращения к верхней поверхности планшета для PCR и прижатия.
16. Система для PCR по п. 13, отличающаяся тем, что, при выполнении циклического изменения температуры в отношении планшета (200) для PCR, первый нагревательный блок выполнен с возможностью перемещения в горизонтальном направлении так, чтобы быть обращенным к верхней поверхности планшета для PCR, и нижняя поверхность планшета для PCR выполнена с возможностью перемещения под первый нагревательный блок после горизонтального перемещения первой области пластины постоянной температуры и приложения к ней давления для вхождения в контакт с первым нагревательным блоком с целью повышения первой температуры, верхняя поверхность планшета (200) для PCR выполнена с возможностью перемещения в горизонтальном направлении так, чтобы быть обращенной ко второму нагревательному блоку, и нижняя поверхность планшета для PCR выполнена с возможностью перемещения под второй нагревательный блок после горизонтального перемещения второй области пластины постоянной температуры и приложения к ней давления для вхождения в контакт со вторым нагревательным блоком с целью понижения второй температуры, и верхняя поверхность и нижняя поверхность планшета (200) для PCR выполнены с возможностью одновременного нагрева и охлаждения.
17. Система для PCR по п. 9, отличающаяся тем, что пластина (350) постоянной температуры дополнительно содержит датчик (Т1, Т2) температуры для измерения температуры пластины постоянной температуры в по меньшей мере одном местоположении и часть (351) в виде датчика температуры, содержащую модуль (Ср) управления для управления изменением установленной температуры.
18. Система для PCR по п. 9, отличающаяся тем, что содержит модуль (500) сканирования, который расположен под планшетом (200) для PCR и сканирует концентрацию реагирующего вещества, амплифицированного в реакционной лунке (W), с помощью компонент возбуждающего света при различных диапазонах длин волн и флуоресценции, соответствующей возбуждающему свету.
19. Система для PCR по п. 18, отличающаяся тем, что пластина (350) постоянной температуры содержит множество сквозных конструкций, имеющих светопропускающие части (Н), по которым направляется обнаруживаемый свет модуля (500) сканирования.
| JP 2010078493 A, 08.04.2010 | |||
| JP 0006206688 B2, 04.10.2017 | |||
| US 20150136604 А1, 21.05.2015 | |||
| СИСТЕМА ТЕРМОЦИКЛИРОВАНИЯ ДЛЯ ПРОВЕДЕНИЯ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2017 |
|
RU2658599C1 |
Авторы
Даты
2023-07-24—Публикация
2020-04-09—Подача