Изобретение относится к области медицины, а именно к нейрохирургии, экспериментальной медицине, регенеративной медицине, и может быть использовано для восстановления функций спинного мозга после его анатомического разрыва, пересечения или контузии.
Способ позволяет восстанавливать функциональную и морфологическую целостность спинного мозга после его и полного или частичного пересечения, а также при контузии и разрыве.
Известно, что при позвоночно-спинномозговой травме (ПСМТ) лечение повреждения позвоночника успешно проводится различными методами, с приемами установки имплантов и вертебральной стабилизации. Однако повреждение спинного мозга при ПСМТ зачастую приводит к неврологическому дефициту, сохраняющемуся без значительной динамики пожизненно [1].
Проблема восстановления спинного мозга обусловлена его тканевой организацией и каскадом патофизиологических процессов в месте травмы. В фазу первичного повреждения нервной ткани происходит массивный выброс нейромедиаторов из разрушенных клеток, которые обуславливают эффект эксайтотоксичности [2]. Это приводит к формированию тканевого отека, развитию локальной ишемии, нарушению микроциркуляторного русла, пропотеванию клеточных элементов крови в очаг поражения. Вторичное поражение, вызванное перечисленными процессами, в несколько раз превосходит размеры первичного повреждения, делая нервную ткань в этой области нежизнеспособной. Происходит активная гибель аксонов, развивается пролиферация глиального компонента, и глиальный конгломерат в дальнейшем претерпевает кистозную трансформацию, что уже является механическим барьером для восстановления спинного мозга [2].
В отношении ушибов спинного мозга чаще всего применяется консервативная тактика, а при повреждениях связанных с компрессией нервной ткани или повреждение твердой мозговой оболочки (ТМО), используется хирургический метод. Последний сводится к устранению сдавливающего фактора и восстановлению целостности ТМО. При этом само место травмы, с подвергшейся гибели нервной тканью и развивающимися патофизиологическими процессами оставляют нетронутыми.
Известны способы восстановления спинного мозга с применением клеточных культур, тканевых трансплантатов [3]. Имеются экспериментальные исследования с применением различных гидрогелевых матриц, интегрируемых в место травмы [4-6].
Известен способ хирургического сопоставления отрезков спинного мозга с помощью хирургической техники [7].
Известно действие конъюгата полиэтиленгликоля и фотосшиваемой формы хитозана (конъюгата ПЭГ-хитозана) для восстановления функций спинного мозга после его пересечения [8].
В качестве препарата способствующего созданию благоприятных условий для репарации, изучено применение трипсина, с положительным эффектом при его субдуральном и внутримышечном введении [9-11]. Его действие связано со своевременной эвакуацией подвергшихся некрозу и апоптозу клеток из очага травмы.
Наиболее близким к предлагаемому техническому решению является методика восстановления функций спинного мозга с использованием конъюгата полиэтиленгликоля и фотосшиваемой формы хитозана (конъюгата ПЭГ-хитозана) [8]. Способ заключается в резекции участка травмы спинного мозга, сопоставлении отрезков спинного мозга, наложении швов на мягкую мозговую оболочку, интраоперационом введении в место травмы конъюгата ПЭГ-хитозана с последующей пластикой твердой мозговой оболочки, внутривенном введении водного раствора полиэтиленгликоля, поддержании 12-ти часовой седации и применении жесткого ортеза послеоперационно.
Однако применение клеточных культур и трансплантатов не устраняет образующегося в месте травмы патологического субстрата, трансформирующегося во времени и являющегося механическим препятствием для естественной физиологической репарации. В случае прототипа, игнорировался факт возможной нестабильности отрезков спинного мозга, а также позвоночного столба. Кроме того, при резекции зоны повреждения нервной ткани, для достижения максимальной эффективности конъюгата ПЭГ-хитозана необходимо добиться плотного сопоставления отрезков спинного мозга. В способе принятом за прототип, при отсутствии стабилизации позвоночного столба, после операции возможно нарастание натяжения в области травмы, что может привести к расхождению сопоставленных отрезков. Помимо этого, не уделено достаточного внимания элиминации разрушенных клеточных элементов и послеоперационной терапии.
Целью предлагаемого изобретения является восстановление функциональной и морфологической целостности спинного мозга после его пересечения, а также при его контузии и разрыве.
Технический результат предлагаемого изобретения достигается путем установки системы транспедикулярной фиксации на уровне травмы, резекции фасеточных суставов на двух или четырех уровнях, локальной гибернации спинного мозга ледяной кашицей из физиологического раствора, субдурального введения конъюгата ПЭГ-хитозана (Нейро-ПЭГ), последующего пересечения или поперечного иссечения нежизнеспособной части спинного мозга, интраоперационного введения конъюгата ПЭГ-хитозана в сформированный диастаз спинного мозга, с последующим сближением и сопоставлением отрезков спинного мозга, коррекцией плоскости транспедикулярной фиксации для создания дорсального сгибания и увеличения плотности сопоставления отрезков спинного мозга, путем выполнения субтракционной спондилотомии, одновременным введением водного раствора полиэтиленгликоля внутривенно и последующей терапией состоящей из курса внутривенного введения водного раствора полиэтиленгликоля, внутримышечного введения трипсина и нейромиоэлектростимуляции.
Предлагаемый способ обладает следующими отличительными признаками:
1) установкой системы транспедикулярной фиксации позвоночника в области травмы;
2) резекцией фасеточных суставов на двух или четырех уровнях;
3) локальной гибернацией спинного мозга ледовой кашицей из физиологического раствора;
4) интраоперационным введением конъюгата полиэтиленгликоля и хитозана (ПЭГ-хитозан, Нейро-ПЭГ) субдурально до иссечения спинного мозга, и после его иссечения в сформированный диастаз;
5) выполнением субтракционной спондилотомии;
6) коррекцией плоскости транспедикулярной фиксации для создания дорсального сгибания и увеличения плотности сопоставления отрезков спинного мозга;
7) внутривенным введением водного раствора полиэтиленгликоля интраоперационно и в составе послеоперационной терапии;
8) внутримышечным введением трипсина в составе послеоперационной терапии;
9) нейромиоэлектростимуляцией в составе послеоперационной терапии;
Возможность реализации предлагаемого изобретения была подтверждена экспериментом на 10 свиньях, весом от 30 до 45 кг. Животных разделили на 2 группы: А - экспериментальную и В - контрольную. После премедикации животных золетил-кслилазиновой смесью (1:4), подготавливали операционное поле шириной 15 см, в проекции остистых отросков Th5-Th12 позвонков. В качестве основного наркоза использовали внутривенное введение пропофола 1% в комбинации с ингаляцией изофлюраном, с переводом на искусственную вентиляцию легких. Перед операцией устанавливают уретральный мочевой катетер с мочеприемником.
Способ осуществляют следующим образом.
Путем ковалентного связывания ПЭГ с фотосшитым хитозаном получают препарат конъюгата ПЭГ-хитозана, по методу, описанному в патенте на изобретение RU № 2782119 C1 от 08.07.2021 [8].
Выполняют линейный разрез в проекции остистых отростков от V до XII грудного позвонков, производят послойный доступ и скелетирование дужек и фасеточных суставов VII, VIII, IX грудных позвонков. Производят установку транспедикулярных полиаксиальных винтов по анатомическим ориентирам (фиг. 1), в VII и IX позвонки, с использованием free-hand методики, или с помощью интраоперационного рентген-контроля. При необходимости, устанавливают дополнительные винты на уровень выше и ниже. Выполняют ляминэктомию дужек VII, VIII, IX грудных позвонков, резецируют фасеточные суставы, визуализируют твердую мозговую оболочку спинного мозга. На фиг. 1 схематично отображен первый этап операции: А - вид позвоночного столба в боковой проекции до операции, где показаны тела позвонков (1), остистые отростки (2), фасеточные суставы (3); В - выполненная ламинэктомия, удаленные фасеточные суставы (4), спинной мозг (5) и место травмы спинного мозга (6); С - установленные транспедикулярные винты (7) с поперечной штангой (8).
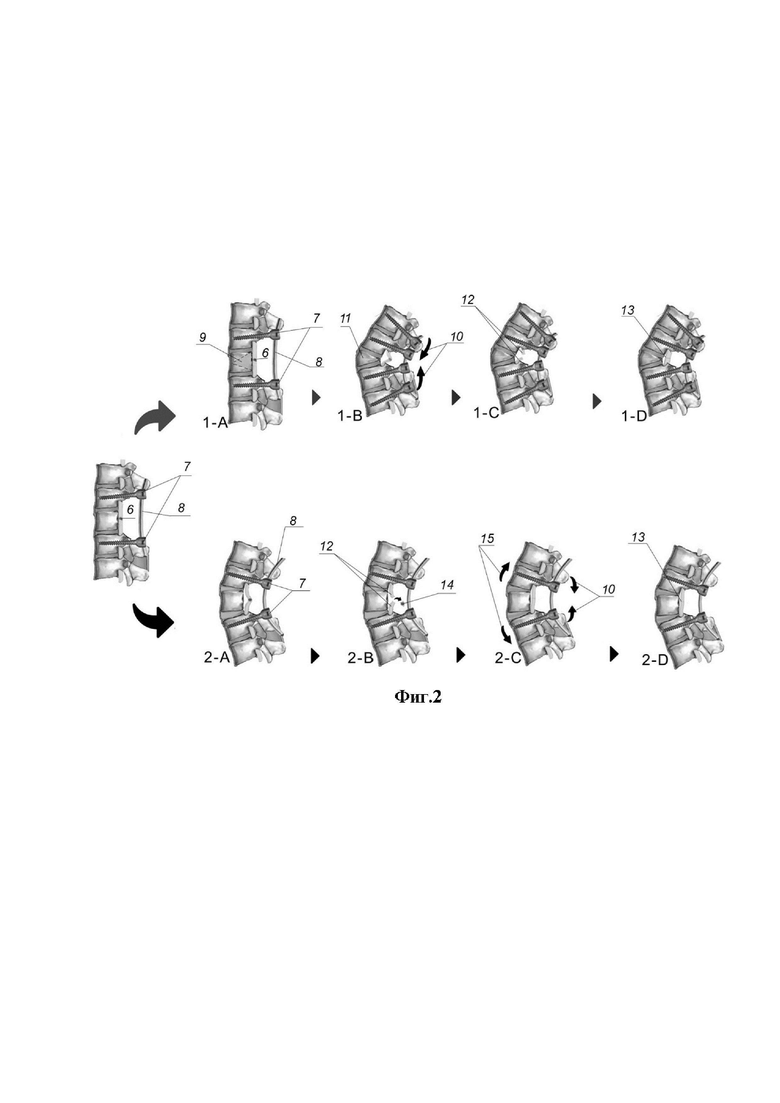
Далее выполняют субтракционную спондилотомию одним из известных способов: спондилотомию Смит-Петерсона (фиг. 2. 1-А - 1-B) или педикулярную субтракционную спондилотомию (фиг. 2. 2-А), в зависимости от анатомических особенностей. Устанавливают заранее изогнутые продольные штанги в головки винтов, и неплотно фиксируют их гайками. В область выполненной ляминэктомии помещают ледяную кашицу из стерильного физиологического раствора. Через 3 минуты ТМО вскрывают продольно и разводят в стороны нитями-держалками. Мягкую мозговую оболочку надсекают поперечно. Добиваются тщательного гемостаза. В субдуральное пространство вводят 1 мл охлажденного до +4 C° конъюгата ПЭГ-хитозана так, чтобы спинной мозг был погружен в него. Под спинной мозг помещают тонкий изогнутый мягкий мозговой шпатель. Спинной мозг пересекают поперечно и резецируют на протяжении 3 мм лезвием скальпеля №11. Останавливают кровотечение. В диастаз вводят 0,2 мл конъюгата ПЭГ-хитозана. Одновременно производят максимальную дорсальную тракцию позвоночного столба, для «захлопывания» зоны спондилотомии и создания дорсального сгибания, с окончательной фиксацией продольных балок гайками транспедикулярных винтов (фиг. 2. 1-B - 1-D; 2-B - 2-D).
На фиг. 2 схематично отображено выполнение субтракционной спондилотомии двумя способами, с резекцией спинного мозга. На фиг. 2, 1А-1D показана клиновидная резекция тела позвонка, педикулярная субтракционная спондилотомия. 1-А - указана область резекции кости (9); 1-B - установлены дополнительные транспедикулярные винты, выполнено сведение головок винтов (10) и «схлопывание» зоны резекции тела позвонка (11); 1-С - выполнена резекция участка спинного мозга, показаны культи спинного мозга (12); 1-D - выполнено сопоставление отрезков спинного мозга (13);
На фиг. 2, 2А-2D, показана спондилотомия Смит-Петерсона. 2-А - выполнено сведение головок винтов (7) по поперечной штанге (8); 2-B - резекция участка спинного мозга, где показаны культи спинного мозга (12) и резецированный участок (14); 2-С - сопоставление отрезков спинного мозга и усиление дорсального сгибания путем сведения головок винтов (10) и разгибание по передней поверхности позвоночного столба (15); 2-D - окончательный вид, где показаны сопоставленные отрезки спинного мозга (13);
После спондилотомии и создания дорсального сгибания и окончательной фиксации, ушивают твердую мозговую оболочку обвивным швом проленом 7/0. В перидуральное пространство устанавливают дренажную трубку. Рану ушивают послойно. Внутривенно, струйно, медленно выполняют инъекцию водного раствора полиэтиленгликоля, из расчета 2,5 мл/кг массы тела.
На 2-й день убирают дренажную трубку. В течение 10 дней применяют анальгетики, противовоспалительные препараты, антибиотики, проводят противоотечную терапию. В течение 15 дней выполняют внутримышечные инъекции трипсина 10 мг - 1 раз в день, и внутривенные инъекции водного раствора полиэтиленгликоля из расчета 0,75 мл/кг массы тела - 2 раза в день. В течение 30-ти дней после операции применяют ежедневную нейромиоэлектростимуляцию, с использованием импульсного элетростимулятора, генератора однополярных прямоугольных импульсов, с диапазоном дискретных частот 1, 2, 3, 5, 8, 13, 21, 34, 55, 89 Гц, диапазоном регулируемой длительности импульсов 0,1-100 мсек, и диапазоном регулируемой амплитуды 0-100В. Режим электростимуляции подбирают индивидуально. Положительный электрод устанавливают в проекции остистых отростков краниальнее области операции на 10 см, а отрицательный электрод устанавливают на заднюю конечность в области лодыжки. Кратность и длительность сеанса - 3 раза в день, по 20 минут стимуляции каждой задней конечности. Мочевой катетер удаляют на 5-7-е сутки.
У животных обеих групп спинной мозг пересекали полностью. В первой группе - экспериментальной (N=6) использовали предлагаемый способ, с введением конъюгата ПЭГ-хитозана, установкой металлоконструкции и послеоперационной реабилитацией. Во второй группе (N=4) предлагаемый способ не использовали. После пересечения спинного мозга в диастаз вводили физиологический раствор, а послеоперационное ведение включало симптоматическую и посиндромную терапию, анальгетики, антибиотики.
Результаты первой группы: в группе отсутствовала летальность. После операции у 5-ти животных диагностировали нижнюю параплегию и анестезию. У одного животного после операции отмечались незначительные спонтанные движения в правой задней конечности.
В течение 5 дней, у 2 животных развились трофические нарушения в виде пролежней, которые, однако не прогрессировали и поддавались лечению. У всех животных в период между 5-ми и 7-ми сутками отмечали восстановление болевой и температурной чувствительности, а также попытки одернуть конечность в ответ на раздражение. На 5-е сутки у всех животных были удалены уретральные мочевые катетеры, с наблюдением в течение 5 часов. Если в этот период не наблюдалось мочеиспускание, катетер устанавливали повторно. К 7-ым суткам у всех животных наблюдали регулярное мочеиспускание без катетера и самостоятельную дефекацию. Одно животное на 7-е сутки активно двигало задними конечностями, но без возможности сопротивления и вертикализации. На 14-е сутки из эксперимента было выведено 2 животных. К 30-му дню эксперимента 3 из 4 животных вертикализировались, и самостоятельно передвигались, используя при ходьбе передние и задние конечности, однако сохранялась неустойчивость, животные быстро уставали. В этот срок было выведено 2 животных. К 45-му дню эксперимента оставшиеся животные самостоятельно передвигались, задействуя все конечности, однако сохранялась неустойчивость при ходьбе.
Результаты второй группы: из 4 животных до конца эксперимента выжило только 1. У всех животных в течение первых 3-5 дней отмечалось быстрое развитие и прогрессирование трофических нарушений в виде пролежней. В течение всего эксперимента отмечался стойкий неврологический дефицит в виде нижней параплегии и анестезии. К 3-му дню, у всех животных контрольной группы отмечалась гипо/атония кишечника, отсутствие самостоятельной дефекации, что обуславливало необходимость выполнения клизм. На 4-е, 5-е и 14-е сутки умерло по одному животному. Причина смерти в первом случае - токсический шок вследствие массивной ишемии кишечника, во втором - тромбоэмболия легочной артерии, в третьем случае отмечалась картина цистита, пиелонефрита, инфаркта почки, полисегментарная пневмония. На 7-е, 10-е, 15-е, 21-е сутки выполняли пробное удаление мочевого уретрального катетера, с наблюдением в течение 5 часов. При наполнении мочевого пузыря, мочеиспускания не происходило, отмечалась задержка мочеиспускания по центральному типу, что требовало установки мочевого катетера.
При гистологическом исследовании спинного мозга опытных животных выявлены «аксональные мостики» в месте травмы, укрупнение глиальных клеток. В остальном картина мало отличалась от гистологической картины нормального спинного мозга. В контрольной группе, в месте травмы, отмечались явления кистозно-глиозной трансформации с элементами фиброза, очагами некроза, с различной степенью его организации.
Таким образом, результаты исследований дают основание утверждать, что в условиях данного эксперимента, конъюгат ПЭГ-хитозан вместе с хирургическим сопоставлением отрезков спинного мозга, использованием методики субтракционной спондилотомии с транспедикулярной фиксацией, послеоперационным введением трипсина и полиэтиленгликоля, а также электростимуляцией, способствуют восстановлению функций спинного мозга, что подтверждается клинически и морфологически. Препарат конъюгата ПЭГ-хитозана действует местно, вероятно создавая буферную среду для аксонального роста, ограничивая развитие вторичного повреждения нервной ткани, способствуя слиянию мембран поврежденных клеток. Количество введения препарата в субдуральное пространство и диастаз, может варьироваться от 0,1 мл до 10 мл, в зависимости от размеров спинного мозга объекта. Субтракционная спондилотомия с транспедикулярной фиксацией обеспечивает плотное сопоставление отрезков спинного мозга, исключая их свободное перемещение в позвоночном канале, и нивелируя возможное натяжение. Транспедикулярная фиксация также обеспечивает стабилизацию позвоночного столба в месте травмы, что приводит к иммобилизации поврежденного спинного мозга, и устраняет необходимость длительного обездвиживания и фиксации в жестком ортезе. Раствор полиэтиленгликоля, в составе послеоперационной терапии, вводимый внутривенно, обеспечивает поддержание концентрации ПЭГ в зоне травмы. Внутримышечные инъекции трипсина способствуют ускоренной элиминации из очага травмы и послеоперационной раны нежизнеспособной ткани, оказывают противоотечный и противовоспалительный эффект. Электростимуляция импульсными токами способствует восстановлению трофики мышц, создает электрическую направленность для аксонального роста, способствует ускоренной реабилитации в составе послеоперационной терапии.
При обширных повреждениях спинного мозга, возможно расширение хирургического пособия и выполнение резекции спинного мозга на протяжении, в сочетании с вертерброэктомией для облегчения сопоставления отрезков спинного мозга, Данный способ также может быть дополнен последующим комплексом реабилитации, включающим прямую электростимуляцию спинного мозга, магнитотерапию.
Изобретение может быть применено в нейрохирургии, для лечения пациентов с травмой спинного мозга, а также с иными ограниченными поражениями спинного мозга.
Источники информации
1. Воронович И.Р., Белецкий А.В., Дулуб О.И., Макаревич С.В. и др. Диагностика и лечение травматических полисегментарных поражений спинного мозга. Матер. научн. конф. посвящ. 40-летию отделения патологии позвоночника «Хирургия позвоночника - полный спектр». М. 2007. С. 281-283.
2. Смирнов В.А., Гринь А.А. Регенеративные методы лечения травмы спинного мозга. Обзор литературы. Часть 1. Нейрохирургия 2019;21(2):66-75.
3. Патент RU № 2489176 C1. Способ тканевой инженерии спинного мозга после его анатомического разрыва. - МПК7: A61M 37/00(2006.01), A61K 35/48(2006.01), A61K 31/722(2006.01), A61K 31/726(2006.01), A61P 25/00(2006.01) - 14.02.2012 г.)
4. Патент RU № 2644278 С1. Способ микрохирургической реконструкции спинного мозга на животной модели с использованием биодеградируемого гидрогеля на основе поливинилового спирта. - МПК7: G09B 23/28(2006.01), A61K 31/74(2006.01), A61P 41/00(2006.01) - 21.12.2016 г.
5. Canavero S, Ren X, Kim CY. Reconstructing the severed spinal cord. Surg Neurol Int. 2017;8:285. Published 2017 Nov 21. doi:10.4103/sni.sni_406_17.
6. Cho Y, Borgens RB. Polymer and nano-technology applications for repair and reconstruction of the central nervous system. Exp Neurol. 2012;233(1):126-144. doi:10.1016/j.expneurol.2011.09.028,
7. Патент RU № 2341830 C1. Способ восстановления функций спинного мозга при моделировании его полного анатомического перерыва в остром периоде в эксперименте. - МПК7: G09B 23/28(2006.01), A61B 17/00(2006.01), A61K 31/02(2006.01), A61N 2/00(2006.01) - 26.06.2007г.
8. Патент RU № 2782119 C1. Способ восстановления функций спинного мозга после его пересечения, с помощью конъюгата ПЭГ-хитозана. - МПК7: G09B 23/28(2006.01), A61B 17/00(2006.01), A61K 31/02(2006.01), A61N 2/00(2006.01) - 08.07.2021г.
9. Freeman LW.editorsProceedings, X Congreso Latinoamericano de Neurochirurgia. Brazil: Editorial Don Bosco; 1963. p. 135-44
10. Freeman LW. Experimental observations upon axonal regeneration in the transected spinal cord of mammals. Clin Neurosurg. 1962. 8: 294-319
11. Freeman LW. Return of spinal cord function in mammals after transecting lesions. Ann NY Acad Med Sci. 1954. 58: 564-9.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВОССТАНОВЛЕНИЯ ФУНКЦИЙ СПИННОГО МОЗГА ПОСЛЕ ЕГО ПЕРЕСЕЧЕНИЯ, С ПОМОЩЬЮ КОНЪЮГАТА ПЭГ-ХИТОЗАНА | 2021 |
|
RU2782119C1 |
| СПОСОБ ЛАМИНОПЛАСТИКИ ПРИ ПЕРВИЧНЫХ ОПУХОЛЯХ СПИННОГО МОЗГА | 2023 |
|
RU2810244C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ПОЗВОНОЧНОГО КАНАЛА ПРИ ОПУХОЛИ СПИННОГО МОЗГА | 2014 |
|
RU2567824C1 |
| СПОСОБ ТРЕХКОЛОННОЙ ВЕРТЕБРОТОМИИ ПРИ ДИАСТЕМАТОМИЕЛИИ | 2018 |
|
RU2698618C1 |
| СПОСОБ ЗАДНЕЙ ДЕКОМПРЕССИИ СПИННОГО МОЗГА ПРИ СТЕНОЗЕ ПОЗВОНОЧНОГО КАНАЛА | 2022 |
|
RU2791410C1 |
| Способ реконструкции позвоночного канала при многоуровневом стенозе шейного отдела позвоночника | 2019 |
|
RU2728106C2 |
| СПОСОБ ПЕРЕДНЕЙ ДЕКОМПРЕССИИ СПИННОГО МОЗГА ПОСЛЕ ЛАМИНЭКТОМИИ | 2004 |
|
RU2306887C2 |
| СПОСОБ ТКАНЕВОЙ ИНЖЕНЕРИИ СПИННОГО МОЗГА ПОСЛЕ ЕГО АНАТОМИЧЕСКОГО РАЗРЫВА | 2012 |
|
RU2489176C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ФУНКЦИЙ СПИННОГО МОЗГА ПРИ МОДЕЛИРОВАНИИ ЕГО ПОЛНОГО АНАТОМИЧЕСКОГО ПЕРЕРЫВА В ОСТРОМ ПЕРИОДЕ В ЭКСПЕРИМЕНТЕ | 2007 |
|
RU2341830C1 |
| Способ декомпрессии спинного мозга при переломах грудных и поясничных позвонков | 2022 |
|
RU2798042C1 |

Изобретение относится к области медицины, а именно к экспериментальной медицине, нейрохирургии и регенеративной медицине, и может быть использовано для лечения травмы спинного мозга с восстановлением его функций конъюгатом ПЭГ-хитозана. Осуществляют синтез ПЭГ-хитозана путем ковалентного связывания ПЭГ с фотосшитым хитозаном. После доступа к спинному мозгу устанавливают транспедикулярные винты в тела позвонков выше и ниже места травмы, выполняют спондилотомию одним из способов, вскрывают твердую и мягкую мозговые оболочки, охлаждают спинной мозг ледяной кашицей из стерильного физиологического раствора. В субдуральное пространство вводят синтезированный методом ковалентного связывания препарат конъюгата ПЭГ-хитозана. Пересекают и резецируют спинной мозг в пределах жизнеспособной части, с последующим введением конъюгата ПЭГ-хитозана в субдуральное пространство и диастаз спинного мозга, в количестве, необходимом для покрытия поверхности отрезков спинного мозга и заполнения диастаза. Производят максимальную дорсальную тракцию позвоночника для создания дорсального сгибания в зоне спондилотомии, окончательно фиксируют транспедикулярную систему. Выполняют плотное сближение отрезков спинного мозга, ушивание твердой мозговой оболочки, выполняют внутривенную инъекцию водного раствора полиэтиленгликоля, а в послеоперационном периоде используют внутримышечные инъекции трипсина и нейромиоэлектростимуляцию. Способ обеспечивает восстановление функциональной и морфологической целостности спинного мозга после его пересечения, а также при его контузии и разрыве за счет использования конъюгата ПЭГ-хитозана вместе с хирургическим сопоставлением отрезков спинного мозга, а также проведения субтракционной спондилотомии с транспедикулярной фиксацией и послеоперационным введением трипсина и полиэтиленгликоля. 2 ил.
Способ лечения травмы спинного мозга с восстановлением его функций конъюгатом ПЭГ-хитозана, включающий хирургическое сопоставление отрезков спинного мозга, отличающийся тем, что осуществляют синтез ПЭГ-хитозана путем ковалентного связывания ПЭГ с фотосшитым хитозаном, после доступа к спинному мозгу устанавливают транспедикулярные винты в тела позвонков выше и ниже места травмы, выполняют спондилотомию одним из способов, вскрывают твердую и мягкую мозговые оболочки, охлаждают спинной мозг ледяной кашицей из стерильного физиологического раствора и в субдуральное пространство вводят синтезированный методом ковалентного связывания препарат конъюгата ПЭГ-хитозана, пересекают и резецируют спинной мозг в пределах жизнеспособной части, с последующим введением конъюгата ПЭГ-хитозана в субдуральное пространство и диастаз спинного мозга, в количестве, необходимом для покрытия поверхности отрезков спинного мозга и заполнения диастаза, производят максимальную дорсальную тракцию позвоночника для создания дорсального сгибания в зоне спондилотомии, окончательно фиксируют транспедикулярную систему, выполняют плотное сближение отрезков спинного мозга, ушивание твердой мозговой оболочки, выполняют внутривенную инъекцию водного раствора полиэтиленгликоля, а в послеоперационном периоде используют внутримышечные инъекции трипсина и нейромиоэлектростимуляцию.
| СПОСОБ ВОССТАНОВЛЕНИЯ ФУНКЦИЙ СПИННОГО МОЗГА ПОСЛЕ ЕГО ПЕРЕСЕЧЕНИЯ, С ПОМОЩЬЮ КОНЪЮГАТА ПЭГ-ХИТОЗАНА | 2021 |
|
RU2782119C1 |
| СПОСОБ МИКРОХИРУРГИЧЕСКОЙ РЕКОНСТРУКЦИИ СПИННОГО МОЗГА НА ЖИВОТНОЙ МОДЕЛИ С ИСПОЛЬЗОВАНИЕМ БИОДЕГРАДИРУЕМОГО ГИДРОГЕЛЯ НА ОСНОВЕ ПОЛИВИНИЛОВОГО СПИРТА | 2016 |
|
RU2644278C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ФУНКЦИЙ СПИННОГО МОЗГА ПРИ МОДЕЛИРОВАНИИ ЕГО ПОЛНОГО АНАТОМИЧЕСКОГО ПЕРЕРЫВА В ОСТРОМ ПЕРИОДЕ В ЭКСПЕРИМЕНТЕ | 2007 |
|
RU2341830C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ СПИННОГО МОЗГА В ЭКСПЕРИМЕНТЕ | 1996 |
|
RU2136242C1 |
| Sogolie Kouhzaei et al., Protective effect of low molecular weight polyethylene glycol on the repair of experimentally damaged neural membranes in rat’s spinal cord, Neurological Research, 2013, 35:4, 415-423. | |||
Авторы
Даты
2023-08-09—Публикация
2022-11-02—Подача