ОБЛАСТЬ ТЕХНИКИ
[0001]
По данной патентной заявке испрашивается приоритет ч соответствии с заявкой на патент Японии № 2018-175758, все содержание которой включено в настоящий документ посредством ссылки.
Настоящее изобретение относится к соединению, обладающему антагонистической активностью в отношении рецептора DP, его фармацевтически приемлемой соли и лекарственному средству, содержащему их в качестве активного ингредиента. Более подробно, к соединению, представленному общей формулой (I),
[Химическая формула 1]

(где все символы имеют значения, описанные ниже) или его фармацевтически приемлемой соли (в дальнейшем именуемой соединением по настоящему изобретению) и лекарственному средству, содержащему их в качестве активных ингредиентов.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002]
Простагландин D2 (сокращенно PGD2) известен как метаболит каскада арахидоновой кислоты и, как известно, участвует в аллергических заболеваниях, сне, секреции гормонов, боли, агрегации тромбоцитов, метаболизме гликогена, регуляции внутриглазного давления и тому подобное (непатентная литература 1-11). Известно, что рецепторы DP и рецепторы CRTH2 представлены как рецепторы PGD2, и известно, что из них рецепторы DP, присутствующие в головном мозге, особенно в субарахноидальном пространстве в вентральной области рострального базального отдела переднего мозга, связаны с вызывающим сон действием PGD2 (непатентная литература 12). То есть, чтобы ингибировать вызывающее сон действие PGD2 и использоваться в качестве терапевтического лекарственного средства при нарушениях сна и бодрствования, необходимо иметь лекарственное средство, обладающее не только DP антагонистической активностью, но также способностью проникать в центральную нервную систему.
[0003]
С другой стороны, в патентной литературе 1 описано, что соединение, представленное следующей общей формулой (A), специфически связывается с рецептором DP и антагонизирует его.
[Химическая формула 2]

где R1A представляет собой (1) атом водорода, (2) C1-4 алкильную группу и т.д., EA представляет собой -C(=O)- и т.д., R2A представляет собой (1) атом галогена, (2) C1-6 алкильную группу и т.д., R3A представляет собой (1) атом галогена, 2) C1-6 алкильную группу и т.д., WA представляет собой C5-12 моноциклический или бициклический карбоцикл или 5-12-членный моноциклический или бициклический гетероцикл, R4A представляет собой (1) атом водорода, (2) C1-6 алкильную группу и т.д., R5A представляет собой C1-6 алкильную группу и т.д., (1) GA представляет собой (1) C1-6 алкиленовую группу, содержащую 0-2 гетероатома, выбранных из атома азота, атома кислорода и атома серы, JA представляет собой C5-12 моноциклический или бициклический карбоцикл или 5-12-членный моноциклический или бициклический гетероцикл, mA обозначает целое число 0 или 1-4, nA обозначает целое число 0 или 1-4, и iA обозначает целое число 0 или 1-11.
[0004]
Кроме того, в патентной литературе 2 описывается, что соединение, представленное следующей общей формулой (B), является соединением, которое специфически связывается с рецептором DP и антагонизирует его.
[Химическая формула 3]

где R1B представляет собой (1) атом водорода, (2) C1-4 алкильную группу и т.д., EB представляет собой -CO- группу и т.д., R2B представляет собой (1) атом галогена, (2) C1-6 алкильную группу и т.д., R3B представляет собой (1) атом галогена, (2) C1-6 алкильную группу и т.д., R4B представляет собой (1) атом водорода, (2) C1-6 алкильную группу и т.д., R5B представляет собой C1-6 алкильную группу и т.д., WB представляет собой C5-12 моноциклический или бициклический карбоцикл или 5-12-членный моноциклический или бициклический гетероцикл, GB представляет собой (1) C1-6 алкиленовую группу, содержащую 0-2 гетероатома, выбранных из атома азота, атома кислорода и атома серы, JB представляет собой C5-12 моноциклический или бициклический карбоцикл или 5-12-членный моноциклический или бициклический гетероцикл, mB обозначает целое число 0 или 1-4, nB обозначает целое число 0 или 1-4, iB обозначает целое число 0 или 1-11 и R12B и R13B, каждый, независимо, представляют собой (1) C1-4 алкильную группу, которая может быть окислена, (2) атом водорода и т.д.
Однако в этих документах предшествующего уровня техники не описывается и не предлагается то, что могло бы быть способным проникать в центральную нервную систему.
СПИСОК ЦИТИРУЕМОЙ ЛИТЕРАТУРЫ
Патентная литература
[0005]
Патентная литература 1: WO 2003/078409 A
Патентная литература 2: WO 2005/028455 A
Непатентная литература
[0006]
Непатентная литература 1: The NEW ENGLAND JOURNAL of MEDICINENE, Vol. 303, 1400-1404, 1980
Непатентная литература 2: American Review of Respiratory Disease, Vol. 128, 597-602, 1983
Непатентная литература 3: The Journal of Allergy and Clinical Immunology, Vol. 88, 33-42, 1991
Непатентная литература 4: Archives of Otolaryngology-Head and Neck Surgery, Vol. 113, 179-83, 1987
Непатентная литература 5: The Journal of Allergy and Clinical Immunology, Vol. 82, 869-77, 1988
Непатентная литература 6: The Journal of Immunology, Vol. 146, 671-676, 1991
Непатентная литература 7: The Journal of Allergy and Clinical Immunology, Vol. 83, 905-912, 1989
Непатентная литература 8: The NEW ENGLAND JOURNAL of MEDICINENE, Vol. 315, 800-804, 1986
Непатентная литература 9: American Review of Respiratory Disease, Vol. 142, 126-132, 1990
Непатентная литература 10: The Journal of Allergy and Clinical Immunology, Vol. 87, 540-548, 1991
Непатентная литература 11: The Journal of Allergy and Clinical Immunology, Vol. 78, 458-461, 1986
Непатентная литература 12: Proceedings of the National Academy of Sciences of the United States of America, Vol. 98, 11674-11679, 2001
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКИЕ ЗАДАЧИ
[0007]
Цель настоящего изобретения состоит в том, чтобы разработать соединение, обладающее как сильной антагонистической активностью против рецепторов DP, так и хорошей способностью проникать в ЦНС, и предложить соединение, которое может использоваться в качестве профилактического и/или терапевтического агента при заболеваниях, вызванных активацией рецептора DP, в частности, терапевтического агента при расстройстве режима сна и бодрствования.
РЕШЕНИЕ ЗАДАЧ
[0008]
В результате интенсивных исследований авторы настоящего изобретения обнаружили, что соединение, представленное общей формулой (I), описанное далее, решает вышеупомянутые задачи, и в результате дальнейших исследований создали настоящее изобретение.
Таким образом, в настоящем изобретении в одном аспекте предложено
[1] Соединение, представленное общей формулой (I):
[Химическая формула 4]
 ,
,
где R1 представляет собой атом водорода, C1-4 алкильную или бензильную группу,
R2, R3 и R4, каждый, независимо, представляют собой (1) атом галогена, (2) C1-4 алкильную группу, необязательно замещенную атомом галогена, или (3) C1-4 алкокси группу, необязательно замещенную атомом галогена,
когда имеется несколько из R2 или R4, они могут быть одинаковыми или разными,
J представляет собой связь, -O- или -S-,
L представляет собой связь, C1-6 алкиленовую, C2-6 алкениленовую или C2-6 алкиниленовую группу,
R5 представляет собой атом водорода, C3-10 карбоцикл или 3-10-членный гетероцикл,
C3-10 карбоцикл и 3-10-членный гетероцикл в R5 могут быть 1-6 замещены R7,
при условии, что, когда L представляет собой связь, R5 не является атомом водорода,
R7 представляет собой (1) атом галогена, (2) C1-4 алкильную группу, необязательно замещенную атомом галогена, или (3) C1-4 алкокси группу, необязательно замещенную атомом галогена,
когда имеется несколько R7, они могут быть одинаковыми или разными,
Q представляет собой атом кислорода или атом серы,
при условии, что, когда Q представляет собой атом кислорода, (1) L представляет собой C1-6 алкиленовую, C2-6 алкениленовую или C2-6 алкиниленовую группу и R5 представляет собой C3-8 моноциклический карбоцикл или 3-8-членный моноциклический гетероцикл, или (2) L представляет собой связь и R5 представляет собой C3-10 карбоцикл или 3-10-членный гетероцикл,
R6 представляет собой атом водорода или C1-4 алкильную группу,
R11 представляет собой атом водорода, атом галогена или C1-4 алкильную группу, необязательно замещенную атомом галогена,
R12 представляет собой атом водорода, атом галогена или C1-4 алкильную группу, необязательно замещенную атомом галогена,
R11 и R12 могут быть взяты вместе с атомом углерода, к которому они присоединены, с образованием C3-6 насыщенного карбоцикла,
n обозначает целое число от 0 до 4, и
m обозначает целое число от 0 до 3, или
его фармацевтически приемлемая соль,
[2] Соединение в соответствии с [1] выше, в котором Q представляет собой атом серы, или его фармацевтически приемлемая соль,
[3] Соединение в соответствии с [1] или [2] выше, представленное общей формулой (I-1):
[Химическая формула 5]
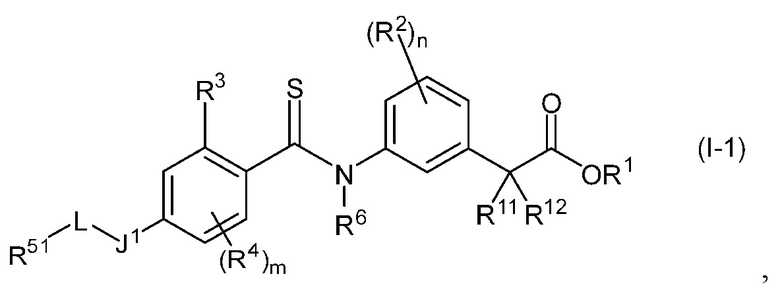
где R51 представляет собой C3-10 карбоцикл или 3-10-членный гетероцикл, J1 представляет собой связь или -O-, и другие символы имеют те же значения, что и описанные в [1] выше, или его фармацевтически приемлемая соль,
[4] Соединение в соответствии с [3] выше, в котором R51 представляет собой C3-8 моноциклический карбоцикл или 3-8-членный моноциклический гетероцикл, или его фармацевтически приемлемая соль,
[5] Соединение в соответствии с [3] выше, в котором R51 представляет собой 3-8-членный насыщенный моноциклический гетероцикл, или его фармацевтически приемлемая соль,
[6] Соединение в соответствии с [1] выше, в котором Q представляет собой атом кислорода, R5 представляет собой C3-8 моноциклический карбоцикл или 3-8-членный моноциклический гетероцикл, или его фармацевтически приемлемая соль,
[7] Соединение в соответствии с [1] выше, в котором соединение представляет собой
(1) (4-хлор-3-{4-[2-(оксан-2-ил)этокси]-2-(трифторметил)бензамид}фенил)уксусную кислоту,
(2) {4-хлор-3-[4-(2-циклогексилэтокси)-2-(трифторметил)бензамид]фенил}уксусную кислоту,
(3) {4-хлор-3-[4-(2-фенилэтокси)-2-(трифторметил)бензамид]фенил}уксусную кислоту,
(4) {4-хлор-3-[4-(2-циклопропилэтокси)-2-(трифторметил)бензамид]фенил}уксусную кислоту,
(5) (4-хлор-3-{2,6-диметил-4-[2-(оксан-2-ил)этокси]бензамид}фенил)уксусную кислоту,
(6) {4-хлор-3-[4-(2-циклогексилэтокси)-2,6-диметилбензамид]фенил}уксусную кислоту,
(7) {4-хлор-3-[4-(2-циклопропилэтокси)-2,6-диметилбензамид]фенил}уксусную кислоту,
(8) (3-{4-[(2,3-Дигидро-1H-инден-2-ил)окси]-2,6-диметилбензамид}-4-фторфенил)уксусную кислоту,
(9) {4-хлор-3-[4-(3-циклогексилпроп-1-ин-1-ил)-2,6-диметилбензамид]фенил}уксусную кислоту,
(10) (4-хлор-3-{4-[(1E)-3-циклогексилпроп-1-ен-1-ил]-2,6-диметилбензамид}фенил)уксусную кислоту,
(11) (4-хлор-3-{[4-(2-циклогексилэтокси)-2,6-диметилбензол-1-карботиоил]амино}фенил)уксусную кислоту,
(12) [4-хлор-3-({4-[2-(оксан-2-ил)этокси]-2-(трифторметил)бензол-1-карботиоил}амино)фенил]уксусную кислоту,
(13) (4-хлор-3-{[4-(2-циклогексилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусную кислоту,
(14) (4-хлор-3-{[4-(2-фенилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусную кислоту,
(15) (4-хлор-3-{[4-(2-циклопропилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусную кислоту,
(16) [4-хлор-3-({2,6-диметил-4-[2-(оксан-2-ил)этокси]бензол-1-карботиоил}амино)фенил]уксусную кислоту,
(17) {4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусную кислоту,
(18) {4-хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусную кислоту,
(19) 2-{3-[({2,6-Диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}пропионовую кислоту,
(20) 1-{3-[({2,6-Диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}циклопропанкарбоновую кислоту,
(21) 2-{4-хлор-3-[({2,6-диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]фенил}-2-метилпропионовую кислоту,
(22) 2-{4-хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропионовую кислоту,
(23) 2-{4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропионовую кислоту,
(24) 2-{3-[({2,6-Диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}-2-метилпропионовую кислоту или
(25) 2-(4-хлор-3-{[(2,6-диметил-4-{2-[(2R)-тетрагидро-2H-пиран-2-ил]этокси}фенил)карботиоил]амино}фенил)пропионовую кислоту,
или его фармацевтически приемлемая соль,
[8] Фармацевтическая композиция, содержащая соединение, представленное общей формулой (I), или его фармацевтически приемлемую соль,
[9] Фармацевтическая композиция в соответствии с [8] выше, которая является антагонистом рецептора DP,
[10] Фармацевтическая композиция в соответствии с [9] выше, которая является профилактическим и/или терапевтическим агентом при заболевании, опосредованном рецептором DP,
[11] Фармацевтическая композиция в соответствии с [10] выше, где заболеванием, опосредованным рецептором DP, является аллергическое заболевание, системный мастоцитоз, системное нарушение активации тучных клеток, анафилактический шок, сужение дыхательных путей, крапивница, экзема, акне, аллергический бронхолегочный аспергиллез, синусит, мигрень, полипы в носу, гиперчувствительный васкулит, эозинофилия, контактный дерматит, заболевание, сопровождающееся зудом, заболевание, вызванное вторично в результате состояния, сопровождающегося зудом, заболевание, сопровождающееся покраснением кожи, воспаление, хроническая обструктивная болезнь легких, ишемия-реперфузионное повреждение, нарушение мозгового кровообращения, аутоиммунное заболевание, церебральная травма, нарушение функции печени, отторжение трансплантата, ревматоидный артрит, плеврит, остеоартрит, болезнь Крона, язвенный колит, синдром раздраженного кишечника, интерстициальный цистит, мышечная дистрофия, полимиозит, злокачественное новообразование, лейкемия, вирусная инфекция, рассеянный склероз, нарушение сна и бодрствования или агрегация тромбоцитов,
[12] Фармацевтическая композиция в соответствии с [11] выше, где заболевание, опосредованное рецептором DP, представляет собой нарушение режима сна и бодрствования,
[13] Фармацевтическая композиция в соответствии с [12] выше, где нарушение сна и бодрствования представляет собой заболевание, основанное на гиперсомнии, бессоннице, остаточной сонливости синдрома апноэ во сне, расстройстве циркадного ритма сна и бодрствования, гиперсомнии, связанной с нейродегенеративным заболеванием, гиперсомнии, связанной с психическим заболеванием, или патологическом апноэ во сне в дневное время,
[14] Способ профилактики и/или лечения заболевания, опосредованного рецептором DP, включающего введение млекопитающему эффективного количества соединения, представленного общей формулой (I), или его фармацевтически приемлемой соли в соответствии с [1] выше,
[15] Соединение, представленное общей формулой (I), или его фармацевтически приемлемая соль в соответствии с [1] выше, которое используется для профилактики и/или лечения заболевания, опосредованного рецептором DP,
[16] Применение соединения, представленного общей формулой (I), или его фармацевтически приемлемой соли в соответствии с [1] выше при изготовлении профилактического и/или терапевтического агента, используемого при заболевании, опосредованного рецептором DP,
[17] Профилактический и/или терапевтический агент, используемый при заболевании, опосредованном рецептором DP, содержащий соединение, представленное общей формулой (I), или его фармацевтически приемлемую соль в соответствии с [1] выше, и тому подобное.
ПОЛОЖИТЕЛЬНЫЙ ЭФФЕКТ ИЗОБРЕТЕНИЯ
[0009]
Поскольку соединение по настоящему изобретению обладает сильной антагонистической активностью в отношении рецепторов DP, а также обладает хорошей способностью проникать в ЦНС, его можно использовать в качестве профилактического и/или терапевтического агента при заболеваниях, вызванных активацией рецептора DP, в частности, терапевтического агента при нарушении сна и бодрствования. Кроме того, соединение по настоящему изобретению является превосходным с точки зрения безопасности, поскольку оно избирательно антагонизирует рецептору DP.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0010]
Далее настоящее изобретение будет описано подробно.
В настоящем описании C1-4 алкильная группа включает метильную, этильную, пропильную и бутильную группы и их изомеры.
[0011]
В настоящем описании C1-4 алкокси группа включает метокси, этокси, пропокси и бутокси группы и их изомеры.
[0012]
В настоящем описании примеры C1-6 алкиленовой группы включают метиленовую, этиленовую, пропиленовую, бутиленовую, пентиленовую, гексиленовую группы и их изомеры.
[0013]
В настоящем описании C2-6 алкениленовая группа означает, например, C2-6 алкениленовую группу, имеющую одну или две двойные связи, и, в частности, включает этениленовую, пропениленовую, бутениленовую, бутадиениленовую, пентениленовую, пентадиениленовую, гексениленовую, гексадиениленовую группы и их изомеры.
[0014]
В настоящем описании C2-6 алкиниленовая группа означает, например, C2-6 алкиниленовую группу, имеющую одну или две тройные связи, и, в частности, включает этиниленовую, пропиниленовую, бутиниленовую, бутадииниленовую, пентиниленовую, пентадииниленовую, гексиниленовую, гексадииниленовую группы и их изомеры.
[0015]
В настоящем описании атом галогена включает атомы фтора, хлора, брома и йода.
[0016]
В настоящем описании C3-10 карбоцикл представляет собой моноциклический или бициклический C3-10 карбоцикл, и его примеры включают циклопропановое, циклобутановое, циклопентановое, циклопентеновое, циклопентадиеновое, циклогексановое, циклогексеновое, циклогексадиеновое, бензольное, циклогептановое, циклогептановое, циклогептадиеновое, циклооктановое, циклооктеновое, циклооктадиеновое, циклононановое, циклононеновое, циклононадиеновое, циклодекановое, циклодеценовое, пенталеновое, пергидропенталеновое, азуленовое, пергидроазуленовое, инденовое, пергидроинденовое, индановое, нафталиновое, дигидронафталиновое, тетрагидронафталиновое и пергидронафталиновое кольца и тому подобное.
[0017]
В настоящем описании 3-10-членный гетероцикл означает 3-10-членный моноциклический или бициклический гетероцикл, содержащий от 1 до 5 гетероатомов, выбранных из атома кислорода, атома азота и атома серы, и его примеры включают азиридиновое, оксирановое, тиирановое, азетидиновое, оксетановое, тиетановое, пиррольное, имидазольное, триазольное, тетразольное, пиразольное, фурановое, тиофен, оксазольное, изооксазольное, тиазольное, изотиазольное, фуразановое, оксадиазольное, тиадиазольное, пирролиновое, пирролидиновое, имидазолиновое, имидазолидиновое, триазолиновое, триазолидиновое, тетразолиновое, тетразолидиновое, пиразолиновое, пиразолидиновое, дигидрофурановое, тетрагидрофурановое, дигидротиофеновое, тетрагидротиофеновое, дигидрооксазольное, тетрагидрооксазольное (оксазолидиновое), дигидроизоксазольное, тетрагидроизоксазольное (изооксазолидиновое), дигидротиазольное, тетрагидротиазольное (тиазолидиновое), дигидроизотиазольное, тетрагидроизотиазольное (изотиазолидиновое), дигидрофуразановое, тетрагидрофуразановое, дигидрооксадиазольное, тетрагидрооксадиазольное (оксадиазолидиновое), дигидротиадиазольное, тетрагидротиадиазольное (тиадиазолидиновое), диоксолановое, дитиолановое, пиридиновое, пиразиновое, пиримидиновое, пиридазиновое, пирановое, тиопирановое, оксазиновое, оксадиазиновое, тиазиновое, тиадиазиновое, дигидропиридиновое, тетрагидропиридиновое, пиперидиновое, дигидропиразиновое, тетрагидропиразиновое, пиперазиновое, дигидропиримидиновое, тетрагидропиримидиновое, пергидропиримидиновое, дигидропиридазиновое, тетрагидропиридазиновое, пергидропиридазиновое, дигидропирановое, тетрагидропирановое, дигидротиопирановое, тетрагидротиопирановое, дигидрооксазиновое, тетрагидрооксазиновое, дигидрооксадиазиновое, тетрагидрооксадиазиновое, дигидротиазиновое, тетрагидрооксадиазиновое, дигидротиазиновое, тетрагидротиазиновое, дигидротиадиазиновое, тетрагидротиадиазиновое, морфолиновое, тиоморфолиновое, оксатиановое, диоксановое, дитиановое, азабицикло[2.2.1]гептановое, оксабицикло[2.2.1]гептановое, азабицикло[3.1.1]гептановое, азабицикло[2.2.2]октановое, диазабицикло[2.2.2]октановое, азепиновое, диазепиновое, оксепиновое, тиепиновое, оксазепиновое, оксадиазепиновое, тиазепиновое, тиадиазепиновое, дигидроазепиновое, тетрагидроазепиновое, пергидроазепиновое, дигидродиазепиновое, тетрагидродиазепиновое, пергидродиазепиновое, дигидрооксепиновое, тетрагидрооксепиновое, пергидрооксепиновое, дигидротиепиновое, тетрагидротиепиновое, пергидротиепиновое, дигидрооксазепиновое, тетрагидрооксазепиновое, пергидрооксазепиновое, дигидрооксадиазепиновое, тетрагидрооксадиазепиновое, пергидрооксадиазепиновое, дигидротиазепиновое, тетрагидротиазепиновое, пергидротиазепиновое, дигидротиадиазепиновое, тетрагидротиадиазепиновое, пергидротиадиазепиновое, азабицикло[3.2.1]октановое, оксабицикло[3.2.1]октановое, индольное, изоиндольное, индолизиновое, бензофурановое, изобензофурановое, бензотиофен, изобензотиофен, индазольное, пуриновое, бензоксазольное, бензотиазольное, бензимидазольное, бензофуразановое, бензотиадиазольное, бензотриазольное, индолиновое, изоиндолиновое, дигидробензофурановое, пергидробензофурановое, дигидроизобензофурановое, пергидроизобензофурановое, дигидробензотиофеновое, пергидробензотиофеновое, дигидроизобензотиофеновое, пергидроизобензотиофеновое, дигидроиндазольное, пергидроиндазольное, дигидробензоксазольное, пергидробензоксазольное, дигидробензотиазольное, пергидробензотиазольное, дигидробензимидазольное, пергидробензимидазольное, диоксаиндановое, бензодитиолановое, азаспиро[4.4]нонановое, оксазаспиро[4.4]нонановое, диоксаспиро[4.4]нонановое, дитианафталиновое, хинолиновое, изохинолиновое, хинолизиновое, фталаиновое, птеридиновое, нафтиридиновое, хиноксалиновое, хиназолиновое, циннолиновое, хроменовое, дигидрохинолиновое, тетрагидрохинолиновое, пергидрохинолиновое, дигидроизохинолиновое, тетрагидроизохинолиновое, пергидроизохинолиновое, дигидрофталаиновое, тетрагидрофталаиновое, пергидрофталаиновое, дигидронафтиридиновое, тетрагидронафтиридиновое, пергидронафтиридиновое, дигидрохиноксалиновое, тетрагидрохиноксалиновое, пергидрохиноксалиновое, дигидрохиназолиновое, тетрагидрохиназолиновое, пергидрохиназолиновое, дигидроциннолиновое, тетрагидроциннолиновое, пергидроциннолиновое, бензооксатиановое, дигидробензоксазиновое, дигидробензотиазиновое, пиразиноморфолиновое, бензодиоксановое, хромановое, бензодитиановое, азаспиро[4.5]декановое, тиаспиро[4.5]декановое, дитиаспиро[4.5]декановое, диоксаспиро[4.5]декановое и оксазаспиро[4.5]декановое кольца и тому подобное.
[0018]
В настоящем описании C3-8 моноциклический карбоцикл включает кольца циклопропановое, циклобутановое, циклопентановое, циклопентеновое, циклопентадиеновое, циклогексановое, циклогексеновое, циклогексадиеновое, бензольное, циклогептановое, циклогептеновое, циклогептадиеновое, циклооктановое, циклооктеновое и циклооктадиеновое кольца и тому подобное.
[0019]
В настоящем описании C3-6 насыщенный карбоцикл включает циклопропан, циклобутан, циклопентан и циклогексан.
[0020]
В настоящем описании 3-8-членный моноциклический гетероцикл относится к 3-8-членному моноциклическому гетероциклу, содержащему от 1 до 3 гетероатомов, выбранных из атома кислорода, атома азота и атома серы, и его примеры включают азиридиновое, оксирановое, тиирановое, азетидиновое, оксетановое, тиетановое, пиррольное, имидазольное, триазольное, тетразольное, пиразольное, фурановое, тиофеновое, оксазольное, изоксазольное, тиазольное, изотиазольное, фуразановое, оксадиазольное, тиадиазольное, пирролиновое, пирролидиновое, имидазолиновое, имидазолидиновое, триазолиновое, триазолидиновое, тетразолиновое, тетразолидиновое, пиразолиновое, пиразолидиновое, дигидрофурановое, тетрагидрофурановое, дигидротиофеновое, тетрагидротиофеновое, дигидрооксазольное, тетрагидрооксазольное (оксазолидиновое), дигидроизоксазольное, тетрагидроизоксазольное (изооксазолидиновое), дигидротиазольное, тетрагидротиазольное (тиазолидиновое), дигидроизотиазольное, тетрагидроизотиазольное (изотиазолидиновое), дигидрофуразановое, тетрагидрофуразановое, дигидрооксадиазольное, тетрагидрооксадиазольное (оксадиазолидиновое), дигидротиадиазольное, тетрагидротиадиазольное (тиадиазолидиновое), диоксолановое, дитиолановое, пиридиновое, пиразиновое, пиримидиновое, пиридазиновое, пирановое, тиопирановое, оксазиновое, оксадиазиновое, тиазиновое, тиадиазиновое, дигидропиридиновое, тетрагидропиридиновое, пиперидиновое, дигидропиразиновое, тетрагидропиразиновое, пиперазиновое, дигидропиримидиновое, тетрагидропиримидиновое, пергидропиримидиновое, дигидропиридазиновое, тетрагидропиридазиновое, пергидропиридазиновое, дигидропирановое, тетрагидропирановое, дигидротиопирановое, тетрагидротиопирановое, дигидрооксазиновое, тетрагидрооксазиновое, дигидрооксадиазиновое, тетрагидрооксадиазиновое, дигидротиазиновое, тетрагидротиазиновое, дигидротиадиазиновое, тетрагидротиадиазиновое, морфолиновое, тиоморфолиновое, оксатиановое, диоксановое, дитиановое, азепиновое, диазепиновое, оксепиновое, тиепиновое, оксазепиновое, оксадиазепиновое, тиазепиновое, тиадиазепиновое, дигидроазепиновое, тетрагидроазепиновое, пергидроазепиновое, дигидродиазепиновое, тетрагидродиазепиновое, пергидродиазепиновое, дигидрооксепиновое, тетрагидрооксепиновое, пергидрооксепиновое, дигидротиепиновое, тетрагидротиепиновое, пергидротиепиновое, дигидрооксазепиновое, тетрагидрооксазепиновое, пергидрооксазепиновое, дигидрооксадиазепиновое, тетрагидрооксадиазепиновое, пергидрооксадиазепиновое, дигидротиазепиновое, тетрагидротиазепиновое, пергидротиазепиновое, дигидротиадиазепиновое, тетрагидротиадиазепиновое и пергидротиадиазепиновое кольца и тому подобное.
[0021]
В настоящем описании 3-8-членный насыщенный моноциклический гетероцикл включает азиридиновое, оксирановое, тиирановое, азетидиновое, оксетановое, тиетановое, пирролидиновое, имидазолидиновое, триазолидиновое, тетразолидиновое, пиразолидиновое, тетрагидрофурановое, тетрагидротиофеновое, тетрагидрооксазольное (оксазолидиновое), тетрагидроизоксазольное (изооксазолидиновое), тетрагидротиазольное (тиазолидиновое), тетрагидроизотиазольное (изотиазолидиновое), тетрагидрофуразановое, тетрагидрооксадиазольное (оксадиазолидиновое), тетрагидротиадиазольное (тиадиазолидиновое), диоксолановое, дитиолановое, пиперидиновое, пиперазиновое, пергидропиримидиновое, пергидропиридазиновое, тетрагидропирановое, тетрагидротиопирановое, тетрагидрооксазиновое, тетрагидрооксадиазиновое, тетрагидротиазиновое, тетрагидротиадиазиновое, морфолиновое, тиоморфолиновое, оксатиановое, диоксановое, дитиановое, пергидроазепиновое, пергидродиазепиновое, пергидрооксепиновое, пергидротиепиновое, пергидрооксазепиновое, пергидрооксадиазепиновое, пергидротиазепиновое и пергидротиадиазепиновое кольца и тому подобное.
[0022]
В настоящем описании символ
[Химическая формула 6]

означает, что он прикреплен с другой стороне листа бумаги (то есть α-конфигурация), символ
[Химическая формула 7]

указывает, что он прикреплен с лицевой стороне бумаги (то есть β-конфигурация), и символ
[Химическая формула 8]

обозначает α-конфигурацию, β-конфигурацию или их смесь в любом соотношении.
[0023]
Из соединений, представленных общей формулой (I), предпочтительными вариантами являются, например, соединения, представленные общей формулой (I-a):
[Химическая формула 9]
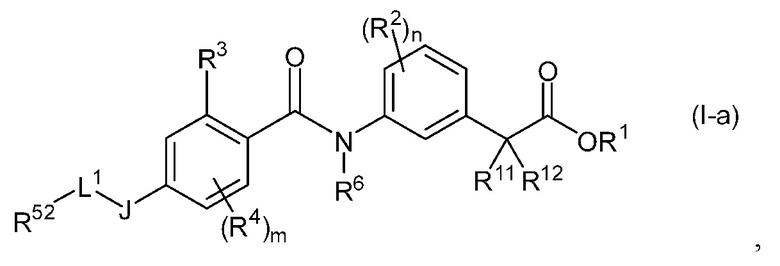
(где L1 представляет собой C1-6 алкиленовую, C2-6 алкениленовую или C2-6 алкиниленовую группу, R52 представляет собой C3-8 моноциклический карбоцикл или 3-8-членный моноциклический гетероцикл, и другие символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли, другими предпочтительными вариантами являются соединения, представленные общей формулой (I-b):
[Химическая формула 10]

(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли, и особенно предпочтительными вариантами являются соединения, представленные общей формулой (I-c-0):
[Химическая формула 11]

(где R1c представляет собой атом водорода или метильную группу, R2c представляет собой атом фтора или атом хлора, R3c представляет собой метильную группу или трифторметильную группу и R4c представляет собой атом водорода, метильную группу или трифторметильную группу, и, когда-Lc-Jc- представляет собой -O-, R54 представляет собой
[Химическая формула 12]
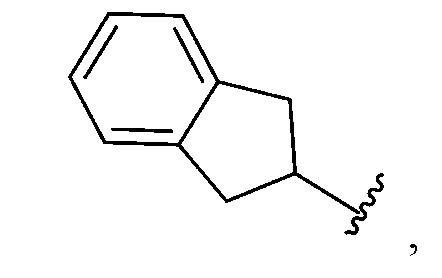
или, когда -Lc-Jc- представляет собой
[Химическая формула 13]
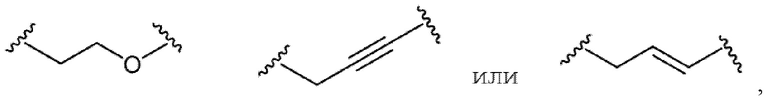
R54 представляет собой
[Химическая формула 14]
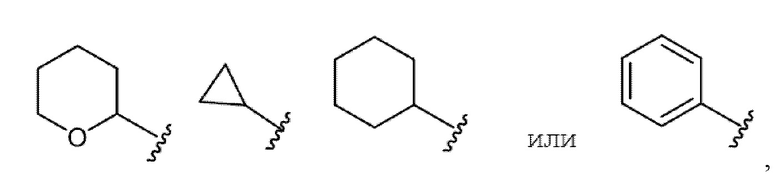
и другие символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли.
[0024]
Другими особенно предпочтительными вариантами являются соединения, представленные общей формулой (I-c):
[Химическая формула 15]

(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли.
[0025]
В общей формуле (I) другими предпочтительными вариантами являются соединения, представленные общей формулой (I-d):
[Химическая формула 16]
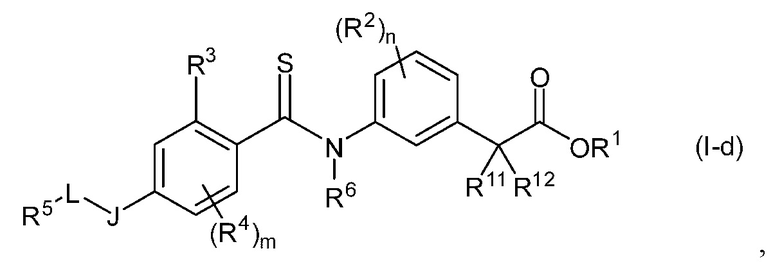
(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли. Более предпочтительными вариантами являются соединения, представленные общей формулой (I-1):
[Химическая формула 17]

(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли, и еще более предпочтительными вариантами являются соединения, представленные общей формулой (I-2-0):
[Химическая формула 18]

(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли, и другими более предпочтительными вариантами являются соединения, представленные общей формулой (I-2):
[Химическая формула 19]
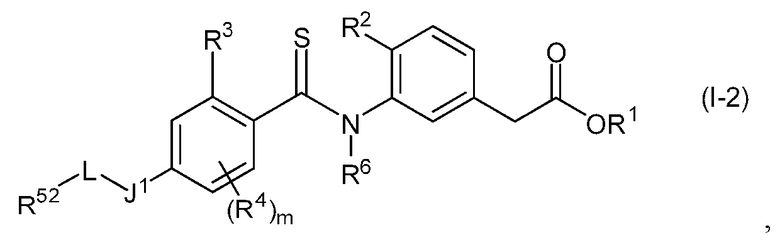
(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли. Наиболее предпочтительными вариантами являются соединения, представленные общей формулой (I-3-0):
[Химическая формула 20]

(где R53 представляет собой 3-8-членный насыщенный моноциклический гетероцикл, и другие символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли. Другими наиболее предпочтительными вариантами являются соединения, представленные общей формулой (I-3):
[Химическая формула 21]

(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли.
Альтернативно, наиболее предпочтительными вариантами являются соединения, представленные общей формулой (I-4):
[Химическая формула 22]
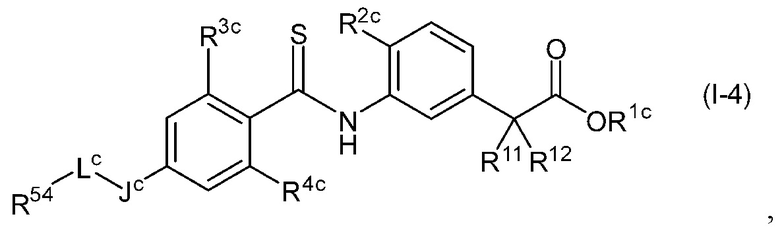
(где все символы имеют те же значения, которые описаны выше), и их фармацевтически приемлемые соли.
[0026]
В любой из общих формул (I), (I-a), (I-b), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) R1, предпочтительно, представляет собой атом водорода или C1-4 алкильную группу, более предпочтительно, атом водорода или метильную группу, и, особенно предпочтительно, атом водорода.
[0027]
Также в любой из общих формул (I-c-0), (I-c) и (I-4) R1c, предпочтительно, представляет собой атом водорода.
[0028]
В любой из общих формул (I), (I-a), (I-b), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) R2, предпочтительно, представляет собой атом галогена, более предпочтительно, атом фтора или атом хлора, и, особенно предпочтительно, атом хлора.
[0029]
Также, в любой из общих формул (I-c-0), (I-c) и (I-4) R2c, предпочтительно, представляет собой атом хлора.
[0030]
В любой из общих формул (I), (I-a), (I-b), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) R3, предпочтительно, представляет собой C1-4 алкильную группу, которая может быть замещена атомом галогена, и, особенно предпочтительно, метильную группу или трифторметильную группу.
[0031]
В любой из общих формул (I), (I-a), (I-b), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) R4, предпочтительно, представляет собой C1-4 алкильную группу, которая может быть замещена атомом галогена, более предпочтительно, метильную группу или трифторметильную группу, и, особенно предпочтительно, метильную группу.
[0032]
В общей формуле (I-c-0), (I-c) или (I-4) R4c, предпочтительно, представляет собой атом водорода или метильную группу.
[0033]
Также в любой из общих формул (I), (I-a), (I-b) и (I-d) J, предпочтительно, представляет собой связь или -O-, и, более предпочтительно, -O-.
[0034]
В любой из общих формул (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) J1, предпочтительно, представляет собой -O-.
[0035]
В общей формуле (I) или (I-d) R5, предпочтительно, представляет собой C3-10 карбоцикл или 3-10-членный гетероцикл, более предпочтительно, C3-8 моноциклический карбоцикл или 3-8-членный моноциклический гетероцикл, и, кроме того, предпочтительно, 3-8-членный насыщенный моноциклический гетероцикл. Альтернативно, в общей формуле (I) или (I-d) R5, предпочтительно, представляет собой циклопропановое, циклобутановое, циклопентановое, циклогексановое, бензольное или тетрагидропирановое кольцо, более предпочтительно, циклогексановое, бензольное, циклопропановое или тетрагидропирановое кольцо, и, наиболее предпочтительно, тетрагидропирановое кольцо. Кроме того, предпочтительно, R5 может быть замещен (предпочтительно, от 1 до 3) R7.
[0036]
В общей формуле (I-b) или (I-1) R51, предпочтительно, представляет собой C3-8 моноциклический карбоцикл или 3-8-членный моноциклический гетероцикл, и, более предпочтительно, 3-8-членный насыщенный моноциклический гетероцикл. Альтернативно, в общей формуле (I-b) или (I-1) R51, предпочтительно, представляет собой циклопропановое, циклобутановое, циклопентановое, циклогексановое, бензольное или тетрагидропирановое кольцо, более предпочтительно, циклогексановое, бензольное, циклопропановое или тетрагидропирановое кольцо, и, наиболее предпочтительно, тетрагидропирановое кольцо.
[0037]
В общей формуле (I-a), (I-2-0) или (I-2) R52, предпочтительно, представляет собой 3-8-членный насыщенный моноциклический гетероцикл. Альтернативно, в общей формуле (I-a), (I-2-0) или (I-2) R52, предпочтительно, представляет собой циклопропановое, циклобутановое, циклопентановое, циклогексановое, бензольное или тетрагидропирановое кольцо, более предпочтительно, циклопропановое, циклогексановое, бензольное или тетрагидропирановое кольцо, и, наиболее предпочтительно, тетрагидропирановое кольцо.
[0038]
В общей формуле (I-3-0) или (I-3) R53, предпочтительно, представляет собой тетрагидропирановое кольцо.
[0039]
В общей формуле (I-c-0), (I-c) или (1-4) R54, предпочтительно, представляет собой тетрагидропирановое кольцо.
[0040]
В общей формуле (I) Q, предпочтительно, представляет собой атом серы.
[0041]
В любой из общих формул (I), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) L, предпочтительно, представляет собой C1-6 алкиленовую, C2-6 алкениленовую или C2-6 алкиниленовую группу, более предпочтительно, этиленовую, пропениленовую или пропиниленовую, и, более предпочтительно, этиленовую группу.
[0042]
В общей формуле (I-a) L1, предпочтительно, представляет собой этиленовую, пропениленовую или пропиниленовую, и более предпочтительно, этиленовую группу.
[0043]
В общей формуле (I), (I-a), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) или (I-3) -L-J-, -L1-J- или -L-J1-, предпочтительно, представляет собой -O-,
[0043]
[Химическая формула 23]

и, более предпочтительно,
[Химическая формула 24]

[0044]
В любой из общих формул (I), (I-a), (I-b), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) R6, предпочтительно, представляет собой атом водорода.
[0045]
В любой из общих формул (I), (I-a), (I-b), (I-c), (I-d), (I-1), (I-2-0), (I-3-0) и (I-4) R11, предпочтительно, представляет собой атом водорода, метильную группу или этильную группу, более предпочтительно, атом водорода или метильную группу, и, наиболее предпочтительно, атом водорода.
[0046]
В любой из общих формул (I), (I-a), (I-b), (I-c), (I-d), (I-1), (I-2-0), (I-3-0) и (I-4) R12, предпочтительно, представляет собой атом водорода, метильную группу или этильную группу, более предпочтительно, атом водорода или метильную группу, и, наиболее предпочтительно, атом водорода.
[0047]
В любой из общих формул (I), (I-a), (I-b), (I-c), (I-d), (I-1), (I-2), (I-3) и (I-4) R11 и R12 могут быть взяты вместе с атомами углерода, к которым они присоединены, с образованием C3-6 насыщенного карбоцикла, и C3-6-членный насыщенный карбоцикл, предпочтительно, представляет собой циклопропановое кольцо.
[0048]
В любой из общих формул (I), (I-a), (I-b), (I-d) и (I-1) n, предпочтительно, обозначает 1.
[0049]
В любой из общих формул (I), (I-a), (I-b), (I-d), (I-1), (I-2-0), (I-2), (I-3-0) и (I-3) m, предпочтительно, обозначает 0 или 1, и, более предпочтительно, 1.
[0050]
В качестве соединения, представленного общей формулой (I), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R5, R6, R11, R12, J, L, Q, n и m объединены, являются предпочтительными.
[0051]
В качестве соединения, представленного общей формулой (I-a), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R52, R6, R11, R12, J, L1, n и m объединены, являются предпочтительными.
[0052]
В качестве соединения, представленного общей формулой (I-b), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R51, R6, R11, R12, J, n и m объединены, являются предпочтительными.
[0053]
В качестве соединения, представленного общей формулой (I-c-0), соединения, в которых некоторые или все из указанных выше предпочтительных R1c, R2c, R3c, R4c, R11, R12, Jc, Lc и R54 объединены, являются предпочтительными.
[0054]
В качестве соединения, представленного общей формулой (I-c), соединения, в которых некоторые или все из указанных выше предпочтительных R1c, R2c, R3c, R4c, Jc, Lc и R54 объединены, являются предпочтительными.
[0055]
В качестве соединения, представленного общей формулой (I-d), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R5, R6, R11, R12, J, L, n и m объединены, являются предпочтительными.
[0056]
В качестве соединения, представленного общей формулой (I-1), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R51, R6, R11, R12, J1, L, n и m объединены, являются предпочтительными.
[0057]
В качестве соединения, представленного общей формулой (I-2-0), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R52, R6, R11, R12, J1, L и m объединены, являются предпочтительными.
[0058]
В качестве соединения, представленного общей формулой (I-2), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R52, R6, J1, L и m объединены, являются предпочтительными.
[0059]
В качестве соединения, представленного общей формулой (I-3-0), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R53, R6, R11, R12, J1, L и m объединены, являются предпочтительными.
[0060]
В качестве соединения, представленного общей формулой (I-3), соединения, в которых некоторые или все из указанных выше предпочтительных R1, R2, R3, R4, R53, R6, J1, L и m объединены, являются предпочтительными.
[0061]
В качестве соединения, представленного общей формулой (I-4), соединения, в которых некоторые или все из указанных выше предпочтительных R1c, R2c, R3c, R4c, Jc, Lc, R11, R12 и R54 объединены, являются предпочтительными.
[0062]
В настоящем описании другой вариант общей формулы (I) наиболее предпочтительно представляет собой соединение по настоящему изобретению, описанное в примерах ниже, или его фармацевтически приемлемую соль.
[0063]
[Изомер]
В настоящем изобретении, если не указано иное, охватываются все изомеры. Например, алкильные группы, алкоксигруппы, алкиленовые группы и тому подобное включают группы с прямой и разветвленной цепью. Кроме того, настоящим изобретением охватываются изомеры (E, Z, цис-, транс-изомеры) по двойной связи, в кольце или конденсированном кольце, изомеры из-за наличия асимметричного углерода или тому подобное (R-, S-форма, α-, β-конфигурация, энантиомеры, диастереомеры), оптически активные вещества с рацемическими свойствами (D, L, d, l-формы), полярные соединения, полученные хроматографическим разделением (высокополярные соединения, низкополярные соединения), равновесные соединения, изомеры вращения и смеси в любых соотношениях и их рацемические смеси в любом соотношении. Более того, настоящим изобретением также охватываются все изомеры, образованные из-за таутомерии.
В настоящем изобретении все ссылки на соединение по настоящему изобретению включают соединения, представленные общей формулой (I), их фармацевтически приемлемые соли, их N-оксиды, их сольваты или их сокристаллы.
[0064]
[Соль]
Соединение, представленное общей формулой (I), преобразуют в соль известным способом.
Соль представляет собой фармацевтически приемлемую соль.
Предпочтительно соль является водорастворимой.
Примеры фармацевтически приемлемой соли включают кислотно-аддитивные соли, соли щелочных металлов, соли щелочноземельных металлов, соли аммония, соли аминов и тому подобное.
Примеры кислотно-аддитивных солей включают соли неорганических кислот, такие как гидрохлориды, гидробромиды, гидройодиды, сульфаты, фосфаты и нитраты, и соли органических кислот, такие как ацетаты, лактаты, тартраты, бензоаты, цитраты, метансульфонаты, этансульфонаты, трифторацетаты, бензолсульфонаты, толуолсульфонаты, изетионаты, глюкуронаты и глюконаты.
Примеры соли щелочного металла включают соли калия, соли натрия и тому подобное.
Примеры соли щелочноземельного металла включают соли кальция, соли магния и тому подобное.
Примеры соли аммония включают соли тетраметиламмония и тому подобное.
Примеры соли амина включают соли триэтиламина, соли метиламина, соли диметиламина, соли циклопентиламина, соли бензиламина, соли фенетиламина, соли пиперидина, соли моноэтаноламина, соли диэтаноламина, соли трис(гидроксиметил)аминометана, соли лизина, соли аргинина, соли N-метил-D-глюкамина и тому подобное.
[N-оксид]
Соединение, представленное общей формулой (I), можно преобразовать в N-оксид любым способом. N-оксид представляет собой соединение, в котором атом азота в соединении, представленном общей формулой (I), окислен. N-оксид соединения, представленного общей формулой (I), может быть солью.
[0066]
[Сольват]
Соединение, представленное общей формулой (I), его фармацевтически приемлемая соль и его N-оксид могут существовать в несольватированной форме или могут существовать в сольватированной форме с фармацевтически приемлемым растворителем, таким как вода или этанол. Соединение, представленное общей формулой (I), его фармацевтически приемлемая соль и его N-оксид можно преобразовать в сольват известным способом.
Сольват, предпочтительно, является нетоксичным и водорастворимым. Примеры подходящего сольвата включают сольваты, подобные гидратам или со спиртовыми растворителями (например, этанолом и т.д.).
[0067]
[Сокристалл]
Соединение, представленное общей формулой (I), его фармацевтически приемлемая соль и его N-оксид могут образовывать сокристаллы с подходящим агентом, образующим сокристаллы. Агент, образующий сокристаллы, предпочтительно, является фармацевтически приемлемым. Сокристалл обычно определяется как кристалл, в котором две или более различных молекул образованы межмолекулярными взаимодействиями, которые отличаются от ионных связей. Кроме того, сокристалл может быть комплексом нейтральной молекулы и соли. Состав сокристалла можно регулировать известными методами, такими как кристаллизация из расплава, перекристаллизация из растворителя или совместное физическое измельчение компонентов. Подходящий агент, образующий сокристаллы, включает агенты, описанные в WO 2006/007448 A.
[0068]
[Пролекарство]
Соединение, представленное общей формулой (I), можно вводить в виде пролекарства. Пролекарство соединения, представленного общей формулой (I), относится к соединению, которое преобразуется в соединение, представленное общей формулой (I), путем in vivo взаимодействия с ферментом, желудочной кислотой или подобным. Примеры пролекарства соединения, представленного общей формулой (I), включают такие, когда соединение, представленное общей формулой (I), имеет карбоксильную группу, соединения, в которых карбоксильная группа этерифицирована или амидирована (например, соединения, в которых карбоксильная группа соединения, представленного общей формулой (I), является этилэтерифицированной, фенилэтерифицированной, карбоксиметилэтерифицированной, диметиламинометилэтерифицированной, пивалоилоксиметилэтерифицированной, 1-{(этоксикарбонил)окси}этилэтерифицированной, фталидилэтерифицированной, (5-метил-2-оксо-1,3-диоксолен-4-ил)метилэтерифицированной, 1-{[(циклогексилокси)карбонил]окси}этилэтерифицированной, метиламидированной и т.д.) и тому подобное. Эти соединения могут быть получены известным способом. Кроме того, пролекарство соединения, представленного общей формулой (I), может быть заменено на соединение, представленное общей формулой (I), в физиологических условиях, описанных в обзоре «Development of Drug», опубликованном в 1990 Hirokawa Shoten, т. 7, «Molecular Design», стр. 163-198. Пролекарство соединения, представленного общей формулой (I), может быть солью или сольватом или может образовывать сокристалл с подходящим агентом, образующим сокристаллы.
[0069]
[Меченое соединение]
Соединение по настоящему изобретению также включает так называемые меченые соединения, в которых некоторые или все составляющие их атомы заменены на свои изотопы. Эти меченые соединения могут быть получены известным способом. В качестве изотопов, используемых для мечения, можно подходящим образом использовать, например, 2H, 3H, 11C, 13C, 14C, 13N, 15N, 17O, 18O, 18F, 35S, 36Cl, 77Br, 125I и тому подобное, но этим не ограничивается.
[0070]
[Способ получения соединения по настоящему изобретению]
Соединение по настоящему изобретению, представленное общей формулой (I), может быть получено известным способом, например, способом, описанным в руководстве Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition (Richard C. Larock, John Wiley & Sons Inc, 2018), способом, показанным ниже, способом, эквивалентный им, или способом, показанным в примерах. В каждом из следующих способов получения исходное соединение может использоваться в виде соли. В качестве такой соли предпочтительны соли, описанные как фармацевтически приемлемые соли соединения по настоящему изобретению, представленного общей формулой (I).
[0071]
Из соединений, представленных общей формулой (I), соединение в котором R1 представляет собой атом водорода, J представляет собой -O- или -S- и Q представляет собой атом кислорода, то есть соединение, представленное общей формулой (Ia):
[Химическая формула 25]

(где Ja представляет собой -O- или -S-, и другие символы имеют те же значения, что и выше)
может быть получено в соответствии со следующей схемой A стадий реакций.
[Химическая формула 26]
Схема A стадий реакций

(где P представляет собой защитную группы для группы карбокси, а другие символы имеют те же значения, которые описаны выше)
То есть соединение, представленное общей формулой (IIa), и соединение, представленное общей формулой (IIIa), подвергают реакции Мицунобу с получением соединения, представленного общей формулой (IVa), и затем проводят реакцию удаления защитной группы у карбоксильной группы, в результате чего может быть получено соединение, представленное общей формулой (Ia).
[0072]
Реакция Мицунобу известна и проводится, например, путем взаимодействия спирта с производным фенола или производным тиофенола при температуре от 0 до 60°C в органическом растворителе (дихлорметан, диэтиловый эфир, тетрагидрофуран, ацетонитрил, бензол, толуол и т.д.) в присутствии комбинации реагента Мицунобу (диазосоединение (диэтилазодикарбоновая кислота (DEAD), диизопропилазодикарбоксилат, 1,1ʼ-(азодикарбонил)дипиперидин, 1,1ʼ-азобис(N, N-диметилформамид) и т.д.) и фосфиновое соединение (трифенилфосфин, трибутилфосфин, триметилфосфин, трифенилфосфин на полимерной основе и т.д.) или илидный реагент (цианометилентриметилфосфоран (CMMP), цианометилентрибутилфосфоран (CMBP) и т.д.).
[0073]
Соединение, представленное общей формулой (IVa), также может быть получено, подвергая реакции алкилирования соединение, представленное общей формулой (Va):
[Химическая формула 27]
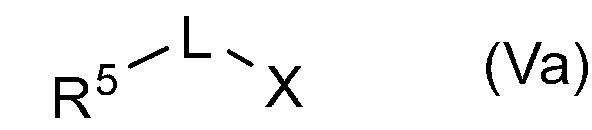
(где X представляет собой удаляемую группу, такую как атом галогена, тозилокси группа (TsO-) или мезилокси группа (MsO-), и другие символы имеют те же значения, которые описаны выше) и соединение, представленное общей формулой (IIIa).
Эта реакция алкилирования известна и проводится при температуре от 0 до 100°C, например, в органическом растворителе (диметилформамид, диметилсульфоксид, хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран, метил-трет-бутиловый эфир и т.д.), в присутствии гидроксида щелочного металла (гидроксид натрия, гидроксид калия, гидроксид лития и т.д.), гидроксида щелочноземельного металла (гидроксид бария, гидроксид кальция и т.д.) или карбоната (карбонат натрия, карбонат калия и т.д.) или их водного раствора, или их смесей.
[0074]
На схеме A стадий реакций реакция удаления защиты у карбокси группы известна и может быть проведена следующим образом.
Примеры защитной группы для карбокси группы включают метильную группу, этильную группу, аллильную группу, трет-бутильную группу, трихлорэтильную группу, бензильную (Bn) группу, фенацильную группу и тому подобное. Защитная группа для карбокси группы особо не ограничивается при условии, что это группа, которая может быть легко и селективно отщеплена, помимо тех, которые описаны выше. Например, используются группы, описанные Peter G. M. Wuts, Green's Protective Groups in Organic Synthesis, Fifth Edition, Wiley, New York, 2014.
Реакция удаления защиты у карбокси группы хорошо известна, и ее примеры включают:
(1) щелочной гидролиз,
(2) реакция удаления защиты в кислых условиях,
(3) реакция удаления защиты путем гидрирования,
(4) реакция удаления защитной силильной группы,
(5) реакция удаления защиты с использованием металла,
(6) реакция удаления защиты с использованием комплекса металла и тому подобное.
Эти методы конкретно описаны ниже.
(1) Реакцию удаления защиты щелочным гидролизом проводят, например, в органическом растворителе (метанол, тетрагидрофуран, диоксан и т.д.), с использованием гидроксида щелочного металла (гидроксид натрия, гидроксид калия, гидроксид лития и т.д.), гидроксида щелочноземельного металла (гидроксид бария, гидроксид кальция и т.д.) или карбоната (карбонат натрия, карбонат калия и т.д.) или их водного раствора или их смеси при температуре от 0 до 60°C.
(2) Реакцию удаления защиты в кислых условиях проводят, например, в органическом растворителе (дихлорметан, хлороформ, диоксан, этилацетат, анизол и т.д.), в органической кислоте (уксусная кислота, трифторуксусная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.д.) или неорганической кислоте (соляная кислота, серная кислота и т.д.) или их смеси (бромистый водород/уксусная кислота и т.д.) при температуре от 0 до 100°С.
(3) Реакцию удаления защиты путем гидрирования проводят, например, в растворителе (простые эфиры (тетрагидрофуран, диоксан, диметоксиэтан, диэтиловый эфир и т.д.), спирты (метанол, этанол и т.д.), бензолы (бензол, толуол и т.д.), кетоны (ацетон, метилэтилкетон и т.д.), нитрилы (ацетонитрил и т.д.), амиды (диметилформамид и т.д.), вода, этилацетат, уксусная кислота или смесь двух или более из них и т.д.) в присутствии катализатора (палладий на угле, палладиевая чернь, гидроксид палладия, оксид платины, никель Ренея и т.д.) в атмосфере водорода при нормальном или повышенном давлении или в присутствии формиата аммония при температуре от 0 до 200°C.
(4) Реакцию удаления защитной силильной группы проводят, например, в смешивающемся с водой органическом растворителе (тетрагидрофуран, ацетонитрил и т.д.), с использованием фторида тетрабутиламмония при температуре от 0 до 40°C.
(5) Реакцию удаления защиты с использованием металла проводят, например, в кислотном растворителе (уксусная кислота, буфер с pH от 4,2 до 7,2 или их смешанный раствор с органическим растворителем, таким как тетрагидрофуран) в присутствии порошка цинка, при необходимости, с применением ультразвука, при температуре от 0 до 40°C.
(6) Реакцию удаления защиты с использованием комплекса металла проводят, например, в органическом растворителе (дихлорметан, диметилформамид, тетрагидрофуран, этилацетат, ацетонитрил, диоксан, этанол и т.д.), воде или их смешанном растворителе, в присутствии реагента-улавливателя (гидрид трибутилолова, триэтилсилан, димедон, морфолин, диэтиламин, пирролидин и т.д.), в присутствии органической кислоты (уксусная кислота, муравьиная кислота, 2-этилгексановая кислота и т.д.) и/или соли органической кислоты (2-этилгексаноат натрия, 2-этилгексаноат калия и т.д.), в присутствии или в отсутствие фосфинового реагента (трифенилфосфин и т.д.), с использованием комплекса металлов (тетракистрифенилфосфинпалладий (0), дихлорид бис(трифенилфосфин)палладия (II), ацетат палладия (II), хлорид трис(трифенилфосфин)родия (I) и т.д.) при температуре от 0 до 40°С.
В дополнение к вышесказанному, реакция удаления защиты может быть проведена способом, описанным, например, Peter G. M. Wuts, Green's Protective Groups in Organic Synthesis, Fifth Edition, Wiley, New York, 2014.
Специалистам в данной области легко понять, что целевое соединение по настоящему изобретению может быть легко получено при правильном использовании этих реакций удаления защиты.
[0075]
Из соединений, представленных общей формулой (I), соединение в котором R1 представляет собой атом водорода, Q представляет собой атом кислорода, J представляет собой связь и L представляет собой алкиниленовую группу, то есть соединение, представленное общей формулой (Ib):
[Химическая формула 28]
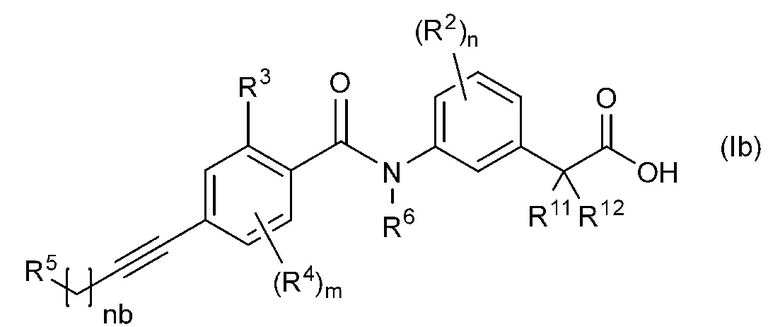
(где nb обозначает целое число от 0 до 4, и другие символы имеют те же значения, что и выше),
может быть получено, подвергая реакции сочетания соединение, представленное общей формулой (IIIb):
[Химическая формула 29]

(где X представляет собой атом галогена или трифторметансульфонилокси группу (TfO-), и другие символы имеют те же значения, которые описаны выше) и соединение, представленное общей формулой (Vb):
[Химическая формула 30]

(где все символы имеют те же значения, что и выше),
а затем реакции удаления защиты у карбокси группы. Эта реакция сочетания известна, и соединение может быть получено взаимодействием соединения, представленного общей формулой (IIIb), и соединения, представленного общей формулой (Vb), например, в органическом растворителе (например, тетрагидрофуран, N, N-диметилформамид, ацетонитрил и т.д.) в присутствии палладиевого катализатора (хлорид бистрифенилфосфинпалладия (II) и т.д.), в присутствии медного катализатора (йодид меди (I) и т.д.) и в присутствии основания (триэтиламин и т.д.) при температуре от комнатной до температуры кипения.
[0076]
Из соединений, представленных общей формулой (I), соединение, в котором R1 представляет собой атом водорода, Q представляет собой атом кислорода, J представляет собой связь и L представляет собой алкениленовую или алкиленовую группу, может быть получено, подвергая соединение, представленное общей формулой (Ib), реакции восстановления.
Реакция восстановления известна и ее проводят, например, в атмосфере водорода в органическом растворителе (например, метанол, этанол, этилацетат, тетрагидрофуран, уксусная кислота, 1,2-диметоксиэтан или растворитель, полученный смешиванием соответствующим образом этих органических растворителей и т.д.) или в смешанном растворителе из органических растворителей и воды в присутствии палладиевого катализатора (например, палладий на угле, гидроксид палладия, катализатор Линдлара и т.д.) при температуре от комнатной до около 80°C.
[0077]
Из соединений, представленных общей формулой (I), соединение, в котором R1 представляет собой атом водорода и Q представляет собой атом серы, то есть соединение, представленное общей формулой (Ic):
[Химическая формула 31]
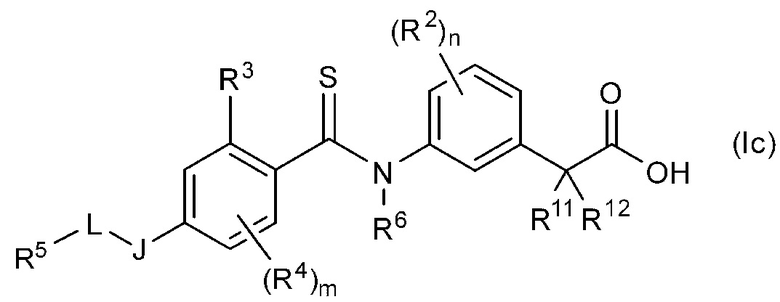
(где все символы имеют те же значения, которые описаны выше), может быть получено в соответствии со следующей схемой C стадий реакций.
[Химическая формула 32]
Схема C стадий реакций

(где все символы имеют те же значения, что и выше).
То есть соединение, представленное общей формулой (IVa), подвергают реакции тиолирования с получением соединения, представленного общей формулой (Vc), а затем проводят реакцию удаления защиты у карбокси группы, в результате чего может быть получено соединение, представленное общей формулой (Ic).
[0078]
На схеме C стадий реакций реакция тиолирования является известной, и соединение может быть получено путем взаимодействия амидного соединения в органическом растворителе (например, тетрагидрофуран, толуол, бензол, ацетонитрил, дихлорметан, пиридин и т.д.) в присутствии или в отсутствие основания (бикарбонат натрия и т.д.) в присутствии или в отсутствие реагента тиолирования (например, реагент Лавессона (2,4-бис(4-метоксифенил)-1,3,2,4-дитиадифосфетан-2,4-дисульфид), декасульфид тетрафосфора, пентасульфид дифосфора, сероводород, сера и т.д.) и фосфинового реагента (например, трихлорфосфат и т.д.) при температуре от комнатной до температуры дефлегмации.
[0079]
В каждой из вышеуказанных реакций соединение, используемое в качестве исходного материала, известно или может быть легко получено известным способом.
Например, соединение, представленное общей формулой (IIIa):
[Химическая формула 33]

(где все символы имеют такое же значение, как описано выше), может быть получено путем проведения реакции введения защиты/удаления защиты, если необходимо, согласно следующей схемой D стадий реакций.
[Химическая формула 34]
Схема D стадий реакций
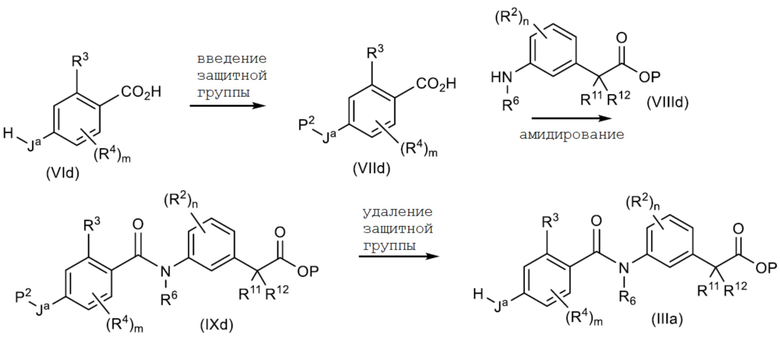
(где P2 представляет собой защитную группу для гидроксильной группы или тиольной группы, а другие символы имеют такие же значения, как описано выше)
То есть соединение, представленное общей формулой (VId), подвергают реакции введения защиты для гидроксильной группы или тиольной группы с получением соединения, представленного общей формулой (VIId), а затем подвергают реакции амидирования с соединением, представленным общей формулой (VIIId), посредством которой может быть получено соединение, представленное общей формулой (IXd). Затем соединение, представленное общей формулой (IXd), подвергают реакции удаления защиты у гидроксильной группы или тиольной группы, в результате чего может быть получено соединение, представленное общей формулой (IIIa).
[0080]
Примеры защитной группы для гидроксильной группы включают метильную группу, тритильную группу, метоксиметильную (MOM) группу, 1-этоксиэтильную (EE) группу, метоксиэтоксиметильную (MEM) группу, 2-тетрагидропиранильную (THP) группу, триметилсилильную (TMS) группу, триэтилсилильную (TES) группу, трет-бутилдиметилсилильную (TBDMS) группу, трет-бутилдифенилсилильную группу (TBDPS), ацетильную (Ac) группу, пивалоильную группу, бензоильную группу, бензильную (Bn) группу, п-метоксибензильную группу, аллилоксикарбонильную (Alloc) группу, 2,2,2-трихлорэтоксикарбонильную (Troc) группу и тому подобное.
Примеры защитной группы для тиольной группы включают бензильную группу, метоксибензильную группу, метоксиметильную (MOM) группу, 2-тетрагидропиранильную (THP) группу, дифенилметильную группу и ацетильную (Ac) группу.
[0081]
Защитная группа для гидроксильной группы или тиольной группы особо не ограничивается при условии, что она представляет собой группу, которая может быть легко и селективно отщеплена, помимо тех, которые описаны выше. Например, используются группы, описанные Peter G. M. Wuts, Green's Protective Groups in Organic Synthesis, Fifth Edition, Wiley, New York, 2014.
[0082]
На схеме D стадий реакций реакция амидирования является известной, и ее примеры включают:
(1) способ с использованием галогенида кислоты,
(2) способ с использованием смешанного ангидрида кислоты,
(3) способ с использованием конденсирующего агента и тому подобное.
Эти методы конкретно описаны ниже.
(1) Способ с использованием галогенангидрида осуществляется, например, путем взаимодействия карбоновой кислоты с кислотным галогенирующим агентом (оксалилхлорид, тионилхлорид и т.д.) в органическом растворителе (хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран и т.д.) или в отсутствие растворителя при температуре от -20°C до температуры кипения с обратным холодильником и взаимодействия полученного галогенангидрида с амином в присутствии основания (пиридин, триэтиламин, диметиланилин, диметиламинопиридин, диизопропилэтиламин и т.д.) в органическом растворителе (хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран и т.д.) при температуре от 0 до 80°C. Альтернативно, реакцию также можно проводить путем взаимодействия полученного галогенангидрида с амином в органическом растворителе (диоксан, тетрагидрофуран и т.д.) с использованием щелочного водного раствора (раствор бикарбоната натрия, раствор гидроксида натрия и т.д.) при температуре от 0 до 40°C.
(2) Способ с использованием смешанного ангидрида кислоты осуществляют, например, путем взаимодействия карбоновой кислоты с галогенангидридом (пивалоилхлорид, тозилхлорид, мезилхлорид и т.д.) или производным кислоты (этилхлорформиат, изобутилхлорформиат и т.д.) при температуре от 0 до 40°C в присутствии основания (пиридин, триэтиламин, диметиланилин, диметиламинопиридин, диизопропилэтиламин и т.д.) в органическом растворителе (хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран и т.д.) или в отсутствие растворителя и взаимодействия полученного смешанного ангидрида кислоты с амином при температуре от 0 до 40°C в органическом растворителе (хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран и т.д.).
(3) Способ с использованием конденсирующего агента осуществляют, например, путем взаимодействия карбоновой кислоты с амином в органическом растворителе (хлороформ, дихлорметан, диметилформамид, диэтиловый эфир, тетрагидрофуран и т.д.) или в отсутствие растворителя при температуре от 0 до 80°C в присутствии или в отсутствие основания (пиридин, триэтиламин, диметиланилин, диметиламинопиридин и т.д.) с использованием конденсирующего агента (1,3-дициклогексилкарбодиимид (DCC), 1-этил-3-[3-(диметиламино)пропил]карбодиимид (EDC), 1,1′-карбонилдиимидазол (CDI), 2-хлор-1-метилпиридиний йод, циклический ангидрид 1-пропилфосфоновой кислоты (циклический ангидрид 1-пропанфосфоновой кислоты, T3P) и т.д.) присутствии или в отсутствие 1-гидроксибензтриазола (HOBt).
Желательно, чтобы все реакции (1), (2) и (3) проводились в атмосфере инертного газа (аргон, азот и т.д.) в безводных условиях.
[0083]
Реакция удаления защиты у гидроксильной группы или тиольной группы в реакционной стадии формулы D известна и может быть проведена таким же образом, как реакция удаления защиты у карбокси группы по схеме A стадий реакций.
Специалистам в данной области легко понять, что целевое соединение по настоящему изобретению может быть легко получено при правильном использовании этих реакций удаления защитных групп.
[0084]
Соединения, используемые в качестве других исходных материалов, и соединения, используемые в качестве реагентов, известны сами по себе или могут быть легко получены с использованием способов в сочетании с известным методом, например, способом, описанным в руководстве Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition (Richard C. Larock, John Wiley & Sons Inc, 2018).
[0085]
В реакциях, описанных в настоящем описании, каждая группа может быть защищена, когда требуется защита, и соединение с защищенной защитной группой может быть соответствующим образом подвергнуто известной реакции удаления защиты.
[0086]
Реакции, описанные в настоящем описании, включающие нагревание, могут быть осуществлены, как очевидно специалистам в данной области, с использованием водяной бани, масляной бани, песочной бани или микроволновой печи.
[0087]
В реакциях, описанных в настоящем описании, может использоваться твердофазный реагент на носителе, который нанесен на высокомолекулярный полимер (например, полистирол, полиакриламид, полипропилен, полиэтиленгликоль и т.д.).
[0088]
В реакциях, описанных в настоящем описании, продукты реакции могут быть очищены в соответствии с обычными способами очистки, такими как перегонка при нормальном или пониженном давлении, высокоэффективная жидкостная хроматография с использованием силикагеля, силиката магния и тому подобное, тонкослойная хроматография, ионообменные смолы, смолы-поглотители или колоночная хроматография, или промывка и перекристаллизация. Очистку можно проводить после каждой реакции или после нескольких реакций.
[0089]
[Токсичность]
Соединение по настоящему изобретению имеет очень низкую токсичность и достаточно безопасно для использования в качестве лекарственного средства.
[0090]
[Применение в фармацевтических препаратах]
Поскольку соединение по настоящему изобретению обладает превосходной антагонистической активностью к рецепторам DP, оно может быть использовано для лечения заболевания, опосредованного рецептором DP, такого как аллергическое заболевание, системный мастоцитоз, системное нарушение активации тучных клеток, анафилактический шок, сужение дыхательных путей, крапивница, экзема, акне, аллергический бронхолегочный аспергиллез, синусит, мигрень, полипы в носу, гиперчувствительный васкулит, эозинофилия, контактный дерматит, заболевание, сопровождающееся зудом, заболевание, вызванное вторично состоянием, сопровождающимся зудом, заболевание, сопровождающееся покраснением кожи, воспаление, хроническая обструктивная болезнь легких, ишемически-реперфузионное повреждение, нарушение мозгового кровообращения, аутоиммунное заболевание, церебральная травма, заболевание печени, отторжение трансплантата, ревматоидный артрит, плеврит, остеоартрит, болезнь Крона, язвенный колит, синдром раздраженного кишечника, интерстициальный цистит, мышечная дистрофия, полимиозит, злокачественное новообразование, лейкемия, вирусная инфекция, рассеянный склероз, нарушение сна или агрегация тромбоцитов. Кроме того, поскольку соединение по настоящему изобретению обладает превосходной способностью проникать в центральную нервную систему, оно особенно полезно при нарушении сна и бодрствования, например, гиперсомнии (например, нарколепсия, внезапная гиперсомния, рецидивирующая гиперсомния и синдром Кляйне-Левина и т.д.), бессоннице, остаточной сонливости синдрома апноэ во сне, расстройстве циркадного ритма сна и бодрствования (например, нарушение циркадного ритма сменной работы, нарушение ритма нерегулярного сна и бодрствования и т.д.), гиперсомнии, связанной с нейродегенеративным заболеванием (например, болезнь Паркинсона, деменция с тельцами Леви, деменция Альцгеймера и т.д.), гиперсомнии, связанной с психическим заболеванием (например, депрессия, биполярное расстройство и т.д.) и патологическом апноэ во сне в дневное время.
[0091]
Соединение по настоящему изобретению можно комбинировать с другим лекарственным средством, чтобы вводить в качестве сопутствующего лекарственного средства, чтобы:
1) дополнить и/или усилить профилактический и/или терапевтический эффект соединения;
2) улучшить кинетику и поглощение и снизить дозу соединения; и/или
3) уменьшить побочный эффект соединения.
[0092]
Сопутствующее лекарственное средство соединения по настоящему изобретению и другое лекарственное средство можно вводить в форме комбинированного агента, содержащего оба компонента в одном препарате, или можно вводить в виде отдельных препаратов. При введении в виде отдельных препаратов включаются одновременное введение и поэтапное введение. Кроме того, для ступенчатого введения соединение по настоящему изобретению можно вводить первым, а другое лекарство можно вводить позже, или другое лекарство можно вводить первым, а соединение по настоящему изобретению можно вводить позже. Все способы введения могут быть одинаковыми или разными.
[0093]
Заболевание, на которое сопутствующее лекарственное средство оказывает профилактический и/или терапевтический эффект, особо не ограничивается, и это может быть любым заболеванием, при котором дополняется и/или усиливается профилактический и/или терапевтический эффект соединения по настоящему изобретению.
[0094]
Примеры другого лекарственного средства для дополнения и/или усиления профилактического и/или терапевтического действия соединений по настоящему изобретению на нарушения сна и бодрствования включают психостимуляторы (например, модафинил, метилфенидат (гидрохлорид), метамфетамин (гидрохлорид), пемолин и т.д.), средства для лечения нарколепсии (например, гамма-гидроксимасляная кислота, кломипрамин и т.д.), ингибиторы ацетилхолинэстеразы (например, донепезил (гидрохлорид), физостигмин, ривастигмин (тартрат), галантамин (гидробромид), занапезил (фумарат); TAK-147, такрин, метрифонат и т.д.), антагонисты рецепторов NMDA (например, кетамин, мемантин, гидробромид декстрометорфана и т.д.), агонисты дофаминовых рецепторов (например, леводопа, бромокриптин, перголид, талипексол, прамипексол (гидрохлорид) (гидрат), каберголин, амантадин (гидрохлорид) и т.д.), трициклические антидепрессанты (например, гидрохлорид амитриптилина, гидрохлорид имипрамина и т.д.), селективные ингибиторы обратного захвата серотонина (например, пароксетин, эсциталопрам и т.д.), средства для лечения мании (например, карбонат лития и т.д.), антипсихотические средства (например, клофектон, спиперон, сульпирид, зотепин, тимиперон, галоперидол деканоат, галоперидол, пимозид, проперициазин, бромперидол, перфеназин, малеат левомепромазина, хлорпромазина гидрохлорид, тиоридазина гидрохлорид, тразодона гидрохлорид, мосапрамина гидрохлорид, рисперидон, оланзапин и т.д.), ингибиторы обратного захвата норадреналина (например, атомоксетин и т.д.) и тому подобное.
[0095]
Массовое отношение соединения настоящего изобретения к другому лекарственному средству особо не ограничивается.
Другое лекарство можно вводить в комбинации двух или более типов.
[0096]
Кроме того, другой агент, который дополняет и/или усиливает профилактический и/или терапевтический эффект соединения по настоящему изобретению, включает такой, который до сих пор были обнаружены на основе вышеуказанного механизма, а также такие, которые будут обнаружены в будущем.
[0097]
Чтобы использовать соединение по настоящему изобретению в качестве единственного агента или в комбинации с другим агентом в качестве сопутствующего лекарственного средства, с целью профилактики и/или лечения вышеуказанных заболеваний, вещество в качестве активного ингредиента обычно готовят с различными добавками или фармацевтически приемлемыми носителями, такими как растворитель, а затем их вводят системно или местно в пероральной или парентеральной форме. В настоящем документе фармацевтически приемлемый носитель означает вещество, отличное от активного ингредиента, которое обычно используется при изготовлении фармацевтических препаратов. Фармацевтически приемлемый носитель, предпочтительно, не оказывает фармакологического действия в дозе препарата, безвреден и не влияет на терапевтический эффект активного ингредиента. Кроме того, фармацевтически приемлемый носитель также можно использовать с целью повышения полезности активного ингредиента и препарата, упрощения составления препарата, стабилизации качества, улучшения удобства использования или тому подобное. В частности, надлежащим образом в соответствии с целью могут быть выбраны вещества, подобные тем, которые описаны в «Энциклопедии фармацевтических добавок» (под редакцией Международного совета по фармацевтическим вспомогательным веществам Японии), опубликованной в 2016 году компанией Yakuji Nippo, Limited.
[0098]
Примеры лекарственной формы, используемой для введения, включают препараты для перорального введения (например, таблетки, капсулы, гранулы, порошки, жидкости и растворы для перорального введения, сиропы, желе для перорального введения и т.д.), препараты для нанесения на слизистые оболочки полости рта (например, таблетки для нанесения на слизистые оболочки рта, спреи для нанесения на слизистые оболочки полости рта, полутвердые препараты для нанесения на слизистые оболочки полости рта, препараты для полосканий и т.д.), препараты для диализа (например, диализные агенты и т.д.), препараты для ингаляции (например, летучий препарат и т.д.), препараты для офтальмологического применения (например, глазные жидкости и растворы, офтальмологические мази и т.д.), препараты для ушных аппликаций (например, ушные препараты и т.д.), препараты для назального применения (например, назальные препараты и т.д.), препараты для ректального применения (например, суппозитории для ректального применения, полутвердые препараты для ректального применения, клизмы для ректального применения и т.д.), препараты для вагинального применения (например, вагинальные таблетки, вагинальные суппозитории и т.д.), препараты для кожного применения (например, твердые препараты для кожного применения, жидкости и растворы для кожного применения, спреи для кожного применения, мази, кремы, гели, пластыри и т.д.) и тому подобное.
[0099]
[Препараты для перорального введения]
Примеры препаратов для перорального введения включают таблетки, капсулы, гранулы, порошки, жидкости и растворы для перорального введения, сиропы, желе для перорального введения и тому подобное. Кроме того, препараты для перорального введения включают быстрораспадающиеся препараты, в которых высвобождение активного ингредиента(ов) из препарата специально не регулируется, и препараты с регулируемым высвобождением, в которых в соответствии с целью регулируется высвобождение с помощью уникальной разработанной рецептуры и способа производства, например, препараты с энтеросолюбильным покрытием, препараты с замедленным высвобождением и тому подобное. Препарат с энтеросолюбильным покрытием относится к препарату, разработанному таким образом, что активный ингредиент(ы) высвобождается не в желудке, а в основном в тонком кишечнике с целью предотвращения разложения активного(ых) ингредиента(ов) в желудке или уменьшения раздражающего действия активного ингредиента(ов) на желудок, и его обычно можно получить путем нанесения пленки с использованием нерастворимой в кислоте энтеросолюбильной основы. Препарат с замедленным высвобождением относится к препарату, в котором скорость высвобождения, время высвобождения и место высвобождения активного ингредиента(ов) из препарата регулируются с целью уменьшения количества введений, уменьшения побочных эффектов или тому подобного, и обычно он может быть получен с использованием подходящего агента замедленного высвобождения. Препараты для перорального введения, капсулы, гранулы, таблетки и т.д. также могут быть покрыты соответствующими покрывающими веществами, такими как сахара, сахарные спирты или полимерные соединения, с целью облегчения введения или предотвращения разложения активного ингредиента.
[0100]
(1) Таблетки
Таблетки представляют собой твердые препараты, имеющие определенную форму и размер, предназначенные для перорального введения, а также быстро распадающиеся во рту таблетки, жевательные таблетки, шипучие таблетки, диспергируемые таблетки, растворимые таблетки и тому подобное, помимо тех, которые обычно называются таблетками, такие как таблетки без покрытия, таблетки с пленочным покрытием, таблетки с сахарным покрытием, многослойные таблетки и таблетки с сухим покрытием. Таблетки без покрытия обычно изготавливаются с использованием следующих способов (a), (b) или (c):
(a) Гомогенное смешивание активного ингредиента(ов) с такими добавками, как эксципиенты, связующие и дезинтегрирующие вещества, гранулирование смеси с водой или раствором, содержащим связующее, подходящим способом, затем смешивание с лубрикантом и тому подобным и формование смеси под давлением;
(b) Гомогенное смешивание активного ингредиента(ов) с добавками, такими как эксципиенты, связующие и дезинтегрирующие вещества, и непосредственное формование смеси прессованием, или гомогенное смешивание гранул, предварительно изготовленных с добавками, с активным ингредиентом(ами), лубрикантом и тому подобным, и затем прессование смеси; и
(c) Гомогенное смешивание активного ингредиента(ов) с такими добавками, как эксципиенты и связующие, заливка смешанного продукта, смоченного растворителем, в определенную форму для формования, а затем сушка формованного продукта подходящим методом.
Таблетки с пленочным покрытием обычно могут быть получены путем покрытия таблеток без покрытия тонкими пленками с использованием подходящих покрывающих агентов, таких как полимерные соединения. Таблетки, покрытые сахарной оболочкой, обычно могут быть получены путем покрытия таблеток без оболочки с использованием покрывающих агентов, включающих сахар или сахарные спирты. Многослойные таблетки можно изготавливать, складывая частицы, имеющие различный состав, в слои и прессуя их соответствующим способом. Таблетки с сухим покрытием могут быть получены путем покрытия таблеток с внутренним ядром наружными слоями, имеющими различный состав. Кроме того, таблетки могут быть также изготовлены в виде таблеток с энтеросолюбильным покрытием или таблеток с замедленным высвобождением с использованием подходящего известного метода. Интраоральные быстро распадающиеся таблетки, жевательные таблетки, шипучие таблетки, диспергируемые таблетки и растворимые таблетки представляют собой таблетки, которым при соответствующем выборе добавок были приданы уникальные функции, и их можно изготовлять в соответствии со способом производства таблеток, описанным выше. Таблетки, быстро распадающиеся во рту, относятся к таблеткам, которые могут быстро растворяться или распадаться в полости рта и приниматься; жевательные таблетки представляют собой таблетки, которые нужно жевать и принимать; шипучие таблетки относятся к таблеткам, которые растворяются или диспергируются с энергичным выделением пузырьков газа в воде; диспергируемые таблетки относятся к таблеткам, которые диспергируют в воде и принимают; и растворимые таблетки относятся к таблеткам, которые растворяют в воде и принимают. Шипучие таблетки могут быть получены с использованием в качестве добавок подходящего кислотного вещества, карбоната, гидрокарбоната или тому подобного.
[0101]
(2) Капсулы
Капсулы представляют собой препараты, наполненные в капсулы или инкапсулированные с помощью оснований капсул, в которые включены твердые капсулы, мягкие капсулы и тому подобное. Твердые капсулы могут быть получены способом, при котором гомогенная смесь, полученная путем смешивания активного ингредиента(ов) с добавками, такими как эксципиенты, или гранулы или формованный продукт, полученные соответствующим способом, заполняются в капсулу как таковые или после небольшого формования. Мягкие капсулы могут быть изготовлены способом, при котором смесь, полученная путем добавления добавок к активному ингредиенту(ам), формуют в капсулах в определенной форме с подходящими основами капсул, такими как желатин, пластифицированный путем добавления глицерина, D-сорбита или тому подобное. Капсулы могут быть приготовлены в виде капсул с энтеросолюбильным покрытием или капсул с замедленным высвобождением с использованием подходящего известного метода, и к основе капсулы также могут быть добавлены краситель, консервант или тому подобное.
[0102]
(3) Гранулы
Гранулы представляют собой препараты, гранулированные в гранулы, и в дополнение к тем, которые обычно называются гранулами включены шипучие гранулы и тому подобное. Гранулы обычно производятся с использованием следующего способа (a), (b) или (c):
(a) Гомогенное смешивание измельченного активного ингредиента(ов) с наполнителем, связующим, разрыхлителем или другими добавками, а затем гранулирование смеси соответствующим способом;
(b) Гомогенное смешивание активного ингредиента(ов), предварительно приготовленного в гранулах, с такими добавками, как эксципиенты; и
(c) Смешивание активного ингредиента(ов), предварительно приготовленного в гранулах, с добавками, такими как эксципиенты, и гранулирование смеси подходящим методом.
При необходимости на гранулы также может быть нанесено покрытие, и их также можно изготовить в виде гранул с энтеросолюбильным покрытием или гранул с замедленным высвобождением с использованием подходящего известного метода. Шипучие гранулы можно получить с использованием подходящего кислотного вещества, карбоната, гидрокарбоната или тому подобного в качестве добавок. Шипучие гранулы относятся к гранулам, которые растворяются или диспергируются с энергичным выделением пузырьков газа в воде. Гранулы можно также получить в виде мелких гранул, регулируя размер частиц.
[0103]
(4) Порошки
Порошки представляют собой препараты в виде порошка, и их обычно можно получить путем смешивания гомогенно активного ингредиента(ов) с эксципиентом или другими добавками.
[0104]
(5) Жидкости и растворы для перорального введения
Жидкости и растворы для перорального введения представляют собой жидкие или текучие, вязкие и гелеобразные препараты, а также эликсиры, суспензии, эмульсии, лимонады и тому подобное, помимо тех, которые обычно называются пероральными растворами. Жидкости и растворы для перорального введения обычно могут быть получены путем смешивания активного ингредиента(ов) с добавками и очищенной водой, гомогенного растворения, эмульгирования или суспендирования смеси и, если необходимо, фильтрации смеси. Эликсиры относятся к прозрачным, подслащенным и ароматическим жидкостям и растворам для перорального введения в жидкой форме, содержащим этанол, и обычно могут быть получены путем добавления этанола, очищенной воды, ароматического агента и сахарозы, других сахаров или подсластителей к твердому активному ингредиенту(ам) или его экссудату и растворение их, и осветление раствора фильтрацией или другими методами. Суспензии относятся к жидкостям и растворам для перорального введения тонко и однородно суспендированного активного ингредиента(ов) и обычно могут быть получены путем добавления суспендирующего агента или других добавок и очищенной воды или масла к твердому активному ингредиенту(ам) и их суспендирования посредством подходящего способа гомогенизации всей суспензии. Эмульсии относятся к жидкостям и растворам для перорального введения активного ингредиента(ов), тонко и гомогенно эмульгированного, и обычно могут быть получены путем добавления эмульгирующего агента и очищенной воды к жидким активным ингредиентам и их эмульгирования соответствующим способа гомогенизации всей суспензии. Кроме того, к кисло-сладким, прозрачным жидкостям и растворам для перорального приема в жидкой форме относятся лимонады.
[0105]
(6) Сиропы
Сиропы представляют собой вязкие жидкие или твердые препараты, содержащие сахара или подслащивающие агенты, а также препараты для сиропов и т. п. Сиропы обычно могут быть получены путем добавления активного ингредиента(ов) в раствор сиропа, других сахаров или подсластителей или простого сиропа и растворения, смешивания, суспендирования или эмульгирования их и, при необходимости, кипячения и затем фильтрования смеси в горячем состоянии. Препараты для сиропов относятся к препаратам в виде гранул или порошков, которые преобразуются в сиропы при добавлении воды, и их также можно назвать сухими сиропами. Препараты для сиропов обычно могут быть получены с использованием сахаров или подсластителей в качестве добавок в соответствии со способом производства гранул или порошков.
[0106]
(7) Желе для перорального введения
Желе для перорального введения представляют собой нетекучие формованные гелеобразные препараты и обычно они могут быть получены путем смешивания активного ингредиента(ов) с добавками и полимерной гелевой основой, а также желатинизации и формования смеси с приданием определенной формы подходящим способом.
[0107]
[Препараты для инъекций]
(1) Инъекции
Инъекции представляют собой стерильные препараты для подкожного, внутримышечного, внутрисуставного введения или непосредственно в ткани или органы тела, такие как кровеносные сосуды, в виде раствора, суспензии или эмульсии, или твердого вещества, которое необходимо растворить или суспендировать перед использованием, и лиофилизированные инъекции, порошки для инъекций, предварительно заполненные шприцы для инъекций, картриджи для инъекций, парентеральные инфузии, имплантаты/гранулы, инъекции с пролонгированным высвобождением и тому подобное. Инъекции обычно производятся следующим способом (a) или (b):
(a) Гомогенное растворение, суспендирование или эмульгирование активного ингредиента(ов) в том виде, в каком он есть, или добавление с добавками в воду для инъекций, другой водный растворитель или неводный растворитель или тому подобное, заполнение смесью контейнера для инъекций, герметизация и стерилизация; и
(b) Гомогенное растворение, суспендирование или эмульгирование активного ингредиента(ов) в том виде, в каком он есть, или добавление с добавками в воду для инъекций, другой водный растворитель или неводный растворитель или тому подобное, и асептическое фильтрование смеси или приготовление асептической гомогенной жидкости, заливка смеси в емкость для инъекций и герметизация.
Лиофилизированные инъекции обычно можно изготавливать путем растворения активного ингредиента(ов) в том виде, в каком он есть, или активного ингредиента(ов) с добавками, такими как эксципиенты, в воде для инъекций, асептической фильтрацией раствора, заполнения фильтрата в контейнер для инъекций, а затем подвергая лиофилизации, или путем лиофилизации фильтрата в специальных контейнерах с последующим заполнением его в индивидуальные контейнеры для инъекций. Порошки для инъекций обычно могут быть получены путем фильтрации асептически активного ингредиента(ов), добавления порошков, полученных путем кристаллизации, или порошков, добавленных со стерилизованными добавками, и заполнения порошками контейнера для инъекций. Предварительно заполненные шприцы для инъекций обычно можно изготавливать путем заполнения шприцев активным ингредиентом(ами) в том виде, в каком он есть, или раствором, суспензией или эмульсией, приготовленными с использованием активного ингредиента(ов) и добавок. Картриджи для инъекций относятся к инъекциям, используемым путем фиксации картриджа, заполненного химическим раствором, в инжекторе для исключительного использования. Картридж, заполненный химическим раствором, обычно может быть изготовлен путем заполнения картриджа активным ингредиентом(ами) в том виде, в каком он есть, или раствором, суспензией или эмульсией, приготовленными с использованием активного ингредиента(ов) и добавок. Парентеральные инфузии обычно относятся к инъекциям объемом 100 мл или более, предназначенным для внутривенного введения. Имплантаты/гранулы относятся к твердым или гелеобразным инъекциям, вводимым подкожно, внутримышечно и т.д. с использованием имплантата или посредством оперативного лечения с целью высвобождения активного ингредиента(ов) в течение длительного периода времени. Имплантаты/гранулы обычно могут быть изготовлены в виде гранул, микросфер или геля с использованием биоразлагаемых полимерных соединений. Инъекции с пролонгированным высвобождением относятся к инъекциям, которые вводятся внутримышечно или внутрисуставно с целью высвобождения активного ингредиента(ов) в течение длительного периода времени, и обычно могут изготавливаться растворением или суспендированием активного ингредиента(ов) в растительном масле или тому подобным, или путем приготовления суспензии микросфер с использованием биоразлагаемых полимерных соединений.
[0108]
Доза соединения по настоящему изобретению или сопутствующего лекарственного средства с соединением по настоящему изобретению и другого лекарственного средства варьируется в зависимости от возраста, веса, симптома, терапевтического эффекта, способа введения, времени лечения и тому подобное. Однако соединение по настоящему изобретению или сопутствующее лекарственное средство с соединением по настоящему изобретению и другое лекарственное средство вводят перорально, обычно в диапазоне от 1 нг до 1000 мг за один раз для взрослого от одного до нескольких раз в день, или вводят парентерально в диапазоне от 0,1 нг до 100 мг за один раз для взрослого от одного до нескольких раз в день, или вводят непрерывно внутривенно в диапазоне от 1 до 24 часов в день. Как описано выше, поскольку доза варьируется в зависимости от различных условий, может быть достаточна доза, меньшая, чем указанная выше, или может потребоваться введение за пределы диапазона.
[0109]
Если не указано иное, все технические термины, научные термины и сокращенные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в той области, к которой относится данное изобретение.
Кроме того, содержание всей патентной литературы и непатентной литературы или ссылок, конкретно цитируемых в данном документе, может быть полностью включено в настоящий документ как часть настоящего описания.
ПРИМЕРЫ
[0110]
Далее настоящее изобретение будет подробно описано со ссылкой на примеры, но настоящее изобретение ими не ограничивается.
[Пример синтеза]
Растворители, приведенные в скобках в разделе «Хроматографическое разделения и ТСХ», означает применяемые растворители для элюирования или растворители для проявки, а соотношение является объемным соотношением.
Растворитель, приведенный в скобках в разделе ЯМР, означает растворитель, применяемый при измерении.
Названия соединений, используемые в данном описании, даны с помощью компьютерной программы, которая обычно присваивает названия в соответствии с правилами IUPAC, ACD/Name (зарегистрированный товарный знак) или Chemdraw Ultra (версия 12.0, произведена компанией Cambridge Soft), или соединения называют в соответствии с номенклатурой IUPAC.
ЖХ-МС/ELSD проводили в следующих условиях.
Колонка: Waters Triart C18 (диаметр частиц: 1,9×10-6 м; длина колонки: 30×2,0 мм внутренний диаметр); скорость потока: 1,0 мл/мин; температура колонки: 30°C; подвижная фаза (A): 0,1% водный раствор трифторуксусной кислоты; подвижная фаза (B): раствор 0,1% трифторуксусная кислота-ацетoнитрил; градиент (соотношение подвижная фаза (A):подвижная фаза (B)): [0 мин] 95:5; [0,1 мин] 95:5; [1,2 мин] 5:95; [1,4 мин] 5:95; [1,41 мин] 95:5; [1,5 мин] 95:5; детекторы: УФ (PDA), ELSD, МС.
Время удерживания ВЭЖХ позывает время удерживания в условиях, описанных при ЖХ-МС/ELSD, если не указано иное.
Сверхкритическую жидкостную хроматографию (SFC) проводили в следующих условиях.
Колонка: CHIRALPAK IC/SFC (Daicel Corporation), внутренний диаметр 20 мм×длина 250 мм, диаметр частиц 5 мкм; скорость потока: 100 мл/мин: сорастворитель/CO2=12/88: ISOCRATIC 21 мин (сорастворитель: MeCN/MeOH=9/1); Противодавление: 120 бар.
[0111]
Ссылочный пример 1: 4-(Ацетокси)-2-(трифторметил)бензойная кислота
К раствору 4-гидрокси-2-(трифторметил)бензойной кислоты (регистрационный № 320-32-1, 500 мг) в этилацетате (7,5 мл) добавляли пиридин (0,392 мл) и уксусный ангидрид (0,573 мл) и смесь перемешивали в течение ночи. В реакционную смесь добавляли воду и разбавленную соляную кислоту, затем смесь экстрагировали этилацетатом. Органический слой промывали водой и насыщенным солевым раствором, сушили над сульфатом натрия и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (528 мг), имеющего следующие значения физических характеристик.
1H-ЯМР (ДМСО-d6): δ 2,34, 7,56, 7,70, 7,91, 13,66.
[0112]
Ссылочный пример 2: 4-(Хлоркарбонил)-3-(трифторметил)фенил ацетат
К раствору в смеси толуол (1,6 мл)-ацетoнитрил (0,26 мл) соединения (1,0 г), полученного в ссылочном примере 1, добавляли тионилхлорид (0,17 мл) и смесь перемешивали при температуре 60°C в течение 4 часов. Соединение, полученное концентрированием реакционного раствора при пониженном давлении, использовали в следующей реакции без очистки.
[0113]
Ссылочный пример 3: Метил {3-[4-(ацетокси)-2-(трифторметил)бензамид]-4-хлорфенил}ацетат
К раствору в смеси толуол (1,6 мл)-ацетoнитрил (1,6 мл) соединения, полученного в ссылочном примере 2, добавляли пиридин (0,342 мл) и метил 2-(3-амино-4-хлорфенил)ацетат (регистрационный № 59833-69-1, 422 мг) и смесь перемешивали в течение ночи при комнатной температуре. В реакционную смесь добавляли воду и смесь экстрагировали этилацетатом. Органический слой последовательно промывали 1 моль/л соляной кислотой, водой и насыщенным солевым раствором, сушили над сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=70:30) с получением указанного в заголовке соединения (715 мг), имеющего следующие значения физических характеристик.
1H-ЯМР (CDCl3): δ 2,37, 3,68, 3,72, 7,07, 7,37, 7,43, 7,53, 7,71, 7,93, 8,45.
[0114]
Ссылочный пример 4: Метил {4-хлор-3-[4-гидрокси-2-(трифторметил)бензамид]фенил}ацетат
К раствору соединения (1,75 г), полученного в ссылочном примере 3, в смеси метанол (8,8 мл)-тетрагидрофуран (8,8 мл) добавляли карбонат калия (404 мг) и смесь перемешивали при комнатной температуре в течение 2 часов. В реакционную смесь добавляли воду и 1 моль/л соляной кислоты, затем смесь экстрагировали этилацетатом. Органический слой промывали водой и насыщенным солевым раствором, сушили над сульфатом натрия и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (1,36 г), имеющего следующие значения физических характеристик.
ТСХ: Rf 0,55 (гексан:этилацетат=1:1);
1H-ЯМР (CDCl3): δ 3,63, 3,75, 7,12-7,16, 7,19, 7,49, 7,52, 7,59, 10,07, 10,52.
[0115]
Пример 1: Метил (4-хлор-3-{4-[2-(оксан-2-ил)этокси]-2-(трифторметил)бензамид}фенил)ацетат
[Химическая формула 35]

К раствору в толуоле (5 мл) соединения (500 мг), полученного в ссылочном примере 4, 2-(тетрагидропиран-2-ил)этанол (номер в реестре CAS 38786-79-7, 218 мг), добавляли цианометилен трифенилфосфин (0,507 мл) и смесь перемешивали в течение ночи при температуре 60°C. Реакционный раствор концентрировали при пониженном давлении, затем полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=3:1) с получением указанного в заголовке соединения (564 мг), имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,15;
1H-ЯМР (CDCl3): δ 1,37, 1,47-1,68, 1,86, 1,94, 3,40-3,53, 3,67, 3,72, 3,98, 4,13, 4,20, 7,04, 7,13, 7,29, 7,36, 7,62, 7,93, 8,47.
[0116]
Пример 2: (4-Хлор-3-{4-[2-(оксан-2-ил)этокси]-2-(трифторметил)бензамид}фенил)уксусная кислота
[Химическая формула 36]

К раствору в диметоксиэтане (0,4 мл) соединения (40,0 мг), полученного в примере 1, добавляли 2 моль/л водного раствора гидроксида лития (0,12 мл) и смесь перемешивали при комнатной температуре в течение 1 часа. После добавления в реакционную смесь 1 моль/л соляной кислоты смесь экстрагировали этилацетатом. Органический слой промывали водой и насыщенным солевым раствором, сушили над сульфатом натрия и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (29 мг), имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,03;
1H-ЯМР (ДМСО-d6): δ 1,25, 1,41-1,53, 1,63, 1,77, 1,83-1,89, 3,45, 3,63, 3,88, 4,14-4,23, 7,19, 7,32, 7,35, 7,48, 7,51, 7,68, 10,14, 12,46.
[0117]
Примеры от 2-1 до 2-3
Те же операции, что и в примере 1 и примере 2, выполняли с использованием соответствующей спиртовой формы вместо 2-(тетрагидро-2H-пиран-2-ил)этанола с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Пример 2-1: {4-Хлор-3-[4-(2-циклогексилэтокси)-2-(трифторметил)бензамид]фенил}уксусная кислота
[Химическая формула 37]
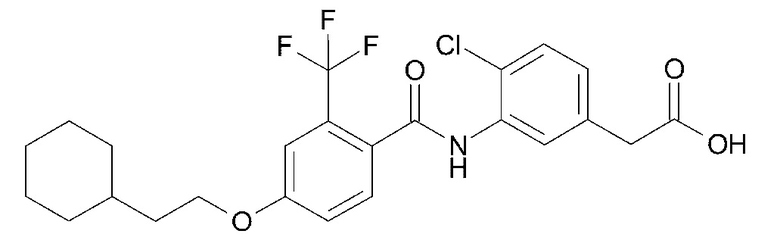
TLC: Rf 0,60 (этилацетат:метанол=9:1);
1H-ЯМР (CDCl3): δ 0,85-1,10, 1,13-1,35, 1,52, 1,63-1,83, 3,71, 4,08, 7,05, 7,10, 7,38, 7,62, 7,94, 8,49.
Пример 2-2: {4-Хлор-3-[4-(2-фенилэтокси)-2-(трифторметил)бензамид]фенил}уксусная кислота
[Химическая формула 38]

Время удерживания ВЭЖХ (мин): 1,07;
1H-ЯМР (ДМСО-d6): δ 3,09, 3,63, 4,36, 7,18, 7,24, 7,31-7,37, 7,48, 7,51, 7,68, 10,14, 12,45.
Пример 2-3: {4-Хлор-3-[4-(2-циклопропилэтокси)-2-(трифторметил)бензамид]фенил}уксусная кислота
[Химическая формула 39]
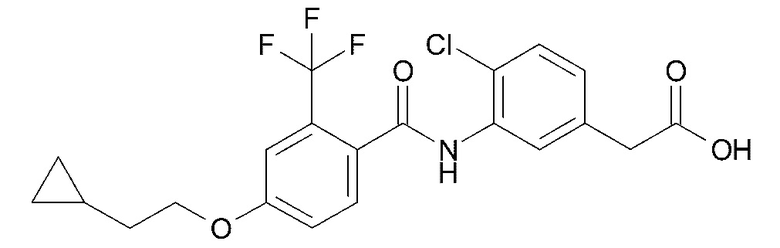
Время удерживания ВЭЖХ (мин): 1,05;
1H-ЯМР (ДМСО-d6): δ -0,02-0,01, 0,28-0,32, 0,70, 1,51, 3,48, 4,02, 7,03, 7,16, 7,20, 7,33, 7,36, 7,53, 9,99, 12,29.
[0118]
Пример 3: Метил (4-хлор-3-{2,6-диметил-4-[2-(оксан-2-ил)этокси]бензамид}фенил)ацетат
[Химическая формула 40]
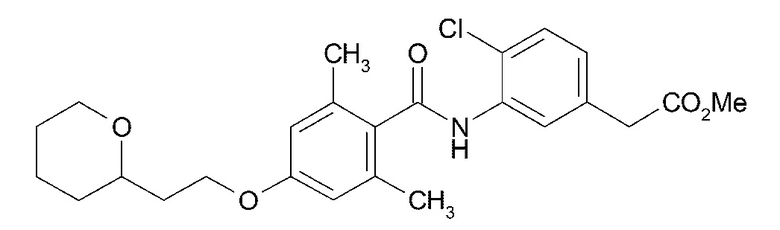
Ту же реакцию, что и в примере 1, проводили с использованием метил {4-хлор-3-[(4-гидрокси-2,6-диметилбензоил)амино]фенил}ацетата (номер в реестре CAS 1351163-96-6, Bioorganic & Medicinal Chemistry 19 (2011) 6935-6948, соединение 44) вместо соединения, полученного в ссылочном примере 4, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
TLC: Rf 0,75 (гексан:этилацетат=1:1);
1H-ЯМР (CDCl3): δ 1,33, 1,51, 1,63, 1,85, 1,91, 2,38, 3,43, 3,50, 3,68, 3,73, 3,97, 4,08, 6,63, 7,03, 7,35, 7,74, 8,49.
[0119]
Пример 3-1: Метил {4-хлор-3-[4-(2-циклогексилэтокси)-2,6-диметилбензамид]фенил}ацетат
[Химическая формула 41]
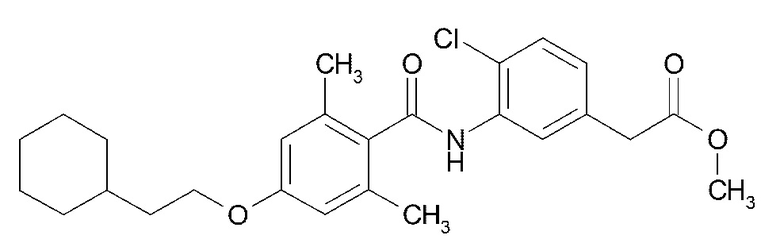
Ту же реакцию, что и в примере 1, проводили с использованием метил {4-хлор-3-[(4-гидрокси-2,6-диметилбензоил)амино]фенил}ацетата вместо соединения, полученного в ссылочном примере 4, и используя 2-циклогексилэтанол (номер в реестре CAS 28438-52-0) вместо 2-(тетрагидро-2H-пиран-2-ил)этанола с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
TLC: Rf 0,68 (этилацетат:гексан=2:1);
1H-ЯМР (CDCl3): δ 0,80-1,05, 1,10-1,35, 1,40-1,55, 1,65-1,80, 2,35, 3,53, 3,68, 3,73, 4,00, 4,19, 6,61, 7,04, 7,36, 7,74, 8,50.
[0120]
Пример 4: (4-Хлор-3-{2,6-диметил-4-[2-(оксан-2-ил)этокси]бензамид}фенил)уксусная кислота
[Химическая формула 42]
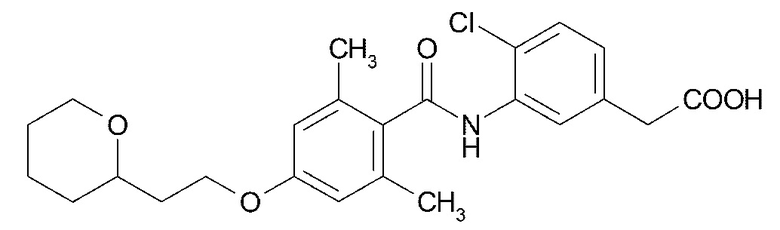
Ту же реакцию, что и в примере 2, проводили с использованием соединения, полученного в примере 3, вместо соединения, полученного в примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,02;
1H-ЯМР (ДМСО-d6): δ 1,16-1,83, 2,32, 3,39, 3,61, 3,86, 4,02, 6,66, 7,15, 7,45, 7,49, 9,95, 12,44.
[0121]
Примеры 4-1 и 4-2:
Те же операции, что и в примере 1 и примере 2, выполняли с использованием соответствующей спиртовой формы вместо 2-(тетрагидро-2H-пиран-2-ил)этанола и используя метил {4-хлор-3-[(4-гидрокси-2,6-диметилбензоил)амино]фенил}ацетат вместо соединения, полученного в ссылочном примере 4, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Пример 4-1: {4-Хлор-3-[4-(2-циклогексилэтокси)-2,6-диметилбензамид]фенил}уксусная кислота
[Химическая формула 43]
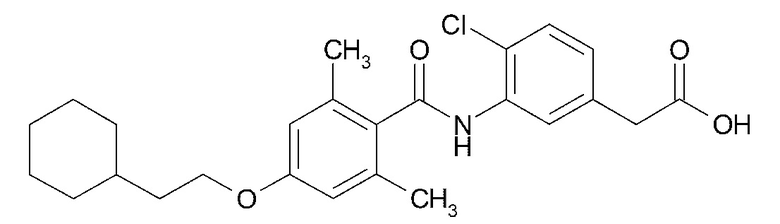
TLC: Rf 0,27 (гексан:этилацетат=1:2);
1H-ЯМР (CD3OD): δ 0,83-1,08, 1,13-1,38, 1,42-1,59, 1,60-1,91, 2,41, 3,64, 4,01, 6,65, 7,19, 7,43, 7,72.
Пример 4-2: {4-Хлор-3-[4-(2-циклопропилэтокси)-2,6-диметилбензамид]фенил}уксусная кислота
[Химическая формула 44]

Время удерживания ВЭЖХ (мин): 1,05;
МС (ESI, положит.): 402 (M+H)+;
[0122]
Пример 5: (3-{4-[(2,3-Дигидро-1H-инден-2-ил)окси]-2,6-диметилбензамид}-4-фторфенил)уксусная кислота
[Химическая формула 45]
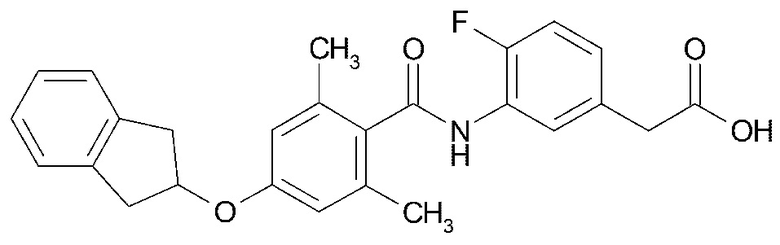
Те же реакции, что и в ссылочном примере 1→ссылочном примере 2→ссылочном примере 3→ссылочном примере 4→примере 1→примере 2 осуществляли, используя метил 2-(3-амино-4-фторфенил)ацетат (номер в реестре CAS 257632-77-2) вместо метил 2-(3-амино-4-хлорфенил)ацетата, используя 4-гидрокси-2,6-диметилбензойную кислоту (номер в реестре CAS 75056-97-2) вместо 4-гидрокси-2-(трифторметил)бензойной кислоты и используя 2-инданол (номер в реестре CAS 4254-29-9) вместо 2-(тетрагидро-2H-пиран-2-ил)этанола с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,02;
1H-ЯМР (ДМСО-d6): δ 2,29, 3,02, 3,39, 3,60, 5,27, 6,70, 7,13-7,28, 7,57, 10,07, 12,38.
[0123]
Ссылочный пример 5: Метил (4-хлор-3-{2,6-диметил-4-[(трифторметансульфонил)окси]бензамид}фенил)ацетат
К раствору в дихлорметане (15 мл) метил [4-хлор-3-(4-гидрокси-2,6-диметилбензамид)фенил]ацетата (1,00 г) добавляли триэтиламин (0,52 мл) и N, N-бис(трифторметилсульфонил)анилин (1,23 г) и смесь перемешивали при комнатной температуре в течение 4 часов. В реакционную смесь добавляли воду и смесь экстрагировали этилацетатом. Органический слой промывали водой и насыщенным солевым раствором, сушили над сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=10:0→7:3) с получением указанного в заголовке соединения (1,38 г), имеющего следующие значения физических характеристик.
TLC: Rf 0,39 (гексан:этилацетат=2:1);
1H-ЯМР (CDCl3): δ 1,55, 2,45, 3,69, 3,73, 7,02, 7,08, 7,37, 7,40, 7,73, 8,43.
[0124]
Пример 6: Метил {4-хлор-3-[4-(3-циклогексилпроп-1-ин-1-ил)-2,6-диметилбензамид]фенил}ацетат
[Химическая формула 46]
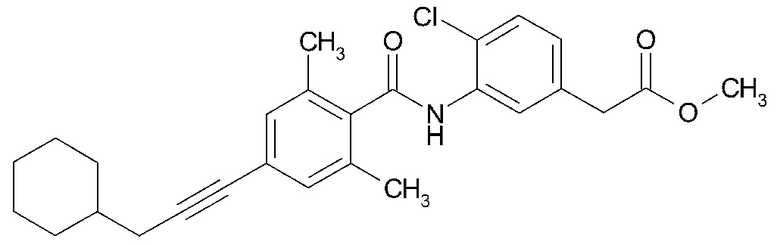
К раствору в N, N-диметилформамиде (12 мл) соединения (1,38 г), полученного в ссылочном примере 5, добавляли 3-циклогексил-1-пропин (1,26 мл) и триэтиламин (8,1 мл) и атмосферу заменяли на атмосферу аргона. Добавляли йодид меди (55 мг) и дихлорид бис(трифенилфосфин)палладия(II) (204 мг) и смесь перемешивали в течение ночи при температуре 50°C. В реакционную смесь добавляли воду и смесь экстрагировали смешанным растворителем из этилацетата/гексана. Органический слой промывали водой и насыщенным солевым раствором, сушили над сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=10:0→7:3) с получением указанного в заголовке соединения (1,46 г), имеющего следующие значения физических характеристик.
ТСХ: Rf 0,45 (гексан:этилацетат=4:1);
1H-ЯМР (CDCl3): δ 0,95-1,40,1,45-1,78, 1,85-1,90, 2,30, 2,37, 3,68, 3,73, 7,05, 7,14, 7,35, 7,38, 7,71, 8,47.
[0125]
Пример 7: {4-Хлор-3-[4-(3-циклогексилпроп-1-ин-1-ил)-2,6-диметилбензамид]фенил}уксусная кислота
[Химическая формула 47]

Ту же реакцию, что и в примере 2, проводили с использованием соединения, полученного в примере 6, вместо соединения, полученного в примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
ТСХ: Rf 0,61 (этилацетат:метанол=9:1);
1H-ЯМР (CDCl3): δ 0,98-1,35, 1,56, 1,65-1,80, 1,82-1,90, 2,30, 2,38, 3,72, 7,06, 7,14, 7,36, 7,39, 7,71, 8,48.
[0126]
Пример 8: (4-Хлор-3-{4-[(1E)-3-циклогексилпроп-1-ен-1-ил]-2,6-диметилбензамид}фенил)уксусная кислота
[Химическая формула 48]

К раствору в диоксане (12 мл) соединения (1000 мг), полученного в ссылочном примере 5, добавляли 2-[(E)-3-Циклогексилпропен-3-ил]-4,4,5,5-тетраметил-1,3,2-диоксаборолан (626 мг), фосфат калия (884 мг) и аддукт дихлорида [1,1ʼ-бис(дифенилфосфино)ферроцен]палладия(II) и дихлорметана и смесь перемешивали при температуре 50°C в течение 18 часов. В реакционную смесь добавляли воду и этилацетат, затем смесь фильтровали через Celite (торговое наименование). Фильтрат экстрагировали этилацетатом, органический слой промывали водой и насыщенным солевым раствором, сушили над сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем с получением производного метилового сложного эфира (533 мг) указанного в заголовке соединения. Используя полученное производное метилового сложного эфира, осуществляли ту же реакцию, что и в примере 2, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
ТСХ: Rf 0,38 (гексан:этилацетат:уксусная кислота=14:5:1);
Время удерживания ВЭЖХ (мин): 1,31;
МС (ESI, положит.): 440 (M+H)+.
[0127]
Пример 9: Метил [4-хлор-3-({2,6-диметил-4-[2-(оксан-2-ил)этокси]бензол-1-карботиоил}амино)фенил]ацетат
[Химическая формула 49]

К раствору в толуоле (0,4 мл) соединения (40 мг), полученного в примере 3, добавляли реагент Лавессона (номер в реестре CAS 19172-47-5, 21 мг) и смесь перемешивали при температуре 100°C в течение 24 часов. Реакционную смесь концентрировали при пониженном давлении, и полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=20:1→4:1) с получением указанного в заголовке соединения (40 мг), имеющего следующие значения физических характеристик.
ТСХ: Rf 0,50 (гексан:этилацетат=2:1);
1H-ЯМР (ДМСО-d6): δ 1,25, 1,46, 1,62, 1,81, 2,37, 3,44, 3,64, 3,80, 3,87, 4,02, 6,68, 7,30, 7,42, 7,55, 11,74.
[0128]
Пример 10: [4-Хлор-3-({2,6-диметил-4-[2-(оксан-2-ил)этокси]бензол-1-карботиоил}амино)фенил]уксусная кислота
[Химическая формула 50]

Ту же реакцию, что и в примере 2, проводили с использованием соединения, полученного в примере 9, вместо соединения, полученного в примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
ТСХ: Rf 0,28 (дихлорметан:метанол=9:1);
1H-ЯМР (ДМСО-d6): δ 1,25, 1,47, 1,62, 1,80, 2,37, 3,42, 3,67, 3,87, 4,04, 6,68, 7,29, 7,39, 7,54, 11,74, 12,46.
[0129]
Примеры от 10-1 до 10-5:
Те же операции, что и в примере 9→примере 2, осуществляли, используя соединения, полученные в примере 1 и примере 3-1, и производные метилового сложного эфира соединений, полученных в примерах от 2-1 до 2-3, вместо соединения, полученного в примере 3, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Пример 10-1: (4-Хлор-3-{[4-(2-циклогексилэтокси)-2,6-диметилбензол-1-карботиоил]амино}фенил)уксусная кислота
[Химическая формула 51]
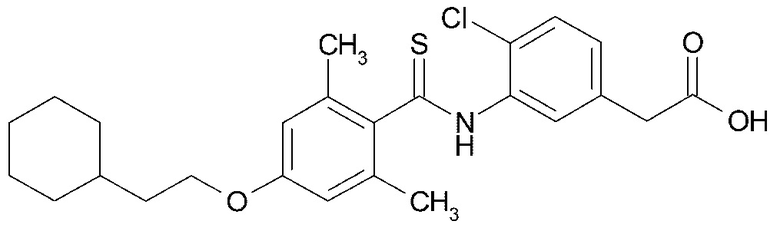
ТСХ: Rf 0,46 (этилацетат:метанол=9:1);
1H-ЯМР (ДМСО-d6): δ 0,85-1,02, 1,10-1,30, 1,43, 1,55-1,75, 2,35, 3,65,3,99, 6,67, 7,28, 7,36, 7,51, 7,54, 11,71, 12,44.
Пример 10-2: [4-Хлор-3-({4-[2-(оксан-2-ил)этокси]-2-(трифторметил)бензол-1-карботиоил}амино)фенил]уксусная кислота
[Химическая формула 52]
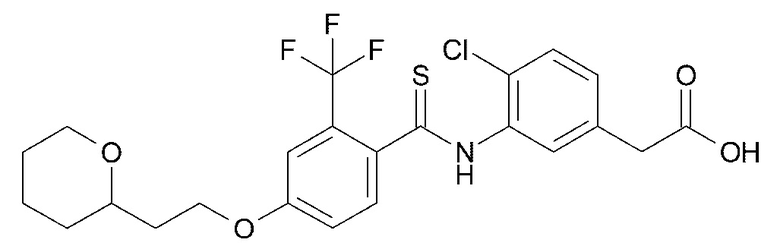
Время удерживания ВЭЖХ (мин): 1,05;
1H-ЯМР (ДМСО-d6): δ 1,25, 1,42-1,51, 1,63, 1,77, 1,83-1,89, 3,45, 3,67, 3,88, 4,12-4,21, 7,25, 7,29-7,32, 7,35, 7,47, 7,55, 11,90, 12,46.
Пример 10-3: (4-Хлор-3-{[4-(2-циклогексилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусная кислота
[Химическая формула 53]

Время удерживания ВЭЖХ (мин): 1,21;
1H-ЯМР (ДМСО-d6): δ 0,92-1,02, 1,13-1,29, 1,49, 1,63-1,77, 3,66, 4,14, 7,24, 7,29-7,32, 7,34, 7,46, 7,54, 11,89, 12,46.
Пример 10-4: (4-Хлор-3-{[4-(2-фенилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусная кислота
[Химическая формула 54]

Время удерживания ВЭЖХ (мин): 1,09;
1H-ЯМР (ДМСО-d6): δ 3,08, 3,66, 4,34, 7,23-7,27, 7,29-7,37, 7,46, 7,55, 11,90, 12,50.
Пример 10-5: (4-Хлор-3-{[4-(2-циклопропилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусная кислота
[Химическая формула 55]
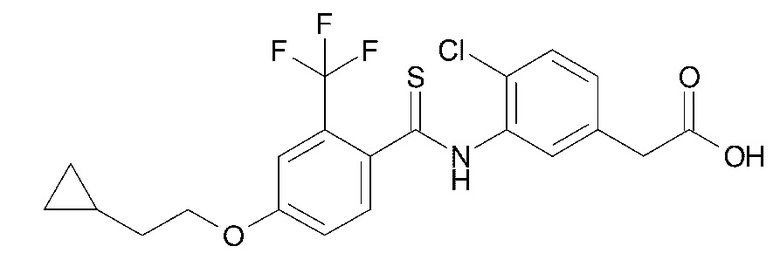
Время удерживания ВЭЖХ (мин): 1,06;
1H-ЯМР (ДМСО-d6): δ -0,02-0,01, 0,28-0,32, 0,70, 1,51, 3,50, 4,00, 7,08, 7,13-7,18, 7,31, 7,38, 11,74, 12,30.
[0130]
Пример 11:
Используя соединение, полученное в примере 9, оптическое разделение осуществляли с помощью сверхкритической жидкостной хроматографии (SFC) с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Пример 11-1: Метил {4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}ацетат
[Химическая формула 56]
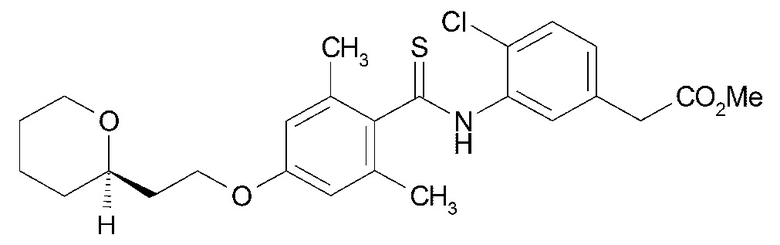
Время удерживания ВЭЖХ (мин): 13,2 (CHIRAL PAK IC, гексан:изопропанол=70:30);
Пример 11-2: Метил {4-хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}ацетат
[Химическая формула 57]

Время удерживания ВЭЖХ (мин): 11,8 (CHIRAL PAK IC, гексан:изопропанол=70:30);
[0131]
Пример 12: {4-Хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусная кислота
[Химическая формула 58]

Ту же реакцию, что и в примере 2, проводили с использованием соединения, полученного в примере 11-1, вместо соединения, полученного в примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
ТСХ: Rf 0,28 (дихлорметан:метанол=9:1);
Время удерживания ВЭЖХ (мин): 1,05;
МС (ESI, положит.): 462(M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,25, 1,47, 1,62, 1,80, 2,37, 3,42, 3,67, 3,87, 4,04, 6,68, 7,29, 7,39, 7,54, 11,74, 12,46.
[0132]
Пример 13: {4-Хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусная кислота
[Химическая формула 59]
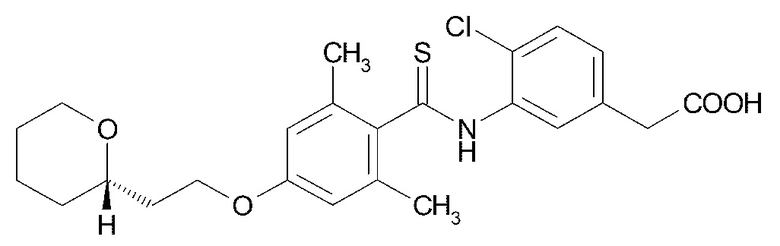
Ту же реакцию, что и в примере 2, проводили с использованием соединения, полученного в примере 11-2, вместо соединения, полученного в примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
ТСХ: Rf 0,28 (дихлорметан:метанол=9:1);
Время удерживания ВЭЖХ (мин): 1,05;
МС (ESI, положит.): 462(M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,25, 1,47, 1,62, 1,80, 2,37, 3,42, 3,67, 3,87, 4,04, 6,68, 7,29, 7,39, 7,54, 11,74, 12,46.
[0133]
Ссылочный пример 6: Метил 2-(3-амино-4-фторфенил)пропаноат
Раствор в уксусной кислоте (5 мл) метил 2-(4-фтор)-3-нитрофенил)пропаноата (номер в реестре CAS 1428790-43-5, 3,9 г), полученного способом, описанным в WO 2013/045451, добавляли к смеси, полученной добавлением порошка железа (4,8 г) в уксусную кислоту (34 мл) и воду (4,0 мл) и нагреванием до температуры 65°C, и реакционную смесь перемешивали при температуре 65°C в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры и затем фильтровали через Celite (торговое наименование) и фильтрат охлаждали до температуры 0°C. Затем приливали 2н водный раствор гидроксида натрия (345 мл) и смесь опять фильтровали через Celite (торговое наименование). Фильтрат два раза экстрагировали трет-бутил-метиловым эфиром и органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния, и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=99:1→65:35) с получением указанного в заголовке соединения (3,4 г), имеющего следующие значения физических характеристик.
1H-ЯМР (CDCl3): δ 1,45, 3,60, 3,63, 3,71, 6,60, 6,73, 6,91.
[0134]
Пример 14: 2-{3-[({2,6-Диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}пропионовая кислота
[Химическая формула 60]
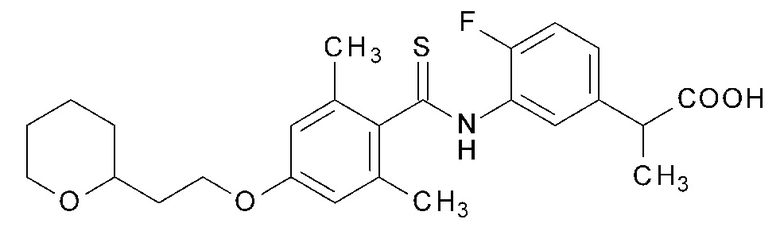
Те же реакции, что и в ссылочном примере 2→ссылочном примере 3→ссылочном примере 4→примере 1→примере 9→примере 2, осуществляли, используя соединения, полученные в ссылочном примере 6, вместо метил 2-(3-амино-4-хлорфенил)ацетата и 4-ацетокси-2,6-диметилбензойную кислоту (номер в реестре CAS 1351163-93-3), полученную способом, описанным в Bioorganic & Medicinal Chemistry, vol. 19, 6935-6948, 2011, вместо соединения, полученного в ссылочном примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,07;
МС (ESI, положит., 20 В): 460 (M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,18, 1,19-1,29, 1,38, 1,39-1,55, 1,62, 1,71-1,87, 2,32, 3,26-3,52, 3,77, 3,87, 4,04, 6,69, 7,26-7,43, 11,64, 12,44.
[0135]
Пример 15: 1-{3-[({2,6-Диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}циклопропанкарбоновая кислота
[Химическая формула 61]

Те же реакции, что и в ссылочном примере 6→ссылочном примере 2→ссылочном примере 3→ссылочном примере 4→примере 1→примере 9→примере 2, осуществляли, используя метил 1-(4-фтор-3-нитрофенил)циклопропан-1-карбоксилат (номер в реестре CAS, 2260554-65-0), полученный способом, описанным в WO 2019/003143 A, и 4-ацетокси-2,6-диметилбензойную кислоту вместо соединения, полученного в ссылочном примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,09;
МС (ESI, положит., 20 В): 472 (M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,12-1,31, 1,38-1,54, 1,61, 1,71-1,86, 2,32, 3,27-3,47, 3,87, 4,03, 6,68, 7,26, 7,36, 7,43, 11,64, 12,42.
[0136]
Пример 16: Метил 2-[4-хлор-3-({2,6-диметил-4-[2-(оксан-2-ил)этокси]бензол-1-карботиоил}амино)фенил]-2-метилпропаноат
[Химическая формула 62]
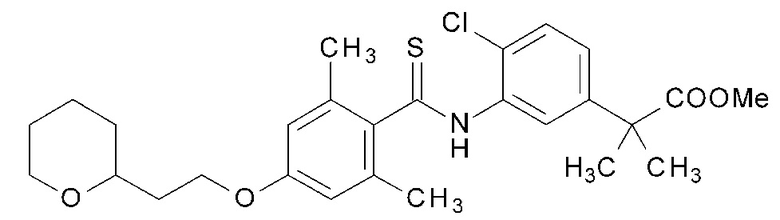
Те же реакции, что и в ссылочном примере 2→ссылочном примере 3→ссылочном примере 4→примере 1→примере 9, осуществляли, используя метил 2-(3-амино-4-хлорфенил)-2-метилпропаноат (номер в реестре CAS 343326-75-0), полученный способом, описанным в Bioorganic Medicinal Chemistry, 2011, vol. 19, 6935-6948, и 4-ацетокси-2,6-диметилбензойную кислоту вместо соединения, полученного в ссылочном примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
1H-ЯМР (ДМСО-d6): δ 1,20-1,28, 1,42-1,50, 1,53, 1,58-1,65, 1,72-1,85, 2,36, 3,28-3,48, 3,61, 3,85-3,90, 4,00-4,08, 6,68, 7,35, 7,43, 7,58 11,75.
[0137]
Пример 17: 2-{4-Хлор-3-[({2,6-диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]фенил}-2-метилпропионовая кислота
[Химическая формула 63]
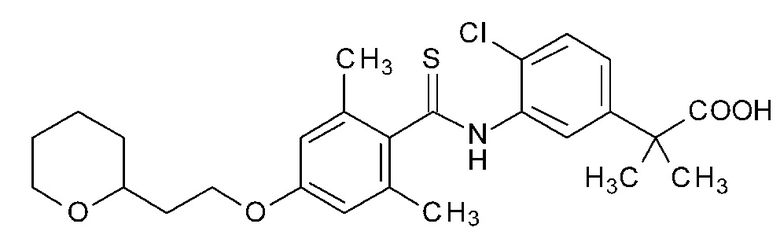
Используя соединения, полученное в примере 16, осуществляют ту же реакцию, что и в примере 2, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,14;
МС (ESI, положит., 20 В): 490(M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,20-1,25, 1,43-1,49, 1,49, 1,58-1,65, 2,36, 3,26-3,48, 3,77, 4,00-4,08, 6,68, 7,38, 7,46, 7,58 11,74, 12,57.
[0138]
Пример 18: Метил 2-{4-хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропаноат и метил 2-{4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропаноат
Используя соединение, полученное в примере 16, оптическое разделение осуществляли с помощью сверхкритической жидкостной хроматографии (SFC) с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Условия разделения, колонка: CHIRALPAK IC 5 мкм 20 мм×250 (производство компании Daicel Corporation); CO2: (этилацетат/метанол=9/1)=78/22
Пример 18-1: (первый пик)
Время удерживания SFC (мин): 3,69 (CHIRALPAK IC 5 мкм 20 мм×250 (производство компании Daicel Corporation); CO2: (этилацетат/метанол=9:1)=78:22)
Пример 18-2: (второй пик)
Время удерживания SFC (мин): 5,32 (CHIRALPAK IC 5 мкм 20 мм×250 (производство компании Daicel Corporation); CO2: (этилацетат/метанол=9:1)=78:22)
[0139]
Пример 19: 2-{4-Хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропионовая кислота и 2-{4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропионовая кислота
Используя соединение, полученное в примере 18-1 или примере 18-2, осуществляют ту же реакцию, что и в примере 2, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Пример 19-1: (Соединение, полученное с использованием соединения, полученного в примере 18-1)
Время удерживания ВЭЖХ (мин): 1,14;
МС (ESI, положит., 20 В): 490(M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,20-1,25, 1,43-1,49, 1,49, 1,58-1,65, 2,36, 3,26-3,48, 3,77, 4,00-4,08, 6,68, 7,38, 7,46, 7,58 11,74, 12,57.
Пример 19-2: (Соединение, полученное с использованием соединения, полученного в примере 18-2)
Время удерживания ВЭЖХ (мин): 1,14;
МС (ESI, положит., 20 В): 490(M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,20-1,25, 1,43-1,49, 1,49, 1,58-1,65, 2,36, 3,26-3,48, 3,77, 4,00-4,08, 6,68, 7,38, 7,46, 7,58 11,74, 12,57.
[0140]
Пример 20: 2-{3-[({2,6-Диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}-2-метилпропионовая кислота
[Химическая формула 64]
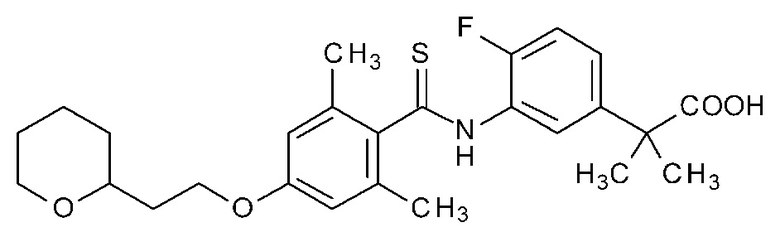
Те же реакции, что и в ссылочном примере 6→ссылочном примере 2→ссылочном примере 3→ссылочном примере 4→примере 1→примере 9→примере 2, осуществляли, используя метил 2-(4-фтор-3-нитрофенил)-2-метилпропаноат, полученный способом, описанным в WO 2018/116107 A, и 4-ацетокси-2,6-диметилбензойную кислоту вместо соединения, полученного в ссылочном примере 1, с получением указанного в заголовке соединения, имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,09;
МС (ESI, положит., 20 В): 474(M+H)+;
1H-ЯМР (ДМСО-d6): δ 1,25, 1,41-1,48, 1,49, 1,62, 1,71-1,85, 2,31, 3,32, 3,43, 3,87, 3,99-4,08, 6,68, 7,31, 7,38, 7,44, 11,65, 12,51.
[0141]
Пример 21: 2-(4-Хлор-3-{[(2,6-диметил-4-{2-[(2R)-тетрагидро-2H-пиран-2-ил]этокси}фенил)карботиоил]амино}фенил)-пропионовая кислота
[Химическая формула 65]
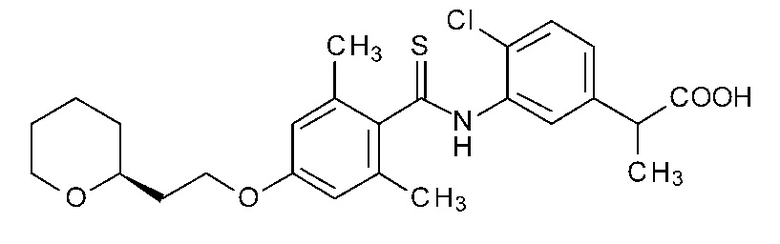
К раствору в дихлорметане (25 мл) соединения (1200 мг), полученного в примере 11-1, при температуре 0°C добавляли DIPEA (2,2 мл) и метоксиметил хлорид (0,57 мл) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционный раствор очищали хроматографией на колонке с силикагелем (гексан:этилацетат=95:5→35:65) с получением сырого продукта (1300 мг). К раствору в диметилацетамиде (10 мл) сырого продукта добавляли карбонат цезия (4,1 г) и метилйодид (0,78 мл) и реакционную смесь перемешивали при температуре 35°C в течение 16 часов. Реакционную смесь охлаждали до комнатной температуры и затем приливали водный раствор хлорида аммония. Смесь два раза экстрагировали трет-бутил-метиловым эфиром и органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=90:10→0:100) с получением сырого продукта (410 мг). К раствору в диоксане (10 мл) сырого продукта добавляли 5 моль/л водного раствора соляной кислоты (5 мл) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь два раза экстрагировали трет-бутил-метиловым эфиром и органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=90:10→0:100) с получением сырого продукта (320 мг). К раствору в тетрагидрофуране (4 мл) сырого продукта добавляли метанол (4 мл) и 2 моль/л водного раствора гидроксида натрия (4 мл) и реакционную смесь перемешивали при комнатной температуре в течение 3 часов. В реакционную смесь добавляли 2 моль/л водного раствора соляной кислоты, смесь два раза экстрагировали трет-бутил-метиловым эфиром и органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=90:10→0:100) с получением указанного в заголовке соединения (275 мг), имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,10;
МС (ESI, положит., 20 В): 476(M+H)+;
1H-ЯМР (CDCl3): δ 0,78-0,84, 1,30-1,90, 2,17-2,25, 2,39, 3,39-3,60, 3,90-4,12, 4,54, 6,37, 6,52-6,65, 7,01-7,04, 7,25-7,30, 7,42-7,45, 8,71, 8,88, 9,70.
[0142]
Пример 22: [4-Хлор-3-({[4-(2-циклогексилэтокси)-2,6-диметилфенил]карботиоил}амино)фенил]ацетат натрия
[Химическая формула 66]

К раствору в диоксане (2 мл) соединения (60 мг), полученного в примере 10-1, добавляли 1 моль/л водного раствора гидроксида натрия (0,13 мл) и затем смесь лиофилизовали с получением указанного в заголовке соединения (49 мг), имеющего следующие значения физических характеристик.
Время удерживания ВЭЖХ (мин): 1,38;
МС (ESI, положит., 20 В): 460 (M+H-Na)+;
1H-ЯМР (ДМСО-d6): δ 0,87-1,02, 1,10-1,28, 1,47, 1,67-1,79, 2,36, 3,26, 3,99, 6,65, 7,12-7,28, 7,38, 11,70.
[0143]
[Фармакологические примеры]
Биологический пример 1: Определение антагонистической активности рецептора DP с использованием клеток, экспрессирующих рецептор DP человека
Для определения антагонистической активности рецептора DP использовали набор cAMP-HTRF (SCETI MEDICAL LABO K.K., 62AM6PEJ). В 384-луночный планшет добавляли 10 мкл/лунку соединения по настоящему изобретению, приготовленного в различных концентрациях, и простагландина D2 (конечная концентрация 10 нмоль/л). Клетки, экспрессирующие рецептор DP человека, суспендировали в фосфатном буфере, содержащем 2 мкл/л диклофенака и 1 ммоль/л IBMX (3-изобутил-1-метилксантин), и высевали до 5000 клеток/10 мкл/лунку. После посева клеток клетки инкубировали при комнатной температуре в течение 1 часа. После этого добавляли конъюгат анти-цАМФ-криптат и раствор цАМФ-d2 в соответствии с методом набора для измерения, и смесь инкубировали при комнатной температуре в течение 1 часа, затем определяли концентрацию цАМФ в образце.
Интенсивность антагонистической активности соединений по настоящему изобретению в отношении рецептора DP была представлена значением IC50 (концентрация соединения по настоящему изобретению, необходимая для ингибирования 50% продукции цАМФ в отсутствие соединения по настоящему изобретению), рассчитанного по ингибированию отношение к продукции цАМФ увеличивалось при стимуляции простагландином D2 на 10 нмоль/л. В таблице 1 показана антагонистическая активность соединений по настоящему изобретению в отношении рецептора DP.
[Таблица 1]
IC50 (мкм)
Соединения по настоящему изобретению проявили сильную антагонистическую активность против рецепторов DP.
[0144]
Фармакокинетический тест 1. Определение концентрации соединения по настоящему изобретению в спинномозговой жидкости (ниже, CSF).
(1) Сбор CSF
Смешивали пять исследуемых веществ и готовили раствор исследуемого вещества таким образом, чтобы доза каждого исследуемого вещества составляла 3 мг/5 мл/кг. Используемая среда представляла собой 5% ДМСО, 20% коллифор HS15/пропиленгликоль (7:3). Раствор исследуемого вещества вводили перорально самцам крыс линии Wistar в возрасте 8-10 недель, приобретенных у компании Charles River Japan. Через три часа после введения крыс анестезировали и собирали спинномозговую жидкость (CSF) путем цистернальной пункции. Такое же количество этанола (wako), что и CSF, брали шприцем, используемым для сбора, и соединение, адсорбированное на шприце, выделяли промыванием.
(2) Измерение
В качестве вещества внутреннего стандарта использовали кандесартан (TRC), к 10 мкл полученного образца CSF добавляли 40 мкл ацетонитрила и 160 мкл кандесартан-содержащего ацетонитрила/этанола (7:3) и смесь перемешивали. Для построения калибровочной кривой 40 мкл раствора соединения и 160 мкл кандесартан-содержащего ацетонитрил/этанол (7: 3) добавляли к 10 мкл плазмы и смесь перемешивали. Все количество каждого раствора переносили на пластину фильтра для депротеинизации и фильтровали в вакууме. Полученный фильтрат соответствующим образом разбавляли ацетонитрилом/водой (1:1) и использовали для измерения. При измерении стандартные образцы для калибровочной кривой были приготовлены в той же матрице и проанализированы таким же образом. Измерение проводилось в следующих условиях.
Система жидкостной хроматографии: Prominence UFLCXR (Shimadzu Corporation),
Колонка: Shim-pack XR-ODSII 2,0 мм внутренний диаметр×75 мм (Shimadzu Corporation),
Температура колонки: 40°C,
Подвижная фаза: A: 0,2% муравьиная кислота 5 ммоль/л водного раствора ацетата аммония, B: ацетoнитрил,
Градиентная программа:
Время (подвижная фаза B (%)): 0 мин (10)→1,5 мин (90)→3,0 мин (90)→3,1 мин (10)→4 мин (10),
Скорость потока: 0,5 мл/мин
Система масс-спектрометрии: API4000, API5000 (AB SCIEX)
(3) Анализ
Уравнение регрессии рассчитывали на основе отношения площадей пиков (площадь пика исследуемого вещества/площадь пика вещества внутреннего стандарта), полученного путем измерения стандартных образцов для калибровочной кривой с использованием программного обеспечения для анализа Analyst ver. 1.5.2 (AB SCIEX). Вычисляли уравнение регрессии. Отношение площадей пиков также получали для измеряемого образца и подставлено в уравнение регрессии для расчета количественного значения. При расчете среднего значения и стандартного отклонения точки ниже нижнего предела количественного определения рассчитывались как 0.
Результаты представлены в таблице 2.
[Таблица 2]
Используя соединение, описанное в примере 13-24 в патентной литературе 2 документа предшествующего уровня техники, в качестве соединения для сравнения, определяли концентрацию соединения в CSF, которая составила 4,8 нг/мл. Концентрация соединения в CSF у соединений по настоящему изобретению была выше, чем у соединения сравнения, и была показана хорошая способность проникать в центральную нервную систему.
[0145]
Биологический пример 2: Эффект продления нормального времени пробуждения крысы
В мозг и шейные мышцы крыс помещали хронические электроды, чтобы подготовить крыс для измерения электроэнцефалограммы и электромиограммы. После периода восстановления продолжительностью одну неделю или более в защитной коробке, которая блокировала звук и электрический шум, к крысе присоединяли усилитель биологического сигнала. После акклиматизации в измерительной клетке в течение 1 часа или более крысам вводили перорально различные дозы соединения по настоящему изобретению в виде однократной дозы, и через 6 часов после перорального введения регистрировали электроэнцефалограмму и электромиограмму. После завершения измерения крыс каждый раз возвращали в клетку для разведения и оценивали носитель и каждое соединение с периодом вымывания в течение одной недели или более.
Записанные электроэнцефалограмма и электромиограмму анализировали с помощью SleepSign Ver. 3 и разделяли на периоды каждые 10 секунд, и определяли стадии пробуждения, медленного сна или быстрого сна со ссылкой на характеристики электроэнцефалограммы и электромиограммы, а также результаты спектрального анализа каждого частотного компонента мозговой волны. Стадию определяли как «пробуждение», когда наблюдалась электромиограмма высокой амплитуды, «сон без быстрого сна», когда наблюдались медленная волна высокой амплитуды и электромиограмма низкой амплитуды, и «быстрый сон», когда наблюдалась электроэнцефалограмма с низкой амплитудой, включая тета-волновую составляющую и электрокардиограмму с низкой амплитудой. Период, стадию которой было трудно определить из-за шума и т. п., был основан на результате определения предыдущей эпохи.
После определения состояния сна и бодрствования разница между общим временем пробуждения, равным 6 часам после введения соединения группе, получавшей соединение по настоящему изобретению, и общим временем пробуждения, равным 6 часам после введения группе, которой вводили носитель, выражали как индекс эффекта продления времени пробуждения.
В результате оценки эффекта продления времени пробуждения соединения по настоящему изобретению, например, соединение примера 8 и соединение примера 12, показали эффекты продления времени пробуждения на 48 минут и 60 минут при дозе 3 мг/кг, соответственно, и было показано, что соединение по настоящему изобретению может быть использовано в качестве терапевтического агента при нарушении режима сна и бодрствования.
[0146]
[Пример состава]
Типичный пример состава, используемого в настоящем изобретении, показан ниже.
{4-Хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусную кислоту (100 г), кальций карбокиметилцеллюлозу (20 г), стеарат магния (10 г) и микрокристаллическую целлюлозу (870 г) смешивают обычным способом, а затем прессуют, чтобы получить около 10000 таблеток, содержащих 10 мг активного ингредиента в одной таблетке.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
[0147]
Поскольку соединение по настоящему изобретению обладает сильной антагонистической активностью к рецепторам DP и отличной способностью проникать в центральную нервную систему, оно может использоваться в качестве профилактического и/или терапевтического агента при заболеваниях, опосредованных рецептором DP, в частности, нарушений режима сна и бодрствования.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ КАРБОНОВЫХ КИСЛОТ И МЕДИЦИНСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2004 |
|
RU2375353C2 |
| СОЕДИНЕНИЯ ФЕНИЛУКСУСНОЙ КИСЛОТЫ | 2008 |
|
RU2470926C2 |
| ПРЕДОТВРАЩАЮЩИЙ ПРЕЖДЕВРЕМЕННУЮ ОВУЛЯЦИЮ АГЕНТ | 2006 |
|
RU2419435C2 |
| СОДЕРЖАЩИЕ ФОСФОР СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНА3 | 2012 |
|
RU2598849C2 |
| НОВЫЕ ГИДРОКСИСЛОЖНОЭФИРНЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2016 |
|
RU2734418C2 |
| ПРОИЗВОДНЫЕ 6-АМИНОХИНАЗОЛИНА ИЛИ 3-ЦИАНОХИНОЛИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРА РЕЦЕПТОРНЫХ ТИРОЗИНКИНАЗ EGFR ИЛИ HER-2 | 2010 |
|
RU2536102C2 |
| ДЕСТРУКТОРЫ БЕЛКА MDM2 | 2017 |
|
RU2743432C2 |
| АКТИВАТОР KCNQ2-5 КАНАЛОВ | 2015 |
|
RU2712163C2 |
| СОЕДИНЕНИЕ, СПОСОБНОЕ К СВЯЗЫВАНИЮ С РЕЦЕПТОРОМ S1P, И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2004 |
|
RU2390519C2 |
| АНТИГИПЕРТРИГЛИЦЕРИДЕМИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ГИПЕРТРИГЛИЦЕРИДЕМИИ | 1995 |
|
RU2166320C2 |
Изобретение относится к антагонисту рецептора DP, представляющему собой соединение общей формулы (I), где R1, R2-R6, R11, R12, L, J, m, n определены в формуле изобретения, или его фармацевтически приемлемую соль. Соединения являются высоко безопасными и могут использоваться в качестве активных ингредиентов фармацевтических препаратов при заболеваниях, опосредованных рецептором DP. Соединение, представленное общей формулой (I), и его фармацевтически приемлемая соль также обладают хорошей способностью проникать в центральную нервную систему и, таким образом, особенно полезны в качестве профилактического и/или терапевтического агента для заболеваний, связанных с рецепторами DP, присутствующими в центральной нервной системе, в частности нарушений режима сна и бодрствования. 7 н. и 7 з.п. ф-лы, 2 табл., 22 пр.
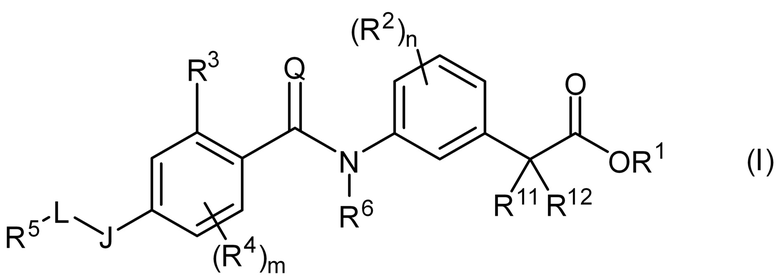
1. Соединение, представленное общей формулой (I):
[Химическая формула 1]
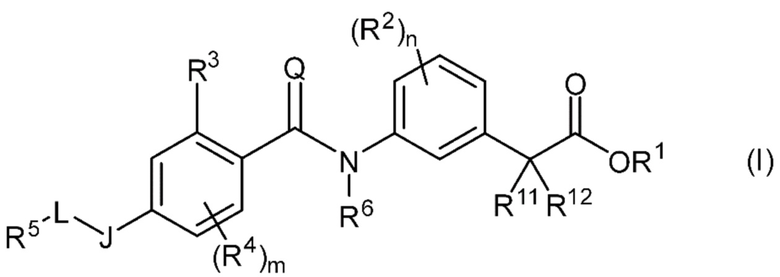 ,
,
где R1 представляет собой атом водорода, C1-4 алкильную или бензильную группу,
R2, R3 и R4, каждый, независимо, представлят собой (1) атом галогена, (2) C1-4 алкильную группу, необязательно замещенную атомом галогена, или (3) C1-4 алкокси группу, необязательно замещенную атомом галогена,
когда имеется несколько из R2 или R4, они могут быть одинаковыми или разными,
J представляет собой связь, -O- или -S-,
L представляет собой связь, C1-6 алкиленовую, C2-6 алкениленовую или C2-6 алкиниленовую группу,
R5 представляет собой атом водорода, C3-10 карбоцикл или 3-10-членный моноциклический или бициклический гетероцикл, содержащий от 1 до 5 гетероатомов, выбранных из атома кислорода, атома азота и атома серы,
C3-10 карбоцикл и 3-10-членный гетероцикл в R5 могут быть замещены 1-6 R7
при условии, что, когда L представляет собой связь, R5 не является атомом водорода,
R7 представляет собой (1) атом галогена, (2) C1-4 алкильную группу, необязательно замещенную атомом галогена, или (3) C1-4 алкокси группу, необязательно замещенную атомом галогена,
когда имеется несколько R7, они могут быть одинаковыми или разными,
Q представляет собой атом серы,
R6 представляет собой атом водорода или C1-4 алкильную группу,
R11 представляет собой атом водорода, атом галогена или C1-4 алкильную группу, необязательно замещенную атомом галогена,
R12 представляет собой атом водорода, атом галогена или C1-4 алкильную группу, необязательно замещенную атомом галогена,
R11 и R12 могут быть взяты вместе с атомом углерода, к которому они присоединены, с образованием C3-6 насыщенного карбоцикла,
n обозначает целое число от 0 до 4 и
m обозначает целое число от 0 до 3, или
его фармацевтически приемлемая соль.
2. Соединение по п.1, представленное общей формулой (I-1):
[Химическая формула 2]
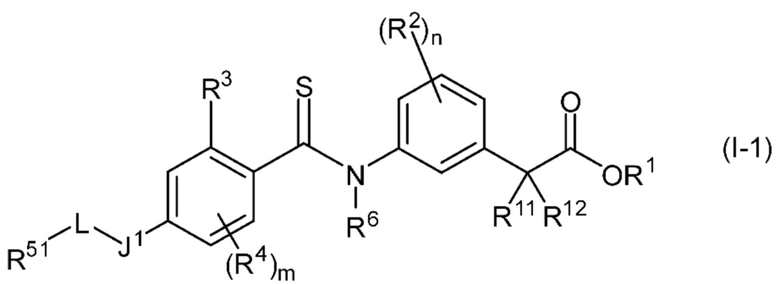 ,
,
где R51 представляет собой C3-10 карбоцикл или 3-10-членный моноциклический или бициклический гетероцикл, содержащий от 1 до 5 гетероатомов, выбранных из атома кислорода, атома азота и атома серы, J1 представляет собой связь или -O-, и другие символы имеют такое же значение, как указано в п.1, или его фармацевтически приемлемая соль.
3. Соединение по п.2, где R51 представляет собой 3-8-членный насыщенный моноциклический гетероцикл, содержащий от 1 до 3 гетероатомов, выбранных из атома кислорода, атома азота и атома серы, или его фармацевтически приемлемая соль.
4. Соединение по п.1, где соединение представляет собой
(11) (4-хлор-3-{[4-(2-циклогексилэтокси)-2,6-диметилбензол-1-карботиоил]амино}фенил)уксусную кислоту,
(12) [4-хлор-3-({4-[2-(оксан-2-ил)этокси]-2-(трифторметил)бензол-1-карботиоил}амино)фенил]уксусную кислоту,
(13) (4-хлор-3-{[4-(2-циклогексилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусную кислоту,
(14) (4-хлор-3-{[4-(2-фенилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусную кислоту,
(15) (4-хлор-3-{[4-(2-циклопропилэтокси)-2-(трифторметил)бензол-1-карботиоил]амино}фенил)уксусную кислоту,
(16) [4-хлор-3-({2,6-диметил-4-[2-(оксан-2-ил)этокси]бензол-1-карботиоил}амино)фенил]уксусную кислоту,
(17) {4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусную кислоту,
(18) {4-хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусную кислоту,
(19) 2-{3-[({2,6-диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}пропионовую кислоту,
(20) 1-{3-[({2,6-диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}циклопропанкарбоновую кислоту,
(21) 2-{4-хлор-3-[({2,6-диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]фенил}-2-метилпропионовую кислоту,
(22) 2-{4-хлор-3-[(2,6-диметил-4-{2-[(2S)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропионовую кислоту,
(23) 2-{4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}-2-метилпропионовую кислоту,
(24) 2-{3-[({2,6-диметил-4-[2-(тетрагидро-2H-пиран-2-ил)этокси]фенил}карботиоил)амино]-4-фторфенил}-2-метилпропионовую кислоту или
(25) 2-(4-хлор-3-{[(2,6-диметил-4-{2-[(2R)-тетрагидро-2H-пиран-2-ил]этокси}фенил)карботиоил]амино}фенил)пропионовую кислоту, или
его фармацевтически приемлемая соль.
5. Фармацевтическая композиция, которая является антагонистом рецептора DP, содержащая эффективное количество соединения, представленного общей формулой (I), или его фармацевтически приемлемую соль по п.1.
6. Фармацевтическая композиция по п.5, которая является профилактическим и/или терапевтическим агентом при заболевании, опосредованном рецептором DP.
7. Фармацевтическая композиция по п.6, где заболевание, опосредованное рецептором DP, представляет собой аллергическое заболевание, системный мастоцитоз, системное нарушение активации тучных клеток, анафилактический шок, сужение дыхательных путей, крапивницу, экзему, акне, аллергический бронхолегочный аспергиллез, синусит, мигрень, полипы в носу, гиперчувствительный васкулит, эозинофилию, контактный дерматит, заболевание, сопровождающееся зудом, заболевание, вторично вызванное состоянием, сопровождающимся зудом, заболевание, сопровождающееся покраснением кожи, воспаление, хроническую обструктивную болезнь легких, ишемию-реперфузионное повреждение, нарушение мозгового кровообращения, аутоиммунное заболевание, церебральную травму, заболевание печени, отторжение трансплантата, ревматоидный артрит, плеврит, остеоартрит, болезнь Крона, язвенный колит, синдром раздраженного кишечника, интерстициальный цистит, мышечную дистрофию, полимиозит, злокачественное новообразование, лейкемию, вирусную инфекцию, рассеянный склероз, нарушение режима сна и бодрствования или агрегацию тромбоцитов.
8. Фармацевтическая композиция по п.7, где заболевание, опосредованное рецептором DP, представляет собой нарушение режима сна и бодрствования и нарушение режима сна и бодрствования представляет собой заболевание, основанное на гиперсомнии, бессоннице, остаточной сонливости синдрома апноэ во сне, расстройстве циркадного ритма сна и бодрствования, гиперсомнии, связанной с нейродегенеративным заболеванием, гиперсомнии, связанной с психическим заболеванием, или патологическом апноэ во сне в дневное время.
9. Способ профилактики и/или лечения заболевания, опосредованного рецептором DP, включающего введение эффективного количества соединения, представленного общей формулой (I), или его фармацевтически приемлемой соли по п.1 пациенту, нуждающемуся в профилактике и/или лечении заболевания, опосредованного рецептором DP.
10. Соединение, представленное общей формулой (I), или его фармацевтически приемлемая соль по п.1, которое используется для профилактики и/или лечения заболевания, опосредованного рецептором DP.
11. Применение соединения, представленного общей формулой (I), или его фармацевтически приемлемой соли по п.1 для изготовления профилактического и/или терапевтического агента, используемого при заболевании, опосредованном рецептором DP.
12. Соединение, которое представляет собой {4-хлор-3-[(2,6-диметил-4-{2-[(2R)-оксан-2-ил]этокси}бензол-1-карботиоил)амино]фенил}уксусную кислоту или её фармацевтически приемлемую соль.
13. Соединение, представленное следующей структурной формулой:
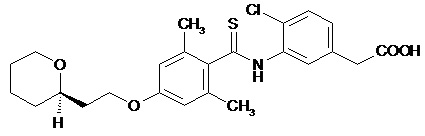 .
.
14. Фармацевтически приемлемая соль соединения, представленного следующей структурной формулой:
 .
.
| WO 2005080367 A1, 01.09.2005 | |||
| СОЕДИНЕНИЯ КАРБОНОВЫХ КИСЛОТ И МЕДИЦИНСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2004 |
|
RU2375353C2 |
| EP 1486491 A1, 15.12.2004 | |||
| СПОСОБ ВЫРАЩИВАНИЯ МОНОКРИСТАЛЛОВ КРЕМНИЯ | 2000 |
|
RU2177513C1 |
Авторы
Даты
2023-09-11—Публикация
2019-09-19—Подача