Область техники, к которой относится изобретение
Изобретение относится к трансфузиологии, а именно к способам получения фибринового клея.
Уровень техники
Актуальной проблемой трансфузиологии является разработка способов получения биоклея для герметизации хирургических дефектов из компонентов донорской крови.
Известен способ изготовления официнального фибрин-тромбинового клея, который включает смешивание плазмы, полученной от нескольких доноров, выделение из нее фибриногена и тромбина и помещение данных компонентов в изолированном друг от друга виде в стерильные шприцы. Хирург наносит оба компонента на дефект мягких тканей, и под воздействием тромбина происходит расщепление фибриногена до молекул фибрина-мономера, которые полимеризуются с образованием фибриновой пленки, закрывающей данный дефект.
Указанный способ характеризуется следующими недостатками:
1) Высокое остаточное количество тромбина снижает регенерацию костной и хрящевой тканей.
2) Официнальный клей является полидонорским продуктом, при этом отсутствует возможность идентифицировать важные характеристики донорской плазмы, включая группу крови и наличие гемотрансмиссивных заболеваний. Из этого вытекает высокий риск аллоиммунизации пациента.
3) Фибрин-тромбиновый клей отличается относительно медленной полимеризацией: стекает с вертикальных поверхностей до окончательного застывания.
4) Ограниченное время хранения готового клея (до 1 года).
5) Высокая стоимость клея.
Известен способ изготовления аутологичного фибрина с регулируемым содержанием фибриногена без использования экзогенного тромбина [1], включающий забор крови с цитратом натрия 3,8%, получение обогащенной тромбоцитами плазмы крови с помощью центрифугирования, выделение преципитата из плазмы крови методом этаноловой преципитации с низким содержанием этанола путем медленного добавления ледяного раствора 16% этанола рН 7,4 до соотношения с плазмой 1:1, инкубации при постоянном перемешивании 60 мин при 4°С и центрифугировании 4°С и скорости вращения 1000-2000 G в течение 20-30 мин, регулирование концентрации фибриногена в преципитате путем разведения Heres-буфером на NaCl рН 7,2-7,5, запуск полимеризации фибриногена с помощью активации эндогенного тромбина, содержащегося в преципитате, путем внесения раствора кальция хлорида в финальной концентрации 0,1-2%.
Данный способ содержит следующие недостатки:
1) Остаточный тромбин, содержащийся в преципитате, все еще представляет риск нарушения регенерации костной и хрящевой ткани.
2) Клей содержит остаточный этанол, что препятствует его использованию в нейрохирургии в связи с раздражающим действием этанола на нервную ткань и риском развития эпиприступов.
3) Готовится вне закрытой системы (практически в пробирке), что предполагает высокий риск контаминации микробами, пылью и другими мелкими объектами.
4) Процесс включает центрифугирование плазмы, что также предполагает риск контаминации в момент переливания ингредиентов в пробирку.
5) Не решена проблема идентификации донорских продуктов.
6) Процедура не автоматизирована, включает множество ручных манипуляций, что препятствует стандартизации и массовому внедрению методики.
Раскрытие изобретения
Технический результат предлагаемого изобретения заключается в повышении эффективности изготовления и идентификации фибринового клея.
Для достижения указанного технического результата разработан способ, включающий забор плазмы донора и сепарацию плазмы с расщеплением плазменного фибриногена на молекулы фибрина-мономера без использования экзогенного тромбина, отличающийся тем, что забирают плазму донора методом афереза, смешивают с раствором цитрата натрия и карантинизируют в течение 4 месяцев путем хранения в индивидуальной упаковке в морозильной камере при температуре -40°С; при запросе лечащего врача об изготовлении фибринового клея идентифицируют плазму донора, прошедшего двукратное обследование в отношении группы крови, наличия резус-фактора и антигенов гемотрансмиссивных заболеваний; размороженную плазму подвергают сепарации в закрытой замкнутой системе при температуре 37°С в течение 30 минут, при добавлении транексамовой кислоты в присутствии тромбиноподобного фермента батроксобина и буферного раствора с рН 4,0; по завершении сепарации из 120 мл плазмы получают 6 мл фибринового клея и аликвотируют в стерильные шприцы в условиях ламинарного шкафа при температуре 22-24°С в течение 3-5 минут; шприцы с фибриновым клеем маркируют с помощью технологической этикетки, содержащей индивидуальный штрих-код донации донорской плазмы, включающий закодированную информацию о коде региона, коде учреждения-заготовителя, годе донации, индивидуальном коде продукта и типе донорского продукта; закодированную информацию регистрируют в компьютер-реализуемой базе данных; маркированные шприцы с фибриновым клеем замораживают при температуре -20°С до востребования, при максимальном сроке хранения 5 недель; максимум за 20 минут до клинического применения идентифицируют шприцы с фибриновым клеем, изготовленным из плазмы от подходящего донора, при помощи сканирования технологической этикетки и сопоставления закодированной на ней информацией с информацией, содержащейся в базе данных; идентифицированные шприцы с фибриновым клеем размораживают и доставляют в операционную, где клей наносят на раневую поверхность в присутствии стерильного буферного раствора с рН 10, герметизируя хирургические дефекты; после клинического применения заполняют индивидуальный протокол, содержащий копию технологической этикетки, который включают в историю болезни.
Для сепарации плазмы можно использовать систему для автоматизированного приготовления фибринового клея «Vivostat System».
В качестве буферного раствора с рН 4,0 можно использовать буферный раствор «Вивостат» объемом 5,6 мл, содержащий 98% воды для инъекций, 1,1% ледяной уксусной кислоты, 0,4% хлорида кальция и 0,5% тригидрата ацетата кальция.
Аликвоты фибринового клея могут иметь объем 1, 2 или 4 мл.
Фибриновый клей можно наносить на раневую поверхность с помощью ручки-распылителя «Spraypen».
В качестве буферного раствора с рН 10 можно использовать буферный раствор «Вивостат» объемом 2,1 мл, содержащий 84% воды для инъекций, 12,9% декагидрата карбоната натрия и 3,1% бикарбоната натрия.
Индивидуальный протокол может содержать данные пациента: фамилию, имя, отчество, номер истории болезни, группу крови, объем фактически использованного фибринового клея, а также фамилию, имя и отчество исполнителя процедуры.
Описанные в формуле манипуляции по приготовлению донорской плазмы (забор методом афереза, карантинизация в течение 4 месяцев в индивидуальной упаковке при температуре -40°С) обеспечивают качественный состав плазмы, используемой для приготовления клея.
Двукратное обследование донора в отношении группы крови, наличия резус-фактора и антигенов гемотрансмиссивных заболеваний обеспечивает чистоту донорского продукта и минимизацию риска аллоиммунизации пациента.
Сепарация плазмы в закрытой замкнутой системе устраняет возможность контаминации раствора микроорганизмами. При этом указанное время (30 мин) и температурный режим (37°С) создают оптимальные условия для реакции перехода фибриногена в фибрин-мономер.
Использование тромбиноподобного фермента батроксобина вместо тромбина позволяет исключить тромбин из реакции и минимизировать его неблагоприятное влияние на регенерацию костной и хрящевой ткани.
Транексамовая кислота ингибирует фибринолиз, что позволяет сделать клеевой сгусток более стабильным после полимеризации.
Использование буферного раствора с рН 4,0 позволяет уменьшить риск контаминации плазмы микроорганизмами.
Стандартизированные объемы вступающей в реакцию плазмы (120 мл) и получаемого фибринового клея (6 мл) являются оптимальными для массового внедрения технологии.
Аликвотирование клея в стерильные шприцы в условиях ламинарного шкафа при температуре 22-24°С в течение 3-5 минут устраняет риск контаминации.
Идентификация шприцов с фибриновым клеем с помощью технологических этикеток с индивидуальным штрих-кодом и компьютер-реализуемой базы данных позволяет быстро и легко установить происхождение донорского продукта, а также его совместимость по отношению к пациенту, что исключает риск аллоиммунизации.
Использование буферного раствора с рН 10 на этапе нанесения клея обеспечивает полимеризацию фибрин-мономера и получение стабильного клеевого сгустка.
Учитывая простоту забора и хранения плазмы в больших объемах, а также сроки хранения плазмы (3 года) и готовых аликвот фибринового клея (5 недель) описанный способ обеспечивает возможность создания постоянного запаса клеевых ресурсов, эффективного как технологически, так и экономически.
Еще одно преимущество изготовления фибринового клея из донорской плазмы по предлагаемому способу заключается в возможности применения у пациентов всех возрастных групп, включая маленьких детей и пациентов с патологиями системы гемостаза. Данным категориям больных противопоказан забор аутоплазмы - альтернативного источника ингредиентов для изготовления клея. Предлагаемый нами способ лишен этого недостатка.
Протоколирование процедуры обеспечивает прослеживаемость фибринового клея после его клинического использования в послеоперационном периоде.
Таким образом, заявленный способ повышает эффективность изготовления и идентификации фибринового клея.
Описание чертежей
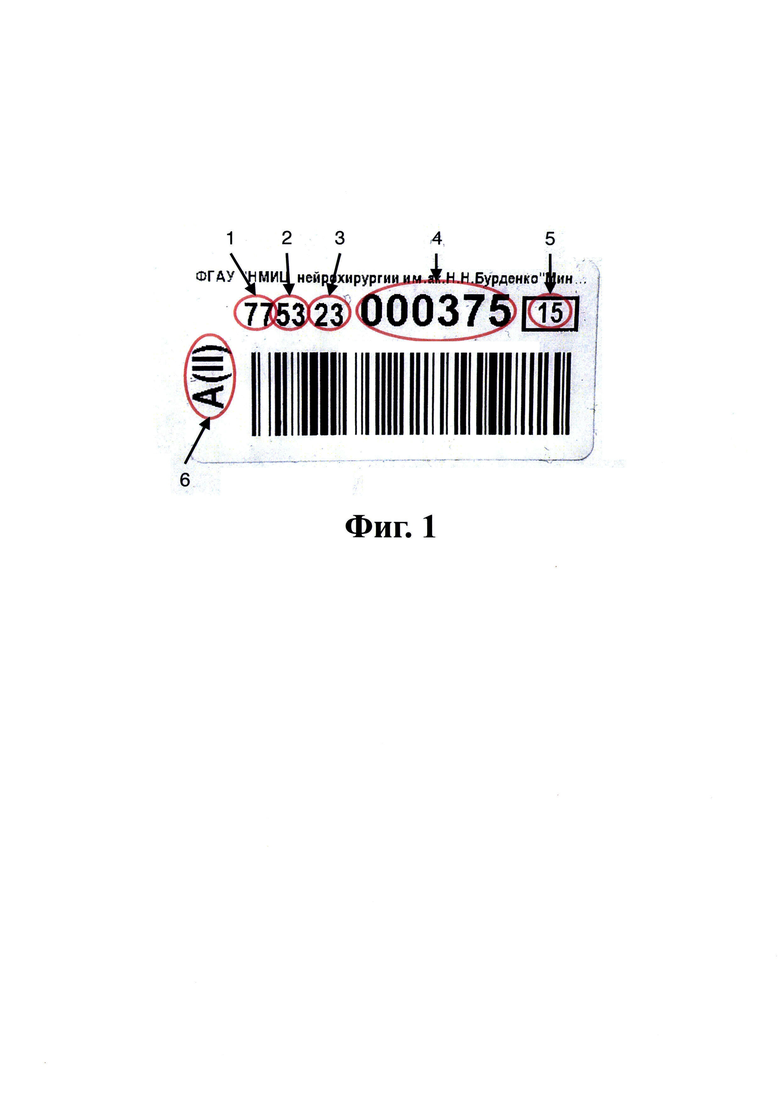
На фиг.1 представлена технологическая этикетка с индивидуальным штрих-кодом донации. Дополнительно этикетка содержит обозначение группы крови.
На фиг.2 представлены шприцы с готовым фибриновым клеем. Видны технологические этикетки.
Символами обозначены:
1 - Код региона
2 - Код учреждения-заготовителя
3 - Год донации
4 - Индивидуальный код продукта
5 - Тип донорского продукта
6 - Группа крови
Осуществление изобретения
Способ получения фибринового клея из донорской плазмы и его идентификации включает забор плазмы донора и сепарацию плазмы с расщеплением плазменного фибриногена на молекулы фибрина-мономера без использования экзогенного тромбина и отличается тем, что забирают плазму донора методом афереза, смешивают с раствором цитрата натрия и карантинизируют в течение 4 месяцев путем хранения в индивидуальной упаковке в морозильной камере при температуре -40°С; при запросе лечащего врача об изготовлении фибринового клея идентифицируют плазму донора, прошедшего двукратное обследование в отношении группы крови, наличия резус-фактора и антигенов гемотрансмиссивных заболеваний; размороженную плазму подвергают сепарации в закрытой замкнутой системе при температуре 37°С в течение 30 минут, при добавлении транексамовой кислоты в присутствии тромбиноподобного фермента батроксобина и буферного раствора с рН 4,0; по завершении сепарации из 120 мл плазмы получают 6 мл фибринового клея и аликвотируют в стерильные шприцы в условиях ламинарного шкафа при температуре 22-24°С в течение 3-5 минут; шприцы с фибриновым клеем маркируют с помощью технологической этикетки, содержащей индивидуальный штрих-код донации донорской плазмы, включающий закодированную информацию о коде региона, коде учреждения-заготовителя, годе донации, индивидуальном коде продукта и типе донорского продукта; закодированную информацию регистрируют в компьютер-реализуемой базе данных; маркированные шприцы с фибриновым клеем замораживают при температуре -20°С до востребования, при максимальном сроке хранения 5 недель; максимум за 20 минут до клинического применения идентифицируют шприцы с фибриновым клеем, изготовленным из плазмы от подходящего донора, при помощи сканирования технологической этикетки и сопоставления закодированной на ней информацией с информацией, содержащейся в базе данных; идентифицированные шприцы с фибриновым клеем размораживают и доставляют в операционную, где клей наносят на раневую поверхность в присутствии стерильного буферного раствора с рН 10, герметизируя хирургические дефекты; после клинического применения заполняют индивидуальный протокол, содержащий копию технологической этикетки, который включают в историю болезни.
Более подробно, предлагаемый способ используется следующим образом.
Для забора плазмы вызывается активный донор, прошедший двухкратное обследование в отношении группы крови, наличия резус-фактора и антигенов гемотрансмиссивных заболеваний. После первичного лабораторного обследования производят донацию плазмы донора с лейкоредукцией на аферезной платформе (например, Haemonetics MCS+) до 640 мл одноигольным контуром в замкнутой системе, с последующим разделением на две порции по 320 мл и заморозкой в шоковом замораживателе (например, Dometic). Оптимальный температурный режим составляет от -45 до -40°С, что сохраняет эффективность факторов свертывания. При проведении афереза весь клеточный состав (тромбоциты, лейкоциты, эритроциты) сразу возвращаются в кровеносное русло донора. Экстракорпоральный контур аферезной платформы заполняется 4% раствором цитрата натрия в соотношении 1:16, т.е. 1 мл раствора цитрата натрия на 16 мл цельной крови, которая проходит через экстракорпоральный контур для плазмафереза. Цитрат натрия выступает в качестве консерванта, антикоагулянтный эффект обеспечивается за счет связывания ионов кальция.
Полученная плазма проходит карантинизацию в течение 120 суток при низкой температуре (-40°С). Максимальный срок хранения плазмы составляет 36 месяцев.
Для производства фибринового клея отбирается только валидированная плазма, полученная методом автоматизированной заготовки и прошедшая карантинизацию.
Плазму размораживают и подвергают сепарации в закрытой замкнутой системе - например, «Vivostat System» (производитель - Вивостат А/С, Дания) - при температуре 37°С в течение 30 минут, при добавлении транексамовой кислоты в присутствии тромбиноподобного фермента батроксобина и буферного раствора с рН 4,0. Оптимальным является буферный раствор «Вивостат» (производитель - Вивостат А/С, Дания) объемом 5,6 мл, который изготовлен из расчета: 98% воды для инъекций, 1,1% ледяной уксусной кислоты, 0,4% хлорида кальция и 0,5% тригидрата ацетата кальция. Кислая среда буферного раствора позволяет минимизировать риск контаминации, т.к. большинство микроорганизмов не приспособлено к существованию в кислой среде.
По завершении сепарации из 120 мл плазмы получают 6 мл фибринового клея, который аликвотируют в стерильные шприцы объемом 1, 2 или 4 мл в условиях ламинарного шкафа при температуре 22-24°С в течение 3-5 минут.
В процессе аликвотирования можно получить разные объемы клея; в нашем учреждении (НМИЦ нейрохирургии имени акад. Н.Н. Бурденко) наиболее часто требуется клей в количестве 1, 2 или 4 мл, с учетом операционных подходов к реконструкции операционной раны после удаления новообразований.
Сразу после изготовления клея шприцы проходят маркировку с помощью технологической этикетки, содержащей индивидуальный штрих-код донации донорской плазмы. Он включает 14 цифр: код региона (2 цифры), код учреждения-заготовителя (2 цифры), год донации (2 цифры), индивидуальный код продукта (6 цифр) и тип донорского продукта (2 цифры).
После аликвотирования получается несколько доз клея, каждая из которых маркируется технологической этикеткой и отличается двумя крайними цифрами цифрового кода (тип донорского продукта). Таким образом, фибриновый клей, полученный из одной дозы свежезамороженной плазмы, имеет полную прослеживаемость.
Конкретный пример кодирования информации: технологическая этикетка, содержащая код 77-53-23-000375-15 (см. Фиг. 1). Расшифровка цифр:
77 - код региона (Москва)
53 - код учреждения (НМИЦ нейрохирургии имени акад. Н.Н. Бурденко)
23 - год донации
000375 - индивидуальный код продукта; он привязан к конкретному коду донора -индивидуального цифрового значения, которое присваивается донору раз в жизни и действует на протяжении всей истории донорства конкретного человека на территории РФ.
15 - тип донорского продукта, например, цельная кровь (01), плазма (02), эритроциты (03), тромбоциты (04). Эти цифры могут быть любыми, но не повторяются. При маркировке шприцов с фибриновым клеем каждая аликвота содержит этикетку со своим кодом типа продукта.
Закодированную информацию регистрируют в компьютер-реализуемой базе данных. Примером такой базы является национальная автоматизированная система трансфузиологии (НАИСТ); данная программа позволяет проследить весь путь заготовки донорского продукта крови от донора до реципиента.
Маркированные шприцы с фибриновым клеем замораживают при температуре -20°С до востребования, при максимальном сроке хранения 5 недель.
При получении запроса от лечащего врача о необходимости использования фибринового клея идентифицируют шприцы с фибриновым клеем, изготовленным из плазмы от подходящего по группе крови донора, при помощи сканирования штрих-сканером технологической этикетки и сопоставления закодированной на ней информацией с информацией, содержащейся в базе данных.
Идентифицированные шприцы с фибриновым клеем размораживают и доставляют в операционную, где клей наносят на раневую поверхность в присутствии стерильного буферного раствора с рН 10, герметизируя хирургические дефекты. Для нанесения используют ручку-распылитель, например, «Spraypen» (производитель - Вивостат А/С, Дания). Стоит подчеркнуть, что полимеризация фибрин-мономера происходит только в присутствии стерильного буферного раствора с рН 10, при этом происходит сшивка фибрина и - в результате - образование пленки. В качестве подходящей среды лучше использовать раствор «Вивостат» (производитель - Вивостат А/С, Дания) объемом 2,1 мл, который изготовлен из расчета: 84% воды для инъекций, 12,9% декагидрата карбоната натрия и 3,1% бикарбоната натрия.
После клинического применения на пациента заполняется индивидуальный протокол, который содержит данные пациента: фамилию, имя, отчество, номер истории болезни, группу крови, объем фактически использованного фибринового клея, а также фамилию, имя и отчество исполнителя процедуры.
Клинические примеры
Пациентка Н., 33 года. Диагноз: краниофациальная опухоль справа. 05.04.2023 проведена операция в объеме микрохирургического удаления краниофациальной опухоли справа с пластикой дефекта твердой мозговой оболочки сложносоставным аутотрансплантатом; для пластики хирургического дефекта использован фибриновый клей, изготовленный из донорской плазмы по предлагаемому способу. Из 120 мл плазмы получено 6 мл фибринового клея. Клей аликвотировали в шесть стерильных шприцов (объем каждой аликвоты 1 мл) в условиях ламинарного шкафа при температуре 22°С в течение 3 минут.
Пациентка О., 68 лет. Диагноз: дефект основания черепа в области задней стенки лобной пазухи слева. Спонтанная назальная ликворея слева. 15.03.2023 проведена операция в объеме пластики дефекта основания черепа комбинированным трансназально-трансфронтальным доступом с применением сложносоставного аутотрансплантата; для пластики дефекта использован фибриновый клей, изготовленный из донорской плазмы по предлагаемому способу. Из 120 мл плазмы получено 6 мл фибринового клея. Клей аликвотировали в три стерильных шприца (объем каждой аликвоты 2 мл) в условиях ламинарного шкафа при температуре 24°С в течение 5 минут.
Пациент М., 36 лет. Диагноз: краниофациальная опухоль слева. 27.03.2023 проведена операция в объеме микрохирургического удаления краниофациальной опухоли слева с пластикой дефекта основания черепа сложносоставным аутотрансплантатом; для пластики хирургического дефекта использован фибриновый клей, изготовленный из донорской плазмы по предлагаемому способу. Из 120 мл плазмы получено 6 мл фибринового клея. Клей аликвотировали в два стерильных шприца (объем аликвот 4 и 2 мл, соответственно) в условиях ламинарного шкафа при температуре 24°С в течение 5 минут.
По сравнению с прототипом, во всех случаях отмечено упрощение и автоматизирование производства фибринового клея, а также удобная и систематизированная идентификация клея как донорского продукта. На операциях выявлена быстрая полимеризация клея в течение 2-4 секунд после нанесения, а также достигнута хорошая степень герметичности дефектов мягких тканей. Ни у одного пациента не возникло аллергических реакций.
Список использованной литературы 1. Антонова Л.В., Матвеева В.Г., Ханова М.Ю., Барбараш О.Л., Барбараш Л.С. Способ изготовления аутологичного фибрина с регулируемым содержанием фибриногена без использования экзогенного тромбина. Патент RU 2758260 С1. Дата подачи заявки 24.12.2020. Дата публикации и выдачи патента 27.10.2021.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОРГАНОСПЕЦИФИЧЕСКИЙ РЕГЕНЕРАНТ GI | 2011 |
|
RU2462255C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРАТА ТРОМБИНА | 2014 |
|
RU2583931C2 |
| Способ приготовления аутологичного двухкомпонентного фибринового клея | 2019 |
|
RU2704256C1 |
| Способ определения функционального фибриногена | 2017 |
|
RU2669796C1 |
| СПОСОБЫ ИСПОЛЬЗОВАНИЯ ФИБРИНОВОГО ГЕРМЕТИКА, СПОСОБ ПОЛУЧЕНИЯ СОСТАВА, СОСТАВЫ, НАБОРЫ | 1993 |
|
RU2143924C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМОГО ФИБРИН-МОНОМЕРА | 2003 |
|
RU2253474C1 |
| Способ определения фибриногена при рекальцификации цитратной плазмы и оценка его функциональности | 2019 |
|
RU2703541C1 |
| ПРЕПАРАТ, ИНГИБИРУЮЩИЙ РАЗВИТИЕ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ, СОДЕРЖАЩИЙ ДЕЗ-А-ФИБРИН | 2005 |
|
RU2358754C2 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ ПОЛУЧЕНИЯ СЫВОРОТКИ С ТРОМБИНОМ ОТ ОДНОГО ДОНОРА | 2013 |
|
RU2589648C2 |
| СПОСОБ ГЕРМЕТИЗАЦИИ МЕЖКИШЕЧНОГО АНАСТОМОЗА | 2011 |
|
RU2464942C1 |
Изобретение относится к трансфузиологии. Раскрыт способ получения фибринового клея из донорской плазмы и его идентификации, который включает забор плазмы донора методом афереза, после чего плазму смешивают с раствором цитрата натрия и карантинизируют в течение 4 месяцев путем хранения в индивидуальной упаковке в морозильной камере при температуре -40°С. При запросе лечащего врача об изготовлении фибринового клея идентифицируют плазму донора, прошедшего двукратное обследование в отношении группы крови, наличия резус-фактора и антигенов гемотрансмиссивных заболеваний. Размороженную плазму подвергают сепарации в закрытой замкнутой системе при температуре 37°С в течение 30 минут, при добавлении транексамовой кислоты в присутствии тромбиноподобного фермента батроксобина и буферного раствора с рН 4,0. По завершении сепарации из 120 мл плазмы получают 6 мл фибринового клея и аликвотируют в стерильные шприцы в условиях ламинарного шкафа при температуре 22-24°С в течение 3-5 минут. Шприцы с фибриновым клеем маркируют с помощью технологической этикетки, содержащей индивидуальный штрихкод донации донорской плазмы, включающий закодированную информацию о коде региона, коде учреждения-заготовителя, годе донации, индивидуальном коде продукта и типе донорского продукта. Закодированную информацию регистрируют в компьютер-реализуемой базе данных. Маркированные шприцы с фибриновым клеем замораживают при температуре -20°С до востребования, при максимальном сроке хранения 5 недель. Максимум за 20 минут до клинического применения идентифицируют шприцы с фибриновым клеем, изготовленным из плазмы от подходящего донора, при помощи сканирования технологической этикетки и сопоставления закодированной на ней информации с информацией, содержащейся в базе данных. Идентифицированные шприцы с фибриновым клеем размораживают и доставляют в операционную, где клей наносят на раневую поверхность в присутствии буферного раствора с рН 10, герметизируя хирургические дефекты. После клинического применения заполняют индивидуальный протокол, содержащий копию технологической этикетки, который включают в историю болезни. Изобретение обеспечивает повышение эффективности изготовления и идентификации фибринового клея. 7 з.п. ф-лы, 2 ил., 3 пр.
1. Способ получения фибринового клея из донорской плазмы и его идентификации, включающий забор плазмы донора и сепарацию плазмы с расщеплением плазменного фибриногена на молекулы фибрина-мономера без использования экзогенного тромбина, отличающийся тем, что забирают плазму донора методом афереза, смешивают с раствором цитрата натрия и карантинизируют в течение 4 месяцев путем хранения в индивидуальной упаковке в морозильной камере при температуре -40°С; при запросе лечащего врача об изготовлении фибринового клея идентифицируют плазму донора, прошедшего двукратное обследование в отношении группы крови, наличия резус-фактора и антигенов гемотрансмиссивных заболеваний; размороженную плазму подвергают сепарации в закрытой замкнутой системе при температуре 37°С в течение 30 минут, при добавлении транексамовой кислоты в присутствии тромбиноподобного фермента батроксобина и буферного раствора с рН 4,0; по завершении сепарации из 120 мл плазмы получают 6 мл фибринового клея и аликвотируют в стерильные шприцы в условиях ламинарного шкафа при температуре 22-24°С в течение 3-5 минут; шприцы с фибриновым клеем маркируют с помощью технологической этикетки, содержащей индивидуальный штрихкод донации донорской плазмы, включающий закодированную информацию о коде региона, коде учреждения-заготовителя, годе донации, индивидуальном коде продукта и типе донорского продукта; закодированную информацию регистрируют в компьютер-реализуемой базе данных; маркированные шприцы с фибриновым клеем замораживают при температуре -20°С до востребования, при максимальном сроке хранения 5 недель; максимум за 20 минут до клинического применения идентифицируют шприцы с фибриновым клеем, изготовленным из плазмы от подходящего донора, при помощи сканирования технологической этикетки и сопоставления закодированной на ней информации с информацией, содержащейся в базе данных; идентифицированные шприцы с фибриновым клеем размораживают и доставляют в операционную, где клей наносят на раневую поверхность в присутствии стерильного буферного раствора с рН 10, герметизируя хирургические дефекты; после клинического применения заполняют индивидуальный протокол, содержащий копию технологической этикетки, который включают в историю болезни.
2. Способ по п. 1, в котором для сепарации плазмы используют систему для автоматизированного приготовления фибринового клея «Vivostat System».
3. Способ по п. 1, в котором используют 100 мг транексамовой кислоты.
4. Способ по п. 1, в котором в качестве буферного раствора с рН 4,0 используют раствор объемом 5,6 мл, который изготовлен из расчета: 98% воды для инъекций, 1,1% ледяной уксусной кислоты, 0,4% хлорида кальция и 0,5% тригидрата ацетата кальция.
5. Способ по п. 1, в котором аликвоты фибринового клея имеют объем 1, 2 или 4 мл.
6. Способ по п. 1, в котором фибриновый клей наносят на раневую поверхность с помощью ручки-распылителя «Spraypen».
7. Способ по п. 1, в котором в качестве буферного раствора с рН 10 используют раствор объемом 2,1 мл, который изготовлен из расчета: 84% воды для инъекций, 12,9% декагидрата карбоната натрия и 3,1% бикарбоната натрия.
8. Способ по п. 1, в котором индивидуальный протокол содержит данные пациента: фамилию, имя, отчество, номер истории болезни, группу крови, объем фактически использованного фибринового клея, а также фамилию, имя и отчество исполнителя процедуры.
| KJAERGARD H.K | |||
| et al | |||
| Vivostat System Autologous Fibrin Sealant: Preliminary Study in Elective Coronary Bypass Grafting // Ann Thorac Surg., 1998, V.66, pp.482-486 | |||
| Способ приготовления аутологичного двухкомпонентного фибринового клея | 2019 |
|
RU2704256C1 |
| US 20140154233 A1, 05.06.2014 | |||
| US 6613325 B1, 02.09.2003 | |||
| THORN J.J | |||
| et al | |||
| Autologous fibrin glue with growth factors in reconstructive maxillofacial | |||
Авторы
Даты
2023-09-11—Публикация
2023-05-15—Подача