Изобретение относится к медицине, в частности, к офтальмологии, касается клеящих веществ и позволяет получить двухкомпонентный аутологичный фибриновый клей, состоящий из обогащенной тромбоцитами плазмы объемом 1.0 мл, содержащей фибриноген, факторы свертывания крови в физиологических концентрациях и живые тромбоциты, продуцирующие различные факторы роста и адгезивные молекулы в качестве 1-го компонента, получаемого из собственной плазмы крови пациента и 2-го компонента содержащего от 0.5 до 5.0% раствор хлорида кальция и тромбин в концентрации от 0.5 до 500 ME, рассчитываемой исходя из показателей фибриногена крови пациента и необходимого времени возникновения адгезии, отличающийся простотой в исполнении, безопасностью для пациентов и меньшей стоимостью по сравнению с прототипом. Изобретение обеспечивает получение клея с высокой адгезивностью, биосовместимостью, способностью к биодеградации, а также с противовоспалительным и гемостатическим эффектом.
Известен органоспецифический регенерат GI (Патент РФ №2462255 от 23.06.2011, А61K 35/16, A61L 27/22, A61L 27/44, В82В 3/00), для получения которого используется криопреципитат, полученный из карантинизированной свежезамороженной донорской плазмы; концентрат тромбоцитов, взвешенных в плазме и подвергшихся многократному замораживанию и размораживанию с целью получения плазмы, обедненной тромбоцитами, обогащенной факторами роста (тромболизат); тромбин человеческий (лиофильно высушенный) 5-500 ЕД; 0,9% раствор натрия хлорида; 10% раствор кальция хлорида.
Тромболизат готовят следующим образом. Полученный из крови концентрат тромбоцитов (в стерильном пластиковом контейнере) подвергается замораживанию на быстрозамораживателе с последующим размораживанием в специальном размораживателе. По истечении трехкратно повторяющихся циклов замораживания - размораживания плазма подвергается центрифугированию. Надосадочная жидкость перемещается в пустой пластиковый контейнер и повторно центрифугируется при тех же условиях. Плазму с уменьшенным содержанием тромбоцитов фильтруют через стерильный однослойный ватно-марлевый фильтр в условиях бокса, затем пропускают через стерильный бумажный фильтр и в заключение - через фильтр (Millipore IRELAND Ltd). Полученный тромболизат хранится при температуре ниже -25°С в течение 36 месяцев.
Для приготовления криопреципитата «Органоспецифического регенеранта GI» используют ультрацентрифугирование, т.е. разделение частиц размером менее 100 нм в течение 15 мин при температуре +2°С+-2°С со скоростью 4200 об/мин. Тем самым добиваются наноструктурирования фибриновой матрицы, благодаря чему она становится более прочной и эластичной. Использование ультрацентрифуги позволяет сократить время центрифугирования и, тем самым, исключить негативное воздействие на качество криопреципитата и увеличить активность VIII фактора до 70 ME. Хранится он при температуре ниже -60°С. Это позволяет материалу длительное время (в течение 36 месяцев) сохранять свои первоначальные свойства.
Подготовленные компоненты (криопреципитат, тромболизат, раствор тромбина) используются в равных объемах. В первый шприц набирается 1 мл размороженного криопреципитата; во второй шприц - 1 мл тромбина 5-500 ЕД, разведенного в 2 мл 0,9% хлористого натрия с добавлением 1 мл 10% раствора хлористого кальция; в третий шприц набирается 1 мл тромболизата.
Основными недостатками «Органоспецифического регенерата GI» являются его сложная многокомпонентная структура (криопреципит, тромболизат, тромбин), изготовление каждого компонента занимают длительное время и проводится в несколько этапов, длительное время и особые условия центрифугирования, а так же для изготовления необходима карантинизированная свежезамороженная донорская плазма, что полностью не исключает риск аллергической реакции.
Известен способ хирургического лечения сквозных идиопатических макулярных разрывов сетчатки, патент РФ №2652076 от 19.05.2017, A61F 9/007, А61K 35/19, А61Р 27/02. В данном патенте в качестве биологического клея используют аутологичный тромбоцитарный лизат, приготовленный из обогащенной тромбоцитами аутоплазмы, содержащей не менее 1000×103 кл/мл. Получение аутологичного тромбоцитного лизата (pHPL) осуществляют следующим образом: в 6-8 специализированных пробирок с коммерческим названием Plasmolifting, содержащих гепарин и уникальный гель, производят забор крови объемом 9 мл, пробирки помещают в центрифугу и центрифугируют в течение 6-7 минут при 3700-3800 об/мин. В ходе вращения в центрифуге, кровь разделяется на две основные фракции - эритроцитарно-лейкоцитарный сгусток и плазму крови, содержащую тромбоциты (тромбоцитарная аутоплазма). Затем шприцем (10,0-20,0 мл) из пробирок забирают супернатант, содержащий аутоплазму, обогащенную тромбоцитами, находящуюся в верхней части пробирки над разделительным гелем, помещают в одну пробирку объемом 15,0-50,0 мл и производят повторное центрифугирование в течение 12-15 минут при 3500-3600 об/мин. Концентрация тромбоцитов в аутоплазме составляет не менее 1000×103 кл/мл. Из обогащенной тромбоцитами аутоплазмы готовят лизат путем лизиса мембраны тромбоцитов. Тромбоциты аутологичной плазмы лизируют путем двукратного замораживания в жидком азоте (-196°С) и быстрого оттаивания на водяной бане (+37°С). Полученный аутологичный тромбоцитный лизат (pHPL) фильтруют через фильтр (0,22 нм) и хранят до использования при температуре - 20°С.
Основными недостатками аутологичного тромбоцитарного лизата является большой объем необходимой крови пациента, несколько обязательных этапов центрифугирования, ограничено минимальное количество концентрации тромбоцитов в аутоплазме, а так же обязательное техническое оснащение лаборатории (наличие жидкого азота).
Наиболее близким является патент РФ №2520829 от 15.11.2012 «Способ пластики глазных век», A61F 9/007. В данном патенте используется аутологичный фибриновый клей для фиксации кожного лоскута. Фибриновый клей получают следующим способом: Забирают 25-35 мл крови пациента, разводят в отношении 9:1 в 3,8% растворе цитрата натрия и далее центрифугируют в течение 10 мин при 3000 об/мин. Плазму декантируют и далее очищают (фибриноген) глицерином, - осадок обезвоживают MgSO4 и BaSO4 и затем возвращают к исходному объему раствора - 20 мл. Слой фибрина в растворе центрифугируют и отделяют, повторно обрабатывают смесью безводных MgSO4 и BaSO4, отделяют верхний слой и снова возвращают к первоначальному объему (20 мл) 0,055 М раствором цитрата натрия при рН 7,4 и снова осаждают глицерином, очищают и разделяют на необходимые порции.
Основными недостатками данного способа получения аутологичного фибринового клея являются сложная методика выделения фибриногена и обработки осадка, отсутствие второго компонента, который позволяет регулировать время застывания и силу адгезии, в качестве способа его получения предлагается дорогостоящая методика с применением мини-лаборатории «CRYOSIL FS».
В основу настоящего изобретения положена идея создания простого и быстрого способа приготовления аутологичного двухкомпонентного фибринового клея. Поэтому отличительными чертами предлагаемого нами способа является простота и скорость приготовления компонентов фибринового клея с использованием минимального объема крови пациента, когда не требуется разведение и дополнительное очищение плазмы крови, отсутствует необходимость в очищении фибрина и обработке осадка, а применяемые условия центрифугирования оказываются оптимальными для выделения и сохранения в течение недели жизнеспособности тромбоцитов, которые продуцируют факторы роста, адгезивные молекулы и цитокины, что обеспечивает ускорение репаративных процессов не только за счет снижения воспалительной реакции, но и за счет обеспечения адгезии пролиферирующих клеток, том числе и эпителиальных.
Технический результат достигается тем, что в предлагаемом способе приготовления аутологичного двухкомпонентного фибринового клея, состоящего из аутологичной свежезабранной плазмы крови пациента, содержащей живые тромбоциты, фибриноген и факторы свертывания крови в физиологических концентрациях, заключающимся в заборе крови в стерильные пробирки с цитратом натрия 3.8%, центрифугирование плазмы крови, при котором забор венозной крови осуществляют в стерильную пробирку, позволяющую получить обогащенную тромбоцитами плазму, центрифугировании забранной крови в течение 4 минут при 3500 об/мин, последующем заборе обогащенной тромбоцитами плазмы объемом 1.0 мл, содержащей фибриноген, факторы свертывания крови в физиологических концентрациях и живые тромбоциты, продуцирующие различные факторы роста и адгезивные молекулы, и смешивании со вторым компонентом, содержащим от 0.5 до 5.0% раствор хлорида кальция и тромбин в концентрации от 0.5 до 500 ME, рассчитываемой исходя из показателей фибриногена крови пациента и необходимого времени возникновения адгезии.
Использование отличных от прототипа параметров центрифугирования, в частности меньшего времени и в оптимальном соотношении увеличенной скорости, позволяет получить компонент с большей концентрацией живых тромбоцитов, выделяющих факторы роста и адгезивные молекулы, снизив вероятность их повреждения, не снижая необходимую для адгезии концентрацию фибриногена.
Объем забираемой крови согласно предлагаемому способу является достаточным для получения 1 мл первого компонента клея в связи с тем, что именно в этом 1 мл после центрифугирования оказывается наибольшая концентрация живых тромбоцитов.
Способ приготовления аутологичного фибринового клея предусматривает получение готового первого компонента сразу после центрифугирования забранной крови пациента, что не требует выполнение дополнительных манипуляций, в разы ускоряет и упрощает данную процедуру.
Конечный объем 1 го компонента кроме фибриногена содержит живые тромбоциты, факторы роста и адгезивные молекулы, которые дополнительно усиливают склеивающие характеристики полученного фибринового клея, обеспечивая прочную и быструю адгезию склеиваемых тканей. Таким образом, отсутствует необходимость в отдельном выделении из всего объема забранной крови фибриногена с целью повышения его концентрации.
Использование от 0,5 до 5.0% раствора хлорида кальция и тромбина в концентрации от 0.5 до 500 ME позволяет регулировать время застывания, адгезию.
Изобретение поясняется с помощью фиг. 1, на которой отражены этапы приготовления двухкомпонентного аутологичного фибринового клея согласно предлагаемому способу. В 4 стерильные пробирки с цитратом натрия 3.8% объемом 5.0 мл производится забор свежей аутологичной плазмы крови пациента, далее вся кровь собирается в 1 стерильный шприц объемом 20.0 мл, после чего перемещается в стерильную пробирку «YCELLBIO-KIT» (фиг. 1а), или иную пробирку, позволяющую получить обогащенную тромбоцитами плазму, далее происходит ее центрифугирование в течение 4 минут при 3500 об/мин (параметры указаны для «YCELLBIO-KIT»), после этого из пробирки производится забор обогащенной тромбоцитами плазмы объемом 1.0 мл (фиг. 1б), содержащей фибриноген, факторы свертывания крови в физиологических концентрациях и живые тромбоциты, продуцирующие различные факторы роста и адгезивные молекулы, таким образом мы получаем первый компонент двухкомпонентного аутофибринового клея без необходимости выделения фибриногена и факторов свертывания, который в последующем смешивается со вторым компонентом, содержащим от 0.5 до 5.0% раствор хлорида кальция и тромбин в концентрации от 0.5 до 500 ME, рассчитываемой исходя из показателей фибриногена крови пациента и необходимого времени возникновения адгезии. В итоге подготовленные компоненты в равных объемах набираются в 2 разных стерильных шприца (фиг. 1в). Активирование клея происходит при смешивании двух его компонентов.
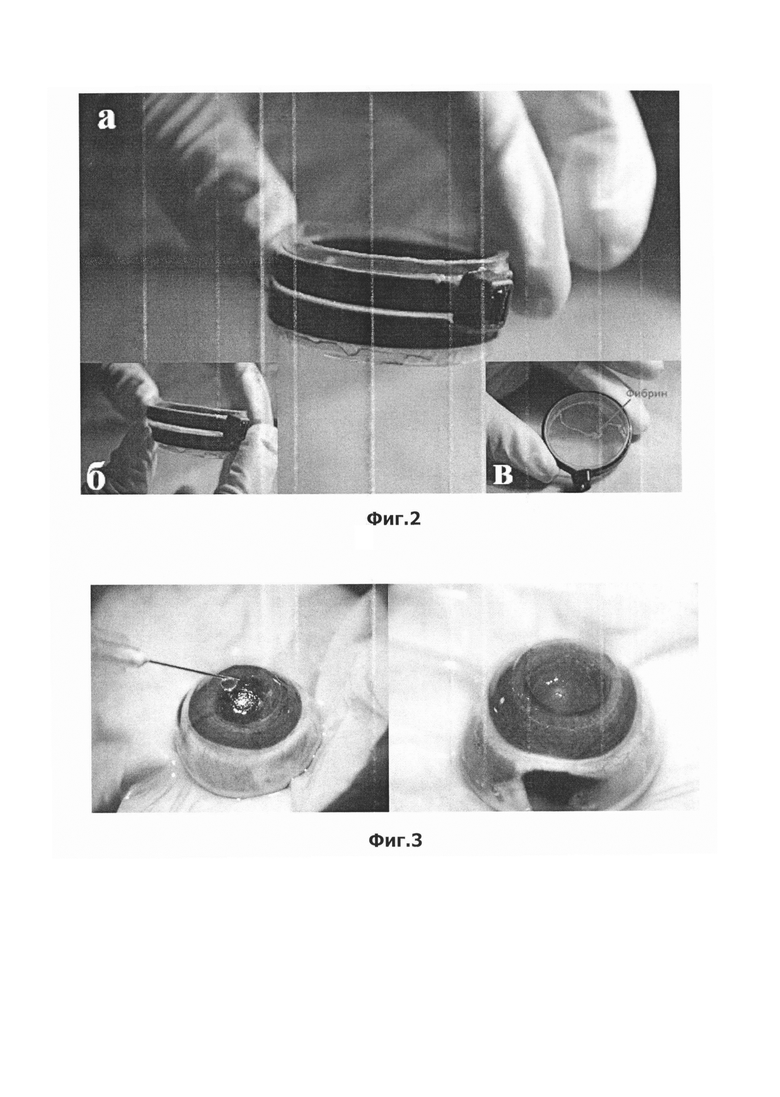
На фиг. 2 показана серия экспериментов in vitro с целью оценки адгезивных свойств. Произведена склейка амниотических мембран зажатых в устройстве для фиксации при помощи фибринового клея, полученного согласно предлагаемому способу (фиг. 2а). Спустя 1 минуту после склейки амниотических мембран при попытке их отрыва друг от друга визуально определяется четкая фиксация мембран между собой и ощущается сопротивление к разрыву (фиг. 2б). После разъединения мембран на одной из них визуализируется край фибриновой пленки (фиг. 2в).
На фиг. 3 показано апробирование in vivo на кроликах вклейки амниотической мембраны после поверхностной кератэктомии (проведена реконструкция Боуменовой мембраны). Этапы выполнения фиксации амниотической мембраны при помощи двухкомпонентного фибринового клея, полученного согласно предлагаемому способу, следующие. Заранее проводится заготовка 1 го и 2 го компонентов фибринового клея. Трепаном на дозированную глубину в 100-150 мкм выполняется поверхностная кератэктомия. На строму роговицы наносится половина объемов компонентов, смешанных в одном шприце. Сразу после этого производится выкройка амниотической мембраны необходимого диаметра, ее наложение на строму роговицы и экспозиция в течение 1 минуты. Далее на роговичную поверхность наносятся смешанные в одном шприце остаточные объемы компонентов полученного двухкомпонентного фибринового клея.
Техническим результатом является то, что приготовленный согласно предлагаемому способу (фиг. 1) двухкомпонентный аутофибриновый клей позволяет не только эффективно склеивать поврежденные ткани (фиг. 2, фиг. 3), обеспечивать качественный гемостаз и создавать условия для купирования воспаления в месте его нанесения, но и снизить стоимость приготовления двухкомпонентного фибринового клея и риск аллергической реакции.
Данный способ зарекомендовал себя как надежный и простой способ приготовления аутологичного фибринового клея.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОРГАНОСПЕЦИФИЧЕСКИЙ РЕГЕНЕРАНТ GI | 2011 |
|
RU2462255C1 |
| СПОСОБ ФИКСАЦИИ АУТОТРАНСПЛАНТАТА ПРИ МИРИНГОПЛАСТИКЕ | 2019 |
|
RU2708038C1 |
| Способ изготовления аутологичного фибрина с регулируемым содержанием фибриногена без использования экзогенного тромбина | 2020 |
|
RU2758260C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУХКОМПОНЕНТНОГО ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЯ СУСТАВОВ ПУТЕМ МАЛОИНВАЗИВНОГО ВВЕДЕНИЯ В СУСТАВНУЮ СУМКУ И ПРЕПАРАТ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2016 |
|
RU2638796C1 |
| ТКАНЕВАЯ КОМПОЗИЦИЯ ИЛИ АДГЕЗИВ, ПОЛУЧЕННЫЕ ИЗ КОМПОЗИЦИИ КРОВИ, СОДЕРЖАЩЕЙ ТРОМБОЦИТЫ, И СПОСОБ ПРИГОТОВЛЕНИЯ УКАЗАННОЙ КОМПОЗИЦИИ | 2020 |
|
RU2820448C2 |
| Способ получения обогащенного тромбоцитами фибринового матрикса с фиксированным в фибриновой сети остеозамещающим материалом или аутокрошкой из костной или хрящевой ткани | 2023 |
|
RU2802583C1 |
| СПОСОБ, ПРОБИРКА И УСТРОЙСТВО ДЛЯ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2011 |
|
RU2667964C1 |
| Способ получения обогащенного тромбоцитами фибринового матрикса различных форм и размеров | 2023 |
|
RU2811233C1 |
| СПОСОБ, ПРОБИРКА И УСТРОЙСТВО ДЛЯ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2011 |
|
RU2614722C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФИБРИНОВОГО КЛЕЯ ИЗ ДОНОРСКОЙ ПЛАЗМЫ И ЕГО ИДЕНТИФИКАЦИИ | 2023 |
|
RU2803272C2 |

Изобретение относится к медицине, в частности к способу приготовления аутологичного двухкомпонентного фибринового клея. Способ приготовления аутологичного двухкомпонентного фибринового клея, включающий забор крови в стерильные пробирки с цитратом натрия, центрифугирование плазмы крови, затем производят забор полученной обогащенной тромбоцитами плазмы, содержащей фибриноген, факторы свертывания крови в физиологических концентрациях и живые тромбоциты, продуцирующие различные факторы роста, и смешивают со вторым компонентом, содержащим раствор хлорида кальция и тромбин, при определенных условиях. Вышеописанный способ позволяет получить аутологичный двухкомпонентный фибриновый клей, обеспечивающий прочную и быструю адгезию. 3 ил.
Способ приготовления аутологичного двухкомпонентного фибринового клея, состоящего из аутологичной свежезабранной плазмы крови пациента, содержащей живые тромбоциты, фибриноген и факторы свертывания крови в физиологических концентрациях, включающий забор крови в стерильные пробирки с цитратом натрия 3.8%, центрифугирование плазмы крови, отличающийся тем, что забор венозной крови осуществляют в стерильную пробирку, позволяющую получить обогащенную тромбоцитами плазму, затем производят ее центрифугирование в течение 4 минут при 3500 об/мин, затем производят забор обогащенной тромбоцитами плазмы объемом 1.0 мл, содержащей фибриноген, факторы свертывания крови в физиологических концентрациях и живые тромбоциты, продуцирующие различные факторы роста, и смешивают со вторым компонентом, содержащим от 0.5 до 5.0% раствор хлорида кальция и тромбин в концентрации от 0.5 до 500 ME, рассчитываемой исходя из показателей фибриногена крови пациента и необходимого времени возникновения адгезии.
| СПОСОБ ПЛАСТИКИ ГЛАЗНЫХ ВЕК | 2012 |
|
RU2520829C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУХКОМПОНЕНТНОГО ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЯ СУСТАВОВ ПУТЕМ МАЛОИНВАЗИВНОГО ВВЕДЕНИЯ В СУСТАВНУЮ СУМКУ И ПРЕПАРАТ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2016 |
|
RU2638796C1 |
| ОРГАНОСПЕЦИФИЧЕСКИЙ РЕГЕНЕРАНТ GI | 2011 |
|
RU2462255C1 |
| US 4432347 A, 21.02.1984 | |||
| SLOMOVIC A.R | |||
| Новая методика использования фибринового клея для лечения конъюнктивохалазиса //Новое в офтальмологии | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| THOMAS C | |||
| SPOOR | |||
| ATLAS of OCULOPLASTIC and ORBITAL SURGERY | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
Авторы
Даты
2019-10-25—Публикация
2019-02-18—Подача