Область техники, к которой относится изобретение
Изобретение относится к области биотехнологии, а именно к выделению внеклеточных везикул (экзосом), секретируемых в культуральную среду клетками, зараженными вирусом гриппа А, методом хроматографии с использованием сорбента на основе гранул поперечносшитого полиакриламида.
Уровень техники
В настоящее время в области молекулярной биологии, цитологии и биотехнологии активно изучаются и применяются экзосомы. Экзосомы - это наноразмерные (30-150 нм) мембранные везикулы, которые секретируются практически всеми типами клеток и, как следствие, присутствуют практически во всех биологических жидкостях организма, например, показано присутствие экзосом в моче [1], слюне [2], крови [3], грудном молоке [4], амниотической [5] и бронхоальвеолярной [6] жидкостях. Известно, что данные наноразмерные частицы содержат в своем составе различные типы биомолекул, в том числе белки, липиды, углеводы, а также ДНК и РНК [7].
Отличительной особенностью экзосом является способность переносить функциональные белки и нуклеиновые кислоты между клетками, а также преодолевать различные биологические барьеры, что определяет одну из ключевых функций экзосом - участие в межклеточной коммуникации. При этом состав экзосом (набор и концентрация белков, РНК и других биологических молекул) может варьироваться в зависимости от физиологических или патологических процессов, происходящих внутри клеток [8]. Таким образом, изучение состава экзосом может в дальнейшем быть использовано при разработке диагностических маркеров различных патологических состояний.
Экзосомы играют важную роль в жизненном цикле различных вирусов. В частности, экзосомы помогают некоторым ускользать от иммунного ответа, способствуя распространению вирусной инфекции. Показана роль экзосом в жизненных циклах таких вирусов, как вирус простого герпеса [9], иммунодефицита человека [10], Эпштейна-Барр [11], гепатита A и C [12,13]. Однако, литература, посвященная изучению состава и роли экзосом в жизненном цикле вируса гриппа, весьма ограничена, что связано, по-видимому, с отсутствием протокола выделения экзосом, не контаминированных вирусными частицами, от клеток, зараженных вирусом гриппа. Это является следствием схожести физико-химических свойств экзосом и вирионов вируса гриппа (таких как плавучая плотность, размер, наличие хозяйских белков в составе частиц [14,15]), а также с продолжительностью одного цикла репликации вируса гриппа в клетках, которая в среднем составляет 8 часов, тогда как любые протоколы выделения экзосом предполагают их накопление в клеточной среде как минимум 24 часа [16].
Таким образом, в связи со значительным потенциалом экзосом в области современной диагностики и терапии, а также для улучшения понимания их роли в организме, в том числе при гриппозной инфекции, необходимо разработать способ выделения чистых экзосом, не содержащих вирусных частиц.
Известен способ выделения экзосом из внеклеточной среды с помощью ультрацентрифугирования клеточной среды [16,17], который состоит из двух этапов: 1) центрифугирование среды на низких скоростях (около 3000g для очистки среды от клеток и их обломков, а затем около 10000g для удаления внеклеточных везикул большого размера), при этом для последующих этапов используется надосадочная жидкость, а осадок отбрасывается; 2) ультрацентрифугирование среды на скорости 100000g для концентрирования экзосом. Однако, данный способ не может быть использован для разделения экзосом и вирусов гриппа и получения чистой фракции экзосом, поскольку объекты одного размера выделяются данным способом совместно, а известно, что размер экзосом составляет 30-150 нм [18], вирусов гриппа - около 100 нм.
Также известен способ выделения экзосом методом за счет специфического взаимодействия антител с поверхностными белками экзосом, то есть при помощи иммунноаффинной хроматографии [19]. В качестве неподвижной фазы используют магнитные или полимерные частицы, функционализированные специфическими антителами, чаще всего, к тетраспанинам (CD9, CD63 и CD81). Данный метод оказывается дорогостоящим из-за использования антител, в связи с чем его применение не оправдано для выделения экзосом из больших объемов биологического материала. При этом, для разделения экзосом и вирусов эта методика также не применима: биогенез экзосом и вируса гриппа является сходным, в связи с чем составы клеточных белков на поверхности экзосом и вирионов вируса гриппа также являются близкими, что не позволяет разделить их за счет различия в наборе поверхностных белков.
Также известен способ выделения экзосом при помощи гель-фильтрационной хроматографии. В данной методике исходная биологическая жидкость выступает в качестве подвижной фазы, а пористый гель-фильтрационный полимер - в качестве стационарной. Свойства стационарной фазы (например, диаметр пор) определяют скорость перемещения частиц разного размера в колонке: большие частицы выходят из колонки раньше, маленькие - позднее, за счет чего достигается разделение по размерам, то есть возможно отделить фракцию, соответствующую экзосомам по размерам. В качестве стационарной фазы используют сшитые декстраны (Sephadex), агарозу (Sepharose), полиакриламид (Biogel P) или аллилдекстран (Сефакрил) [20]. Описан способ выделения экзосом из клеточной методом гель-фильтрации с использованием сорбента Sephacryl S500HR (Sigma) [21], где на первом этапе проводят концентрирование образца (культуральной среды) методом тангенциальной фильтрации с использованием системы Akta flux (GE Healthcare) и фильтр MWCO (molecular weight cut-off) с размером пор 750 кДа, а на втором этапе проводят гель-фильтрацию с использованием хроматографа хроматограф Akta pure (GE Healthcare) и колонки, содержащей Sephacryl S500HR. Культуральная среда в процессе тангенциальной фильтрации переводилась в фосфатно-солевой буфер, pH 7.4, и после этого выступала в качестве подвижной фазы при хроматографии на колонке, предварительно уравновешенной фосфатно-солевым буфером. Элюцию проводили также фосфатно-солевым буфером, после чего собирали и объединяли фракции, соответствующие первому пику. Данные объединенные фракции содержали частицы, соответствующие по размерам и маркерным белкам экзосомам. Данный способ выделения экзосом из клеточной среды методом гель-фильтрации с использованием сорбента Sephacryl S500HR (Sigma) был принят за ближайший аналог.
Также известен способ выделения вариантов рекомбинантного нуклеопротеина вируса гриппа методами аффинной хроматографии на гепарин-сефарозе с последующей гель-хроматографией с использованием Sephacryl S300 [22], отличающийся тем, что Sephacryl S300 использовался как классический сорбент для фракционирования по гидродинамическому радиусу, а не для фракционирования за счет гидрофобного (либо какого-либо другого) взаимодействия, что не позволяет разделить экзосомы и частицы вируса гриппа.
Из вышеприведенных аналогов известно выделение экзосом из культуральной среды, а также известно использование метода гель-фильтрации, в том числе с использованием сорбента Sephacryl. При этом на сегодняшний день не известен способ выделения экзосом, продуцируемых зараженными вирусом гриппа А клетками, из культуральной среды, которая также содержит вирус гриппа, то есть не известен способ разделения экзосом и вирионов вирусов гриппа А.
Таким образом, техническая проблема состоит в необходимости разработки методики, позволяющей выделить экзосомы (не контаминированные вирусными частицами) из клеточной среды от зараженных вирусом гриппа клеток, которая содержит помимо экзосом также и вирионы вируса гриппа.
Раскрытие сущности изобретения
Технический результат состоит в обеспечении возможности выделения экзосом из клеточной среды и разделения их от вирионов вируса гриппа хроматографическим методом за счет гидрофобного взаимодействия экзосом с сорбентом на основе гранул поперечносшитого полиакриламида.
Технический результат достигается тем, что в способе хроматографической очистки экзосом и их разделения от вирионов вируса гриппа А на основе гидрофобного взаимодействия с сорбентом на основе гранул поперечносшитого полиакриламида, в ходе которого получают концентрированный образец из клеточной среды, содержащий экзосомы и вирусные частицы, добавляют в образец буфер для сорбции, осуществляют фильтрацию с использованием хроматографической колонки, упакованной сорбентом Sephacryl S-500HR, после чего осуществляют элюцию экзосом, согласно изобретению используют буфер, включающий 500 мМ хлорида натрия и 10 мМ фосфата натрия, а элюирование экзосом осуществляют деионизированной водой.
Краткое описание чертежей
Фиг. 1. Результаты электронной микроскопии образца, полученного после выделения из клеточной среды экзосом, секретируемых (А) контрольными клетками или (Б) зараженными вирусом гриппа А клетками. Стрелками на (А) отмечены экзосомы, стрелками на (Б) отмечены экзосомы и вирусы гриппа А. «Э» - экзосомы, «ВГ» - вирус гриппа.
Фиг. 2. Типичная хроматограмма образца, содержащего экзосомы. Красная линия - проводимость мСм/см; Фиолетовая линия - оптическая плотность на длине волны 280 нм. Стрелками отмечено начало элюции водой и начало выхода экзосом. Желтым и синим прямоугольниками обозначены фракции, объединенные под названиями «С» (солевая) и «В» (водная).
Фиг. 3. Результаты анализа фракций, полученных после хроматографии с сорбентом Сефакрил чистых экзосом, с использованием разных солевых буферов (Буфер 1, Буфер 2 и Буфер 3). (А) Дот-блоттинг с маркерными антителами экзосом (CD9 и MFG-E8). Красные стрелки указывают место, куда наносили образец. С - фракции после промывки солевым буфером, В - элюция водой, ПК - положительный контроль, Э - экзосомы, АТ - антитела. (Б) Просвечивающая электронная микроскопия водной фракции, полученной после сорбции экзосом в Буфере 3. Белыми стрелками отмечены экзосомы, длина масштабного отрезка составляет 200 нм.
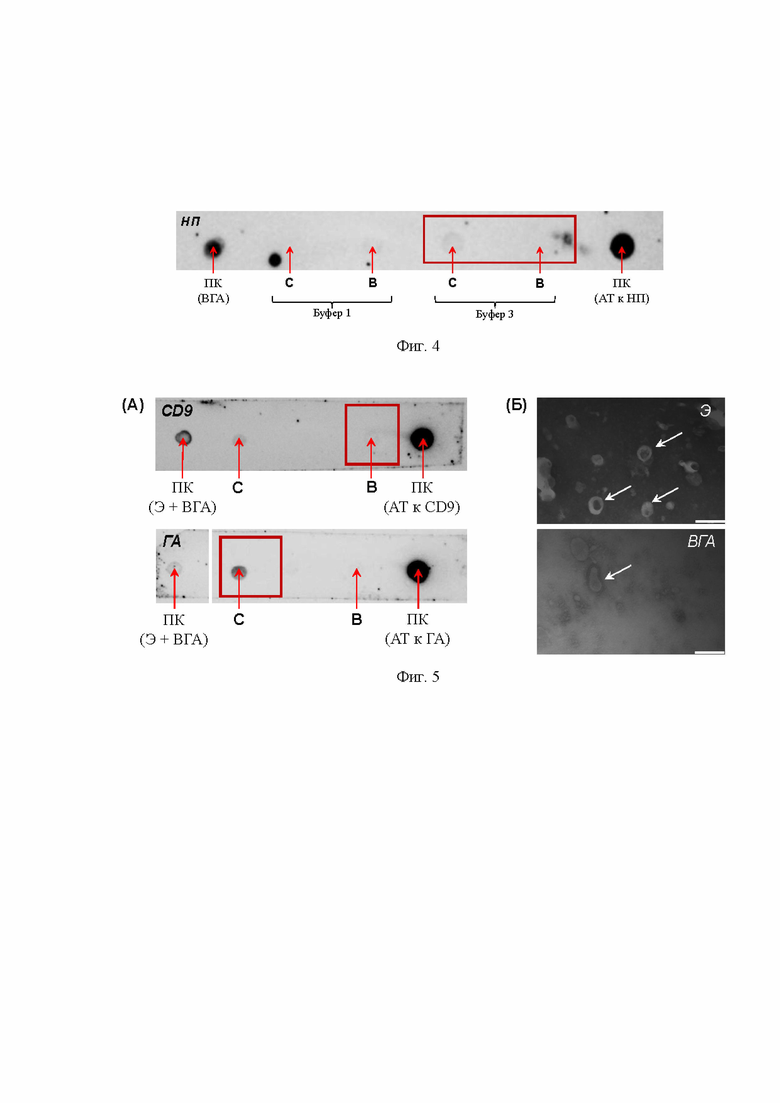
Фиг. 4. Результаты дот-блоттинга фракций, полученных после хроматографии с сорбентом Сефакрил чистых вирусов с использованием разных солевых буферов (Буфер 1 и Буфер 3), с антителами к нуклеопротеину (НП) вируса гриппа А (ВГА). Красные стрелки указывают место, куда наносили образец. С - фракции после промывки солевым буфером, В - элюция водой, ПК - положительный контроль, АТ - антитела.
Фиг. 5. Результаты анализа фракций, полученных после хроматографии с сорбентом Сефакрил смеси экзосом и вирусом с использованием Буфера 3. (А) Дот-блоттинг с маркерными антителами экзосом (CD9) и поверхностному белку гемагглютинину (ГА) вируса гриппа А (ВГА). Красные стрелки указывают место, куда наносили образец. С - фракции после промывки солевым буфером, В - элюция водой, ПК - положительный контроль, Э - экзосомы, АТ - антитела. (Б) Просвечивающая электронная микроскопия (сверху) водной фракции, полученной после сорбции экзосом в Буфере 3, и (снизу) солевой фракции. Белыми стрелками отмечены экзосомы (сверху) и вирусы гриппа А (снизу), длина масштабного отрезка составляет 200 нм.
Осуществление изобретения
Предложена методика, позволяющая разделить экзосомы и частицы вируса гриппа, при их выделении из клеточной среды от инфицированных вирусом гриппа клеток, которая состоит из следующих этапов:
1) Получение концентрированного образца из клеточной среды, содержащего экзосомы и вирусные частицы.
2) Добавление в образец буфера с высокой ионной силой (буфер для сорбции).
3) Уравновешивание хроматографической колонки, упакованной сорбентом Sephacryl S-500HR, буфером для сорбции.
4) Нанесение образца на колонку и промывка буфером для сорбции.
5) Элюирование экзосом деионизованной водой.
Первый этап - получение концентрированных образцов экзосом, секретируемых зараженными вирусом гриппа клетками, - проводится любым стандартным способом и не является предметом данного изобретения. В качестве исходного материала может быть использована клеточная среда, сыворотка или плазма крови, моча, бронхоальвеолярная или другая биологическая жидкость, содержащая экзосомы и частицы вируса гриппа. Концентрирование экзосом может быть проведено, например, последовательным центрифугированием клеточной среды, для очистки от обломков клеток и микровезикул, а затем концентрированием экзосом и вирусов при ультрацентрифугировании, а также методом тангенциальной фильтрации, или другими методами.
На втором этапе в образец, содержащий экзосомы, контаминированные вирионами вируса гриппа, добавляют буфер с высокой ионной силой (сорбционный буфер), который в дальнейшем при проведении хроматографии будет способствовать связыванию экзосом с сорбентом Сефакрил по гидрофобному принципу и тем самым обеспечит их удерживание на сорбенте. Вирионы вируса гриппа, в свою очередь, не способны связываться с сорбентом по гидрофобному принципу, поэтому их удерживания не произойдет. В качестве такого сорбционного буфера может быть использован, например, раствор 500 мМ хлорида натрия, 10 мМ фосфата натрия, рН 7.4 (конечная концентрация в образце). Таким образом, использование буфера с высокой ионной силой для подвижной фазы в процессе хроматографии отличает данный метод от известного метода выделения экзосом методом гель-фильтрационной хроматографии, а также определяет не только разделение по размерам в процессе хроматографии (как в случае использования стандартного буфера для гель-фильтрации, например, фосфатно-солевого буфера или исходной биологической жидкости в качестве подвижной фазы), но и по принципу гидрофобности, что обусловливает дальнейшее разделение экзосом и частиц вируса гриппа.
На третьем этапе хроматографическая колонка, упакованная сорбентом на основе гранул поперечносшитого полиакриламида, например, Sephacryl S500HR или S1000HR, предпочительней S500HR, уравновешивается сорбционным буфером, используемым на предыдущем этапе.
На четвертом этапе образец в сорбционном буфере наносят на колонку, после чего промывают сорбционным буфером. На данном этапе экзосомы связываются с сорбентом Сефакрил за счет гидрофобных взаимодействий и удерживаются. При этом вирионы вируса гриппа выходят из колонки в свободном объеме (образец А).
На пятом, заключительном, этапе колонка с сорбированными экзосомами промывается деионизованной водой, в результате чего экзосомы элюируются и выходят из колонки в водной фазе (образец Б).
Далее методика разделения экзосом и частиц вирусов гриппа, основанная на гидрофобном взаимодействии экзосом и сорбента Сефакрил, будет описана в виде примеров, которые предназначены для иллюстрирования изобретения и никоим образом не ограничивают его.
Заявляемое изобретение поясняется примерами.
Пример 1. Получение концентрированного образца, содержащего экзосомы и вирионы вируса гриппа.
Для накопления экзосом использовали клеточную линию А549 (ATCC, CCl-185, клетки человеческой карциномы легкого). Клеточную линию вели на культуральной среде (Питательной среде ДМЕМ, Биолот, Россия) с 10% бычей сывороткой (FBS, Biowest, США) и с добавлением антибиотика/антимикотика. Клетки вели на флаконах T300 (Nunc™ 300 cm2 Cell Culture Treated Flasks, Thermo Fisher, США). При достижении 90% клеточного монослоя, проводили заражение клеток вирусом гриппа A/Puerto Rico/8/1934 (H1N1) в инфекционной дозе 1 moi (один вирус на клетку). Плотность клеточного монослоя для заражения составляла 1.3*105 клеток/см2. На один флакон T300 одна инфекционная доза составила 3.9*107 TUD 50. После клетки отмывали от вируса фосфатно-солевым буфером, и добавляли среду без содержания бычей сыворотки. После инкубации в течение 24 часов при температуре +37°С в атмосфере 5% CO2 культуральную среду собирали и использовали для выделения экзосом.
Для получения контрольного образца (экзосомы, не содержащие вирусные частицы) на этапе достижения 90% монослоя клетки A549 не заражали, а переводили на среду, не содержащую бычью эмбриональную сыворотку, и инкубировали далее аналогично в течение 24 часов.
Для концентрирования экзосом культуральную среду центрифугировали на скорости 3000g в течение 30 минут при температуре +4°С на центрифуге Centrifuge 5810 R (Eppendorf), осадок удаляли. Собранную надосадочную жидкость повторно центрифугировали на скорости 10000g в течение 30 минут при температуре +4°С на центрифуге Optima XPN (Beckman Coulter), осадок удаляли. Собранную надосадочную жидкость центрифугировали на скорости 110000g в течение 2 часов при температуре +4°С на центрифуге Optima XPN (Beckman Coulter). Полученный осадок, содержащий экзосомы (контрольный образец, Фиг. 1А) или смесь экзосом и вирионов вируса гриппа (Фиг.1Б), ресуспендировали в фосфатно-солевом буфере.
Пример 2. Хроматография с сорбентом сефакрил чистых экзосом (контрольный образец) с использованием буферов с разной ионной силой
Для изучения связывания экзосом с сорбентом Сефакрил по гидрофобному принципу сравнивали три сорбционных буфера с разной ионной силой: Буфер 1) 100 мМ хлорид натрия, 10 мМ фосфат натрия, рН 7.4; Буфер 2) 250 мМ хлорид натрия, 10 мМ фосфат натрия, рН 7.4; Буфер 3) 500 мМ хлорид натрия, 10 мМ фосфат натрия, рН 7.4. Использовали хроматографическую систему AKTA pure 25 (GE Healthcare) при температуре +5°С, хроматографическую колонку объемом 5 мл (Biotoolomics), упакованную сорбентом Sephacryl S500HR. Уравновешивание системы проводили с помощью 10 мл буфера для сорбции со скоростью потока 1 мл/мин. Исследуемый препарат в объеме 1 мл вносили в колонку посредством инжекторной петли, после чего проводили промывку 15 мл буфера для сорбции, а затем элюцию 2 мл деионизированной воды (со скорость потока 0,25 мл/мин). Во время промывки и элюирования собирали фракции объемом по 0.5 мл. Типичная хроматограмма представлена на Фиг. 2. Для дальнейшего анализа фракции объединяли в солевую («С») и водную («В»). Полученные фракции анализировали методами просвечивающей электронной микроскопии (для подтверждения формы и размера полученных частиц) и дот-блоттинга (для подтверждения наличия маркерных белков).
Дот-блоттинг проводили с антителами к маркерным белкам экзосом (CD9, MFG-E8). Из результатов дот-блоттинга (Фиг. 3А) видно, что с увеличением ионной силы буфера количество экзосом, сорбировавшихся на колонке, увеличивается, поскольку точки, соответствующие водным фракциям («В»), обладают большей интенсивностью, чем точки, соответствующие солевым фракциям («С»). Наибольшее различие наблюдается для Буфера 3, содержащего наибольшую концентрация хлорида натрия. Методом просвечивающей электронной микроскопии было показано, что водная фракция, полученная после сорбции экзосом в Буфере 3, содержит экзосомы (Фиг. 3Б), поскольку наблюдаются чашевидные частицы размером около 80-100 нм. Таким образом, было показано, что экзосомы присутствуют преимущественно в водных фракциях, причем с увеличением ионной силы раствора наблюдается увеличение концентрации экзосом в водной фракции, максимальный эффект достигается при использовании Буфера 3.
Пример 3. Хроматография с сорбентом сефакрил вируса гриппа с использованием буферов с разной ионной силой
Хроматографию с образцом, содержащим только вирус гриппа A/Puerto Rico/8/1934 (H1N1), проводили аналогично Примеру 2 с использованием Буфера 1 и Буфера 3. Сбор и объединение фракций проводили также аналогичным образом. Для детекции вируса был проведен дот-блоттинг со структурным белком вируса гриппа - нуклеопротеином (Фиг. 4). Показано, что нуклеопротеин присутствует в солевой фракции при использовании Буфера 3, то есть не связывается с Сефакрилом в буфере с высокой ионной силой, в отличии от экзосом.
Пример 4. Хроматография с сорбентом сефакрил смеси экзосом и вируса гриппа с использованием буфера с высокой ионной силой
Смесь экзосом и вируса гриппа была получена, как описано в Примере 1. Хроматографию, сбор и объединение фракций проводили аналогично Примеру 2 с использованием Буфера 3. Для детекции маркерных белков экзосом методом дот-блоттинга использовали антитела к CD9, а для детекции вируса гриппа А использовали антитела к поверхностному белку вируса гриппа гемагглютинину. По результатам дот-блоттинга с антителами к гемагглютинину можно заключить, что вирус гриппа присутствует в солевой фракции («С») и отсутствует в водной («В»), при этом маркерный белок экзосом CD9 (Фиг. 5А) обнаруживается как в водной фракции, так и в солевой, что указывает на присутствие экзосом в водной фракции, а также на наличие белка CD9 в структуре вириона вируса гриппа, что ранее было описано в литературе [15]. Полученные фракции также анализировали методом просвечивающей электронной микроскопии для подтверждения формы и размера полученных частиц (Фиг. 5Б). Было показано присутствие экзосом в водной фракции и вирусов гриппа - в солевой. Таким образом, использование буфера с высокой ионной силой (содержащего 500 мМ хлорида натрия) позволяет разделить экзосомы и вирусные частицы за счет взаимодействия экзосом с сорбентом Сефакрилом по гидрофобному принципу.
Источники информации
1. Conde-Vancells J. et al. Candidate biomarkers in exosome-like vesicles purified from rat and mouse urine samples // PROTEOMICS - Clin. Appl. Proteomics Clin Appl, 2010. Vol. 4, №4. P. 416-425.
2. Michael A. et al. Exosomes from human saliva as a source of microRNA biomarkers // Oral Dis. Oral Dis, 2010. Vol. 16, № 1. P. 34-38.
3. Caby M.-P. et al. Exosomal-like vesicles are present in human blood plasma // Int. Immunol. Oxford Academic, 2005. Vol. 17, №7. P. 879-887.
4. Admyre C. et al. Exosomes with Immune Modulatory Features Are Present in Human Breast Milk // J. Immunol. American Association of Immunologists, 2007. Vol. 179, №3. P. 1969-1978.
5. Keller S. et al. CD24 is a marker of exosomes secreted into urine and amniotic fluid // Kidney Int. Elsevier, 2007. Vol. 72, №9. P. 1095-1102.
6. Prado N. et al. Exosomes from Bronchoalveolar Fluid of Tolerized Mice Prevent Allergic Reaction // J. Immunol. American Association of Immunologists, 2008. Vol. 181, №2. P. 1519-1525.
7. Chahar H.S. et al. Respiratory Syncytial Virus Infection Changes Cargo Composition of Exosome Released from Airway Epithelial Cells // Sci. Rep. Nature Publishing Group, 2018. Vol. 8, №1. P. 387.
8. Familtseva A., Jeremic N., Tyagi S.C. Exosomes: cell-created drug delivery systems // Mol. Cell. Biochem. Springer, 2019. Vol. 459, №1-2. P. 1-6.
9. Kharkwal H., Smith C.G., Wilson D.W. Herpes Simplex Virus Capsid Localization to ESCRT-VPS4 Complexes in the Presence and Absence of the Large Tegument Protein UL36p // J. Virol. / ed. Sandri-Goldin R.M. American Society for Microbiology, 2016. Vol. 90, №16. P. 7257-7267.
10. Votteler J., Sundquist W.I. Virus Budding and the ESCRT Pathway // Cell Host Microbe. Cell Press, 2013. Vol. 14, №3. P. 232-241.
11. Flanagan J., Middeldorp J., Sculley T. Localization of the Epstein-Barr virus protein LMP 1 to exosomes // J. Gen. Virol. Microbiology Society, 2003. Vol. 84, № . P. 1871-1879.
12. Jiang W. et al. Hepatitis A virus structural protein pX interacts with ALIX and promotes the secretion of virions and foreign proteins through exosome like vesicles // J. Extracell. Vesicles. J Extracell Vesicles, 2020. Vol. 9, №1. P. 1716513.
13. Zhang J. et al. CD81 Is Required for Hepatitis C Virus Glycoprotein-Mediated Viral Infection // J. Virol. J Virol, 2004. Vol. 78, №3. P. 1448-1455.
14. Cantin R. et al. Discrimination between exosomes and HIV-1: Purification of both vesicles from cell-free supernatants // J. Immunol. Methods. Elsevier, 2008. Vol. 338, №1-2. P. 21-30.
15. Hutchinson E.C. et al. Conserved and host-specific features of influenza virion architecture // Nat. Commun. Nature Publishing Group, 2014. Vol. 5. P. 4816.
16. Théry C. et al. Isolation and Characterization of Exosomes from Cell Culture Supernatants and Biological Fluids // Curr. Protoc. Cell Biol. 2006. Vol. 30, №1. P. 3.22.1-3.22.29.
17. Johnstone R.M. The Jeanne Manery-Fisher Memorial Lecture 1991. Maturation of reticulocytes: formation of exosomes as a mechanism for shedding membrane proteins // Biochem. Cell Biol. Biochem Cell Biol, 1992. Vol. 70, №3-4. P. 179-190.
18. Kowal J., Tkach M., Théry C. Biogenesis and secretion of exosomes // Curr. Opin. Cell Biol. Elsevier Current Trends, 2014. Vol. 29, №1. P. 116-125.
19. Zhang Y. et al. Exosome: A Review of Its Classification, Isolation Techniques, Storage, Diagnostic and Targeted Therapy Applications // Int. J. Nanomedicine. Dove Press, 2020. Vol. Volume 15. P. 6917-6934.
20. Sidhom K., Obi P.O., Saleem A. A Review of Exosomal Isolation Methods: Is Size Exclusion Chromatography the Best Option? // Int. J. Mol. Sci. Int J Mol Sci, 2020. Vol. 21, №18. P. 1-19.
21. Горшков А.Н. et al. Сравнительный анализ методов выделения экзосом из культуральной среды // Цитология. 2021. Vol. 63, №2. P. 193-204.
22. ДЕЛЬ КАМПО АСКАРАТЕЙЛЬ Жюдит, ИЛЛЬ Фергаль. Вакцины на основе нуклеопротеина вируса гриппа. Патент на изобретение RU 2662667 C2. Заявка от 18.03.2014. Опубликовано: 26.07.2018 Бюл. № 21.
| название | год | авторы | номер документа |
|---|---|---|---|
| Композиция на основе пептида, подавляющего репликацию вируса гриппа А | 2018 |
|
RU2695336C1 |
| Способ выделения вирусных нуклеиновых кислот из различных фракций экстраклеточных везикул | 2018 |
|
RU2696075C2 |
| ЭКЗОСОМЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ВАКЦИНЫ | 2016 |
|
RU2763524C2 |
| Штамм бактерий Escherichia coli - продуцент рекомбинантного белка NS1 | 2021 |
|
RU2789735C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЭКЗОСОМ ИЗ ПЛАЗМЫ КРОВИ | 2020 |
|
RU2741638C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОСТАВА ИНДИВИДУАЛЬНЫХ ВНЕКЛЕТОЧНЫХ ВЕЗИКУЛ В КРОВИ ЧЕЛОВЕКА | 2014 |
|
RU2583940C1 |
| Моноклональное антитело, специфичное к вирусу Эбола | 2018 |
|
RU2705763C1 |
| Биологический микрочип для обнаружения опухолевых экзосом в сыворотке крови человека для диагностики колоректального рака | 2016 |
|
RU2682721C2 |
| Штамм бактерий Escherichia Coli - продуцент рекомбинантного внеклеточного домена белка GP | 2018 |
|
RU2701337C1 |
| Способ получения рекомбинантного фолликулостимулирующего гормона человека, клеточная линия - продуцент и плазмидные экспрессионные векторы | 2019 |
|
RU2697273C1 |

Изобретение относится к биохимии. Описан способ хроматографической очистки экзосом и их разделения от вирионов вируса гриппа А на основе гидрофобного взаимодействия с сорбентом на основе гранул поперечносшитого полиакриламида. Получают концентрированный образец из клеточной среды, содержащий экзосомы и вирусные частицы. Добавляют в образец буфер для сорбции. Осуществляют хроматографическое разделение с использованием колонки, упакованной сорбентом Sephacryl S-500HR. После чего осуществляют элюцию экзосом. При этом используют буфер, включающий 500 мМ хлорида натрия и 10 мМ фосфата натрия, а элюирование экзосом осуществляют деионизированной водой. Технический результат состоит в обеспечении возможности выделения экзосом из клеточной среды и разделения их от вирионов вируса гриппа хроматографическим методом за счет гидрофобного взаимодействия экзосом с сорбентом на основе гранул поперечносшитого полиакриламида. 5 ил., 4 пр.
Способ хроматографической очистки экзосом и их разделения от вирионов вируса гриппа А на основе гидрофобного взаимодействия с сорбентом на основе гранул поперечносшитого полиакриламида, в ходе которого получают концентрированный образец из клеточной среды, содержащий экзосомы и вирусные частицы, добавляют в образец буфер для сорбции, осуществляют хроматографическое разделение с использованием колонки, упакованной сорбентом Sephacryl S-500HR, после чего осуществляют элюцию экзосом, отличающийся тем, что используют буфер, включающий 500 мМ хлорида натрия и 10 мМ фосфата натрия, а элюирование экзосом осуществляют деионизированной водой.
| НОВЫЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ И ОХАРАКТЕРИЗОВАНИЯ МИКРОВЕЗИКУЛ В ЖИДКОСТЯХ ОРГАНИЗМА ЧЕЛОВЕКА | 2009 |
|
RU2520741C2 |
| EP 3181705 A1, 21.06.2017 | |||
| Забродская Я.А., Шалджян А.А | |||
| и др., МЕТОДИЧЕСКИЕ ОСНОВЫ ВЫДЕЛЕНИЯ ЭКЗОСОМ ИЗ КУЛЬТУРАЛЬНОЙ СРЕДЫ, СОДЕРЖАЩЕЙ ВИРУС ГРИППА, Научно-практическая конференция-биеннале "Грипп: вирусология, эпидемиология, профилактика и лечение" Санкт-Петербург, 22-23 октября 2014 года, стр.41. | |||
Авторы
Даты
2023-09-21—Публикация
2022-12-07—Подача