Изобретение относится к медицине и может быть использовано в кардиологии, терапии, кардиохирургии, реабилитологии для повышения качества прогнозирования прогрессирования хронической сердечной недостаточности c сохраненной фракцией выброса (ХСНсФВ) у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения.
Исследования последних 10 лет показали, что ХСНсФВ становится все более превалирующей формой сердечной недостаточности, распространенность которой за указанный срок, по сравнению с ХСН со сниженной ФВ, увеличилась в среднем на 10-20% [1]. Во многом это обусловлено тем, что в настоящее время ни для одного класса препаратов не доказана способность достоверно снижать смертность и заболеваемость при ХСНсФВ [2], что, в свою очередь, связано с отсутствием единого взгляда на механизмы формирования данной патологии [3].
Известно, что окклюзирующее поражение коронарных артерий (КА) является одним из пусковых механизмов формирования и прогрессирования ХСНсФВ. Однако в последнее время появились данные, свидетельствующие о том, что пациенты с необструктивным атеросклерозом КА, несмотря на сохраненную ФВ ЛЖ, более подвержены госпитализации по причине декомпенсации ХСН [4]. Недавно была предложена новая инновационная теория развития и прогрессирования ХСНсФВ, в частности у больных с неокклюзирующим атеросклерозом КА, в основе которой лежит поражение коронарного микрососудистого русла [5]. Установлено, что у 53% пациентов с необструктивным поражением КА и ангинозными болями выявляются признаки стресс-индуцируемой ишемии миокарда [6]. Согласно данным мета-анализа 56 исследований с участием 14 427 пациентов, доля пациентов с поражением коронарного микрососудистого русла в общей популяции составляла 41%, а у пациентов с ХСНсФВ распространенность возрастала до 75-85% [7].
Признанным методом визуализации микрососудистой дисфункции венечного кровообращения является позитронная эмиссионная томография (ПЭТ) [8]. Однако на данный момент использование ПЭТ для оценки абсолютных показателей перфузии миокарда не нашло широкого применения в клинической практике ввиду сложности и высокой стоимости процедур. Другим методом определения абсолютных показателей перфузии является динамическая однофотонная эмиссионная томография (ОФЭКТ) миокарда [9]. Эта методика появилась относительно недавно, с появлением нового класса гамма-камер, оснащенных полупроводниковыми кадмий-цинк-теллуровыми детекторами (Cadmium-Zinc-Telluride, CZT), которые позволяют количественно определять резерв миокардиального кровотока (MFR) и миокардиальный кровоток посредством динамической визуализации с хорошей точностью и корреляцией. При этом метод, наравне с ПЭТ, в достаточной степени апробирован и валидизирован, а также является более доступным методом визуализации микроциркуляторных изменений коронарного русла [10].
Новым инструментом для неинвазивной идентификации широкого спектра биологических процессов, протекающих в ткани органа при развитии заболевания еще до проявления значимых анатомических особенностей или развития осложнений, в частности, при атерогенезе, становятся методы молекулярной визуализации [11]. Использование молекулярных биомаркеров как компонента стратегии комбинированной визуализации, с учетом данных ПЭТ или ОФЭКТ, может повысить эффективность диагностики, предоставив дополнительную информацию, относящуюся к морфологии и функции, которая важна для дальнейшего клинического ведения пациентов [12]. Этим обусловлен выбор метода для разработки способа неинвазивного прогнозирования прогрессирования хронической сердечной недостаточности с сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий.
Известен способ неинвазивной ранней диагностики поражения коронарного микрососудистого русла у пациентов с необструктивным атеросклерозом коронарных артерий. В сыворотке крови больных после выявления необструктивного атеросклеротического поражения коронарных артерий определяют концентрацию растворимого ST2 посредством иммуноферментного анализа. При значении уровня растворимого ST2 31,304 нг/мл и более диагностируют поражение коронарного микрососудистого русла [13]. Однако с помощью данного способа у пациентов с необструктивным атеросклерозом коронарных артерий диагностируется непосредственно поражение коронарного микрососудистого русла, но не характер течения развившейся ХСНсФВ.
В проанализированной патентной и научной медицинской литературе адекватного прототипа не обнаружено.
Задача изобретения - создание способа прогнозирования прогрессирования хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения. Поставленная задача решается путем определения NT-proBNP в сыворотке крови посредством иммуноферментного метода и MFR с помощью динамической однофотонной эмиссионной томографии миокарда сразу после установления диагноза ХСНсФВ. При значениях NT-proBNP 760,5 пг/мл и более и MFR 1,62 и менее прогнозируют высокий риск прогрессирования хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения (AUC 0,935; чувствительность 90,1%, специфичность 87,5%; p<0,001).
Новым в предлагаемом способе является то, что для оценки риска прогрессирования ХСНсФВ у больных с необструктивным атеросклерозом коронарных артерий с помощью иммуноферментного метода определяют в сыворотке крови уровни NT-proBNP и с помощью динамической однофотонной эмиссионной томографии сердца оценивают величину MFR.
В настоящее время наиболее признанная гипотеза о патогенезе ХСНсФВ дает основание считать, что сопутствующие заболевания, такие как метаболический синдром, ожирение, артериальная гипертония, сахарный диабет, хроническая болезнь почек и т.д., могут инициировать системную воспалительную реакцию, которая способствует развитию оксидативного стресса в эндотелиальных клетках, ухудшению их функции и снижению биодоступности оксида азота либо за счет непосредственного воздействия, либо гиперэкспресии эндотелина-1 [4]. Эндотелий играет ключевую роль в предотвращении агрегации тромбоцитов и адгезии лейкоцитов, регулировании пролиферации клеток и модулировании сосудистого тонуса путем синтеза и высвобождения эндотелиальных вазодилатирующих компонентов, включая простагландины, оксид азота и эндотелий-зависимые факторы гиперполяризации. Таким образом, с одной стороны, нарушения как в миоцитарном, так и немиоцитарном компартаментах эндотелия на фоне хронического системного воспаления вызывает адгезию и инфильтрацию моноцитов и стимуляцию интегрированных макрофагов, что приводит к дифференцировке миофибробластов и, в конечном итоге, секреции коллагена и, как следствие, развитию миокардиального фиброза, повышенной ригидности, диастолической дисфункции и, как следствие, развитию ХСНсФВ [7]. Это говорит о том, что факторы, склоняющие чашу весов в сторону повреждения кардиомиоцитов, могут ухудшать миокардиальную механику и повышать риск прогрессирования ХСНсФВ даже при необструктивном поражении КА. Сочетание одного из динамических показателей ОФЭКТ резерва миокардиального кровотока, отражающего поражение микроциркуляторного русла, с биомаркером объемной перегрузки - NT-proBNP - свидетельствует о более тесной связи между этими процессами, что, в частности, подтверждает патогенез развития ХСНсФВ [5].
Преимуществом предлагаемого изобретения является повышение эффективности прогнозирования прогрессирования социально значимого заболевания, что дает возможность:
- прогнозировать прогрессирование ХСНсФВ на ранних стадиях и назначить патогенетическую, оптимально персонифицированную терапию, направленную на восстановление коронарного кровотока и метаболизма миокарда;
- выделить приоритетную группу больных с необструктивным поражением коронарных артерий и повышенным риском прогрессирования хронической сердечной недостаточности для диспансерного наблюдения и оптимизации целевых профилактических мероприятий, направленных на предотвращение исключительно высокой преждевременной смертности населения;
- снизить большие финансовые затраты здравоохранения, связанные с дорогостоящим лечением широко распространенной патологии трудоспособного населения государства.
Существенные признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не очевидные для специалиста. Идентичной совокупности признаков в проанализированной литературе не обнаружено. Предлагаемое изобретение может быть использовано в здравоохранении.
Исходя из вышеизложенного, следует считать изобретение соответствующим условиям патентоспособности “Новизна”, “Изобретательский уровень”, “Промышленная применимость”.
Изобретение будет понятно из следующего описания и приложенных к нему фигур.
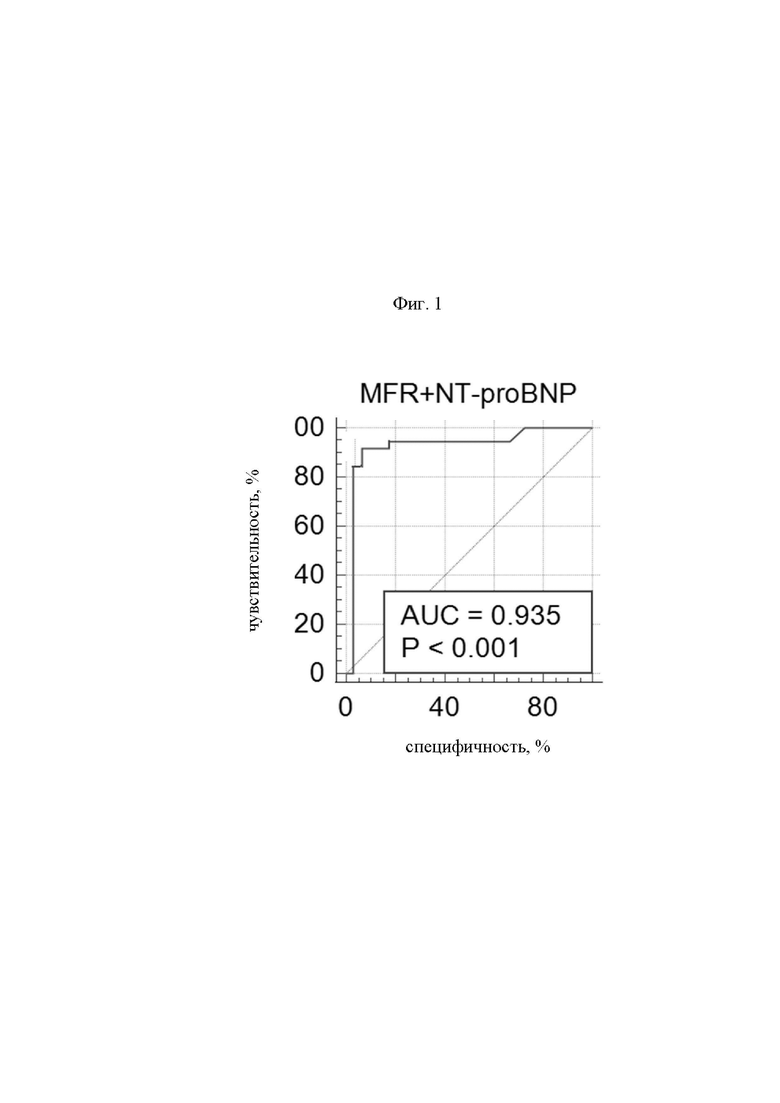
На фиг. 1 представлены результаты ROC-анализа. Изображена ROC-кривая характеристик чувствительности и специфичности NT-proBNP и MFR в оценке риска прогрессирования у пациентов с необструктивным атеросклерозом коронарных артерий: по оси ординат - частота (%) истинно положительных результатов (чувствительность), по оси абсцисс - частота (%) ложноположительных результатов (100 минус специфичность). По данным анализа следует, что «точкой отсечения» - cut off, характеризующей риск прогрессирования ХСНсФВ является уровень NT-proBNP равно и более 760,5 пг/мл и уровень MFR равно и менее 1,62 (AUC 0,935; чувствительность 90,1%, специфичность 87,5%; p<0,001) (фиг. 1).
Способ осуществляют следующим образом:
Cразу после установления диагноза ХСНсФВ у пациентов с необструктивным атеросклерозом коронарных артерий в сыворотке крови определяют содержание NT-proBNP и проводят динамическую ОФЭКТ.
Определение уровня NT-proBNP в сыворотке крови проводят методом иммуноферментного твердофазного анализа (ELISA), используется коммерческий набор Biomedica, Австрия.
Используемый материал: для теста Biomedica используют образцы сыворотки человека, полученные из периферической венозной крови, забранной из локтевой вены утром, натощак в вакуумные системы для забора крови.
Сбор и хранение образцов: центрифугирование и отделение сыворотки или плазмы от форменных элементов крови проводят в течение 4-х часов с момента забора крови. Для получения сыворотки или плазмы периферическую кровь центрифугируют при 3000 об/мин в течение 10 минут. Аликвоты образцов хранят при - 24°C.
Подготовка к проведению динамической ОФЭКТ включает в себя отмену приема бета-адреноблокаторов, нитратов, антагонистов кальциевых каналов за 24 часов, производных метилксантина (чай, кофе, шоколад) за 24 часа до проведения фармакологической пробы.
Исследование выполняют в утренние часы, натощак, по двухдневному протоколу «покой-нагрузка». В первый день проводят исследование в состояние функционального покоя. Пациент размещается лежа на спине под детектором гамма-камеры, левая рука за головой. В правую руку пациента устанавливают периферический внутривенный катетер. Для точного позиционирования левого желудочка в центре поля зрения детекторов проводят бесконтрастную компьютерную томографию области сердца (лучевая нагрузка 0,25 мЗв). Затем начинают запись сцинтиграфического исследования. Через 5 с через катетер болюсно вводят 99mTc-МИБИ (метокси-изобутил-изотнитрил) в дозе 260-444 МБк в объеме 5 мл со скоростью 1 мл/с, непосредственно, после чего вводят раствор NaCl 0,9% в объеме 30 мл со скоростью 2 мл/с. Регистрацию сцинтиграфических изображений проводят в течение 10 минут в томографическом ЭКГ-синхронизированном режиме (16 кадров на сердечный цикл). Общая продолжительность исследования (с укладкой пациента) - 20 минут. Через 60 минут выполняют стандартную ЭКГ-синхронизированную перфузионную сцинтиграфию миокарда (ПСМ).
Во второй день проводят исследование в условиях нагрузочной пробы (фармакологический стресс-тест). Пациент размещается лежа на спине под детектором гамма-камеры, левая рука за головой. В правую и левую руки пациента устанавливают по одному периферическому внутривенному катетеру. Для точного позиционирования левого желудочка в центре поля зрения детекторов проводят бесконтрастную компьютерную томографию области сердца (лучевая нагрузка 0,25 мЗв). Для выполнения исследования используют стресс-агент аденозинтрифосфат (АТФ), который вводят внутривенно в левую руку при помощи инфузомата в дозировке 160 мкг/кг/мин в течение четырех минут. На второй минуте начинают запись сцинтиграфических изображений и вводят в катетер в правой руке болюсно 99mTc-МИБИ в дозе 260-444 МБк в объеме 5 мл со скоростью 1 мл/с, после чего вводят раствор NaCl 0,9% в объеме 30 мл со скоростью 2 мл/с. Исследование проводят под контролем частоты сердечных сокращений, артериального давления, электрокардиограммы. Регистрацию сцинтиграфических изображений проводят в течение 10 минут в томографическом ЭКГ-синхронизированном режиме (16 кадров на сердечный цикл). Общая продолжительность исследования (с укладкой пациента) - 20 минут. Через 60 минут выполняют стандартную ЭКГ-синхронизированную ПСМ.
Все исследования выполняют на гибридном компьютерном томографе Discovery NM/CT 570с (GE Healthcare, Milwaukee, WI, USA), оснащенном гамма-камерой с высокочувствительными полупроводниковыми кадмий-цинк-теллуровыми детекторами (Cadmium-Zinc-Telluride, CZT). Сцинтиграфические изображения записывают с использованием низкоэнергетического мульти-пинхол коллиматора в 19 проекциях в матрицу 32×32 пикселя (2,46х2,46 мм). Центр энергетического окна устанавливают на фотопик 99mTc 140 кЭв; ширина энергетического окна симметрична и составляет 20%.
Полученные сцинтиграфические изображения обрабатывают на специализированной рабочей станции Xeleris II (GE Healthcare, Haifa, Israel). Оценку миокардиальной перфузии, кровотока и резерва осуществляют с использованием специализированного программного обеспечения Corridor 4DM SPECT и 4DM Reserve v.2015 (INVIA, Ann Arbor, MI, USA).
По данным динамической однофотонной эмиссионной компьютерной томографии миокарда определяют величины коронарного кровотока на фоне фармакологического стресс-теста и в условиях покоя, и далее определяют глобальный резерв коронарного кровотока (как отношение кровотока в покое к кровотоку на нагрузке.
Для определения количественных показателей перфузии миокарда - расчета резерва коронарного кровотока (MFR) на основе нативных данных прохождения болюса радиофармацевтического препарата по полостям и ткани миокарда левого желудочка строят кривые активность-время. На основании полученных кривых и модели кровотока Net Retention (1) рассчитывают индекс накопления радионуклидного индикатора тканью миокарда -R [14]:
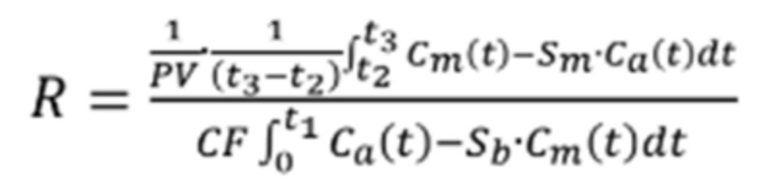
В последующем с помощью уравнения Renkin-Crone рассчитывают величину миокардиального кровотока (MBF) [Klein. 2010]:
R=MBF (1-0,874*e-0,443/MBF)
Расчет резерва коронарного кровотока выполняют по формуле:
MFR = stress-MBF/rest - MBF,
где stress-MBF - величина миокардиального кровотока на фоне фармакологического стресс-теста, (мл/мин/г); rest-MBF - величина миокардиального кровотока в условиях покоя, (мл/мин/г).
В исследование включено 59 пациентов с необструктивным поражением КА и СНсФВ (ФВЛЖ 62 [58; 66]%). Исследование было проведено в соответствии с положением Хельсинкской декларации и одобрено локальным Этическим комитетом Научно-исследовательского института кардиологии, Томского национального исследовательского медицинского центра Российской академии наук (протокол №177 от 30.10.2018 г.). Информированное письменное согласие было получено от всех пациентов до включения в исследование. На каждого больного заполнялась специально разработанная клиническая карта.
Всем включенным в исследование пациентам проводили тест 6-минутной ходьбы (ТШХ), спирометрию для исключения патологии легочной системы как проявление одышки. Эхокардиографию (ЭхоКГ) с оценкой параметров диастолической дисфункции выполняли на аппарате EPIQ (Philips Ultrasound, Inc., США).
Всем пациентам была выполнена коронарная компьютерная томографическая ангиография для верификации атеросклероза и оценки степени стенозирования коронарных артерий. Для сканирования с контрастным усилением 70-90 мл неионогенного контрастного вещества (йопамидол 370 мг, Bracco Diagnostics, Италия) вводили внутривенно через кубитальный катетер 18G со скоростью потока 5-5,5 мл/с.
Статистическая обработка результатов проводилась с использованием пакета статистических программ STATISTICA (StatSoft, Inc.) и MedCalc 11.5.0.0. Количественные переменные определяли в виде медианы (Ме), а также 25-го и 75-го квартилей (25Q и 75Q). Для проверки статистических гипотез при сравнении 2-х независимых групп использовали критерий Манна-Уитни. При анализе качественных признаков проводили анализ таблиц сопряженности с использованием критерия X2 Пирсона. Если имелись ячейки с ожидаемой частотой меньше 5, то применяли двусторонний точный критерий Фишера или поправку Йетса (для таблиц 2х2). Для определения уровней NT-proBNP и MFR в качестве прогностических маркеров прогрессирования ХСНсФВ использовали ROC-анализ с расчетом площади под кривой (AUC). Критический уровень значимости p-value для всех используемых процедур статистического анализа принимали равным 0,05.
Через 12 месяцев наблюдения пациенты ретроспективно были разделены на 2 группы: в группу 1 (n=11) вошли больные с неблагоприятным течением ХСНсФВ, в группу 2 (n=47) - с благоприятным. По основным клинико-демографическим характеристикам группы были сопоставимы, кроме значений натрийуретического пептида (р<0,001). В группе 1 уровень NT-proBNP был выше в 3,8 раз, чем в группе 2 (284,5 [183,42; 716,73] и 1071,4 [272,4; 2168,1] пг/мл, соответственно), а значения MFR были ниже в группе 1 на 45,4% (p<0,001), чем в группе 2 (1,19 [0,86; 1,55] vs. 2,18 [1,7; 2,55], соответственно) (Таблица 1).
Неблагоприятное течение
n=11
Благоприятное течение
n=48
При анализе данных установлено, уровни MFR ≤1,62 (AUC=0,827; чувствительность 84,2%, специфичность 75,9%; p<0,001) и NT-proBNP ≥760,5 пг/мл (AUC=0,708; чувствительность 63,6%, специфичность 82,1%; p=0,040) можно рассматривать в качестве маркеров неблагоприятных исходов. При этом комбинированное определение NT-proBNP с MFR обладало большей значимостью (AUC 0,935; чувствительность 90,1%, специфичность 87,5%; p<0,001) в стратификации риска по сравнению с мономаркерной моделью.
ПРИМЕР 1: Пациент Л. (мужчина, 53 года)
Жалобы на одышку смешанного характера при умеренных нагрузках - подъем на 2 этаж, ходьбе по прямой до 200-300 метров. Принимает кардиомагнил 75 мг/сут., аторвастатин 40 мг/сутки, периндоприл 5 мг/сутки. ИМТ 28,7 кг/м2. Стаж артериальной гипертензии - 2 года, ИБС - 6 мес.
При объективном исследовании: пульс 71 уд/мин., АД 120/70 мм рт. ст., частота дыхания 14 в минуту, отеков нет.
ЭКГ: ритм синусовый, изменений не выявлено.
ТШХ 410 метров.
МСКТ-КАГ: сбалансированный тип, сужение ствола ЛКА - 10%; проксимального сегмента ПНА - 20%; среднего сегмента ПНА - 20%; среднего сегмента ОА - 20%; проксимальный сегмент ПКА - 30%.
ЭхоКГ: ФВ - 64%; КДО - 117 мл; КСО - 39 мл; Полости не увеличены, гипертрофии камер нет. Общая сократимость в норме, нарушение локальной сократимости не выявлено. Диастолическая дисфункция 1 типа. Клапаны без изменений.
NT-proBNP - 2168,1 пг/мл.
По данным динамической однофотонной эмиссионной томографии миокарда у пациента Л., резерв миокардиального кровотока был равен 1,31.
Диагноз: ИБС: стенокардия напряжения ФК I. Фон: гипертоническая болезнь 3 стадии, контролируемое течение. Риск 4. ХСН I, ФК II (NYHA).
Через 10 месяцев у пациента зарегистрировано прогрессирование ХСНсФВ в виде увеличения со II до III функционального класса (по NYHA). В лечении добавлен торасемид 5 мг. Таким образом, у пациента Л. с впервые диагностированной ХСНсФВ с необструктивным атеросклерозом коронарных артерий, с уровнем MFR менее 1,62 и NT-proBNP более 760,5 пг/мл зарегистрировано прогрессирования ХСНсФВ в течение 12 месяцев наблюдения.
Пример 2: пациент В. (51 год, мужчина)
Жалобы на одышку смешанного характера при умеренных нагрузках - подъем на 3-4 этаж, ходьбе по прямой до 400 метров, быстрый подъем в гору. Принимает кардиомагнил 75 мг/сут., розувастатин 10 мг/сутки, рамиприл 2,5 мг/сутки. ИМТ 30,1 кг/м2. Стаж артериальной гипертензии - 3 года, ИБС - 3 мес.
При объективном исследовании: пульс 68 уд/мин., АД 120/80 мм рт. ст., частота дыхания 14 в минуту, отеков нет.
ЭКГ: ритм синусовый, изменений не выявлено.
ТШХ 480 метров.
МСКТ-КАГ: сбалансированный тип, стеноз проксимального сегмента ПНА - 30%; среднего сегмента ПНА - 30%; проксимальный сегмент ПКА - 40%.
ЭхоКГ: ФВ - 64%; КДО - 119 мл; КСО - 40 мл; Полости не увеличены, гипертрофии камер нет. Общая сократимость в норме, нарушение локальной сократимости не выявлено. Диастолическая дисфункция 1 типа. Клапаны без изменений.
NT-proBNP - 165,8 пг/мл.
По данным динамической однофотонной эмиссионной томографии миокарда у пациента В. резерв миокардиального кровотока был равен 2,83.
Диагноз: ИБС: стенокардия напряжения ФК I. Фон: гипертоническая болезнь 3 стадии, контролируемое течение. Риск 4. ХСН I, ФК I (NYHA).
В течение 12 месяцев у пациента не зарегистрировано прогрессирования ХСНсФВ. Таким образом, у пациента В. с впервые диагностированной ХСНсФВ с необструктивным атеросклерозом коронарных артерий, с уровнем MFR более 1,62 и NT-proBNP менее 760,5 пг/мл не зарегистрировано прогрессирование ХСНсФВ в течение 12 месяцев наблюдения.
Предлагаемый способ апробирован на 59 пациентах и позволяет прогнозировать риск прогрессирования хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения после сразу после установления диагноза ХСНсФВ. Это дает возможность выделить приоритетную группу пациентов с необструктивным атеросклерозом коронарных артерий для диспансерного наблюдения с организацией эффективных целевых мероприятий, направленных на профилактику прогрессирования ХСНсФВ и предотвращение у этих пациентов высокой преждевременной смертности.
СПИСОК ЛИТЕРАТУРЫ
1. McDonagh T.A., Metra M., Adamo M., Gardner R.S., Baumbach A., et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) With the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2021 42(36):3599-3726. DOI: 10.1093/eurheartj/ehab368
2. Агеев Ф.Т., Овчинников А.Г. Лечение пациентов с сердечной недостаточностью и сохраненной фракцией выброса: опора на клинические фенотипы. Кардиология. 2022; 62(7): 44-53. https://doi.org/10.18087/cardio.2022.7.n2058
3. Wintrich J., Kindermann I., Ukena C., Selejan S., Werner C., Maack C., Laufs U., Tschöpe C., Anker S.D., Lam C.S.P., Voors A.A., Böhm M. Therapeutic approaches in heart failure with preserved ejection fraction: past, present, and future. Clin Res Cardiol. 2021;109:1079-1098. DOI: 10.1007/s00392-020-01633-w
4. Murthy VL, Naya M, Taqueti VR, et al. Effects of sex on coronary microvascular dysfunction and cardiac outcomes. Circulation. 2014;129:2518-27. doi:10.1161/CIRCULATIONAHA.113.008507
5. Tona F., Montisci R., Iop L., Civieri G. Role of coronary microvascular dysfunction in heart failure with preserved ejection fraction. Rev Cardiovasc Med. 2021;22(1):97-104. DOI: 10.31083/j.rcm.2021.01.277
6. Murthy V.L., Naya M., Taqueti V.R., Foster C.R., Gaber M., Hainer J., Dorbala S., Blankstein R., et al. Effects of sex on coronary microvascular dysfunction and cardiac outcomes. Circulation. 2014;129:2518-2527. DOI: 10.1161/CIRCULATIONAHA.113.008507
7. Mileva N., Nagumo S., Mizukami T., Sonck J., Berry C., Gallinoro E., Monizzi G., Candreva A., Munhoz D., Vassilev D., Penicka M., Barbato E., De Bruyne B., Collet C. Prevalence of Coronary Microvascular Disease and Coronary Vasospasm in Patients With Nonobstructive Coronary Artery Disease: Systematic Review and Meta-Analysis. Journal of the American Heart Association. 2022;11:e023207. http//doi.org/10.1161/JAHA.121.023207
8. Driessen RS, Raijmakers PG, Stuijfzand WJ, et al. Myocardial perfusion imaging with PET. Int J Cardiovasc Imaging. 2017;33:1021-31. doi:10.1007/s10554-017-1084-4
9. Zavadovsky KV, Mochula AV, Boshchenko AA, et al. Absolute myocardial blood flows derived by dynamic CZT scan vs invasive fractional flow reserve: Correlation and accuracy. J Nucl Cardiol. 2021;28(1):249-59. doi:10.1007/s12350-019-01678-z.
10. Agostini D, Roule V, Nganoa C, et al. First validation of myocardial flow reserve assessed by dynamic 99mTc-sestamibi CZT-SPECT camera: head to head comparison with 15O-water PET and fractional flow reserve in patients with suspected coronary artery disease. The WATERDAY study. Eur J Nucl Med Mol Imaging. 2018;45(7):1079-90. doi:10.1007/s00259-018-3958
11. Guo B., Li Z., Tu P., Tang H., Tu Y. Molecular Imaging and Non-molecular Imaging of Atherosclerotic Plaque Thrombosis // Front Cardiovasc Med. 2021 Jul 5;8:692915. doi: 10.3389/fcvm.2021.692915
12. Dobrucki L.W., Sinusas A.J. PET and SPECT in cardiovascular molecular imaging // Nat Rev Cardiol. 2010 Jan;7(1):38-47. doi: 10.1038/nrcardio.2009.201
13. Способ неинвазивной диагностики микроваскулярной дисфункции у пациентов с дислипидемией и необструктивным атеросклеротическим поражением коронарных артерий. [Текст]: пат 2781411 Рос. Федерация: G01N 33/68 (2006.01), G01N 33/573 (2006.01) / Копьева К.В., Мальцева А.Н., Мочула А.В., Гусакова А.М., Гракова Е.В., Бощенко А.А., Завадовский К.В.; заявитель и патентообладатель Федеральное государственное бюджетное научное учреждение "Томский национальный исследовательский медицинский центр Российской академии наук" (Томский НИМЦ) (RU). - 2022122253, заявл. 17.08.2022; опубл 11.10.2022, Бюл. № 29. - 14 с.
14. Leppo JA, Meerdink DJ. Comparison of the myocardial uptake of a technetium-labeled isonitrile analogue and thallium // Circ Res. - 1989;65(3):632-9.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностики сердечной недостаточности с сохраненной фракцией выброса левого желудочка у пациентов с ишемической болезнью сердца на фоне неокклюзирующего атеросклероза коронарных артерий | 2022 |
|
RU2789429C1 |
| Способ неинвазивной диагностики микроваскулярной дисфункции у пациентов с дислипидемией и необструктивным атеросклеротическим поражением коронарных артерий | 2022 |
|
RU2780337C1 |
| Способ неинвазивной ранней диагностики поражения коронарного микрососудистого русла у пациентов с необструктивным атеросклерозом коронарных артерий | 2022 |
|
RU2781411C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ С СОХРАНЕННОЙ ФРАКЦИЕЙ ВЫБРОСА У ПАЦИЕНТОВ С НЕОБСТРУКТИВНЫМ АТЕРОСКЛЕРОЗОМ КОРОНАРНЫХ АРТЕРИЙ ПО АНАЛИЗУ ВАРИАБЕЛЬНОСТИ РИТМА СЕРДЦА | 2023 |
|
RU2800862C1 |
| СПОСОБ ПРОВЕДЕНИЯ ФЕНОТИПИРОВАНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ НА ОСНОВЕ МЕТАБОЛОМНОГО ПРОФИЛИРОВАНИЯ | 2024 |
|
RU2841230C1 |
| Способ прогнозирования развития неблагоприятных сердечно-сосудистых событий у больных с острой декомпенсацией ишемической хронической сердечной недостаточности с систолической дисфункцией левого желудочка сердца после полной реваскуляризации миокарда | 2021 |
|
RU2770271C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАРДИАЛЬНОГО СИНДРОМА Х | 2012 |
|
RU2496420C1 |
| Способ интраоперационного прогнозирования высокого риска ранней дисфункции коронарных шунтов по флоуметрической оценке резерва кровотока | 2023 |
|
RU2813797C1 |
| Способ диагностики ишемии миокарда методом объёмной компьютерной томографии в сочетании с фармакологической пробой аденозинтрифосфатом | 2019 |
|
RU2729030C1 |
| Способ оценки резерва миокардиальной перфузии с использованием системы однофотонно-эмиссионной томограции с NaI-кристаллами с КТ-коррекцией поглощения излучения | 2022 |
|
RU2801545C1 |
Изобретение относится к медицине, а именно к кардиологии, ангиологии, кардиохирургии, реабилитологии, и может быть использовано для прогнозирования риска прогрессирования хронической сердечной недостаточности c сохраненной фракцией выброса (ХСНсФВ) у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения. У пациентов сразу после установления диагноза ХСНсФВ определяют содержание в сыворотке крови N-концевого фрагмента мозгового натрийуретического гормона (В-типа) (NT-proBNP) посредством иммуноферментного анализа и величину резерва миокардиального кровотока (MFR) с помощью динамической однофотонной эмиссионной томографии миокарда. При значении уровня NT-proBNP 760,5 пг/мл и более и MFR 1,62 или менее прогнозируют высокий риск прогрессирования ХСНсФВ. Способ обеспечивает возможность повышения качества прогнозирования риска прогрессирования ХСНсФВ у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения за счет определения содержания в сыворотке крови NT-proBNP и величины резерва миокардиального кровотока MFR. 1 ил., 1 табл., 2 пр.
Способ прогнозирования риска прогрессирования хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения, характеризующийся тем, что у пациентов сразу после установления диагноза хронической сердечной недостаточности c сохраненной фракцией выброса определяют содержание в сыворотке крови N-концевого фрагмента мозгового натрийуретического гормона (В-типа) (NT-proBNP) посредством иммуноферментного анализа и величину резерва миокардиального кровотока (MFR) с помощью динамической однофотонной эмиссионной томографии миокарда и при значении уровня NT-proBNP 760,5 пг/мл и более и MFR 1,62 или менее прогнозируют высокий риск прогрессирования хронической сердечной недостаточности c сохраненной фракцией выброса.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЫЖИВАЕМОСТИ БОЛЬНОГО ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ С НИЗКОЙ ФРАКЦИЕЙ ВЫБРОСА ЛЕВОГО ЖЕЛУДОЧКА В ТЕЧЕНИЕ 1 ГОДА | 2017 |
|
RU2646750C9 |
| СПОСОБ ДИАГНОСТИКИ ФУНКЦИОНАЛЬНОГО КЛАССА ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2012 |
|
RU2526800C2 |
| US 20220412991 A1, 29.12.2022 | |||
| WO 2009154818 A1, 23.12.2009 | |||
| КОПЬЕВА К.В | |||
| и др | |||
| Прогностическая роль резерва миокардиального кровотока у больных с сердечной недостаточностью с сохраненной фракцией выброса | |||
| Бюллетень сибирской медицины | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| КИРИЛЛОВА В.В | |||
| и др | |||
| Уровень | |||
Авторы
Даты
2023-10-04—Публикация
2023-02-20—Подача