Изобретение относится к медицине и может быть использовано в кардиологии, терапии, реабилитологии.
Известно, что дисбаланс вегетативной нервной системы является одной из возможных причин инициации хронической сердечной недостаточности (ХСН) [1]. Имеются единичные исследования, в которых была установлена взаимосвязь изменений вариабельности ритма сердца (ВРС) с развитием ИБС и ХСН, а также с увеличением смертности от всех причин, однако данных о наличии подобных ассоциаций в зависимости от фенотипа ХСН в зависимости от величины ФВ ЛЖ в научной литературе явно недостаточно [2, 3]. В частности, Patel V.N. и соавт. (2017) опубликовали результаты исследования, доказавших влияние сниженного SDNN - параметра временной области общей активности ВРС, с повышением риска госпитализации по причине ХСН у женщин с сердечной недостаточностью (СН) с сохраненной фракцией выброса (СНсФВ), но не с СН со сниженной фракцией выброса (СНнФВ) в период постменопаузы.
Анализ ВСР у пациентов с ИБС показал, что вегетативная дисрегуляция связана с многососудистым поражением коронарного русла, наличием окклюзий венечных артерий и поражением левой коронарной артерии, а также играет важную роль как инструмент скрининга групп высокого риска [4]. При этом, по мере увеличения функционального класса (ФК) стенокардии и тяжести атеросклероза коронарных артерий наблюдается снижение ВСР [5, 6]. Вместе с тем, работ, посвященных оценке вариабельности ритма сердца у больных СНсФВ на фоне неокклюзирующего коронарного атеросклероза в доступной научной литературе нам обнаружить не удалось.
Важным аспектом в разработке изобретения является и тот факт, что оценка ВСР, проводимая по результатам проведения суточного мониторирования ЭКГ (СМ ЭКГ) проста в выполнении, хорошо воспроизводима и может выполняться как в стационарных, так и в амбулаторных условиях, а сам метод СМ ЭКГ доступен и не требует больших финансовых затрат для его выполнения. Этим обусловлен выбор метода для разработки способа ранней диагностики СНсФВ у пациентов с необструктивным атеросклерозом коронарных артерий по анализу вариабельности ритма сердца.
Из анализа данных 28 603 женщин в постменопаузе в среднем возрасте 62,6 лет без ИБС и ХСН известно, что низкая ВСР связана с повышенным риском СНсФВ (OR 1,22, 95% ДИ 1,02; 1,47) [2]. Недостатком этого способа является то, что: 1) в нем оценивается не индексированный показатель SDNN; 2) показатели ВРС SDNN и RMSSD оценивают по данным анализа 10-секундной ЭКГ, но не 24-часовой регистрации, что, следовательно, значительно повышает вероятность ошибок регистрации; 3) способ применяется только в неорганизованной женской популяции, в которой не было данных об отсутствии атеросклеротического поражения коронарного русла или степени выраженности при его наличии.
В проанализированной патентной и научной медицинской литературе адекватного прототипа не обнаружено.
Задача изобретения – повышение качества диагностики хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным коронарным атеросклерозом.
Поставленная задача решается путем определения SDNNidx и pNN50 посредством проведения суточного мониторирования электрокардиограммы в течение 24 часов пациентам с неокклюзирующим коронарным атеросклерозом c сохраненной фракцией выброса при подозрении на наличие хронической сердечной недостаточности. При наличии у таких пациентов уровней SDNNidx 49 мс и менее (AUS=0,768; р=0,012; чувствительность 71,4% и специфичность 75,0%) и pNN50 5% и менее (AUS=0,777; р=0,007; чувствительность 71,4% и специфичность 75,0%) диагностируют наличие хронической сердечной недостаточности c сохраненной фракцией выброса.
Новым в предлагаемом способе является то, что для ранней диагностики хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным коронарным атеросклерозом определяются уровни двух параметров временной области общей вариабельности ритма сердца - среднее значение стандартных отклонений N-N интервалов для каждых 5 минут (SDNNidx, мс) и доля последовательных интервалов N-N, отличающихся более чем на 50 мс, по отношению к общему количеству интервалов N-N (pNN50, %). При этом, как известно, использование индексированного показателя повышает точность измерений, особенно в случае повторных исследований при наблюдении за развитием заболевания у пациента, а проведение мониторирования электрокардиограммы осуществляется в течение 24-часовой регистрации ЭКГ.
Предлагаемый способ не требует наличия дорогостоящего оборудования и позволяет неинвазивными методами обследования как в стационарах, так и в амбулаторных условиях выявлять наиболее частое осложнение сердечно-сосудистых заболеваний, приводящее к высокой смертности трудоспособного населения государства, и выделить приоритетную группу больных для диспансерного наблюдения и раннего назначения оптимальной медикаментозной терапии.
Рассматривается, что лидирующим механизмом того, как ИБС приводит к нарушению вегетативной регуляции сердца, может являться изменение баланса между краткосрочными и долгосрочными компонентами ВСР в сторону парасимпатической абстиненции с приматом симпатической регуляции при прогрессировании коронарного атеросклероза [7, 8]. Также высказана гипотеза о том, что причиной данных изменений у пациентов с типичным сердечно-болевым синдромом может быть и дисфункция микроциркуляции миокарда [9], которая, в свою очередь, обладает триггерным потенциалом в отношении изменения метаболизма миокарда, активации нейрогуморальной системы и развития СНсФВ [10]. В итоге на фоне неокклюзирующего коронарного атеросклероза СНсФВ фактически "запускается" за счет прогрессирующего нарушения эндотелиальной функции, влияющей на снижение коронарного и миокардиального резервов, инициацию диастолической функции, гиперпродукцию гуморальных факторов, приводящих к периваскулярному фиброзу и апоптозу кардиомиоцитов [11]. С другой стороны, нейрогормональная активация, проявляющаяся гиперэкспрессией провоспалительных цитокинов (IL-6, ФНО-α) и С-реактивного белка [12], нарушением регуляции тонуса сосудистой стенки на фоне снижения выработки оксида азота и избыточной активности биомаркеров (ренин, альдостерон, норадреналин) моделирует вегетативные расстройства за счет влияния на симпатическую ее компоненту [13].
Преимуществом предлагаемого изобретения является повышение эффективности диагностики социально значимого заболевания, что дает возможность:
- диагностировать ранние проявления поражения коронарного микрососудистого русла и назначить патогенетическую, оптимально персонифицированную терапию, направленную на восстановление коронарного кровотока и метаболизма миокарда;
- выделить приоритетную группу больных с поражением коронарного микрососудистого русла и повышенным риском развития сердечной недостаточности для диспансерного наблюдения и оптимизации целевых профилактических мероприятий, направленных на предотвращение исключительно высокой преждевременной смертности населения;
- снизить большие финансовые затраты здравоохранения, связанные с дорогостоящим лечением широко распространенной патологии трудоспособного населения государства.
Существенные признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не очевидные для специалиста. Идентичной совокупности признаков в проанализированной литературе не обнаружено. Предлагаемое изобретение может быть использовано в здравоохранении.
Исходя из вышеизложенного, следует считать изобретение соответствующим условиям патентоспособности “Новизна”, “Изобретательский уровень”, “Промышленная применимость”.
Изобретение будет понятно из следующего описания и приложенных к нему фигур.
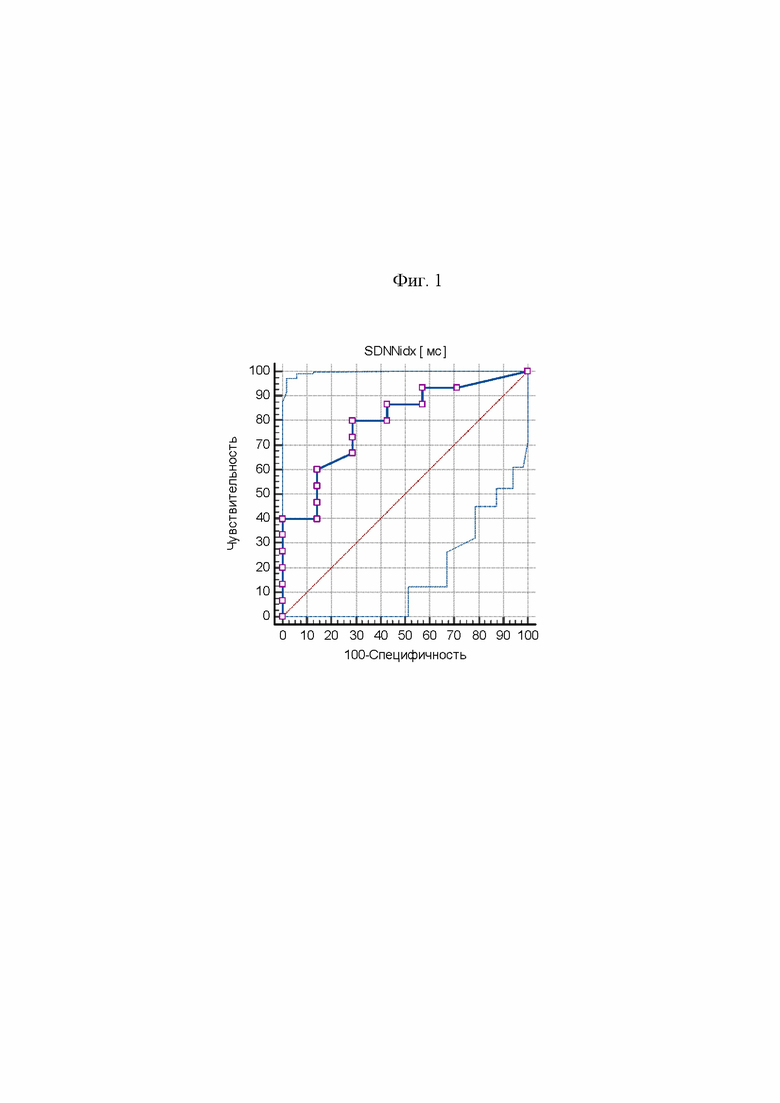
На фиг. 1 представлены результаты ROC-анализа. Изображена ROC-кривая характеристик чувствительности и специфичности показателя временного параметра вегетативной регуляции SDNNidx для ранней диагностики хронической сердечной недостаточности с сохраненной ФВ ЛЖ (СНсФВ) у пациентов с необструктивным атеросклерозом коронарных артерий: по оси ординат – частота (%) истинно положительных результатов (чувствительность), по оси абсцисс – частота (%) ложноположительных результатов (100 минус специфичность). По данным анализа следует, что «точкой отсечения» - cut off, характеризующей наличие СНсФВ с чувствительностью данного критерия 71,4% при специфичности 75,0%, является уровень SDNNidx ≤ 49 мс (AUS=0,768; р=0,012).
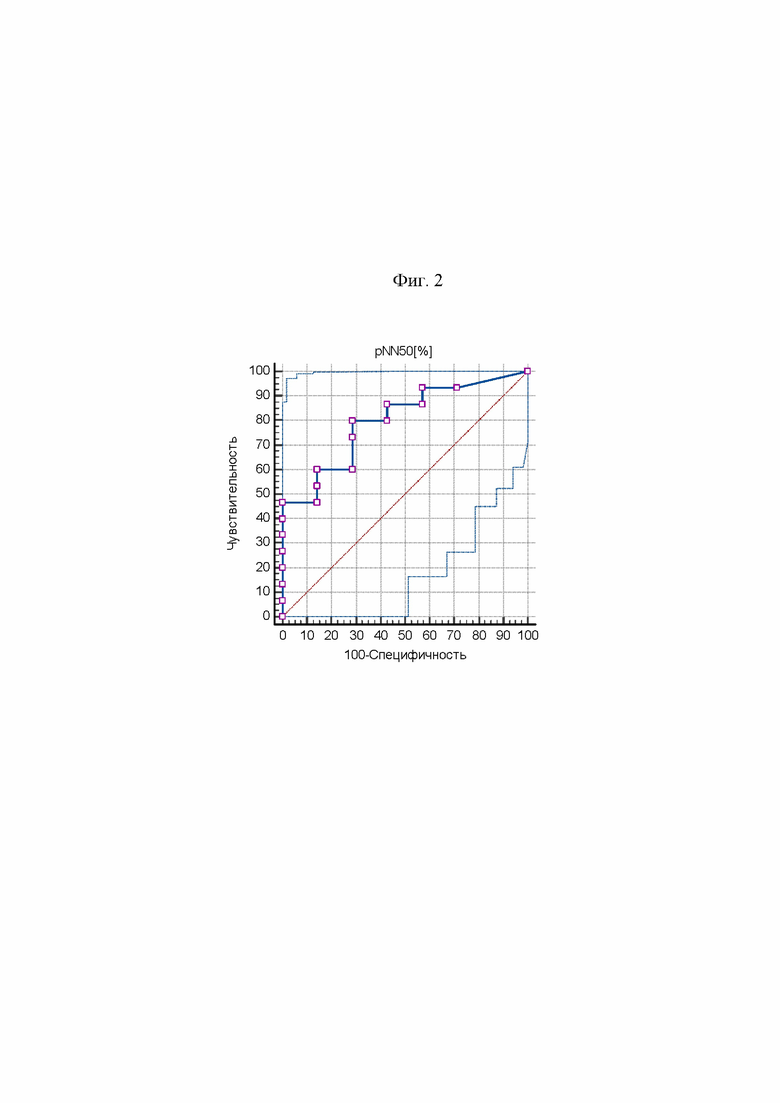
На фиг. 2 представлены результаты ROC-анализа. Изображена ROC-кривая характеристик чувствительности и специфичности показателя парасимпатического звена вегетативной регуляции pNN50 для ранней диагностики хронической сердечной недостаточности с сохраненной ФВ ЛЖ (СНсФВ) у пациентов с необструктивным атеросклерозом коронарных артерий: по оси ординат – частота (%) истинно положительных результатов (чувствительность), по оси абсцисс – частота (%) ложноположительных результатов (100 минус специфичность). По данным анализа следует, что «точкой отсечения» - cut off, характеризующей наличие СНсФВ с чувствительностью данного критерия 71,4% при специфичности 75,0%, является уровень pNN50 ≤ 5% (AUS=0,777; р=0,007).
Способ осуществляют следующим образом:
При подозрении на наличие хронической сердечной недостаточности c сохраненной фракцией выброса левого желудочка у пациентов с ИБС на фоне необструктивного атеросклеротического поражения коронарных артерий проводится мониторирование электрокардиограммы по Холтеру (Shiller MT-101, Швейцария) в течение 24 часов. При обработке результатов мониторирования ЭКГ определяют два показателя вариабельности ритма сердца - SDNNidx и pNN50. При наличии уровней SDNNidx равно или менее 49 мс (AUS=0,768; р=0,012) и pNN50 равно или менее 5% (AUS=0,777; р=0,007) у пациентов с неокклюзирующим коронарным атеросклерозом диагностируют наличие хронической сердечной недостаточности c сохраненной фракцией выброса левого желудочка.
Всего обследовано 48 пациентов (60,4% мужчин) с СНсФВ и ИБС на фоне необструктивного поражения коронарных артерий (наличие стенозов коронарных артерий, суживающих просвет сосуда на ≤50%) в возрасте 61,1 (55,0; 68,0) лет и 17 человек без СНсФВ сопоставимого возраста. По данным ЭХОКГ фракция выброса левого желудочка (ФВ ЛЖ) была более 50% - 62 (56; 67)%.
Исследование было проведено в соответствии с положением Хельсинкской декларации и одобрено локальным Этическим комитетом Научно-исследовательского института кардиологии, Томского национального исследовательского медицинского центра Российской академии наук (протокол №177 от 30.10.2018 г.). Информированное письменное согласие было получено от всех пациентов до включения в исследование. На каждого больного заполнялась специально разработанная клиническая карта.
Всем включенным в исследование пациентам проводили тест 6-минутной ходьбы (ТШХ), спирометрию для исключения патологии легочной системы как проявление одышки. Эхокардиографию с оценкой параметров диастолической дисфункции выполняли на аппарате EPIQ (Philips Ultrasound, Inc., США).
Всем пациентам, учитывая наличие клиники стенокардии напряжения или ее эквивалентов, выполнялась коронарная компьютерная томографическая ангиография для верификации атеросклероза и оценки степени стенозирования коронарных артерий. Для сканирования с контрастным усилением 70-90 мл неионогенного контрастного вещества (йопамидол 370 мг, Bracco Diagnostics, Италия) вводили внутривенно через кубитальный катетер 18G со скоростью потока 5-5,5 мл/с.
Статистическая обработка результатов проводилась с использованием пакета статистических программ STATISTICA (StatSoft, Inc.) и MedCalc 11.5.0.0. Количественные переменные определяли в виде медианы (Ме), а также 25-го и 75-го квартилей (25Q и 75Q). Для проверки статистических гипотез при сравнении 2-х независимых групп использовали критерий Манна-Уитни. При анализе качественных признаков проводили анализ таблиц сопряженности с использованием критерия X2 Пирсона. Если имелись ячейки с ожидаемой частотой меньше 5, то применяли двусторонний точный критерий Фишера или поправку Йетса (для таблиц 2х2). Для определения уровней показателей вариабельности ритма сердца в качестве диагностического маркера наличия сердечной недостаточности с сохраненной фракцией выброса ЛЖ использовали ROC-анализ с расчетом площади под кривой (AUC). Критический уровень значимости p-value для всех используемых процедур статистического анализа принимали равным 0,05.
Распределение пациентов в группы проводилось в зависимости от наличия или отсутствия впервые диагностированной СНсФВ по данным ЭХОКГ и оценки уровня NTproBNP (таблица 1) в соответствии с Рекомендациями ESC по диагностике и лечению острой и хронической сердечной недостаточности (2021).
(+) СНсФВ
(-) СНсФВ
При анализе данных вариабельности ритма сердца выявлено, что у пациентов с СНсФВ, по сравнению с лицами группы контроля, имеет место подавление вегетативной регуляции (показателей восстановления функциональных резервов) на протяжении всего 24-часового периода мониторирования, проявившееся снижением (p<0,01) временных параметров: SDNNidx (ночь) на 29,9% (47 [44; 65] и 67 [52; 208] мс, соответственно) и SDNNidx (сутки) на 14,3% (56 [52; 71] и 64 [55;183] мс, соответственно), а также подавлением активности большинства показателей парасимпатического звена вегетативной регуляции (p<0,01) преимущественно в ночное время - rMSSD на 73,9% (23 [12; 31] и 40 [32; 328] мс, соответственно), NN50, NN100, NN200 в ночные часы - в 5,4-7,8 раз, pNN 50, 100, 200 - в 2,5-6 раз.
У пациентов с СНсФВ выявлено значимое изменение частотных характеристик ВРС, свидетельствующее о преобладании симпатических влияний над парасимпатическими: увеличение VLF (р=0,004) и снижение HF (р=0,016) в сравнении с пациентами без СНсФВ. Остальные показатели значимо не различались между группами.
По данным ROC-анализа уровни таких показателей электрического ремоделирования сердца как SDNNidx ≤ 49 мс (AUS=0,768; р=0,012) и pNN50 ≤ 5 мс (AUS=0,777; р=0,007) были определены как пороговые значения, связанные с наличием СНсФВ у пациентов с необструктивным поражением КА.
Способ ранней диагностики хронической сердечной недостаточности с сохраненной фракцией выброса (СНсФВ) у пациентов с необструктивным атеросклерозом коронарных артерий по анализу вариабельности ритма сердца иллюстрируется следующими клиническими примерами, свидетельствующими о том, что такие показатели вариабельности ритма сердца как SDNNidx и pNN50 проявляют себя в качестве маркеров ранней диагностики СНсФВ.
Пример 1: Пациент П., женщина 60 лет
Жалобы на дискомфорт в прекардиальной области и одышку смешанного характера при физической нагрузке – ходьба до 1000 метров, подъем на 7 этаж, купирующиеся в покое. Принимает кардиомагнил 75 мг/сут., аторвастатин 20 мг/сутки, престариум 2,5 мг/сутки. ИМТ 31,8 кг/м2. Стаж артериальной гипертензии – 5 лет, ИБС – 4 мес.
При объективном исследовании: пульс 67 уд/мин. АД 120/60 мм рт. ст., частота дыхания 14 в минуту, отеков нет.
ЭКГ: ритм синусовый, изменений не выявлено.
ТШХ 580 м.
МСКТ-КАГ: сбалансированный тип, сужение проксимального сегмента ПНА - 30%; среднего сегмента ПНА – 40%; среднего сегмента ВТК – 15%; проксимальный сегмент ПКА – 30%; средний сегмент – 25%.
ЭхоКГ: ФВ – 64%; КДО – 95 мл; КСО – 34 мл; Полости не увеличены, гипертрофии камер нет. Общая сократимость в норме, нарушение локальной сократимости не выявлено. Клапаны без изменений.
По данным суточного мониторирования ЭКГ у пациентки SDNNinx равен 52 мс и pNN50 равен 9,6%.
NT-proBNP – 98,3 пг/мл (N < 125 пг/мл).
Диагноз: ИБС: стенокардия напряжения ФК I. Фон: гипертоническая болезнь 3 стадии, контролируемое течение. Ожирение 1 степени. Риск 4.
Таким образом, у пациентки П. при подозрении на наличие СНсФВ на фоне неокклюзирующего коронарного атеросклероза показатели вариабельности ритма сердца, определенные посредством анализа данных суточного мониторирования ЭКГ по Холтеру, SDNNinx оказался более 49 мс и pNN50 более 5%, что позволило заключить, что у данного пациента нет СНсФВ. Уровень NT-proBNP подтверждает отсутствие СНсФВ.
Пример 2: Пациент Ш., мужчина 72 года
Жалобы на сжимающую боль в прекардиальной области при подъеме на 2-3 этажа, сопровождающаяся одышкой смешанного характера, купируется валидолом в течение 2-3 минут. Принимает кардиомагнил 75 мг/сут., розувастатин 20 мг/сутки, лозартан 25 мг/сутки. ИМТ 32 кг/м2. Стаж артериальной гипертензии – 12 лет, ИБС – 2 года.
При объективном исследовании: пульс 72 уд/мин. АД 128/76 мм рт. ст., частота дыхания 17 в минуту, отеков нет.
ТШХ 450 м.
МСКТ-КАГ: правый тип, сужение ствола ЛКА - 15%; в сегменте ПНА – 40%; проксимальный сегмент ПКА – 15%.
ЭхоКГ: ФВ – 66%; КДО – 126 мл; КСО – 43 мл; Полости не увеличены, гипертрофии камер, ремоделирования нет. Общая сократимость в норме, нарушение локальной сократимости не выявлено. Диастолическая дисфункция 1 типа. Клапаны без изменений.
По данным суточного мониторирования ЭКГ у пациента SDNNinx равен 45 мс и pNN50 равен 4%.
NT-proBNP – 234,9 пг/мл (N < 125 пг/мл).
Диагноз: ИБС: стенокардия напряжения ФК II. Фон: гипертоническая болезнь 3 стадии, достигнуто целевое АД. Ожирение 1 степени. Риск 4. ХСН ФК I (NYHA).
Таким образом, у пациента Ш., с симптомами и признаками ХСН на фоне неокклюзирующего коронарного атеросклероза, по данным по данным суточного мониторирования ЭКГ SDNNinx оказался менее 49 мс и pNN50 менее 5%, что дало основание диагностировать наличие СНсФВ на ранней стадии. Уровень NT-proBNP, превышающий референсное значение, подтверждает наличие СНсФВ. В соответствии с действующими рекомендациями по лечению ХСН для оптимизации терапии назначен бета-блокатор и антагонист минералокортикоидых рецепторов.
Предлагаемый способ апробирован на 48 пациентах и позволяет на ранних стадиях заболевания диагностировать наличие сердечной недостаточности с сохраненной фракцией выброса левого желудочка у пациентов с необструктивным атеросклеротическим поражением коронарных артерий по анализу уровня двух показателей вариабельности ритма сердца, определенных посредством проведения мониторирования ЭКГ в течение 24 часов. Это дает возможность выделить приоритетную группу пациентов с одним из самых распространенных заболеваний трудоспособного населения мира для диспансерного наблюдения и назначения персонифицированного лечения. Предлагаемый способ не требует наличия дорогостоящего оборудования и позволяет неинвазивными методами обследования как в стационарах, так и в амбулаторных условиях выявлять наиболее частое осложнение сердечно-сосудистых заболеваний, приводящее к высокой смертности трудоспособного населения государства, и выделить приоритетную группу больных для диспансерного наблюдения и раннего назначения оптимальной медикаментозной терапии.
СПИСОК ЛИТЕРАТУРЫ
1. Baig M, Moafi-Madani M, Qureshi R, Roberts MB, Allison M, Manson JE, LaMonte MJ, Liu S, Eaton CB. Heart rate variability and the risk of heart failure and its subtypes in post-menopausal women: The Women's Health Initiative study. PLoS One. 2022 Oct 25;17(10): e0276585. doi: 10.1371/journal.pone.0276585.
2. Patel VN, Pierce BR, Bodapati RK, Brown DL, Ives DG, Stein PK. Association of Holter-Derived Heart Rate Variability Parameters With the Development of Congestive Heart Failure in the Cardiovascular Health Study. JACC Heart Fail. 2017 Jun;5(6):423-431. doi: 10.1016/j.jchf.2016.12.015.
3. Mizobuchi Asako, Osawa Kazuhiro, Tanaka Masamichi, Yumoto Akihisa, Saito Hironori, Fuke Soichiro. Detrended fluctuation analysis can detect the impairment of heart rate regulation in patients with heart failure with preserved ejection fraction // Journal of Cardiology Volume 77, Issue 1, January 2021, Pages 72-78. https://doi.org/10.1016/j.jjcc.2020.07.027
4. Chen, Linlin Hou, Chunmiao Luo, Yongjing Jiang, Jianyuan Pan. Altered heart rate variability depend on the characteristics of coronary lesions in stable angina pectoris // Anatol J Cardiol 2015; 15: 496-501. DOI: 10.5152/akd.2014.5642
5. Амиров Н.Б., Чухнин Е.В. Вариабельность сердечного ритма у лиц с постинфарктным кардиосклерозом // Современные проблемы науки и образования. – 2008. – № 2 – С. 7-11. https://science-education.ru/ru/article/view?id=681
6. Лысенкова Н. О., Румянцев М. И., Кратнов А. Е. Роль вегетативной нервной системы в развитии фатальных нарушений ритма сердца у пациентов с ишемической болезнью сердца // Доктор.Ру. 2016. № 11 (128). С. 33–35. https://journaldoctor.ru/catalog/kardiologiya/rol-vegetativnoy-nervnoy-sistem.
7. Arshi, B., Geurts, S., Tilly, M.J. et al. Heart rate variability is associated with left ventricular systolic, diastolic function and incident heart failure in the general population. BMC Med 20, 91 (2022). https://doi.org/10.1186/s12916-022-02273-9
8. Ksela, J.; Rupert, L.; Djordjevic, A.; Antonic, M.; Avbelj, V.; Jug, B. Altered Heart Rate Turbulence and Variability Parameters Predict 1-Year Mortality in Heart Failure with Preserved Ejection Fraction. J. Cardiovasc. Dev. Dis. 2022, 9, 213. https://doi.org/10.3390/jcdd9070213
9. Elhakeem RF, Lutfi MF, Ali ABM, Sukkar MY. Can short-term heart rate variability predict coronary artery disease in patients undergoing elective coronary angiography due to typical chest pain? J Clin Transl Res. 2020 Aug 12;6(2):66-70. PMID: 33426355; PMCID: PMC7787221.
10. Копьева К.В., Мальцева А.Н., Мочула А.В., Гракова Е.В., Завадовский К.В. Роль микроваскулярной дисфункции в патогенезе сердечной недостаточности с сохранённой фракцией выброса. Казанский медицинский журнал. 2022. Т. 103. № 6. С. 918-927. https://doi.org/10.17816/KMJ109034
11. Гракова Е.В., Копьева К.В., Гусакова А.М., Сморгон А.В., Мальцева А. Н., Мочула А.В., Завадовский К.В. Роль гуморальных маркеров в патогенезе сердечной недостаточности с сохраненной фракцией выброса левого желудочка у больных с неокклюзирующим коронарным атеросклерозом. Российский кардиологический журнал. 2022;27(10):51-62. doi:10.15829/1560-4071-2022-5162
12. Adamczak DM, Oduah MT, Kiebalo T, Nartowicz S, Bęben M, Pochylski M, Ciepłucha A, Gwizdała A, Lesiak M, Straburzyńska-Migaj E. Heart Failure with Preserved Ejection Fraction-a Concise Review. Curr Cardiol Rep. 2020 Jul 9;22(9):82. doi: 10.1007/s11886-020-01349-3.
13. Aronson D, Mittleman MA, Burger AJ. Role of endothelin in modulation of heart rate variability in patients with decompensated heart failure. Pacing Clin Electrophysiol. 2001 Nov;24(11):1607-15. doi: 10.1046/j.1460-9592.2001.01607.x.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностики сердечной недостаточности с сохраненной фракцией выброса левого желудочка у пациентов с ишемической болезнью сердца на фоне неокклюзирующего атеросклероза коронарных артерий | 2022 |
|
RU2789429C1 |
| Способ прогнозирования риска прогрессирования хронической сердечной недостаточности с сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий в течение 12 месяцев наблюдения | 2023 |
|
RU2804705C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2008 |
|
RU2391044C2 |
| СПОСОБ ВЫЯВЛЕНИЯ ДИСФУНКЦИИ ЭНДОТЕЛИЯ КОРОНАРНЫХ АРТЕРИЙ | 2001 |
|
RU2199266C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ВНЕЗАПНОЙ СЕРДЕЧНОЙ СМЕРТИ У БОЛЬНЫХ, ПЕРЕНЕСШИХ ИНФАРКТ МИОКАРДА | 2012 |
|
RU2485884C1 |
| СПОСОБ ДИАГНОСТИКИ ЭПИЗОДОВ ПРЕХОДЯЩЕЙ ИШЕМИИ МИОКАРДА | 2001 |
|
RU2199265C1 |
| Способ диагностики рестеноза стента коронарной артерии у больных ишемической болезнью сердца с хронической сердечной недостаточностью | 2017 |
|
RU2649131C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕБЛАГОПРИЯТНОГО КЛИНИЧЕСКОГО ТЕЧЕНИЯ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ С СОХРАНЕННОЙ ФРАКЦИЕЙ ВЫБРОСА ЛЕВОГО ЖЕЛУДОЧКА В ТЕЧЕНИЕ 12 МЕСЯЦЕВ | 2024 |
|
RU2826921C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОСУДОРАСШИРЯЮЩЕЙ РЕАКЦИИ НИТРОГЛИЦЕРИНА У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2010 |
|
RU2444278C2 |
| Способ неинвазивной ранней диагностики поражения коронарного микрососудистого русла у пациентов с необструктивным атеросклерозом коронарных артерий | 2022 |
|
RU2781411C1 |
Изобретение относится к медицине и может быть использовано в кардиологии, терапии, реабилитологии. У пациента определяют SDNNidx и pNN50 посредством проведения суточного мониторирования электрокардиограммы в течение 24 часов пациентам с неокклюзирующим коронарным атеросклерозом c сохраненной фракцией выброса при подозрении на наличие хронической сердечной недостаточности. При получении уровня SDNNidx 49 мс и менее и pNN50 5% и менее диагностируют наличие хронической сердечной недостаточности c сохраненной фракцией выброса. Способ позволяет повысить качество диагностики хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий по уровню двух параметров временной области общей вариабельности ритма сердца SDNNidx и pNN50. 2 пр., 2 ил., 1 табл.
Способ ранней диагностики хронической сердечной недостаточности c сохраненной фракцией выброса у пациентов с необструктивным атеросклерозом коронарных артерий, характеризующийся тем, что проводят суточное мониторирование ЭКГ в течение 24 часов с определением уровней двух параметров временной области – среднее значение стандартных отклонений N-N интервалов для каждых 5 минут - SDNNidx и доли последовательных интервалов N-N - pNN50 и при значении уровней SDNNidx 49 мс и менее и pNN50 5% и менее диагностируют хроническую сердечную недостаточность c сохраненной фракцией выброса.
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА КАРДИАЛЬНЫХ ОСЛОЖНЕНИЙ ПОСЛЕ ИШЕМИЧЕСКОГО ИНСУЛЬТА | 2014 |
|
RU2545430C1 |
| Способ оценки развития неблагоприятного течения хронической обструктивной болезни легких и артериальной гипертензии при их сочетании | 2018 |
|
RU2711453C1 |
| Алиева А.М | |||
| и др | |||
| ВАРИАБЕЛЬНОСТЬ СЕРДЕЧНОГО РИТМА ПРИ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ (ЛИТЕРАТУРНЫЙ ОБЗОР), Архивъ внутренней медицины, 2013, 6 (14), 47-52 | |||
| Анкудинов А.С., Марченко Д.В | |||
| Диагностика хронической сердечной недостаточности, ассоциированной с ревматоидным артритом, роль | |||
Авторы
Даты
2023-07-31—Публикация
2023-03-31—Подача