Изобретение относится к области медицины, а именно - к кардиологии, к способу классификации хронической сердечной недостаточности (ХСН) с помощью методов машинного обучения на основе анализа содержания метаболитов в плазме крови методом высокоэффективной жидкостной хроматографии в сочетании с масс-спектрометрией. Изобретение может быть использовано для оценки метаболомного фенотипа ХСН в ходе лабораторного анализа плазмы крови в качестве дополнения к существующим диагностическим критериям.
Сердечно-сосудистые заболевания (ССЗ) ежегодно уносят миллионы жизней и служат причиной инвалидизации населения. По данным официального отчета ВОЗ, в 2022 г. ССЗ являются причиной смерти 17,9 млн человек [1]. Синдром ХСН может явиться последней стадией любого сердечно-сосудистого заболевания. Течение ХСН может значительно различаться в зависимости от целого ряда факторов: причины развития, возраста, пола, наличия сопутствующих заболеваний, характера структурных и функциональных нарушений сердца. Терапевтические подходы значительно варьируются в зависимости от варианта течения сердечной недостаточности [2]. Создание различных классификаций ХСН (то есть распределение по общим характеристикам) своей задачей ставит выделение определенных фенотипов, которые имеют свои особенности течения заболевания и различные подходы к лечению. Несмотря на все современные диагностические методики, проблема классификации и верификации фенотипов ХСН остается не решенной задачей [3]. Крайне важно правильно подобрать классификационные признаки, чтобы они отражали патогенетические процессы, лежащие в основе развития ХСН в конкретном случае.
Первый известный способ классификации ХСН был предложен Г.Ф. Лангом в 1935 г. [4]. В 2002 году Обществом Специалистов по Сердечной Недостаточности (ОССН) была предложена видоизмененная классификация ХСН 1935 года по стадиям (табл. 1), которая широко применяется и в настоящее время [5].
Следует отметить, что данная классификация имеет ряд недостатков, связанных с неясностью трактовок «адаптивное» и «дезадаптивное» ремоделирование и необходимостью оценки большого количества показателей ЭХОКГ для определения стадии. Это обуславливает сложности применения данной классификации в условиях клинической практики.
Известен способ классификации, который в 2016 году был предложен Европейским кардиологическим обществом и основывался на выделении 3 фенотипов ХСН по уровню фракции выброса (ФВ) левого желудочка [6]. Основанием к такому разделению была попытка простимулировать исследования по изучению характеристик, патофизиологии и подходов к лечению пациентов с умеренно сниженной (или промежуточной) ФВ левого желудочка (ХСНунФВ). Однако, последующие годы показали, что ХСНунФВ носит черты, как ХСН с сохраненной ФВ (ХСНсФВ), так и ХСН с низкой ФВ (ХСНнФВ). При этом отнесение пациента к подгруппе с умеренной сниженной или к низкой ФВ ЛЖ полностью зависит от квалификации врача, проводящего эхокардиографию (ЭХОКГ). Определенных рекомендаций по лечению пациентов с ХСНунФВ также предложено не было. Таким образом, признанная на сегодня классификация ХСН по уровню ФВ имеет ряд ограничений и вопросов.
Другой известный способ классификации ХСН [7] основывается на оценке совокупности заболеваний, натрийуретических пептидов и параметров ЭХОКГ которые предлагают стадировать ХСН по этапам сердечно-сосудистого континуума - начиная со стадии A, или пациентов с риском развития ХСН без симптомов или признаков ХСН, без структурного поражения сердца и при отсутствии генетических маркеров и биомаркеров ССЗ до стадии D, которая характеризует пациентов с крайне тяжелым течением заболевания, требующей применения высокотехнологических методов лечения (имплантации искусственного левого желудочка или трансплантации сердца). Данная классификация имеет схожие черты с классификацией 2002 г. Её преимуществом является выделение группы пациентов с предсердечной недостаточностью, которым необходимо начать профилактические мероприятия для предотвращения развития симптомов. Недостатком же использования такой классификации служит необходимость анализа большого количества эхокардиографических параметров и данных анамнеза, для отнесения пациента к той или иной стадии и высокой квалификации врача.
Anker, S.D. с соавт. был предложен способ фенотипирования ХСН, основанный на наличии сопутствующих заболеваний [8]. Этот подход предлагает сделать акцент на тех состояниях, которые требуют дополнительных или особенных методов лечения, в зависимости от пола, индекса массы тела (ИМТ), наличия или отсутствия сахарного диабета (СД) 2 типа, артериальной гипертензии (АГ), хронической обструктивной болезни легких (ХОБЛ), фибрилляции предсердий (ФП) и ишемической болезни сердца (ИБС). Такой подход представляется удобным и доступным, в то же время он охватывает только группу пациентов с ХСНсФВ и не учитывает обширную группу пациентов с низкой и умеренно сниженной ФВ.
Другой известный способ фенотипирования ХСН основан на клинических проявлений заболевания, обнаруженных в неструктурированных клинических записях большой базы данных [9]. Эти фенотипы были обнаружены с использованием метода извлечения информации на основе нейролингвистического программирования и неконтролируемого кластерного подхода для разделения пациентов с ХСН на подгруппы. Фенотипы были построены на кластеризации жалоб (упоминаний болезней и симптомов), извлеченных из неструктурированных заметок. Несмотря на всю привлекательность метода в отношении простоты использования, данный подход имеет ряд недостатков, так как не дает полного представления о механизмах развития и течения заболевания, а значит затрудняет подбор патогенетической терапии.
Значимость метаболомного профилирования, т.е. количественного измерения уровня содержания метаболитов для дифференциальной диагностики различных заболеваний была доказана в ряде исследований [10-13]. Изменения метаболомного профиля могут не только четко охарактеризовать заболевание, но и предоставить информацию о вовлеченности тех или иных метаболомных путей в патогенез изучаемого состояния, а, следовательно, разработать таргетный подход к лечению. Так как ХСН является гетерогенным синдромом, течение которого определяется не только характером ремоделирования миокарда, но и степенью выраженности сопутствующей патологии, метаболомный профиль пациентов с разными вариантами ХСН может различаться. Следовательно, перспективным направлением для поиска возможных детерминант - классификаторов ХСН является изучение метаболома. Предложенный в настоящем изобретении способ классификация ХСН на основе метаболомного профилирования имеет большое практическое значение, так как позволяет быстро определить патогенетический вариант течения ХСН и определить тактику ведения пациента.
Настоящее изобретение направлено на решение технической проблемы, не решенной в настоящее время известными способами и состоящей в расширении арсенала технических средств для классификации ХСН по содержанию набора метаболитов в плазме крови при помощи машинного обучения.
Технический результат предлагаемого изобретения - повышение точности классификации за счет распределения пациентов с ХСН на феногруппы при помощи биостатистической обработки результатов количественного определения выделенных метаболитов плазмы крови.
Для достижения технического результата первым этапом проводится кластеризация пациентов по схожим характеристикам метаболомного профиля. Затем охарактеризовывается описательная статистика каждого кластера, включая демографическую информацию, такую как возраст и пол, ИМТ, сопутствующие заболевания, данные анамнеза, лабораторные данные и параметры ЭХОКГ. После определения значимых концепций и описательной статистики для каждого кластера выявляются наиболее значимые клинические факторы, позволяющие фенотипировать метаболомные кластеры. Наконец на основе числовых значений значимых факторов разрабатывается формула, позволяющая на основе клинических данных охарактеризовать тот или иной метаболомный кластер.
Технический результат достигается за счет того, что с помощью количественного хромато-масс-спектрометрического анализа в плазме крови определяют концентрацию циркулирующих метаболитов: ацилкарнитинов (С5-ОН, С6-DC, C14, C12, C18-1, C6, C5-DC, C5-1, C8-1, C10, C16-1, C16, C14-2, C12-1), метаболитов триптофан-кинуренинового (хинолоновая кислота, ксантуриновая кислота, 3-ОН-антраниловая кислота, триптофан) и триптофан-серотонинового путей (5-метилтриптамин, 5-гидрокситриптофан), метаболитов цикла глутамин-глутамат (глутамин, глутамат), аминокислота (серин), витаминов (рибофлавин), метионин сульфоксид и нейромедиаторов (норэпинефрин); затем при помощи методов машинного обучения определяют метаболомный кластер на основе результатов широкоформатного метаболомного профилирования плазмы крови пациентов с хронической сердечной недостаточностью, для чего методом главных компонент проводят предварительное понижение размерности данных до девяти главных компонент и далее выполняют иерархический кластерный анализ, при котором расстояние между кластерами определяют по методу Уорода:
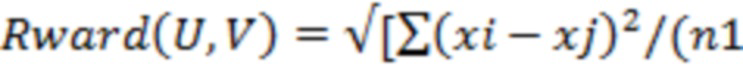 *n2)] -
*n2)] - 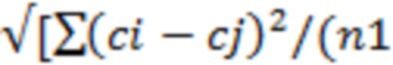 *n2)],
*n2)],
который соответствует клиническому фенотипу, вычисленному по следующей формуле:
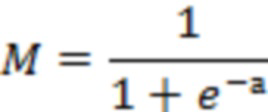
где xi и xj - средние значения признаков объектов в кластерах U и V соответственно, ci и cj - средние значения признаков объектов в объединенном кластере, n1 и n2 - количество объектов в кластерах U и V соответственно, U и V - кластеры, между которыми определяется расстояние, а расчетный показатель «а» для каждого кластера определяют по следующим формулам:
для дифференциации кластера 1:

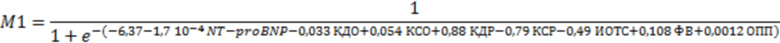
для дифференциации кластера 2:

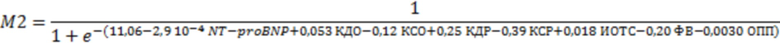
для дифференциации кластера 3:
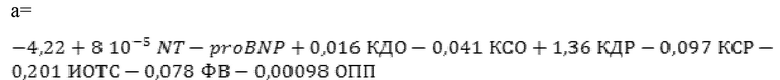

для дифференциации кластера 4:

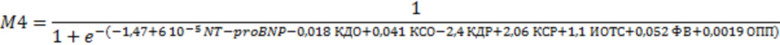
и путем расчета показателя М для каждого кластера определяют принадлежность пациента с хронической сердечной недостаточностью к одному из метаболомных кластеров путем выбора наибольшего процента, который будет свидетельствовать о принадлежности данного пациента к определенному кластеру.
Также технический результат достигается за счет способа, включающего анализ в плазме крови уровня NT-proBNP и параметров эхокардиографии - конечный систолический размер левого желудочка, конечный диастолический размер левого желудочка, конечный систолический объем левого желудочка, конечный диастолический объем левого желудочка, фракцию выброса, индекс относительной толщины стенки левого желудочка, объем правого предсердия и отличающийся тем, что в случае невозможности проведения метаболомного профилирования, кластер определяется при помощи классификационных моделей с использованием алгоритма «Дерево принятия решений», где NT-proBNP - концентрация N-концевого фрагмента натрийуретического пептида (пг/мл); КДО - конечный диастолический объем (мл); КСО - конечный систолический объем (мл); КСР - конечный систолический размер (см); ИОТС - индекс относительной толщины стенки левого желудочка; ОПП - объем правого предсердия (мл); ФВ - фракция выброса левого желудочка (%).
Структура дерева принятия решений, используется в машинном обучении, анализе данных и статистике, включает себя признаки (уровень NT-proBNP и параметры ЭХОКГ - КСР, КДР, КСО, КДО, ФВ, ИОТС, ОПП), которые помогают описать, классифицировать и обобщить набор данных.
Гиперпараметры модели:
criterion='entropy', min_samples_leaf=4, max_features = 'log2', max_depth = 9, min_samples_split=10, random_state=42
обучающая выборка - 80% от общей выборки пациентов.
Метрики качества модели: One-vs-rest
AUC ROC 0.90
Accuracy 0.74
Recall 0.74
F1 0.74
Матрица ошибок, характеризующая качество модели «Дерево принятия решений» (табл. 2).
Краткое описание чертежей
Изобретение поясняется чертежами, схемами, таблицами.
На фиг. 1 представлен алгоритм «Дерево принятия решений» (или дерево классификации, регрессионное дерево), который был выбран как наиболее оптимальный для создания модели, характеризующей тот или иной метаболомный кластер ХСН , где NT-proBNP - концентрация N-концевого фрагмента натрийуретического пептида (пг/мл); КДО - конечный диастолический объем (мл); КСО - конечный систолический объем (мл); КСР - конечный систолический размер (см); ИОТС - индекс относительной толщины стенки левого желудочка; ОПП - объем правого предсердия (мл); ФВ - фракция выброса левого желудочка (%).
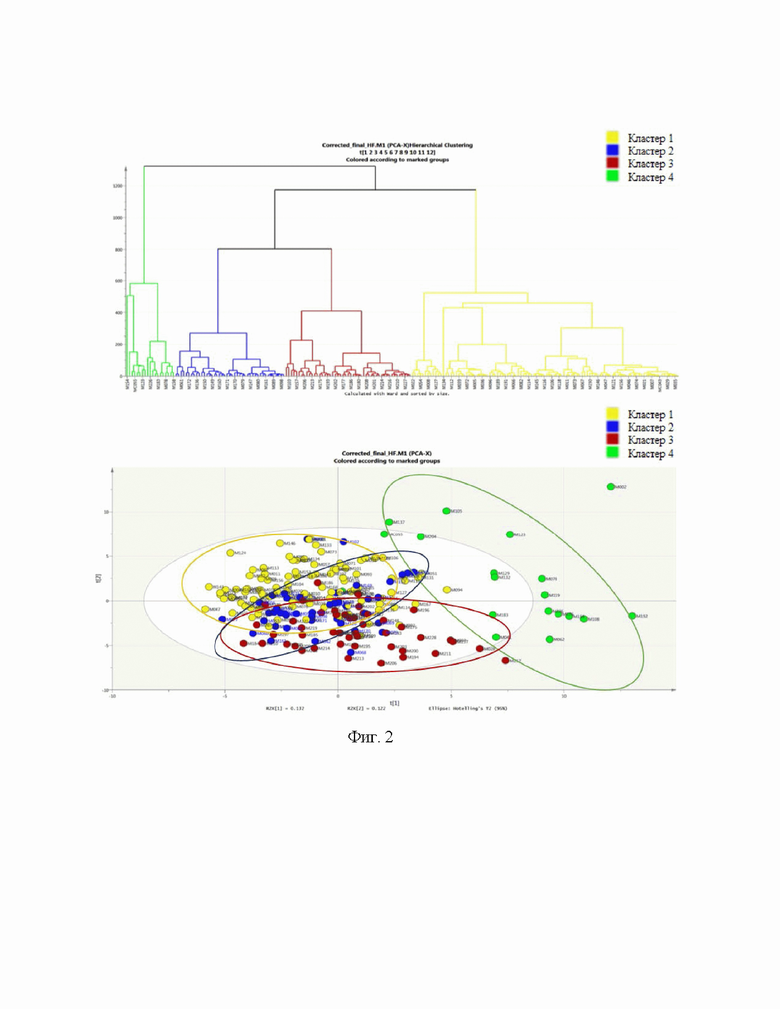
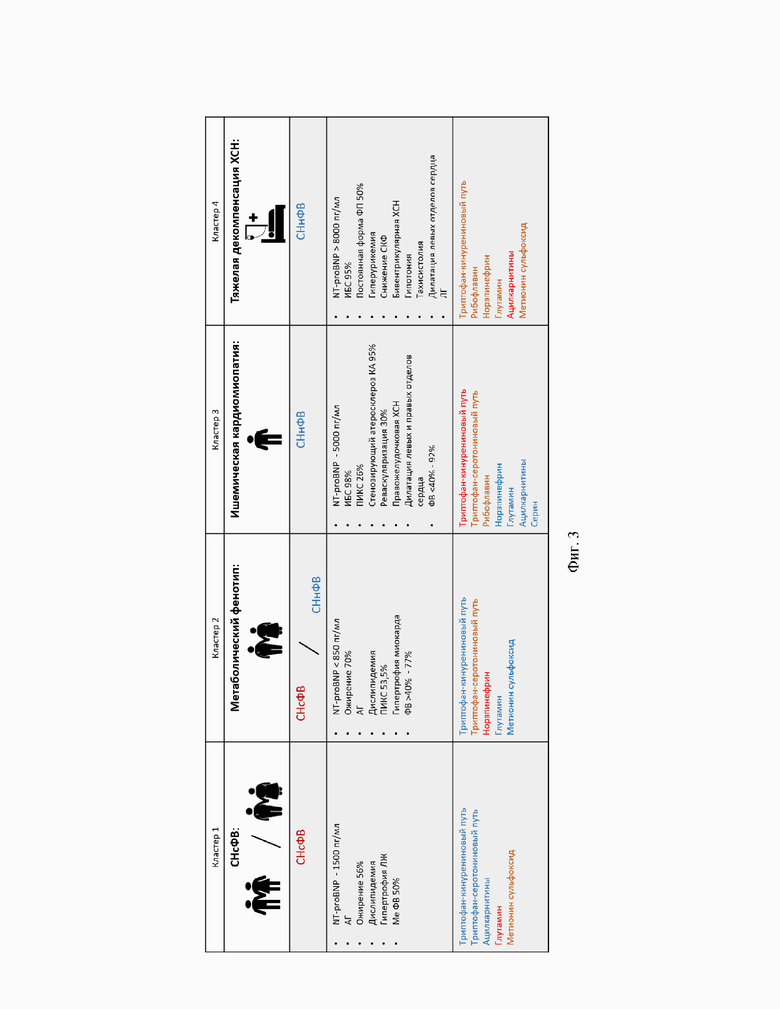
Также изобретение поясняется чертежами, в которых представлены блок-схема кластеризации пациентов ХСН на основе данных метаболомного профилирования пациента (фиг. 2) и описание феногрупп кластеров, основанных на метаболомном профилировании (фиг. 3). Кроме того, изобретение поясняется таблицами, где представлена информация о метриках качества модели классификации по фенотипу ХСН на основе результатов иерхарической кластеризации (таблица 3), информация о значимых метаболитах, оказывающих влияние на кластеризацию (таблица 4), о факторах риска и ассоциированных состояниях в группах кластеризации по метаболомному профилированию (таблица 5), информацию об уровне систолического артериального давления пациентов относящихся к разным кластерам (таблица 6), различия этиологии ХСН (таблица 7), различия концентрации натрийуретического пептида в кластерах ХСН по метаболомному профилированию (таблица 8), сравнительная характеристика параметров эхокардиографии в кластерах ХСН по метаболомному профилированию (таблица 9).
Осуществление изобретения
Способ реализуется с использованием системы высокоэффективной жидкостной хроматографии Waters Acquity I, подключенной к тройному квадрупольному масс-спектрометру Waters TQ-S-micro (Waters Corp, Милфорд, США) или ее аналога. Хроматографическое разделение проводят с использованием обращено-фазной колонки С18 или аналогичной ей. Для проведения метаболомного анализа образцы плазмы крови необходимо отбирать после ночного голодания между 8 и 10 часами утра из вены в вакуумных пробирках, содержащих дегидрат дикалийной соли этилендиаминтетрауксусной кислоты (K2EDTA). Сразу после этого образцы необходимо центрифугировать при 2000 об/мин в течение 1 мин и хранить при -80°C до проведения анализа.
Для кластеризации ХСН по метаболомному профилю нами было проведено одномоментное наблюдательное исследование, выполненное на базе ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет). В исследовании приняли участие 218 участников с ХСН, среди которых 132 мужчины (60,6%), возраст пациентов составил 68 [63;73] лет, а индекс массы тела (ИМТ) 31 [27;35] кг/м2. Исследуемая группа пациентов с ХСН была представлена в равном соотношении пациентами с ХСНнФВ (n=81, 37,0%) и ХСНсФВ (n=50, 40,0%) и в меньшей степени пациентами ХСНунФВ (n= 50, 23%). Половину пациентов группы ХСН составили больные с IV функциональный класс (ФК) по данным теста 6 минутной ходьбы (6ШТХ) (47,9%). 33% пациентов имели III ФК по NYHA, 19,1% пациентов имели II ФК по NYHA. В группе ХСН уровень NT-proBNP, пг/мл составил: у пациентов с синусовым ритмом 1372 [337;2947]: у пациентов с ФП - 2396 [980-3262]. Критерии включения: 1. Наличие письменного информированного согласия на участие в исследовании; 2. Возраст более 35 лет; 3. Наличие ХСН согласно Клиническим рекомендациям Минздрава России 2020 года. Критерии невключения/исключения: вторичная АГ; наследственные и приобретенные (токсическая, воспалительная, стресс-индуцированная, послеродовая) кардиомиопатии; врожденные и приобретенные пороки сердца; острый миокардит, перикардит; острое нарушение мозгового кровообращения или транзиторная ишемическая атака в течение предшествующих 6 месяцев; острая почечная недостаточность, хроническая болезнь почек (ХБП) 5 стадии; хроническое легочное сердце; тяжелые нарушения функции печени (с синдромом цитолиза и явлениями печеночно-клеточной недостаточности); бронхиальная астма, хроническая обструктивная болезнь легких; язвенная болезнь желудка или 12-п. кишки в фазе обострения; хронический панкреатит в фазе обострения; злокачественные новообразования; заболевания щитовидной железы (гипотиреоз и гипертиреоз); синдром Иценко-Кушинга, СД 1 типа; СД 2 типа в стадии декомпенсации; тромбоцитопении любого генеза, геморрагический синдром; хронические вирусные и бактериальные инфекции; аутоиммунные заболевания; психическое заболевание; злоупотребление алкоголем или применение наркотических веществ; беременность, лактация.
Кластеризацию полученных данных метаболомного анализа проводили на языке программирования Python (Python Software Foundation. Python Language Reference, version 3.1. Available at http://www.python.org). Для исключения возможного влияния различных клинических факторов на результат исследования, проводился корреляционный анализ с последующей проверкой влияния фактора в классификационной модели. Было установлено, что значимое влияние оказывает возраст, поэтому, с использованием коммерчески доступных пакетов Python, была выполнена поправка на возраст. Статистический анализ для характеристики изменений в биохимических и метаболических путях выполняли с помощью пакета Python stats. Для оценки нормальности распределения применяли критерий Шапиро-Уилка, по результатам которого выполняли параметрический или непараметрический анализ различий выборочных средних отдельно для каждого метаболита. Значения p-value < 0.05 считались значимыми. Для кластеризации образцов пациентов с ХСН применяли метод иерархической кластеризации и метод k-ближайших соседей по первой главной компоненте.
Дальнейшую статистическую обработку полученных в программе данных проводили с помощью программы STATTECHv3.0.9. Статистическую значимость различия концентраций исследуемых метаболитов между группами оценивали по значению p-value теста Манна-Уитни. При величине p-value ≤ 0,05 отличие принимали за статистически значимое, при p-value ≤ 0,01 - за очень значимое, при p-value ≤ 0,001 - за максимально значимое.
В результате были проанализированы 218 образцов плазмы крови с оценкой концентраций 93 метаболитов.
Для создания новой классификации ХСН на основе их метаболомного фенотипа был применен метод кластеризации (фиг. 1). Были рассмотрены несколько видов кластеризации: k-средняя кластеризация и иерархическая кластеризация. Наилучшее качество было получено для иерархической кластеризации. Для оценки качества новой классификации на основе проведенной кластеризации были получены следующие метрики качества: точность 0.95, полнота 0.95, F1 0.95, площадь под ROC-кривой 0.96 (таблица 3). Таким образом, модель продемонстрировала высокую прогностическую значимость. Были выделены 26 наиболее значимых метаболитов для данной классификации, относящихся преимущественно к классу ацилкарнитинов (С5-ОН, С6-DC, C14, C12, C18-1, C6, C5-DC, C5-1, C8-1, C10, C16-1, C16, C14-2, C12-1), метаболитов триптофан-кинуренинового (хинолоновая кислота, ксантуриновая кислота, 3-ОН-антраниловая кислота, триптофан) и триптофан-серотонинового путей (5-метилтриптамин, 5-гидрокситриптофан), метаболиты цикла глутамин-глутамат (глутамин, глутамат), аминокислота (серин), витамин (рибофлавин), метионин сульфоксид и нейромедиатр (норэпинефрин) (таблица 4).
Далее был проведен сравнительный анализ клинических данных для выявления потенциальных фенотипических факторов, различающих кластеры. Клинический анализ групп кластеризации, основанной на метаболомном профилировании, показал, что 4 кластера не различались по возрасту. При сравнении групп по полу, установлено, что в группе 3 преобладали мужчины (77,6%), что значимо отличало эту группу от группы 2, в которой мужчины и женщины были представлены в равных долях (мужчин 51.2%), p=0.037. Группы статистически не различались по наличию ожирения, однако кластер 2 характеризовался наличием ожирения в 67,4% случаев, в то время как доля ожирения в кластерах 4 и 3 составила менее 47%. Статистически значимых различий по степени тяжести ХБП между группами не выявлено, однако кластер 4 характеризовался большим процентом ХБП 3 стадии (72.2%) и статистически значимо более высокими цифрами уровня креатинина, чем во 2 и 1 кластерах (124.0 [103.5;149.5], p<0.05). Группы не различались по наличию нарушений углеводного обмена и фибрилляции предсердий. Дислипидемия статистически чаще была установлена в группах 2 и 4, вероятно это обусловлена более частым приемом статинов в группах 4 и 3. Гиперурекимия встречалась часто во всех группах, однако кластер 4 характеризовался наличием гиперурикемии в 87,5% случаев. Инфаркт миокарда в анамнезе достоверно реже встречался в группе 3 (26,5%) по сравнению с группой 2 (53,5%) (таблица 5). В группах 4 и 1 постинфарктный кардиосклероз был установлен в 31,6% и 47,1 % случаев соответственно. Пациенты не различались по ФК, как измеренному в 6ШТХ, так и при помощи шкалы ШОКС, что может быть обусловлено исходно тяжелым состоянием большей части участников исследования. В то же время кластер 3 характеризовался преобладанием отеков, которые были выявлены в 95,6% случаев, что значимо отличало эту группу от пациентов 2 и 1 кластера, в которых только в половине процентов случаев были отеки (pкластер 2 - кластер 3 = 0,000024, pкластер 3 - кластер 1 = 0,000004) и отсутствием одышки в 11% случаев, тогда как другие кластеры в 100% характеризовались наличием одышки. Обращали на себя внимание различия цифр АД, так для кластера 1 было характерно наличие гипотонии, в то время как, в кластере 2 и 1 преобладали пациенты с артериальной гипертензией (таблица 6). Также пациента кластера 4 имели тахикардию. При сравнении этиологических факторов формирования ХСН в разных кластерах, было показано, что кластер 3 и 4 практически полностью представлены пациентами с ИБС. В то же время, кластер 1 и 2 в 27% случаев были представлены ХСН+АГ (таблица 7). Группы статистически значимо отличались по уровню NT-proBNP: крайне высокие значения, превышающие в 10 раз таковые в кластере 2, были установлены для кластера 4, высокие были характерны и для кластера 3, кластер 1 характеризовался промежуточным уровнем NT-proBNP (таблица 8). При сравнении кластеров по показателям ЭХОКГ было показано статистически значимое различие групп по размерам полостей сердца: для кластера 1 и 3 была характерна более выраженная дилатация левого желудочка (ЛЖ), левого и правого предсердий по сравнению с кластером 2 и 4. Группы значимо различались по уровню ФВ ЛЖ средние значения которой составляли менее 37% в группах 4 и 3, 47% в группе 2 и 50% в группе 1 и по уровню систолического давления в легочной артерии (СДЛА), которое также было повышено в группах 3 и 4 по сравнению с группой 1. Таким образом, группы значимо различались по структурным и функциональным параметрам сердца. Распределение кластеров по фенотипам ХСН на основе ФВ ЛЖ, продемонстрировал статистически значимые различия между группами. Так кластер 3 отличался от кластера 2 и 1 преобладанием ХСНнФВ и ХСНунФВ (91,2%), кластер 1 был представлен пациентами с ХСНсФВ (медиана ФВ 50%), в свою очередь кластер 2 на 44,2% был представлен ХСНсФВ и на 32,6% ХСНунФВ (pкластер 2 - кластер 3 = 0,000290, pкластер 3 - кластер 1 = 0,000001) (таблица 9).
При сравнении клинических характеристик метаболических кластеров, была выявлена схожесть кластера 3 и 4. В то же время, кластер 4 отличается значимо более тяжелым состоянием пациентов, по сравнению со всеми кластерами. Кластер 4 полностью соответствует классической модели ХСНсФВ. Кластер 2 имеет схожие черты со всеми представленными кластерами и наиболее соответствует модели выраженного метаболического синдрома. Таким образом, проведенный анализ позволил клинически охарактеризовать кластеры основанные на метаболомном профилировании.
Для оценки диагностической значимости количественных признаков при прогнозировании определенного исхода, применялся метод анализа ROC-кривых.
Была разработана прогностическая модель для определения вероятности показателя "Кластеризация " в зависимости от показателя "NT-proBNP, пг/мл ", показателя "КДО, мл", показателя "КСО, мл", показателя "КДР, см", показателя "КСР, см", показателя "ИОТС", показателя "ФВ, %", показателя "Объем правого предсердия, мл" методом бинарной логистической регрессии. Наблюдаемая зависимость описывается уравнением:
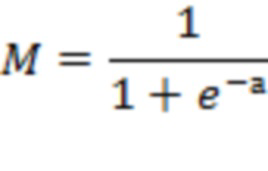
где М - определенный кластер ХСН, e - основание натурального логарифма, а - расчетный показатель для каждой формулы.
Формула для дифференциации кластера 1:
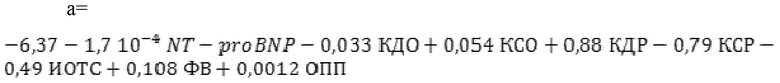
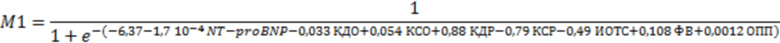
Формула для дифференциации кластера 2:

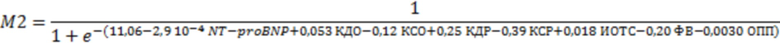
Формула для дифференциации кластера 3:


Формула для дифференциации кластера 4:
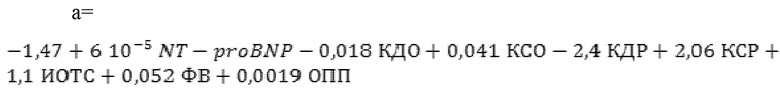
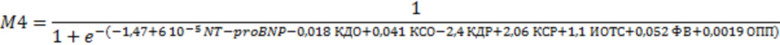
Для того, чтобы определить принадлежность пациента с ХСН к одному из метаболомных кластеров, необходимо рассчитать показатель М для каждого кластера, полученный наибольший процент будет свидетельствовать о принадлежности данного пациента к определенному кластеру.
Изобретение подтверждается следующими клиническими примерами.
Клинические примеры определения кластера с помощью предлагаемой формулы.
Клинический пример 1.
Пациент: женщина, 73 года, обратилась на амбулаторный прием к терапевту с жалобами на одышку при минимальной физической нагрузке и в покое, на отеки нижних конечностей, общую слабость. Была осмотрен терапевтом. В анамнезе: Постоянная форма фибрилляции предсердий, тахисистолия желудочков. Гипертоническая болезнь 3 степени. Острое нарушение мозгового кровообращения от 2016 г. При осмотре: Рост 160 см, вес 60 кг. ИМТ 23,44 кг/м2. Кожный покров обычной окраски, чистый. Температура тела в пределах нормальных значений. Над легкими аускультативно дыхание жесткое, ослаблено в нижних отделах, мелкопузырчатые хрипы. ЧДД 16 в минуту. Тоны сердца приглушены, ритм неправильный с ЧЖС 78-88 ударов в минуту. АД 120 и 75 мм рт.ст. Живот при пальпации мягкий, безболезненный, печень +2 см из-под края реберной дуги. Селезенка не пальпируется. Симптом Пастернацкого отрицательный. Отеков голеней и стоп симметричные.
Предположительный диагноз: Хроническая сердечная недостаточность?
Выполнено обследование: общий анализ крови, биохимический анализ крови, анализ мочи, оценка уровня NT-proBNP, электрокардиография, эхокардиография, рентгенография органов грудной клетки. В общем анализе крови и общем анализе мочи отклонений не выявлено. В биохимическом анализе крови обращает на себя внимание наличие гиперурикемии, дислипидемии. Уровень NT-proBNP 376 пг/мл. Электрокардиография: ритм фибрилляции предсердий с ЧЖС ср. 86 в минуту. Рентгенография органов грудной клетки: застойные явления в легких. Эхокардиография: КДР 4,3 см, КСР 2,8 см, КДО 85 мл, КСО 28 мл, ФВ 50%, гипертрофия миокарда левого желудочка (толщина межжелудочковой перегородки 16 мм, толщина задней стенки 14 мм), ОТС 0,70, ИММЛЖ 187 г/м2, расширение левого и правого предсердий и правого желудочка (объем левого предсердия 74 мл, объем правого предсердия 58 мл, правый желудочек 4,1 см), аортальная недостаточность 1 степени, митральная недостаточность 2 степени, трикуспидальная недостаточность 2 степени, легочная гипертензия (СДЛА 50 мм рт.ст.), уплотнение стенок аорты и створок аортального и митрального клапанов.
Таким образом у пациентки - ХСНсФВ и признаки дилатации полостей сердца и легочной гипертензии и может относиться как к кластеру 1, так и к кластеру 2. Для верификации фенотипа ХСН использована расчетная формула:
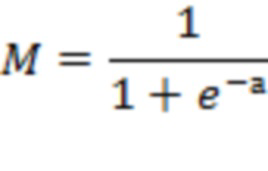
а= -1,02832
М1= 26%
а= -2,49906
М3= 7,59%
а= 1,91756
М2= 87,19%
а= -2,90124
М4= 5,21%
Максимальное значение М получено по формуле М2, что свидетельствует о соответствии пациента кластеру 2.
Добровольцу было предложено пройти скрининговое обследование с определением метаболомного профиля. На основе метаболомного профиля пациент был отнесен к кластеру 2.
Установлен диагноз: Гипертоническая болезнь 3 степени, III стадии, риск ССО 4. Нарушения ритма сердца: постоянная форма фибрилляции предсердий. Хроническая сердечная недостаточность с сохраненной фракцией выброса, III ФК по NYHA. Фенотип - «Метаболический фенотип» - кластер 2. Дислипидемия. Гиперурикемия. Острое нарушение мозгового кровообращения от 2016 г.
Таким образом необходимо начать терапию согласно клиническим рекомендациям по лечению ХСН с большим акцентом на лекарственную терапию, рекомендованную для ХСНсФВ.
Клинический пример 2.
Пациент: мужчина, 68 лет, обратился на амбулаторный прием к терапевту с жалобами на одышку при физической нагрузке, общую слабость. Был осмотрен терапевтом. В анамнезе: Ишемическая болезнь сердца: постинфарктный кардиосклероз (инфаркт миокарда от 2017г.). Гипертоническая болезнь 3 степени. Постоянная форма фибрилляции предсердий. Атеросклероз артерий нижних конечностей. При осмотре: Рост 178 см, вес 99 кг. ИМТ 31,24 кг/м2. Кожный покров бледно-розовый, чистый. Температура тела в пределах нормальных значений. Над легкими аускультативно дыхание везикулярное, ослабленное, хрипы не выслушиваются. ЧДД 19 в минуту. Тоны сердца приглушены, ритм неправильный с ЧЖС 98 ударов в минуту. АД 130 и 80 мм рт.ст. Живот при пальпации мягкий, безболезненный, печень у края реберной дуги. Селезенка не пальпируется. Симптом Пастернацкого отрицательный. Отеков голеней и стоп симметричные.
Предположительный диагноз: Хроническая сердечная недостаточность?
Выполнено обследование: общий анализ крови, биохимический анализ крови, анализ мочи, оценка уровня NT-proBNP, электрокардиография, эхокардиография, рентгенография органов грудной клетки. В общем анализе крови и общем анализе мочи отклонений не выявлено. В биохимическом анализе крови обращает на себя внимание наличие дислипидемии, гипергликемия, уровень гликированного гемоглобина 6,6%. Уровень NT-proBNP 17443 пг/мл. Электрокардиография: ритм фибрилляции предсердий с ЧЖС 86-121-153 в минуту. Рентгенография органов грудной клетки: признаки застойных явлений в легких, пневмосклероза. Эхокардиография: КДР 6,4 см, КСР 5,8 см, КДО 288 мл, КСО 211 мл, ФВ 26%, гипертрофия миокарда левого желудочка (толщина межжелудочковой перегородки 12 мм, толщина задней стенки 12 мм), ОТС 0,37, ИММЛЖ 188 г/м2, расширение всех камер сердца (объем левого предсердия 132 мл, объем правого предсердия 97 мл, правый желудочек 4,6 см), митральная недостаточность 2 степени, трикуспидальная недостаточность 2 степени, легочная гипертензия (СДЛА 49 мм рт.ст.), уплотнение стенок аорты и створок аортального и митрального клапанов, умеренное количество жидкости в полости перикарда (200 мл).
Таким образом у пациента - ХСНнФВ и признаки дилатации полостей сердца и легочной гипертензии и может относится как к кластеру 2, так и к кластеру 3 или 4. Для верификации фенотипа ХСН использована расчетная формула:
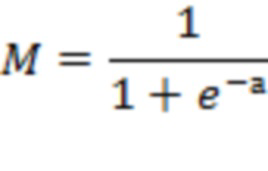
а= -3,65466
М1= 3%
а= -0,92459
М3= 28,40%
а= -10,2007
М2= 0,00%
а= 1,58038
М4= 82,93%
Максимальное значение М получено по формуле М4, что свидетельствует о соответствии пациента кластеру 4.
Добровольцу было предложено пройти скрининговое обследование с определением метаболомного профиля. На основе метаболомного профиля пациент был отнесен к кластеру 4.
Установлен диагноз:
Ишемическая болезнь сердца: постинфарктный кардиосклероз (инфаркт миокарда от 2017г.). Гипертоническая болезнь 3 степени, III стадии, риск ССО 4. Сахарный диабет 2 типа впервые выявленный. Целевое значение гликированного гемоглобина менее 8,0 %. Нарушения ритма сердца: постоянная форма фибрилляции предсердий. Хроническая сердечная недостаточность со сниженной фракцией выброса, III ФК по NYHA. Фенотип «Тяжелая декомпеснация ХСН» -кластер 4. Дислипидемия. Атеросклероз артерий нижних конечностей.
Таким образом необходимо начать терапию согласно клиническим рекомендациям по лечению ХСН с большим акцентом на лекарственную терапию, рекомендованную для ХСНнФВ.
Клинические примеры определения кластера с помощью «Дерева принятия решений».
Клинический пример 3.
Пациент: мужчина, 74 года, обратился на амбулаторный прием к терапевту с жалобами на одышку при физической нагрузке, перебои в работе сердца, нестабильность цифр АД, отеки ног.Был осмотрен терапевтом. В анамнезе: Ишемическая болезнь сердца: стенокардия 2 ФК. Постинфарктный кардиосклероз (инфаркт миокарда от 2017г.). Стенозирующий атеросклероз коронарных артерий (ствол левой коронарной артерии стеноз 40%, передняя межжелудочковая артерия стенозирована до 70%, огибающая артерия - 70%, правая коронарная артрерия - 50%). Балонная ангиопластика, стентирования передней межжелудочковой артерии и диагональной ветви в сентябре 2019г. Гипертоническая болезнь 3 степени. Дислипидемия. Сахарный диабет 2 типа. Атеросклероз артерий нижних конечностей, брахиоцефальных артерий. Пароксизмальная форма фибрилляции предсердий. Острое нарушение мозгового кровообращения в 2016 г. При осмотре: Рост 166 см, вес 75 кг. ИМТ 27,22 кг/м2. Кожный покров обычной окраски, чистый. Температура тела в пределах нормальных значений. Над легкими аускультативно дыхание везикулярное, хрипы не выслушиваются. ЧДД 16 в минуту. Тоны сердца приглушены, ритм правильный с ЧСС 80 ударов в минуту. АД 120 и 80 мм рт.ст. Живот при пальпации мягкий, безболезненный, печень у края реберной дуги. Селезенка не пальпируется. Симптом Пастернацкого отрицательный. Отеков голеней и стоп симметричные.
Предположительный диагноз: Хроническая сердечная недостаточность?
Выполнено обследование: общий анализ крови, биохимический анализ крови, анализ мочи, оценка уровня NT-proBNP, электрокардиография, эхокардиография.
В общем анализе крови и общем анализе мочи отклонений не выявлено. В биохимическом анализе крови обращает на себя внимание наличие гипергликемии. Уровень NT-proBNP 1642 пг/мл. Электрокардиография: ритм синусовый с ЧСС 41-69 в минуту, синусовая аритмия, изменения процессов реполяризации по передне-боковой стенке.
Эхокардиография: КДР 4,5 см, КСР 2,8 см, КДО 70 мл, КСО 31 мл, ФВ 56%, незначительная гипертрофия миокарда левого желудочка (толщина межжелудочковой перегородки 11 мм, толщина задней стенки 11 мм), ОТС 0,49, ИММЛЖ 188 г/м2, объем левого предсердия 56 мл, объем правого предсердия 52 мл, диастолическая дисфункция (Е/А 0,6), уплотнение стенок аорты и створок аортального и митрального клапанов.
Таким образом у пациента - ХСНсФВ и признаки дилатации полостей сердца и легочной гипертензии и может относится как к кластеру 1, так и к кластеру 2. Для верификации фенотипа ХСН использован алгоритм «Дерево принятия решений». Данные, полученные в ходе лабораторно-инструментального обследования (уровень NT-proBNP и параметры ЭХОКГ - КСР, КДР, КСО, КДО, ФВ, ИОТС, ОПП), позволили верификации фенотипа ХСН: кластер 1.
Установлен диагноз:
Ишемическая болезнь сердца: стенокардия 2 ФК. Постинфарктный кардиосклероз (инфаркт миокарда от 2017г.). Стенозирующий атеросклероз коронарных артерий (ствол левой коронарной артерии стеноз 40%, передняя межжелудочковая артерия стенозирована до 70%, огибающая артерия - 70%, правая коронарная артрерия - 50%). Балонная ангиопластика, стентирования передней межжелудочковой артерии и диагональной ветви в сентябре 2019г. Гипертоническая болезнь 3 степени. Дислипидемия. Сахарный диабет 2 типа. Атеросклероз артерий нижних конечностей, брахиоцефальных артерий. Пароксизмальная форма фибрилляции предсердий. Острое нарушение мозгового кровообращения в 2016г. Хроническая сердечная недостаточность с сохраненной фракцией выброса, III ФК по NYHA. Фенотип - «СНсФВ» - кластер 1.
Таким образом необходимо начать терапию согласно клиническим рекомендациям по лечению ХСН с большим акцентом на лекарственную терапию, рекомендованную для ХСНсФВ.
Клинический пример 4.
Пациент: мужчина, 66 лет, обратился на амбулаторный прием к терапевту с жалобами на одышку при незначительной физической нагрузке и в покое, отеки нижних конечностей. Был осмотрен терапевтом. В анамнезе: Ишемическая болезнь сердца: постинфарктный кардиосклероз (неизвестной давности). Гипертоническая болезнь 3 степени. АВ-блокада 2 степени. Имплантация ЭКС от 2019 года. Желудочковая экстрасистолия. Пароксизмы неустойчивой желудочковой тахикардии. Сахарный диабет 2 типа. Целевой уровень HbA1c менее 7,5%. Дислипидемия. При осмотре: Рост 178 см, вес 90 кг. ИМТ 28,40 кг/м2. Кожный покров бледно-розовый, чистый. Температура тела в пределах нормальных значений. Над легкими аускультативно дыхание жесткое, ослабленное в нижних отделах, хрипы в нижних отделах. ЧДД 19 в минуту. Тоны сердца приглушены, ритм правильный с ЧСС 75 ударов в минуту. АД 120 и 80 мм рт.ст. Живот при пальпации мягкий, безболезненный, печень у края реберной дуги. Селезенка не пальпируется. Симптом Пастернацкого отрицательный. Отеков голеней и стоп симметричные.
Предположительный диагноз: Хроническая сердечная недостаточность?
Выполнено обследование: общий анализ крови, биохимический анализ крови, анализ мочи, оценка уровня NT-proBNP, электрокардиография, эхокардиография, рентгенография органов грудной клетки. В общем анализе крови и общем анализе мочи отклонений не выявлено. В биохимическом анализе крови обращает на себя внимание наличие дислипидемии, гиперурикемии, гипергликемия. Уровень NT-proBNP 22564 пг/мл.
Электрокардиография: ритм синусовый с ЧСС 70 в минуту.
Рентгенография органов грудной клетки: признаки застойных явлений в легких.
Эхокардиография: КДР 6,8 см, КСР 5,7 см, КДО 240 мл, КСО 165 мл, ФВ 30%, гипертрофия миокарда левого желудочка (толщина межжелудочковой перегородки 12 мм, толщина задней стенки 12 мм), ОТС 0,35, ИММЛЖ 233 г/м2, расширение всех камер сердца (объем левого предсердия 135 мл, объем правого предсердия 89 мл, правый желудочек 4,3 см), митральная недостаточность 2 степени, трикуспидальная недостаточность 2 степени, легочная гипертензия (СДЛА 54 мм рт.ст.), уплотнение стенок аорты и створок аортального и митрального клапанов.
Таким образом у пациента - ХСНнФВ и признаки дилатации полостей сердца и легочной гипертензии и может относится как к кластеру 2, так и к кластеру 3 или 4. Для верификации фенотипа ХСН использован алгоритм «Дерево принятия решений». Данные, полученные в ходе лабораторно-инструментального обследования (уровень NT-proBNP и параметры ЭХОКГ - КСР, КДР, КСО, КДО, ФВ, ИОТС, ОПП), позволили верификации фенотипа ХСН: кластер 3.
Установлен диагноз:
Ишемическая болезнь сердца: постинфарктный кардиосклероз (неизвестной давности). Гипертоническая болезнь 3 степени, III стадии, риск ССО 4. Сахарный диабет 2 типа. Целевой уровень HbA1c менее 7,5%. Нарушения ритма и проводимости сердца: АВ-блокада 2 степени. Имплантация ЭКС от 2019 года. Желудочковая экстрасистолия. Пароксизмы неустойчивой желудочковой тахикардии. Хроническая сердечная недостаточность со сниженной фракцией выброса, III ФК по NYHA. Фенотип - «Ишемическая кардиомиопатия» - кластер 3. Дислипидемия.
Таким образом необходимо начать терапию согласно клиническим рекомендациям по лечению ХСН с большим акцентом на лекарственную терапию, рекомендованную для ХСНнФВ.
Предлагаемое изобретение позволяет использовать возможности метаболомного профилирования для быстрой и простой в использовании (требуется только забор крови) классификации ХСН, которая может явиться альтернативой классификации на основании большого количества дорогостоящих исследований с использованием сложных формул, включающих большое количество параметров. Более того, предлагаемая новая классификация позволяет охарактеризовать характер патогенетических процессов, что может помочь определить приоритеты в подборе терапии.
Список использованных источников:
1. World Health Statistics 2023 - Monitoring Health for the SDGs. 2023.
2. общество (РКО), Р. кардиологическое Хроническая сердечная недостаточность. Клинические рекомендации 2020. Российский кардиологический журнал 2020, 25, 4083.
3. Шляхто, Е.В. Классификация сердечной недостаточности: фокус на профилактику. Российский кардиологический журнал 2023, 28.
4. Книга «Вопросы кардиологии. Выпуск 1. Вопросы патологии кровообращения и клиники сердечно-сосудистых болезней (сборник)»;
5. Мареев, В.Ю.; Фомин, И.В.; Агеев, Ф.Т.; Беграмбекова, Ю.Л.; Васюк, Ю.А.; Гарганеева, А.А.; Гендлин, Г.Е.; Глезер, М.Г.; Готье, С.В.; Довженко, Т.В.; et al. КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ОССН - РКО - РНМОТ. СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ: ХРОНИЧЕСКАЯ (ХСН) И ОСТРАЯ ДЕКОМПЕНСИРОВАННАЯ (ОДСН). ДИАГНОСТИКА, ПРОФИЛАКТИКА И ЛЕЧЕНИЕ. Кардиология 2018, 58, 8-158, doi:10.18087/cardio.2475.
6. Ponikowski, P.; Voors, A.A.; Anker, S.D.; Bueno, H.; Cleland, J.G.F.; Coats, A.J.S.; Falk, V.; Gonz?lez-Juanatey, J.R.; Harjola, V.-P.; Jankowska, E.A.; et al. 2016 ESC Guidelines for the Diagnosis and Treatment of Acute and Chronic Heart Failure: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure of the European Society of Cardiology (ESC)Developed with the Special Contribution of the Heart Failure Association (HFA) of the ESC. European Heart Journal 2016, 37, 2129-2200, doi:10.1093/eurheartj/ehw128.
7. Heidenreich, P.A.; Bozkurt, B.; Aguilar, D.; Allen, L.A.; Byun, J.J.; Colvin, M.M.; Deswal, A.; Drazner, M.H.; Dunlay, S.M.; Evers, L.R.; et al. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation 2022, 145, e895-e1032, doi:10.1161/CIR.0000000000001063.
8. Anker, S.D.; Usman, M.S.; Anker, M.S.; Butler, J.; B?hm, M.; Abraham, W.T.; Adamo, M.; Chopra, V.K.; Cicoira, M.; Cosentino, F.; et al. Patient Phenotype Profiling in Heart Failure with Preserved Ejection Fraction to Guide Therapeutic Decision Making. A Scientific Statement of the Heart Failure Association, the European Heart Rhythm Association of the European Society of Cardiology, and the European Society of Hypertension. European Journal of Heart Failure 2023, 25, 936-955, doi:10.1002/ejhf.2894.
9. Nagamine, T.; Gillette, B.; Pakhomov, A.; Kahoun, J.; Mayer, H.; Burghaus, R.; Lippert, J.; Saxena, M. Multiscale Classification of Heart Failure Phenotypes by Unsupervised Clustering of Unstructured Electronic Medical Record Data. Sci Rep 2020, 10, 21340, doi:10.1038/s41598-020-77286-6.
10. Sowton, A.P.; Griffin, J.L.; Murray, A.J. Metabolic Profiling of the Diabetic Heart: Toward a Richer Picture. Frontiers in Physiology 2019, 10.
11. Li, Y.; Gray, A.; Xue, L.; Farb, M.G.; Ayalon, N.; Andersson, C.; Ko, D.; Benjamin, E.J.; Levy, D.; Vasan, R.S.; et al. Metabolomic Profiles, Ideal Cardiovascular Health, and Risk of Heart Failure and Atrial Fibrillation: Insights From the Framingham Heart Study. Journal of the American Heart Association 2023, 12, e028022, doi:10.1161/JAHA.122.028022.
12. Saleem, T.H.; Algowhary, M.; Kamel, F.E.M.; El-Mahdy, R.I. Plasma Amino Acid Metabolomic Pattern in Heart Failure Patients with Either Preserved or Reduced Ejection Fraction: The Relation to Established Risk Variables and Prognosis. Biomed Chromatogr 2021, 35, e5012, doi:10.1002/bmc.5012.
13. Moskaleva, N.E.; Shestakova, K.M.; Kukharenko, A.V.; Markin, P.A.; Kozhevnikova, M.V.; Korobkova, E.O.; Brito, A.; Baskhanova, S.N.; Mesonzhnik, N.V.; Belenkov, Y.N.; et al. Target Metabolome Profiling-Based Machine Learning as a Diagnostic Approach for Cardiovascular Diseases in Adults. Metabolites 2022, 12, 1185, doi:10.3390/metabo12121185.
Способ классификации хронической сердечной недостаточности на основе метаболомного профилирования
Таблица 1
Таблица 2
Таблица 3
Таблица 4
Таблица 5
(n=104)
(n=43)
(n=49)
(n =18)
pкластер 2 - кластер 3 = 0,048086
pкластер 2 - кластер 4= 0,003404
pкластер 1 - кластер 4= 0,035219
pкластер 2 - кластер 3 = 0,049245
* - различия показателей статистически значимы (p < 0,05).
Используемый метод: Хи-квадрат Пирсона.
Примечания: ПИКС - постинфарктный кардиосклерозз; ФП- фибрилляция предсердий; ХБП - хроническая болезнь почек.
Таблица 6
pкластер 1 - кластер 3 = 0,036995
* - различия показателей статистически значимы (p < 0,05)
Примечания: САД -систолическое артериальное давление, ЧСС - частота сердечных сокращений.
Таблица 7
1- ХСН+АГ, 2-ХСН+ИБС, 3-АГ, 4-ИБС, 5-Контроль
pкластер 2 - кластер 3 = 0,001900
pкластер 1 - кластер 3 = 0,001491
* - различия показателей статистически значимы (p < 0,05)
Примечания: АГ - артериальная гипертензия; ИБС -ишемическая болезнь сердца; ХСН -хроническая сердечная недостаточность.
Таблица 8
pкластер 2 - кластер 4 = 0,000365
pкластер 1 - кластер 4 = 0,000672
pкластер 2 - кластер 3 = 0,000066
pкластер 1 - кластер 3 = 0,000066
* - различия показателей статистически значимы (p < 0,05)
Примечания: Me [Q1-Q3] - медиана и квартили.
Таблица 9
95,0 - 160,0
90,0 - 148,0
128,0 - 196,0
131,0 - 195,0
pкластер 2 - кластер 4 = 0,011701
pкластер 1 - кластер 4 = 0,013597
pкластер 3 - кластер 2 = 0,000597
pкластер 1 - кластер 3 = 0,000352
58,58 - 89,54
55,22 - 79,28
71,215 - 114,51
85,11 - 115,81
pкластер 2 - кластер 4 = 0,005763
pкластер 1 - кластер 4 = 0,006316
pкластер 3 - кластер 2 = 0,000300
pкластер 1 - кластер 3 = 0,000145
40,0 - 92,0
45,6 - 86,0
64,0 - 135,0
70,0 - 142,0
pкластер 2 - кластер 4 = 0,007661
pкластер 1 - кластер 4 = 0,006293
pкластер 3 - кластер 2 = 0,000122
pкластер 1 - кластер 3 = 0,000007
4,7 - 5,6
4,6 - 5,4
5,2 - 6,4
5,3 - 6,0
pкластер 2 - кластер 4 = 0,022782
pкластер 1 - кластер 4 = 0,048467
pкластер 3 - кластер 2 = 0,000338
pкластер 1 - кластер 3 = 0,000434
3,3 - 4,5
3,4 - 4,4
3,8 - 5,2
4,1 - 5,3
pкластер 2 - кластер 4 = 0,010262
pкластер 1 - кластер 4 = 0,012856
pкластер 3 - кластер 2 = 0,000513
pкластер 1 - кластер 3 = 0,000384
11 - 13
12 - 14
11 - 13
11 - 13
10 - 12
11 - 12
10 - 12
10 - 12
0,39 - 0,48
0,42 - 0,50
0,34 - 0,45
0,33 - 0,45
pкластер 2 - кластер 4 = 0,001
pкластер 3 - кластер 2 = 0,008
pкластер 1 - кластер 3 = 0,002
207,0 - 286,0
207,0 - 276,0
219,7 - 305,3
230,0 - 287,0
102,0 - 138,03
103,0 - 136,0
110,6 - 147,6
117,0 - 149,0
50 - 70
45 - 68
51 - 67
47 - 63
38 - 58
42 - 55
28 - 46
26 - 49
pкластер 2 - кластер 4 = 0,043767
pкластер 1 - кластер 4 = 0,003714
pкластер 3 - кластер 2 = 0,000635
pкластер 1 - кластер 3 < 0,000001
0,70 - 0,86
0,70 - 0,82
0,78 - 1,80
0,73 - 2,10
3,1 - 4,2
3,4 - 4,4
3,6 - 4,6
3,9 - 4,6
pкластер 1 - кластер 4 = 0,013817
pкластер 1 - кластер 3 = 0,001197
0,4 - 0,4
0,3 - 0,4
0,3 - 0,4
0,4 - 0,4
64 - 100
68 - 99
77 - 114
73 - 125
pкластер 1 - кластер 3 = 0,019097
38,47 - 56,34
41,03 - 56,66
43,12 - 4259
46,71 - 71,90
pкластер 1 - кластер 3 = 0,039134
46 - 80
46 - 75
60 - 89
52 - 97
pкластер 3 - кластер 2 = 0,008059
pкластер 1 - кластер 3 = 0,007842
28,98 - 46,07
26,35 - 44,12
30,00 - 44,48
32,91 - 57,88
1,7 - 2,2
1,7 - 2,4
2,0 - 2,4
1,8 - 2,5
pкластер 1 - кластер 3 = 0,004867
27 - 48
27 - 51
34 - 54
35 - 62
pкластер 1 - кластер 4 = 0,029069
pкластер 1 - кластер 3 = 0,011055
Используемый метод: Критерий Краскела-Уоллиса.
Примечания: Me [Q1-Q3] - медиана и квартили, М±SD - среднее ± стандартное отклонение, м- мужской пол, ж - женский пол.
Е/А - отношение скоростей раннего (E) и позднего (A) наполнения левого желудочка, АГ - артериальная гипертензия, ТЗС - толщина задней стенки, ИММЛЖ - индекс массы миокарда левого желудочка, ИОЛП - индекс объема левого предсердия, ИОПП - индекс объема правого предсердия, ИОТС - индекс относительной толщины стенки, КДО - конечно-диастолический объем, КДР - конечно-диастолический размер, КСО - конечно-систолический объем, КСР - конечно-систолический размер, ЛЖ - левый желудочек, МЖП - межжелудочковая перегородка, ММЛЖ - масса миокарда левого желудочка, ОЛП - объем левого предсердия, ОПП - объем правого предсердия, ПЖ - правый желудочек, СДЛА - систолическое давление в легочной артерии, УО - ударный объем, ФВ - фракция выброса.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностики сердечной недостаточности с сохраненной фракцией выброса | 2023 |
|
RU2814392C1 |
| СПОСОБ ДИАГНОСТИКИ ФУНКЦИОНАЛЬНОГО КЛАССА ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2012 |
|
RU2526800C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ЛЕТАЛЬНОГО ИСХОДА У КОМОРБИДНЫХ ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2024 |
|
RU2838522C1 |
| Способ диагностики дисфункции миокарда при сохраненной фракции выброса левого желудочка в зависимости от состояния мембранного потенциала лейкоцитов крови у пациентов с инфарктом миокарда | 2023 |
|
RU2832976C1 |
| Способ диагностики хронической сердечной недостаточности у пациентов с артериальной гипертензией и синдромом старческой астении в возрасте 80 лет и старше | 2024 |
|
RU2832935C1 |
| Способ прогнозирования развития ремоделирования левого желудочка после инфаркта миокарда с подъемом сегмента ST и сердечной недостаточности с использованием многофакторной регрессионной модели | 2022 |
|
RU2806237C1 |
| Способ прогнозирования положительного ответа на терапию модуляции сердечной сократимости у пациентов с хронической сердечной недостаточностью со сниженной фракцией выброса левого желудочка и фибрилляцией предсердий | 2023 |
|
RU2807230C1 |
| Способ диагностики сердечной недостаточности с сохраненной фракцией выброса левого желудочка у пациентов с ишемической болезнью сердца на фоне неокклюзирующего атеросклероза коронарных артерий | 2022 |
|
RU2789429C1 |
| Способ прогнозирования развития неблагоприятных сердечно-сосудистых событий у больных с острой декомпенсацией ишемической хронической сердечной недостаточности с систолической дисфункцией левого желудочка сердца после полной реваскуляризации миокарда | 2021 |
|
RU2770271C1 |
| Способ прогнозирования риска прогрессирования хронической сердечной недостаточности у пациентов с перенесенным инфарктом миокарда | 2019 |
|
RU2734671C1 |

Группа иобретений относится к медицине, а именно к кардиологии, и может быть использована для определения фенотипа хронической сердечной недостаточности из четырех фенотипов: фенотипа хронической сердечной недостаточности с сохраненной фракцией выброса, метаболического фенотипа, фенотипа ишемической кардиомиопатии, фенотипа тяжелой декомпенсации хронической сердечной недостаточности двумя способами. Проводят забор крови у пациентов с хронической сердечной недостаточностью. В первом способе с помощью количественного хромато-масс-спектрометрического анализа в плазме крови определяют концентрацию циркулирующих метаболитов: ацилкарнитинов: С5-ОН, С6-DC, C14, C12, C18-1, C6, C5-DC, C5-1, C8-1, C10, C16-1, C16, C14-2, C12-1; метаболитов триптофан-кинуренинового пути: хинолоновой кислоты, ксантуриновой кислоты, 3-ОН-антраниловой кислоты, триптофана; и триптофан-серотонинового пути: 5-метилтриптамина, 5-гидрокситриптофана; метаболитов цикла глутамин-глутамат: глутамина, глутамата; аминокислоты серина; витамина рибофлавина; метионин сульфоксида и нейромедиатора норэпинефрина. При помощи методов машинного обучения определяют фенотип пациентов с хронической сердечной недостаточностью, в соответствии с коэффициентами 26 метаболитов, представленными в таблице 4 описания. Методом главных компонент проводят предварительное понижение размерности данных до девяти главных компонент и далее выполняют иерархический кластерный анализ, при котором расстояние между кластерами определяют по методу Уорда. Во втором способе определяют в плазме крови концентрацию N-концевого фрагмента натрийуретического пептида (NT-proBNP). Проводят эхокардиографию, определяют параметры эхокардиографии: конечный систолический размер левого желудочка, конечный диастолический размер левого желудочка, конечный систолический объем левого желудочка, конечный диастолический объем левого желудочка, фракцию выброса, индекс относительной толщины стенки левого желудочка, объем правого предсердия. Рассчитывают каждый из четырех показателей фенотипов М1-М4 по заявленным формулам. Проводят сравнение показателей М1, М2, М3 и М4. Выбирают показатель с наибольшим процентом. При наибольшем показателе М1 определяют фенотип хронической сердечной недостаточности с сохраненной фракцией выброса. При наибольшем М2 - метаболический фенотип. При наибольшем М3 - фенотип ишемической кардиомиопатии. При наибольшем М4 - фенотип тяжелой декомпенсации хронической сердечной недостаточности. Способы обеспечивают возможность повышения точности определения фенотипа хронической сердечной недостаточности из четырех заявленных фенотипов за счет распределения пациентов с хронической сердечной недостаточностью на феногруппы при помощи биостатистической обработки результатов количественного определения 26 выделенных метаболитов плазмы крови, а также определения концентрации NT-proBNP в крови и параметров эхокардиографии. 2 н.п. ф-лы, 3 ил. 11 табл., 4 пр.
1. Способ определения фенотипа хронической сердечной недостаточности из четырех фенотипов: фенотипа хронической сердечной недостаточности с сохраненной фракцией выброса, метаболического фенотипа, фенотипа ишемической кардиомиопатии, фенотипа тяжелой декомпенсации хронической сердечной недостаточности, включающий забор крови у пациентов с хронической сердечной недостаточностью, характеризующийся тем, что с помощью количественного хромато-масс-спектрометрического анализа в плазме крови определяют концентрацию циркулирующих метаболитов: ацилкарнитинов: С5-ОН, С6-DC, C14, C12, C18-1, C6, C5-DC, C5-1, C8-1, C10, C16-1, C16, C14-2, C12-1; метаболитов триптофан-кинуренинового пути: хинолоновой кислоты, ксантуриновой кислоты, 3-ОН-антраниловой кислоты, триптофана; и триптофан-серотонинового пути: 5-метилтриптамина, 5-гидрокситриптофана; метаболитов цикла глутамин-глутамат: глутамина, глутамата; аминокислоты серина; витамина рибофлавина; метионин сульфоксида и нейромедиатора норэпинефрина; затем при помощи методов машинного обучения определяют фенотип пациентов с хронической сердечной недостаточностью, в соответствии с коэффициентами 26 метаболитов, представленными в таблице 4 описания, для чего методом главных компонент проводят предварительное понижение размерности данных до девяти главных компонент и далее выполняют иерархический кластерный анализ, при котором расстояние между кластерами определяют по методу Уорда:
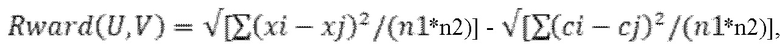
где
xi и xj – средние значения признаков объектов в кластерах U и V соответственно;
ci и cj – средние значения признаков объектов в объединенном кластере;
n1 и n2 – количество объектов в кластерах U и V соответственно;
U и V – кластеры, между которыми определяется расстояние.
2. Способ определения фенотипа хронической сердечной недостаточности из четырех фенотипов: фенотипа хронической сердечной недостаточности с сохраненной фракцией выброса, метаболического фенотипа, фенотипа ишемической кардиомиопатии, фенотипа тяжелой декомпенсации хронической сердечной недостаточности, включающий забор крови у пациентов с хронической сердечной недостаточностью, характеризующийся тем, что определяют в плазме крови концентрацию N-концевого фрагмента натрийуретического пептида (NT-proBNP), проводят эхокардиографию, определяют параметры эхокардиографии: конечный систолический размер левого желудочка, конечный диастолический размер левого желудочка, конечный систолический объем левого желудочка, конечный диастолический объем левого желудочка, фракцию выброса, индекс относительной толщины стенки левого желудочка, объем правого предсердия, и рассчитывают каждый из четырех показателей фенотипов М1-М4 по формуле: 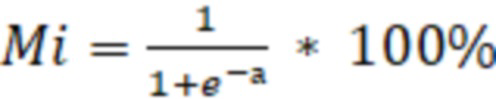 , где i = 1-4,
, где i = 1-4,
расчетный показатель M для каждого фенотипа определяют по следующим формулам:
для фенотипа 1:
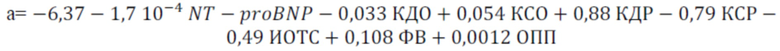

для фенотипа 2:

для фенотипа 3:

для фенотипа 4:
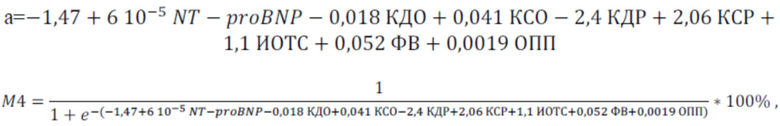
где NT-proBNP – концентрация N-концевого фрагмента натрийуретического пептида, пг/мл;
КДО – конечный диастолический объем левого желудочка, мл;
КСО – конечный систолический объем левого желудочка, мл;
КДР – конечный диастолический размер левого желудочка, см;
КСР – конечный систолический размер левого желудочка, см;
ИОТС – индекс относительной толщины стенки левого желудочка;
ОПП – объем правого предсердия, мл;
ФВ – фракция выброса левого желудочка, %;
проводят сравнение показателей М1, М2, М3 и М4, выбирают показатель с наибольшим процентом, и при наибольшем показателе М1 определяют фенотип хронической сердечной недостаточности с сохраненной фракцией выброса, при наибольшем М2 - метаболический фенотип, при наибольшем М3 - фенотип ишемической кардиомиопатии, при наибольшем М4 - фенотип тяжелой декомпенсации хронической сердечной недостаточности.
| ЦЫГАНКОВА О.В | |||
| и др | |||
| Фенотипические кластеры пациентов с хронической сердечной недостаточностью с сохраненной и промежуточной фракцией выброса: новые данные и перспективы | |||
| Российский кардиологический журнал | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| ДРАГОМИРЕЦКАЯ Н.А | |||
| и др | |||
| Фенотипические кластеры и профиль биомаркеров у больных с хронической сердечной | |||
Авторы
Даты
2025-06-04—Публикация
2024-09-30—Подача