ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к нутрицевтической офтальмологической композиции, содержащей, в частности, ресвератрол, предназначенной для введения субъекту, получающему средство лечения, противодействующее VEGF, в частности, в рамках контроля патологии сетчатки с неоваскулярным компонентом.
Настоящая заявка демонстрирует, что совместное введение такой композиции и средства, противодействующего VEGF, оказывает благоприятный эффект на уровень вырабатываемого VEGF и открывает многообещающие перспективы для лечения этих заболеваний глаз.
УРОВЕНЬ ТЕХНИКИ
По всей Европе большинство случаев слепоты и тяжелой потери зрения вызваны возрастными заболеваниями сетчатки. С учетом текущих демографических тенденций ожидается, что распространенность и частота встречаемости этих заболеваний будет возрастать. Значительное давление на европейские системы здравоохранения будет одним из прямых экономических последствий.
На сегодняшний день возрастная макулярная дегенерация (AMD) поразила примерно 34 миллионов человек в Европе. Ожидается, что число пациентов с AMD увеличится почти на 25% к 2050 году с учетом предполагаемого характера роста и старения населения. Кроме того, текущая и будущая ситуация является аналогичной для заболеваний глаз, связанных с диабетом, в том числе диабетического макулярного отека (DMO). Более 25% пациентов с диабетом поражены диабетическими заболеваниями глаз (DED), что составляет почти 4 миллиона человек по всей Европе. Поскольку распространенность диабета значительно возрастает вследствие демографических тенденций и изменений образа жизни, этот тип заболевания также будет нарастать.
В частности, AMD является ведущей причиной ухудшения зрения у людей в возрасте старше 50 лет. Во всех своих формах это заболевание поражает приблизительно 8% населения Франции, но его частота значительно увеличивается с возрастом: оно поражает 1% людей в возрасте от 50 до 55 лет, примерно 10% людей в возрасте от 65 до 75 лет и от 25% до 30% людей в возрасте более 75 лет. Если учитывать только поздние формы заболевания в сочетании с потерей центрального зрения, эти цифры можно уменьшить примерно вдвое.
Заболевание избирательно поражает область желтого пятна, т. е. центральную зону сетчатки, что приводит к прогрессирующей потере центрального зрения, а именно поля зрения, пригодного для чтения, распознавания лиц или вождения и т. д. Это является основной причиной слабого зрения у пожилых людей.
Заболевание начинается с ранней недегенеративной фазы, называемой возрастной макулопатией (ARM или «ранняя стадия сухой формы»). Эта фаза характеризуется накоплением небольших беловатых отложений (или «мягких друз») внутри и вокруг желтого пятна. Эти отложения видны при простом осмотре глазного дна. Эта фаза обычно является бессимптомной, но пациент может ощущать искажения прямых линий («метаморфопсии») и размытые пятна.
На самых поздних стадиях появляются симптомы, различающиеся в зависимости от тяжести заболевания:
• снижение остроты зрения с необходимостью лучшего освещения для чтения или любой точной работы;
• все более размытое центральное зрение, изменение цветового восприятия, искажение прямых линий, которые кажутся искаженными и искривленными;
• появление темного пятна в центре поля зрения, называемого скотомой, трудности с распознаванием лиц, зрительные галлюцинации или резкое снижение остроты зрения;
• серьезное повреждение второго глаза сильно варьируется между субъектами: оно может появиться быстро, в течение одного года, в течение 10 лет или вообще не появиться.
ARM может оставаться стабильной на протяжении всей жизни. Тем не менее, примерно в половине случаев и под влиянием нескольких факторов ARM переходит в поздние дегенеративные формы:
- атрофическую форму, представляющую собой сухую форму, при которой желтое пятно с возрастом атрофируется и постепенно замещается рубцовой тканью; или
- влажную форму, которая представляет собой экссудативную форму, при которой под желтым пятном развиваются мелкие кровеносные сосуды. Эти вновь образованные сосуды легко кровоточат и поэтому ответственны за экссудаты и кровоизлияния глазного дна. Если экссудативная AMD присутствует на одном глазу, существует риск ее развития на втором глазу.
Эти две поздние формы характеризуются примерно равнозначным влиянием. Они вызывают необратимое повреждение желтого пятна и потерю центрального зрения, поражающие только один глаз или оба глаза. Могут наблюдаться смешанные формы.
С точки зрения механизма влажная форма AMD, называемая неоваскулярной или экссудативной AMD, а также диабетическая ретинопатия, макулярный отек, окклюзия вены сетчатки (RVO) или даже сильная миопия приводят к разрастанию новых аномальных сосудов под сетчаткой. Эти хрупкие сосуды позволяют диффундировать сыворотке крови, которая отвечает за поднятие сетчатки, и/или крови, вызывая появление кровоизлияний в сетчатку. Эта форма быстро развивается, если ее не лечить, с потерей зрения в течение нескольких недель или даже нескольких дней. Этот процесс можно замедлить, принимая лекарственные препараты типа средств, противодействующих VEGF.
VEGF (фактор роста эндотелия сосудов) представляет собой фактор роста сосудистого эндотелия, который играет роль в процессах ангиогенеза, т. е. прорастания уже существующих сосудов, и васкулогенеза, соответствующего образованию новых сосудов из эндотелиальных предшественников. VEGF, и более конкретно изоформа VEGF-A, связывается с поверхностью рецепторов с тирозинкиназной активностью, в частности VEGF-R1 и VEGF-R2, которые играют ключевую роль в ангиогенезе.
Таким образом, с 2006 года определенные заболевания глаз, такие как влажная форма AMD (или «влажная AMD»), лечили с помощью ингибиторов VEGF. Эти методы лечения также все больше применяются при лечении других неоваскулярных заболеваний, таких как диабетический макулярный отек (DMO или DME), окклюзия вены сетчатки (RVO) или миопическая хориоидальная неоваскуляризация (CNV или PM).
Средства, противодействующие VEGF, включают, в частности, антитела или фрагменты антител, направленные против VEGF, или рекомбинантные белки, способные связываться с рецепторами VEGF. Примеры включают ранибизумаб (например, LUCENTIS®, продаваемый NOVARTIS PHARMA SAS, или его биоаналоги, разработанные в SAMSUNG, INTAS или FORMYCON), бевацизумаб (например, AVASTIN®, продаваемый ROCHE), афлиберцепт (например, EYLEA®, продаваемый BAYER SANTE), абиципар пегол (разрабатываемый в ALLERGAN), конберцепт (например, продукт, разрабатываемый CHENGDU KANGHON BIOTECH INC), фарицимаб (например, продукт RG7716, разрабатываемый в ROCHE) или бролуцизумаб (NOVARTIS).
Эти средства, противодействующие VEGF, обычно вводят путем интравитреальной инъекции, т. е. инъекции через конъюнктиву и склеру непосредственно в полость глаза за хрусталиком, т. е. полость стекловидного тела, содержащую стекловидное тело.
Это предусматривает прямую инъекцию лекарственных препаратов в глаз. Этот метод лечения имеет несколько преимуществ по сравнению с другими путями введения, в частности местным:
- уменьшение количества активного ингредиента;
- более эффективное действие;
- эффективное нацеливание на область, подлежащую обработке;
- уменьшение нежелательных эффектов или уменьшение прохождения в системный кровоток.
Однако интравитреальная инъекция остается технической процедурой, выполняемой специализированными практикующими работниками и требующей особых асептических и антисептических условий. Более того, эта инъекция может быть причиной определенного количества довольно проблемных побочных эффектов: эндофтальмита, отслоения сетчатки, глазной гипертензии/глаукомы, катаракты, воспаления, субконъюнктивального кровоизлияния, системной токсичности, воспаления, появления «плавающих тел» и т. д. Кроме того, обычно не рекомендуется выполнять инъекции в оба глаза в один и тот же день, чтобы избежать полной потери зрения в случае проблем или побочных эффектов после инъекции. В действительности за этими инъекциями обычно следует очень болезненный период для пациентов, который может потребовать от них провести несколько часов в полной темноте.
Дозировка, в частности доза и частота введения, могут в значительной степени зависеть от активного ингредиента, а также от патологии, подлежащей лечению, при среднем количестве семь инъекций в год.
Например, лечение AMD с помощью ранибизумаба или бевацизумаба начинается с индукционной фазы с 1 инъекцией в месяц в течение 3 последовательных месяцев, за которой следует поддерживающая фаза, во время которой проверяют остроту зрения пациентов один раз в месяц. Если у пациента наблюдается потеря остроты зрения более чем на 5 букв по шкале «Исследование раннего лечения диабетической ретинопатии» (ETDRS) или эквивалентно одной строке по шкале Снеллена, средство следует ввести повторно. Интервал между 2 дозами должен быть не менее 1 месяца.
Что касается DMO, рекомендуются ежемесячные инъекции ранибизумаба или бевацизумаба до стабилизации остроты зрения при трех последовательных ежемесячных оценках в рамках лечения.
Что касается RVO, рекомендуются ежемесячные инъекции ранибизумаба или бевацизумаба до стабилизации остроты зрения. Отсутствие улучшения остроты зрения после 3 последовательных ежемесячных инъекций служит основанием для прекращения лечения.
При наличии афлиберцепта протокол немного отличается.
Что касается AMD, в начале лечения, как и в случае с другими средствами, противодействующими VEGF, афлиберцепт инъецируют один раз в месяц в течение 3 последовательных месяцев, затем выполняют одну инъекцию каждые 2 месяца без визитов последующего наблюдения между инъекциями. После первых 12 месяцев лечения интервал между 2 инъекциями может быть увеличен в зависимости от результатов исследования зрительной функции и анатомических структур. В этом случае график последующих наблюдений должен определять врач, проводящий лечение, и визиты последующего наблюдения могут быть более частыми, чем запланированные инъекции.
Что касается RVO, рекомендуемая доза составляет 2 мг афлиберцепта, что соответствует 50 мкл. После первой инъекции лечение проводят ежемесячно. Интервал между 2 инъекциями должен быть не менее 1 месяца. Если после первых трех инъекций не наблюдается улучшения зрительных и анатомических параметров, то дальнейшее лечение не рекомендуется. Ежемесячное лечение продолжают до достижения стабильных результатов исследования зрительной функции и анатомических структур во время трех ежемесячных оценок. Затем можно повторно оценить необходимость дальнейшего лечения. При необходимости лечение можно продолжить с постепенным увеличением интервала между инъекциями для поддержания ответа со стороны зрительной функции и анатомических структур.
Параллельно с этими методами лечения с применением средств, противодействующих VEGF, вводимых путем интравитреальной инъекции, применяют другие методики для разрушения вновь образованных сосудов, в частности фотокоагуляцию (термическое разрушение аномальных сосудов) и фотодинамическую терапию. Последняя методика предусматривает внутривенную инъекцию фоточувствительного продукта (например, вертепорфина), который становится токсичным под действием красного света, применяемого локально с помощью лазера.
До этих тяжелых методов лечения, которые проводят на поздних стадиях заболевания, проводились исследования в попытке найти более ранние и «более легкие» методы лечения с целью предупреждения начала проявления и задержки прогрессирования заболевания.
Таким образом, исследования под названием AREDS 1 (Age-Related Eye Disease Study Research Group. A Randomized, Placebo-Controlled, Clinical Trial of High-Dose Supplementation With Vitamins C and E, Beta Carotene, and Zinc for Age-Related Macular Degeneration and Vision Loss: AREDS Report No. 8 and 9. Arch Ophthalmol. 2001) и AREDS 2 (Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013 May 15; 309(19):2005-15. doi: 10.1001/jama.2013.4997) проводили, чтобы продемонстрировать благоприятный эффект биологически активных добавок в отношении заболеваний глаз.
Эти исследования выявили, что биологически активные добавки на основе антиоксидантов потенциально являются благоприятными в отношении лечения заболеваний глаз, в частности возрастных заболеваний, особенно AMD.
На практике в исследовании AREDS 1 рекомендуется ежедневный прием антиоксидантов, таких как микроэлементы и витамины, как указано ниже:
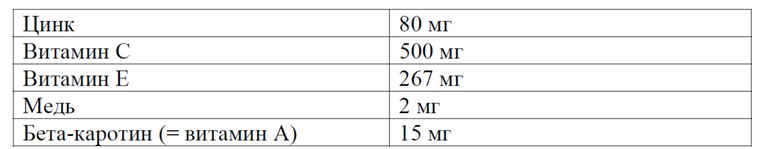
Эти добавки могут снизить риск потери зрения у пациентов с AMD на поздней стадии.
Исследование AREDS 2 проводили для иллюстрации эффектов добавок на основе лютеина, зеаксантина (в качестве заменителя бета-каротина) и омега-3-жирных кислот. В этом исследовании рекомендовалось исключить витамин A и сообщалось о пользе дополнительного ежедневного приема следующих веществ:
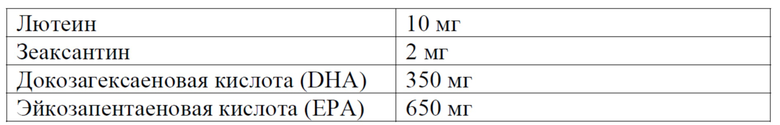
Таким образом, на основании результатов исследований AREDS рекомендуется ежедневно принимать биологически активные добавки людям с высоким риском развития AMD, особенно пациентам с ARM на одном или обоих глазах, а также пациентам с AMD на поздней стадии, которая затрагивает все еще только один глаз. Однако данные исследования не проиллюстрировали положительный эффект этих составов в отношении прогрессирования заболевания у пациентов с AMD на поздней стадии или в отношении потери зрения.
В исследовании NAT 2 (Merle et al., Invest Ophthalmol Vis Sci. 2014 Mar 28;55(3):2010-9. doi: 10.1167/iovs.14-13916), включающем 300 пациентов за период трех лет, продемонстрировано 68% снижение рисков развития неоваскулярной AMD после значительного увеличения количества DHA в клетках. Таким образом, это исследование является первым, в котором изучается потенциал длительного перорального приема добавок на основе DHA для предупреждения развития AMD.
Наконец, в документе WO 2016/151269 описаны биологически активная добавка, в которой сочетаются витамины, микроэлементы, каротиноиды, омега-3-жирные кислоты и ресвератрол, и ее применение для лечения и/или предупреждения заболеваний глаз. В частности, в этом документе сообщается, что комбинация различных перечисленных соединений оказывает дифференциальное и благоприятное действие на экспрессию и активность VEGF или его рецепторов (VEGF-R).
Однако существует очевидная потребность в разработке новых решений для улучшения контроля заболеваний глаз, в частности заболеваний сетчатки с неоваскулярным компонентом, отвечающих, в частности, следующим ожиданиям: увеличение интервалов между интравитреальными инъекциями средства, противодействующего VEGF, уменьшение связанных с ними побочных эффектов, снижение затрат на общественное здравоохранение и улучшение качества жизни пациентов.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Заявитель проиллюстрировал, что введение биологически активной добавки позволит увеличить, продлить или даже улучшить эффекты применяемых в настоящее время средств лечения, противодействующих VEGF, в частности средств лечения, вводимых путем интравитреальной инъекции, у пациентов, получающих такие методы лечения.
Согласно своему первому аспекту настоящее изобретение относится к нутрицевтической офтальмологической композиции, содержащей ресвератрол, и введению такой композиции субъекту, получающему средство лечения, противодействующее VEGF, в частности, подвергающемуся лечению с помощью средства, противодействующего VEGF.
В рамках объема настоящего изобретения «нутрицевтическая композиция» определяется как композиция, предназначение которой состоит в том, чтобы дополнять нормальный рацион и представлять собой концентрированный источник питательных веществ или других веществ, которые обладают питательным или физиологическим эффектом по отдельности или в комбинации. Она преимущественно предусматривает биологически активную добавку.
В рамках объема настоящего изобретения композиция со свойствами, благоприятными для здоровья глаз, называется «офтальмологической композицией». Однако это не исключает возможности того, что такая композиция может оказывать благоприятный эффект на другие органы человека или животных.
Ресвератрол представляет собой полифенольное соединение, являющееся производным стильбена, у которого есть два изомера, но преимущественно активной является транс-форма. Поэтому в остальной части настоящего описания термин «ресвератрол» может использоваться вместо транс-ресвератрола.
Ресвератрол представляет собой полифенол, в обильных количествах присутствующий в определенных плодах, в частности в винограде, семенах масличных культур и вине. В настоящее время существует несколько коммерческих источников ресвератрола, которые можно использовать для получения композиции, входящей в объем настоящего изобретения:
• Vitis vinifera:
• кожица винограда
• семя винограда
• Polygonum cuspidatum:
• получение путем ферментации
Предпочтительные источники включают:
- источник ресвератрола Vitis vinifera, кожица винограда: например, натуральный экстракт с содержанием 5%;
- 99% синтетический ресвератрол (номер CAS: 501–36–0).
Ресвератрол преимущественно присутствует в количестве (суточной дозе), которое больше или равняется 1 мг, или даже 2 мг, 5 мг, 10 мг, 20 мг, 30 мг, 50 мг, 60 мг, или даже 100 мг или 200 мг. Согласно конкретному варианту осуществления его суточное количество больше или равняется 20 мг или даже больше 20 мг, больше или равняется 30 мг или даже больше 30 мг, больше или равняется 50 мг, больше или равняется 60 мг или даже больше или равняется 100 мг. Преимущественно оно меньше или равняется 1 г, предпочтительно меньше или равняется 500 мг, особенно предпочтительно меньше или равняется 200 мг. Согласно конкретному варианту осуществления композиция, входящая в объем настоящего изобретения, содержит суточную дозу ресвератрола, равную 50 мг, 60 мг, 70 мг, 80 мг, 90 мг, 100 мг, 150 мг или 200 мг.
Согласно преимущественному варианту осуществления композиция дополнительно содержит витамины, микроэлементы, каротиноиды и омега-3-жирные кислоты. Ингредиенты, представляющие собой витамины, микроэлементы, омега-3-жирные кислоты и каротиноиды, известные своими антиоксидантными свойствами, еще более преимущественно выбраны в соответствии с рекомендациями исследований AREDS.
Согласно конкретному варианту осуществления композиция содержит по меньшей мере один витамин, преимущественно комбинацию витаминов. Она преимущественно содержит витамин C и/или витамин E.
Также это могут быть следующие витамины:
- никотинамид, ниацинамид или витамин B3 или PP;
- пиридоксин, например, в форме пиридоксина-HCl, или витамин B6;
- рибофлавин или витамин В2;
- тиамин, например, в форме нитрата тиамина, или витамин B1;
- цианокобаламин или витамин B12;
- фолиевая кислота или витамин B9;
- витамин B5;
- витамин B8;
- витамин D.
Витамин C, доступный в форме аскорбиновой кислоты или аскорбата кальция, преимущественно присутствует в количестве (суточной дозе) от 50 мг до 500 мг, например 240 мг или 120 мг.
Витамин E или альфа-токоферол, например, доступный в форме 67% масла, преимущественно присутствует в количестве (суточной дозе) от 10 мг до 500 мг, например, равном 30 мг.
Согласно другому варианту осуществления следующие суточные количества, выраженные в мг, могут рассматриваться для следующих витаминов:
- витамин B3 или PP: от 1 до 100, например 18;
- витамин B6: от 1 до 10, например 2;
- витамин B2: от 1 до 10, например 1,6;
- витамин B1: от 1 до 10, например 1,4;
- витамин B12: от 0,0005 до 0,01, например 0,001;
- витамин B9: от 0,1 до 1, например 0,2.
Согласно конкретному варианту осуществления композиция не содержит витамин A или бета-каротин.
Согласно конкретному варианту осуществления композиция содержит по меньшей мере один микроэлемент, преимущественно комбинацию микроэлементов. Она преимущественно содержит цинк (Zn) и/или медь (Cu). Также это могут быть следующие микроэлементы:
- марганец, например безводный сульфат марганца;
- селен, например селенит натрия;
- магний, например оксид магния.
Цинк (Zn), доступный в виде оксида цинка или (моногидрата) сульфата цинка, преимущественно присутствует в количестве (суточной дозе) от 5 мг до 100 мг, например 12,5 мг.
Медь (Cu), доступная в форме сульфата меди, моногидрата меди или безводной меди, преимущественно присутствует в количестве (суточной дозе) от 0,2 мг до 10 мг, например, в количестве, равном 1 мг.
Согласно другому варианту осуществления следующие суточные количества, выраженные в мг, могут рассматриваться для следующих микроэлементов:
- марганец: от 1 мг до 10 мг, например 1 мг;
- селен: от 0,01 мг до 0,1 мг, например 0,025 мг; и
- магний: от 1 мг до 50 мг, например 10 мг.
Согласно конкретному варианту осуществления композиция содержит по меньшей мере один каротиноид, преимущественно комбинацию каротиноидов. Она преимущественно содержит лютеин и/или зеаксантин. Также это могут быть следующие каротиноиды:
- мезозеаксантин;
- ликопин;
- астаксантин.
Лютеин, доступный в форме 20% лютеина по весу, преимущественно присутствует в количестве (суточной дозе) от 2 мг до 50 мг, например 10 мг или 20 мг.
Зеаксантин, доступный в форме 5% или 14% зеаксантина по весу, преимущественно присутствует в количестве (суточной дозе) от 0,5 мг до 10 мг, например, равном 2 мг или 4 мг.
Согласно конкретному варианту осуществления композиция содержит по меньшей мере одну полиненасыщенную жирную кислоту омега-3-типа, преимущественно комбинацию омега-3-жирных кислот. Она преимущественно содержит эйкозапентаеновую кислоту (EPA) и/или докозагексаеновую кислоту (DHA). Также это могут быть следующие омега-3-жирные кислоты:
- альфа-линоленовая кислота (ALA);
- докозапентаеновая кислота (DPA).
Согласно конкретному варианту осуществления композиция содержит по меньшей мере одну полиненасыщенную жирную кислоту омега-3-типа, преимущественно комбинацию омега-3-жирных кислот.
Омега-3-жирные кислоты, применяемые в такой композиции, могут быть получены из рыбьего жира, богатого омега-3-жирными кислотами, или из растительного масла, например льняного масла. Эти жирные кислоты преимущественно присутствуют в количестве (суточной дозе) от 100 мг до 1000 мг. В более общем случае рыбий жир может присутствовать в суточном количестве от 400 мг до 1000 мг или даже от 800 мг до 1000 мг.
В данном случае EPA преимущественно присутствует в количестве (суточной дозе) от 100 мг до 1000 мг, например 172 мг.
В данном случае DHA преимущественно присутствует в количестве (суточной дозе) от 100 мг до 1000 мг, например, равном 366 мг.
Согласно конкретным вариантам осуществления композиция, применяемая в рамках объема настоящего изобретения, может содержать другие активные ингредиенты, такие как:
- один или более других полифенолов, таких как эпигаллокатехин-3-галлат (EGCG);
- глутатион, например, от 1 мг до 10 мг в день или даже 2 мг в день;
- антоцианозид(антоцианозиды);
- гидрокситирозол.
Содержание каждого из этих ингредиентов легко определяется и корректируется специалистом в данной области.
Таким образом, и согласно одному варианту осуществления, композиция содержит следующие ингредиенты или состоит из них:
- витамин C;
- витамин E;
- возможно витамин D;
- цинк;
- медь;
- лютеин;
- зеаксантин;
- омега-3-жирные кислоты из рыбьего жира, в частности EPA и DHA;
- ресвератрол.
Согласно другому варианту осуществления композиция содержит следующие ингредиенты в расчете на суточную дозу или состоит из них:
- от 50 мг до 500 мг витамина C, преимущественно 240 мг, более преимущественно 120 мг;
- от 10 мг до 500 мг витамина E, преимущественно 30 мг;
- от 5 мг до 100 мг цинка, преимущественно 12,5 мг;
- от 0,2 мг до 10 мг меди, преимущественно 1 мг;
- от 2 мг до 50 мг лютеина, преимущественно 20 мг;
- от 0,5 мг до 10 мг зеаксантина, преимущественно 4 мг;
- от 400 мг до 1000 мг рыбьего жира, особенно преимущественно от 800 до 1000 мг;
- ресвератрол, преимущественно в количестве, которое больше или равняется 20 мг, преимущественно больше 30 мг, особенно преимущественно больше 50 мг, весьма преимущественно в количестве, которое больше или равняется 60 мг;
- необязательно витамин D, преимущественно 5 мкг.
Согласно предпочтительному варианту осуществления композиция содержит следующие ингредиенты в расчете на суточную дозу или состоит из них:
- 120 мг витамина C;
- 30 мг витамина E;
- 12,5 мг цинка;
- 1 мг меди;
- 20 мг лютеина;
- 4 мг зеаксантина;
- 950 мг рыбьего жира, преимущественно содержащего 366 мг DHA и 172 мг EPA;
- ресвератрол, преимущественно в количестве, которое больше или равняется 50 мг, весьма преимущественно в количестве, которое больше или равняется 60 мг.
В качестве альтернативы композиция содержит следующее или состоит из этого:
- 240 мг витамина C;
- 30 мг витамина E;
- 12,5 мг цинка;
- 1 мг меди;
- 10 мг лютеина;
- 2 мг зеаксантина;
- 950 мг рыбьего жира;
- ресвератрол, преимущественно в количестве, которое больше или равняется 20 мг, весьма преимущественно в количестве, которое больше или равняется 30 мг.
Согласно конкретному варианту осуществления такая композиция не содержит по меньшей мере одного из ингредиентов из следующего перечня:
- шафран;
- металлохелатирующее средство, такое как EDTA или фитиновая кислота;
- нуклеотид;
- пикногенол;
- экстракт Ginkgo biloba.
Согласно этому варианту осуществления в применяемой композиции не сочетаются ресвератрол с шафраном, или ресвератрол с металлохелатирующим средством и одним или более нуклеотидами, или ресвератрол и пикногенол и/или экстракт Ginkgo biloba.
Композиция, входящая в объем настоящего изобретения, может присутствовать в форме жидкости, раствора, суспензии, пасты или геля.
Она преимущественно представлена в твердой форме, такой как порошок, таблетки, в том числе шипучие таблетки, пилюли, капсулы или лепешки, полученной традиционным способом с использованием приемлемых добавок, таких как связующие средства, наполнители, смазывающие вещества, разрыхлители или смачивающие средства. На таблетки необязательно может быть нанесено покрытие способом, известным специалисту в данной области, с использованием сахаров, пленок или энтеросолюбильных покрытий.
В качестве альтернативы можно применять другие системы доставки, такие как препараты в мягких желатиновых капсулах или капсулах на основе желатина или составы, полученные с помощью нанотехнологии, такие как нанодисперсии, наноэмульсии или нанокапсулы.
Такая композиция может дополнительно содержать одну или более добавок, таких как красители, пигменты или ароматизаторы и т. д.
Согласно конкретному варианту осуществления композиция представлена в форме капсул, определяющих заданный объем, в котором содержится композиция. Капсула разрушается в пищеварительной системе для целей высвобождения активных ингредиентов и обеспечения их усвоения организмом.
В данном случае традиционными добавками являются:
- глицерин, например моностеарат глицерина; и/или
- соевое масло; и/или
- пчелиный воск; и/или
- соевый лецитин.
В подходящем случае эти добавки добавляют в композицию благодаря их способности улучшать, например, ее свойства сыпучести или гомогенизацию.
Кроме того, и как известно специалисту в данной области, оболочку капсулы можно изготовить из следующих ингредиентов:
- желатин; и/или
- оксид железа красный; и/или
- оксид железа черный; и/или
- сорбит; и/или
- глицерин.
Как известно специалисту в данной области, распределение в этом типе упаковки представляет собой компромисс между:
- ограниченным количеством доз для целей обеспечения надлежащего соблюдения режима лечения;
- подходящим объемом доз, позволяющим составлять все ингредиенты и легко проглатывать.
Такую композицию преимущественно вводят ежедневно, т. е. каждый день.
Согласно преимущественному варианту осуществления данная композиция составлена в виде 2 капсул, каждая из которых содержит ингредиенты, перечисленные выше, в половинном количестве.
Согласно первому альтернативному варианту все эти ингредиенты смешивают и вводят в виде единой композиции. В качестве альтернативы эти ингредиенты можно комбинировать различными способами для составления и/или введения одновременно или с разнесением по времени.
Характерно, что композицию, применяемую в рамках объема настоящего изобретения, вводят перорально, преимущественно в форме 2 ежедневных доз. Согласно конкретному варианту осуществления композиция представлена в форме 2 капсул, которые можно принимать с небольшим количеством воды. Их можно принимать одновременно, например, в начале основного приема пищи или во время основного приема пищи.
С учетом эффекта, проиллюстрированного в примерах, такая композиция предназначена для введения субъекту, получающему средство лечения, противодействующее VEGF.
Согласно другому аспекту средство лечения, противодействующее VEGF, как будет подробно описано ниже, предназначено для введения субъекту, принимающему композицию, определенную выше, преимущественно перорально, еще более преимущественно перорально и ежедневно.
Согласно конкретному варианту осуществления и в рамках объема настоящего изобретения лечение, противодействующее VEGF, соответствует приему средства, противодействующего VEGF, точнее говоря, средства, подавляющего сигнальный путь VEGF.
Средство, противодействующее VEGF, преимущественно выбрано из антитела, фрагмента антитела, рекомбинантного белка, слитого белка и их смеси.
Согласно конкретному варианту осуществления средство, противодействующее VEGF, выбрано из группы, состоящей из ранибизумаба, бевацизумаба, афлиберцепта, абиципара пегола, конберцепта, фарицимаба, бролуцизумаба, их биоаналогов и их смесей.
В рамках настоящего изобретения под биоаналогом в общепринятом смысле этого термина понимается лекарственный препарат, подобный биологическому веществу, получаемому из живой клетки или организма, называемому оригинальным лекарственным препаратом. Этот лекарственный препарат-биоаналог должен характеризоваться аналогичными физико-химическими и биологическими свойствами, такой же фармацевтической субстанцией и такой же фармацевтической формой по сравнению с оригинальным лекарственным продуктом, а также эквивалентной эффективностью и безопасностью.
Ранибизумаб представляет собой фрагмент гуманизированного моноклонального антитела к VEGF-A.
Бевацизумаб представляет собой рекомбинантное гуманизированное моноклональное антитело к VEGF.
Афлиберцепт представляет собой рекомбинантный слитый белок, соответствующий внеклеточным доменам рецепторов VEGF человека 1 и 2 типов (VEGF-R1 и VEGF-R2), слитым с кристаллизующимся фрагментом (Fc) иммуноглобулина IgG1 человека.
Абиципар пегол представляет собой белок с анкириновыми повторами, который связывается со всеми изоформами VEGF-A. Его небольшой размер (34 кДа) позволяет предположить, что он характеризуется коротким периодом полужизни в глазу, но он приобретает фармакокинетические характеристики более крупного белка, в частности более длительный период полужизни, благодаря пегилированию, т. е. добавлению молекул полиэтиленгликоля.
Конберцепт похож на афлиберцепт в том, что он подразумевает под собой рекомбинантный слитый белок, соответствующий ключевым внеклеточным доменам рецепторов VEGF 1 и 2 типов и Fc IgG человека. Однако конберцепт также содержит четвертый домен рецептора VEGF-2.
Фарицимаб представляет собой биспецифическое моноклональное антитело к ангиопоэтину 2 и к VEGF.
Бролуцизумаб (или RTH258, Novartis) представляет собой одноцепочечное антитело, которое обеспечивает гораздо более высокое содержание антител в глазу, чем одобренные в настоящее время средства лечения. Это антитело характеризуется очень высокой аффинностью ко всем изоформам VEGF-A и, как ожидается, позволяет увеличить интервал между интравитреальными инъекциями.
Обычно эти средства, противодействующие VEGF, вводят путем интравитреальной инъекции. Однако с учетом усиления их эффекта в присутствии композиции, описанной выше, можно рассмотреть возможность их местного применения, преимущественно на поверхности глаз.
Комбинация этих двух средств лечения (нутрицевтической офтальмологической композиции для перорального применения и средства лечения, противодействующего VEGF, вводимого путем интравитреальной инъекции или местно) является преимущественной в отношении лечения заболеваний глаз, преимущественно заболеваний сетчатки с неоваскулярным компонентом, еще более преимущественно выбранных из группы, состоящей из:
- возрастной макулярной дегенерации, преимущественно влажной формы AMD;
- диабетического макулярного отека (DMO);
- окклюзии вены сетчатки (RVO);
- миопической хориоидальной неоваскуляризации (mCNV);
- неоваскулярной глаукомы (NVG) и
- пролиферативной диабетической ретинопатии (PDR).
Согласно другому аспекту настоящее изобретение относится к комбинированному продукту или комбинированному препарату, содержащему нутрицевтическую композицию и средство лечения, противодействующее VEGF, описанные выше, для одновременного, раздельного или последовательного применения при лечении заболевания глаз, преимущественно заболевания сетчатки с неоваскулярным компонентом, еще более преимущественно выбранного из группы, состоящей из:
- возрастной макулярной дегенерации, преимущественно влажной формы AMD;
- диабетического макулярного отека (DMO);
- окклюзии вены сетчатки (RVO);
- миопической хориоидальной неоваскуляризации (mCNV);
- неоваскулярной глаукомы (NVG) и
- пролиферативной диабетической ретинопатии (PDR).
Как уже упоминалось, в данном случае нутрицевтическую композицию преимущественно вводят перорально, еще более преимущественно ежедневно, например, в форме 2 капсул, принимаемых в начале или посреди основного приема пищи.
В то же время средство лечения, противодействующее VEGF, вводят путем интравитреальной инъекции или местно. Интравитреальная инъекция остается предпочтительным путем введения, но современные разработки позволяют рассмотреть возможность местного применения, преимущественно путем нанесения на поверхность глаза.
Действительно, как было продемонстрировано, эта комбинация позволяет снизить дозировку, в частности, средства лечения, противодействующего VEGF. Таким образом, можно снизить применяемые дозы или, преимущественно, увеличить интервал между введениями (или сократить частоту введения), которые обычно разделены интервалами, составляющими 1-3 месяца.
Другими словами, этот комбинированный продукт позволяет снизить дозу и/или частоту введения средства лечения, противодействующего VEGF, по сравнению с дозой и/или частотой, применяемыми у субъекта, не получающего нутрицевтическую композицию.
Согласно другому аспекту интервал между двумя введениями средства лечения, противодействующего VEGF, может составлять более 30 дней, преимущественно более 45 дней, предпочтительно более 60 дней или даже 75 дней, более преимущественно более 90 дней, по сравнению с используемой в данный момент дозировкой.
Таким образом, и согласно другому аспекту, интервал между двумя введениями средства лечения, противодействующего VEGF, составляет более 30 дней, преимущественно более 45 дней, предпочтительно более 60 дней или даже 75 дней, более преимущественно более 90 дней.
Таким образом, можно снизить потенциальную токсичность средств лечения, противодействующих VEGF, в частности, их побочные эффекты. Интервал между их введениями, требующий вмешательства специалистов, также представляет интерес с экономической точки зрения.
Иллюстративные варианты осуществления настоящего изобретения
Настоящее изобретение и вытекающие из него преимущества станут более очевидными из следующих фигур и примеров, которые даны для иллюстрации настоящего изобретения и без ограничения.
ОПИСАНИЕ ФИГУР
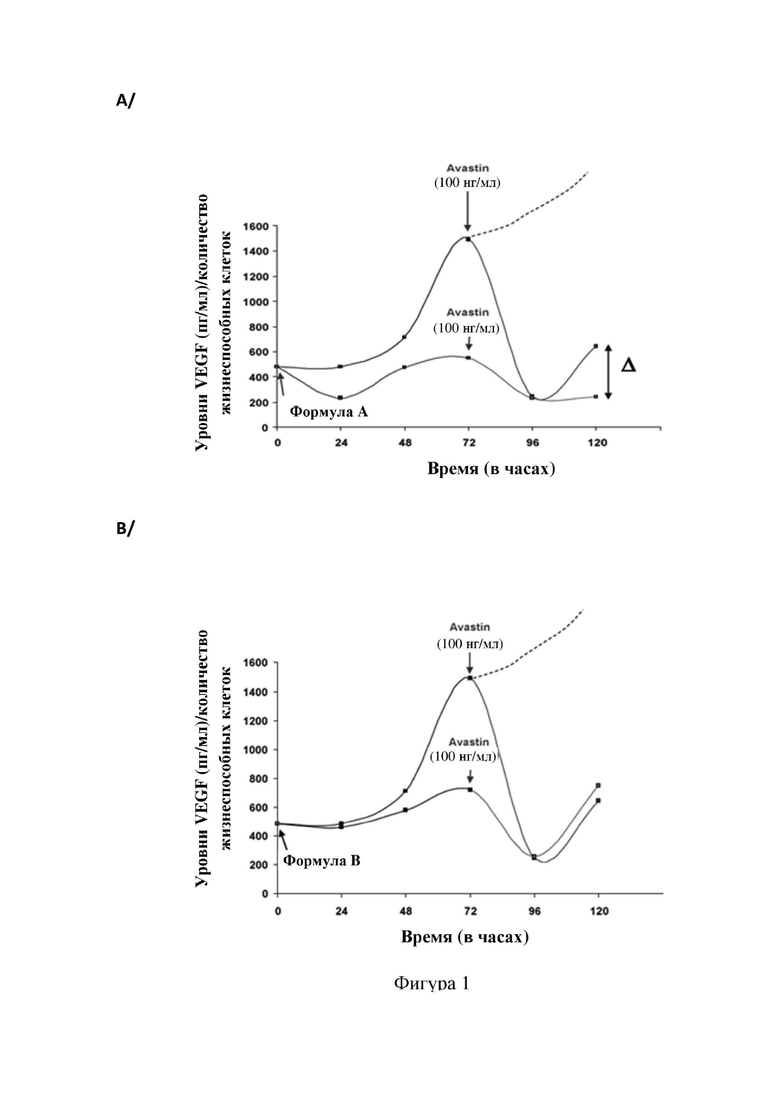
На фигуре 1 сравнивается динамика изменения уровней VEGF после введения AVASTIN® в инкубированных недифференцированных (патологических) клетках сетчатки (A) в присутствии (нижняя кривая) и в отсутствие (верхняя кривая) формулы A или (B) в присутствии (нижняя кривая) и в отсутствие (верхняя кривая) формулы B.
A. Протокол
Культура клеток
Недифференцированные клетки сетчатки человека ARPE-19 (ATCC® CRL-2302™) культивируют in vitro в DMEM (среда Игла в модификации Дульбекко/питательная смесь F12 (1:1, Gibco, Пейсли, Великобритания), обогащенной 10% фетальной телячьей сывороткой (FCS, Dominique DUTSCHER, южноамериканского происхождения, №°партии S15197S1810), 1% PSA (коктейль антибиотиков: пенициллин, стрептомицин и амфотерицин B соответственно при 10000 ед/мл: 10 мг/мл: 25 мкг/мл, PAN Biotech) и 15 мM HEPES (pH 7,4, Gibco). Клетки выращивают в атмосфере при 37°C и 5% CO2. Эти клетки могут становиться подобными пораженным или патологическим клеткам сетчатки.
Виды обработки
Клетки выращивали и высевали в 24-луночные культуральные чашки по 60000 клеток на лунку в среде DMEM/F12, 10% SVF и 1% PSA. Через 24 часа после посева среду для роста удаляли и заменяли ограничительной средой для роста DMEM/F12 с 1% SVF и 1% PSA без фенолового красного. Еще через 24 часа клетки помещали в условия присутствия или отсутствия формулы A (с ресвератролом) или формулы B (без ресвератрола).
Состав формул A и B описан ниже.
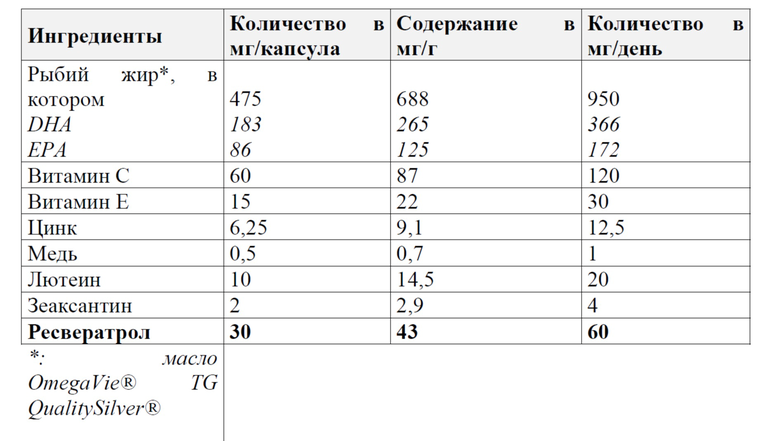
Таблица 1. Состав формулы A (с ресвератролом)
Обратите внимание, что одна капсула содержит 690 мг препарата, и рекомендуется одна суточная доза, составляющая 2 капсулы.
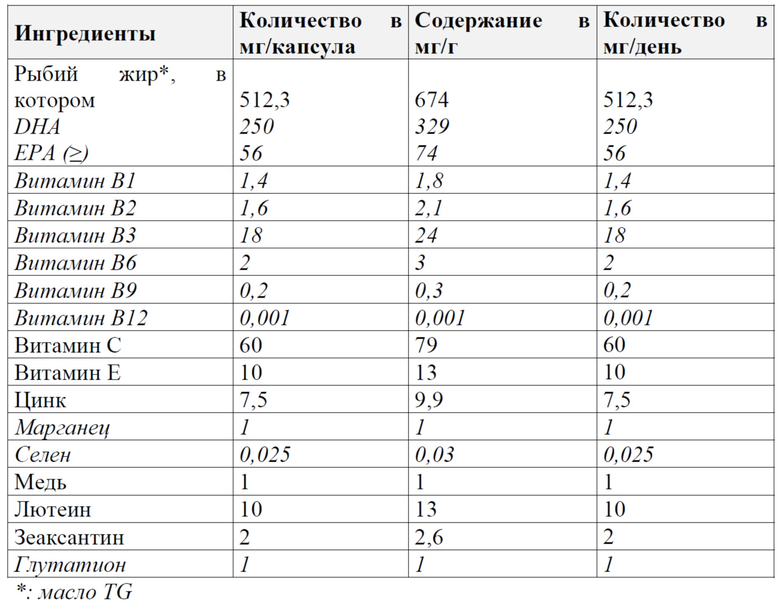
Таблица 2. Состав формулы B (без ресвератрола)
Обратите внимание, что одна капсула содержит 760 мг препарата, и рекомендуется принимать только 1 капсулу в день.
Формулы A и B берутся по массе 0,115 г в 1 мл DMSO (диметилсульфоксида), чтобы получить эквивалент ресвератрола 10 мМ для формулы A и 0 мМ для формулы B. Показатели содержания рыбьего жира, витаминов C и E, цинка, меди, лютеина и зеаксантина считаются эквивалентными в этих 2 препаратах. Из этого раствора производят разведения непосредственно в среде для роста DMEM/F12 с 1% SVF, 1% PSA без фенолового красного для достижения показателей содержания 10 мкМ и 20 мкМ, необходимых для эксперимента.
После 24 часов предварительной инкубации клетки обрабатывают с помощью 100 нг/мл AVASTIN® (± формула A или B).
ELISA (твердофазный иммуноферментный анализ)
В момент обработки (t0) с помощью 100 нг/мл Avastin®, а также через 24 часа, 48 часов и 72 часа после обработки надосадочную жидкость культуры клеток собирают для анализа количества высвободившегося VEGF-A. Каждый ELISA проводят в соответствии с точными инструкциями производителя (набор для ELISA VEGF-A человека BMS277, Affymetrix, eBioscience).
Кристаллический фиолетовый
Слой клеток анализируют с помощью кристаллического фиолетового для определения жизнеспособности клеток. Можно провести определение соотношения между уровнями VEGF-A в надосадочной жидкости и соответствующем слое клеток.
Слой клеток дважды осторожно ополаскивают 1X буфером PBS. При удалении избытка жидкости слой клеток фиксируют на подложке с помощью абсолютного этанола. После инкубации в течение периода по меньшей мере 30 минут абсолютный этанол удаляют. Клетки приводят в контакт с окрашивающим раствором кристаллического фиолетового в течение 20 минут при комнатной температуре и под действием колебаний (25 колебаний в минуту).
Раствор кристаллического фиолетового удаляют, и лунки 4 раза ополаскивают водой для удаления избытка красителя. Затем планшеты высушивают при комнатной температуре (в течение от 16 до 24 часов). Затем окрашенные клетки ресуспендируют в 33% растворе уксусной кислоты, планшеты помещают в условия воздействия колебаний, и оптическую плотность можно считать спектрометрическим методом при длине волны 570 нм (OD570).
B. Результаты
Можно наблюдать, что присутствие формулы A позволяет ограничить количество вырабатываемого VEGF, а также значительно задерживает повышение этого уровня после обработки с помощью средства, противодействующего VEGF, что позволит увеличить интервалы между инъекциями средства, противодействующего VEGF.
В то же время формула B приводит к снижению количества вырабатываемого VEGF, но не приводит к задержке восстановления выработки VEFG в клетках сетчатки, обработанных средством, противодействующим VEGF.
Это неожиданное различие связано с наличием высокого содержания ресвератрола в формуле А.
Изобретение относится к области медицины, а именно к офтальмологии и терапии, и предназначено для лечения заболевания глаз у субъекта, получающего средство лечения, противодействующее VEGF. Применяют офтальмологическую нутрицевтическую композицию при лечении заболевания глаз у субъекта, получающего средство лечения, противодействующее VEGF. Указанная композиция содержит ресвератрол, витамин C, витамин E, цинк, медь, лютеин, зеаксантин и омега-3-жирные кислоты из рыбьего жира. Использование изобретения позволяет повысить эффективность лечения заболевания глаз у субъекта, получающего средство лечения, противодействующее VEGF. 20 з.п. ф-лы, 1 ил., 2 табл.
1. Применение офтальмологической нутрицевтической композиции, содержащей ресвератрол в количестве более 20 мг, при лечении заболевания глаз у субъекта, получающего средство лечения, противодействующее VEGF, отличающееся тем, что композиция содержит:
- витамин C в количестве от 50 мг до 500 мг;
- витамин E в количестве от 10 мг до 500 мг;
- цинк в количестве от 5 мг до 100 мг;
- медь в количестве от 0,2 мг до 10 мг;
- лютеин в количестве от 2 мг до 50 мг;
- зеаксантин в количестве от 0,5 мг до 10 мг;
- омега-3-жирные кислоты из рыбьего жира в количестве от 100 мг до 1000 мг.
2. Применение по п. 1, отличающееся тем, что композиция содержит витамин С в количестве 120 мг.
3. Применение по п. 1, отличающееся тем, что композиция содержит витамин E в количестве 30 мг.
4. Применение по п. 1, отличающееся тем, что композиция содержит цинк в количестве 12,5 мг.
5. Применение по п. 1, отличающееся тем, что композиция содержит медь в количестве 1 мг.
6. Применение по п. 1, отличающееся тем, что композиция содержит лютеин в количестве 20 мг.
7. Применение по п. 1, отличающееся тем, что композиция содержит зеаксантин в количестве 4 мг.
8. Применение по п. 1, отличающееся тем, что композиция содержит омега-3-жирные кислоты из рыбьего жира в количестве от 800 мг до 1000 мг.
9. Применение по п. 1, отличающееся тем, что омега-3-жирные кислоты из рыбьего жира выбраны из группы, состоящей из эйкозапентаеновой кислоты (EPA) и докозагексаеновой кислоты (DHA).
10. Применение по п. 1, отличающееся тем, что композиция содержит ресвератрол в количестве, которое больше или равняется 30 мг, преимущественно больше 30 мг, еще более преимущественно больше или равняется 50 мг.
11. Применение по любому из предыдущих пунктов, отличающееся тем, что композиция вводится перорально.
12. Применение по любому из предыдущих пунктов, отличающееся тем, что композиция вводится ежедневно.
13. Применение по любому из предыдущих пунктов, отличающееся тем, что лечение, противодействующее VEGF, соответствует введению ингибитора сигнального пути VEGF, преимущественно выбранного из следующей группы: антитело, фрагмент антитела, рекомбинантный белок, слитый белок и их смеси.
14. Применение по любому из предыдущих пунктов, отличающееся тем, что ингибитор выбран из следующей группы: ранибизумаб, бевацизумаб, афлиберцепт, абиципар пегол, конберцепт, фарицимаб, бролуцизумаб и их смеси.
15. Применение по любому из предыдущих пунктов, отличающееся тем, что средство лечения, противодействующее VEGF, вводится путем интравитреальной инъекции или местно.
16. Применение по любому из предыдущих пунктов, отличающееся тем, что заболевание глаз выбрано из группы, состоящей из возрастной макулярной дегенерации, диабетического макулярного отека, окклюзии вены сетчатки, миопической хориоидальной неоваскуляризации, неоваскулярной глаукомы и пролиферативной диабетической ретинопатии.
17. Применение по любому из пп. 1-10 со средством, противодействующим VEGF, преимущественно указанным в пп. 13 и 14, при лечении заболевания глаз, преимущественно выбранного из группы, состоящей из возрастной макулярной дегенерации, диабетического макулярного отека, окклюзии вены сетчатки, миопической хориоидальной неоваскуляризации, неоваскулярной глаукомы и пролиферативной диабетической ретинопатии.
18. Применение по п. 17, отличающееся тем, что композиция вводится перорально, преимущественно ежедневно.
19. Применение по п. 17 или 18, отличающееся тем, что средство, противодействующее VEGF, вводится путем интравитреальной инъекции или местно.
20. Применение по любому из пп. 17-19, отличающееся тем, что доза и/или частота введения средства, противодействующего VEGF, снижены по сравнению с дозой и/или частотой, применяемыми у субъекта, который не получает композицию.
21. Применение по п. 20, отличающееся тем, что интервал между двумя введениями средства, противодействующего VEGF, составляет более 30 дней, преимущественно более 45 дней, предпочтительно более 60 дней или даже более 75 дней, более преимущественно более 90 дней, по сравнению с интервалом между двумя введениями средства, противодействующего VEGF, у субъекта, не получающего композицию.
| WO 2012006065 A1, 12.01.2012 | |||
| US 2018042894 A1, 15.02.2018 | |||
| US 2018207233 A1, 26.07.2018 | |||
| WO 2010062824 A2, 03.06.2010 | |||
| MURALI SUBRAMANI et al | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Sci Rep., 2017, 7(1):12242, doi: 10.1038/s41598-017-12496-z | |||
| STUART RICHER et al | |||
| Observation of human retinal remodeling | |||
Авторы
Даты
2023-10-26—Публикация
2019-12-19—Подача