Настоящее изобретение относится к медицине, а именно - к урологии, и может быть использовано для определения тактики лечения инфертильности, ассоциированной с папилломавирусной инфекцией у мужчин.
Мужская инфертильность - многофакторное состояние, которое может быть следствием различных причин (Чалый М.Е., Ахвледиани Н.Д., Харчилава P.P., 2017; Durairajanayagam, D., 2018; Agarwal A., Panner Selvam M.K., Baskaran S., 2020).
В настоящее время существует несколько классификаций мужской инфертильности, в основе которых лежат различные аспекты: этиологические факторы, патогенетические механизмы формирования этого заболевания, топологический уровень поражения (Чалый М.Е., Ахвледиани Н.Д., Харчилава P.P., 2017).
При экскреторном бесплодии сперматогенез, как правило, сохранен, а причина инфертильности заключается во врожденной или приобретенной облитерации или отсутствии семявыносящих путей (Li L., Liang С, 2016; Chiang H.S. et al. 2019; Tan M.Q., Tang Y., 2021). В зависимости от причин обструкции выполняются соответствующие инвазивные вмешательства (Wang J.A. et al. 2018).
Секреторное бесплодие является следствием недостаточности секреторной функции тестикул из-за врожденной или приобретенной патологии (Шевырин А.А., 2018).
По данным разных авторов, основными причинами секреторного бесплодия могут быть эндокринные нарушения, варикоцеле, врожденные аномалии развития (крипторхизм, аплазия яичек), экзогенные экологические факторы, действия лекарственных препаратов, хромосомные и генетические мутации, последствия заболеваний, передающихся половым путем (ЗППП) и др. (Ибишев Х.С., Волкова Н.И., Гусова З.Р. и соавт., 2022; Raad G., Azour J., Rizk К. et al., 2019, Loebenstein M., Thorup J., Cortes D. et al., 2020; Henkel, R., 2020).
Роль инфекций, передающихся половым путем (ИППП), в параметрах эякулята и мужском бесплодии до сих пор остается обсуждаемым разделом изучаемой проблемы (Bai S., Li Y., Wan Y. et al., 2021; Gholami M., Moosazadeh M., Haghshenash M.R. et al., 2022).
Более 30 инфекций, передающихся половым путем (ИППП), в том числе вирус простого герпеса (ВПГ), Chlamydia trachomatis, Ureaplasma spp., Mycoplasma hominis, Mycoplasma genitalium и Neisseria gonorrhoeae признаны как патогенные, обуславливающие развитие инфертильности как у женщин, так и у мужчин (Корнеев И.А., Зассеев Р.Д., Шевчук И.Г. и соавт., 2018). Кроме того, вышеперечисленные микроорганизмы являются признанными этиологическими агентами ряда заболеваний мочевыводящих путей и репродуктивных органов у мужчин (простатит, уретрит, эпидидимит, везикулит, орхит), которые в большинстве случаев ассоциированы с инфертильностью (Kim S.J., Paik D.J., Lee J.S. et al., 2017; Zhang Q.F., Zhang Y.J., Wang S. et al., 2020; Farahani L., Tharakan Т., Yap T. et al., 2021; Gholami M., Moosazadeh M., Haghshenash M.R. et al., 2022).
Кроме того, инфекционно-воспалительные заболевания мочевыводящих путей и репродуктивных органов у мужчин, вызванные условно-патогенной флорой, могут служить основополагающим звеном для развития инфертильности мужчин (Motrich R.D., Salazar F.C., Breser M.L. et al., 2018; Marchiani S., Baccani I., Tamburrino L. et al., 2021). Однако несмотря на то, что острое и хроническое воспаление репродуктивной системы считается причиной примерно 15% случаев мужского бесплодия, вероятно, из-за пагубного воздействия на сперматозоиды некоторых микроорганизмов, выделяемых при культуральном исследовании, связь между инфекционно-воспалительным процессом и плохим качеством спермы четко не определена. При мужском бесплодии в эякуляте наблюдаются количественные изменения бактериальных и вирусных паттернов по сравнению с показателями у здоровых мужчин, но данные вопросы требуют дальнейших исследований (Fraczek М., Kurpisz М., 2015; Коган М.И., Ибишев Х.С., Набока Ю.Л. и соавт., 2022).
Причастность вирусных инфекций имеет фундаментальную основу и основывается на большом опыте многоцентровых клинических исследований (Amirjannati N., Yaghmaei F., Akhondi M.M. et al., 2014; Bai S., Li Y., Ни M.H. et al., 2022). Вирусные инфекции так же, как и бактериальные и внутриклеточные, патогенны, могут приводить к прямому и косвенному угнетению сперматогенеза и развитию мужского бесплодия. Вирусные патогены могут вызывать нарушения репродуктивной функции посредством токсических и иммунологических реакций в репродуктивной системе. Кроме того, точкой приложения вирусных агентов могут быть все составляющие эякулята: спермоплазма, сперматозоиды, эпителиальные клетки и лейкоциты. Среди вирусных представителей, участвующих в развитии инфертильности у мужчин, лидирует герпетическая инфекция (Tavakolian S., Goudarzi Н., Nazarian Н. et al., 2021; Alazzam M.B., Al-Radaideh A.T., Binsaif N. et al., 2022).
Дискутабельным вопросом остается причастность папилломавирусной инфекции (ПВИ) к развитию мужской инфертильности. Вирус папилломы человека (ВПЧ) является наиболее распространенным в мире вирусом, передающимся половым путем; было зарегистрировано более 200 его генотипов (Ибишев Х.С., 2022; Lyu Z., Feng X., Li N. et al., 2017). В зависимости от связи с различными злокачественными новообразованиями ВПЧ можно разделить на две группы: ВПЧ высокого риска (HR-HPV) и ВПЧ низкого риска (LR-HPV) (Schiffman М., Doorbar J., Wentzensen N. et al., 2016; Luttmer R., Dijkstra M.G., Snijders P.J. et al., 2016; Boeri L., Capogrosso P., Ventimiglia E. et al., 2019; Cao X., Wei R., Zhang X. et al., 2020; Moreno-Sepulveda J., Rajmil O., 2021).
Недавние сообщения предполагают, что ВПЧ может влиять на различные параметры эякулята и приводить к нарушениям других патологических звеньев развития мужской инфертильности (Moghimi М., Zabihi-Mahmoodabadi S., Kheirkhah-Vakilabad A. et al., 2019).
Инфицирование ВПЧ, особенно высокого онкогенного риска, влияет на различные этапы репродуктивного потенциала у мужчин, приводя к ряду неблагоприятных патологических процессов: 1) снижению мужской фертильности, характеризующемуся качественными и количественными изменениями эякулята; 2) нарушению фертильности пары с усилением апоптоза бластоцисты и уменьшением имплантации в эндометрий трофобластических клеток; 3) пороку развития зародыша и плода с увеличением числа самопроизвольных абортов и самопроизвольных преждевременных родов (Jersoviene V., Gudleviciene Z., Rimiene J. et al., 2019; Isaguliants M., Krasnyak S., Smirnova O. et al., 2021). Тем не менее, механизм, с помощью которого происходит запуск звеньев негативных реакций, приводящих к патоспермии, остается не до конца изученным. Известно то, что ВПЧ-инфекция, с одной стороны, оказывает непосредственное патогенное действие, вызывая генетическую нестабильность/повреждение ДНК сперматозоидов, а с другой, ингибируя иммунокомпетентную составляющую репродуктивной системы, активизирует аутоиммунные процессы в тестикулах, в том числе и запуск цитокиногенеза, усугубляющие сперматогенез в целом (Damke Е., Kurscheidt F.A., Balani V.A. et al., 2017; Perez-Soto E., Medel-Flores M.O., Fernandez-Martinez E. et al., 2021).
В некоторых случаях папилломавирусная инфекция после инфицирования устраняется иммунной системой в течение 12-24 месяцев, что позволяет избежать каких-либо клинических исходов. Неспособность элиминировать вирус при дисфункции иммунной системы приводит к персистирующему течению ПВИ и вызывает ряд патологических состояний, и не только онкологического генеза. ВПЧ как с высоким, так и с низким патогенным потенциалом способствуют развитию инфекционно-воспалительных заболеваний уретры, мочевого пузыря, простаты, яичек и могут влиять на репродуктивное здоровье и фертильность как женщин, так и мужчин и пары в целом. Главный вопрос: лечить или не лечить; нет четких признаков активации патогенного потенциала.
Проведенными исследованиями научно-медицинской и патентной литературы выявлены различные способы определения тактики лечения папилломавирусной инфекции.
Известен способ диагностики папилломавирусной инфекции, который осуществляют путем сбора анамнеза и комплексного клинико-лабораторного обследования. В качестве анамнестических признаков принимают отягощенную онкологическую наследственность, раннее начало половой жизни, возраст до 20 лет и промискуитет; в качестве клинических -аногенитальные бородавки, эрозии и эктопии шейки матки, контактную кровоточивость, Ovuli nabotti, воспалительные заболевания органов малого таза и наличие внутриматочной спирали. При этом в качестве лабораторных признаков принимают инфекции, передаваемые половым путем, микст-инфицирование, дефицит лактобактерий, дисбиоз влагалища, вызванный условно-патогенной флорой, бактериальный вагиноз, вирус-вирусные ассоциации, урогенитальный герпес, урогенитальную микоплазменную инфекцию, урогенитальную уреаплазменную инфекцию, урогенитальный кандидоз, урогенитальную хламидийную инфекцию и инфицирование различными генотипами вируса папилломы человека. Каждый из признаков оценивают по балльной системе и в зависимости от количества баллов диагностируют персистирующее или транзиторное течение папилломавирусной инфекции или подвергают дополнительному обследованию (патент РФ №2379690, от 20.01.2010).
Недостатком способа является то, что идентификация папилломавирусной инфекции осуществляется косвенными признаками, нет достоверных признаков наличия самого вируса и его патогенного действия.
Описан способ использования интерферона в лечении бесплодия у мужчин, вызванного герпетической вирусной инфекцией (ГВИ) (Рищук С.В., Кахиани Е.И., Мирский В.Е., Гогуа М.С., Россолько Д.С., Нилова Л.Ю., Дудниченко Т.А. Перспективы использования интерферона в лечении бесплодия у мужчин. Лечащий Врач. 2018; (4):75). В целях подтверждения влияния ВПГ на сперматогенез и качество сперматозоидов проведены цитологическое и молекулярно-цитогенетическое исследования клеток образцов спермы пациентов, у которых с помощью вирусологического и иммуноцитохимического методов выявлено инфицирование сперматозоидов вирусом простого герпеса (ВПГ). Сравнительный количественный анализ незрелых половых клеток эякулята пациентов с герпетическим инфицированием сперматозоидов и мужчин-доноров показал достоверное и значительное (в три раза) увеличение количества сперматоцитов I у инфицированных пациентов на предпахитенных стадиях профазы I мейоза: прелептотены, лептотены и зиготены. В то же время у пациентов с вирусинфицированными сперматозоидами выявлено статистически значимое уменьшение количества сперматоцитов I на стадиях пахитены и диплотены, сперматоцитов II и сперматид, а также двукратное увеличение количества неидентифицируемых незрелых половых клеток. Таким образом, в совокупности данные о высокой частоте выявления ВПГ в эякуляте мужчин с бесплодием, ухудшении показателей качества спермы, изменении состава популяции НПК у ВПГ-инфицированных лиц, а также о гаметотоксическом воздействии вируса в экспериментальных модельных системах указывают на то, что ВПГ играет определенную патогенетическую роль в формировании мужского бесплодия. Это позволило использовать полученные данные для выбора специфической противовирусной терапии в лечении данных пациентов. Базовая терапия должна включать противогерпетические препараты (внутривенно, перорально, местно) с обязательным увеличением дозы химиопрепарата примерно в 2 раза по сравнению с дозой для лиц с нормальной иммунной системой и продолжительностью курса лечения и профилактики рецидивов у лиц с иммунодефицитными состояниями.
К недостаткам данного метода относится то, что он рассматривает у мужчин тактику лечения бесплодия, вызванного только герпетической вирусной инфекцией, и не рассматривает другие причины. Также недостатком является то, что не уточняется, какими патогенетическими механизмами оказывается негативное действие вируса на сперматозоид.
Описан способ диагностики идиопатического мужского бесплодия, сочетающегося с ПВИ (Ибишев Х.С., Рябенченко Н.Н., Магомедов Г.А. Идиопатическое мужское бесплодие и папилломавирусная инфекция. Вестник урологии. 2019; 7(2):51-58. DOI: 10.21886/2308-6424-2019-7-2-51-58).
Авторами установлено, что ПВИ может приводить к различным видам патоспермии. При бесплодии, ассоциированном с ПВИ, отмечается нарушение подвижности сперматозоидов и ухудшение морфологических характеристики эякулята. При анализе эякулята среди различных вариантов патозооспермии наиболее часто была выявлена астенозооспермия - 56%, реже регистрировались астенотератозооспермия - 21% и олигоастенотератозооспермия - 16%. Небольшой удельный вес составила олигоастенозооспермия - 6%. Патозооспермия в большинстве случаев сочеталась с 16, 18, 33 типами ПВИ. При бесплодии, ассоциированном с ПВИ, отмечается нарушение подвижности сперматозоидов и ухудшение морфологических характеристик эякулята.
Недостатком данного метода является то, что в нем не акцентируется вопрос тактики дальнейшего ведения пациентов с ПВИ с целью лечения инфертильности. Также способ не определяет механизмы патогенного воздействия на эякулят. Кроме того, не приведено достоверного подтверждения цитоморфологических изменений сперматозоидов, обусловленных патогенным воздействием вируса.
Данный способ выбран нами за прототип.
Недостатки способа-прототипа устраняются в заявляемом изобретении.
Задачей, на решение которой направлено заявляемое изобретение, является разработка достоверных критериев определения информативных маркеров, позволяющих определить тактику лечения инфертильности, ассоциированной с папилломавирусной инфекцией у мужчин.
Поставленная задача решается тем, что определение тактики лечения инфертильности, ассоциированной с вирусом папилломы человека у мужчин, включает исследование эякулята методом трансмиссионной электронной микроскопии, определение в эякуляте вируса папилломы человека, наличие адгезии вируса папилломы человека на поверхности сперматозоида, наличие патоспермии, которая характеризуется:
- отсутствием акросомы сперматозида у 20% и выше сперматозоидов в эякуляте;
- наличием патологии постакросомной пластины акросомы сперматозоида у 55% и выше сперматозоидов в эякуляте;
- наличием патологии хроматина сперматозоида у 35% и выше сперматозоидов в эякуляте.
При наличии вышеизложенных признаков у пациента диагностируют инфертильность, ассоциированную с вирусом папилломы человека, и проводят иммунноактивную, противовирусную терапию.
Если по данным трансмиссионной электронной микроскопии в эякуляте не выявляют вирус папилломы человека и патоспермия характеризуется отсутствием сперматозоидов без акросомы и дефектов акросомной пластины, и наличием патологии хроматина сперматозоида у менее 10,5% сперматозоидов в эякуляте, то назначают антиоксидантную терапию.
Технический результат заявляемого способа заключается в повышении точности и достоверности выбора тактики лечения пациентов с инфертильностью, ассоциированной с папилломавирусной инфекцией, что позволяет повысить эффективность лечения при данной нозологии, тем самым повысить возможность зачатия ребенка у бесплодной пары при одновременной простоте, достоверности и доступности предлагаемого способа для широкого практического применения.
При анализе нашего клинического материала (трансмиссионной электронной микроскопии эякулята) у 107 обследованных пациентов в возрасте от 22 до 44 лет с патоспермией и диагнозом бесплодие была выявлена четкая связь между наличием вируса папилломы человека и микроскопическими цитоморфологическими изменениями эякулята.
Длительность заболевания до первичного обращения к врачу составила от 3 до 16 лет.
При оценке инфертильности, ассоциированной с папилломавирусной инфекцией, пациентам выполнялось комплексное мультидисциплинарное урологическое обследование для оценки других критериев-причин, которые могли воздействовать на эякулят.
Критерии невключения в исследование: другие ЗППП, инфекционно-воспалительные заболевания репродуктивных органов бактериальной этиологии (простатит, везикулит, орхит, уретрит), инфравезикальная обструкция (стриктура уретры, нейрогенная дисфункция нижних мочевых путей и др.), сопутствующая сердечно-сосудистая, неврологическая, эндокринная, системная и др. патологии, онкологические заболевания в настоящее время или в анамнезе, гормональные нарушения со стороны репродуктивной системы, аномалии со стороны мочевыводящих путей и репродуктивных органов, любое иммунодефицитное состояние.
После тщательного сбора жалоб и анамнеза заболевания, объективного осмотра больного применяли лабораторные, уродинамические, ультразвуковые методы диагностики и отсутствие критериев невключения, выполняли исследование эякулята.
Оценка оплодотворяющей способности эякулята проводилась в соответствии с данными и параметрами, рекомендованными ВОЗ (2010) в клинико-диагностической лаборатории. Для идентификации типа вируса использован амплификационный метод ДНК-диагностики (полимеразная цепная реакция - ПЦР).
Результаты исследования были обработаны с использованием электронных таблиц Microsoft Excel из пакета программ Microsoft Office 2007. Статистическая обработка данных проводилась с использованием статистического пакета STATISTICA 6.1 (StatSoft Inc., США). Проведение расчетов и интерпретация результатов осуществлялись согласно руководству О.Ю. Ребровой. Соответствие распределения признаков закону нормального распределения проводилось с применением критерия Шапиро-Уилка.
При наличии вируса папилломы человека в эякуляте нами отмечались следующие микроскопические изменения эякулята: отсутствие акросомы у 20% и выше сперматозоидов, наличие патологии постакросомной пластины у 55% и выше сперматозоидов, наличие патологии хроматина у 35% и выше сперматозоидов. В таком случае, у пациента диагностируют инфертильность ассоциированную с вирусом папилломы человека, и проводят иммунноактивную, противовирусную терапию.
Если по данным трансмиссионной электронной микроскопии в эякуляте не выявляют вирус папилломы человека и патоспермия характеризуется отсутствием сперматозоидов без акросомы и дефектов акросомной пластины, и наличием патологии хроматина сперматозоида у менее 10,5% сперматозоидов в эякуляте, то назначают антиоксидантную терапию.
Микроскопические значимые изменения были изучены на достаточном клиническом материале у пациентов с инфертильностью, которые в зависимости от наличия вируса в эякуляте были разделены на две группы: 1 группа - в эякуляте выявлен вирус папилломы человека, 2 группа - в эякуляте не выявлено вируса папилломы человека; данные приведены в таблице.

Для диагностики и лечения пациенты были рандомизированы в 3 группы.
С целью уточнения эффективности противовирусной, иммуноактивной терапии и предложенной нами тактики лечения, а также с целью двойного контроля результатов исследования первая группа рандомизирована в 1А (исследовательская группа) и 1 В (первая контрольная группа).
- 1А группа - у 37 пациентов по данным трансмиссионной электронной микроскопии выявлено наличие в эякуляте вируса папилломы человека, отсутствие акросомы сперматозида у 20% и выше сперматозоидов в эякуляте, наличие патологии постакросомной пластины акросомы сперматозида у 55% и выше сперматозоидов в эякуляте, наличие патологии хроматина сперматозоида у 35% и выше сперматозоидов в эякуляте. Назначена терапия: иммунноактивная, противовирусная терапия (Аллокин-альфа в дозе 1 мг через день, всего на курс 6 инъекций, подкожное введение).
- 1 В группа - у 21 пациента по данным трансмиссионной электронной микроскопии выявлено наличие в эякуляте вируса папилломы человека, отсутствие акросомы сперматозида у 20% и выше сперматозоидов в эякуляте, наличие патологии постакросомной пластины акросомы сперматозида у 55% и выше сперматозоидов в эякуляте, наличие патологии хроматина сперматозоида у 35% и выше сперматозоидов в эякуляте. Но пациентам данной группы была назначена антиоксидантная метаболическая терапия согласно клиническим рекомендациям Министерства здравоохранения Российской Федерации: (Селцинк плюс, по 1 таблетке 1 раз в день, во время приема пищи, продолжительность приема 1 месяц).
- 2 группа (вторая контрольная группа) - у 49 пациентов по данным трансмиссионной электронной микроскопии в эякуляте не выявлено наличие вируса папилломы человека и патоспермия характеризовалась отсутствием сперматозоидов без акросомы и дефектов акросомной пластины, и с наличием патологии хроматина сперматозоида у менее 10,5% сперматозоидов в эякуляте. Назначена антиоксидантная метаболическая терапия согласно клиническим рекомендациям Министерства здравоохранения Российской Федерации: (Селцинк плюс, по 1 таблетке 1 раз в день, во время приема пищи, продолжительность приема 1 месяц).
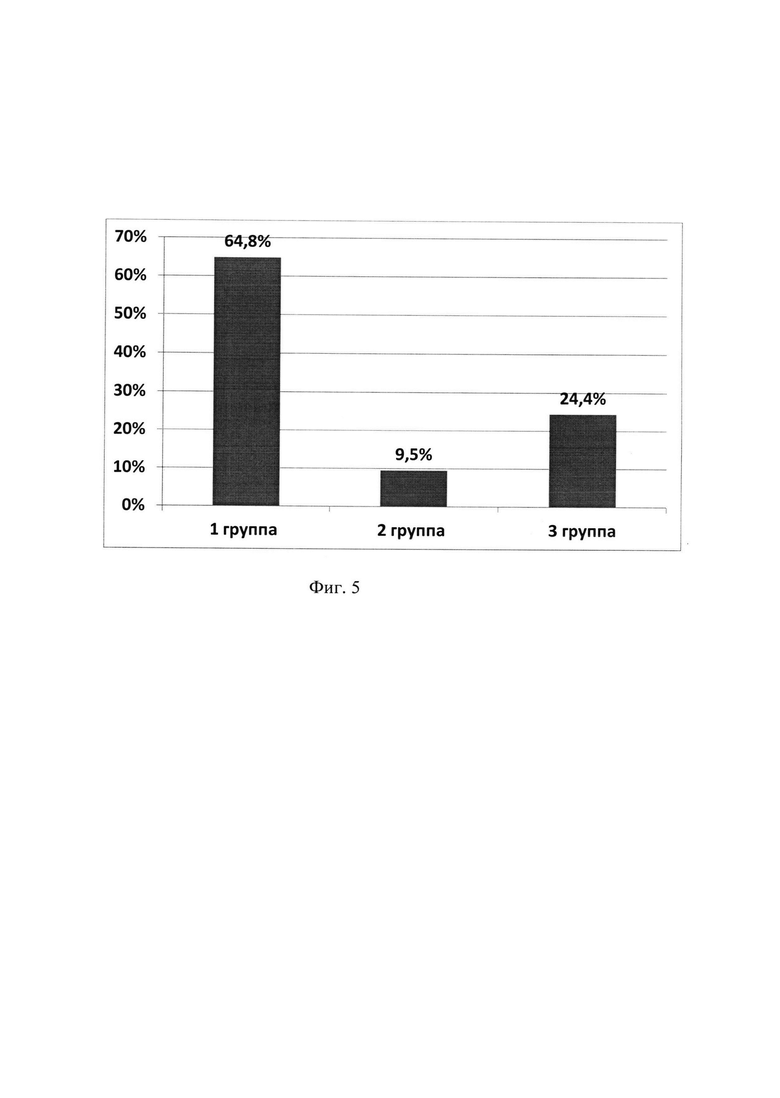
Эффективность лечения оценивали через 24 месяца от начала терапии; беременность среди пациентов 1А группы наступила в 64,8% случаев, у пациентов 1 В группы - в 9,5% случаев, а у пациентов 2 группы - в 24,4% случаев (р<0,005) (Фиг. 5.).
Таким образом, в двух контрольных группах: 1 В группа и 2 группа, пролеченных в соответствии с клиническими рекомендациями МЗ РФ с применением антиоксидантной метаболической терапии эффективность лечения не превысила 24,4%. В исследовательской 1А группе эффективность лечения согласно разработанной нами тактики лечения достигнута в 64,8% случаев (р<0,005).
Таким образом, способ определения тактики лечения инфертильности, ассоциированной с папилломавирусной инфекцией у мужчин, достоверен не только полученными результатами трансмиссионной электронной микроскопии эякулята, но и по результатам лечения, подтвержденным достоверной значимой разницей по количеству наступления беременностей в указанных группах.
Заявляемый способ иллюстрируется фотографиями и рисунками, показанными на Фиг. 1-5.
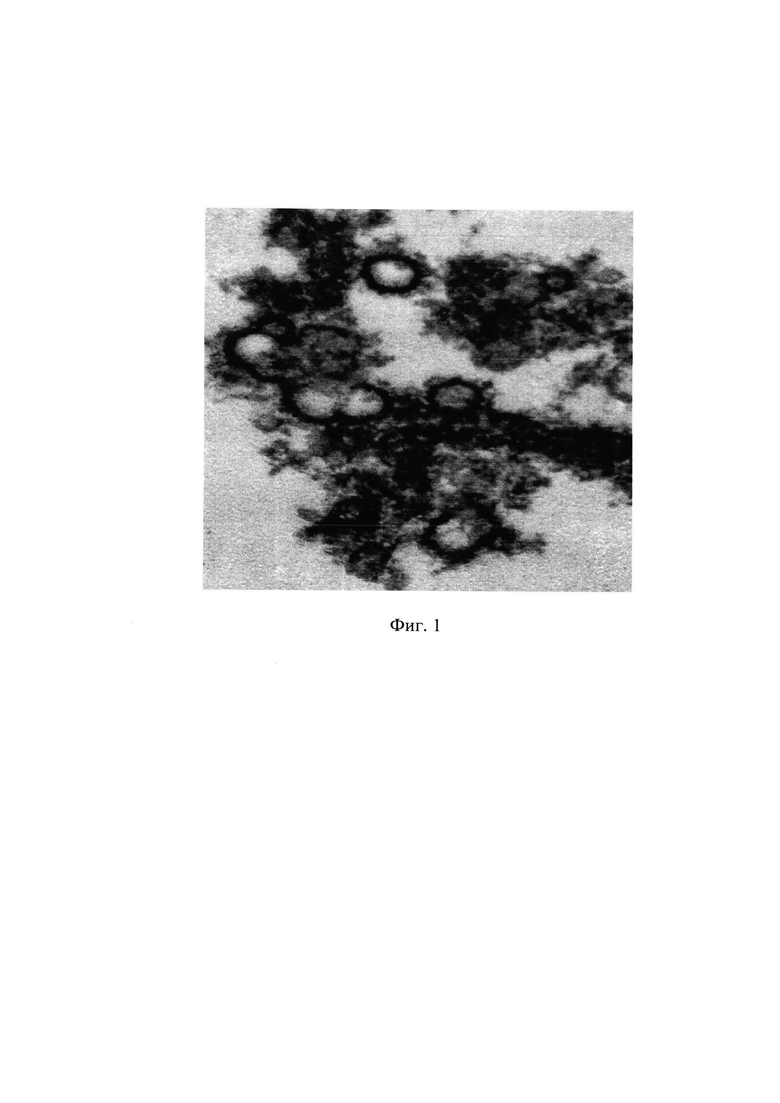
Фиг. 1. Трансмиссионная микроскопия эякулята. Показано наличие большого количества капсидов вируса папилломы человека. Ув. 25k.jpg. Вирус папилломы человека, свободно лежащий в эякуляте.
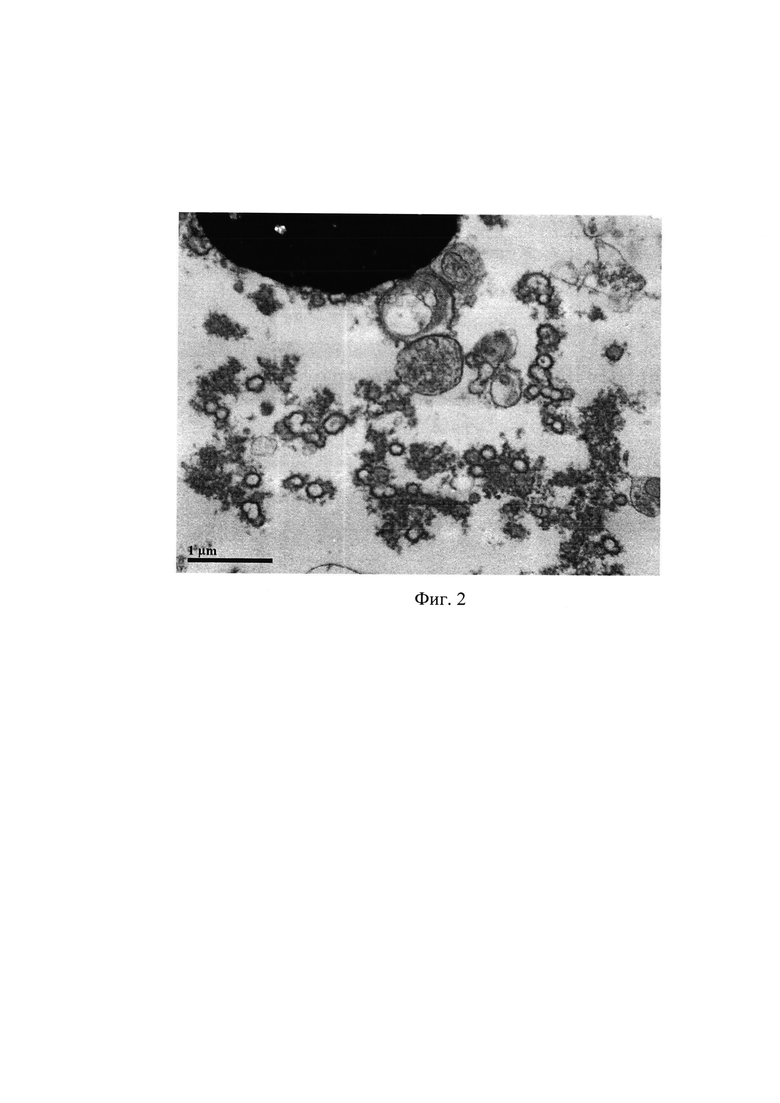
Фиг. 2. Трансмиссионная микроскопия эякулята. Показано наличие капсидов вируса, адгезированных на поверхности аномальной головки сперматозоида и свободно лежащие капсиды вируса папилломы человека в эякуляте. Ув. 25k.jpg. Вирус папилломы человека, адгезированный на сперматозоиде.
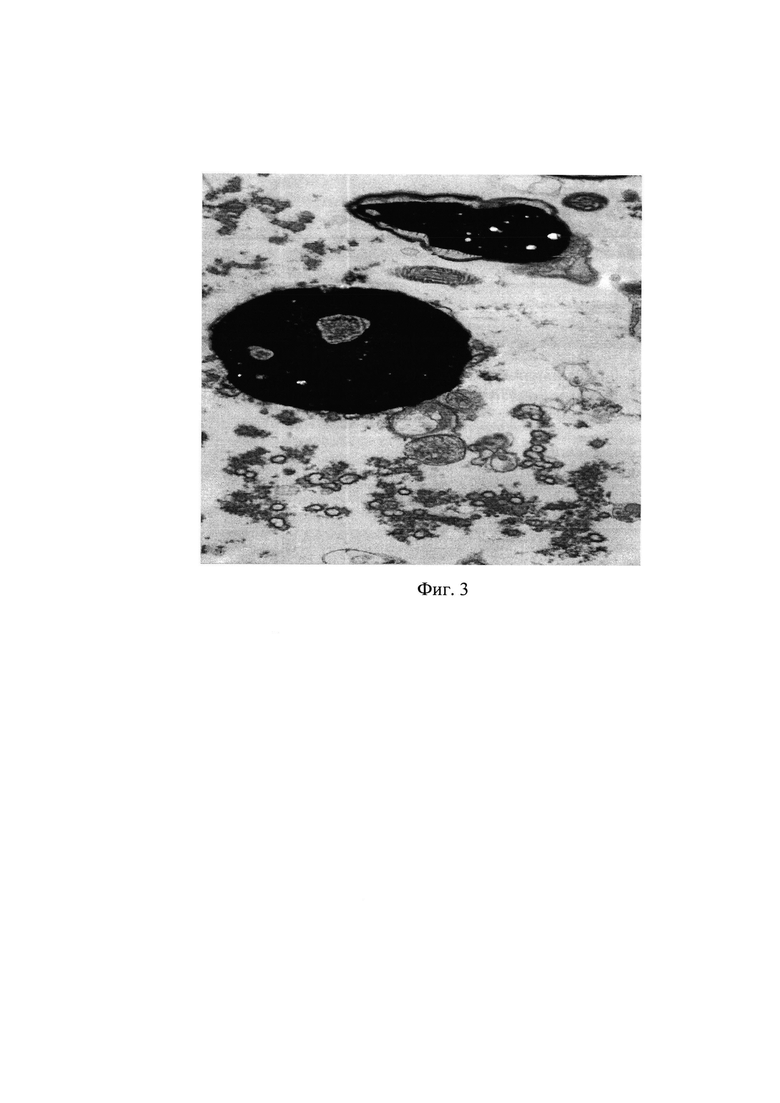
Фиг. 3. Трансмиссионная микроскопия эякулята. Показано наличие большого количества капсидов вируса папилломы человека и патология акросомы головки сперматозоида. Ув. 25k.jpg. Патология пластины акросомы сперматозоида.
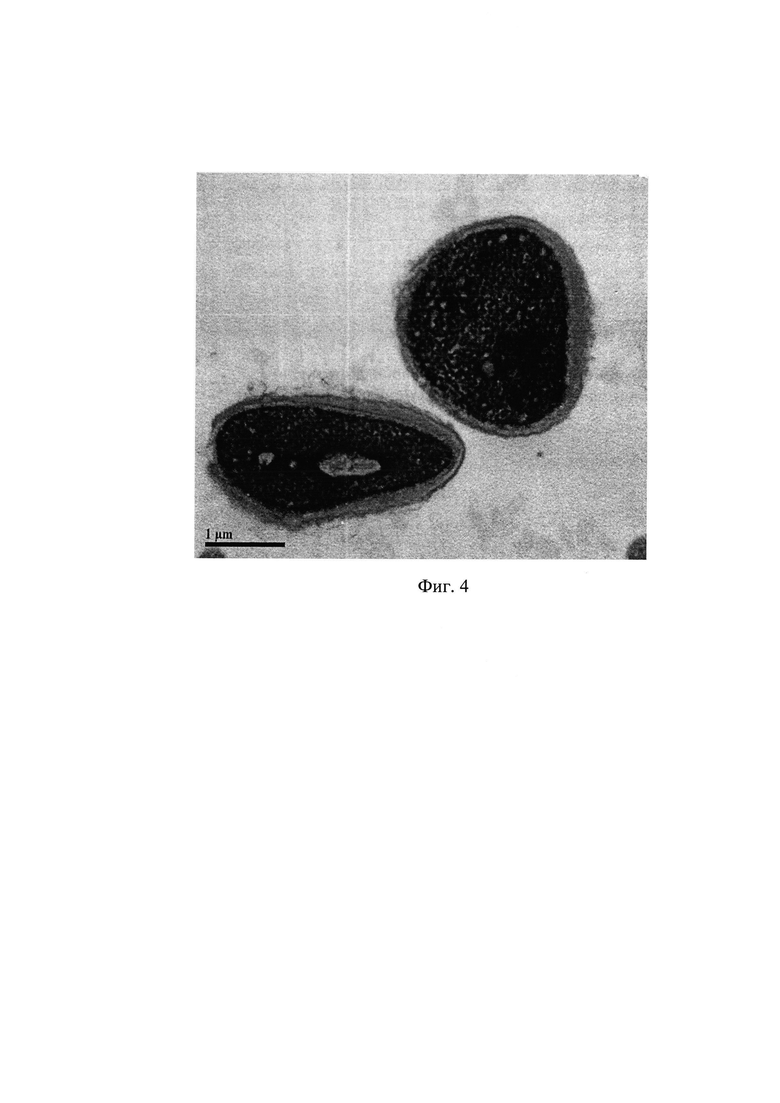
Фиг. 4. Трансмиссионная микроскопия эякулята. Показано наличие патологии головки сперматозоида. Ув. 25k.jpg. Патология хроматина сперматозоида.
Фиг. 5. Результаты лечения (наступления беременности) в 3 группах. Подробное описание способа и примеры его клинического выполнения.
Перед забором эякулята для выполнения трансмиссионной электронной микроскопии пациент за 3-4 дня до исследования исключает: прием лекарственных препаратов, алкоголь, посещение бани и сауны и воздерживается от половой жизни. Образцы эякулята были собраны в специальный стерильный контейнер путем мастурбации после рекомендуемого периода полового воздержания в течение 3-4 дней. После разжижения при комнатной температуре оценивали концентрацию, подвижность и нормальную морфологию сперматозоидов в соответствии с рекомендациями Всемирной организации здравоохранения по анализу спермы (2010). Аликвоту общей спермы каждого пациента отправляли в клиническую и морфологическую лаборатории.
Для электронной микроскопии нативный материал эякулята фиксировали 2,5% глютаровомальдегидом (AppliChem, Германия) в течение суток. После фиксации материал трехкратно (по 15 мин.) промывался в фосфатном буфере. После обработки в буферах исследуемые образцы помещались в 1% раствор Os04 (AcrosOrganics, Бельгия) на фосфатном буфере рН 7,2-7,4 на 1,5 часа, затем обезвоживались в спиртах восходящей концентрации и ацетоне, заключались в эпоксидную смолу Эпон-812 плоскопараллельным методом и полимеризовались при 60°). Полученные блоки из эпоксидной смолы вытачивались на высокоскоростной фрезе Leica ЕМ TRIM для получения полутонких срезов, окрашенных толуидиновым синим и поиска в них клубочков. Блоки из эпоксидной смолы, содержащие клубочки, подвергались ультрамикротомии алмазным ножом на ультрамикротоме Ultracut-UC6 (Leica, Германия). Толщина ультратонких срезов составляла 70 нм. Для контрастирования срезы обрабатывались 1,5% раствором уранилацетата на 70° этаноле и цитратом свинца. После контрастирования срезы просматривались в трансмиссионном электронном микроскопе Jem 1011 (Jeol, Япония) с помощью цифровой камеры Erlangshen ES500W (Gatan, США, Канада). Измерение размеров ультраструктур осуществлялось в абсолютных единицах (мкм и нм). При необходимости проводилась морфометрия ультраструктур с помощью программного обеспечения DigitalMicrograph (Gatan, США).
Если по данным трансмиссионной электронной микроскопии выявляют в эякуляте: 1. Вирус папилломы человека. 2. Адгезию вируса папилломы человека на поверхность сперматозоида. 3. Патоспермию, которая характеризуется:
- отсутствием акросомы сперматозида у 20% и выше сперматозоидов в эякуляте,
- наличием патологии постакросомной пластины акросомы сперматозида у 55% и выше сперматозоидов в эякуляте,
- наличием патологии хроматина сперматозоида у 35% и выше сперматозоидов в эякуляте,
то пациенту проводят иммунноактивную, противовирусную терапию.
Если по данным трансмиссионной электронной микроскопии не выявляют в эякуляте вируса папилломы человека и патоспермия характеризуется отсутствием сперматозоидов без акросомы и дефектов акросомной пластины, и наличием патологии хроматина сперматозоида у менее 10,5% сперматозоидов в эякуляте, то пациенту проводят терапию антиоксидантами (согласно клиническим рекомендациям Министерства здравоохранения Российской Федерации по лечению пациентов с идиопатической инфертильностью (нет известных причин)).
Таким образом, врач получает индивидуальные объективные критерии и информативные маркеры, позволяющие использовать обоснованную тактику лечения, подобрать соответствующую медикаментозную терапию.
Работоспособность заявляемого способа подтверждается следующими клиническими примерами.
Пример 1.
Больной П-ов, 31 год, обратился с жалобами на отсутствие беременности при регулярной половой жизни без использования противозачаточных средств в течение 5 лет.
Результаты обследования пациента:
У пациента нет критериев невключения.
По данным трансмиссионной электронной микроскопии выявлено наличие в эякуляте: 1. Вируса папилломы человека. 2. Адгезии вируса папилломы человека на поверхность сперматозоида. 3. Патоспермии, которая характеризуется: отсутствием акросомы сперматозида у 20% сперматозоидов в эякуляте, наличием постакросомной пластины акросомы сперматозида у 55% сперматозоидов в эякуляте, наличием патологии хроматина сперматозоида у 35% сперматозоидов в эякуляте.
Резюме: у пациента инфертильность, ассоциированная с вирусом папилломы человека. Согласно заявляемой методике, пациенту назначена иммунноактивная, противовирусная терапия (Аллокин-альфа в дозе 1 мг через день, всего на курс 6 инъекций, подкожно). При мониторинге через 16 мес.от начала лечения была зарегистрирована беременность в паре пациента.
Пример 2.
Больной Т-ев, 29 лет, обратился с жалобами на отсутствие беременности при регулярной половой жизни без использования противозачаточных средств в течение 5 лет (для чисто сравниваемых признаков, с одинаковой длительностью бесплодия).
Результаты обследования пациента:
У пациента нет критериев невключения.
По данным трансмиссионной электронной микроскопии в эякуляте не выявлено наличие вируса папилломы человека и патоспермия характеризуется отсутствием сперматозоидов без акросомы и дефектов акросомной пластины, и наличием патологии хроматина сперматозоида у 10% сперматозоидов в эякуляте.
Резюме: у пациента идиопатическая инфертильность. Согласно заявляемой методике, пациенту назначена антиоксидантная метаболическая терапия: (Селцинк плюс, по 1 таблетке 1 раз в день, во время приема пищи, продолжительность приема 1 месяц), что соответствует клиническим рекомендациям Министерства здравоохранения Российской Федерации по лечению пациентов с идиоптатической инфертильностью (нет известных причин).
При мониторинге за пациентом через 16 мес.от начала лечения отмечено, что беременность в паре пациента не наступила.
Преимущества заявляемой методики: способ безболезнен, безопасен, не инвазивен, доступен к применению как в стационаре, так и в амбулаторных условиях.
Использование заявленного заявляемого способа определения тактики лечения инфертильности ассоциированной с папилломавирусной инфекцией у мужчин позволяет обеспечить этиотропную тактику лечения инфертильности, ассоциированной с папилломавирусной инфекцией и может быть рекомендован к применению в широкой клинической практике андрологов, урологов и репродуктологов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ХРОНИЧЕСКОГО РЕЦИДИВИРУЮЩЕГО ЦИСТИТА | 2020 |
|
RU2723024C1 |
| Способ дифференциальной диагностики хронического простатита | 2019 |
|
RU2711657C1 |
| СПОСОБ ДИАГНОСТИКИ БЕСПЛОДИЯ У МУЖЧИН | 2008 |
|
RU2371720C1 |
| Способ определения тактики лечения хронического рецидивирующего бактериального простатита | 2020 |
|
RU2723997C1 |
| Способ прогнозирования рецидива хронического бактериального простатита | 2020 |
|
RU2738011C1 |
| Способ определения тактики лечения симптомов нижних мочевых путей, ассоциированных с доброкачественной гиперплазией простаты на фоне дефицита тестостерона | 2022 |
|
RU2795840C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ МУЖСКОГО БЕСПЛОДИЯ НА ОСНОВЕ АНАЛИЗА ФРАГМЕНТАЦИИ ДНК СПЕРМАТОЗОИДОВ | 2023 |
|
RU2804207C1 |
| Способ прогнозирования манифестации гипогонадизма у мужчин | 2022 |
|
RU2786597C1 |
| ПРЕПАРАТ НА ОСНОВЕ ГРИБА PLEUROTUS 1137, ВЛИЯЮЩИЙ НА МУЖСКУЮ РЕПРОДУКТИВНУЮ ФУНКЦИЮ | 2010 |
|
RU2422151C1 |
| Способ исследования мужской репродуктивной функции | 2023 |
|
RU2819094C1 |
Настоящее изобретение относится к медицине, а именно к урологии, и может быть использовано для определения тактики лечения инфертильности, ассоциированной с вирусом папилломы человека. Выполняют трансмиссионную электронную микроскопию эякулята и оценивают его вирусологические и качественные характеристики: присутствие в эякуляте вируса папилломы человека, адгезию вируса папилломы человека на поверхности сперматозоида, наличие патоспермии. Если по данным трансмиссионной электронной микроскопии в эякуляте выявляют вирус папилломы человека, адгезию вируса папилломы человека на поверхности сперматозоида и патоспермию, которая характеризуется: отсутствием акросомы сперматозида у 20% и выше сперматозоидов в эякуляте, наличием патологии постакросомной пластины акросомы сперматозида у 55% и выше сперматозоидов в эякуляте, наличием патологии хроматина сперматозоида у 35% и выше сперматозоидов в эякуляте, то пациенту проводят иммуноактивную, противовирусную терапию. Если по данным трансмиссионной электронной микроскопии в эякуляте не выявляют вирус папилломы человека и патоспермия характеризуется: отсутствием сперматозоидов без акросомы и дефектов акросомной пластины и наличием патологии хроматина сперматозоида у менее 10,5% сперматозоидов в эякуляте, то пациенту проводится антиоксидантная терапия. Изобретение обеспечивает повышение точности и достоверности выбора тактики лечения инфертильности, ассоциированной с вирусом папилломы человека, что позволяет повысить эффективность терапии пациентов с данной нозологией. 2 пр., 5 ил.
Способ определения тактики лечения инфертильности, ассоциированной с папилломавирусной инфекцией у мужчин, включающий выполнение трансмиссионной электронной микроскопии эякулята и назначение иммуноактивной противовирусной терапии, отличающийся тем, что осуществляют исследование эякулята методом трансмиссионной электронной микроскопии, определение в эякуляте вируса папилломы человека, адгезию вируса папилломы человека на поверхности сперматозоида, наличие патоспермии, и если по данным трансмиссионной электронной микроскопии в эякуляте выявляют вирус папилломы человека, адгезию вируса папилломы человека на поверхности сперматозоида и патоспермию, которая характеризуется: отсутствием акросомы сперматозида у 20% и выше сперматозоидов в эякуляте, наличием патологии постакросомной пластины акросомы сперматозида у 55% и выше сперматозоидов в эякуляте, наличием патологии хроматина сперматозоида у 35% и выше сперматозоидов в эякуляте, то пациенту назначают иммуноактивную, противовирусную терапию; если же по данным трансмиссионной электронной микроскопии в эякуляте не выявляют вирус папилломы человека и патоспермия характеризуется отсутствием сперматозоидов без акросомы и дефектов акросомной пластины, наличием патологии хроматина сперматозоида у менее 10,5% сперматозоидов в эякуляте, то пациенту назначают антиоксидантную терапию.
| СПОСОБ ЛЕЧЕНИЯ ПАПИЛЛОМАВИРУСНОЙ ИНФЕКЦИИ | 2011 |
|
RU2478390C2 |
| СПОСОБ ЛЕЧЕНИЯ ПАПИЛЛОМАВИРУСНЫХ ИНФЕКЦИЙ, РЕАЛИЗУЕМЫЙ ЧЕРЕЗ ИНДУКЦИЮ ИНТЕРЛЕЙКИНА-18 | 2010 |
|
RU2482866C2 |
| GEP 20022749 B, 26.08.2002 | |||
| Ибишев Х.С., Рябенченко Н.Н., Магомедов Г.А | |||
| Идиопатическое мужское бесплодие и папилломавирусная инфекция | |||
| Вестник урологии | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Маркелова Е.В., Тулупова М.С., Хамошина М.Б., Чепурнова Н.С., Невежкина Т.А | |||
| Роль мужского фактора в невынашивании | |||
Авторы
Даты
2023-11-07—Публикация
2023-06-13—Подача