ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение относится к области биофармацевтических и терапевтических препаратов. Более конкретно, данное изобретение относится к соединениям, композициям и способам, включающим фузогенные молекулы, которые обеспечивают наночастицы для доставки и распределения действующих агентов или лекарственных соединений в клетках, тканях, органах и субъектах.
УРОВЕНЬ ТЕХНИКИ
[0002] Терапевтические агенты, такие как лекарственные соединения, молекулы нуклеиновых кислот и другие действующие агенты, функционируют после поглощения клетками, тканями и органами субъекта. Перенос агентов и молекул в клетки часто является лимитирующим этапом для их терапевтической активности.
[0003] Когда молекулы действующего агента чувствительны к атаке или деградации в сыворотке или в другом биологическом окружении, возникает необходимость защиты молекулы для достижения ее лекарственного эффекта.
[0004] Например, одним из способов осуществления трансфекции нуклеиновых кислот является включение или инкапсуляция действующих молекул в наночастицы. Недостатком такой методологии может являться низкая степень проникновения в клетки.
[0005] Существует давняя потребность в молекулах, обладающих фузогенными свойствами, которые позволяли бы получить наночастицы, обладающими хорошими трансфекционными свойствами, для увеличения степени проникновения и доставки действующих агентов в клетки.
[0006] Необходимыми являются композиции и соединения для создания наночастиц для действующих веществ. Существует постоянная потребность в молекулах и композициях для эффективной трансфекции и распределения молекул нуклеиновых кислот и других агентов в клетках и субъектах.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
[0007] Настоящее изобретение относится к молекулам и их композициям для использования в биофармацевтических и терапевтических препаратах. Более конкретно, данное изобретение относится к соединениям, композициям и способам получения наночастиц для доставки и распределения действующих агентов или лекарственных соединений в клетках, тканях, органах и субъектах.
[0008] Данное изобретение относится к ряду фузогенных соединений. Фузогенные соединения по данному изобретению могут быть использованы для образования наночастиц для доставки и распределения действующих агентов.
[0009] Примеры действующих агентов по данному изобретению включают биологически активные молекулы, нуклеиновые кислоты, ДНК, РНК, мРНК, киРНК и микроРНК, среди других форм.
[0010] Варианты осуществления данного изобретения включают в себя следующее:
[0011] Фузогенное соединение, имеющее формулу I:
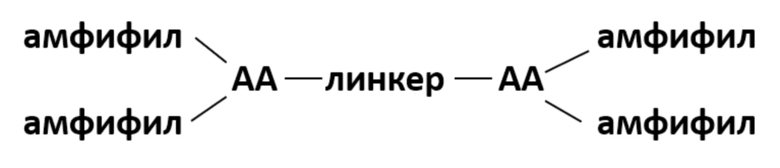 Формула I,
Формула I,
где каждый амфифил независимо содержит от одной до двух липофильных цепей, где каждая липофильная цепь независимо содержит от 8 до 22 атомов углерода;
где каждый АА независимо представляет собой аминокислоту, содержащую боковую цепь, имеющую аминогруппу, где аминокислота присоединена к амфифилу по каждой из своих аминогрупп и присоединена к линкеру на своем С-конце;
где линкер имеет структуру
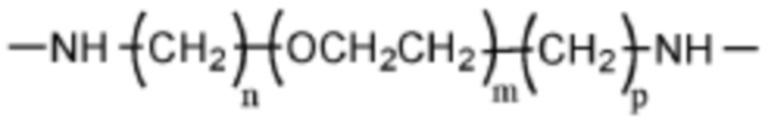
или
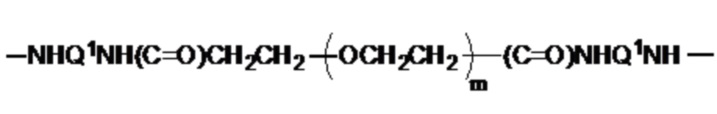 ,
,
где Q1 представляет собой разветвленный или неразветвленный C(2-8)алкандиил, разветвленный или неразветвленный C(2-8)алкендиил, разветвленный или неразветвленный C(2-8)алкиндиил или
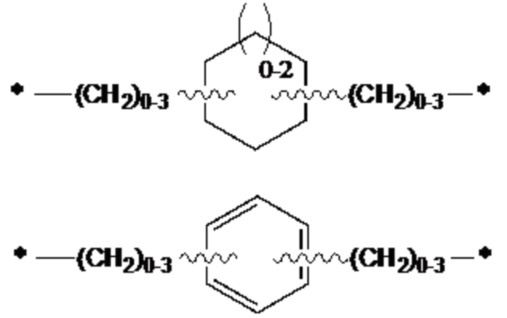
или
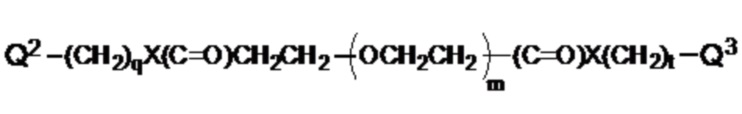 ,
,
где Q2 представляет собой
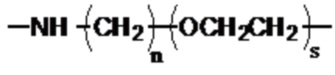 ,
,
где Q3 представляет собой
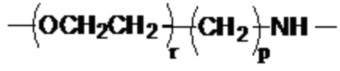 ,
,
где X представляет собой -O-, -S- или -NH-;
n, p, q и t независимо для каждого случая составляют от 1 до 3;
m независимо составляет от 1 до 10;
r и s независимо для каждого случая составляют от 1 до 5.
[0012] Указанное выше фузогенное соединение, где АА выбирают из следующих структур и любых их стереоизомеров:
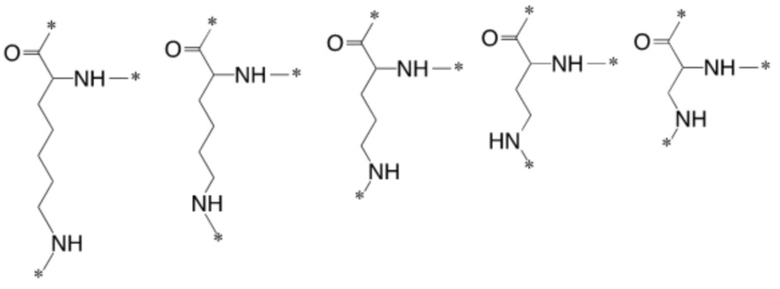
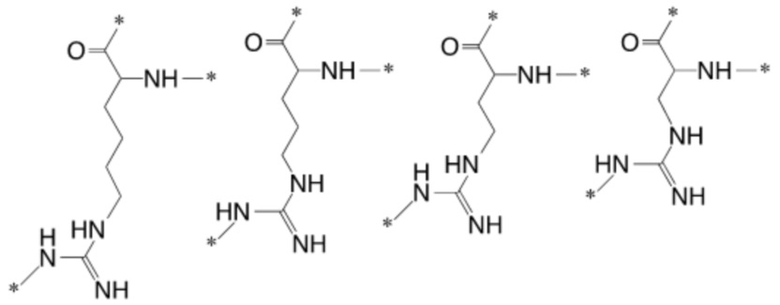
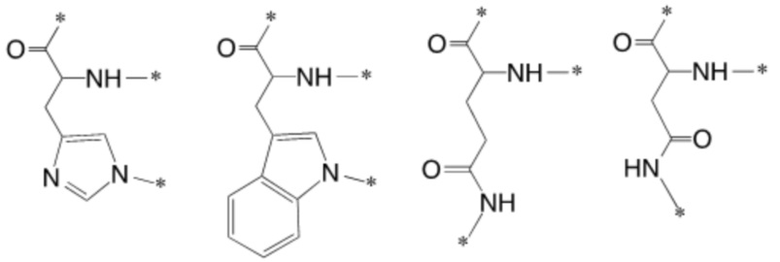 .
.
[0013] Указанное выше фузогенное соединение, где один или два амфифила отсутствуют и замещены алкильной группой или фармацевтически приемлемой органической химической группой, имеющей 1-400 атомов, выбранных из углерода, кислорода, азота, серы, фтора и водорода.
[0014] Указанное выше фузогенное соединение, где фармацевтически приемлемая органическая химическая группа представляет собой алкил, алкенил, алкинил, ацетил, Boc, Fmoc, TFA или CBZ, предпочтительно алкил, ацетил, более предпочтительно, ацетил.
[0015] Указанное выше фузогенное соединение, где соединение выбирают из следующих соединений:
[0016] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле II
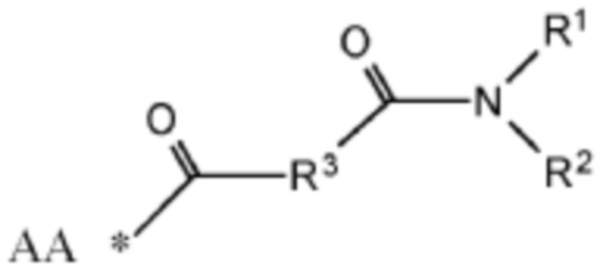 Формула II,
Формула II,
где R1 и R2 представляют собой
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
где n и m, каждый независимо, составляют от 1 до 2; и R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 выбирают из разветвленного или неразветвленного С(1-8)алкандиила, замещенного или незамещенного С(2-8)алкендиила, замещенного или незамещенного С(2-8)алкиндиила, замещенного или незамещенного С(3-8)циклоалкандиила, замещенного или незамещенного арилена, замещенного или незамещенного С(4-8)гетероарилена и замещенного или незамещенного гетероциклоалкандиила и их комбинаций; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0017] R3, предпочтительно, представляет собой разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0018] Используемый в настоящем документе термин «и их комбинации» применительно к формулам указывает на дополнительные изменения в структуре на основе объединения перечисленных групп. Например, комбинация C(1-8)алкандиила и C(4-8)гетероарилена относится к C(1-8)алкандиил-C(4-8)гетероарилену, а также к C(1-8)алкандиил-C(4-8)гетероарилен-C(1-8)алкандиилу.
[0019] Указанное выше фузогенное соединение, где R3 выбирают из разветвленного или неразветвленного C(2-8)алкандиила,
замещенного или незамещенного С(2-8)алкендиил,
замещенного или незамещенного С(2-8)алкиндиила,
замещенного или незамещенного С(3-8)циклоалкандиила,
замещенного или незамещенного С(4-8)гетероарилена,
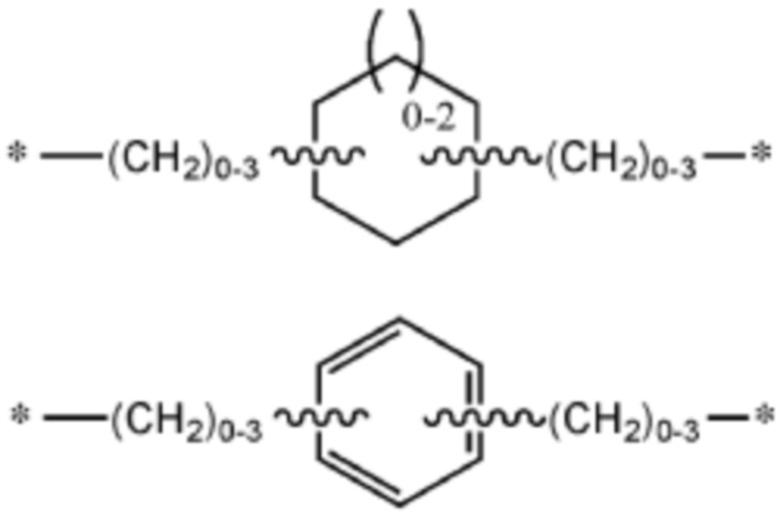 ;
;
предпочтительно, разветвленного или неразветвленного С(2-8)алкандиила, замещенного или незамещенного С(3-8)циклоалкандиила.
[0020] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле III:
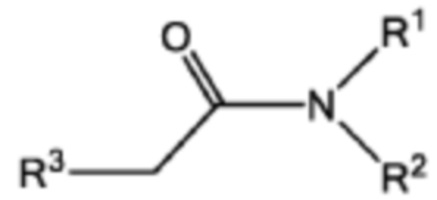 Формула III,
Формула III,
где R1 и R2 представляют собой:
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
где n и m, каждый независимо, составляют от 1 до 2; и R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 выбирают из:
-алкил-(C=O)-, который присоединен к AA;
-алкил-O(C=O)-, который присоединен к AA;
-алкил-NH(C=O)-, который присоединен к AA;
-алкил-(C=O)-алкил-(C=O)-, который присоединен к AA;
-алкил-O(C=O)-алкил-(C=O)-, который присоединен к AA;
-алкил-NH(C=O)-алкил-(C=O)-, который присоединен к AA;
-алкенил-(C=O)-, который присоединен к AA;
-алкенил-O(C=O)-, который присоединен к AA;
-алкенил-NH(C=O)-, который присоединен к AA;
-алкенил-(C=O)-алкенил-(C=O)-, который присоединен к AA;
-алкенил-O(C=O)-алкенил-(C=O)-, который присоединен к AA;
-алкенил-NH(C=O)-алкенил-(C=O)-, который присоединен к AA;
-алкинил-(C=O)-, который присоединен к AA;
-алкинил-O(C=O)-, который присоединен к AA;
-алкинил-NH(C=O)-, который присоединен к AA;
-алкинил-(C=O)-алкинил-(C=O)-, который присоединен к AA;
-алкинил-O(C=O)-алкинил-(C=O)-, который присоединен к AA;
-алкинил-NH(C=O)-алкинил-(C=O)-, который присоединен к AA,
где любой алкил в R3 представляет собой разветвленный или неразветвленный C(1-6)алкил, любой алкенил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкенил, и любой алкинил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкинил;
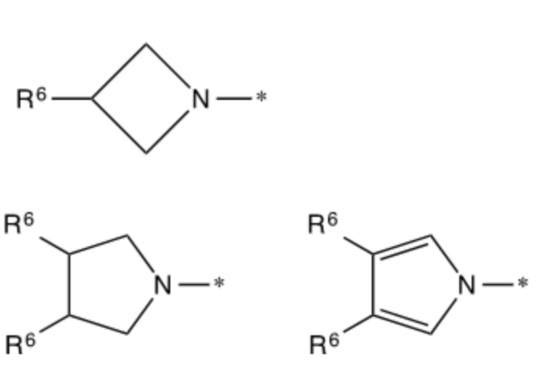

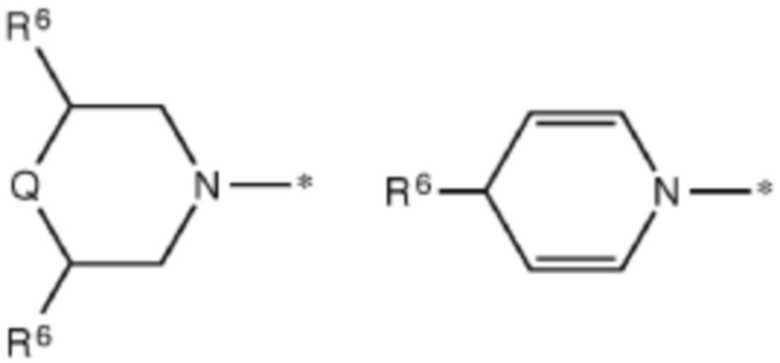
и их позиционные изомеры;
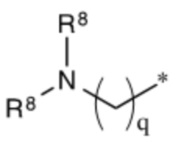
 ,
,
где каждый R6 независимо выбирают из H, алкила, алкокси-группы и алкоксиалкокси-группы, при условии, что один R6 представляет собой -(C=O)- или -алкил-(C=O)-, который присоединен к AA;
каждый R8 независимо выбирают из H, алкила, при условии, что один R8 представляет собой -(C=O)- или -алкил-(C=O)-, который присоединен к AA;
q составляет от нуля до четырех;
Q является О или N.
[0021] Указанное выше фузогенное соединение, где алкил в R6 и R8, каждый независимо, представляет собой разветвленный или неразветвленный C(1-6)алкил, алкокси-группа в R6 представляет собой C(1-6)алкокси, и алкоксиалкокси-группа в R6 представляет собой C(1-6)алкокси-C(1-6)алкокси.
[0022] Указанное выше фузогенное соединение, где R4 и R5 независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу, предпочтительно, C(14-18)алкенильную группу, имеющую от 2 до 4 двойных связей.
[0023] Указанное выше фузогенное соединение, где соединение выбирают из следующих соединений:
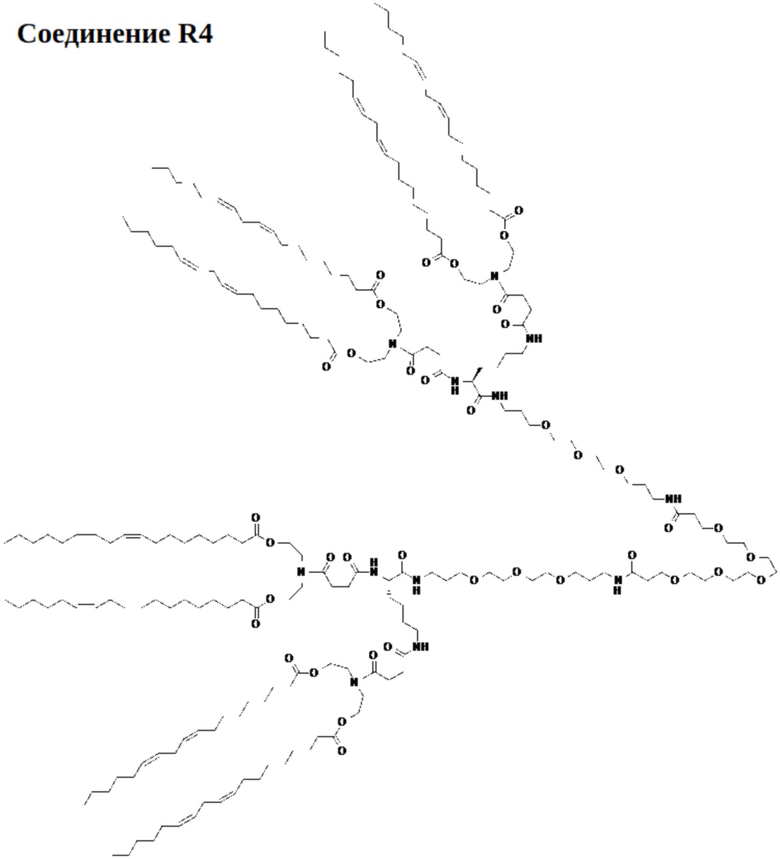
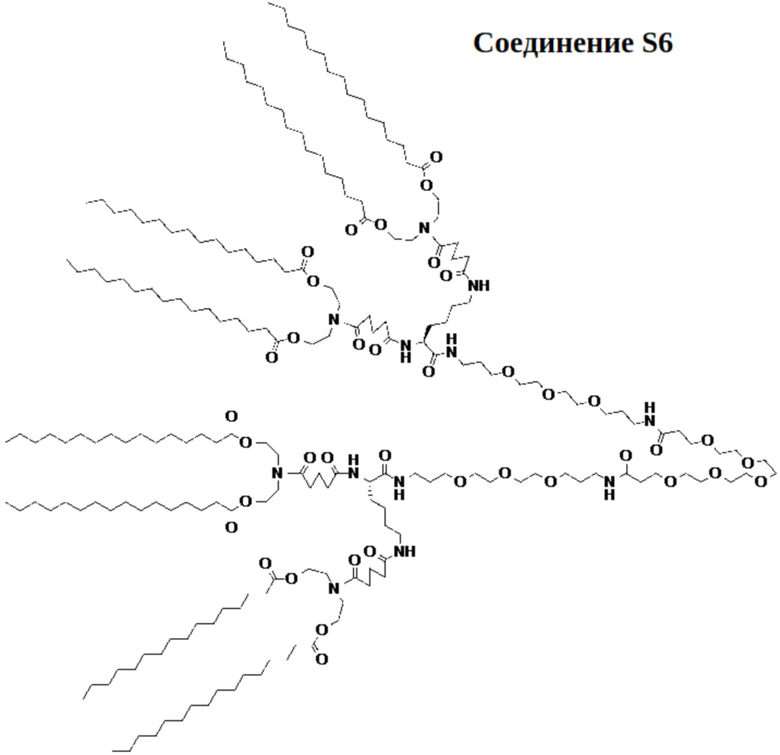
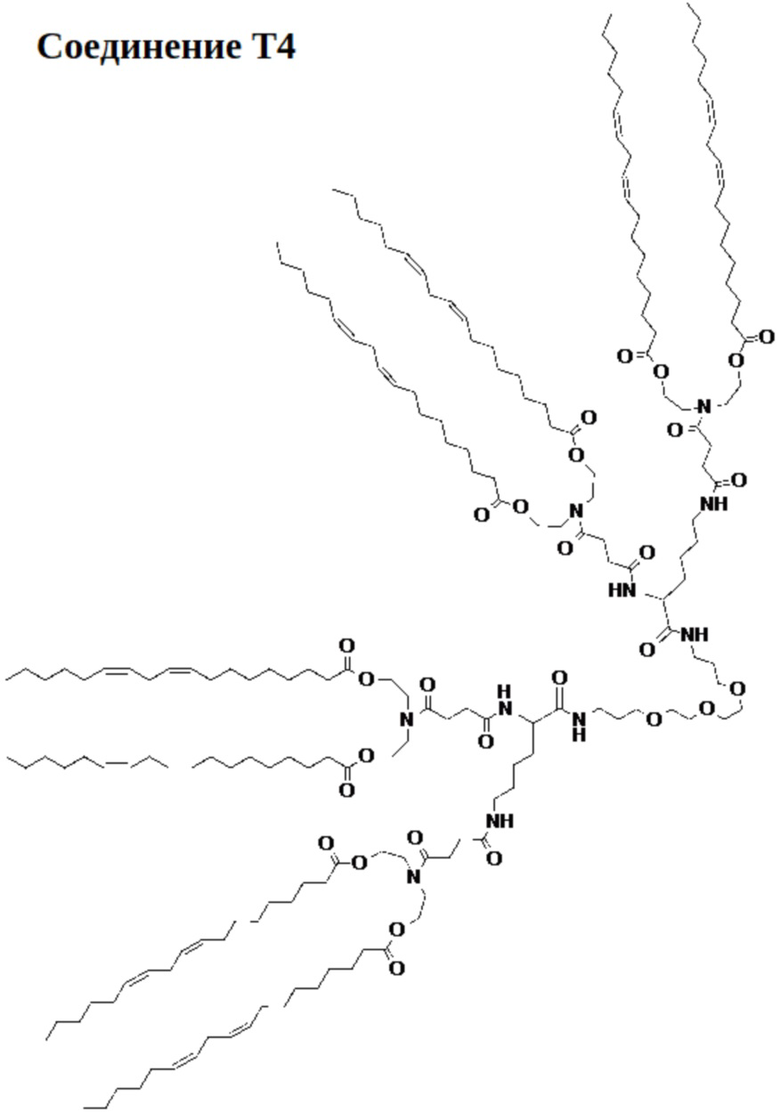
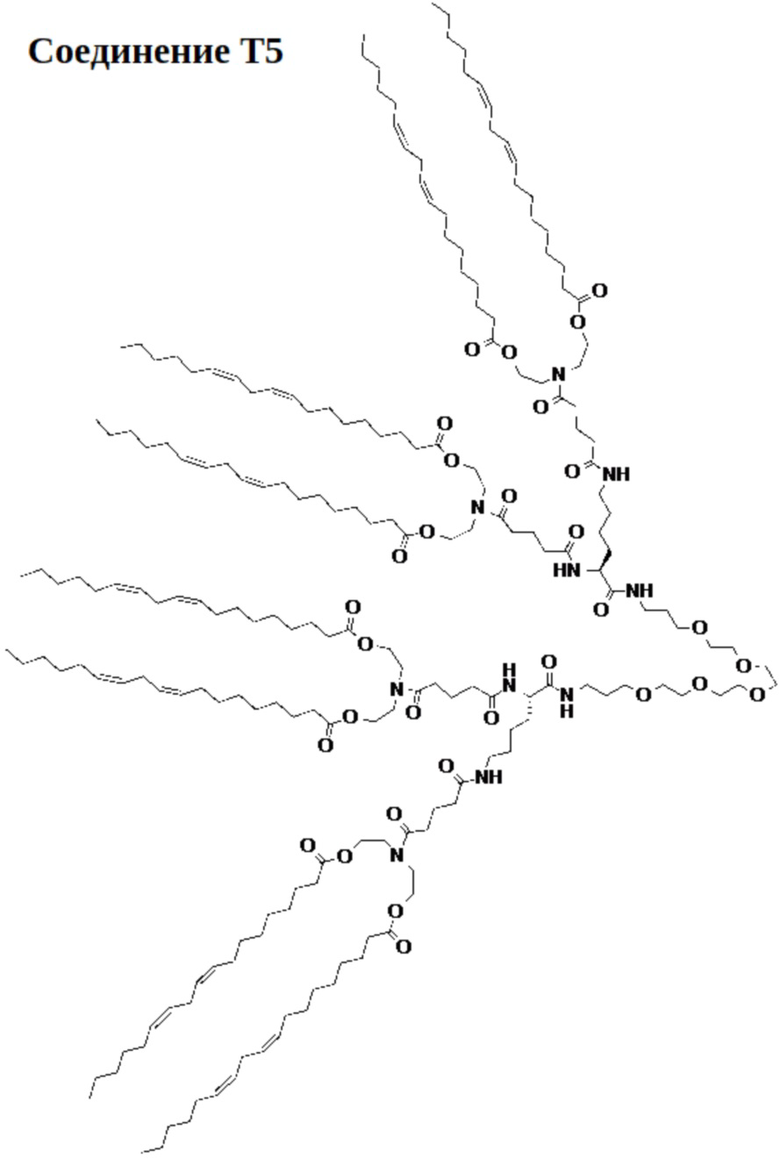
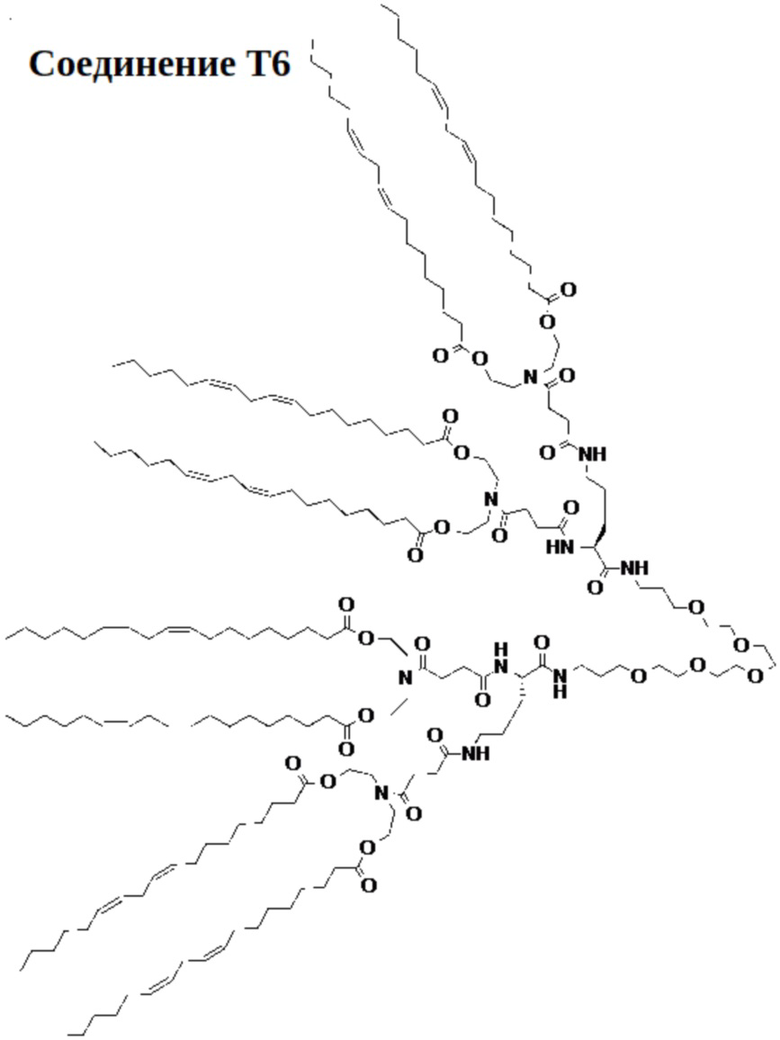
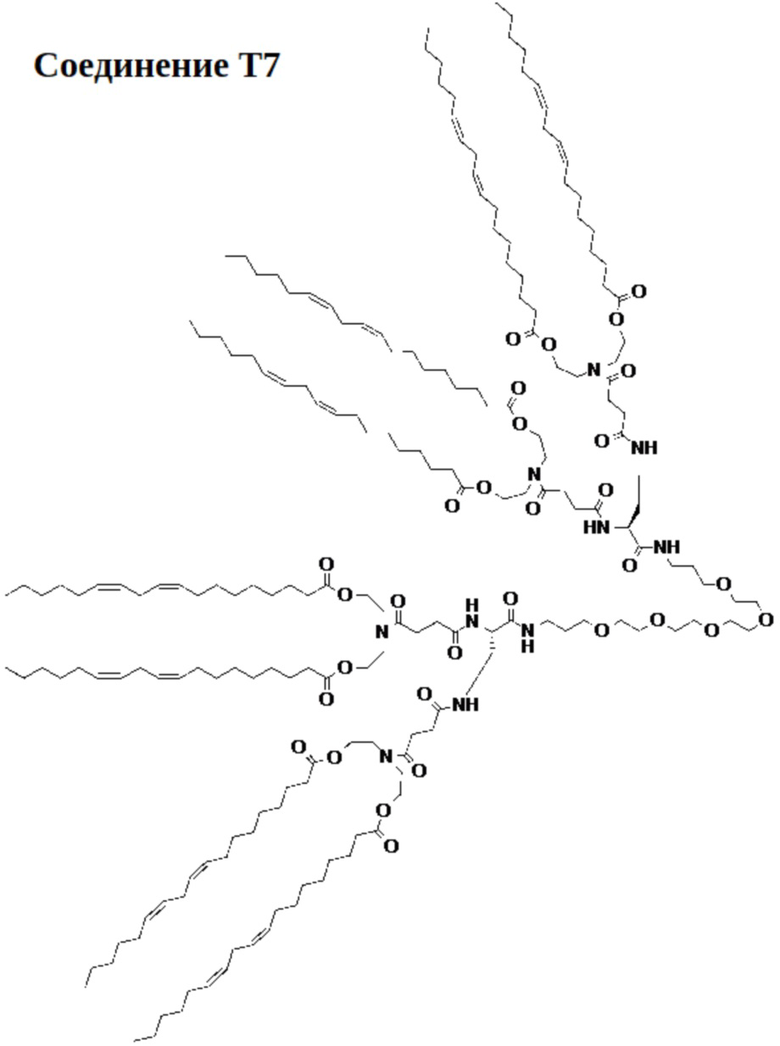
 .
.
[0024] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле III:
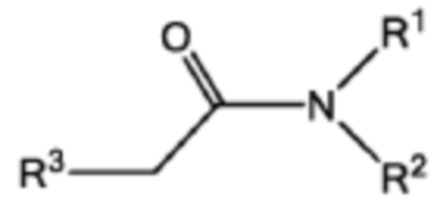 Формула III,
Формула III,
где R1 и R2 представляют собой:
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
где
n и m, каждый независимо, составляют от 1 до 2;
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
R3 представляет собой C(1-12)алкильную группу или C(4-12)алкенильную группу, которая замещена -(C=O)- или -алкил-(C=O)-, которые присоединены к AA.
[0025] Указанное выше фузогенное соединение, где R4 и R5 независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу, предпочтительно, C(14-18)алкенильную группу, имеющую от 2 до 4 двойных связей.
[0026] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле IV:
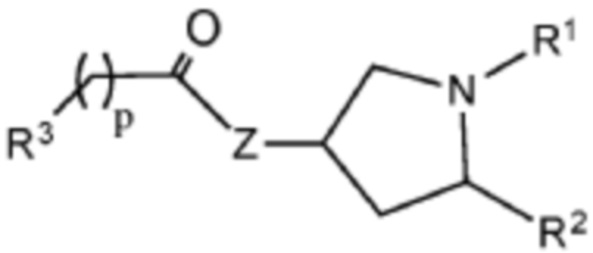 Формула IV,
Формула IV,
где R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, (C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5
где R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
Z является О или NH; р составляет от 0 до 5;
где R3 выбирают из разветвленного или неразветвленного С(1-8)алкандиил-(C=O)-, который присоединен к АА, замещенного или незамещенного С(2-8)алкендиил-(C=O)-, который присоединен к AA, замещенного или незамещенного C(2-8)алкиндиил-(C=O)-, который присоединен к AA, замещенного или незамещенного C(3-8)циклоалкандиил-(C=O)-, который присоединен к AA, замещенного или незамещенного арилен-(C=O)-, который присоединен к АА, замещенного или незамещенного С(4-8)гетероарилен-(C=O)-, который присоединен к АА, и замещенного или незамещенного гетероциклоалкандиил-(C=O)-, который присоединен к АА; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0027] R3, предпочтительно, представляет собой разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0028] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле IV:
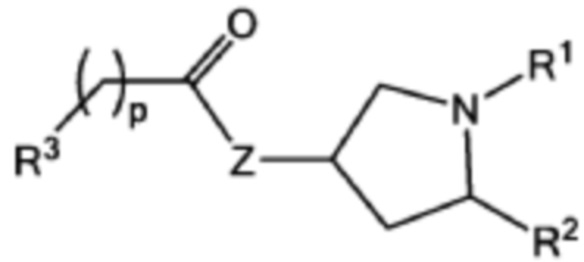 Формула IV,
Формула IV,
где R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, (C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5,
где R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
Z является О или NH; р составляет от 0 до 5;
где R3 выбирают из C(1-12)алкильной группы или C(2-12)алкенильной группы, которая замещена -(C=O)-группой, которая присоединена к AA,


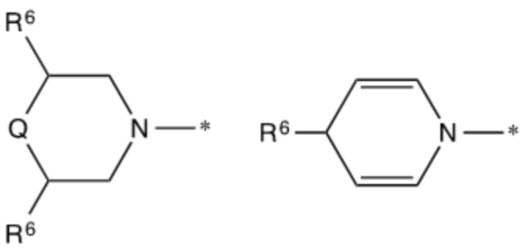
и их позиционных изомеров;
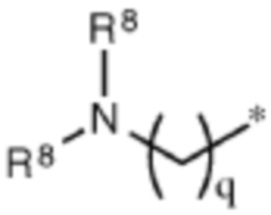 ,
,
где каждый R6 независимо выбирают из H, алкила, алкокси-группы и алкоксиалкокси-группы, при условии, что один R6 представляет собой -(C=O)- или -алкил-(C=O)-, который присоединен к AA;
каждый R8 независимо выбирают из H, алкила, при условии, что один R8 представляет собой -(C=O)- или -алкил-(C=O)-, который присоединен к AA;
q составляет от нуля до четырех;
Q является О или N.
[0029] Указанное выше фузогенное соединение, где R4 и R5 независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу, предпочтительно, C(14-18)алкенильную группу, имеющую от 2 до 4 двойных связей.
[0030] Указанное выше фузогенное соединение, где соединение представляет собой соединение T10:
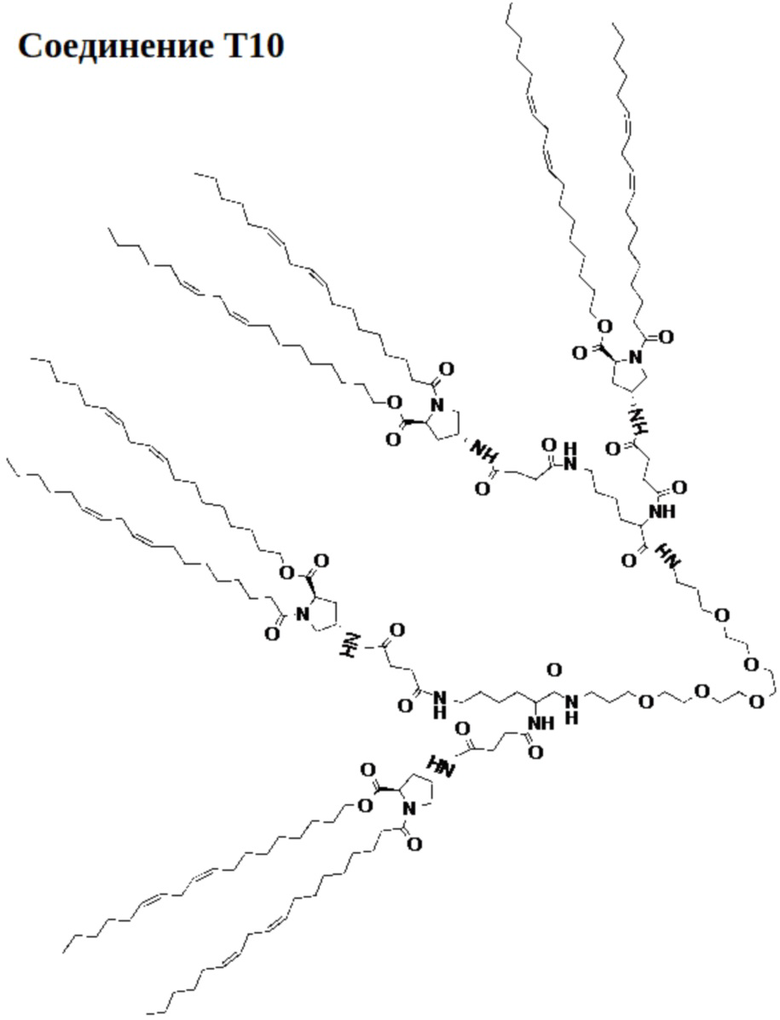 .
.
[0031] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле IV:
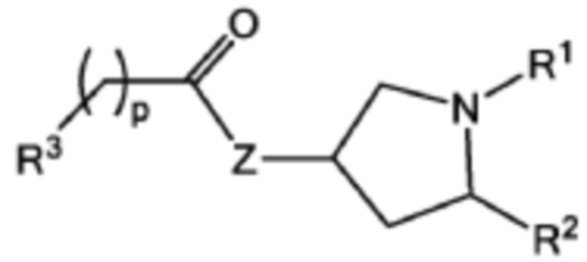 Формула IV,
Формула IV,
где R1 и R2 представляют собой:
R1 представляет собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
R2 представляет собой (CH2)nXR4, где n составляет от 0 до 3, Х представляет собой О, S, SO, SO2, NH;
где R4 представляет собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где Z представляет собой О или NH;
где р равно 1;
где R3 выбирают из
C(1-12)алкильной группы или C(2-12)алкенильной группы, которая замещена -(C=O)-группой, которая присоединена к AA.
[0032] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в Формуле V:
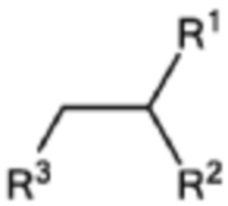 Формула V,
Формула V,
где R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, NH(C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5,
где R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 выбирают из разветвленного или неразветвленного -O(C=O)-C(1-8)алкандиил-(C=O)-, который присоединен к АА, замещенного или незамещенного -O(C=O)-C(2-8)алкендиил-(C=O)-, который присоединен к АА, замещенного или незамещенного -O(C=O)-C(2-8)алкиндиил-(C=O)-, который присоединен к АА, замещенного или незамещенного -O(C=O)-C(3-8)циклоалкандиил-(C=O)-, который присоединен к АА, замещенного или незамещенного -O(C=O)-арилен-(C=O)-, который присоединен к АА, замещенного или незамещенного -O(C=O)-C(4-8)гетероарилен-(C=O)-, который присоединен к АА, и замещенного или незамещенного -O(C=O)-гетероциклоалкандиил-(C=O)-, который присоединен к АА; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0033] R3, предпочтительно, представляет собой разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0034] Указанное выше фузогенное соединение, где R4 и R5 независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу, предпочтительно, C(14-18)алкенильную группу, имеющую от 2 до 4 двойных связей.
[0035] Указанное выше фузогенное соединение, где соединение представляет собой соединение T12:
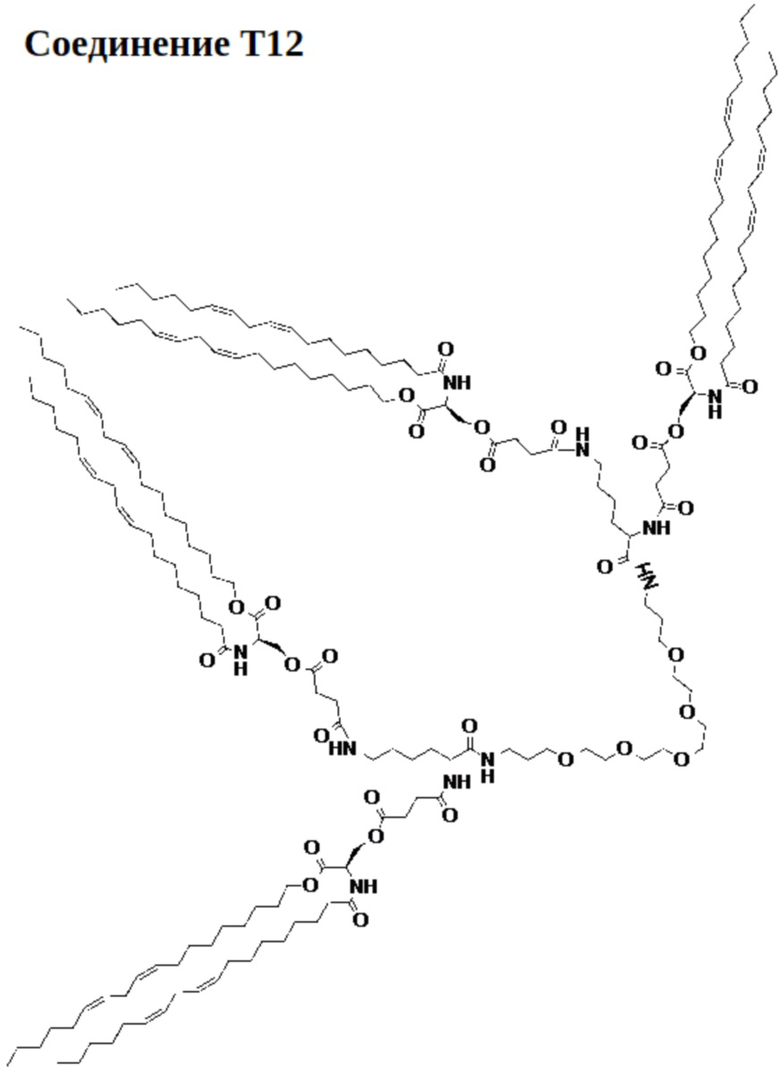
[0036] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле V:
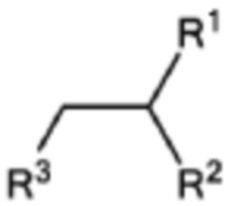 Формула V,
Формула V,
где R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, NH(C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5,
где R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 выбирают из:
-(C=O)- или -алкил-(C=O)-, который присоединен к АА;
-O(C=O)- или -алкил-O(C=O)-, который присоединен к АА;
-O(C=O)-алкандиил-(C=O)-, который присоединен к АА;
-O(C=O)-алкендиил-(C=O)-, который присоединен к АА;
-O(C=O)-алкиндиил-(C=O)-, который присоединен к АА;
-NH(C=O)- или -алкил-NH(C=O)-, который присоединен к АА;
-алкил-(C=O)-алкил-(C=O)-, который присоединен к АА;
-алкил-O(C=O)-алкил-(C=O)-, который присоединен к АА;
-алкил-NH(C=O)-алкил-(C=O)-, который присоединен к АА;
-алкенил-(C=O)-, который присоединен к АА;
-алкенил-O(C=O)-, который присоединен к АА;
-алкенил-NH(C=O)-, который присоединен к АА;
-алкенил-(C=O)-алкендиил-(C=O)-, который присоединен к АА;
-алкенил-O(C=O)-алкендиил-(C=O)-, который присоединен к АА;
-алкенил-NH(C=O)-алкендиил-(C=O)-, который присоединен к АА;
-алкинил-(C=O)-, который присоединен к АА;
-алкинил-O(C=O)-, который присоединен к АА;
-алкинил-NH(C=O)-, который присоединен к АА;
-алкинил-(C=O)-алкиндиил-(C=O)-, который присоединен к АА;
-алкинил-O(C=O)-алкиндиил-(C=O)-, который присоединен к АА;
-алкинил-NH(C=O)-алкиндиил-(C=O)-, который присоединен к АА;
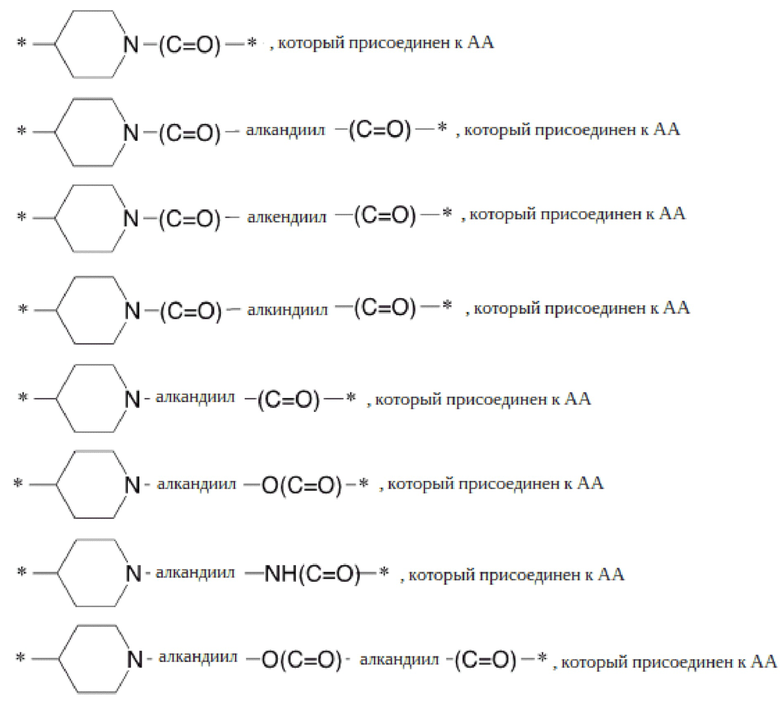
и их позиционных изомеров;
где любой алкил в R3 представляет собой разветвленный или неразветвленный C(1-6)алкил, любой алкенил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкенил, и любой алкинил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкинил.
[0037] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле VI:
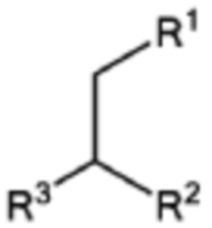 Формула VI,
Формула VI,
где R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, NH(C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5,
где
R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 выбирают из разветвленного или неразветвленного С(1-8)алкандиил-(C=O)-, который присоединен к АА, замещенного или незамещенного С(2-8)алкендиил-(C=O)-, который присоединен к AA, замещенного или незамещенного C(2-8)алкиндиил-(C=O)-, который присоединен к AA, замещенного или незамещенного C(3-8)циклоалкандиил-(C=O)-, который присоединен к AA, замещенного или незамещенного арилен-(C=O)-, который присоединен к АА, замещенного или незамещенного С(4-8)гетероарилен-(C=O)-, который присоединен к АА, и замещенного или незамещенного гетероциклоалкандиил-(C=O)-, который присоединен к АА; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0038] R3, предпочтительно, представляет собой разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0039] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле VI:
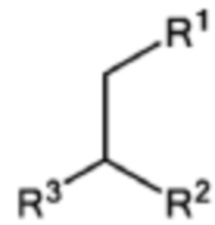 Формула VI,
Формула VI,
где R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, NH(C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5,
Где
R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 выбирают из:
-алкил-(C=O)-, который присоединен к AA;
-алкил-O(C=O)-, который присоединен к AA;
-алкил-NH(C=O)-, который присоединен к AA;
-алкил-(C=O)-алкил-(C=O)-, который присоединен к AA;
-алкил-O(C=O)-алкил-(C=O)-, который присоединен к AA;
-алкил-NH(C=O)-алкил-(C=O)-, который присоединен к AA;
-алкенил-(C=O)-, который присоединен к AA;
-алкенил-O(C=O)-, который присоединен к AA;
-алкенил-NH(C=O)-, который присоединен к AA;
-алкенил-(C=O)-алкенил-(C=O)-, который присоединен к AA;
-алкенил-O(C=O)-алкенил-(C=O)-, который присоединен к AA;
-алкенил-NH(C=O)-алкенил-(C=O)-, который присоединен к AA;
-алкинил-(C=O)-, который присоединен к AA;
-алкинил-O(C=O)-, который присоединен к AA;
-алкинил-NH(C=O)-, который присоединен к AA;
-алкинил-(C=O)-алкинил-(C=O)-, который присоединен к AA;
-алкинил-O(C=O)-алкинил-(C=O)-, который присоединен к AA;
-алкинил-NH(C=O)-алкинил-(C=O)-, который присоединен к AA,
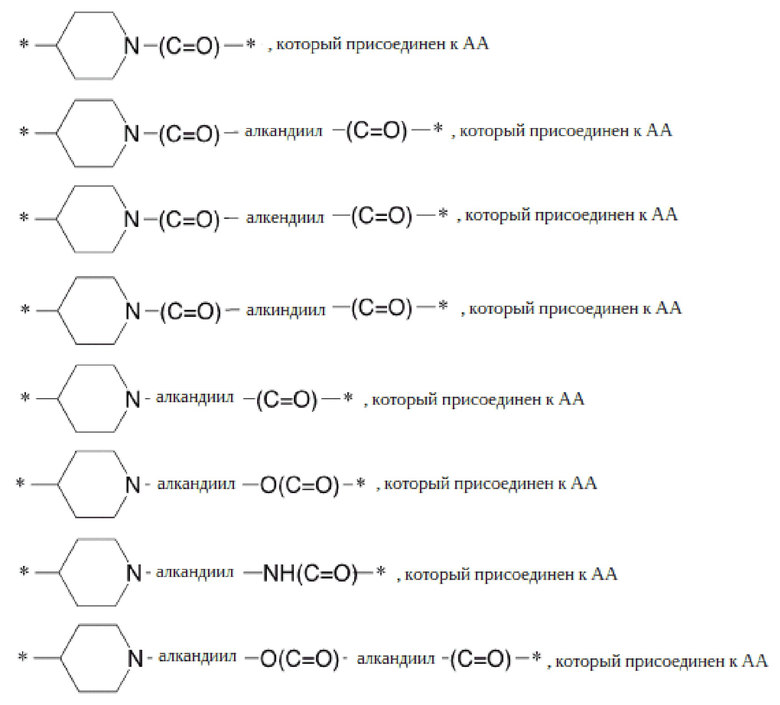
и их позиционных изомеров;
где любой алкил в R3 представляет собой разветвленный или неразветвленный C(1-6)алкил, любой алкенил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкенил, и любой алкинил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкинил.
[0040] Указанное выше фузогенное соединение, где R4 и R5 независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу, предпочтительно, C(14-18)алкенильную группу, имеющую от 2 до 4 двойных связей.
[0041] Указанное выше фузогенное соединение, где соединение представляет собой соединение Т11:
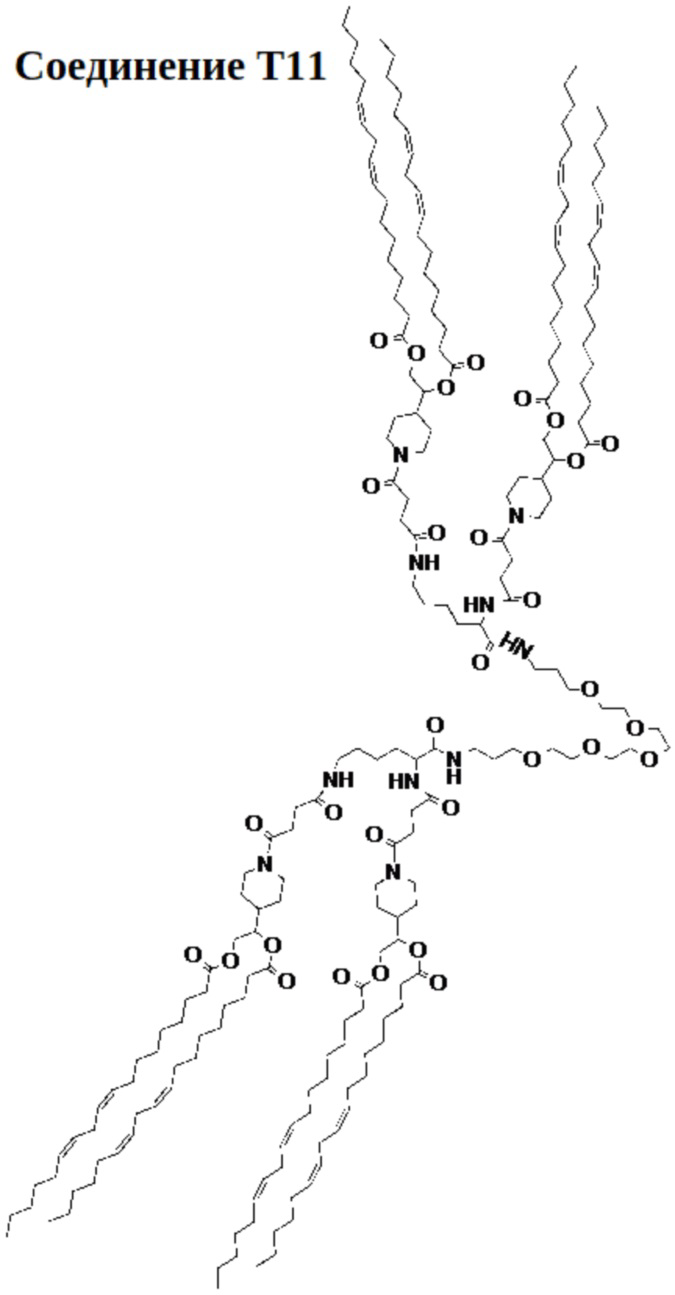
[0042] Фузогенное соединение, имеющее формулу VII:
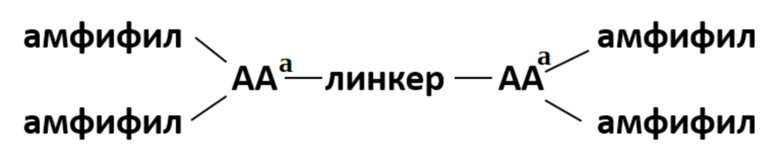 Формула VII,
Формула VII,
где каждый амфифил независимо содержит от одной до двух липофильных цепей, где каждая липофильная цепь независимо содержит от 8 до 22 атомов углерода;
где каждый AAa независимо представляет собой аминокислоту, содержащую боковую цепь, имеющую ацильную группу, где аминокислота присоединена к амфифилу по каждой из своих ацильных групп и присоединена к линкеру на своем N-конце;
где линкер имеет структуру:
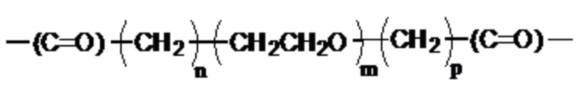
или
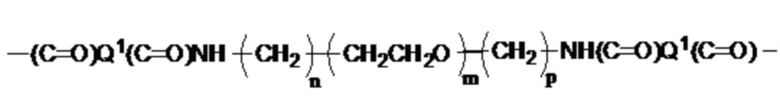
где Q1 представляет собой разветвленный или неразветвленный C(2-8)алкандиил, разветвленный или неразветвленный C(2-8)алкендиил, разветвленный или неразветвленный C(2-8)алкиндиил, или

или
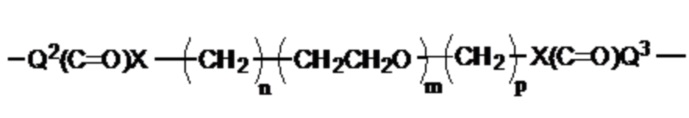 ,
,
где Q2 представляет собой
 ,
,
где Q3 представляет собой
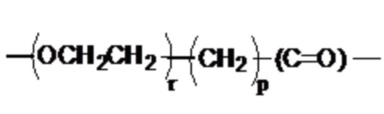 ,
,
где X представляет собой -O-, -S- или -NH-;
n и p независимо для каждого случая составляют от 1 до 3;
m независимо составляет от 1 до 10;
r и s независимо для каждого случая составляют от 1 до 5.
[0043] Указанное выше фузогенное соединение, где AAa выбирают из следующих структур, и любого их стереоизомера:
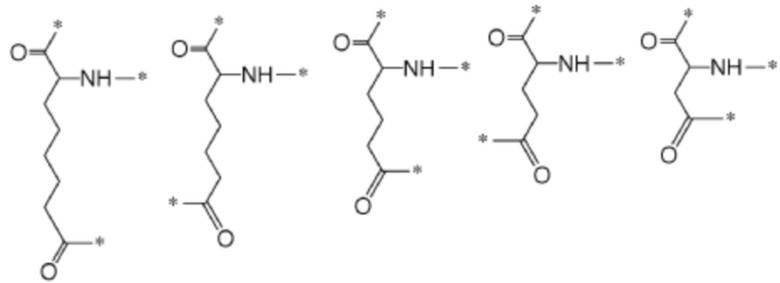 .
.
[0044] Указанное выше фузогенное соединение, где один или два амфифила отсутствуют и замещены алкильной группой или фармацевтически приемлемой органической химической группой, имеющей 1-400 атомов, выбранных из углерода, кислорода, азота, серы, фтора и водорода.
[0045] Указанное выше фузогенное соединение, где фармацевтически приемлемая органическая химическая группа выбрана из алкила, алкенила, алкинила, алкилового эфира, арилового эфира, алкокси- и алкоксиакокси-групп.
[0046] Указанное выше фузогенное соединение, где фармацевтически приемлемая органическая химическая группа выбрана из метокси-группы, этокси-группы, трет-бутилового эфира и бензилокси-группы.
[0047] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле VIII:
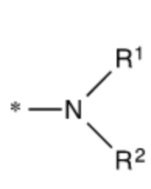 Формула VIII,
Формула VIII,
где R1 и R2 представляют собой
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
где n и m, каждый независимо, составляют от 1 до 2;
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу.
[0048] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле IX:
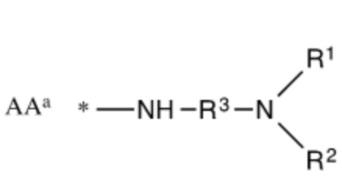 Формула IX
Формула IX
где R1 и R2 представляют собой
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
где
n и m, каждый независимо, составляют от 1 до 2;
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 выбирают из разветвленного или неразветвленного С(1-8)алкандиила, замещенного или незамещенного С(2-8)алкендиила, замещенного или незамещенного С(2-8)алкиндиила, замещенного или незамещенного С(3-8)циклоалкандиила, замещенного или незамещенного арилена, замещенного или незамещенного С(4-8)гетероарилена и замещенного или незамещенного гетероциклоалкандиила; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0049] R3, предпочтительно, представляет собой разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0050] Указанное выше фузогенное соединение, где R4 и R5 независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу, предпочтительно, C(14-18)алкенильную группу, имеющую от 2 до 4 двойных связей.
[0051] Указанное выше фузогенное соединение, где соединение представляет собой соединение T9:
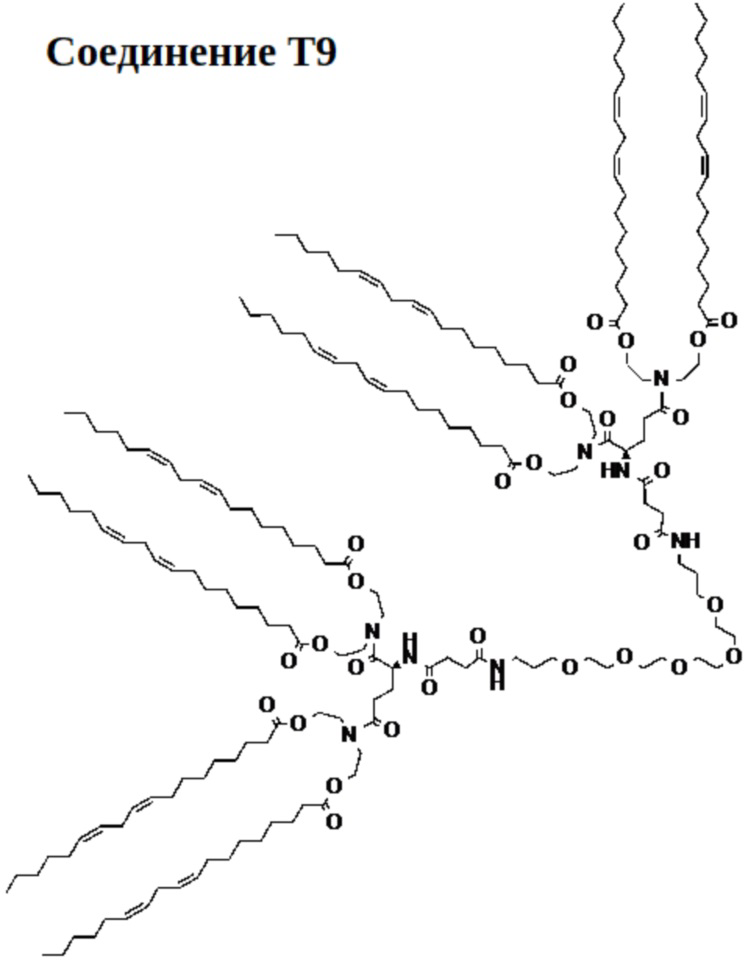 .
.
[0052] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле X:
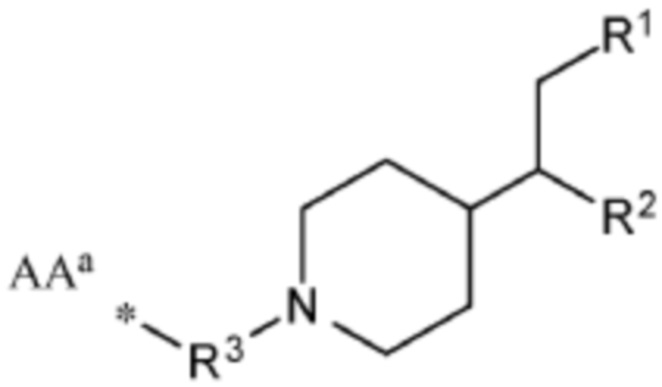 Формула Х,
Формула Х,
где R1 и R2 представляют собой:
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 отсутствует, или его выбирают из разветвленного или неразветвленного *-NH-C(1-8)алкандиил-(C=O)-, замещенного или незамещенного *-NH-C(2-8)алкендиил-(C=O)-, замещенного или незамещенного *-NH-C(2-8)алкиндиил-(C=O)-, замещенного или незамещенного *-NH-C(3-8)циклоалкандиил-(C=O)-, замещенного или незамещенного *-NH-арилен-(C=O)-, замещенного или незамещенного *-NH-C(4-8)гетероарилен-(C=O)- и замещенного или незамещенного -NH-гетероциклоалкандиил-(C=O)-, где * обозначает конец, присоединенный к AAa; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0053] R3, предпочтительно, представляет собой разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0054] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле XI:
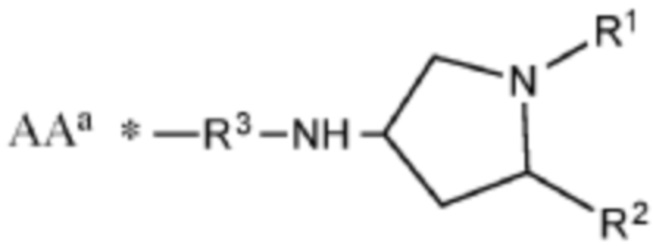 Формула XI,
Формула XI,
где
R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, NH(C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 отсутствует, или его выбирают из разветвленного или неразветвленного *-NH-C(1-8)алкандиил-(C=O)-, замещенного или незамещенного *-NH-C(2-8)алкендиил-(C=O)-, замещенного или незамещенного *-NH-C(2-8)алкиндиил-(C=O)-, замещенного или незамещенного *-NH-C(3-8)циклоалкандиил-(C=O)-, замещенного или незамещенного *-NH-арилен-(C=O)-, замещенного или незамещенного *-NH-C(4-8)гетероарилен-(C=O)- и замещенного или незамещенного -NH-гетероциклоалкандиил-(C=O)-, где * обозначает конец, присоединенный к AAa; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0055] R3, предпочтительно, представляет собой разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0056] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в формуле III
 Формула III,
Формула III,
где R1 и R2 представляют собой:
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5
где n и m, каждый независимо, составляют от 1 до 2; и R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где
R3 выбирают из:
-(C=O)-алкил-NH-, который присоединен к AAa;
-(C=O)-алкенил-NH-, который присоединен к AAa;
-(C=O)-алкинил-NH-, который присоединен к AAa;
где любой алкил в R3 представляет собой разветвленный или неразветвленный C(1-6)алкил, любой алкенил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкенил, и любой алкинил в R3 представляет собой разветвленный или неразветвленный C(2-6)алкинил;



и их позиционные изомеры;

 ,
,
где
каждый R6 независимо выбирают из H, алкила, алкокси-группы и алкоксиалкокси-группы, при условии, что один R6 представляет собой -(C=O)-алкил-NH-, где NH присоединен к AAa;
каждый R8 независимо выбирают из H, алкила, при условии, что один R8 представляет собой -(C=O)-алкил-NH-, где NH присоединен к AAa;
q составляет от нуля до четырех;
Q является О или N.
[0057] Указанное выше фузогенное соединение, где один или несколько амфифилов имеют структуру, показанную в Формуле V:
 Формула V,
Формула V,
где R1 и R2 представляют собой:
R1 = (C=O)OR4, (C=O)NHR4, O(C=O)R4, NH(C=O)R4
R2 = (C=O)OR5, (C=O)NHR5, O(C=O)R5, NH(C=O)R5,
где R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 отсутствует, или его выбирают из разветвленного или неразветвленного *-NH-C(1-8)алкандиил-(C=O)-, замещенного или незамещенного *-NH-C(2-8)алкендиил-(C=O)-, замещенного или незамещенного *-NH-C(2-8)алкиндиил-(C=O)-, замещенного или незамещенного *-NH-C(3-8)циклоалкандиил-(C=O)-, замещенного или незамещенного *-NH-арилен-(C=O)-, замещенного или незамещенного *-NH-C(4-8)гетероарилен-(C=O)- и замещенного или незамещенного -NH-гетероциклоалкандиил-(C=O)-, где * обозначает конец, присоединенный к AAa; где R3 необязательно прерван одной или несколькими из групп -O-, -S-, -SO-, -SO2-, -NH-, -NR6-, -NH(C=O)-, -O(C=O)-, где R6 представляет собой С(1-6)алкил-, С(1-6)алкокси- или С(1-6)алкокси-С(1-6)алкокси-.
[0058] R3 такой, как описано выше, предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(2-8)алкендиил, замещенный или незамещенный С(2-8)алкиндиил, С(3-8)циклоалкандиил, замещенный или незамещенный С(4-8)арилен и, еще более предпочтительно, разветвленный или неразветвленный С(2-8)алкандиил, замещенный или незамещенный С(3-8)циклоалкандиил.
[0059] Варианты осуществления данного изобретения дополнительно предусматривают композиции, содержащие вышеуказанное фузогенное соединение и фармацевтически приемлемый носитель. Композиция может содержать наночастицы или липосомы.
[0060] Фармацевтическая композиция по данному изобретению может включать фузогенное соединение, действующий агент и фармацевтически приемлемый носитель. В композиции фузогенное соединение может составлять от 0,01 до 20 мол.% от липидов в композиции. Композиция может содержать наночастицы или липосомы.
[0061] Фузогенные молекулы и составы по настоящему изобретению могут быть использованы для доставки действующего агента.
[0062] В некоторых вариантах осуществления действующий агент представляет собой одну или несколько нуклеиновых кислот.
[0063] В некоторых вариантах осуществления действующий агент представляет собой одну или несколько ДНК, РНК, мРНК, киРНК или микроРНК. Действующий агент может представлять собой одну или несколько молекул РНК.
[0064] Действующий агент может представлять собой одну или несколько молекул РНКи, одну или несколько молекул мРНК и их модифицированные формы.
[0065] Варианты осуществления данного изобретения включают композиции для применения для распределения действующего агента для лечения состояния или заболевания у субъекта. Композиция может содержать действующий агент, фузогенное соединение, ионизируемый липид, структурный липид, стабилизирующий липид и липид для снижения иммуногенности композиции.
[0066] Настоящее изобретение включает способы предупреждения, облегчения или лечения заболевания или состояния у нуждающегося субъекта, включающие введение субъекту вышеуказанной композиции. Композиции по данному изобретению могут быть использованы при лечении организма человека или животного.
[0067] Варианты осуществления этого изобретения также включают в себя нижеследующие соединения:
соединение по формуле (А)
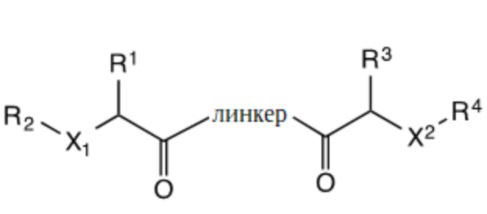 формула А,
формула А,
где линкер представляет собой двухвалентную группу, содержащую участок ПЭГ,
X1 и X2 независимо представляют собой С1-С5алкандиильную группу,
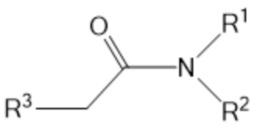
R1, R2, R3 и R4 независимо представляют собой:
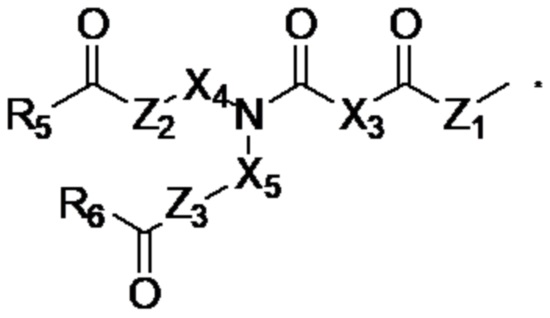
X3 представляет собой одинарную связь, С1-С5алкандиильную группу или С2-С5алкендиильную группу, X4 и X5 независимо представляют собой C2-5алкандиильную группу,
Z1, Z2 и Z3 независимо представляют собой -O-, -S- или -NH-, и
R5 и R6 независимо представляют собой C11-23алкильную или C11-23алкенильную группу.
[0068] Варианты осуществления данного изобретения также включают в себя нижеследующие соединения:
соединение по формуле (В):
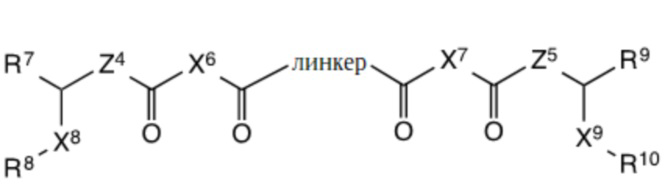 формула В,
формула В,
где линкер представляет собой двухвалентную группу, содержащую участок ПЭГ,
X6 и X7 независимо представляют собой С1-С5алкандиильную группу,
X8 и X9 независимо представляют собой С1-С5алкандиильную группу,
Z4 и Z5 независимо представляют собой -O-, -S- или -NH-,
R7, R8, R9 и R10 независимо представляют собой:
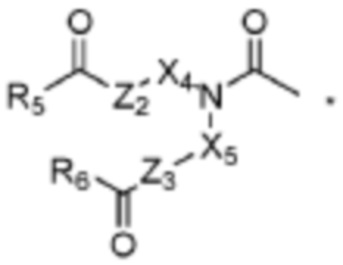 ,
,
X4 и X5 независимо представляют собой C2-5алкандиильную группу,
Z2 и Z3 независимо представляют собой -O-, -S- или -NH-, и
R5 и R6 независимо представляют собой C11-23алкильную или C11-23алкенильную группу.
[0069] Соединение, указанное выше, где линкер представляет собой:
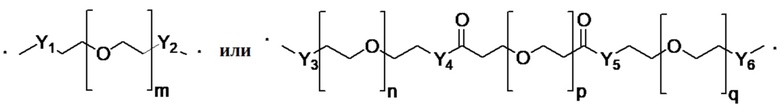 ,
,
где m представляет собой целое число от 1 до 12,
Y1 представляет собой -O-, -NH- или -NHCH2-,
Y2 представляет собой -O-, -NH- или -CH2NH-,
n и q независимо представляют собой целое число от 1 до 5,
р представляет собой целое число от 1 до 5,
Y3 и Y5 независимо представляют собой -O-, -NH- или -NHCH2-, и
Y4 и Y6 независимо представляют собой -O-, -NH- или -CH2NH-.
[0070] Соединение, указанное выше, где X1 и X2 независимо представляют собой C1-C5 прямую алкандиильную группу, предпочтительно, C2-C4 прямую алкандиильную группу, более предпочтительно, C4 прямую алкандиильную группу.
[0071] Соединение, указанное выше, где R1, R2, R3 и R4 являются одинаковыми группами.
[0072] Соединение, указанное выше, где X3 представляет собой одинарную связь или C1-C5 прямую алкандиильную группу, X3 предпочтительно представляет собой C2-C4 прямую алкандиильную группу, более предпочтительно, этилен, то есть этандиильную группу.
[0073] Соединение, указанное выше, где X4 и X5 независимо представляют собой C2-5 прямую алкандиильную группу, X4 и X5, предпочтительно, представляют собой C2-4 прямую алкандиильную группу, более предпочтительно, этилен, то есть этандиильную группу.
[0074] Соединение, указанное выше, где Z1 представляет собой -NH-.
[0075] Соединение, указанное выше, где Z2 и Z3 представляют собой -O-.
[0076] Соединение, указанное выше, где R5 и R6 независимо представляют собой C11-23 прямую алкенильную группу.
[0077] Соединение, указанное выше, где R5 и R6 независимо представляют собой C11-23 прямую алкенильную группу с 1-6 двойными связями, где число двойных связей, предпочтительно, составляет 1-3, более предпочтительно, 2-3, еще более предпочтительно, 2.
[0078] Соединение, указанное выше, где R5 и R6 независимо представляют собой C11-23 прямую алкенильную группу с 2 двойными связями.
[0079] Соединение, указанное выше, где R5 и R6 независимо представляют собой C13-17 прямую алкенильную группу, R5 и R6, предпочтительно, представляют собой C15-17 прямую алкенильную группу, более предпочтительно, С17 прямую алкенильную группу.
[0080] Соединение, указанное выше, где R5 и R6 независимо представляют собой C17 прямую алкенильную группу.
[0081] Соединение, указанное выше, где R5 и R6 представляет собой гептадека-8,1-диенильную группу.
[0082] Композиция, указанная выше, которая содержит катионный липид, ионизируемый липид и липид указанного выше соединения в липидной наночастице, содержащей бислой липидных молекул.
[0083] Композиция, указанная выше, которая дополнительно содержит нуклеиновую кислоту.
[0084] Композиция, указанная выше, где нуклеиновая кислота представляет собой киРНК, мРНК или микроРНК.
[0085] Композиция, указанная выше, где композиция представляет собой фармацевтическую композицию.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0086] На фиг.1 показана схема получения соединения R1.
[0087] На фиг.2 показана схема получения соединения R2.
[0088] На фиг.3А показана схема получения соединения R3.
[0089] На фиг.3В показана структура соединения R3.
[0090] На фиг. 4А показана схема получения соединения R4.
[0091] На фиг.4В показана структура соединения R4.
[0092] На фиг.5 показана схема получения соединения R5.
[0093] На фиг.6 показана схема получения соединения R6.
[0094] На фиг.7 показана альтернативная схема получения соединения R6.
[0095] На фиг.8 показана схема получения соединения S2.
[0096] На фиг.9 показана схема получения соединения S3.
[0097] На фиг.10А показана схема получения соединения S4.
[0098] На фиг.10B показана структура соединения S4.
[0099] На фиг.11 показана схема получения соединения S5.
[00100] На фиг.12А показана схема получения соединения S6.
[00101] На фиг.12В показана структура соединения S6.
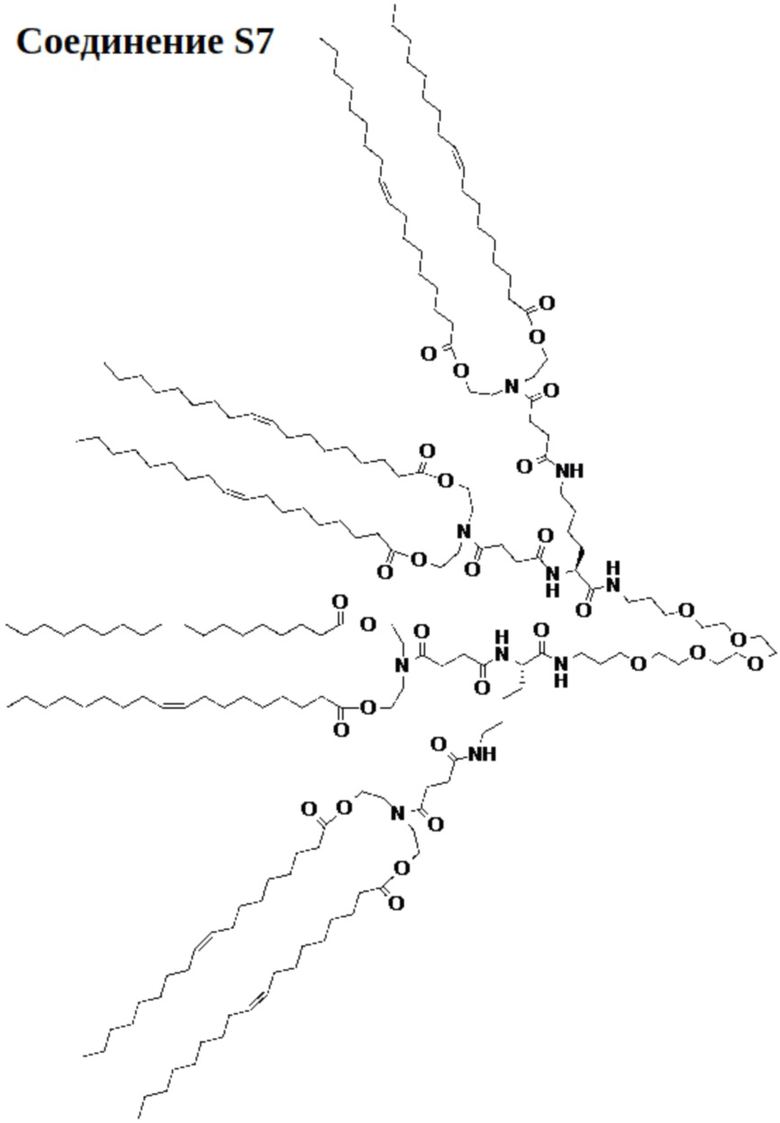
[00102] На фиг.13А показана схема получения соединения S7.
[00103] На фиг.13B показана структура соединения S7.
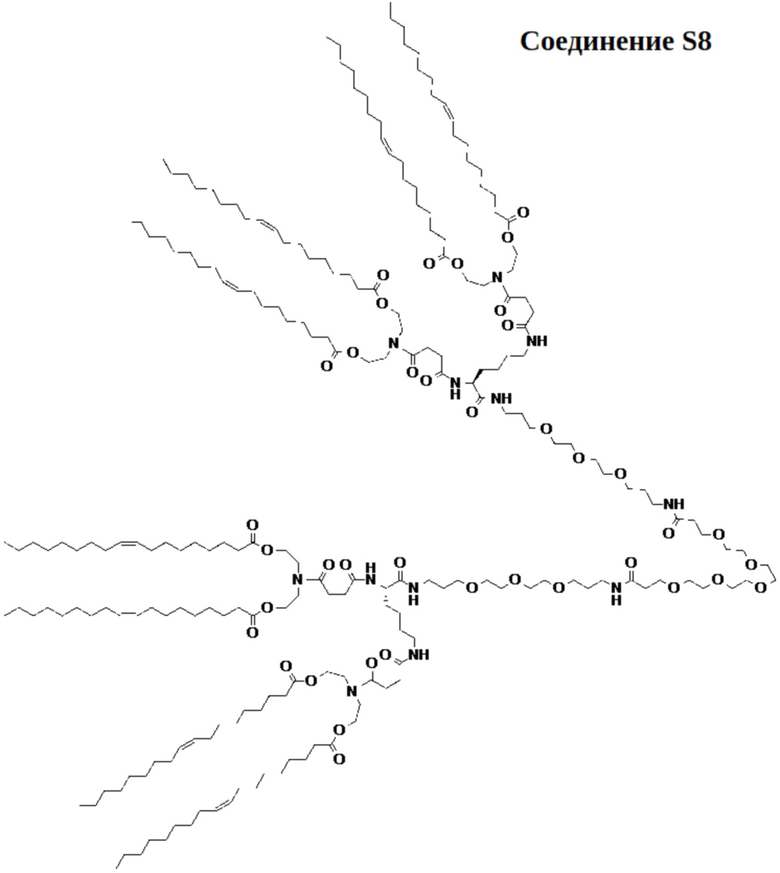
[00104] На фиг.14А показана схема получения соединения S8.
[00105] На фиг.14B показана структура соединения S8.
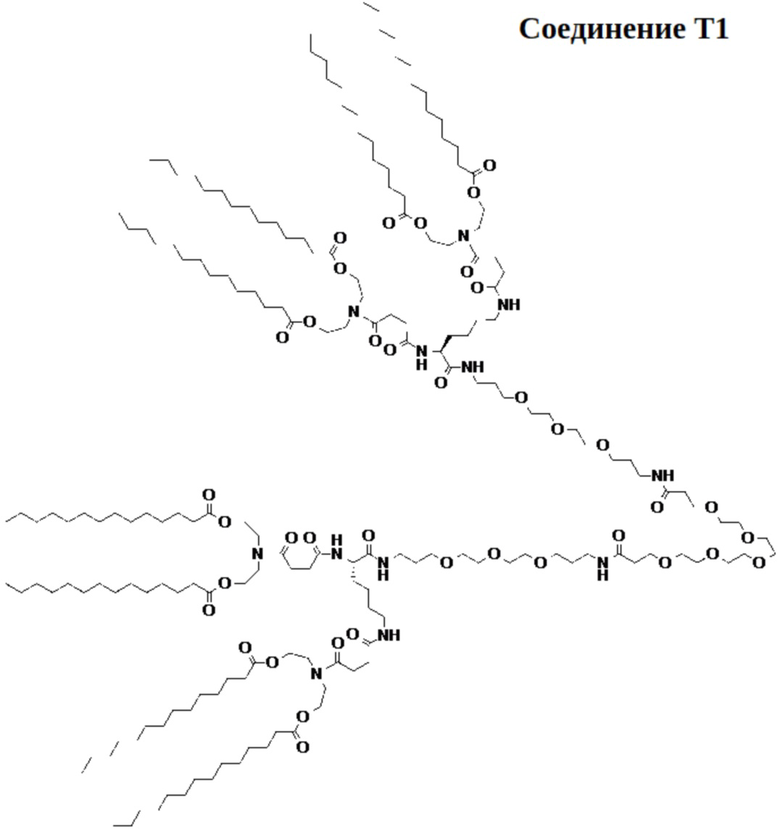
[00106] На фиг.15А показана схема получения соединения T1.
[00107] На фиг.15B показана структура соединения T1.
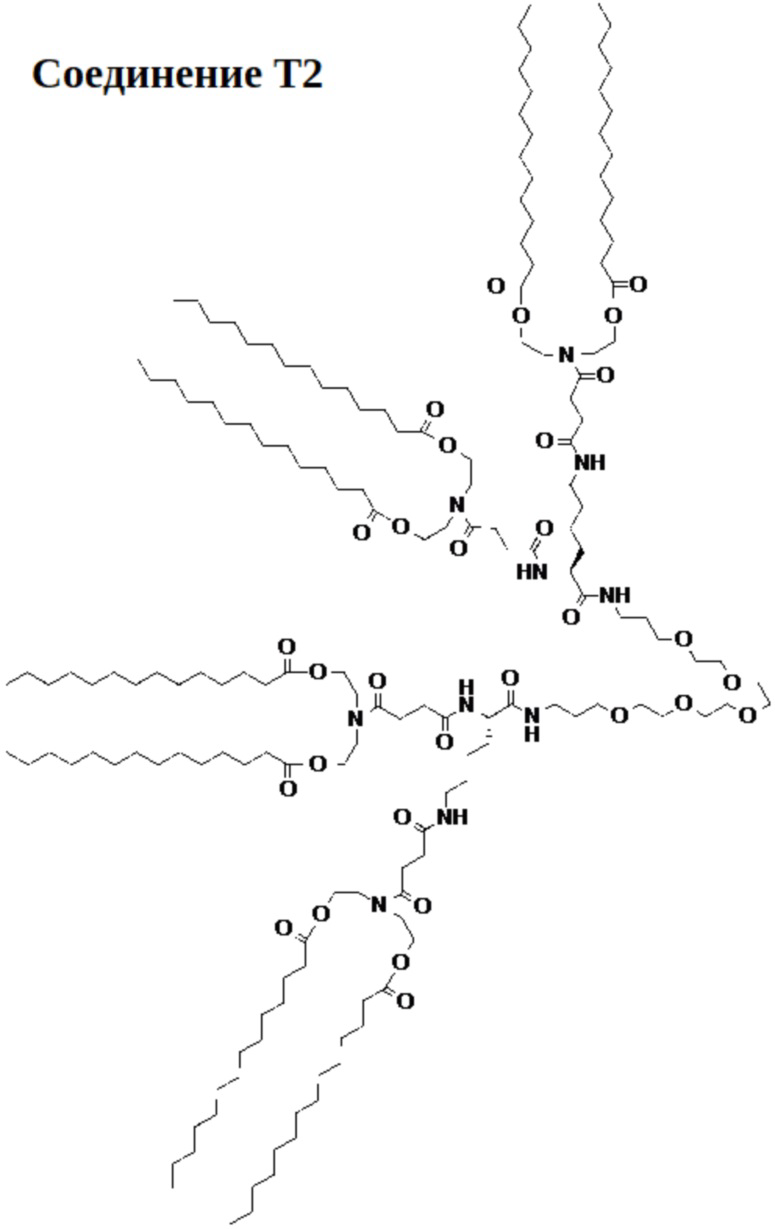
[00108] На фиг.16А показана схема получения соединения Т2.
[00109] На фиг.16B показана структура соединения T2.
[00110] На фиг.17А показана схема получения соединения Т4.
[00111] На фиг.17B показана структура соединения T4.
[00112] На фиг.18A показана схема получения соединения T5.
[00113] На фиг.18B показана структура соединения T5.
[00114] На фиг.19А показана схема получения соединения Т6.
[00115] На фиг.19B показана структура соединения T6.
[00116] На фиг.20А показана схема получения соединения Т7.
[00117] На фиг.20B показана структура соединения T7.
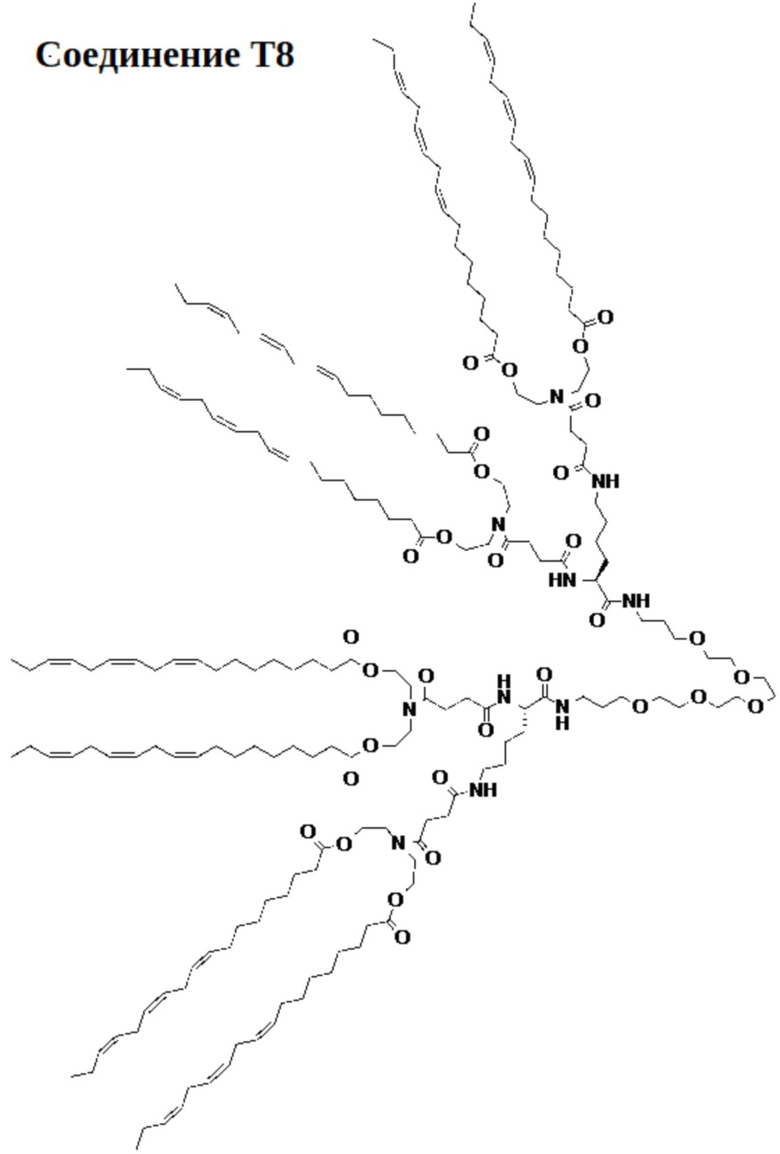
[00118] На фиг.21А показана схема получения соединения Т8.
[00119] На фиг.21В показана структура соединения Т8.
[00120] На фиг.22А показана схема получения соединения Т9.
[00121] На фиг.22B показана структура соединения T9.
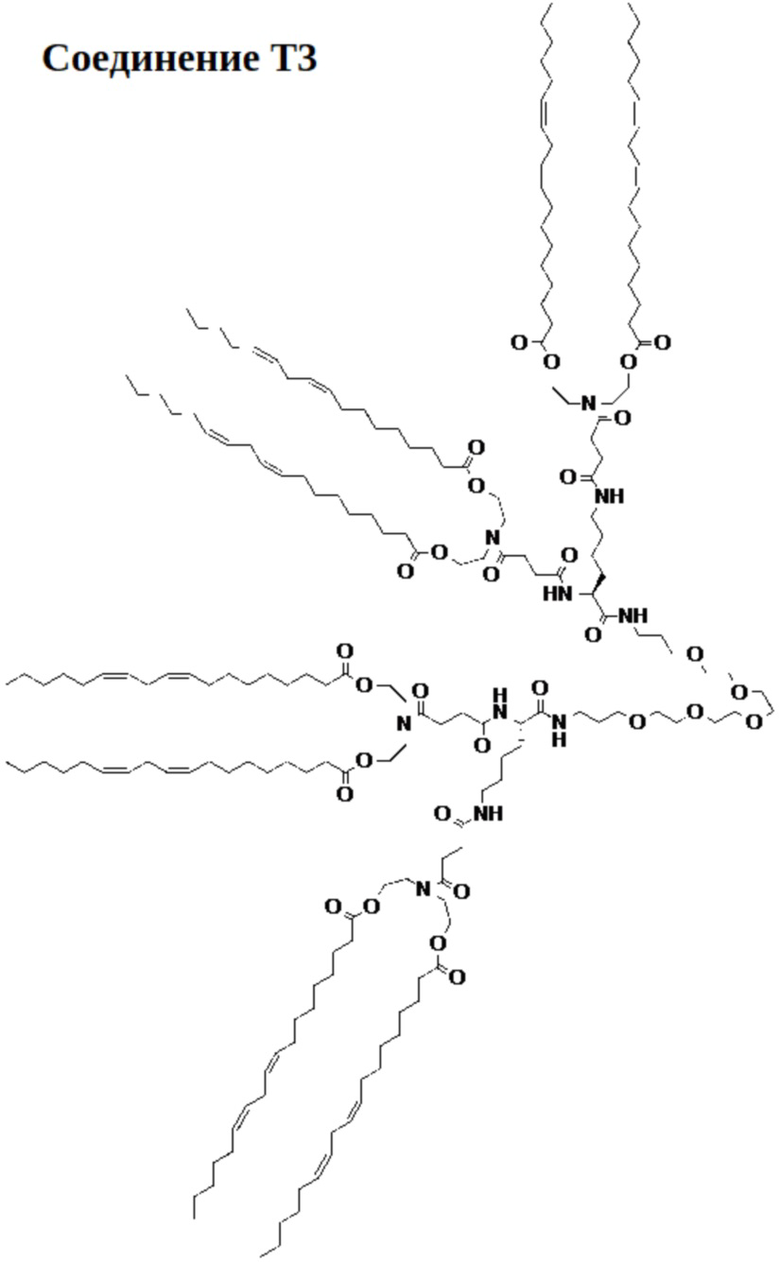
[00122] На фиг.23А показана схема получения соединения Т3.
[00123] На фиг.23B показана структура соединения T3.
[00124] На фиг.24 показаны результаты доставки биологически активных молекул in vitro с использованием фузогенных молекул по настоящему изобретению. Как показано на фиг.24, состав № 5 для липосомальной доставки, который содержал 2% (от общего количества липидов) фузогенного соединения R4 по настоящему изобретению, обеспечивал неожиданное повышение активности направленной против HSP47 иллюстративной киРНК в отношении нокдауна экспрессии гена в звездчатых клетках по сравнению с контрольным составом № 1, который не содержал фузогенного соединения по настоящему изобретению.
[00125] На фиг.25 показаны результаты доставки биологически активных молекул in vitro с использованием фузогенных молекул по настоящему изобретению. Была измерена степень нокдауна экспрессии гена HSP47 для нескольких составов с липосомальной доставкой киРНК. Составы обеспечивали высокую активность в отношении подавления экспрессии генов в звездчатых клетках. Составы содержали 2% (от общего количества липидов) фузогенного соединения по настоящему изобретению и обеспечивали высокую активность киРНК, направленной против HSP47.
[00126] На фиг.26 показаны результаты доставки биологически активных молекул in vivo с использованием фузогенных молекул по настоящему изобретению. Составы с липосомальной доставкой демонстрировали активность в отношении подавления экспрессии генов in vivo (в мышах) с использованием киРНК, направленной против HSP47. Активные составы №2-№8 содержали 2% (от общего количества липидов) указанного фузогенного соединения по настоящему изобретению.
[00127] На фиг.27 показана левая половина структуры соединения T10.
[00128] На фиг.28 показана правая половина структуры соединения T10.
[00129] На фиг.29 показана схема получения соединения T10.
[00130] На фиг.30 показана схема получения соединения T10.
[00131] На фиг.31 показана левая половина структуры соединения T11.
[00132] На фиг.32 показана правая половина структуры соединения T11.
[00133] На фиг.33 показана схема получения соединения T11.
[00134] На фиг.34 показана схема получения соединения T11.
[00135] На фиг.35 показана левая половина структуры соединения T12.
[00136] На фиг.36 показана правая половина структуры соединения T12.
[00137] На фиг.37 показана схема получения соединения T12.
[00138] На фиг.38 показана схема получения соединения T12.
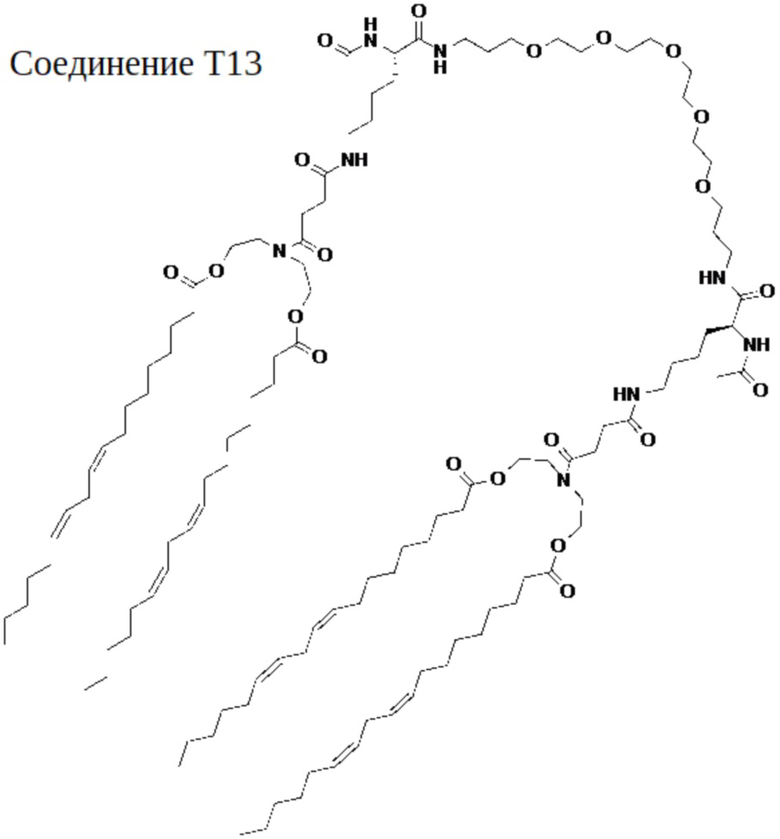
[00139] На фиг.39 показана левая половина структуры соединения T13.
[00140] На фиг.40 показана правая половина структуры соединения T13.
[00141] На фиг.41 показана схема получения соединения T13.
[00142] На фиг.42 показана схема получения соединения T13.
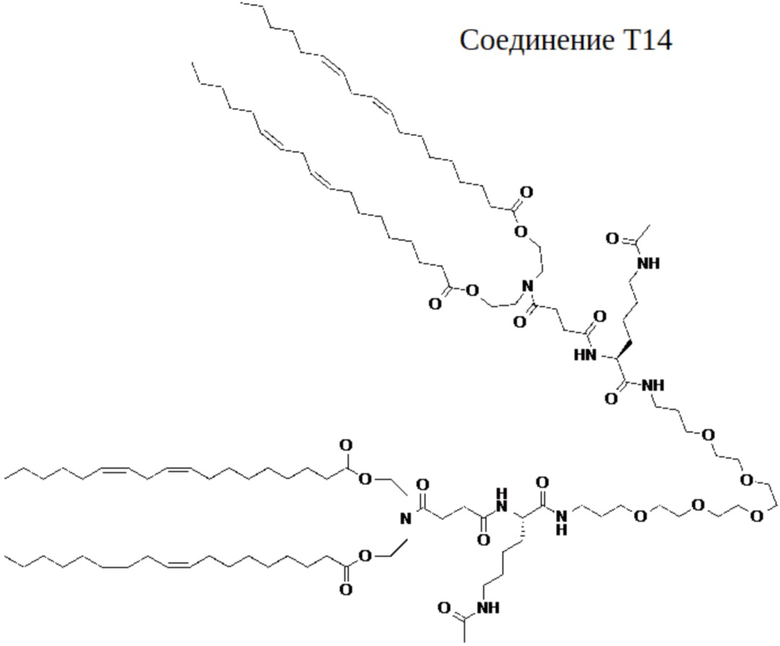
[00143] На фиг.43 показаны правая и левая половины структуры соединения T14.
[00144] На фиг.44 показана схема получения соединения Т14.
[00145] На фиг.45 показана схема получения соединения T14.
[00146] На фиг.46 показана активность in vitro в отношении нокдауна экспрессии гена при использовании иллюстративной киРНК в звездчатых клетках крысы для липосомальных составов, содержащих фузогенное соединение по настоящему изобретению. (1) Результаты для липосомального состава, состоящей из липидов HEDC и S104, который не содержал фузогенного соединения по настоящему изобретению. (2) Результаты для липосомального состава, аналогичного (1), за исключением того, что он содержал 2% (от общего количества липидов) фузогенного соединения R4. (3) Результаты для липосомального состава, аналогичного (1), за исключением того, что он содержал 10% (от общего количества липидов) фузогенного соединения R4. Присутствие фузогенного соединения R4 в препарате значительно увеличивало «доставляемую» активность иллюстративной киРНК, и повышенная активность была непосредственно связана с присутствием фузогенного соединения R4.
[00147] На фиг.47 показана активность in vitro в отношении нокдауна экспрессии гена с использованием иллюстративной киРНК в звездчатых клетках крысы с использованием липосомального состава, содержащего фузогенное соединение по настоящему изобретению. (1) Результаты для липосомального состава, состоящего из липидов HEDC и S104, который не содержал фузогенного соединения по настоящему изобретению. (2) Результаты для липосомального состава, аналогичного (1), за исключением того, что он содержал 2% (от общего количества липидов) фузогенного соединения R4. (3) Результаты для липосомального состава, аналогичного (1), за исключением того, что он содержал 2% (от общего количества липидов) фузогенного соединения Т3. Присутствие фузогенных соединений R4 и T3, соответственно, в композициях значительно увеличивало «доставляемую» активность иллюстративной киРНК, и эта повышенная активность была непосредственно связана с присутствием фузогенных соединений R4 и T3.
[00148] На фиг.48 показаны результаты доставки и трансфекции мРНК GFP в концентрации 5 нМ (вверху) и 2 нМ (внизу) в клетки A549 in vitro в наночастицах LNP по настоящему изобретению, имеющих состав HEDC:S104:CH:DOPE:DMPE-PEG2000:соединение T3. Флуоресцентные изображения (слева) экспрессии GFP были получены с помощью флуоресцентного микроскопа через 48 часов после трансфекции. Наложение (справа) флуоресцентных изображений на изображения, полученные в световом поле (BF), демонстрирует, что почти 100% клеток были трансфицированы и экспрессируют GFP.
[00149] На фиг.49 показаны результаты доставки мРНК GFP in vivo с использованием фузогенных липидоподобных молекул по настоящему изобретению. Мышей Balb/c трансфицировали мРНК GFP с помощью наночастиц LNP по настоящему изобретению, имеющих состав HEDC:S104:CH:DOPE:DMPE-PEG2000:соединение T3. Как показано на фиг.49, доставку мРНК в различные ткани и клетки определяли с помощью MAXDISCOVER GFP ELISA. Удивительно, но мРНК GFP селективно трансфицировалась и/или транслировалась в легких, с более низкой трансфекцией и/или трансляцией в мышцах, печени, сердце и почках.
[00150] На фиг.50 показаны результаты доставки мРНК люциферазы in vivo с использованием фузогенных липидоподобных молекул по настоящему изобретению. Мышей Balb/c трансфицировали мРНК люциферазы с помощью наночастиц LNP по настоящему изобретению, имеющих состав HEDC:S104:CH:DOPE:DMPE-PEG2000:соединение T3. Как показано на фиг.50, относительную доставку, трансфекцию и/или трансляцию мРНК в различных тканях и клетках определяли с помощью набора для анализа Promega E4510. Удивительно, но мРНК Fluc (люциферазы светлячка) избирательно доставлялась, трансфицировалась и/или транслировалась в легких и селезенке, с более низкой доставкой, трансфекцией и/или трансляцией в печени, сердце, почках и мышцах.
[00151] На фиг.51 показаны результаты доставки мРНК люциферазы in vivo с использованием фузогенных липидоподобных молекул по настоящему изобретению. Мышей Balb/c трансфицировали мРНК люциферазы с помощью наночастиц LNP по настоящему изобретению, имеющих состав:
(-01) HE2DC:S104:CH:DOPE:DMPE-PEG2000:соединение T3 или
(-02) HEDC:S104:CH:DOPE:DMPE-PEG200:соединение T3,
вводимых в количестве 2 мг/кг. Как показано на фиг.51, относительную доставку, трансфекцию и/или трансляцию мРНК в различных тканях и клетках определяли с помощью набора E4510 Promega. мРНК Fluc селективно доставлялась, трансфицировалась и/или транслировалась в легкие и селезенку, с более низкой доставкой, трансфекцией и/или трансляцией в поджелудочную железу, почки, печень, яички и тонкую кишку.
[00152] На фиг.52 показаны результаты измерения биолюминесценции для доставки мРНК люциферазы мышам in vivo с использованием фузогенных липидоподобных молекул по настоящему изобретению. Как показано на фиг.52, относительную доставку, трансфекцию и/или трансляцию мРНК в различных тканях определяли с помощью измерения люминесценции через 7 часов после инъекции.
[00153] На фиг.53 показаны результаты доставки мРНК люциферазы мышам in vivo с использованием фузогенных липидоподобных молекул по настоящему изобретению. Как показано на фиг.53, относительная доставка мРНК была намного выше для составов, содержащих фузогенные молекулы по настоящему изобретению (2035-03-03), чем для таких же составов без фузогенных молекул (2035-13-01).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[00154] Настоящее изобретение относится к ряду фузогенных молекул. Фузогенные соединения по настоящему изобретению можно использовать для доставки терапевтических агентов в клетки, ткани или органы, организмы и субъектов.
[00155] В некоторых аспектах настоящее изобретение относится к платформе соединений для образования фузогенных молекул. Фузогенные молекулы могут быть образованы присоединением одной или множества нейтральных молекул, таких как углеводородные молекулы, алифатическая молекула, молекула насыщенной жирной кислоты, молекула ненасыщенной жирной кислоты, молекула мононенасыщенной жирной кислоты или молекула полиненасыщенной жирной кислоты, к структуре платформы.
[00156] Примеры фузогенного соединения по настоящему изобретению включают, но не ограничиваются этим, соединение R4, показанное на фиг.4B; соединение S6, показанное на фиг.12B; соединение S7, показанное на фиг.13B; соединение S8, показанное на фиг.14B; соединение T1, показанное на фиг.15B; соединение T2, показанное на фиг.16B; соединение T4, показанное на фиг.17B; соединение T5, показанное на фиг.18B; соединение T6, показанное на фиг.19B; соединение T7, показанное на фиг.20B; соединение T8, показанное на фиг.21B; соединение T9, показанное на фиг.22B; соединение T3, показанное на фиг.23B; соединение Т10, показанное на фиг.27 и 28; соединение T11, показанное на фиг.31 и 32; соединение T12, показанное на фиг.35 и 36; соединение T13, показанное на фиг.39 и 40; соединение T14, показанное на фиг.43.
[00157] Соединения, показанные на фиг.1, 2, 3A, 3B и 6-11, приведены в целях иллюстрации способов синтеза соединений.
[00158] В некоторых аспектах настоящее изобретение относится к ряду слитых молекул, которые можно использовать в составах для формирования и применения липидных наночастиц для доставки действующих агентов в клетки и субъектов.
[00159] Фузогенное соединение по настоящему изобретению может иметь одну или две амфифильных группы (амфифила), присоединенных к аминокислотной группе, причем эта аминокислотная группа присоединена линкером к отдельной аминокислотной группе, несущей один или два дополнительных амфифила.
[00160] Липофильные цепи амфифила могут независимо содержать от 8 до 22 атомов углерода.
[00161] Амфифильная группа может представлять собой липидоподобную группу, имеющую одну или две липофильные цепи, присоединенные к органической химической группе. Органическая химическая группа может иметь до 400 атомов, или 20-400 атомов, или 10-400 атомов, или 4-400 атомов, или 3-400 атомов, или 2-400 атомов, или 1-400 атомов, выбранных из углерода, кислорода, азота, серы, фтора и водорода, и может иметь любую структуру, подходящую для присоединения одной или двух липофильных цепей и присоединения к аминокислотной группе. Органическая химическая группа может быть нейтральной или цвиттерионной, или может обеспечивать гидрофильную природу. В некоторых вариантах осуществления органическая химическая группа может ионизироваться. Примеры органической химической группы включают алкил, алкенил, алкинил и ацетил, а также защитные группы, такие как Boc, Fmoc, TFA и CBZ (бензилоксикарбонил).
[00162] Не желая быть связанными какой-либо конкретной теорией, авторы предполагают, что амфифил может иметь липидоподобную структуру, так что амфифил может входить в липидный бислой в ориентации, аналогичной липидным молекулам бислоя, оставаясь при этом связанным с более крупным слитым соединением. Фузогенное соединение по настоящему изобретению может нарушать динамическую структуру бислоя для усиления фузогенности (способности к слиянию) с клетками.
[00163] Аминокислотная группа фузогенного соединения (обозначаемая АА или ААа) может быть модифицирована заместителями. Аминокислотная группа фузогенного соединения может представлять собой любую D- или L-аминокислотную группу, имеющую формулу -NRN-CR1R2-(C=O)-, где R1 представляет собой замещенную или незамещенную боковую цепь некоторых природных аминокислот. R2 и RN, каждый, могут представлять собой независимо водород или органическую группу, состоящую из атомов углерода, кислорода, азота, серы и водорода и имеющую от 1 до 20 атомов углерода, или могут представлять собой C(1-6)алкил, циклоалкил, циклоалкилалкил, C(2-6)алкенил, C(2-6)алкинил, C(1-6)алканоил, C(1-6)алканоилокси, C(1-6)алкокси, C(1-6)алкокси-C(1-6)алкил, С(1-6)алкокси-С(1-6)алкокси.
[00164] Используемый в настоящем документе термин «который присоединен к AA» используется для обозначения точки присоединения группы к AA. Например, термин «-алкил-(C=O)-, который присоединен к AA» относится к присоединению к AA через (C=O)-группу, так что образуется -алкил-(C=O)-AA. Если не указано иное, то предполагается, что последняя группа, которая появляется рядом с фразой «который присоединен к АА», является группой, присоединенной к АА.
[00165] Данное изобретение может относиться к композициям для применения в распределении действующего агента в клетках, тканях или органах, организмах и субъектах, где композиция включает одну или несколько фузогенных молекул по настоящему изобретению.
[00166] Фузогенные соединения по настоящему изобретению могут обеспечивать композиции и составы, применяющиеся при доставке терапевтических агентов в клетки, ткани и субъектов предпочтительно без значительной агрегации компонентов композиции.
[00167] Фузогенное соединение по настоящему изобретению может обеспечить липосомальную композицию для применения при доставке терапевтических агентов в клетки, ткани и субъекты предпочтительно без значительной агрегации липосом в композиции.
[00168] Композиции по настоящему изобретению могут включать одну или несколько фузогенных молекул вместе со структурным липидом и один или несколько липидов для снижения иммуногенности композиции.
[00169] В некоторых аспектах настоящее изобретение относится к новым фузогенным липидам, которые облегчают доставку биологически активных молекул в клетки. Фузогенные липиды могут быть включены в составы, такие как наночастицы или липосомы, для доставки терапевтических молекул, включая нуклеиновые кислоты или олигонуклеотиды, в клетки, включая опухоли. В некоторых вариантах осуществления наночастицы или липосомы, содержащие фузогенные липиды, могут сливаться с плазматической мембраной клетки или внутриклеточной мембраной клетки и облегчать высвобождение терапевтических молекул, а также повышать эффективность трансфекции.
[00170] В дополнительных вариантах осуществления ряд новых слитых липидов может быть синтезирован и включен в наночастицы или липосомы. Наночастицы или липосомы могут включать или инкапсулировать в себя терапевтические молекулы, включая молекулы на основе нуклеиновых кислот, такие как киРНК, микроРНК или мРНК, а также низкомолекулярные лекарственные средства и любые действующие терапевтические агенты, которые могут быть доставлены с использованием наночастиц или липосом.
[00171] Размер частиц для наночастиц или липосом может находиться в диапазоне 50-200 нм с полидисперсностью менее 0,2. Эффективность трансфекции наночастиц или липосом в различных клеточных линиях может быть улучшена по сравнению с наночастицами или липосомами, в которых отсутствует один или несколько новых фузогенных липидов.
[00172] В дополнительных вариантах осуществления, среди прочего может быть усилено поглощение клетками наночастиц или липосом по настоящему изобретению по эндоцитарному пути или с помощью механизма микропиноцитоза.
[00173] Наночастицы или липосомы по настоящему изобретению также могут снижать лизосомальную деградацию терапевтических молекул при доставке.
[00174] В некоторых вариантах осуществления данное изобретение включает композиции, содержащие одну или несколько фузогенных молекул, наряду с другими липидными молекулами для формирования наночастиц. В некоторых вариантах осуществления фузогенные молекулы могут составлять от 0,1 до 40 мол.% от липидов композиции. В других вариантах осуществления фузогенное соединение может составлять от 1 до 20 мол.% от липидов композиции. В дополнительных вариантах осуществления фузогенное соединение может составлять от 1 до 10 мол.% или от 2 до 10 мол.% от липидов композиции. В других вариантах осуществления фузогенные молекулы могут содержать 2 мол.% от липидов композиции.
[00175] В некоторых вариантах осуществления фузогенное соединение может содержать четвертый или пятый компонент липидов композиции, или фузогенные молекулы могут заменять один из компонентов липидов композиции.
[00176] Фузогенные молекулы по настоящему изобретению могут состоять из платформенной структуры и иметь прикрепленную к платформенной структуре от одной до четырех амфифильных групп с подходящими химическими связями.
[00177] Композиция по настоящему изобретению может включать фузогенную молекулу по настоящему изобретению. Фузогенная молекула может составлять 1-10 мол.% от композиции или более. Композиция может образовывать наночастицу или липосому.
[00178] В некоторых вариантах осуществления композиция по настоящему изобретению может включать катионный липид, ионизируемый липид и молекулу фузогенного липида, которые могут объединяться с образованием липидной наночастицы. В некоторых вариантах осуществления липидная наночастица может иметь бислой из липидных молекул.
[00179] В некоторых вариантах осуществления один или два амфифила могут отсутствовать, а в случае отсутствия могут быть заменены защитной группой Rp.
[00180] В дополнительных вариантах осуществления один или два амфифила могут отсутствовать, и в случае отсутствия они могут быть заменены алкильной, алкенильной или алкинильной группой или органической химической группой, имеющей до 400 атомов, или 20-400 атомов, или 10-400 атомов, или 4-400 атомов, или 3-400 атомов, или 2-400 атомов, или 1-400 атомов, выбранных из углерода, кислорода, азота, серы, фтора и водорода.
[00181] Способы получения различных органических групп и защитных групп известны в данной области техники, и их использование и модификация обычно входят в компетенцию специалиста в данной области. См., например, Stanley R. Sandler and Wolf Karo, Organic Functional Group Preparations (1989); Greg T. Hermanson, Bioconjugate Techniques (1996); Leroy G. Wade, Compendium Of Organic Synthetic Methods (1980); некоторые примеры защитных групп приведены в T. W. Greene and P. G. M. Wuts, Protective Groups In Organic Synthesis (3rd ed. 1991). См., например, Helmut Vorbrüggen, Handbook of Nucleoside Synthesis (2001).
[00182] Примеры защитной группы Rp включают Fmoc (флуоренилметилоксикарбонил).
[00183] Примеры защитной группы Rp включают Boc (трет-бутилоксикарбонил).
[00184] Примеры защитной группы Rp включают OTrt(O-трифенилметил).
[00185] Примеры аминозащитной группы Rp включают Ac (ацетамид) (C=O)CH3).
[00186] Примеры аминозащитной группы включают Fmoc, Boc, Trt, Dde и Alloc.
[00187] Примеры алкоксизащитных групп включают OTrt, OClt, OMmt, OMtt, ODpm и OtBu.
[00188] Примеры защитной группы включают трет-бутиловый эфир.
[00189] Примеры защитной группы для карбоновой кислоты включают бензиловый эфир.
[00190] Катионные липиды и ионизируемые липиды
[00191] Примеры катионных липидов и ионизируемых липидов данного изобретения приведены в US20130022665A и US20130330401A.
[00192] Структура HEDC приведена в US2013/0022665A в абзаце [0146].
[00193] Структура S104 приведена в US 2013/0115274A1 в абзаце [0046].
[00194] Композиции с тремя или более компонентами
[00195] В контексте настоящего изобретения компонент состава, такой как «липид», может представлять собой одно соединение или может представлять собой комбинацию одного или нескольких подходящих липидных соединений. Например, термин «стабилизирующий липид» может относиться к одному стабилизирующему липиду или к комбинации одного или нескольких подходящих стабилизирующих липидов. Специалист в данной области может легко понять, что определенные комбинации соединений, описанных в настоящем документе, могут использоваться без чрезмерных экспериментов, и что описание компонента состава охватывает различные комбинации соединений.
[00196] Ионизируемые соединения композиции по настоящему изобретению могут составлять от 20 до 80 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления ионизируемые молекулы композиции могут составлять от 55 до 65 мол.% от липидных компонентов композиции. В других вариантах осуществления ионизируемые молекулы композиции могут составлять около 60 мол.% от липидных компонентов композиции.
[00197] Структурный липид композиции по настоящему изобретению может составлять от 20 до 50 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления структурный липид композиции может составлять от 35 до 45 мол.% от липидных компонентов композиции.
[00198] Один или несколько липидов для снижения иммуногенности композиции могут составлять от 1 до 8 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления один или несколько липидов для снижения иммуногенности композиции могут составлять от 1 до 5 мол.% от липидных компонентов композиции.
[00199] В дополнительных аспектах композиция по настоящему изобретению может дополнительно включать катионный липид, который может составлять от 5 до 25 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления композиция по настоящему изобретению может дополнительно включать катионный липид, который может составлять от 5 до 15 мол.% от липидных компонентов композиции. В этих аспектах молярное соотношение концентраций катионного липида и ионизируемых молекул композиции по настоящему изобретению может составлять от 5:80 до 25:50.
[00200] В композициях по настоящему изобретению набор липидных компонентов может включать один или несколько молекулярных компонентов ионизируемого соединения, структурный липид и один или несколько липидов для снижения иммуногенности композиции.
[00201] В дополнение к вышеуказанным компонентам композиция по настоящему изобретению может дополнительно включать фузогенную молекулу по настоящему изобретению. Фузогенная молекула может составлять 1-10 мол.% от композиции.
[00202] Композиции с четырьмя или более компонентами
[00203] Ионизируемые молекулы композиции по настоящему изобретению могут составлять от 15 до 40 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления ионизируемые молекулы композиции могут составлять от 20 до 35 мол.% от липидных компонентов композиции. В других вариантах осуществления ионизируемые молекулы композиции могут составлять от 25 до 30 мол.% от липидных компонентов композиции.
[00204] Структурный липид композиции по настоящему изобретению может составлять от 25 до 40 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления структурный липид композиции может составлять от 30 до 35 мол.% от липидных компонентов композиции.
[00205] Суммарное количество стабилизирующих липидов композиции по настоящему изобретению может составлять от 25 до 40% мол.% от липидных компонентов композиции. В некоторых вариантах осуществления суммарное количество стабилизирующих липидов композиции может составлять от 30 до 40 мол.% от липидных компонентов композиции.
[00206] В некоторых вариантах осуществления композиция по настоящему изобретению может включать два или несколько стабилизирующих липидов, где каждый из стабилизирующих липидов по отдельности может составлять от 5 до 35 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления композиция по настоящему изобретению может включать два или несколько стабилизирующих липидов, где каждый из стабилизирующих липидов по отдельности может составлять от 10 до 30 мол.% от липидных компонентов композиции.
[00207] В некоторых вариантах осуществления суммарное количество одного или нескольких стабилизирующих липидов может составлять от 25 до 40 мол.% от липидов композиции, где каждый из стабилизирующих липидов по отдельности может составлять от 5 до 35 мол.%.
[00208] В некоторых вариантах осуществления суммарное количество одного или нескольких стабилизирующих липидов может составлять от 30 до 40 мол.% от липидов композиции, где каждый из стабилизирующих липидов в отдельности может составлять от 10 до 30 мол.%.
[00209] Один или несколько липидов для снижения иммуногенности композиции могут составлять от 1 до 8 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления один или несколько липидов для снижения иммуногенности композиции могут составлять от 1 до 5 мол.% от липидных компонентов композиции.
[00210] В дополнительных аспектах композиция по настоящему изобретению может дополнительно включать катионный липид, который может составлять от 5 до 25 мол.% от липидных компонентов композиции. В некоторых вариантах осуществления композиция по настоящему изобретению может дополнительно включать катионный липид, который может составлять от 5 до 15 мол.% от липидных компонентов композиции. В этих аспектах молярное соотношение концентраций катионного липида и ионизируемых молекул композиции по настоящему изобретению может составлять от 5:35 до 25:15.
[00211] В некоторых вариантах осуществления, набор липидных компонентов композиции может включать один или несколько из молекулярных компонентов ионизируемого соединения, структурный липид, один или нескольких липидов для снижения иммуногенности композиции и один или несколько стабилизирующих липидов.
[00212] В дополнение к вышеуказанным компонентам композиция по настоящему изобретению может дополнительно включать фузогенную молекулу по настоящему изобретению. Фузогенная молекула может составлять 1-10 мол.% от композиции.
[00213] Примеры липидных композиций
[00214] В некоторых вариантах осуществления композиция может содержать одну или несколько ионизируемых молекул, структурный липид, один или несколько липидов для снижения иммуногенности композиции и фузогенную молекулу по настоящему изобретению, что будет представлять 100% липидных компонентов композиции. В некоторых вариантах осуществления может быть включен катионный липид.
[00215] Примеры композиций по настоящему изобретению приведены в таблице 1.
Таблица 1: композиции липидных компонентов (количество каждого выражено в мол.% от общего количества)
[00216] Примеры композиций по настоящему изобретению приведены в таблице 2.
Таблица 2: Композиции липидных компонентов (количество каждого выражено в мол.% от общего количества)
[00217] Структурные липиды
[00218] Примеры структурных липидов включают холестерины, стеролы и стероиды.
[00219] Примеры структурных липидов включают холаны, холестаны, эргостаны, кампестаны, пориферастаны, стигмастаны, горгостаны, ланостаны, гонаны, эстраны, андростаны, прегнаны и циклоартаны.
[00220] Примеры структурных липидов включают стерины и зоостеролы, такие как холестерин, ланостерол, зимостерол, зимостенол, десмостерол, стигмастанол, дигидроланостерол и 7-дегидрохолестерин.
[00221] Примеры структурных липидов включают пегилированные холестерины и 3-оксо-(C1-22)ацильные соединения холестана, например, холестерилацетат, холестериларахидонат, холестерилбутират, холестерилгексаноат, холестерилмиристат, холестерилпальмитат, холестерилбегенат, холестерилстеарат, холестерилкаприлат, холестерил-н-деканоат, холестерилдодеканоит, холестерилнервонат, холестерилпеларгонат, холестерил-н-валерат, холестерилолеат, холестерилэлаидат, холестерилэрукат, холестерилгептаноат, холестериллинолелаидат и холестериллинолеат.
[00222] Примеры структурных липидов включают стерины, такие как фитостеролы, бета-ситостерол, кампестерол, эргостерол, брассикастерол, дельта-7-стигмастерол и дельта-7-авенастерол.
[00223] Стабилизирующие липиды
[00224] Примеры стабилизирующих липидов включают цвиттерионные липиды.
[00225] Примеры стабилизирующих липидов включают такие соединения, как фосфолипиды.
[00226] Примеры фосфолипидов включают фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозитол, фосфатидную кислоту, пальмитоилолеоилфосфатидилхолин, лизофосфатидилхолин, лизофосфатидилэтаноламин, дипальмитоилфосфатидилхолин, диолеоилфосфатидилхолин, дистеароилфосфатидилхолин и ордилинолеоилфосфатидилхолин.
[00227] Примеры стабилизирующих липидов включают соединения фосфатидилэтаноламина и соединения фосфатидилхолина.
[00228] Примеры стабилизирующих липидов включают 1,2-диолеоил-sn-глицеро-3-фосфохолин (DOPC).
[00229] Примеры стабилизирующих липидов включают дифитаноилфосфатидилэтаноламин (DPhPE) и 1,2-дифитаноил-sn-глицеро-3-фосфохолин (DPhPC).
[00230] Примеры стабилизирующих липидов включают 1,2-дистеароил-sn-глицеро-3-фосфохолин (DSPC), 1,2-дипальмитоил-sn-глицеро-3-фосфохолин (DPPC), 1,2-дипальмитоил-sn-глицеро-3-фосфоэтаноламин (DPPE) и 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин (DOPE).
[00231] Примеры стабилизирующих липидов включают 1,2-дилауроил-sn-глицерин (DLG); 1,2-димиристоил-sn-глицерин (DMG); 1,2-дипальмитоил-sn-глицерин (DPG); 1,2-дистеароил-sn-глицерин (DSG); 1,2-диарахидоил-sn-глицеро-3-фосфохолин (DAPC); 1,2-дилауроил-sn-глицеро-3-фосфохолин (DLPC); 1,2-димиристоил-sn-глицеро-3-фосфохолин (DMPC); 1,2-дипальмитоил-sn-глицеро-O-этил-3-фосфохолин (DPePC); 1,2-дилауроил-sn-глицеро-3-фосфоэтаноламин (DLPE); 1,2-димиристоил-sn-глицеро-3-фосфоэтаноламин (DMPE); 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин (DSPE); 1-пальмитоил-2-линолеил-sn-глицеро-3-фосфохолин; 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолин (POPC); 1-пальмитоил-2-лизо-sn-глицеро-3-фосфохолин (P-Lyso-PC); и 1-стеароил-2-лизо-sn-глицеро-3-фосфохолин (S-Lyso-PC).
[00232] Липиды для снижения иммуногенности
[00233] Примеры липидов для снижения иммуногенности включают полимерные соединения и полимер-липидные конъюгаты.
[00234] Примеры липидов для снижения иммуногенности включают пегилированные липиды, содержащие области с молекулами полиэтиленгликоля (ПЭГ). Молекулы ПЭГ могут иметь любую молекулярную массу. В некоторых вариантах осуществления молекула ПЭГ может иметь молекулярную массу 200, 300, 350, 400, 500, 550, 750, 1000, 1500, 2000, 3000, 3500, 4000 или 5000 Да.
[00235] Примеры липидов для снижения иммуногенности включают соединения, имеющие метоксиполиэтиленгликолевую область.
[00236] Примеры липидов для снижения иммуногенности включают соединения, имеющие карбонилметоксиполиэтиленгликолевую область.
[00237] Примеры липидов для снижения иммуногенности включают соединения, имеющие область с разветвленными молекулами ПЭГ.
[00238] Примеры липидов для снижения иммуногенности включают соединения, имеющие полиглицериновую область.
[00239] Примеры липидов для снижения иммуногенности включают полимерные липиды, такие как DSPE-mPEG, DMPE-mPEG, DPPE-mPEG и DOPE-mPEG.
[00240] Примеры липидов для снижения иммуногенности включают ПЭГ-фосфолипиды и ПЭГ-церамиды.
[00241] Катионные липиды
[00242] Примеры катионных липидов включают катионные соединения HEDC (2-(бис(2-(тетрадеканоилокси)этил)амино)-N-(2-гидроксиэтил)-N, N-диметил-2-оксоэтанаминийбромид), описанные в US2013/0330401A1. Некоторые примеры катионных липидов приведены в US2013/0115274A1.
[00243] Липидные композиции
[00244] В некоторых вариантах осуществления композиция может содержать фузогенную молекулу, ионизируемое соединение, холестерин, липиды DOPC и DOPE и DPPE-mPEG. В некоторых вариантах осуществления фузогенная молекула может составлять 1-20 мол.% от композиции, ионизируемая молекула может составлять от 15 до 25 мол.% от композиции; все вместе холестерин, DOPC и DOPE могут составлять от 75 до 85 мол.% от композиции; и DPPE-mPEG может составлять 2-5 мол.% от композиции.
[00245] В одном варианте осуществления фузогенная молекула может составлять 2 мол.% от композиции, ионизируемая молекула может составлять 24 мол.% от композиции; холестерин может составлять 29 мол.% от композиции, DOPC может составлять 20 мол.% от композиции, DOPE может составлять 20 мол.% от композиции; и DPPE-mPEG (2000) может составлять 5 мол.% от композиции.
[00246] Наночастицы
[00247] Варианты осуществления настоящего изобретения могут предоставить липосомальные композиции наночастиц. Фузогенные молекулы по настоящему изобретению могут быть использованы для образования липосомальных композиций, которые могут иметь одну или несколько бислойных структур из липидоподобных молекул.
[00248] Композиция наночастиц может содержать одну или несколько фузогенных молекул по настоящему изобретению в липосомальной структуре, бислойной структуре, мицелле, ламеллярной структуре или в их смеси.
[00249] В некоторых вариантах осуществления композиция может включать один или несколько компонентов жидкого носителя. Жидкий носитель, подходящий для доставки действующих агентов по настоящему изобретению, может представлять собой фармацевтически приемлемый жидкий носитель. Жидкий носитель может включать органический растворитель или комбинацию воды и органического растворителя.
[00250] Варианты осуществления данного изобретения могут предоставить липидные наночастицы, имеющие размер от 10 до 1000 нм. В некоторых вариантах осуществления липосомальные наночастицы могут иметь размер от 10 до 150 нм.
[00251] Фармацевтические композиции
[00252] Данное изобретение дополнительно предусматривает способы распределения действующего агента в органе субъекта для лечения фиброза путем введения субъекту композиции по настоящему изобретению. Органы, которые подходят для лечения, включают легкое, печень, поджелудочную железу, почку, толстую кишку, сердце, костный мозг, кожу, кишечник, головной мозг и глаз.
[00253] В некоторых вариантах осуществления настоящее изобретение относится к способам лечения заболевания фиброзом легких путем введения субъекту композиции по настоящему изобретению.
[00254] Примеры фиброза включают идиопатический фиброз легких и цирроз печени.
[00255] В дополнительных аспектах настоящее изобретение относится к ряду фармацевтических составов.
[00256] Фармацевтический состав в настоящем документе может включать действующий агент, а также носитель лекарственного средства или липид по настоящему изобретению вместе с фармацевтически приемлемым носителем или разбавителем.
[00257] В общем, действующие агенты в данном описании включают киРНК, действующие агенты при фиброзе, а также любое низкомолекулярное лекарственное средство. Действующий агент может представлять собой нуклеиновую кислоту, киРНК, мРНК или микроРНК.
[00258] Фармацевтический состав по настоящему изобретению может содержать одно или несколько из следующих веществ: поверхностно-активное вещество, разбавитель, наполнитель, консервант, стабилизатор, краситель и суспензионный агент.
[00259] Некоторые фармацевтические носители, разбавители и компоненты для фармацевтического состава, а также способы составления и введения соединений и композиций по настоящему изобретению описаны в Remington's Pharmaceutical Sciences, 18th Ed., Mack Publishing Co., Easton, Penn. (1990).
[00260] Примеры консервантов включают бензоат натрия, аскорбиновую кислоту и сложные эфиры п-гидроксибензойной кислоты.
[00261] Примеры поверхностно-активных агентов включают спирты, сложные эфиры, сульфатированные алифатические спирты.
[00262] Примеры наполнителей включают сахарозу, глюкозу, лактозу, крахмал, кристаллическую целлюлозу, маннит, легкий безводный силикат, алюминат магния, метасиликаталюминат магния, синтетический силикат алюминия, карбонат кальция, кислый карбонат натрия, гидрофосфат кальция и кальциевую карбоксиметилцеллюлозу.
[00263] Примеры суспензионных агентов включают кокосовое масло, оливковое масло, кунжутное масло, арахисовое масло, сою, ацетатфталат целлюлозы, метилацетатметакрилатный сополимер и сложноэфирные фталаты.
[00264] Структуры молекулярных хвостов
[00265] Соединение по настоящему изобретению может иметь один или несколько липофильных хвостов, которые содержат одну или несколько алкильных или алкенильных групп. Примеры липофильных хвостов, имеющих алкенильные группы, включают C(14:1(5))алкенил, C(14:1(9))алкенил, C(16:1(7))алкенил, C(16:1(9))алкенил, C(18:1(3))алкенил, C(18:1(5))алкенил, C(18:1(7))алкенил, C(18:1(9))алкенил, C(18:1(11))алкенил, C(18:1(12))алкенил, C(18:2(9,12))алкенил, C(18:2(9,11))алкенил, C(18:3(9,12,15))алкенил, C(18:3(6,9,12))алкенил, C(18:3(9,11,13))алкенил, C(18:4(6,9,12,15))алкенил, C(18:4(9,11,13,15))алкенил, C(20:1(9))алкенил, C(20:1(11))алкенил, C(20:2(8,11))алкенил, C(20:2(5,8))алкенил, C(20:2(11,14))алкенил, C(20:3(5,8,11))алкенил, C(20:4(5,8,11,14))алкенил, C(20:4(7,10,13,16))алкенил, C(20:5(5,8,11,14,17))алкенил, C(20:6(4,7,10,13,16,19))алкенил, C(22:1(9))алкенил, C(22:1(13))алкенил, and C(24:1(9))алкенил. Некоторые примеры хвостовых структур можно найти в Donald Voet and Judith Voet, Biochemistry, 3rd Edition (2005), p. 383.
[00266] Некоторые примеры липофильных хвостов включают следующие структуры:

[00267] Любая из этих примерных структур липофильных хвостов может иметь одну или несколько дополнительных химических ветвей.
[00268] Дополнительные варианты осуществления
[00269] Варианты осуществления данного изобретения дополнительно включают в себя:
[00270] Соединение по формуле (А)
 формула А,
формула А,
где линкер представляет собой двухвалентную группу, содержащую участок ПЭГ,
X1 и X2 независимо представляют собой С1-С5алкандиильную группу,
R1, R2, R3 и R4 независимо представляют собой:
 ,
,
X3 представляет собой одинарную связь, С1-С5алкандиильную группу или С2-С5алкендиильную группу,
X4 и X5 независимо представляют собой C2-5алкандиильную группу,
Z1, Z2 и Z3 независимо представляют собой -O-, -S- или -NH-, и
R5 и R6 независимо представляют собой C11-23алкильную или C11-23алкенильную группу.
Соединение по формуле (В)
 формула (В),
формула (В),
где линкер представляет собой двухвалентную группу, содержащую участок ПЭГ,
X6 и X7 независимо представляют собой С1-С5алкандиильную группу,
X8 и X9 независимо представляют собой С1-С5алкандиильную группу,
Z4 и Z5 независимо представляют собой -O-, -S- или -NH-,
R7, R8, R9 и R10 независимо представляют собой:
 ,
,
X4 и X5 независимо представляют собой C2-5алкандиильную группу,
Z2 и Z3 независимо представляют собой -O-, -S- или -NH-, и
R5 и R6 независимо представляют собой C11-23алкильную или C11-23алкенильную группу.
Соединение, указанное выше, где линкер представляет собой:
 ,
,
где m представляет собой целое число от 1 до 12,
Y1 представляет собой -O-, -NH- или -NHCH2-,
Y2 представляет собой -O-, -NH- или -CH2NH-,
n и q независимо представляют собой целое число от 1 до 5,
р представляет собой целое число от 1 до 5,
Y3 и Y5 независимо представляют собой -O-, -NH- или -NHCH2-, и
Y4 и Y6 независимо представляют собой -O-, -NH- или -CH2NH-.
Соединение, указанное выше, где X1 и X2 независимо представляют собой C1-C5 прямую алкандиильную группу, предпочтительно, C2-C4 прямую алкандиильную группу, более предпочтительно, C4 прямую алкандиильную группу.
Соединение, указанное выше, где R1, R2, R3 и R4 являются одинаковыми группами.
Соединение, указанное выше, где X3 представляет собой одинарную связь или C1-C5 прямую алкандиильную группу, X3 предпочтительно представляет собой C2-C4 прямую алкандиильную группу, более предпочтительно, этилен, то есть этандиильную группу.
Соединение, указанное выше, где X4 и X5 независимо представляют собой C2-5 прямую алкандиильную группу, X4 и X5, предпочтительно, представляют собой C2-4 прямую алкандиильную группу, более предпочтительно, этилен, то есть этандиильную группу.
Соединение, указанное выше, где Z1 представляет собой -NH-.
Соединение, указанное выше, где Z2 и Z3 представляют собой -O-.
Соединение, указанное выше, где R5 и R6 независимо представляют собой C11-23 прямую алкенильную группу.
Соединение, указанное выше, где R5 и R6 независимо представляют собой C11-23 прямую алкенильную группу с 1-6 двойными связями, где число двойных связей, предпочтительно, составляет 1-3, более предпочтительно, 2-3, еще более предпочтительно, 2.
Соединение, указанное выше, где R5 и R6 независимо представляют собой C11-23 прямую алкенильную группу с 2 двойными связями.
Соединение, указанное выше, где R5 и R6 независимо представляют собой C13-17 прямую алкенильную группу, R5 и R6 предпочтительно представляют собой C15-17 прямую алкенильную группу, более предпочтительно, С17 прямую алкенильную группу.
Соединение, указанное выше, где R5 и R6 независимо представляют собой C17 прямую алкенильную группу.
Соединение, указанное выше, где R5 и R6 представляет собой гептадека-8,1-диенильную группу.
Композиция, указанная выше, которая содержит катионный липид, ионизируемый липид и липид указанного выше соединения в липидной наночастице, содержащей бислой липидных молекул.
Композиция, указанная выше, которая дополнительно содержит нуклеиновую кислоту.
Композиция, указанная выше, где нуклеиновая кислота представляет собой киРНК, мРНК или микроРНК.
Композиция, указанная выше, где композиция представляет собой фармацевтическую композицию.
[00271] Химические определения
[00272] Используемый в настоящем документе термин «алкил» относится к гидрокарбильному радикалу насыщенной алифатической группы, который может иметь любую длину, если не указано иное. Алкильная группа может представлять собой разветвленную или неразветвленную, замещенную или незамещенную алифатическую группу, содержащую от 1 до 22 атомов углерода. Это определение также применимо к алкильной части других групп, таких как, например, циклоалкил, алкокси, алканоил и аралкил.
[00273] Например, используемый в настоящем документе, термин, такой как «С(1-5)алкил», включает в себя C(1)алкил, C(2)алкил, C(3)алкил, C(4)алкил и C(5)алкил. Аналогичным образом, например, термин «C(3-22)алкил» включает в себя C(1)алкил, C(2)алкил, C(3)алкил, C(4)алкил, C(5)алкил, C(6)алкил, C(7)алкил, C(8)алкил, C(9)алкил, C(10)алкил, C(11)алкил, C(12)алкил, C(13)алкил, C(14)алкил, C(15)алкил, C(16)алкил, C(17)алкил, C(18)алкил, C(19)алкил, C(20)алкил, C(21)алкил и C(22)алкил.
[00274] В настоящем описании алкильная группа может обозначаться таким термином, как Me (метил, -CH3), Et (этил, -CH2CH3), Pr (любая пропильная группа), nPr (n-Pr, н-пропил), iPr (i-Pr, изопропил), Bu (любая бутильная группа), nBu (n-Bu, н-бутил), iBu (i-Bu, изобутил), sBu (s-Bu, втор-бутил) и tBu (t-Bu, трет-бутил).
[00275] Используемый в настоящем документе термин «алкенил» относится к гидрокарбильному радикалу, имеющему, по меньшей мере, одну углерод-углеродную двойную связь. Алкенильная группа может представлять собой разветвленный или неразветвленный, замещенный или незамещенный гидрокарбильный радикал, имеющий от 2 до 22 атомов углерода и по меньшей мере одну углерод-углеродную двойную связь. «Алкенильная» группа имеет одну или несколько углерод-углеродных двойных связей.
[00276] Используемый в настоящем документе термин «замещенный» относится к атому, имеющему одну или несколько замещающих групп или один или несколько заместителей, которые могут быть одинаковыми или разными и могут включать водородный заместитель. Таким образом, термины алкил, циклоалкил, алкенил, алкокси, алканоил и арил, например, относятся к группам, которые могут включать замещенные варианты. Замещенные варианты включают линейные, разветвленные и циклические варианты и группы, имеющие заместитель или заместители, замещающие один или несколько атомов водорода, присоединенных к любому атому углерода в группе.
[00277] В общем, соединение может содержать один или несколько хиральных центров. Соединения, содержащие один или несколько хиральных центров, могут включать соединения, описанные как «изомер», «стереоизомер», «диастереомер», «энантиомер», «оптический изомер» или как «рацемическая смесь». В данной области техники известны условные обозначения стереохимической номенклатуры, например правила наименования стереоизомеров Кана-Ингольда-Прелога, а также способы определения стереохимии и разделения стереоизомеров. См., например, Michael B. Smith and Jerry March, March’s Advanced Organic Chemistry, 5th edition, 2001. Соединения и структуры по настоящему изобретению, включая химические чертежи, подразумевают охват всех возможных изомеров, химически приемлемых позиционных изомеров, стереоизомеров, диастереомеров, энантиомеров и/или оптических изомеров, которые могли бы существовать для конкретных соединения или структуры, включая любую их смесь, рацемическую или какую-либо еще.
[00278] Данное изобретение охватывает любые и все таутомерные, сольватированные или несольватированные, гидратированные или негидратированные формы, а также любые изотопные формы атомов соединений и композиций, раскрытых в настоящем документе.
[00279] Данное изобретение охватывает любые и все кристаллические полиморфы или различные кристаллические формы соединений и композиций, раскрытых в настоящем документе.
[00280] Используемые сокращения:
DMAP - 4-N, N-диметиламинопиридин
DCM - дихлорметан
TEA - триэтиламин
EDC - 1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорид
Na2SO4 - сульфат натрия
EtOAc - этилацетат
DMF - N, N-диметилфорамид
ELSD - испарительный детектор светорассеяния
NaCl - хлорид натрия
K2CO3 - карбонат калия
MeOH - метанол
TFA - трифторуксусная кислота
DIEA - N, N-диизопропилэтиламин
ПЭГ/PEG - полиэтиленгликоль или полиэтиленоксид
MgSO4 - сульфат магния
LCMS - жидкостная хроматография-масс-спектрометрия
NaHCO3 - бикарбонат натрия
H2O - вода
HCl - гидрохлорид
KI - калия йодид
DMSO - диметилсульфоксид
TBAF - тетра-N-бутиламмонийфторид
NaBH4 - боргидрид натрия
THF - тетрагидрофуран
TBDMS - трет-бутилдиметилсилил
LiOH - гидроксид лития
MeI - йодистый метил
BOC - трет-бутилоксикарбонил
Fmoc - флуоренилметилоксикарбонил
[00281] ПРИМЕРЫ
[00282] Пример 1: фузогенные молекулы по настоящему изобретению были полезны для доставки одного или нескольких биологически действующих агентов в клетки. В данном примере было показано, что фузогенные молекулы по настоящему изобретению обеспечивают неожиданно эффективную доставку иллюстративной киРНК, мишенью которой является HSP47, для нокдауна экспрессии гена. Доставку иллюстративной киРНК осуществляли в липосомальной композиции, содержащей фузогенные молекулы. Присутствие фузогенных молекул по настоящему изобретению в составе для доставки неожиданно обеспечивало высокую активность состава для подавления экспрессии генов с помощью киРНК.
[00283] Активность in vitro для нокдауна экспрессии гена с использованием киРНК измеряли с использованием звездчатых клеток крысы в среде DMEM в соответствии со следующим протоколом: за один день до трансфекции клетки высевают в 96-луночный планшет в количестве 3×103 клеток на лунку для звездчатых клеток в 100 мкл среды, содержащей 10% FBS, и культивируют при 37°C в инкубаторе в атмосфере увлажненного воздуха, содержащего 5% CO2. Перед трансфекцией среду меняют на 90 мкл среды без антибиотиков. Подготавливают соответствующие разведения раствора, собранного из диализных мешков в буфере PBS, так чтобы добавление 10 мкл в каждую лунку было достаточным для достижения желаемой концентрации. Через 48 часов после трансфекции клетки промывают один раз ледяным PBS. Клетки лизируют в 50 мкл лизирующего буфера Cell-to-Ct Lysis Buffer в течение 5-30 минут при комнатной температуре. Добавляют 5 мкл стоп-раствора и инкубируют в течение 2 минут при комнатной температуре окружающей среды. Уровень мРНК измеряют немедленно с помощью кПЦР с TAQMAN-пробами. В альтернативном варианте, образцы могут быть заморожены при -80°C и проанализированы позднее. Для анализа кОТ-ПЦР: размораживают все реагенты на льду. Смешивают объединенные реагенты в 0,2-миллилитровых пробирках для ПЦР. Распределяют готовую смесь по лункам 384-луночного планшета, по 10 мкл на лунку в трех повторах. Планшет запечатывают пленкой, смесь сбрасывают центрифугированием на дно лунок. Выполняют анализ кОТ-ПЦР.
[00284] В этом примере киРНК HSP47 была использована для нокдауна гена HSP47. Для TaqMan-анализа экспрессии гена использовали специфичный для гена HSP47 TaqMan-зонд.
[00285] Экспериментальные результаты в отношении активности подавления экспрессии генов генов in vitro в звездчатых клетках крысы показаны в таблицах 3 и 4.
Таблица 3: активность in vitro в звездчатых клетках крысы
Таблица 4: активность in vitro в звездчатых клетках крысы
[00286] Эти данные показывают, что препарат киРНК, содержащий фузогенную молекулу по настоящему изобретению, был удивительно эффективным для доставки действующего агента киРНК в клетки. Было показано, что фузогенные молекулы по настоящему изобретению обеспечивают неожиданно эффективную доставку для нокдауна экспрессии гена с использованием иллюстративной киРНК, направленной против HSP47.
[00287] Пример 2: было показано, что широкий спектр фузогенных молекул по настоящему изобретению полезен для доставки действующего агента в клетки. В этом примере было показано, что ряд фузогенных молекул по настоящему изобретению обеспечивают неожиданно эффективную доставку иллюстративной киРНК, направленной против HSP47, для нокдауна экспрессии гена. Доставку иллюстративной киРНК осуществляли в липосомальной композиции, содержащей фузогенные молекулы.
[00288] Активность in vitro для нокдауна экспрессии генов, измеренная в звездчатых клетках с использованием иллюстративной киРНК в липосомальной композиции, содержащей различные фузогенные молекулы по настоящему изобретению, приведена в таблице 5.
Таблица 5: % экспрессии HSP47 в звездчатых клетках
[00289] Как показано в таблице 5, присутствие фузогенных молекул по настоящему изобретению в составе для липосомальной доставки неожиданно обеспечивало высокую активность состава для нокдауна экспрессии гена с использованием иллюстративной киРНК.
[00290] Пример 3: фузогенные молекулы по настоящему изобретению оказались неожиданно активными в отношении увеличения эффективности доставки действующего агента в клетки. Активность агента, доставляемого в липосомальной композиции, содержащей фузогенную молекулу по настоящему изобретению, была значительно увеличена по сравнению с активностью агента, доставляемого в липосомальной композиции, которая не содержала фузогенную молекулу по настоящему изобретению.
[00291] В этом примере активность в отношении нокдауна экспрессии гена с помощью иллюстративной киРНК, направленной против HSP47, была неожиданно увеличена с использованием липосомальной композиции для доставки, которая включала соединение R4 по настоящему изобретению.
[00292] Липосомальную композицию для доставки получали в соответствии со следующим протоколом: HEDC (2-(бис(2-(тетрадеканоилокси)этил)амино)-N-(2-гидроксиэтил)-N, N-диметил-2-оксоэтан-аминия бромид) и S104 ( ((2-((2-(диметиламино)этил)тио)ацетил)азандиил)бис(этан-1,2-диил)дитетрадеканоат) растворяли в абсолютном EtOH (100%-е содержание спирта)) в молярном соотношении 1:1. киРНК HSP47 солюбилизировали в 50 мМ цитратном буфере, и температуру доводили до 35-40°С. Затем смесь этанол/липид добавляли в киРНК-содержащий буфер при перемешивании, чтобы самопроизвольно сформировались нагруженные киРНК липосомы. Липиды объединяли с киРНК до достижения конечного общего отношения липида к киРНК от 5:1 до 15:1 (по массе). Нагруженные киРНК липосомы подвергали диафильтрации против 10 объемов PBS (pH 7,2) для удаления этанола и обмена буфера. Конечный продукт фильтровали через стерилизующий PES-фильтр с размером пор 0,22 мкм для уменьшения бионагрузки.
[00293] В этом примере активность in vitro в отношении нокдауна экспрессии гена с использованием иллюстративной киРНК в звездчатых клетках крысы проводили таким же образом, как и в примере 1. Результаты показаны на фиг.46. Липосомальная композиция содержала липиды HEDC и S104, а также фузогенное соединение.
[00294] На фиг.46 приведены результаты для липосомальной композиции, состоящей из липидов HEDC и S104, которая не содержала фузогенного соединения (1). Нокдаун экспрессии гена HSP47 для этой контрольной композиции был выраженным только при самой высокой концентрации в 300 нМ.
[00295] На фиг.46 приведены результаты для липосомальной композиции, состоящей из липидов HEDC и S104, которая содержала фузогенное соединение R4 (2). Количество фузогенного соединения R4 в этой композиции составляло 2% от общего количества липидов. Нокдаун экспрессии гена HSP47 для этого состава был значительно и неожиданно увеличен при всех концентрациях киРНК по сравнению с контрольным составом, который не содержал фузогенное соединение R4. Таким образом, присутствие фузогенного соединения R4 в препарате значительно увеличивало доставляемую активность иллюстративной киРНК, и повышенная активность была непосредственно связана с присутствием фузогенного соединения R4.
[00296] На фиг.46 приведены результаты для липосомальной композиции, состоящей из липидов HEDC и S104, которая содержала фузогенное соединение R4 (3). Количество фузогенного соединения R4 в этой композиции составляло 10% от общего количества липидов. Нокдаун экспрессии гена HSP47 для этого состава был значительно и неожиданно увеличен при всех концентрациях киРНК по сравнению с контрольным составом, который не содержал фузогенное соединение R4. Таким образом, присутствие фузогенного соединения R4 в составе значительно повышало доставляемую активность иллюстративной киРНК, и повышенная активность была непосредственно связана с присутствием фузогенного соединения R4.
[00297] Как показано на фиг.46, в случае липосомальных композиций для доставки, содержащих липиды HEDC и S104, активность в отношении нокдауна экспрессии гена в звездчатых клетках с использованием иллюстративной киРНК, направленной против HSP47, неожиданно увеличилась в композициях, содержащих от 2 до 10% (от общего количества липидов) фузогенного соединения R4.
[00298] Пример 4: фузогенные молекулы по настоящему изобретению обеспечивали неожиданно повышенную активность действующего агента, нуклеиновой кислоты, в клетках. Активность агента, нуклеиновой кислоты, доставляемого в липосомальном составе, содержащем фузогенную молекулу по настоящему изобретению, была значительно увеличена по сравнению с активностью липосомального состава, который не содержал фузогенную молекулу по настоящему изобретению.
[00299] В этом примере эксперимент по анализу активности in vitro для нокдауна экспрессии гена с использованием иллюстративной киРНК в звездчатых клетках крысы проводили аналогично примеру 1. Результаты показаны на фиг.47. Липосомная композиция содержала липиды HEDC и S104, а также фузогенное соединение.
[00300] На фиг.47 приведены результаты для липосомальной композиции, состоящей из липидов HEDC и S104, которая не содержала фузогенного соединения по настоящему изобретению (1). Нокдаун экспрессии гена HSP47 для этой контрольной композиции был выраженным только при самой высокой концентрации киРНК в 300 нМ.
[00301] На фиг.47 приведены результаты для липосомальной композиции, состоящей из липидов HEDC и S104, которая содержала фузогенное соединение R4 (2). Количество фузогенного соединения R4 в этой композиции составляло 2% от общего количества липидов. Нокдаун экспрессии гена HSP47 для этого состава был значительно и неожиданно увеличен при всех концентрациях киРНК по сравнению с контрольным составом, который не содержал фузогенное соединение R4. Таким образом, присутствие фузогенного соединения R4 в составе значительно увеличивало доставляемую активность иллюстративной киРНК, и повышенная активность была непосредственно связана с присутствием фузогенного соединения R4.
[00302] На фиг.47 приведены результаты для липосомальной композиции, состоящей из липидов HEDC и S104, которая содержала фузогенное соединение T3 (3). Количество фузогенного соединения Т3 в этой композиции составляло 2% от общего количества липидов. Нокдаун экспрессии гена HSP47 для этого состава был значительно и неожиданно увеличен при всех концентрациях киРНК по сравнению с контрольным составом, который не содержал фузогенное соединение Т3. Таким образом, присутствие фузогенного соединения Т3 в составе значительно увеличивало доставляемую активность иллюстративной киРНК, и повышенная активность была непосредственно связана с присутствием фузогенного соединения Т3.
[00303] Пример 5: фузогенные молекулы по настоящему изобретению были эффективны для доставки одной или нескольких биологически активных молекул in vitro. Например, активность по подавлению экспрессии генов с использованием киРНК (киРНК HSP47, см. пример 1) была неожиданно увеличена благодаря присутствию фузогенного соединения по настоящему изобретению в составе для липосомальной доставки.
[00304] В этом примере липосомальные препараты для доставки изготавливали для соединений сравнения, а также для фузогенного соединения R4. Композиции для липосомальной доставки получали таким же образом, как в примере 1, с композициями, приведенными в таблице 6 (СН обозначает холестерин).
Таблица 6: фузогенные липосомальные составы
[00305] Как показано на фиг.24, для составов с липосомальной доставкой из таблицы 6 активность для нокдауна экспрессии гена в звездчатых клетках с помощью иллюстративной киРНК, направленной против HSP47, неожиданно увеличилась в составах, содержащих 2% (от общего количества липидов) фузогенного соединения R4 по настоящему изобретению по сравнению с контрольной композицией, которая не содержала фузогенное соединение по настоящему изобретению. Структура фузогенного соединения R4 по настоящему изобретению обеспечивала удивительную эффективность доставки в отношении нокдауна экспрессии гена в звездчатых клетках с помощью иллюстративной киРНК.
[00306] Пример 6: фузогенные липидные молекулы по настоящему изобретению были эффективны для доставки одной или нескольких биологически активных молекул в клетки. В этом примере составы для липосомальной доставки, содержащие иллюстративную киРНК (киРНК HSP47, см. пример 1), а также фузогенное соединение по настоящему изобретению, обеспечивали эффективный нокдаун экспрессии гена. В этом примере, как показано в таблице 7, были изготовлены содержащие различные соединения от T3 до T9 (от 1 до 7) липосомальные составы для доставки киРНК, каждый из которых содержал по 2% (от общего количества липидов) фузогенного соединения по настоящему изобретению. Композиции для липосомальной доставки получали таким же образом, как в примере 1.
Таблица 7: фузогенные липосомальные составы
[00307] Как показано на фиг.25, при этом измерении активности составов для липосомальной доставки киРНК из таблицы 7 данные составы обеспечивали высокую активность нокдауна экспрессии гена в звездчатых клетках. Таким образом, составы, содержащие 2% (от общего количества липидов) фузогенного соединения по настоящему изобретению, обеспечивали высокую активность киРНК, направленной против HSP47.
[00308] Пример 7: активность in vivo фузогенных составов. Фузогенные молекулы по настоящему изобретению были полезны для доставки действующего агента in vivo. Например, составы для липосомальной доставки для нокдауна экспрессии гена с использованием иллюстративной киРНК, направленной против HSP47, были активными благодаря присутствию фузогенного соединения по настоящему изобретению.
[00309] Как показано на фиг.26, составы для липосомальной доставки демонстрировали активность в отношении нокдауна экспрессии генов in vivo (мыши) с использованием киРНК, направленной против HSP47. Композиции содержали 2% (от общего количества липидов) указанного фузогенного соединения по настоящему изобретению. Доставку составов осуществляли инфузионным болюсом. Параметры доставки приведены в таблице 8.
Таблица 8: фузогенные липосомальные составы in vivo
[00310] Пример протокола для этих результатов приведен ниже.
[00311] 1.1. Животные
[00312] Восемьдесят самцов крыс Sprague-Dawley в возрасте ~49 дней были приобретены в Charles River Laboratories и доставлены в испытательный центр. Средний вес животных при получении составлял около 200-210 граммов. Животных содержали в стандартных клеточных системах с 2 животными на клетку при чередующемся цикле свет/темнота продолжительностью 12 часов. Температура в помещении поддерживалась на уровне 64-79°F (18-26°C), а влажность - на уровне 30-70%, при этом не менее осуществляли 10 смен объемов воздуха в час при использовании 100% свежего воздуха без рециркуляции. Животным давали сертифицированную стерилизованную радиацией стандартную свежую еду для грызунов и водопроводную воду ad-libitum.
[00313] Семидесяти двум животным вводили DMN в дни 0-5 и затем случайным образом разделяли на 9 групп по 8 крыс на группу, исходя из их массы тела, так чтобы не было значительного различия в массе тела между группами до введения киРНК. Это подтверждали с помощью однофакторного анализа ANOVA. Как и ожидалось, животные, которые получали DMN, имели значительно меньшую массу тела, чем животные, которым не вводили DMN («чистые животные»).
[00314] 1.2. Введение DMN
[00315] DMN получали от Wako (номер партии DSP2369) и подготавливали для внутрибрюшинной (IP) инъекции в фосфатно-солевом буфере (PBS), приготавливая раствор соединения в концентрации 5 мг/мл. Семидесяти двум крысам ежедневно вводили DMN в дозе 10 мг/кг в объеме 2 мл/кг с 0-го дня до 2-го дня и затем 5 мг/кг в объеме 1 мл/кг с 3-го дня до 5-го дня; восемь животных, которым не вводили DMN, использовали в качестве отрицательного контроля для этой процедуры. Животных ежедневно взвешивали и соответственно корректировали дозу DMN.
[00316] 1.3. Введение киРНК
[00317] В экспериментальный день 5, животных распределяли по разным группам лечения и вводили препараты согласно соответствующей схеме лечения. Тестируемые препараты использовались для групп лечения 2-8 (от №№1-8) соответственно; тогда как животные в группе 1 (№1) получали только носитель (физиологический раствор) в дозе 3 мл/кг однократной внутривенной инъекцией в латеральную хвостовую вену. Животные в группе 9 (чистая группа, № 9) не получали лечения.
[00318] 1.4. Эвтаназия и вскрытие
[00319] В экспериментальный день 6, через 24 часа после введения, животных умерщвляли путем ингаляционной передозировки диоксида углерода. Печень немедленно промывали PBS, pH 7,4 (40 мл со скоростью 20 мл/мин) через печеночную воротную вену для удаления остаточной крови и связанного с кровью препарата. Один поперечный срез печени толщиной 2 мм брали из левой боковой доли и сразу погружали в 2 мл буфера RNAlater в микроцентрифужной пробирке. Образцы хранили при 4°С до дальнейшей обработки для выделения РНК.
[00320] 1.6. Анализ РНК
[00321] Оценивали содержание мРНК HSP47 в образцах печени. Тотальную РНК экстрагировали с использованием колонок RNeasy (Qiagen) в соответствии с инструкциями производителя. Концентрацию РНК для каждого образца определяли количественно с использованием спектрофотометра Nanodrop, а затем разбавляли до 10 нг/мл, используя безнуклеазную воду. Для каждой реакции ПЦР использовали 20 нг суммарной РНК. Вкратце, общая РНК из среза левой доли ткани печени будет извлечена с использованием колонок RNeasy (Qiagen) в соответствии с инструкциями производителя. Спектрофотометр Nanodrop использовали для количественного определения РНК. Концентрацию РНК доводили до 10 нг/мкл с помощью безнуклеазной воды. ПЦР в реальном времени проводили в системе ViiA7 в 96-луночном формате. Каждый образец измеряли в трех экземплярах, используя мастер-смесь TaqMan Gene Expression Master Mix. Параметры циклов были установлены следующими: 48°C в течение 15 минут, 95°С в течение 10 минут с последующими 40 циклами при 95°С в течение 15 с и 60°С в течение 1 мин. Среднее значение порогового цикла для гена домашнего хозяйства, MRP119, использовалось для нормализации необработанных данных пороговых циклов и расчета ΔCt. ΔΔCt для каждого представляющего интерес гена (GOI) рассчитывали путем вычитания среднего значения ΔCt для GOI в контрольном образце из ΔCt для каждого GOI в исследуемых образцах. Данные для каждого животного выражали как процент от среднего для группы, получавшей носитель, так и кратное изменение по сравнению с чистой группой. Различия между группами, получавшими киРНК, и группой, получавшей носитель, анализировали с использованием однофакторного анализа ANOVA с последующим апостериорным тестом парных множественных сравнений Даннетта. Для всех анализов значение р менее 0,05 считалось значимым.
[00322] Пример 8: получение наночастиц мРНК. Катионные липиды, такие как HEDC или HE2DC (2-(бис(2-(пальмитоилокси)этил)амино)-N, N-бис(2-гидроксиэтил)-N-метил-2-оксоэтан-1-аминия бромид), ионизируемые липиды, такие как S104 или TU104 Dlin ((9Z, 9'Z,12Z,12'Z)-((2-((2-(диметиламино)этил)тио)ацетил)азандиил)бис(этан-1,2,1-диил)бис(октадека-9,1,2-диеноат)) и вспомогательные липиды, холестерин и DOPE, растворяли в этаноле. мРНК растворяли в 50 мМ цитратном буфере (рН 3,5). Липидные наночастицы (LNP) готовили путем введения соответствующего количества этанольного раствора липидов в цитратный буфер, содержащий мРНК, со скоростью потока 25 мл/мин при 37°C. Молярное процентное отношение для композиции LNP составляло 20% HEDC, 20% S104, 30% DOPE (1,2-диолеоил-sn-глицеро-3-фосфоэтаноламина) (Avanti Polar Lipid), 25% холестерина (категории Puriss) (Wilshire Technologies), 5% DMPE-PEG (1,2-димиристоил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000] (аммониевая соль) и 2% фузогенной молекулы по настоящему изобретению, например, соединения Т3.
[00323] Высокая скорость введения приводила к высокой степени инкапсуляции мРНК, а также к контролируемому распределению размеров частиц. Смешанный раствор LNP затем разбавляли до 20 мМ HEPES-буфером в 9%-й сахарозе (вес/объем) в соотношении 1:1, что уменьшало содержание этанола в растворе LNP с 35% до 17,5%. Разбавленный раствор LNP подвергали фильтрации с тангенциальным потоком (TFF) для ультрафильтрации и диафильтрации с 20 мМ HEPES-буфером в 9%-й сахарозе (вес/объем). Для удаления этанола из раствора LNP использовали всего 10 объемов диафильтрационного буфера HEPES в 9%-й сахарозе. Концентрированный раствор LNP после TFF разделяли по порции в центрифужные пробирки с фильтром (EMD Millipore) для дальнейшей концентрации, однако этот этап требовался только для небольших партий. После конечной концентрации LNP фильтровали через фильтры с размером пор 0,2 мкм. Эффективность инкапсуляции и выход мРНК вычисляли с использованием красителя RiboGreen.
[00324] Пример 9: трансфекционная доставка мРНК в клетки in vitro. Трансфекцию клеток in vitro молекулами мРНК проводили в трех разных клеточных линиях: Hek-293, A549 и линии клеток легочных фибробластов. JET MESSENGER (Polyplus Transfection Company) использовали в качестве положительного контроля трансфекции. мРНК GFP (TriLink), которая была инкапсулирована в наночастицы LNP по настоящему изобретению или смешана с контрольным трансфекционным агентом JET MESSENGER, использовали для трансфекции клеток в различных концентрациях. Через 24, 48 и 72 часа после трансфекции клетки наблюдали под конфокальным микроскопом, а затем детектировали и фиксировали флуоресценцию, генерируемую экспрессированным GFP в клетках. мРНК GFP хорошо трансфицировалась во все три линии клеток с помощью наночастиц LNP по настоящему изобретению, и происходила трансляция мРНК.
[00325] Пример 10: трансфекционная доставка мРНК в клетки in vivo. мРНК трансфицировали в ткани и клетки in vivo с помощью наночастиц LNP по настоящему изобретению. Осуществляли доставку и трансфекцию мышам Balb/c двух разных мРНК, имеющих разные размеры, мРНК GFP и мРНК люциферазы (TriLink). В некоторых исследованиях доставки мРНК люциферазы, в качестве положительного контроля доставку мРНК также осуществляли с использованием реагента для трансфекции мРНК in vivo, Viromer. Животным вводили внутривенно с помощью одной инъекции мРНК, инкапсулированную в наночастицах LNP по настоящему изобретению или в частицах положительного контроля, в дозировке 1,0, 2,0 или 4,0 мг/кг. Мышей анестезировали через 6-8 часов после инъекции мРНК, и для исследований доставки мРНК люциферазы флуоресценцию всего тела детектировали и анализировали с помощью системы IVIS. Животных немедленно умерщвляли, и различные органы извлекали и сохраняли при -80°С до дальнейшего анализа. Доставку мРНК в различные ткани и клетки определяли с помощью набора MAXDISCOVER GFP ELISA для анализа уровня белка GFP в тканях из исследований по доставке мРНК GFP. Для исследований доставки мРНК люциферазы, ткани гомогенизировали в лизирующем буфере CCLR и центрифугировали. Полученные супернатанты использовали для анализа активности люциферазы с использованием реагентов из набора Promega E4510. Удивительно, но трансфекция и/или трансляции как мРНК GFP, так и мРНК люциферазы, преимущественно наблюдались в легких и селезенке со значительно меньшей трансфекцией и/или трансляцией в других тканях.
[00326] Пример 11: трансфекционная доставка мРНК в клетки in vitro.
В соответствии со способом, описанным в примерах 9 и 10 выше, мРНК GFP (CleanCap EGFP мРНК, 5 moU) трансфицировали в клетки A549 in vitro с использованием наночастиц LNP по настоящему изобретению, имеющих состав HEDC:S104:CH:DOPE:DMPE-PEG2000:соединение T3. Результаты после 48 часов трансфекции показаны на фиг.48. Клетки наблюдали под конфокальным микроскопом и детектировали флуоресценцию, генерируемую в результате экспрессии GFP в клетках. Результаты показали, что мРНК GFP трансфицировалась и транслировалась в клетках A549.
[00327] Пример 12: трансфекционная доставка мРНК в клетки in vivo.
В соответствии со способом, описанным в примерах 9 и 10 выше, мРНК GFP (CleanCap EGFP мРНК, 5 moU) трансфицировали мышам Balb/c в наночастицах LNP по настоящему изобретению, имеющими состав HEDC:S104:CH:DOPE:DMPE-PEG2000:соединение T3, как показано в таблице 9:
Таблица 9: трансфекция in vivo у мышей Balb/c
[00328] Как показано на фиг.49, доставку мРНК в различные ткани и клетки определяли с помощью набора MAXDISCOVER GFP ELISA. Удивительно, но мРНК GFP селективно трансфицировалась и/или транслировалась в легких, с более низкой трансфекцией и/или трансляцией в мышцах, печени, сердце и почках.
[00329] Пример 13: трансфекционная доставка мРНК в клетки in vivo.
В соответствии со способом, описанным в примерах 9 и 10 выше, мРНК люциферазы (мРНК Fluc (5meC)) трансфицировали мышам Balb/c с помощью наночастиц LNP по настоящему изобретению, имеющих состав HEDC:S104:CH:DOPE:DMPE-PEG2000:соединение Т3, как показано в таблице 10:
Таблица 10: трансфекция in vivo у мышей Balb/c
[00330] Как показано на фиг.50, относительную доставку, трансфекцию и/или трансляцию мРНК в различные ткани и клетки определяли с помощью аналитического набора Promega E4510. Удивительно, но мРНК Fluc (люциферазы светлячка) избирательно доставлялась, трансфицировалась и/или транслировалась в легких и селезенке, с более низкой доставкой, трансфекцией и/или трансляцией в печени, сердце, почках и мышцах.
[00331] Пример 14: трансфекционная доставка мРНК в клетки in vivo.
В соответствии со способом, описанным в примерах 9 и 10 выше, мРНК люциферазы (мРНК Fluc (5meC)) трансфицировали мышам Balb/c с помощью наночастиц LNP по настоящему изобретению, имеющих композицию:
(-01) HE2DC:S104:CH:DOPE:DMPE-PEG2000:соединение T3 или
(-02) HEDC:S104:CH:DOPE:DMPE-PEG2000:соединение T3,
которые вводили с помощью инъекций в количестве 2 мг/кг, с люминесцентной визуализацией через 7 часов после инъекции.
[00332] Как показано на фиг.51, относительную доставку, трансфекцию и/или трансляцию мРНК в различные ткани и клетки определяли с помощью набора Promega E4510. Удивительно, но мРНК Fluc избирательно доставлялась, трансфицировалась и/или транслировалась в легких и селезенке, с более низкой доставкой, трансфекцией и/или трансляцией в поджелудочной железе, почках, печени, яичках и тонкой кишке.
[00333] Как показано на фиг.52, относительную доставку, трансфекцию и/или трансляцию мРНК в различных тканях определяли с помощью визуализации люминесцентного свечения через 7 часов после инъекции. На фиг.52, на фотографиях в верхнем ряду показаны мыши Balb/c, трансфицированных наночастицами LNP (-01). На фотографиях в нижнем ряду показаны мыши Balb/c, трансфицированные наночастицами LNP (-02).
[00334] Пример 15: доставка мРНК в клетки in vivo с использованием фузогенных соединений. Фузогенные соединения по настоящему изобретению значительно усиливают доставку действующих агентов в клетки, органы и ткани in vivo.
[00335] В этом примере препараты для доставки мРНК in vivo приготавливали с фузогенным соединением Т3 и сравнивали с таким же препаратом без фузогенного соединения, как показано в таблице 11.
Таблица 11: составы для доставки препаратов in vivo мышам
[00336] На фиг.53 показаны результаты доставки мРНК люциферазы мышам in vivo с использованием фузогенных липидоподобных молекул по настоящему изобретению. Как показано на фиг.53, относительная доставка мРНК была намного выше в составах, содержащих фузогенную молекулу по настоящему изобретению (2035-03-03), чем в таком же составе без фузогенной молекулы (2035-13-01). Во всех наблюдаемых органах, включая поджелудочную железу, селезенку, печень, почку, легкие, яички и кишечник, доставка была предпочтительно и неожиданно выше для состава, содержащего фузогенное соединение Т3.
[00337] Варианты осуществления, описанные в данном документе, не являются ограничивающими, и специалист в данной области может легко оценить, что конкретные комбинации модификаций, описанных в данном документе, могут быть протестированы без чрезмерных экспериментов по идентификации молекул нуклеиновых кислот с улучшенной активностью РНК-интерференции.
[00338] Все публикации, патенты и литературные источники, конкретно указанные в данном документе, полностью включены путем ссылки для любых целей.
[00339] Понятно, что данное изобретение не ограничено конкретной описанной методологией, протоколами, материалами и реагентами, поскольку они могут варьировать. Также следует понимать, что используемая в настоящем документе терминология предназначена только для описания конкретных вариантов осуществления изобретения и не предназначена для ограничения объема настоящего изобретения. Специалисту в данной области техники будет очевидно, что могут быть осуществлены различные замены и модификации в описании, раскрытом в данном документе, без отступления от объема и сущности описания, и что эти варианты осуществления находятся в пределах объема данного описания и прилагаемой формулы изобретения.
[00340] Следует отметить, что используемые в настоящем документе и в прилагаемой формуле изобретения формы единственного числа включают в себя множественное число, если только контекст явно не предписывает иное. Также термины в единственном числе, «один или несколько» и «по меньшей мере один» могут использоваться в настоящем документе взаимозаменяемо. Также следует отметить, что термины «содержат», «содержащий», «включающий», «включающий в себя» и «имеющий» могут использоваться взаимозаменяемо и должны истолковываться в широком объеме и без ограничений.
[00341] Указание диапазонов значений в данном документе предназначено просто для того, чтобы служить кратким способом индивидуальной ссылки на каждое отдельное значение, попадающее в диапазон, если в настоящем документе не указано иное, и каждое отдельное значение включается в описание, как если бы оно было индивидуально указано в данном описании. Для групп Маркуша специалисты в данной области техники должны понимать, что это описание включает отдельные члены, а также подгруппы членов группы Маркуша.
[00342] Соединение, молекула или композиция по настоящему изобретению могут иметь ионную форму, для которой соответствующий противоион или противоионы не показаны. Специалист в данной области техники сразу поймет, что противоион или противоионы будут присутствовать по мере необходимости. Примеры противоионов включают ионы щелочных металлов, Cl- и фармацевтически приемлемые противоионы.
[00343] Например, когда приведен список примеров или компонентов, таких как список соединений, молекул или композиций, подходящих для данного изобретения, специалистам в данной области техники будет очевидно, что также могут быть подходящими смеси перечисленных соединений, молекул или композиций.
[00344] Без дальнейшего уточнения считается, что специалист в данной области техники может на основании приведенного выше описания использовать настоящее изобретение в его наиболее полной степени. Следовательно, нижеследующие конкретные варианты осуществления следует истолковывать просто как иллюстративные и никоим образом не ограничивающие остальную часть раскрытия.
[00345] Все признаки, раскрытые в этом описании, могут быть объединены в любой комбинации. Каждый признак, раскрытый в этом описании, может быть заменен альтернативным признаком, служащим такой же, эквивалентной или аналогичной цели.
[00346] Чертежи в прилагаемой формуле изобретения приведены таким образом, чтобы они соответствовали размеру страницы, и появление молекул на чертежах не обязательно отражает какую-либо существенные форму или свойства изображенного соединения.
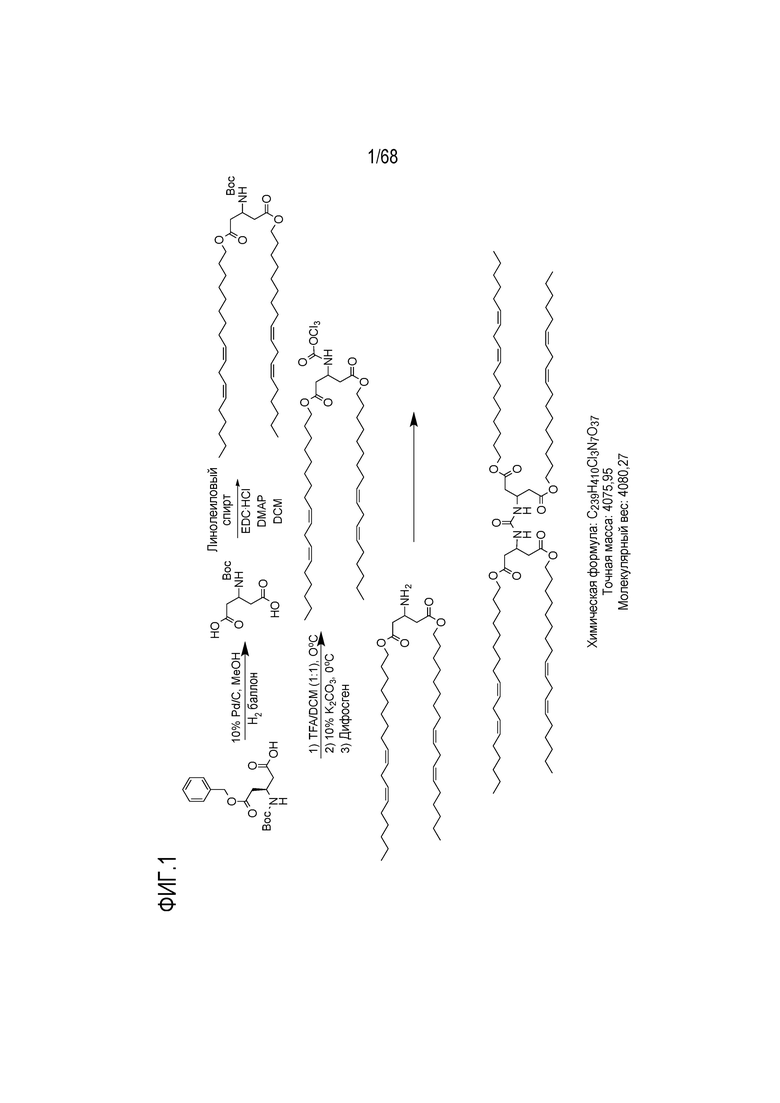
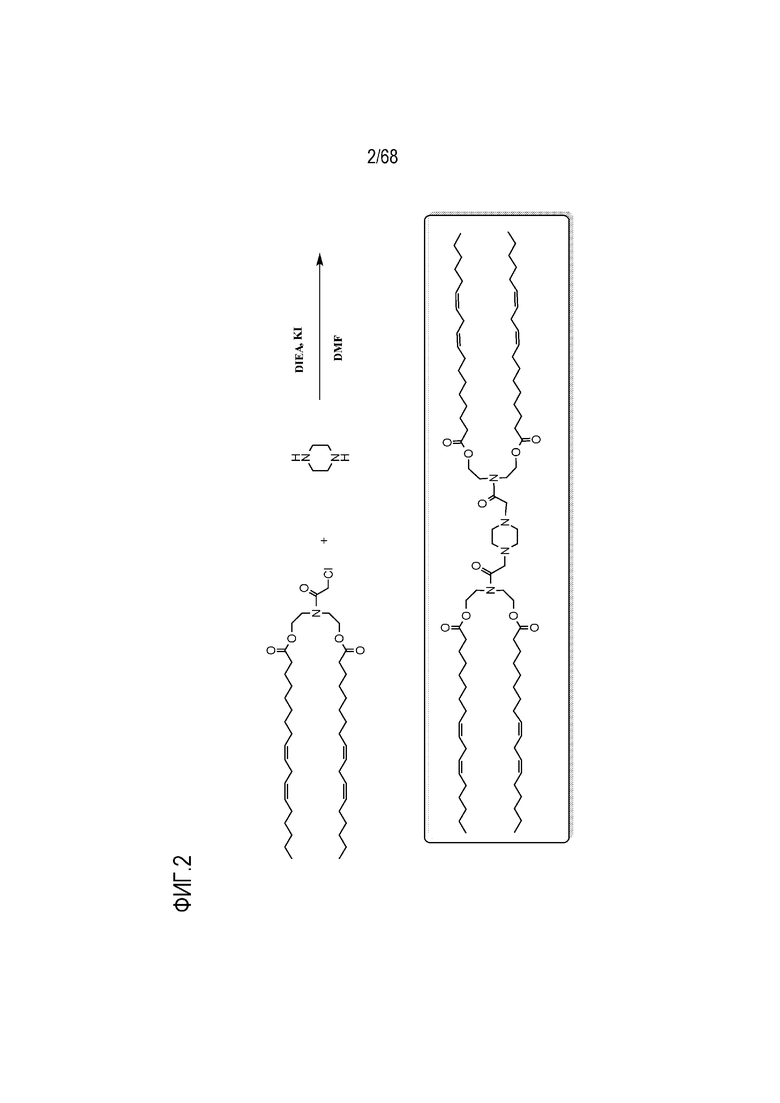
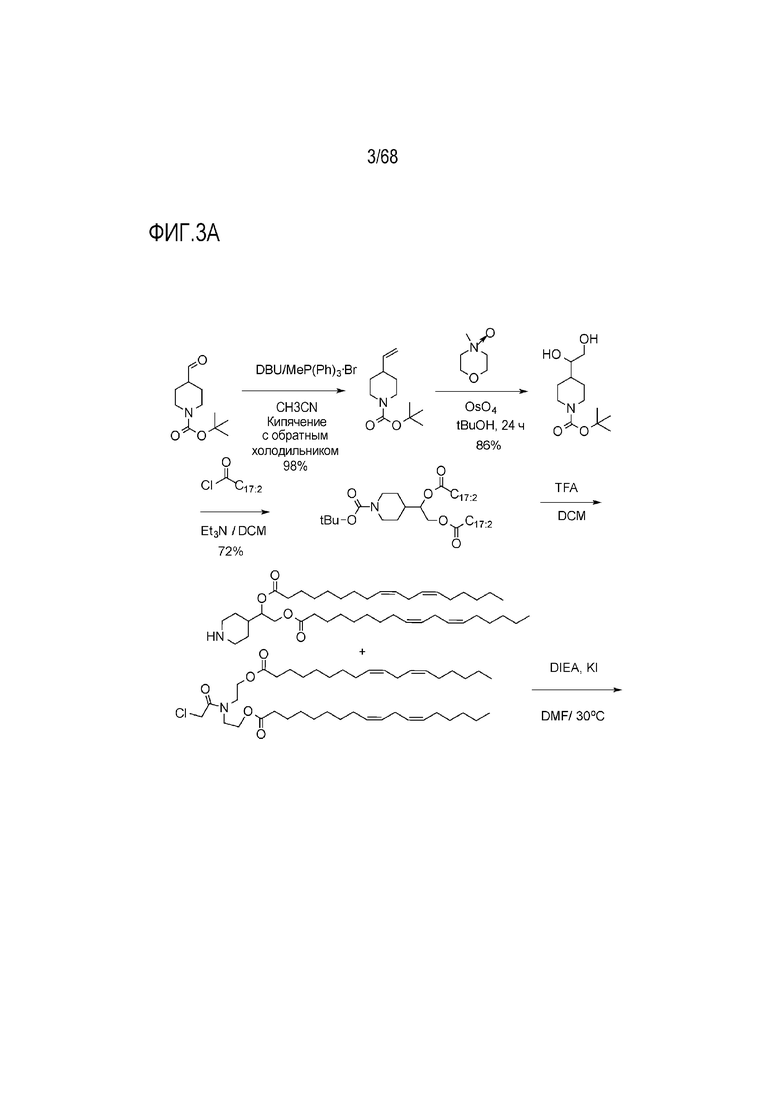

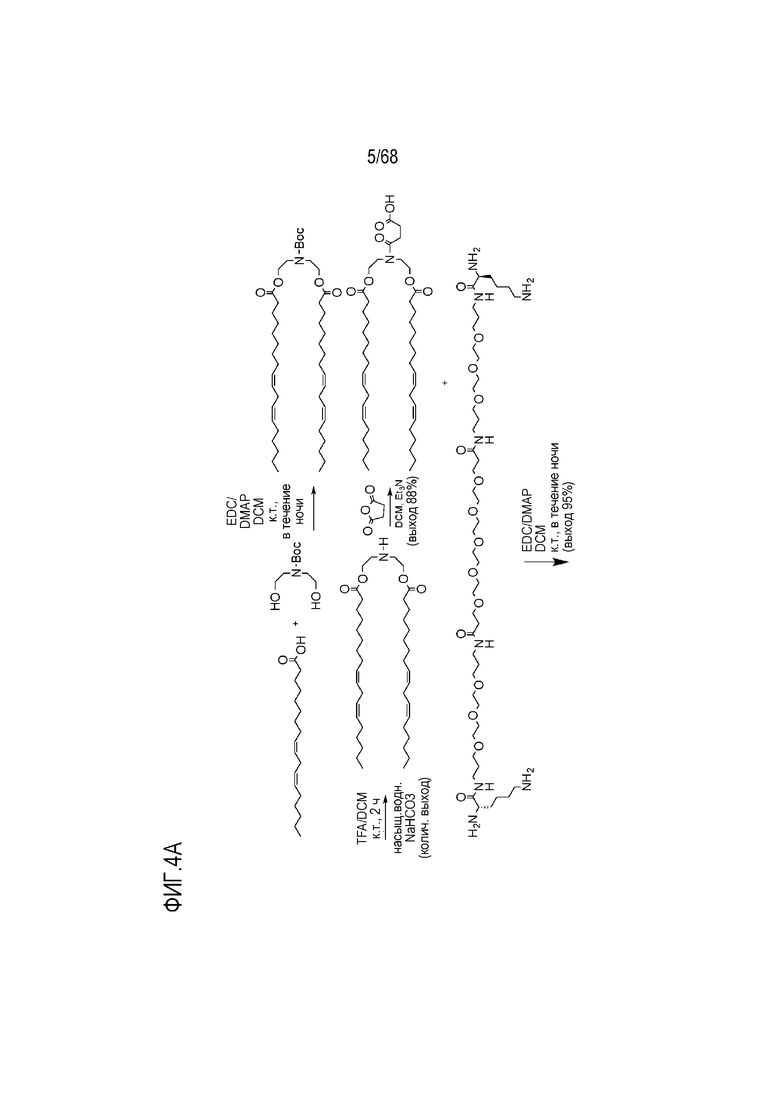

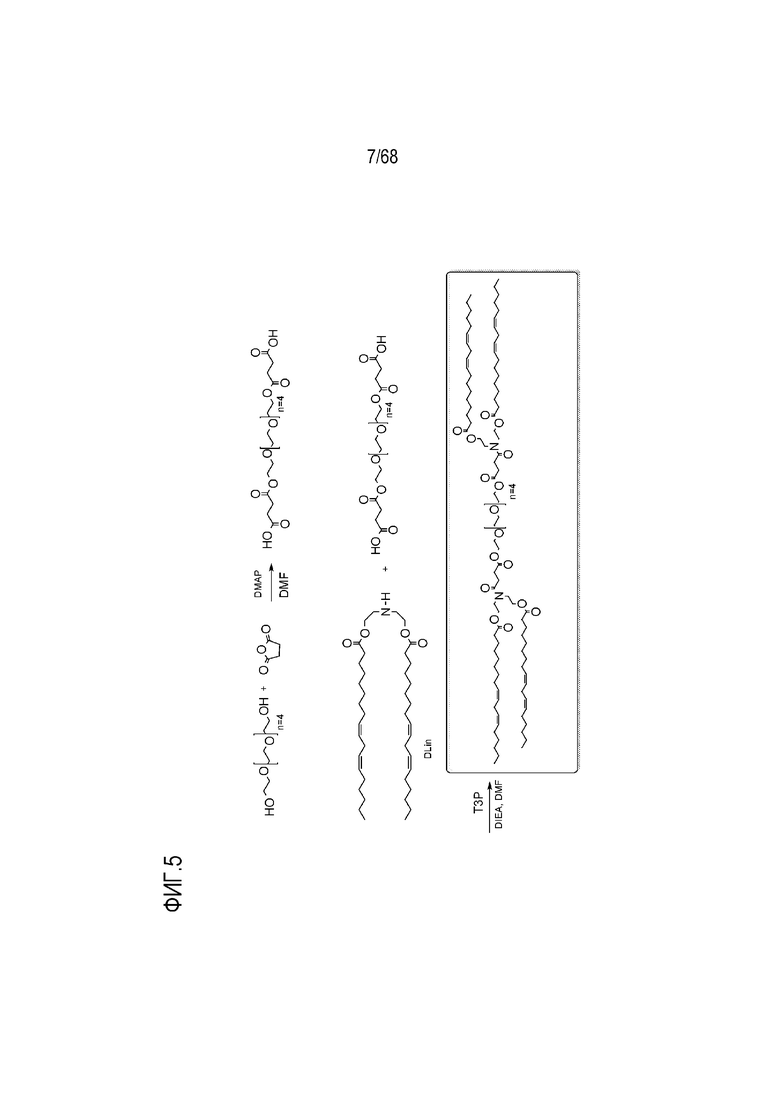
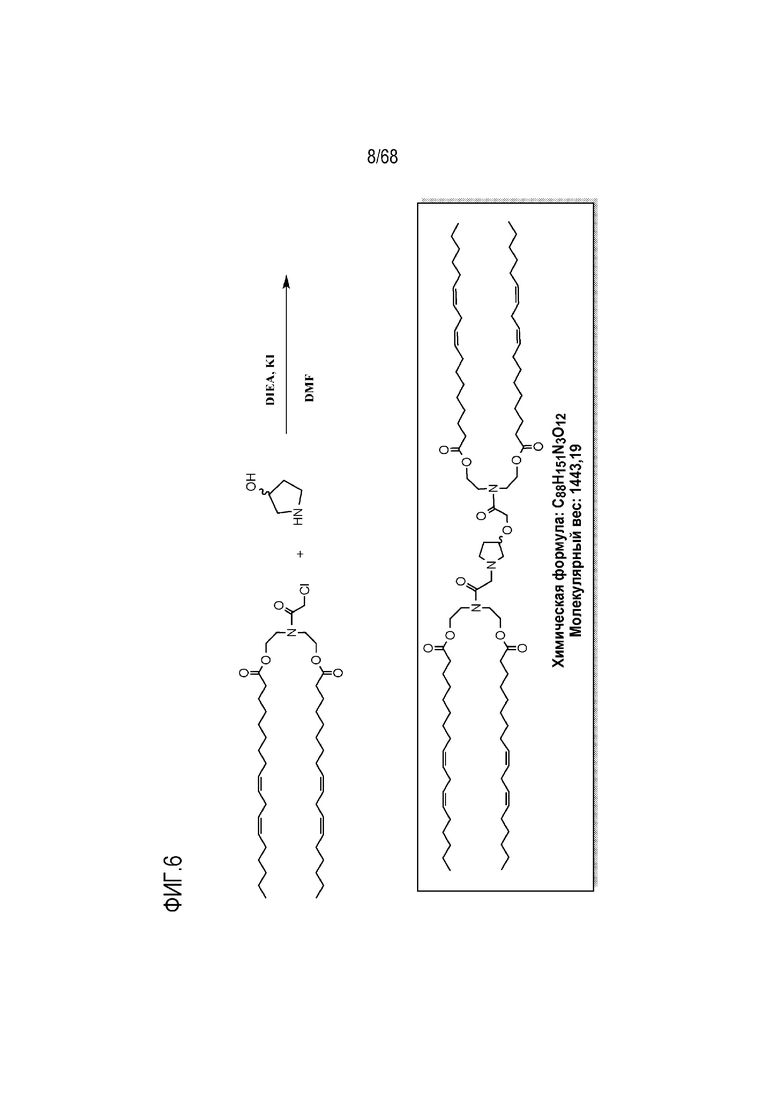
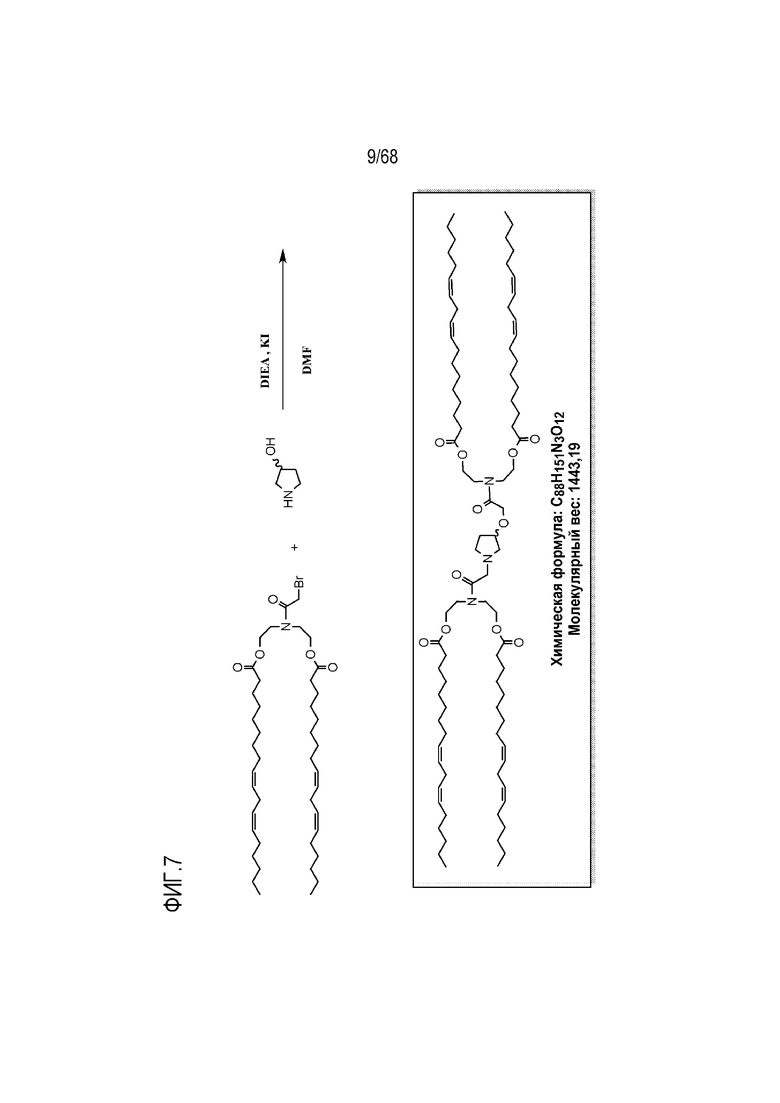
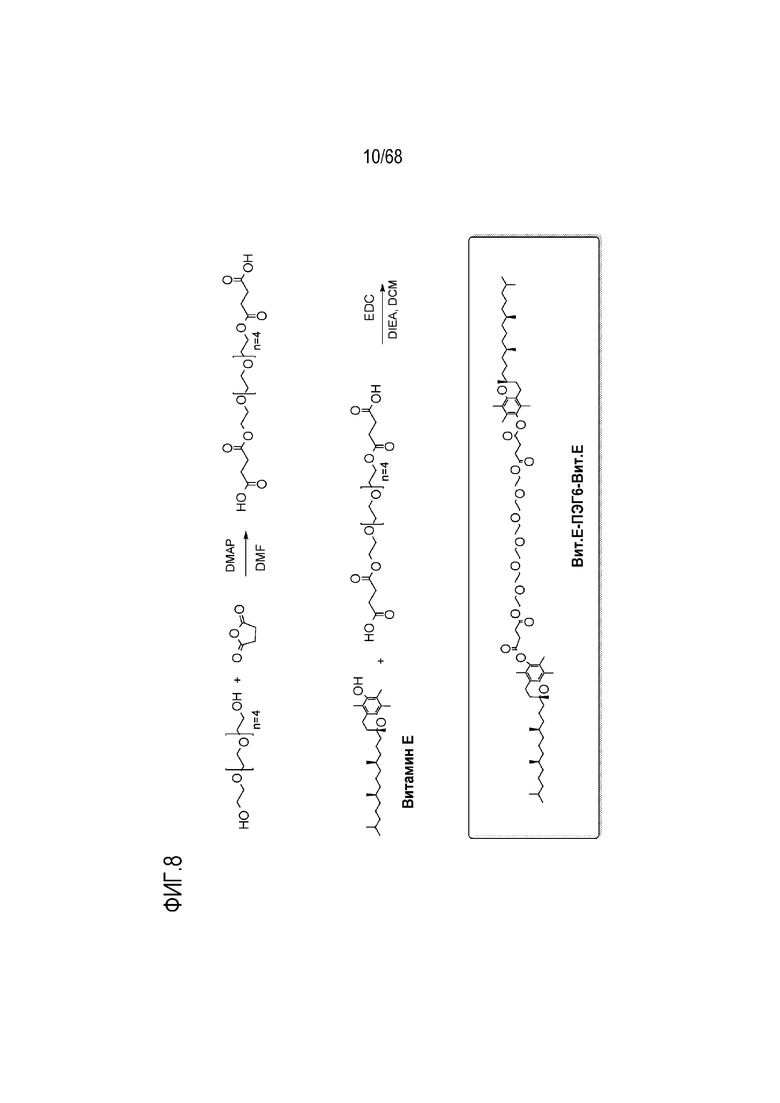
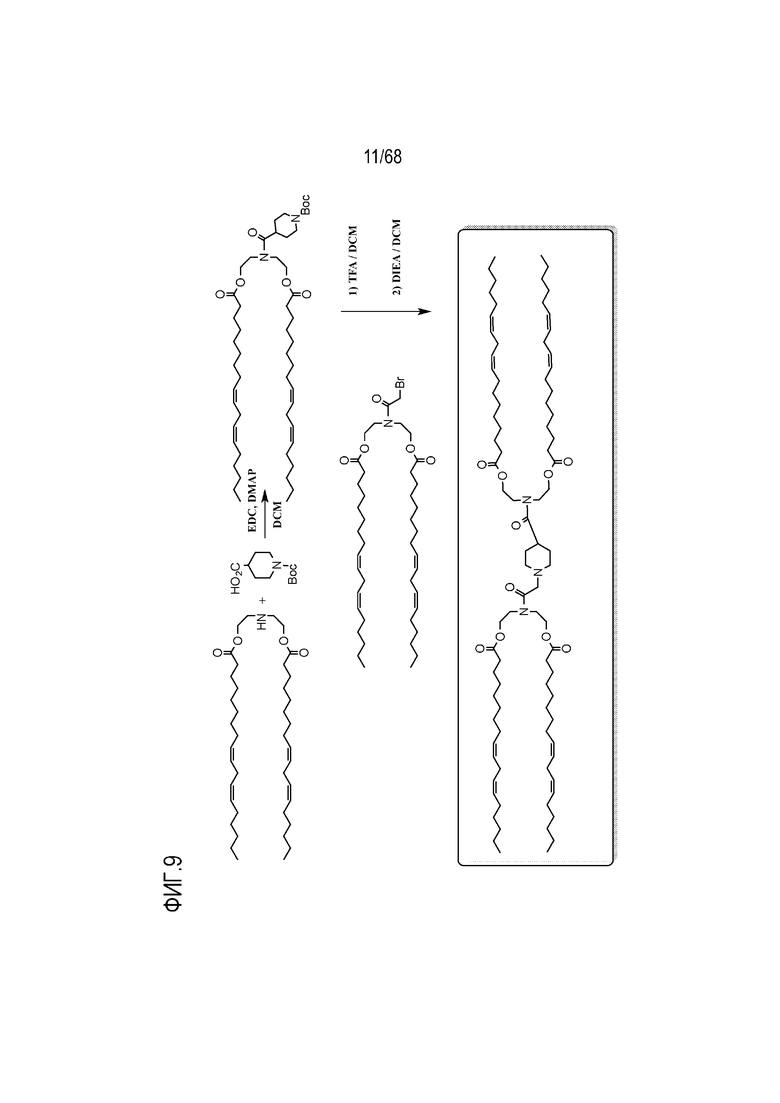


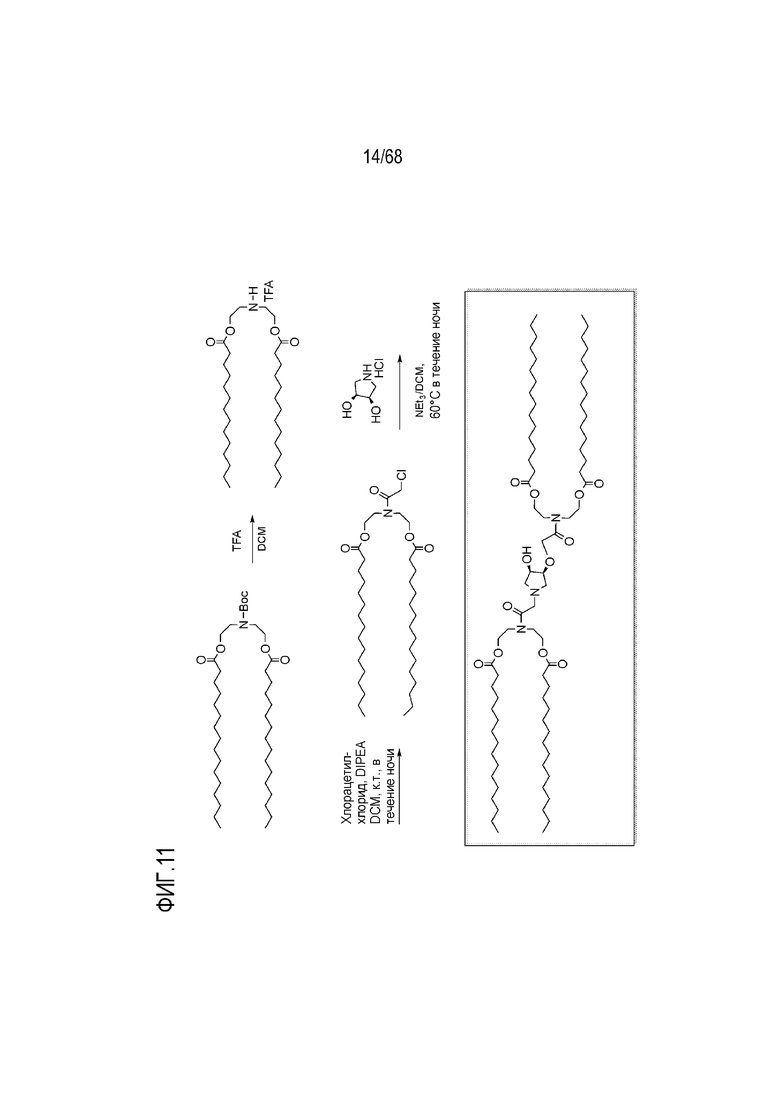

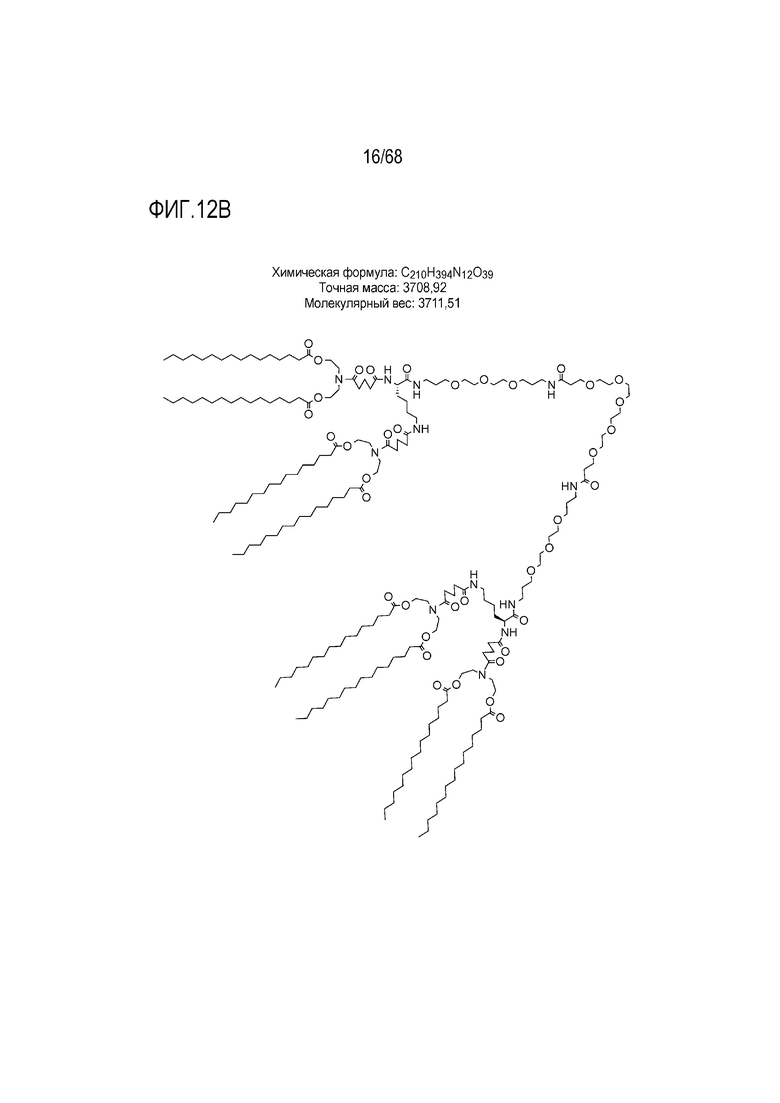
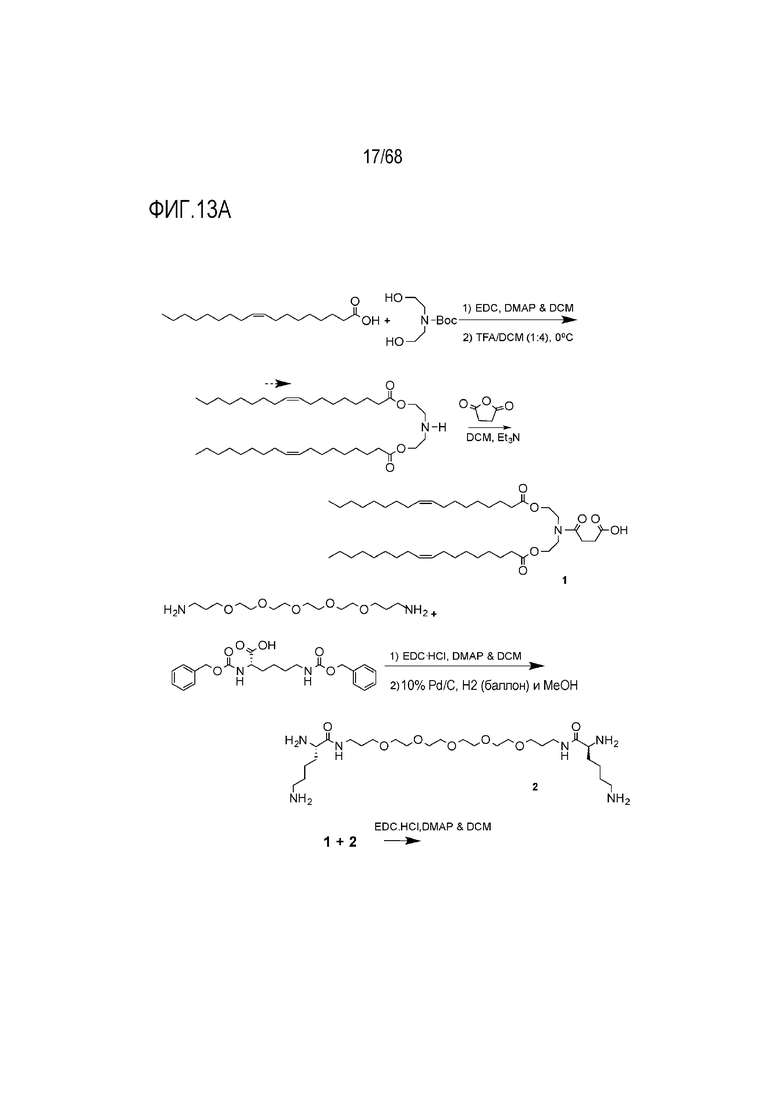
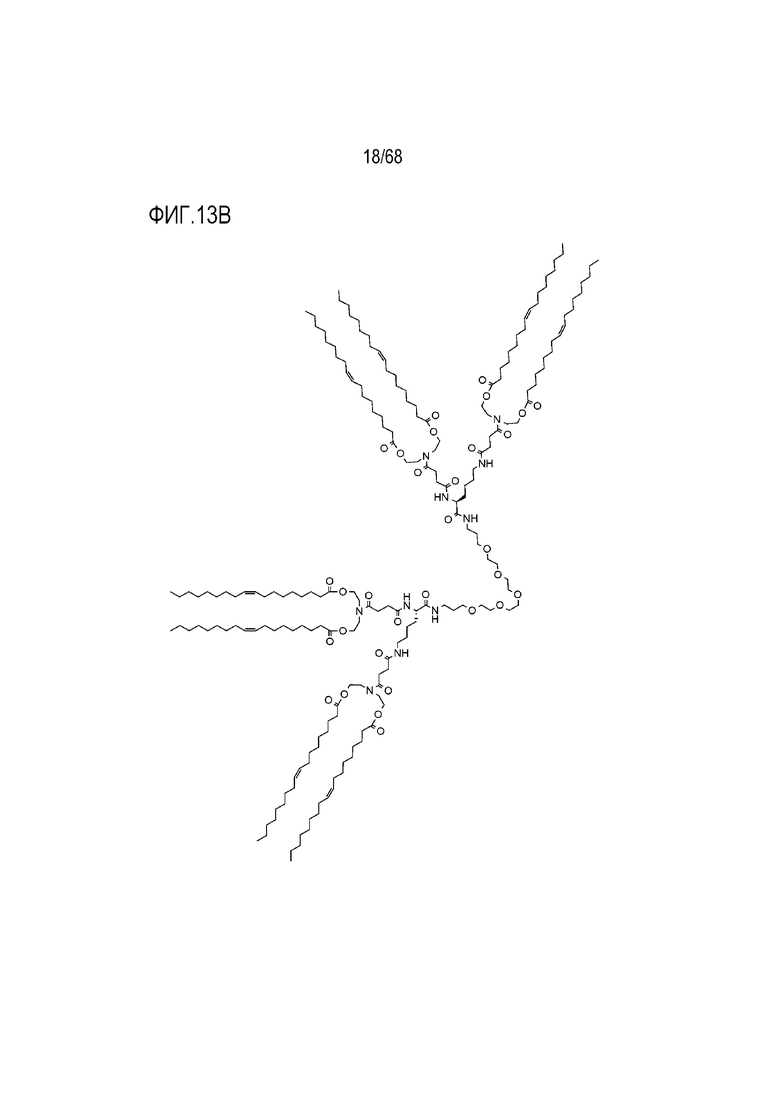
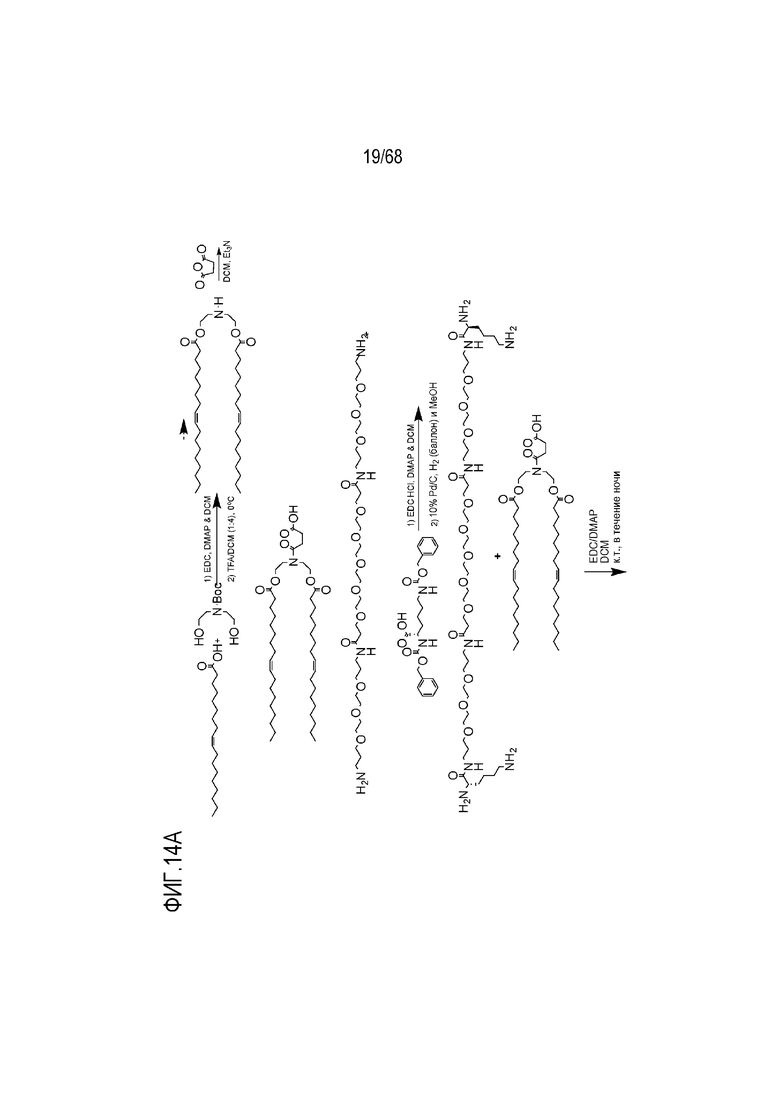
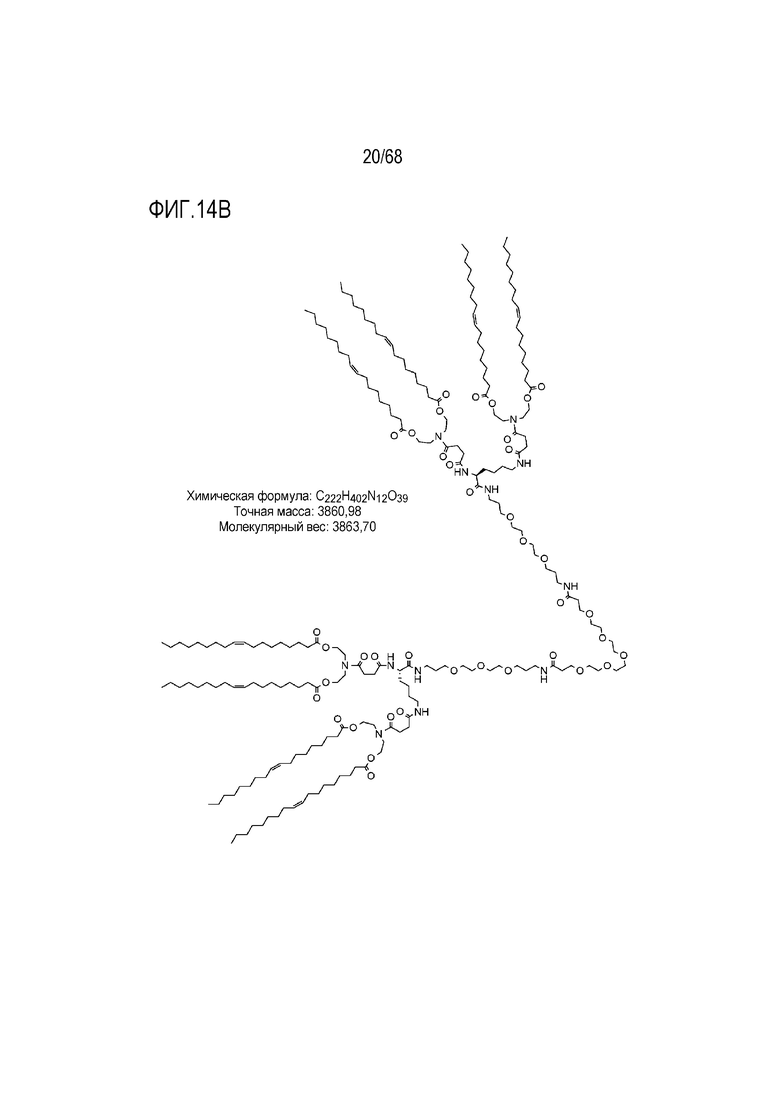
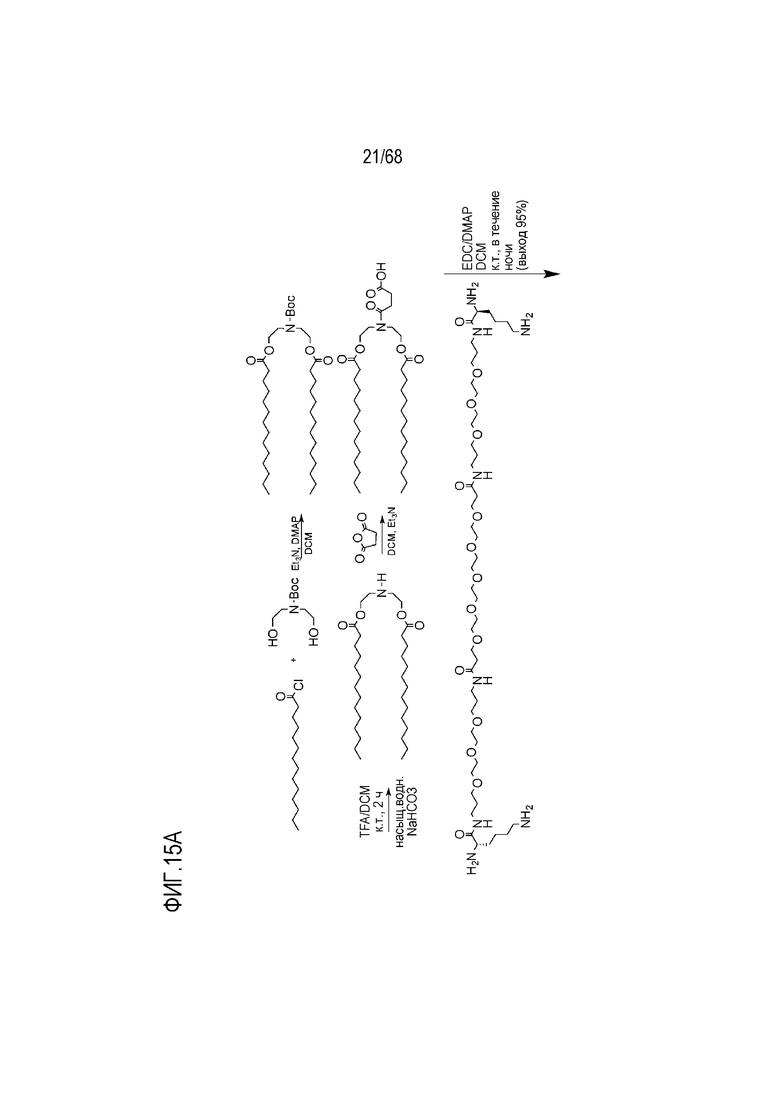
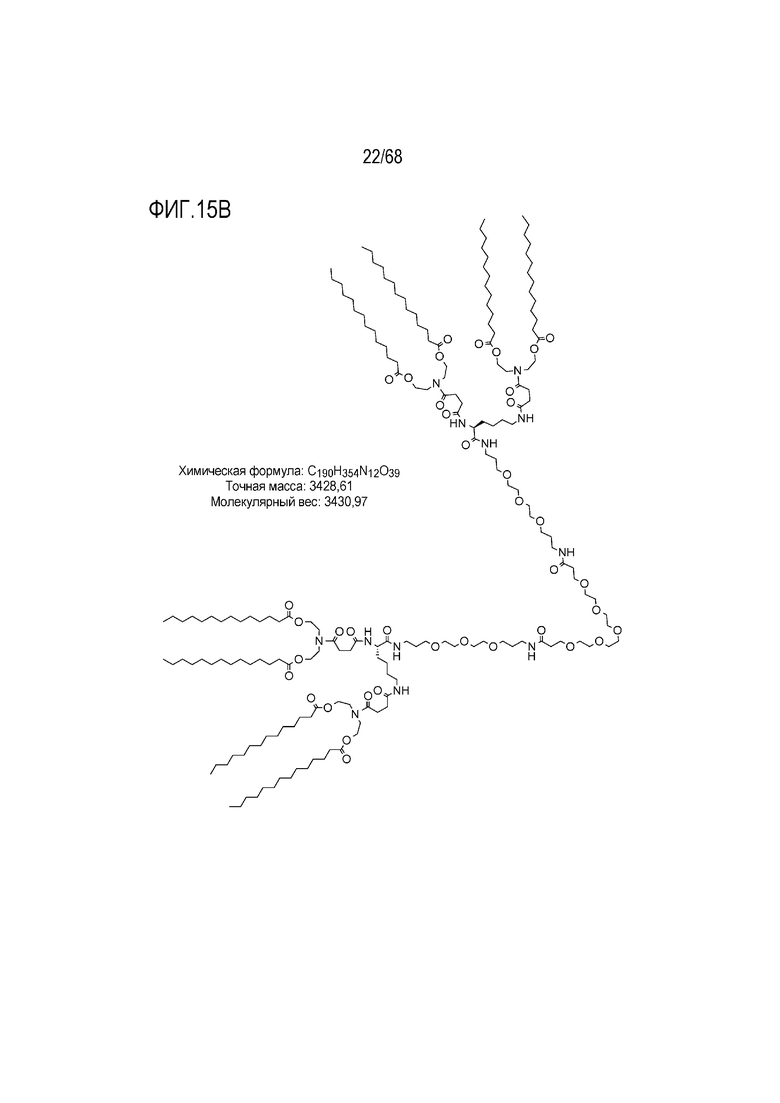
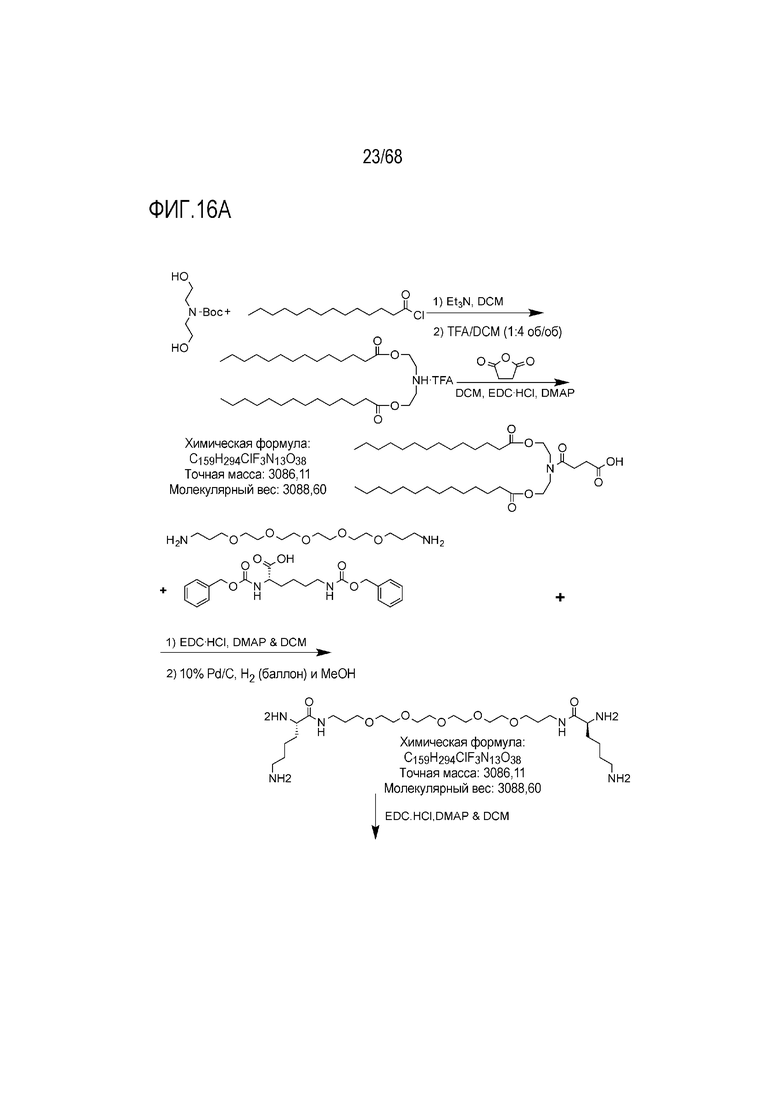
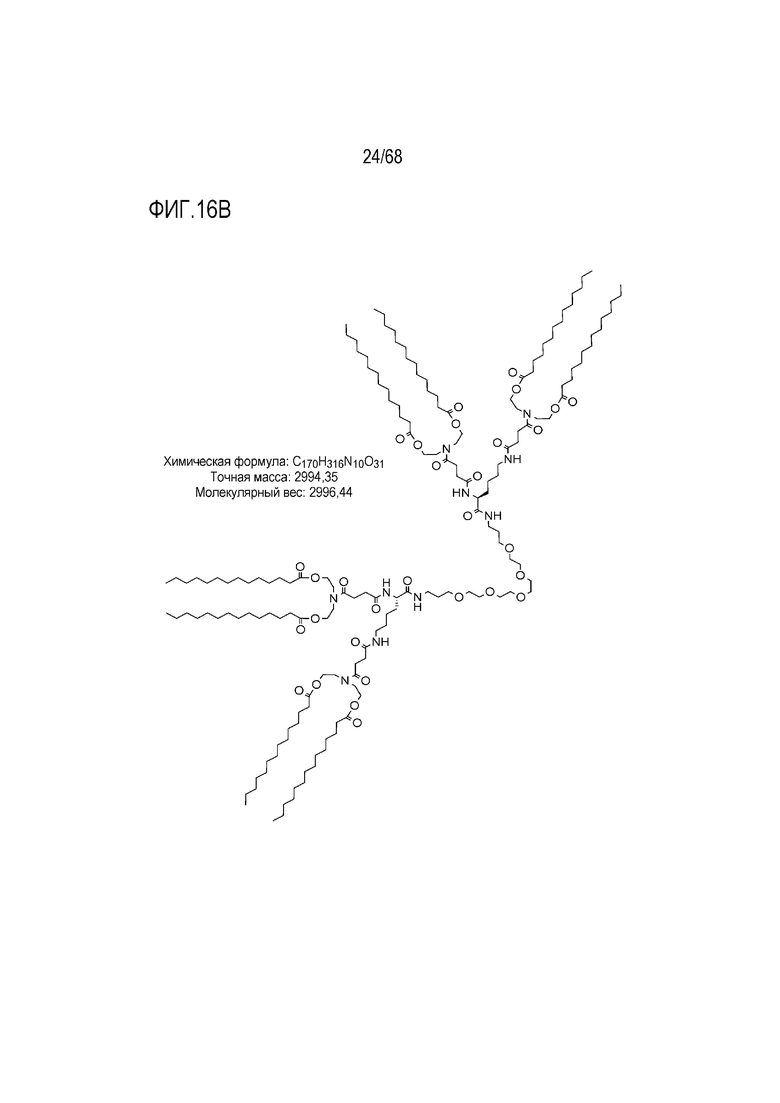
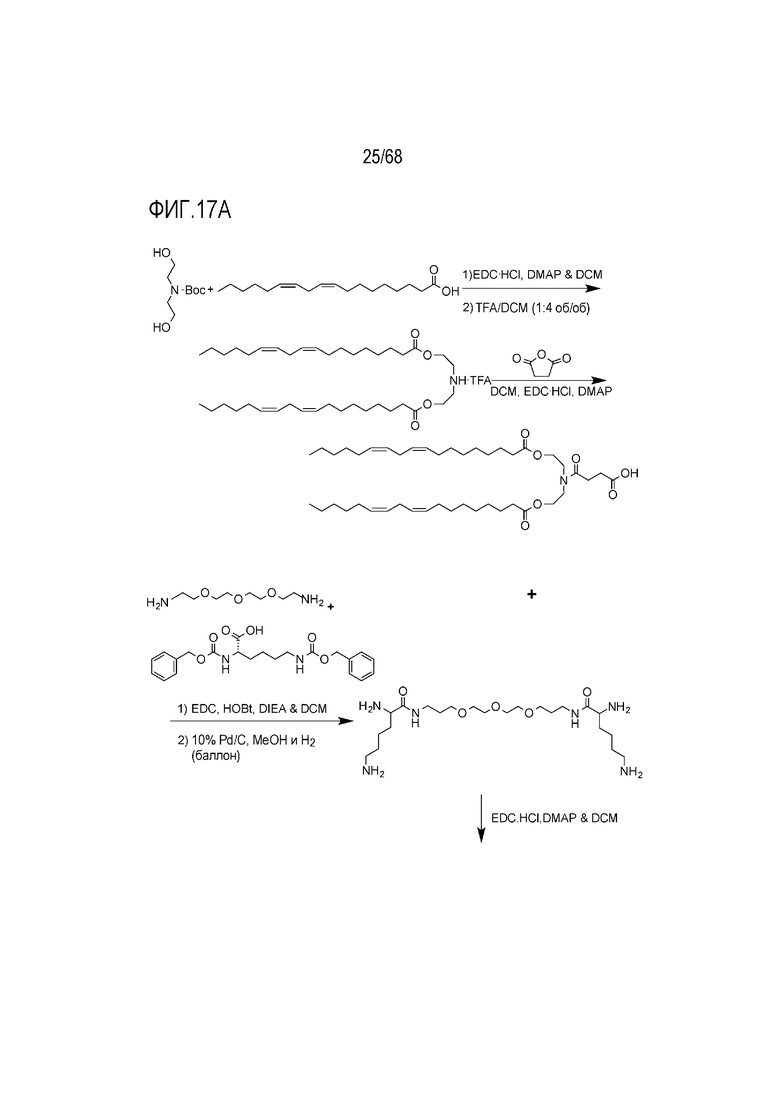
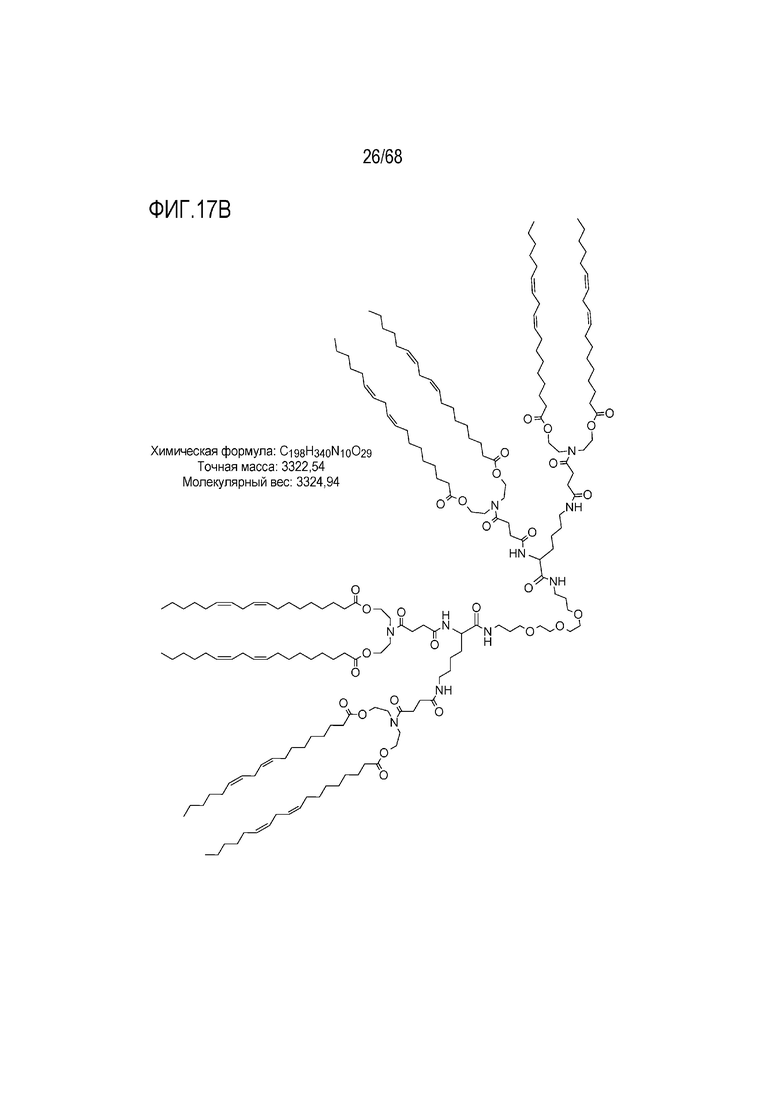
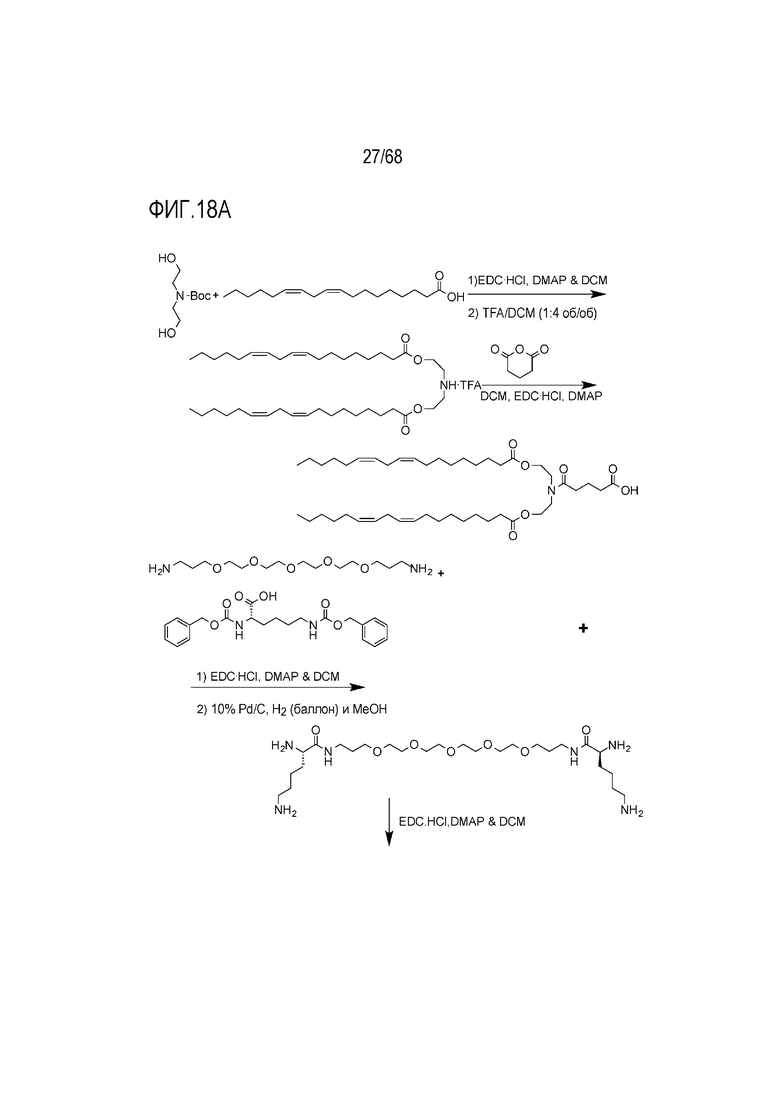
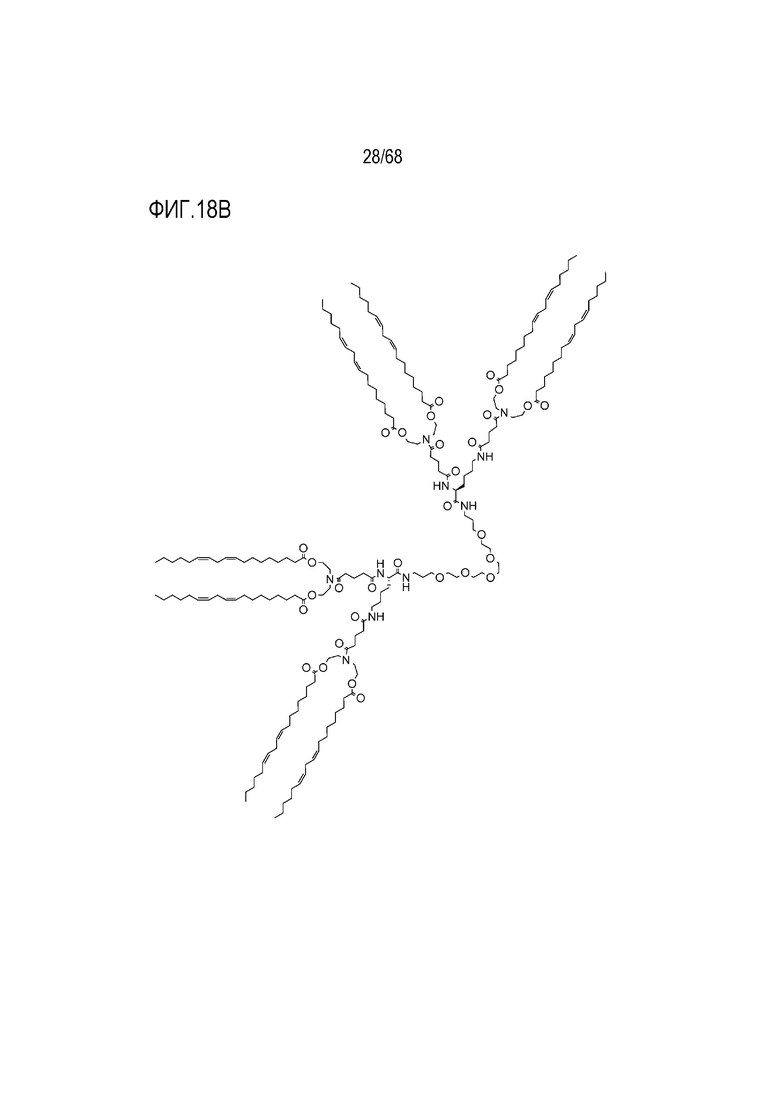
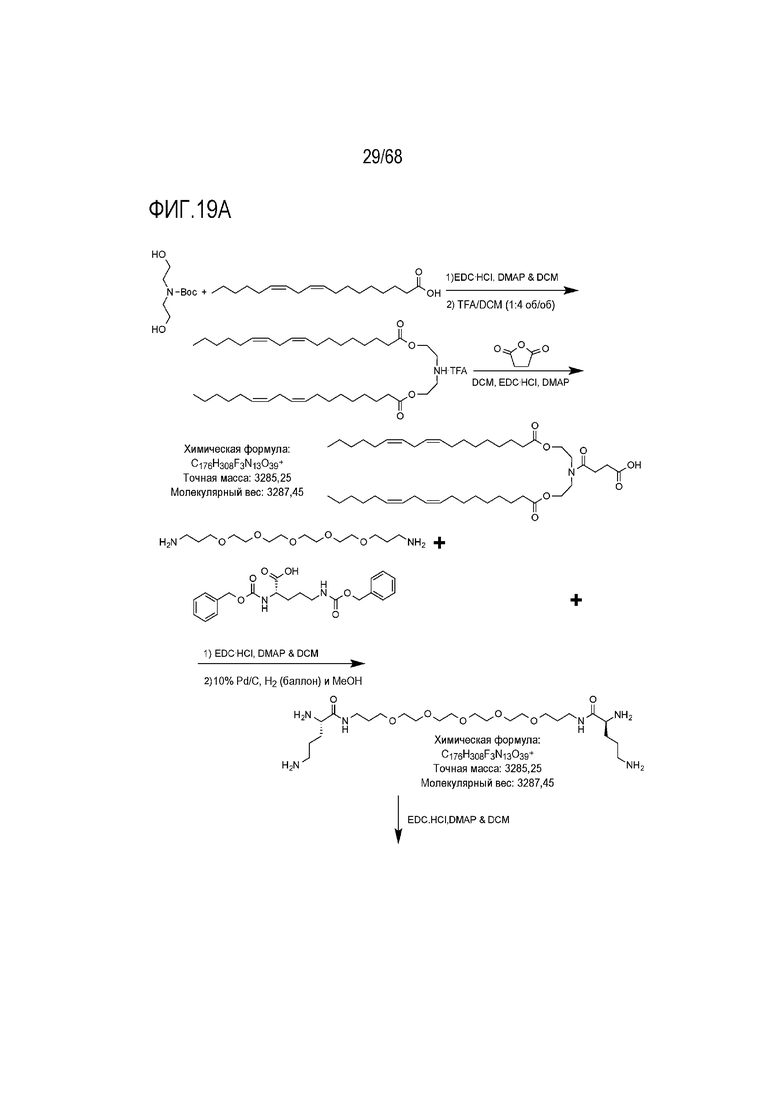

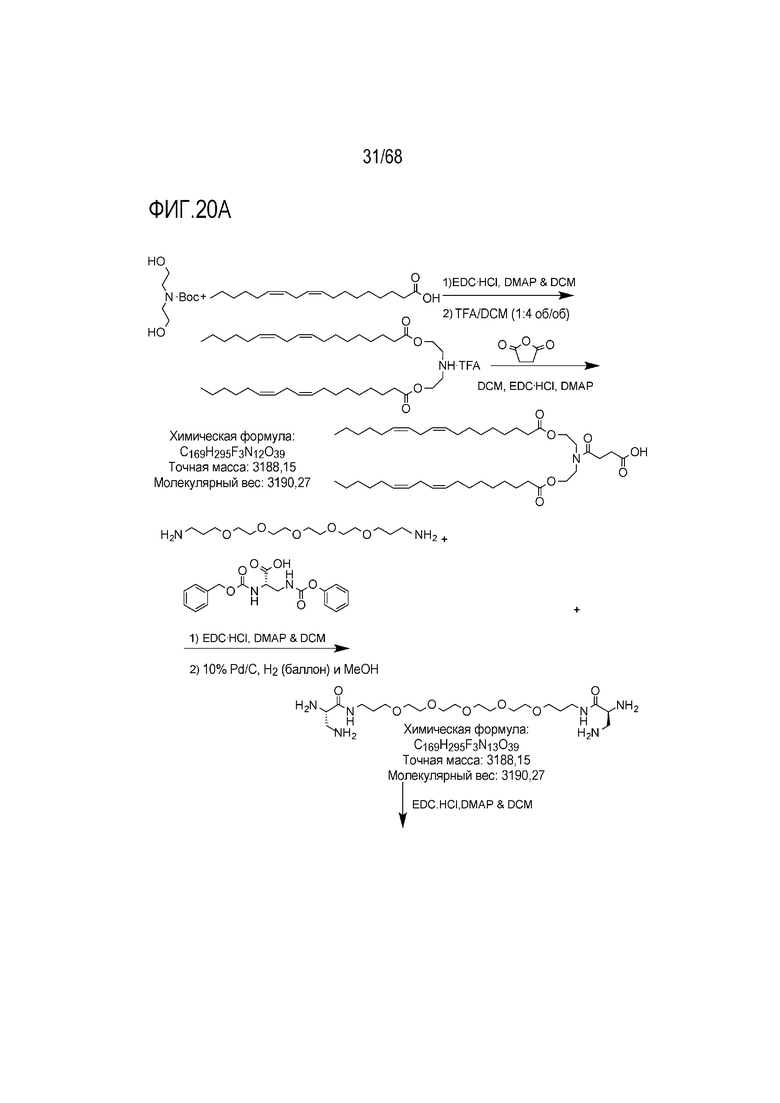
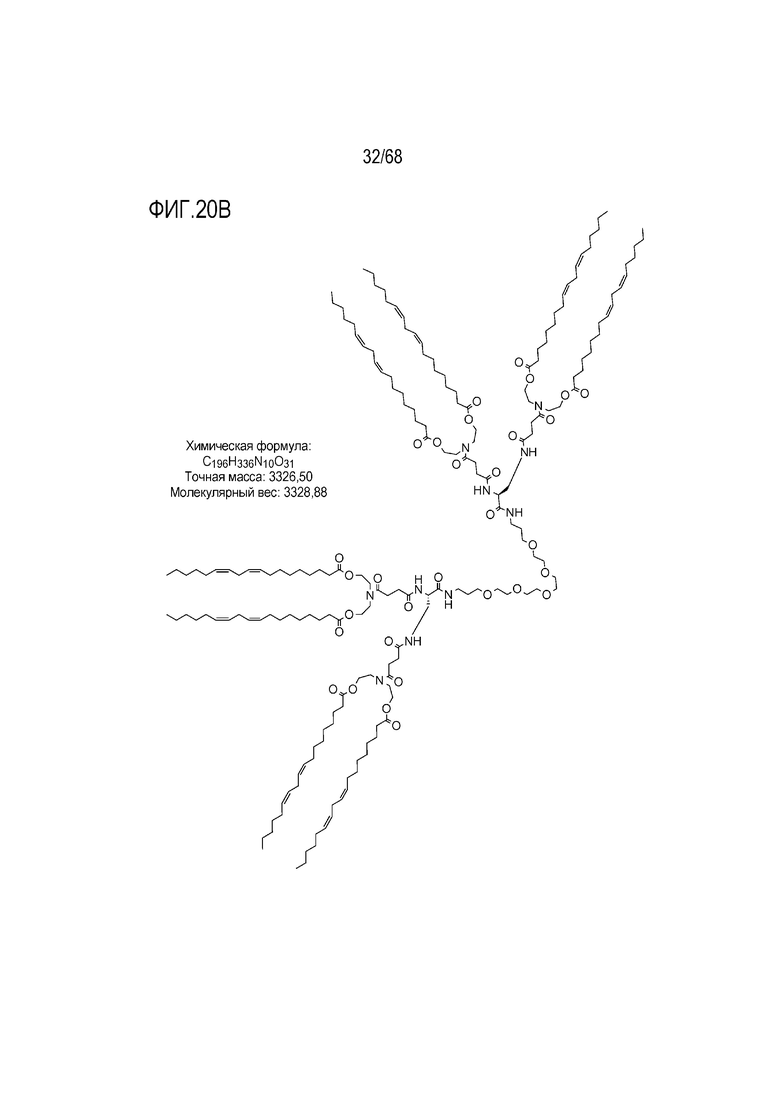
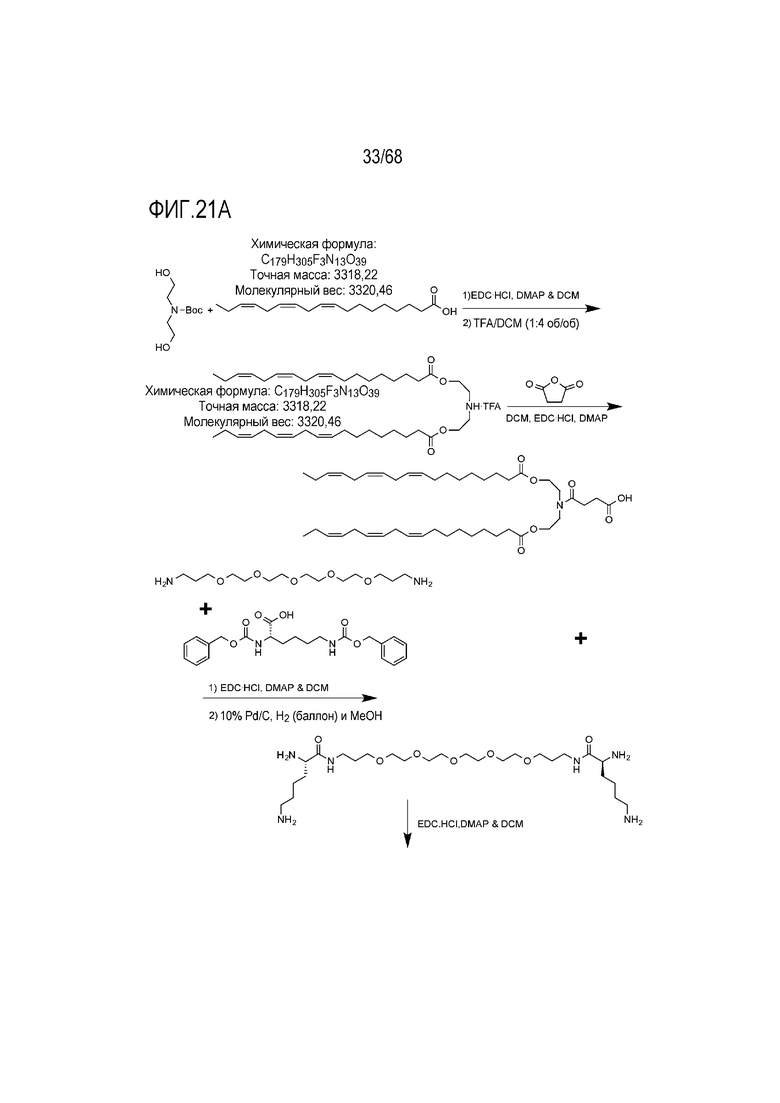
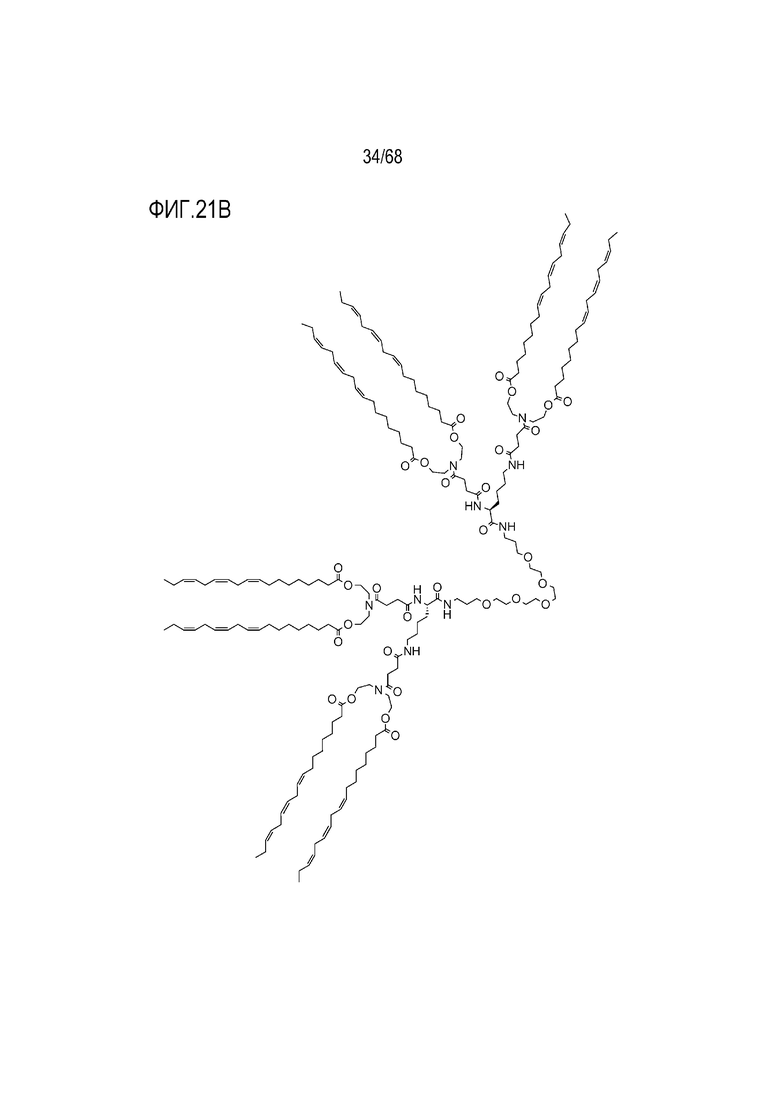

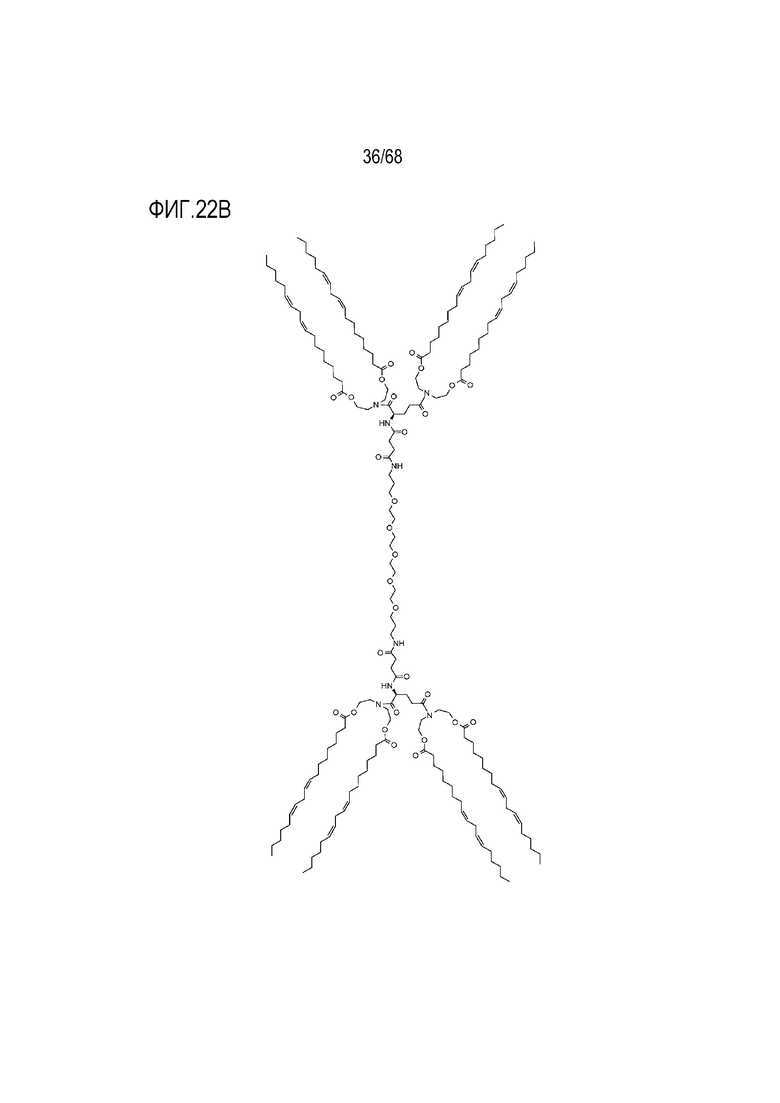
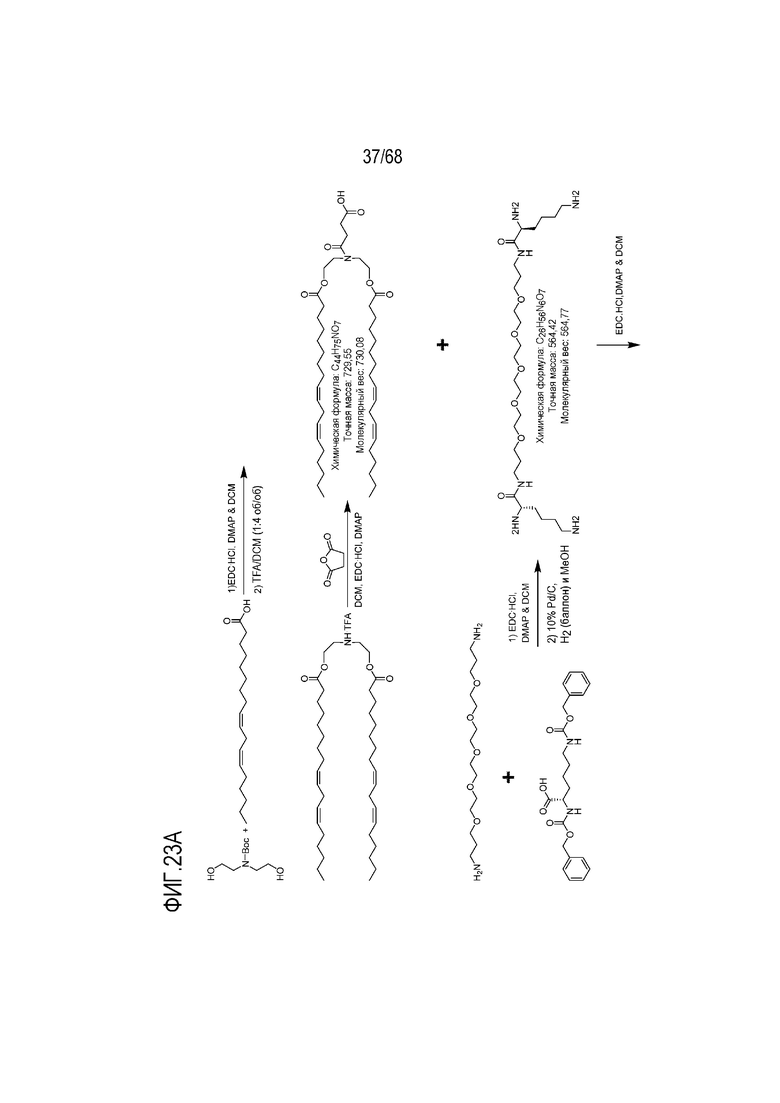
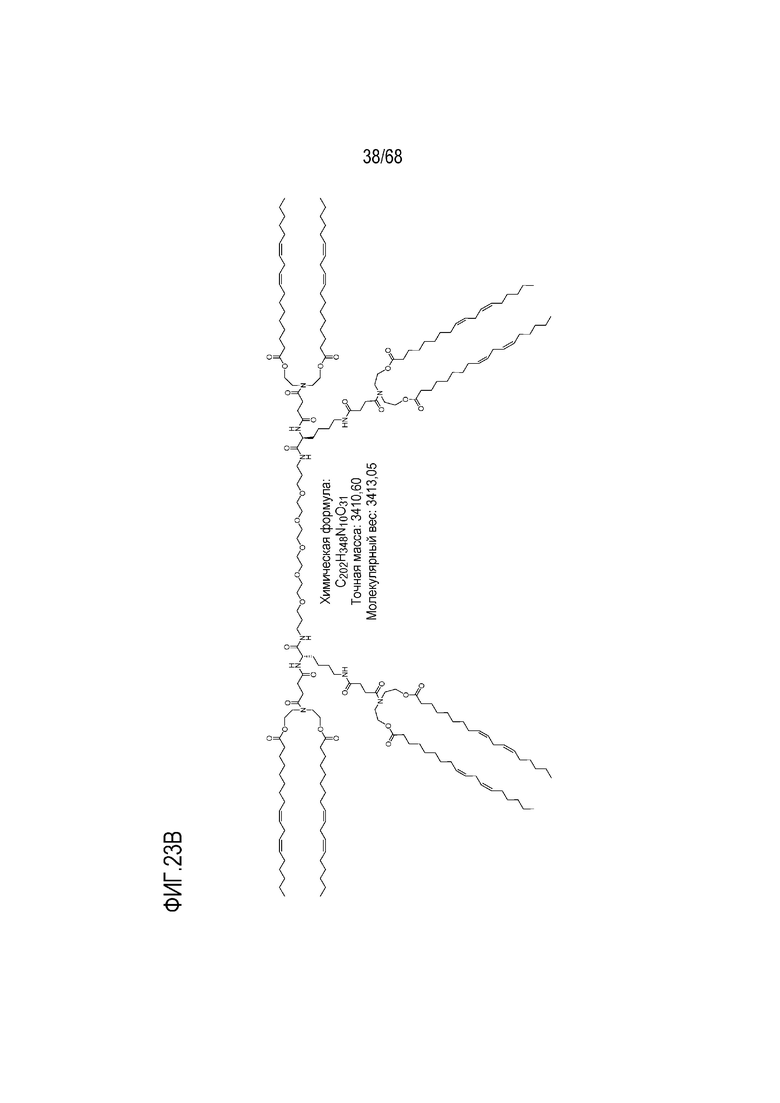


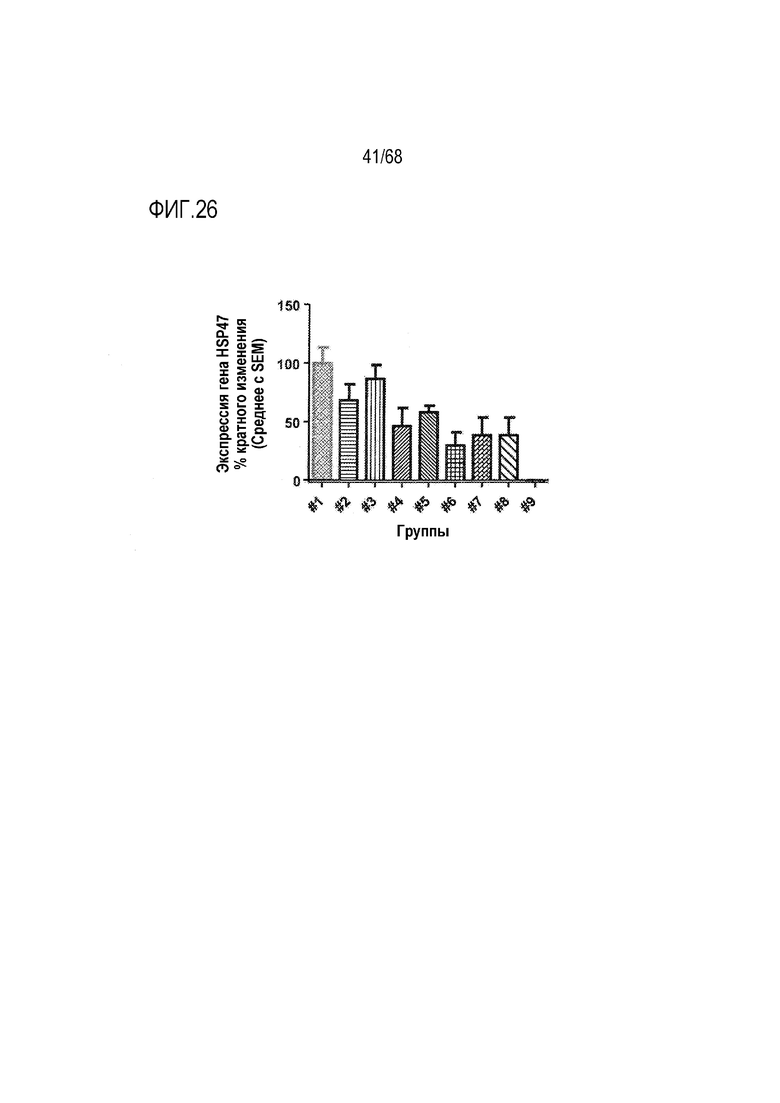
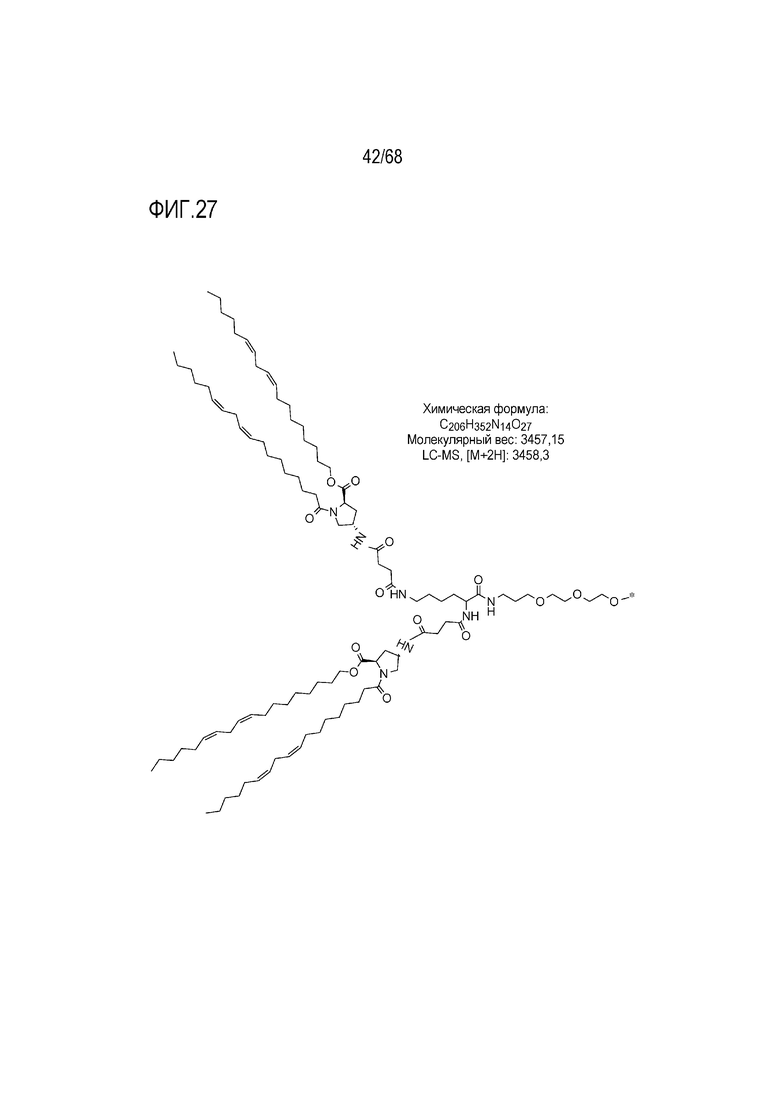
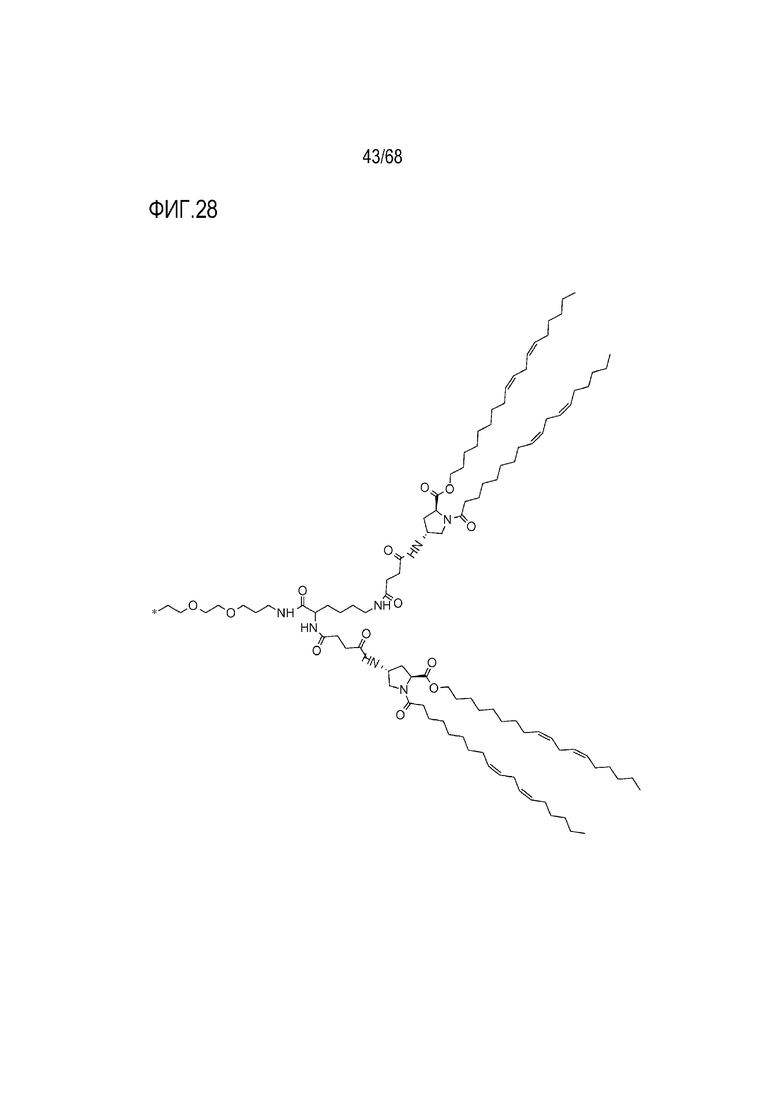

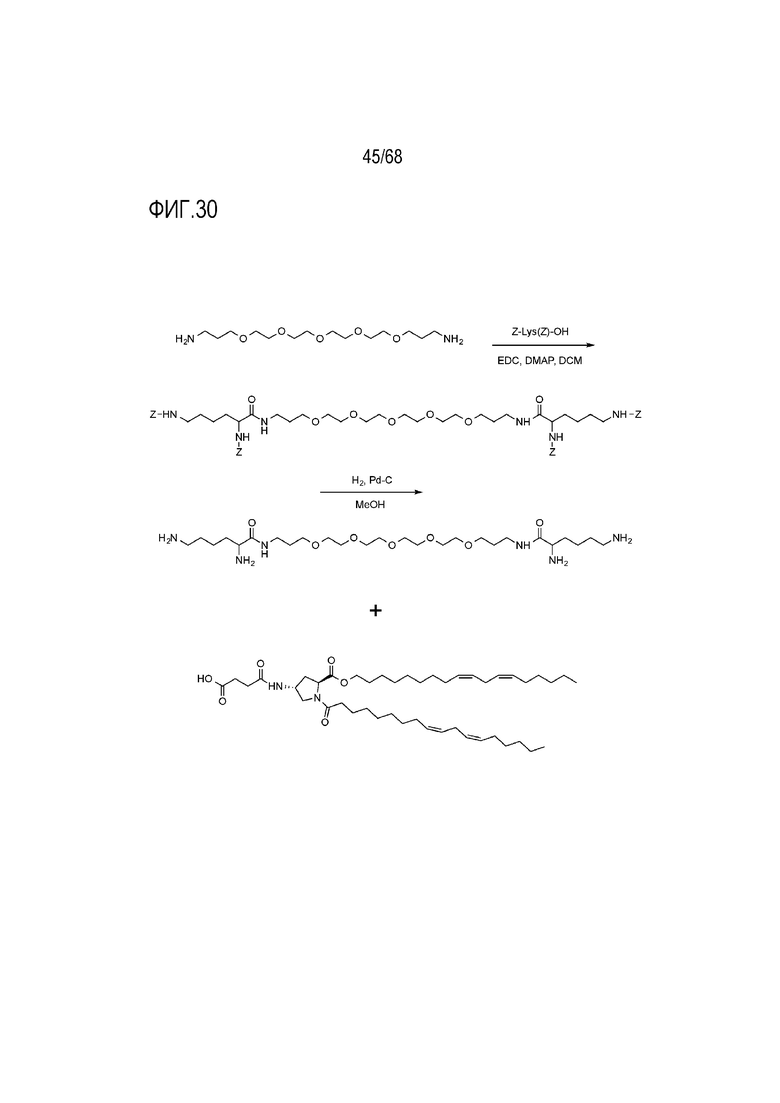
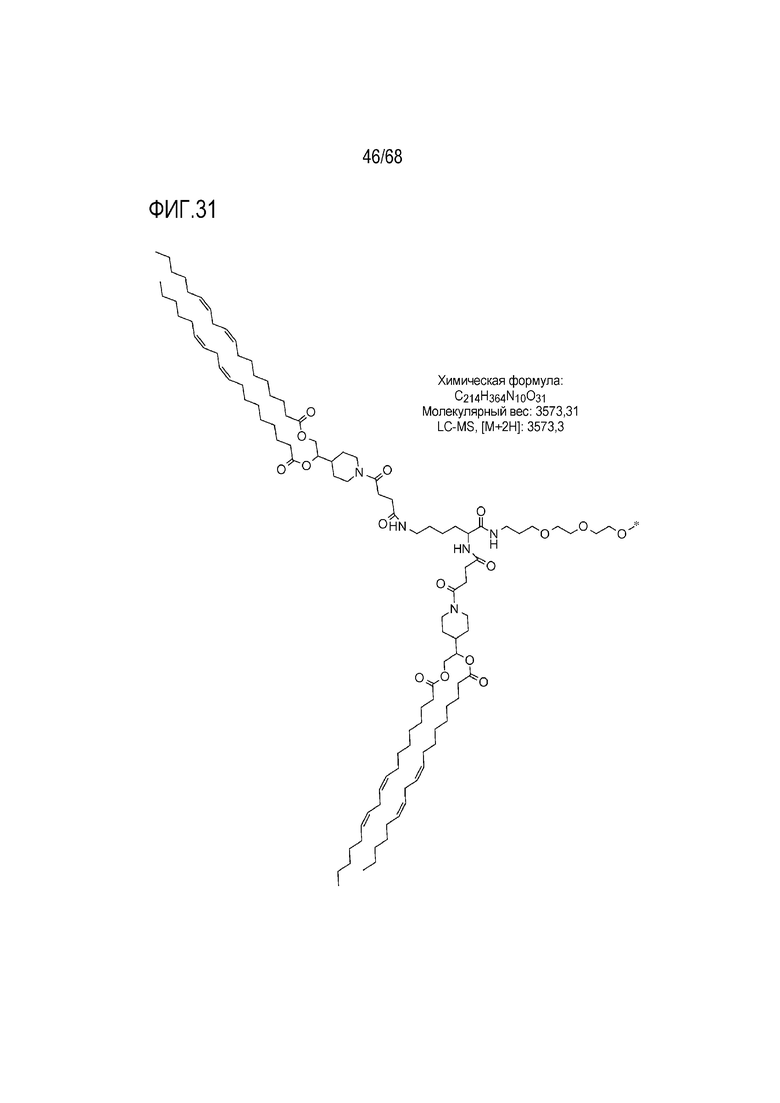
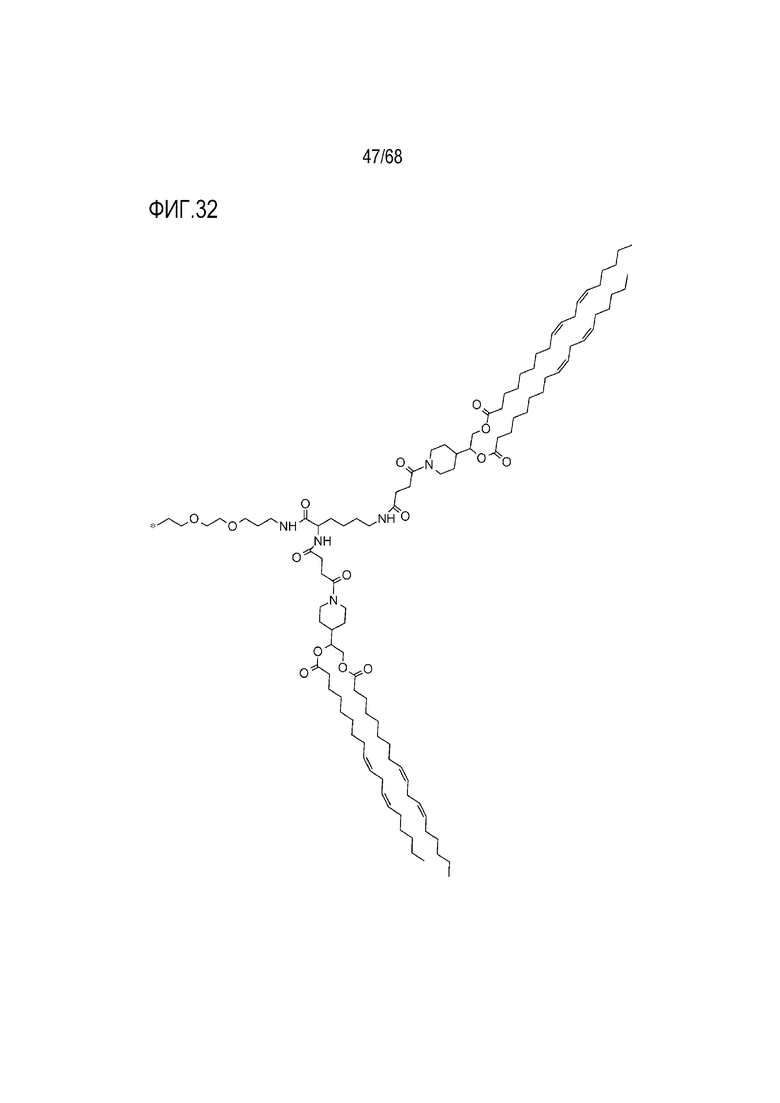
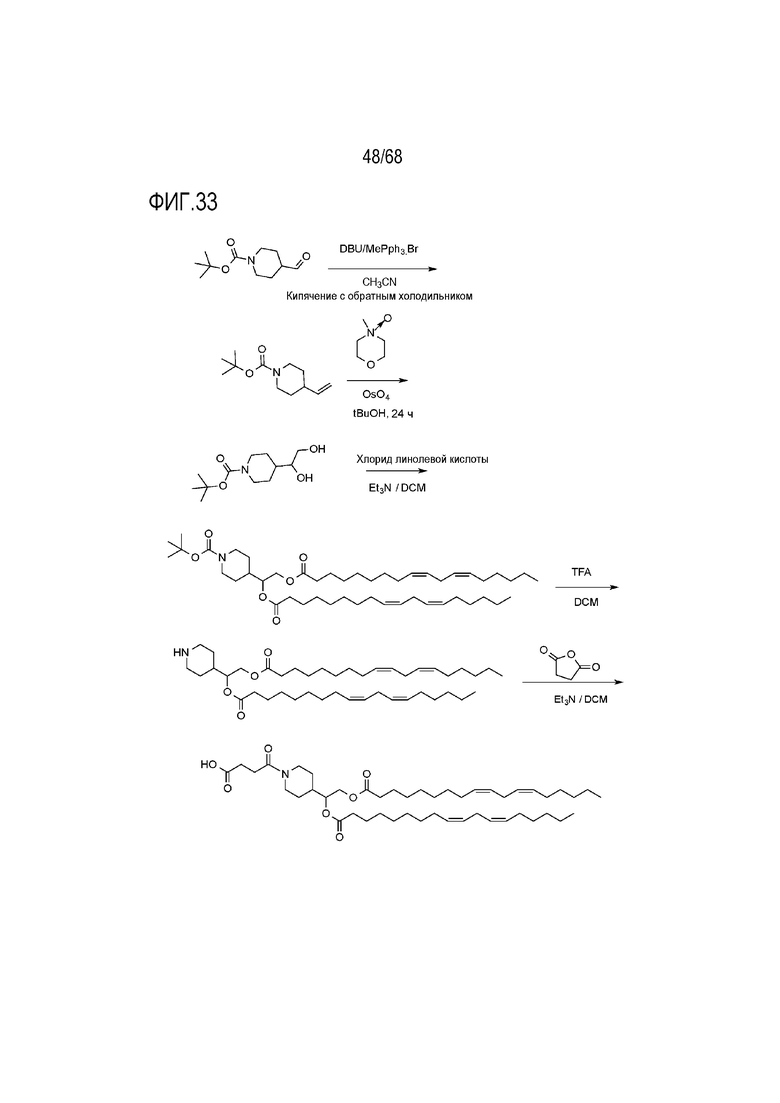
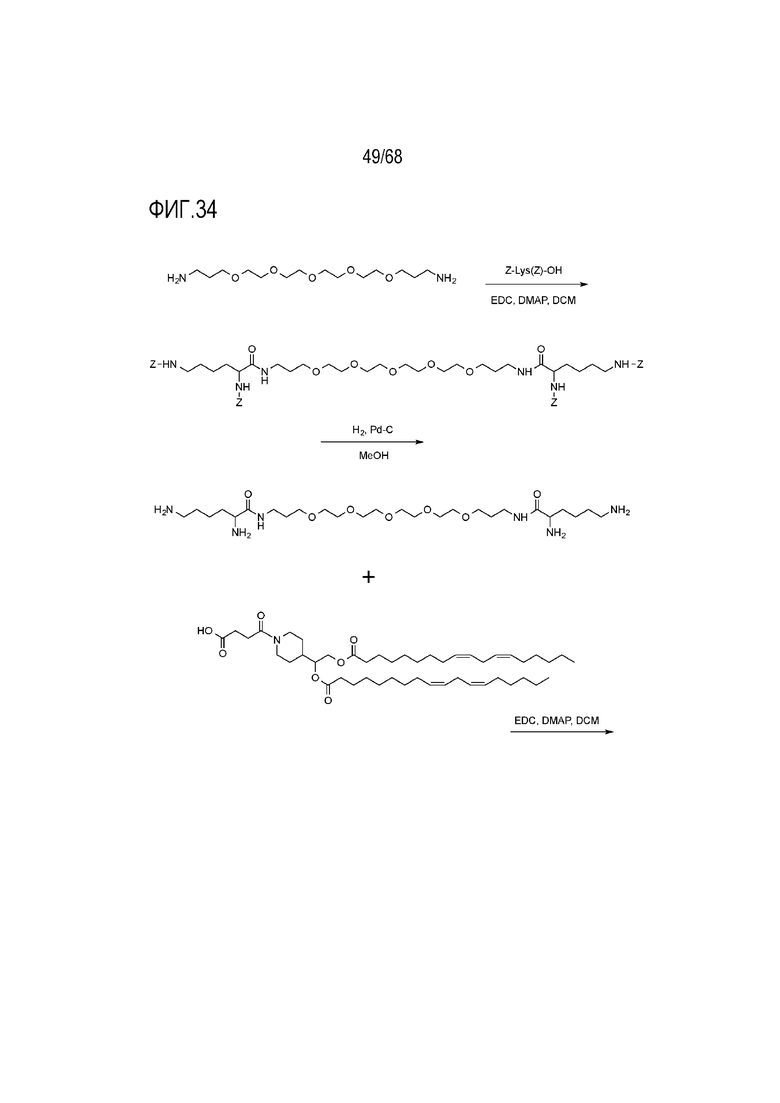
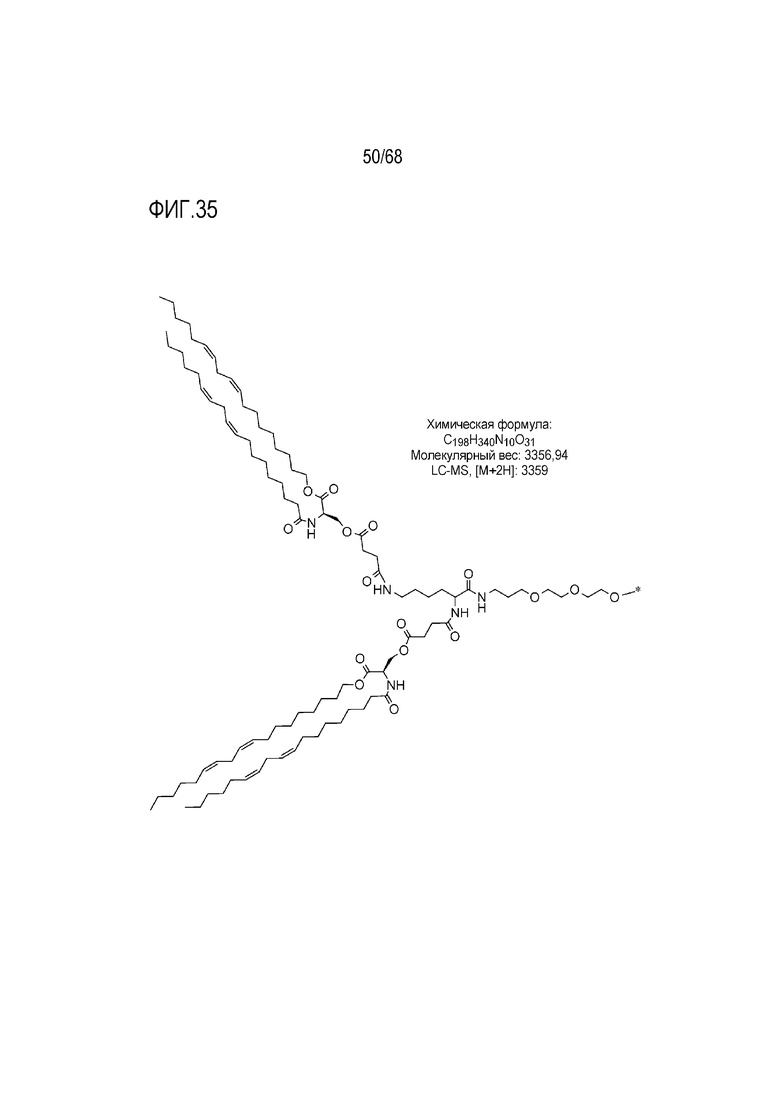


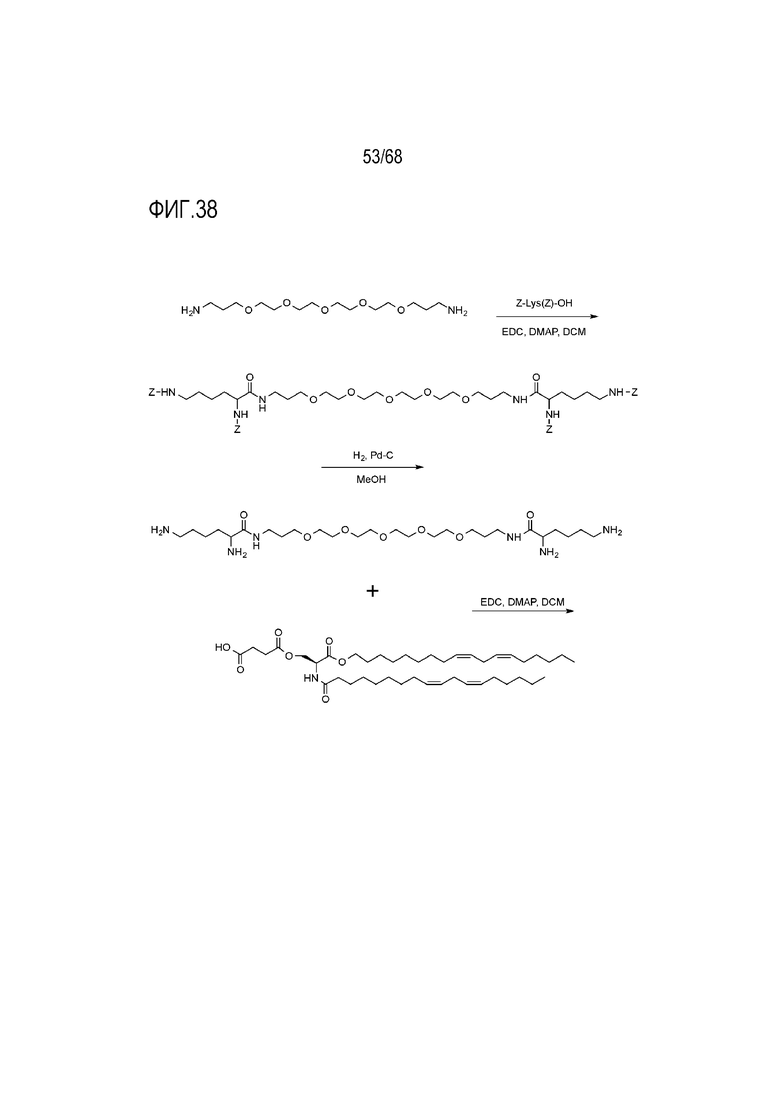
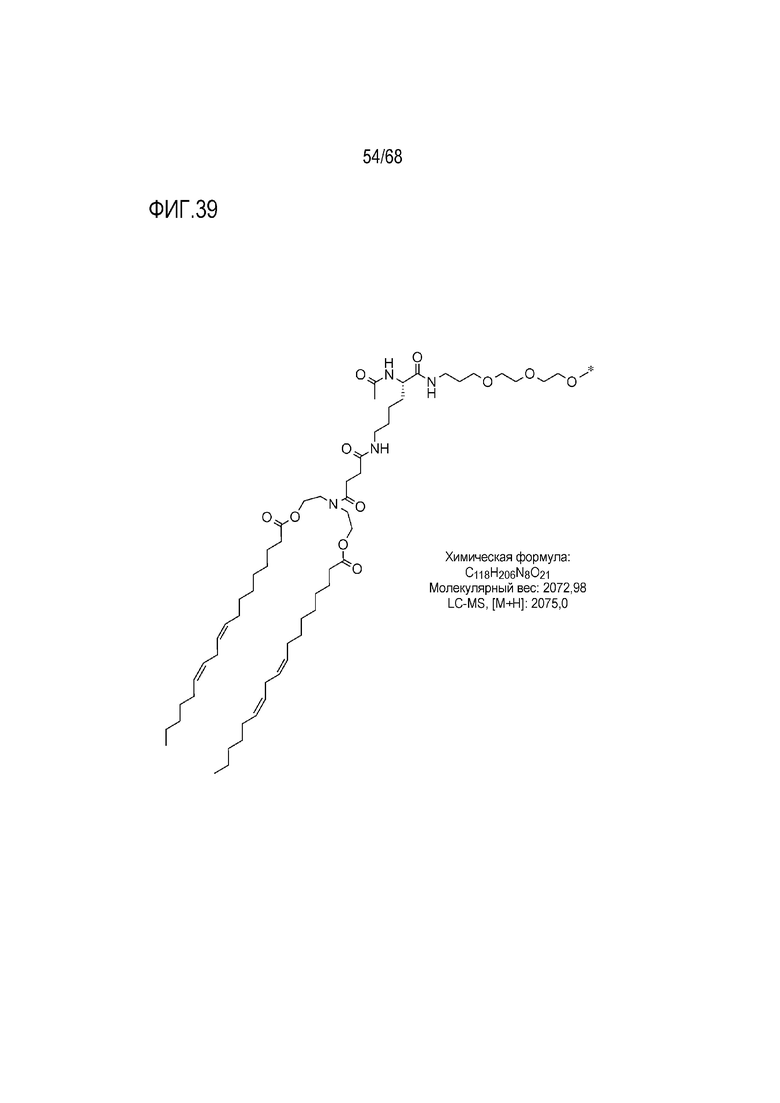
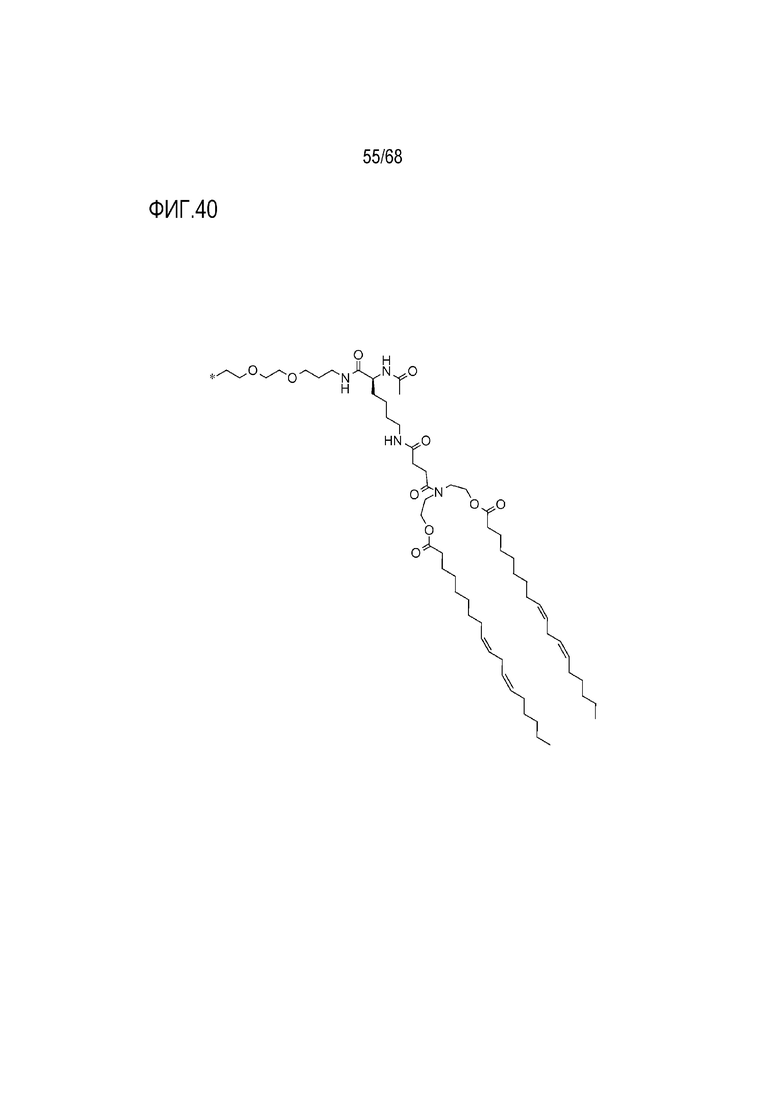
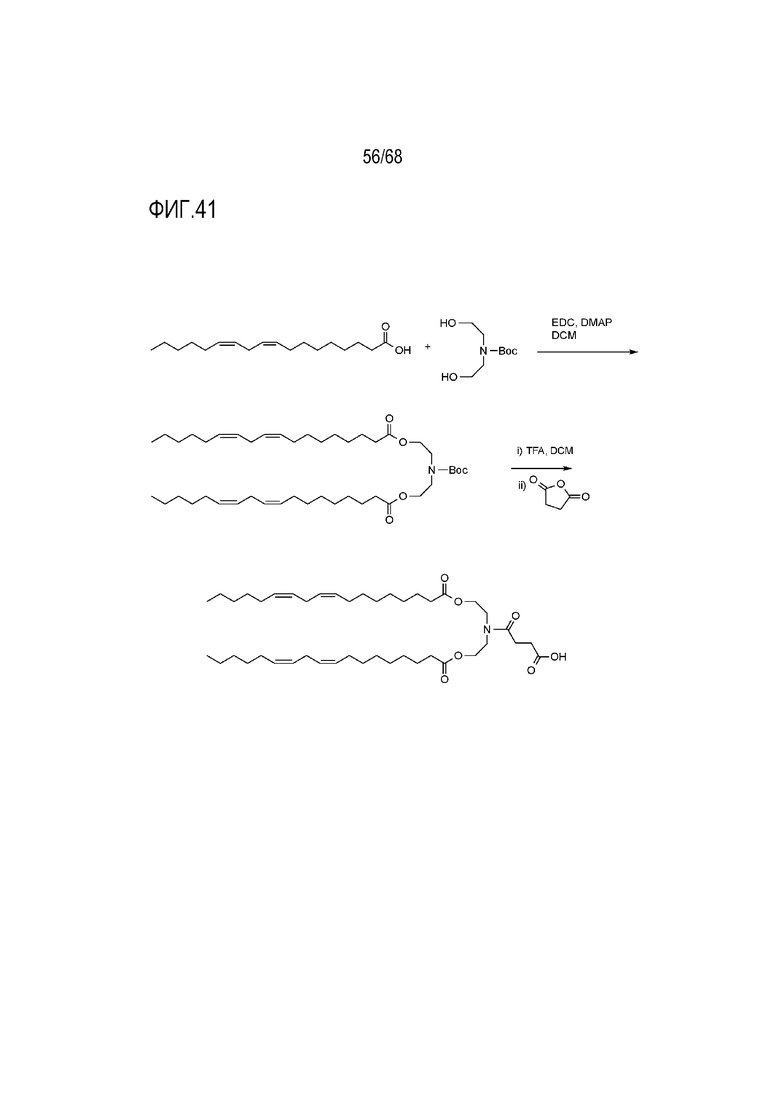
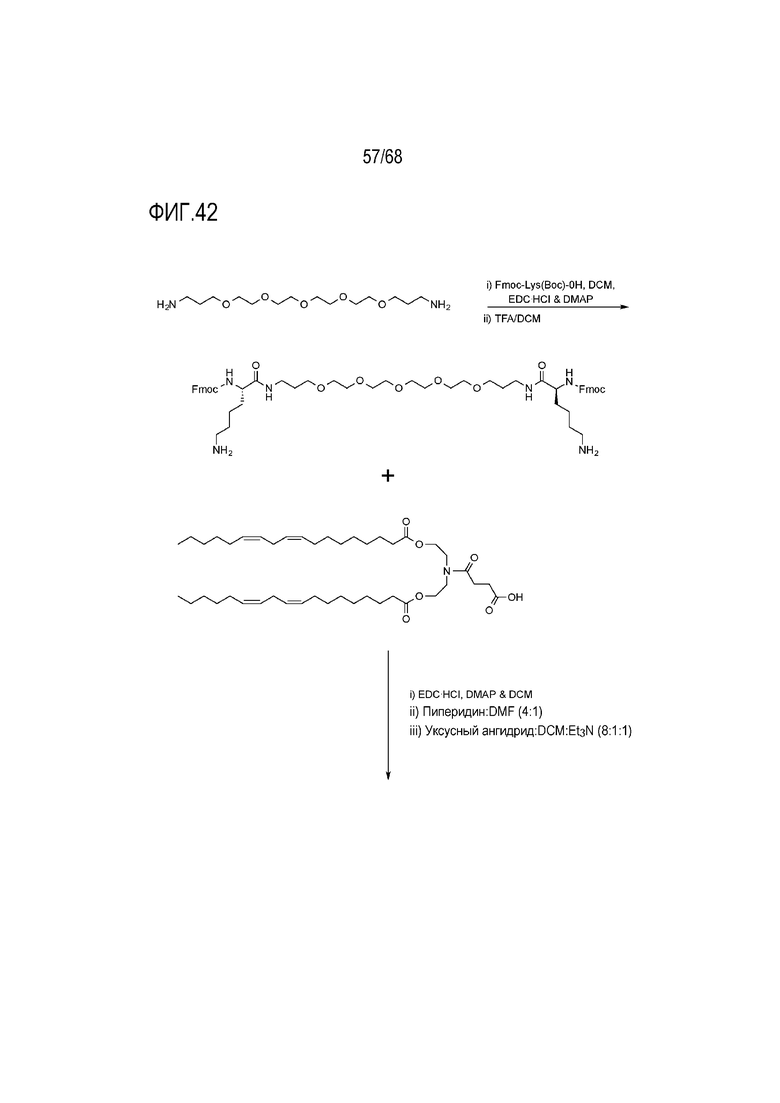
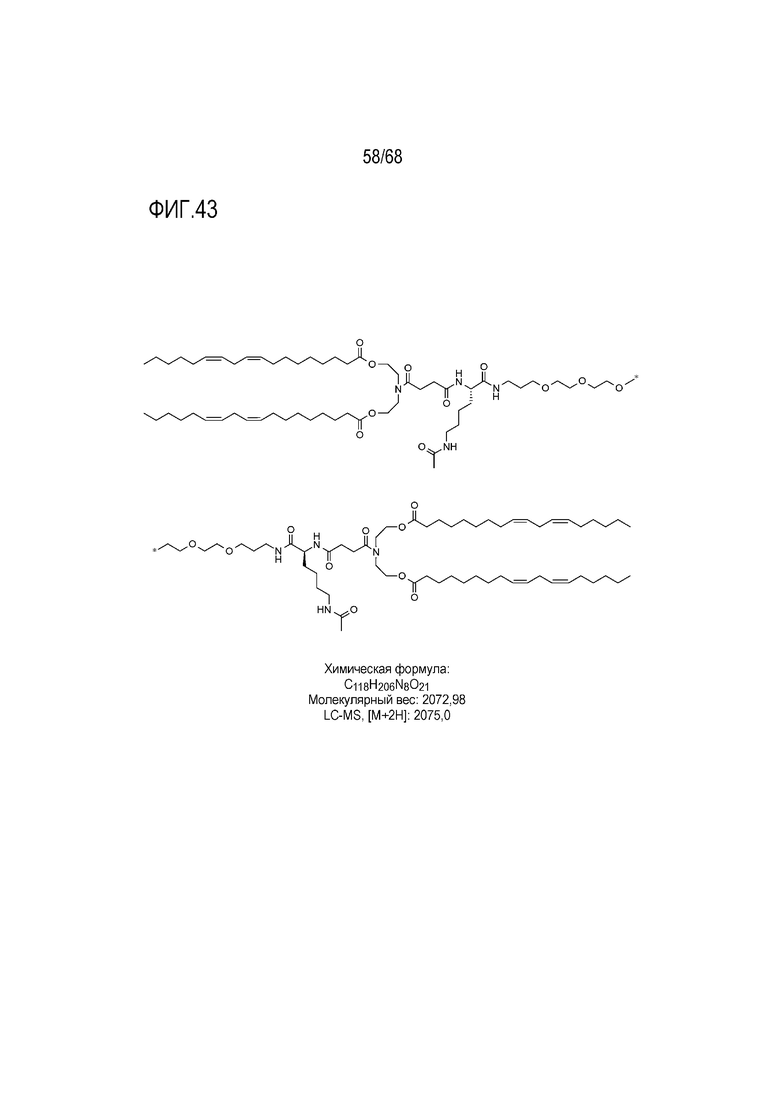
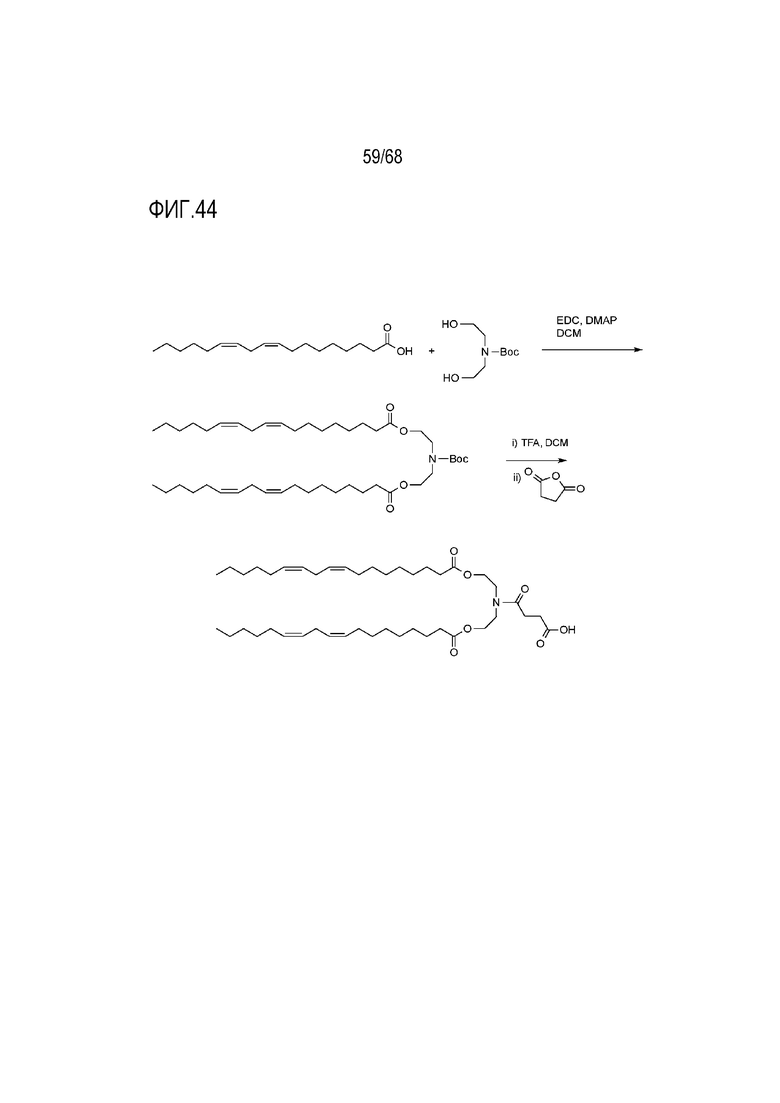
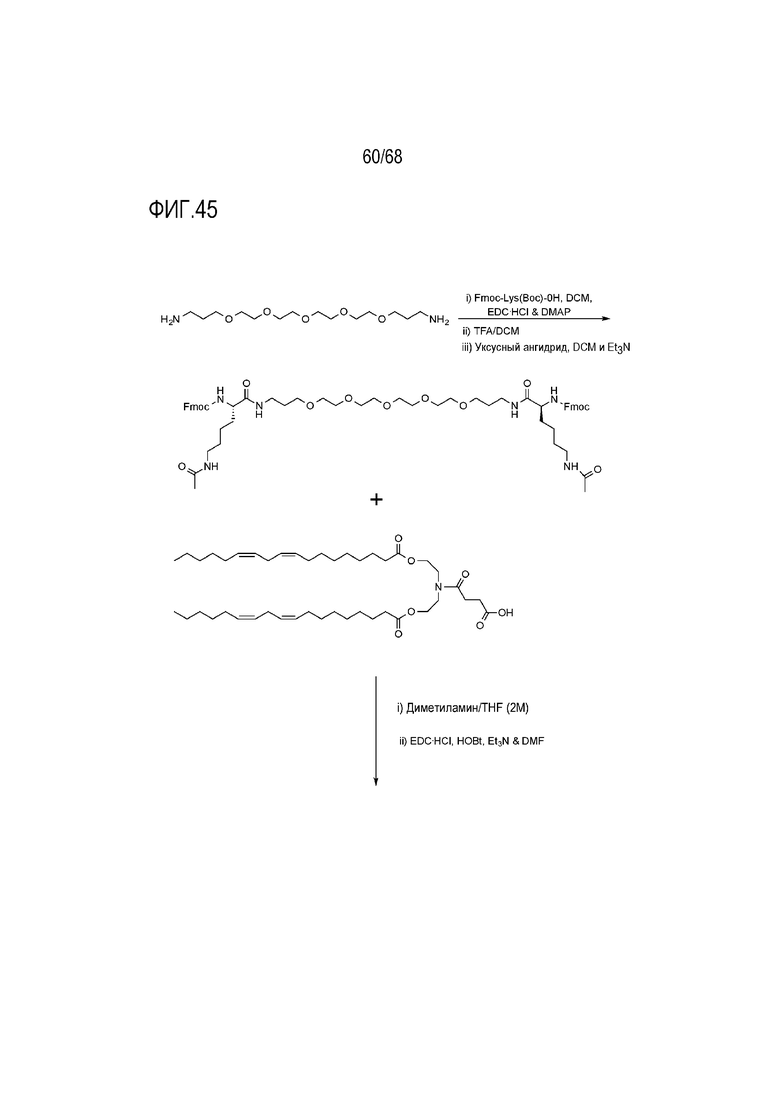
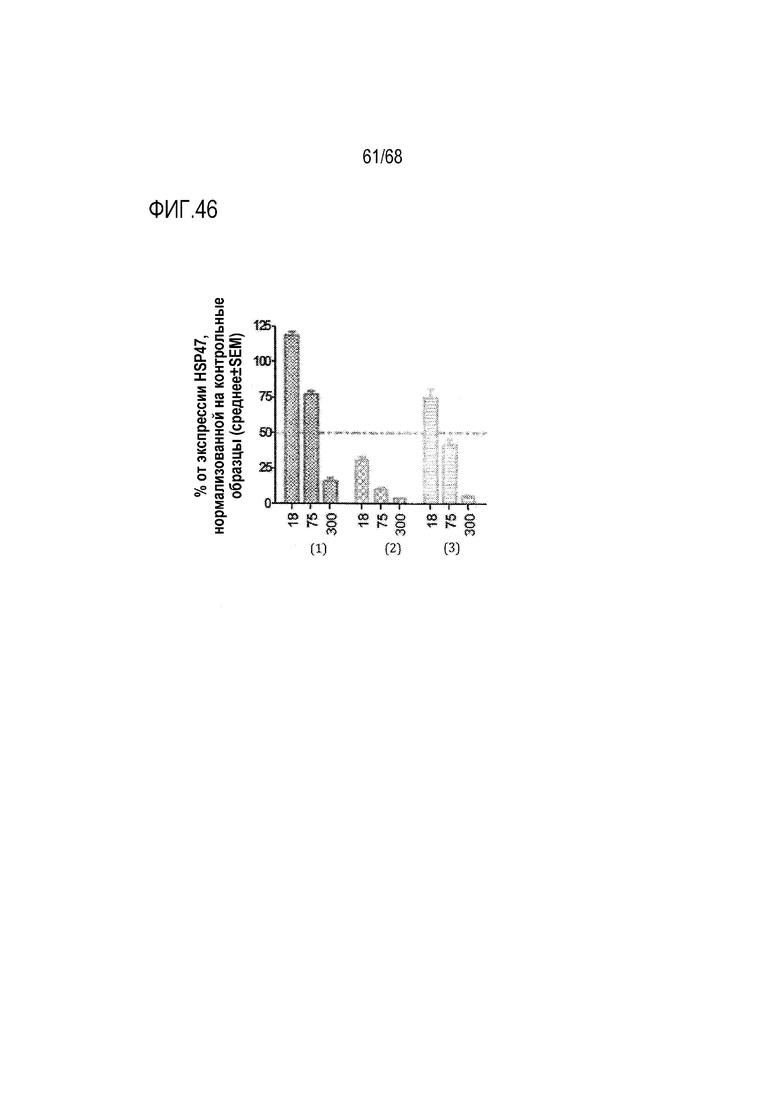
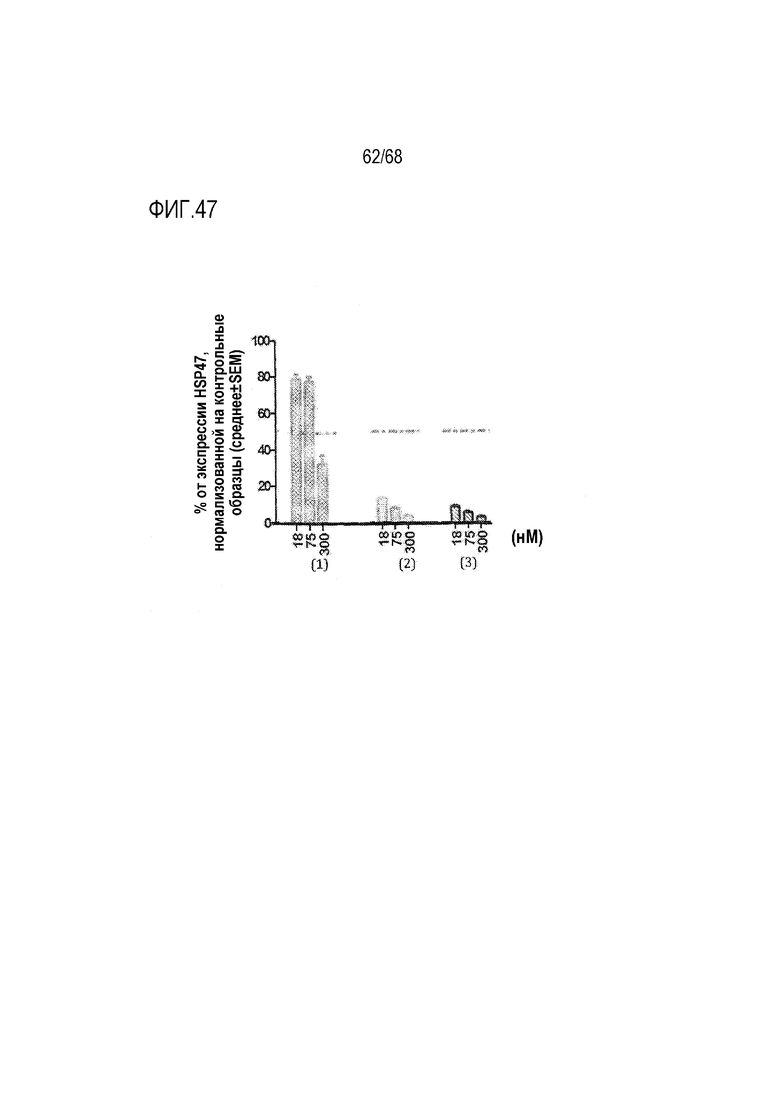

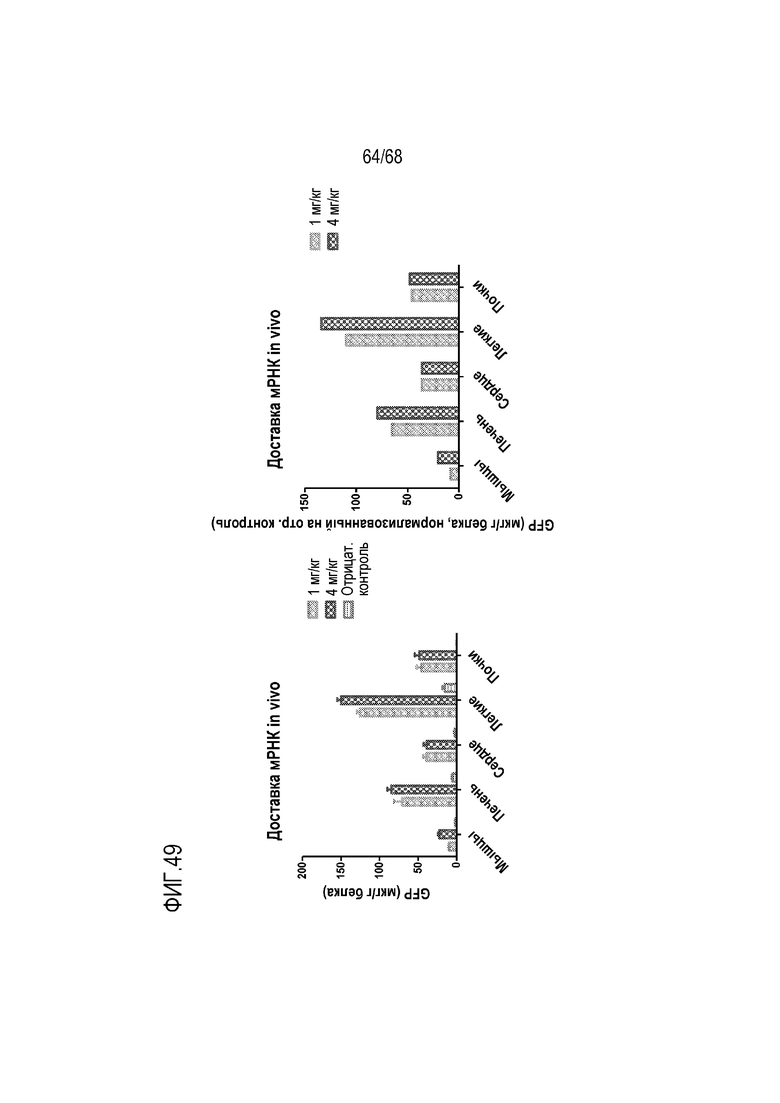
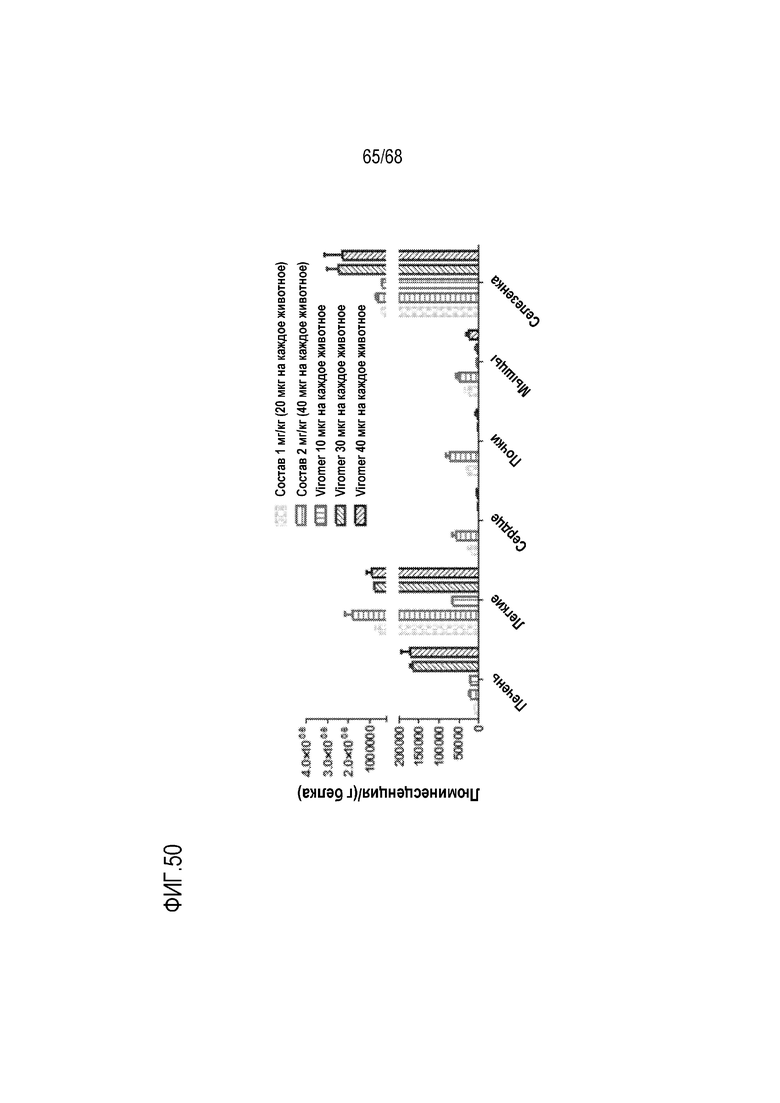
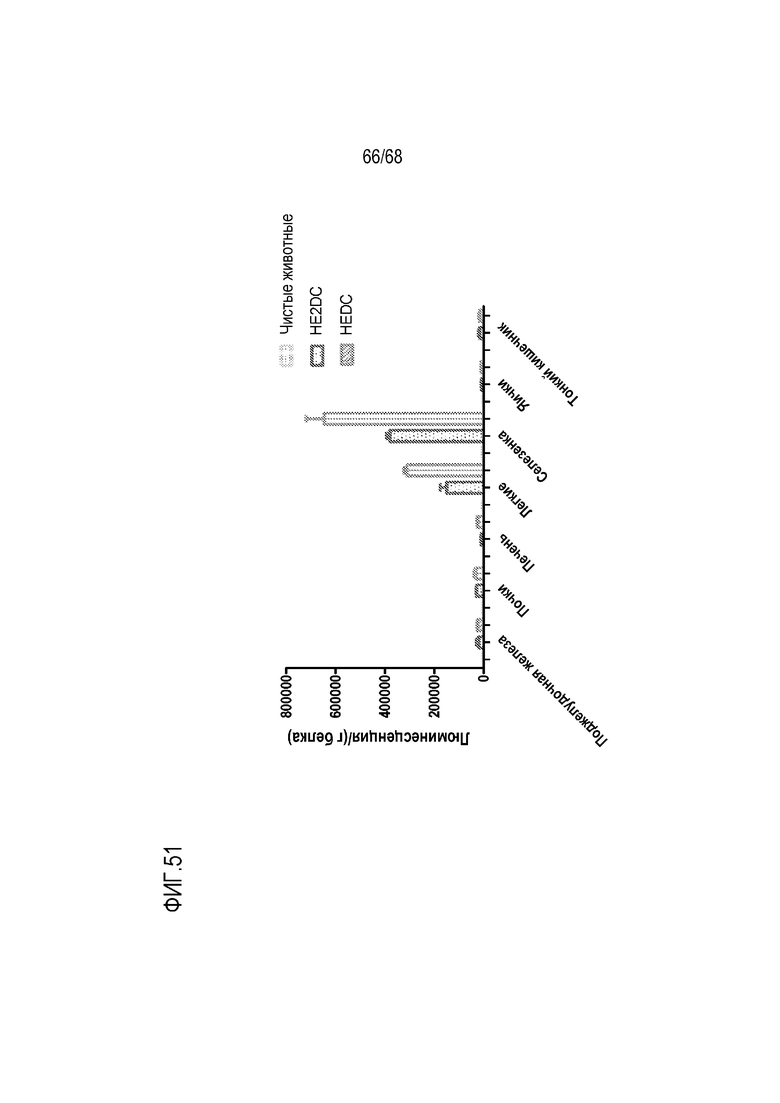

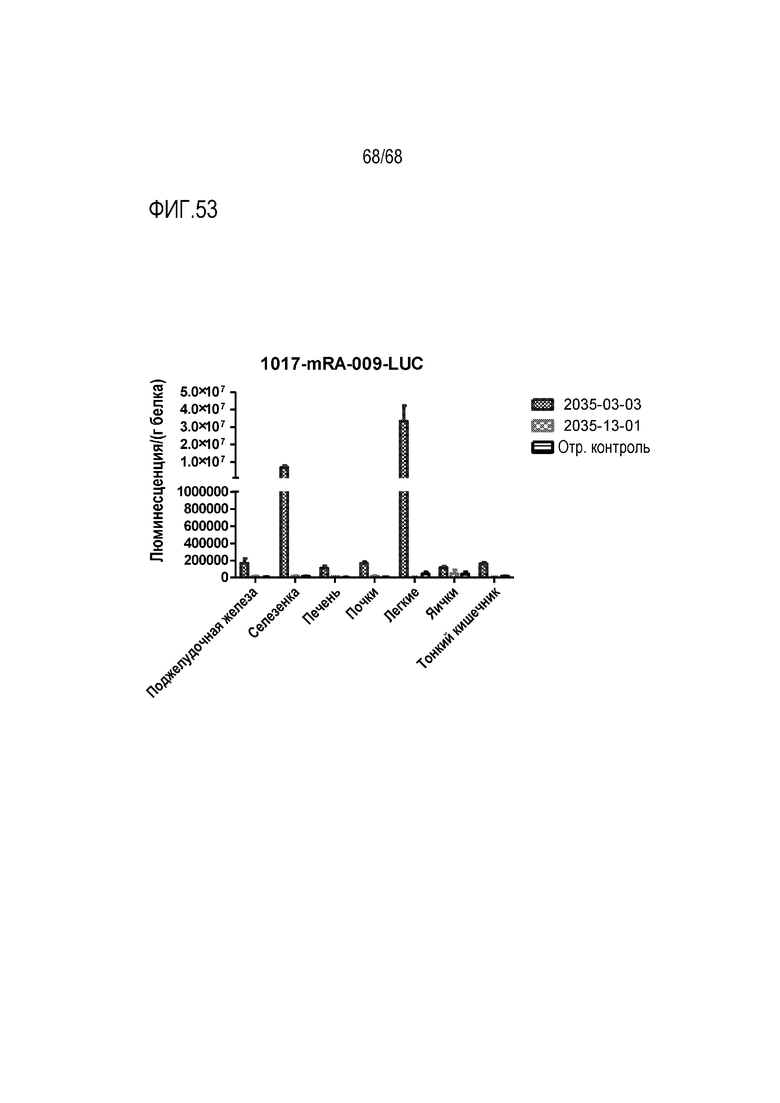
Настоящее изобретение относится к фузогенным соединениям, а также к композициям, содержащим такие соединения. Фузогенные соединения могут быть использованы для изготовления композиций наночастиц для включения или инкапсуляции действующих агентов, для доставки и распределения действующих агентов в клетках, тканях, органах и субъектах. 3 н. и 17 з.п. ф-лы, 53 ил., 11 табл., 15 пр.
1. Фузогенное соединение, имеющее формулу I
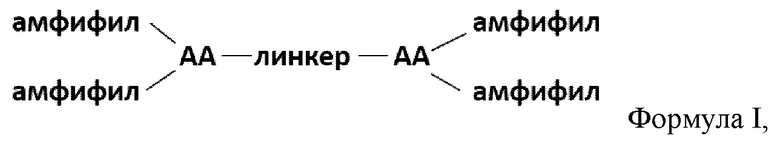
где каждый АА независимо представляет собой аминокислоту, выбранную из следующих структур, или ее стереоизомер:
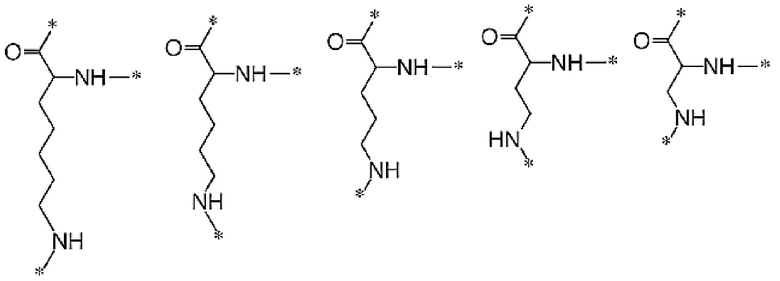
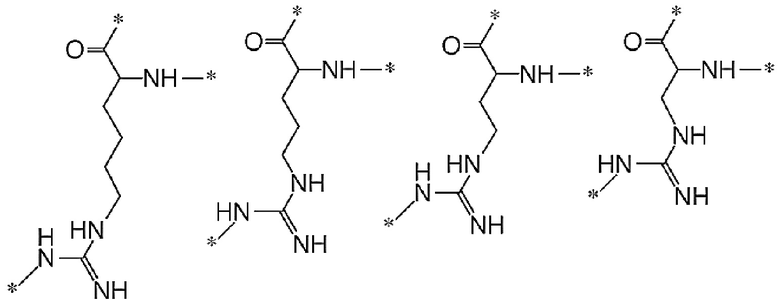
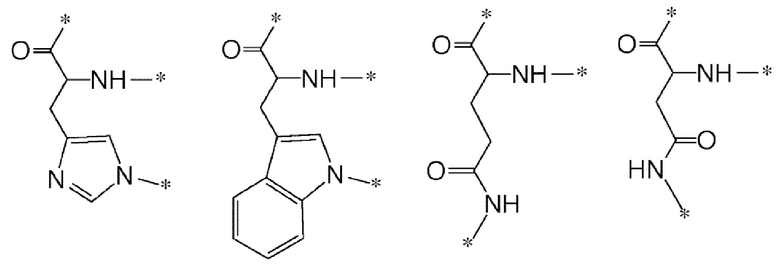
где аминокислота присоединена к амфифилу по каждой из своих аминогрупп и присоединена к линкеру на своем С-конце;
где линкер имеет структуру
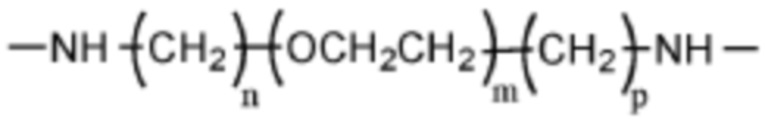
или
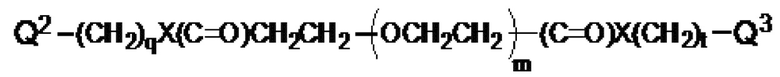 ,
,
где Q2 представляет собой
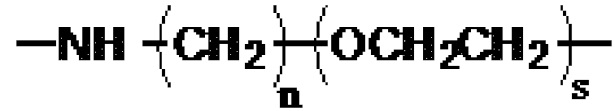 ,
,
где Q3 представляет собой
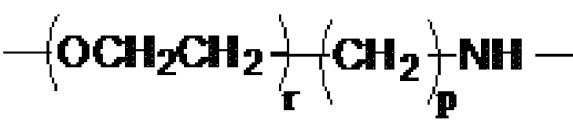 ,
,
где X представляет собой -O-, -S- или -NH-;
где n, p, q и t независимо для каждого случая составляют от 1 до 3;
где m независимо составляет от 1 до 10;
где r и s независимо для каждого случая составляют от 1 до 5; и
где каждый амфифил независимо выбран из формулы II, формулы IV, формулы V и формулы VI:

где R1 в формуле II представляет собой CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4 или CH2(CH2)n(C=O)NHR4;
где R2 в формуле II представляет собой CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5 или CH2(CH2)m(C=O)NHR5;
где n и m в формуле II, каждый независимо, составляют от 1 до 2; и R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу; и
где R3 в формуле II представляет собой разветвленный или неразветвленный С(1-8)алкандиил;
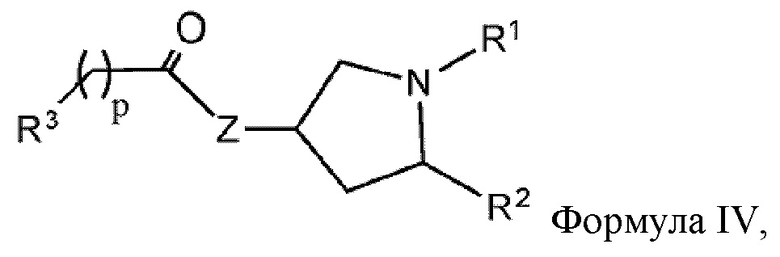
где R1 в формуле IV представляет собой (C=O)R4;
где R2 в формуле IV представляет собой (C=O)OR5,
где R4 и R5 в формуле IV представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где Z в формуле IV представляет собой NH;
где р в формуле IV составляет от 1 до 4;
где R3 в формуле IV представляет собой С(1-12)алкильную группу, замещенную -(С=О)-, которая присоединена к АА;
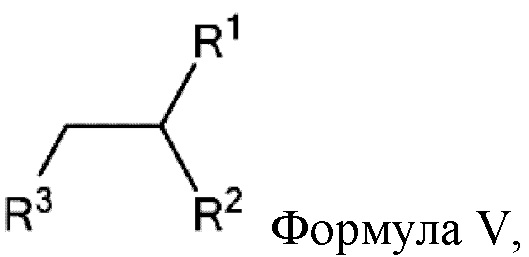
где R1 в формуле V представляет собой (C=O)OR4;
где R2 в формуле V представляет собой NH(C=O)R5;
где R4 и R5 в формуле V представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 в формуле V представляет собой разветвленный или неразветвленный -O(C=O)-C(1-8)алкандиил-(C=O)-, который присоединен к АА;
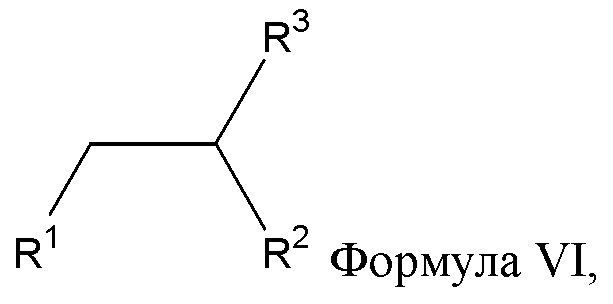
где R1 в формуле VI представляет собой О(C=O)OR4;
где R2 в формуле VI представляет собой О(C=O)OR5;
где R4 и R5 в формуле VI представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 в формуле VI представляет собой
 ;
;
где один или два амфифила могут необязательно отсутствовать и заменены фармацевтически приемлемой органической химической группой, выбранной из алкильной группы, алкенила, алкинила, ацетила, Boc, Fmoc, TFA и CBZ, имеющей 1-400 атомов, выбранных из углерода, кислорода, азота, серы, фтора и водорода.
2. Фузогенное соединение по п. 1, где один или два амфифила отсутствуют и заменены фармацевтически приемлемой органической химической группой.
3. Фузогенное соединение по п. 2, где фармацевтически приемлемая органическая химическая группа представляет собой алкил, алкенил, алкинил, ацетил, Boc, Fmoc, TFA или CBZ.
4. Фузогенное соединение по п. 3, где соединение выбирают из следующих соединений:
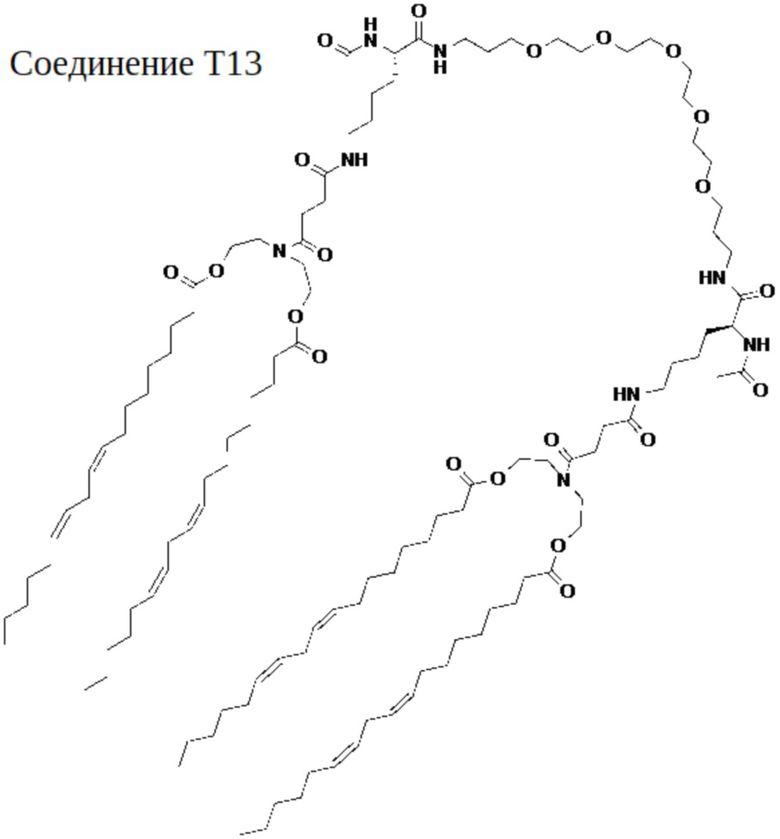
 .
.
5. Фузогенное соединение по п. 1, где R3 в формуле II представляет собой разветвленный или неразветвленный С(2-8)алкандиил.
6. Фузогенное соединение по п. 1, где соединение выбирают из следующих соединений:
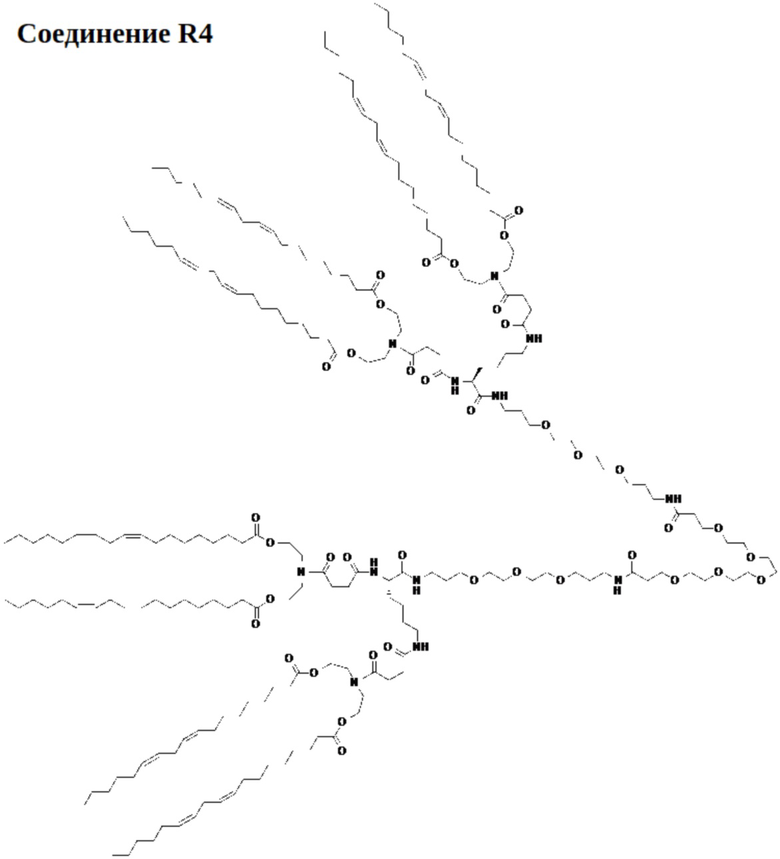
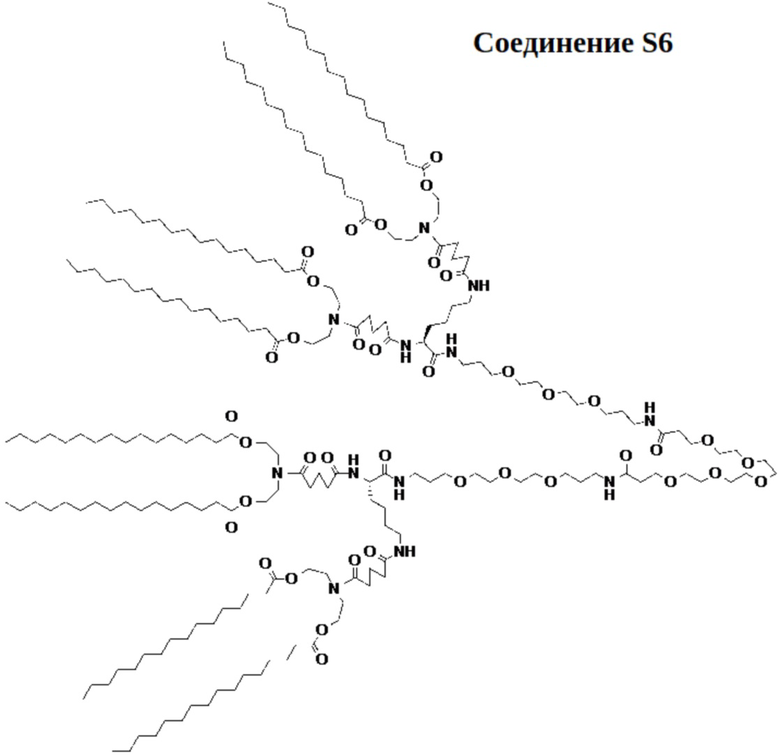

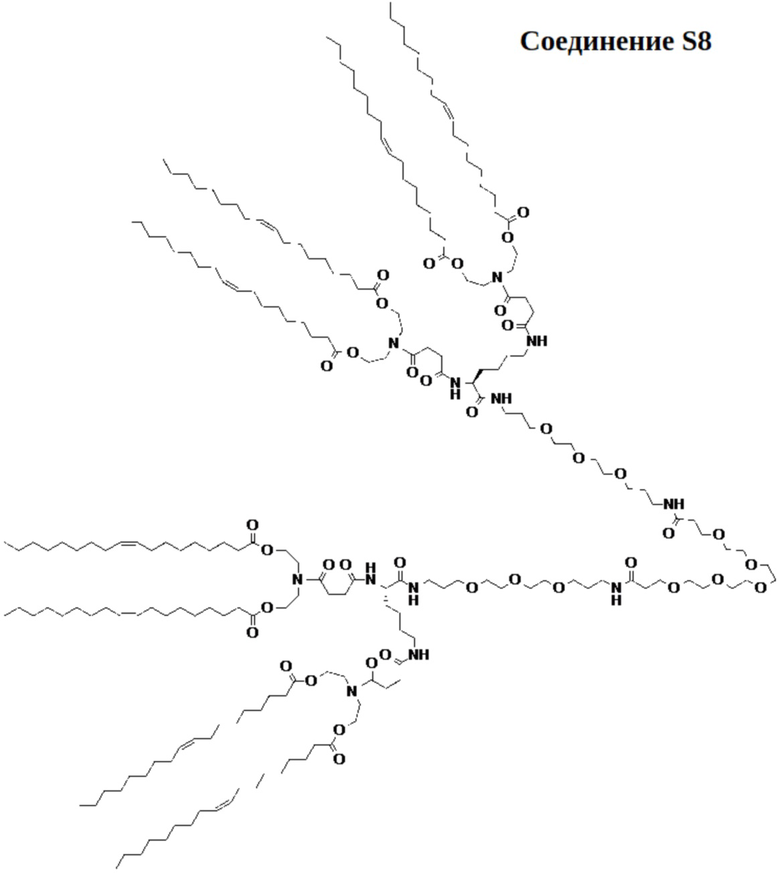
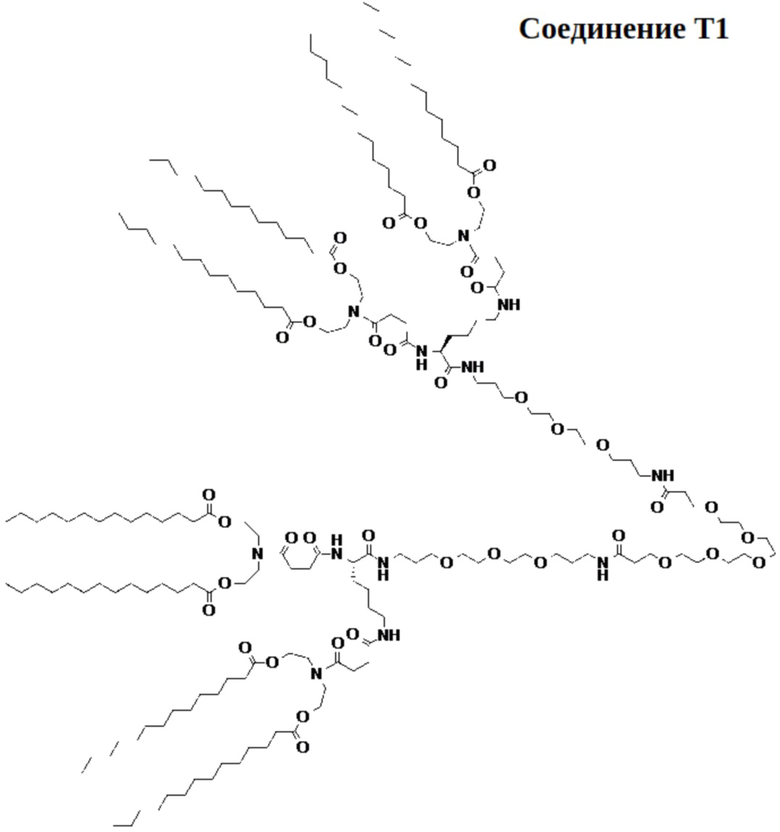
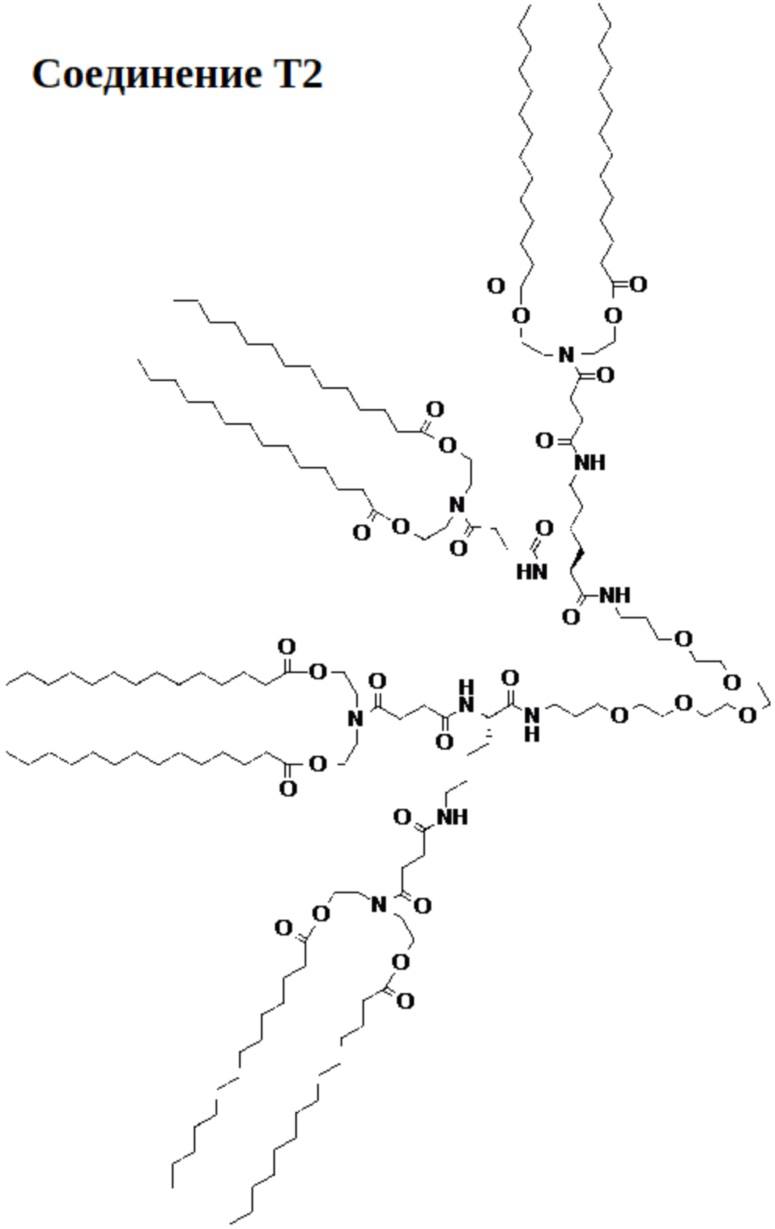
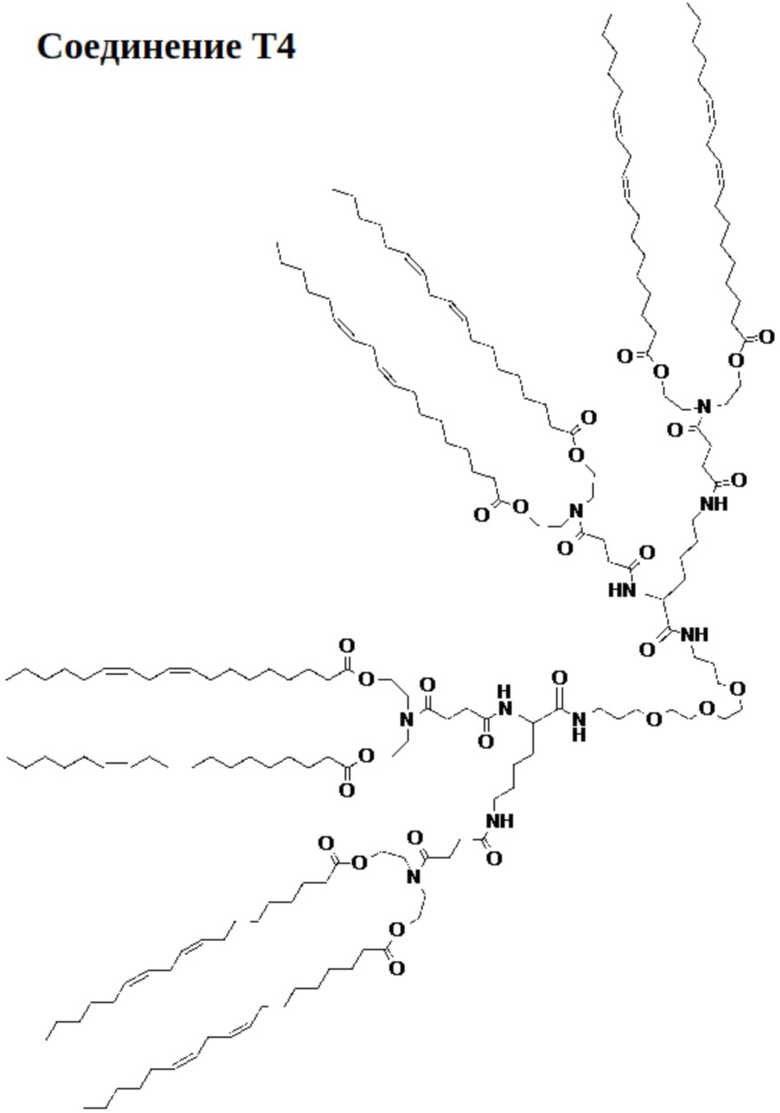
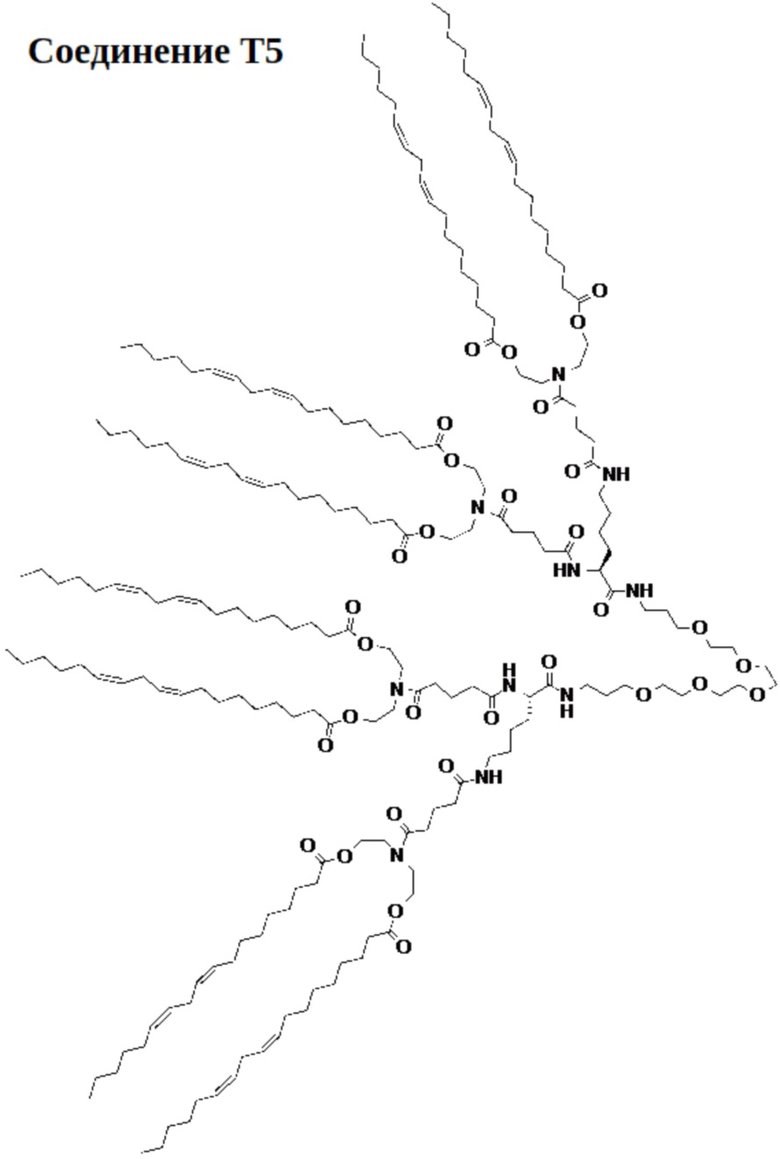
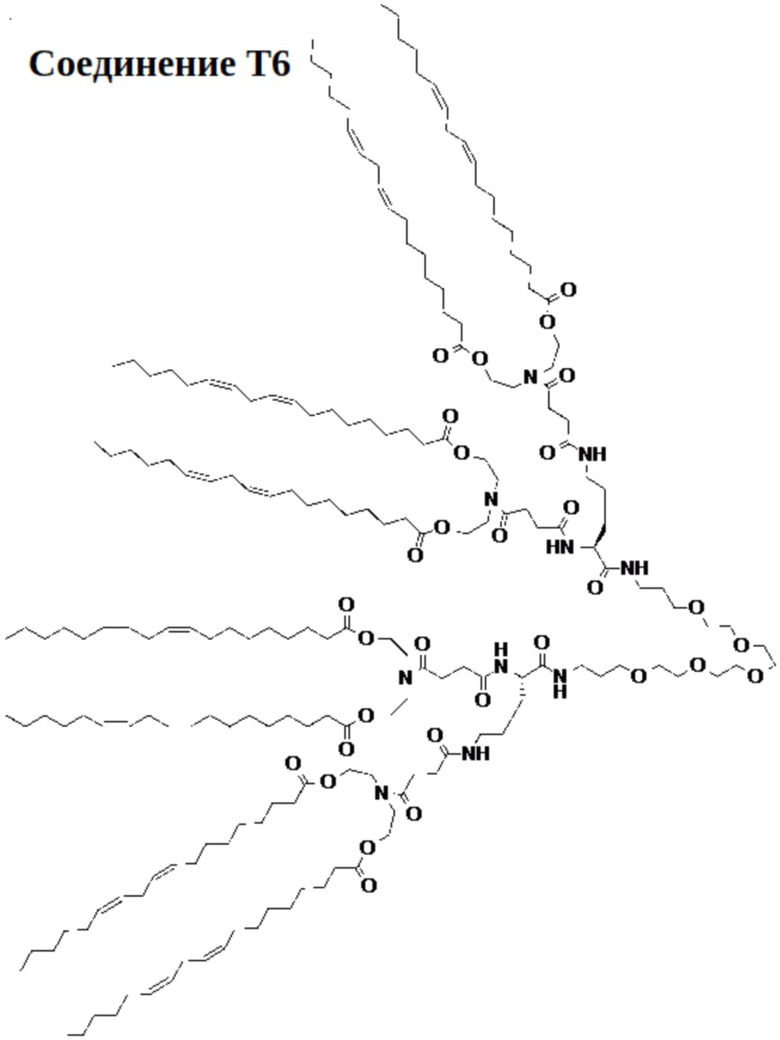
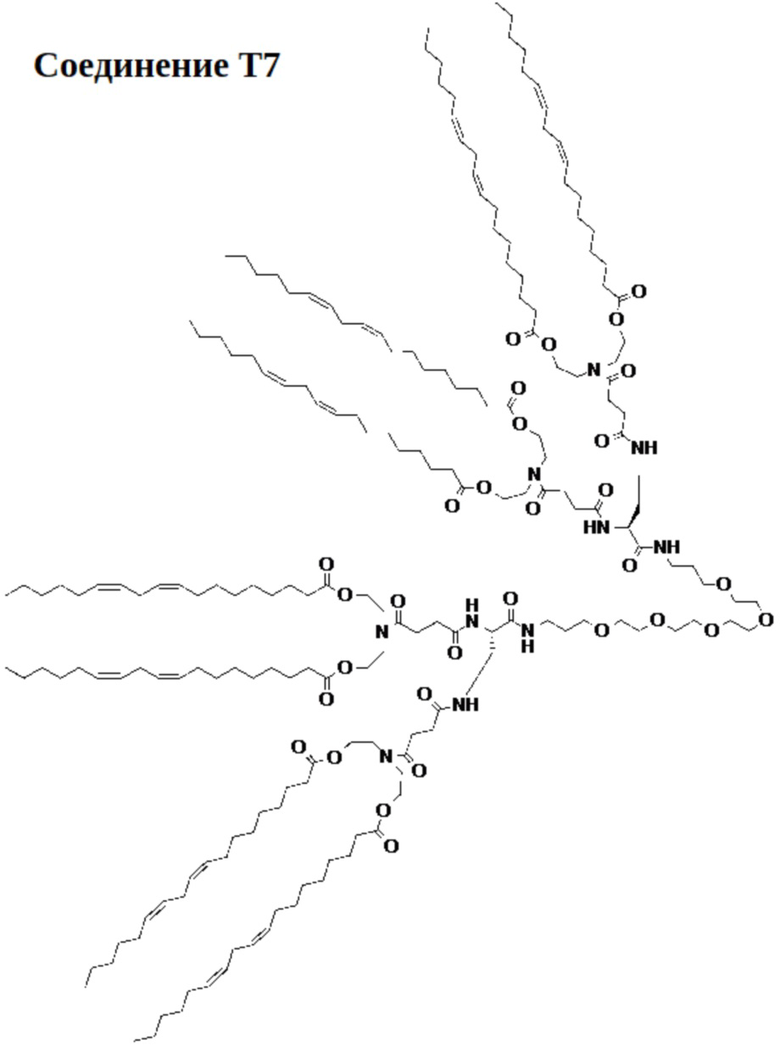
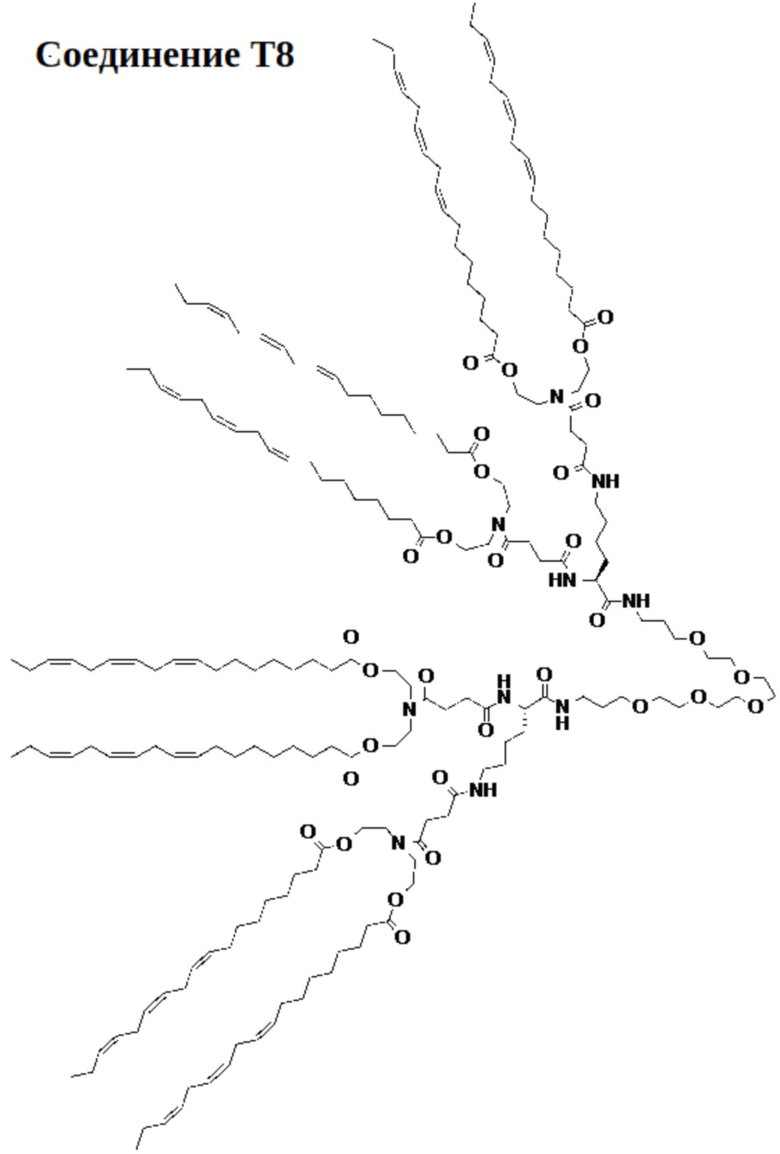
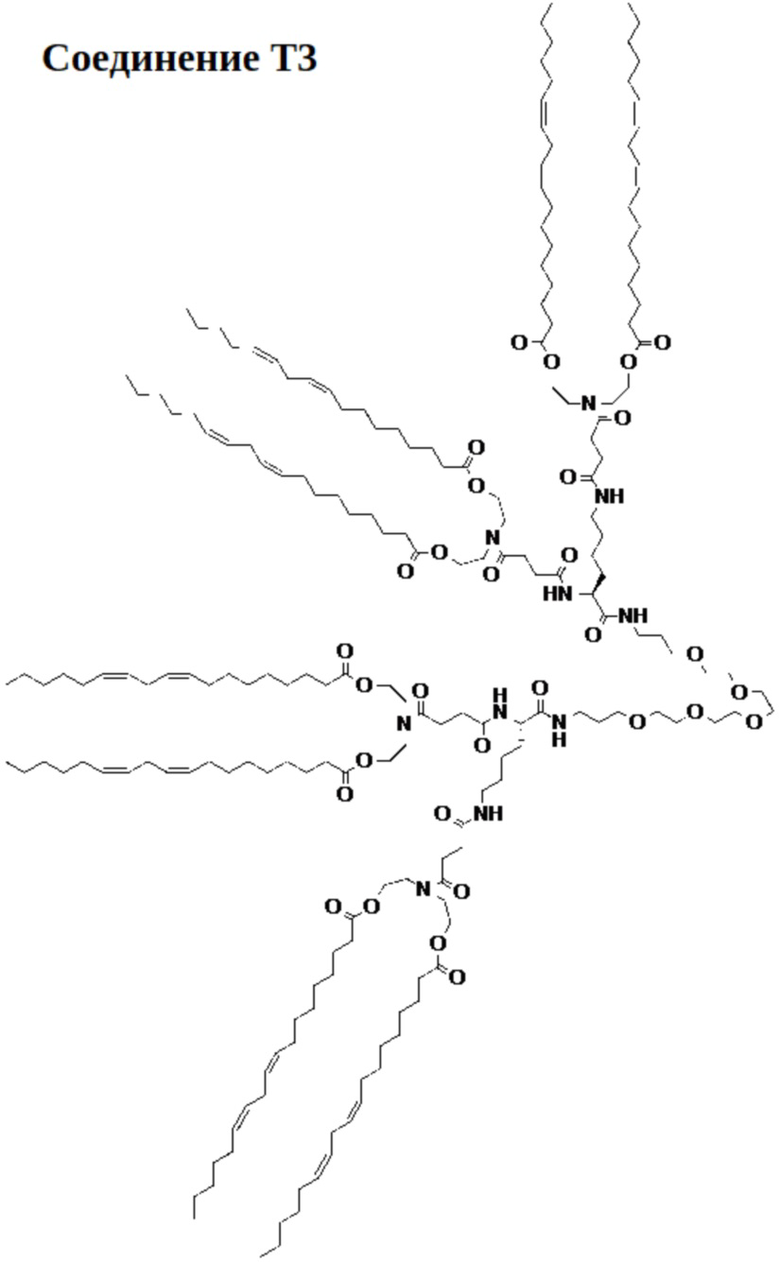 .
.
7. Фузогенное соединение по п. 1, где в формуле IV R4 и R5 независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу.
8. Фузогенное соединение по п. 1, где соединение представляет собой соединение T10:
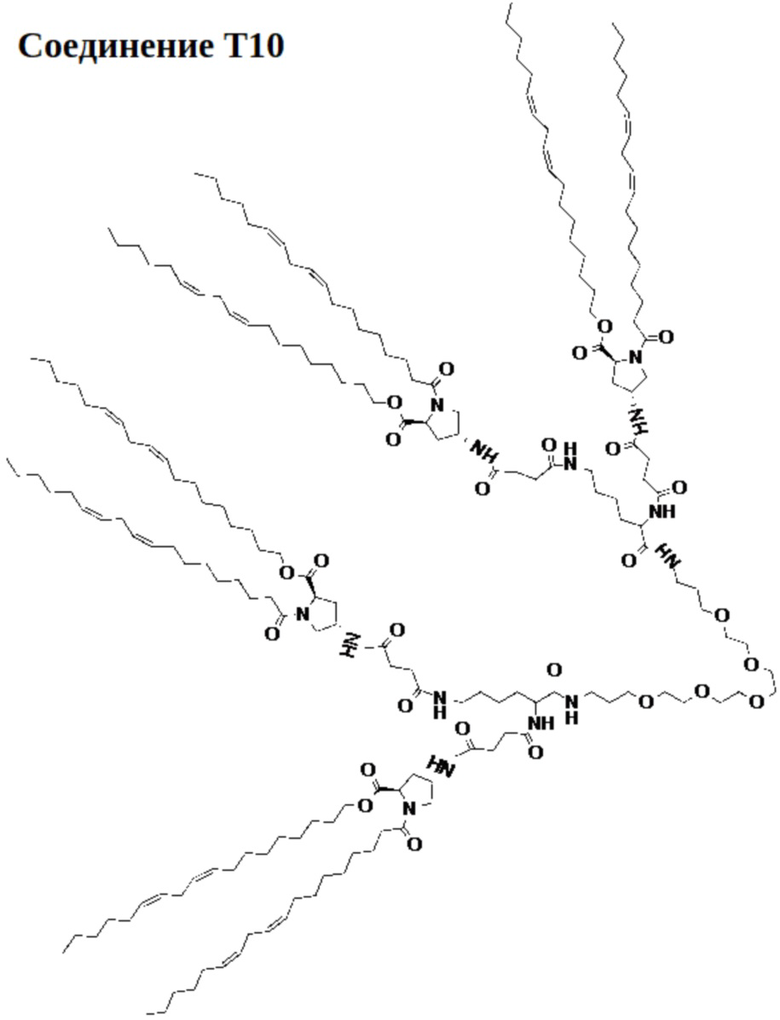 .
.
9. Фузогенное соединение по п. 1, где R4 и R5 в формуле V независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу.
10. Фузогенное соединение по п. 1, где соединение представляет собой соединение T12:
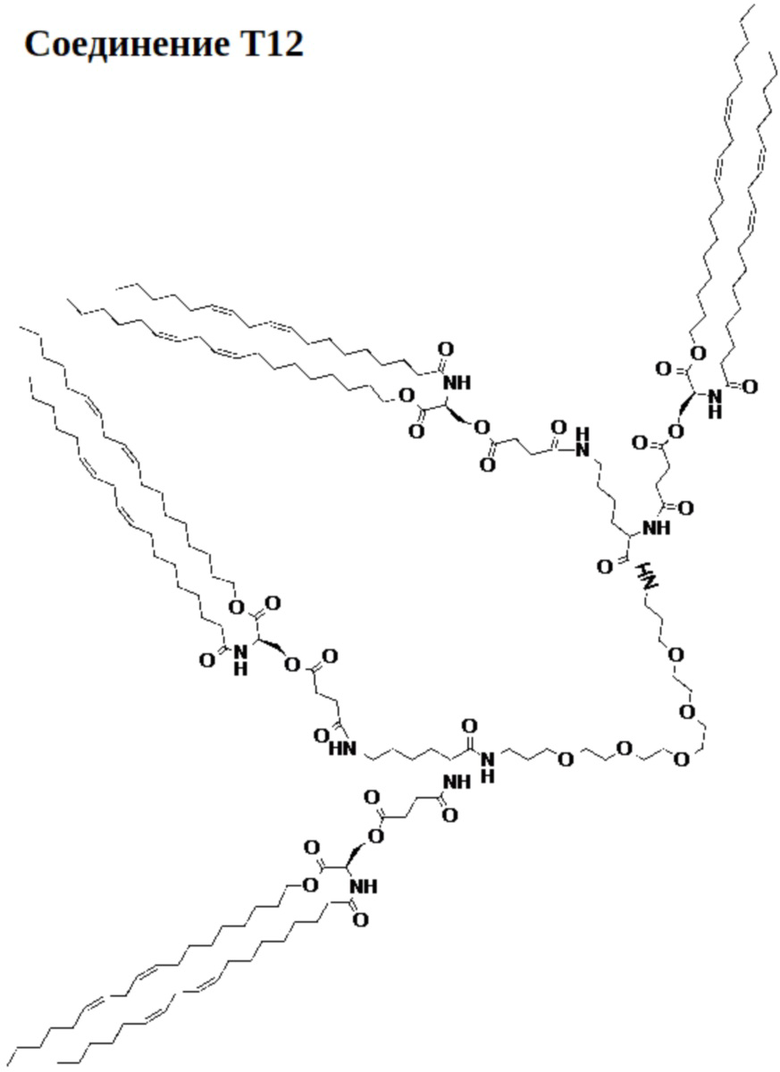 .
.
11. Фузогенное соединение по п. 1, где R4 и R5 в формуле VI независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу.
12. Фузогенное соединение по п. 1, где соединение представляет собой соединение Т11:
 .
.
13. Фузогенное соединение, имеющее формулу VII
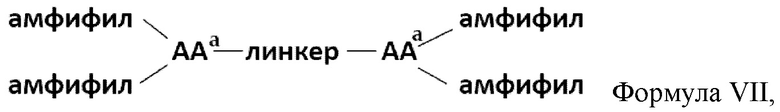
где каждый AAa независимо представляет собой аминокислоту, выбранную из следующих структур, или ее стереоизомер:
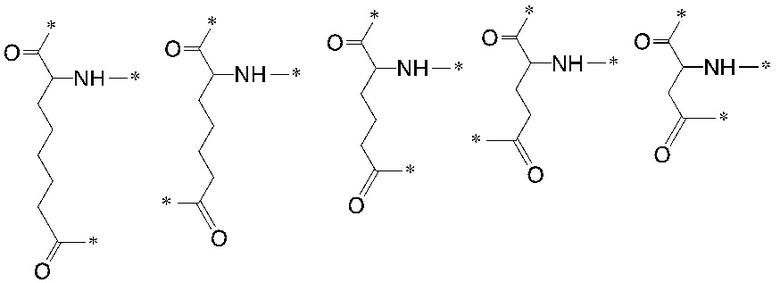
где аминокислота присоединена к амфифилу по каждой из своих карбоксильных групп и присоединена к линкеру на своем N-конце;
где линкер имеет структуру
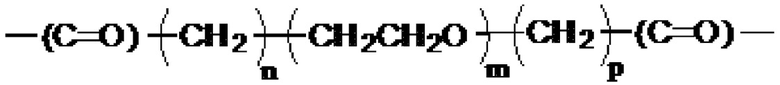
или
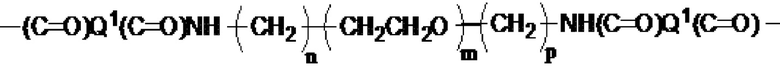 ,
,
где Q1 представляет собой разветвленный или неразветвленный C(2-8)алкандиил, или
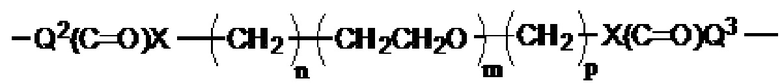 ,
,
где Q2 представляет собой
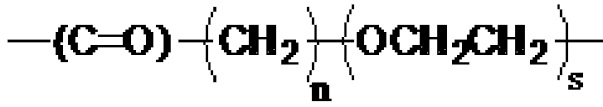 ,
,
где Q3 представляет собой
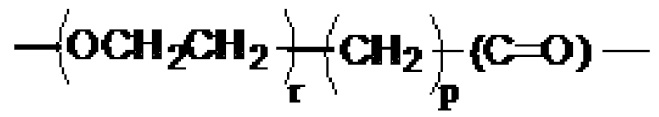 ,
,
где X представляет собой -O-, -S- или -NH-;
n и p независимо для каждого случая составляют от 1 до 3;
m независимо составляет от 1 до 10;
r и s независимо для каждого случая составляют от 1 до 5, где каждый амфифил независимо выбран из формулы VIII, формулы IX, формулы XI и формулы V:
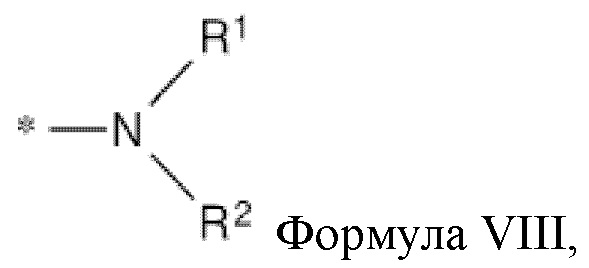
где R1 и R2 представляют собой
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4,
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
где n и m, каждый независимо, составляет от 1 до 2;
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
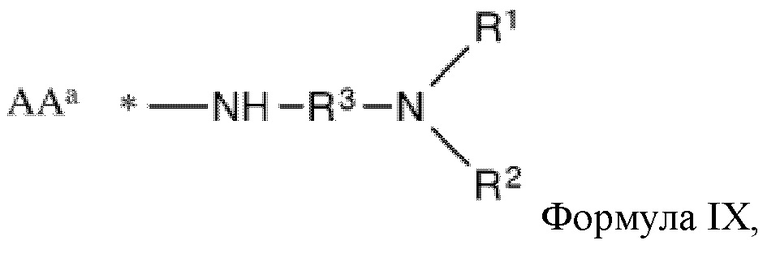
где R1 и R2 представляют собой
R1=CH2(CH2)nO(C=O)R4, CH2(CH2)nNH(C=O)R4, CH2(CH2)n(C=O)OR4, CH2(CH2)n(C=O)NHR4,
R2=CH2(CH2)mO(C=O)R5, CH2(CH2)mNH(C=O)R5, CH2(CH2)m(C=O)OR5, CH2(CH2)m(C=O)NHR5,
где n и m, каждый независимо, составляют от 1 до 2;
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 представляет собой разветвленный или неразветвленный С(1-8)алкандиил;
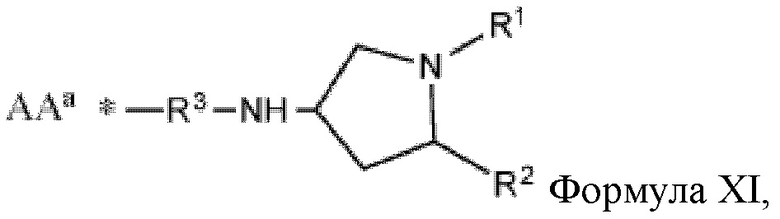
где R1 и R2 представляют собой:
R1=(C=O)OR4,
R2=(C=O)OR5,
R4 и R5 независимо для каждого случая представляют собой C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 представляет собой разветвленный или неразветвленный *-NH-C(1-8)алкандиил-(C=O)-, где * обозначает конец, присоединенный к AAa;
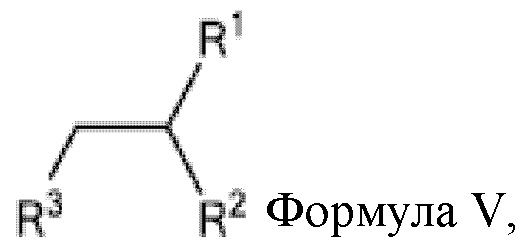
где R1 и R2 представляют собой:
R1=(C=O)OR4,
R2=(C=O)OR5,
где R4 и R5 представляют собой независимо для каждого случая C(12-20)алкильную группу или C(12-20)алкенильную группу;
где R3 представляет собой разветвленный или неразветвленный *-NH-C(1-8)алкандиил-(C=O)-, где * обозначает конец, присоединенный к AAa;
где один или два амфифила могут необязательно отсутствовать и заменены фармацевтически приемлемой органической химической группой, выбранной из алкильной группы, алкенила, алкинила, ацетила, Boc, Fmoc, TFA и CBZ, имеющей 1-400 атомов, выбранных из углерода, кислорода, азота, серы, фтора и водорода.
14. Фузогенное соединение по п. 13, где один или два амфифила отсутствуют и заменены фармацевтически приемлемой органической химической группой.
15. Фузогенное соединение по п. 14, где фармацевтически приемлемая органическая химическая группа выбрана из алкила, алкенила, алкинила, алкилового эфира, арилового эфира, алкокси- и алкоксиакоксигрупп.
16. Фузогенное соединение по п. 14, где фармацевтически приемлемая органическая химическая группа выбрана из метоксигруппы, этоксигруппы, трет-бутилового эфира и бензилоксигруппы.
17. Фузогенное соединение по п. 13, где R4 и R5 в формуле IX независимо для каждого случая представляют собой C(14-18)алкильную группу или C(14-18)алкенильную группу.
18. Фузогенное соединение по п. 13, где соединение представляет собой соединение T9:
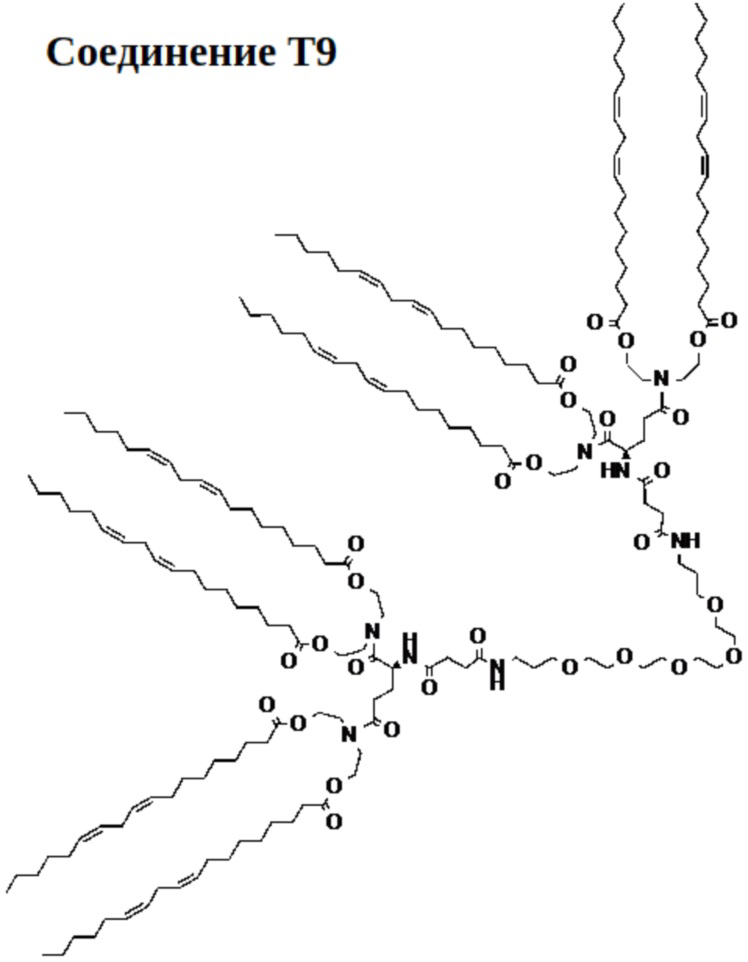 .
.
19. Композиция для применения для распределения действующего агента для лечения состояния или заболевания у субъекта, причем композиция содержит действующий агент, фузогенное соединение по любому одному из пп. 1-18, ионизируемый липид, структурный липид, стабилизирующий липид и липид для снижения иммуногенности композиции, где фузогенное соединение составляет 1-10 мол. % от композиции.
20. Композиция по п. 19, где действующий агент представляет собой одну или несколько нуклеиновых кислот.
| EA 20140857 A1, 30.12.2014 | |||
| EP 2998289 A1, 23.03.2016 | |||
| US 20110223257 A1, 15.09.2011 | |||
| EP 2069500 B1, 24.09.2014 | |||
| WO 2005026372 A1, 24.03.2005 | |||
| Самодоставляющие PHKi соединения уменьшенного размера | 2011 |
|
RU2615143C2 |
| RU 2015119409 A, 10.01.2017 | |||
| Способ преобразования выпрямленного напряжения постоянного тока | 1930 |
|
SU26374A1 |
Авторы
Даты
2023-12-05—Публикация
2018-11-06—Подача