Область техники
Настоящее изобретение относится к питательной композиции для младенцев или детей младшего возраста, специально адаптированной для ночного кормления, которая содержит смесь, способную имитировать эффект ночного грудного молока.
Питательная композиция изобретения содержит ионные комплексы лактоферрина с кислыми молочными белками, причем указанные комплексы имеют отрицательный заряд при рН детской смеси.
Композиция сочетает в себе пищевую ценность и структуру продукта питания, сформированную в виде функциональных блоков, близких к грудному молоку, что дает чувство насыщения и комфорт в кишечнике для улучшения циркадного цикла, обеспечения лучшего сна и ограничения ночного пробуждения.
Предпосылки создания изобретения
Изобретение относится к питательным композициям и их применениям в питательных композициях для младенцев и детей младшего возраста для стимулирования чувства насыщения, улучшения сна и/или ограничения ночного пробуждения. Питательные композиции содержат белки, углеводы и липиды. Питательная композиция изобретения представляет собой синтетическую композицию, т.е. искусственно созданную питательную композицию.
Грудное вскармливание считается идеальным источником питательных веществ и является предпочтительным выбором для кормления младенцев в возрасте до по меньшей мере 6 месяцев. Таким образом, в течение длительного времени при разработке детских смесей (IF) ориентировались на грудное молоко (HM). Хотя за последние десятилетия в питательных композиция IF наблюдаются заметные улучшения, все еще остаются значительные различия по сравнению с композицией и функциональными полезными эффектами, которыми обладает HM.
Самыми распространенными видами нарушения сна у младенцев и детей являются нарушения сна, связанные с бодрствованием (т.е. либо сложности при подготовке ко сну, либо отсутствие непрерывного сна в течение ночи). Было установлено, что эти нарушения встречаются у 15–35% младенцев младше 24 месяцев (France et al, "Infant Sleep Disturbance: Description of a problem behaviour process", Sleep Medicine Reviews, Vol 3, No 4, pp 265–280, 1999).
Процессы регуляции сна и бодрствования, а также состояний сна быстро меняются в первый год жизни и продолжают развиваться в течение детского возраста. В возрасте около 10–12 недель начинает проявляться циркадный ритм, и сон младенца все в большей степени приходится на ночное время. На характер сна и бодрствования также влияет взаимодействие биологических процессов и факторов окружающей среды, поведения и социальных факторов. Возрастные данные измерений сна в виде количества эпизодов сна в сутки, количества случаев пробуждения во время ночного сна, времени засыпания (латентный период сна), самого длительного эпизода сна в сутки и количества эпизодов короткого сна в дневное время у детей от рождения до 12-летнего возраста представлены в работе B.C. Galland et al., Normal sleep patterns in infants and children: A systemic review of observational studies, Sleep Medicine Reviews, 2012, 213–222. Качество сна (и, следовательно, улучшение качества сна) можно измерять любым традиционно известным способом, например, с помощью вышеуказанных параметров, а также по показателям фаз REM/NREM (фазы быстрого движения глаз / фазы небыстрого движения глаз).
Также есть данные о все более частых сменах режимов сна в ходе развития ребенка и о том, что влияние параметров времени сна на развитие ожирения, по-видимому, начинает сказываться по меньшей мере в раннем детстве (CA Magee et al., The longitudinal relationship between sleep duration and body mass index in children: a growth mixture modeling approach. J Dev Behav Pediatr. 2013, 34:165–173).
Таким образом, существует потребность в питательных композициях, которые помогают обеспечивать хорошее качество сна и/или нормальное время сна у младенцев и детей младшего возраста. В частности, существует потребность в питательных композициях, обеспечивающих такие полезные эффекты и при этом гарантирующих наиболее удовлетворительный энергетический баланс и потребление питательных веществ.
Лактоферрин представляет собой железосвязывающий гликопротеин, который является основным компонентом человеческого грудного молока. Считается, что молоко выполняет ряд биологических функций у младенцев, в том числе принимая участие в созревании кишечника, развитии иммунной системы, профилактике инфекций и всасывании железа. Лактоферрин в очень высоких концентрациях присутствует в молозиве человека (есть данные о концентрации до 10 г/л), причем его содержание в зрелом грудном молоке значительно уменьшается с возрастом младенца (2–3 г/л в возрасте 1 месяц, 1 г/л в возрасте 6 месяцев). На протяжении некоторого времени лактоферрин представляет интерес для применения в детской смеси, но его применению, по существу, препятствует высокая стоимость.
Применение лактоферрина в детской смеси в качестве пищевого ингредиента для стимуляции развития желудочно-кишечного тракта описано в EP 0 295 009.
WO2011/051482 относится к питательной композиции для младенцев и/или детей, содержащей лактоферрин и пробиотики для обеспечения полезных для здоровья эффектов.
Недавно было показано, что состав молока, и в частности уровень лактоферрина материнского молока, продуцируемого эпителиальными клетками молочной железы и секретируемого в молоко, естественным образом изменяется в зависимости от состояния здоровья и потребностей младенца (A.A Breakey et al., Evolution, Medicine and Public Health, 2015, volume 2015, 21–31).
Структура лактоферрина влияет на его биологическую активность. Его активность может модулироваться посредством взаимодействий с различными компонентами биологических жидкостей, в частности с компонентами грудного молока.
Добавление чистого лактоферрина в питательный состав зачастую затруднительно, так как лактоферрин сложно диспергировать в присутствии кислых молочных белков, таких как казеин или сывороточный белок, поскольку лактоферрин имеет изоэлектрическую точку примерно pH 9, в то время как у казеина или сывороточных белков изоэлектрическая точка составляет приблизительно pH 5.
Таким образом, добавление лактоферрина может вызывать образование агрегатов в контейнере для перемешивания, что приводит к формированию неоднородной дисперсии. В связи с этим желательно получить однородный состав с точки зрения, в частности, дисперсии белковых компонентов, обеспечивая при этом надлежащее количество лактоферрина в питательной композиции.
Альфа-лактальбумин (ALAC) является мажорным белком человеческого грудного молока (20–25% от общего содержания белков), относящимся к фракции сывороточных белков. Он также присутствует в коровьем молоке, хотя и в гораздо меньшей концентрации (2–5% от общего содержания белков). ALAC представляет собой небольшой (MW ≈ 14 кДа) кислый белок.
АLAC обеспечивает представляющие интерес полезные для здоровья эффекты, такие как противомикробное/противоинфекционное действие, иммуномодулирующий, антигипертензивный, противоопухолевый, антиоксидантный эффекты, стимуляция когнитивной функции. Есть данные о биодоступности триптофана из ALAC у младенцев (W. Heine et al., alpha-Lactalbumin-enriched low-protein infant formulas: a comparison to breast milk feeding, Acta Paediatr. 1996, 85, 1024–8).
Исследования эффекта триптофана показали, что его потребление влияет как на качество, так и на количество/продолжительность сна.
Триптофан представляет собой незаменимую аминокислоту, влияние которой на сон связано с его ролью в синтезе нейромедиатора головного мозга серотонина). Для реализации данного эффекта триптофану необходимо пройти через гематоэнцефалический барьер в головной мозг, где он используется для синтеза серотонина, который, в свою очередь, превращается в мелатонин. Серотонин представляет собой нейромедиатор, который влияет на настроение и аппетит, а также на другие процессы в организме, в то время как мелатонин является гормоном, очень важным для наступления сна (N. Schneider et al., Diet and nutrients in the modulation of infant sleep: A review of the literature, Nutritional Neuroscience, 2018, 21, 151–161).
О благоприятном эффекте ALAC, содержащегося в питании людей, и его влиянии на регуляцию циклов сна/бодрствования говорится в публикации D.K. Layman et al., Applications for α-лактальбумин in human nutrition, Nutr Rev. 2018,76, 444–460, где указано, что поступающий с пищей триптофан влияет на синтез как нейромедиатора серотонина в головном мозге, так и гормона мелатонина в кишечнике, которые участвуют в регуляции сна, и максимальные концентрации триптофана в грудном молоке наблюдаются в ночное время. В заключение авторы отмечают, что влияние смесей, обогащенных альфа-лактальбумином, на характер сна у младенца не изучен.
Продолжается изучение взаимосвязи содержания микроэлементов и характера сна (J. Xiaopeng et al., Public Health Nutr, 2017, 20(4), 687–701).
Кроме того, было высказано предположение о том, что содержание некоторых питательных веществ в грудном молоке подвержено циркадным изменениям, что свидетельствует об их роли в развитии и созревании циклов сна/бодрствования у младенца (N. Schneider et al., Nutritional Neuroscience, 2018, 21, 151–161). В частности, концентрации соединений-индукторов, таких как триптофан, нуклеотиды, гормоны и нейромедиаторы, колеблются в течение суток, а максимальных концентраций триптофан и мелатонин достигают в ночное время.
Таким образом, существует потребность в дальнейшей разработке питательных композиций для младенцев и детей младшего возраста, специально адаптированных для ночного кормления и способных имитировать действие ночного грудного молока, которое отличается от дневного грудного молока.
Существует потребность в создании питательных композиций для младенцев и детей младшего возраста, специально адаптированных для ночного кормления, в которых учитываются биохронологические требования посредством доставки питательных веществ и микроэлементов в то самое время, когда они будут способствовать улучшению сна и ограничению бодрствования.
Таким образом, целью изобретения является получение питательной композиции, адаптированной для ночного кормления, которую можно применять в повседневном рационе питания, адаптированном к состоянию младенца или ребенка младшего возраста (циркадный цикл, комфорт в кишечнике и т.д.), и которая будет создавать желаемое чувство насыщения и влиять на сон.
Кроме того, целью изобретения является получение питательной композиции, которая обеспечивает сбалансированное потребление питательных веществ и позволяет избегать перекармливания дополнительной бутылкой с обычной смесью в ночное время.
По существу, существует потребность в обеспечении вышеупомянутых полезных эффектов без влияния на любые другие параметры здоровья, такие как рост, развитие иммунной системы, когнитивное развитие или функции желудочно-кишечного тракта.
Существует потребность в обеспечении вышеупомянутых полезных эффектов с одновременным улучшением других параметров здоровья, например, непрямым стимулированием когнитивного развития (посредством высокого качества сна) и улучшением функций кишечника/переваривания (хорошее качество сна также связано с упрощением переваривания).
Существует потребность в обеспечении вышеупомянутых полезных эффектов при использовании питательной композиции у младенцев, в особенности у младенцев первых месяцев жизни, в качестве корректировки питания, а не в виде фармацевтического вмешательства (отдельного приема лекарственных средств).
Изложение сущности изобретения
В настоящее время было обнаружено, что питательная композиция, в которой лактоферрин представлен в форме ионных комплексов с молочными белками, может быть полезна для обеспечения желаемого чувства насыщения у младенцев и детей младшего возраста, а также может влиять на качество и количество сна, в частности посредством обеспечения надлежащих концентраций микроэлементов, таких как триптофан, таким образом предотвращая или ограничивая ночное пробуждение.
Преимуществом является то, что указанные ионные комплексы лактоферрина и ионные комплексы с молочными белками имеют структуру, близкую к структуре, в естественных условиях присутствующей в грудном молоке.
Без ограничений, накладываемых теорией, предполагается, что указанные ионные комплексы лактоферрина с молочными белками могут играть роль в обеспечении медленного переваривания белков, в частности сывороточных белков, таких как альфа-лактальбумин и бета-лактоглобулин, а также казеина и липидов, и надлежащем высвобождении микроэлементов, таких как минеральные вещества и витамины, таким образом обеспечивая желаемое чувство насыщения и влияние на сон.
В частности, было установлено, что для улучшения сна можно адаптировать состав минеральных веществ и витаминов посредством увеличения содержания микроэлементов, благоприятных для сна, таких как Fe, Zn, Mg и витамин D, и уменьшения содержания микроэлементов, отрицательно влияющих на сон, например, K или витамин В12, сохраняя при этом оптимальный баланс питательных веществ.
В первом аспекте изобретения предложена питательная композиция для младенцев и детей младшего возраста, содержащая белки, углеводы и липиды, причем указанные белки содержат ионные комплексы лактоферрина с кислыми молочными белками, при этом указанные комплексы имеют отрицательный заряд при рН детской смеси, а именно при рН 7,0 ± 0,5.
В частности, указанный кислый молочный белок выбран из группы, состоящей из альфа-лактальбумина (ALAC), бета-лактоглобулина (BLG), изолята сывороточного белка (WPI), гидролизованного WPI, казеина и их комбинаций.
Во втором аспекте питательная композиция изобретения применяется для обеспечения чувства насыщения, и/или улучшения сна, и/или ограничения ночного пробуждения у младенцев или детей младшего возраста. Преимуществом является то, что питательная композиция обеспечивает медленное переваривание сывороточных белков и надлежащее высвобождение микроэлементов.
В соответствии с одним вариантом осуществления питательная композиция изобретения применяется у младенцев или детей младшего возраста, имеющих расстройства сна, связанные с качеством сна или временем сна.
В соответствии с одним вариантом осуществления питательная композиция в соответствии с изобретением может представлять собой, например, детскую смесь, начальную детскую смесь или смесь для прикармливаемых детей либо смесь последующего уровня.
Изобретение особенно подходит для стимулирования более зрелого характера сна у младенцев и, следовательно, для улучшения качества их сна и уменьшения эпизодов бодрствования. В одном варианте осуществления изобретение связано с уменьшением выраженности нарушения сна и/или улучшением режимов сна у младенцев или детей младшего возраста.
В одном варианте осуществления улучшение качества или характера сна характеризуется, включает в себя или ограничено уменьшением количества эпизодов бодрствования и/или уменьшением фрагментации сна.
В одном варианте осуществления улучшение качества сна характеризуется более длительными ночами без вынужденного бодрствования и более спокойным сном.
В одном варианте осуществления улучшение качества сна характеризуется лучшей способностью засыпать.
Краткое описание графических материалов
На фиг. 1 представлено изменение дзета-потенциала комплексов лактоферрина (LF) и альфа-лактальбумина (ALAC) для различных концентраций ALAC при рН 6,0. С левой стороны черным треугольником обозначен дзета-потенциал только для LF, а черным кругом — дзета-потенциал только для ALAC.
На фиг. 2 представлено изменение дзета-потенциала комплексов LF и ALAC в зависимости от pH.
На фиг. 3 представлено изменение дзета-потенциала комплексов LF и ALAC в зависимости от pH после замораживания и размораживания.
На фиг. 4 представлено изменение дзета-потенциала комплексов LF (0,1%) и бета-лактоглобулина (Blg) для различных концентраций Blg при рН 7,0.
На фиг. 5 представлено изменение дзета-потенциала комплексов LF (1%) и бета-лактоглобулина (Blg) для различных концентраций Blg при рН 7,0.
На фиг. 6 представлено изменение дзета-потенциала комплексов LF (0,1%) и трипсинового гидролизата сывороточных белков (Lactry) для различных концентраций Lactry при рН 7,0.
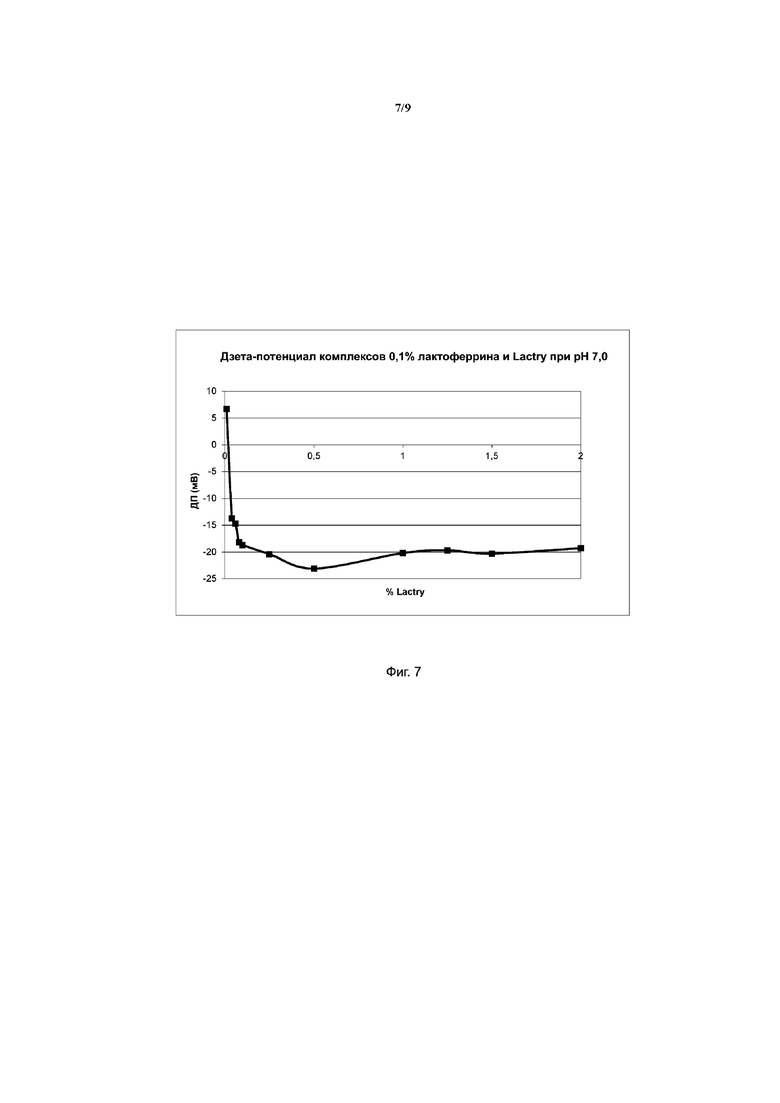
На фиг. 7 представлено изменение дзета-потенциала комплексов LF (0,1%) и трипсинового гидролизата сывороточных белков (Lactry) для различных концентраций Lactry при рН 7,0.
На фиг. 8 представлено изменение дзета-потенциала комплексов LF (2%) и бета-лактоглобулина (Blg) для различных концентраций Blg при рН 7,0.
На фиг. 9 представлено изменение дзета-потенциала комплексов LF (10%) и бета-лактоглобулина (Blg) для различных концентраций Blg при рН 7,0.
Подробное описание
Любую ссылку на документы предшествующего уровня техники в данном описании не следует рассматривать как признание того, что такой предшествующий уровень техники широко известен или составляет часть общеизвестных знаний в данной области.
В данном описании слова «содержит», «содержащий» и аналогичные слова не следует интерпретировать в исключительном или исчерпывающем смысле. Иными словами, предполагается, что они означают «включая, без ограничений».
Если не указано иное, все процентные значения, указанные в настоящем документе, приведены в мас./мас.
Все применяемые в настоящем документе технические и научные термины, если не дано их иное определение, имеют общепринятое значение, понятное среднему специалисту в данной области.
Термин «младенец» в контексте настоящего изобретения будет означать ребенка в возрасте до 12 месяцев.
Термин «ребенок младшего возраста» относится к ребенку в возрасте от 12 месяцев до 3 лет.
В контексте настоящего изобретения младенец может представлять собой любого доношенного младенца или недоношенного младенца. В одном варианте осуществления изобретения младенец выбран из группы недоношенных младенцев и доношенных младенцев.
Термин «детская смесь» (или IF), применяемый в контексте настоящего изобретения, относится к питательной композиции, предназначенной для младенцев в первые месяцы жизни, в соответствии с определением, приведенным в Codex Alimentarius (Кодекс STAN 72-1981), и к специальным продуктам для младенцев (включая продукты питания для специальных медицинских целей) в соответствии с определением, приведенным в Codex Alimentarius (Кодекс STAN 72-1981).
Термин «смесь для прикармливаемых детей» или «смесь последующего уровня» обозначает смеси, предназначенные для применения у детей в возрасте от 6 месяцев и обычно до 12 месяцев. Она составляет главный жидкий элемент в постепенно увеличивающемся разнообразии рациона питания младенцев.
Термин «молочная смесь для детей от 1 до 3 лет» обозначает смеси, предназначенные для применения у детей, начиная с одного года и обычно до возраста трех лет. По существу, это напиток на основе молока, адаптированный для специфических потребностей детей младшего возраста.
Термин «композиция для применения в смесях для младенцев или детей младшего возраста» в контексте настоящего изобретения также относится к самой смеси, например, детской смеси (IF), которая содержит все питательные вещества, необходимые для соответствия стандартам для детской смеси, определенным в Codex Alimentarius. Кроме того, «композиция для применения в смесях для младенцев или детей младшего возраста» может представлять собой композицию, содержащую питательные вещества, которую можно смешивать вместе с другими питательными веществами для получения смеси, т.е. такую «композицию для применения в составе для младенцев» можно добавлять в смесь, предназначенную для применения в качестве детской смеси.
В описании будут взаимозаменяемо применяться термины «ионные комплексы лактоферрина с молочным (-и) белком (-ами)» и «электростатические комплексы лактоферрина с молочным (-и) белком (-ами)».
Белки
Питательная композиция изобретения может содержать источник белка в количестве менее чем или равном 2,5 г/100 ккал, предпочтительно от 1,68 до 2,3 г/100 ккал, наиболее предпочтительно от 1,8 до 2,2 г/100 ккал.
Тип белка не считается критическим для настоящего изобретения, при условии, что соблюдены минимальные требования по содержанию незаменимых аминокислот и обеспечивается удовлетворительной рост.
В некоторых преимущественных вариантах осуществления в качестве источника белка в питательной композиции преобладают сывороточные белки (т.е. более 50% белков представлены сывороточными белками, например, 60% или 70%). В другом варианте осуществления содержание сывороточных белков составляет от 35 до 70% от общего содержания белков.
В частности, сывороточные белки можно применять в форме «мицелл сывороточного белка», как описано в EP183492, в форме жидкого концентрата или порошка.
Можно применять источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои.
В одном варианте осуществления изобретения питательная композиция содержит белок, который представляет собой смесь сывороточного белка и казеина, причем соотношение сывороточного белка и казеина составляет от 50 : 50 до 80 : 20. Например, соотношение сывороточного белка и казеина может составлять 70 : 30 для начальной смеси или 50 : 50 для смеси последующего уровня
Что касается сывороточных белков, то источник белка может быть основан на кислой молочной сыворотке или сладкой молочной сыворотке или на их смесях и может включать альфа-лактальбумин и/или бета-лактоглобулин в любых желаемых соотношениях.
В частности, можно применять сывороточный белок с содержанием альфа-лактальбумина по меньшей мере 10 мас.%, предпочтительно по меньшей мере 14 мас.%, более предпочтительно по меньшей мере 20 мас.%, по меньшей мере 25 мас.%, по меньшей мере 30 мас.%, или по меньшей мере 40 мас.%, или по меньшей мере 45 мас.%, или по меньшей мере 50 мас.%. Под выражением «сывороточный белок обогащен альфа-лактальбумином (ALAC)» в контексте настоящего изобретения следует понимать, что содержание ALAC в сывороточном белке выше, чем оно в естественных условиях содержится в сырье, из которого выделяют/экстрагируют сывороточный белок.
Например, если ALAC в естественных условиях присутствует в коровьем молоке в концентрации приблизительно 1,2–1,5 г/л и составляет приблизительно 18–20% от общего содержания сывороточных белков, то любое соотношение выше указанного представляет собой обогащение.
Например, в этом отношении можно применять сывороточный белок, обогащенный альфа-лактальбумином (ALAC), как описано в WO2018202636 или WO2003055322.
В одном варианте осуществления изобретения источник сывороточных белков обогащен комплексами лактоферрина с кислыми молочными белками, такими как альфа-лактальбумин (ALAC) и/или бета-лактоглобулин (BLG), как указано ниже.
В одном варианте осуществления изобретения источник белков обогащен комплексами лактоферрина с казеином, как указано ниже.
Изменение состава белков, в частности посредством увеличения содержания лактальбумина и/или обеспечения комплексов лактоферрина с кислыми молочными белками, позволяет имитировать состав грудного молока и обеспечивать благоприятное воздействие на стимулирование медленного высвобождения содержащегося триптофана, влияние которого на сон хорошо описано в публикациях.
Лактоферрин может представлять собой лактоферрин молозива человека, лактоферрин грудного молока или лактоферрин коровьего молока либо лактоферрин из другого источника. Предпочтительным источником лактоферрина является лактоферрин коровьего молока, который, как показано, обеспечивает ожидаемые полезные эффекты при добавлении в композицию изобретения.
Лактоферрин может быть выделен из молока животного или может представлять собой рекомбинантную форму лактоферрина (такую как рекомбинантный человеческий лактоферрин или рекомбинантный коровий лактоферрин). Лактоферрин, рассматриваемый в настоящем изобретении, может представлять собой чистый выделенный лактоферрин (или иметь высокую степень чистоты). В одном варианте осуществления лактоферрин содержится в обогащенной лактоферрином фракции и сопровождается другими питательными веществами. Лактоферрин может присутствовать в обогащенной лактоферрином фракции коровьего молока (под термином «обогащенный» подразумевается, что содержание лактоферрина выше, чем в интактном ингредиенте). Лактоферрин доступен в продаже и может поставляться, например, компаниями DMV International (Нидерланды), Murray-Goulburn (Австралия), Tatua (Новая Зеландия), Fonterra (Новая Зеландия), Milei/Morinaga (Германия/Япония).
Из-за высокой изоэлектрической точки лактоферрин имеет положительный заряд при физиологических условиях рН молока, что обеспечивает неспецифическое электростатическое связывание с, помимо прочего, другими молочными белками при экстракции лактоферрина из молока, обработке продукта или переваривании.
Ионные комплексы лактоферрина и кислых молочных белков (т.е. белков, имеющих изоэлектрическую точку ниже pH 7,0) могут быть получены, например, как описано в WO 2012/045801.
Однако ионные комплексы лактоферрина и кислых молочных белков, которые можно применять в соответствии с изобретением, могут быть получены и без соблюдения физико-химических требований (ионная сила, температура и т.д.), установленных для получения коацерватов в WO 2012/045801.
Например, указанные ионные комплексы лактоферрина могут быть получены следующим образом:
- получение белкового раствора посредством диспергирования лактоферрина в концентрации от 1 до 20% в воде
- получение растворов белка, диспергирующих кислый молочный белок или комбинацию кислых молочных белков в концентрации от 20 до 50%;
- доведение pH каждого раствора до одинакового pH, предпочтительно от 6,0 до 7,0;
- смешивание двух растворов белка в соответствии с предварительно определенными массовыми соотношениями.
Получение можно осуществлять при температуре от 4°C до 65°C, предпочтительно при комнатной температуре, например, от 15°C до 25°C.
В одном варианте осуществления массовое соотношение лактоферрина и кислого молочного белка находится в диапазоне от 1 : 0,25 до 1 : 3, в частности 1 : 1; 1 : 1,5 или 1 : 2.
Преимуществом является то, что лактоферрин добавляют к питательной композиции в форме комплексов с кислыми молочными белками, причем указанные комплексы имеют отрицательный заряд при pH детской смеси, т.е. при pH 7,0 ± 0,5.
Предпочтительно дзета-потенциал указанных комплексов при pH 7,0 составляет от -3 мВ до -20 мВ, предпочтительно от -10 мВ до -15 мВ при общем содержании белка 0,1%.
Отрицательный заряд можно изменять в зависимости от pH.
Преимуществом является то, что, как было показано, ионные комплексы лактоферрина и молочного (-ых) белка (-ов) в соответствии с комплексами изобретения были стабильными (поддержание дзета-потенциала) после замораживания и размораживания — физического процесса, который, как известно, сильно влияет на структуру белка.
Указанный кислый молочный белок можно выбирать, например, из группы, состоящей из альфа-лактальбумина (ALAC), бета-лактоглобулина (BLG), изолята сывороточного белка (WPI), концентрата белка молочной сыворотки (WPC), гидролизованного сывороточного белка, казеина и их комбинаций, которые доступны в продаже.
Как указано выше, «сывороточный белок» и полученные из него продукты могут быть представлены в виде препарата, в котором, например, альфа-лактальбумин и/или бета-лактоглобулин присутствуют в любых желаемых соотношениях.
Для цели настоящего изобретения можно применять все типы казеина. Однако для добавления в продукты для младенцев и детей младшего возраста, такие как детская смесь или смесь для прикармливаемых детей, предпочтительными являются β-казеин, κ-казеин и α-s1-казеин, более предпочтительно β-казеин, поскольку они в естественных условиях присутствуют в человеческом грудном молоке. В предпочтительном аспекте казеин представлен в форме мицеллярного казеина.
В одном варианте осуществления изобретения лактоферрин добавляют к питательной композиции в форме комплексов с кислым (-и) молочным (-и) белком (-ами), где:
- массовое соотношение лактоферрина и ALAC находится в диапазоне от 1 : 0,25 до 1 : 3, например 1 : 1; 1 : 1,5 или 1 : 2; и/или
- массовое соотношение лактоферрина и BLG находится в диапазоне от 1 : 0,25 до 1 : 3, например 1 : 1; 1 : 1,5 или 1 : 2; и/или
- массовое соотношение лактоферрина и казеина находится в диапазоне от 1 : 0,25 до 1 : 3, например 1 : 1; 1 : 1,5 или 1 : 2.
В одном варианте осуществления лактоферрин в форме ионных комплексов с
кислым (-и) молочным (-и) белком (-ами) может составлять от 1 мас.% до 20 мас.%, предпочтительно от 2 мас.% до 10 мас.% сывороточного белка.
В одном варианте осуществления лактоферрин в форме ионных комплексов с казеином может составлять от 1 мас.% до 20 мас.%, предпочтительно от 2 мас.% до 10 мас.% общего содержания белка.
Количество лактоферрина в настоящей композиции предпочтительно составляет от 2 г до 0,12 г на литр растворенной питательной композиции (или на литр готовой к употреблению жидкой композиции). В порошковой форме композиции количество лактоферрина может составлять, например, от 1,6 до 0,4 г сухой композиции (мас.%).
Белки могут быть нативными или гидролизованными либо они могут представлять собой смесь нативных и гидролизованных белков. Под термином «нативный» подразумевают, что основная часть белков является нативной, т.е. их молекулярная структура не изменена, например, не изменено по меньшей мере 80% белков, например, не изменено по меньшей мере 85% белков, предпочтительно не изменено по меньшей мере 90% белков, еще более предпочтительно не изменено по меньшей мере 95% белков, например, не изменено по меньшей мере 98% белков. В конкретном варианте осуществления не изменено 100% белков.
Может быть желательно вводить частично гидролизованные белки (степень гидролиза от 2 до 20%), например, младенцам, предположительно подверженным риску развития аллергии на коровье молоко. Если применяются гидролизованные белки, то процесс гидролиза можно проводить по желанию и так, как известно в данной области. Например, гидролизат сывороточного белка можно получать ферментативным гидролизом фракции молочной сыворотки на одной или более стадий. Если фракция молочной сыворотки, применяемая в качестве исходного материала, по существу, не содержит лактозы, установлено, что в процессе гидролиза блокировка лизина белка проявляется в гораздо меньшей степени. Это позволяет снизить степень блокировки лизина с приблизительно 15 мас.% общего лизина до менее приблизительно 10 мас.% лизина; например, приблизительно 7 мас.% лизина, что значительно улучшает питательное качество источника белка.
Липиды
Питательная композиция может содержать липиды в количестве, ниже или равном 6 г/100 ккал, например, от 4,0 до 6 г/100 ккал.
Это особенно важно, если питательная композиция изобретения представляет собой детскую смесь. В этом случае источником липидов может быть любой липид или жир, который подходит для применения в детских смесях. Некоторые подходящие источники жира включают пальмовое масло, структурированное триглицеридное масло, подсолнечное масло с высоким содержанием олеиновой кислоты и сафлоровое масло с высоким содержанием олеиновой кислоты, среднецепочечное триглицеридное масло. Можно также добавлять незаменимые жирные кислоты — линолевую кислоту и α-линоленовую кислоту, а также небольшие количества масел, содержащих большие количества арахидоновой кислоты и докозагексаеновой кислоты в готовом виде, например, рыбьи жиры или микробные масла. Соотношение жирных кислот n-6 и n-3 в источнике жира может составлять от приблизительно 5 : 1 до 15 : 1, например от 8 : 1 до 12 : 1.
Предпочтительно питательная композиция содержит линолевую кислоту, и/или линоленовую кислоту, и/или арахидоновую кислоту (ARA), и/или докозагексаеновую кислоту (DHA).
Углеводы
Питательная композиция в соответствии с настоящим изобретением, по существу, содержит источник углеводов. Это особенно предпочтительно в том случае, когда питательная композиция изобретения представляет собой детскую смесь. В этом случае можно применять любой источник углеводов, обычно находящийся в детских смесях, такой как лактоза, сахар, сахароза, мальтодекстрин, крахмал и их смеси, хотя одним из предпочтительных источников углеводов является лактоза.
Лактоза может составлять по меньшей мере 90%, предпочтительно по меньшей мере 98% углеводов, присутствующих в композиции.
Минеральные вещества и витамины
Питательная композиция может также содержать все витамины и минеральные вещества, которые считаются незаменимыми для ежедневной диеты, в значимых с точки зрения питания количествах. Для определенных витаминов и минеральных веществ установлены минимальные требования. Примеры минеральных веществ, витаминов и других питательных веществ, присутствующих в питательной композиции, включают витамин А, витамин В1, витамин В2, витамин В6, витамин B12, витамин Е, витамин К, витамин С, витамин D, фолиевую кислоту, инозитол, ниацин, биотин, пантотеновую кислоту, холин, кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлорид, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минеральные вещества обычно добавляют в форме соли.
В одном варианте осуществления изобретения минеральные вещества и витамины могут быть адаптированы для поддержания сна посредством увеличения содержания микроэлементов, способствующих наступлению сна, например, железа (Fe), цинка (Zn), магния (Mg) и витамина D.
В другом варианте осуществления изобретения минеральные вещества и витамины могут быть адаптированы для уменьшения содержания микроэлементов, отрицательно влияющих на сон, например, калия (K) или витамина В12.
Соответственно, количества Fe, Zn, Mg и витамина D, взятые по отдельности или в комбинации, могут находиться в следующем диапазоне:
- Fe: от 1 до 2, предпочтительно от 1,2 до 1,8 мг/100 ккал,
- Zn: от 0,7 до 1,5, предпочтительно от 1 до 1,5 мг/100 ккал,
- Mg: от 5,5 до 16,5, предпочтительно от 10 до 15 мг/100 ккал,
- витамин D: от 1 до 2,6, предпочтительно от 1,3 до 2,5 мкг/100 ккал,
а количества K или витамина В12, взятые по отдельности или в комбинации, могут находиться в следующем диапазоне:
- K: от 70 до 170, предпочтительно от 70 до 100 мг/100 ккал,
- витамин B12: от 0,25 до 1,5, предпочтительно от 0,25 до 0,8 мкг/100 ккал.
Другие минеральные вещества и витамины можно адаптировать в соответствии с возрастом, потребностями и/или состоянием сна младенца или ребенка младшего возраста.
Другие питательные вещества
При необходимости композиция изобретения может содержать эмульгаторы и стабилизаторы, такие как соя, лецитин, сложноэфирные моно- и диглицериды лимонной кислоты и т.п.
Композиция может также содержать другие вещества, которые могут оказывать благоприятный эффект, такие как нуклеотиды, нуклеозиды, ганглиозиды, полиамины и т.п.
Энергетическая ценность
Плотность калорий детской смеси для младенцев должна находиться в пределах 60–70 ккал/100 мл (Codex STAN 72-1981).
Преимуществом является то, что питательная композиция изобретения обеспечивает описанные полезные эффекты, одновременно обеспечивая соответствующую энергетическую ценность. Действительно, стимулирование улучшения сна младенца без увеличения общего потребления энергии, в особенности перед сном, может быть полезно, так как повышенное потребление энергии может отрицательно повлиять на общее развитие младенца и состояние его здоровья.
Таким образом, изобретение относится к обеспечению полезного влияния на сон без влияния на рост младенца и без перегрузки пищеварительной системы питательными веществами в количественном или качественном отношении, при которой переваривание может оказаться длительным или затруднительным.
В одном варианте осуществления энергетическая ценность композиции изобретения составляет менее 65 ккал/100 мл, или предпочтительно менее 62 ккал/100 мл, или от 60 до 65 ккал/100 мл, или предпочтительно от 60 до 62 ккал/100 мл.
В одном варианте осуществления питательная композиция изобретения обеспечивает описанные полезные эффекты, одновременно обеспечивая надлежащую энергетическую ценность. Действительно, стимулирование улучшения сна младенца без увеличения общего потребления энергии, в особенности перед сном, может быть полезно, так как повышенное потребление энергии может отрицательно повлиять на общее развитие младенца и состояние его здоровья.
Таким образом, изобретение относится к обеспечению полезного влияния на сон без влияния на рост младенца и без перегрузки пищеварительной системы питательными веществами в количественном или качественном отношении, при которой переваривание может оказаться длительным или затруднительным.
В одном варианте осуществления энергетическая ценность композиции изобретения составляет менее 65 ккал/100 мл, или предпочтительно менее 62 ккал/100 мл, или от 60 до 65 ккал/100 мл, или предпочтительно от 60 до 62 ккал/100 мл.
Формы питательных композиций для младенцев и детей младшего возраста
В соответствии с одним вариантом осуществления изобретения питательная композиция представляет собой детскую смесь.
Детская смесь в соответствии с настоящим изобретением может представлять собой начальную смесь для младенцев от рождения до 4–6 месяцев и обеспечивает полноценное питание для этой возрастной группы (как для доношенных, так и для недоношенных младенцев). Кроме того, детская смесь может представлять собой смесь для прикармливаемых детей в возрасте в диапазоне от четырех–шести месяцев до двенадцати месяцев, которую дают младенцам в комбинации с увеличивающими количествами продуктов питания, таких как детские каши и фруктовые, овощные пюре, и других продуктов питания по мере отлучения младенца от груди.
В соответствии с одним вариантом осуществления изобретения питательная композиция представляет собой молочную смесь для детей от 1 до 3 лет.
Питательная композиция настоящего изобретения может находиться в твердой (например, в форме порошка), жидкой или клейстеризованной форме. В частности, питательные композиции изобретения могут быть представлены в форме дегидратированных порошков, которые готовят к употреблению посредством растворения в воде или молоке.
Питательные композиции изобретения могут быть в текучей (жидкой) форме. Они могут продаваться готовыми к употреблению (без дополнительного разведения).
Единица с суточной дозой питательной композиции в соответствии с изобретением может представлять собой одноразовые капсулы, снабженные открывающим средством, содержащимся внутри капсулы, чтобы обеспечить сток растворенной детской смеси непосредственно из капсулы в приемную емкость, такую как бутылочка. Такой способ применения капсул для выдачи питательной композиции для младенца или ребенка младшего возраста описан в WO2006/077259. Разные питательные композиции могут быть упакованы в отдельные капсулы и предложены потребителю в групповых упаковках, содержащих достаточное количество капсул для удовлетворения потребностей младенцев и детей младшего возраста, например, в течение одной недели. Подходящие конструкции капсул описаны в WO2003/059778.
Приготовление питательных композиций
Питательные композиции в соответствии с настоящим изобретением можно приготовить любым известным или другим подходящим образом. Например, детскую смесь можно получать посредством смешивания источника белков, источника углеводов и источника липидов в соответствующих соотношениях. На данной стадии можно добавлять эмульгаторы, если они применяются. Витамины и минеральные вещества можно добавлять на этой стадии, но также можно добавлять и позднее, чтобы избежать термического разложения. Затем можно добавлять и примешивать воду, предпочтительно воду, очищенную обратным осмосом, или деионизированную воду для образования жидкой смеси. Температура смешивания предпочтительно должна быть комнатной, но также может быть выше. После этого жидкую смесь можно подвергать термообработке для снижения бактериальных нагрузок. Затем смесь можно гомогенизировать.
Если желательно получить порошковую композицию, гомогенизированную смесь высушивают в подходящем сушильном аппарате, таком как распылительная сушилка или сублимационная сушилка, и превращают в порошок.
Способы, применяемые при производстве смесей для младенцев и детей младшего возраста, основаны на представлении о том, что продукты должны иметь надлежащие питательные характеристики и должны быть микробиологически безопасными для употребления. Таким образом, ключевое значение в процессах производства имеют стадии, которые устраняют или ограничивают рост микроорганизмов. Технология обработки каждой конкретной смеси патентуется производителем, но в общем случае она включает консервирование эмульсии типа «масло в воде» посредством дегидратации в случае порошковых продуктов или стерилизации в случае готовых к употреблению или концентрированных жидких продуктов. Порошковую детскую смесь можно получать с применением различных процессов, таких как сухое смешивание дегидратированных ингредиентов для получения однородной смеси или гидратация и мокрое смешивание смеси макроингредиентов, таких как жировые, белковые и углеводные ингредиенты, с последующим выпариванием и распылительной сушкой полученной смеси. Можно применять комбинацию двух описанных выше процессов, когда сначала получают основу порошка посредством мокрого смешивания и распылительной сушки всех или некоторых из макроингредиентов, а затем посредством сухого смешивания добавляют остальные ингредиенты, включая углеводы, минеральные вещества, витамины и другие питательные микроэлементы, для создания готовой смеси. Жидкие смеси доступны в готовом к употреблению формате или в виде жидкого концентрата, который необходимо разводить водой, обычно в соотношении 1 : 1. Для производства этих продуктов применяются такие же процессы, как и для производства рекомбинированного молока.
Если желательно получить жидкую детскую смесь, гомогенизированную смесь разливают в подходящие контейнеры, предпочтительно асептическим способом. Однако жидкую композицию также можно автоклавировать в контейнере, подходящий аппарат для выполнения разливания и автоклавирования такого типа доступен в продаже.
Изобретение дополнительно описано со ссылкой на следующие примеры. Следует понимать, что изобретение в заявленном виде не будет каким-либо образом ограничено этими примерами.
Хотя изобретение описано посредством примера, следует понимать, что возможно внесение изменений и модификаций без отклонения от объема изобретения, определяемого пунктами формулы изобретения. Более того, если существуют эквиваленты конкретных признаков, такие эквиваленты включены так, как если бы они были конкретно упомянуты в настоящем описании».
Примеры 1–4 относятся к измерениям дзета-потенциала комплексов лактоферрина и альфа-лактальбумина (ALAC), бета-лактоглобулина (Blg) или гидролизата сывороточного белка (Lactry).
Примеры 5 и 6 относятся к питательным композициям в соответствии с изобретением.
Измерения дзета-потенциала
Материалы
Альфа-лактальбумин (ALAC) (партия 001-8-415-6-922) был приобретен в компании Davisco Foods International, Inc. (Le Sueur, MN, США). Содержание белка составляло 89,6% (анализ Кьельдаля: N x 6,38).
Бета-лактоглобулин (Blg) (партия JE 003-6-922) был приобретен в компании Davisco Foods International, Inc. (Le Sueur, MN, США). Содержание белка составляло 90,3%, а чистота — 97% (предоставлено поставщиком).
Лактоферрин (LF) (партия 10376514) был приобретен в компании DMV (Нидерланды). Содержание белка составляло 96,5%, а чистота — 88,2% (предоставлено поставщиком).
Lactry (трипсиновый гидролизат сывороточного белка) был приобретен в компании ARLA Foods (DK) (партия 26996513). Содержание белка определяли с помощью анализа Кьельдаля (Nt x 6,38).
Способы
Растворы белка (ALAC, Blg, LF или Lactry) готовили посредством диспергирования образца порошка (на основе чистоты) в воде Millipore (18,2 МОм.см) и доводили pH до 7,0 с помощью 1 M NaOH или 1 M HCl.
Дисперсию фильтровали при 0,22 мкм (Millipore Stericup&Steritop) и инкубировали в течение ночи при 4°C. В это время получали конечный препарат в желаемой концентрации.
В зависимости от желаемых диапазонов концентраций (1, 2, 10 или 20%) и массовых соотношений готовили маточные растворы для LF, ALAC и Blg, а рН доводили до рН 7,0 с помощью 1 M NaOH или 1 M HCl.
Конечное приготовленное количество составляло 250 мл.
Дзета-потенциал определяли по рассеянию света при приложении к измерительной ячейке переменного электрического поля при концентрации белка 0,1 мас.% после фильтрации через фильтры 0,22 мкм. Дисперсии при выбранных pH помещали в электрофоретическую подвижную ячейку и анализировали под углом рассеяния 173° с помощью Nanosizer ZS (Malvern Instruments, Великобритания), оснащенного лазером с длиной волны 633 нм. Эффективное электрическое поле E, приложенное к измерительной ячейке, составляло от 50 до 150 В в зависимости от электропроводности образцов. Определяли общую подвижность частиц и затем рассчитывали соответствующий дзета-потенциал (V) с помощью уравнения Смолуховского.
Пример 1. Комплексы лактоферрина (LF) и альфа-лактальбумина (ALAC)
На фиг. 1 представлено изменение дзета-потенциала комплексов лактоферрина (LF) и альфа-лактальбумина (ALAC) для различных концентраций ALAC при рН 6,0.
Результаты показывают, что LF и ALAC могут образовывать электростатические комплексы. При добавлении ALAC (от 1 мас.% до 4 мас.%) к LF 1 мас.% происходит нейтрализация исходного дзета-потенциала (+ 13 мВ), что указывает на образование электростатических комплексов, до тех пор, пока не будет наблюдаться насыщение заряда, когда дзета-потенциал достигает значения приблизительно -10 мВ.
Пример 2. Комплексы лактоферрина (LF) и альфа-лактальбумина (ALAC), полученные с содержанием белка 20%
1) Комплексы LF и ALAC, полученные с содержанием белка 20% в соотношении 1 : 1,25.
На фиг. 2 представлено изменение дзета-потенциала комплексов LF и ALAC, полученных с содержанием белка 20% в соотношении 1 : 1,25 при разных pH.
Для измерения дзета-потенциала образец разводили до содержания белка 0,1%. Результаты показывают, что комплексы отрицательно заряжены в диапазоне pH от 5,5 до 8,0.
2) Комплексы LF и ALAC, полученные с содержанием белка 20% в соотношении 1 : 1,25 после замораживания и размораживания
На фиг. 3 представлено изменение дзета-потенциала комплексов LF и ALAC, полученных с содержанием белка 20% в соотношении 1 : 1,25 при разных pH после замораживания и размораживания. Для измерения дзета-потенциала образец разводили до содержания белка 0,1%.
Образцы замораживали в течение ночи при -20°C в тестовых пробирках объемом 50 мл и оставляли при комнатной температуре для размораживания.
Результаты указывают на обнаружение тех же значений дзета-потенциала, хотя комплексы подвергались замораживанию и размораживанию, физическому процессу, который, как известно, сильно влияет на структуру белка.
В данном случае комплексы не подвергались разложению и демонстрировали высокую стабильность. Они отрицательно заряжены в диапазоне pH от 5,5 до 8,0.
Пример 3. Комплексы лактоферрина (LF) и бета-лактоглобулина (Blg)
На фиг. 4 представлено изменение дзета-потенциала комплексов LF (0,1%) и бета-лактоглобулина (Blg) для различных концентраций Blg при pH 7,0. В тестируемых условиях комплексы демонстрируют отрицательный заряд при соотношениях LF : Blg в диапазоне от 1 : 0,5 до 1 : 1.
На фиг. 5 представлено изменение дзета-потенциала комплексов LF (1%) и бета-лактоглобулина (Blg) для различных концентраций Blg при pH 7,0. В тестируемых условиях комплексы демонстрируют отрицательный заряд при соотношениях LF : Blg в диапазоне от 1 : 0,4 до 1 : 1.
Пример 4. Комплексы LF (0,1%) и гидролизата сывороточного белка (Lactry)
На фиг. 6 представлено изменение дзета-потенциала комплексов LF (0,1%) и трипсинового гидролизата сывороточного белка для различных концентраций Lactry при рН 7,0.
В тестируемых условиях комплексы демонстрируют отрицательный заряд в соотношениях LF : гидролизат сывороточного белка в диапазоне от 1 : 0,4 до 1 : 21.
На фиг. 7 представлено изменение дзета-потенциала комплексов LF (1%) и трипсинового гидролизата сывороточного белка для различных концентраций Lactry при рН 7,0. В тестируемых условиях комплексы демонстрируют отрицательный заряд в соотношениях LF : гидролизат сывороточного белка в диапазоне от 1 : 0,5 до 1 : 1.
Пример 5. Комплексы лактоферрина (LF) и бета-лактоглобулина (Blg) с концентрациями LF 2% и 10%
На фиг. 8 представлено изменение дзета-потенциала комплексов LF (2%) и бета-лактоглобулина (Blg) для различных концентраций Blg при pH 7,0. В тестируемых условиях комплексы демонстрируют отрицательный заряд в соотношениях LF : Blg в диапазоне от 2 : 0,7 до 2 : 2.
На фиг. 9 представлено изменение дзета-потенциала комплексов LF (10%) и бета-лактоглобулина (Blg) для различных концентраций Blg при pH 7,0. В тестируемых условиях комплексы демонстрируют отрицательный заряд в соотношениях LF : Blg в диапазоне от 1 : 0,4 до 1 : 0,2.
Пример 6. Начальная детская смесь
В таблице 1 ниже приведен пример композиции питательной смеси (начальная детская смесь) в соответствии с изобретением.
Таблица 1
альфа-линоленовая кислота
Таблица 1 (продолжение)
Таблица 1 (продолжение)
Пример 7. Смесь последующего уровня
В таблице 2 ниже приведен пример композиции питательной смеси (смесь последующего уровня) в соответствии с изобретением.
Таблица 2
альфа-линоленовая кислота
Таблица 2 (продолжение)
Пример 8. Детская смесь, имеющая энергетическую ценность менее 65 ккал/100 мл
Питательную смесь (начальную детскую смесь) в соответствии с изобретением готовили по таблице 1 примера 6, за исключением того, что содержание жира доводили до значений, позволявших получать энергетическую ценность 620 ккал на литр.








Изобретение относится к питательной композиции для младенцев и детей младшего возраста. Питательная композиция для младенцев или детей младшего возраста содержит белки, углеводы и липиды, причем указанные белки включают ионные комплексы лактоферрина с кислыми молочными белками. При этом указанные комплексы имеют отрицательный заряд при pH детской смеси, а указанный кислый молочный белок выбран из группы, состоящей из альфа-лактальбумина (ALAC), бета-лактоглобулина (BLG), изолята сывороточного белка (WPI), концентрата белка молочной сыворотки (WPC), гидролизата сывороточного белка, казеина и их комбинаций. Причем в ионном комплексе массовое соотношение лактоферрина и кислого молочного белка находится в диапазоне от 1:0,25 до 1:3. Изобретение позволяет получить стабильную питательную композицию, обеспечивающую чувство насыщения и/или улучшение сна и/или ограничивающую ночное пробуждение у младенцев или детей младшего возраста. 15 з.п. ф-лы, 9 ил., 2 табл., 8 пр.
1. Питательная композиция для младенцев или детей младшего возраста, содержащая белки, углеводы и липиды, причем указанные белки содержат ионные комплексы лактоферрина с кислыми молочными белками, при этом указанные комплексы имеют отрицательный заряд при pH детской смеси,
причём указанный кислый молочный белок выбран из группы, состоящей из альфа-лактальбумина (ALAC), бета-лактоглобулина (BLG), изолята сывороточного белка (WPI), концентрата белка молочной сыворотки (WPC), гидролизата сывороточного белка, казеина и их комбинаций;
и при этом в указанном ионном комплексе массовое соотношение лактоферрина и кислого молочного белка находится в диапазоне от 1:0,25 до 1:3, в частности 1:1, 1:1,5 или 1:2.
2. Композиция по п. 1, в которой указанный белок представляет собой смесь сывороточного белка и казеина, причем соотношение сывороточного белка и казеина составляет от 50:50 до 80:20.
3. Композиция по п. 2, в которой сывороточный белок обогащен альфа-лактальбумином (ALAC).
4. Композиция по п. 3, в которой содержание ALAC в сывороточном белке составляет по меньшей мере 10 мас.%, предпочтительно 14 мас.%, более предпочтительно по меньшей мере от 20 до 50 мас.%.
5. Композиция по любому из пп. 1–4, в которой лактоферрин в форме ионных комплексов лактоферрина с кислыми молочными белками составляет от 1 до 20%, предпочтительно от 2 до 10% от содержания сывороточного белка.
6. Композиция по любому из пп. 3–5, в которой указанный ионный комплекс имеет:
- массовое соотношение лактоферрина и ALAC в диапазоне от 1:0,25 до 1:3, предпочтительно 1:1, более предпочтительно 1:1,5, а наиболее предпочтительно 1:2; и/или
- массовое соотношение лактоферрина и BLG в диапазоне от 1:0,25 до 1:3, предпочтительно 1:1, более предпочтительно 1:1,5, а наиболее предпочтительно 1:2; и/или
- массовое соотношение лактоферрина и казеина в диапазоне от 1:0,25 до 1:3, предпочтительно 1:1, более предпочтительно 1:1,5, а наиболее предпочтительно 1:2.
7. Композиция по любому из пп. 1–6, в которой дзета-потенциал указанных комплексов при pH 7,0 составляет от -3 до -20 мВ, предпочтительно от -10 до -15 мВ при общем содержании белка 0,1%.
8. Композиция по любому из пп. 1–7, в которой липиды содержат линолевую кислоту, и/или линоленовую кислоту, и/или арахидоновую кислоту (ARA), и/или докозагексаеновую кислоту (DHA).
9. Композиция по любому из пп. 1–8, в которой указанный углевод состоит из по меньшей мере 90%, предпочтительно по меньшей мере 98% лактозы.
10. Композиция по любому из пп. 1–9, в которой количества Fe, Zn, Mg, витамина D, K или витамина B12, взятые по отдельности или в комбинации, составляют следующие значения:
- Fe: от 1 до 2, предпочтительно от 1,2 до 1,8 мг/100 ккал,
- Zn: от 0,7 до 1,5, предпочтительно от 1 до 1,5 мг/100 ккал,
- Mg: от 5,5 до 16,5, предпочтительно от 10 до 15 мг/100 ккал,
- витамин D: от 1 до 2,6, предпочтительно от 1,3 до 2,5 мкг/100 ккал,
- K: от 70 до 170, предпочтительно от 70 до 100 мг/100 ккал,
- витамин B12: от 0,25 до 1,5, предпочтительно от 0,25 до 0,8 мкг/100 ккал.
11. Композиция по любому из пп. 1–10, причем энергетическая ценность композиции составляет менее 65 ккал/100 мл, предпочтительно менее 62 ккал/100 мл, или от 60 до 65 ккал/100 мл, или предпочтительно от 60 до 62 ккал/100 мл.
12. Композиция по любому из пп. 1–11 для применения в обеспечении чувства насыщения, и/или улучшении сна, и/или ограничении ночного пробуждения у младенцев или детей младшего возраста.
13. Композиция для применения по п. 12, которая обеспечивает медленное переваривание белков, в частности сывороточного белка, и/или надлежащее высвобождение микроэлементов.
14. Композиция для применения по п. 12 или 13 у младенцев или детей младшего возраста, имеющих расстройства сна в отношении качества или времени сна, для улучшения качества или характера сна.
15. Композиция для применения по любому из пп. 12–14, причем улучшение качества или характера сна включает уменьшение количества эпизодов бодрствования, и/или уменьшение фрагментации сна, и/или более длительные ночные периоды без вынужденного бодрствования, и/или более спокойный сон, и/или улучшение способности засыпать.
16. Питательная композиция для применения по любому из пп. 12–15, которая представляет собой начальную детскую смесь или детскую смесь последующего уровня.
| CN 104012657 B, 13.04.2016 | |||
| WO 2012045801 A1, 12.04.2012 | |||
| WO 03055322 A1, 10.07.2003 | |||
| US 2014242050 A1, 28.08.2014 | |||
| US 2016193302 A1, 07.07.2016 | |||
| CN 108813632 A, 16.11.2018 | |||
| КОМПОЗИЦИЯ ПРЕБИОТИКОВ ДЛЯ НОРМАЛИЗАЦИИ МИКРОФЛОРЫ ОРГАНИЗМА | 2011 |
|
RU2473347C1 |
Авторы
Даты
2023-12-25—Публикация
2019-12-06—Подача