Родственные заявки
Данная заявка заявляет приоритет по первоначальной заявке США №62/776022, поданной 6 декабря 2018 года, содержание которой включено в данный документ посредством ссылки во всей своей полноте во всех отношениях.
Область изобретения
В данном документе описаны фармацевтические композиции, разработанные для эффективной доставки липофильных средств (например, молекул лекарственных средств и питательных веществ) к глазам, и способы использования вышеуказанного. Более конкретно, предусмотрены офтальмологические фармацевтические композиции для применения в лечении нарушений переднего и заднего сегментов глаза и для поддержания здорового состояния глаз. Офтальмологические фармацевтические композиции, описанные в данном документе, могут также быть использованы для замедления процесса старения глаза, например, за счет эффективной доставки к глазу питательных веществ (например, витамина D), которые оказывают оздоровительное благоприятное действие на него. Композиция может также использоваться в качестве медицинского изделия, которое, оказавшись на поверхности глаза, создают слой, который фильтрует электромагнитное излучение в разных длинах волн. Композицию можно также использовать в качестве медицинского изделия, которое облегчает симптомы и признаки патологических состояний глазной поверхности.
Предшествующий уровень техники
Глаз защищен множеством структур на передней поверхности глаза, включая веки, конъюнктиву и роговицу. Задние поверхности век покрыты слизистой оболочкой и конъюнктивой века, которая загибается на глаз, становясь бульбарной конъюнктивой. Эпителий бульбарной конъюнктивы носит непрерывный характер с эпителием роговицы, который составляет примерно 10% передней поверхности глаза и находится, где происходит большая часть постоянной рефракции. Эпителий роговицы имеет толщину 4-5 клеток, и его поверхностные клетки содержат много микроворсинок, структуры которых помогают в сохранении влаги поверхности эпителия в результате стимуляции адгезии слезной пленки. Слезная пленка смазывает внешнюю поверхность глаза, уменьшая, таким образом, силы трения, возникающие в результате моргания век глаза, наличия чужеродных частиц на поверхности глаза и вращательных движений глазного яблока. Слезная пленка также обеспечивает среду, которая переносит кислород из воздуха окружающей среды к роговице.
Внешняя поверхность глаза является чувствительной к повреждению, вызываемому разными повреждающими факторами из-за механического истирания роговицы; применения контактных линз; самопроизвольного отслоения эпителия; поврежденного эпителия и стромы после фоторефракционной кератэктомии; химических ожогов; на протяжении воздействия ультрафиолетового излучения, включая солнечный свет; системных заболеваний, таких как синдром Шегрена, синдром Стивенса - Джонсона, синдром рубцующего пемфигоида; хроническая эдема роговицы с рецидивирующей эрозией эпителия; нарушенное образование слезной пленки и состояния, являющиеся результатом эпителия, поврежденного радиальной кератотомией.
Старение также ассоциировано с расстройствами, являющимися результатом медленной регенерации эпителия. Плохое восстановление, связанное с возрастом, и клеточные патологии могут вызывать истончение эпителиального слоя и нарушенное прилипание эпителиального слоя к базальной пластинке, таким образом, уменьшая способность роговицы сохранять слезную пленку, что, в свою очередь, приводит к дальнейшему повреждению эпителия.
После повреждения эпителия роговицы соседние клетки немного сжимаются, закручиваются и начинают амебоидную миграцию от базального слоя через выступающую базальную мембрану, покрывая дефект новым монослоем клеток. Данные клетки затем приобретают характеристики нового базального слоя и подвергаются митозу с постепенным заполнением дефекта с полным дополнением четырех-пяти слоев клеток. Настоящая обработка ран роговицы включает нанесение глазных капель на поверхность для защиты тонкого процесса заживления от эрозии вследствие моргания и других источников механического трения. В настоящее время отсутствуют используемые лекарственные средства, которые стимулируют сам процесс заживления.
Электромагнитное излучение в разных длинах волн является генератором повреждения как поверхности, так и внутренних камер глаза. Документально подтверждено, что и УФ (ультрафиолет)-излучение и синий свет вызывают повреждение тканей и создают высокую окислительную нагрузку.
Краткое изложение сущности изобретения
Охваченные воплощения определены формулой изобретения, не данным кратким изложением сущности изобретения. Данное краткое изложение сущности изобретения является обобщенным обзором разных аспектов и вводит некоторые понятия, которые дополнительно описаны ниже в разделе Подробное Описание. Данное краткое изложение сущности изобретения не предназначено для идентификации ключевых или существенных признаков заявленного предмета, а также не предназначено для использования отдельно для определения объема заявленного предмета. Предмет следует понимать посредством ссылки на соответствующие части полного описания изобретения, частично или полностью на графические материалы и каждый пункт формулы изобретения.
Настоящее изобретение основано по меньшей мере частично на неожиданном открытии того факта, что наноэмульсии, описанные в данном документе, могут действовать как эффективный фильтр энергетического света в спектральном диапазоне рядом с видимым светом, который облегчает и усиливает защиту разных компонентов глаза от его вредного воздействия. Значимость данного раскрытия особо отмечена неожиданным открытием того факта, что наноэмульсии, описанные в данном документе, облегчают защиту компонентов глаза с минимальным - отсутствующим воздействием на спектральный диапазон видимого света.
Результаты, представленные в данном документе, обнаруживают, что неожиданные свойства композиций наноэмульсий, описанных в данном документе, включают липофильное средство, конкретно витамин D, который, как известно, является раздражительным для глаза, демонстрируя, что они могут быть приспособлены для максимизации доставки конкретных липофильных средств (например, молекул лекарственных средств и питательных веществ) к глазу, которые обычно не считаются переносимыми пациентами, особенно в случае увеличенной продолжительности.
В конкретном воплощении наноэмульсии, содержащие фосфолипиды, описанные в данном документе, демонстрируют следующие новые свойства:
- наноэмульсии фосфолипидов облегчают более продолжительное время контакта на поверхности роговицы, по сравнению с любыми другими формами глазных капель. Более продолжительное время контакта улучшает диффузию молекул лекарственного средства в эпителиальные клетки роговицы, улучшая, таким образом, эффективность лечения лекарственным средством;
- наноэмульсии фосфолипидов облегчают более тесный контакт между масляными, неполярными молекулами лекарственного средства и полярной поверхностью эпителиальных клеток роговицы. Напротив, тесный контакт не может быть достигнут без масляных глазных капель, поскольку физиологическая водная фаза образует полярный барьер, предотвращающий приближение масляных молекул. Наличие фосфолипидов в наноэмульсиях создает локализованную окружающую среду, где масляные молекулы могут быть погружены в водной фазе, таким образом, вступая в более тесный контакт с роговицей и улучшая поглощение масляных молекул клетками роговицы. Неожиданный эффект наноэмульсий, описанных в данном документе, обусловлен по меньшей мере частично локализованной окружающей микросредой, которую наноэмульсия фосфолипида создает по поверхности глаза и между масляной и водной фазами. Стабильная структура масляной фазы, по сравнению с водной фазой, дополнена и усилена присутствием погруженных масляных молекул в пределах водной фазы. См., например, Фиг. 1.
В одном аспекте представлена фармацевтическая композиция, содержащая витамин D в наноэмульсии фосфолипида, в которой витамин D находится в интервале от 0,2 до 2 масс./об. %, предпочтительно на уровне примерно 0,1 масс./об. %, фармацевтической композиции: где эмульгированные частицы в наноэмульсии фосфолипида имеют размер частиц, находящийся в интервале от 100 до 300 нанометров в диаметре; где фосфолипиды и витамин D в фармацевтической композиции находятся в соотношении по меньшей мере 3:1 и где фосфолипиды находятся в интервале от 0,1 до 5 масс./об. %, предпочтительно на уровне примерно 0,3 масс./об. %; и где терапевтически эффективное количество фармацевтической композиции является достаточным для поглощения света в диапазоне длин волн 220-520 нм. В одном его воплощении витамин D находится в интервале от 0,05 до 0,5% наноэмульсии фосфолипида. В еще одном его воплощении витамин D находится в количестве примерно 1000 мкг на 1 мл наноэмульсии фосфолипида или находится в количестве примерно 100 мкг на 1 мл. В еще одном его воплощении диапазон длин волн включает 230-520 нм. В более конкретных воплощениях диапазон длин волн включает 280-320 нм; диапазон длин волн включает 320-400 нм; диапазон длин волн включает 400-495 нм; диапазон длин волн включает 415-455 нм; или диапазон длин волн включает 280-315 нм. В одном его воплощении поглощение света измеряют с использованием спектрофотометра. В еще одном его воплощении фармацевтическая композиция не содержит сжиженный или сжатый газ-пропеллент.
В одном его воплощении фармацевтическая композиция предназначена для использования в уменьшении поглощения света в диапазоне длин волн 220-520 нм в глазах субъекта, нуждающегося в этом. В еще одном его воплощении фармацевтическая композиция предназначена для применения в уменьшении поглощения света в диапазоне длин волн 220-520 нм в глазах субъекта, нуждающегося в этом, где фармацевтическая композиция может быть введена на ткань роговицы глаз данного субъекта.
В одном его воплощении фармацевтическая композиция предназначена для уменьшения поглощения света в диапазоне длин волн 220-500 нм в глазах субъекта, нуждающегося в этом. В еще одном его воплощении фармацевтическая композиция предназначена для уменьшения поглощения света в диапазоне длин волн 220-500 нм в глазах субъекта, нуждающегося в этом, где фармацевтическая композиция может быть введена на ткань роговицы глаз данного субъекта.
В еще одном его воплощении фармацевтическая композиция предназначена для использования в лечении патологического состояния глаза у субъекта, нуждающегося в этом. В еще одном его воплощении патологическое состояние глаза включает по меньшей мере одно из воспаления глаза, сухого глаза или глаукомы.
В еще одном его воплощении фармацевтическая композиция предназначена для использования в получении лекарственного средства для уменьшения поглощения света в диапазоне длин волн 220-520 нм в глазах субъекта, нуждающегося в этом. В еще одном его воплощении фармацевтическая композиция предназначена для применения в получении лекарственного средства для уменьшения поглощения света в диапазоне длин волн 220-500 нм в глазах субъекта, нуждающегося в этом.
В еще одном аспекте представлена фармацевтическая композиция, содержащая витамин D в наноэмульсии фосфолипида, в которой витамин D содержится в интервале от 0,02 до 2 масс./об. % или 0,07-1,4 масс./об. % наноэмульсии фосфолипида в фармацевтической композиции: в которой эмульгированные частицы в наноэмульсии фосфолипида имеют размер частиц, находящийся в интервале от 100 до 300 нанометров в диаметре; в которой фосфолипиды и витамин D в фармацевтической композиции находятся в соотношении по меньшей мере 3:1 ив которой фосфолипиды находятся в интервале от 0,1 до 5 масс./об. %, предпочтительно в количестве примерно 0,3 масс./об. %; и в которой терапевтически эффективное количество фармацевтической композиции достаточно для доставки витамина D к ткани роговицы глаза на протяжении увеличенной продолжительности, где увеличенная продолжительность составляет по меньшей 1-10 минут. В его воплощении увеличенная продолжительность определяется посредством флуорофотометрии. В еще одном его воплощении увеличенная продолжительность составляет по меньшей мере одну минуту. В еще одном его воплощении увеличенная продолжительность составляет по меньшей мере одну минуту и меньше чем 12 минут. В еще одном его воплощении фармацевтическая композиция не содержит сжиженного или сжатого газа-пропеллента.
В одном его воплощении фармацевтическая композиция предназначена для применения в доставке витамина D к глазам субъекта, нуждающегося в этом. В еще одном его воплощении фармацевтическая композиция предназначена для применения в доставке витамина D к глазам субъекта, нуждающегося в этом, где фармацевтическая композиция может быть введена на ткань роговицы глаз субъекта.
В одном его воплощении фармацевтическая композиция предназначена для применения в лечении патологического состояния глаза у субъекта, нуждающегося в этом. В одном его воплощении патологическое состояние глаза включает по меньшей мере одно из воспаления глаза, сухого глаза или глаукомы.
В одном его воплощении фармацевтическая композиция предназначена для применения в получении лекарственного средства для лечения патологического состояния глаза у субъекта, нуждающегося в этом. В одном его воплощении патологическое состояние глаза включает по меньшей мере одно из воспаления глаза, сухого глаза или глаукомы.
В одном его воплощении фармацевтическая композиция выполнена с возможностью доставки витамина D к ткани роговицы с минимальным раздражением ткани роговицы.
В одном его воплощении фармацевтическая композиция включена в медицинское изделие.
В еще одном аспекте представлен способ уменьшения воздействия света на глаза субъекта, где свет включает диапазон длин волн 220-520 нм, причем данный способ включает: приведение ткани роговицы глаза в контакт с фармацевтической композицией, где терапевтически эффективное количество фармацевтической композиции является достаточным для поглощения света, включающего диапазон длин волн 220-520 нм. В одном воплощении способ дополнительно включает подвергание глаз субъекта воздействию света, включающего диапазон длин волн 220-520 нм, где приведение в контакт уменьшает количество света, включающего диапазон длин волн 220-520 нм, поглощаемое тканью роговицы глаз субъекта, с которыми контактирует фармацевтическая композиция, относительно количества света, поглощаемого тканью роговицы глаз субъекта до приведения в контакт с фармацевтической композицией, с уменьшением, таким образом, воздействия света, включающего диапазон длин волн 220-520 нм, на ткань роговицы глаз субъекта, с которыми контактирует фармацевтическая композиция. В еще одном воплощении количество света определяют, используя измеритель спектрального поглощения в нанокаплях.
В еще одном аспекте предложен способ лечения патологического состояния глаза у субъекта, нуждающегося в этом, причем способ включает: введение фармацевтической композиции в ткань роговицы глаз субъекта, где терапевтически эффективное количество фармацевтической композиции является достаточным для лечения патологического состояния глаза у субъекта. В одном воплощении патологическое состояние глаза представляет собой по меньшей мере одно из воспаления глаза, сухого глаза или глаукомы.
В одном конкретном воплощении предусмотрены наноэмульсии фосфолипида, содержащие витамин D. Витамин D представляет собой особенно сложный агент для доставки к глазу по многим причинам. Прежде всего, он является сложным, поскольку витамин D является раздражающим в отношении поверхности глаза. Соответственно, пациенты обычно не хотят терпеть дискомфорт, связанный с введением в глаз витамина D в любой форме. Доставка витамина D к глазу также является проблематичной, поскольку данное питательное вещество представляет собой масляную молекулу и само по себе имеет очень короткое время удерживания на поверхности глаза из-за природной водной окружающей среды поверхности глаза и полярной природы эпителия роговицы. Непродолжительное время удерживания витамина D на поверхности глаза, в свою очередь, затрудняет достижение минимальной терапевтической или другой концентрации витамина D на поверхности глаза.
Наноэмульсии фосфолипида, содержащие витамин D, обходят упомянутые выше проблемы, связанные с доставкой витамина D к глазу. Неожиданно, когда витамин D вводили в глаз в наноэмульсии фосфолипида, не выявлялось никакого раздражения. См. ниже Таблицы 1-6, в которых показано, что группа глазных капель витамина D (композиция витамин D-Lipitear; исследуемый препарат 1) не вызывает раздражения при введении животной модели, у которой рутинно оценивается раздражение глаза. Кроме того, когда витамин D был приготовлен в наноэмульсии фосфолипида, время удерживания на поверхности глаза было значимо увеличено. Эти данные демонстрируют, что наноэмульсии фосфолипида делают введение витамина D через местное нанесение непосредственно на глаз конкурентоспособной терапевтической схемой. Витамин D в форме наноэмульсий фосфолипида проникает в роговицу и внутреннюю камеру глаза до неожиданной степени, настоящие раскрытия также демонстрируют, что терапевтически эффективные количества витамина D могут быть доставлены к глазу посредством местного введения. Данные признаки обусловлены по меньшей мере частично увеличенным временем удерживания и более тесным контактом с эпителием роговицы, ставшим возможным за счет наноэмульсий фосфолипида, описанных в данном документе.
Настоящие наноэмульсии фосфолипида обеспечивают быстрое облегчение симптомов, связанных с недостатком витамина D в глазу, и эффективную доставку витамина D.
В конкретном воплощении наноэмульсии фосфолипида, содержащие витамин D, создают неожиданную физическую способность фильтровать электромагнитное излучение в разных длинах волн. Витамин D в наноэмульсии фосфолипидов, при введении в глаз и, таким образом, размещении по всей поверхности глаза, фильтровали синий свет и УФ-излучение. Данное свойство является неожиданным не только в аспекте качества, но также количественно, поскольку толщина наноэмульсии витамина D на поверхности глаза соответствует толщине слезной пленки, и еще продемонстрирована способность фильтровать электромагнитное излучение.
Изобретение в настоящее время будет проиллюстрировано со ссылкой на некоторые неограничивающие графические материалы и примеры.
Краткое описание графических материалов
Некоторые воплощения раскрытия описаны в данном документе исключительно в качестве примера со ссылкой на прилагаемые графические материалы. С конкретной ссылкой в настоящее время на графические материалы подробно, сделан акцент на том, что воплощения показаны в качестве примера и в целях иллюстративного обсуждения воплощений раскрытия. В данном отношении описание в сочетании с графическими материалами делает очевидным специалистам в данной области то, как можно использовать на практике воплощения раскрытия.
На Фиг. 1 представлено динамическое изображение, изображающее то, как композиции на основе наноэмульсий, описанные в данном документе, образуют динамическую структуру, содержащую три слоя на поверхности глаза. Самый верхний слой композиции/препарата на основе наноэмульсии, который находится дальше всего от роговицы, содержит масляную фазу; средний слой содержит фосфолипиды; и нижний слой, который находится в контакте с роговицей, содержит главным образом воду.
Фиг. 2 представляет собой фотографию микроскопического препарата, на котором расположена содержащая фосфолипид наноэмульсия, содержащая витамин D, толщиной слезной пленки.
Фиг. 3 представляет собой фотографию микроскопического препарата, на котором расположена содержащая фосфолипид наноэмульсия, содержащая витамин D, толщиной слезной пленки.
Фиг. 4 представляет собой фотографию микроскопического препарата, на котором расположена содержащая фосфолипид наноэмульсия, содержащая витамин D, толщиной слезной пленки, изображая референсное разрешение 20 линий 60 нанометров в ширину, над линией 1200 нанометров, как наблюдается при увеличении 40х.
Фиг. 5 представляет собой фотографию, изображающую разрешение через содержащую фосфолипид наноэмульсию, содержащую витамин D, толщиной слезной пленки, как описано в данном документе.
Фиг. 6 представляет собой гистограмму, изображающую свойства поглощения витамина D в воде, отдельно Lipimix или наноэмульсии витамина D (витамин D в Lipimix) в спектральном диапазоне синего света, как измерено через слой, толщиной слезной пленки.
Фиг. 7 представляет собой линейный график, изображающий свойства поглощения витамина D в воде, только Lipimix или наноэмульсии витамина D (витамин D в Lipimix) в спектральном диапазоне синего света, как измерено через слой, толщиной слезной пленки.
Фиг. 8 представляет собой линейный график, изображающий свойства поглощения витамина D в воде, только Lipimix или наноэмульсии витамина D (витамин D в Lipimix) в спектральном диапазоне УФ-В (280-315 нм), как измерено через слой толщиной слезной пленки.
Фиг. 9 представляет собой линейный график, изображающий свойства поглощения разных концентраций наноэмульсии витамина D или отдельно наноэмульсии в спектральном диапазоне УФ-синий свет, как измерено через слой толщиной слезной пленки.
Фиг. 10 представляет собой линейный график, изображающий свойства поглощения разных концентраций наноэмульсии витамина D или отдельно наноэмульсии в спектральном диапазоне УФ-синий свет, как измерено через слой толщиной слезной пленки. Концентрации представляют собой ×5 ниже относительно концентраций, используемых относительно 00, для стимуляции условий на поверхности глаза.
Фиг. 11 представляет собой линейный график, изображающий свойства поглощения витамина D в воде, отдельно Lipimix или наноэмульсии витамина D (витамин D в Lipimix) в спектральном диапазоне УФ-синий свет, измерения которых проводят параллельно с анализами, изображенными на Фиг. 8 и Фиг. 9.
Фиг. 12 А-С представляют линейные графики, изображающие свойства поглощения разных концентраций наноэмульсии витамина D или отдельно наноэмульсии в диапазоне (А) УФ-В; (В) диапазоне УФ-А; и (С) спектральном диапазоне синего света. Разные концентрации наноэмульсии витамина D являются такими же, как концентрации, изображенные на Фиг. 9.
Подробное описание изобретения
Среди тех преимуществ и улучшений, которые раскрыты, другие цели и преимущества данного раскрытия станут очевидными из следующего описания, во взаимосвязи с прилагаемыми графическими материалами. Подробные воплощения настоящего раскрытия раскрыты в данном документе; однако, следует понимать, что раскрытые воплощения лишь иллюстрируют данное раскрытие, которое может воплощаться в разных формах. Кроме того, каждый из примеров приведен в отношении разных воплощений раскрытия, которые предназначены для иллюстрации, и не для ограничения.
На протяжении описания изобретения и формулы изобретения следующие термины имеют значения, явным образом ассоциированные в данном документе, если контекстом явным образом не продиктовано иное. Фразы «в одном воплощении», «в воплощении» и «в некоторых воплощениях», в том виде, в котором они используются в данном документе, не обязательно относятся к одному(им) и тому(ем) же воплощению(ям), хотя и возможно. Кроме того, фразы «в другом воплощении» и «в некоторых других воплощениях», в том виде, в котором они используются в данном документе, не обязательно относятся к другому воплощению, хотя и возможно. Все воплощения раскрытия предназначены для того, чтобы быть комбинируемыми, не отклоняясь от объема и сущности раскрытия.
В том виде, в котором он используется в данном документе, термин «на основе» не является исключительным и позволяет быть основанным на дополнительных факторах, не описанных, если контекстом явным образом не продиктовано иное. Кроме того, на всем протяжении описания изобретения значение в единственном числе включает ссылки на множественное число. Значение «в» включает «в» и «на».
Все патенты, публикации и способы анализа предшествующего уровня техники, на которые ссылаются в данном документе, включены посредством ссылки во всей своей полноте.
Роговица представляет собой орган, лишенный сосудов, который получает питание из сосудистой системы лимба посредством диффузии. Она, таким образом, является чувствительной к лишению питательных веществ ввиду ее физиологически обособленного расположения. Кроме того, по той причине, что роговица представляет собой полутвердую структуру, содержащую клетки, которые сильно примыкают с образованием относительно непроницаемой ткани, она представляет собой сложный барьер для фармакологического вмешательства. Действительно, роговица представляет барьер, в который сложно диффундировать и который даже сложнее пересечь. Доставка молекул липофильного лекарственного средства к роговице особенно нарушается из-за полярной природы окружающей среды эпителия роговицы. В результате, липофильные молекулы повреждаются относительно их способности сталкиваться с эпителиальными клетками на уровне переднего сегмента глаза и, таким образом, даже менее вероятно могут оказывать фармакологическое действие в данных клетках. Дополнительные фармакологические проблемы возникают из-за плохого поглощения липофильных лекарственных средств через передний сегмент глаза, что снижает шансы достижения минимальной активной концентрации липофильного лекарственного средства в заднем сегменте. Объединенное влияние упомянутых выше проблем в отношении доставки липофильных лекарственных средств к глазу заключается в том, что вероятность достижения фармакологических эффектов на уровне заднего сегмента глаза чрезвычайно мала.
Эмульсии представляют собой носители лекарственного средства, используемые во множестве фармацевтических препаратов. Основное фармацевтическое преимущество эмульсий заключается в их способности объединять масляную фазу с водной средой, где поверхностное натяжение между маслом и водой поддерживается поверхностно-активными веществами. За последние годы разработаны новые методики получения наноэмульсий, в которых масляные капли имеют размер меньше чем 300 нанометров. Размер частиц в наноэмульсиях предлагает более стабильное термодинамическое состояние, по сравнению с регулярными эмульсиями. Фармацевтически, технология на основе наноэмульсий предлагает возможность приготовить местные эмульсии молекул лекарственных средств, которые не были стабильными с использованием ранее раскрытых методик. В качестве практичного носителя наноэмульсии в настоящее время используются в разных препаратах для местного применения.
Авторы настоящего изобретения раскрыли, что конкретные композиции на основе наноэмульсий, описанные в данном документе, могут неожиданно использоваться в качестве системы доставки лекарственных средств для доставки к глазу липофильных лекарственных средств и питательных веществ (например, витамина D). Неожиданное свойство данных композиций на основе наноэмульсий обеспечивает способность доставлять липофильные лекарственные средства и питательные вещества эффективно в и через барьер-роговицу. Местные препараты, предназначенные для применения для глаза, должны учитывать физические свойства глаза и трудности, связанные с ними. Поверхность роговицы является, например, очень гладкой и непрерывно промывается слезами и очищается посредством век глаза. Данные признаки минимизируют время удерживания, на протяжении которого терапевтическое средство или питательное вещество может поглощаться эпителием роговицы. Кроме того, плотные соединения между слоями эпителия роговицы делают роговицу относительно непроницаемой, делая почти невозможной диффузию молекул лекарственных средств в роговицу. Дополнительные проблемы возникают из-за липофильной структуры роговицы. Упомянутые выше физические свойства роговицы делают диффузию через роговицу с достижением задних сегментов глаза даже более проблематичной.
Результаты, представленные в данном документе, обнаруживают, что неожиданные свойства композиций на основе наноэмульсий, описанных в данном документе, могут быть заданы для максимизации доставки конкретных липофильных средств (например, молекул лекарственных средств и питательных веществ) к глазу, даже липофильных средств, которые, как известно, являются раздражителями для глаза и, таким образом, обычно не считаются переносимыми пациентами, особенно в случае увеличенной продолжительности. Типичное липофильное средство, для которого были оптимизированы композиции на основе наноэмульсий, описанных в данном документе, представляет собой витамин D.
Уникальные и неожиданные свойства композиций на основе наноэмульсий, описанных в данном документе, обеспечивают более длительное время удерживания на роговице, усиленный стабильный контакт между липофильными средствами и роговицей, и усиленное проникновение в роговицу. Относительно более длительного времени удерживания на роговице композиции на основе наноэмульсий, описанные в данном документе, имитируют поведение липидной фракции природной слезной пленки, поддерживая, таким образом, контакт между липофильным средством в композиции и роговицей на протяжении вплоть до нескольких минут. Это заметно контрастирует со стандартными композициями глазных капель, содержащими молекулы лекарственных средств, которые обычно остаются в контакте с роговицей в течение лишь нескольких секунд. Действительно, настоящие композиции на основе наноэмульсий разработаны для демонстрации увеличенных продолжительностей удерживания для контакта с роговицей, которые совпадают с липидной фазой слезной пленки на протяжении десяти минут. Соответственно, композиции на основе наноэмульсий, описанные в данном документе, обеспечивают терапию увеличенной продолжительности, достаточной для улучшения диффузии липофильных средств в эпителиальные слои роговицы и в задний сегмент глаза. Данные свойства максимизируют терапевтическую эффективность композиций на основе наноэмульсий, содержащих липофильные средства, описанные в данном документе.
Относительно обеспечения усиленного стабильного контакта между липофильными средствами и роговицей, композиции на основе наноэмульсий, описанные в данном документе, образуют динамическую структуру из трех слоев при введении в глаз. См. Фиг. 1. Самый верхний слой композиции на основе наноэмульсии, который является самым удаленным от роговицы, содержит масляную фазу; средний слой содержит фосфолипиды; и нижний слой, который контактирует с роговицей, содержит главным образом воду. Соответственно, водный слой находится в непосредственном контакте с роговицей и служит в качестве резервуара, в котором погружены эпителиальные клетки роговицы. Молекула лекарственного средства, таким образом, должно быть находится в водном слое в достаточной концентрации для достижения уровней поглощения, необходимых для достижения терапевтической эффективности. Поскольку липофильные молекулы термодинамически склонны к прилипанию к верхней масляной среде, они обычно исключаются из водного слоя, нарушая, вследствие этого, свою доставку к клеткам эпителия роговицы. Композиции на основе наноэмульсий, описанные в данном документе, преодолевают данное препятствие для доставки посредством создания динамической структуры, в которой сферы липофильных средств (например, молекул лекарственных средств или питательных веществ), окруженные фосфолипидами, непрерывно циркулируют в водном слое и доставляют туда липофильные молекулы в непосредственной близости к клеткам эпителия. Данный структурный/функциональный признак композиций на основе наноэмульсий, описанных в данном документе, создает динамическое равновесие, которое облегчает эффективную доставку липофильных молекул к эпителиальным клеткам роговицы и, таким образом, поглощение ими.
Относительно обеспечения усиленного проникновения в роговицу, композиции на основе наноэмульсий, описанные в данном документе, конкретно предназначены для проникновения в склеру и роговицу. Склера почти непроницаема, и роговица высокоустойчива к диффузии вследствие наличия специализированных тесных соединений между клетками роговицы. При применении в подходящих концентрациях и соотношениях, содержания фосфолипидов композиций на основе наноэмульсий по настоящему изобретению неожиданно действуют как усилители проникновения, которые стимулируют диффузию липофильных молекул в или через роговицу, обеспечивая, таким образом, лучшее поглощение липофильных молекул и полученную в результате улучшенную терапевтическую эффективность.
Объединенный эффект более продолжительного времени удерживания роговицей, усиленного стабильного контакта между липофильными средствами и роговицей и усиленного проникновения в роговицу придает композициям на основе наноэмульсий, описанным в данном документе, определенно большее поглощение липофильных молекул в передних и задних сегментах глаза. Соответственно, данные композиции на основе наноэмульсий обеспечивают эффективную систему доставки лекарственного средства к глазу для липофильных лекарственных средств и липофильных питательных веществ. В дополнение к вышеуказанному, представлены фармацевтические композиции для лечения расстройств переднего и заднего сегмента глаза, содержащие по меньшей мере одно липофильное средство (например, липофильное лекарственное средство или липофильное питательное вещество), фосфолипиды и офтальмологически приемлемый носитель.
Термин «лечение» относится к облегчению некоторых нежелательных симптомов разных расстройств глаза и/или к излечиванию расстройства глаза. Препараты и/или композиции на основе наноэмульсий можно также использовать для сохранения нормального здоровья глаза.
Термин «передний сегмент глаза» относится к эпителию роговицы и конъюнктивы и включает эпителиальные клетки, а также железы, находящиеся в эпителии.
Термин «расстройства переднего сегмента глаза» относится к расстройствам, которые вызывают или являются результатом физического повреждения по меньшей мере одного из эпителия роговицы или конъюнктивы, пониженной скорости регенерации в отношении клеток, содержащих эпителий роговицы или конъюнктивы, и уменьшенных секреций из желез, находящихся в эпителии конъюнктивы. Для лечения расстройств переднего сегмента глаза нужно достигать по меньшей мере минимальной концентрации, где активный фармацевтический ингредиент (API - от англ. active pharmaceutical ingredient) является фармакологически эффективным в переднем сегменте глаза.
Типичные расстройства переднего сегмента глаза, вызываемые физическим или химическим повреждением, являются результатом механической абразии роговицы, дефектов эпителия роговицы, создаваемых ношением контактных линз, дефектов эпителия роговицы, создаваемых самопроизвольным отслоением эпителия, повреждения роговицы после фотореактивной кератэктомии, травм, вызываемых химическими веществами, повреждения, вызванного воздействием ультрафиолетового излучения, системных заболеваний, которые повреждают эпителий роговицы и конъюнктивы, например, синдрома Шегрена, синдрома Стивенса - Джонсона, синдрома рубцующего пемфигоида, хронической эдемы роговицы с рецидивирующей эрозией эпителия и т.п.
Типичные расстройства переднего сегмента глаза, вызываемые уменьшением скорости регенерации клеток, включают повреждение глаза вследствие пожилого возраста или антипролиферативного лечения. Фармацевтическая композиция по настоящему изобретению может быть введена индивидам, страдающим от расстройств, которые вызывают повреждение эпителия роговицы или конъюнктивы или совместно с видами лечения, которые, как известно, вызывают такое повреждение, например, с лазерной или радиальной кератэктомией или введением разных системных или местных лекарственных средств.
Термин «фосфолипиды» относится к классу липидов, содержащих платформу глицерина или сфингозина, к которой присоединена одна или более жирных кислот, и фосфатную группу, с которой связан спирт. Встречающиеся в природе фосфолипиды включают, например, фосфатидилхолин, фосфатидилсерин и фосфатидилинозитол.
В конкретном воплощении масляная фаза содержит среднецепочечные триглицериды и/или растительное масло, включающее соевое масло, но, не ограничивающееся им. В более конкретном воплощении масляная фаза состоит из среднецепочечных триглицеридов и соевого масла.
Фармацевтические препараты и композиции, описанные в данном документе, содержат масляную фазу в пределах 0,1-20%, более конкретно 0,2-10%. Концентрация фосфолипидов должна находиться в пределах 0,01-10% (масса/объем). В конкретном воплощении фосфолипиды содержат 12% масляной фазы. Концентрация активного фармацевтического ингредиента может составлять всего лишь 0,0001% (масса/объем). Конкретные соотношения масляной фазы и содержания фосфолипидов регулируют в зависимости от конкретного активного фармацевтического ингредиента, добавляемого к препарату/композиции.
Фосфолипиды, используемые в фармацевтических препаратах/композициях, описанных в данном документе, включают, без ограничения, фосфолипиды, которые можно получать от коммерческих поставщиков, таких как, например Lipoid AG. Типичные фосфолипиды включают Е80 и S-75, которые могут быть приобретены у Lipoid AG.
Наноэмульсия витамина D в качестве средства защиты от УФ-излучения в форме глазных капель
Повреждающий эффект прямого солнечного света на кожу человека хорошо известен и подтвержден документально. Кожная эритема, пигментации и карциномы кожи все связаны с чрезмерным воздействием прямого солнечного света. Однако, свет высокой энергии и яркий свет также продуцирует значительное подтверждение глаза человека. Солнечная ретинопатия, фотокератит, точечный кератит и лучевая катаракта представляют собой лишь несколько примеров медицинских патологических состояний, относящихся к солнечному свету. Главное повреждение вызвано УФ-излучением (100-400 нм), переносом его энергии на роговицу, хрусталик и сетчатку при поглощении.
Повреждение ткани глаза показано неоднократно, чаще всего у профессиональных кадров и людей, которые тратят много времени на открытом воздухе, как например, военный персонал, работники сферы обслуживания, спортсмены водных видов спорта, зимних видов спорта и всех видов спорта на открытом воздухе, кто подвергается действию прямого солнечного света. Связанные с УФ заболевания глаза также находятся на подъеме и вызывают значительное беспокойство у лечащих врачей и систем здравоохранения. Согласно докладу о предупреждении травматизма армии США 2008 года, сверх 10% посещений с травмой глаз обусловлены фотокератитом и точечным кератитом, и те и другие подвержены сильному влиянию прямого солнечного света. Кроме того, исследования показали, что УФ-фотокератит может возникать, после всего лишь 30 минутного пребывания на солнце, которое подвергает среднестатистического человека воздействию пороговой дозы ежедневно. Солнечные очки действительно защищают глаз довольно хорошо, но они обладают ограничивающим эффектом на разрешающую способность глаза, и их использование не всегда применимо.
Как описано в данном документе, технология на основе наноэмульсий витамина D уменьшает УФ-излучение, которое проходит через тонкий слой, напоминающий природную слезную пленку на глазе. Композиция на основе наноэмульсий в виде глазных капель уменьшает количество излучения, достигающего ткани глаз. Композиция является эффективной в диапазоне УФ-В, причем данный диапазон является наиболее повреждающим в отношении глаза (280-320 нм). Наноэмульсии витамина D, описанные в данном документе, уменьшают интенсивность эффективного излучения вплоть до 75% при воздействии полного прямого солнечного света. Кроме непосредственной защиты от УФ, наноэмульсии витамина D, описанные в данном документе, поддерживают поверхность роговицы в гидратированном и смазанном состоянии, таким образом, продолжая делать поверхность глаза менее чувствительной к суровым условиям окружающей среды.
Прямое действие синего света на глаз
Хорошо известно, что использование переносных светоизлучающих устройств непосредственно перед сном оказывает биологическое действие, которое может способствовать сохранению недосыпа и нарушать циркадные ритмы, из которых и то и другое может оказывать вредное воздействие на производительность, здоровье и безопасность.
Совместно с увеличенным использованием компьютеров, имеет место одновременное увеличение цифрового перенапряжения глаз, причем примерно 50% пользователей компьютеров страдает от симптомов, которые попадают в данные две основные категории: симптомы, связанные со стрессом аккомодационного или бинокулярного зрения, и симптомы, связанные с внешними симптомами, связанными с сухим глазом.
Научная литература показывает, что действие синего света не ограничивается перенапряжением глаз, а что синий свет также оказывает прямое действие на глаз. Термин «опасность синего света» придуман для описания опасности данного света, которую данный свет представляет в отношении критических структур в пределах глаза, и компании, сосредоточенные на предотвращении, разрабатывают технологии для защиты глаза от данной опасности. Синий свет высокой энергии может проходить через роговицу и хрусталик до самой сетчатки, способствуя заболеваниям, таким как сухой глаз, катаракты и возрастная макулодистрофия, а также ингибированию секреции мелатонина и усилению продукции гормона коры надпочечников, наряду с другими вредными воздействиями. Исследователи предположили, что пользователи должны принимать соответствующие защитные меры при использовании продуктов, связанных с синим светом, особенно ночью.
Наблюдаемые эффекты включают эффекты на поверхности глаза. Исследователи показали, что применение терминалов визуального отображения на протяжении короткого периода времени может снижать стабильность слезной пленки у добровольцев и что режим ночной смены может вызывать меньшее повреждение поверхности глаза, чем нормальный режим. Исследователи сделали заключение, что синий свет высокой энергии из терминалов визуального отображения может представлять собой фактор риска в повреждении поверхности глаза. Однако, данное повреждение может быть исправлено.
Большое исследование было проведено для определения механизмов повреждения глаза, вызываемого синим светом. Исследования in vitro синего света на эпителиальных клетках роговицы человека показали, что синий свет увеличивает продукцию активных форм кислорода (АФК) и связанное с ними повреждение. Исследования на заболевании сухого глаза показали связь между гиперосмолярностью слезной пленки и тяжестью воспаления, вызванного посредством сигнальных путей, индуцируемых АФК. Также исследовали воздействие видимого света на эпителиальные клетки роговицы человека и воздействие природных антиоксидантов на окислительный стресс, вызванный чрезмерным воздействием света.
Другие исследователи исследовали влияние чрезмерного воздействия света, происходящего из светоизлучающего диода (СИД), с разными длинами волн на поверхность глаза мыши. Они сделали вывод, что чрезмерное воздействие синего света с короткими длинами волн может вызывать окислительное повреждение и апоптоз роговицы, которые могут быть выражены в виде увеличенного воспаления поверхности глаза и полученного в результате сухого глаза. Также показано, что гиперосмолярный стресс влияет на фототоксичность, что дополнительно указывает на то, что пациенты с болезнью сухого глаза могли быть более чувствительными к токсичности синего света в отношении глаза. Действительно, ранее показано, что пациенты с сухим глазом имеют значимое улучшение в средней функциональной остроте зрения и доли сохранения зрения при ношении очков с линзами, блокирующими синий свет на 50%, эффект не наблюдали в здоровых контролях.
Воздействие синего света не ограничивается поверхностью глаза. Повреждение синим светом сетчатки поддержано исследованиями как с кратковременным, так и длительным воздействием. Сетчатка наиболее чувствительна к свету при более коротких длинах волн (максимальная чувствительность показана при 441 нм). Повреждение сетчатки при более коротких длинах волн видимого света (вплоть до 500 нм) главным образом было фотохимическим по своей природе (по сравнению с исключительно тепловым действием). Фотохимическая травма сетчатки от синего света, кроме того, показана как in vitro, так и in vivo. Исследования in vitro клеток сетчатки человека идентифицировали клеточные сигнальные пути, которые приводят к окислительному повреждению, которое увеличивает риск фотоповреждения сетчатки и способствует развитию возрастной макулопатии. Даже при низкой интенсивности, используемой в визуальных устройствах отображения, синий свет может индуцировать продукцию АФК и апоптоз в клетках сетчатки. Исследования in vivo с воздействием синего света СИД показали, что такое воздействие вызывает травму сетчатки у находящихся в сознании, проблемно-ориентированных животных с преобладанием палочек. Данное повреждение может быть вызвано коммерческими светоизлучающими диодами (СИД), причем фототоксичность характеризуется тяжелым повреждением фоторецепторов и индукцией некроза. Дополнительное исследование in vivo (крысиная модель) показала, что синий компонент СИД с белым спектром излучения может вызывать токсичность у сетчатки при внутренней освещенности на рабочем месте и не только в экстремальных условиях эксперимента. Современные нормы и стандарты по освещению установлены в отношении сильного кратковременного воздействия света и не учитывают эффекты повторяющегося воздействия.
Интересно, также показано, что синий компонент белого света вызывает дисфункцию гематоретинального барьера на уровне пигментного эпителия сетчатки. Исследователи предположили, что фильтр, блокирующий синий свет, нужно использовать в офтальмологических операциях на человеке при использовании операционного микроскопа.
Фильтры можно использовать для уменьшения воздействий синего света. У пациентов с сухим глазом фильтры синего света (обматываются вокруг защитных очков) использовались для попытки улучшить синдром компьютерного зрения. Исследователи показали уменьшенные балльные оценки опросника жалоб на состояние глаз со всеми уровнями фильтров. Другие исследования показали уменьшение в критической частоте слияния мельканий и боли вокруг/внутри глаз и меньшее чувство зуда после задачи. Очковые линзы, фильтрующие синий свет, могут частично фильтровать коротковолновый свет высокой энергии по существу без деградации зрительной работоспособности и качества сна. Данные линзы могут служить в качестве дополнительного варианта для защиты сетчатки от потенциальной опасности синего света.
Фильтры синего света использовали in vitro. Одно такое исследование рассматривало облучение синим светом первичных клеток человека, происходящих из поверхности роговицы. При оценке жизнеспособности через 24 часа после дозы синего света сделали вывод о том, что синий свет травмирует клетки поверхности глаза. Клетки защищены от повреждения посредством тени. Исследователи рекомендовали защиту от синего света для сохранения здоровья глаза, особенно у популяций, находящихся в зоне высокого риска, таких как люди с сухим глазом, люди, использующие контактные линзы, люди, имеющие неполноценное питание, и пожилые люди. В действительности, вставка внутриглазных линз, фильтрующих синий свет, которые имитируют природный человеческий хрусталик глаза, используется с 1980-х годов у пациентов с катарактой. Обзоры доступных клинических исследований по данным внутриглазным фильтрам указывают на то, что они должны рассматриваться как безопасная и относительно недорогая превентивная мера для снижения возможного риска фототоксичности в отношении сетчатки и связанного с этим возможного риска возрастной макулодистрофии (AMD - от англ. age-related macular degeneration) в псевдофакических глазах.
Увеличенное время удерживания
Как указано выше в данном документе, поверхность глаза является уникальной тканью, которая создает сложную среду для доставки терапевтических молекул в терапевтически эффективных количествах. Гладкость поверхности, постоянный поток слез и регулярное перемещение век глаза уменьшают количество времени, имеющееся для поглощения терапевтических молекул эпителием роговицы. Это является проблематичным для гидрофильных молекул и даже более проблематичным для липофильных молекул, которые должны преодолевать свое физико-химическое отклонение от полярной среды поверхности глаза. При условии, что витамин D представляет собой масляную/липофильную молекулу, он имеет очень короткое время удерживания на поверхности глаза при введении в него местно. Данное явление обусловлено природной водной средой поверхности глаза и обусловлено полярностью эпителия роговицы в комбинации с потоком слез и «сметающим» эффектом век глаза. Полученное быстрое удаление витамина D с поверхности глаза очень усложняет местное введение витамина D в глаз в эффективных количествах для обеспечения терапии или питания. Неожиданное открытие того, что конкретные комбинации витамина D в фосфолипид-содержащих наноэмульсиях демонстрируют увеличенное время удерживания на поверхности глаза при нанесении местно на глаз, и, таким образом, облегчение усиленного поглощения витамина D эпителием роговицы решило проблему того, как вводить терапевтически и/или питательно эффективные количества витамина D в глаз местно, не вызывая раздражения. Данные результаты привели к получению местных, глазных фосфолипид-содержащих композиций на основе наноэмульсий, содержащих витамин D, и способов использования вышеуказанного.
Концентрации и соотношения
Ввиду вышесказанного, предусмотрены конкретные композиции витамина D в фосфолипидной наноэмульсии, где размер частиц эмульгированных частиц находится в интервале, имеющем диаметр 100-300 нанометров; концентрация витамина D находится в интервале от 0,02 масс./масс. % до 2 масс./масс. %; и фосфолипиды находятся в конкретном интервале соотношении, обычно 3:1, с содержанием витамина D в композиции. Витамин D, включенный в композиции, описанные в данном документе, может находиться в неактивной, частично активной или активной форме.
В конкретном воплощении фосфолипидсодержащая наноэмульсия, содержащая витамин D, выглядит следующим образом:
- инертная наноэмульсия (без API) содержит 0,3 масс./об. % фосфолипидов;
- фосфолипиды содержат по меньшей мере один из фосфолипидов яйца и сои;
- концентрация фосфолипидов варьирует от 0,1% до 10 масс./об. %;
- концентрация витамина D находится в интервале от 0,001 до 1 масс./об. %. В конкретном воплощении концентрация витамина D составляет 0,01 масс./об. %;
- фосфолипид-содержащую наноэмульсию, содержащую витамин D, вводят по каплям, где каждая капля составляет приблизительно 0,05 мл.
В конкретном воплощении препараты/композиции, содержащие витамин D в наноэмульсии фосфолипида, описанной в данном документе, не содержат сжиженного или сжатого газа-пропеллента. Иными словами, препараты/композиции, содержащие витамин D в наноэмульсии фосфолипида, как описано в данном документе, содержат 0% сжиженного или сжатого газа-пропеллента.
Соответственно, настоящие препараты/композиции, содержащие витамин D, в наноэмульсии фосфолипида, не являются пенными аэрозолями.
Композиции, описанные в данном документе, являются прозрачными и не содержат сильных поверхностно-активных веществ, которые используются в пенных аэрозолях. Такие сильные поверхностно-активные вещества противопоказаны, по меньшей мере поскольку они будут раздражать глаз.
Как понятно в данной области и определено, например, в фармакопее США, пропеллент создает необходимое давление в аэрозольной системе для выталкивания вещества из контейнера и, в комбинации с другими компонентами, для превращения вещества, в которое он включен, в желательную физическую форму. Пропелленты широко классифицированы как сжиженные или сжатые газы, имеющие давления насыщенного пара, обычно превышающие атмосферное давление.
Как понятно в данной области и определено в, например, Фармакопее США, пенный аэрозоль представляет собой эмульсию, содержащую один или более активных ингредиентов, поверхностно-активных веществ, водных или неводных жидкостей и пропеллент/пропелленты.
Размер частиц
Как описано в данном документе, эмульгированные частицы в наноэмульсии фосфолипида имеют размер частиц, находящийся в интервале 100-300 нанометров в диаметре. В конкретных воплощениях эмульгированные частицы в наноэмульсии фосфолипида имеют размер частиц, находящийся в интервале от 100-150, 100-200, 100-250, 100-300, 150-200, 150-250, 150-300, 200-250, 200-300 или 250-300 нанометров (нм) в диаметре. В конкретном воплощении эмульгированные частицы в наноэмульсии фосфолипида имеют размер частиц примерно 200 нм в диаметре. В конкретном воплощении эмульгированные частицы в наноэмульсии фосфолипида содержат популяцию эмульгированных частиц, имеющую средний размер частиц примерно 200 нм в диаметре. В еще одном конкретном воплощении эмульгированные частицы в наноэмульсии фосфолипида содержат популяцию эмульгированных частиц, где 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% или более популяции имеют средний размер частиц примерно 200 нм в диаметре.
Витамин D
Витамин D играет существенную роль в организме человека и является важным в поддержании нормальной функции во множестве систем органов. Знания авторов изобретения относительно влияния недостатка витамина D существенно растут, и специалисты здравоохранения удовлетворяют вновь признанные потребности посредством прописывания регулярной добавки витамина D. Системы органов и их функции, на которые пагубно влияет недостаток витамина D, включают, без ограничения: минерализацию кости, слабость мышц, иммунную систему и сердечно-сосудистую систему.
Ученые и практикующие врачи недавно сконцентрировали свое внимание на важности витамина D для системы глаза. Было показано, что витамин D крайне способствует жизнеспособности и здоровью глаз со значительным участием как на переднем, так и на заднем сегменте глаза.
Клетки роговицы, например, могут превращать Витамин D в его активный метаболит 1.25D3 (витамин D3), способом, напоминающим процесс превращения, который протекает в коже. Кроме того, также было показано, что эпителиальные клетки роговицы продуцируют витамин D de novo при воздействии УФ-В. Данные основные способности обнаруживают биологическую значимость витамина D в системе глаза и подтверждают целый ряд фундаментальных и клинических исследований, в которых был задействован витамин D и система глаза и их функции. Дополнительное доказательство связи между витамином D и системой глаза обнаружено в идентификации положительной корреляции между миопией и уровнями витамина D в сыворотке в большой популяции исследуемых субъектов, являющихся человеком. Дополнительные исследования подтвердили данные результаты и утвердили, что исследуемые участники с миопией имели более низкие уровни витамина D. Оптическая когерентная томография (СТ - от англ. coherence tomography) для измерения патологических изменений, предшествующих заболеванию, также обнаружила, что недостаток витамина D ассоциирован с уменьшенной толщиной макулы.
Дополнительные исследования показали, что пациенты с возрастной макулодистрофией (AMD) с субретинальным фиброзом имели значимо более низкие уровни витамина D в сыворотке, чем у пациентов без фиброза.
Способность витамина D ингибировать неоваскуляризацию привела исследователей к изучению его участия в развитии диабетической ретинопатии. Эпидемиологические исследования сообщили, что концентрация витамина D в сыворотке обратно связана с тяжестью ретинопатии у пациентов с диабетом. Генетические вариации в метаболизме витамина D также были связаны с увеитом, воспалением среднего слоя глазного яблока, известного как средняя сосудистая оболочка глаза.
Другие исследования предоставили доказательство того, что добавка витамина D могла быть полезной не только во время активного воспалительного состояния, но также для предотвращения таких патологических состояний посредством поддержания нормального здоровья и функции глаза.
В конкретном воплощении фармацевтическую композицию, описанную в данном документе, вводят в форме глазных капель или глазных мазей. В более конкретном воплощении фармацевтическую композицию, описанную в данном документе, вводят в виде глазных капель или глазных мазей, которые дополнительно содержат офтальмологически приемлемые носители. Как описано в данном документе, композиция находится в виде наноэмульсии.
По некоторым показаниям, фармацевтическая композиция, описанная в данном документе, представляет собой гипотоническую композицию. В его конкретном воплощении гипотонический фармацевтический препарат используют, когда расстройство глаза ассоциировано с высокой концентрацией солей на поверхности глаза. В еще одном воплощении физико-химические ограничения, накладываемые на конкретную фармацевтическую композицию, предполагают необходимость гипотонического препарата. Обычно, однако, композиции, подлежащие введению в глаз, представляют собой изотонические глазные препараты таким образом, чтобы минимизировать раздражение глаз, к которым они были применены. Уникальная композиция наноэмульсий фосфолипида, описанных в данном документе, однако предоставляет гипотонический глазной препарат, который не раздражает глаз. Данный признак композиций на основе наноэмульсий, описанных в данном документе, обеспечивает пациентов, нуждающихся в этом, новыми вариантами терапевтического вмешательства, которые были невозможными или очень неудобными до настоящих открытий.
По некоторым показаниям, фармацевтическая композиция, описанная в данном документе, представляет собой гиперосмотическую композицию. В его конкретном воплощении гипотонический фармацевтический препарат используют, когда расстройство глаза, подлежащего лечению, ассоциировано с уменьшенным оттоком жидкости из глаза и полученным удерживанием воды, которое в конечном итоге приводит к разрушению мембран глаза. В таких случаях композиции, описанные в данном документе, представлены в гиперосмотической композиции, которая служит для выведения избыточной жидкости из глаза. Такие гиперосмотические композиции могут быть образованы, например, в результате добавления солей (например, NaCl) к композиции.
Кроме того, некоторые физико-химические свойства фармацевтически активных ингредиентов предполагают необходимость применения гипертонических композиций в глазных препаратах. Высокое осмотическое давление таких глазных лекарственных средств, однако, является раздражительным для глаза и, таким образом, ограничивает применение иным образом эффективных терапевтических средств для нарушений глаза. Фармацевтические препараты, описанные в данном документе, уменьшают раздражающее действие гиперосмотических препаратов и, тем самым, предлагают новые возможности для развития глазных лекарственных средств, содержащих терапевтические средства, которые не могли ранее быть приготовлены в качестве способов лечения глаза из-за их гипертоничности. Фармацевтические препараты, описанные в данном документе, могут также обеспечивать возможности для повторного приготовления существующих гипертонических препаратов для получения менее раздражающих способов лечения глаза.
В еще одном аспекте предусмотрены препарат или композиция для хранения и поддержания выделенных роговиц (например, в хранилище глаз). Для сохранения жизнеспособности эпителиальных клеток, а также открытого эндотелия газа, необходимо обеспечить проникание липофильных питательных веществ к клеткам роговицы. Композиции наноэмульсий, описанные в данном документе, можно использовать в качестве среды для хранения выделенных роговиц, которая оптимизирует срок годности и качество сохраняемой ткани.
Свойства прозрачности наноэмульсий витамина D
Авторы настоящего изобретения показали, что при длинах волн видимого света (400-700 нм), содержащие фосфолипид наноэмульсии, содержащие витамин D, не рассеивают свет и, таким образом, не будут портить зрение субъекта (например, пациента, являющегося человеком, или субъекта, являющегося животным), получающего лечение вышеуказанным. Данные результаты представлены, например, на Фиг. 4. Как показано на Фиг. 4, изображения высокого разрешения можно видеть чрез слой наноэмульсии в спектральном диапазоне видимого света (лампа белого света). Тонкий слой имитирует фактическую толщину слезной пленки на роговице. Данные результаты иллюстрируют значимое свойство настоящих фосфолипид-содержащих наноэмульсий, содержащих витамин D, описанных в данном документе.
Дополнительные физические/структурные свойства наноэмульсий витамина D
Авторы настоящего изобретения дополнительно охарактеризовали фосфолипид-содержащие наноэмульсии, содержащие витамин D, описанные в данном документе, посредством анализа размера эмульгированных частиц и диаметра любых пузырьков воздуха в наноэмульсиях. Их анализы показали, что очень мало пузырьков воздуха обнаружено в наноэмульсиях по настоящему изобретению. Как показано на Фиг. 2, которая представляет собой фотографию микроскопического препарата, на котором расположена фосфолипид-содержащая наноэмульсия, содержащая витамин D, только 5 пузырьков воздуха были найдены в области 3×5 м2 композиции на основе наноэмульсии. Диаметр пузырьков составляет примерно 90 микрометров. Авторы настоящего изобретения также определили, что размер эмульгированных частиц в фосфолипид-содержащих наноэмульсиях, содержащих витамин, составляет примерно 200 нанометров.
В еще одном эксперименте авторы настоящего изобретения под микроскопом исследовали фосфолипид-содержащую наноэмульсию, содержащую витамин D, и определили, что не смогло быть выявлено пузырьков в области микропрепарата 7x5 мм2, где была равномерно распределена наноэмульсия между двумя стеклами. См. Фиг. 3.
Авторы настоящего изобретения также исследовали прозрачность фосфолипид-содержащей наноэмульсии, содержащей витамин D, и обнаружили, что разрешение хорошо сохраняется через тонкий слой наноэмульсии. См. Фиг. 5. Данное определение было сделано относительно референсного разрешения 20 линий из 60 нанометров в ширину, над линией 1200 нанометров, как наблюдается с использованием увеличения 40х. См. Фиг. 4.
Результаты, представленные, например, на Фиг. 2-5, показывают, что фосфолипид-содержащие наноэмульсии, содержащие витамин D, описанные в данном документе, являются прозрачными и не ухудшают разрешение. Соответственно, фосфолипид-содержащие наноэмульсии, содержащие витамин D, описанные в данном документе, обладают свойствами, которые будут сохранять остроту зрения субъекта, которому местно в глаза введены данные наноэмульсии. Результаты, представленные в данном документе, также демонстрируют, что настоящие наноэмульсии не являются пенами.
Исследования, сравнивающие проникновение витамина D в клетку
Поглощение витамина D можно определять, используя линию лимбальных эпителиальных клеток роговицы человека в качестве модельной системы для поглощения эпителиальными клетками роговицы. В конкретном воплощении поглощение витамина D из фосфолипид-содержащей наноэмульсии, содержащей витамин D, можно сравнивать с поглощением из масляного препарата, содержащего витамин D.
Кратко, клетки инкубируют или в масляной среде/препарате или в фосфолипид-содержащей наноэмульсионной среде, где каждая содержит 10 мкМ 7-дегидрохолестерин, в течение 24 часов. Затем клетки подвергают воздействию УФ-В (302 нм). Клетки пополняют свежей средой непосредственно перед воздействием УФ-В. Среду не меняют после исходного воздействия УФ-В для обеспечения накопления синтезированных метаболитов витамина D. Клетки два раза в сутки подвергают воздействию УФ-В, при общей дозе 10 или 20 мДж/см2/сутки в разделенных дозах, вводят с интервалом 6 часов на протяжении трех суток. Среду собирают через 1 час после конечного воздействия УФ-В и хранят при -80°С до проведения масс-спектроскопического анализа для анализа образованных метаболитов витамина D.
В качестве альтернативы, или кроме того, клетки можно инкубировать в масляной среде/препарате или в фосфолипид-содержащей наноэмульсионной среде, где каждая содержит 10 мкМ 7-дегидрохолестерин, в течение 24 часов. Культуральную среду могут затем пополнять свежей средой, и содержание витамина D двух клеточных культур, обработанных различным образом, можно сравнивать, используя масс-спектроскопический анализ для витамина D.
Защитные действия, обеспечиваемые наноэмульсиями витамина D Спектрофотометрические анализы, а именно сканирование через длину волны света (энергия) и оценка поглощения при каждой определенной энергии, использовали для оценки защитного действия наноэмульсий витамина D, описанных в данном документе. При введении в глаз наноэмульсии витамина D, описанные в данном документе, обеспечивают эффект «солнцезащитных очков», без надевания очков. Обычно люди используют солнцезащитные очки при воздействии дневного света для того, чтобы блокировать воздействие разных частот света. Однако, при чтении с экранов или при работе в среде искусственного освещения, люди обычно не используют защитных очков. Наноэмульсии витамина D, описанные в данном документе, обеспечивают усиленную защиту от УФ по всему спектральному диапазону [УФ-С: 100-280 нм, УФ-В: 280-315 нм, УФ-А: 315-400 нм, синий свет: 400-495 нм]. Защита в диапазоне синего света особенно важна в отношении защиты от светового излучения с экранов и в средах с искусственным освещением. Соответственно, защита обеспечивается введением наноэмульсий витамина D, описанных в данном документе, в полном диапазоне УФ плюс синий свет (100-495 нм), включая каждый из следующих спектральных диапазонов: УФ-А, В и С и диапазон синего света.
На Фиг. 6 - 12 представлены результаты с NanoEm (матрица Lipimix) и Vit-D NanoEm [Lipimix, загруженная витамином D (композиция витамина D)], которая разведена, как указано. Размеры частиц (сфер) и соотношения (PL:vit-D) являются, таким образом, неизменными, и меняется только концентрация витамина D (масс./масс.).
Каждую из указанных композиций тестируют в отношении поглощения (на одном и том же инструменте, длительные прогоны) в широком диапазоне энергий (длины волн), охватывающем УФ-А, В, С и спектры синего света. Удивительные и неожиданные эффекты показаны, например, на Фиг. 11, которая обнаруживает, что включение витамина D в сферы сильно изменяет характеристики поглощения матрицы. Наблюдаемое увеличение поглощения намного превышает простое накопление эффектов (в смысле суммирования значений поглощения витамина D в воде и матрице Lipimix). Удивительные и неожиданные эффекты показаны, например, на Фиг. 10, которая обнаруживает, что повторное разведение наноэмульсии витамина D не вызывает постоянного уменьшения в поглощении. Данный результат является неожиданным, по меньшей мере поскольку можно было ожидать, что уменьшение плотности сфер будет приводить к одновременному уменьшению поглощения. Это особенно очевидно при поглощении Lipimix,наблюдаемом между 2-м и 3-м разведением композиции витамина D.
В дополнение к вышеуказанному, фактор защиты от солнца (SPF - от англ. sun protection factor) рутинно измеряют посредством спектрофотометрии. Она является общепринятым способом и обычно используется в литературе для оценки, например, повреждения кожи УФ-светом.
Измерение УФ-В SPF глазных капель Lipitear и Lipicare
В другом анализе, описанном в данном документе, используется устройство (Digital UV Meter), которое осуществляет интеграцию по всему диапазону УФ-В для того, чтобы посмотреть, сколько энергии достигает детектора, который служит эквивалентом поверхности глаза. Кратко: тонкий слой наноэмульсии может быть образован между 2 прозрачными полимерными полосами, имитируя толщину слоя на глазе. В дневное время (1000 и 1430 часов):
- «Энергия УФ-В в мВт/см2 - исходный уровень» - Авторы настоящего изобретения измеряли общую энергию спектрального диапазона УФ-В с использованием выдвинутого детектора. Это представляет количество потенциально опасного излучения, которое может достигать глаза в данном конкретном спектральном диапазоне;
- «Исходный уровень полимера» - авторы настоящего изобретения повторяли тест с 2 холостыми каркасами полимера для того, чтобы посмотреть их воздействие на данный тест (без жидкости посередине);
- «Энергия УФ-В в мВт/см2 - инертная наноэмульсия» - авторы настоящего изобретения добавили наноэмульсию с похожими физическими характеристиками, но без витамина D (отдельно пустая матрица) и показали отсутствие получения уменьшения в общем количестве излучения, достигающего глаза;
- «Энергия УФ-В в мВт/см2 - наноэмульсия витамина D» - авторы настоящего изобретения заменили пустую матрицу наноэмульсией, содержащей витамин D (загруженная матрица) и демонстрировали 50-70%-ное уменьшение в количестве излучения УФ-В, достигающего глаза.
Зимнее время, Израиль, высота 0-50 м над уровнем моря.
Способ: 0,3 мл жидкости между двумя слоями прозрачного полипропилена, слой 45 микрометров, 2×3 см2
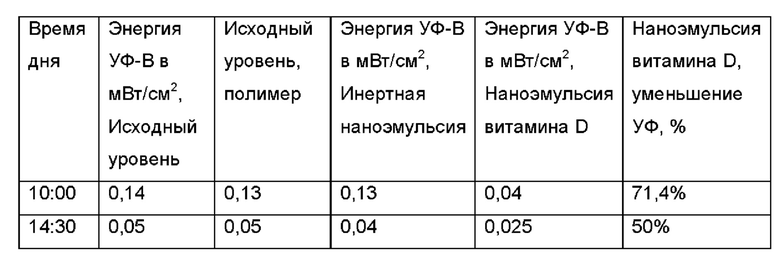
Соответственно, наноэмульсия, содержащая витамин D, придавала свойство поглощения в данном анализе, подтверждая, таким образом, другие результаты, представленные в данном документе.
Исследование безопасности LIPITEAR™ для глаз у кроликов
Цель данного исследования заключалась в анализе безопасности трех исследуемых препаратов, по сравнению с двумя препаратами сравнения, приготовленными в LIPITEAR™, после местного введения в глаза кроликов.
Клиническое наблюдение три раза на протяжении первых 24 часов после дозирования с особым вниманием на протяжении первых четырех часов и впоследствии в общей сложности дважды в сутки в течение трех суток. Изменения в коже и шерсти, конкретно вокруг глаз и слизистой оболочки.
Офтальмологическая оценка (по шкале Дрейза, оба глаза); исходный уровень, через 1 ч после введения и один раз в сутки через 24 ч, 48 ч, 72 ч, 96 ч и 120 ч после первого введения посредством лампы для всех групп исследования (последняя оценка для обоих глаз).
Заболеваемость и смертность - два раза в сутки (один раз в сутки за выходные дни).
Измерения массы тела - перед началом исследования.
Обоснование выбора системы тестирования
Использовали линию кроликов NZW. Использовали здоровых взрослых животных (2,2-2,7 кг в начале исследования) данной широко используемой лабораторной линии. Кролики представляли собой вид, выбранный для данного исследования, и они исторически используются для исследований безопасности в отношении глаз.
Обоснование выбранного размера тестируемой группы
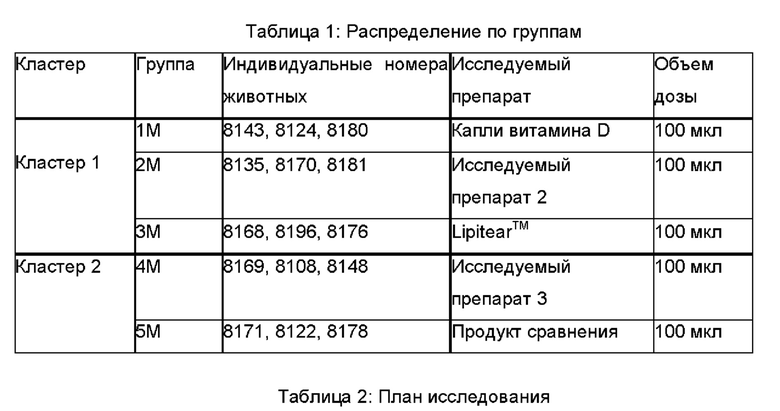
В общей сложности 15 кроликов использовали и делили на пять групп, каждая из трех кроликов: одна группа глазных капель витамина D (композиция витамин D-Lipitear; Тестируемый препарат 1); альтернативная группа глазных капель соединения А (композиция Соединение A-Lipitear; Тестируемый препарат 2); один референс: группа Lipitear (существующий продукт); альтернативная группа глазных капель соединения В (композиция Соединение B-Lipitear; Тестируемый препарат 3) и один референс: группа продукта сравнения. Концентрация витамина D в композиции Витамина D-Lipitear составляет 100 мг витамина D в 100 мл конечной эмульсии. Число групп и общее число животных представляет собой минимальное число животных на группу, достаточное для получения показательной/значимой информации.
Экспериментальная модель:
Животные.
Вид / Линия.
Кролик / NZW.
Пол / количество / возраст.
Самцы /15/ 2,2-2,7 кг в начале исследования.
Источник
Envigo RMS (Israel) Ltd. Масса тела
Средняя МТ (масса тела) животных (плюс/минус SD) в начале исследования составляла 2,4 плюс/минус 0,2 кг. Минимальная и максимальная масса животных находилась в интервале плюс/минус 20% средней массы группы.
Период акклиматизации:
Животные акклиматизировались в течение семи суток. Животные оставались в Pharmaseed до начала исследования в течение еще 20 суток до тех пор, пока они не достигали требуемой массы тела.
Идентификация
Животных идентифицировал специалист по разведению животных по сделанным красителем номерам на ухе. Данный номер также появлялся на табличке, расположенной на клетке, которая была видна спереди каждой клетки. На табличке, расположенной на клетке, дополнительно содержался номер исследования и релевантные подробности, относящиеся копытной группе.
Содержание животных. Размещение
С животными обращались в соответствии с руководствами национального института здоровья (NIH - от англ. National Institute of Health) и ассоциации по оценке и аккредитации условий содержания лабораторных животных (AAALAC - от англ. Association for Assessment and Accreditation of Laboratory Animal Care). Кроликов размещали по отдельности в пластмассовые клетки, вмонтированные в элементы питания. Размер клеток составляет 60 (L (длина)) * 60 (W (ширина)) × 40 (Н (высота)) см. Клетки были оснащены перфорированными пластмассовыми полами над располагающимися под ними лотками. Лестницы и барабаны из ПВХ (поливинилхлорид) были предоставлены для развлекательного обогащения.
Рацион кормления
Обеспечивали имеющийся в продаже корм для кроликов (корм для кроликов Teklad Doe, кат. №: 7078S), и животные имели свободный доступ к пище и к подкисленной питьевой воде (рН от 2,5 до 3,5), полученной в поставке муниципалитетом и обработанной в соответствии с Pharmaseed's SOP №214 «Система воды».
Загрязняющие вещества
Пища, получаемая от поставщика (Envigo), с сертификатом анализа. Воду обрабатывали, как указанно выше.
Условия окружающей среды
Животных размещали в стандартных лабораторных условиях, с кондиционированным и отфильтрованным (НЕРА F6/6) воздухом с достаточной подачей свежего воздуха (минимум 15 смен воздуха/час). Животных держали в среде с контролируемыми климатическими условиями. Температурный интервал представлял собой 18-24°С и интервал относительной влажности 30-70% с циклом свет/темнота 12 часов/12 часов (6АМ/6РМ).
Рандомизация
Кроликов распределяли в одну из пяти групп в соответствии с их массой тела.
Дизайн и условия эксперимента
Способы уменьшения боли
Данная процедура не причиняла боли у животных во время исследования, и никакое животное не демонстрировало тяжелых клинических симптомов во время исследования. Таким образом, не было необходимости в болеутоляющих средствах.
Концевые точки человека
Ни одного животного из всех опытных групп не умерщвляли во время данного исследования из соображений гуманности.
Продолжительность периода эксперимента
Первые сутки дозирования считались Сутками 1, и сутки окончания для большинства животных представляли собой Сутки 6. Ввиду признаков реакции, наблюдаемых у одного животного (#8168), дополнительное исследование проводили в Сутки 8, и все еще наблюдалось небольшое покраснение. Поскольку это было животное, обрабатываемое препаратом сравнения, и ни один из других исследуемых препаратов не показал никаких реакций глаза в Сутки 5 и 6, дополнительного исследования не проводили, и данное исследование оканчивалось в Сутки 8.
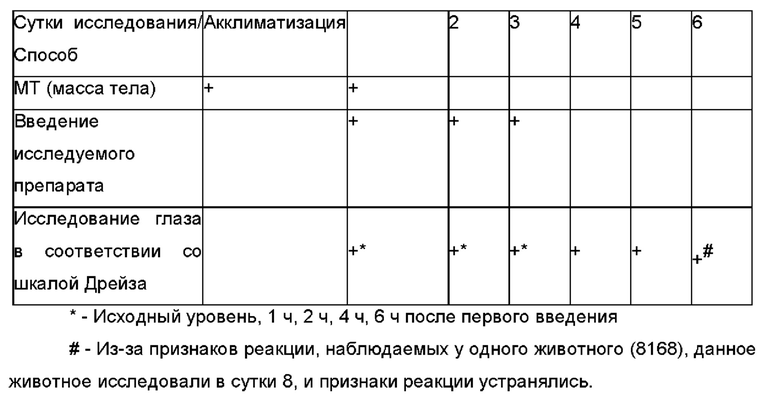
План исследования
Исследование проводили за один цикл, в соответствии с Таблицей 1 и Таблицей 2.
Введение исследуемых препаратов
Исследуемое вещество помещали в конъюнктивальный мешок одного глаза каждого животного после аккуратного оттягивания нижнего века от глазного яблока. Затем веки аккуратно удерживали вместе на протяжении примерно одной секунды для предотвращения потери вещества. Другой глаз, который остается необработанным, служил в качестве контроля. Каждый исследуемый и референсный препарат вводили трем животным на группу, в соответствии с Таблицей 1. План исследования соответствовал Таблице 2. Схемы дозирования соответствовали Таблице 3.

Тесты и оценки
Наблюдение за заболеваемостью и смертностью
Проверку заболеваемости и смертности проводили два раза в сутки (один раз в сутки на протяжении выходных дней).
Масса тела
Массу тела регистрировали при прибытии и перед началом исследования, в соответствии с Pharmaseed' SOP №010 «Взвешивание лабораторных животных».
Клинические наблюдения
Клинические наблюдения проводили периодически на протяжении первых 24 ч, с особым вниманием на протяжении первых 4 ч, и затем два раза в сутки на протяжении в общей сложности трех суток. Изменения в коже и шерсти, глазах и слизистых оболочках, в дыхательной, кровеносной, автономной и центральной нервных системах, соматомоторной активности и характере поведения, такого как дрожание, судороги, слюноотделение, диарея, летаргия, сон и кома. Особое внимание было направлено на глаза. Наблюдения были задокументированы в особым образом разработанной форме.
Исследование глаз
Оценку реакции глаза проводили перед введением исследуемого препарата (исходный уровень) и через приблизительно (1 плюс/минус 0,1) ч, (2 плюс/минус 0,1) ч, (4 плюс/минус 0,1) ч, (6 плюс/минус 0,1)ч, (24 плюс/минус 0,2) ч, (48 плюс/минус 0,2) ч, (72 плюс/минус 2) ч, (96 плюс/минус 2) ч и (120 плюс/минус 2) ч после первого введения исследуемого препарата (в соответствии с Таблицей 4, как требуется в ISO 10993-10:2010, раздел В.2.7). В сутки 2 и 3 дополнительные исследования проводили приблизительно через (1 плюс/минус 0,1) ч, (2 плюс/минус 0,1) ч, (4 плюс/минус 0,1) ч, (6 плюс/минус 0,1) ч после первого введения.
Расширенное наблюдение вплоть до 168 часов необходимо для одного животного, для определения купирования поражения.



Согласно руководству ISO (от англ. International Organization for Standardization - Международная организация по стандартизации), тестируемое вещество считается раздражителем глаза, если более половины животных в опытной группе демонстрирует положительный результат (градации в подстрочном примечании приведены в Таблице 4) на любой стадии наблюдения.
Окончание исследования
В соответствии с результатами по поражениям глаз, через 120 часов или 168 часов (животное #8168) после первого введения исследуемого препарата, исследование завершали. При окончании исследования животных посылали на реабилитацию в соответствии с Pharmaseed's SOP №043 «Освобождение кроликов и морских свинок для реабилитации».
Результаты
Наблюдение за заболеваемостью и смертностью
Ни одно животное из любой из групп не умирало или не наблюдалось с признаками заболеваемости на протяжении исследования.
Измерения массы тела (МТ)
Все животные находились в требуемом диапазоне в начале исследования. Масса тела при поступлении и в начале исследования представлены в Таблице 5.
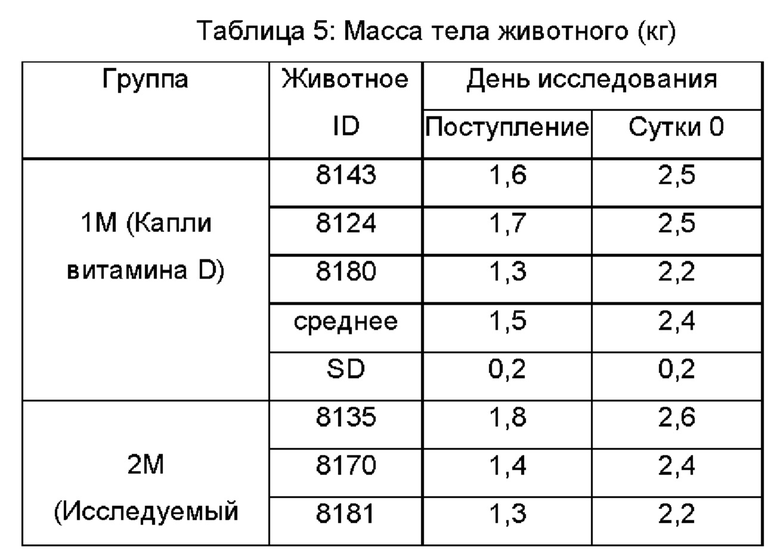
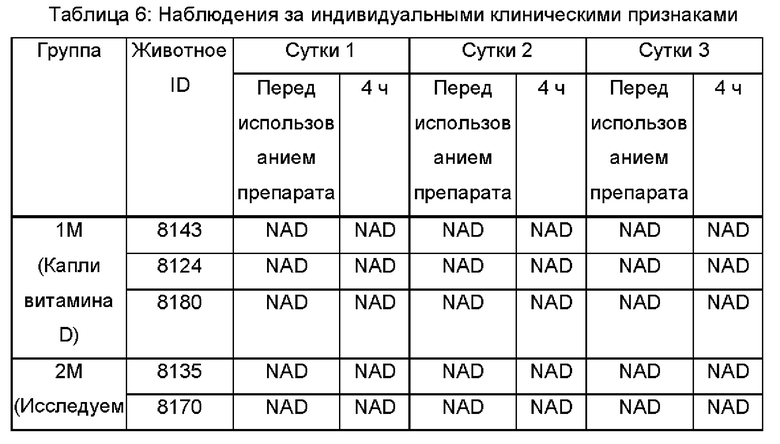
Клинические признаки
Патологических клинических признаков не наблюдали ни у кого из животных на протяжении периода исследования. Наблюдения за индивидуальными клиническими признаками представлены в Таблице 6.
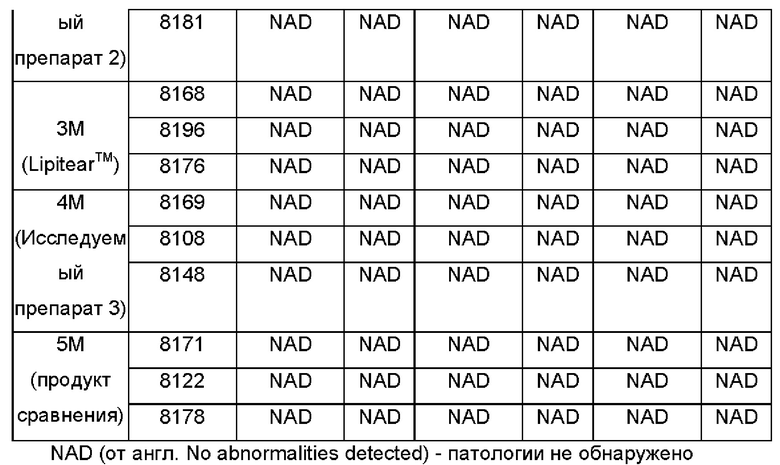
Исследование глаз с использованием теста Дрейза
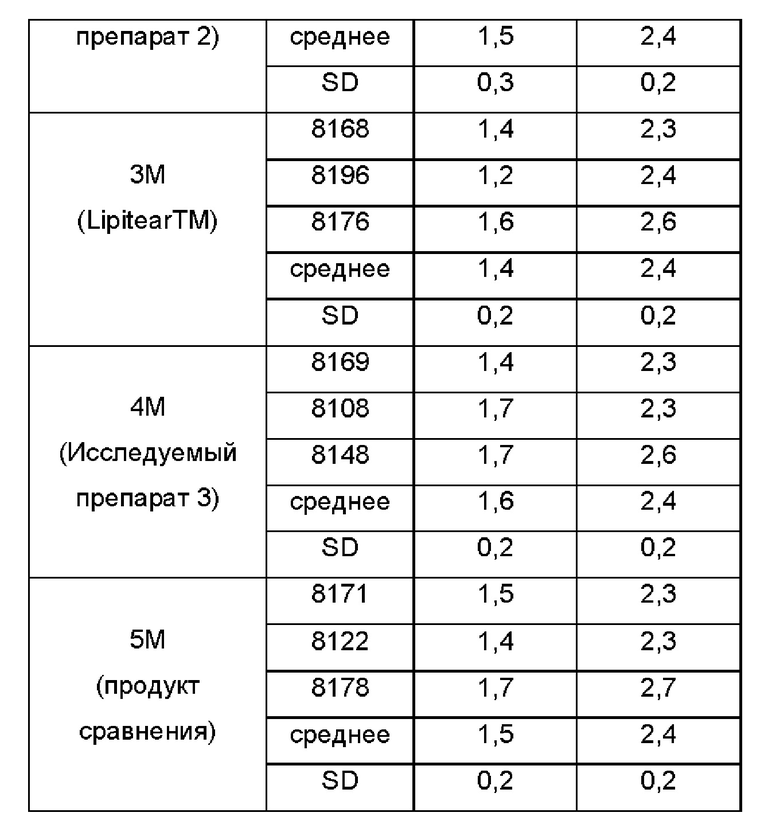
Имели место только незначительные признаки глазных реакций или наблюдаемых патологий, что могло быть связано с исследуемыми препаратами или препаратами сравнения. Незначительная краснота конъюнктивы была единственным признаком наблюдаемой глазной реакции. Максимальная числовая градация красноты конъюнктивы, наблюдаемая на протяжении данного исследования, составляла «1». В соответствии с руководством ISO, числовая градация «О» или «1» в отношении красноты конъюнктивы не считается положительной градацией. Ни одно из животных не демонстрировало положительного результата, указывающего на вредное воздействие, и, таким образом, ни один из исследуемых препаратов, вводимых в данном исследовании, не нужно рассматривать как раздражитель глаза.
Данное незначительное покраснение наблюдалось у животного №8168 из группы №3 (Lipitear) в Сутки 6. Дополнительное исследование проводили в Сутки 8, и незначительное покраснение все еще наблюдалось. Поскольку Lipitear представляет собой препарат сравнения, и ни один из других исследуемых препаратов не демонстрировал никакой глазной реакции в Сутки 5 и 6, дополнительного исследования не проводилось, и исследование заканчивали в Сутки 8.
Обсуждение и заключение
Ни одно животное не из какой из групп не умирало или не наблюдалось с признаками заболеваемости на протяжении исследования. Патологические клинические признаки не наблюдались ни у кого из животных на протяжении периода исследования. Никаких долговременных признаков раздражения глаза или патологий не наблюдали, которые могли быть связаны с исследуемыми препаратами или препаратами сравнения. Ни одно из животных не демонстрировало вредного воздействия в исследовании глаза, и все незначительные наблюдаемые временные реакции и патологии считались связанными с введением, наблюдались как в опытных, так и контрольных группах, и считались приемлемыми в данном виде процедуры.
На основе приведенных выше данных и в условиях данного исследования, сделан вывод, что трехсуточная схема, включающая повторное введение исследуемых препаратов на глаз кролика, хорошо переносилась и не вызывала никаких значимых вредных клинических воздействий, по сравнению с обработкой коммерческими препаратами сравнения. Ни один из исследуемых препаратов, вводимых в данном исследовании, не нужно рассматривать как раздражитель глаза.
Вариации, модификации и изменения воплощений настоящего раскрытия, описанных выше, станут очевидными специалистам в данной области. Все такие вариации, модификации, изменения и т.п. предназначены для попадания в сущность и объем настоящего раскрытия, ограничены исключительно прилагаемой формулой изобретения.
В то время, как описано несколько воплощений настоящего раскрытия, понятно, что данные воплощения являются только иллюстративными, и не являются ограничивающими, и что многие модификации могут стать очевидными обычным специалистам в данной области. Например, все измерения, обсуждаемые в данном документе, предложены исключительно в качестве примеров, и предназначены быть иллюстративными, а не ограничивающими.
Любой признак или элемент, который положительно идентифицирован в данном описании, может быть также конкретно исключен в качестве признака или элемента воплощения настоящего изобретения, как определено в формуле изобретения.
Раскрытие, описанное в данном документе, можно использовать на практике в отсутствии любого элемента или элементов, ограничения или ограничений, которое конкретно не раскрыто в данном документе. Таким образом, например, в каждом примере в данном документе любой из терминов «содержащий», «состоящий по существу из» и «состоящий из» может быть заменен любым из других данных двух терминов. Термины и выражения, которые были использованы, используют в качестве терминов описания и не ограничения, и отсутствует намерение в использовании таких терминов и выражений с исключением каких-либо эквивалентов признаков, показанных и описанных, или их частей, а признано, что в пределах объема раскрытия возможны разные модификации.
Краткое изложение анализа поглощения LIPITEAR™
Типичную наноэмульсию, наноэмульсию Lipimix (LIPITEAR™), отбирали для оценки в качестве механизма доставки активных ингредиентов к поверхности глаза. Результаты, представленные в данном примере, однако, не ограничиваются использованием LIPITEAR™.
Ноноэмульсии фосфолипида, содержащие витамин D, создают неожиданную физическую способность фильтровать электромагнитное излучение при разных длинах волн. Наноэмульсия фосфолипида, содержащая витамин D, при расположении поверх глаза, как обнаружили, фильтрует синий свет и УФ-излучение. Данное свойство является неожиданным не только качественно, но также количественно, поскольку толщина наноэмульсии витамина D на поверхности глаза соответствует толщине слезной пленки, и еще способность наноэмульсии витамина D фильтровать электромагнитное излучение является значимым.
УФ-излучение и глаз
Роговица, подобно коже, сильно подвержена воздействию ультрафиолетового излучения (УФ-излучение). Эпидемиологические данные указывают на то, что УФ-излучение представляет собой фактор, способствующий множеству заболеваний роговицы, включая птеригиум, фотокератит, климатическую капельную кератопатию и плоскоклеточную неоплазию поверхности глаза (OSSN - от англ. ocular surface squamous neoplasia). УФ-излучение представляет собой хорошо известное генотоксичное средство, и его действие хорошо охарактеризовано в органах, таких как кожа. Идентифицировано несколько воздействий УФ-излучения на роговицу, таких как характерные для УФ-излучения превращения С→Т и СС→ТТ, идентифицированные посредством секвенирования, и повышенные степени пролиферации и отслоения в ответ на воздействие УФ-излучения. Воздействие одной единственной низкой дозы УФ-излучения на роговицу является достаточным для того, чтобы вызвать генетические, молекулярные и клеточные изменения, что поддерживает рассмотрение использования защитных мер на роговице.
Наноэмульсия витамина D, описанная в данном документе, фильтрует УФ-излучение и синий свет до степени, которая может обеспечить защитное действие в отношении глаза.
Композиции, содержащие разные концентрации Витамина-D (Vit-D), оценивали в отношении их активности относительно глаза. Нижеследующее описывает анализы поглощения, проводимые на композициях, содержащих Витамин D, приготовленных в LIPITEAR™. Композиции предназначены для использования в качестве глазных капель и при целевом приготовлении содержат 100 мг Витамина D в 100 мл наноэмульсии или 4% липидной фракции, содержащей наноэмульсию. Характеристики поглощения, зависимого от концентрации витамина D, оценивали, и они кратко обобщены ниже. См., также, Фиг. 7-13. При условии, что композиции разбавляются слезами при введении в глаз, эффект водного разведения также оценивали (См. Таблицу 8 ниже и 0).
Эксперимент
Блок спектрофотометра Denovix DS-11 FX использовали для всех анализов. Все композиции оценивали одну за другой за один единственный цикл работы. Был зафиксирован диапазон длин волн 220-520 нм, в частности, охватывающий диапазон синего света (400-495 нм) и «хвост» УФ (X меньше 400 нм).
Анализировали два набора композиций:
1. Получали набор из 6 наноэмульсий, начиная с двух исходных композиций LIPITEAR™ и Vit-D NanoEm и посредством серийного разведения последней композиции в 5 раз в следующую наноэмульсию:
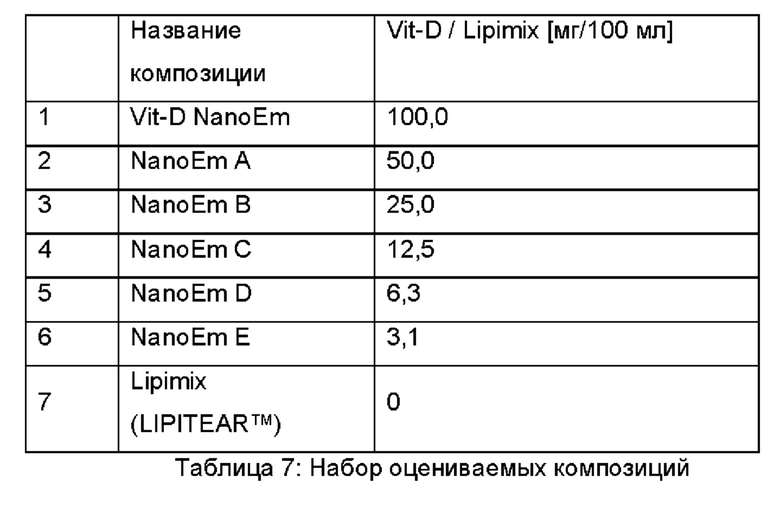
2. Набор похожих композиций, разведенных в соотношении 1:4, названных Vit-D NanoEm 0.2, Vit-D NanoEm 0.2 А и т.д.
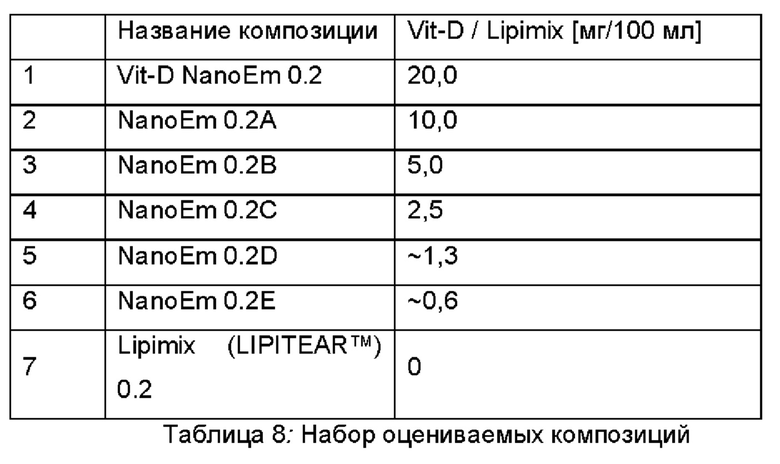
Препарат получали из одной композиции Vit-D NanoEm лишь посредством разведения.
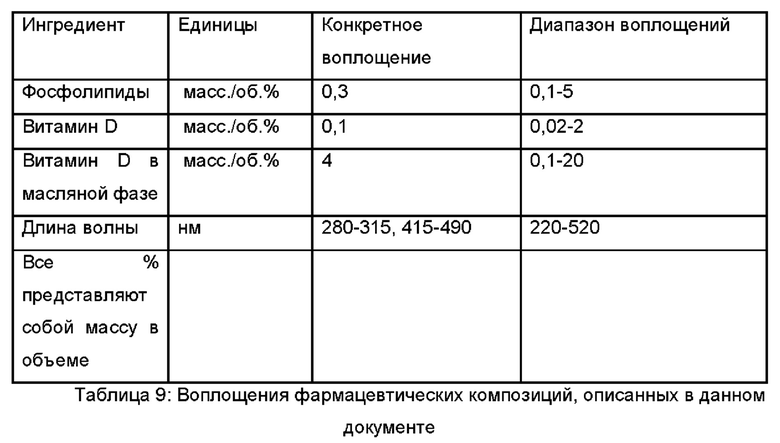
Результаты
Фиг. 10 и 11 представляют свойства поглощения 2 наборов композиций. На Фиг. 10 изображены неожиданные свойства Vit-D в композициях, анализируемых в диапазоне 220-520 нм. Преимущественные свойства поглощения Vit-D NanoEm (композиции, содержащие Vit-D, как представлено в Таблице 7), хорошо продемонстрированы при длинах волн, превышающих 230 нм.
На Фиг. 11 изображены неожиданные свойства Vit-D NanoEm (композиции, содержащие Vit-D, как представлено в Таблице 8) в диапазоне 220-520 нм, свойства которой сохранены и усилены при разведении водой в пять раз. Пятикратное разведение выбирали для стимуляции ожидаемого разведения, когда композицию, как описано в данном документе, вводят в глаз, и она разводится слезами на поверхности глаза.
Спектры поглощения при 238 нм, например, стабилизируются в соответствии с концентрацией Vit-D, и линии поглощения сохраняют свое относительное расположение от начала до самого конца измеряемого диапазона с минимальным значением до непересечения линий. См. Фиг. 9. Оптимально выравненное изображение можно видеть в случае набора композиций, разведенных водой, на всем спектральном диапазоне. См. Фиг. 11.
Как изображено на Фиг. 9, свойства поглощения композиции Vit-D можно разделить по эффективности на 3 группы, причем Vit-D NanoEm превосходит все, начиная на уровне 238 нм, группу относительно эквивалентного поглощения Lipimix и наноэмульсии А, В и С, и поглощение на низком уровне в случае наноэмульсий D и Е.
Как изображено на Фиг. 10, свойства поглощения композиций Vit-D при разведении в пять раз (концентрации в Таблице 8) обычно согласуются со свойствами поглощения композиций Vit-D Таблицы 7. Более конкретно, Vit-D NanoEm 0.2 превосходит всех, за которой следует Vit-D NanoEm 0.2 В, Lipimix, Vit-D NanoEm 0.2A, Vit-D NanoEm 0.2C, Vit-D NanoEm 0.2E и Vit-D NanoEm 0.2D. Vit-D NanoEm 0.2D и Vit-D NanoEm 0.2E имеют пренебрежимо малое поглощение.
Для справочной информации, записывали отдельный спектр поглощения Vit-D в растворе дистиллированной воды в сравнении с Lipimix и Vit-D NanoEm, и он представлен на Фиг. 11. На Фиг. 11 изображено сравнение спектров поглощения Lipimix, водного раствора Vit-D и Vit-D NanoEm, демонстрирующее неожиданные превосходные свойства поглощения Vit-D NanoEm в спектральном диапазоне 230-520 нм.
В анализах поглощения обнаружили неожиданный синергетический эффект Vit-D в наноэмульсии, который охватывает широкий спектральный диапазон 220-540 нм и особенно выражен при длинах волн 240 нм и выше. Данный спектральный диапазон света охватывает как широкий диапазон УФ, так и полный спектральный диапазон синего света.
Как изображено на Фиг. 11, существует четкое различие между почти пренебрежимо малым поглощением Vit-D в водном растворе (в общем и более конкретно от 300 нм и выше), по сравнению со свойствами поглощения наноэмульсии Vit-D. На Фиг. 11 также показано, что наноэмульсия Vit-D имеет значительно более высокий уровень поглощения, по сравнению с уровнем поглощения Lipimix. Наноэмульсия Vit-D сохраняет приоритет при длинах волн выше 240 нм измеряемого спектра.
Воздействие добавления Vit-D к наноэмульсии Lipimix характеризовали в последовательном наборе наноэмульсий Vit-D, которые были получены посредством разведения каждой из наноэмульсий Vit-D в каждом случае наполовину (См. Таблица 7). Как показано на Фиг. 10, воздействия Vit-D на поглощение наблюдают в широком диапазоне 12,5-100 мг Vit-D/мл Lipimix. Зависимые от Vit-D поглотительные эффекты особенно выражены при концентрации 100 мг/мл Vit-D, что является очевидным в случае почти всего спектрального диапазона (240-520 нм). Кроме того, данные результаты наблюдают даже с композициями, разведенными посредством добавления воды с достижением разведенного раствора 80% воды.
Результаты, представленные в данном документе, демонстрируют неожиданный эффект добавления витамина D в композицию Lipimix. Добавление более 10 мг/мл Vit-D (например,12,5 мг/мл) к наноэмульсии не только не уменьшает спектры поглощения, но неожиданно при концентрациях Vit-D (больше 50 мг/мл) усиливают блокирующее действие УФ синего цвета синергетическим образом.
Животные модели и процедуры экспериментов
Животная модель повреждения эпителия роговицы и эпителия конъюнктивы Повреждение синим светом сетчатки показано в исследованиях, исследующих кратковременное и длительное воздействие. Сетчатку находили наиболее чувствительной к свету при более коротких длинах волн (максимальная чувствительность, показанная при 441 нм). Фотохимическое повреждение сетчатки синим светом было показано как in vitro, так и in vivo. Исследования in vitro человеческих клеток сетчатки идентифицировали клеточные сигнальные пути, которые приводят к окислительному повреждению, которое повышает риск фотоповреждения сетчатки и способствует развитию возрастной макулодистрофии. Даже при низкой интенсивности, используемой в устройствах визуализации (таких как, например, компьютерные мониторы и ТВ-экраны), синий свет может вызывать продукцию активных форм кислорода (АФК) и апоптоз в клетках сетчатки. Данное повреждение может быть вызвано рыночными светоизлучающими диодами (LED -от англ. light emitting diode). Интересно, также было показано, что синий компонент белого света вызывает дисфункцию гематоретинального барьера на уровне пигментного эпителия сетчатки.
Модель кролика (Новозеландские белые кролики) для кератоконъюнктивита известна в данной области и описана, например, Gilbard et al. (1987, J. Inv. Ophthal. Vis. Sci., 28:225-228). Небольшие модификации данной модели Gilbard et al. (1987, выше) описаны в Патенте США номер (USPN) 7723287; полное содержание которого включено в данный документ посредством ссылки. Кратко, хирургическую операцию можно проводить на кроликах под наркозом с использованием хирургического микроскопа (Inami, Япония), которая предусматривает удаление пликальной складки над глазом, окклюзию слезного канала и очистку пальпебральной и бульбарной конъюнктивы. Данная хирургическая операция может проводиться на одном глазе 20 кроликов, имеющих средний возраст 3 месяца и любой пол. Хирургическое вмешательство и все последующие обработки проводили в соответствии с правилами ARVO (от англ. Association For Research In Vision And Ophthalmology - Ассоциация исследований в области зрения и офтальмологии) по уходу за животными в исследовании. Осмолярность слезной пленки повышается к послеоперационному дню 1. Уровни гликогена эпителия роговицы неуклонно снижаются, и плотность бокаловидных клеток конъюнктивы уменьшается. Данные патологии приводят к повреждению эпителия роговицы, охватывая всю поверхность роговицы к пятому послеоперационному дню. В одном воплощении обработка поврежденных глаз может начинаться на пятые послеоперационные сутки.
Оценка роговицы кролика
Поражения в роговицах, окрашенных флуоресцеином, можно клинически оценивать посредством биомикроскопии с использованием освещения щелевой лампой (Haag Streit, Швейцария) с кобальтовым фильтром. Фотография окраски флуоресцеином может быть сделана камерой с вмонтированной щелевой лампой (Торсоп, Япония). В конце каждого эксперимента кроликов умерщвляют, и их роговицы вырезают, фиксируют в параформальдегиде и исследуют в отношении повреждений эпителия.
Гистологическое исследование
В конце обработки кроликов умерщвляют посредством летальной дозы внутривенно инъецируемого пентобарбитона. Их глаза были вылущены, и роговицы фиксировали в 4%-ном параформальдегиде. Роговицы вставляют в парафиновые блоки, разделяют на секции и окрашивают гематоксилином-эозином для исследования посредством световой микроскопии.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОФТАЛЬМОЛОГИЧЕСКИЕ КОМПОЗИЦИИ | 2017 |
|
RU2756758C2 |
| СЛОЖНЫЕ ЭФИРЫ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2640506C9 |
| СЛОЖНЫЕ ЭФИРЫ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2707961C2 |
| СРЕДСТВО НА ОСНОВЕ БИСНАФТАЗАРИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2669374C2 |
| ОФТАЛЬМОЛОГИЧЕСКАЯ ЭМУЛЬСИЯ НА ОСНОВЕ ЛИПИДОВ | 2019 |
|
RU2793333C2 |
| СЛОЖНЫЕ ЭФИРЫ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2747953C2 |
| ТЕРАПЕВТИЧЕСКОЕ ВОССТАНОВЛЕНИЕ И УСИЛЕНИЕ УВЛАЖНЕНИЯ ПОВЕРХНОСТИ ГЛАЗА | 2009 |
|
RU2510274C2 |
| СЛОЖНЫЕ ЭФИРЫ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2673230C1 |
| СЛОЖНЫЕ ЭФИРЫ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2627438C2 |
| ГЛАЗНЫЕ КАПЛИ НА ОСНОВЕ КОМПОЗИЦИИ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМОЙ АДДИТИВНОЙ СОЛИ КИСЛОТЫ И МЕТИЛЭТИЛПИРИДИНОЛА И ТАУРИНА, СОДЕРЖАЩИЕ КОМПОЗИЦИЮ ВИТАМИНОВ ГРУППЫ В | 2013 |
|
RU2533276C1 |
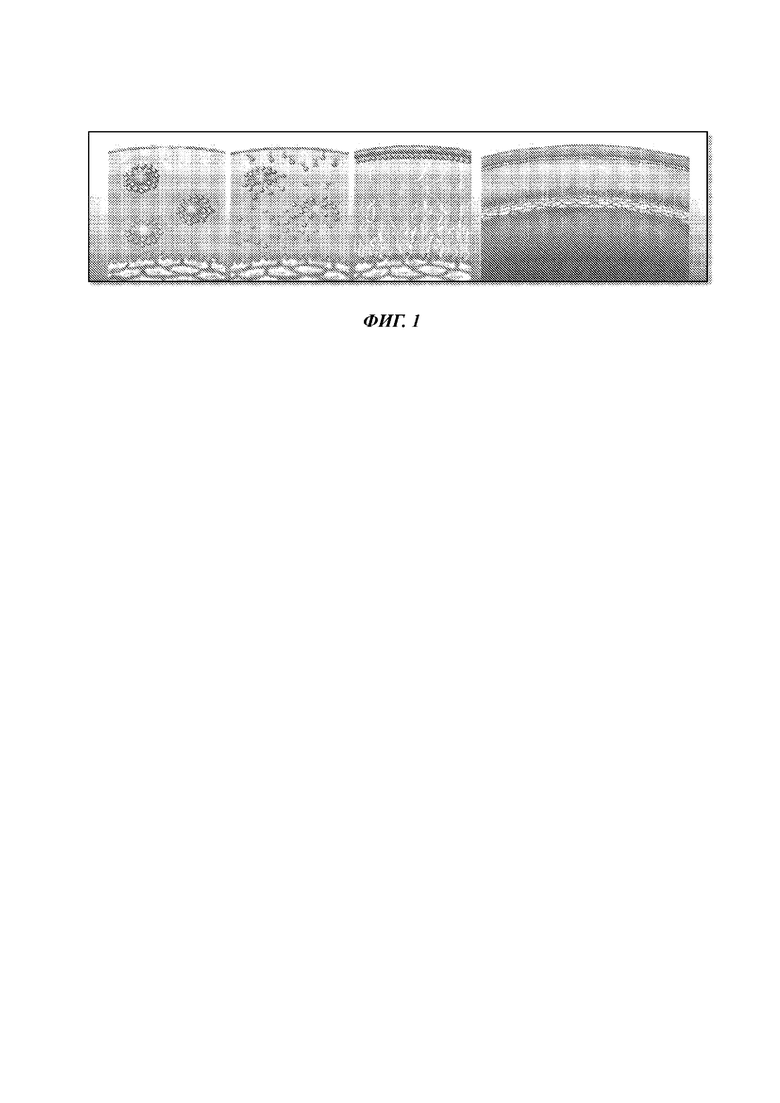




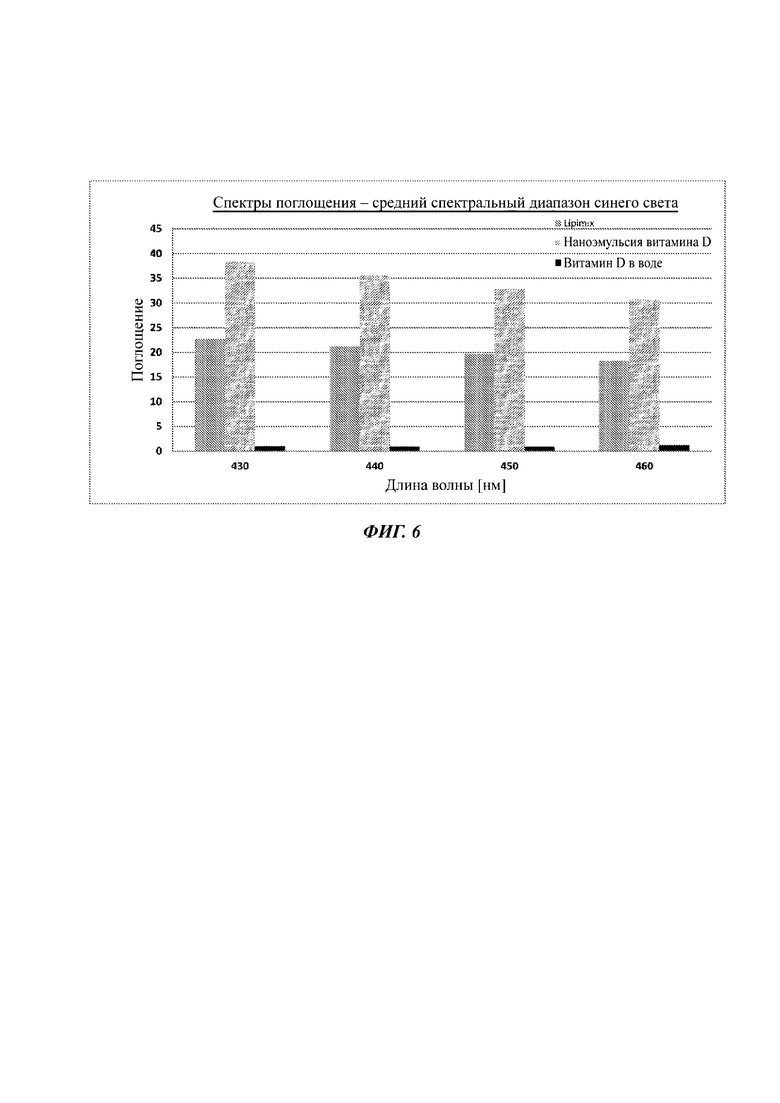

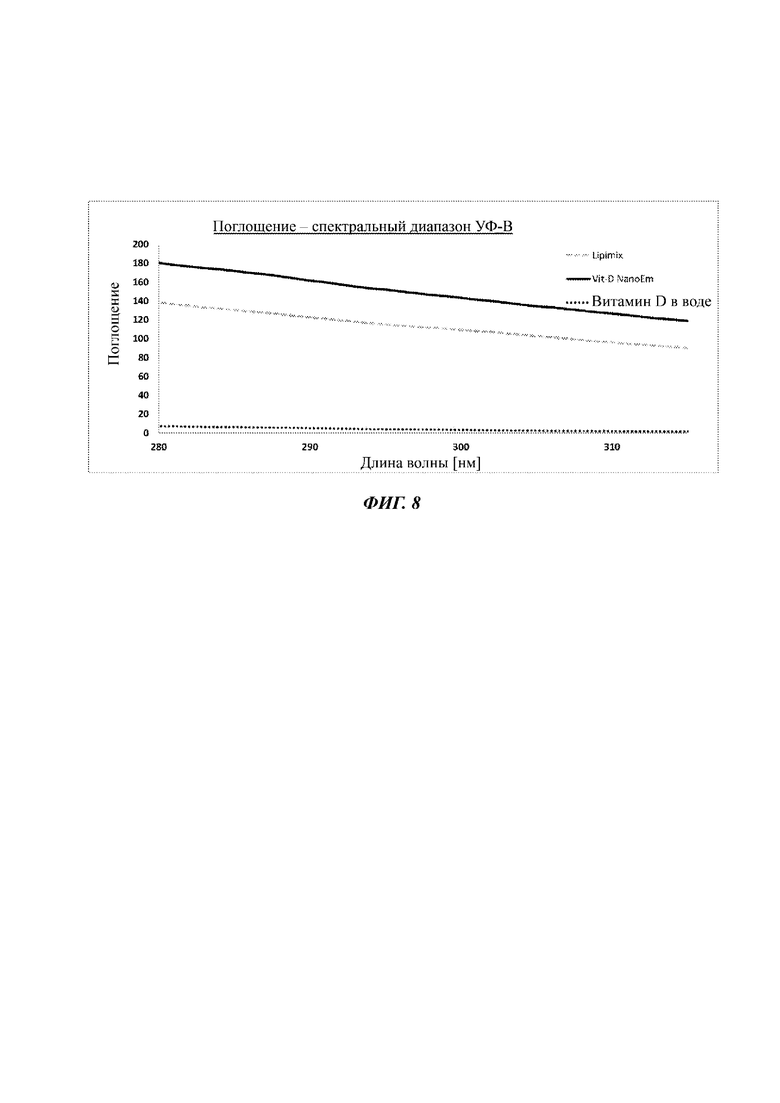
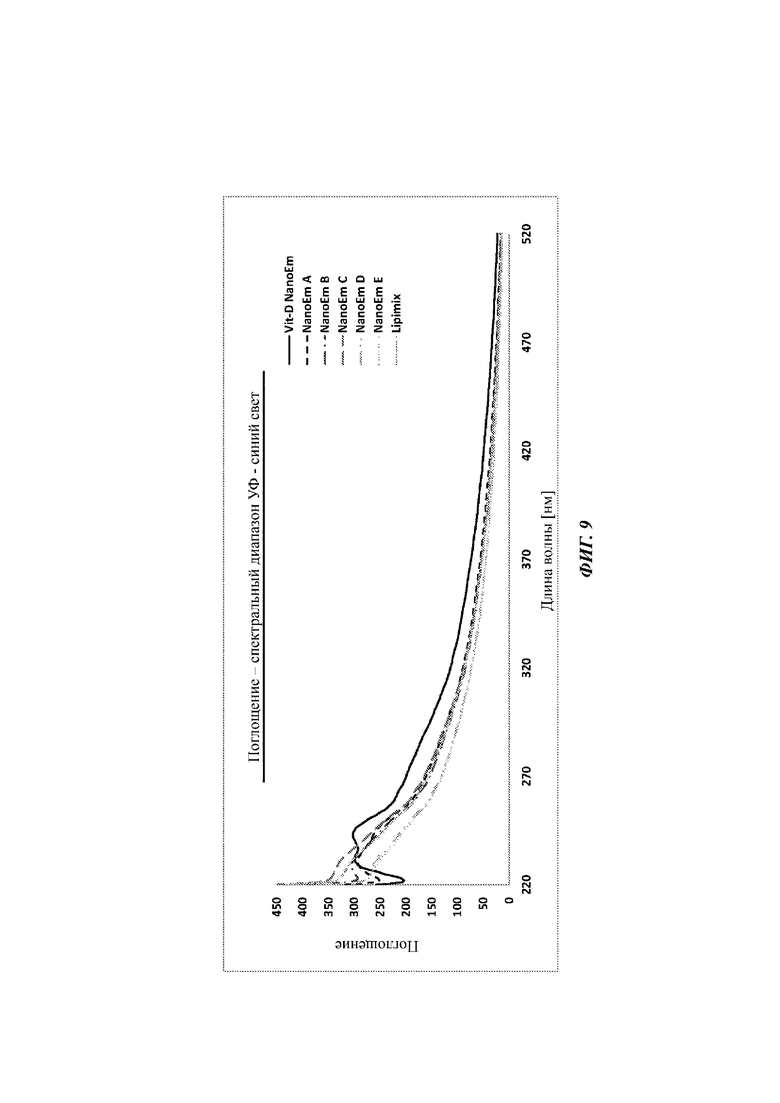
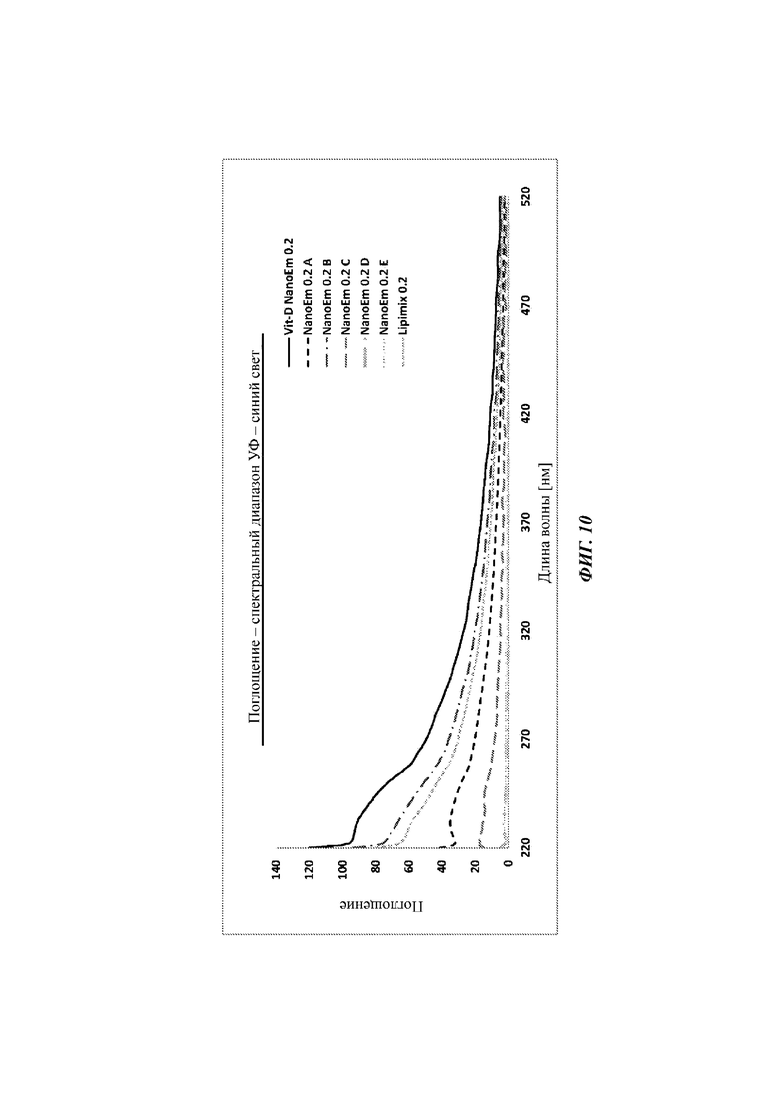
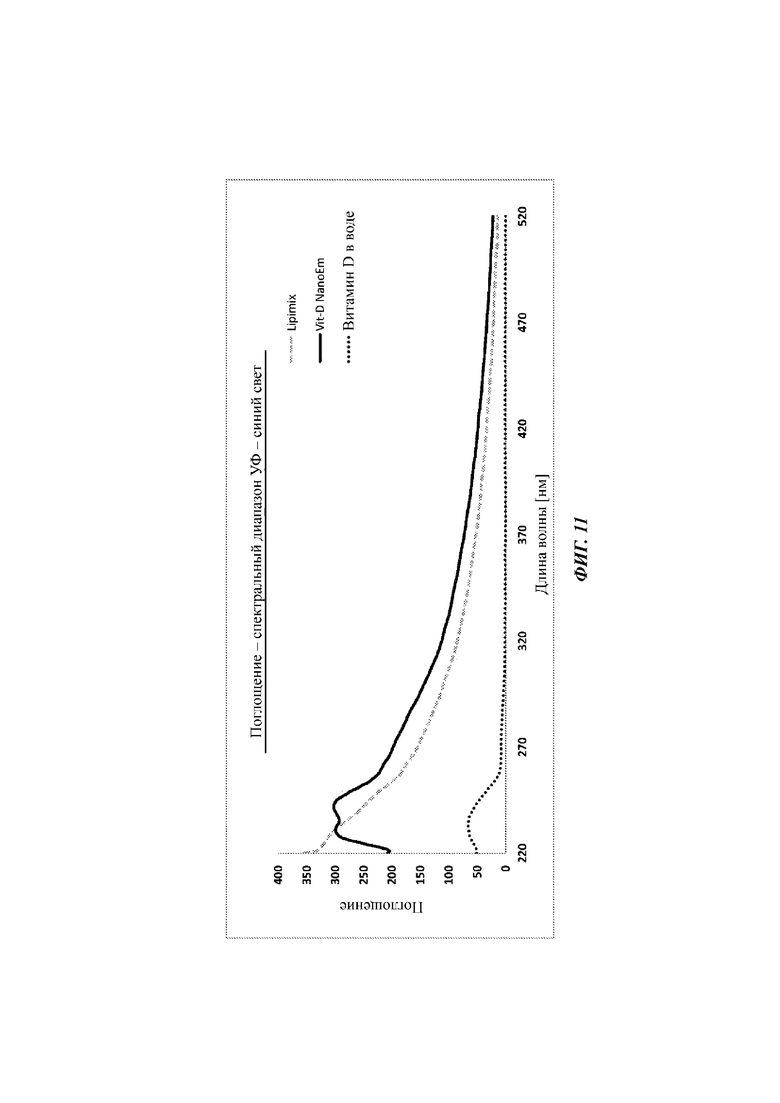
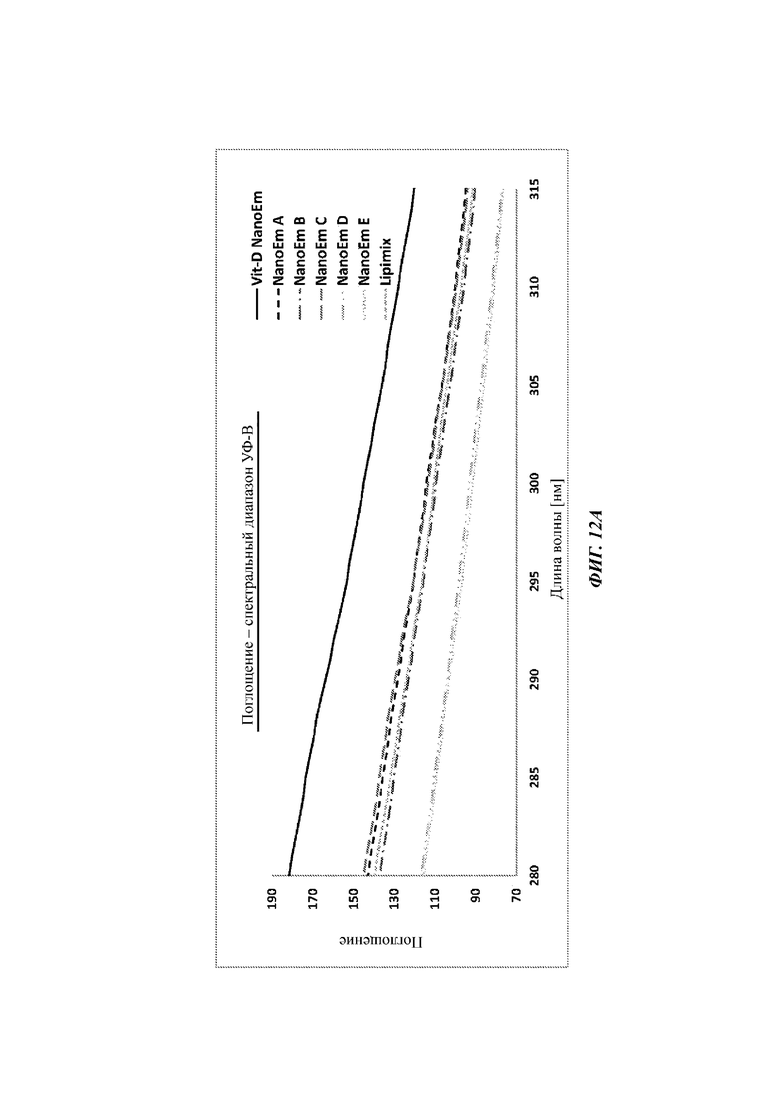
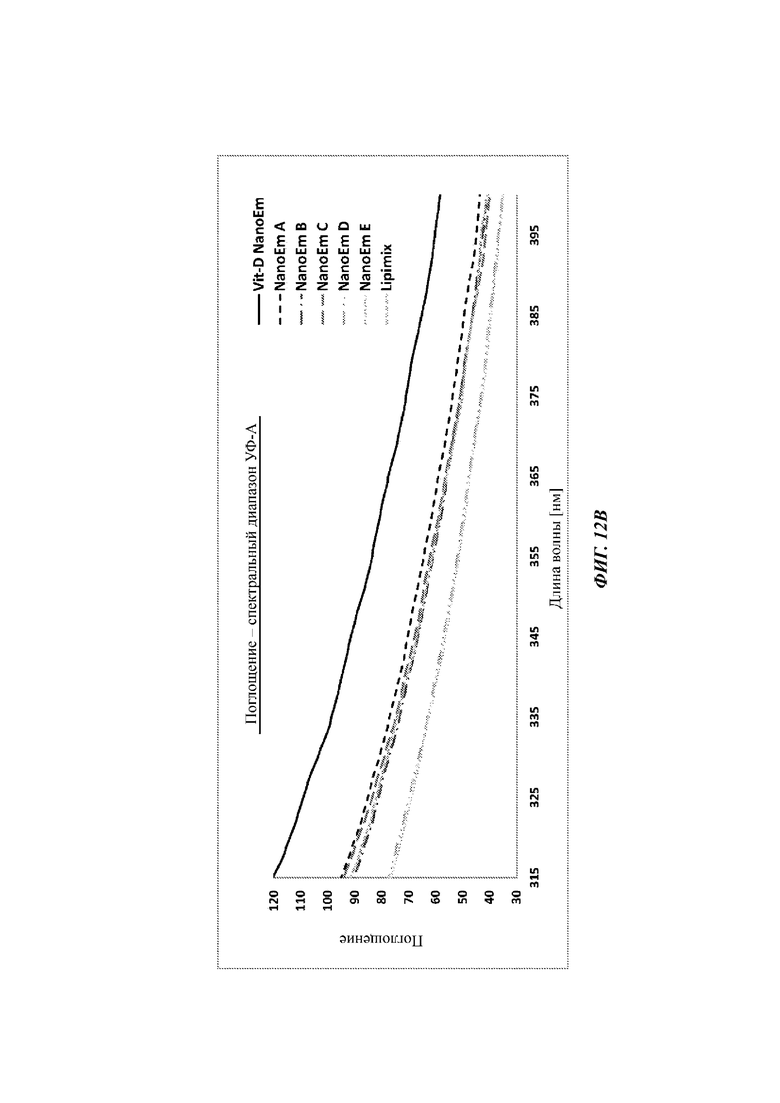
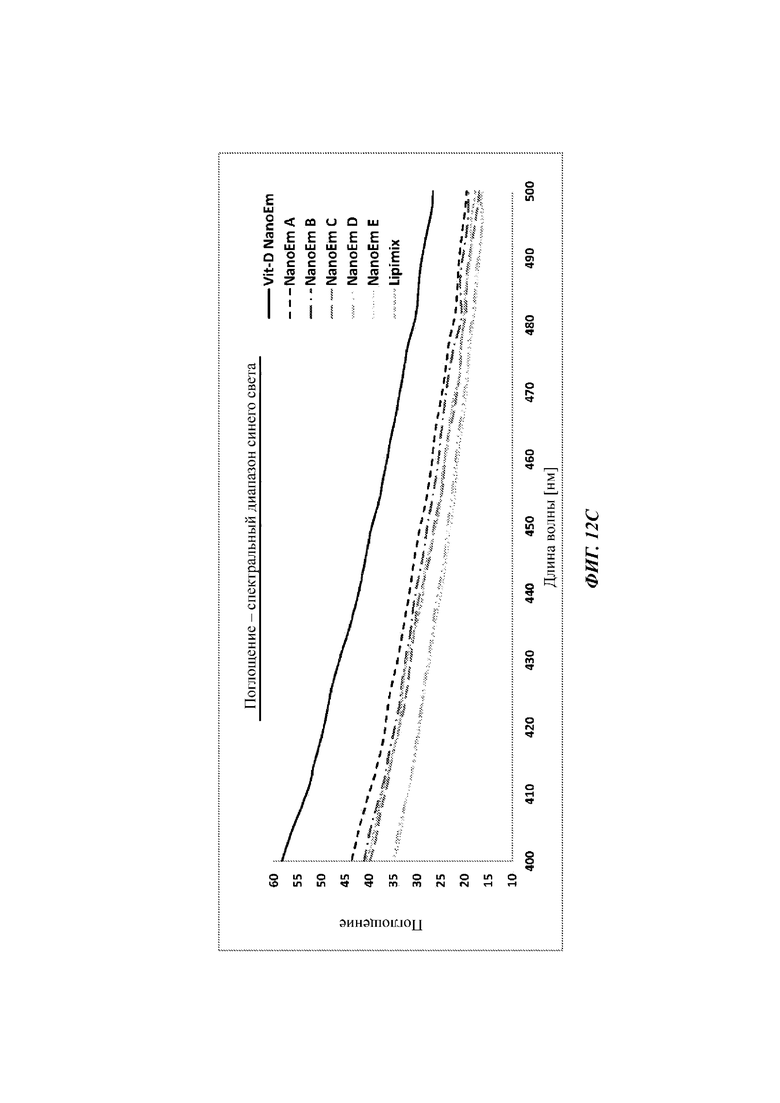
Группа изобретений относится к области фармацевтической промышленности, а именно к офтальмологической фармацевтической композиции и ее применениям. Офтальмологическая местная фармацевтическая композиция, содержащая наноэмульсию фосфолипида, содержащую витамин D в диапазоне от 0,02 до 1,4 масс./об.% и фосфолипиды в диапазоне от 0,1 до 5 масс./об.%, где эмульгированные частицы имеют размер частиц, варьирующийся от 100 до 300 нанометров в диаметре, и фосфолипиды и витамин D находятся в соотношении по меньшей мере 3:1. Применение указанной фармацевтической композиции для хранения или поддержания выделенных роговиц; применение офтальмологической фармацевтической композиции для изготовления местного лекарственного средства для уменьшения поглощения света в диапазоне длин волн 220-520 нм в глазах; применение офтальмологической фармацевтической композиции для изготовления местного лекарственного средства для улучшенной доставки витамина D к глазам; применение офтальмологической фармацевтической композиции для изготовления местного лекарственного средства для лечения глазного заболевания или состояния. Использование группы изобретений обеспечивает местную терапию, не вызывающую раздражения, увеличенной продолжительности, достаточной для улучшения диффузии липофильных средств в эпителиальные слои роговицы и в задний сегмент глаза. 6 н. и 17 з.п. ф-лы, 12 ил., 9 табл.
1. Офтальмологическая местная фармацевтическая композиция, содержащая наноэмульсию фосфолипида, содержащую витамин D в диапазоне от 0,02 до 1,4 масс./об.% и фосфолипиды в диапазоне от 0,1 до 5 масс./об.%,
где эмульгированные частицы имеют размер частиц, варьирующий от 100 до 300 нанометров в диаметре, и фосфолипиды и витамин D находятся в соотношении по меньшей мере 3:1.
2. Офтальмологическая фармацевтическая композиция по п. 1, в которой витамин D варьирует от 0,05 до 0,5% наноэмульсии фосфолипида.
3. Офтальмологическая фармацевтическая композиция по п. 1, в которой витамин D находится в количестве примерно 1000 мкг на 1 мл наноэмульсии фосфолипида или находится в количестве примерно 100 мкг на 1 мл наноэмульсии.
4. Офтальмологическая фармацевтическая композиция по п. 1, где фармацевтическая композиция не содержит сжиженного или сжатого газа-пропеллента.
5. Офтальмологическая фармацевтическая композиция по п. 1, которая представляет собой гипотоническую композицию.
6. Офтальмологическая фармацевтическая композиция по любому из пп. 1-5, где композиция находится в форме капель или глазной мази и необязательно дополнительно содержит офтальмологически приемлемый носитель.
7. Офтальмологическая фармацевтическая композиция по любому из пп. 1-6 для применения в уменьшении поглощения света в диапазоне длин волн 220-520 нм в глазах субъекта, нуждающегося в этом, где композиция может быть введена на ткань роговицы глаз.
8. Офтальмологическая фармацевтическая композиция для применения по п. 7, где композиция имеет более длительное время удерживания и/или усиленное проникновение в роговицу.
9. Офтальмологическая фармацевтическая композиция по любому из пп. 1-6 для применения в лечении глазного состояния у субъекта, нуждающегося в этом.
10. Офтальмологическая фармацевтическая композиция для применения по п. 9, где глазное состояние включает по меньшей мере одно из воспаления глаза, сухого глаза или глаукомы.
11. Офтальмологическая фармацевтическая композиция для применения по п. 9, где глазное состояние включает расстройство переднего сегмента глаза и/или физическое или химическое повреждение эпителия роговицы или конъюнктивы.
12. Применение фармацевтической композиции по любому из пп. 1-6 для хранения или поддержания выделенных роговиц.
13. Офтальмологическая местная фармацевтическая композиция, содержащая наноэмульсию фосфолипида, содержащую витамин D в диапазоне от 0,02 до 1,4 масс./об.% и фосфолипиды в диапазоне от 0,1 до 5 масс./об.%,
где эмульгированные частицы имеют размер частиц, варьирующий от 100 до 300 нанометров в диаметре, и фосфолипиды и витамин D находятся в соотношении по меньшей мере 3:1.
14. Офтальмологическая фармацевтическая композиция по п. 13, где фармацевтическая композиция не содержит сжиженный или сжатый газ-пропеллент.
15. Офтальмологическая фармацевтическая композиция по любому из пп. 13-14, где композиция находится в форме капель или глазной мази и необязательно дополнительно содержит офтальмологически приемлемый носитель.
16. Офтальмологическая фармацевтическая композиция по любому из пп. 13-15 для применения в улучшенной доставке витамина D к глазам субъекта, нуждающегося в этом, где фармацевтическая композиция может быть введена на ткань роговицы глаз субъекта.
17. Офтальмологическая фармацевтическая композиция по любому из пп. 13-15 для применения в лечении глазного состояния у субъекта, нуждающегося в этом.
18. Офтальмологическая фармацевтическая композиция по п. 17, где глазное состояние включает по меньшей мере одно из воспаления глаза, сухого глаза или глаукомы.
19. Офтальмологическая фармацевтическая композиция для применения по п. 17, где глазное состояние включает расстройство переднего сегмента глаза и/или физическое или химическое повреждение эпителия роговицы или конъюнктивы.
20. Офтальмологическая фармацевтическая композиция по любому из пп. 1-19, включенная в медицинское изделие.
21. Применение офтальмологической фармацевтической композиции по любому из пп. 1-12 для изготовления местного лекарственного средства для уменьшения поглощения света в диапазоне длин волн 220-520 нм в глазах.
22. Применение офтальмологической фармацевтической композиции по любому из пп. 13-19 для изготовления местного лекарственного средства для улучшенной доставки витамина D к глазам.
23. Применение офтальмологической фармацевтической композиции по любому из пп. 1-19 для изготовления местного лекарственного средства для лечения глазного заболевания или состояния.
| CN 105746730 A, 13.07.2016 | |||
| EP 3328214 A1, 06.06.2018 | |||
| US 2011034568 A1, 10.02.2011 | |||
| US 7723287 B1, 25.05.2010 | |||
| WO 9922703 A1, 14.05.1999. |
Авторы
Даты
2024-01-22—Публикация
2019-12-06—Подача