Изобретение относится к композициям высокомолекулярных соединений, а именно к биоразрушаемым композициям высокомолекулярных соединений с использованием фосфорсодержащих соединений в качестве компонентов, и может быть использовано для 3D печати изделий медицинского назначения.
Известен полимерный композиционный материал с памятью формы для 3D-печати медицинских изделий [RU 2631890 C1, МПК (2006.01) A61L 27/12, 61L 27/14, A61L 27/46, опубл. 28.09.2017], состоящий из «жесткой» и «мягкой» фаз на основе биоразлагаемых и биосовместимых полимерных композиций. «Жесткая» фаза представлена кристаллической фазой полимерной матрицы, химическими и физическими сшивками и биоактивным компонентом в виде гидроксиапатита с размером частиц от 100 до 1000 нм, а «мягкая» фаза представлена аморфной фазой полимерной матрицы и пластификатором в виде полиэтиленгликоля при следующем соотношении компонентов, мас.%:
Химическим агентом для сшивки является триаллилизоцианурат или дикумилпероксид.
Недостатком полимерного композиционного материала является формирование химически сшитой структуры полимерной матрицы, что в значительной степени влияет на физико-химические свойства, скорость и механизм биоразложения.
Известен композиционный материал для 3D печати медицинских изделий [RU 2679632 C1, МПК (2006.01) A61L 27/12, опубл. 12.02.2019], содержащий гидроксиапатит с размером частиц 20-100 нм, глицерин и сорбит при следующем соотношении, мас.%:
Известен, выбранный в качестве прототипа, полимерный композиционный материал для 3D-печати медицинских изделий [RU 2679127 C1, МПК (2006.01) A61L 27/46, A61L 27/48, опубл. 06.02.2019], содержащий полилактид, гидроксиапатит с размером частиц 20-100 нм и дополнительно глицерин при следующем соотношении компонентов, мас.%:
Недостатком двух вышеупомянутых полимерных композиционных материалов является жесткость и хрупкость материала, являющаяся следствием большого массового содержания гидроксиапатита.
Техническим результатом предлагаемого изобретения является получение полимерного композиционного материала для 3D печати изделий медицинского назначения.
Полимерный композиционный материал для 3D печати изделий медицинского назначения, так же как в прототипе, содержит гидроксиапатит с размером частиц 100 нм и биоразлагаемый алифатический полиэфир.
Согласно изобретению в качестве алифатического полиэфира полимерный композиционный материал содержит ε-поликапролактон со среднечисловой молекулярной массой 70000-90000 г/моль, содержит -гидроксиапатит с размером частиц 101-20000 нм и дополнительно - полисорбат 20 при следующем соотношении компонентов, мас.%:
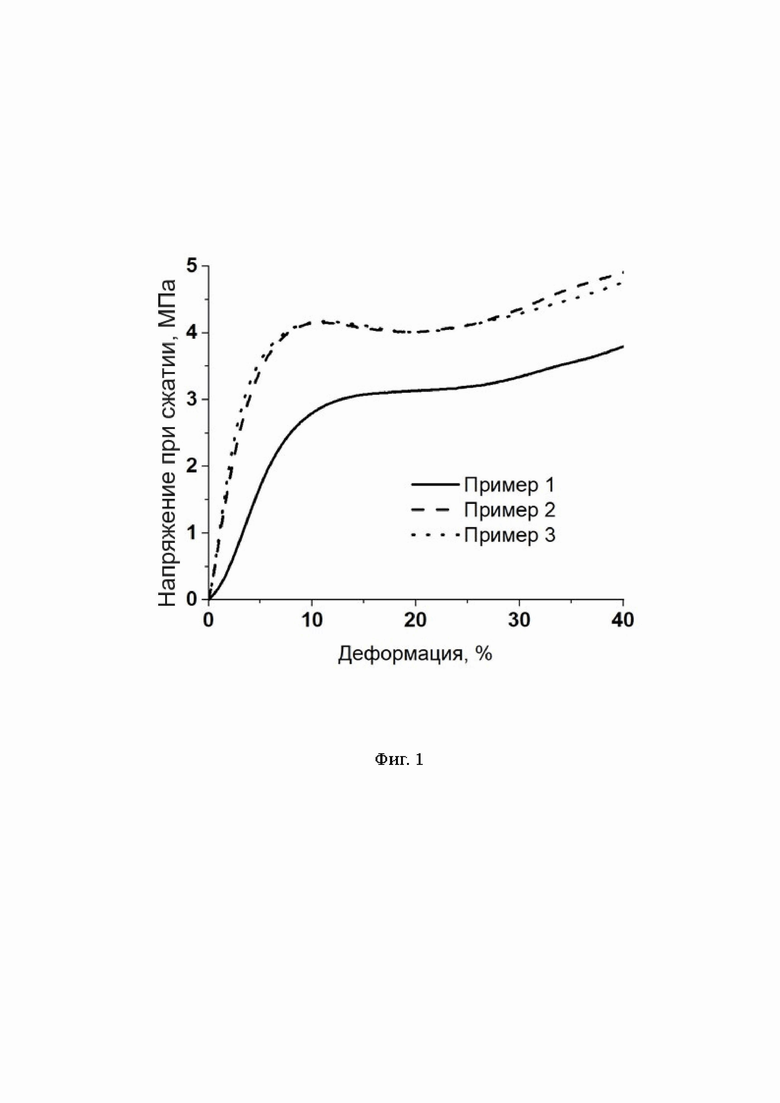
Использование ε-поликапролактона со среднечисловой молекулярной массой от 70000 до 90000 г/моль влияет на упругое восстановление формы медицинского изделия, изготовленного методом 3D печати из предложенного полимерного композиционного материала, после снятия нагрузки с сохранением его исходных геометрических размеров. Такие упругие свойства важны для медицинского изделия как с точки зрения его биомеханического поведения в условиях организма, так и для обеспечения удобства работы врача с изделием в процессе хирургического вмешательства - медицинское изделие может быть упруго деформировано при имплантации без риска разрушения и потери исходных формы и размеров. Гидроксиапатит в качестве наполнителя обеспечивает биоактивные остеоиндуктивные свойства композиционного материала. Добавление гидроксиапатита с размером частиц 100-20000 нм в ε-поликапролактон в концентрации от 1 до 21 мас.% приводит к упрочнению композиционного материала, обеспечивая его предел прочности при сжатии 13 - 17,4 МПа. Предел текучести при сжатии предложенного композиционного материала составляет 3 - 4,2 МПа. Возвращаемая упругая деформация при содержании гидроксиапатита от 1 до 21 мас.% обеспечивается на уровне 5 - 10 % от исходных размеров испытуемого образца (фиг. 1). Добавление полисорбата 20 в концентрации от 1 до 3 мас.% обеспечивает высокую сыпучесть и позволяет предотвратить агломерацию гранул композиционного материала на стадиях осаждения из раствора, вакуумного фильтрования и сушки (фиг. 2).
На фиг. 1 показаны участки диаграмм сжатия пористых образцов, изготовленных методом 3D печати из композиционных материалов полученных согласно примерам 1, 2 и 3, отображающие регион перехода от упругой к пластической деформации.
На фиг. 2 показаны фотографии сыпучих гранул композиционных материалов с содержанием гидроксиапатита от 1 до 21 мас.%, полученных: а) - согласно примеру 1, б) - согласно примеру 2, в) - согласно примеру 3.
Пример 1
В двугорлую круглодонную колбу объемом 250 мл с обратным холодильником и якорем верхнеприводной мешалки внесли 140 грамм ацетона и 8,97 грамм (98 мас.%) ε-поликапролактона со среднечисловой молекулярной массой 70000 г/моль. Колбу поместили на водяную баню и перемешивали содержимое колбы при скорости вращения верхнеприводной мешалки 200 об/мин и нагреве до 40 °С в течение 25 минут. По истечение 25 минут в колбе образовался гомогенный 6 мас.% раствор ε-поликапролактона в ацетоне. В колбу с раствором внесли 0,09 грамм (1 мас.%) полисорбата 20 и 0,09 грамм (1 мас.%) порошка гидроксиапатита с размером частиц от 100 до 2000 нм и продолжили перемешивание при скорости вращения верхнеприводной мешалки 200 об/мин и температуре 40 °С в течение 20 минут. Через 20 минут колбу перенесли на ледяную баню и охлаждали без перемешивания до -20 °С. После достижения температуры в колбе -20 °С, выдерживали содержимое колбы при этой температуре в течение 20 минут до осаждения гранул. Суспензию осажденных гранул интенсивно перемешивали при скорости вращения верхнеприводной мешалки 400 об/мин в течение 5 минут. Содержимое колбы перенесли на воронку Шотта с размером пор 3-10 мкм и выполнили вакуумное фильтрование для отделения ацетона. Влажный композиционный порошок промыли на воронке Шотта изопропиловым спиртом в течение 5 минут и выполнили вакуумное фильтрование для отделения изопропилового спирта. Промытый влажный порошок сушили в вакуумной камере при давлении 10 мбар до постоянной массы в течение 6 часов при температуре 30 °С.
Сухой порошок загрузили в бункер одношнекового экструдера и экструдировали в виде филамента для 3D печати необходимого диаметра. Филамент использовали для 3D печати пористых образцов путем послойной экструзии расплава. Предел текучести при сжатии изготовленного методом 3D печати пористого образца в виде цилиндра диаметром 10 мм и высотой 10 мм с размером пор 1 мм составил 3 МПа, предел прочности при сжатии - 13 МПа.
Пример 2
В двугорлую круглодонную колбу объемом 250 мл с обратным холодильником и якорем верхнеприводной мешалки внесли 150 грамм ацетона и 7,96 грамм (87 мас.%) ε-поликапролактона со среднечисловой молекулярной массой 80000 г/моль. Колбу поместили на водяную баню и перемешивали содержимое колбы при скорости вращения верхнеприводной мешалки 235 об/мин и нагреве до 45 °С в течение 32 минут. По истечение 32 минут в колбе образовался гомогенный 5 мас.% раствор ε-поликапролактона в ацетоне. В колбу с раствором внесли 0,18 грамм (2 мас.%) полисорбата 20 и 1,01 грамм (11 мас.%) порошка гидроксиапатита с размером частиц от 2000 до 10000 нм и продолжили перемешивание при скорости вращения верхнеприводной мешалки 235 об/мин и температуре 45 °С в течение 27 минут. Через 27 минут колбу перенесли на ледяную баню и охлаждали без перемешивания до -10 °С. После достижения температуры в колбе -10 °С, выдерживали содержимое колбы при этой температуре в течение 30 минут до осаждения гранул. Суспензию осажденных гранул интенсивно перемешивали при скорости вращения верхнеприводной мешалки 500 об/мин в течение 7 минут. Содержимое колбы перенесли на воронку Шотта с размером пор 3-10 мкм и выполнили вакуумное фильтрование для отделения ацетона. Влажный композиционный порошок промыли на воронке Шотта изопропиловым спиртом в течение 5 минут и выполнили вакуумное фильтрование для отделения изопропилового спирта. Промытый влажный порошок сушили в вакуумной камере при давлении 10 мбар до постоянной массы в течение 6 часов при температуре 30 °С.
Сухой порошок загрузили в бункер одношнекового экструдера и экструдировали в виде филамента для 3D печати необходимого диаметра. Филамент использовали для 3D печати пористых образцов путем послойной экструзии расплава. Предел текучести при сжатии изготовленного методом 3D печати пористого образца, аналогичного образцу в примере 1, составил 4,2 МПа, предел прочности при сжатии - 17 МПа.
Пример 3
В двугорлую круглодонную колбу объемом 250 мл с обратным холодильником и якорем верхнеприводной мешалки внесли 160 грамм ацетона и 6,95 грамм (76 мас.%) ε-поликапролактона со среднечисловой молекулярной массой 90000 г/моль. Колбу поместили на водяную баню и перемешивали содержимое колбы при скорости вращения верхнеприводной мешалки 270 об/мин и нагреве до 50 °С в течение 40 минут. По истечение 40 минут в колбе образовался гомогенный 4 мас.% раствор ε-поликапролактона в ацетоне. В колбу с раствором внесли 0,27 грамм (3 мас.%) полисорбата 20 и 1,92 грамм (21 мас.%) порошка гидроксиапатита с размером частиц от 10000 до 20000 нм и и продолжили перемешивание при скорости вращения верхнеприводной мешалки 270 об/мин и температуре 50 °С в течение 35 минут. Через 35 минут колбу перенесли на ледяную баню и охлаждали без перемешивания до 0 °С. После достижения температуры в колбе 0 °С, выдерживали содержимое колбы при этой температуре в течение 40 минут до осаждения гранул. Суспензию осажденных гранул интенсивно перемешивали при скорости вращения верхнеприводной мешалки 600 об/мин в течение 12 минут. Содержимое колбы перенесли на воронку Шотта с размером пор 3-10 мкм и выполнили вакуумное фильтрование для отделения ацетона. Влажный композиционный порошок промыли на воронке Шотта изопропиловым спиртом в течение 5 минут и выполнили вакуумное фильтрование для отделения изопропилового спирта. Промытый влажный порошок сушили в вакуумной камере при давлении 10 мбар до постоянной массы в течение 6 часов при температуре 30 °С.
Сухой порошок загрузили в бункер одношнекового экструдера и экструдировали в виде филамента для 3D печати необходимого диаметра. Филамент использовали для 3D печати пористых образцов путем послойной экструзии расплава. Предел текучести при сжатии изготовленного методом 3D печати пористого образца, аналогичного образцу в примере 1, составил 4,2 МПа, предел прочности при сжатии - 17,4 МПа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО КОМПОЗИЦИОННОГО МАТЕРИАЛА ДЛЯ ИЗГОТОВЛЕНИЯ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ | 2023 |
|
RU2815644C1 |
| КОМПОЗИТ ДЛЯ 3D-ПЕЧАТИ МЕДИЦИНСКИХ ИЗДЕЛИЙ | 2018 |
|
RU2679632C1 |
| Полимерный композит с эффектом памяти формы для 3D-печати медицинских изделий | 2016 |
|
RU2631890C1 |
| КОМПОЗИТ ДЛЯ 3D-ПЕЧАТИ МЕДИЦИНСКИХ ИЗДЕЛИЙ | 2018 |
|
RU2679127C1 |
| СПОСОБ ОЧИСТКИ ПОЛИКАПРОЛАКТОНА ОТ ПРИМЕСИ ОЛОВА | 2023 |
|
RU2824007C1 |
| Биоактивный полимерный пористый каркас | 2016 |
|
RU2665175C2 |
| Биоактивная полимерная нить для осуществления послойной 3D-печати | 2015 |
|
RU2637841C2 |
| КОМПОЗИТНЫЕ ФИЛАМЕНТЫ ИЗ СУЛЬФОНИРОВАННОГО СЛОЖНОГО ПОЛИЭФИРА И СЕРЕБРЯНЫХ НАНОЧАСТИЦ, ПОКРЫТЫЕ ПОЛИМЕРОМ, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2742118C2 |
| КОМПОЗИТНЫЕ ФИЛАМЕНТЫ ИЗ СУЛЬФОНИРОВАННОГО СЛОЖНОГО ПОЛИЭФИРА И СЕРЕБРЯНЫХ НАНОЧАСТИЦ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2742117C2 |
| ГИДРОГЕЛЬ ДЛЯ ПОЛУЧЕНИЯ КОМПОЗИЦИОННЫХ МАТЕРИАЛОВ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ ДЛЯ ЗАМЕЩЕНИЯ КОСТНО-ХРЯЩЕВЫХ ДЕФЕКТОВ МЕТОДОМ 3D ПЕЧАТИ | 2016 |
|
RU2632431C2 |

Изобретение относится к композициям высокомолекулярных соединений, а именно к биоразрушаемым композициям высокомолекулярных соединений с использованием фосфорсодержащих соединений в качестве компонентов, и может быть использовано для 3D- печати изделий медицинского назначения. Полимерный композиционный материал для 3D- печати изделий медицинского назначения содержит ε-поликапролактон со среднечисловой молекулярной массой 70000-90000 г/моль, гидроксиапатит с размером частиц 100-20000 нм и полисорбат 20 при следующем соотношении компонентов, мас.%: ε-поликапролактон 76-98, гидроксиапатит 1-21, полисорбат 20 1-3. Технический результат: получение полимерного композиционного материала для 3D-печати изделий медицинского назначения с упругими свойствами. 2 ил.
Полимерный композиционный материал для 3D-печати изделий медицинского назначения, содержащий алифатический полиэфир и гидроксиапатит, отличающийся тем, что в качестве алифатического полиэфира содержит ε-поликапролактон со среднечисловой молекулярной массой от 70000 до 90000 г/моль, содержит гидроксиапатит с размером частиц 101-20000 нм и дополнительно полисорбат 20 при следующем соотношении компонентов, мас.%:
| КОМПОЗИТ ДЛЯ 3D-ПЕЧАТИ МЕДИЦИНСКИХ ИЗДЕЛИЙ | 2018 |
|
RU2679127C1 |
| CN 109395171 A, 01.03.2019 | |||
| СПОСОБ ПОЛУЧЕНИЯ СТАБИЛЬНОГО ВОДНОГО РАСТВОРА ДИОКСИДА ХЛОРА | 2011 |
|
RU2567937C2 |
| АКИМЧЕНКО И.О | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Химия и химическая технология в XXI веке: материалы XXI Международной научно-практической конференции студентов и молодых | |||
Авторы
Даты
2024-02-15—Публикация
2023-11-29—Подача