Изобретение относится к способам приготовления композиций высокомолекулярных веществ путем осаждения из раствора, а именно биоразрушаемых композиций высокомолекулярных соединений с фосфорсодержащими соединениями в качестве компонентов, и может быть использовано для изготовления изделий медицинского назначения.
Известен способ получения полимерного композиционного материала для 3D-печати медицинских изделий [RU 2679127 C1, МПК (2006.01) A61L 27/46, A61L 27/48, опубл. 06.02.2019], заключающийся в том, что в раствор 12,5-98,9 мас.% биоразлагаемого алифатического полиэфира полилактида в трихлорметане с вязкостью 1,5-2 Па·с добавляют 0,1-12,5мас.% глицерина при постоянном перемешивании. Полученную массу подвергают ультразвуковому воздействию и примешивают малыми порциями 1-75 мас.% фосфорсодержащего наполнителя гидроксиапатита с размером частиц 20-100 нм. Массу сушат и доводят до значения вязкости 5-7 Па·с, после чего выливают на фторопластовую подложку и сушат в вакуумном сушильном шкафу при температуре 75-80°С в течение 6-7 часов до прекращения потери массы. Твердый композиционный материал измельчают в роторной дробилке до получения гранулята со средним размером 1-4 мм.
Известен способ получения полимерного композиционного материал для 3D печати костных имплантатов [Kim, C.G.; Han, K.S.; Lee, S.; Kim, M.C.; Kim, S.Y.; Nah, J. Fabrication of Biocompatible Polycaprolactone–Hydroxyapatite Composite Filaments for the FDM 3D Printing of Bone Scaffolds. Appl. Sci. 2021, 11, 6351. https://doi.org/10.3390/app11146351], заключающийся в том, что отдельно готовят раствор 75-95 мас.% биоразлагаемого алифатического полиэфира поликапролактона в диметилформамиде и суспензию 5-25 мас.% фосфорсодержащего наполнителя гидроксиапатита в диметилформамиде при нагреве до 100 °С и перемешивании в течение 8-12 часов. Раствор полимера и суспензию гидроксиапатита смешивают и перемешивают в течение 60 минут, после чего подвергают ультразвуковому воздействию в течение 30 минут. Смесь переливают в открытую тару и нагревают до температуры 100°С при постоянном перемешивании до полного испарения диметилформамида. После затвердевания смесь подвергают ультразвуковой обработке для отделения от тары и измельчают, а затем сушат при комнатной температуре.
Недостатком этих известных способов получения полимерных композиционных материалов является использование токсичных растворителей 2-го класса токсичности согласно фармакопейной статье ОФС.1.1.0008.15, необходимость ультразвуковой обработки при перемешивании компонентов, а также необходимость дополнительной операции измельчения для получения гранулята.
Известен, выбранный в качестве прототипа, способ получения полимерного композиционный материал для изготовления биорезорбируемых имплантатов путем осаждения из раствора [Oosterbeek, R. N., Zhang, X. C., Best, S. M., & Cameron, R. E. (2021). A technique for improving dispersion within polymer–glass composites using polymer precipitation. Journal of the Mechanical Behavior of Biomedical Materials, 123, 104767. https://doi.org/10.1016/J.JMBBM.2021.104767], включающий следующее: фосфорсодержащий наполнитель фосфатное стекло с размером частиц 1400 нм примешивают в раствор 70 мас.% биоразлагаемого алифатического полиэфира полилактида в дихлорметане концентрацией 0,1 г/мл до достижения массовой концентрации фосфатного стекла в смеси 30 мас.%. Смесь перемешивают в течение 15 минут, после чего подвергают ультразвуковому воздействию в течение 15 минут при комнатной температуре. В смесь добавляют этанол до достижения соотношения этанол:дихлорметан, равного 3:1, и наблюдают осаждение композиционного материала в виде суспензии гранул. Полученную суспензию выливают на стальной сушильный лоток и испаряют этанол и дихлорметан до прекращения потери массы. Композиционный материал сушат в вакуумной камере при температуре 50°С в течение 10 дней.
Недостатками такого способа получения композиционного материала является необходимость добавления этанола для инициации осаждения композиционного материала из раствора, использование токсичного растворителя дихлорметана 2-го класса токсичности согласно фармакопейной статье ОФС.1.1.0008.15, необходимость ультразвуковой обработки при перемешивании компонентов, а также необходимость длительной сушки композиционного материала в течение десяти дней.
Техническим результатом предлагаемого изобретения является получение полимерного композиционного материала для изготовления изделий медицинского назначения.
Способ получения полимерного композиционного материала для изготовления изделий медицинского назначения, так же как в прототипе, включает перемешивание порошка фосфорсодержащего наполнителя с раствором биоразлагаемого алифатического полиэфира в органическом растворителе, последующее осаждение гранул из раствора и их сушку в вакуумной камере до постоянной массы.
Согласно изобретению, в качестве фосфорсодержащего наполнителя используют гидроксиапатит с размером частиц 100-20000 нм. В качестве биоразлагаемого алифатического полиэфира используют ε-поликапролактон со среднечисловой молекулярной массой от 70000 до 90000 г/моль. В качестве органического растворителя используют ацетон. В раствор 76-98 мас.% ε-поликапролактона в ацетоне концентрацией 4-6 мас.% добавляют 1-3 мас.% полисорбата 20 и 1-21 мас.% гидроксиапатита, смесь нагревают до 40-50 °С при механическом перемешивании со скоростью 200-270 об/мин, выдерживают в течение 20-35 минут при перемешивании, а затем охлаждают без перемешивания до -20…+0 °С до осаждения в виде суспензии гранул. Затем суспензию гранул перемешивают со скоростью 400-600 об/мин и подвергают вакуумному фильтрованию. Влажные гранулы промывают изопропиловым спиртом в течение 5-12 минут и сушат в вакуумной камере при давлении 10 мбар в течение 6 часов при температуре 30 °С.
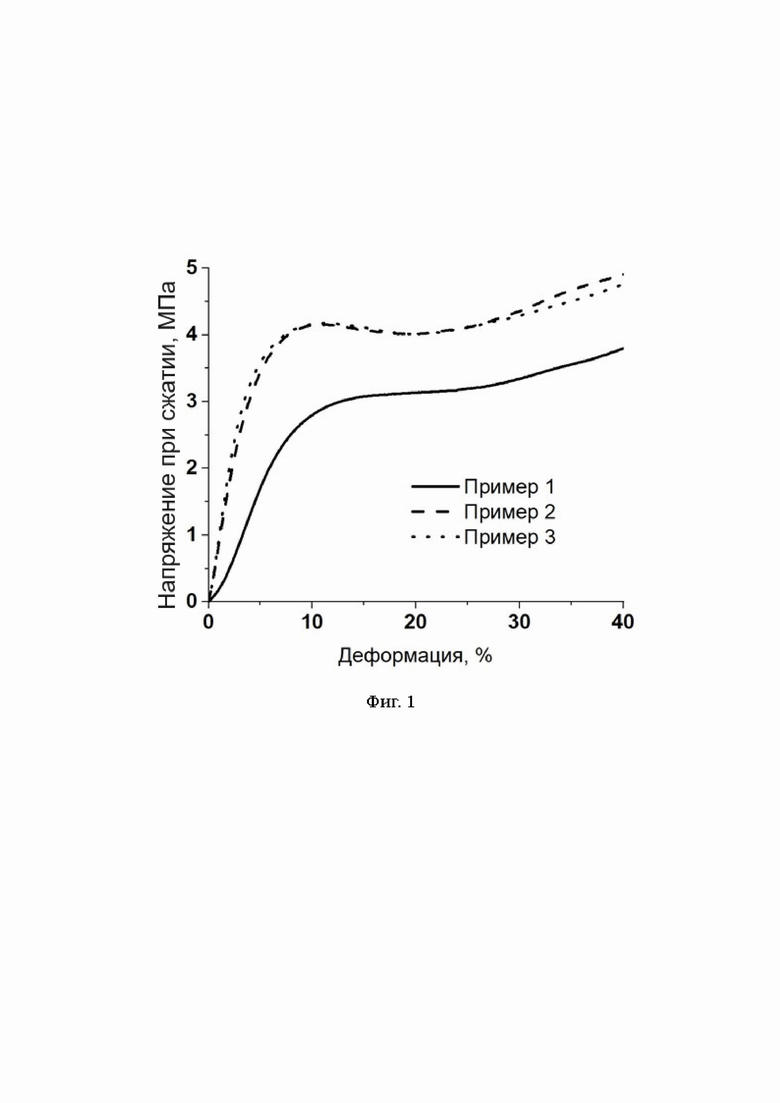
Использование ε-поликапролактона со среднечисловой молекулярной массой от 70000 до 90000 г/моль влияет на восстановление формы изделия, изготовленного из предложенного полимерного композиционного материала, после снятия нагрузки с сохранением его исходных геометрических размеров. Такие упругие свойства важны для медицинского изделия как с точки зрения его биомеханического поведения в условиях организма, так и для обеспечения удобства работы врача с изделием в процессе хирургического вмешательства – медицинское изделие может быть упруго деформировано при имплантации без риска разрушения и потери исходных формы и размеров. Гидроксиапатит в качестве наполнителя обеспечивает биоактивные остеоиндуктивные свойства композиционного материала. Использование гидроксиапатита с размером частиц 100-20000 нм в концентрации от 1 до 21 мас.% приводит к упрочнению композиционного материала, обеспечивая его предел прочности при сжатии, например, пористых образцов изготовленных методом 3D-печати, до 13-17,4 МПа, и предел текучести при сжатии 3-4,2 МПа. Возвращаемая упругая деформация при содержании гидроксиапатита от 1 до 21 мас.% обеспечивается на уровне 5-10 % от исходных размеров испытуемого образца (фиг. 1). Использование полисорбата 20 в концентрации от 1 до 3 мас.% обеспечивает высокую сыпучесть и позволяет предотвратить агломерацию гранул композиционного материала на стадиях осаждения из раствора, вакуумного фильтрования и сушки (фиг. 2). Используемый для изготовления композиционного материала растворитель ацетон относится к низкотоксичным остаточным органическим растворителям 3-го класса токсичности согласно фармакопейной статье ОФС.1.1.0008.15. Ацетон является естественным метаболитом организма человека, что обуславливает низкую токсичность получаемого композиционного материала. Нагрев смеси раствора ε-поликапролактона в ацетоне с гидроксиапатитом до 40-50°С при механическом перемешивании со скоростью 200-270 об/мин в течение 20-35 позволяет получить стабильную суспензию гидроксиапатита в гомогенном полимерном растворе и не приводит к термической деструкции полимера. Инициация осаждения гранул композиционного материала осуществляется за счет понижения растворимости ε-поликапролактона в ацетоне при охлаждении до -20…+0°С. Такой способ инициации не требует добавления дополнительных инициаторов осаждения. Промывка 150-170 мл изопропилового спирта в течение 5-12 минут позволяет экстрагировать остаточный ацетон с поверхности влажных гранул композиционного материала и предотвратить их слипание во время последующей сушки. Сушка гранулированного композиционного материала в вакуумной камере при давлении 10 мбар и температуре 30°С в течение 6 часов позволяет эффективно удалить из материала остаточный растворитель и подготовить его для последующей переработки.
На фиг. 1 показаны участки диаграмм сжатия пористых образцов, изготовленных методом 3D-печати из композиционных материалов, полученных согласно примерам 1, 2 и 3, отображающие регион перехода от упругой к пластической деформации.
На фиг. 2 показаны фотографии сыпучих гранул композиционных материалов с содержанием гидроксиапатита от 1 до 21 мас.%, полученных: а) – согласно примеру 1, б) – согласно примеру 2, в) – согласно примеру 3.
Пример 1
В двугорлую круглодонную колбу объемом 250 мл с обратным холодильником и якорем верхнеприводной мешалки внесли 140 грамм ацетона и 8,97 грамм (98 мас.%) ε-поликапролактона со среднечисловой молекулярной массой 70000 г/моль. Колбу поместили на водяную баню и перемешивали содержимое колбы при скорости вращения верхнеприводной мешалки 200 об/мин и нагреве до 40°С в течение 25 минут. По истечении 25 минут в колбе образовался гомогенный 6 мас.% раствор ε-поликапролактона в ацетоне. В колбу с раствором внесли 0,09 грамм (1 мас.%) полисорбата 20 и 0,09 грамм (1 мас.%) порошка гидроксиапатита с размером частиц от 100 до 2000 нм и продолжили перемешивание при скорости вращения верхнеприводной мешалки 200 об/мин и температуре 40°С в течение 20 минут. Через 20 минут колбу перенесли на ледяную баню и охлаждали без перемешивания до -20 °С. После достижения температуры в колбе -20 °С, выдерживали содержимое колбы при этой температуре в течение 20 минут до осаждения гранул. Суспензию осажденных гранул интенсивно перемешивали при скорости вращения верхнеприводной мешалки 400 об/мин в течение 5 минут. Содержимое колбы перенесли на воронку Шотта с размером пор 3-10 мкм и выполнили вакуумное фильтрование для отделения ацетона. Влажный композиционный порошок промыли на воронке Шотта изопропиловым спиртом в течение 5 минут и выполнили вакуумное фильтрование для отделения изопропилового спирта. Промытый влажный порошок сушили в вакуумной камере при давлении 10 мбар до постоянной массы в течение 6 часов при температуре 30 °С.
Сухой порошок загрузили в бункер одношнекового экструдера и экструдировали в виде филамента для 3D-печати необходимого диаметра. Филамент использовали для 3D-печати пористых образцов путем послойной экструзии расплава. Предел текучести при сжатии изготовленного методом 3D-печати пористого образца составил 3 МПа, предел прочности при сжатии 13 МПа.
Пример 2
В двугорлую круглодонную колбу объемом 250 мл с обратным холодильником и якорем верхнеприводной мешалки внесли 150 грамм ацетона и 7,96 грамм (87 мас.%) ε-поликапролактона со среднечисловой молекулярной массой 80000 г/моль. Колбу поместили на водяную баню и перемешивали содержимое колбы при скорости вращения верхнеприводной мешалки 235 об/мин и нагреве до 45 °С в течение 32 минут. По истечение 32 минут в колбе образовался гомогенный 5 мас.% раствор ε-поликапролактона в ацетоне. В колбу с раствором внесли 0,18 грамм (2 мас.%) полисорбата 20 и 1,01 грамм (11 мас.%) порошка гидроксиапатита с размером частиц от 2000 до 10000 нм и продолжили перемешивание при скорости вращения верхнеприводной мешалки 235 об/мин и температуре 45°С в течение 27 минут. Через 27 минут колбу перенесли на ледяную баню и охлаждали без перемешивания до -10 °С. После достижения температуры в колбе -10 °С, выдерживали содержимое колбы при этой температуре в течение 30 минут до осаждения гранул. Суспензию осажденных гранул интенсивно перемешивали при скорости вращения верхнеприводной мешалки 500 об/мин в течение 7 минут. Содержимое колбы перенесли на воронку Шотта с размером пор 3-10 мкм и выполнили вакуумное фильтрование для отделения ацетона. Влажный композиционный порошок промыли на воронке Шотта изопропиловым спиртом в течение 7 минут и выполнили вакуумное фильтрование для отделения изопропилового спирта. Промытый влажный порошок сушили в вакуумной камере при давлении 10 мбар до постоянной массы в течение 6 часов при температуре 30°С.
Сухой порошок загрузили в бункер одношнекового экструдера и экструдировали в виде филамента для 3D-печати необходимого диаметра. Филамент использовали для 3D-печати пористых образцов путем послойной экструзии расплава. Предел текучести при сжатии изготовленного методом 3D-печати пористого образца составил 4,2 МПа, предел прочности при сжатии17 МПа.
Пример 3
В двугорлую круглодонную колбу объемом 250 мл с обратным холодильником и якорем верхнеприводной мешалки внесли 160 грамм ацетона и 6,95 грамм (76 мас.%) ε-поликапролактона со среднечисловой молекулярной массой 90000 г/моль. Колбу поместили на водяную баню и перемешивали содержимое колбы при скорости вращения верхнеприводной мешалки 270 об/мин и нагреве до 50 °С в течение 40 минут. По истечение 40 минут в колбе образовался гомогенный 4 мас.% раствор ε-поликапролактона в ацетоне. В колбу с раствором внесли 0,27 грамм (3 мас.%) полисорбата 20 и1,92 грамм (21 мас.%) порошка гидроксиапатита с размером частиц от 10000 до 20000 нм и продолжили перемешивание при скорости вращения верхнеприводной мешалки 270 об/мин и температуре 50°С в течение 35 минут. Через 35 минут колбу перенесли на ледяную баню и охлаждали без перемешивания до 0 °С. После достижения температуры в колбе 0 °С, выдерживали содержимое колбы при этой температуре в течение 40 минут до осаждения гранул. Суспензию осажденных гранул интенсивно перемешивали при скорости вращения верхнеприводной мешалки 600 об/мин в течение 12 минут. Содержимое колбы перенесли на воронку Шотта с размером пор 3-10 мкм и выполнили вакуумное фильтрование для отделения ацетона. Влажный композиционный порошок промыли на воронке Шотта изопропиловым спиртом в течение 12 минут и выполнили вакуумное фильтрование для отделения изопропилового спирта. Промытый влажный порошок сушили в вакуумной камере при давлении 10 мбар до постоянной массы в течение 6 часов при температуре 30 °С.
Сухой порошок загрузили в бункер одношнекового экструдера и экструдировали в виде филамента для 3D-печати необходимого диаметра. Филамент использовали для 3D-печати пористых образцов путем послойной экструзии расплава. Предел текучести при сжатии изготовленного методом 3D-печати пористого образца составил 4,2 МПа соответственно, предел прочности при сжатии 17,4 МПа.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМЕРНЫЙ КОМПОЗИЦИОННЫЙ МАТЕРИАЛ ДЛЯ 3D ПЕЧАТИ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ | 2023 |
|
RU2813693C1 |
| КОМПОЗИТ ДЛЯ 3D-ПЕЧАТИ МЕДИЦИНСКИХ ИЗДЕЛИЙ | 2018 |
|
RU2679632C1 |
| КОМПОЗИТ ДЛЯ 3D-ПЕЧАТИ МЕДИЦИНСКИХ ИЗДЕЛИЙ | 2018 |
|
RU2679127C1 |
| СПОСОБ ОЧИСТКИ ПОЛИКАПРОЛАКТОНА ОТ ПРИМЕСИ ОЛОВА | 2023 |
|
RU2824007C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО ТРЕХМЕРНОГО КАРКАСА ДЛЯ ЗАМЕЩЕНИЯ КОСТНО-ХРЯЩЕВЫХ ДЕФЕКТОВ | 2015 |
|
RU2606041C2 |
| Способ получения биорезорбируемого материала на основе магния и гидроксиапатита с защитным многокомпонентным покрытием | 2021 |
|
RU2763138C1 |
| БИОСОВМЕСТИМЫЙ БИОРАЗЛАГАЕМЫЙ СКАФФОЛД НА ОСНОВЕ ПОЛИМЕРНОГО КОМПОЗИТА, СОДЕРЖАЩЕГО НАНОЧАСТИЦЫ ГИДРОКСИАПАТИТА | 2019 |
|
RU2756551C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОМПОЗИЦИОННОГО НЕТКАНОГО ПОЛИМЕРНОГО МАТЕРИАЛА ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2024 |
|
RU2836608C1 |
| СПОСОБ НАНЕСЕНИЯ БИОАКТИВНОГО ПОКРЫТИЯ НА ОСНОВЕ ХИТОЗАНА НА ПОЛИМЕРНЫЕ ПОРИСТЫЕ КОНСТРУКЦИИ | 2015 |
|
RU2600652C1 |
| ГИДРОГЕЛЬ ДЛЯ ПОЛУЧЕНИЯ КОМПОЗИЦИОННЫХ МАТЕРИАЛОВ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ ДЛЯ ЗАМЕЩЕНИЯ КОСТНО-ХРЯЩЕВЫХ ДЕФЕКТОВ МЕТОДОМ 3D ПЕЧАТИ | 2016 |
|
RU2632431C2 |

Изобретение относится к области химии высокомолекулярных соединений, а именно к способу получения полимерного композиционного материала для изготовления изделий медицинского назначения. Согласно предложенному способу: в 4-6 мас.%-ный раствор 76-98 мас.% ε-поликапролактона со среднечисловой молекулярной массой 70000-90000 г/моль (биоразлагаемый алифатический полиэфир) в ацетоне (органический растворитель) добавляют 1-3 мас.% полисорбата 20 и 1-21 мас.% гидроксиапатита с размером частиц 100-20000 нм (фосфорсодержащий наполнитель), смесь нагревают до 40-50 °С при механическом перемешивании со скоростью 200-270 об/мин, выдерживают 20-35 мин при перемешивании, затем, не перемешивая, охлаждают до -20…+0 °С до осаждения в виде суспензии гранул, далее суспензию гранул перемешивают со скоростью 400-600 об/мин и подвергают вакуумному фильтрованию, влажные гранулы промывают изопропиловым спиртом 5-12 мин и сушат в вакуумной камере до постоянной массы 6 ч при давлении 10 мбар и температуре 30 °С. Изобретение обеспечивает получение полимерного композиционного материала, используемого для изготовления изделий медицинского назначения. 2 ил., 3 пр.
Способ получения полимерного композиционного материала для изготовления изделий медицинского назначения, включающий перемешивание порошка фосфорсодержащего наполнителя с раствором биоразлагаемого алифатического полиэфира в органическом растворителе, последующее осаждение гранул из раствора, их сушку в вакуумной камере до постоянной массы, отличающийся тем, что в качестве фосфорсодержащего наполнителя используют гидроксиапатит с размером частиц 100-20000 нм, в качестве биоразлагаемого алифатического полиэфира используют ε-поликапролактон со среднечисловой молекулярной массой от 70000 до 90000 г/моль, а в качестве органического растворителя используют ацетон, причем в раствор 76-98 мас.% ε-поликапролактона в ацетоне концентрацией 4-6 мас.% добавляют 1-3 мас.% полисорбата 20 и 1-21 мас.% гидроксиапатита, смесь нагревают до 40-50 °С при механическом перемешивании со скоростью 200-270 об/мин, выдерживают в течение 20-35 минут при перемешивании, а затем, не перемешивая, охлаждают до -20…+0 °С до осаждения в виде суспензии гранул, затем суспензию гранул перемешивают со скоростью 400-600 об/мин и подвергают вакуумному фильтрованию, влажные гранулы промывают изопропиловым спиртом в течение 5-12 минут и сушат в вакуумной камере при давлении 10 мбар в течение 6 часов при температуре 30 °С.
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТЫХ ПОЛИМЕРНЫХ БИОДЕГРАДИРУЕМЫХ ИЗДЕЛИЙ ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2006 |
|
RU2327709C2 |
| Coombes A.G.A | |||
| et al | |||
| Precipitation casting of polycaprolactone for applications in tissue engineering and drug delivery / Biomaterials, 2004, V | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Способ очищения амида ортотолуолсульфокислоты | 1921 |
|
SU315A1 |
| Iman Shirzaei Sani et al | |||
| Preparation and characterization of polycaprolactone/chitosan-g-polycaprolactone/hydroxyapatite electrospun nanocomposite scaffolds | |||
Авторы
Даты
2024-03-19—Публикация
2023-11-30—Подача