Область техники
[0001] Настоящее изобретение относится к соединениям, которые можно использовать в качестве зондов на основе активности и/или ингибиторов цистеиновых протеаз, таких как катепсин X, способам детектирования активности цистеиновой протеазы и связанным диагностическим и терапевтическим способам и применениям.
Уровень техники
[0002] Согласно Lechtenberg et al., ACS Chem. Biol. 2015, 10, 945-951, «протеазы являются центральными медиаторами многочисленных физиологических процессов». События протеолитического расщепления лежат в основе деградации белка, активации ферментов и созревания белка и регулируют широкий спектр путей от гибели, миграции и пролиферации клеток, воспаления и иммунного ответа, до свертывания крови (Rawlings N. D. and Salvesen G. (2012) Handbook of Proteolytic Enzymes, Third edition, Academic Press, Waltham, MA). С другой стороны, аберрантный протеолиз часто связан с серьезными нарушениями. Кроме того, протеазы обычно экспрессируются в клетке или секретируются в виде неактивных зимогенов, которые нуждаются в активации посредством таких процессов, как протеолитическое расщепление или димеризация. Активация протеаз лежит в основе жесткой временной и пространственной регуляции, и, таким образом, обычно расположение протеазы не является идеальным маркером функции протеазы. Напротив, пространственно-временное расположение активной формы данной протеазы необходимо для понимания ее функции. С этой целью были разработаны зонды, основанные на активности, для различных протеаз (Deu E., Verdoes M. and Bogyo M. (2012), New approaches for dissecting protease functions to improve probe development and drug discovery. Nat. Struct. Mol. Biol. 19, 9−16). Данные зонды сконструированы в виде ингибиторов протеаз, взаимодействующих с активными центрами, для того, чтобы специфически метить активную протеазу, и, таким образом, они являются эффективными инструментами для исследований и диагностики. Кроме того, эти зонды дополнительно открывают путь для разработки сильных ингибиторов выбранных протеаз для потенциального терапевтического применения (Deu et al. 2012, Nat. Struct. Mol. Biol. 19, 9-16)».
[0003] Среди целевых ферментов, представляющих интерес, находятся цистеиновые протеазы, включая цистеиновые катепсины и, в частности, катепсин X.
[0004] Цистеиновые катепсины представляют собой семейство лизосомальных протеаз, которые часто активируются при различных злокачественных заболеваниях человека и участвуют в различных онкогенных процессах, таких как ангиогенез, пролиферация, апоптоз и инвазия. Семейство цистеиновых катепсинов составляет самое большое семейство катепсинов с 11 протеазами у людей, относящихся у клану CA, семейству CI a: катепсины B, C (также известные как катепсин J и дипептидил-пептидаза 1), F, H, K (также известные как катепсин 02), L, O, S, W, V (также известные как катепсин L2) и Z (также известный как катепсин X и катепсин P). Катепсины становятся важными участниками в процессе прогрессирования опухолей, что делает их потенциальными мишенями для лечения широкого спектра окологических заболеваний человека.
[0005] Катепсин X (также относящийся к катепсину Z/P) представляет собой цистеиновую протеазу катепсин, которая является уникальной среди членов своего семейства в том отношении, что проявляет строгую карбоксипептидазную активность. Предполагается, что катепсин X лежит в основе многих заболеваний человека. Его экспрессия была связана с несколькими типами рака и нейродегенеративными заболеваниями, хотя его роль в нормальной физиологии все еще плохо изучена. Прогрессу в нашем понимании его функции препятствует отсутствие доступных инструментов, которые могут специфически измерить протеолитическую активность катепсина X.
[0006] Катепсин X способствует адгезии и созреванию макрофагов и дендритных клеток (Obermajer et al., 2008) и подавляет клатрин-зависимый фагоцитоз посредством расщепления профилей (Pečar Fonović and Kos, 2015). Катепсин X регулирует передачу сигналов гормонов, где его расщепление на брадикинин, каллидин или ангиотензин приводит к изменениям специфичности по отношению к их родственным рецепторам и дивергентной передаче сигналов ниже (Nägler et al., 2010). Катепсин X также экспрессируется нейронами, где его расщепление α-енолазой регулирует выживание и рост нейритов (Obermajer et al., 2009). Кроме того, экспрессия катепсина X является высокой в амилоидных бляшках, где он может оказывать защитное действие против нейродегенеративных расстройств, таких как болезнь Альцгеймера (Hafner et al., 2013; Wendt et al., 2007), и в спинном мозге при нейропатической боли (Leichsenring et al., 2008). Сообщалось о повышении регуляции мРНК катепсина X в не имеющих патологии областях мозга, пораженного рассеянным склерозом (Huynh et al., 2014), и он был вовлечен в генерацию IL-1β (Allan et al., 2017; Orlowski et al., 2015) и в опосредовании нейровоспаления (Allan et al., 2017). Он также активируется в микросреде опухолей молочной железы (Edgington-Mitchell et al., 2015), поджелудочной железы (Akkari et al., 2014), предстательной железы (Nägler et al., 2004) и желудка (Bernhardt et al., 2010; Krueger et al., 2005), где он, вероятно, способствует инвазированию опухоли. Таким образом, катепсин X является многообещающим клиническим биомаркером и терапевтической мишенью при различных заболеваниях.
[0007] Как и большинство катепсинов, катепсин X синтезируется в виде зимогена, который активируется в кислой среде эндолизосом. После активации он также может отрицательно регулироваться эндогенными ингибиторами, хотя, вероятно, не цистатином С или стефином А (Duivenvoorden et al., 2017; Nägler et al., 1999). Помимо своих протеолитических функций, катепсин X может также способствовать передаче сигналов, опосредованной интегрином, через мотив Arg-Gly-Asp (RGD) в своем продомене (Akkari et al., 2014). В результате этих сложных механизмов посттрансляционной регуляции традиционные биохимические методы, с помощью которых определяют уровни общего белка, редко отражают пул протеолитически активного фермента. Следовательно, возможность специфически измерять его активность в естественной среде, необходима для точного определения его протеолитических функций в здоровом и болезненном состоянии.
[0008] С этой целью были сосредоточены усилия на разработке зондов на основе флуоресцентной активности (ABP) для катепсина X. Флуоресцентные ABP представляют собой небольшие молекулы, которые содержат электрофильную группу (активную группу), последовательность распознавания, которая придает селективность, и флуорофор для детектирования (Edgington и Bogyo, 2013; Edgington et al., 2011; Sanman, Bogyo, 2014). В активном состоянии протеаза инициирует нуклеофильную атаку на активную группу, в результате чего образуется ковалентная необратимая связь. Затем оценку мечения зонда можно использовать для количественной оценки протеазной активности с помощью SDS-PAGE (флуоресценция в геле), флуоресцентной микроскопии, проточной цитометрии или оптической визуализации целых тканей или организмов. Важно отметить, что ковалентный характер связывания зонда позволяет подтвердить мишень посредством иммунопреципитации специфическими антителами или аффинной очистки с последующим протеомным анализом.
[0009] О зондах с абсолютной специфичностью для катепсина X ранее не сообщалось. BMV109, флуоресцентно гасящий ABP с тетрафторфеноксиметилкетоновой группой, представляет собой пан-катепсиновый зонд, нацеленный на катепсин X, B, S и L (Verdoes et al., 2013; Edgington-Mitchell et al., 2015). Поскольку размер катепсина X аналогичен катепсину B, одному из наиболее распространенных и повсеместно экспрессируемых катепсинов, то может быть трудно четко разделить эти две протеазы с помощью SDS-PAGE. Это препятствует точному количественному определению с помощью флуоресценции в геле. MGP140 представляет собой эпоксидный зонд на основе активности, который проявляет большую специфичность к катепсину X, чем BMV109, но также активно реагирует с катепсином B (Paulick and Bogyo, 2011). Если мышей предварительно обработали GB11-NH2, ингибитором катепсина B, S и L, перед инъекцией MGP140, то можно достичь специфического мечения катепсина X. Однако такая манипуляция с системой приводит к гиперактивации катепсина X, возможно, компенсаторного характера за потери активности катепсина B. Таким образом, критически важно разработать зонды на основе активности с повышенной специфичностью к катепсину X, чтобы можно было оценить его физиологическую активность.
[0010] Shaw раскрывает синтез солей пептидилсульфония и их ингибирующее действие на цистеинилпротеазы, папаин и катепсин B (Shaw, 1988).
[0011] Gordon et al., патент США № 5223486, раскрывают пептидилдиазометилкетоны и соли пептидилсульфония в качестве ингибиторов опухолевого прокоагулянта, цистеиновой протеазы.
[0012] Paulick et al. описывают синтез и характеристику нескольких зондов на основе флуоресцентной активности, несущих либо ацилоксиметилкетон (AOMK), либо эпоксидную активную группу, предназначенных для нацеливания на катепсин X. Было обнаружено, что зонды на основе эпоксида метили катепсин X, тогда как зонды AOMK были неспособны метить данную протеазу (Paulick and Bogyo, 2011).
[0013] Таким образом, остается потребность в соединениях, функционирующих в качестве зондов (или ингибиторов) на основе активности цистеиновых протеаз, таких как цистеиновые катепсины и, более конкретно, катепсин X. Такие соединения пригодны для исследования роли соответствующей цистеиновой протеазы в нормальной физиологии и при заболеваниях. Кроме того, такие соединения могут быть пригодны в диагностике и/или лечении заболеваний, ассоциированных с соответствующей активностью цистеиновой протеазы.
[0014] Авторы настоящего изобретения попытались изыскать новые потенциальные активные группы для цистеиновых протеаз и неожиданно обнаружили, что соединения, описанные ниже, несущие фрагмент илида сульфоксония в качестве активной группы, могут функционировать в качестве зондов на основе активности для цистеиновых протеаз, таких как цистеиновые катепсины, и более конкретно катепсин X, с повышенной эффективностью и селективностью по сравнению с ранее описанными зондами (такими как BMV109 и MGP140).
Цели и сущность изобретения
[0015] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность цистеиновой протеазы в биологических образцах, таких как лизаты клеток или лизаты тканей.
[0016] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность цистеиновой протеазы в живых клетках.
[0017] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность цистеиновой протеазы in vivo.
[0018] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность катепсина X в биологических образцах, таких как клеточные лизаты или лизаты тканей.
[0019] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность катепсина X в живых клетках.
[0020] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность катепсина X in vivo.
[0021] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение зондов на основе активности, которые позволяют детектировать активность цистеиновой протеазы с повышенной селективностью по сравнению с зондами, основанными на активности, BMV109 и MGP140.
[0022] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность катепсина X с повышенной селективностью по сравнению с зондами, основанными на активности, BMV109 и MGP140.
[0023] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность катепсина X с высокой эффективностью для катепсина X, такую как повышенная эффективность для катепсина X по сравнению с зондами на основе активности, BMV109 и MGP140.
[0024] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений-зондов на основе активности, которые позволяют детектировать активность катепсина X (например, в клеточных лизатах, тканевых лизатах, живых клетках и in vivo) и которые не проявляют перекрестной реактивности с катепсином B и/или катепсином L.
[0025] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение ингибиторов цистеиновой протеазы.
[0026] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение ингибиторов катепсина X.
[0027] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение ингибиторов катепсина X, которые не проявляют перекрестной реактивности с катепсином B и/или катепсином L.
[0028] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений, которые можно использовать для диагностики заболевания, ассоциированного с активностью цистеиновой протеазы.
[0029] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений, которые можно использовать для диагностики заболевания, ассоциированного с активностью катепсина X.
[0030] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений, которые можно использовать для диагностики заболевания, выбранного из группы, состоящей из рака, воспалительных заболеваний и нейродегенеративных заболеваний.
[0031] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений, которые можно использовать для лечения заболевания, ассоциированного с активностью цистеиновой протеазы.
[0032] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений, которые можно использовать для лечения заболевания, ассоциированного с активностью катепсина X.
[0033] Целью некоторых вариантов осуществления настоящего изобретения является обеспечение соединений, которые можно использовать для лечения заболевания, выбранного из группы, состоящей из рака, воспалительных заболеваний и нейродегенеративных заболеваний.
[0034] Следует понимать, что вышеуказанные цели также относятся к соответствующим способам, а также к соединениям/ композициям для применения в соответствующем способе.
[0035] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I:
[0036]
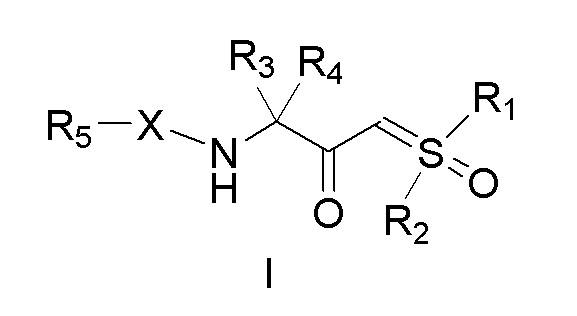
[0037] или его соли,
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R3 представляет собой боковую цепь альфа-аминокислоты;
R4 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R5 выбран из группы, состоящей из детектируемого элемента, аминозащитной группы, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила, (C2-C8) алкинила, (C1-C8) алкилкарбонила, (C1-C8) гидроксиалкилкарбонила, (C1-C8) галогеналкилкарбонила, (C3-C8) циклоалкилкарбонила, (C1-C8) алкилоксикарбонила, бензилоксикарбонила и атома водород;
X представляет собой:
(i) связь; или
(ii) бирадикальный фрагмент формулы II или III, который связан с заместителем R5 через аминогруппу,
[0038]
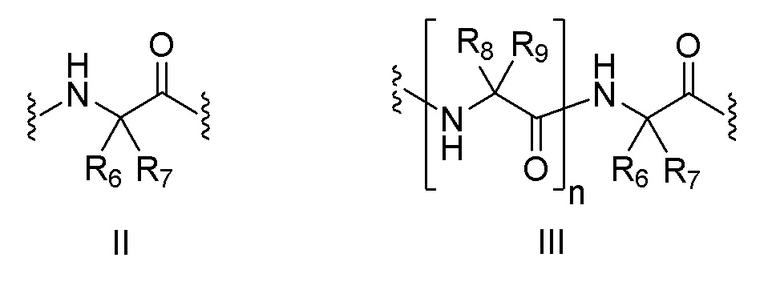
где:
R6 представляет собой боковую цепь альфа-аминокислоты;
R7 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R8 представляет собой боковую цепь альфа-аминокислоты;
R9 выбран из группы, состоящей из атома водорода и (C1-C4) алкила; и
n равно 1, 2, 3 или 4.
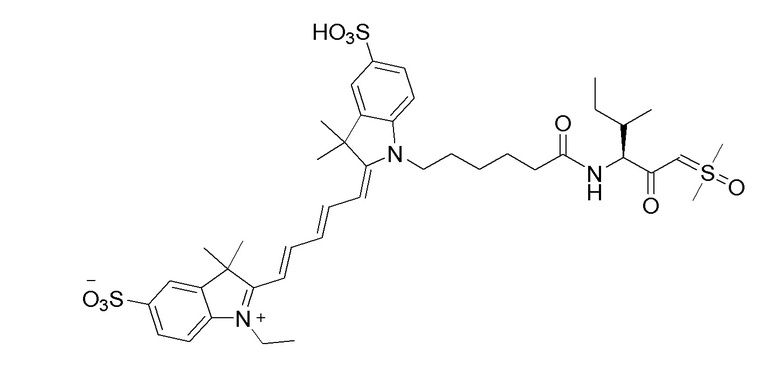
[0039] В некоторых вариантах осуществления настоящее изобретение относится к соединению (формулы I), имеющему формулу, выбранную из следующей группы формул:
[0040]
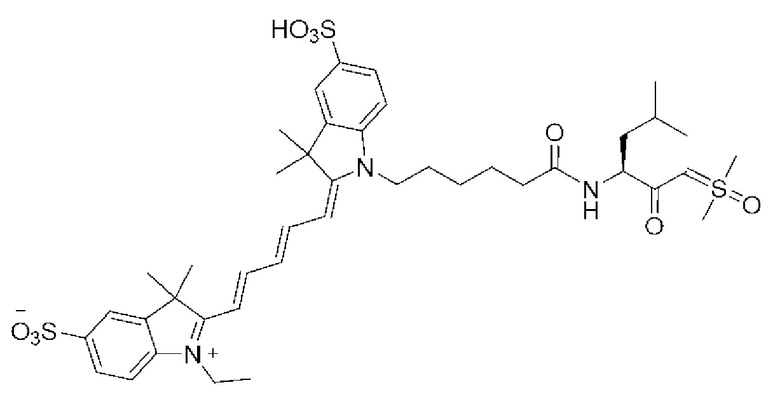
[0041]
[0042]
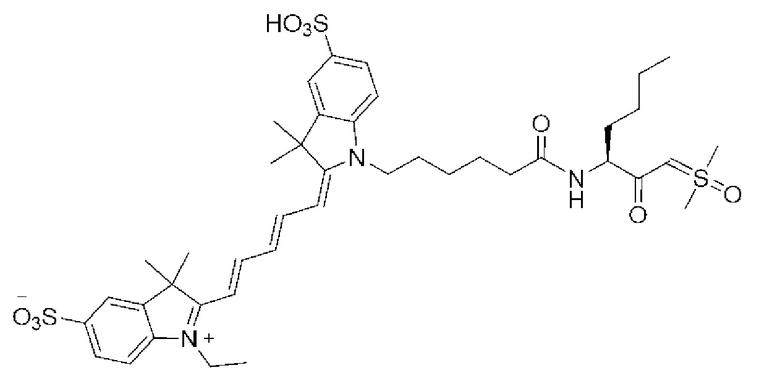
[0043]
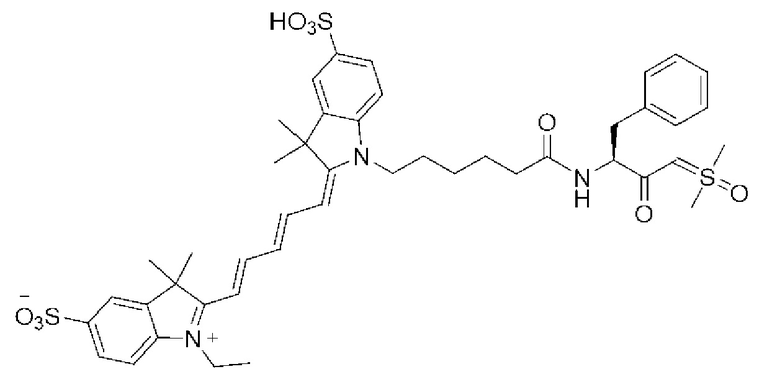
[0044]
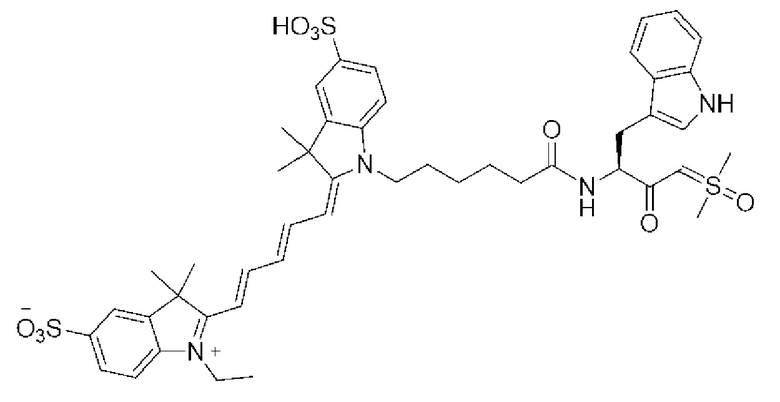
[0045]
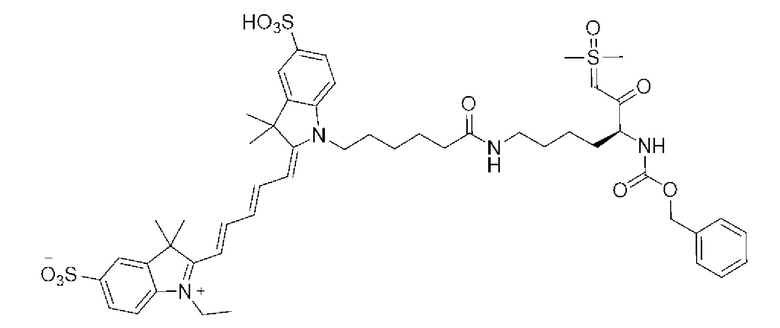
[0046]
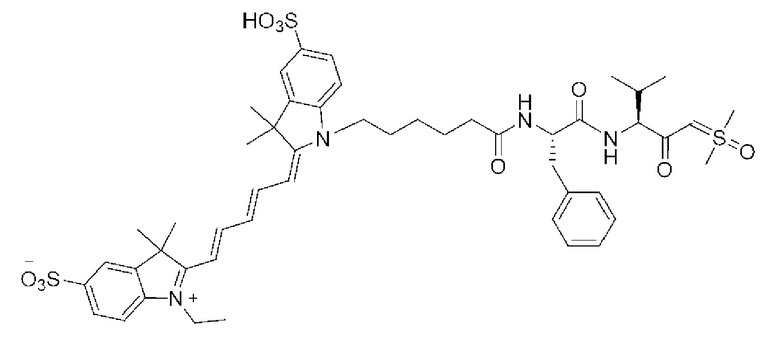
[0047] или его соли.
[0048] В некоторых вариантах осуществления настоящее изобретение относится к соединению (формулы I), имеющему следующую формулу:
[0049]
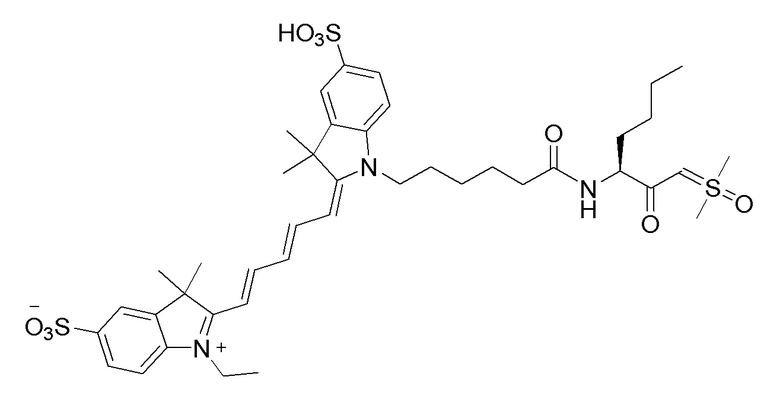
[0050] или его соли.
[0051] В некоторых вариантах осуществления настоящее изобретение относится к композиции, содержащей соединение формулы I, как здесь описано, или его соль, и эксципиент.
[0052] В некоторых вариантах осуществления настоящее изобретение относится к композиции, содержащей соединение формулы I, как здесь описано, или его соль, и эксципиент, где соединение содержит, по меньшей мере, один детектируемый элемент.
[0053] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) контактирование цистеиновой протеазы с соединением-зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ цистеиновой протеазы, включающий измерение детектируемого сигнала.
[0054] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеинпротеазы in vitro, включающему:
(1) контактирование биологического образца с соединением зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0055] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы в биологическом образце, полученном от субъекта, включающему:
(1) контактирование биологического образца in vitro с соединением-зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0056] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) контактирование цистеиновой протеазы с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ цистеиновой протеазы, включающий измерение детектируемого сигнала.
[0057] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы in vitro, включающему:
(1) контактирование биологического образца с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0058] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы в биологическом образце, полученном от субъекта, включающему:
(1) контактирование биологического образца in vitro с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0059] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) введение субъекту соединения-зонда на основе активности, содержащего фрагмент илида сульфоксония, в качестве активной группы,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0060] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0061] В некоторых вариантах осуществления настоящее изобретение относится к способу in vivo детектирования активности цистеиновой протеазы у субъекта, включающему:
(1) введение субъекту соединения-зонда на основе активности, содержащего фрагмент илид сульфоксония в качестве активной группы, и
(2) последующее обследование субъекта, включающее измерение обнаруживаемого сигнала.
[0062] В некоторых вариантах осуществления настоящее изобретение относится к способу in vivo детектирования активности цистеиновой протеазы у субъекта, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
[0063] В некоторых вариантах осуществления настоящее изобретение относится к способу ингибирования цистеиновой протеазы, включающему контактирование цистеиновой протеазы с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано.
[0064] В некоторых вариантах осуществления настоящее изобретение относится к способу ингибирования цистеиновой протеазы in vitro, включающему контактирование биологического образца с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано.
[0065] В некоторых вариантах осуществления настоящее изобретение относится к способу ингибирования цистеиновой протеазы в биологическом образце, полученном от субъекта, включающему контактирование биологического образца in vitro с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано.
[0066] В некоторых вариантах осуществления настоящее изобретение относится к способу in vivo ингибирования цистеиновой протеазы у субъекта, включающему введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано.
[0067] В некоторых вариантах осуществления настоящее изобретение относится к способу диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающему:
(1) контактирование биологического образца, полученного от субъекта in vitro, с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0068] В некоторых вариантах осуществления настоящее изобретение относится к способу диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0069] В некоторых вариантах осуществления настоящее изобретение относится к способу in vivo диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано, и
(2) последующее обследование субъекта, включающее измерение обнаруживаемого сигнала.
[0070] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, как здесь описано, или его соли для применения в способе диагностики заболевания, ассоциированного с активностью цистеинпротеазы, у субъекта, где способ включает:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0071] В некоторых вариантах осуществления настоящее изобретение относится к композиции, как здесь описано, для применения в способе диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту композиции, как здесь описано,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0072] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, как здесь описано, или его соли для применения в способе диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта in vivo, где способ включает:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, и
(2) последующее обследование субъекта, включающее измерение обнаруживаемого сигнала.
[0073] В некоторых вариантах осуществления настоящее изобретение относится к композиции, как здесь описано, для применения в способе диагностики in vivo заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту композиции, как здесь описано, и
(2) последующее обследование субъекта, включающее измерение обнаруживаемого сигнала.
[0074] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения заболевания, ассоциированного с активностью цистеиновой протеазы, включающему введение пациенту, нуждающегося в этом, терапевтически эффективного количества соединения формулы I, как здесь описано, или его соли, или терапевтически эффективное количество композиции, как здесь описано.
[0075] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, как здесь описано, или его соли для применения в лечении заболевания, ассоциированного с активностью цистеиновой протеазы.
[0076] В некоторых вариантах осуществления настоящее изобретение относится к композиции для применения в лечении заболевания, ассоциированного с активностью цистеиновой протеазы, содержащую соединение формулы I, как здесь описано, или его соль и фармацевтически приемлемый эксципиент.
[0077] В некоторых вариантах осуществления настоящее изобретение относится к применению соединения формулы I, как здесь описано, или его соли в производстве лекарственного средства для лечения заболевания, ассоциированного с активностью цистеиновой протеазы.
[0078] В некоторых вариантах осуществления настоящее изобретение относится к применению композиции, описанной здесь, в производстве лекарственного средства для лечения заболевания, ассоциированного с активностью цистеиновой протеазы.
[0079] В некоторых вариантах осуществления настоящее изобретение относится к способу получения соединения, несущего хлорметилкетоновую группу, включающему взаимодействие соединения, несущего фрагмента илида сульфоксония, с получением соединения, несущего хлорметилкетоновую группу.
[0080] В некоторых вариантах осуществления настоящее изобретение относится к способу получения соединения-зонда на основе активности, несущего ацилоксиметилкетоновую группу в качестве активной группы, включающему:
(i) получение промежуточного соединения, несущего хлорметилкетоновую группу, взаимодействием соединения, содержащего фрагмент илида сульфоксония, с получением соединения, несущего хлорметилкетоновую группу; и
(ii) дальнейшую обработку соединения, содержащего хлорметилкетоновый фрагмент, с получением указанного соединения-зонда на основе активности.
Краткое описание фигур
[0081] На фиг. 1А приведена структура зонда sCy5-Val-SY.
На фиг. 1В представлен предполагаемый механизм связывания зонда sCy5-Val-SY с цистеиновой протеазой.
На фиг. 2А приведены результаты примера 3 (мечение лизатов RAW264.7 sCy5-Val-SY (при 1 мкМ в течение 20 мин) или BMV109 (при 1 мкМ в течение 20 мин) самостоятельно или после предварительной обработки 10 мкМ MDV-590 (ингибитор катепсина S) или JPM-OEt (панингибитор цистеинового катепсина).
На фиг. 2A-1 приведены результаты примера 3 (мечение лизатов RAW264.7 указанными концентрациями sCy5-Val-SY в течение 20 мин по данным анализа флуоресценции в геле).
На фиг. 2A-2 приведены результаты примера 3 (мечение лизатов RAW264.7 1 мкМ sCy5-Val-SY в течение указанного времени, по данным анализа флуоресценции в геле).
На фиг. 2В приведены результаты примера 3 (иммунопреципитация образцов, меченных sCy5-Val-SY (мечение при 1 мкМ в течение 20 мин), с антителом, специфичным к катепсину X).
На фиг. 2С приведены результаты примера 4 (мечение лизатов селезенки от мышей дикого типа или мышей с дефицитом катепсина X с помощью sCy5-Val-SY или BMV109).
На фиг. 2D приведены результаты примера 5 (мечение живых клеток RAW264.7 возрастающими дозами sCy5-Val-SY или BMV109 в течение 2 ч).
На фиг. 2D-1 приведены результаты примера 5 (мечение живых (интактных) клеток RAW264.7 1 мкМ sCy5-Val-SY в течение указанного времени, анализировано с помощью флуоресценции в геле).
На фиг. 2E приведены результаты примера 5 (иммунопреципитация образцов, меченных sCy5-Val-SY (мечение живых клеток при 1 мкМ в течение 2 ч), с антителом, специфичным к катепсину X).
На фиг. 2F приведены результаты примера 5 (мечение живых клеток RAW264.7 с предварительной обработкой в течение ночи 10 мкМ MDV-590, sCy5-Val-SY или BMV109 (1 мкМ, 2 ч) и без нее.
На фиг. 3A приведены результаты примера 6 (мечение лизатов RAW264.7 указанным зондом на основе илида сульфоксония или BMV109 (зонд вносили в возрастающих концентрациях 0,01, 0,05, 0,1, 0,5, 1, 5 мкМ, как показано стрелкой с возрастающим фоном)).
На фиг. 3В приведены результаты примера 7 (мечение лизатов почек указанным зондом на основе илида сульфоксониевого или BMV109 (зонд вносили в возрастающих концентрациях 0,1, 0,5, 1,5 мкМ, как показано стрелкой с возрастающим фоном)).
На фиг. 3C приведены результаты примера 8 (мечение живых клеток RAW264.7 указанным зондом на основе илида сульфоксония или BMV109 (зонд вносили в возрастающих концентрациях 0,1, 0,5, 1, 5 мкМ, как показано стрелкой с возрастающим фоном)).
На фиг. 3D приведены результаты примера 9 (мечение живых клеток MDA-MB-231HM указанным зондом на основе илида сульфоксония или BMV109 (зонд вносили в возрастающих концентрациях 0,1, 0,5, 1, 5 мкМ, как показано стрелкой с возрастающим фоном)).
На фиг. 4A приведены результаты примера 10 (SDS-PAGE и флуоресценция в геле тканей мышей, которые не получали зонд (NP), sCy5-Nle-SY или BMV109. Образцы, меченные BMV109, вырезаны из того же геля и представлены при той же настройке усиления, что и другие образцы в соответствующей ткани. Усиления для каждой ткани были установлены индивидуально для отображения оптимального контраста для мечения катепсина X. Аутофлуоресцентную полосу наблюдали в контроле без зонда.
На фиг. 4В приведены результаты примера 10 (иммунопреципитация образцов печени и почек с антителом, специфичным к катепсину X).
На фиг. 5 приведены результаты примера 10 (конфокальная микроскопия мечения катепсина X в почках с помощью sCy5-Nle-SY. Срезы почек мышей, которым инъецировали sCy5-Nle-SY, или контрольных животных без зонда, анализировали на флуоресценцию sCy5 или иммунореактивность катепсина X.
На фиг. 6A приведены результаты примера 11 (мечение живых клеток RAW264.7 указанными зондами AOMK и илидом сульфоксония (в возрастающих концентрациях 0,1, 0,5, 1 и 5 мкМ, как показано стрелкой с возрастающим фоном), как было анализировано с помощью флуоресценции в геле. На верхней панели настройки усиления одинаковы для всех образцов. На нижней панели настройки усиления были индивидуально установлены для отображения оптимального контраста для зондов AOMK.
На фиг. 6В приведены результаты примера 12 (мечение толстого кишечника in vivo зондом sCy5-Nle-AOMK. Верхняя полоса представляет собой аутофлуоресцентный белок, который появляется в контролях без зонда).
На фиг. 7 приведены результаты экспериментов по идентификации протеаз, меченных зондом. (A, C-G): Иммунопреципитация меченых зондами лизатов (клетки RAW264.7 или почки, с указанным зондом, который вводили в живые клетки или лизаты, как указано) с катепсин-специфическими антителами. (B) Мечение живых клеток RAW264.7 с и без предварительной обработки в течение ночи ингибиторами катепсина S MDV590 (10 мкМ) или Z-FL (20 мкМ) с sCy5-Nle-SY (1 мкМ, 2 ч).
На фиг. 8A приведены результаты примера 13 (мечение лизатов, полученных из ткани плоскоклеточной карциномы ротовой полости человека или подобранной пациенту нормальной слизистой оболочки полости рта, sCy5-Nle-SY (инкубация при 5 мкМ в течение 20 мин) и анализ с помощью флуоресценции в геле, а также иммуноблоттинг образцов).
На фиг. 8B приведены результаты примера 13 (иммунопреципитация лизатов ткани карциномы ротовой полости человека, меченных Cy5-Nle-SY, с антителом, специфичным к катепсину X).
На фиг.9 приведены результаты примера 14 (мечение клеток RAW264.7, которые были предварительно обработаны Boc-Val-SY (0, 10 или 100 мкМ) в течение ночи с помощью sCy5-Val-SY, и анализ лизированных клеток с помощью флуоресценции в геле).
Подробное описание изобретения
[0082] При описании настоящего изобретения следует использовать следующие термины, как указано ниже.
[0083] В рамках настоящего изобретения, формы единственного числа включают множественные ссылки, если контекст явно не указывает иное.
[0084] Если не указано иное, то все технические и научные термины, используемые здесь, имеют те же значения, которые обычно понимаются специалистами в данной области.
[0085] Подразумевается, что термин «зонд на основе активности» имеет такое же значение, какое обычно понимается специалистами в данной области. Зонды, основанные на активности (ABP), представляют собой небольшие молекулы, которые ковалентно связываются с активным сайтом фермента (например, протеазы) или группы ферментов в зависимости от активности (т. е. для реакции мечения требуется активность фермента). ABP обычно включают три элемента: (i) электрофильную группу, называемую «активной группой», (ii) линкер или последовательность распознавания и (iii) детектируемый элемент или «репортерный фрагмент» для детектирования. Фермент атакует электрофильную активную группу, что приводит к образованию ковалентного аддукта, который затем можно детектировать либо непосредственно (например, если детектируемый элемент представляет собой флуоресцентную метку), либо с помощью двухэтапного мечения (например, постмечение модификации маркера для лигирования).
[0086] Термин «детектируемый элемент» или «репортерная группа/фрагмент» относится к функциональной группе в соединении (зонд на основе активности), который можно детектировать с использованием методов, включая, помимо прочего, оптические методы (например, измерение флуоресценции или поглощение УФ-излучения), радиография, биохимические методы (например, с использованием иммунохимического реагента, такого как антитело) и т.д. Термин «детектируемый элемент» включает функциональные группы, которые могут детектироваться «напрямую» (например, измерением флуоресценции после анализа SDS-PAGE), а также функциональные группы, которые можно детектировать после выполнения стадии вторичного мечения и последующего детектирования вторичной метки. Примером таких групп является биотиновая метка, которую можно детектировать, например, после вторичного мечения флуоресцентно-меченным стрептавидином и последующего измерения флуоресценции. Еще одним примером таких групп является клик-химическая метка (биоортогональный маркер для лигирования), которую можно детектировать, например, после вторичного мечения флуоресцентной меткой с использованием клик-химической (биоортогональной) реакции и последующего измерения флуоресценции.
[0087] Таким образом, «биоортогональный маркер для лигирования» представляет собой функциональную группу, присутствующую в соединениях по настоящему изобретению на начальной стадии мечения зондом (in vivo или ex vivo контактирование протеазы/биологического образца/субъекта с соединениями по настоящему изобретению), что обеспечивает последующее присоединение вторичной метки (соответствующей фактически детектированной метке) на стадии вторичного мечения с использованием, например, клик-химической (биоортогональной) реакции, которая проводится in vitro.
[0088] Клик-химические метки и соответствующие реакции клик-химические реакции для вторичного мечения, т. е. присоединения метки, которая должна быть фактически детектирована, описаны, например, в Martell et al., Applications of Copper-Catalyzed Click Chemistry in Activity-Based Protein Profiling, Molecules 2014, 19, 1378-1393, и в Willems et al., Bioorthogonal chemistry: Applications in activity-based protein profiling, Acc. Chem. Res. 2011, 44, 718-729.
[0089] Термин «активность цистеиновой протеазы» относится к протеолитической активности цистеиновой протеазы. В случае катепсина X термин «активность цистеиновой протеазы» или «активность катепсина X» относится к протеолитической активности, которая представляет собой карбоксипептидазную активность.
[0090] Катепсин X, S, B и L каждый относится к семейству цистеиновых протеаз. Термин «катепсин X» обозначает белок, полученный из локуса гена CTSZ. «Катепсин X» также называют «катепсином Z» или «катепсином P». Термин «катепсин S» обозначает белок, полученный из локуса гена CTSS. Термин «катепсин B» обозначает белок, полученный из локуса гена CTSB. Термин «катепсин L» обозначает белок, полученный из локуса гена CTSL.
[0091] Термин «пациент» означает субъекта, в частности человека, у которого появилось клиническое проявление конкретного симптома или симптомов, указывающих на необходимость лечения, которого лечат превентивно или профилактически от состояния, или у которого было диагностировано состояние, подлежащее лечению.
[0092] Термин «субъект» предназначен для включения субъектов-млекопитающих, в частности субъектов-людей, и включает определение термина «пациент» и не исключает субъектов, которые являются полностью нормальными во всех отношениях или в отношении конкретного состояния.
[0093] В рамках настоящего изобретения, термин «терапевтически эффективное» относится к количеству лекарственного средства или уровню введения лекарственного средства, необходимых для получения желаемого терапевтического результата.
[0094] В рамках настоящего изобретения, термины, подобные «введению» или «проводить введение», включают различные пути введения, такие как внутривенно, подкожно, внутримышечно, перорально, интраназально, сублингвально или местно.
[0095] Термин «образец ткани» или «биопсийный материал ткани» относится к образцу биологической ткани, полученному от субъекта, такому как образец, полученный путем иссечения, пункционной аспирации, биопсийных щипцов или мазка. Образцы тканей также включают биопсийный материал слизистой оболочки и образцы кала. Отобранная ткань может быть живой, мертвой, здоровой или больной и содержать гетерогенную смесь типов клеток и внеклеточных факторов
[0096] «Биопсийный материал слизистой оболочки» обычно получают отбором слизи, скопившейся на поверхности другой ткани, например слизистые оболочки или эпителий кишечного тракта. Биопсийный материал слизистой оболочки содержит клетки, выделенные из ткани, на которой скопилась слизь.
[0097] Термин «образец мокроты» относится к образцу, который представляет собой смесь слюны и слизи, откашливаемой из дыхательных путей. «Образец мокроты» можно получить инвазивным или неинвазивным способом. Инвазивные методы включают ротоглоточное или эндотрахеальное отсасывание во время интубации пациента, и полученное содержимое собирают в ловушку для мокроты. С помощью неинвазивных методов собирают содержимое, образующееся при кашле у субъекта, иногда после распыления физиологического раствора для разжижения секрета.
[0098] Термин «образец фекалий» или «образец кала» относится к образцу, взятому из кала субъекта. Образцы кала содержат клетки, выделенные из желудочно-кишечного тракта, и выделения клеток из желудочно-кишечного тракта субъекта.
[0099] Термин «лизат образца ткани» относится к раствору, полученному лизированием клеток образца ткани. Термин «лизирование» или «лизис» относится к дезинтеграции или разрыву клеточных мембран, что приводит к высвобождению содержимого клетки и/или последующей гибели клетки. Лизис может быть выполнен, например, посредством механического, ферментативного или осмотического разрушения клеточных мембран.
[0100] В рамках настоящего изобретения, термин «заболевание, ассоциированное с активностью цистеиновой протеазы» обозначает заболевание, при котором активность цистеиновой протеазы участвует в патогенезе заболевания. При «заболевании, ассоциированном с активностью цистеиновой протеазы», уровень активности цистеиновой протеазы при болезненном состоянии или в пораженной области тела (например, части тела, органе, патологической ткани, включая опухолевую ткань) отклоняется от соответствующего уровня активности цистеиновой протеазы, детектированной в состоянии без патологии или в соответствующей области тела без патологии. В некоторых вариантах осуществления уровень активности цистеиновой протеазы при болезненном состоянии или в пораженной области тела повышен по сравнению с соответствующим уровнем активности цистеиновой протеазы, детектированный в состоянии без патологии или в соответствующей области тела без патологии. Например, при патологическом состоянии или в области без патологии уровень активности цистеиновой протеазы может быть ниже определяемого предела, тогда как при болезненном состоянии или в пораженной области уровень активности цистеиновой протеазы выше определяемого предела. Заболевания, ассоциированные с активностью цистеиновой протеазы, включают целиакию, расстройства перистальтики желудочно-кишечного тракта, боль, зуд, кожное заболевание, ожирение, вызванное рационом, метаболическое нарушение, астму, ревматоидный артрит, пародонтит, воспалительное заболевание желудочно-кишечного тракта, функциональное расстройство желудочно-кишечного тракта, рак, фиброзное заболевание, метаболическую дисфункцию, неврологическое заболевание, хроническую обструктивную болезнь легких (COPD) и инфекцию. В некоторых вариантах осуществления «заболевание, ассоциированное с активностью цистеиновой протеазы», представляет собой «заболевание, ассоциированное с активностью катепсина X».
[0101] В рамках настоящего изобретения, термины «воспалительное заболевание желудочно-кишечного тракта», «воспалительное желудочно-кишечное расстройство», «воспалительное расстройство желудочно-кишечного тракта» или «воспалительное желудочно-кишечное заболевание» обозначают желудочно-кишечные заболевания, т. е. заболевания, затрагивающие желудочно-кишечный тракт, а именно ротовую полость, пищевод, желудок, тонкий кишечник, толстый кишечник (ободочную кишку) и прямую кишку, а также дополнительные органы пищеварения (например, язык, слюнные железы, поджелудочную железу, печень и желчный пузырь), в которых наблюдается воспаление одной или более частей желудочно-кишечного тракта. Воспалительные заболевания желудочно-кишечного тракта включают, например, воспалительные заболевания кишечника, инфекционную диарею, ишемию брыжейки, дивертикулит и некротический энтероколит (NEC).
[0102] Термин «воспалительное заболевание кишечника» или «IBD» относится к совокупности заболеваний, характеризующихся хроническим и рецидивирующим воспалением в желудочно-кишечном тракте. IBD, в первую очередь, включает язвенный колит (UC) и болезнь Крона (CD), оба из которых связаны с диареей, ректальным кровотечением, повышенными позывами к дефекации и болью, но также включают менее распространенные заболевания, такие как острый колит, иммуноонкологический колит, колит в результате химиотерапии/лучевой терапии, колит на фоне синдрома «трансплантат против хозяина» (GvHD), коллагенозный колит, лимфоцитарный колит, микроскопический колит, диверсионный колит, болезнь Бехчета и колит неопределенной этиологии и поухит.
[0103] В рамках настоящего изобретения, термин «функциональные расстройства желудочно-кишечного тракта», «функциональные желудочно-кишечные расстройства» или «функциональные заболевания желудочно-кишечного тракта» обозначает нарушения взаимодействия кишечника и головного мозга. Это группа расстройств, классифицируемых по желудочно-кишечным симптомам, связанным с любой комбинацией следующих факторов: нарушение моторики, висцеральная гиперчувствительность, изменение слизистой оболочки и иммунной функции, измененная микробиота кишечника и измененный процессинг центральной нервной системы (ЦНС). Термин «функциональный» обычно применяется к расстройствам, при которых нарушается нормальная деятельность организма с точки зрения моторики кишечника, чувствительности нервов кишечника или того, как мозг контролирует некоторые из этих функций. Однако структурные аномалии, которые можно увидеть с помощью эндоскопии, рентгена или анализов крови, отсутствуют. Таким образом, эти расстройства во многом идентифицируются по характеристикам симптомов. Функциональные расстройства желудочно-кишечного тракта включают синдром раздраженного кишечника, функциональную боль в груди, функциональную диспепсию, тошноту и рвоту, функциональные запоры, функциональную диарею, недержание кала, функциональную аноректальную боль и функциональные нарушения дефекации
[0104] Термин «инфекция» относится к процессу или состоянию, при котором инфекционный агент (например, такой как патогенные бактерии, грибы, простейшие, вирусы, прионы, вироиды, нематоды и другие гельминты) проникает и размножается в тканях тела инфицированного субъекта.
[0105] Термин «рак» относится к совокупности заболеваний, характеризующихся неконтролируемым аномальным ростом клеток с возможностью проникновения или распространения в другие части тела. Рак может поражать любую ткань, и получает название по ткани, из которой он развивается. Термин «рак ротовой полости» относится к раку ротовой полости, т. е. к любому разрастанию раковой ткани, локализованному в полости рта субъекта. Типичными гистологическими типами рака ротовой полости являются тератома, аденокарцинома, происходящая из большой или малой слюнной железы, лимфома из миндалин или другой лимфоидной ткани или меланома из клеток слизистой оболочки полости рта, продуцирующих пигмент. Наиболее распространенным типом рака полости рта является плоскоклеточная карцинома, возникающая в тканях, выстилающих ротовую полость и губы, с менее распространенными типами, включающими саркому Капоши. Рак ротовой полости чаще всего поражает язык, но может также развиться на дне ротовой полости, на подкладке щек, деснах, губах или небе. Термин «рак молочной железы» относится к раку молочной железы. Примеры рака молочной железы включают протоковую карциному in situ (DCIS), лобулярную карциному in situ (LCIS), инвазивную протоковую карциному (IDC), инвазивную лобулярную карциному (ILC), рак соска Педжета, филлоидную опухоль и ангиосаркому. Термин «рак предстательной железы» относится к раку предстательной. Примеры рака предстательной железы включают аденокарциномы предстательной железы. Термин «колоректальный рак» относится к раку толстой и/или прямой кишки. Примеры колоректального рака представляют собой аденокарциномы, карциноидные опухоли, стромальные опухоли желудочно-кишечного тракта (GIST), лимфомы и саркомы, происходящие из толстой или прямой кишки.
[0106] Термин «альфа-аминокислота» означает природные и неприродные альфа-аминокислоты.
[0107] Термин «природная аминокислота» включает протеиногенные и непротеиногенные аминокислоты.
[0108] В отношение боковых цепей альфа-аминокислот, то термин «структурный аналог» относится к боковой цепи, в которой группа CH2 заменена на O, S или NH, и/или где группа -CH2-CH2- заменена на -CH=CH- группу.
[0109] В отношение боковых цепей альфа-аминокислот, то термин «гомолог» относится к боковой цепи, которая удлиняется на одну группу CH2.
[0110] Термин «(Cy-Cz)» при использовании в сочетании с химической группой, такой как алкил, алкенил, алкинил, циклоалкил, алкокси, арил и т. д., указывает возможное число атомов углерода в группе (т. е. от y до z атомов углерода).
[0111] В рамках настоящего изобретения, термин «алкил» обозначает алкильную группу с прямой или разветвленной цепью. Примеры алкильных групп включают метил, этил, н-пропил, изопропил, н-бутил, 2-бутил, изобутил, трет-бутил, н-пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил и 2,2-диметилпропил.
[0112] В рамках настоящего изобретения, термин «галогеналкил» обозначает алкильную группу с прямой или разветвленной цепью, в которой атомы водорода данной группы частично или полностью замещены атомами галогена. Примеры галогеналкильных групп включают фторметил, дифторметил, трифторметил, 1-фторэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил и тому подобное. В одном варианте от 1 до 3 атомов водорода заменены атомами галогена.
[0113] В рамках настоящего изобретения, термин «гидроксиалкил» обозначает алкильную группу с прямой или разветвленной цепью, в которой, по меньшей мере, один атом водорода этой группы заменен гидроксигруппой. В некоторых вариантах осуществления один или два атома водорода заменены гидроксигруппой. В некоторых вариантах осуществления один атом водорода заменен гидроксигруппой.
[0114] В рамках настоящего изобретения, термин «циклоалкил» означает насыщенный моноциклический углеводородный радикал. Примеры циклоалкильных групп включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил и циклодецил.
[0115] В рамках настоящего изобретения, термин «алкенил» обозначает, по меньшей мере, один ненасыщенный углеводородный радикал с прямой или разветвленной цепью, т. е. углеводородный радикал с прямой или разветвленной цепью, имеющий, по меньшей мере, одну двойную углерод-углеродную связь. Примеры алкенильных групп включают, например, винил, аллил (2-пропен-1-ил), 1-пропен-1-ил, 2-пропен-2-ил, металлил (2-метилпроп-2-ен-1-ил), 2-бутен-1- ил, 3-бутен-1-ил, 2-пентен-1-ил, 3-пентен-1-ил, 4-пентен-1-ил, 1-метилбут-2-ен-1-ил, 2-этилпроп- 2-ен-1-ил и т.п.
[0116] В рамках настоящего изобретения, термин «алкинил» означает углеводородный радикал с прямой или разветвленной цепью, имеющий, по меньшей мере, одну тройную углерод-углеродную связь. Примеры алкинильных групп включают этинил, пропаргил (2-пропин-1-ил, также называемый проп-2-ин-1-ил), 1-пропин-1-ил (также называемый проп-1-ин- 1-ил), 1-метилпроп-2-ин-1-ил, 2-бутин-1-ил, 3-бутин-1-ил, 1-пентин-1-ил, 3-пентин-1-ил, 4 -пентин-1-ил, 1-метилбут-2-ин-1-ил, 1-этилпроп-2-ин-1-ил и т.п.
[0117] В рамках настоящего изобретения, термин «арил» обозначает группы, полученные из моноциклических или полициклических ароматических углеводородов путем удаления атома водорода от атома углерода кольца. Примеры арильных групп включают фенил и нафтил.
[0118] В рамках настоящего изобретения, термин «гетероарил» обозначает группы, полученные из гетероаренов удалением атома водорода от любого кольцевого атома. Примеры гетероарильных групп включают группы, производные от пиррола, фурана, тиофена, имидазола, оксазола, тиазола, пиразола, пиридина, пиразина, пиридазина, пиримидина, индола и т.п. Типичными гетероатомами гетероаренов являются азот, кислород и сера.
[0119] Термин «галоген» или «атом галогена» в контексте настоящего описания обозначает фтор, бром, хлор или йод, в частности фтор или хлор.
[0120] В рамках настоящего изобретения, термин «алкокси» обозначает алкильную группу с прямой или разветвленной цепью, которая связана через кислородную группу с остальной частью молекулы. Примеры алкоксигрупп включают метокси, этокси, н-пропокси, изопропокси, н-бутилокси, 2-бутилокси, изобутилокси, трет-бутилокси и т.п.
[0121] Термин «алкилкарбонил» относится к линейной или разветвленной алкильной группе, которая связана через атом углерода карбонильной группы (C=O) с остальной частью молекулы.
[0122] Термин «аминозащитная группа» относится к химической группе, которая делает аминогруппу нереакционноспособной, но которую также можно удалть с восстановлением аминогруппы. Примеры аминозащитных групп включают бензилоксикарбонил (Cbz), 9-флуоренилметилоксикарбонил (Fmoc), трет-бутилоксикарбонил (Boc), аллилоксикарбонил (Alloc), п-толуолсульфонил (Tos), 2,2,5,7,8-пентаметилхроман-6-сульфонил (Pmc), 2,2,4,6,7-пентаметил-2,3-дигидробензофуран-5-сульфонил (Pbf), мезитил-2-сульфонил (Mts), 4-метокси-2,3,6-триметилфенилсульфонил (Mtr), ацетамидо, фталимидо и т.п. Другие аминозащитные группы известны специалистам в данной области, включая, например, группы, описанные Green and Wuts (Protective Groups in Organic Synthesis, 4-е изд. 2007, Wiley-Interscience, New York) и P. Kocienski (Thieme , 2005).
[0123] В рамках настоящего изобретения, термин «(C6-C10) арилметил» обозначает метильную группу, замещенную (C6-C10) арильной группой. Примером (C6-C10) арилметильной группы является бензил.
[0124] В рамках настоящего изобретения, термин «(C3-C9) гетероарилметил» обозначает метильную группу, замещенную (C3-C9) гетероарилметильной группой. Примером (C3-C9) гетероарилметильной группы является (1H-индол-3-ил)метил.
[0125] Термин «сульфо», используемый здесь, признан в данной области техники и относится к группе -SO3H или ее солевой форме (такой как фармацевтически приемлемая соль).
[0126] Формулы, указывающие положительно или отрицательно заряженные атомы или группы (такие как N+ или SO3-), означают солевые формы соответствующей формулы (включая «внутренние соли» в случае цвиттерионов).
[0127] Для целей настоящего изобретения термин «соль» включает соли неорганических кислот, такие как гидрохлорид, гидробромид, сульфат, фосфат и т.п.; и соли органических кислот, такие как миристат, формиат, ацетат, трифторацетат, малеат, тартрат, битартрат и т.п.; сульфонаты, такие как метансульфонат, бензолсульфонат, п-толуолсульфонат и т.п.; и соли аминокислот, такие как аргинат, аспарагинат, глутамат и т.п. Термин «соль» включает сольваты, такие как гидраты, соответствующей соли.
[0128] В некоторых вариантах осуществления термин «соль», используемый здесь, означает диагностически и/или фармацевтически приемлемую соль. В некоторых вариантах осуществления настоящего изобретения, где соединение вводят или предназначено для введения субъекту, термин «соль» означает фармацевтически приемлемую соль или диагностически и фармацевтически приемлемую соль.
[0129] В рамках настоящего изобретения, термин «фармацевтически приемлемая соль» означает соль соединения настоящего изобретения, которая безопасна и эффективна для местного или системного применения у млекопитающих и которая обладает желаемой биологической активностью. Противоион подходит для предполагаемого применения, нетоксичен и не мешает проявлению желаемого биологического действия соединения. Фармацевтически приемлемые соли в контексте настоящего изобретения включают соли, приведенные в IUPAC Handbook of Pharmaceutically Acceptable Salts (Wermuth, CG и Stahl, PH, Pharmaceutical Salts: Properties, Selection and Use - A Handbook, Verlag Helvetica Chimica Acta (2002)).
[0130] В рамках настоящего изобретения, термин «диагностически приемлемая соль» относится к соли соединения по настоящему изобретению, которая пригодна и эффективна для желаемого диагностического метода. Его противоион не мешает реакции, необходимой для детектирования целевого белка, или методу детектирования.
[0131] В некоторых вариантах осуществления соединения по настоящему изобретению находятся в виде трифторацетатной соли, например, после очистки ВЭЖХ в элюирующем растворителе, включающем трифторуксусную кислоту (ТФК).
[0132] В некоторых вариантах осуществления «эксципиент» означает диагностически и/или фармацевтически приемлемый эксципиент. В некоторых вариантах осуществления настоящего изобретения, где композиция вводится или предназначена для введения субъекту, термин «наполнитель» обозначает фармацевтически приемлемый эксципиент или диагностически и фармацевтически приемлемый эксципиент.
[0133] В формулах с волнистой линией, волнистая линия представляет или указывает точку соединения с остальной частью молекулы.
[0134] Соединение формулы (I) (и, возможно, как дополнительно определено формулами II и III) может содержать один или более асимметричных центров и, таким образом, может давать энантиомеры, диастереомеры и другие стереоизомерные формы. Если специально не указано иное, описание охватывает соединения со всеми такими возможными формами, а также их рацемические и разделенные формы или любую их смесь. Когда Соединение формулы (I) содержит олефиновую двойную связь или другой центр геометрической асимметрии, и если специально не указано иное, предполагается, что оно включает все «геометрические изомеры», например, как геометрические изомеры E, так и Z. Если специально не указано иное, все «таутомеры», например, таутомеры кетон-енол, амид-имидная кислота, лактам-лактим, енамин-имин, амин-имин и енамин-енимин, также охватываются настоящим описанием.
[0135] В рамках настоящего изобретения, термины «стереоизомер», «стереоизомерная форма» и т.п. являются общими терминами для всех изомеров индивидуальных молекул, которые различаются только ориентацией их атомов в пространстве. Он включает энантиомеры и изомеры соединений с более чем одним хиральным центром, которые не являются зеркальным отображением друг друга («диастереомеры»).
[0136] Термин «хиральный центр» относится к атому углерода, к которому присоединены четыре разные группы.
[0137] Термин «энантиомер» или «энантиомер» относится к молекуле, которая не накладывается на свое зеркальное изображение и, следовательно, оптически активна, когда энантиомер вращает плоскость поляризованного света в одном направлении, а его зеркальное изображение вращает плоскость поляризованного света в противоположном направлении.
[0138] Термин «рацемический» относится к смеси равных частей энантиомеров, которая оптически неактивна.
[0139] Термин «разделение» относится к разделению, концентрации или истощению одной из двух энантиомерных форм молекулы. Оптические изомеры соединения формулы (I) могут быть получены известными методами, такими как хиральная хроматография или образование диастереомерных солей из оптически активной кислоты или основания.
[0140] Оптическую чистоту можно выразить в единицах энантиомерного избытка (% ее), который определяется по формуле:
[0141]
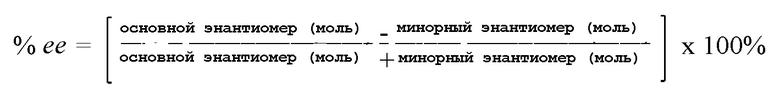
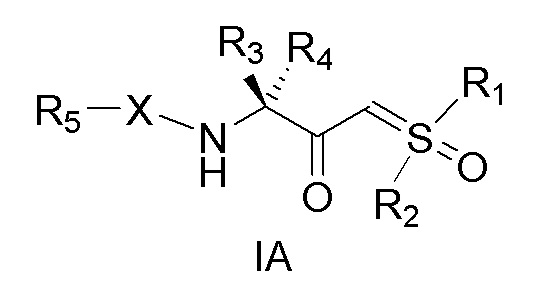
[0142] В одном варианте осуществления изобретение относится к соединениям, имеющим абсолютную стереохимию, как указано формулами IA (и как необязательно дополнительно определяется формулами IIA и IIIA).
[0143] Соединения по настоящему изобретению могут можно синтезировать с использованием стандартных синтетических химических методик, например, с использованием способов, описанных в разделе «Примеры» ниже. Другие пригодные синтетические методы описаны, например, в March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 7th Ed., (Wiley, 2013); Carey and Sundberg, Advanced Organic Chemistry 4th Ed., Vols. A and B (Plenum 2000, 2001); Fiesers ' Reagents for Organic Synthesis, Volumes 1 -27 (Wiley, 2013); Rodd's Chemistry of Carbon Compounds, Volumes 1-5 and Supplementals (Elsevier Science Publishers, 1989); Organic Reactions, Volumes 1-81 (Wiley, 2013); and Larock's Comprehensive Organic Transformations (VCH Publishers Inc., 1989) (все они в полном объеме включены здесь посредством ссылки). Соединения обычно синтезируют с использованием исходных веществ, которые обычно доступны из коммерческих источников или которые можно легко получить с использованием методов, хорошо известных специалистам в данной области. См., Например, Fiesers' Reagents for Organic Synthesis, Volumes 1-27 (Wiley, 2013), or Beilsteins Handbuch der organischen Chemie, 4, Aufl. ed. Springer-Verlag, Berlin, включая приложения.
[0144] Соединения
[0145] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I:
[0146]
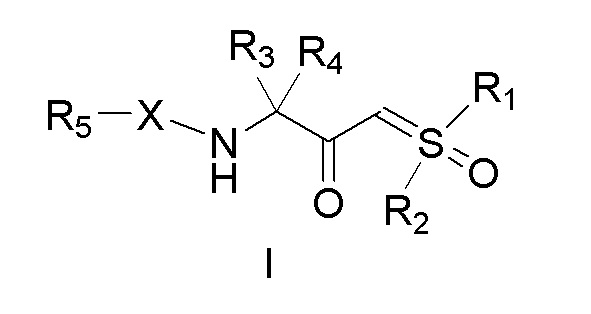
[0147] или его соли.
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R3 представляет собой боковую цепь альфа-аминокислоты;
R4 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R5 выбран из группы, состоящей из детектируемого элемента, аминозащитной группы, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила, (C2-C8) алкинила, (C1-C8) алкилкарбонила, (C1-C8) гидроксиалкилкарбонила, (C1-C8) галогеналкилкарбонила, (C3-C8) циклоалкилкарбонила, (C1-C8) алкилоксикарбонила, бензилоксикарбонила и атома водорода;
[0148] X представляет собой:
(i) связь; или
(ii) бирадикальный фрагмент формулы II или III, который связан с заместителем R5 через аминогруппу:
[0149]

где:
R6 представляет собой боковую цепь альфа-аминокислоты;
R7 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R8 представляет собой боковую цепь альфа-аминокислоты;
R9 выбран из группы, состоящей из атома водорода и (C1-C4) алкила; и
n равно 1, 2, 3 или 4.
[0150] В некоторых вариантах осуществления соединение формулы I отличается тем, что R3 представляет собой боковую цепь природной альфа-аминокислоты или структурный изомер, гомолог и/ или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0151] В некоторых вариантах осуществления R3 представляет собой боковую цепь протеиногенной альфа-аминокислоты или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0152] В некоторых вариантах осуществления R3 представляет собой боковую цепь протеиногенной альфа-аминокислоты, за исключением лизина, или структурный изомер или гомолог указанной боковой цепи,
где указанная боковая цепь, или структурный изомер, или его гомолог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0153] В некоторых вариантах осуществления R3 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина, или структурного изомера, гомолога и/или структурного аналога указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0154] В некоторых вариантах осуществления R3 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина, или структурного изомера, гомолога и/или структурного аналога указанной боковой цепи,
где указанная боковая цепь, или структурный изомер, или его гомолог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси. В некоторых таких вариантах осуществления альфа-аминокислота выбрана из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина и селенэтионина. В некоторых таких вариантах осуществления альфа-аминокислота выбрана из группы, состоящей из аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, фенилаланина и триптофана. В некоторых таких вариантах осуществления альфа-аминокислота выбрана из группы, состоящей из валина, норвалина, лейцина, изолейцина, норлейцина и гомонорлейцина. В некоторых таких вариантах осуществления альфа-аминокислота выбрана из группы, состоящей из валина, лейцина, изолейцина и норлейцина. В некоторых таких вариантах осуществления альфа-аминокислота представляет собой лейцин или норлейцин. В некоторых таких вариантах осуществления альфа-аминокислота представляет собой норлейцин.
[0155] В некоторых вариантах осуществления R3 выбран из группы, состоящей из атома водорода, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2- C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила, (C3-C9) гетероарилметила и -CH2CH2CH2CH2N(R3a)(R3b); где:
R3a выбран из группы, состоящей из детектируемого элемента, аминозащитной группы, атома водорода и (C1-C8) алкила; и
R3b выбран из группы, состоящей из атома водорода и (C1-C4) алкила. В некоторых вариантах осуществления R3 выбран из группы, состоящей из (C1-C8) алкила, (C2-C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила, (C3-C9) гетероарилметила и -CH2CH2CH2CH2N(R3a) (R3b). В некоторых вариантах осуществления R3 выбран из группы, состоящей из (C1-C8) алкила, (C6-C10) арилметила, (C3-C9) гетероарилметила и -CH2CH2CH2CH2N(R3a)(R3b). В некоторых вариантах осуществления R3 выбран из группы, состоящей из (C1-C8) алкила, бензила, (1H-индол-3-ил)метила и -CH2CH2CH2CH2N(R3a)(R3b). В некоторых вариантах осуществления R3 выбран из группы, состоящей из (C1-C6) алкила, бензила, (1H-индол-3-ил)метила и -CH2CH2CH2CH2N(R3a)(R3b). В некоторых вариантах осуществления R3 выбран из группы, состоящей из этила, н-пропила, изопропила, н-бутила, втор-бутила, изобутила, н-пентила, бензила, (1H-индол-3-ил)метила и -CH2CH2CH2CH2N(R3a)(R3b). В некоторых вариантах осуществления R3b представляет собой атом водорода.
[0156] В некоторых вариантах осуществления R3 не представляет собой аминозащитную группу, атом водорода или (С1-С8) алкил, если X представляет собой связь. В некоторых вариантах осуществления R3 представляет собой -CH2CH2CH2CH2N(R3a)(R3b), если Х представляет собой связь.
[0157] В других таких вариантах осуществления R3a представляет собой детектируемый элемент (независимо от природы Х). В еще одних таких вариантах осуществления R3a представляет собой атом водорода. В еще одних таких вариантах осуществления R3a представляет собой аминозащитную группу. В еще одних таких вариантах осуществления R3a представляет собой (C1-C8) алкил.
[0158] В некоторых вариантах осуществления R3b представляет собой атом водорода.
[0159] В некоторых вариантах осуществления R3 выбран из группы, состоящей из атома водорода, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2- C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила и (C3-C9) гетероарилметила. В некоторых таких вариантах осуществления R3 выбран из группы, состоящей из (C1-C8) алкила, (C2-C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила и (C3-C9) гетероарилметила. В некоторых таких вариантах осуществления R3 выбран из группы, состоящей из (C1-C8) алкила, (C6-C10) арилметила и (C3-C9) гетероарилметила. В некоторых таких вариантах осуществления R3 выбран из группы, состоящей из (C1-C8) алкила, бензила и (1H-индол-3-ил)метила. В некоторых таких вариантах осуществления R3 выбран из группы, состоящей из (C1-C6) алкила, бензила и (1H-индол-3-ил)метила. В некоторых таких вариантах осуществления R3 выбран из группы, состоящей из этила, н-пропила, изопропила, н-бутила, втор-бутила, изобутила, н-пентила, бензила и (1H-индола)-3-ил)метила. В некоторых таких вариантах осуществления R3 выбран из группы, состоящей из н-бутила, втор-бутила и изобутила. В некоторых таких вариантах осуществления R3 представляет собой н-бутил.
[0160] В некоторых вариантах осуществления соединение формулы I отличается тем, что R3 представляет собой -CH2CH2CH2CH2N(R3a)(R3b); где:
R3a выбран из группы, состоящей из детектируемого элемента, аминозащитной группы, атома водорода и (C1-C8) алкила; и
R3b выбран из группы, состоящей из атома водорода и (C1-C4) алкила. В еще одних таких вариантах осуществления R3a не представляет собой аминозащитную группу, атом водорода или (C1-C8) алкил, если Х представляет собой связь. В еще одних таких вариантах осуществления R3a представляет собой атом водорода (независимо от природы Х). В еще одних таких вариантах осуществления R3a представляет собой аминозащитную группу. В еще одних таких вариантах осуществления R3a представляет собой (C1-C8) алкил. В некоторых вариантах осуществления R3b представляет собой атом водорода.
[0161] В некоторых вариантах осуществления R1 представляет собой (C1-C8) алкил. В некоторых таких вариантах осуществления R1 представляет собой метил.
[0162] В некоторых вариантах осуществления R2 представляет собой (C1-C8) алкил. В некоторых таких вариантах осуществления R2 представляет собой метил.
[0163] В некоторых вариантах осуществления R4 представляет собой атом водород.
[0164] В некоторых вариантах осуществления R5 выбран из группы, состоящей из детектируемого элемента, аминозащитной группы и атома водорода.
[0165] В некоторых вариантах осуществления R6 представляет собой:
(i) боковую цепь природной альфа-аминокислоты, или
(ii) боковую цепи протеиногенной альфа-аминокислоты, или
(iii) боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина, или
(iv) боковую цепь фенилаланина,
или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или несколькими, одинаковыми или разными заместителями R6x, где:
R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0167] В некоторых вариантах осуществления R6 представляет собой боковую цепь фенилаланина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи.
[0168] В некоторых вариантах осуществления R8 представляет собой:
(i) боковую цепь природной альфа-аминокислоты, или
(ii) боковую цепи протеиногенной альфа-аминокислоты, или
(iii) боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина, или
(iv) боковую цепь фенилаланина,
или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или несколькими, одинаковыми или разными заместителями R8x, где:
R8x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0170] В некоторых вариантах осуществления R7 представляет собой атом водород.
[0171] В некоторых вариантах осуществления R9 представляет собой атом водород.
[0172] В некоторых вариантах осуществления, когда заместитель представляет собой аминозащитную группу, то аминозащитная группа может быть выбрана из группы, состоящей из бензилоксикарбонила (Cbz), 9-флуоренилметилоксикарбонила (Fmoc), трет-бутилоксикарбонила (Boc), аллилоксикарбонила (Alloc), п-толуолсульфонила (Tos), 2,2,5,7,8-пентаметилхроман-6-сульфонила (Pmc), 2,2,4,6,7-пентаметил-2,3-дигидробензофуран-5-сульфонила (Pbf), мезитил-2-сульфонила (Mts), 4-метокси-2,3,6-триметилфенилсульфонила (Mtr), ацетамидо и фталимидо. В некоторых таких вариантах осуществления аминозащитная группа представляет собой бензилоксикарбонил.
[0173] В некоторых из вышеуказанных вариантов осуществления соединение формулы I демонстрирует абсолютную стереохимию в соответствии с формулой IA:
[0174]
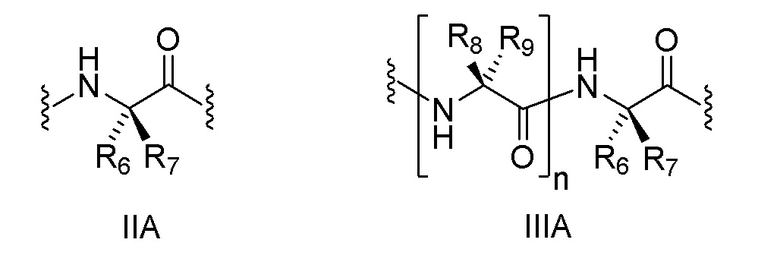
[0175] В некоторых таких вариантах осуществления в соединении формулы I или IA, X представляет собой (i) связь или (ii) бирадикальный фрагмент формулы II или III, проявляющий абсолютную стереохимию согласно формулам IIA и IIIA, соответственно:
[0176]
[0177] В некоторых вариантах осуществления X представляет собой связь.
[0178] В некоторых других вариантах осуществления X представляет собой бирадикальный фрагмент формулы II. В некоторых таких вариантах осуществления X представляет собой бирадикальный фрагмент формулы IIA.
[0179] В некоторых других вариантах осуществления X представляет собой бирадикальный фрагмент формулы III. В некоторых таких вариантах осуществления X представляет собой бирадикальный фрагмент формулы IIIA. В некоторых таких вариантах осуществления n равен 1.
[0180] В некоторых вариантах осуществления детектируемый элемент выбран из группы, состоящей из флуоресцентной метки, биотиновой метки, радиоактивной метки, хелатора (например, для радиоактивной метки) и биоортогонального маркера для лигирования.
[0181] Детектируемый элемент, такой как флуоресцентная метка, биотиновая метка, радиоактивная метка, хелатор или биоортогональный маркер для лигирования, может включать линкер для включения в соединения по настоящему изобретению (т.е. для присоединения детектируемого элемента или метки к остальной части молекулы). Подходящие линкеры известны специалистам в данной области. Примеры линкеров, которые можно использовать в соединениях по настоящему изобретению, описаны в WO 2012/118715 A2 (см. с. 18, строки 9-18), содержание которой включено здесь посредством ссылки. Линкер может также включать фрагмент полиэтиленгликоля (ПЭГ), такого как ПЭГ-4, ПЭГ-6 или ПЭГ-8, для присоединения к остальной части молекулы.
[0182] Определение термина «радиоактивная метка» и примеры радиоактивных меток, которые можно использовать в соединениях по настоящему изобретению, описаны в WO 2009/124265 A1 (см. с. 11, строка 25 - с. 13, строка 3), содержание которой включено здесь посредством ссылки.
[0183] Определение термина «хелатор» и примеры хелаторов, которые можно использовать в соединениях по настоящему изобретению, описаны в WO 2009/124265 A1 (см. с. 10, строка 26 - с. 11, строка 14), содержание которой включено здесь посредством ссылки.
[0184] Определение термина «биоортогональный маркер для лигирования» и примеры биоортогонального маркера для лигирования, которые можно использовать в соединениях по настоящему изобретению, и соответствующие «клик»-реакции описаны, например, в Martell et al., Applications of Copper-Catalyzed Click. Chemistry in Activity-Based Protein Profiling, Molecules 2014, 19, 1378-1393, который включен здесь посредством ссылки. Адаптация этих методов для получения или модификации соединений по настоящему изобретению находится в пределах компетенции специалистов в данной области.
[0185] Биоортогональные реакции или клик-реакции для присоединения вторичной метки включают:
A. бесследное сочетание азидов лигированием по Штаудингеру с триарилфосфинами с образованием амидной связи,
B. циклоприсоединение тетразина с использованием 1,2,4,5-тетразина и напряженного диен (транс-циклооктена),
C. катализируемая медью (I) реакция азид-алкинового циклоприсоединения (CuAAC) между азидом и концевым алкином с образованием 1,4-дизамещенного 1,2,3-триазола, и
D. вариант азид-алкинового циклоприсоединения без присутствия меди с использованием напряженного алкина для ускорения реакции.
[0186] В этом отношении, в частности, делается ссылка на фиг. 1B и фиг. 2 в публикации Martell et al., Molecules 2014, 19, 1378-1393, содержание которой включено здесь посредством ссылки.
[0187] Таким образом, в некоторых вариантах осуществления биоортогональный маркер для лигирования содержит функциональную группу, выбранную из группы, состоящей из азида, 1,2,4,5-тетразина и алкина (такого как концевой алкин). Эти функциональные группы позволяют присоединить вторичную метку с использованием одной из вышеуказанных биоортогональных реакций (A)-(D).
[0188] В некоторых вариантах осуществления детектируемый элемент представляет собой флуоресцентную метку. Как известно специалистам в данной области техники, флуоресцентные метки излучают электромагнитное излучение, предпочтительно видимый свет, когда стимулируются поглощением падающего электромагнитного излучения. Является коммерчески доступным широкий спектр флуоресцентных меток, включая метки, содержащие реактивные группы, которые можно использовать для связывания метки с реактивными группами, такими как, например, аминогруппы, тиоловые группы и т.п. См., например, The Molecular Probes® Handbook - Руководство по флуоресцентным зондам и технологиям маркировки, которое в полном объеме включено здесь посредством ссылки.
[0189] Примеры флуоресцентных меток, которые можно использовать в соединениях по настоящему изобретению, описаны в WO 2018/119476 A1 (см. абзацы [0084]-[0095]) и в WO 2012/118715 A2 (см. стр. 15, стр. 18 до стр. 17, строка 12, и страница 18, строка 19 - страница 21, строка 1), содержание которых включено здесь посредством ссылки. Такие флуоресцентные метки могут включать линкер для включения в соединения по настоящему изобретению, например, как описано в WO 2012/118715 A2 (см. стр. 18, строки 9-18), содержание которой включено здесь посредством ссылки.
[0190] В некоторых вариантах осуществления детектируемый элемент представляет собой флуоресцентную метку. В некоторых таких вариантах осуществления флуоресцентная метка выбрана из группы, состоящей из флуоресцеина, Oregon green (фторированное производное флуоресцеина), борадиазаиндеценового красителя, родаминового красителя (такого как тетраметилродамин и карбокситетраметилродамин), красителя на основе бензопириллия, кумаринового красителя, цианиновой метки или бензоиндольной метки (например, индоцианиновый зеленый).
[0191] Коммерчески доступные примеры таких красителей включают красители BODIPY® (борадиаза-индеценовые красители), красители серии Alexa Fluor® (сульфированные родамины), красители серии DyLight® (содержащие, например, сульфированный или несульфированный кумарин, родамин, бензопирил, или цианин в качестве основной структуры), красители серии IRDye® и цианиновые (Cy) красители (например, Cy2, Cy3, Cy3.5, Cy5, Cy5.5, Cy7, Cy7.5, sCy3, sCy5 и sCy7). Такие цианиновые метки можно приобрести, например, у компаний Abcam, Tocris, GoldBio, ThermoFisher, Kerafast, Lumiprobe, AAT Bioquest или W&J Pharmachem.
[0192] В некоторых вариантах осуществления флуоресцентная метка представляет собой цианиновую метку. В некоторых таких вариантах осуществления флуоресцентная метка представляет собой цианиновую метку, выбранную из группы, состоящей из Cy2, Cy3, Cy3.5, Cy5, Cy5.5, Cy7, Cy7.5, sCy3, sCy5 и sCy7. В некоторых таких вариантах осуществления флуоресцентная метка представляет собой Cy5 или sCy5. В некоторых вариантах осуществления флуоресцентная метка представляет собой sCy5.
[0193] В некоторых вариантах осуществления флуоресцентная метка представляет собой цианиновую метку, имеющую формулу, выбранную из следующей группы формул:
[0194]
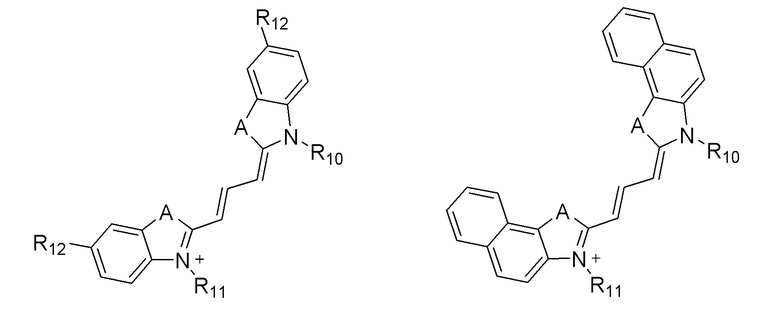
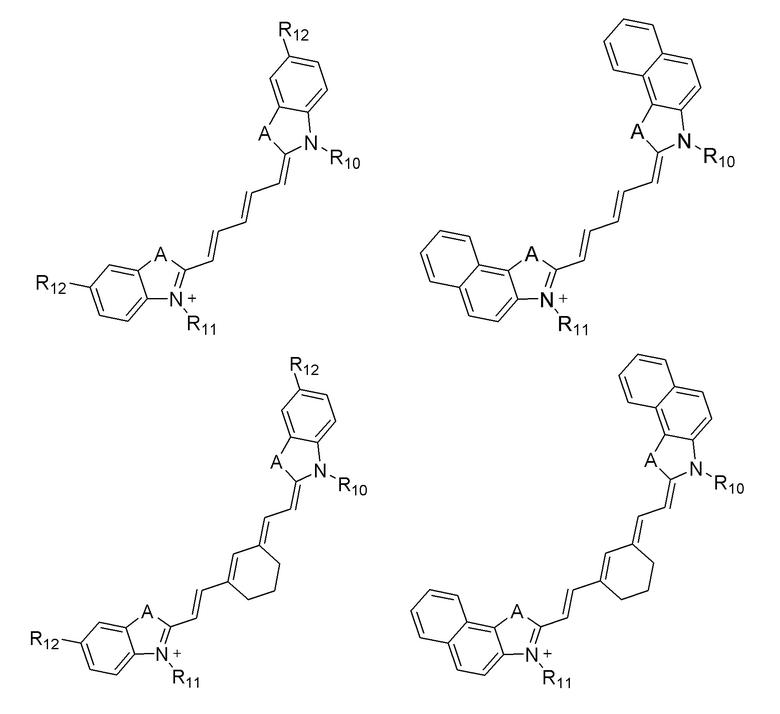
[0195] где в каждой из вышеприведенных формул,
A выбран из группы, состоящей из CH2, C(CH3)2, C(C2H5)2, NH, N(CH3), N(C2H5), O, S и Se;
R10 выбран из группы, состоящей из $-(CH2)p-C(= O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 2, 3, 4, 5, 6, 7 или 8;
q равно 2, 3, 4, 5, 6, 7 или 8;
r равно 2, 3, 4, 5, 6, 7 или 8;
$ представляет собой точку соединения с атомом азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 выбран из группы, состоящей из (C1-C8) алкила и (C6-C10) арила; и
R12 представляет собой H или сульфогруппу. В некоторых вариантах осуществления р равно 5, q равно 5 и r равно 4.
[0196] В некоторых вариантах осуществления, где флуоресцентная метка представляет собой цианиновую метку, имеющую одну из вышеуказанных формул,
A выбран из группы, состоящей из CH2, C(CH3)2 и C(C2H5)2;
R10 выбран из группы, состоящей из $-(CH2)p-C(=O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 2, 3, 4, 5 или 6;
q равно 2, 3, 4, 5 или 6;
r равно 2, 3, 4, 5 или 6;
$ представляет собой точку присоединения к атому азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой (C1-C8) алкил; и
R12 представляет собой H или сульфогруппу. В некоторых вариантах осуществления р равно 5, q равно 5 и r равно 4.
[0197] В некоторых вариантах осуществления, где флуоресцентная метка представляет собой цианиновую метку, имеющую одну из вышеуказанных формул,
А представляет собой C(CH3)2 или C(C2H5)2;
R10 выбран из группы, состоящей из $-(CH2)p-C(=O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 2, 3, 4, 5 или 6;
q равно 2, 3, 4, 5 или 6;
r равно 2, 3, 4, 5 или 6;
$ представляет собой точку присоединения к атому азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил, этил или пропил; и
R12 представляет собой H или сульфогруппу. В некоторых вариантах осуществления р равно 5, q равно 5 и r равно 4.
[0198] В некоторых вариантах осуществления, где флуоресцентная метка представляет собой цианиновую метку, имеющую одну из вышеуказанных формул,
А представляет собой C(CH3)2;
R10 выбран из группы, состоящей из $-(CH2)p-C(=O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 4, 5 или 6;
q равно 4, 5 или 6;
r равно 3, 4, 5 или 6;
$ представляет собой точку соединения с атомом азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил или этил; и
R12 представляет собой H или сульфогруппу. В некоторых вариантах осуществления р равно 5, q равно 5 и r равно 4.
[0199] В некоторых вариантах осуществления, где флуоресцентная метка представляет собой цианиновую метку, имеющую одну из вышеуказанных формул,
А представляет собой С(СН3)2;
R10 представляет собой $-(CH2)p-C(=O)-&; где:
p равно 4, 5 или 6; и
$ представляет собой точку присоединения к атому азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил или этил; и
R12 представляет собой сульфогруппу. В некоторых вариантах осуществления р равно 5.
[0200] В некоторых вариантах осуществления, где флуоресцентная метка представляет собой цианиновую метку, имеющую одну из вышеуказанных формул,
А представляет собой С(СН3)2;
R10 представляет собой $-(CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(= O)-&;
где:
q равно 4, 5 или 6;
r равно 3, 4, 5 или 6;
$ представляет собой точку присоединения к атому азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил или этил; и
R12 представляет собой H. В некоторых вариантах осуществления р равно 5 и r равно 4.
[0201] В некоторых вариантах осуществления, где флуоресцентная метка представляет собой цианиновую метку, имеющую одну из вышеприведенных формул, R5 представляет собой детектируемый элемент, и & представляет собой точку соединения с X.
[0202] В некоторых вариантах осуществления флуоресцентная метка представляет собой цианиновую метку, имеющую формулу, выбранную из следующей группы формул:
[0203]
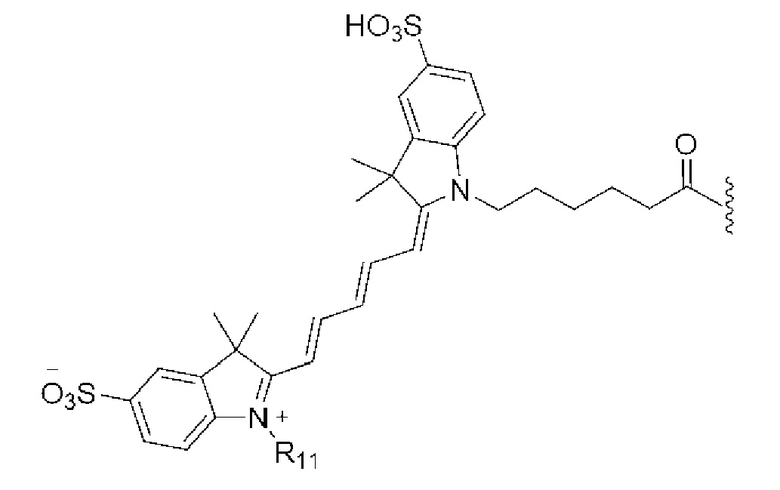
[0204]
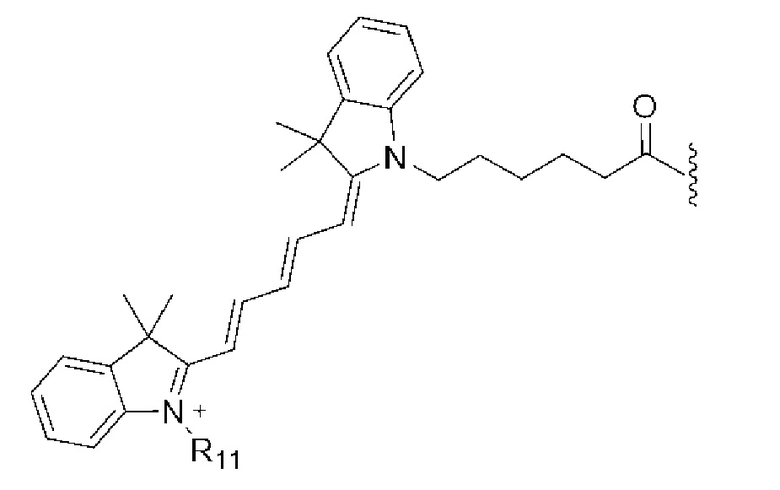
[0205]
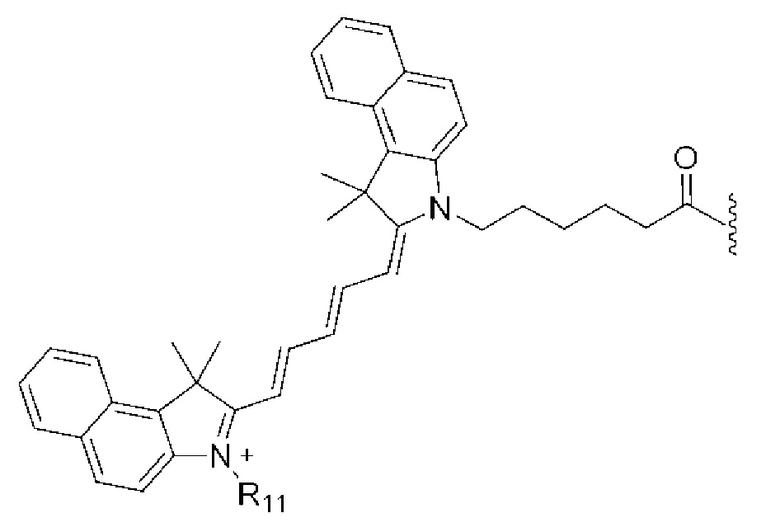
[0206] где в каждой из вышеприведенных формул,
волнистая линия представляет собой точку соединения с остальной частью молекулы;
и R11 выбран из группы, состоящей из (C1-C8) алкила и (C6-C10) арила. В некоторых таких вариантах осуществления R11 представляет собой (C1-C8) алкил. В некоторых таких вариантах осуществления R11 представляет собой метил или этил.
[0207] В некоторых вариантах осуществления флуоресцентная метка представляет собой цианиновую метку, имеющую формулу,
[0208]
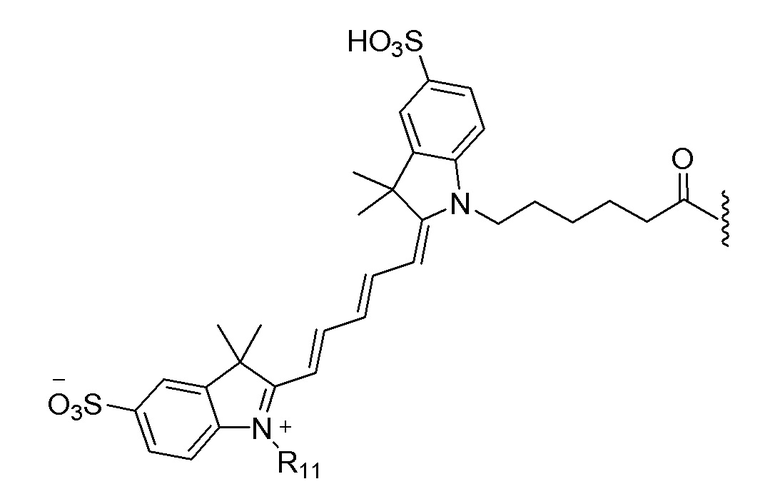
где волнистая линия представляет собой точку соединения с остальной частью молекулы; и R11 представляет собой метил или этил.
[0209] В некоторых вариантах осуществления, где флуоресцентная метка представляет собой цианиновую метку, имеющую одну из вышеприведенных формул, R5 представляет собой детектируемый элемент, и волнистая линия представляет точку соединения с X.
[0210] В некоторых вариантах осуществления соединение формулы I (или IA) содержит, по меньшей мере, один детектируемый элемент, например, один, два или три детектируемых элемента. В некоторых таких вариантах осуществления соединение формулы I (или IA), как определено выше, содержит один детектируемый элемент.
[0211] В некоторых вариантах осуществления R5 представляет собой детектируемый элемент.
[0212] В некоторых вариантах осуществления R3 несет детектируемый элемент. В некоторых таких вариантах осуществления R3 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи, где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и, возможно, дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси. В некоторых таких вариантах осуществления R3 представляет собой -CH2CH2CH2CH2N(R3a)(R3b); где:
R3a представляет собой детектируемый элемент; и
R3b выбран из группы, состоящей из атома водорода и (C1-C4) алкила.
[0213] В некоторых вариантах осуществления, где R3 несет детектируемый элемент, R5 выбран из группы, состоящей из аминозащитной группы, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила, (C2-C8) алкинила, (C1-C8) алкилкарбонила, (C1-C8) гидроксиалкилкарбонила, (C1-C8) галогеналкилкарбонила, (C3-C8) циклоалкилкарбонила, (C1-C8) алкилоксикарбонила, бензилоксикарбонила и атома водорода. В некоторых таких вариантах осуществления R5 представляет собой аминозащитную группу.
[0214] В некоторых вариантах осуществления X представляет собой бирадикальный фрагмент формулы II или IIA, и R6 несет детектируемый элемент. В некоторых таких вариантах осуществления R6 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R6x, где R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0215] В некоторых вариантах осуществления X представляет собой бирадикальный фрагмент формулы III или IIIA, и R6 несет детектируемый элемент. В некоторых таких вариантах осуществления R6 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R6x, где R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0216] В некоторых вариантах осуществления X представляет собой бирадикальный фрагмент формулы III или IIIA, и R8 несет детектируемый элемент. В некоторых таких вариантах осуществления R8 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R8x, где R8x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0217] В некоторых вариантах осуществления соединение формулы I представляет собой соединение, имеющее одну из следующих формул (с абсолютной стереохимией, как указано):
[0218]
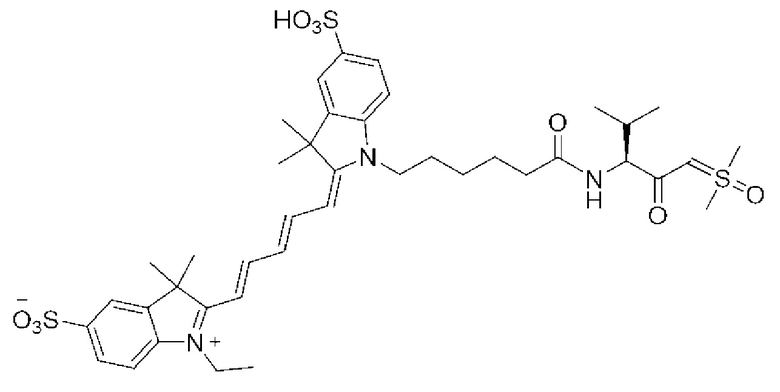
[0219]
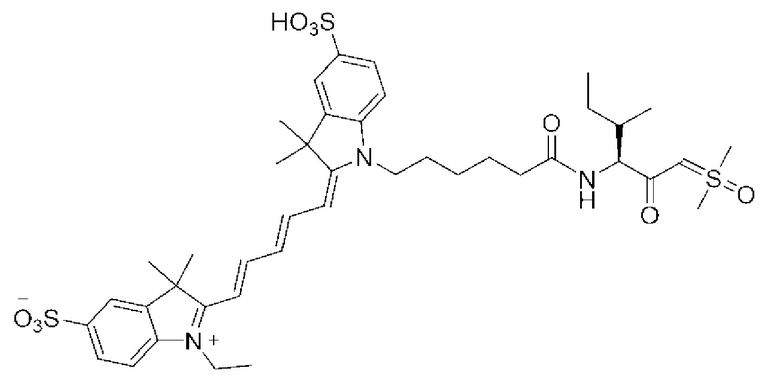
[0220]
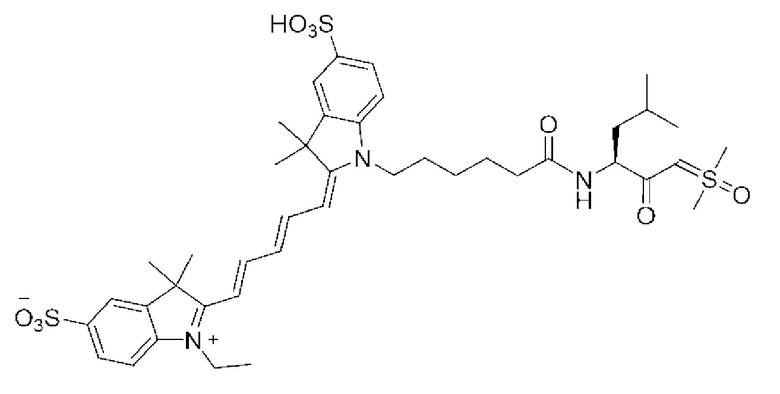
[0221]
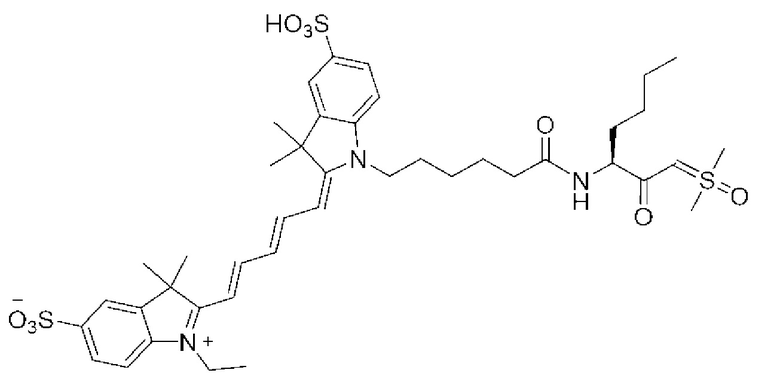
[0222]
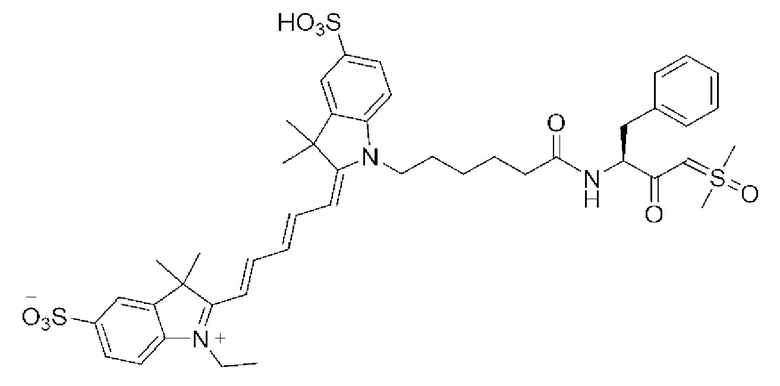
[0223]
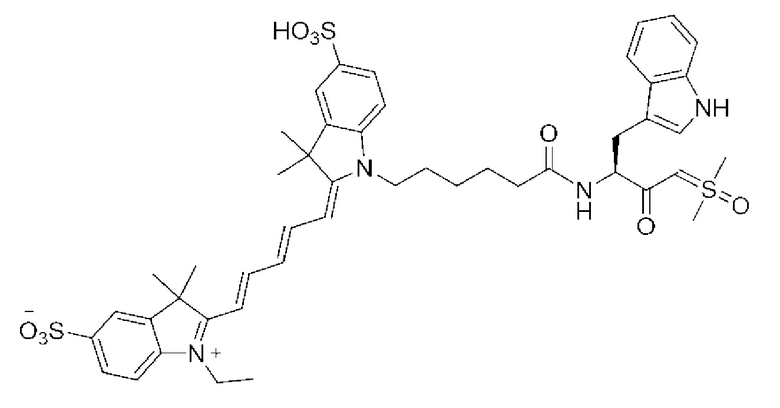
[0224]
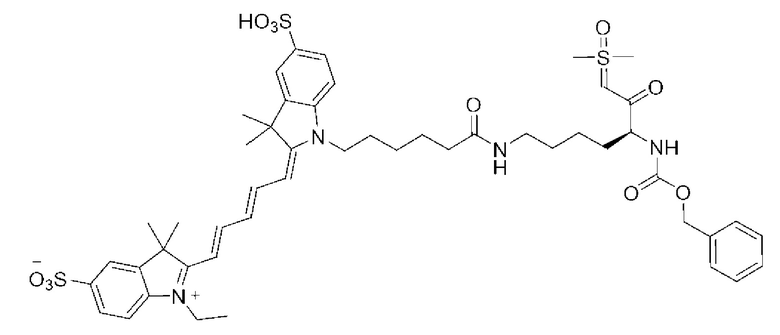
[0225]
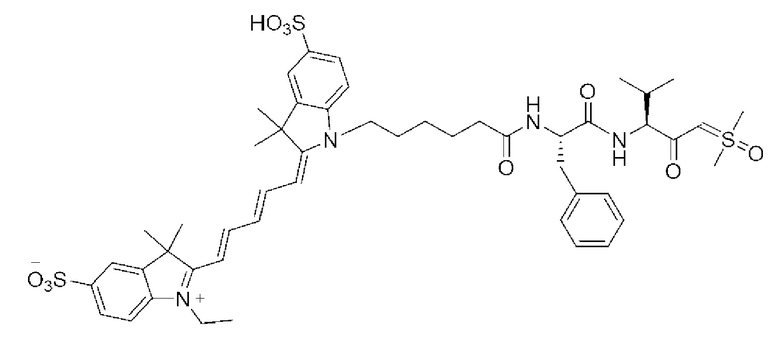
[0226] или его соль.
[0227] В некоторых предпочтительных вариантах осуществления соединение формулы I представляет собой соединение, имеющее следующую формулу (с абсолютной стереохимией, как указано):
[0228]
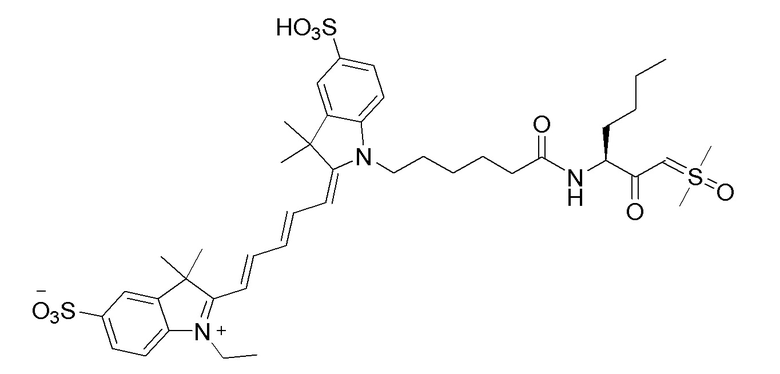
[0229] или его соль.
[0230] Композиции
[0231] В некоторых вариантах осуществления настоящее изобретение относится к композиции, содержащей соединение формулы I (или IA), как описано выше, или его соль, и эксципиент (например, фармацевтически и/или диагностически приемлемый эксципиент).
[0232] Фармацевтически приемлемые эксципиенты, которые можно использовать в композициях по настоящему изобретению, известны специалистам в данной области. Примеры таких фармацевтически приемлемых эксципиентов включают, например, те, что описаны в абзацах [0114] - [0118] в WO 2018/119476, содержание которой тем самым включено в настоящее раскрытие.
[0233] В некоторых вариантах осуществления композиция представляет собой водный раствор, содержащий, например, воду, забуференный фосфатом физиологический раствор или буферный раствор в качестве фармацевтически приемлемого эксципиента. Такие композиции можно использовать, например, для внутривенной инъекции.
[0234] Способы детектирования активности цистеиновых протеаз
[0235] В способах детектирования активности цистеиновой протеазы по настоящему изобретению детектируются только протеолитически активные формы соответствующей(их) цистеиновой протеазы(з).
[0236] Детектируемый сигнал измеряется после взаимодействия соединения-зонда на основе активности и цистеиновой протеазы, которое привело к образованию ковалентной связи. Измеренный детектируемый сигнал испускается меченым ферментом, т. е. детектируемым элементом соединения-зонда на основе активности, ковалентно присоединенного к цистеиновой протеазе. В некоторых вариантах осуществления детектируемый сигнал измеряется после того, как меченый фермент был подвергнут вторичной стадии мечения.
[0237] Концепция детектирования активности фермента с использованием зондов на основе активности и соответствующие способы детектирования и лежащие в основе экспериментальные протоколы известны специалистам в данной области (см., например, Edgington and Bogyo, 2013; Edgington-Mitchell, L.E., and Bogyo, M. (2016). Detection of Active Caspases During Apoptosis Using Fluorescent Activity-Based Probes. Methods Mol Biol. 1419, 27-39; and Edgington-Mitchell, L.E., Bogyo, M., and Verdoes, M. (2017). Live Cell Imaging and Profiling of Cysteine Cathepsin Activity Using a Quenched Activity-Based Probe. Methods Mol Biol. 1491, 145-159; содержание которых в полном объеме включено здесь посредством ссылки). Специалисты в данной области знают, как соответствующим образом адаптировать данные способы/протоколы для применения в способах по настоящему изобретению.
[0238] Способы детектирования in vitro
[0239] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) контактирование цистеиновой протеазы с соединением-зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ цистеиновой протеазы, включающий измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ представляет собой способ in vitro.
[0240] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы in vitro, включающему:
(1) контактирование биологического образца с соединением- зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0241] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы в биологическом образце, полученном от субъекта, включающему:
(1) контактирование биологического образца in vitro с соединением-зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0242] В некоторых вариантах осуществления вышеуказанных способов соединение-зонд на основе активности содержит фрагмент илид сульфоксония, имеющий формулу:
[0243]
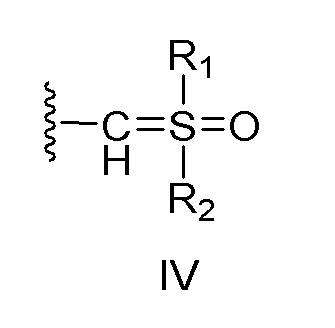
[0244] где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила. В некоторых вариантах осуществления R1 представляет собой метил, и R2 представляет собой метил.
[0245] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) контактирование цистеиновой протеазы с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ цистеиновой протеазы, включающий измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ представляет собой способ in vitro.
[0246] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы in vitro, включающему:
(1) контактирование биологического образца с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0247] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы в биологическом образце, полученном от субъекта, включающему:
(1) контактирование биологического образца in vitro с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0248] В некоторых вариантах осуществления каждого из вышеуказанных способов стадия (2) включает выполнение, по меньшей мере, одного аналитического метода, выбранного из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, гель-электрофореза и последующей радиографии, гель-электрофореза и последующего иммуноблоттинга, флуоресцентной микроскопии, проточной цитометрии, оптической визуализации ex vivo, радиографии, аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики.
[0249] В некоторых вариантах осуществления каждого из вышеуказанных способов детектируемый сигнал измеряется посредством измерения флуоресценции. В некоторых таких вариантах осуществления, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, флуоресцентной микроскопии и проточной цитометрии. В некоторых таких вариантах осуществления, по меньшей мере, один аналитический метод выбран из гель-электрофореза и последующей флуоресценции в геле и флуоресцентной микроскопии. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде флуоресцентной метки (например, как здесь описано). В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в форме биоортогонального маркера для лигирования, и стадия (2) включает вторичное мечение с помощью клик-химии для включения флуоресцентной метки перед выполнением, по меньшей мере, одного аналитического метода. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в форме биотина, и стадия (2) включает вторичное мечение флуоресцентно-меченным стрептавидином или вторичное мечение флуоресцентно-меченным антителом, специфичным для биотина, перед выполнением, по меньшей мере, одного аналитического метода.
[0250] В некоторых вариантах осуществления каждого из вышеуказанных методов, по меньшей мере, один аналитический метод выбран из группы, состоящей из радиографии, гель-электрофореза и последующей радиографии. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде радиоактивной метки. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде хелатора для радиоактивной метки. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (2) включает вторичное мечение с помощью клик-химии для включения радиоактивной метки или хелатора для радиоактивной метки перед выполнением, по меньшей мере, одного аналитического способа.
[0251] В некоторых вариантах осуществления каждого из вышеуказанных способов, по меньшей мере, один аналитический способ выбран из группы, состоящей из аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде биотиновой метки. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (2) включает вторичное мечение с помощью клик-химии для включения биотиновой метки перед выполнением, по меньшей мере, одного аналитического споосба. В случае мечения биотином аффинную очистку можно проводить с использованием, например, гранул, покрытых стрептавидином, или гранул, покрытых антителом, специфичным к биотину.
[0252] В некоторых вариантах осуществления аффинную очистку можно проводить с использованием гранул, покрытых антителом, специфичным к определенной метке. В некоторых таких вариантах осуществления указанное соединение включает указанную метку в качестве детектируемого элемента. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (2) включает вторичное мечение с помощью клик-химии для включения указанной метки перед выполнением аффинной очистки.
[0253] В некоторых вариантах осуществления каждого из вышеуказанных способов, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующего иммуноблоттинга. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде биотиновой метки, и стадия (2) включает вторичное мечение, например, стрептавидином, меченным HRP, перед выполнением, по меньшей мере, одного аналитического метода. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (2) включает вторичное мечение с помощью клик-химии для нанесения биотиновой метки и последующее мечение, например, стрептавидином, меченным HRP, до выполнения, по меньшей мере, одного аналитического метода.
[0254] В некоторых вариантах осуществления гель-электрофорез представляет собой одномерный или двумерный гель-электрофорез (такой как SDS-PAGE или нативный PAGE). В некоторых вариантах осуществления гель-электрофорез представляет собой SDS-PAGE.
[0255] Способы детектирования in vitro с предварительным введением субъекту
[0256] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) введение субъекту соединения-зонда на основе активности, содержащего фрагмент илида сульфоксония, в качестве активной группы,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0257] В некоторых таких вариантах осуществления соединение-зонд на основе активности вводят внутривенно. В некоторых вариантах осуществления этого способа соединение-зонд на основе активности содержит фрагмент илида сульфоксония, имеющий формулу (IV):
[0258]
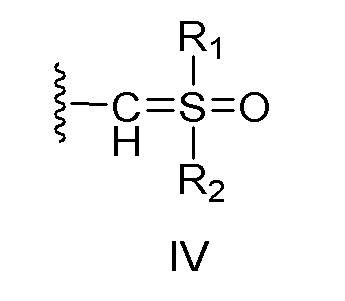
[0259] где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила. В некоторых вариантах осуществления R1 представляет собой метил, и R2 представляет собой метил.
[0260] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования активности цистеиновой протеазы, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
В некоторых таких вариантах осуществления соединение или его соль, или композицию вводят внутривенно.
[0261] В некоторых вариантах осуществления каждого из вышеуказанных методов стадия (3) включает выполнение, по меньшей мере, одного аналитического метода, выбранного из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, гель-электрофореза и последующей радиографии, гель-электрофореза и последующего иммуноблоттинга, флуоресцентной микроскопии, проточной цитометрии, оптической визуализации ex vivo, радиографии, аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики.
[0262] В некоторых вариантах осуществления каждого из вышеуказанных методов детектируемый сигнал измеряется посредством измерения флуоресценции. В некоторых таких вариантах осуществления, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, флуоресцентной микроскопии и проточной цитометрии. В некоторых таких вариантах осуществления, по меньшей мере, один аналитический метод выбран из гель-электрофореза и последующей флуоресценции в геле и флуоресцентной микроскопии. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде флуоресцентной метки (например, как здесь описано). В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (3) включает вторичное мечение с помощью клик-химии для включения флуоресцентной метки перед выполнением, по меньшей мере, одного аналитического метода. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в форме биотина, и стадия (3) включает вторичное мечение флуоресцентно-меченным стрептавидином или вторичное мечение флуоресцентно-меченным антителом, специфичным к биотину, перед выполнением, по меньшей мере, одного аналитического метода.
[0263] В некоторых вариантах осуществления каждого из вышеуказанных методов, по меньшей мере, один аналитический метод выбран из группы, состоящей из радиографии, гель-электрофореза и последующей радиографии. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде радиоактивной метки. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде хелатора для радиоактивной метки. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (3) включает вторичное мечение с помощью клик-химии для нанесения радиоактивной метки или хелатора для радиоактивной метки перед выполнением, по меньшей мере, одного аналитического метода.
[0264] В некоторых вариантах осуществления каждого из вышеуказанных методов, по меньшей мере, один аналитический метод выбран из группы, состоящей из аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде биотиновой метки. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (3) включает вторичное мечение с помощью клик-химии для включения биотиновой метки перед выполнением, по меньшей мере, одного аналитического метода. В случае мечения биотином аффинную очистку можно проводить с использованием, например, гранул, покрытых стрептавидином, или гранул, покрытых антителом, специфичным к биотину. В некоторых вариантах осуществления аффинную очистку можно проводить с использованием гранул, покрытых антителом, специфичным к определенной метке. В некоторых таких вариантах осуществления указанное соединение содержит указанную метку в качестве детектируемого элемента. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (3) включает вторичное мечение с помощью клик-химии для включения указанной метки перед выполнением аффинной очистки.
[0265] В некоторых вариантах осуществления каждого из вышеуказанных методов, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующего иммуноблоттинга. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде биотиновой метки, и стадия (3) включает вторичное мечение, например, стрептавидином, меченным HRP, перед выполнением, по меньшей мере, одного аналитического метода. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в форме биоортогонального маркера для лигирования, и стадия (3) включает вторичное мечение с помощью клин-химии для нанесения биотиновой метки и последующее мечение, например, стрептавидином, меченным HRP, до выполнения, по меньшей мере, одного аналитического метода.
[0266] В некоторых вариантах осуществления гель-электрофорез представляет собой одномерный или двумерный гель-электрофорез (такой как SDS-Page или нативный PAGE). В некоторых вариантах осуществления гель-электрофорез представляет собой SDS-PAGE. В некоторых вариантах осуществления субъектом является человек.
[0267] Способы детектирования in vivo
[0268] В некоторых вариантах осуществления настоящее изобретение относится к способу in vivo детектирования активности цистеиновой протеазы у субъекта, включающему:
(1) введение субъекту соединения-зонда на основе активности, содержащего фрагмент илида сульфоксония в качестве активной группы, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
В некоторых таких вариантах осуществления соединение-зонд на основе активности вводят внутривенно. В некоторых вариантах осуществления этого способа соединение-зонд на основе активности содержит фрагмент илида сульфоксония, имеющий формулу (IV):
[0269]
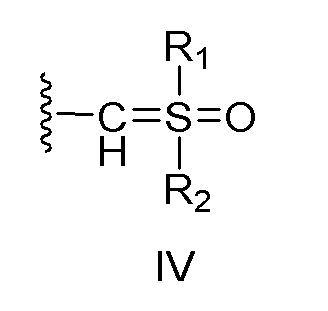
[0270] где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила. В некоторых вариантах осуществления R1 представляет собой (C1-C8) алкил, и R2 представляет собой (C1-C8) алкил. В некоторых вариантах осуществления R1 представляет собой метил, и R2 представляет собой метил.
[0271] В некоторых вариантах осуществления настоящее изобретение относится к способу детектирования in vivo активности цистеиновой протеазы у субъекта, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
В некоторых таких вариантах осуществления соединение или его соль, или композицию вводят внутривенно.
[0272] В некоторых вариантах осуществления каждого из вышеуказанных способов (in vivo) детектируемый сигнал измеряется с помощью оптической визуализации in vivo, радиографии или позитронно-эмиссионной томографии. В некоторых таких вариантах осуществления детектируемый сигнал измеряется с помощью радиографии или позитронно-эмиссионной томографии. В некоторых таких вариантах осуществления указанное соединение содержит детектируемый элемент в виде радиоактивной метки. В некоторых других вариантах осуществления указанное соединение содержит детектируемый элемент в виде хелатора для радиоактивной метки. В некоторых вариантах осуществления субъектом является человек.
[0273] Способы ингибирования цистеиновых протеаз
[0274] В некоторых вариантах осуществления настоящее изобретение относится к способу ингибирования цистеиновой протеазы, включающему контактирование цистеиновой протеазы с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано. В некоторых таких вариантах осуществления способ представляет собой способ in vitro.
[0275] В некоторых вариантах осуществления настоящее изобретение относится к способу ингибирования цистеиновой протеазы in vitro, включающему контактирование биологического образца с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано.
[0276] В некоторых вариантах осуществления настоящее изобретение относится к способу ингибирования цистеиновой протеазы в биологическом образце, полученном от субъекта, включающему контактирование биологического образца in vitro с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано.
[0277] В некоторых вариантах осуществления настоящее изобретение относится к способу ингибирования in vivo цистеиновой протеазы у субъекта, включающему введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано. В некоторых таких вариантах осуществления соединение или его соль, или композицию вводят внутривенно.
[0278] В некоторых вариантах осуществления способов ингибирования цистеиновой протеазы, как здесь описано, соединение формулы I, как здесь описано, не содержит детектируемого элемента, такого как флуоресцентная метка, биотиновая метка, радиоактивная метка, хелатор и биоортогональный маркер для лигирования.
[0279] Цистеиновые протеазы
[0280] В способах детектирования активности цистеиновой протеазы, как здесь описано, и в способах ингибирования цистеиновой протеазы, как здесь описано, цистеиновая протеаза может, например, представлять собой цистеиновую протеазу млекопитающих. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновую протеазу человека. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновый катепсин. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновый катепсин млекопитающих. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновый катепсин человека. В некоторых вариантах осуществления цистеиновая протеаза представляет собой катепсин S и/или катепсин X. В некоторых вариантах осуществления цистеиновая протеаза представляет собой катепсин X. В определенных вариантах осуществления цистеиновая протеаза представляет собой катепсин X млекопитающих. В некоторых вариантах осуществления цистеиновая протеаза представляет собой катепсин X человека.
[0281] В некоторых вариантах осуществления способов детектирования активности цистеиновой протеазы, как здесь описано, детектируется активность катепсина X, и активность катепсина B и/ или активность катепсина L не детектируется. В некоторых вариантах осуществления детектируют активность катепсина X и активность катепсина S, и активность катепсина B и/или активность катепсина L не детектируют.
[0282] В некоторых вариантах осуществления способов ингибирования цистеиновой протеазы, как здесь описано, ингибируется катепсин X, и катепсин B и/или катепсин L не ингибируются. В некоторых вариантах осуществления катепсин X и катепсин S ингибируются, и катепсин B и/или катепсин L не ингибируются.
[0283] В способах детектирования активности цистеиновой протеазы in vitro, как здесь описано, идентичность меченого белка можно анализировать, например, подвергая аликвоту меченого зондом образца иммунопреципитационному тесту (например, преципитация с антителом, специфичным для соответствующей цистеиновой протеазе (например, катепсин X).
[0284] Способы диагностики и соответствующие соединения/ композиции для применения в диагностике
[0285] В некоторых вариантах осуществления настоящее изобретение относится к способу диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающему:
(1) контактирование биологического образца, полученного от субъекта in vitro, с соединением формулы I, как здесь описано, или его солью, или с композицией, как здесь описано, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ включает детектирование активности цистеиновой протеазы в соответствии с любым из способов, описанных здесь в разделе «Способы детектирования (in vitro)».
[0286] В некоторых вариантах осуществления настоящее изобретение относится к способу диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ включает определение активности цистеиновой протеазы в соответствии с любым из способов, описанных здесь в разделе «Способы детектирования (in vitro) с предварительным введением субъекту».
[0287] В некоторых вариантах осуществления настоящее изобретение относится к способу диагностики in vivo заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающему:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, или композиции, как здесь описано, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ включает определение активности цистеиновой протеазы в соответствии с любым из способов, описанных здесь в разделе «Способы детектирования in vivo».
[0288] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, как здесь описано, или его соли для применения в способе диагностики заболевания, асоциированного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ включает определение активности цистеинпротеазы в соответствии с любым из способов, описанных здесь в разделе «Способы детектирования (in vitro) с предварительным введением субъекту».
[0289] В некоторых вариантах осуществления настоящее изобретение относится к композиции, как здесь описано, для применения в способе диагностики заболевания, ассоциирвоанного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту композиции, как здесь описано,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ включает определение активности цистеиновой протеазы в соответствии с любым из способов, описанных здесь в разделе «Способы детектирования (in vitro) с предварительным введением субъекту».
[0290] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, как здесь описано, или его соли для применения в способе диагностики in vivo заболевания, ассоциированного с активностью цистеиновой протеазы у субъекта, где способ включает:
(1) введение субъекту соединения формулы I, как здесь описано, или его соли, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ включает определение активности цистеиновой протеазы в соответствии с любым из способов, описанных здесь в разделе «Способы детектирования in vivo».
[0291] В некоторых вариантах осуществления настоящее изобретение относится к композиции, описанной здесь, для применения в способе диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта in vivo, где указанный способ включает:
(1) введение субъекту композиции, как здесь описано, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
В некоторых таких вариантах осуществления способ включает определение активности цистеиновой протеазы в соответствии с любым из способов, описанных здесь в разделе «Способы детектирования in vivo».
[0292] Биологические образцы
[0293] В некоторых вариантах осуществления биологический образец выбран из группы, состоящей из клеток, клеточных лизатов, образцов тканей, лизатов тканей и жидкостей организма. В некоторых вариантах осуществления биологический образец представляет собой лизат клеток или лизат ткани, такой как лизат очищенных клеток или лизат очищенных тканей. В некоторых вариантах осуществления биологический образец представляет собой живые клетки. В некоторых вариантах осуществления способа детектирования, как описано выше, живые клетки лизируются и очищаются между стадией (1) и стадией (2) и между стадией (2) и (3), соответственно. В некоторых вариантах осуществления биологический образец получают от человека.
[0294] В некоторых вариантах осуществления биологический образец получают из ротовой полости (например, слизистой оболочки ротовой полости), легких, головного мозга, спинного мозга, поджелудочной железы, желудка, предстательной железы, печени, костного мозга, толстого кишечника (такого как дистальный отдел толстого кишечника или проксимальный отдел толстого кишечника), прямой кишки, молочной железы, кожи, слизистой оболочки или слизи субъекта, или из кала или мокроты субъекта (такого как млекопитающее, конкретнее человека-субъекта). Биологический образец может представлять собой опухолевую ткань, полученную из ротовой полости, легких, головного мозга, спинного мозга, поджелудочной железы, желудка, предстательной железы, печени, костного мозга, толстого кишечника (например, дистального отдела толстого кишечника или проксимального отдела толстого кишечника), прямой кишки, молочной железы, кожи, слизистой оболочки или слизи субъекта.
[0295] В некоторых таких вариантах осуществления биологический образец получают из ротовой полости (такой как слизистая оболочка рта) субъекта. В некоторых таких вариантах осуществления биологический образец представляет собой лизат клеток или лизат ткани. В некоторых вариантах осуществления биологический образец представляет собой биопсийный материал ротовой полости. В некоторых вариантах осуществления биологический образец представляет собой биопсийный материал слизистой оболочки ротовой полости.
[0296] В некоторых вариантах осуществления биологический образец получают из желудочно-кишечного тракта субъекта. В некоторых таких вариантах осуществления биологический образец представляет собой лизат клеток или лизат ткани. В некоторых таких вариантах осуществления биологический образец представляет собой биопсийный материал ротовой полости, образец пищевода, образец желудка, образец тонкого кишечника, образец толстого кишечника, образец проксимального отдела толстого кишечника, образец дистального отдела толстого кишечника, образец прямой кишки, образец кала или биопсийый материал слизистой оболочки. В некоторых вариантах осуществления, в которых биологический образец получают из желудочно-кишечного тракта субъекта, биологический образец представляет собой биопсийный материал слизистой оболочки, выбранный из группы, состоящей из биопсийного материала слизистой оболочки ротовой полости, биопсийного материала слизистой оболочки пищевода, биопсийного материала слизистой оболочки тонкого кишечника, биопсийного материала толстого кишечника слизистой оболочки или биопсийного материала слизистой оболочки прямой кишки.
[0297] В некоторых вариантах осуществления биологический образец получают из толстого кишечника (такого как дистальный отдел толстого кишечника или проксимальный отдел толстого кишечника) субъекта. В некоторых таких вариантах осуществления биологический образец представляет собой лизат клеток или лизат ткани. В некоторых вариантах осуществления биологический образец представляет собой биопсию толстого кишечника. В некоторых вариантах осуществления биологический образец представляет собой биопсийный материал слизистой оболочки толстого кишечника. В некоторых вариантах осуществления, в которых биологический образец получают из толстого кишечника, биологический образец представляет собой образец кала.
[0298] В некоторых вариантах осуществления биологический образец получают из предстательной железы субъекта. В некоторых таких вариантах осуществления биологический образец представляет собой лизат клеток или лизат ткани. В некоторых вариантах осуществления биологический образец представляет собой биопсийный материал предстательной железы.
[0299] В некоторых вариантах осуществления биологический образец может представлять собой клетки, клеточные лизаты, образцы тканей и лизаты тканей, полученные из молочной железы субъекта женского пола (в частности, субъекта женского пола).
[0300] В некоторых вариантах осуществления биологический образец представляет собой лизат ткани, выбранный из группы, состоящей из биопсийного материала ротовой полости, образца легкого, образца головного мозга, образца спинного мозга, образца поджелудочной железы, образца желудка, образца предстательной железы, образца печени, образца костного мозга, образца толстого кишечника (например, образца дистального отдела толстого кишечника и образца проксимального отдела толстого кишечника), образца прямой кишки, образца молочной железы, образца кожи, биопсийного материала слизистой оболочки, образца кала, образца мокроты и образца опухоли.
[0301] Способы лечения и соответствующие соединения/ композиции для применения в лечении
[0302] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения заболевания, ассоциированного с активностью цистеиновой протеазы, включающему введение пациенту, нуждающегося в этом, терапевтически эффективного количества соединения формулы I, как здесь описано, или терапевтически эффективного количества соединения композиция, как здесь описано.
[0303] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, как здесь описано, для применения в лечении заболевания, ассоциированного с активностью цистеиновой протеазы.
[0304] В некоторых вариантах осуществления настоящее изобретение относится к композиции для применения в лечении заболевания, ассоциированного с активностью цистеиновой протеазы, содержащкй соединение формулы I, как здесь описано, и эксципиент.
[0305] В некоторых вариантах осуществления настоящее изобретение относится к применению соединения формулы I, как здесь описано, в производстве лекарственного средства для лечения заболевания, ассоциированного с активностью цистеиновой протеазы.
[0306] В некоторых вариантах осуществления настоящее изобретение относится к применению композиции, описанной здесь, в производстве лекарственного средства для лечения заболевания, ассоциированного с активностью цистеиновой протеазы.
[0307] В некоторых из вышеуказанных вариантов осуществления соединение формулы I, как здесь описано, при введении или применении (или для применения) в лечении заболевания не содержит детектируемого элемента, такого как флуоресцентная метка, биотиновая метка, радиоактивная метка, хелатор и биоортогональный маркер для лигирования.
[0308] Заболевания
[0309] В некоторых вариантах осуществления заболевание (которое необходимо диагностировать или лечить), ассоциированное с активностью цистеиновой протеазы, выбрано из группы, состоящей из целиакии, расстройства моторики желудочно-кишечного тракта, боли, зуда, заболевания кожи (такого как атопический дерматит), ожирения, вызванного рационом, нарушение обмена веществ (включая, помимо прочего, неалкогольный стеатогепатит (NASH), заболевания печени и поджелудочной железы), астмы, ревматоидного артрита, пародонтита, воспалительного заболевания (включая воспалительное заболевание ЖКТ, такое как воспалительное заболевание кишечника), функционального расстройства желудочно-кишечного тракта (например, синдром раздраженного кишечника, функциональная боль в груди, функциональная диспепсия, тошнота и рвота, функциональный запор, функциональная диарея, недержание кала, функциональная аноректальная боль и функциональное расстройство дефекации), рака, фиброзного заболевания, метаболической дисфункции, неврологического заболевания и нейродегенеративного заболевания.
[0310] В некоторых вариантах осуществления заболевание (которое необходимо диагностировать или лечить), ассоциированное с активностью цистеиновой протеазы, выбрано из группы, состоящей из рака, воспалительного заболевания и нейродегенеративного заболевания.
[0311] В некоторых вариантах осуществления заболевание (которое необходимо диагностировать или лечить) представляет собой рак, выбранный из группы, состоящей из рака молочной желеыз, рака мозга (глиобластомы), рака костного мозга, рака поджелудочной железы, рака легких, рака предстательной железы, рака печени (гепатоцеллюлярной карциномы), рака ротовой полости, колоректального рака и рака желудка.
[0312] В некоторых вариантах осуществления заболевание (подлежащее диагностике или лечению) представляет собой воспалительное заболевание, выбранное из группы, состоящей из воспалительного заболевания желудочно-кишечного тракта, панкреатита и инфекции. В некоторых таких вариантах осуществления воспалительное заболевание желудочно-кишечного тракта выбрано из группы, состоящей из воспалительного заболевания кишечника, инфекционной диареи, ишемии брыжейки, дивертикулита и некротического энтероколита (NEC). В некоторых вариантах воспалительное заболеваник желудочно-кишечного тракта представляет собой воспалительное заболевание кишечника. В некоторых вариантах осуществления воспалительное заболевание кишечника выбрано из группы, состоящей из язвенного колита, болезни Крона, диверсионного колита, колита неопределенной этиологии и паухита, микроскопического колита, иммуноонкологического колита, колита в результате химиотерапии/лучевой терапии, колита на фоне синдрома «трансплантат против хозяина» (GvHD), острого колита, болезни Бехчета, коллагенозного колита, лимфоцитарного колита. В некоторых вариантах воспалительное заболевание желудочно-кишечного тракта выбрано из язвенного колита и болезни Крона.
[0313] В некоторых вариантах осуществления заболевание (подлежащее диагностике или лечению) представляет собой воспалительное заболевание, выбранное из группы, состоящей из язвенного колита, болезни Крона, диверсионного колита, колита неопределенной этиологии и паухита, микроскопического колита, иммуноонкологического колита, колита в результате химиотерапии/лучевой терапии, колита на фоне синдрома «трансплантат против хозяина» (GvHD), острого колита, болезни Бехчета, коллагенозного колита, лимфоцитарного колита, инфекционной диареи, ишемии брыжейки, дивертикулита и некротического энтероколита (NEC), панкреатита и инфекции.
[0314] В некоторых вариантах осуществления заболевание (подлежащее диагностике или лечению) представляет собой воспалительное заболевание, выбранное из воспалительных заболеваний кишечника. В некоторых таких вариантах воспалительное заболевание кишечника представляет собой язвенный колит или болезнь Крона.
[0315] В некоторых вариантах осуществления заболевание (подлежащее диагностике или лечению) представляет собой нейродегенеративное заболевание, выбранное из группы, состоящей из болезни Альцгеймера, рассеянного склероза и нейропатической боли.
[0316] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак молочной железы, биологический образец представляет собой образец, как описано выше, который получают из молочной железы субъекта, например из опухолевой ткани, расположенной в молочной железе.
[0317] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак головного мозга, биологический образец представляет собой образец, как описано выше, который получают из головного мозга субъекта, например из опухолевой ткани, расположенной в головном мозге.
[0318] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак костного мозга, биологический образец представляет собой образец, как описано выше, который получают из костного мозга субъекта, например из опухолевой ткани, расположенной в костном мозге.
[0319] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак поджелудочной железы, биологический образец представляет собой образец, как описано выше, который получают из поджелудочной железы субъекта, например из опухолевой ткани, расположенной в поджелудочной железе.
[0320] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак легких, биологический образец представляет собой образец, как описано выше, который получают из легких субъекта, например из опухолевой ткани, расположенной в легком.
[0321] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак предстательной железы, биологический образец представляет собой образец, как описано выше, который получают из предстательной железы субъекта, например из опухолевой ткани, расположенной в предстательной железе.
[0322] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак печени, биологический образец представляет собой образец, как описано выше, который получают из печени субъекта, например из опухолевой ткани, расположенной в печени.
[0323] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак ротовой полости, биологический образец представляет собой образец, как описано выше, который получают из ротовой полости субъекта, например из опухолевой ткани, расположенной в ротовой полости.
[0324] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой колоректальный рак, биологический образец представляет собой образец, как описано выше, который получают из толстой или прямой кишки субъекта, например из опухолевой ткани, расположенной в толстой или прямой кишке.
[0325] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рак желудка, биологический образец представляет собой образец, как описано выше, который получают из желудка субъекта, например из опухолевой ткани, расположенной в желудке.
[0326] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой воспалительное заболевание желудочно-кишечного тракта или функциональное расстройство желудочно-кишечного тракта, биологический образец представляет собой образец, как описано выше, который получают из желудочно-кишечного тракта (такого как толстая кишка) субъекта.
[0327] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой воспалительное заболевание кишечника, биологический образец представляет собой образец, как описано выше, который получают из желудочно-кишечного тракта (такого как толстый кишечник) субъекта.
[0328] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой язвенный колит, болезнь Крона, диверсионный колит, колит неопределенной этиологии и поухит, микроскопический колит, иммуноонкологический колит, колит в результате химиотерапии/лучевой терапии, колит на фоне синдрома «трансплантат против хозяина» (GvHD), острый колит, болезнь Бехчета, коллагенозный колит, лимфоцитарный колит, инфекционную диарею, ишемию брыжейки, дивертикулит или некротический энтероколит (NEC), биологический образец представляет собой образец, как описано выше, который получают из желудочно-кишечного тракта (например, толстого кишечника) субъекта.
[0329] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой панкреатит, биологический образец представляет собой образец, как описано выше, полученный из поджелудочной железы субъекта.
[0330] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой инфекцию, биологический образец представляет собой образец, как описано выше, полученный из инфицированной области или части тела субъекта.
[0331] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой болезнь Альцгеймера, биологический образец представляет собой образец, как описано выше, который получают из головного мозга субъекта.
[0332] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой рассеянный склероз, биологический образец представляет собой образец, как описано выше, который получают из головного мозга субъекта.
[0333] В некоторых вариантах осуществления, относящихся к диагностике заболевания, где заболевание представляет собой невропатическую боль, биологический образец представляет собой образец, как описано выше, полученный из спинного мозга субъекта.
[0334] В некоторых вариантах осуществления биологический образец включает образец, полученный из патологической ткани субъекта (например, опухолевой ткани, воспаленной ткани и/или инфицированной ткани). В некоторых вариантах осуществления биологический образец включает образец, полученный из патологической ткани субъекта, и образец, полученный из нормальной (непатологической) ткани того же субъекта в качестве контроля.
[0335] В некоторых вариантах осуществления заболевание (которое необходимо диагностировать или лечить) представляет собой рак ротовой полости. В некоторых таких вариантах осуществления рак ротовой полости представляет собой плоскоклеточную карциному ротовой полости. Для диагностики рака ротовой полости, такого как плоскоклеточная карцинома ротовой полости, биологический образец может представлять собой образец ткани (лизат ткани), полученный из полости рта субъекта, например из опухолевой ткани, расположенной в ротовой полости. В некоторых таких вариантах осуществления биологический образец представляет собой биопсийный материал слизистой оболочки ротовой полости, полученный от субъекта (например, включая биопсийный материал из опухолевой ткани и из нормальной (непатологической) ткани того же субъекта).
[0336] В некоторых вариантах осуществления заболевание, ассоциированное с активностью цистеиновой протеазы, представляет собой заболевание, ассоциированное с активностью цистеиновой протеазы, где цистеиновая протеаза представляет собой цистеиновую протеазу млекопитающих. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновую протеазу человека. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновый катепсин. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновый катепсин млекопитающих. В некоторых вариантах осуществления цистеиновая протеаза представляет собой цистеиновый катепсин человека. В некоторых вариантах осуществления цистеиновая протеаза представляет собой катепсин S и/или катепсин X. В некоторых вариантах осуществления цистеиновая протеаза представляет собой катепсин X. В определенных вариантах осуществления цистеиновая протеаза представляет собой катепсин X млекопитающих. В некоторых вариантах осуществления цистеиновая протеаза представляет собой катепсин X человека.
[0337] В некоторых вариантах осуществления заболевание, ассоциированное с активностью цистеиновой протеазы, представляет собой заболевание, ассоциированное с активностью катепсина X.
[0338] Синтез хлорметилкетонов через промежуточный илид сульфоксония
[0339] Многие из зарегистрированных зондов на основе активности цистеиновых протеаз включают активные группы из ацилоксиметилкетона (AOMK) или феноксиметилкетона (PMK) (Edgington et al., 2009; 2012; 2013; Oresic Bender et al., 2015; Verdoes et al., 2013; 2012). Для синтеза этих электрофилов требуется образования промежуточных соединений хлорметилкетона, процесса, который исторически достигался за счет образования диазометана, чрезвычайно взрывоопасного желтого газа. Авторы настоящего изобретения теперь открыли новый путь синтеза для доступа к хлорметилкетонам через промежуточный илид сульфоксония (схема 2), который не требует образования диазометанов, тем самым избегая этой потенциально опасной реакции и, таким образом, обеспечивая более безопасную альтернативу ранее используемым методам. Этот метод также позволяет обойтись без N-метил-N-нитрозо-п-толуолсульфонамида (Diazald®), продукта, который недавно был снят с производства Sigma Aldrich.
[0340] Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к способу получения соединения, содержащего хлорметилкетоновую группу, включающему взаимодействие соединения, несущего фрагмент илида сульфоксония, с получением соединения, несущего хлорметилкетоновую группу.
[0341] В некоторых вариантах осуществления настоящее изобретение относится к способу получения соединения-зонда на основе активности, несущего ацилоксиметилкетоновый фрагмент или феноксиметилкетоновый фрагмент в качестве активной группы, включающему:
(i) получение промежуточного соединения, содержащего хлорметилкетоновую группу, взаимодействием соединения, содержащего фрагмент илида сульфоксония, с получением соединения, несущего хлорметилкетоновую группу; и
(ii) последующую обработку соединения, содержащего хлорметилкетоновую группу, с получением указанного соединения-зонда на основе активности.
[0342] В некоторых из вышеуказанных вариантов осуществления способ включает взаимодействие соединения, несущего фрагмент илида сульфоксония, с соляной кислотой с получением соединения, содержащего фрагмент хлорметилкетона. В некоторых таких вариантах осуществления соединение, несущее фрагмент илида сульфоксония, взаимодействует с соляной кислотой при повышенной температуре. В некоторых таких вариантах осуществления соединение, несущее фрагмент илида сульфоксония, взаимодействует с соляной кислотой при повышенной температуре и в органическом растворителе. В некоторых таких вариантах осуществления органический растворитель включает простой эфир, такой как тетрагидрофуран.
[0343] В некоторых вариантах осуществления фрагмент илида сульфоксония имеет формулу (IV):
[0344]
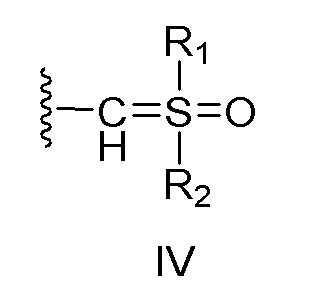
[0345] где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила. В некоторых вариантах осуществления R1 представляет собой (C1-C8) алкил, и R2 представляет собой (C1-C8) алкил. В некоторых вариантах осуществления где R1 представляет собой метил, и R2 представляет собой метил.
[0346] Используя усовершенстованный способ, описанный выше, были успешно созданы три зонда AOMK, несущие Lys, Phe и Nle, что позволяет предположить, что данный способ может широко применяться для синтеза различных ABP. Сравнение синтезированных зондов AOMK с зондами на основе илида сульфоксония, несущими идентичные последовательности распознавания, показало, что соответствующие зонды на основе илида сульфоксония более эффективны и специфичны, чем аналоги ацилоксиметилкетона, что дополнительно подтверждает пригодность новой активной группы из илида сульфоксония. Таким образом, зонды на основе илида сульфоксония представляют собой очевидный прогресс в инструментах, доступных для изучения функции цистеиновых протеаз, таких как катепсин X.
[0347] В дополнительном аспекте изобретение относится к соединению, имеющему формулу, выбранную из группы формул, состоящей из:
[0348]
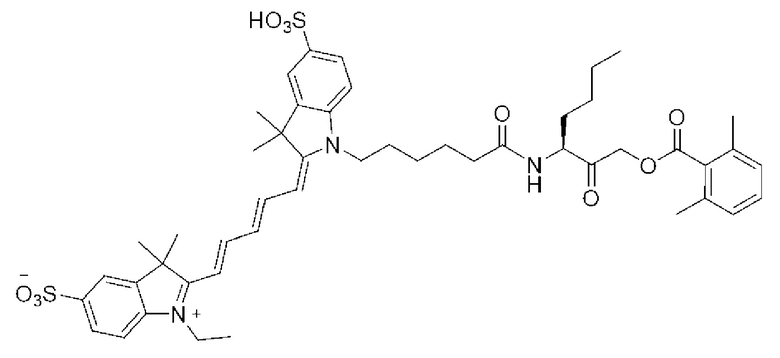
[0349]
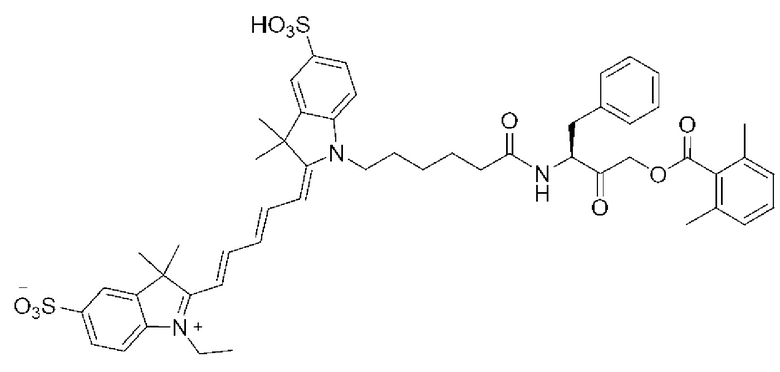
[0350]

[0351] или его соли.
Подробное описание изобретения
[0352] Настоящее изобретение теперь более полно описано со ссылкой на сопроводительные примеры. Однако следует понимать, что нижеследующее описание является только иллюстративным и никоим образом не должно рассматриваться в качестве ограничения изобретения.
[0353] Примеры
[0354] Синтез и характеристика соединений
[0355] Общая информация
[0356] Все реагенты были приобретены у коммерческих поставщиков и использовались без дополнительной очистки.
[0357] Сульфо-Cy5 (форма свободной карбоновой кислоты) был приобретен в W&J Pharmachem.
[0358] Все использованные растворители были чистыми для ВЭЖХ. Все водочувствительные реакции проводили в безводных растворителях в атмосфере аргона.
[0358] ОФ-ВЭЖХ выполняли на колонке Phenomenex Luna C-8 (100 Å, 10 мкм, 250 × 21,5 мм) с использованием полупрепаративной ВЭЖХ Waters 600, включающей УФ-детектор Waters 486. Профиль элюирования представлял собой линейный градиент от 0-60% буфера A до буфера B (буфер A: 0,1% ТФК в воде; буфер B: 0,1% ТФК в ацетонитриле) в течение 60 мин со скоростью потока 15 мл/мин. Идентичность соединения подтверждали с помощью ESI-MS с использованием прибора Shimadzu LCMS2020, включающего колонку Phenomenex Luna C-8 (100 Å, 3 мкм, 100×2,00 мм). Профиль элюирования представлял собой 0,1% ТФК в воде в течение 4 мин с последующим линейным градиентом от 0-60% буфера A до буфера B в течение 10 мин со скоростью потока 0,2 мл/мин.
[0359] Спектры ядерного магнитного резонанса (ЯМР) получали с использованием спектрометра Bruker Avance III Nanobay, соединенного с автоматическим устройством смены образцов BACS 60. Спектрометр был снабжен зондом PABBO BB‐1H/DZ‐GRD 5 мм. Спектры ЯМР 1H получены при 400 МГц. Каждый резонанс относили согласно следующему условию: химический сдвиг (δ), измеренный в частях на миллион (ppm) относительно остаточного недейтерированного пика растворителя хлороформа (если не указано иное) в качестве внутреннего эталона относительно триметилсилана (= 0), множественность, константы взаимодействия (J Гц), число протонов и отнесение. Кратности обозначаются как (с) синглет, (д) дублет, (дд) дублет дублетов, (т) триплет, (кв) квартет или (м) кратность.
[0360] Спектры углеродного ядерного магнитного резонанса (13С ЯМР) получали при 100 МГц. Каждый резонанс относили согласно следующему условию: химический сдвиг (δ), измеренный в частях на миллион (ppm) относительно остаточного недейтерированного пика растворителя хлороформа (если не указано иное) в качестве внутреннего эталона относительно триметилсилана (= 0), количество атомов углерода и назначение.
[0361] Масс-спектрометрию-жидкостную хроматографию (ЖХМС) проводили на приборе Agilent UHPLC/MS 1260 (насос для четырехкомпонентных смесей G1311A серии 1200, автосамплер: термостатированный автосамплер серии 1200 G1329A, детектор: детектор с переменной длиной волны G1314B серии 1200). Профиль элюирования представлял собой линейный градиент 5-100% B в течение 2,5 мин со скоростю потока 0,5 мл/мин. Растворитель A: вода 0,1% муравьиная кислота, растворитель B: ацетонитрил 0,1% муравьиная кислота. Условия жидкостной хроматографии; Анализ с помощью ВЭЖХ с обращенной фазой, Колонка: Poroshell 120 EC-C18 3,0 × 50 мм 2,7 мкм, температура колонки: 35°C, объем инжектирования: 1 мкл, детекция: отслеживается при 254 нм и 214 нм. Условия масс-спектрометра: источник ионов: квадруполь, ионный режим: API-ES, температура осушающего газа: 350°C. Пики основных ионов (m/z) указаны с интенсивностями основного пика в скобках.
[0362] Масс-спектры высокого разрешения (HRMS) получали на масс-спектрометре Agilent 6224 TOF LC/MS, соединенном с Agilent 1290 Infinity (Agilent, Palo Alto, CA). Все данные регистрировали и контрольную массу корректировали с помощью источника ионизации электрораспылением (ESI) с двойным распылением. Условия масс-спектрометра: режим ионизации: ионизация электрораспылением; расход осушающего газа: 11 л/мин, растворитель A=водный раствор 0,1% муравьиной кислоты, растворитель B=ацетонитрил/0,1% муравьиная кислота. Приведены найденные и рассчитанные ионные пики (m/z).
[0363] Все аналитические анализы ВЭЖХ выполняли на Agilent 1260 Infinity Analytical HPLC, соединенном с дегазатором 1260: G1322A, 1260 Binary Pump: G1312B, автосамплером 1260 HiP ALS: G1367E, 1260 TCC: G1316A и детектором 1260 DAD: G4212B. Используемая колонка представляла собой Zorbax Eclipse Plus C18 Rapid Resolution 4,6 мм × 100 мм 3,5 мкм. Объем вводимой пробы составлял 2 мкл, которую обрабатывали в 0,1% ТФК в ацетонитриле с градиентом от 5 до 100% в течение 10 мин со скоростью потока 1 мл/мин. Анализ проводили при 214 нм и 254 нм.
[0364] Пример 1. Синтез соединений илида сульфоксония
[0365] Соединения, содержащие илид сульфоксония (зонды sCy5-AA-SY), синтезировали согласно схеме реакций 1 и в соответствии с общими способами A, B и E, описанными ниже.
[0366]
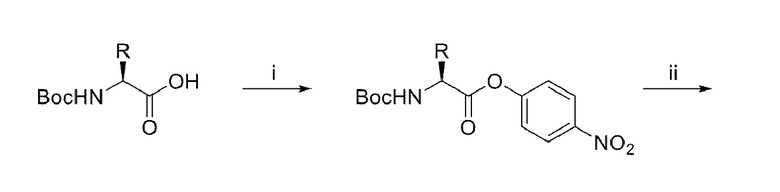
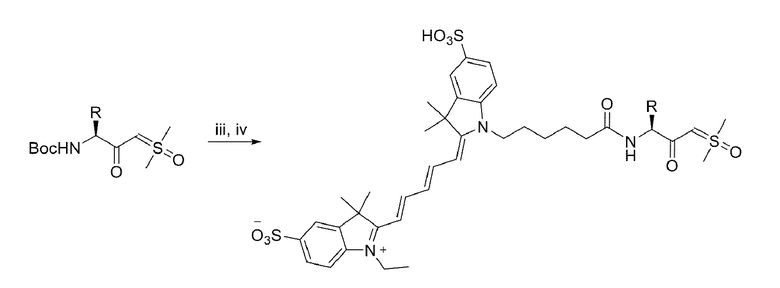
Схема 1. Синтез зондов sCy5-AA-SY. i) 4-нитрофенилхлорформиат, Et3N, DMAP, CH2Cl2, 0°C, 6 ч. ii) SOMe3+ I- KOtBu, ТГФ, кипячение с обратным холодильником → 0°C. iii) смесь ТФК/ CH2Cl2 (1:1), iv) сульфо-Cy5, PyClock, DIPEA, DMF, комнатная температура, 18 ч.
Общий способ А. Получение сложных нитрофениловых эфиров
Триэтиламин (1,2 экв) добавляли к раствору Boc-защищенной аминокислоты (1 экв) в CH2Cl2 (5 мл). Перемешиваемую смесь охлаждали до 0°C и добавляли 4-нитрофенилхлорформиат (1,2 экв). Через 10 мин добавляли DMAP (0,1 экв) и смесь перемешивали при 0°C в течение 6 ч. Реакционную смесь дополнительно разбавляли CH2Cl2 (15 мл) и промывали насыщенным раствором NaHCO3 (10 мл), 0,1 М раствором HCl (10 мл), насыщенным раствором соли (10 мл), и затем сушили (MgSO4), фильтровали и растворитель выпаривали в вакууме с получением сырого продукта.
[0368] Общий способ B. Получение илидов сульфоксония
Иодид триметилсульфоксония (4 экв) суспендировали в сухом ТГФ (5 мл) и добавляли KOtBu (4 экв). Смесь перемешивали при кипячении с обратным холодильником в течение 3 ч в темноте. Реакционную смесь охлаждали до 0°C, по каплям добавляли раствор нитрофенилового эфира (1 экв) в ТГФ и перемешивали в течение 18 ч. Реакцию гасили H2O (30 мл) и раствор концентрировали в вакууме для удаления ТГФ. Оставшийся водный раствор экстрагировали EtOAc (3 × 30 мл). Объединенный органический экстракт промывали насыщенным раствором соли (15 мл), сушили (MgSO4), фильтровали и растворитель удаляли в вакууме с получением сырого продукта.
[0369] Общий способ E: мечение сульфоксониевых илидов сульфоцианином 5
Boc-защищенный илид сульфоксония (1 экв) обрабатывали смесью 1:1 ТФК и CH2Cl2 (2 мл) и перемешивали при температуре окружающей среды в течение 1 ч. Летучие компоненты удаляли в токе азота. К полученному остатку добавляли ДМФА (300 мкл) и DIPEA (4 экв). Отдельно Сульфо-Cy5 (1 экв) и PyClock (2 экв) растворяли в ДМФА (300 мкл) и DIPEA (4 экв) и перемешивали в течение 2 мин перед добавлением к вышеуказанному раствору. Реакционную смесь перемешивали при температуре окружающей среды 18 ч в темноте.
[0370] Пример 1.1: синтез и характеристика промежуточных нитрофениловых эфиров
[0371] 4-нитрофенил (трет-бутоксикарбонил)-L-валинат (SJM-724-20)
[0372]
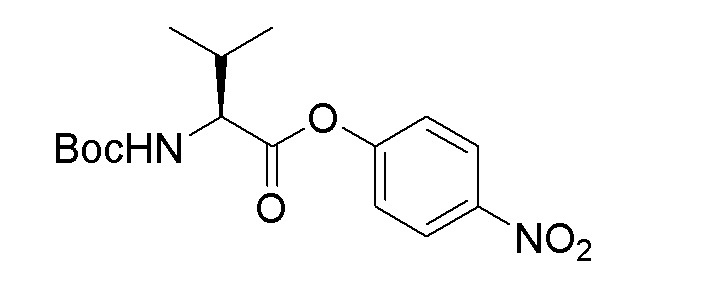
[0373] Охлажденный на льду сухой ДМФА (20 мл) медленно добавляли к 4-нитрофенилхлорформиату (2,27 г, 11,2 ммоль) и перемешивали в течение 10 мин в атмосфере азота. Затем смесь постепенно подогревали до температуры окружающей среды. По каплям добавляли раствор boc-L-валина (2,02 г, 9,30 ммоль) в ДМФА (7 мл), и затем триэтиламин (1,50 мл, 10,8 ммоль). Перемешивание продолжали в течение 1 ч. Реакционную смесь разбавляли EtOAc (50 мл) и промывали H2O (3 × 30 мл) и насыщенным раствором соли (30 мл). Органический слой сушили (MgSO4), фильтровали и концентрировали при пониженном давлении с получением сырого продукта. Очистка колоночной хроматографией (SiO2, 10-13% смесь EtOAc:петролейный спирт) давала продукт в виде вязкого бесцветного масла (2,01 г, 64%). HRMS (ESI+): найдено: m/z 361,1386 (M+Na)+, C16H22N2NaO6+ рассчитано m/z 361,1370. 1H ЯМР (400 МГц, CDCl3) δ 8,29-8,23 (м, 2H), 7,31-7,25 (м, 2H), 5,05 (д, J=8,4 Гц, 1H), 4,44 (дд, J=8,6, 5,1 Гц, 1H), 2,37-2,24 (м, 1H), 1,45 (с, 9H), 1,09 (д, J=6,8 Гц, 3H), 1,03 (д, J=6,9 Гц, 3H). 13C ЯМР (101 МГц, CDCl3) δ 170,6 (C), 155,9 (C), 155,3 (C), 145,7 (C), 125,4 (CH), 122,5 (CH), 80,6 (C), 59,1 (CH), 31,2 (CH), 28,4 (CH3), 19,3 (CH3), 17,9 (CH3). ЖХ-МС (ESI +) m/z: 339,3 (M+H)+ (40%), 360,8 (M+Na)+ (80%).
[0374] 4-нитрофенил (трет-бутоксикарбонил)-L-изолейцинат (SJM-724-64)
[0375]
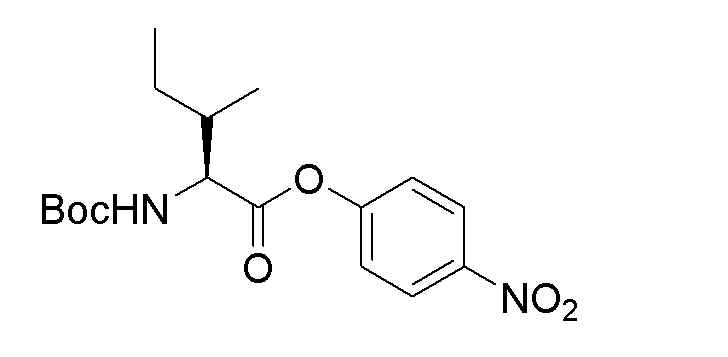
[0376] Указанное в заголовке соединение получали способом A из boc-L-изолейцина (200 мг, 0,86 ммоль), 4-нитрофенилхлорформиата (209 мг, 1,04 ммоль), DMAP (11 мг, 0,09 ммоль) и Et3N (145 мкл, 1,04 ммоль) в CH2Cl2 с получением сырого продукта в виде бесцветного масла. Очистка колоночной хроматографией (SiO2, смесь петролейный спирт:EtOAc 9:1) давала продукт в виде белого твердого вещества (259 мг, 85%). 1H ЯМР (401 МГц, CDCl3) δ 8,31-8,25 (м, 2H), 7,33-7,27 (м, 2H), 5,03 (д, J=7,8 Гц, 1H), 4,49 (дд, J=8,3, 5,2 Гц, 1H), 2,11-1,97 (м, 1H), 1,65-1,52 (м, 1H), 1,47 (с, 9H), 1,38-1,23 (м, 1H), 1,07 (д, J=6,8 Гц, 3H), 1,00 (т, J=7,4 Гц, 3H). ЖХ-МС (ESI+) m/z: 252,9 (M - Boc+ H)+ (100%), 374,9 (M+Na)+ (60%).
[0377] 4-нитрофенил (трет-бутоксикарбонил)-L-лейцинат (SJM-724-76)
[0378]
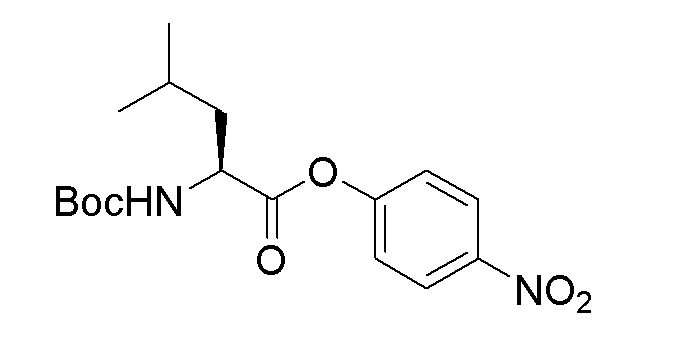
[0379] Указанное в заголовке соединение получали способом A из boc-L-лейцина (200 мг, 0,86 ммоль), 4-нитрофенилхлорформиата (209 мг, 1,04 ммоль), DMAP (11 мг, 0,09 ммоль) и Et3N (145 мкл, 1,04 ммоль) в CH2Cl2 с получением сырого продукта в виде желтого масла. Очистка колоночной хроматографией (SiO2, смесь петролейный спирт:EtOAc 9:1) давала продукт в виде белого твердого вещества (192 мг, 63%). 1H ЯМР (401 МГц, CDCl3) δ 8,32-8,24 (м, 2H), 7,35-7,28 (м, 2H), 4,91 (д, J=7,8 Гц, 1H), 4,59-4,44 (м, 1H), 1,89-1,73 (м, 2H), 1,73-1,62 (м, 1H), 1,46 (с, 9H), 1,03 (д, J=2,1 Гц, 3H), 1,02 (д, J=1,9 Гц, 3H). ЖХ-МС (ESI+) m/z: 252,9 (M - Boc+H)+ (100%), 374,9 (M+Na)+ (55%).
[0380] 4-нитрофенил (S)-2-((трет-бутоксикарбонил)амино) гексаноат (SJM-724-116)
[0381]
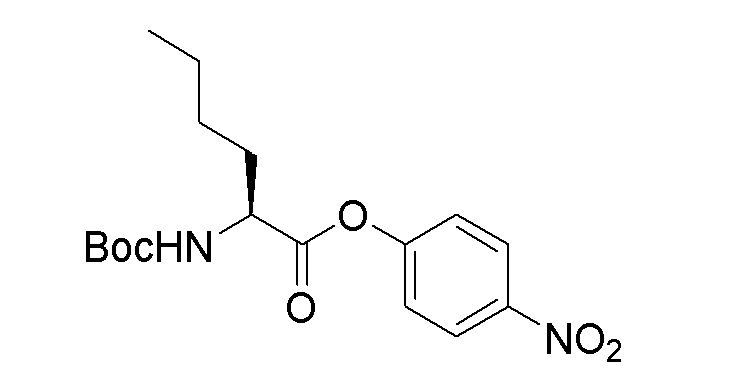
[0382] Указанное в заголовке соединение получали способом A из boc-L-норлейцина (200 мг, 0,86 ммоль), 4-нитрофенилхлорформиата (209 мг, 1,04 ммоль), DMAP (11 мг, 0,09 ммоль) и Et3N (145 мкл, 1,04 ммоль) в CH2Cl2 с получением сырого продукта в виде светло-желтого твердого вещества. Очистка колоночной хроматографией (SiO2, смесь петролейный спирт:EtOAc 9:1) давала продукт в виде белого твердого вещества (198 мг, 65%). HRMS (ESI+): найдено: m/z 375,1534 (M+Na)+, для C17H24N2NaO6+ рассчитано m/z 375,1527. 1H ЯМР (401 МГц, CDCl3) δ 8,32-8,25 (м, 2H), 7,33-7,27 (м, 2H), 4,99 (д, J=7,3 Гц, 1H), 4,50 (дд, J=13,0, 7,4 Гц, 1H), 2,02-1,91 (м, 1H), 1,86-1,74 (м, 1H), 1,51-1,35 (м, 13H), 0,95 (т, J=7,2 Гц, 3H). ЖХ-МС (ESI+) m/z: 252,9 (M - Boc+H) + (100%), 374,9 (M+Na)+ (95%).
[0383] 4-нитрофенил (трет-бутоксикарбонил)-L-фенилаланинат (SJM-724-68)
[0384]
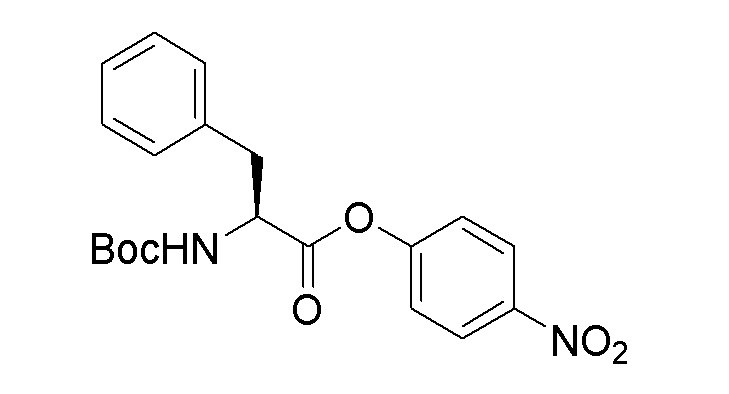
[0385] Указанное в заголовке соединение получали способом A из boc-L-фенилаланина (200 мг, 0,75 ммоль), 4-нитрофенилхлорформиата (182 мг, 0,90 ммоль), DMAP (9 мг, 0,08 ммоль) и Et3N (126 мкл, 0,90 ммоль) в CH2Cl2 с получением сырого продукта в виде белого твердого вещества. Очистка колоночной хроматографией (SiO2, CH2Cl2) давала продукт в виде белого твердого вещества (251 мг, 86%). 1H ЯМР (401 МГц, CDCl3) δ 8,29-8,22 (м, 2H), 7,40-7,29 (м, 3H), 7,25-7,21 (м, 2H), 7,17-7,11 (м, 2H), 5,03 (д, J=7,0 Гц, 1H), 4,80 (дд, J=13,6, 6,4 Гц, 1H), 3,31-3,15 (м, 2H), 1,45 (с, 9H). ЖХ-МС (ESI+) m/z: 286,9 (M - Boc+H)+ (60%), 408,8 (M+Na)+ (40%).
[0386] 4-нитрофенил (трет-бутоксикарбонил)-L-триптонат (SJM-724-112)
[0387]
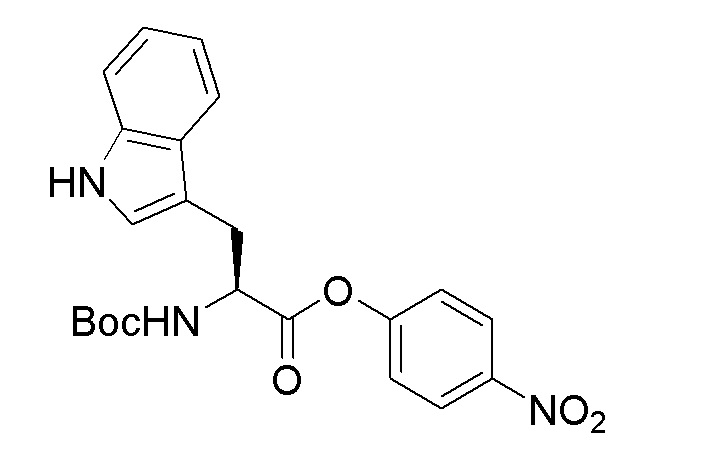
[0388] Указанное в заголовке соединение получали способом A из boc-L-триптофана (200 мг, 0,66 ммоль), 4-нитрофенилхлорформиата (159 мг, 0,79 ммоль), DMAP (8 мг, 0,07 ммоль) и Et3N (110 мкл, 0,79 ммоль) в CH2Cl2 с получением сырого продукта в виде желтого твердого вещества. Очистка колоночной хроматографией (SiO2, смесь петролейный спирт:EtOAc2:1) давала продукт в виде белого твердого вещества (200 мг, 72%). 1H ЯМР (401 МГц, CDCl3) δ 8,22-8,13 (м, 3H), 7,60 (д, J=7,9 Гц, 1H), 7,41 (д, J=8,1 Гц, 1H), 7,25-7,22 (м, 1H) , 7,16-7,11 (м, 2H), 7,03-6,98 (м, 2H), 5,15 (д, J=7,6 Гц, 1H), 4,91-4,80 (м, 1H), 3,50-3,35 (м, 2H), 1,45 (с, 9H). ЖХ-МС (ESI+) m/z: 325,9 (M - Boc+H)+ (100%).
[0389] 4-Нитрофенил Na-((бензилокси)карбонил)-Ne-(трет-бутоксикарбонил)-L-лизинат (SJM-724-40)
[0390]
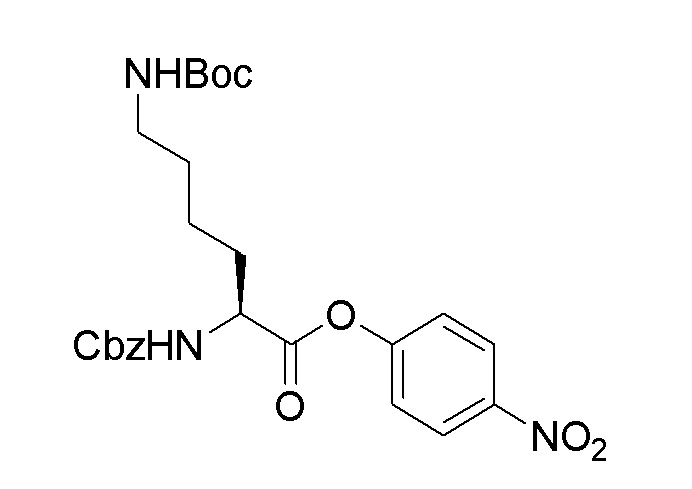
[0391] Охлажденный на льду сухой ДМФА (20 мл) медленно добавляли к 4-нитрофенилхлорформиату (1,27 г, 6,31 ммоль) и перемешивали в течение 10 мин в атмосфере азота. Затем смесь постепенно подогревали до температуры окружающей среды. По каплям добавляли раствор Na-бензилоксикарбонил-Ne-(трет-бутоксикарбонил)-L-лизина (2,00 г, 5,26 ммоль) в ДМФА (5 мл), и затем триэтиламин (879 мкл, 6,31 ммоль). Перемешивание продолжали в течение 20 ч. Реакционную смесь разбавляли EtOAc (50 мл) и промывали H2O (4 × 20 мл) и насыщенным раствором соли (20 мл). Органический слой сушили (MgSO4), фильтровали и концентрировали при пониженном давлении с получением сырого продукта в виде желтого масла. Очистка колоночной хроматографией (SiO2, смесь CH2Cl2:EtOAc 95:5) давала продукт в виде белого твердого вещества (672 мг, 25%). 1H ЯМР (401 МГц, CDCl3) δ 8,27 (д, J=8,9 Гц, 2H), 7,40-7,27 (м, 7H), 5,63-5,49 (м, 1H), 5,14 (с, 2H), 4,64-4,49 (м, 2H), 3,15 (с, 2H), 2,10-1,82 (м, 2H), 1,56-1,47 (м, 4H), 1,42 (с, 9H). ЖХ-МС (ESI+) m/z: 401,9 (M - Boc+H)+ (100%), 524,8 (M+Na)+ (20%).
[0392] (трет-Бутоксикарбонил)-L-фенилаланил-L-валин (MS-4-178)
[0393]
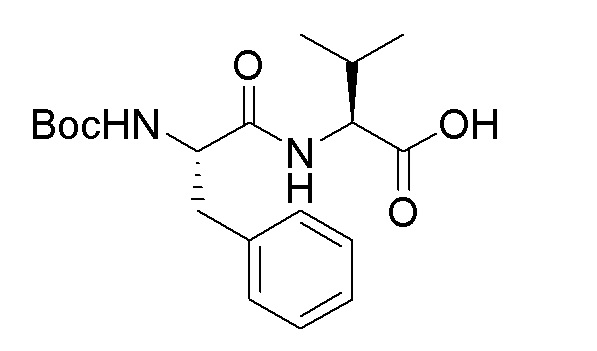
[0394] Fmoc-Val-OH (679 мг, 2,0 ммоль) растворяли в растворе DCM и триэтиламина (842 мкл, 6,0 ммоль) и добавляли к 2-хлортритиловой смоле (1,0 г, 1 ммоль) (1 мэкв/г). Смесь встряхивали при температуре окружающей среды в течение 1 ч. Смолу промывали DCM (3-5 мл). К смоле добавляли раствор MeOH (1 мл) в DCM (5 мл) и триэтиламин (0,5 мл) и встряхивали в течение 30 мин при температуре окружающей среды. Снятие защиты с Fmoc осуществляли обработкой 20% пиперидином в ДМФА в течение 10 мин, и затем промывали ДМФА (3-5 мл). Boc-Phe-OH (531 мг, 2,0 ммоль) и PyBOP (1,04 г, 2,0 ммоль) растворяли в растворе из DCM и триэтиламина (842 мкл, 6,0 ммоль) и добавляли к смоле. Смесь встряхивали при температуре окружающей среды в течение 1 ч, и затем сливали, промывали DCM (3-5 мл) и сушили в вакууме. Дипептид отщепляли от смолы обработкой 20% HFIP в DCM, содержащем 1% TIPS, в течение 2 ч. Смолу фильтровали и фильтрат упаривали в вакууме с получением сырого продукта (180 мг).
[0395] 4-нитрофенил (трет-бутоксикарбонил)-L-фенилаланил-L-валинат (MS-4-182)
[0396]
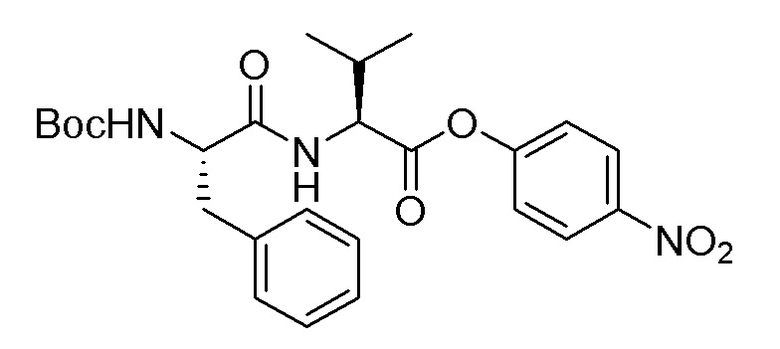
[0397] К раствору 4-нитрофенилхлорформиата (116 мг, 0,58 ммоль) в сухом ТГФ (1 мл) добавляли сухой ДМФА (150 мкл) при 0°C. Реакционную смесь перемешивали в течение 10 мин в атмосфере азота перед постепенным подогреванием до температуры окружающей среды. К указанной выше суспензии по каплям добавляли раствор (трет-бутоксикарбонил)-L-фенилаланил-L-валина (175 мг, 0,48 ммоль) в ТГФ (1 мл) и триэтиламине (80 мкл). Перемешивание продолжали в течение 20 мин. Реакционную смесь разбавляли EtOAc и промывали H2O. Органический слой сушили (MgSO4), фильтровали и концентрировали при пониженном давлении с получением сырого продукта (220 мг) в виде бледно-желтого твердого вещества.
[0398] Пример 1.2. Синтез и характеристика соединений илида сульфоксония
[0399] трет-Бутил (S)-(1-(диметил(оксо)-λ6-6-сульфанилиден)-4-метил-2-оксопентан-3-ил)карбамат (SJM-724-24)
[0400]

[0401] Указанное в заголовке соединение получали способом B из 4-нитрофенил (трет-бутоксикарбонил)-L-валината (SJM-724-20) (100 мг, 0,30 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, EtOAc) и перекристаллизовывали из диэтилового эфира с получением продукта в виде белого твердого вещества (58 мг, 67%). HRMS (ESI+): найдено: m/z 292,1573 (M+H)+, для C13H26NO4S+ рассчитано m/z 292,1577. 1H ЯМР (401 МГц, CDCl3) δ 5,23 (д, J=8,4 Гц, 1H), 4,50 (с, 1H), 3,94 (дд, J=8,6, 5,4 Гц, 1H), 3,42 (с, 3H), 3,39 (с, 3H), 2,10-1,99 (м, 1H), 1,43 (с, 9H), 0,94 (д, J=6,7 Гц, 3H), 0,87 (д, J=6,8 Гц, 3H). 13C ЯМР (101 МГц, CDCl3) δ 187,89 (C), 155,94 (C), 79,11 (C), 70,07 (CH), 61,89 (CH), 42,25 (CH3), 42,00 (CH3), 31,90 (CH), 28,43 (CH3), 19,60 (CH3), 17,66 (CH3). ЖХ-МС (ESI+) m/z: 291,9 (M+H)+ (85%).
[0402] трет-Бутил ((3S,4S)-1-(диметил(оксо)-λ6-6-сульфанилиден)-4-метил-2-оксогексан-3-ил)карбамат (SJM-724-92)
[0403]
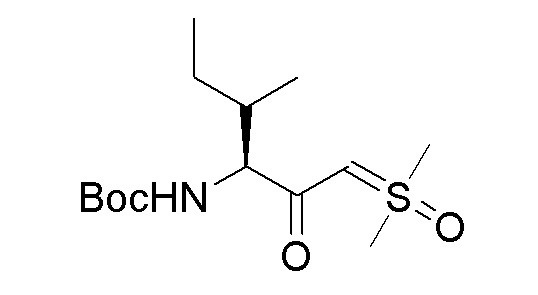
[0404] Указанное в заголовке соединение получали способом B из 4-нитрофенил (трет-бутоксикарбонил)-L-изолейцината (SJM-724-64) (200 мг, 0,57 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь EtOAc:MeOH, 95:5) с получением продукта в виде кремового твердого вещества (126 мг, 73%). HRMS (ESI+): найдено: m/z 306,1735 (M+H)+, C14H28NO4S+ рассчитано m/z 306,1734. 1H ЯМР (401 МГц, CDCl3) δ 5,21 (д, J=8,9 Гц, 1H), 4,49 (с, 1H), 3,97 (дд, J=8,7, 5,7 Гц, 1H), 3,41 (с, 3H), 3,38 (с, 3H), 1,83-1,73 (м, 1H), 1,53-1,46 (м, 1H), 1,43 (с, 9H), 1,18-1,04 (м, 1H), 0,91 (д, J=6,7 Гц, 3H), 0,90 (т, J=7,5 Гц, 3H). 13C ЯМР (101 МГц, CDCl3) δ 187,8 (C), 155,8 (C), 79,1 (C), 70,0 (CH), 61,3 (CH), 42,4 (CH3), 42,1 (CH3), 38,5 (CH), 28,5 (CH3), 24,9 (CH2), 15,9 (CH3), 11,9 (CH3). ЖХ-МС (ESI+) m/z: 305,9 (M+H)+ (100%).
[0405] трет-Бутил (S)-(1-(диметил(оксо)-λ6-6-сульфанилиден) -5-метил-2-оксогексан-3-ил)карбамат (SJM-724-96)
[0406]
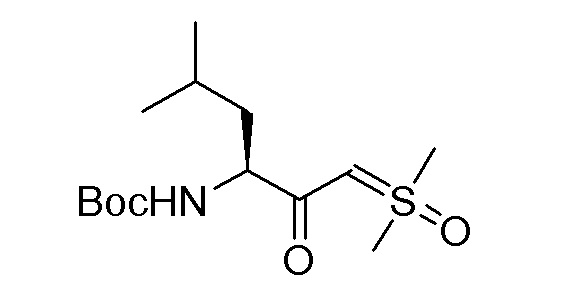
[0407] Указанное в заголовке соединение получали способом B из 4-нитрофенил (трет-бутоксикарбонил)-L-лейцината (SJM-724-76) (170 мг, 0,48 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь EtOAc:MeOH, 95:5) с получением продукта в виде белого твердого вещества (118 мг, 80%). HRMS (ESI+): найдено: m/z 306,1735 (M+H)+, C14H28NO4S+ рассчитано m/z 306,1734. 1H ЯМР (401 МГц, CDCl3) δ 5,04 (д, J=8,3 Гц, 1H), 4,51 (с, 1H), 4,16-4,06 (м, 1H), 3,41 (с, 3H), 3,38 (с, 3H), 1,75-1,62 (м, 2H), 1,62-1,50 (м, 1H), 1,43 (с, 9H), 0,94 (д, J=4,9 Гц, 3H), 0,93 (д, J=4,9 Гц, 3H). 13C ЯМР (101 МГц, CDCl3) δ 189,2 (C), 155,6 (C), 79,2 (C), 68,7 (CH), 55,6 (CH), 43,4 (CH2), 42,4 (CH3), 42,1 (CH3), 28,5 (CH3), 25,0 (CH), 23,2 (CH3), 22,3 (CH3). ЖХ-МС (ESI+) m/z: 305,9 (M+H)+ (80%).
[0408] трет-Бутил (S)-(1-(диметил(оксо)-λ6-6-сульфанилиден) -2-оксогептан-3-ил)карбамат (SJM-724-124)
[0409]
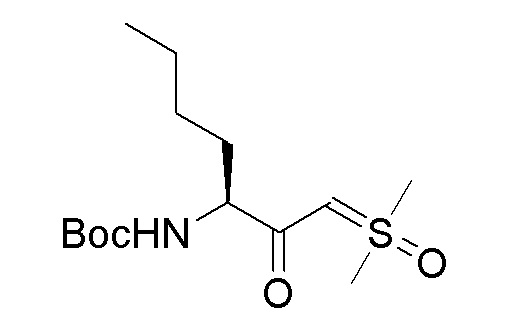
[0410] Указанное в заголовке соединение получали способом B из 4-нитрофенил (S)-2-((трет-бутоксикарбонил)амино)гексаноата (SJM-724-116) (170 мг, 0,48 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь EtOAc:MeOH, 95:5) с получением продукта в виде белого твердого вещества (128 мг, 87%). HRMS (ESI+): найдено: m/z 306,1738 (M+H)+, C14H28NO4S+ рассчитано m/z 306,1734. 1H ЯМР (401 МГц, CDCl3) δ 5,19 (д, J=8,1 Гц, 1H), 4,49 (с, 1H), 4,00 (дд, J=13,4, 7,5 Гц, 1H), 3,37 (с, 3H), 3,35 (с, 3H), 1,78-1,62 (м, 1H), 1,53-1,43 (м, 1H), 1,39 (с, 9H), 1,33-1,18 (м, 4H), 0,84 (т, J=7,0 Гц, 3H). 13C ЯМР (101 МГц, CDCl3) δ 188,6 (C), 155,6 (C), 79,1 (C), 68,9 (CH), 57,0 (CH), 42,3 (CH3), 42,0 (CH3), 33,8 (CH2), 28,4 (CH3), 27,7 (CH2), 22,6 (CH2), 14,0 (CH3). ЖХ-МС (ESI+) m/z: 306,0 (M+H)+ (100%).
[0411] трет-Бутил (S)-(4-(диметил(оксо)-λ6-6-сульфанилиден) -3-оксо-1-фенилбутан-2-ил)карбамат (SJM-724-72)
[0412]
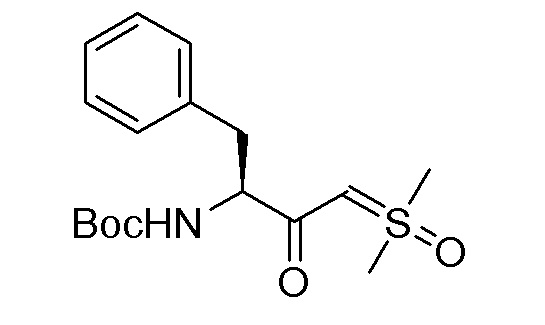
[0413] Указанное в заголовке соединение получали способом B из 4-нитрофенил (трет-бутоксикарбонил)-L-фенилаланината (SJM-724-68) (200 мг, 0,75 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, CH2Cl2) с получением продукта в виде твердого вещества бежевого цвета (141 мг, 80%). МСВР (ESI+): найдено: m/z 340,1579 (M+H)+, для C17H26NO4S+ рассчитано m/z 340,1577. 1H ЯМР (401 МГц, CDCl3) δ 7,29-7,17 (м, 5H), 5,22 (д, J=8,1 Гц, 1H), 4,32 (дд, J=14,5, 7,4 Гц, 1H), 4,26 (с, 1H) , 3,35 (с, 3H), 3,25 (с, 1H), 3,05-2,93 (м, 2H), 1,41 (с, 9H). ЖХ-МС (ESI+) m/z: 339,9 (M+H)+ (100%).
[0414] трет-Бутил (S)-(4-(диметил(оксо)-λ6-6-сульфанилиден) -1-(1H-индол-3-ил)-3-оксобутан-2-ил)карбамат (SJM-724-120)
[0415]
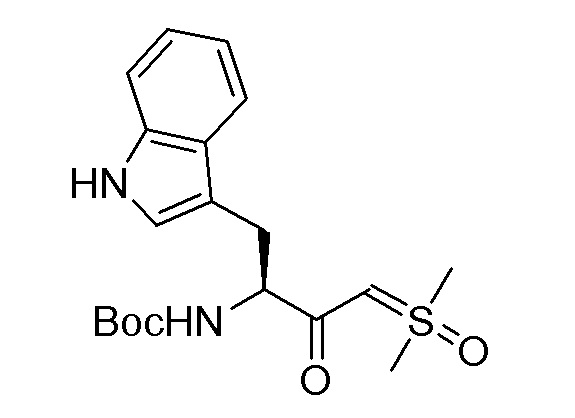
[0416] Указанное в заголовке соединение получали способом B из 4-нитрофенил (трет-бутоксикарбонил)-L-триптофаната (SJM-724-112) (170 мг, 0,40 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь EtOAc:MeOH, 95:5) с получением продукта в виде белого твердого вещества (118 мг, 78%). HRMS (ESI+): найдено: m/z 379,1697 (M+H)+, C19H27N2O4S+рассчитано m/z 379,1686. 1H ЯМР (401 МГц, CDCl3) δ 8,44 (с, 1H), 7,63 (д, J=7,9 Гц, 1H), 7,32 (д, J=8,1 Гц, 1H), 7,13 (т, J=7,3 Гц, 1H), 7,08-6,98 (м, 2H), 5,40 (д, J=7,8 Гц, 1H), 4,37 (дд, J=13,3, 7,1 Гц, 1H), 4,25 (с, 1H), 3,19 (с, 3H) , 3,26-3,09 (м, 2H), 2,99 (с, 3H), 1,43 (с, 9H). 13C ЯМР (101 МГц, CDCl3) δ 187,5 (C), 155,5 (C), 136,1 (C), 128,2 (C), 123,0 (CH), 121,9 (CH), 119,3 (CH), 119,2 (CH), 111,7 (С), 111,3 (СН), 79,4 (С), 70,0 (СН), 57,8 (СН), 41,8 (СН3), 41,6 (СН3), 29,3 (СН2), 28,54 (СН3). ЖХ-МС (ESI+) m/z: 378,9 (M+H)+ (100%).
[0417] Бензил-трет-бутил (7-(диметил(оксо)-λ6-6-сульфанилиден)-6-оксогептан-1,5-диил)(S)-дикарбамат (SJM-724-48)
[0418]
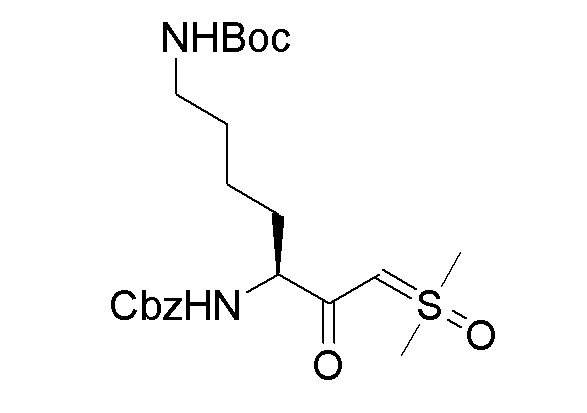
[0419] Указанное в заголовке соединение получали способом B из 4-нитрофенил-Na-((бензилокси)карбонил)-Ne-(трет-бутоксикарбонил)-L-лизината (SJM-724-40) (200 мг, 0,40 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь EtOAc:MeOH, 9:1) с получением продукта в виде белого твердого вещества (138 мг, 76%). HRMS (ESI+): найдено: m/ z 455,2216 (M+H)+, C22H35N2O6S+ требуется m/z 455,2210. 1H ЯМР (401 МГц, CDCl3) δ 7,33-7,23 (м, 5H), 5,79 (д, J=7,9 Гц, 1H), 5,04 (с, 2H), 4,72 (ш.с, 1H), 4,52 (с, 1H) , 4,07 (дд, J=13,1, 7,6 Гц, 1H), 3,32 (с, 3H), 3,30 (с, 3H), 3,09-2,97 (м, 2H), 1,79-1,67 (м, 1H), 1,59-1,50 (м, 1H), 1,50-1,26 (м, 4H), 1,38 (с, 9H). 13C ЯМР (101 МГц, CDCl3) δ 187,6 (C), 156,1 (C), 136,7 (C), 128,5 (CH), 128,1 (CH), 128,0 (CH), 78,9 (C), 69,5 (CH), 66,6 (CH2), 57,1 (CH), 42,0 (CH3), 41,8 (CH3), 40,3 (CH2), 33,4 (CH2), 29,7 (CH2), 28,4 (CH3), 22,5 (CH2). ЖХ-МС (ESI+) m/z: 454,9 (M+H)+ (100%).
[0420] трет-Бутил ((S)-1-(((S)-1-(диметил(оксо)-λ6-6-сульфанилиден)-4-метил-2-оксопентан-3-ил)амино)-1-оксо-3-фенилпропан-2-ил)карбамат (MS-4-186)
[0421]
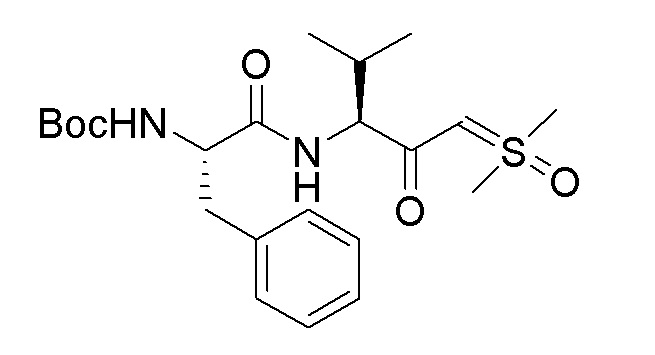
[0422] Указанное в заголовке соединение получали способом B из 4-нитрофенил (трет-бутоксикарбонил)-L-фенилаланил-L-валината (MS-4-182) (200 мг, 0,41 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, CHCl2:MeOH 98:2) с получением указанного в заголовке продукта (68 мг, 38%).
[0423] Пример 1.3: синтез и характеристика зондов на основе илида сульфоксония
[0424] sCy5-Val-SY (SJM-724-28)
[0425]
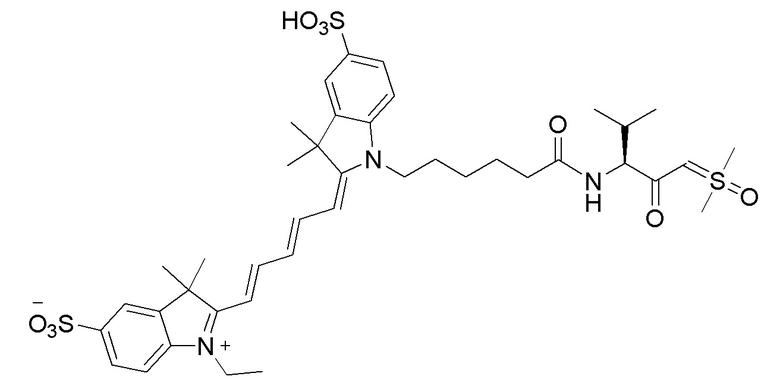
[0426] Указанное в заголовке соединение получали способом E из трет-бутил (S)-(1-(диметил(оксо)-λ6-6-сульфанилиден)-4-метил-2-оксопентан-3-ил)карбамата (SJM-724-24) (5 мг, 0,017 ммоль). Полученный сырой продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (7,9 мг, 56%). HRMS (ESI+): найдено: m/z 830,3159 (M+H)+, C41H56N3O9S3+ рассчитано m/z 830,3173.
[0427] sCy5-Ile-SY (SJM-724-104)
[0428]
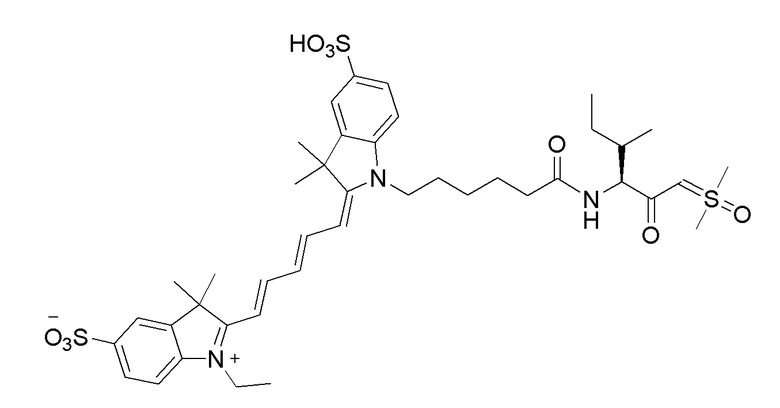
[0429] Указанное в заголовке соединение получали способом E из трет-бутил ((3S, 4S)-1-(диметил (оксо)-λ6-6-сульфанилиден)-4-метил-2-оксогексан-3-ил)карбамата (SJM-724-92) (10 мг, 0,033 ммоль). Полученный сырой продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (3 мг, 11%). HRMS (ESI+): найдено: m/z 844,3340 (M+H)+, C42H58N3O9S3+ рассчитано m/z 844,3330.
[0430] sCy5-Leu-SY (SJM-724-128)
[0431]
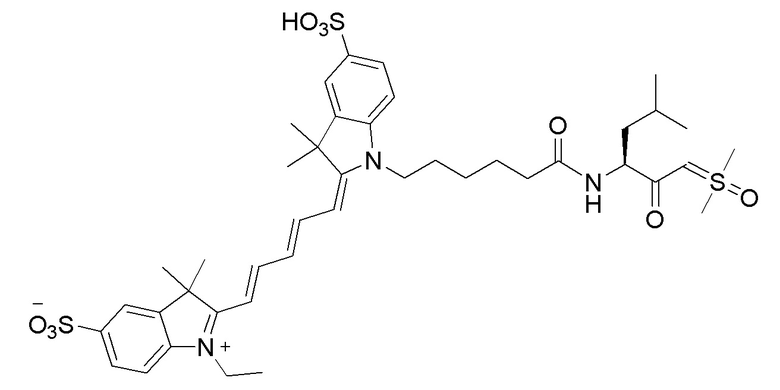
[0432] Указанное в заголовке соединение получали способом E из трет-бутил (S)-(1-(диметил(оксо)-λ6-6-сульфанилиден)-5-метил-2-оксогексан-3-ил)карбамата (SJM-724-96) (10 мг, 0,033 ммоль). Полученный сырой продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (14,7 мг, 53%). HRMS (ESI+): найдено: m/z 844,3328 (M+H)+, C42H58N3O9S3+ рассчитано m/z 844,3330.
[0433] sCy5-Nle-SY (SJM-724-132)
[0434]
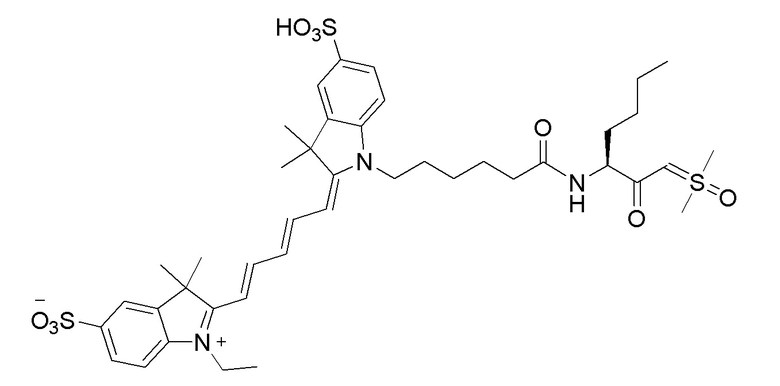
[0435] Указанное в заголовке соединение получали способом E из трет-бутил (S)-(1-(диметил(оксо)-λ6-6-сульфанилиден)-2-оксогептан-3-ил)карбамата (SJM-724-124) (10 мг, 0,033 ммоль). Полученный сырой продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (17,4 мг, 63%). HRMS (ESI+): найдено: m/z 844,3335 (M+H)+, C42H58N3O9S3+ рассчитано m/z 844,3330.
[0436] sCy5-Phe-SY (SJM-724-80)
[0437]
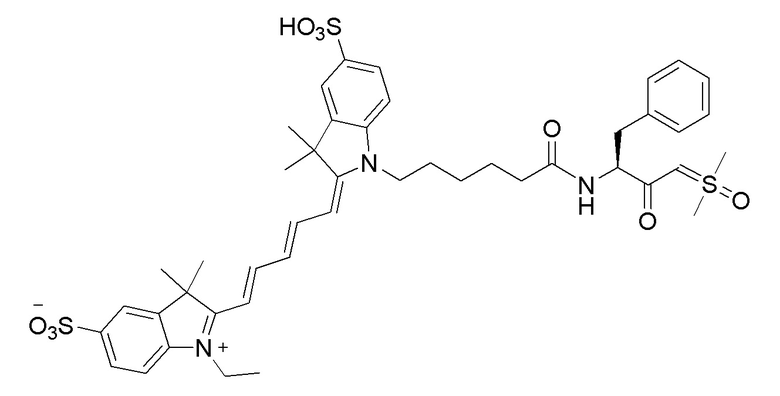
[0438] Указанное в заголовке соединение получали способом E из трет-бутил (S)-(4-(диметил(оксо)-λ6-6-сульфанилиден)-3-оксо-1-фенилбутан-2-ил)карбамата (SJM-724-72) (10 мг, 0,029 ммоль). Полученный сырой продукт очищали с помощью RP-HPLC и лиофилизировали с получением продукта в виде синего твердого вещества (13,1 мг, 51%). HRMS (ESI+): найдено: m/z 878,3157 (M+H)+, C45H56N3O9S3+ рассчитано m/z 878,3173.
[0439] sCy5-Trp-SY (SJM-724-80)
[0440]
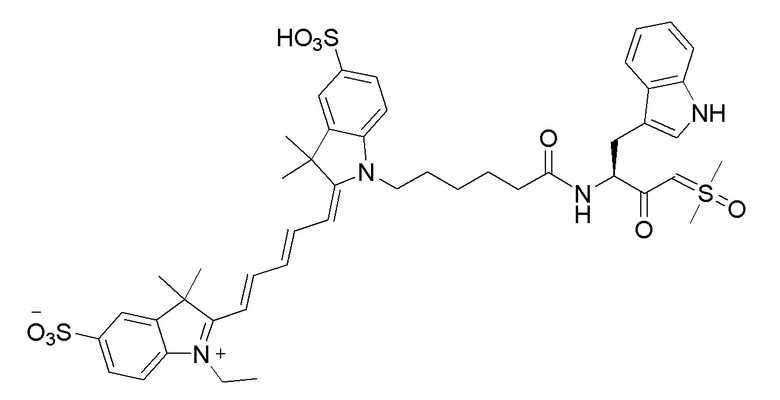
[0441] Указанное в заголовке соединение получали способом E из трет-бутил (S)-(4-(диметил(оксо)-λ6-6-сульфанилиден)-1-(1H-индол-3-ил)-3-оксобутан-2-ила))карбамата (SJM-724-120) (10 мг, 0,026 ммоль). Полученный неочищенный продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (6 мг, 25 HRMS (ESI+): найдено: 917,3277 (M+H)+, C47H57N4O9S3+ рассчитано m/z 917,3282.
[0442] Cbz-Lys(sCy5)-SY (SJM-724-100)
[0443]
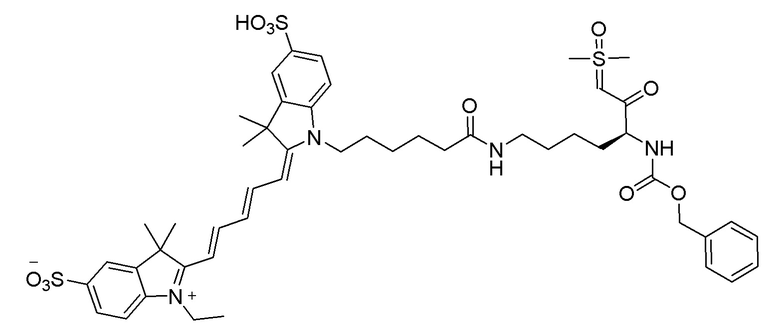
[0444] Указанное в заголовке соединение получали способом E из бензил трет-бутил(7-(диметил(оксо)-λ6-6-сульфанилиден)-6-оксогептан-1,5-диил)(S)-дикарбамата (SJM-724-48) (10 мг, 0,022 ммоль). Полученный сырой продукт очищали с помощью RP-HPLC и лиофилизировали с получением продукта в виде синего твердого вещества (10 мг, 46%). HRMS (ESI+): найдено: 993,3785 (M+H)+, C50H65N4O11S3+ рассчитано m/z 993,3806.
[0445] sCy5-Phe-Val-SY (MS-4-191)
[0446]
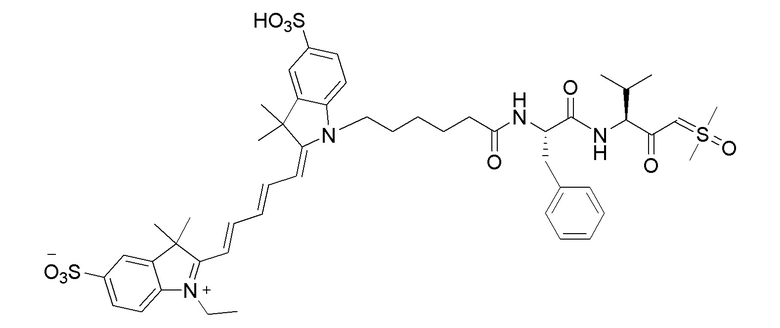
[0447] Указанное в заголовке соединение получали способом E из трет-бутил ((S)-1-(((S)-1-(диметил(оксо)-λ6-6-сульфанилиден) -4-метил-2-оксопентан-3-ила)амино)-1-оксо-3-фенилпропан-2-ил) карбамата (MS-4-186) (10 мг, 0,022 ммоль). Полученный сырой продукт очищали с помощью RP-HPLC и лиофилизировали с получением продукта в виде синего твердого вещества (4,6 мг, 21%).
[0448] Пример 2: синтез ацилоксиметилкетонов (АОМК)
Соединения, имеющие активную ацилоксиметилкетоновую группу (AOMK) (зонды sCy5-AA-AOMK), синтезировали согласно схеме реакций 2 и в соответствии с общими способами C, D и E, описанными ниже.
[0450]
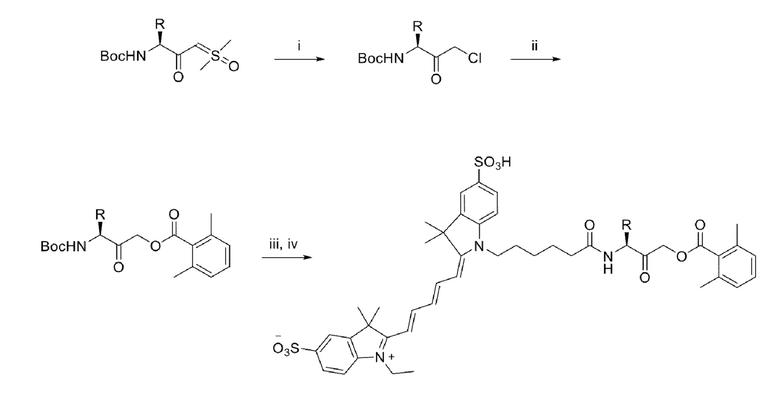
Схема 2. Синтез зондов sCy5-AA-AOMK через промежуточный илид сульфоксония. i) 4M HCl в диоксане, ТГФ, кипячение с обратным холодильником, 4 ч. ii) 2,6-диметилбензойная кислота, KF, ДМФА, комнатная температура, 18 ч. iii) TFA/CH2Cl2 (1:1), iv) сульфо-Cy5, PyClock, DIPEA, DMF, комнатная температура, 18 ч.
[0451] Общий способ C. Получение хлорметилкетонов
К раствору илида сульфоксония (1 экв) в сухом ТГФ (5 мл) добавляли 4 М HCl в диоксане (1,15 экв). Раствор перемешивали при кипячении с обратным холодильником в течение 4 ч. Растворители удаляли в вакууме, и остаток обрабатывали EtOAc (20 мл) и промывали H2O (15 мл) и насыщенным раствором NaHCO3 (15 мл). Органический слой сушили (MgSO4), фильтровали и концентрировали в вакууме с получением сырого продукта.
[0452] Общий способл D. Получение ацилоксиметилкетонов (АОМК)
Фторид калия (3 экв) суспендировали в ДМФА (1 мл) и обрабатывали ультразвуком в течение 1 мин. К суспензии добавляли 2,6-диметилбензойную кислоту (1,1 экв) и перемешивали при температуре окружающей среды в течение 5 мин. Добавляли хлорметилкетон (1 экв) и смесь перемешивали при температуре окружающей среды в течение 18 ч. ДМФА удаляли в вакууме, и полученный остаток обрабатывали EtOAc (20 мл) и промывали насыщенным раствором NaHCO3 (15 мл). Органический слой сушили (MgSO4), фильтровали и растворитель удаляли в вакууме с получением сырого продукта.
[0453] Общий способ E: мечение ацилоксиметилкетонов сульфо-цианином 5 (AOMK)
Boc-защищенный ацилоксиметилкетон (AOMK) (1 экв) обрабатывали смесью 1:1 ТФК и CH2Cl2 (2 мл) и перемешивали при температуре окружающей среды в течение 1 ч. Летучие компоненты удаляли в токе азота. К полученному остатку добавляли ДМФА (300 мкл) и DIPEA (4 экв). Отдельно Sulfo-Cy5 (1 экв) и PyClock (2 экв.) растворяли в ДМФА (300 мкл) и DIPEA (4 экв) и перемешивали в течение 2 мин перед добавлением к вышеуказанному раствору. Реакционную смесь перемешивали при температуре окружающей среды 18 ч темноте.
[0454] Пример 2.1: синтез и характеристика промежуточных хлорметилкетонов
[0455] трет-Бутил (S)-(1-хлор-2-оксогептан-3-ил)карбамат (SJM-724-148)
[0456]
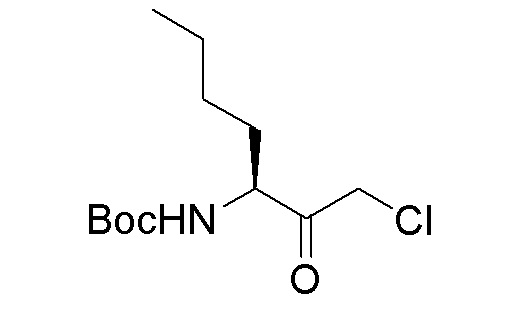
[0457] Указанное в заголовке соединение получали способом C из трет-бутил (S)-(1-(диметил(оксо)-λ6-6-сульфанилиден)-2-оксогептан-3-ил)карбамата (SJM-724-124) (40 мг, 0,13 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, петролейный спирт:EtOAc, 9:1) с получением продукта в виде белого твердого вещества (20 мг, 58%). 1H ЯМР (401 МГц, CDCl3) δ 5,02 (д, J=6,4 Гц, 1H), 4,47 (дд, J=12,6, 7,7 Гц, 1H), 4,26 (д, J=4,8 Гц, 2H), 1,92-1,75 (м, 1H), 1,60-1,47 (м, 1H), 1,43 (с, 9H), 1,39-1,25 (м, 4H), 0,90 (т, J=7,1 Гц, 3H). 13C ЯМР (101 МГц, CDCl3) δ 202,0 (C), 155,6 (C), 80,4 (C), 57,5 (CH), 46,8 (CH2), 31,3 (CH2), 28,4 (CH3), 27,6 (CH2), 22,5 (CH2), 13,9 (CH3). ЖХ-МС (ESI+) m/z: 164,1,0 (M - Boc+H)+ (100%).
[0458] трет-Бутил (S)-(4-хлор-3-оксо-1-фенилбутан-2-ил) карбамат (SJM-724-152)
[0459]
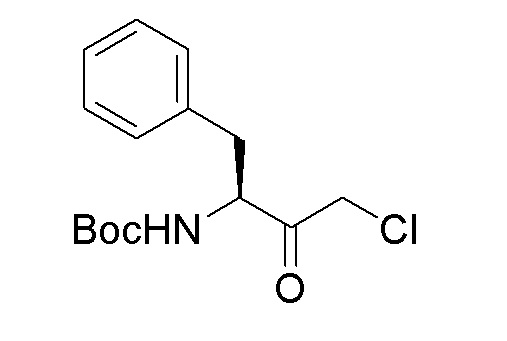
[0460] Указанное в заголовке соединение получали способом C из трет-бутил (S)-(4-(диметил(оксо)-λ6-6-сульфанилиден)-3-оксо-1-фенилбутан-2-ил)карбамата (SJM-724-72) (50 мг, 0,15 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь петролейный спирт:EtOAc, 9:1) с получением продукта в виде белого твердого вещества (30 мг, 68%). МСВР (ESI+): найдено: m/z 320,1018 (M+Na)+, C15H20ClNNaO3+ рассчитано m/z 320,1024. 1H ЯМР (401 МГц, CDCl3) δ 7,35-7,23 (м, 3H), 7,19-7,13 (м, 2H), 5,06 (д, J=5,7 Гц, 1H), 4,66 (дд, J=13,0, 6,0 Гц, 1H), 4,17 (д, J=16,2 Гц, 1H), 3,98 (д, J=16,2 Гц, 1H), 3,08 (дд, J=13,8, 6,7 Гц, 1H), 2,99 (дд, J=13,4, 7,1 Гц, 1H), 1,40 (с, 9H). 13C ЯМР (101 МГц, CDCl3) δ 201,5 (C), 155,3 (C), 135,7 (C), 129,3 (CH), 129,1 (CH), 127,5 (CH), 80,6 (C), 58,6 (CH), 47,6 (CH2), 37,8 (CH2), 28,4 (CH3). ЖХ-МС (ESI+) m/z: 198,0 (M - Boc+H)+ (100%).
[0461] Бензил трет-бутил(7-хлор-6-оксогептан-1,5-диил)(S)-дикарбамат (SJM-724-52)
[0462]

[0463] Указанное в заголовке соединение получали способом C из бензил трет-бутил(7-(диметил(оксо)-λ6-6-сульфанилиден)-6-оксогептан-1,5-диил) (S)-дикарбамата (SJM-724-48) (130 мг, 0,29 ммоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь петролейный спирт:EtOAc, 3:1) с получением продукта в виде белого твердого вещества (60 мг, 51%). HRMS (ESI+): найдено: 435,1664 (M+Na)+, C20H29ClN2NaO5+ рассчитано m/z 435,1657. 1H ЯМР (401 МГц, CDCl3) δ 7,38-7,27 (м, 5H), 5,68 (д, J=5,7 Гц, 1H), 5,09 (с, 2H), 4,62 (с, 1H), 4,59-4,47 (м, 1H), 4,26 (д, J=2,1 Гц, 2H), 3,16-3,00 (м, 2H), 1,92-1,81 (м, 1H), 1,70-1,57 (м, 1H), 1,54-1,27 (м, 4H), 1,40 (с, 9H). 13C ЯМР (101 МГц, CDCl3) δ 201,6 (C), 156,4 (C), 136,1 (C), 128,7 (CH), 128,4 (CH), 128,3 (CH), 79,4 (C), 67,3 (CH2), 57,9 (CH), 46,6 (CH2), 39,6 (CH2), 30,8 (CH2), 29,8 (CH2), 28,5 (CH3), 22,2 (CH2). ЖХ-МС (ESI+) m/z: 434,9,0 (M+Na)+ (100%).
[0464] Пример 2.2: синтез и характеристика ацилоксиметилкетонов (АОМК)
[0465] (S)-3-((трет-бутоксикарбонил)амино)-2-оксогептил 2,6-диметилбензоат (SJM-724-156)
[0466]
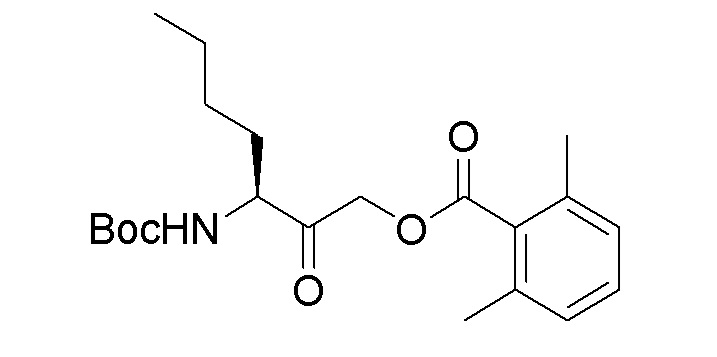
[0467] Указанное в заголовке соединение получали способом D из трет-бутил (S)-(1-хлор-2-оксогептан-3-ил)карбамата (SJM-724-148) (20 мг, 76 мкмоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь петролейный спирт: EtOAc, 95:5) с получением продукта в виде белого твердого вещества (18 мг, 63%). МСВР (ESI+): найдено: m/z 400,2097 (M+Na)+, для C21H31NNaO5+ рассчитано m/z 400,2094. 1H ЯМР (401 МГц, CDCl3) δ 7,23-7,17 (м, 1H), 7,04 (д, J=7,8 Гц, 2H), 5,15-4,96 (м, 3H), 4,40 (дд, J=12,5, 7,7 Гц, 1H), 2,39 (с, 6H), 1,97-1,86 (м, 1H), 1,67-1,54 (м, 1H), 1,45 (с, 9H), 1,41-1,30 (м, 4H), 0,94-0,88 (м, 3H). 13C ЯМР (101 МГц, CDCl3) δ 202,8 (C), 169,1 (C), 155,7 (C), 135,8 (C), 132,7 (C), 129,8 (CH), 127,8 (CH), 80,4 (C), 66,9 (CH2), 57,0 (CH), 31,4 (CH2), 28,4 (CH3), 27,4 (CH2), 22,5 (CH2), 20,0 (CH3), 14,0 (CH3). ЖХ-МС (ESI+) m/z: 399,9 (M+Na) + (100%).
[0468] (S)-3-((трет-бутоксикарбонил)амино)-2-оксо-4-фенилбутил 2,6-диметилбензоат (SJM-724-172)
[0469]
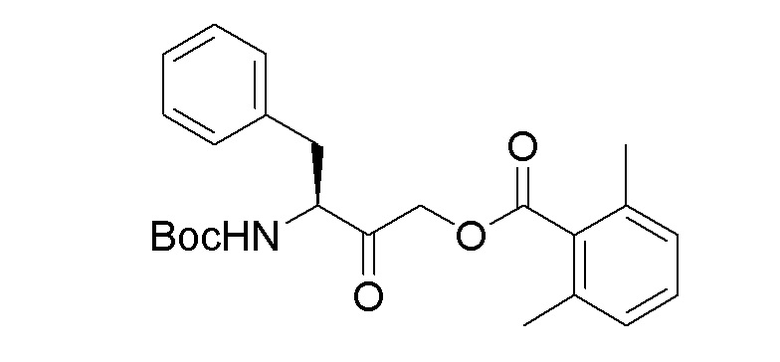
[0470] Указанное в заголовке соединение получали способом D из трет-бутил (S)-(4-хлор-3-оксо-1-фенилбутан-2-ил)карбамата (SJM-724-152) (25 мг, 84 мкмоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь петролейный спирт: EtOAc, 95:5) с получением продукта в виде белого твердого вещества (27 мг, 78%). HRMS (ESI+): найдено: 434,1944 (M+Na)+, C24H29NNaO5+ рассчитано m/z 434,1938. 1H ЯМР (401 МГц, CDCl3) δ 7,35-7,18 (м, 6H), 7,05 (д, J=7,6 Гц, 2H), 5,06 (д, J=7,3 Гц, 1H), 4,94 (дд, J=43,1, 17,0 Гц, 2H), 4,62 (дд, J=14,0, 7,0 Гц, 1H), 3,18 (дд, J=14,0, 6,4 Гц, 1H), 3,04 (дд, J=14,0, 7,2 Гц, 1H), 2,39 (с, 6H), 1,42 (с, 9H). 13C ЯМР (101 МГц, CDCl3) δ 202,2 (C), 169,1 (C), 155,4 (C), 135,9 (C), 135,8 (C), 132,7 (C), 129,8 (CH), 129,5 (CH), 128,9 (CH), 127,8 (CH), 127,3 (CH), 80,5 (C), 67,3 (CH2), 58,1 (CH), 37,5 (CH2), 28,4 (CH3), 20,0 (CH3). ЖХ-МС (ESI+) m/z: 433,8 (M+Na)+ (100%).
[0471] (S)-3-(((бензилокси)карбонил)амино)-7-((трет-бутоксикарбонил)амино)-2-оксогептил 2,6-диметилбензоат (SJM-724-176)
[0472]
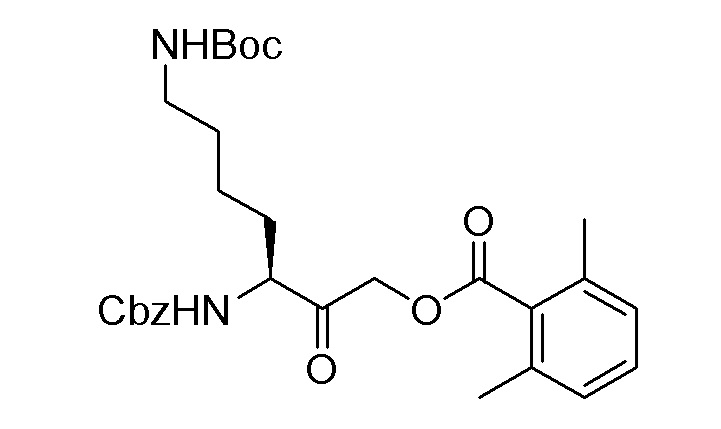
[0473] Указанное в заголовке соединение получали способом D из бензил трет-бутил(7-хлор-6-оксогептан-1,5-диил)(S)-дикарбамата (SJM-724-52) (50 мг, 121 мкмоль). Полученный сырой продукт очищали колоночной хроматографией (SiO2, смесь петролейный спирт:EtOAc, 3:1) с получением продукта в виде белого твердого вещества (57 мг, 89%). HRMS (ESI+): найдено: 549,2571 (M+Na)+, C29H38N2NaO7+ рассчитано m/z 549,2571. 1H ЯМР (401 МГц, CDCl3) δ 7,38-7,29 (м, 5H), 7,23-7,17 (м, 1H), 7,04 (д, J=7,5 Гц, 2H), 5,66 (д, J=5,9 Гц, 1H) , 5,11 (с, 2H), 5,12-4,95 (м, 2H), 4,65 (с, 1H), 4,52-4,41 (м, 1H), 3,18-3,00 (м, 2H), 2,39 (с, 6H), 2,04-1,89 (м, 1H), 1,78-1,64 (м, 1H), 1,58-1,35 (м, 4H), 1,41 (с, 9H). 13C ЯМР (101 МГц, CDCl3) δ 202,3 (C), 169,1 (C), 156,4 (C), 136,2 (C), 135,8 (C), 132,5 (C), 129,9 (CH), 128,7 (CH), 128,4 (CH), 128,3 (CH), 127,8 (CH), 79,3 (C), 67,3 (CH2), 66,8 (CH2), 57,5 (CH), 39,7 (CH2), 30,9 (CH2), 29,8 (CH2), 28,5 (CH3), 22,0 (CH2), 20,0 (CH3). ЖХ-МС (ESI+) m/z: 426,9 (M-Boc+H)+ (100%).
[0474] Пример 2.3: синтез и характеристика зондов на основе ацилоксиметилкетона (АОМК)
[0475] sCy5-Nle-AOMK (SJM-724-160)
[0476]
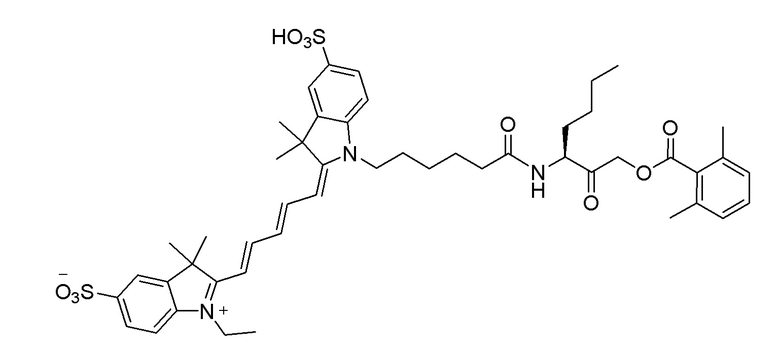
[0477] Указанное в заголовке соединение получали способом E из (S)-3-((трет-бутоксикарбонил)амино)-2-оксогептил-2,6-диметилбензоата (SJM-724-156) (8 мг, 21 мкмоль). Полученный сырой продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (13,9 мг, 72%). HRMS (ESI+): найдено: 916,3869 (M+H)+, C49H62N3O10S2+ рассчитано m/z 916,3871.
[0478] sCy5-Phe-AOMK (SJM-724-180)
[0479]
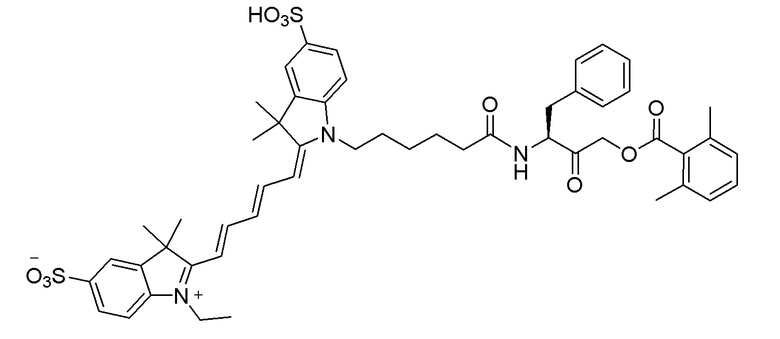
[0480] Указанное в заголовке соединение получали способом E из (S)-3-((трет-бутоксикарбонил)амино)-2-оксо-4-фенилбутил 2,6-диметилбензоата (SJM-724-172) (5 мг, 12 мкмоль). Полученный сырой продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (6,5 мг, 56%). HRMS (ESI+): найдено: 950,3718 (M+H)+, для C52H60N3O10S2+ рассчитано m/z 950,3715.
[0481] Cbz-Lys(sCy5)-AOMK (SJM-724-184)
[0482]
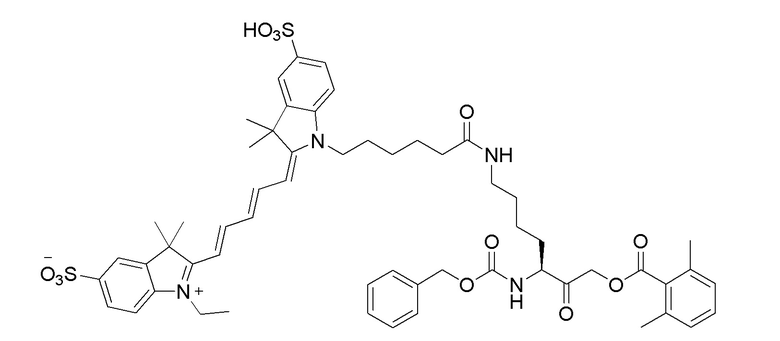
[0483] Указанное в заголовке соединение получали способом E из (S)-3-((((бензилокси)карбонил)амино)-7-((трет-бутоксикарбонил)амино)-2-оксогептил 2,6-диметилбензоата (SJM-724-176) (5 мг, 9 мкмоль). Полученный сырой продукт очищали с помощью ОФ-ВЭЖХ и лиофилизировали с получением продукта в виде синего твердого вещества (6,5 мг, 64%). HRMS (ESI+): найдено: 1065,4351 (M+H)+, C57H69N4O12S2+ рассчитано m/z 1065,4348.
[0484] II. Тестирование зондов
[0485] Общая информация
[0486] Способы
[0487] Таблица основных материалов
[0488] Экспериментальная модель и детали объектов исследования
[0489] Культивирование клеток
Клетки RAW264.7 или MDA-MB-231HM культивировали в среде DMEM, содержащей 10% фетальной бычьей сыворотки и 1% антибиотика/антимикотика. Клетки RAW264.7 пассировали снятием резиновым скребком, в то время как клетки MDA-MB-231HM культивировали с 0,02% ЭДТА в забуференном фосфатом физиологическом растворе (PBS).
[0490] Животные
Все эксперименты с участием животных были одобрены Комитетом по этике животных Университета Монаша. Самцов мышей C57BL/6J получали из питомника Monash Animal Research Platform и использовали в возрасте 8-10 недель. Быстро замороженные селезенки мышей дикого типа и мышей с нокаутом гена катепсина X, как описано в Sevenich et al., 2010, получали из Университета Калгари в соответствии с требованиями Комитета по уходу и использованию животных Университета Калгари.
[0491] Детали метода
[0492] Мечение клеточного лизата и анализ SDS-PAGE
Клетки собирали соскабливанием, один раз промывали PBS и ресуспендировали в буфере для лизиса, содержащем 50 мМ цитрат [pH 5,5], 0,5% CHAPS, 0,1% Triton X-100 и 4 мМ DTT. Клетки инкубировали на льду в течение не менее 10 мин с периодическим встряхиванием с последующим центрифугированием (21× g при 4°C в течение 5 мин). Затем очищенные супернатанты переносили в другую пробирку и определяли концентрацию белка с использованием метода BCA. Общий белок (50 мкг) аликвотировали в пробирки в конечном объеме 20 мкл буфера для лизиса. Там, где указано, JPM-OEt или MDV-590 добавляли из 100× стокового раствора в ДМСО и инкубировали при 37°C в течение 20 мин перед внесением зонда. Зонда в указанной концентрации вносили из 100× стокового раствора в ДМСО. Мечение проводили при 37°C в течение 20 мин (если не указано иное), и реакции гасили добавлением 5× буфера для образцов (200 мМ Трис-Cl [pH 6,8], 8% SDS, 0,04% бромфенолового синего, 5% b-меркаптоэтанола и 40% глицерина). Затем образцы кипятили в течение пяти минут, и белки разделялись на 15% геле SDS-PAGE. Гели сканировали на планшетном лазерном сканере Typhoon 5 при волне возбуждения/эмиссии 633/670 нм для детектирования флуоресценции sCy5.
[0493] Мечение живых клеток
Клетки RAW или клетки MDA-MB-231HM высевали в 12-луночные планшеты. Где указано, MDV-590 или носитель добавляли в концентрации 10 мкМ из 10 мМ ДМСО для инкубации в течение ночи. Когда плотность клеток достигала 80%, указанные зонды добавляли в указанных концентрациях из 1000× стокового раствора в ДМСО и инкубировали в течение указанного периода времени. Затем среду удаляли и заменяли PBS. Затем клетки соскребали и переносили в пробирки, и лизис и анализ SDS-PAGE проводили, как указано выше, за исключением пропуска стадии добавления зонда.
[0494] Анализ тканей
Ткани отбирали у здоровых мышей и мгновенно замораживали. Во время анализа добавляли буфер для лизиса в соотношении 10× объем:масса, и ткани обрабатывали ультразвуком на льду. Очищенные лизаты метили указанным зондом и анализировали, как описано выше.
[0495] Для тканей, меченных in vivo, мышам сначала вводили внутривенно через хвостовую вену sCy5-Nle-SY, BMV109 или sCy5-Nle-AOMK (50 нмоль в 100 мкл 10% ДМСО/PBS или контрольный носитель). Ткани собирали и анализировали, как указано выше, за исключением того, что дополнительное добавление зонда не производилось.
[0496] Анализ иммунопреципитацией
Меченный зондом лизат, указанный выше (в буфере для образца), разделяли на входной или преципитированый (по 50 мкг общего белка в каждом случан). Входной образец хранили при -20°C. Преципитированный образец разбавляли 500 мкл буфера IP (PBS [pH 7,4], 0,5% NP-40, 1 мМ EDTA). Козье антитело против катепсина X (10 мкл) добавляли вместе с 40 мкл суспензии предварительно промытых гранул агарозы с белком A/G. Образцы вращали в течение ночи при 4°C. Затем гранулы промывали четыре раза IP-буфером с последующей последней промывкой 0,9% NaCl. Затем гранулы ресуспендировали в 2-кратном буфере для образцов и кипятили. Преципитированные супернатанты вместе с входными образцами анализировали с помощью флуоресцентного SDS-PAGE, как указано выше.
[0497] Конфокальная микроскопия
Ткани почек мышей, которым вводили sCy5-Nle-SY (или контрольный носитель), как описано выше, фиксировали в течение ночи в 4% параформальдегиде в PBS с последующей криопротектированием в течение ночи в 30% сахарозе. Ткани помещали в OCT, замораживали на сухом льду и готовили срезы толщиной 10 мкм. Иммуноокрашивание на катепсин X проводили по стандартным протоколам. Вкратце, срезы сушили на воздухе, фиксировали в холодном ацетоне в течение 10 минут, снова сушили на воздухе и затем регидратировали в PBS. Срезы блокировали в PBS, содержащем 3% нормальной лошадиной сыворотки с 0,1% Triton X-100. Козий анти-катепсин X добавляли в блокирующем буфере в соотношении 1: 100 в течение ночи при 4°C. Затем срезы промывали и добавляли вторичное антитело осла против козьего AlexaFluor594 в соотношении 1:500 в течение 1 ч при комнатной температуре. Срезы окрашивали DAPI в течение 5 мин, промывали и обрабатывали монтирующей средой ProLong Diamond. Окрашивание анализировали с помощью инвертированного конфокального микроскопа Leica SP8.
[0498] Пример
3 - Мечение sCy5-Val-SY в клеточных лизатах
[0494] В примере 3 зонд на основе илида сульфоксония sCy5-Val-SY инкубировали с белковыми лизатами, полученными из клеток RAW264.7, иммортализованной линии макрофагов мыши, которая содержит высокие уровни активных цистеиновых катепсинов (Verdoes et al., 2013). Клетки лизировали в цитратном буфере (pH 5,5), чтобы обеспечить оптимальные условия для активации катепсина, и добавляли зонд.
- при 1 мкМ в течение 20 мин,
- в различных концентрациях (0 мкМ, 0,01 мкМ, 0,05 мкМ, 0,1 мкМ, 0,5 мкМ или 1 мкМ) в течение 20 мин; или
- при 1 мкМ в течение разного периода времени (0, 1, 2, 5, 10, 20 и 30 мин).
[0500] Затем лизаты разделяли с помощью SDS-PAGE и гель сканировали на флуоресценцию sCy5 с использованием планшетного лазерного сканера. Наблюдали исключительное, зависящее от концентрации и времени, мечение протеазы с молекулярной массой примерно 35 кДа (фиг. 2A, фиг. 2A-1 и фиг. 2A-2). Данное мечение предотвращалось предварительной обработкой лизатов JPM-OEt, ингибитором панцистеинового катепсина, подтверждая, что эта протеаза была членом семейства цистеиновых катепсинов (фиг. 2А). Напротив, MDV-590 - специфический ингибитор катепсина S - не конкурировал за связывание sCy5-Val-SY.
[0501] Профиль мечения sCy5-Val-SY сравнивали с профилем для BMV109, панзонда для катепсинов, повторяя вышеописанный эксперимент с использованием BMV109 в качестве зонда, добавленного в концентрации 1 мкМ в течение 20 мин. Было обнаружено, что меченная sCy5-Val-SY протеаза имеет такую же молекулярную массу, что и меченный BMV109 катепсин X (Verdoes et al., 2013). Было подтверждено, что эта протеаза действительно является катепсином X, с использованием иммунопреципитации лизатов, меченных sCy5-Val-SY (sCy5-Val-SY добавлен в концентрации 1 мкМ в течение 20 мин), с помощью антитела, специфичного к катепсину X (фиг. 2B).
[0502] Пример
4 - Мечение sCy5-Val-SY в лизатах тканей
В примере 4 тестировали способность sCy5-Val-SY метить катепсин X в лизатах селезенки мышей (от мышей дикого типа или мышей с дефицитом катепсина X) (добавление зонда при 1 мкМ в течение 20 мин). Как наблюдали в лизатах макрофагов, зонд проявлял исключительную реактивность с катепсином X в лизатах селезенки мышей дикого типа, и это мечение отсутствовало в лизатах, приготовленных из селезенки мышей с дефицитом катепсина X (фиг. 2C). Для сравнения, BMV109 (добавленный в дозе 1 мкМ в течение 20 мин) сильно метил катепсин B и, в меньшей степени, катепсин S и L (фиг. 2C).
[0504] Таким образом, результаты примеров 3 и 4 демонстрируют исключительную специфичность sCy5-Val-SY в лизатах клеток и тканей.
[0505] Пример
5 - Мечение sCy5-Val-SY в живых клетках
[0506] В примере 5 оценивали проницаемость зонда sCy5-Val-SY и профиль его специфичности в живых клетках RAW264.7 и сравнивали с зондом BMV109. После инкубации зонда (при 1 мкМ) с живыми клетками в течение возрастающего периода времени (0, 1, 5, 10, 15, 25, 35, 45, 55, 65, 90 и 120 мин) или при увеличении концентрации зонда (0 мкМ, 0,01 мкМ, 0,05 мкМ, 0,1 мкМ, 0,5 мкМ и 1 мкМ каждый в течение 2 ч), лизаты анализировали измерением флуоресценции в геле, как указано выше. Здесь наблюдали зависящее от времени и концентрации мечение двух протеаз (рис. 2D, рис. 2D-1). Последние были идентифицированы как катепсин X и S посредством иммунопреципитации (фиг. 2E) и конкуренции с MDV-590 (фиг. 2F) соответственно.
[0507] Было удивительно обнаружить, что мечение катепсина S в живых клетках, учитывая отсутствие у него связывания с sCy5-Val-SY в клеточных лизатах, где с помощью зонда BMV109 были подтверждены высокие уровни активности катепсина S. Полученные данные дают основание предположить, что реакционная способность катепсина S с зондом на основе илида сульфоксония зависит от условий мечения. Была предпринята попытка исследовать это, лизируя клетки в различных буферах, которые могли бы имитировать эндосомную среду катепсина S, но мечение катепсина S в лизатах не увеличивалось (результаты не показаны).
[0508] Тем не менее, зонд на основе илида сульфоксония продемонстрировал четкое мечение катепсина X в лизатах и живых клетках со значительно улучшенной селективностью по сравнению с BMV109 (фиг. 2D, F). Насколько нам известно, зонд на основе илида сульфоксония является первым ковалентным ABP для катепсина X, который также не связывается с катепсином B или L. Как видно на фиг. 2A, 2C, 2D и 2F, трудно определить отличить мечение катепсина X от катепсина B с помощью BMV109 из-за сходства по размеру двух протеаз. Однако sCy5-Val-SY позволяет четко определить активность катепсина X.
[0509] Пример
6 - Мечение зондами на основе илида сульфоксония в клеточных лизатах
[0510] В примере 6 небольшую библиотеку зондов сульфоксоний-илида с различными аминокислотами в положении P1, приготовленную в соответствии с примером 1, тестировали в лизатах RAW264.7 и сравнивали с BMV109. В каждый зонд добавляли увеличивающиеся концентрации зонда (0,01 мкМ, 0,05 мкМ, 0,1 мкМ, 0,5 мкМ, 1 мкМ и 5 мкМ в течение 20 мин).
[0511] В лизатах клеток RAW264.7 все зонды, несущие Ile, Leu, Nle и Phe, показали сходную специфичность к катепсину X с sCy5-Val-SY, где sCy5-Nle-SY был наиболее активным (фиг. 3A). Зонд, несущий Cbz-Lys, в котором sCy5 был присоединен через боковую цепь лизина, демонстрировал потерю специфичности, отдавая предпочтение катепсину S над катепсином X и B. sCy5-Phe-Val-SY, в который был включен остаток P2 Phe, также демонстрируют потерю специфичности (фиг. 3A, фиг. 7). Профиль мечения этого зонда был подобен BMV109, хотя он показал улучшенную активность для катепсина X и S по сравнению с BMV109.
[0512] Пример
[0513] 7 - Мечение зондами на основе илида сульфоксония в лизатах почек
[0513] В примере 7 зонды на основе илида сульфоксония, полученные в соответствии с примером 1, тестировали в лизатах почек, и результаты сравнивали с BMV109. К каждому зонду сульфоксония-илида (и BMV109) добавляли возрастающие концентрации зонда 0,1 мкМ, 0,5 мкМ, 1 мкМ и 5 мкМ в течение 20 мин.
[0514] В лизатах почек Leu и Nle обладали наибольшей эффективностью и специфичностью в отношении катепсина X, где Cbz-Lys, Phe и Phe-Val давали более широкую реактивность, и Val и Ile проявляли более низкое мечение (фиг. 3B, фиг. 7).
[0515] Пример
8 - Мечение зондами на основе илида сульфоксония в живых клетках RAW264.7
[0516] В примере 8 зонды на основе илида сульфоксония, полученные в соответствии с примером 1, применяли к живым клеткам RAW264.7 на два часа, чтобы исследовать эффективность и проницаемость серии зондов на основе илида сульфоксония в живых клетках, и результаты сравнивали с BMV109.
[0517] К каждому зонду на основе илида сульфоксония (и BMV109) добавляли возрастающую концентрации зонда 0,1 мкМ, 0,5 мкМ, 1 мкМ и 5 мкМ на 2 ч.
[0518] Зонды, содержащие Trp, Val, Ile, Leu, Nle и Phe, помеченные катепсином X и S в аналогичной степени и с аналогичной эффективностью, в то время как Cbz-Lys продемонстрировал предпочтение катепсина S и Phe-Val меченного катепсина B и L в дополнение к катепсину X и S (фиг. 3C, фиг. 7).
[0519] Пример
9 - Мечение зондами на основе илида сульфоксония в живых клетках MDA-MB-231HM
[0520] В примере 9 тестировали специфичность зондов на основе илида сульфоксония для катепсина X в линии рака молочной железы человека, которая, как известно, экспрессирует очень низкие уровни катепсина S, MDA-MB-231HM (Chang et al., 2007), и результаты сравнивали с BMV109. Клетки MDA-MB-231HM также позволили проверить, могут ли зонды сульфоксония-илида связываться с катепсином X человека (в дополнение к мышиному катепсину X, показанному ранее).
[0521] Каждый зонд на основе илида сульфоксония (и BMV109) добавляли с увеличивающимися концентрациями зонда (0,1 мкМ, 0,5 мкМ, 1 мкМ и 5 мкМ).
[0522] Когда зонды инкубировали с клетками MDA-MB-231 в течение более коротких периодов времени, наблюдалось очень слабое мечение катепсина X (результаты не показаны). Однако после инкубации в течение ночи наблюдалась четкая маркировка (фиг. 3D). Это, вероятно, отражает различия в скорости эндоцитоза между макрофагами и опухолевыми клетками и предполагает, что зонды могут попадать непосредственно в эндолизосмальный путь, а не за счет диффузии через мембраны. Серия зондов сульфоксония-илида обычно показывала специфическое мечение катепсина X в этих клетках с минимальной перекрестной реактивностью, возникающей только при 5 мкМ. sCy5-Lys-SY и особенно sCy5-Phe-Val-SY показали наибольшую перекрестную реактивность с катепсином B и L.
[0523] Пример
10 - Характеристика sCy5-Nle-SY in vivo
[0524] Принимая во внимание все данные, полученные на клеточных и тканевых лизатах, живых макрофагах мыши и раковых клетках человека, зонд на основе илида сульфоксония sCy5-Nle-SY оказался зондом, демонстрирующим наиболее высокую эффективность и селективность в отношении катепсина X. Таким образом, этот зонд был выбран для исследований in vivo.
[0525] В примере 10 зонд sCy5-Nle-SY, контроль носитель/без зонда (NP) или BMV109 вводили мышам внутривенно. После двух часов циркуляции ткани собирали, лизировали и анализировали на мечение зонда с помощью флуоресцентного SDS-PAGE. Мечение катепсина X наблюдали в печени, почках, толстой кишке, желудке и селезенке (фиг. 4A), и это подтверждали иммунопреципитацией с антителом к катепсину X (фиг. 4B). Хотя также наблюдалась некоторая маркировка катепсина S, общий профиль специфичности был явно улучшен по сравнению с BMV109, который также строго маркирует катепсин B и L.
[0526] Кроме того, после введения зонда in vivo готовили криосрезы почек от мышей, которым инъецировали sCy5-Nle-SY или контроля без зонда, и анализированы конфокальной микроскопией на флуоресценцию sCy5 (красный) или иммунореактивность катепсина X (зеленый) вместе с DAPI (синий) для визуализации ядра. Результаты представлены на фиг. 5. Наблюдали сильную точечную флуоресценцию sCy5, напоминающая эндолизосомальное окрашивание, и этот сигнал в значительной степени перекрывался с иммунореактивным катепсином X (фиг. 5). Таким образом, sCy5-Nle-SY можно использовать для различения активного катепсина X относительно общего катепсина X в тканях после введения in vivo.
[0527] Пример
11 - Характеристика зондов AOMK и на основе илида сульфоксония
[0528] В примере 11 реактивность новых зондов AOMK, полученных согласно примеру 2, сравнивали с соответствующими зондами на основе илида сульфоксония, полученными согласно примеру 1, с использованием эксперимента по мечению на живых клетках RAW264.7.
[0529] Зонды добавляли в возрастающих концентрациях (0,1, 0,5, 1, 5 мкМ) на 2 ч и мечение анализировали с помощью флуоресценции в геле. Результаты показаны на фиг. 6А.
[0530] Зонды AOMK были гораздо менее эффективными, чем зонды илида, что свидетельствует о пониженной реактивности. Эти зонды пометили катепсин B и S, но не X (фиг. 6A), что согласуется с предыдущими данными, демонстрирующими ограниченную реактивность катепсина X с активной группой AOMK (Paulick and Bogyo, 2011).
[0531] Пример
12 - Характеристика sCy5-Nle-AOMK in vivo
[0532] В примере 12 зонд AOMK sCy5-Nle-AOMK тестировали in vivo и анализировали его мечение в тканях. Зонд вводили мышам внутривенно. После двух часов циркуляции, ткани собирали, лизировали и анализировали на мечение зондом с использованием флуоресцентного SDS-PAGE. Только слабое мечение катепсина B и S наблюдали в толстой кишке, но не в других исследованных тканях (фиг. 6B).
[0533] Пример
13 - Мечение sCy5-Nle-SY в тканях человека
[0534] Для исследования способности sCy5-Nle-SY метить катепсин X в тканях человека, были использованы биопсийные материалы, полученные от пациентов с плоскоклеточным раком ротовой полости. Нормальные ткани слизистой оболочки полости рта, взятые на биопсию с противоположной стороны языков тех же пациентов, использовали в качестве контроля.
[0535] У пациентов с плоскоклеточной карциномой ротовой полости человека или у совпадающих субъектов с нормальной слизистой оболочкой ротовой полости проводили биопсию в соответствии с протоколами, одобренными Наблюдательным советом Института при Центре рака ротовой полости Нью-Йоркского университета. Биопсийный материал немедленно замораживали и хранили при -80°C. Ткани лизировали обработкой ультразвуком в цитратном буфере, и супернатанты очищали центрифугированием. Концентрацию общего белка оценивали с помощью анализа BCA, и 80 мкг метили Cy5-Nle-SY. Лизаты, полученные из ткани плоскоклеточной карциномы ротовой полости или совпадающих субъектов с нормальной слизистой оболочкой ротовой полости, инкубировали с sCy5-Nle-SY (5 мкМ для 20 мин), и мечение анализировали с помощью флуоресценции в геле (флуоресцентный SDS-PAGE). Образцы также подвергали иммуноблоттингу для определения общей экспрессии катепсина X (n=10). Кроме того, лизаты рака, меченные sCy5-Nle-SY, подвергали иммунопреципитации с помощью антитела, специфичного к катепсину X, для проверки идентичности меченого белка.
[0536] Результаты приведены на фиг. 8A и 8B. Во всех исследованных образцах карциномы наблюдали четкое и избирательное мечение катепсина X, что подтверждали иммунопреципитацией с антителом, специфичным к катепсину X. Активность катепсина X была значительно повышена в биоптатах карциномы по сравнению с нормальной тканью языка, и это было подтверждено увеличением общего катепсина X, измеренным с помощью иммуноблоттинга. Полученные данные показывают, что sCy5-Nle-SY может успешно детектировать активацию катепсина X в тканях человека и впервые выявить, что катепсин X значительно активирован при плоскоклеточной карциноме ротовой полости.
[0537] Таким образом, результаты проведенных экспериментов демонстрируют, что испытанная новая активная группа на основе илида диметилсульфоксония демонстрирует уникальную селективность по отношению к протеазам цистеиновой протеазе, катепсин, в клеточных лизатах, живых клетках, in vivo (например, у мышей) и в лизатах тканей (мыши и человека). Лучший зонд из тестированных зондов на основе илида сульфоксония, sCy5-Nle-SY, является наиболее эффективным и селективным зондом для катепсина X на сегодняшний день, демонстрируя исключительную специфичность в клеточных лизатах и клетках, которые экспрессируют низкие уровни катепсина S. Несмотря на то, что данный зонд действительно перекрестно реагирует с катепсином S в живых макрофагах и in vivo он не приводит к мечению катепсина B или L, что является явным усовершенствованием по сравнению с другими зондами, нацеленными на катепсин X (BMV109, MGP140). Использование sCy5-Nle-SY позволяет четко измерить активность катепсина X с помощью SDS-PAGE, в то время как это было затруднительно с предыдущими зондами в результате «искажающих» уровней мечения катепсина B. Кроме того, было установлено, что активная группа из илида сульфоксония достаточно стабильна для детектирования катепсина X in vivo и что сигнал sCy5-Nle-SY был достаточно ярким для детектирования с помощью конфокальной микроскопии.
[0538] Пример
14 - Boc-Val-SY в качестве ингибитора катепсина X
[0539] Для тестирования способности соединений илида сульфоксония функционировать в качестве ингибиторов катепсина, немеченый, boc-защищенный вариант Val-SY, т. е. трет-бутил (S)- (1-(диметил(оксо)-6-сульфанилиден)-4-метил-2-оксопентан-3-ил) карбамата (SJM-724-24). Живые клетки RAW264.7 предварительно обрабатывали Boc-Val-SY (0, 10 или 100 мкМ) в течение ночи. Остаточную активность катепсина X измеряли инкубацией живых клеток с sCy5-Val-SY на 2 ч. Клетки лизировали, и меченые белки детектировали с помощью флуоресценции в геле.
[0540] Результаты показаны на фиг. 9. По сравнению с контролями клетки, обработанные 100 мкМ Boc-Val-SY, показали снижение катепсина X и катепсина S на 71% и 51% соответственно. Полученные данные демонстрируют способность Boc-Val-SY конкурировать за мечение sCy5-Val-SY и, таким образом, функционировать в качестве ингибитора катепсина.
[0541] Настоящие примеры, способы, процедуры, конкретные соединения и молекулы приведены для примера и иллюстрации изобретения и никоим образом не должны рассматриваться в качестве ограничивающих объем изобретения, который определяется буквальным и эквивалентным объемом прилагаемой формулы изобретения. Любые патенты или публикации, упомянутые здесь, указывают на уровни специалистов в области, к которой относится патент, и предназначены для приведения деталей изобретения, которые не могут быть подробно изложены, но будут понятны специалистам в данной области. Такие патенты или публикации включены в настоящее описание в качестве ссылки в той же степени, как если бы каждый был специально и индивидуально включен в качестве ссылки и с целью описания и возможности использования указанной метода или материала.
[0542] Akkari L., Gocheva V., Kester J.C., Hunter K.E., Quick M.L., Sevenich L., Wang H.-W., Peters C., Tang L.H., Klimstra D.S., Reinheckel T. and Joyce J.A. (2014). Distinct functions of macrophage-derived and cancer cell-derived cathepsin Z combine to promote tumor malignancy via interactions with the extracellular matrix. Genes Dev., 28, 2134-2150.
Allan E.R.O., Campden R.I., Ewanchuk B.W., Tailor P., Balce D.R., McKenna N.T., Greene C.J., Warren A.L., Reinheckel T. and Yates R.M. (2017). A role for cathepsin Z in neuroinflammation provides mechanistic support for an epigenetic risk factor in multiple sclerosis. J Neuroinflammation 14, 1-11.
Bernhardt A., Kuester D., Roessner A., Reinheckel T. and Krueger S. (2010). Cathepsin X-deficient Gastric Epithelial Cells in Co-culture with Macrophages: Characterization of cytokine response and migration capability after Helicobacter pylori infection. J. Biol. Chem., 285, 33691-33700.
Chang X.-Z., Li D.-Q., Hou Y.-F., Wu J., Lu J.-S., Di G.-H., Jin W., Ou Z.-L., Shen Z.-Z. and Shao, Z.-M. (2007). Identification of the functional role of AF1Q in the progression of breast cancer. Breast Cancer Res. Treat., 111, 65-78.
Duivenvoorden H.M., Rautela J., Edgington-Mitchell L.E., Spurling A., Greening D.W., Nowell C.J., Molloy T.J., Robbins E., Brockwell N.K., Lee C.S., Chen M., Holliday A., Selinger C.I., Hu M., Britt K.L., Stroud D.A., Bogyo M., Möller A., Polyak K., Sloane B.F., O'Toole S.A. and Parker, B.S. (2017). Myoepithelial cell-specific expression of stefin A as a suppressor of early breast cancer invasion. J. Pathol., 243, 496-509.
Edgington L.E., Berger A.B., Blum G., Albrow V.E., Paulick M.G., Lineberry N. and Bogyo, M. (2009). Noninvasive optical imaging of apoptosis by caspase-targeted activity-based probes. Nat. Med., 15, 967-973.
Edgington L.E. and Bogyo M. (2013). In vivo imaging and biochemical characterization of protease function using fluorescent activity-based probes. Curr. Protoc. Chem. Biol., 5, 25-44.
Edgington L.E., van Raam B.J., Verdoes M., Wierschem C., Salvesen G.S. and Bogyo, M. (2012). An Optimized Activity-Based Probe for the Study of Caspase-6 Activation. Chem. Biol., 19, 340-352.
Edgington L.E., Verdoes M. and Bogyo, M. (2011). Functional imaging of proteases: recent advances in the design and application of substrate-based and activity-based probes. Curr. Op. Chem. Biol., 15, 798-805.
Edgington L.E., Verdoes M., Ortega A., Withana N.P., Lee J., Syed S., Bachmann M.H., Blum G. and Bogyo, M. (2013). Functional Imaging of Legumain in Cancer Using a New Quenched Activity-Based Probe. J. Am. Chem. Soc., 135, 174-182.
Edgington-Mitchell L.E., Rautela J., Duivenvoorden H.M., Jayatilleke K.M., van der Linden W.A., Verdoes M., Bogyo M. and Parker B.S. (2015). Cysteine cathepsin activity suppresses osteoclastogenesis of myeloid-derived suppressor cells in breast cancer. Oncotarget, 6, 27008-27022.
Hafner A., Glavan G., Obermajer N., Živin M., Schliebs R. and Kos J. (2013). Neuroprotective role of γ-enolase in microglia in a mouse model of Alzheimer's disease is regulated by cathepsin X. Aging Cell, 12, 604-614.
Huynh J.L., Garg P., Thin T.H., Yoo S., Dutta R., Trapp B.D., Haroutunian V., Zhu J., Donovan M.J., Sharp A.J. and Casaccia, P. (2013). Epigenome-wide differences in pathology-free regions of multiple sclerosis-affected brains. Nat. Neurosci., 17, 121-130.
Krueger S., Kalinski T., Hundertmark T., Wex T., Küster D., Peitz U., Ebert M., Nägler D.K., Kellner U., Malfertheiner P., Naumann M., Röcken C. and Roessner, A. (2005). Up-regulation of cathepsin X inHelicobacter pylori gastritis and gastric cancer. J. Pathol., 207, 32-42.
Leichsenring A., Bäcker I., Wendt W., Andriske M., Schmitz B., Stichel C.C. and Lübbert H. (2008). Differential expression of Cathepsin S and X in the spinal cord of a rat neuropathic pain model. BMC Neurosci., 9, 80-13.
Meara J.P. and Rich, D.H. (1996). Mechanistic studies on the inactivation of papain by epoxysuccinyl inhibitors. J. Med. Chem., 39, 3357-3366.
Nägler D.K., Kraus S., Feierler J., Mentele R., Lottspeich F., Jochum M. and Faussner A. (2010). A cysteine-type carboxypeptidase, cathepsin X, generates peptide receptor agonists. Int. Immunopharmacol., 10, 134-139.
Nägler D.K., Krüger S., Kellner A., Ziomek E., Ménard R., Buhtz P., Krams M., Roessner A. and Kellner U. (2004). Up-regulation of cathepsin X in prostate cancer and prostatic intraepithelial neoplasia. Prostate, 60, 109-119.
Nägler D.K., Zhang R., Tam W., Sulea T., Purisima E.O. and Ménard R. (1999). Human Cathepsin X: A Cysteine Protease with Unique Carboxypeptidase Activity. Biochem., 38, 12648-12654.
Obermajer N., Doljak B., Jamnik P., Fonović U.P. and Kos J. (2009). Cathepsin X cleaves the C-terminal dipeptide of alpha- and gamma-enolase and impairs survival and neuritogenesis of neuronal cells. Int. J. Biochem. Cell Biol., 41, 1685-1696.
Obermajer N., Švajger U., Bogyo M., Jeras M. and Kos J. (2008). Maturation of dendritic cells depends on proteolytic cleavage by cathepsin X. J. Leukocyte Biol., 84, 1306-1315.
Oresic Bender K., Ofori L., van der Linden W.A., Mock E.D., Datta G.K., Chowdhury S., Li H., Segal E., Sanchez Lopez M., Ellman J.A., Figdor C.G., Bogyo M. and Verdoes M. (2015). Design of a Highly Selective Quenched Activity-Based Probe and Its Application in Dual Color Imaging Studies of Cathepsin S Activity Localization. J. Am. Chem. Soc., 137, 4771-4777.
Orlowski G.M., Colbert J.D., Sharma S., Bogyo M., Robertson S.A. and Rock K.L. (2015). Multiple Cathepsins Promote Pro-IL-1β Synthesis and NLRP3-Mediated IL-1β Activation. J. Immunol., 195, 1685-1697.
Paulick M.G. and Bogyo M. (2011). Development of Activity-Based Probes for Cathepsin X. ACS Chem. Biol., 6, 563-572.
Pečar Fonović U. and Kos J. (2015). Cathepsin X Cleaves Profilin 1 C-Terminal Tyr139 and Influences Clathrin-Mediated Endocytosis. PLoS ONE, 10, e0137217-13.
Sanman L.E. and Bogyo M. (2014). Activity-Based Profiling of Proteases. Annu. Rev. Biochem., 83, 249-273.
Sevenich L., Schurigt U., Sachse K., Gajda M., Werner F., Muller S., Vasiljeva O., Schwinde A., Klemm N., Deussing J., Peters C. and Reinheckel T. (2010). Synergistic antitumor effects of combined cathepsin B and cathepsin Z deficiencies on breast cancer progression and metastasis in mice. Proc. Nat. Acad. Sci., 107, 2497-2502.
Shaw E. (1988). Peptidyl sulfonium salts. A new class of protease inhibitors. J. Biol. Chem., 263, 2768-2772.
Verdoes M., Edgington L.E., Scheeren F.A., Leyva M., Blum G., Weiskopf K., Bachmann M.H., Ellman J.A. and Bogyo M. (2012). A Nonpeptidic Cathepsin S Activity-Based Probe for Noninvasive Optical Imaging of Tumor-Associated Macrophages. Chem. Biol., 19, 619-628.
Verdoes M., Oresic Bender K., Segal E., van der Linden W.A., Syed S., Withana N.P., Sanman L.E. and Bogyo M. (2013). Improved Quenched Fluorescent Probe for Imaging of Cysteine Cathepsin Activity. J. Am. Chem. Soc., 135, 14726-14730.
Wendt W., Zhu X.-R., Lübbert H. and Stichel C.C. (2007). Differential expression of cathepsin X in aging and pathological central nervous system of mice. Exp. Neurol., 204, 525-540.
[0543] Дополнительные варианты осуществления изобретения включают:
1. Соединение формулы I
[0544]
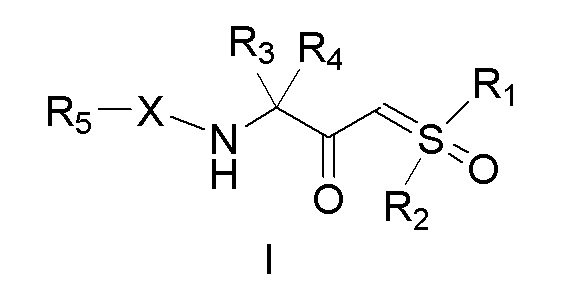
или его соль,
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R3 представляет собой боковую цепь альфа-аминокислоты;
R4 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R5 выбран из группы, состоящей из детектируемого элемента, аминозащитной группы амина, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила, (C2-C8) алкинила, (C1-C8) алкилкарбонила, (C1-C8) гидроксиалкилкарбонила, (C1-C8) галогеналкилкарбонила, (C3-C8) циклоалкилкарбонила, (C1-C8) алкилоксикарбонила, бензилоксикарбонила и атома водород;
X представляет собой:
(i) связь; или
(ii) бирадикальный фрагмент формулы II или III, который связан с заместителем R5 через аминогруппу:
[0545]

где:
R6 представляет собой боковую цепь альфа-аминокислоты;
R7 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R8 представляет собой боковую цепь альфа-аминокислоты;
R9 выбран из группы, состоящей из атома водорода и (C1-C4) алкила; и
n равно 1, 2, 3 или 4.
[0546] 2. Соединение по п.1, где R3 представляет собой боковую цепь природной альфа-аминокислоты или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0547] 3. Соединение по п.1, где R3 представляет собой боковую цепь протеиногенной альфа-аминокислоты или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0548] 4. Соединение по п.1, где R3 представляет собой боковую цепь протеиногенной альфа-аминокислоты, за исключением лизина, или структурный изомер или гомолог указанной боковой цепи,
где указанная боковая цепь, или структурный изомер, или его гомолог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0549] 5. Соединение по п.1, где R3 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О- этилгомосерина, треонина, аспарагина и глутамина, или структурного изомера, гомолога и/или структурного аналога указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0549] 6. Соединение по п.1, где R3 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О- этилгомосерина, треонина, аспарагина и глутамина, или структурного изомера, гомолога и/или структурного аналога указанной боковой цепи,
где указанная боковая цепь, или структурный изомер, или его гомолог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где:
R3x выбран из группы, состоящей из гидрокси, галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0551] 7. Соединение по п.6, где альфа-аминокислота выбрана из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина и селенэтионина.
[0552] 8. Соединение по п.6, где альфа-аминокислота выбрана из группы, состоящей из аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, фенилаланина и триптофана.
[0553] 9. Соединение по п.6, где альфа-аминокислота выбрана из группы, состоящей из валина, норвалина, лейцина, изолейцина, норлейцина и гомонорлейцина.
[0554] 10. Соединение по п.6, где альфа-аминокислота выбрана из группы, состоящей из валина, лейцина, изолейцина и норлейцина.
[0555] 11. Соединение по п.6, где альфа-аминокислота представляет собой лейцин или норлейцин.
[0556] 12. Соединение по п.6, где альфа-аминокислота представляет собой норлейцин.
[0544]
[0557] 13. Соединение по п.1, где R3 выбран из группы, состоящей из атома водорода, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2- C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила, (C3-C9) гетероарилметила и -CH2CH2CH2CH2N(R3a)(R3b); где:
R3a выбран из группы, состоящей из детектируемого элемента, аминозащитной группы, атома водорода и (C1-C8) алкила; и
R3b выбран из группы, состоящей из атома водорода и (C1-C4) алкила.
[0558] 14. Соединение по п.13, где R3 выбран из группы, состоящей из (C1-C8) алкила, (C2-C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила, (C3-C9) гетероарилметила и -CH2CH2CH2CH2N(R3a) (R3b).
[0559] 15. Соединение по п.13, где R3 выбран из группы, состоящей из (C1-C8) алкила, (C6-C10) арилметила, (C3-C9) гетероарилметила и -CH2CH2CH2CH2N(R3a)(R3b).
[0560] 16. Соединение по п.13, где R3 выбран из группы, состоящей из (C1-C8) алкила, бензила, (1H-индол-3-ил)метила и -CH2CH2CH2CH2N(R3a)(R3b).
[0561] 17. Соединение по п.13, где R3 выбран из группы, состоящей из (C1-C6) алкила, бензила, (1H-индол-3-ил)метила и -CH2CH2CH2CH2N(R3a)(R3b).
[0562] 18. Соединение по п.13, где R3 выбран из группы, состоящей из этила, н-пропила, изопропила, н-бутила, втор-бутила, изобутила, н-пентила, бензила, (1H-индол-3-ил)метила и -CH2CH2CH2CH2N(R3a)(R3b).
[0563] 19. Соединение по любому из пп.13-18, где, если X представляет собой связь, то R3a не является аминозащитной группой, атомом водорода или (C1-C8) алкилом.
[0564] 20. Соединение по любому из пп.13-18, где R3a представляет собой детектируемый элемент.
[0565] 21. Соединение по любому из пп.13-18, где, если X представляет собой связь, то R3 не представляет собой -CH2CH2CH2CH2N(R3a)(R3b).
[0566] 22. Соединение по п.1, где R3 выбран из группы, состоящей из атома водорода, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2- C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила и (C3-C9) гетероарилметила.
[0567] 23. Соединение по п.22, где R3 выбран из группы, состоящей из (C1-C8) алкила, (C2-C8) алкенила, (C2-C8) алкинила, (C6-C10) арилметила и (C3-C9) гетероарилметила.
[0568] 24. Соединение по п.22, где R3 выбран из группы, состоящей из (C1-C8) алкила, (C6-C10) арилметила и (C3-C9) гетероарилметила.
[0569] 25. Соединение по п.22, где R3 выбран из группы, состоящей из (C1-C8) алкила, бензила и (1H-индол-3-ил)метила.
[0570] 26. Соединение по п.22, где R3 выбран из группы, состоящей из (C1-C6) алкила, бензила и (1H-индол-3-ил)метила.
[0571] 27. Соединение по п.22, где R3 выбран из группы, состоящей из этила, н-пропила, изопропила, н-бутила, втор-бутила, изобутила, н-пентила, бензила и (1H-индола)-3-ил)метила.
[0572] 28. Соединение по п.22, где R3 выбран из группы, состоящей из н-бутила, втор-бутила и изобутила.
[0573] 29. Соединение по п.22, где R3 представляет собой н-бутил.
[0574] 30. Соединение по п.1, где R3 представляет собой -CH2CH2CH2CH2N(R3a)(R3b); где:
R3a выбран из группы, состоящей из детектируемого элемента, аминозащитной группы, атома водорода и (C1-C8) алкила; и
R3b выбран из группы, состоящей из атома водорода и (C1-C4) алкила.
[0575] 31. Соединение по п.30, где, если X представляет собой связь, то R3a не является аминозащитной группой, атомом водорода или (C1-C8) алкилом.
[0576] 32. Соединение по любому из пп.13-18 и 30, где R3a представляет собой атом водорода.
[0577] 33. Соединение по любому из пп. 13-18 и 30, где R3a представляет собой аминозащитную группу.
[0578] 34. Соединение по любому из пп.13-18 и 30, где R3a представляет собой (C1-C8) алкил.
[0579] 35. Соединение по любому из пп.13-20 и 30-34, где R3b представляет собой атом водорода.
[0580] 36. Соединение по любому из пп.1-35, где R1 представляет собой (C1-C8) алкил.
[0581] 37. Соединение по любому из пп.1-36, где R1 представляет собой метил.
[0582] 38. Соединение по любому из пп.1-37, где R2 представляет собой (C1-C8) алкил.
[0583] 39. Соединение по любому из пп.1-38, где R2 представляет собой метил.
[0584] 40. Соединение по любому из пп.1-39, где R4 представляет собой атом водород.
[0585] 41. Соединение по любому из пп.1-40, где R5 выбран из группы, состоящей из детектируемого элемента, аминозащитной группы и атома водорода.
[0586] 42. Соединение по любому из пп.1-41, где R6 представляет собой боковую цепь природной альфа-аминокислоты или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи.
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R6x, где:
R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0587] 43. Соединение по любому из пп.1-41, где R6 представляет собой боковую цепь протеиногенной альфа-аминокислоты или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи.
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R6x, где
R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0588] 44. Соединение по любому из пп.1-41, где R6 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О- этилгомосерина, треонина, аспарагина и глутамина, или структурного изомера, гомолога и/или структурного аналога указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R6x, где:
R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0589] 45. Соединение по п.44, где альфа-аминокислота представляет собой фенилаланин.
[0590] 46. Соединение по любому из пп.1-41, где R6 представляет собой боковую цепь фенилаланина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи.
[0591] 47. Соединение по любому из пп.1-41, где R6 представляет собой боковую цепь фенилаланина.
[0592] 48. Соединение по любому из пп.1-47, где R7 представляет собой атом водорода.
[0593] 49. Соединение по любому из пп.1-48, где R8 представляет собой боковую цепь природной альфа-аминокислоты или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи.
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R8x, где:
R8x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0594] 50. Соединение по любому из пп.1-48, где R8 представляет собой боковую цепь протеиногенной альфа-аминокислоты или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи.
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R8x, где
R8x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0595] 51. Соединение по любому из пп.1-48, где R8 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О- этилгомосерина, треонина, аспарагина и глутамина, или структурного изомера, гомолога и/или структурного аналога указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог необязательно замещены аминозащитной группой или детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R8x, где R8x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0596] 52. Соединение по любому из пп.1-51, где R9 представляет собой атом водорода.
[0597] 53. Соединение по любому из пп.1-52, где аминозащитная группа выбрана из группы, состоящей из бензилоксикарбонила (Cbz), 9-флуоренилметилоксикарбонила (Fmoc), трет-бутилоксикарбонила (Boc), аллилоксикарбонила (Alloc), п-толуолсульфонила (Tos), 2,2,5,7,8-пентаметилхроман-6-сульфонила (Pmc), 2,2,4,6,7-пентаметил-2,3-дигидробензофуран-5-сульфонила (Pbf), мезитил-2-сульфонила (Mts), 4-метокси-2,3,6-триметилфенилсульфонила (Mtr), ацетамидо и фталимидо.
[0598] 54. Соединение по любому из пп.1-53, где аминозащитная группа представляет собой бензилоксикарбонил.
[0599] 55. Соединение по любому из пп.1-54, имеющее формулу IA:
[0600]
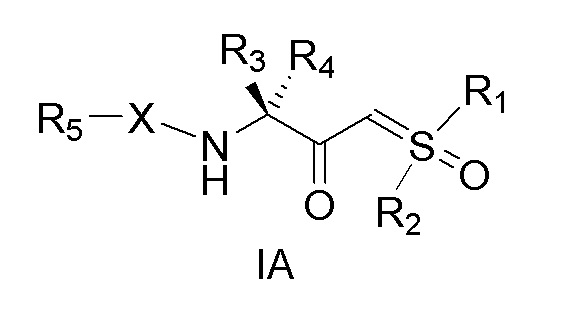
[0601] 56. Соединение по любому из пп.1-55, где бирадикальный фрагмент имеет формулу IIA или IIIA:
[0602]
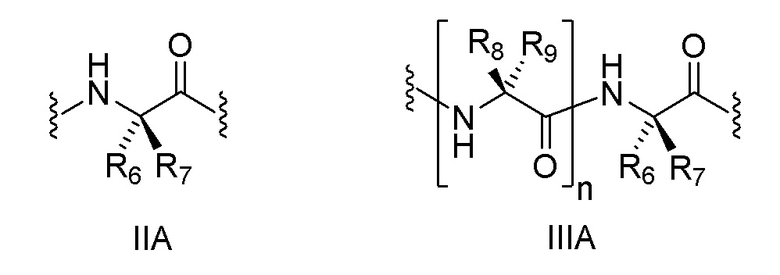
[0603] 57. Соединение по любому из пп.1-55, где X представляет собой связь.
[0604] 58. Соединение по любому из пп.1-55, где X представляет собой бирадикальный фрагмент формулы II.
[0605] 59. Соединение по любому из пп.1-55, где X представляет собой бирадикальный фрагмент формулы III.
[0606] 60. Соединение по п.56, где X представляет собой бирадикальный фрагмент формулы IIA.
[0607] 61. Соединение по п.56, где X представляет собой бирадикальный фрагмент формулы IIIA.
[0608] 62. Соединение по любому из пп.1-61, где n равно 1.
[0609] 63. Соединение по любому из пп.1-62, где детектируемый элемент выбран из группы, состоящей из флуоресцентной метки, биотиновой метки, радиоактивной метки, хелатора и биоортогонального маркера для лигирования.
[0610] 64. Соединение по любому из пп.1-63, где детектируемый элемент представляет собой флуоресцентную метку.
[0611] 65. Соединение по п.64, где флуоресцентная метка выбрана из группы, состоящей из флуоресцеина, Oregon green, борадиазаиндеценового красителя, родаминового красителя, красителя на основе бензопириллия, кумаринового красителя, цианиновой метки или бензоиндольной метки
[0612] 66. Соединение по п.64, где флуоресцентная метка представляет собой цианиновую метку.
[0613] 67. Соединение по п.64, где флуоресцентная метка представляет собой цианиновую метку, имеющую формулу, выбранную из следующей группы формул:
[0614]
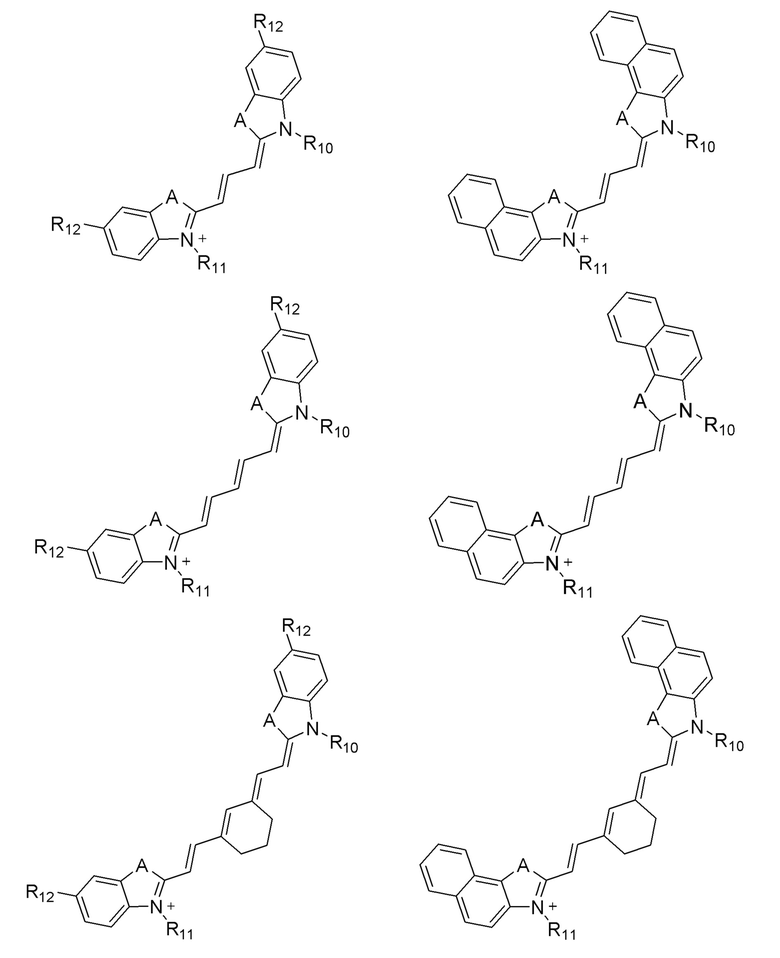
[0615] где в каждой из приведенных выше формул,
A выбран из группы, состоящей из CH2, C(CH3)2, C(C2H5)2, NH, N(CH3), N(C2H5), O, S и Se;
R10 выбран из группы, состоящей из $-(CH2)p-C(= O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 2, 3, 4, 5, 6, 7 или 8;
q равно 2, 3, 4, 5, 6, 7 или 8;
r равно 2, 3, 4, 5, 6, 7 или 8;
$ представляет собой точку соединения с атомом азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 выбран из группы, состоящей из (C1-C8) алкила и (C6-C10) арила; и
R12 представляет собой H или сульфогруппу.
[0616] 68. Соединение по п. 67, где:
A выбран из группы, состоящей из CH2, C(CH3)2 и C(C2H5)2;
R10 выбран из группы, состоящей из $-(CH2)p-C(=O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 2, 3, 4, 5 или 6;
q равно 2, 3, 4, 5 или 6;
r равно 2, 3, 4, 5 или 6;
$ представляет собой точку присоединения к атому азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой (C1-C8) алкил; и
R12 представляет собой H или сульфогруппу.
[0617] 69. Соединение по п. 67, где:
А представляет собой C(CH3)2 или C(C2H5)2;
R10 выбран из группы, состоящей из $-(CH2)p-C(=O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 2, 3, 4, 5 или 6;
q равно 2, 3, 4, 5 или 6;
r равно 2, 3, 4, 5 или 6;
$ представляет собой точку присоединения к атому азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил, этил или пропил; и
R12 представляет собой H или сульфогруппу.
[0618] 70. Соединение по п. 67, где:
А представляет собой C(CH3)2;
R10 выбран из группы, состоящей из $-(CH2)p-C(=O)-& и $- (CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 4, 5 или 6;
q равно 4, 5 или 6;
r равно 3, 4, 5 или 6;
$ представляет собой точку соединения с атомом азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил или этил; и
R12 представляет собой H или сульфогруппу.
[0619] 71. Соединение по п. 67, где:
А представляет собой С(СН3)2;
R10 представляет собой $-(CH2)p-C(=O)-&; где:
p равно 4, 5 или 6; и
$ представляет собой точку присоединения к атому азота цианиновой части; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил или этил; и
R12 представляет собой сульфогруппу.
[0620] 72. Соединение по п. 67, где:
А представляет собой С(СН3)2;
R10 представляет собой $-(CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(= O)-&;
где:
q равно 4, 5 или 6;
r равно 3, 4, 5 или 6;
$ представляет собой точку присоединения к атому азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 представляет собой метил или этил; и
R12 представляет собой H.
[0621] 73. Соединение по любому из пп.67-72, где p равно 5, q равно 5 и r равно 4.
[0622] 74. Соединение по п.64, где флуоресцентная метка представляет собой цианиновую метку, имеющую формулу, выбранную из следующей группы формул:
[0623]
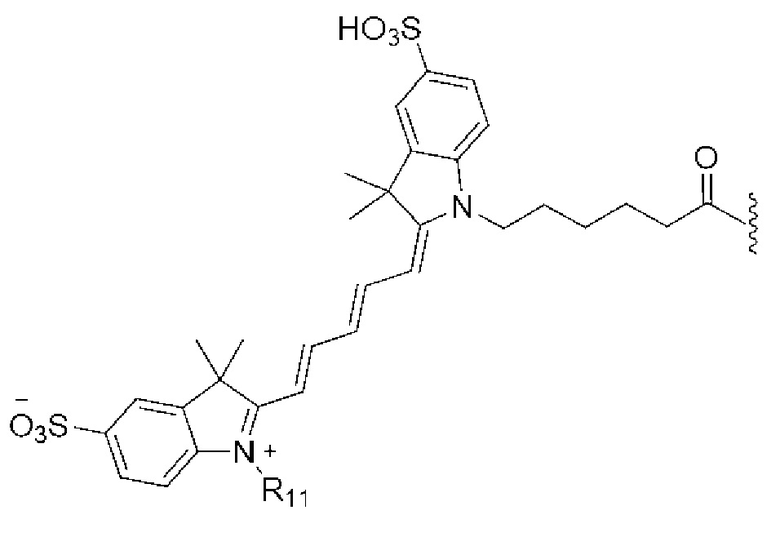
[0624]
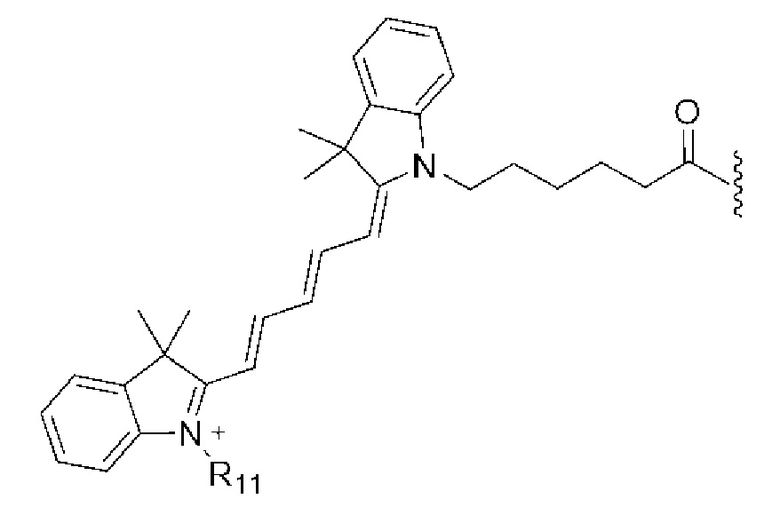
[0625]
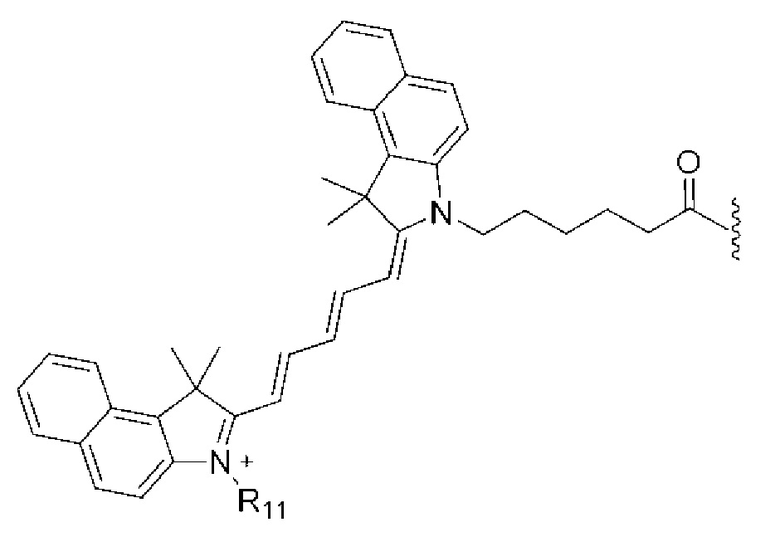
[0626] где в каждой из вышеприведенных формул,
волнистая линия представляет собой точку соединения с остальной частью молекулы;
и R11 выбран из группы, состоящей из (C1-C8) алкила и (C6-C10) арила.
[0600]
[0627] 75. Соединение по п.74, где R11 представляет собой (C1-C8) алкил.
[0628] 76. Соединение по п.74, где R11 представляет собой метил или этил.
[0629] 77. Соединение по п.64, где флуоресцентная метка представляет собой цианиновую метку, имеющую формулу:
[0630]
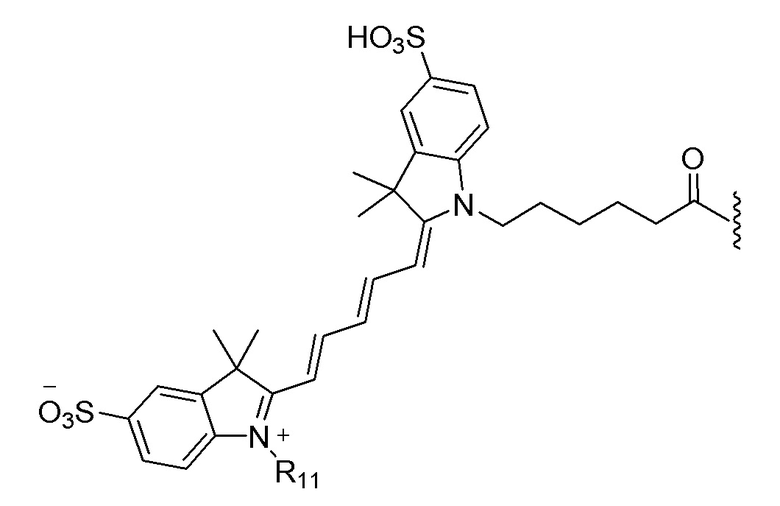
[0631] где волнистая линия представляет собой точку соединения с остальной частью молекулы; и R11 представляет собой метил или этил.
[0632] 78. Соединение по любому из пп.1-77, где соединение содержит, по меньшей мере, один детектируемый элемент.
[0633] 79. Соединение по любому из пп.1-77, где соединение содержит один, два или три детектируемых элемента.
[0634] 80. Соединение по любому из пп.1-77, где соединение содержит один детектируемый элемент.
[0635] 81. Соединение по любому из пп.1-80, где R5 представляет собой детектируемый элемент.
[0636] 82. Соединение по любому из пп.1-81, где R3 содержит детектируемый элемент.
[0637] 83. Соединение по любому из пп.1-82, где R3 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи.
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R3x, где R3x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0638] 84. Соединение по любому из пп.1-82,
где R3 представляет собой -CH2CH2CH2CH2N(R3a)(R3b); где:
R3a представляет собой детектируемый элемент; и
R3b выбран из группы, состоящей из атома водорода и (C1-C4) алкила.
[0639] 85. Соединение по любому из пп.82-84, где R5 выбран из группы, состоящей из аминозащитной группы, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила, (C2-C8) алкинила, (C1-C8) алкилкарбонила, (C1-C8) гидроксиалкилкарбонила, (C1-C8) галогеналкилкарбонила, (C3-C8) циклоалкилкарбонила, (C1-C8) алкилоксикарбонила, бензилоксикарбонила и атома водорода.
[0640] 86. Соединение по любому из пп.82-84, где R5 представляет собой аминозащитную группу.
[0641] 87. Соединение по любому из пп.1-86, где X представляет собой бирадикальный фрагмент формулы II или IIA, и R6 несет детектируемый элемент.
[0642] 88. Соединение по любому из пп.1-87, где X представляет собой бирадикальный фрагмент формулы II или IIA, и R6 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R6x, где R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0643] 89. Соединение по любому из пунктов от 1 до 86, где X представляет собой бирадикальный фрагмент формулы III или IIIA, и R6 несет детектируемый элемент.
[0644] 90. Соединение по любому из пп.1-86 и 89, где X представляет собой бирадикальный фрагмент формулы III или IIIA, и R6 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R6x, где R6x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0645] 91. Соединение по любому из пп.1-86 и 89-90, где X представляет собой бирадикальный фрагмент формулы III или IIIA, и R8 несет детектируемый элемент.
[0646] 92. Соединение по любому из пп.1-86 и 89-91, где X представляет собой бирадикальный фрагмент формулы III или IIIA, и R8 представляет собой боковую цепь лизина или структурный изомер, гомолог и/или структурный аналог указанной боковой цепи,
где указанная боковая цепь или структурный изомер, гомолог и/или структурный аналог замещены детектируемым элементом и необязательно дополнительно замещены одним или более одинаковыми или разными заместителями R8x, где R8x выбран из группы, состоящей из гидрокси, атома галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси.
[0647] 93. Соединение, выбранное из группы формул, состоящей из:
[0648]

[0649]
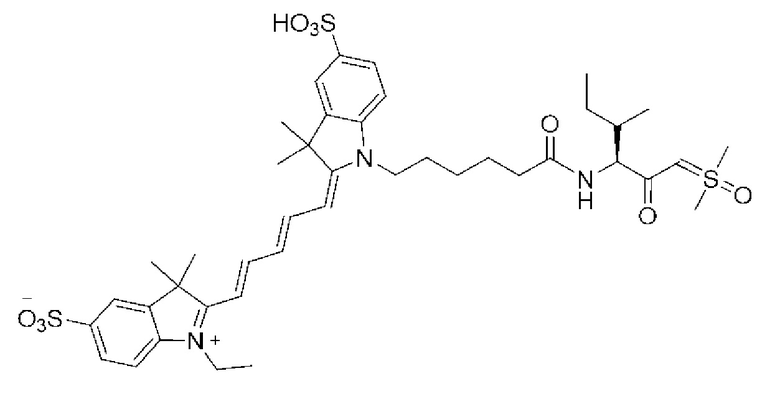
[0649]
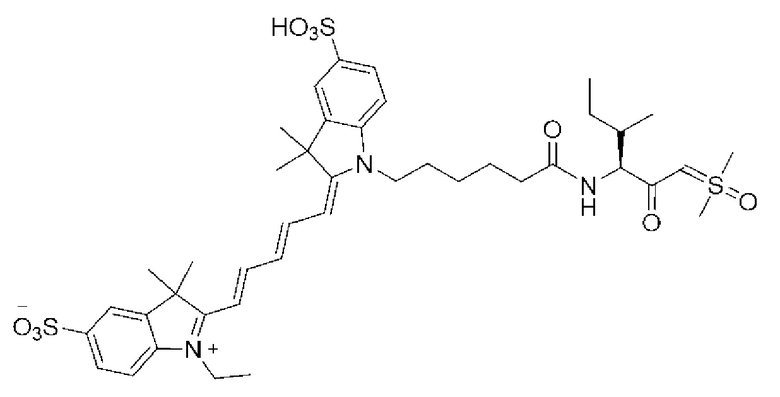
[0650]
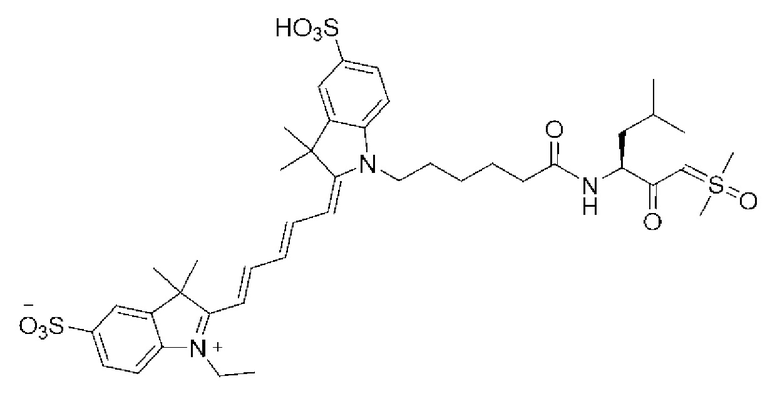
[0651]
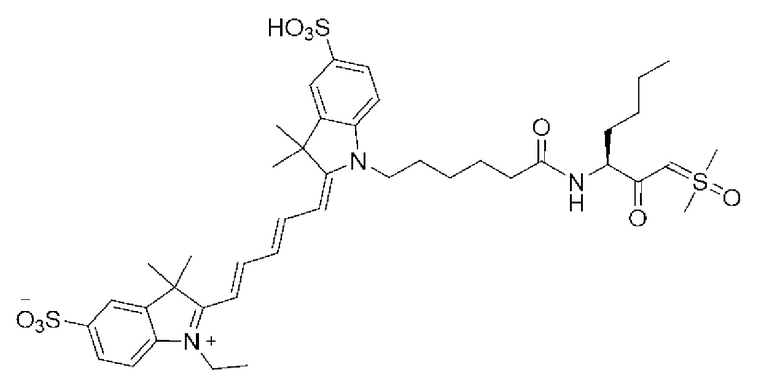
[0652]
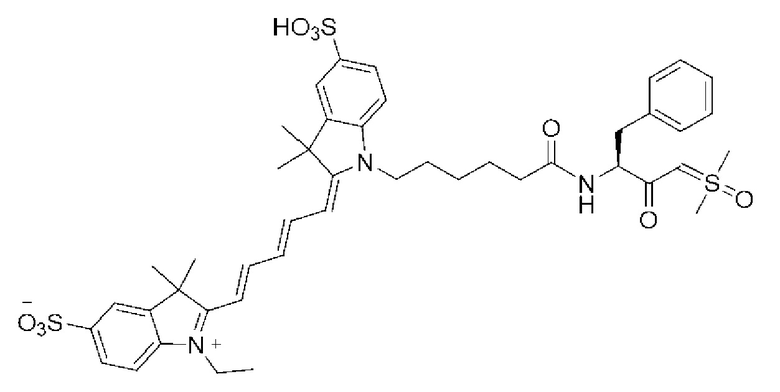
[0653]
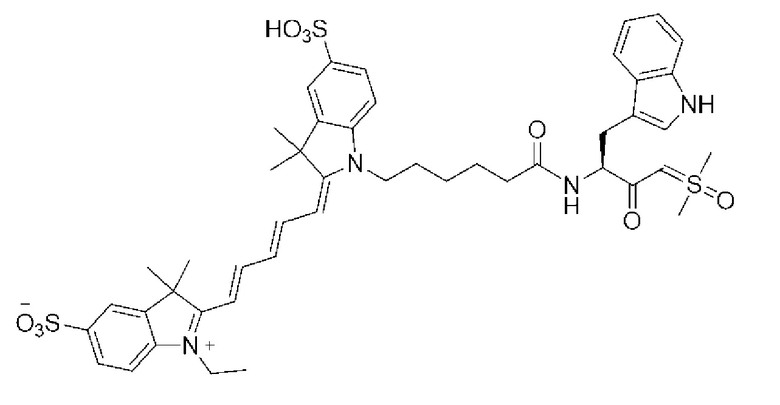
[0654]
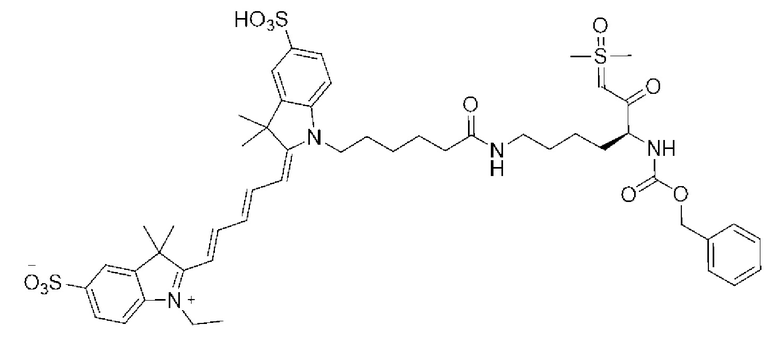
[0655]
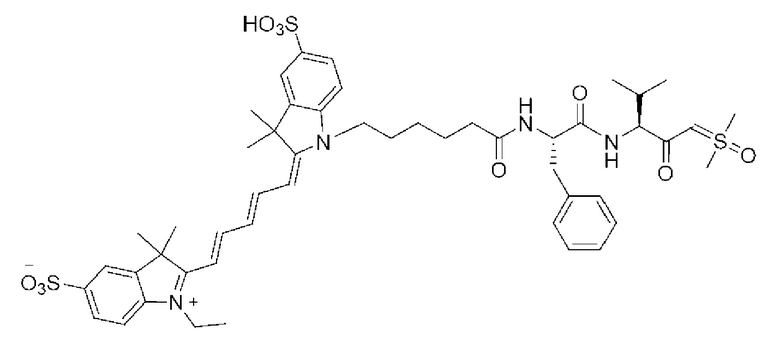
[0656] или его соль.
[0657] 94. Соединение формулы:
[0658]
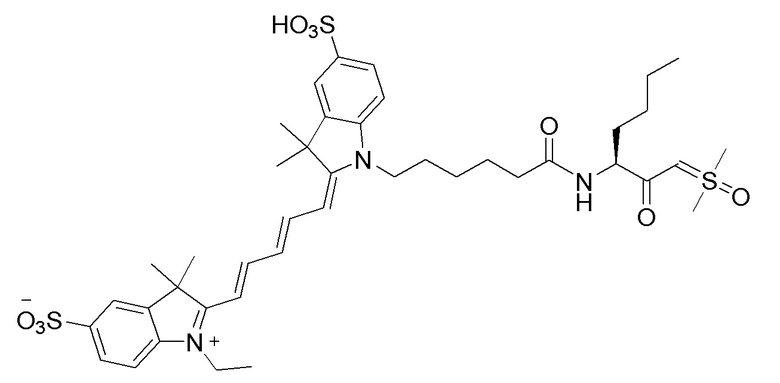
или его соль.
[0659] 95. Композиция, содержащая соединение по любому из пп.1-94 или его соль и эксципиент.
[0660] 96. Композиция по п.95, где композиция содержит соединение по любому из пп.78-94 или его соль и эксципиент.
[0661] 97. Способ детектирования активности цистеиновой протеазы, включающий:
(1) контактирование цистеиновой протеазы с соединением-зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ цистеиновой протеазы, включающий измерение детектируемого сигнала.
[0662] 98. Способ по п.97, где способ представляет собой способ in vitro.
[0663] 99. Способ детектирования активности цистеиновой протеазы in vitro, включающий:
(1) контактирование биологического образца с соединением-зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0664] 100. Способ детектирования активности цистеиновой протеазы в биологическом образце, полученном от субъекта, включающий:
(1) контактирование биологического образца in vitro с соединением-зондом на основе активности, содержащим фрагмент илида сульфоксония в качестве активной группы, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0665] 101. Способ по любому из пп.97-100, где фрагмент илида сульфоксония имеет формулу (IV):
[0666]
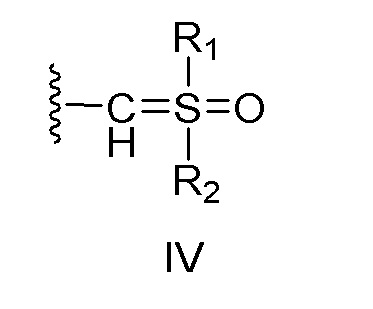
[0667] где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила.
[0668] 102. Способ по п.101, где R1 представляет собой (C1-C8) алкил, и R2 представляет собой (C1-C8) алкил.
[0669] 103. Способ по п.101, где R1 представляет собой метил, и R2 представляет собой метил.
[0600] 104. Способ детектирования активности цистеиновой протеазы, включающий:
(1) контактирование цистеиновой протеазы с соединением по любому из пп.78-94 или его солью, или с композицией по п.96, и
(2) последующий анализ цистеиновой протеазы, включающий измерение детектируемого сигнала.
[0671] 105. Способ по п.104, где способ представляет собой способ in vitro.
[0672] 106. Способ детектирования активности цистеиновой протеазы in vitro, включающий:
(1) контактирование биологического образца с соединением по любому из пп.78-94 или его солью, или с композицией по п.96, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0673] 107. Способ детектирования активности цистеиновой протеазы в биологическом образце, полученном от субъекта, включающий:
(1) контактирование биологического образца in vitro с соединением по любому из пп.78-94 или его солью, или с композицией по п.96, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0674] 108. Способ по любому из пп.97-107, где стадия (2) включает выполнение, по меньшей мере, одного аналитического метода, выбранного из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, гель-электрофореза и последующей радиографии, гель-электрофореза и последующего иммуноблоттинга, флуоресцентной микроскопии, проточной цитометрии, оптической визуализации ex vivo, радиографии, аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики.
[0675] 109. Способ по любому из пп.97-108, где детектируемый сигнал измеряется посредством измерения флуоресценции.
[0676] 110. Способ по пп.108 или 109, где, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, флуоресцентной микроскопии и проточной цитометрии.
[0677] 111. Способ по пп.108 или 109, где, по меньшей мере, один аналитический метод выбран из гель-электрофореза и последующей флуоресценции в геле и флуоресцентной микроскопии.
[0678] 112. Способ по любому из пп.97-111, где указанное соединение содержит детектируемый элемент в виде флуоресцентной метки.
[0679] 113. Способ по любому из пп.109-111, где указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и где стадия (2) включает вторичное мечение с помощью клик-химии для включения флуоресцентной метки перед выполнением, по меньшей мере, одного аналитического метода.
[0680] 114. Способ по любому из пп.109-111, где указанное соединение содержит детектируемый элемент в виде биотина, и где стадия (2) включает вторичное мечение флуоресцентно-меченным стрептавидином или вторичное мечение флуоресцентно-меченным антителом, специфичным к биотину, перед выполнением, по меньшей мере, одного аналитического метода.
[0681] 115. Способ по любому из пп.108-114, где гель-электрофорез представляет собой одномерный или двумерный гель-электрофорез.
[0682] 116. Способ по любому из пп.108-115, где гель-электрофорез представляет собой SDS-PAGE.
[0683] 117. Способ по любому из пп.99-103 и 106-116, где биологический образец выбран из группы, состоящей из клеток, клеточных лизатов, образцов тканей, лизатов тканей и жидкостей организма.
[0684] 118. Способ по п.117, где биологический образец представляет собой лизат клеток или лизат ткани.
[0685] 119. Способ по п.117, где биологический образец представляет собой очищенный лизат клеток или очищенный лизат тканей.
[0686] 120. Способ по п.117, где биологический образец представляет собой живые клетки.
[0687] 121. Способ по п.120, где живые клетки лизируют и очищают между стадией (1) и стадией (2).
[0688] 122. Способ по любому из пп.99-103 и 106-121, где биологический образец получают от человека.
[0689] 123. Способ детектирования активности цистеиновой протеазы, включающий:
(1) введение субъекту соединения-зонда на основе активности, содержащего фрагмент илида сульфоксония, в качестве активной группы,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0690] 124. Способ по п.123, где соединение-зонд на основе активности вводят внутривенно.
[0691] 125. Способ по пп.123 или 124, где фрагмент илида сульфоксония имеет формулу (IV):
[0692]
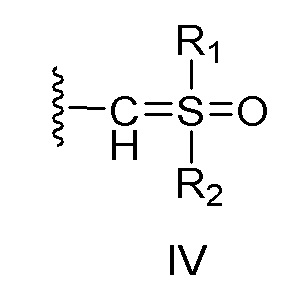
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила.
[0693] 126. Способ по п.125, где R1 представляет собой (C1-C8) алкил, и R2 представляет собой (C1-C8) алкил.
[0694] 127. Способ по п.125, где R1 представляет собой метил, и R2 представляет собой метил.
[0695] 128. Способ определения активности цистеиновой протеазы, включающий:
(1) введение субъекту соединения по любому из пп.78-94 или его соли, или композиции по п.96,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0696] 129. Способ по п.128, где соединение или его соль, или композицию вводят внутривенно.
[0697] 130. Способ по любому из пп.123-129, где стадия (3) включает выполнение, по меньшей мере, одного аналитического метода, выбранного из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, гель-электрофореза и последующей радиографии, гель-электрофореза и последующего иммуноблоттинга, флуоресцентной микроскопии, проточной цитометрии, оптической визуализации ex vivo, радиографии, аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики.
[0698] 131. Способ по любому из пп.123-130, где детектируемый сигнал измеряется посредством измерения флуоресценции.
[0699] 132. Способ по пп.130 или 131, где, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, флуоресцентной микроскопии и проточной цитометрии.
[0700] 133. Способ по пп.130 или 131, где, по меньшей мере, один аналитический метод выбран из гель-электрофореза и последующей флуоресценции в геле и флуоресцентной микроскопии.
[701] 134. Способ по любому из пп.123-133, где указанное соединение содержит детектируемый элемент в виде флуоресцентной метки.
[0702] 135. Способ по любому из пп.131-133, где указанное соединение содержит детектируемый элемент в виде биоортогонального маркера для лигирования, и стадия (3) включает вторичное мечение с помощью клик-химии для включения флуоресцентной метки перед выполнением, по меньшей мере, одного аналитического метода.
[0703] 136. Способ по любому из пп.131-133, где указанное соединение содержит детектируемый элемент в виде биотина, и где стадия (3) включает вторичное мечение флуоресцентно-меченным стрептавидином или вторичное мечение флуоресцентно-меченным антителом, специфичным для биотина, перед выполнением, по меньшей мере, одного аналитического метода.
[0704] 137. Способ по любому из пп.130-136, где гель-электрофорез представляет собой одномерный или двумерный гель-электрофорез.
[0705] 138. Способ по любому из пп.130-137, где гель-электрофорез представляет собой SDS-PAGE.
[0706] 139. Способ по любому из пп.123-138, где биологический образец выбран из группы, состоящей из клеток, клеточных лизатов, образцов тканей, лизатов тканей и жидкостей организма.
[0707] 140. Способ по п.139, где биологический образец представляет собой лизат клеток или лизат ткани.
[0708] 141. Способ по п. 139, где биологический образец представляет собой очищенный лизат клеток или очищенный лизат тканей.
[0709]
[0710] 142. Способ по любому из пп.123-141, где субъектом является человек.
[0711] 143. Способ детектирования активности цистеиновой протеазы у субъекта in vivo, включающий:
(1) введение субъекту соединения-зонда на основе активности, содержащего фрагмент илида сульфоксония в качестве активной группы, и
(2) последующее обследование объекта, включающее измерение детектируемого сигнала.
[0712] 144. Способ по п.143, где соединение-зонд на основе активности вводят внутривенно.
[0713] 145. Способ по пп.143 или 144, где фрагмент илида сульфоксония имеет формулу (IV):
[0714]
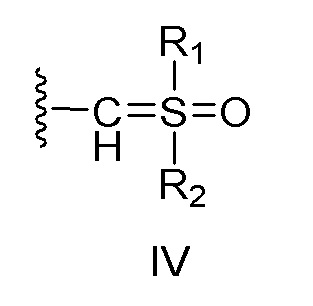
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила.
[0715] 146. Способ по п.145, где R1 представляет собой (C1-C8) алкил, и R2 представляет собой (C1-C8) алкил.
[0716] 147. Способ по п.145, где R1 представляет собой метил, и R2 представляет собой метил.
[0717] 148. Способ определения активности цистеиновой протеазы у субъекта in vivo, включающий:
(1) введение субъекту соединения по любому из пп.78-94 или его соли, или композиции по п.96, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
[0718] 149. Способ по п.148, где соединение или его соль, или композицию вводят внутривенно.
[0719] 150. Способ по любому из пп.143-149, где детектируемый сигнал измеряется с помощью оптического изображения in vivo, радиографии или позитронно-эмиссионной томографии.
[0720] 151. Способ по любому из пп.143-150, где субъектом является человек.
[0721] 152. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой цистеиновую протеазу млекопитающих.
[0722] 153. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой цистеиновую протеазу человека.
[0723] 154. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой цистеиновый катепсин.
[0724] 155. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой цистеиновый катепсин млекопитающих.
[0725] 156. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой цистеиновый катепсин человека.
[0726] 157. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой катепсин X.
[0727] 158. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой катепсин X млекопитающих.
[0728] 159. Способ по любому из пп.97-151, где цистеиновая протеаза представляет собой катепсин X человека.
[0729] 160. Способ по любому из пп.97-159, где детектируется активность катепсина X, и активность катепсина B и/или активность катепсина L не детектируется.
[0730] 161. Способ по любому из пп.97-159, где детектируется активность катепсина X и активность катепсина S, и активность катепсина B и/или активность катепсина L не детектируется.
[0731] 162. Способ ингибирования цистеиновой протеазы, включающий контактирование цистеиновой протеазы с соединением по любому из пп.1-94 или его солью, или с композицией по п.95.
[0732] 163. Способ по п. 162, где способ представляет собой способ in vitro.
[0733] 164. Способ ингибирования цистеиновой протеазы in vitro, включающий контактирование биологического образца с соединением по любому из пп.1-94 или его солью, или с композицией по п.95.
[0734] 165. Способ ингибирования цистеиновой протеазы в биологическом образце, полученном от субъекта, включающий контактирование биологического образца in vitro с соединением по любому из пп.1-94 или его солью, или с композицией по п.95.
[0735] 166. Способ по пп.164 или 165, где биологический образец выбране из группы, состоящей из клеток, клеточных лизатов, образцов тканей, лизатов тканей и жидкостей организма.
[0736] 167. Способ in vivo ингибирования цистеиновой протеазы у субъекта, включающий введение субъекту соединения по любому из пп.1-94 или его соли, или композиции по п.95.
[0737] 168. Способ по п. 167, где соединение или его соль, или композицию вводят внутривенно.
[0738] 169. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой цистеиновую протеазу млекопитающих.
[0739] 170. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой цистеиновую протеазу человека.
[0740] 171. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой цистеиновый катепсин.
[0741] 172. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой цистеиновый катепсин млекопитающих.
[0742] 173. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой цистеиновый катепсин человека.
[0743] 174. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой катепсин X.
[0744] 175. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой катепсин X млекопитающих.
[0745] 176. Способ по любому из пп.162-168, где цистеиновая протеаза представляет собой катепсин X человека.
[0746] 177. Способ по любому из пп.162-176, где ингибируется катепсин X, и катепсин B и/или катепсин L не ингибируются.
[0747] 178. Способ по любому из пп.162-176, где ингибируются катепсин X и катепсин S, и катепсин B и/или катепсин L не ингибируются.
[0748] 179. Способ диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающий:
(1) контактирование биологического образца, полученного от субъекта in vitro, с соединением по любому из пп.78-94 или его солью, или с композицией по п.96, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0749] 180. Способ по п.179, где способ включает определение активности цистеиновой протеазы в соответствии со способом по любому из пп.107-122 и 152-161.
[0750] 181. Способ диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающий:
(1) введение субъекту соединения по любому из пп.78-94 или его соли, или композиции по п.96,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0751] 182. Способ по п.181, где способ включает определение активности цистеиновой протеазы в соответствии со способом по любому из пп.128-142 и 152-161.
[0752] 183. Способ диагностики in vivo заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, включающий:
(1) введение субъекту соединения по любому из пп.78-94 или его соли, или композиции по п.96, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
[0753] 184. Способ по п.183, где способ включает определение активности цистеиновой протеазы в соответствии со способом по любому из пп.148-161.
[0754] 185. Соединение по любому из пп.78-94 или его соль для применения в способе диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту соединения по любому из пп.78-94 или его соли,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0755] 186. Соединение для применения по п.185, где способ включает определение активности цистеиновой протеазы в соответствии со способом по любому из пп.128-142 и 152-161.
[0756] 187. Композиция по п.96 для применения в способе диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту композиции по п.96,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
[0757] 188. Композиция для применения по п.187, где способ включает определение активности цистеиновой протеазы в соответствии со способом по любому из пп.128-142 и 152-161.
[0758] 189. Соединение по любому из пп.78-94 или его соль для применения в способе in vivo диагностики заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту соединения по любому из пп.78-94 или его соли, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
[0759] 190. Соединение для применения по п.189, где способ включает детектирование активности цистеиновой протеазы в соответствии со способом по любому из пп.148-161.
[0760] 191. Композиция по п.96 для применения в способе диагностики in vivo заболевания, ассоциированного с активностью цистеиновой протеазы, у субъекта, где способ включает:
(1) введение субъекту композиции по п.96, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
[0761] 192. Композиция для применения по п.191, где способ включает детектирование активности цистеиновой протеазы в соответствии со способом по любому из пп.148-161.
[0762] 193. Способ лечения заболевания, ассоциированного с активностью цистеиновой протеазы, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения по любому из пп.1-94 или его соли, или терапевтически эффективного количества композиции по п.95.
[0763] 194. Соединение по любому из пп.1-94 или его соль для применения в лечении заболевания, ассоциированного с активностью цистеиновой протеазы.
[0764] 195. Композиция для лечения заболевания, ассоциированного с активностью цистеиновой протеазы, содержащая соединение по любому из пп.1-94 или его соль и фармацевтически приемлемый эксципиент.
[0765] 196. Применение соединения по любому из пп.1-94 или его соли в производстве лекарственного средства для лечения заболевания, ассоциированного с активностью цистеиновой протеазы.
[0766] 197. Применение композиции по п.95 в производстве лекарственного средства для лечения заболевания, ассоциированного с активностью цистеиновой протеазы.
[0767] 198. Способ, применение, соединение для применения или композиция для применения по любому из пп.179-197, где заболевание выбрано из группы, состоящей из целиакии, нарушения моторики желудочно-кишечного тракта, боли, зуда, кожного заболевания, ожирения, вызванного рационом, нарушения обмена веществ, астмы, ревматоидного артрита, пародонтита, воспалительного заболевания, функционального расстройства желудочно-кишечного тракта, рака, фиброзного заболевания, метаболической дисфункции, неврологического заболевания и нейродегенеративного заболевания.
[0768] 199. Способ, применение, соединение для применения или композиция для применения по п.198, где функциональное расстройство желудочно-кишечного тракта выбрано из группы, состоящей из синдрома раздраженного кишечника, функциональной боли в груди, функциональной диспепсии, тошноты и рвоты, функциональных запоров и т. д., функциональной диареи, недержания кала, функциональной аноректальной боли и функциональных нарушений дефекации.
[0769] 200. Способ, применение, соединение для применения или композиция для применения по п.199, где функциональное расстройство желудочно-кишечного тракта представляет собой синдром раздраженного кишечника.
[0770] 201. Способ, применение, соединение для применения или композиция для применения по любому из пп.179-198, где заболевание выбрано из группы, состоящей из рака, воспалительного заболевания и нейродегенеративного заболевания.
[0771] 202. Способ, применение, соединение для применения или композиция для применения по любому из пп.179-198, где заболевание представляет собой рак, выбранный из группы, состоящей из рака молочной железы, рака головного мозга, рака костного мозга, рака поджелудочной железы, рака легкого, рака предстательной железы, рака печени, рака ротовой полости, колоректального рака и рака желудка.
[0772] 203. Способ, применение, соединение для применения или композиция для применения по любому из пп.179-198, где заболевание представляет собой воспалительное заболевание, выбранное из группы, состоящей из воспалительного расстройства желудочно-кишечного тракта, панкреатита и инфекции.
[0773] 204. Способ, применение, соединение для применения или композиция для применения по п.203, где воспалительное расстройство желудочно-кишечного тракта выбрано из группы, состоящей из воспалительного заболевания кишечника, инфекционной диареи, мезентериальной ишемии, дивертикулита и некротического энтероколита (NEC).
[0774] 205. Способ, применение, соединение для применения или композиция для применения по п.204, где воспалительное заболевание кишечника выбрано из группы, состоящей из язвенного колита, болезни Крона, диверсионного колита, колита неопределенной этиологии и паухита, микроскопического колита, иммуноонкологического колита, колита в результате химиотерапии/лучевой терапии, колита на фоне синдрома «трансплантат против хозяина» (GvHD), острого колита, болезни Бехчета, коллагенозного колита и лимфоцитарного колита.
[0775] 206. Способ, применение, соединение для применения или композиция для применения по п.204, где воспалительное заболевание кишечника представляет собой язвенный колит или болезнь Крона.
[0776] 207. Способ, применение, соединение для применения или композиция для применения по любому из пп.179-198, где заболевание представляет собой нейродегенеративное заболевание, выбранное из группы, состоящей из болезни Альцгеймера, рассеянного склероза и нейропатической боли.
[0777] 208. Способ, применение, соединение для применения или композиция для применения по любому из пп.179-207, где заболевание представляет собой заболевание, ассоциированное с активностью катепсина X.
[0778] 209. Способ получения соединения, несущего хлорметилкетоновую группу, включающий взаимодействие соединения, несущего группу илида сульфоксония, с получением соединения, несущего хлорметилкетоновую группу.
[0779] 210. Способ получения соединения-зонда на основе активности, несущего ацилоксиметилкетоновую группу или феноксиметилкетоновую группу в качестве активной группы, включающий:
(i) получение промежуточного соединения, содержащего хлорметилкетоновую группу, взаимодействием соединения, содержащего фрагмент илида сульфоксония, с получением соединения, несущего хлорметилкетоновую группу; и
(ii) дальнейшую обработку соединения, содержащего хлорметилкетоновую группу, с получением указанного соединения-зонда на основе активности.
[0780] 211. Способ по пп.209 или 210, где соединение, несущее фрагмент илида сульфоксония, подвергают взаимодействию с соляной кислотой с получением соединения, содержащего хлорметилкетоновую группу.
[0781] 212. Способ по любому из пп.209-211, где фрагмент илида сульфоксония имеет формулу (IV):
[0782]
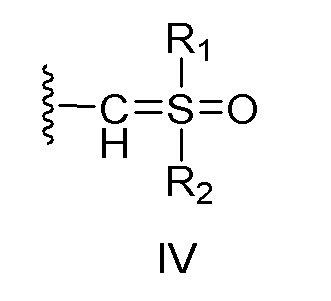
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; и
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила.
[0783] 213. Способ по п.212, где R1 представляет собой (C1-C8) алкил, и R2 представляет собой (C1-C8) алкил.
[0784] 214. Способ по п.212, где R1 представляет собой метил, и R2 представляет собой метил.
[0785] 215. Соединение, выбранное из группы формул, состоящей из:
[0786]
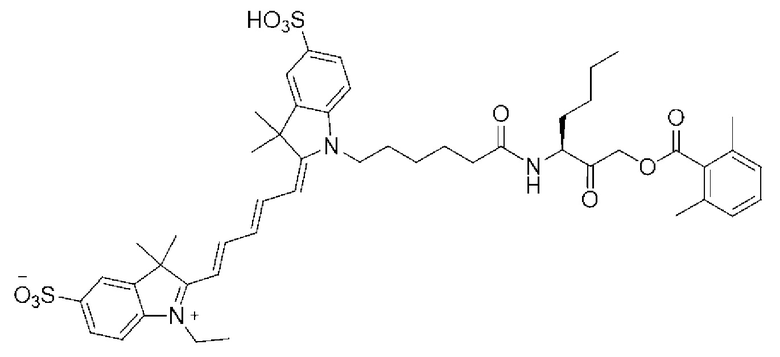
[0787]
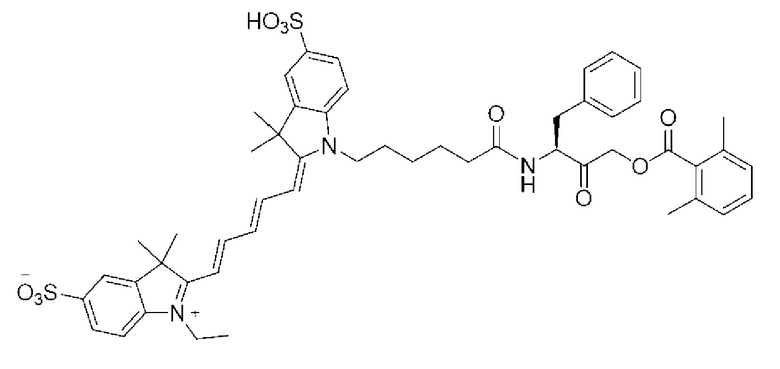
[0788]
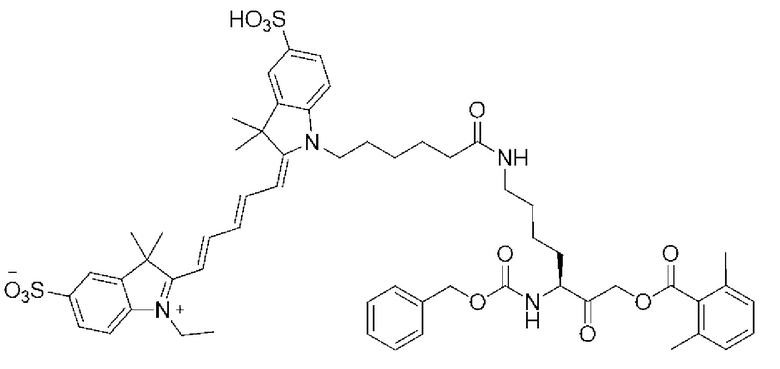
или его соль.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ЗОНДЫ НА ОСНОВЕ АКТИВНОСТИ ДЛЯ НЕЙТРОФИЛЬНОЙ ЭЛАСТАЗЫ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2823716C2 |
| АМИНО-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 3-ГЕТЕРОАРОИЛАМИНОПРОПИОНОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2012 |
|
RU2605600C2 |
| НОВЫЕ ТЕТРАЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ ЦИСТЕИНОВЫХ ПРОТЕАЗ, ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ОБЛАСТИ ИХ ТЕРАПЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2007 |
|
RU2481349C2 |
| ИНГИБИТОРЫ АКТИВИН-РЕЦЕПТОРОПОДОБНОЙ КИНАЗЫ | 2018 |
|
RU2788628C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 3-ТИАЗОЛОАМИНОПРОПИОНОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ | 2012 |
|
RU2617843C2 |
| НОВЫЕ АГОНИСТЫ NPR-B | 2010 |
|
RU2557290C2 |
| СРЕДСТВА ВИЗУАЛИЗАЦИИ ДЛЯ МЕЧЕННОГО РАДИОАКТИВНЫМ ИЗОТОПОМ ЭКЗОГЕННОГО И ЭНДОГЕННОГО АЛЬБУМИНА | 2019 |
|
RU2819907C2 |
| АГЕНТЫ, СВЯЗЫВАЮЩИЕСЯ С АМИЛОИДАМИ | 2010 |
|
RU2517174C2 |
| ПРОИЗВОДНЫЕ РОДАНИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ ГИПОГЛИКЕМИЧЕСКИХ АГЕНТОВ И ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 1993 |
|
RU2131251C1 |
| ПИРРОЛОПИРРОЛОВЫЕ КОМПОЗИЦИИ В КАЧЕСТВЕ АКТИВАТОРОВ ПИРУВАТКИНАЗЫ (PKR) | 2018 |
|
RU2736217C2 |
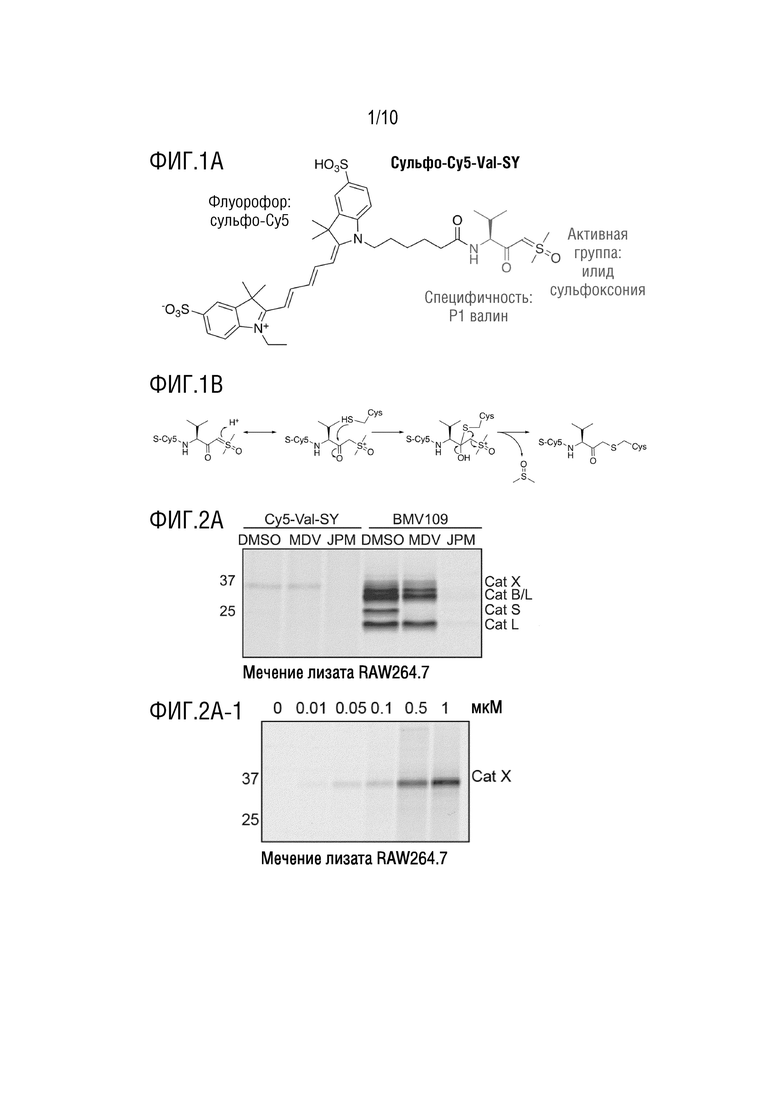
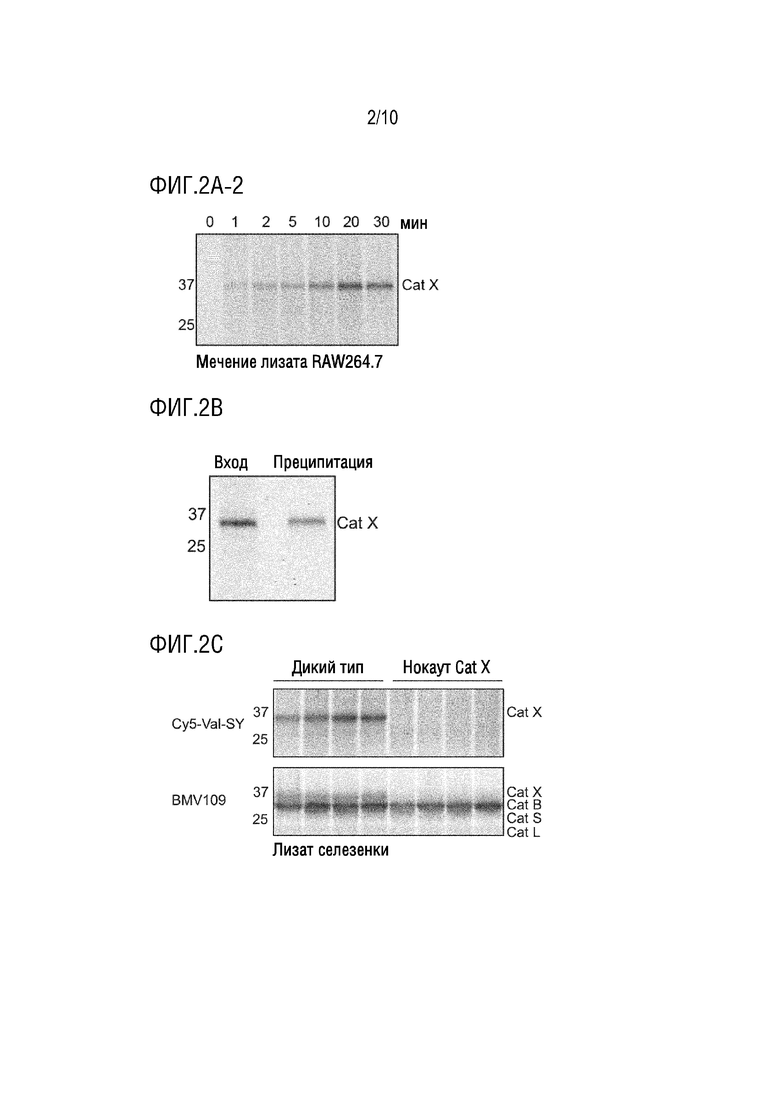
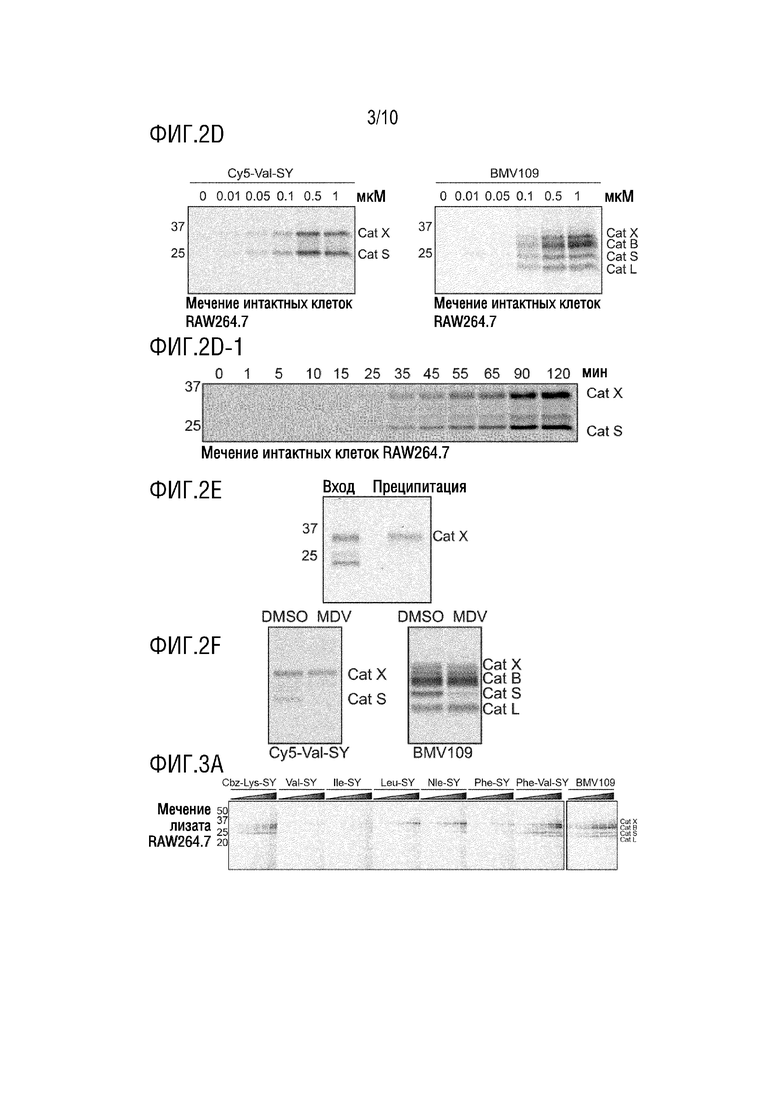

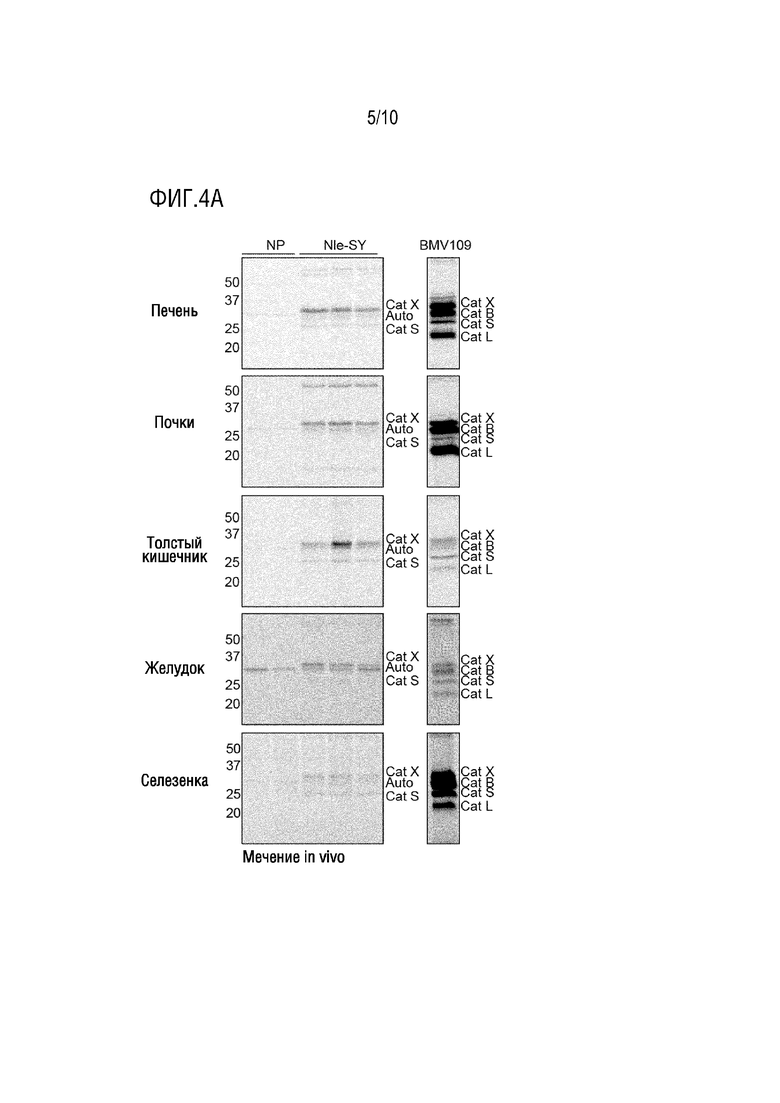
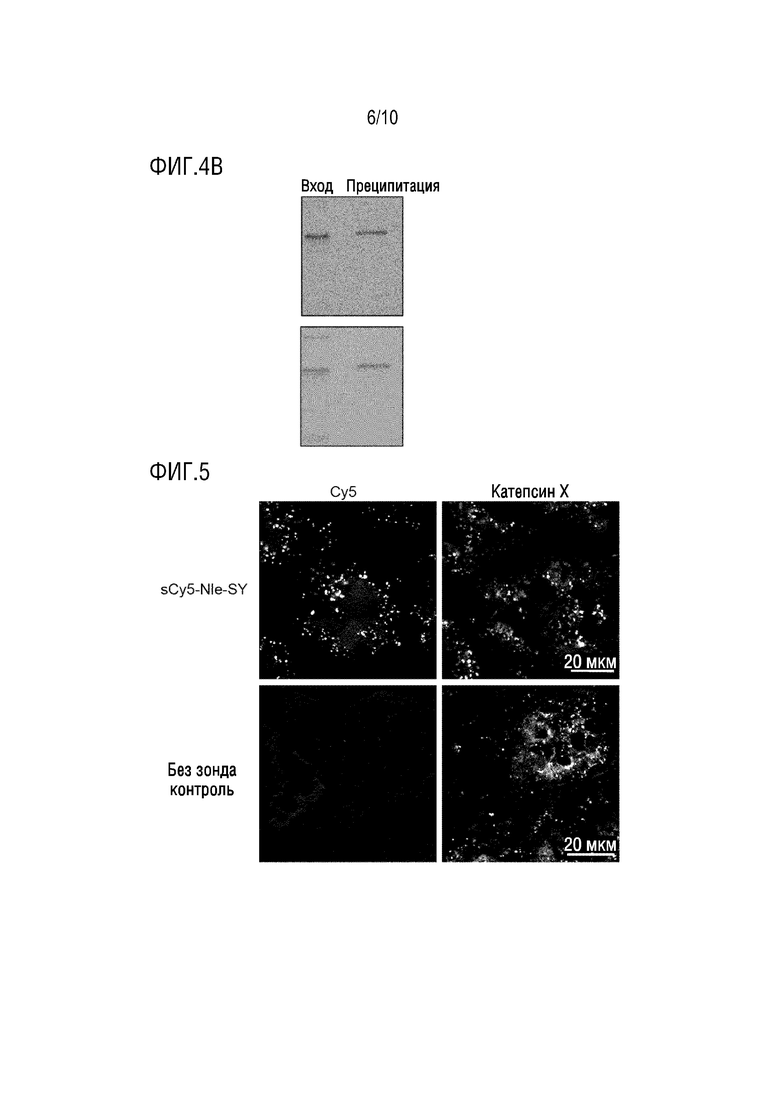
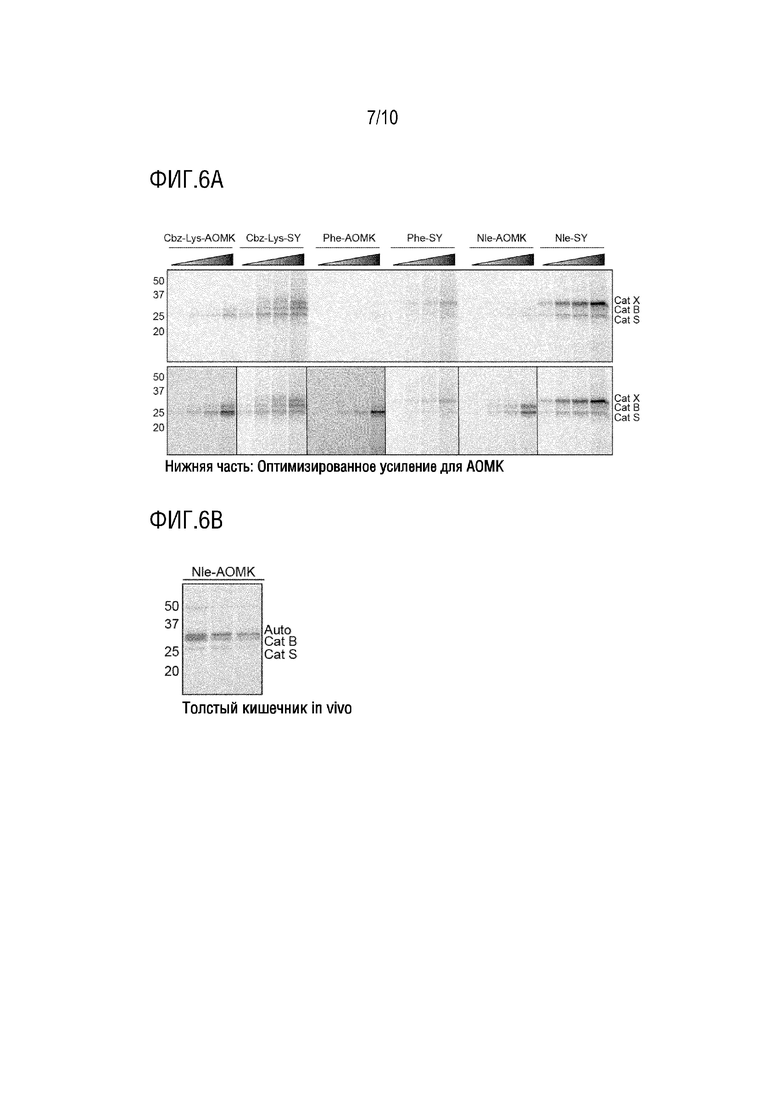
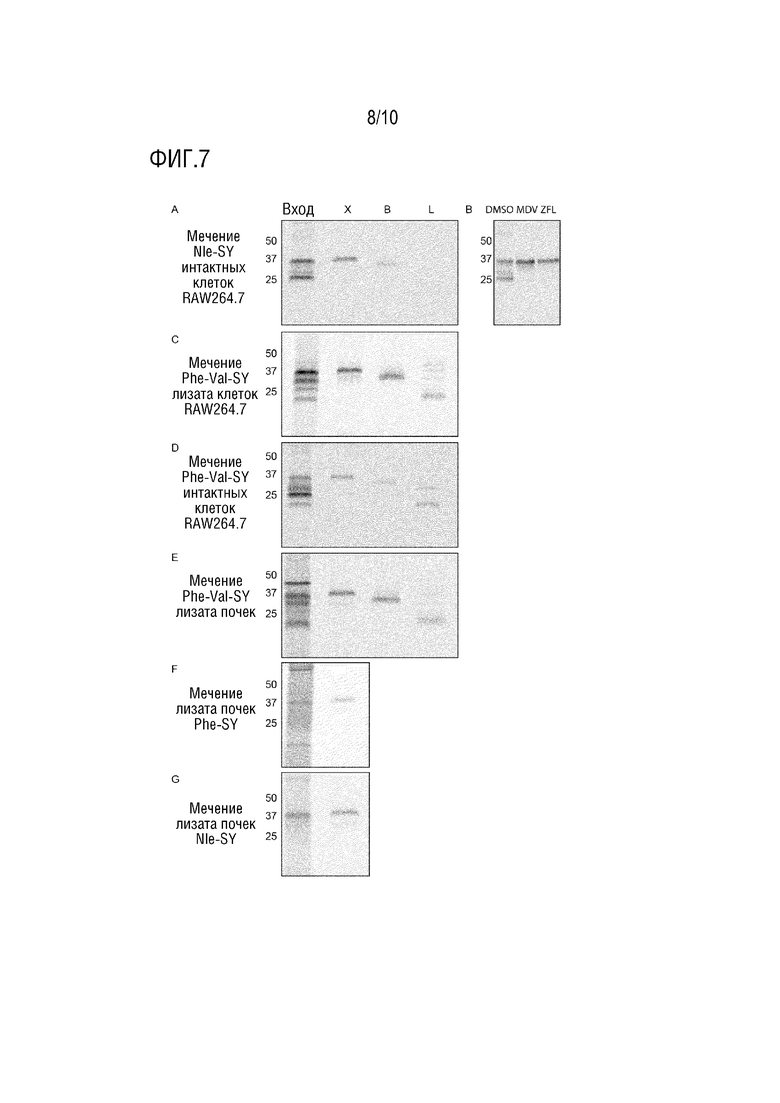
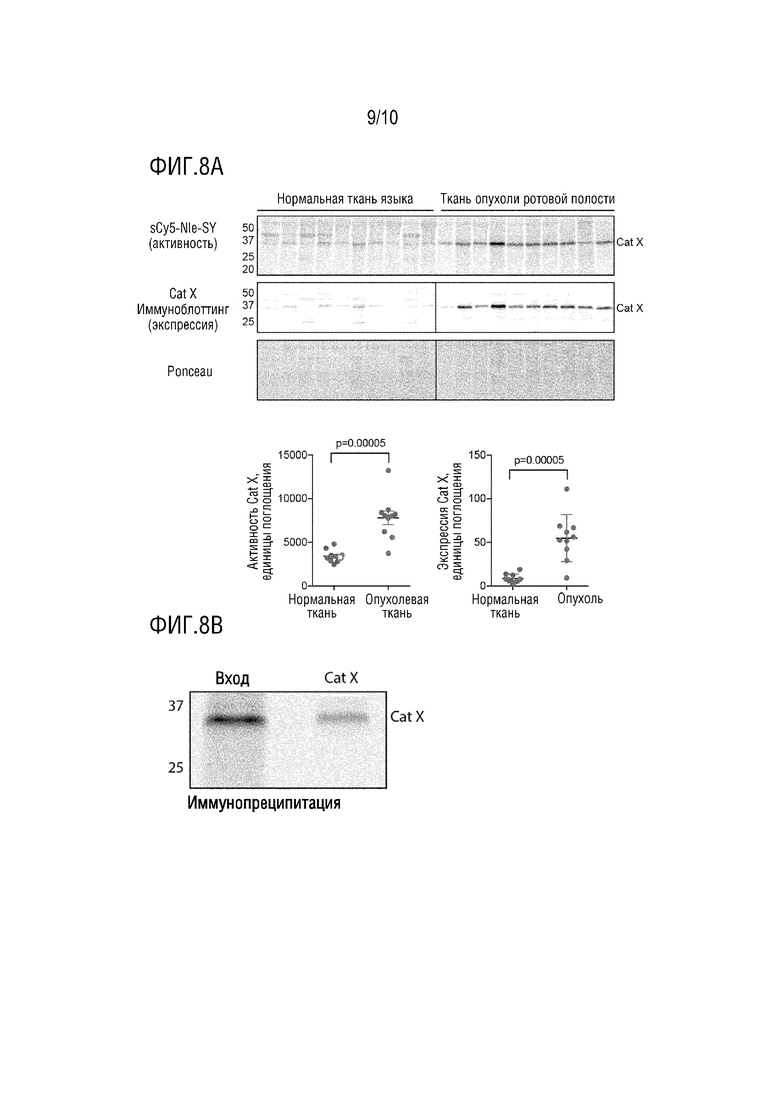

Изобретение относится к соединению формулы I или к его соли, где R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила; R3 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина, где указанная боковая цепь необязательно замещена аминозащитной группой и необязательно дополнительно замещена одним или более одинаковыми или разными заместителями R3x, где R3x выбран из группы, состоящей из гидрокси, галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси; R4 выбран из группы, состоящей из атома водорода и (C1-C4) алкила; R5 представляет собой детектируемый элемент, который представляет собой флуоресцентную метку, представляющую собой цианиновую метку; X представляет собой: (i) связь; или (ii) бирадикальный фрагмент формулы II, который связан с заместителем R5 через аминогруппу, где R6 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина, где указанная боковая цепь необязательно замещена аминозащитной группой и необязательно дополнительно замещена одним или более одинаковыми или разными заместителями R6x, где R6x выбран из группы, состоящей из гидрокси, галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси; R7 выбран из группы, состоящей из атома водорода и (C1-C4) алкила; и где аминозащитную группу выбирают из группы, состоящей из бензилоксикарбонила (Cbz), 9-флуоренилметилоксикарбонила (Fmoc), трет-бутилоксикарбонила (Boc), аллилоксикарбонила (Alloc), п-толуолсульфонила (Tos), 2,2,5,7,8-пентаметилхроман-6-сульфонила (Pmc), 2,2,4,6,7-пентаметил-2,3-дигидробензофуран-5-сульфонила (Pbf), мезитил-2-сульфонила (Mts), 4-метокси-2,3,6-триметилфенилсульфонила (Mtr), ацетамидо, и фталимидо. Изобретение также относится к композициям, действующим в качестве зондов на основе ингибиторов катепсина Х, содержащей соединение формулы I, а также способам детектирования активности катепсина Х. Технический результат – получены новые соединения, которые могут найти применение в медицине в качестве зондов на основе активности для цистеиновых протеаз, таких как катепсин X, а также в способах детектирования активности цистеиновых протеаз и в связанных диагностических или терапевтических способах. 7 н. и 39 з.п. ф-лы, 25 ил., 1 табл., 14 пр.
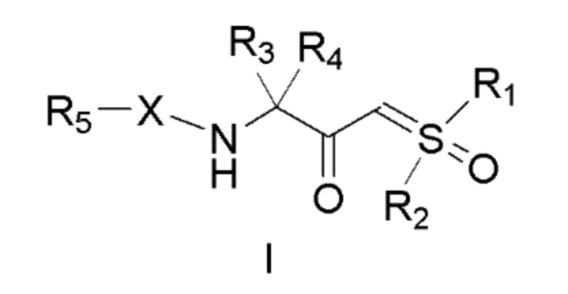
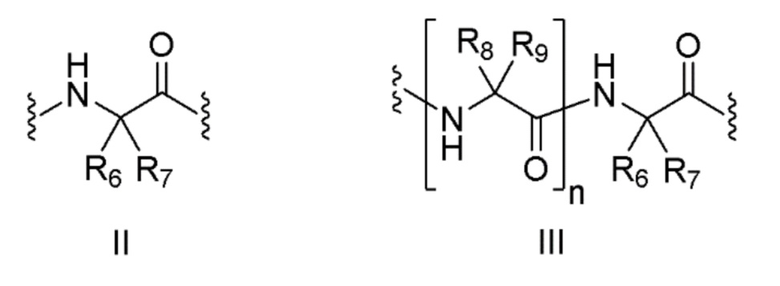
1. Соединение формулы I
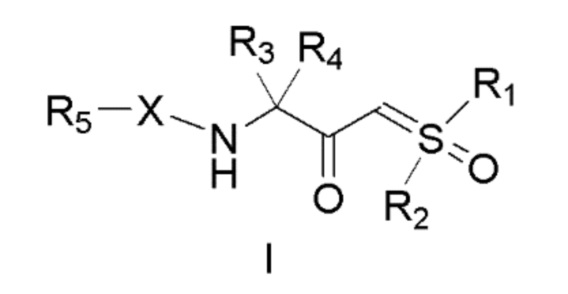
или его соль,
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R3 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина,
где указанная боковая цепь необязательно замещена аминозащитной группой и необязательно дополнительно замещена одним или более одинаковыми или разными заместителями R3x, где R3x выбран из группы, состоящей из гидрокси, галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси;
R4 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R5 представляет собой детектируемый элемент, который представляет собой флуоресцентную метку, представляющую собой цианиновую метку;
X представляет собой:
(i) связь; или
(ii) бирадикальный фрагмент формулы II, который связан с заместителем R5 через аминогруппу:
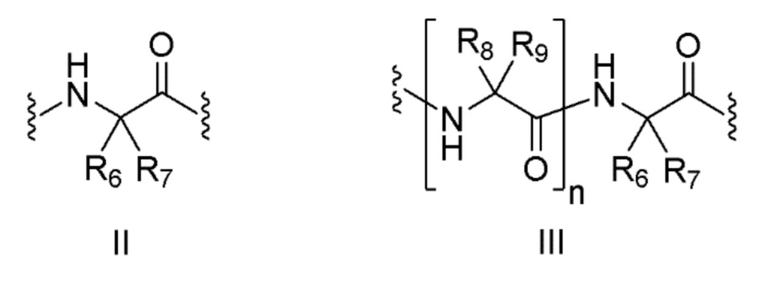
где:
R6 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина,
где указанная боковая цепь необязательно замещена аминозащитной группой и необязательно дополнительно замещена одним или более одинаковыми или разными заместителями R6x, где R6x выбран из группы, состоящей из гидрокси, галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси;
R7 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
и
где аминозащитную группу выбирают из группы, состоящей из бензилоксикарбонила (Cbz), 9-флуоренилметилоксикарбонила (Fmoc), трет-бутилоксикарбонила (Boc), аллилоксикарбонила (Alloc), п-толуолсульфонила (Tos), 2,2,5,7,8-пентаметилхроман-6-сульфонила (Pmc), 2,2,4,6,7-пентаметил-2,3-дигидробензофуран-5-сульфонила (Pbf), мезитил-2-сульфонила (Mts), 4-метокси-2,3,6-триметилфенилсульфонила (Mtr), ацетамидо, и фталимидо.
2. Соединение по п.1,
где R3 представляет боковую цепь альфа-аминокилоты, выбранную из группы, состоящей из аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, фенилаланина и триптофана.
3. Соединение по п.1 или 2, где R3 представляет боковую цепь альфа-аминокилоты, выбранную из группы, состоящей из валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, фенилаланина и триптофана.
4. Соединение формулы I

или его соль,
где:
R1 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R2 выбран из группы, состоящей из (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила и (C2-C8) алкинила;
R3 представляет собой боковую цепь лизина, где указанная боковая цепь замещена детектируемым элементом и необязательно дополнительно замещена одним или более одинаковыми или разными заместителями R3x, где R3x выбран из группы, состоящей из гидрокси, галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси;
R4 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
R5 выбран из группы, состоящей из аминозащитной группы, (C1-C8) алкила, (C1-C8) гидроксиалкила, (C1-C8) галогеналкила, (C3-C8) циклоалкила, (C2-C8) алкенила, (C2-C8) алкинила, (C1-C8) алкилкарбонила, (C1-C8) гидроксиалкилкарбонила, (C1-C8) галогеналкилкарбонила, (C3-C8) циклоалкилкарбонила, (C1-C8) алкилоксикарбонила, бензилоксикарбонила и атома водород;
X представляет собой:
(i) связь; или
(ii) бирадикальный фрагмент формулы II, который связан с заместителем R5 через аминогруппу:

где:
R6 представляет собой боковую цепь альфа-аминокислоты, выбранной из группы, состоящей из глицина, аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина, метионина, этионина, фенилаланина, тирозина, леводопы, триптофана, цистеина, гомоцистеина, селеноцистеина, селеногомоцистеина, селенометионина, селеноэтионина, лизина, гистидина, аргинина, орнитина, аспарагиновой кислоты, глутаминовой кислоты, серина, гомосерина, О-метилгомосерина, О-этилгомосерина, треонина, аспарагина и глутамина,
где указанная боковая цепь необязательно замещена аминозащитной группой и необязательно дополнительно замещена одним или более одинаковыми или разными заместителями R3x, где R3x выбран из группы, состоящей из гидрокси, галогена, (C1-C4) алкила, (C1-C4) гидроксиалкила, (C1-C4) галогеналкила, (C1-C4) алкокси и (C1-C4) галогеналкокси;
R7 выбран из группы, состоящей из атома водорода и (C1-C4) алкила;
где детектируемый элемент представляет собой флуоресцентную метку, где флуоресцентная метка представляет собой цианиновую метку, и
где аминозащитную группу выбирают из группы, состоящей из бензилоксикарбонила (Cbz), 9-флуоренилметилоксикарбонила (Fmoc), трет-бутилоксикарбонила (Boc), аллилоксикарбонила (Alloc), п-толуолсульфонила (Tos), 2,2,5,7,8-пентаметилхроман-6-сульфонила (Pmc), 2,2,4,6,7-пентаметил-2,3-дигидробензофуран-5-сульфонила (Pbf), мезитил-2-сульфонила (Mts), 4-метокси-2,3,6-триметилфенилсульфонила (Mtr), ацетамидо, и фталимидо.
5. Соединение по п.4, где R5 представляет собой аминозащитную группу.
6. Соединение по любому из пп.1-5, где R1 представляет собой (C1-C8) алкил и R2 представляет собой (C1-C8) алкил.
7. Соединение по п.6, где R1 и R2 представляют собой метил.
8. Соединение по любому из пп.1-7, где R4 представляет собой атом водорода.
9. Соединение по любому из пп.1-8,
где R6 представляет собой боковую цепь альфа-аминокислоты, выбранную из группы, состоящей из аланина, альфа-аминомасляной кислоты, валина, норвалина, лейцина, изолейцина, норлейцина, гомонорлейцина и фенилаланина.
10. Соединение по п.9, где R6 представляет собой боковую цепь фенилаланина.
11. Соединение по любому из пп.1-10, где R7 представляет собой атом водорода.
12. Соединение по любому из пп.1-11, где аминозащитная группа выбрана из группы, состоящей из бензилоксикарбонила (Cbz), 9-флуоренилметилоксикарбонила (Fmoc), и трет-бутилоксикарбонила (Boc), аллилоксикарбонила (Alloc).
13. Соединение по п.12, где аминозащитная группа представляет собой бензилоксикарбонил.
14. Соединение по любому из пп.1-13, где формула I имеет формулу IA
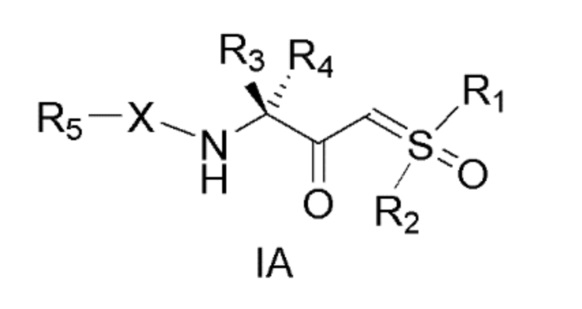
и где бирадикальный фрагмент формулы II имеет формулу IIA:
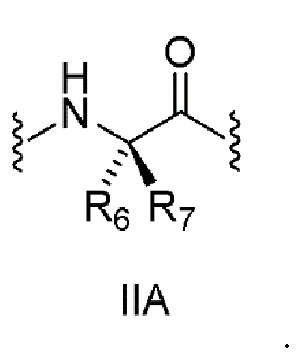
15. Соединение по любому из пп.1-14, где X представляет собой связь.
16. Соединение по любому из пп.1-15, где цианиновая метка имеет формулу, выбранную из следующей группы формул:
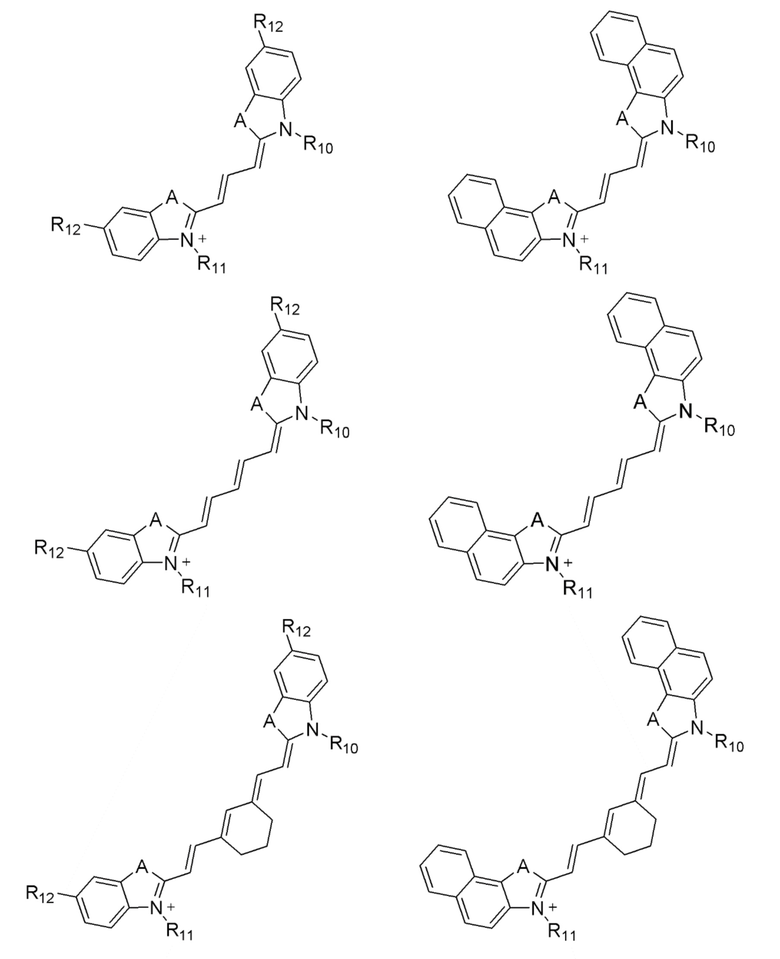
где в каждой из вышеприведенных формул,
A выбран из группы, состоящей из CH2, C(CH3)2, C(C2H5)2, NH, N(CH3), N(C2H5), O, S и Se;
R10 выбран из группы, состоящей из $-(CH2)p-C(=O)-& и $-(CH2)q-C(=O)-NH-[CH2CH2O]r-CH2CH2-C(=O)-&;
где:
p равно 2, 3, 4, 5, 6, 7 или 8;
q равно 2, 3, 4, 5, 6, 7 или 8;
r равно 2, 3, 4, 5, 6, 7 или 8;
$ представляет собой точку соединения с атомом азота цианиновой группы; и & представляет собой точку соединения с остальной частью молекулы;
R11 выбран из группы, состоящей из (C1-C8) алкила и (C6-C10) арила; и
R12 представляет собой H или сульфогруппу.
17. Соединение по п.16, где цианиновая метка, имеет формулу, выбранную из следующей группы формул:
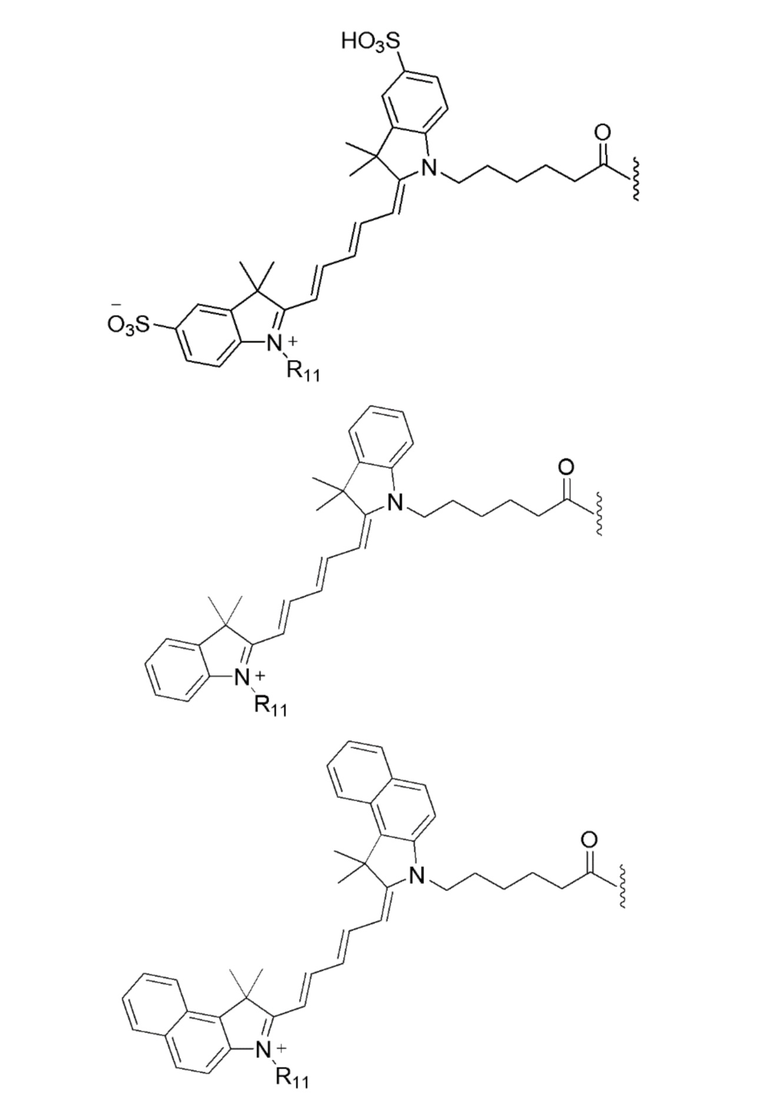
где в каждой из вышеприведенных формул,
волнистая линия представляет собой точку соединения с остальной частью молекулы;
и R11 выбран из группы, состоящей из (C1-C8) алкила и (C6-C10) арила.
18. Соединение по п.17, где цианиновая метка, имеет формулу:
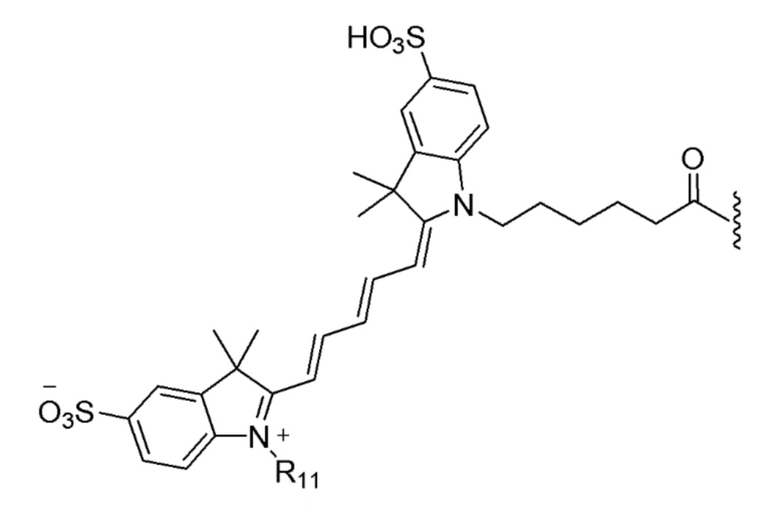
где волнистая линия представляет собой точку соединения с остальной частью молекулы; и R11 представляет собой метил или этил.
19. Соединение по любому из пп.4-18, где R3 представляет собой -CH2CH2CH2CH2N(R3a)(R3b); где:
R3a представляет собой детектируемый элемент; и
R3b выбран из группы, состоящей из атома водорода и (C1-C4) алкила.
20. Соединение по п.1, которое представляет собой соединение, выбранное из группы формул, состоящей из:
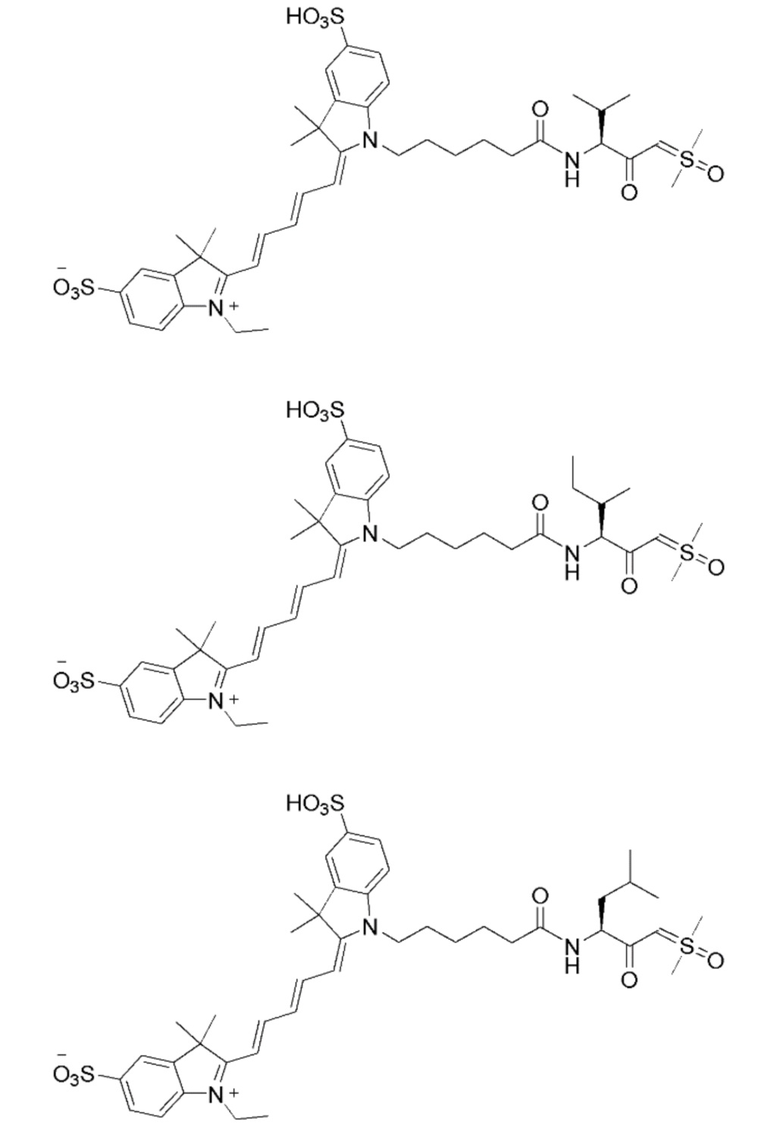
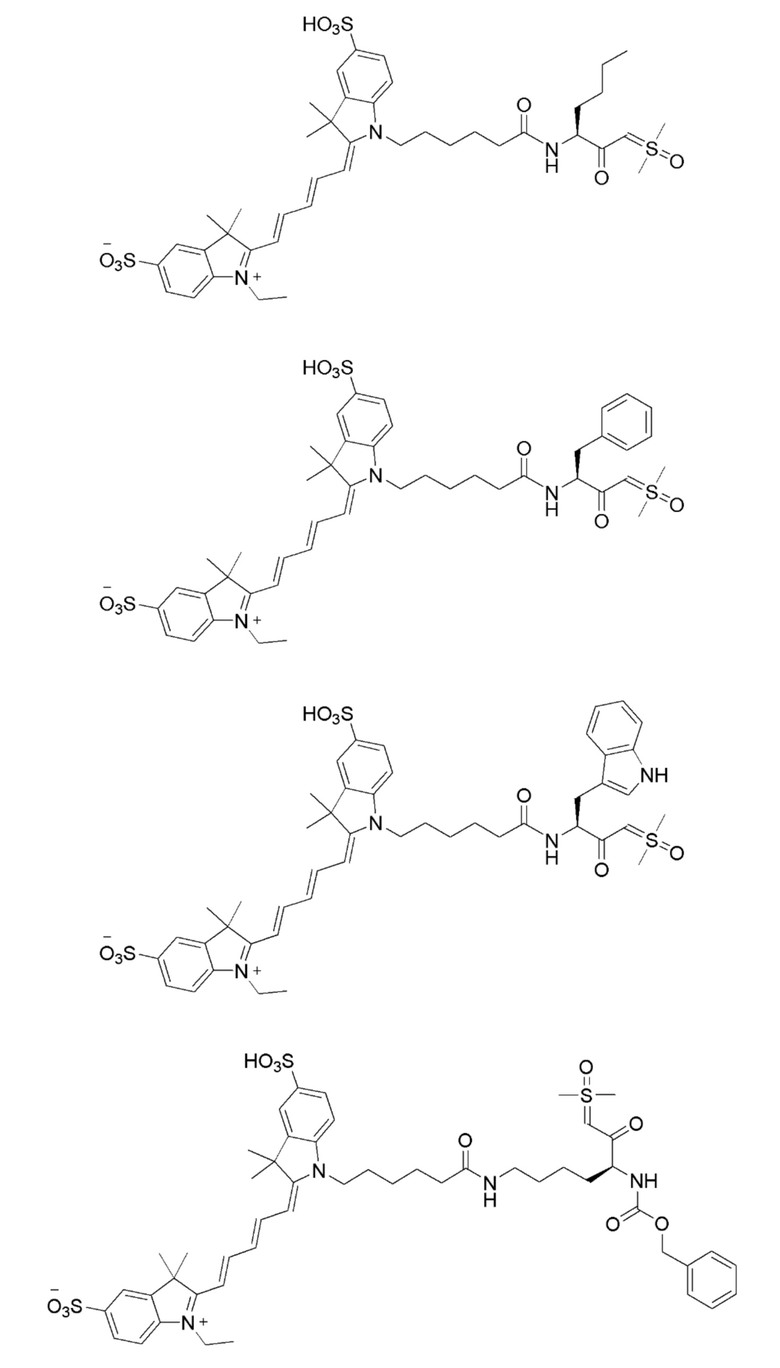
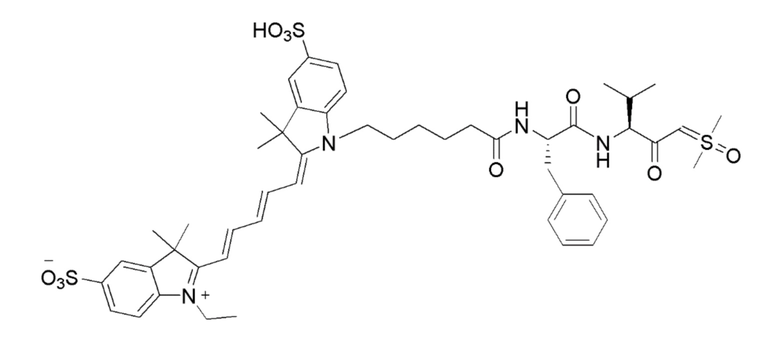
или его соль;
где необязательно соединение представляет собой соединение формулы:
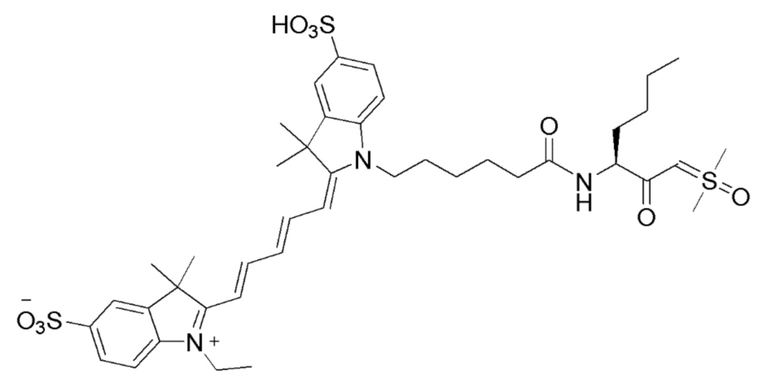
или его соль.
21. Соединение по п.4, которое представляет собой
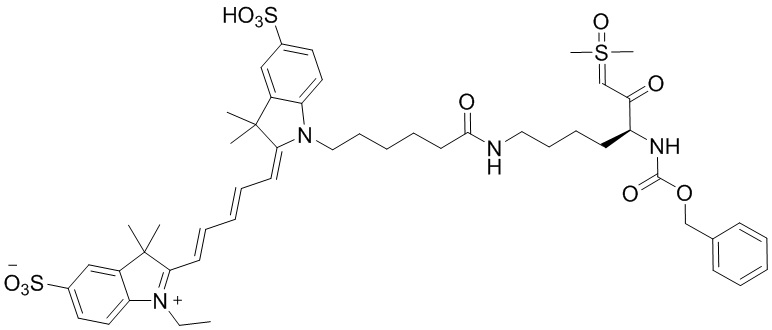
или его соль.
22. Композиция, действующая в качестве зондов на основе активности или ингибиторов катепсина X, содержащая эффективное количество соединения по любому из пп.1-21 или его фармацевтически приемлемой соли, и эксципиент.
23. Композиция, действующая в качестве зондов на основе активности для катепсина X in vitro, содержащая эффективное количество соединения по любому из пп.1-21 или его соли, и эксципиент.
24. Способ детектирования активности катепсина Х в биологическом образце, полученном от субъекта, включающий:
(1) контактирование биологического образца in vitro с соединением по любому из пп.1-21 или его солью, или с композицией по п.23, и
(2) последующий анализ биологического образца, включающий измерение детектируемого сигнала.
25. Способ по п.24, где стадия (2) включает выполнение, по меньшей мере, одного аналитического метода, выбранного из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, гель-электрофореза и последующей радиографии, гель-электрофореза и последующего иммуноблоттинга, флуоресцентной микроскопии, проточной цитометрии, оптической визуализации ex vivo, радиографии, аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики.
26. Способ по любому из пп.24, 25, где детектируемый сигнал измеряется посредством измерения флуоресценции;
где необязательно, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, флуоресцентной микроскопии и проточной цитометрии.
27. Способ по любому из пп.24-26,
где гель-электрофорез представляет собой одномерный или двумерный гель-электрофорез; и/или
где гель-электрофорез представляет собой SDS-PAGE.
28. Способ по любому из пп.24-27,
где биологический образец выбран из группы, состоящей из клеток, клеточных лизатов, образцов тканей, лизатов тканей и жидкостей организма.
29. Способ по п.28,
где биологический образец представляет собой лизат клеток или лизат ткани; или
где биологический образец представляет собой очищенный лизат клеток или очищенный лизат тканей; или
где биологический образец представляет собой живые клетки; или
где живые клетки лизируют и очищают между стадией (1) и стадией (2).
30. Способ детектирования активности катапсина Х, включающий:
(1) введение субъекту соединения по любому из пп.1-21 или его фармацевтически приемлемой соли, или композиции по п.22,
последующее получение биологического образца от субъекта; и
последующий анализ биологического образца, включающий измерение детектируемого сигнала.
31. Способ по п.30, где стадия (3) включает выполнение, по меньшей мере, одного аналитического метода, выбранного из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, гель-электрофореза и последующей радиографии, гель-электрофореза и последующего иммуноблоттинга, флуоресцентной микроскопии, проточной цитометрии, оптической визуализации ex vivo, радиографии, аффинной очистки и последующей масс-спектрометрии, аффинной очистки и последующей протеомики.
32. Способ по любому из пп.30, 31, где детектируемый сигнал измеряется посредством измерения флуоресценции; и/или
где, по меньшей мере, один аналитический метод выбран из группы, состоящей из гель-электрофореза и последующей флуоресценции в геле, флуоресцентной микроскопии и проточной цитометрии.
33. Способ по любому из пп.30-32, где гель-электрофорез представляет собой одномерный или двумерный гель-электрофорез; и/или
где гель-электрофорез представляет собой SDS-PAGE.
34. Способ по любому из пп.30-34,
где биологический образец выбран из группы, состоящей из клеток, клеточных лизатов, образцов тканей, лизатов тканей и жидкостей организма; где необязательно биологический образец представляет собой лизат клеток или лизат ткани; или
где биологический образец представляет собой очищенный лизат клеток или очищенный лизат тканей.
35. Способ по любому из пп.30-34, где субъектом является человек.
36. Способ детектирования активности катапсина Х у субъекта in vivo, включающий:
(1) введение субъекту соединения по любому из пп.1-21 или его фармацевтически приемлемой соли, или композиции по п.22, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала.
37. Способ по п.36,
где детектируемый сигнал измеряется с помощью оптического изображения in vivo, радиографии или позитронно-эмиссионной томографии.
38. Способ по п.36 или 37, где субъектом является человек.
39. Способ по любому из пп.24-38, где катепсин Х представляет собой катепсин X млекопитающих, и необязательно катепсин X человека.
40. Способ по любому из пп.24-39,
где детектируется активность катепсина X, и активность катепсина B и/или активность катепсина L не детектируется.
41. Способ по любому из пп.24-40, где детектируется активность катепсина X и активность катепсина S, и активность катепсина B и/или активность катепсина L не детектируются.
42. Соединение по любому из пп.1-21 или его фармацевтически приемлемая соль для применения в способе диагностики заболевания, ассоциированного с активностью катепсина Х, у субъекта, где способ включает:
(1) введение субъекту соединения по любому из пп.1-21 или его фармацевтически приемлемой соли,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала;
где необязательно способ включает детектирование активности катепсина Х в соответствии со способом по любому из пп.30-35 и 39-41.
43. Композиция по п.22, для применения в способе диагностики заболевания, ассоциированного с активностью катепсина Х, у субъекта, где способ включает:
(1) введение субъекту композиции по п.22,
(2) последующее получение биологического образца от субъекта; и
(3) последующий анализ биологического образца, включающий измерение детектируемого сигнала;
где необязательно способ включает детектирование активности катепсина Х в соответствии со способом по любому из пп.30-35 и 39-41.
44. Соединение по любому из пп.1-21 или его фармацевтически приемлемая соль для применения в способе in vivo диагностики заболевания, ассоциированного с активностью катепсина Х, у субъекта, где способ включает:
(1) введение субъекту соединения по любому из пп.1-21 или его фармацевтически приемлемой соли, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала;
где необязательно способ включает определение активности катепсина Х в соответствии со способом по любому из пп.36-38.
45. Композиция по п.22 для применения в способе диагностики in vivo заболевания, ассоциированного с активностью катепсина Х, у субъекта, где способ включает:
(1) введение субъекту композиции по п.22, и
(2) последующее обследование субъекта, включающее измерение детектируемого сигнала;
где необязательно способ включает детектирование активности катепсина Х в соответствии со способом по любому из пп.36-38.
46. Соединение по любому из пп.1-21 или его фармацевтически приемлемая соль в эффективном количестве для применения при лечении заболевания, ассоциированного с активностью катепсина Х,
где заболевание выбрано из группы, состоящей из целиакии, нарушения моторики желудочно-кишечного тракта, боли, зуда, кожного заболевания, ожирения, вызванного рационом, нарушения обмена веществ, астмы, ревматоидного артрита, пародонтита, воспалительного заболевания, функционального расстройства желудочно-кишечного тракта, рака, фиброзного заболевания, метаболической дисфункции, неврологического заболевания и нейродегенеративного заболевания.
| WO 2010117796 A2, 14.10.2010 | |||
| US 20050090670 A1, 28.04.2005 | |||
| WO 2014145257 A2, 18.09.2014 | |||
| MARGOT G | |||
| PAULICK et al., ACS Chemical Biology, vol.6, no.6, 2011, pp | |||
| РАДИОПРИЕМНИК - ВОЛНОМЕР | 1923 |
|
SU563A1 |
| EA 200901123 A1, 26.02.2010. | |||
Авторы
Даты
2024-03-11—Публикация
2019-12-20—Подача