Изобретение относится к онкологии, молекулярной биологии и клинической лабораторной диагностике, к способам прогнозирования риска опухолевой прогрессии у больных раком яичников (РЯ) до начала лечения.
Рак яичников (РЯ) является одним из главных «онкологических убийц» женского населения в XXI веке: первое место среди смертности от онкогинекологических заболеваний и пятое место среди смертности женского населения по причине онкопатологии [1]. Проблема высокой смертности при раке яичников объясняется многими факторами, важнейшими из которых являются диагностика на запущенных стадиях, скрытым течением заболевания и высокий риск рецидивирования.
В связи с вышесказанным, возникает необходимость разработки и интегрирования в систему здравоохранения алгоритма оценки риска рецидивирования рака яичников для своевременного прогнозирования вероятности опухолевой прогрессии.
В настоящее время известны такие факторы прогноза как: стадия заболевания, гистологический тип опухоли, степень дифференцировки опухоли, объем остаточных опухолевых масс при циторедуктивных операциях, возраст больных. Также имеются данные о прогностической значимости маркера СА-125. Чувствительность для серозного рака яичников колеблется от 42 до 99% при III-IV стадии, поэтому использование СА-125 в комбинации с другими факторами повышает специфичность и чувствительность теста [2]. Однако данный онкомаркер не является строго специфичным, так как его повышение может быть связано с беременностью, эндометриозом, воспалительными заболеваниями в малом тазу, доброкачественными опухолевыми процессами [3].
Одним из основных причин возникновения рецидивов и метастазов являются циркулирующие опухолевые клетки (ЦОК). Известно, что популяция ЦОК гетерогенна [4-6].
Недавние исследования выявили наличие в асцитической жидкости больных раком яичников атипичных/гибридных форм EpCam+CD45+ опухолевых клеток, концентрация которых прямо коррелирует со степенью канцероматоза [7, 8]. Описано обнаружение EpCam+CD45+ клеток задолго до появления метастазов, что потенциально делает их предвестником скорого распространения опухоли [6, 9, 10].
Известен способ прогнозирования рецидива рака яичников, заключающийся в том, что в опухолевой ткани яичников определяют долю клеток в S фазе клеточного цикла, при значении этого показателя менее 15,9% прогнозируют благоприятный исход, а при значении этого показателя более 15,9% прогнозируют неблагоприятный исход (патент RU №2530556 С1, 10.10.2014) [11].
Известен способ прогнозирования продолжительности безрецидивного периода у больных серозным раком яичников (патент RU№2299018 C1, 20.05.2007) включающий оценку следующих морфологических параметров опухоли: степень дифференцировки опухоли в баллах (X1): при низкой степени дифференцировки - 1 балл, при умеренной - 2 балла, при высокой - 3 балла; площадь ядра раковой клетки в мкм (Х2), измеряемого окуляром-микрометром или анализатором телевизионного изображения; митотический индекс (Х3), определяемый путем подсчета общего количества фигур деления на 1000 опухолевых клеток; удельную долю «летальных» форм митозов от общего количества (%) (Х4); количество свободных клеток на 10000 мкм площади стромы (Х5), определяемое анализатором телевизионного изображения; плотность васкуляризации (мкм2) на 1000 мкм2 площади стромы (Х6), определяемую при помощи анализатора телевизионного изображения, и срок наступления рецидива (Y) в месяцах определяют по формуле:
Y(мес)=(-30,42)-12,31⋅Х1+0,04Х2-1,61⋅Х3+1,41 Х4+1,13⋅Х5+1,29Х6.
Недостатком существующих способов является то, что все они основаны на исследовании операционного материала опухолевой ткани и не дают возможности оценить риск рецидива и метастазирования РЯ до начала лечения. Описанные изобретения используют в анализе способы, обладающие недостаточной чувствительностью и специфичностью.
Новый технический результат - повышение точности и снижение инвазивности способа, возможность прогнозирования течения заболевания до проведения лечения для определения более оптимальной тактики ведения и создания персонализированного подхода при лечении таких пациенток.
Для достижения нового технического результата в способе прогнозирования риска опухолевой прогрессии у больных раком яичников, включающем исследование биологического материала пациента, до начала лечения исследуют кровь и асцитическую жидкость в которой методом проточной цитометрии определяют количество атипичных/гибридных Epcam+CD45+клеток, методом ИФА определяют уровень онкомаркеров крови СА125 и НЕ4, вероятность развития опухолевой прогрессии в виде рецидив и метастазов рассчитывают по формуле:
р=1-1/(1+ЕХР(0,099*Х1-0,003*Х2+0,006*ХЗ+0,446*Х4-2,493)),
где
X1 - количество атипичных/гибридных Epcam+CD45+клеток в асцитической жидкости, клеток/мм3;
Х2 - уровень онкомаркера СА125 в крови, Ед/мл;
Х3 - уровень онкомаркера НЕ4 в крови, рМ;
Х4 - количество атипичных/гибридных Epcam+CD45+клеток в крови, клеток/мм3 и при р более 0,5459 определяют высокий, а при р менее, либо равном 0,5459 определяют низкий риск опухолевой прогрессии.
Способ осуществляют следующим образом. До начала лечения исследуют кровь и асцитическую жидкость, в которой методом проточной цитометрии определяют количество атипичных/гибридных Epcam+CD45+клеток, методом ИФА определяют уровень онкомаркеров крови СА125 и НЕ4, вероятность развития опухолевой прогрессии в виде рецидив и метастазов рассчитывают по формуле:
р=1-1/(1+ЕХР(0,099*Х1-0,003*Х2+0,006*Х3+0,446*Х4-2,493)), где
X1 - количество атипичных/гибридных Epcam+CD45+клеток в асцитической жидкости, клеток/мм3;
Х2 - уровень онкомаркера СА125 в крови, Ед/мл;
Х3 - уровень онкомаркера НЕ4 в крови, рМ;
Х4 - количество атипичных/гибридных Epcam+CD45+клеток в крови, клеток/мм и при р более 0,5459 определяют высокий, а при р менее, либо равном 0,5459 определяют низкий риск опухолевой прогрессии.
Сущность предлагаемого способа иллюстрируется следующими клиническими примерами.
Пример 1
Больная С.Р.К, 76 лет обратилась к врачу по поводу увеличения живота в объеме. 10.05.2017 - выполнен лапароцентез, цитология - аденокарцинома. При обследовании - объемные образования яичников, асцит, подозрение на инфильтрат в области лапароцентеза. Направлена в НИИ онкологии Томского НИМЦ для обследования и лечения. Больная была включена в проспективное клиническое исследование NCT04817501 «Фенотипический спектр циркулирующих опухолевых клеток при опухолях женской репродуктивной системы» (Протокол этического комитета №2 от 14.02.2014). Для проведения исследования согласно предлагаемому способу у больной до онкомаркеров СА-125 и НЕ4 методом ИФА. Проведена лапароскопия - стадирование от 06.2017. На этапе хирургического стадирования также для исследования была взята асцитическая жидкость.
Проточная цитометрия показала наличие атипичных/гибридных форм циркулирующих опухолевых клеток как в крови, так и в асцитической жидкости. В крови количество Epcam+CD45+ составило 10,56 клеток/мм3, в асцитической жидкости -58,83 клеток/мм3. Уровень онкомаркеров СА-125 -129 Ед/мл, НЕ4=82,0 рМ.
Вероятность развития опухолевой прогрессии, рассчитанная по формуле:
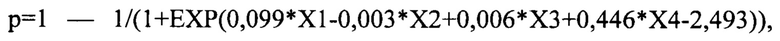 где x1 - количество атипичных/гибридных Epcam+CD45+ клеток в асцитической жидкости (клеток/мм3); х2 - уровень онкомаркера СА125 в крови (Ед/мл); х3 - уровень онкомаркера НЕ4 в крови (рМ); х4 - количество атипичных/гибридных Epcam+CD45+ клеток в крови (клеток/мм3), составила
где x1 - количество атипичных/гибридных Epcam+CD45+ клеток в асцитической жидкости (клеток/мм3); х2 - уровень онкомаркера СА125 в крови (Ед/мл); х3 - уровень онкомаркера НЕ4 в крови (рМ); х4 - количество атипичных/гибридных Epcam+CD45+ клеток в крови (клеток/мм3), составила
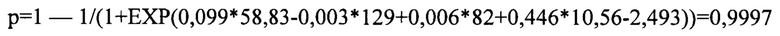
Данная пациентка была отнесена к группе больных с высоким риском опухолевой прогрессии.
Морфологическое исследование гистология + ИГХ (после операции) №14815-16/17 от 21.06.2017: гистологическая структура и иммунофенотип опухолевых элементов соответствует метастазу аденокарциномы яичника.
Данной пациентке был выставлен диагноз Рак яичников IIIc стадии (Т3с Nx М0). Далее проведено 3 курса НАХТ по схеме «паклитаксел + карбоплатин». Эффект частичная регрессия.
В последующем проведена циторедуктивная операция - лапароскопия, экстипация матки с придатками, оментэктомия от 18.10.2017 г. Проведено 3 курса АХТ по схеме "паклитаксел + карбоплатин". Продолженный рост от 28.03.2018 г. Асцит, канцероматоз. Состояние после 3 курсов " винорельбином". Прогрессирование от 12.07.2018 г. Асцит, рост маркеров. Проведено 4 курса XT "оксалиплатином" и авастаном. Прогрессирование. Асцит, канцероматоз (увеличение объема). Проведено 3 курса МХТ "гемцитабином". По результатам инструментальных обследований отмечалось прогрессирование основного процесса - очаговые образования печени и поджелудочной железы (мтс), асцит, гидроторакс справа. В марте 2019 г пациентка погибла.
Пример 2
У больной Е.М.А., 02.11.1981 г. р. (36 лет) в начале октября 2017 года появились тянущие боли внизу живота. Обратилась по месту жительства. Выявлены двухсторонние опухоли яичников. 11.101.2017 - оперативное лечение в объеме лапаротомии, аднексэктомии справа, резекции левого яичника, биопсия сальника и брюшины. Обратилась в НИИ онкологии Томского НИМЦ. Гистология №5361-86к17(пересмотр) от 30.10.17 - фокусы Low-grade серозной карциномы яичников (8460/3) на фоне пограничной опухоли/атипической пролиферативной серозной опухоли (8442/1). Брюшина и сальник -неинвазивные импланты с наличием псаммомных телец. В стенке маточной трубы - хроническое воспаление. Эндометрий с железами пролиферативного типа. В материале «подвеска» кишки - хроническое воспаление с наличием большого количества ксантомных клеток.
Проведено дообследование. Рекомендовано проведение специализированного лечения. Больная была включена в проспективное клиническое исследование NCT04817501. У больной до начала лечения была взята венозная кровь для проведения исследований согласно предлагаемому способу с помощью оценки различных популяций циркулирующих опухолевых клеток методом многоцветной проточной цитометрии и онкомаркеров СА-125 и НЕ4 методом ИФА. 24.11.2017: Проведено оперативное лечение в объеме лапароскопии, конверсии, экстирпации матки с придатками, оментэктомии. Во время лапароскопии у данной пациентки также была взята асцитическая жидкость для исследования атипичных/гибридных клеток методом проточной цитометрии. Проточная цитометрия показала наличие атипичных/гибридных форм циркулирующих опухолевых клеток в крови в количестве 1,56 клеток/мм3, в асцитической жидкости -7,27 клеток/мм3. Уровень СА-125=4 Ед/мл, НЕ4=15,9 рМ.
Вероятность развития опухолевой прогрессии, рассчитанная по формуле, показала низкий риск.
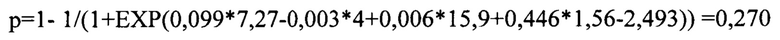
05.12.2017: проведено оперативное лечение в объеме релапаротомии, ушивание дефекта передней стенки прямой кишки, наложения трансверзостомы. Данной пациентке проведена химиотерапии по схеме «паклитаксел+цисплатин» раз в 3-4 недели, 6 курсов. При сроке наблюдения более пяти лет (дата последнего посещения врача - 20.06.2023 г.) признаков рецидива и метастазов не отмечено.
Способ основан на исследовании методом многоцветной проточной цитометрии крови и асцитической жидкости, полученной на этапе диагностического лапароскопического стадирования, оценки уровня онкомаркеров крови методом ИФА (СА125, НЕ4) и анализе данных шестидесяти пяти больных РЯ Ic-IV стадиями по системе FIGO в возрасте от 18 до 80 лет, поступивших на лечение в НИИ Онкологии и/или Томский областной онкологический диспансер, и вошедших в проспектовое клиническое исследование NCT04817501 «Фенотипический спектр циркулирующих опухолевых клеток при опухолях женской репродуктивной системы», проводимом на базе НИИ онкологии Томского НИМЦ (Протоколы этического комитета №2 от 14.02.2014, №4 от 02.04.2018).
Для построения модели дооперационного прогноза опухолевой прогрессии у больных раком яичников был применен метод логистической регрессии. В таблице приведены переменные в уравнении.
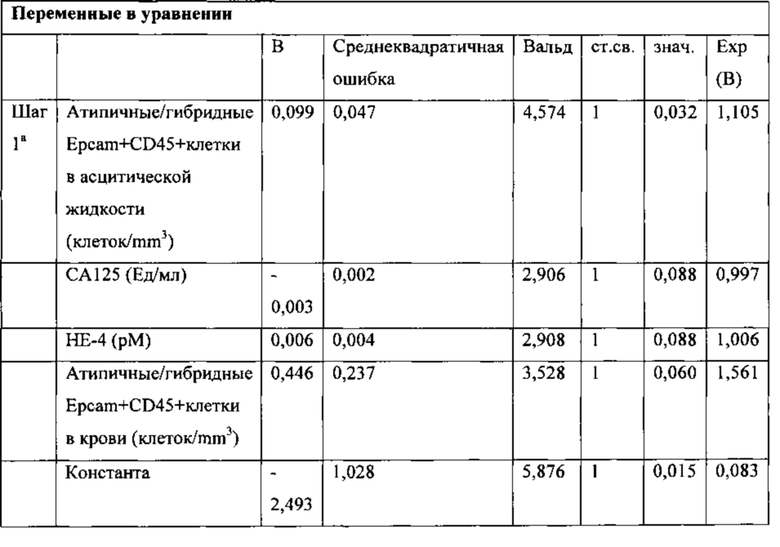
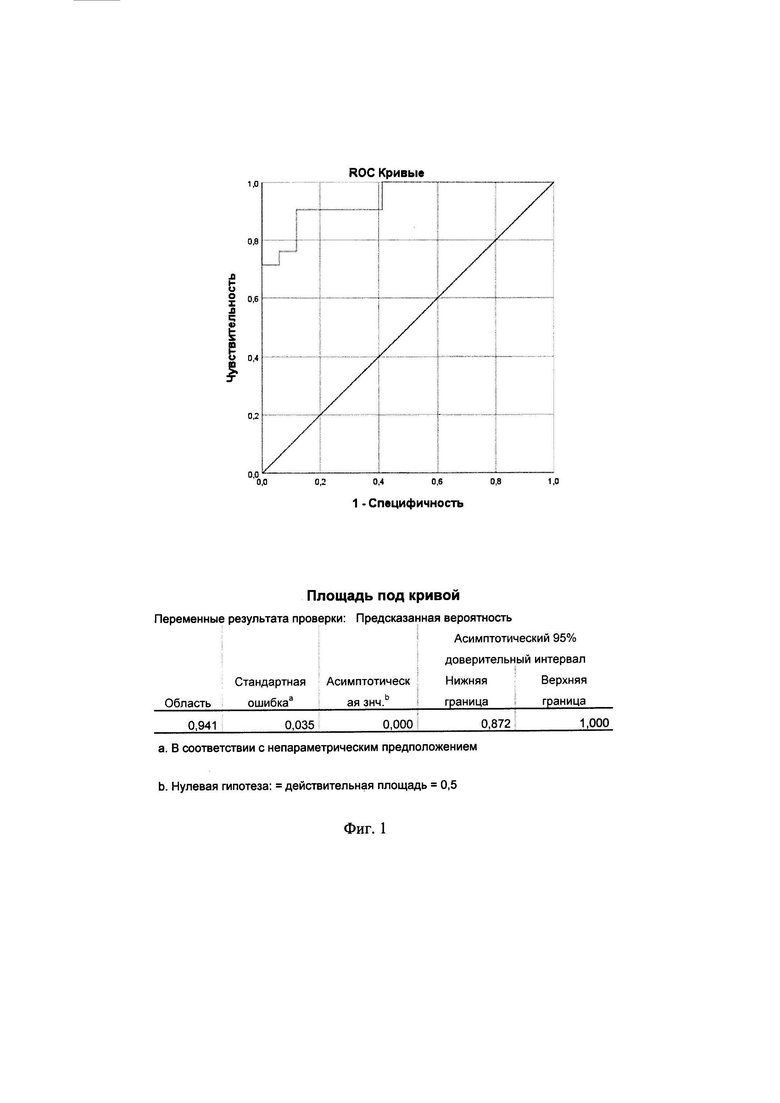
На фиг. 1 приведен РОК анализ модели. С помощью ROC-анализа была оценена полученная модель. Проведенный ROC-анализ показал очень хорошее качество полученной модели. Показатель AUC составил 0,941.
Таким образом, предлагаемый способ позволяет с большей точностью и информативностью прогнозировать риск развития опухолевой прогрессии при раке яичников, что является крайне необходимым для определения тактики ведения и создания персонализированного подхода при лечении таких пациенток. Получены достоверные числовые показатели, характеризующие степень риска возникновения рецидива у конкретной больной, отражающие прогноз течения онкологического заболевания.
Источники информации, принятые во внимание при составлении описания:
1. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой Злокачественные новообразования в России в 2021 году (заболеваемость и смертность) - М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, - 2022. - ил. -252 с.
2. Лактионов К.П., Левкина И.В., Кушлинский Д.Н., Герштейн Е.С. Исследование матриксных металлопротеиназ и их тканевых ингибиторов у больных с новообразованиями яичников. // Опухоли женской репродуктивной системы №2 - 2012 г. С. 48-54.
3. Старинский В.В., Сергеева Н.С., Маршутина Н.В., Корнеева И.А. Проблемы ранней диагностики и скрининга рака яичников: реальность и перспективы. // Онкология. Журнал им. П.А. Герцена №1, 2013 г. С. 56-62.
4. Kaigorodova E.V. CIRCULATING TUMOR CELLS: CLINICAL SIGNIFICANCE IN BREAST CANCER (REVIEW) // Annals of the Russian academy of medical sciences. -2017. - Vol. 72. - N. 6. - P. 450-457. doi: 10.15690/vramn833
5. Кайгородова E.B., Тарабановская H.A., Суркова П.В., Зельчан Р.В., Гарбуков Е.Ю. Наличие в крови различных популяций циркулирующих опухолевых клеток у больных раком молочной железы: связь с пятилетней безметастатической выживаемостью. Сибирский онкологический журнал. 2020;19(6):57-65. https://doi.org/10.21294/1814-4861-2020-19-6-57-65.
6. Kaigorodova E.V., Kozik A.V., Zavaruev I.S., Grishchenko M.Y. Hybrid/Atypical Forms of Circulating Tumor Cells: Current State of the Art. Biochemistry (Mosc). 2022 Apr; 87(4):380-390. doi: 10.1134/S0006297922040071.
7. Кайгородова E.B., Федулова H.B., Очиров M.O., Дьяков Д.А., Молчанов С.В., Часовских Н.Ю. Различные популяции опухолевых клеток в асцитической жидкости больных раком яичников. Бюллетень сибирской медицины. 2020;19(1):50-58. https://doi,org/10.20538/1682-0363-2020-1-50-58
8. Кайгородова Е.В., Очиров М.О., Молчанов СВ., Рогачев P.P., Дьяков Д.Д., Чернышова А.Л., Шпилева О.В., Ковалев О.В., Вторушин С.В. Различные популяции EpCam-положительных клеток в асцитической жидкости у больных раком яичников: связь со степенью канцероматоза. Бюллетень сибирской медицины. 2021;20(2):44-53. https://doi.org/10.20538/1682-0363-2021 -2-44-53
9. Кайгородова Е.В., Заваруев И.С, Грищенко М.Ю., Чернышова А.Л. Особенности встречаемости атипичных (гибридных) форм клеток EpCam+CD45+ у больных раком эндометрия // Материалы VI Всероссийской конференции по молекулярной онкологии. - Текст: электронный // Успехи молекулярной онкологии. - 2021. - Том 8, №4 При л. - С.50. - https://doi.org/10.17650/2313-805Х-2021-8-4-5-163.
10. Manjunath, Y.; Porciani, D.; Mitchem, J.B.; Suvilesh, K.N.; Avella, D.M.; Kimchi, E.T.; Staveley-O’Carroll, K.F.; Burke, D.H.; Li, G.; Kaifi, J.T. Tumor-Cell-Macrophage Fusion Cells as Liquid Biomarkers and Tumor Enhancers in Cancer. Int. J. Mol. Sci. 2020, 21, 1872. https://doi.org/10.3390/ijms21051872
11. RU 2530556 C1, 10.10.2014 Способ прогнозирования рецидива рака яичников.
12. RU 2299018 C1, 20.05.2007 Способ прогнозирования продолжительности безрецидивного периода у больных серозным раком яичников.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска опухолевой прогрессии у больных раком молочной железы | 2024 |
|
RU2838618C1 |
| Способ дооперационного прогнозирования риска рецидива у больных раком эндометрия Т1 стадии | 2021 |
|
RU2762493C1 |
| Способ прогнозирования риска плохого ответа опухоли на неоадъювантную химиотерапию у пациенток с инвазивной карциномой молочной железы | 2018 |
|
RU2682967C1 |
| Способ прогнозирования гематогенного метастазирования при инвазивной карциноме неспецифического типа молочной железы на основе определения различных популяций циркулирующих опухолевых клеток в крови до лечения | 2018 |
|
RU2678202C1 |
| Способ прогнозирования степени вероятности возможности выполнения оптимальной циторедуктивной операции у больных с диссеминированными формами рака яичников | 2017 |
|
RU2637399C1 |
| Способ прогнозирования перитонеального распространения рака яичников | 2019 |
|
RU2722654C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВИРОВАНИЯ СЕРОЗНОЙ КАРЦИНОМЫ ЯИЧНИКОВ | 2020 |
|
RU2749361C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ МЕТАСТАЗИРОВАНИЯ МЕЗОНЕФРОИДНОГО РАКА ЯИЧНИКОВ | 2008 |
|
RU2354302C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВА РАКА ЯИЧНИКОВ | 2013 |
|
RU2530556C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВА СЕРОЗНОГО РАКА ЯИЧНИКОВ | 2005 |
|
RU2290078C1 |
Изобретение относится к медицине, а именно к онкологии, молекулярной биологии и клинической лабораторной диагностике, и может быть использовано для прогнозирования риска опухолевой прогрессии у больных раком яичников. До начала лечения исследуют кровь и асцитическую жидкость, в которой методом проточной цитометрии определяют количество атипичных/гибридных Epcam+CD45+ клеток. Методом ИФА определяют уровень онкомаркеров крови СА125 и НЕ4. Полученные значения подставляют в формулу расчета вероятности развития опухолевой прогрессии Р. При Р более 0,5459 определяют высокий, а при Р менее, либо равном 0,5459, определяют низкий риск опухолевой прогрессии. Способ обеспечивает повышение точности и снижение инвазивности, возможность прогнозирования течения заболевания до проведения лечения за счет определения количества атипичных/гибридных Epcam+CD45+ клеток в крови и асцитической жидкости и уровня онкомаркеров СА125 и НЕ4 в крови. 1 ил., 1 табл., 2 пр.
Способ прогнозирования риска опухолевой прогрессии у больных раком яичников, включающий исследование биологического материала пациента, характеризующийся тем, что до начала лечения исследуют кровь и асцитическую жидкость, в которой методом проточной цитометрии определяют количество атипичных/гибридных Epcam+CD45+ клеток, методом ИФА определяют уровень онкомаркеров крови СА125 и НЕ4, вероятность развития опухолевой прогрессии Р в виде рецидивов и метастазов рассчитывают по формуле:
Р=1-1/(1+ЕХР(0,099*Х1-0,003*Х2+0,006*Х3+0,446*Х4-2,493)),
где
X1 - количество атипичных/гибридных Epcam+CD45+ клеток в асцитической жидкости, клеток/мм3;
Х2 - уровень онкомаркера СА125 в крови, Ед/мл;
Х3 - уровень онкомаркера НЕ4 в крови, рМ;
Х4 - количество атипичных/гибридных Epcam+CD45+ клеток в крови, клеток/мм3,
и при Р более 0,5459 определяют высокий, а при Р менее либо равном 0,5459 определяют низкий риск опухолевой прогрессии.
| Способ прогнозирования перитонеального распространения рака яичников | 2019 |
|
RU2722654C1 |
| Способ определения агрессивности течения рака яичников | 2018 |
|
RU2688008C1 |
| RU 2010147643 A, 27.05.2012 | |||
| WO 2015193678 A1, 23.12.2015 | |||
| КОЗИК А.В | |||
| и др | |||
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| Сибирский онкологический журнал | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
Авторы
Даты
2024-03-28—Публикация
2023-07-31—Подача