Изобретение относится к медицине, а именно, к экспериментальной медицине и внутрисосудистой визуализации. Данное изобретение может быть использовано для in vivo оценки сосудистых протезов в эксперименте на лабораторных животных.
Сосудистые протезы, применяемые при реконструктивных операциях, не оптимальны, ввиду различия в комплаентности материала и тканей стенки артерии, что приводит к изменению кровотока в зоне анастомоза. Основными недостатками сердечно-сосудистых графтов являются: частые тромбозы, аневризмы и рестенозы, особенно в месте анастамоза. Остается актуальной проблема прижизненной визуализации состояния и моделирования сердечнососудистых имплантатов, оценка их функционирования и эндотелизации на разных сроках после имплантации. Поэтому разработка метода in vivo оценки эндотелизации как изделия, используемого в клинике, так и прототипа изделия, разрабатываемого для нужд сердечно-сосудистой хирургии, обладает высокой практической значимостью. Одним из потенциальных решений является использования метода оптической когерентной томографии (ОКТ).
На сегодняшний день все используемые методы in vivo оценки формирования монослоя эндотелиоподобных клеток на поверхности сосудистых протезов, имплантированных в сосудистое русло мелким и крупным лабораторным животным, можно разделить на 2 группы: 1 - прижизненные и 2 - требующие эксплантации. Вторая группа методов более точная, так как работа по детекции новообразованного монослоя эндотелиоподобных клеток связана непосредственно с данными клетками. Существующая прижизненная детекция не обладает необходимой чувствительностью для установления динамики формирования монослоя клеток.
К 1 группе можно отнести метод ультразвукового исследования имплантированного протеза в сосудистое русло лабораторного животного.
На разных сроках in vivo эксперимента по имплантации сосудистых протезов проводят мониторинг проходимости ультразвуковым исследованием (УЗИ) с функцией цветной допплерографии. Для данного исследования животное фиксируют, возможно, анестезируют, далее место исследования тщательно бреют, обрабатывают антисептиком и наносят гель для УЗИ.
Плюсы метода: быстрая on-line визуализация проходимости сосудистого протеза; возможность измерения его диаметра в центральной части и анастомозах; измерение скорости кровотока и его характера; детекция аневризматических, стенотических изменений и развитие тромбоза; получение изображений.
Минусы метода: косвенная установка образования эндотелиоподобной выстилки на внутренней поверхности сосудистого протеза без определения его качества и типирования клеток.
Ко 2 группе можно отнести ряд гистологических методов исследования с сопутствующим микроскопическим анализом.
1. Метод гистологического изучения образцов, основанный на окрашивании гематоксилином и эозином. Эксплантированные образцы фиксируют в 10% забуференном формалине в течение 24 часов, затем промывают проточной водопроводной водой для удаления фиксирующего раствора и обезвоживания в IsoPrep, оставляют в последней порции на ночь. Затем пропитывают образцы 3 порциями парафина при 56°С в течение 60 минут в каждой порции. Пропитанные образцы заливают ГИСТОМИКСОМ. Далее изготавливают срезы толщиной 8 мкм с помощью микротома, помещают в термостат и сушат в течение ночи при 37°С. После полного высыхания образцы депарафинизируют в 3 порциях о-ксилола в течение 1-2 мин и дегидратируют в 3 порциях 96% спирта в течение 1-2 мин. Далее депарафинированные срезы окрашивают гематоксилином и эозином. Срезы окрашивают Гематоксилином Гарриса в течение 15-20 минут, с дальнейшей промывкой в воде до 10 минут. Далее на срез наносят несколько капель эозина на 30 секунд и промывают в воде. После срез помещают в 96% спирт. Просветление срезов проводят в о-ксилоле несколько минут с его дальнейшим удалением. На последнем этапе срезы заключают в монтирующую среду Витрогель. Гистологические срезы исследуют методом световой микроскопии с использованием микроскопа при разном увеличении объективов, например х 50, х 200 и х 400.
Плюсы метода: визуализация клеточного монослоя на поверхности сосудистого протеза, возможность получения изображений на разном увеличении.
Минусы метода: необходимость в эксплантации образца, длительность исполнения метода и невозможность типирования клеток.
2. Метод иммунофлуоресцентного окрашивания образцов с последующей конфокальной микроскопией:
Из замороженных образцов с помощью криотома изготавливают серийные криосрезы толщиной 8 мкм с интервалом 100 мкм. Препараты фиксируют в 4% растворе параформальдегида в течение 10 минут. Для пермеабилизации срезы обрабатывают 0,1% раствором Triton-Х100 в течение 15 мин. Далее на срезы наносят смесь первичных антител мыши к CD31+ крысы, антитела кролика к CD 34+ крысы, а также антитела к фактору фон Виллебранда, конъюгированные с FITC и икубируют в течение ночи при 4°С. При окрашивании неконъюгированными первичными антителами применяют смесь вторичных антител: антитела козы к Ig мыши, конъюгированные с AlexaFluor56 и антитела осла к Ig кролика, конъюгированные с AlexaFluor488 в течение 1 часа при комнатной температуре. На всех этапах окрашивания для промежуточной отмывки срезов использовали фосфатно-солевой буфер с добавлением 0,1% Tween 20. Для удаления автофлуоресценции срезы обрабатывают Autofluorescence Eliminator Reagent по методике, предложенной производителем. Ядра клеток докрашивают DAPI (10 мкг/мл) в течение 30 минут. Готовые препараты заключают под покровное стекло с использованием монтирующей среды ProLong Gold Antifade Mountant. После высушивания препараты анализируют с помощью конфокального микроскопа. С каждого препарата делают снимки с 10 случайно выбранных полей зрения. Полученные фотографии анализируют и измеряют среднюю интенсивность флуоресцентного сигнала для каждого снимка.
Плюсы метода: визуализация клеточного монослоя на поверхности сосудистого протеза, возможность получения качественных (четких) изображений на разном увеличении; микс иммунофлуоресцентных меток позволяет типировать клетки, изучать их функциональность, степень как межклеточного, так и взаимодействия с полимерным материалом.
Минусы метода: необходимость в эксплантации образца, длительность исполнения метода.
3. Наиболее близким к заявленному изобретению метод гистологического изучения образцов, основанный на сканирующей электронной микроскопии. Образцы фиксируют в 4% забуференном формалине в течение 24 часов, затем постфиксируют 1% тетраоксидом осмия в 0,1М фосфатном буфере и окрашивают 2% тетраоксидом осмия в бидистиллированной воде в течение 48 часов. Далее образцы обезвоживают в серии спиртов возрастающей концентрации, окрашивают 2% уранилацетатом в 95% этаноле, обезвоживают 99,7% изопропанолом в течение 5 часов и ацетоном в течение 1 часа, пропитывают смесью ацетона с эпоксидной смолой Ероп в соотношении 1:1 (6 часов), после чего переносят в свежую порцию эпоксидной смолы (на 24 часа) и далее проводят ее полимеризацию в емкостях FixiForm при 60°С. После этого образцы в эпоксидных блоках подвергают шлифовке и полировке на установке TegraPol-11. Контрастирование цитратом свинца проводят по Рейнольдсу в течение 7 минут путем нанесения раствора на поверхность шлифованного образца с последующей его отмывкой бидистиллированной водой. Далее проводят напыление на полированную поверхность эпоксидных блоков углерода (толщина покрытия 10 - 15 нм) с помощью вакуумного напылительного поста. Визуализацию структуры образцов проводят при помощи сканирующей электронной микроскопии в обратно-рассеянных электронах на электронном микроскопе в режиме BSECOMP при ускоряющем напряжении 10 кВ).
Плюсы метода: визуализация клеточного монослоя на поверхности сосудистого протеза, возможность получения изображений на разном увеличении, в том числе более х 5000, что дает визуализацию межклеточных контактов.
Минусы метода: необходимость в эксплантации образца, длительность исполнения метода и невозможность типирования клеток.
Технический результат предлагаемого изобретения достигается за счет использования метода оптической когерентной томографии, разрешающая способность которой составляет до 10 мкм при осевом разрешении и до 20 мкм при боковом разрешении. Эта отличительная особенность оптической когерентной томографии позволяет получать высококачественные изображения сосудистой стенки. В исследованиях было показано, что визуализация при помощи ОКТ сопоставима с гистологическим исследованием соответствующей ткани и может с высоким разрешением определить ее структуру. Также данный метод дает возможность оценить толщину сформированной неоинтимы на поверхности сосудистых протезов, наличие аневризм, диссекций или тромботических компонентов.
Представленное изобретение относится к методу прижизненной, малоинвазивной внутрисосудистой визуализации. Для исследования: животное фиксируют и седатируют, проводят общую анестезию с подключением аппарата искусственной вентиляции легких. Место пункции бреют и обрабатывают антисептиком. Выполняется пункция сосудистого русла на стороне имплантированного графта. Через установленный интродьюсер проводится 0.035 проводник, с последующим заведением проводникового катетера JR4.0 5-6 Fr. Выполняется замена 0,035 проводника на 0.014 коронарный проводник. По коронарному проводнику проводится датчик оптической когерентной томографии дистальнее зоны сосудистой протеза. Вводится 20-25 мл рентгенконтрастного вещества со скоростью 8-10 мл/сек, с параллельной протяжкой датчика со скоростью 5-40 мм/сек.
ОКТ измеряет интенсивность инфракрасного света, возвращающегося от различных структур артериальной стенки. Среда показывает темный и однородный сигнал из-за меньшего количества коллагеновых волокон и обилия гладкомышечных клеток и внеклеточного матрикса. Первым этапом анализа является оценка качества полученных изображений и визуализированных структур, наличие артефактов от форменных элементов крови Вторым этапом является калибровку масштаба изображения для реализации пространственного разрешения путем регулировки z-смещения, настройка нулевой точки системы - это необходимо для полной реализации пространственного разрешения (обычно она проводиться автоматически, но при необходимости возможна и ручная корректировка). Последним этапом выполняют измерение измерения размеров интересующих структур сосудистого протеза.
Основными преимуществами изобретения являются: возможность в режиме реального времени визуализировать проходимость сосудистого протеза; детекция аневризм, а также стенотических изменений и тромботических наложений; оценка формирования неоинтимы и ее толщины, без выведения животных из эксперимента и эксплантации исследуемого графта; получение изображения на всем протяжении графта с возможностью его оценки при разном увеличении; меньшие трудозатратность и продолжительность исследования, по сравнению с представленными методиками.
При сравнении нового способа прижизненной оценки функционирования и эндотелизации сосудистых протезов в эксперименте с предложенными выше методами, ОКТ обладает рядом преимуществ. В отличие от ультразвукового исследования ОКТ позволяет оценить, как проходимость сосудистого протеза и наличие аневризм, стенотических и тромботических изменений, так и толщину, и протяженность эндотелия на поверхности графта, с высокой точностью, сравнимой с гистологическим исследованием. Наиболее близок к заявленному изобретению метод сканирующей электронной микроскопии, обладающей большей разрешающей способностью, но в отличие от представленного изобретения, требует эксплантацию имплантата с выведением животного из эксперимента. ОКТ является менее трудозатратным и требует меньше времени на проведение исследования, по сравнению с гистологическим исследованием и иммунофлуоресцентным окрашиванием, которые также требуют эксплантации исследуемого графта.
Для подтверждения эффективности представленного изобретения было проведено исследование сосудистых протезов через 2 месяца после имплантации в сонную артерию овец. Выполнены имплантации сосудистых протезов из фиброина шелка (RSF-ethanol) и ксеноперикарда (КемПерипалс-Нео) в сонную артерию овец (n=3). Изображения имлантированных протезов с запущенным током крови представлены на рисунке 1.
Каждая овца получила все требуемое медикаментозное сопровождение до, во время операции и в течении 30 дней после нее. Животным проведено ультразвуковое исследование сонной артерии на предмет проходимости зоны артерии с протезом и других основных характеристик: диаметр комплекса артерия + протез, скорость кровотока. При этом скорость кровотока в просвете сосудов с данными разновидностями сосудистых графтов была идентична и достоверно не отличалась от скорости кровотока в интактном сосуде.
В ходе прижизненной визуализации протезов с помощью ОКТ обнаружено, что спустя 2 месяца имплантации протезов в сонную артерию овец в обеих группах сформировалась неоинтима. На ОКТ выявлена равномерная гиперплазия неоинтимы по всей внутренней поверхности протезов из фиброина шелка со средней толщиной 370 микрон; у протеза из ксеноперикарда неоинтима неоднородна, выражена только в зоне анастомоза с толщиной 230 микрон (рис. 2).
Данные сканирующей электронной микроскопии подтвердили выраженную гиперплазию неоинтимы тканеинженерного графта с толщиной 382 микрона; средняя толщина неоинтимы у протеза из ксеноперикарда составила 105 микрон. На неоинтиме тканеинженерного протеза обнаружен непрерывный монослой эндотелиоподобных клеток в отличие от ксеноперикарда с отсутствием целостности выстилки (рис. 3).
Таким образом, продемонстрированы эффективность и безопасность выполнения оптической когерентной томографии с целью оценки ремоделирования и эндотелизации протезов в эксперименте.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФУНКЦИОНАЛЬНО АКТИВНАЯ БИОДЕГРАДИРУЕМАЯ СОСУДИСТАЯ ЗАПЛАТА ДЛЯ АРТЕРИАЛЬНОЙ РЕКОНСТРУКЦИИ | 2019 |
|
RU2707964C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ БИОДЕГРАДИРУЕМЫХ СОСУДИСТЫХ ГРАФТОВ МАЛОГО ДИАМЕТРА С МОДИФИЦИРОВАННОЙ ПОВЕРХНОСТЬЮ | 2018 |
|
RU2675269C1 |
| СПОСОБ НЕИНВАЗИВНОЙ ЭКСПРЕСС-ДИАГНОСТИКИ ПАТОЛОГИЧЕСКИХ ИЗМЕНЕНИЙ В ТКАНЯХ В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ IN VIVO | 2022 |
|
RU2824571C2 |
| Способ изготовления функционально активной полимерной заплаты для артериальной реконструкции, устойчивой к аневризмообразованию | 2024 |
|
RU2835436C1 |
| Способ трансплантации клеток ретинального пигментного эпителия (РПЭ), дифференцированных из индуцированных плюрипотентных стволовых клеток человека, при атрофии ретинального пигментного эпителия | 2019 |
|
RU2730937C1 |
| Технология изготовления функционально активных биодеградируемых сосудистых протезов малого диаметра с лекарственным покрытием | 2019 |
|
RU2702239C1 |
| СПОСОБ ОПТИЧЕСКОЙ КОГЕРЕНТНОЙ ТОМОГРАФИИ ДЛЯ ИНТРАОПЕРАЦИОННОЙ ГИСТОМОРФОЛОГИЧЕСКОЙ ОЦЕНКИ ЦЕЛОСТНОСТИ КОРОНАРНЫХ КОНДУИТОВ ПРИ АОРТОКОРОНАРНОМ ШУНТИРОВАНИИ | 2018 |
|
RU2677785C1 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ СОСУДОВ МИКРОЦИРКУЛЯТОРНОГО РУСЛА | 2014 |
|
RU2555397C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОСТОЯНИЯ СТЕНКИ ПРЯМОЙ КИШКИ ПОСЛЕ РЕКОНСТРУКТИВНО-ВОССТАНОВИТЕЛЬНЫХ ОПЕРАЦИЙ У ДЕТЕЙ | 2005 |
|
RU2290057C1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ВИЗУАЛИЗАЦИИ ЭЛЕМЕНТОВ НЕРВНО-СОСУДИСТОГО ПУЧКА ПРИ РАДИКАЛЬНОЙ ЦИСТЭКТОМИИ И РАДИКАЛЬНОЙ ПРОСТАТЭКТОМИИ | 2008 |
|
RU2375962C1 |


Изобретение относится к медицине, а именно к экспериментальной медицине и внутрисосудистой визуализации. Данное изобретение может быть использовано для in vivo оценки сосудистых протезов в эксперименте на лабораторных животных. Для исследования: животное фиксируют и седатируют, проводят общую анестезию с подключением аппарата искусственной вентиляции легких. Место пункции бреют и обрабатывают антисептиком. Выполняется пункция сосудистого русла на стороне имплантированного графта. Через установленный интродьюсер 6 Fr проводится 0.035 проводник, с последующим заведением проводникового катетера JR4.0 6 Fr. Выполняется замена 0,035 проводника на 0.014 коронарный проводник. По коронарному проводнику проводится датчик оптической когерентной томографии дистальнее зоны сосудистого протеза. Вводится 20 мл рентгенконтрастного вещества со скоростью 10 мл/с, с параллельной протяжкой датчика со скоростью 25 мм/с. ОКТ измеряет интенсивность инфракрасного света, возвращающегося от различных структур артериальной стенки. Среда показывает темный и однородный сигнал из-за меньшего количества коллагеновых волокон и обилия гладкомышечных клеток и внеклеточного матрикса. Первым этапом является оценка качества полученных изображений и визуализированных структур, наличие артефактов от форменных элементов крови; вторым этапом проводят калибровку масштаба изображения для реализации пространственного разрешения и измерения размеров интересующих структур сосудистого протеза. Применение данного изобретения позволяет получать высококачественные изображения сосудистой стенки. 3 ил.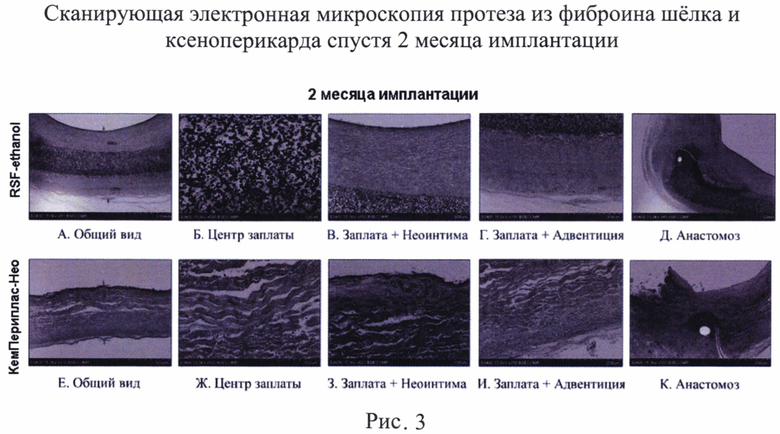
Способ прижизненного исследования функционирования, ремоделирования и эндотелизации протезов для сосудистой реконструкции после имплантации в эксперименте на крупных лабораторных животных, отличающийся тем, что животное фиксируют и седатируют, проводят общую анестезию с подключением аппарата искусственной вентиляции легких; после выполнения сосудистого доступа через установленный интродьюсер 6 Fr проводится 0,035 проводник с последующим заведением проводникового катетера JR4.0 6 Fr, затем выполняют замену 0,035 проводника на 0,014 коронарный проводник, по которому проводят датчик оптической когерентной томографии дистальнее целевой зоны сосудистого протеза; при инфузии 20 мл рентгенконтрастного вещества со скоростью 10 мл/с выполняют параллельную протяжку датчика оптической когерентной томографии со скоростью 25 мм/с, далее анализируют полученные данные: первым этапом является исследование полученных изображений и визуализированных структур, наличие артефактов от форменных элементов крови; вторым этапом проводят калибровку масштаба изображения для реализации пространственного разрешения и измерения размеров интересующих структур сосудистого протеза.
| Способ прогнозирования формирования гиперплазии неоинтимы после выполнения шунтирующих операций у пациентов с облитерирующим атеросклерозом артерий нижних конечностей | 2022 |
|
RU2785888C1 |
| СПОСОБ ОПТИЧЕСКОЙ КОГЕРЕНТНОЙ ТОМОГРАФИИ ДЛЯ ИНТРАОПЕРАЦИОННОЙ ГИСТОМОРФОЛОГИЧЕСКОЙ ОЦЕНКИ ЦЕЛОСТНОСТИ КОРОНАРНЫХ КОНДУИТОВ ПРИ АОРТОКОРОНАРНОМ ШУНТИРОВАНИИ | 2018 |
|
RU2677785C1 |
| Бокерия Л.О | |||
| и др | |||
| Результаты применения биоинженерной конструкции для лечения окклюзионных поражений сосудов в эксперименте на животных | |||
| Ж | |||
| Сеченовский вестник, 2015, N2 (20), с.24-29. | |||
Авторы
Даты
2024-04-12—Публикация
2023-03-28—Подача