Изобретение относится к области медицины, конкретно к кардиологии, и касается способа оценки вегетативной регуляции сердечного ритма для определения стадии кардиальной автономной нейропатии вне зависимости от наличия ее клинических проявлений у пациентов с метаболическим синдромом.
Кардиальная автономная нейропатия (КАН) - осложнение сахарного диабета сахарного диабета (СД) 2 типа, которое ухудшает качество жизни пациентов и повышает риск внезапной смерти [1]. Считается, что основные механизмы КАН запускаются уже при состоянии, предшествующем развитию СД 2 типа, а именно метаболическом синдроме, диагностическими критериями которого наряду с абдоминальным ожирением, является комплекс метаболических нарушений - дислипидемия и/или повышение уровня глюкозы [2]. Смертность больных, имеющих КАН, за 10-летний период составляет 25%, по сравнению с 4% у лиц, не имеющих данной патологии [3].
Современными исследованиями доказано, что на начальных стадиях КАН до определенной степени обратима при условии своевременного лечения [4]. Так как КАН представляет собой повреждение нервных волокон, которые иннервируют сердце и кровеносные сосуды [5], патогенетическое лечение эффективно для предотвращения дальнейшего повреждения нервных структур. Для определения степени обратимости и возможности коррекции на начальных этапах формирования данной патологии необходимо проведение функциональных тестов.
Известен способ определения наличия КАН, основанный на оценке вариабельности ритма сердца (ВРС) при фоновой записи (в положении лежа) в течение 5 минут и при активной ортостатической пробе в течение 5 минут с последующим спектральным анализом [6], При проведении ВРС определяют отношение относительных значений LF и VLF, полученных при проведении активной ортостатической пробы к таковым при фоновой записи. При одновременном отношении %LFортопроба/%LFфон менее 1,0 и %VLFортопроба/%VLFфон более 1,0 диагностируют КАН еще до появления клинических признаков.
Данный способ является наиболее близким к заявленному по технической сущности и достигаемому результату и выбран в качестве прототипа.
Недостатком данного способа является отсутствие возможности выделения стадий КАН вне зависимости от наличия ее клинических проявлений. Определение стадии КАН может лечь в основу разработки тактики назначения препаратов в зависимости от стадии заболевания и позволит провести оценку эффективности назначаемой патогенетической терапии. В настоящее время отсутствует стандарт патогенетического лечения КАН, проводимая терапия носит симптоматический и рекомендательный характер. Это связано с невозможностью оценки эффективности проводимой терапии, именно эту задачу позволит решить предлагаемый способ определения стадии КАН. Помимо планирования лечения, определение стадии КАН с назначением терапии на ранних этапах ее формирования, позволит предотвратить прогрессирование заболевания, уменьшить риск развития клинических проявлений КАН, таких как ортостатическая гипотензия, безболевой инфаркт миокарда и тахикардия покоя [7], определить прогноз для больного, контролировать течение заболевания и эффективность применяемой терапии.
Задачей изобретения является создание способа определения стадии кардиальной автономной нейропатии вне зависимости от наличия ее клинических проявлений у пациентов с метаболическим синдромом, основанного на оценке вегетативной регуляции сердечного ритма.
Поставленная задача решается проведением пациентам с метаболическим синдромом вне зависимости от наличия клинических проявлений КАН 5-ти минутного фонового исследования ВРС в положении лежа и при выполнении активной ортостатической пробы в течение 5 мин с последующим спектральным анализом и расчетом относительных спектральных показателей, представляющих вклад очень низкочастотного (VLF) и низкочастотного (LF) компонентов в общую мощность спектра колебаний ритма сердца; с последующим расчетом отношения каждого относительного показателя при проведении ортостатической пробы к таковому при фоновой записи: %LFортопроба/%LFфон и %VLFортопроба/%VLFфон. У пациентов с метаболическим синдромом при отношении %VLFортопроба/%VLFфон более 1,0 значение отношения %LFортопроба/%LFфон 0,99-0,8 свидетельствуют о 1 стадии КАН, %LFортопроба/%LFфон 0,79-0,5 - 2 стадии КАН, %LFортопроба/%LFфон менее 0,49 - 3 стадии КАН. Значения и %VLFортопроба/%VLFфон и %LFортопроба/%LFфон менее 1,0 свидетельствуют об атипичной форме КАН.
Новым в предлагаемом в качестве изобретения способе является использование отношения низкочастотного показателя ВРС при проведении ортостатической пробы к таковому при фоновой записи для установления стадии кардиальной автономной нейропатии вне зависимости от наличия ее клинических проявлений.
Для диагностики КАН используют метод, основанный на оценке вариабельности ритма сердца. При спектральном анализе ВРС определяют общую мощность спектра (total power - TP), с вычислением спектра мощности колебаний в трех частотных диапазонах: 0,004-0,08 Гц (очень низкие частоты, very low frequency - VLF); 0,09-0,16 Гц (низкие частоты, low frequency - LF); 0,17-0,5 Гц (высокие частоты, high frequency - HF). Выделение трех частотных диапазонов обусловлено различием их формирования: диапазон очень низких частот отражает функциональное состояние надсегментарных структур; диапазон низких частот - симпатическую и диапазон высоких частот - парасимпатическую нервную систему на сегментарном уровне. Оценку показателей проводят с учетом абсолютных и относительных значений мощности спектра каждого частотного диапазона (VLF, LF, HF) в исходном состоянии, направленности их реагирования в ответ на функциональные пробы.
Известно, что ранним признаком КАН является угнетение активности симпатического отдела вегетативной нервной системы, она в этом случае не появляется даже в ответ на проводимые тесты по оценки функционального состояния сердца. При этом фиксированный сердечный ритм у данных пациентов - отсутствие четкой зависимости частоты сердечного ритма от физической активности и фазы дыхания -свидетельствуют о преобладании влияния надсегментарных структур на сердечный ритм [3]. При проведении ВРС проводят оценку влияния симпатического отдела вегетативной нервной системы и надсегментарных структур на ритм сердца как в покое, так и на фоне физической активности (ортостатической пробы) с использованием отношения каждого относительного показателя ВРС при проведении ортостатической пробы к таковому при фоновой записи для определения стадии КАН вне зависимости от наличия ее клинических проявлений у пациентов с метаболическим синдромом, что для специалиста не является очевидным. Ключевым фактором, определяющим развитие КАН, является угнетение активности симпатического отдела вегетативной нервной системы, в следствие чего формируется преобладание влияния надсегментарных структур на сердечный ритм. Таким образом, возможно определение стадии КАН при наличии преобладания влияния надсегментарных структур на сердечный ритм по степени угнетения активности симпатического отдела вегетативной нервной системы, определяемое при вычисляемом по данным ВРС соотношения %LFортопроба/%LFфон. Стадийность КАН зависит от степени снижения вклада симпатического звена вегетативной нервной системы в сердечный ритм, характеризуется снижением показателя %LF. Считается, что раннее определение КАН жизненно важно для успешной терапии, так как угнетение симпатической нервной системы в ответ на функциональные тесты может быть обратимым, если оно диагностировано вскоре после возникновения [5]. Угнетение же активности симпатической нервной системы в ответ на функциональные тесты на 50%, является пограничным и сопряжено с риском внезапной смертности [8], что может быть определено при проведении ВРС и определении отношения LFортопроба/%LFфон менее 0,5.
Существенные признаки предлагаемого в качестве изобретения способа проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники и неочевидные для специалиста.
Идентичной совокупности признаков не обнаружено в патентной и научно-медицинской литературе.
Предлагаемый в качестве изобретения способ может быть использован в практическом здравоохранении для повышения качества лечения больных и улучшения прогноза жизни у пациентов с кардиальной автономной нейропатией вне зависимости от наличия ее клинических проявлений и метаболическим синдромом.
Исходя из вышеизложенного следует считать предлагаемое изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость»
Изобретение будет понятно из следующего описания
Способ осуществляют следующим образом.
Определение стадии кардиальной автономной нейропатии вне зависимости от наличия ее клинических проявлений у пациентов с метаболическим синдромом осуществляют на основании спектрального анализа вариабельности ритма сердца с расчетом отношения каждого относительного показателя при проведении ортостатической пробы к таковому при фоновой записи (%LFортопроба/%LFфон, %VLFортопроба/%VLFфон).
1 стадии КАН соответствует отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон 0,99-0,8;
2 стадии КАН соответствует отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон 0,79-0,5;
3 стадии КАН соответствует отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон менее 0,49.
Атипичной форме КАН соответствует значения обоих отношений %VLFортопроба/%VLFфон и %LFортопроба/%LFфон менее 1,0.
На базе клиники федерального государственного бюджетного научного учреждения «Научно-исследовательского института фармакологии и регенеративной медицины имени Е.Д. Гольдберга» Томского НИМЦ проведено одномоментное поперечное исследование, в рамках которого обследована сплошная выборка из 127 пациентов в возрасте от 32 до 64 лет (средний возраст 53,33±5,12 лет, среди них 36 мужчина и 91 женщина).
Критериями включения являлось наличие у пациентов метаболического синдрома, который верифицировался согласно рекомендациям Всемирной организации здравоохранения (2009 г.) по наличию не менее трех из пяти перечисленных критериев [9]:
- Абдоминальное ожирение (для европеоидов - более 94 см у мужчин и 80 см у женщин);
- Триглицериды более 1,7 ммоль/л или медикаментозная терапия гипертриглицеридемии;
- Снижение ЛПВП (у мужчин: <1,0 ммоль/л, у женщин: <1,3 ммоль/л) или медикаментозная терапия дислипидемии;
- Повышенный уровень АД - более 130/85 мм рт.ст. или прием антигипертензивной терапии пациентом с артериальной гипертензией в анамнезе;
- Повышенный уровень гликемии натощак или прием сахароснижающей терапии.
Критериями исключения из исследования служили: ишемическая болезнь сердца, нарушения ритма и проводимости, пороки сердца, острое нарушение мозгового кровообращения в анамнезе, фракция выброса левого желудочка менее 50%, локальные нарушения сократимости миокарда, выявленные при эхокардиографии, выраженная почечная недостаточность.
Всем пациентам проводили спектральный анализ вариабельности ритма сердца с помощью аппаратно-программного комплекса «Поли-спектр» (ООО «Нейро-Софт», Россия). Функциональные резервы регуляторных систем организма оценивали по пульсовой реакции на активную ортостатическую пробу (смена положения тела - "лежа" - "стоя"). Длительность регистрации ЭКГ для анализа данных составляла 5-минут в положении «лежа», анализ ВРС в ортостазе проводился в течение 5 минут после периода адаптации. Соблюдались следующие требования к условиям исследования ВРС: к исследованию приступали не ранее чем через 1,5 часа после еды, в тихой комнате, в которой поддерживается постоянная температура 20-22°С. Перед исследованием отменялись физиотерапевтические процедуры и медикаменты. Перед началом исследования пациент проходил период адаптации к окружающим условиям в течение 5 минут. В период исследования ВРС предлагалось дышать равномерно и спокойно, не делая глубоких вдохов, не кашлять.
При автоматизированном спектральном анализе ВРС рассчитывались следующие показатели: LF, мс2 - маркер симпатических механизмов регуляции; HF, мс2 - маркер парасимпатических влияний, VLF, мс2 - маркер церебральной симпатико-адреналовой активности; TP, мс2 - интегральный показатель, характеризующий ВРС в целом, отражающий воздействие как симпатического, так и парасимпатического отдела вегетативной нервной системы. Рассчитывались относительные показатели, отражающие вклад каждого компонента спектра в процентах в общий спектр нейрогормонального регулирования (%VLF, %LF, %HF). При этом показатель общей мощности спектра TP принимался за 100%. Каждому пациенту рассчитывались отношения %LFортопроба/%LFфон и %VLFортопроба/%VLFфон. Проведение анализа ВРС с расчетом всех указанных показателей занимало около 15 минут. Критерием включения являлось наличие у пациента верифицированной КАН, на основании значений ВРС - КАН диагностировали в первую очередь при значениях %LFортопроба/%LFфон менее 1,0, как дополнительный критерий использовали отношение %VLFортопроба/%VLFфон более 1,0. Стадию КАН определяли при следующих показателях:
1 стадия КАН - отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон 0,99-0,8;
2 стадия - отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон 0,79-0,5;
3 стадия - отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон менее 0,49.
У одного пациента на фоне отношения %LFортопроба/%LFфон менее 1,0 отношение %VLFортопроба/%VLFфон также был менее 1,0, что было расценено как атипичная стадия КАН.
Для обработки результатов использовали методы вариационной статистики. Количественные показатели выражали в виде «среднее ± стандартная ошибка среднего». Для всех статистических тестов различия считали достоверными при р<0,05. Для порядковых признаков внутри- и межгрупповые различия оценивали непараметрическими тестами: ранговый тест Уилкоксона для парных случаев и U-тест Манна-Уитни.
Все пациенты, принимавшие участие в исследовании, были разделены на группы в зависимости от уровней соотношения %LFортопроба/%LFфон и %VLFортопроба/%VLFфон по данным ВРС.
В 1 группу вошли пациенты с уровнем соотношения VLFортопроба/%VLFфон более 1,0 и %LFортопроба/%LFфон 0,99-0,8 - 54 пациента, средний возраст 50,00±8,56 лет), вторую группу составили пациенты с уровнем соотношения %VLFортопроба/%VLFфон более 1,0 и %LFортопроба/%LFфон 0,79-0,5 - 47 пациентов, средний возраст 53,20±8,90 лет, третью группу - с уровнем соотношения %VLFортопроба/%VLFфон более 1,0 и %LFортопроба/%LFфон менее 0,49-25 пациентов (средний возраст 51,58±8,63 года), четвертая группа %VLFортопроба/%VLфон менее 1,0 и %LFортопроба/%LFфон менее 1,0-1 пациент (возраст 59 лет). 1-3 группы не различались (р>0,05) по возрасту, полу, нозологическим единицам. Выделение групп именно таким образом обусловлено следующими критериями - нижняя граница 0,8 для показателя %LFортопроба/%LFфон обусловлена тем, что именно в этом диапазоне у пациентов отмечалась сохранность компенсаторных механизмах вегетативной регуляции, проявлявшееся увеличением общей мощности спектра TP в ответ на ортостатическую пробу. Увеличение общей мощности спектра, несмотря на угнетение симпатической нервной системы в ответ на функциональные тесты может расцениваться за обратимость, что обусловило определение у этой категории 1 стадии КАН. Порог для %LF обусловлен данными об угнетении активности симпатической нервной системы в ответ на функциональные тесты на 50%, являющимся пограничным и сопряженным с риском внезапной смертности, что определило верификацию 3 стадии при отношении %LFортопроба/%LFфон в 0,49. Таком образом, диапазон отношений %LFортопроба/%LFфон менее 0,8, но более 0,5 соответствовали 2 стадии КАН. Выделение атипичной стадии КАН обусловлено снижением отношений %LFортопроба/%LFфон вне отсутствия снижения уровня VLF в ответ на ортостатическую пробу, что в целом говорит о функциональной активности сегментарных отделов ВНС и требует разработки отдельной стратегии лечения таких пациентов.
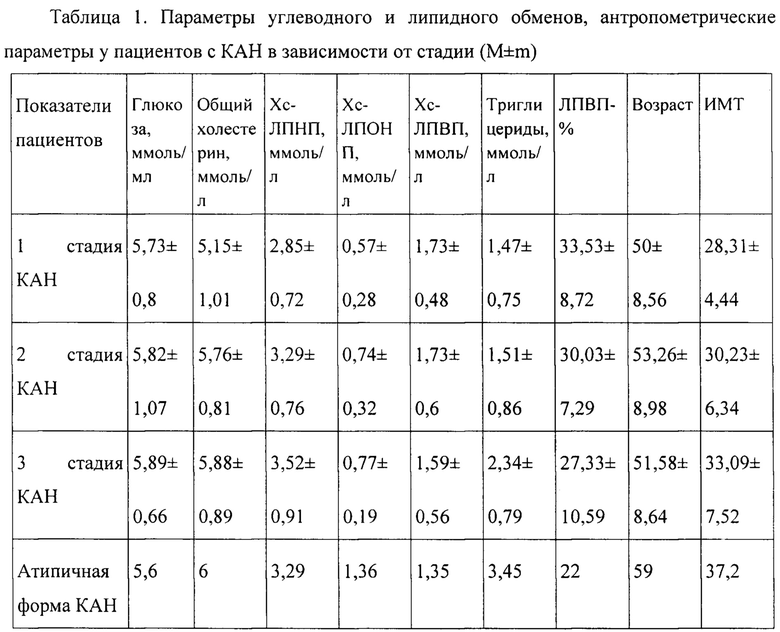
Проведение стандартных рутинных клинических обследований, принятых за «золотой стандарт» у пациентов с метаболическим синдромом, не обеспечило верификацию КАН и ее стадию (табл. 1). Данные пациентов не имели достоверных отличий, что свидетельствует о невозможности даже косвенной оценки состояния вегетативного статуса по стандартным клиническим анализам.
Так как стадийность КАН зависит от степени вклада симпатического звена вегетативной нервной системы в сердечный ритм, снижение показателя %LF можно объяснить прогрессирующим снижением чувствительности барорефлекса, развивающемся на фоне усугубляющихся метаболических нарушений. Угнетение вклада симпатических влияний компенсируется преобладанием центрального контура регуляции сердечным ритмом над автономным, характеризующееся повышением отношения %VLFортопроба/%VLFфон более 1,0. Степень повышения отношения %VLFортопроба/%VLFфон сообразна уменьшению %LFортопроба/%LFфон, поэтому данное отношение не имеет смыла делить по численным показателям, кроме того, такое деление усложнило бы методику расчета стадии КАН.
Атипичное течение КАН на фоне обязательного признака - угнетения активности симпатического отдела вегетативной нервной системы в ответ на физическую нагрузку -характеризуется перераспределением вклада симпатических и парасимпатических влияний на сердечный ритм при неизменном уровне церебральной симпатико-адреналовой активности при проведении ортостатической пробы. Учитывая метаболические показатели пациента с данным типом КАН (табл. 1), следует отметить, что именно оценка вегетативного обеспечения функций позволяет обнаружить клинические признаки и нейрофизиологические корреляты вегетативной дисфункции в виде нарушения симпатико-парасимпатических взаимоотношений.
Пример 1.
Пациентка Г., 47 лет, ИМТ 34,2 кг/м2. Компоненты метаболического синдрома -Повышенный уровень АД - более 130/85 мм рт.ст. (Гипертоническая болезнь I стадии, 2 степени). Повышенный уровень гликемии натощак (Нарушение толерантности к глюкозе). Абдоминальное ожирение (Ожирение 2 ст.) Клинические проявления КАН отсутствуют. Проведена оценка ВРС с помощью аппаратно-программного комплекса «Поли-спектр» (ООО «Нейро-Софт», Россия). Автоматически рассчитаны стандартные показатели ВРС, они приведены в табл. 2.
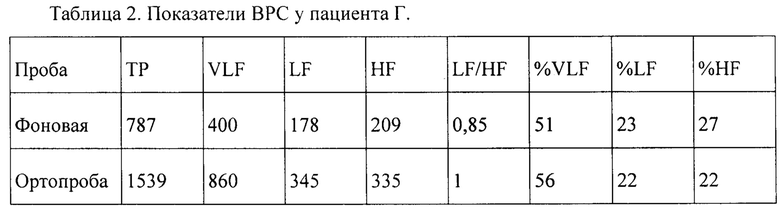
У пациентки в положении лежа в спектре колебаний ритма сердца преобладала очень низкочастотная составляющая VLF как в абсолютных, так и в относительных показателях. При переходе в положение стоя увеличилась общая мощность спектра, что косвенно свидетельствует о сохранных компенсаторных механизмах вегетативной регуляции. Анализ относительных показателей показывает, что при вставании произошло изменение соотношения отдельных составляющих: незначительно повысилась очень низкочастотная составляющая VLF (с 51 до 56%), на фоне незначительного снижения высокочастотной составляющей HF (с 27 до 22%) и низкочастотной составляющей LF (с 23 до 22%). Отношение %VLFортопроба/%VLFфон равен 1,1, то есть более 1,0, а отношение %LFортопроба/%LFфон равен 0,96. Пациентке Г. установлена 1 стадия КАН.
Пример 2.
Пациентка 3., 58 лет, ИМТ 30,8 кг/м2. Компоненты метаболического синдрома: Повышенный уровень АД - более 130/85 мм рт.ст. (Гипертоническая болезнь I стадии, 2 степени). Абдоминальное ожирение (Ожирение I степени). Уровень триглицеридов более 1,7 ммоль/л. (Дислипидемия). Клинические проявление КАН - тахикардия покоя. Проведена оценка ВРС с помощью аппаратно-программного комплекса «Поли-спектр» (ООО «Нейро-Софт», Россия). Автоматически рассчитаны стандартные показатели ВРС, они приведены в табл. 3.

У пациентки 3. в положении лежа в спектре колебаний ритма сердца значительно преобладала очень низкочастотная составляющая VLF как в абсолютных, так и в относительных показателях. При переходе в положение стоя общая мощность спектра значительно уменьшилась. Анализ относительных показателей показывает, что при вставании произошло изменение соотношения этих отдельных составляющих. Значительно повысилась очень низкочастотная составляющая VLF (с 64 до 80%) на фоне выраженного снижения высокочастотной составляющей HF (с 17 до 5%) и умеренного снижения низкочастотной составляющей LF (с 19 до 14%). Такая реакция на ортостатическую пробу не может считаться нормальной, так как не произошло увеличения как общей мощности спектра, так и симпатической нейрорефлекторной активности. Подсчитаны отношения: %LFортопроба/%LFфон равен 0,74, а %VLFортопроба/%VLFфон равен 1,25. Пациентке 3. установлена 2 стадия КАН.
Пример 3.
Пациентка Л., 56 лет, ИМТ 28,7 кг/м2. Компоненты метаболического синдрома: Повышенный уровень АД - более 130/85 мм рт.ст. (Гипертоническая болезнь I стадии, 2 степени). Абдоминальное ожирение. (Избыточная масса тела). Снижение ЛПВП: у мужчин: <1,0 ммоль/л, у женщин: <1,3 ммоль/л. (Дислипидемия). Повышенный уровень гликемии натощак (Нарушение толерантности к глюкозе). Клиническое проявление КАН - тахикардия покоя. Проведена оценка ВРС с помощью аппаратно-программного комплекса «Поли-спектр» (ООО «Нейро-Софт», Россия). Автоматически рассчитаны стандартные показатели ВРС, они приведены в табл. 3.
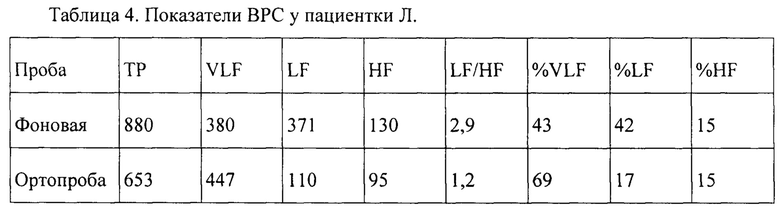
У пациентки Л. в положении лежа в спектре колебаний ритма сердца незначительно преобладала очень низкочастотная составляющая VLF как в абсолютных, так и в относительных показателях. При переходе в положение стоя общая мощность спектра незначительно уменьшилась, что косвенно свидетельствует о выраженной патологической стабилизации сердечного ритма. Анализ относительных показателей показывает, что при вставании произошло изменение соотношения этих отдельных составляющих. Значительно повысилась очень низкочастотная составляющая VLF (с 43 до 69%) на фоне не изменившейся высокочастотной составляющей HF (15%) и значительного снижения низкочастотной составляющей LF (с 42 до 17%). Подсчитаны отношения: %LFортопроба/%LFфон равен 0,4, а %VLFортопроба/%VLFфон равен 1,6. Пациентке Л. установлена 3 стадия КАН.
Пример 4.
Пациент К., 59 лет, ИМТ 37,2 кг/м2. Компоненты метаболического синдрома: Абдоминальное ожирение (Ожирение 2 ст.). Триглицериды более 1,7 ммоль/л. (Дислипидемия). Повышенный уровень гликемии натощак (Нарушение толерантности к глюкозе). Клинические проявления КАН отсутствуют. Проведена оценка ВРС с помощью аппаратно-программного комплекса «Поли-спектр» (ООО «Нейро-Софт», Россия). Автоматически рассчитаны стандартные показатели ВРС, они приведены в табл. 5.
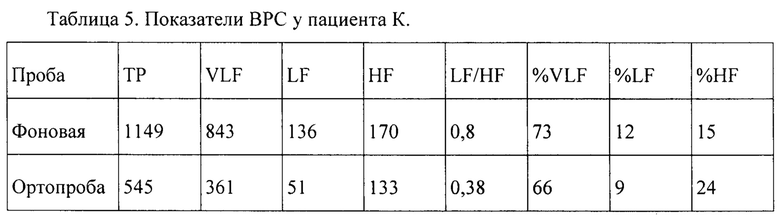
У пациента К. в положении лежа в спектре колебаний ритма сердца преобладала очень низкочастотная составляющая VLF как в абсолютных, так и в относительных показателях. При переходе в положение стоя общая мощность спектра значительно уменьшилась. Анализ относительных показателей показывает, что при вставании произошло изменение соотношения этих отдельных составляющих. Незначительно снизилась очень низкочастотная составляющая VLF (с 73 до 66%) на фоне повысившейся высокочастотной составляющей HF (с 15 до 24%) и снижения низкочастотной составляющей LF (с 12 до 9%). Снижение уровня LF безусловно свидетельствует о характерной диссеминированной нейрональной дегенерацией малых нервных волокон симпатического отдела ВНС, однако отсутствие снижения уровня VLF в ответ на ортостатическую пробу говорит в целом о функциональной активности сегментарных отделов ВНС. Подсчитаны отношения: %LFортопроба/%LFфон равен 0,75, при этом %VLFортопроба/%VLFфон равен 0,9. Пациенту К. установлена атипичная форма КАН.
Таким образом, исследование вегетативной регуляции ритма у пациентов с метаболическим синдромом показало, что применение отношений относительных спектральных показателей вариабельности ритма сердца при проведении активной ортостатической пробы к таковым в покое позволяет определить стадию КАН вне зависимости от наличия ее клинических проявлений при следующих показателях:
1 стадия КАН - отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон 0,99-0,8;
2 стадия - отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон 0,79-0,5;
3 стадия - отношение %VLFортопроба/%VLFфон более 1,0 и отношение %LFортопроба/%LFфон менее 0,49.
Атипичная стадия КАН - отношение %LFортопроба/%LFфон менее 1,0 и значение отношения %VLFортопроба/%VLфон менее 1,0.
Предлагаемый в качестве изобретения способ апробирован на 127 пациентах и позволяет определить стадию кардиальной автономной нейропатии вне зависимости от наличия ее клинических проявлений у пациентов с метаболическим синдромом и тем самым позволит своевременно назначить патогенетически обусловленную терапию для предотвращения прогрессирования заболевания и снижения риска фатальных осложнений. Помимо этого данный способ может лечь в основу разработки подходов к назначаемой терапии, так как позволит оценить ее эффективность.
Список литературы:
1. Vinik A. I., Ziegler D. Diabetic cardiovascular autonomic neuropathy // Circulation. - 2007. - Vol. 115. - P. 387-397
2. Минаков Э.В., Кудаева Л.А. Изучение особенностей формирования кардиальной нейропатии улиц с метаболическим синдромом и нарушением углеводного обмена (по данным анализа вариабельности сердечного ритма) // Саратовский научно-медицинский журнал. - 2010. - Т. 6. - Вып. 3. - С. 582-585.
3. Черникова Н.А. Сердечно-сосудистая форма диабетической автономной нейропатии // Эффективная эндокринология. - 2013. - Спецвыпуск. - С 44-50
4. Pop-Busui R. Cardiac Autonomic Neuropathy in Diabetes. A clinical perspective // Diabetes Care. - 2010. - Vol. 33 (2). - P. 434-441
5. Нурахмедова И.С., and Нурбекова А.А. Диабетическая кардиальная автономная нейропатия: современные перспективы // Вестник Казахского Национального медицинского университета. - 2019. - №1. С. 345-351.
6. Патент №2585741 Российская Федерация «Способ ранней диагностики кардиальной автономной нейропатии у пациентов с артериальной гипертензией и метаболическими нарушениями» / Удут В.В., Ксенева С.И., Бородулина Е.В., Трифонова О.Ю. // Зарегистрирован в Государственном реестре изобретений РФ 10.06.2016
7. Нуждина Е.В., Давыдова Е.В. Автономная кардиальная нейропатия и ремоделирование миокарда левого желудочка у пациентов с сахарным диабетом и сопутствующими болезнями системы кровообращения и почек. // Профилактическая медицина. - 2020. Т. 23 (1). - С. 127-134.
8. Чухнин Е. В., Амиров Н. Б. Вариабельность сердечного ритма. Метод и клиническое применение // Вестник современной клинической медицины. - 2008. - №1. - С 72-78.
9. Alberti KG, Eckel RH, Grundy SM. et al. Harmonizing the metabolic syndrome: a joint interim statement of the International Diabetes Federation Task Force on Epidemiology and Prevention; National Heart, Lung, and Blood Institute; American Heart Association; World Heart Federation; International Atherosclerosis Society; and International Association for the study of Obesity. // Circulation. 2009. - Vol. 120. P. 1640-1645.
Изобретение относится к медицине, а именно к кардиологии, эндокринологии и неврологии. Проводят фоновое исследование вариабельности ритма сердца в положении лежа 5 мин и при выполнении активной ортостатической пробы в течение 5 мин с последующим спектральным анализом и расчетом относительных спектральных показателей, представляющих вклад каждого из компонентов спектра колебаний ритма сердца: VLF - очень низкочастотного, LF - низкочастотного в общую мощность спектра колебаний ритма. Рассчитывают отношение каждого относительного показателя при проведении ортостатической пробы к таковому при фоновой записи. У пациентов с метаболическим синдромом при одновременном значении отношения %VLFортопроба/%VLFфон более 1,0 и значении отношения %LFортопроба/%LFфон 0,99-0,80 определяют 1 стадию КАН; при одновременном значении отношения %VLFортопроба/%VLFфон более 1,0 и значении отношения %LFортопроба/%LFфон 0,79-0,50 определяют 2 стадию КАН; при одновременном значении отношения %VLFортопроба/%VLFфон более 1,0 и значении отношения %LFортопроба/%LFфон менее 0,49 определяют 3 стадию КАН, а при одновременном значении отношения %VLFортопроба/%VLFфон менее 1,0 и значении отношения %LFортопроба/%LFфон менее 1,0 определяют атипичную стадию КАН. Способ обеспечивает определение стадии кардиальной автономной нейропатии вне зависимости от наличия ее клинических проявлений у пациентов с метаболическим синдромом, что позволит своевременно назначить патогенетически обусловленную терапию для предотвращения прогрессирования заболевания и снижения риска фатальных осложнений. 5 табл., 4 пр.
Способ определения стадии кардиальной автономной нейропатии (КАН) вне зависимости от наличия ее клинических проявлений у пациентов с метаболическим синдромом, включающий оценку вегетативной регуляции сердечного ритма при фоновой записи в течение 5 минут и при активной ортостатической пробе в течение 5 минут с последующим спектральным анализом и определением отношений относительных значений LF и VLF, полученных при проведении активной ортостатической пробы, к таковым при фоновой записи, отличающийся тем, что при одновременном значении отношения %VLFортопроба/%VLFфон более 1,0 и значении отношения %LFортопроба/%LFфон 0,99-0,80 определяют 1 стадию КАН; при одновременном значении отношения %VLFортопроба/%VLFфон более 1,0 и значении отношения %LFортопроба/%LFфон 0,79-0,50 определяют 2 стадию КАН; при одновременном значении отношения %VLFортопроба/%VLFфон более 1,0 и значении отношения %LFортопроба/%LFфон менее 0,49 определяют 3 стадию КАН, а при одновременном значении отношения %VLFортопроба/%VLFфон менее 1,0 и значении отношения %LFортопроба/%LFфон менее 1,0 определяют атипичную стадию КАН.
Авторы
Даты
2024-04-22—Публикация
2023-07-31—Подача