Изобретение относится к медицине, а именно к лучевой диагностике, и может быть использовано для стандартизации методики количественной неинвазивной оценки перегрузки печени железом с использованием магнитно-резонансной томографии (МРТ).
Перегрузка железом является системным заболеванием и бывает первичной (генетическим) или вторичной (экзогенное введение железа). Первичная перегрузка железом чаще всего связана с наследственным гемохроматозом, а вторичная перегрузка железом – с неэффективным эритропоэзом (преимущественно вызванным β-талассемией и серповидно-клеточной анемией), что требует длительной трансфузионной терапии и приводит к трансфузионному гемосидерозу. Печень является одним из основных органов хранения железа, и первой страдает от перегрузки железом. Перегрузка железом может привести к сердечно-сосудистым и эндокринным осложнениям, а также, при наиболее неблагоприятном течении, – к циррозу печени и гепатоцеллюлярной карциноме. Следовательно, обнаружение и количественная оценка перегрузки печени железом имеют решающее значение для начала лечения и предотвращения осложнений.
Пункционная биопсия печени исторически была эталонным методом обнаружения и количественной оценки содержания железа в печени (Pietrangelo A. Hereditary hemochromatosis – a new look to an old disease. N. Engl. J. Med. 2004; 350: 2383-2397). Однако у данного метода существует ряд ограничений, таких, как большой разброс значений концентрации железа из-за малого объема биопсийного материала в условиях неравномерности распределения железа в печени, инвазивность и болезненность процедуры, а также риск развития кровотечения, воспалительных осложнений и других нежелательных последствий вмешательства, что особенно опасно в педиатрической практике.
Из современного уровня техники известен неинвазивный способ количественной оценки концентрации железа в печени при помощи МРТ (Alustiza J.M., Artetxe J., Castiella A. MR quantification of hepatic iron concentration. Radiology. 2004; 230: 479-484; Gandon Y., Olivie D., Guyader P.D. Noninvasive assessment of hepatic iron stores by MRI. Lancet. 2004; 363: 357-362). В основе способа лежит метод Т2* картирования. Железо в паренхиме печени в основном представлено в виде фосфатного гидроксида трехвалентного железа, связанного с белком ферритином, и гидроокиси трехвалентного железа в составе пигмента гемосидерина. Так как атомы трехвалентного железа являются парамагнитными, то и данные вещества также проявляют парамагнитные свойства. Они вносят сильные неоднородности в локальные магнитные поля и как следствие оказывают влияние на параметр Т2* релаксации, который сильно зависит от таких неоднородностей.
Стандартной магнитно-резонансной (МР) последовательностью для измерения значений Т2* является последовательность GRE (gradient echo). По полученным изображениям формируется карта распределения значений Т2* (далее – Т2* карта), характеризующая концентрации железа: чем ниже значения Т2* – тем больше железа содержится в выбранной области и тем более высокая степень перегрузки железом. Данный метод является неинвазивным, безболезненным и позволяет сделать оценку перегрузки железом по всему объему печени в течение короткого времени, что, несомненно, решает проблемы биопсии, описанные выше. При этом для стандартизации пересчета значений Т2* в истинные концентрации железа (LIC – liver iron concentration) и установления степени перегрузки железом используется уравнение пересчета Т2*/LIC при сравнении количественных данных МРТ и результатов биопсии. В педиатрической практике у пациентов детского возраста с посттрансфузионной перегрузкой железом для расчетов применяются калибровочные кривые пересчета значений Т2* в LIC (Назарова Э.Э., Терещенко Г.В., Абакумов М.А. и др. Методика проведения Т2*-картирования печени у пациентов со вторичной перегрузкой железом // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. – 2017. – Т. 16. – №3. – С. 23-27). Однако такие калибровочные кривые могут быть специфичны к методам (параметры Т2* картирования, методика проведения биопсии) и условиям (марка магнитно-резонансного томографа, на котором проводится исследование) проведения исследования, поэтому они могут с надежностью использоваться только на тех аппаратах, на которых были получены.
Технический результат заключается в способе стандартизации количественной магнитно-резонансной оценки содержания железа в печени с использованием фантома наночастиц железа.
Технический результат достигается тем, что для стандартизации метода количественного МР-определения концентрации железа в печени создается МР-совместимый фантом различных концентраций железа с заданными референсными значениями и доверительными интервалами по графику Блэнда-Альтмана; получаемые в результате измерения на калибруемом МР-томографе значения Т2* для каждого уровня концентрации железа созданного фантома сравниваются с референсными результатами, полученными на основе предшествующих многократных измерений на двух МР-томографах различных производителей с напряженностью поля 3 и 1,5 Тл; если результаты измерений попадают в доверительные интервалы для референсных значений, то применение формулы пересчета значений Т2* в LIC признается надежным на калибруемом аппарате; в случае отличия значений Т2* от референсных – проводится калибровка параметров МР-последовательности и протокола сканирования до достижения данного соответствия.
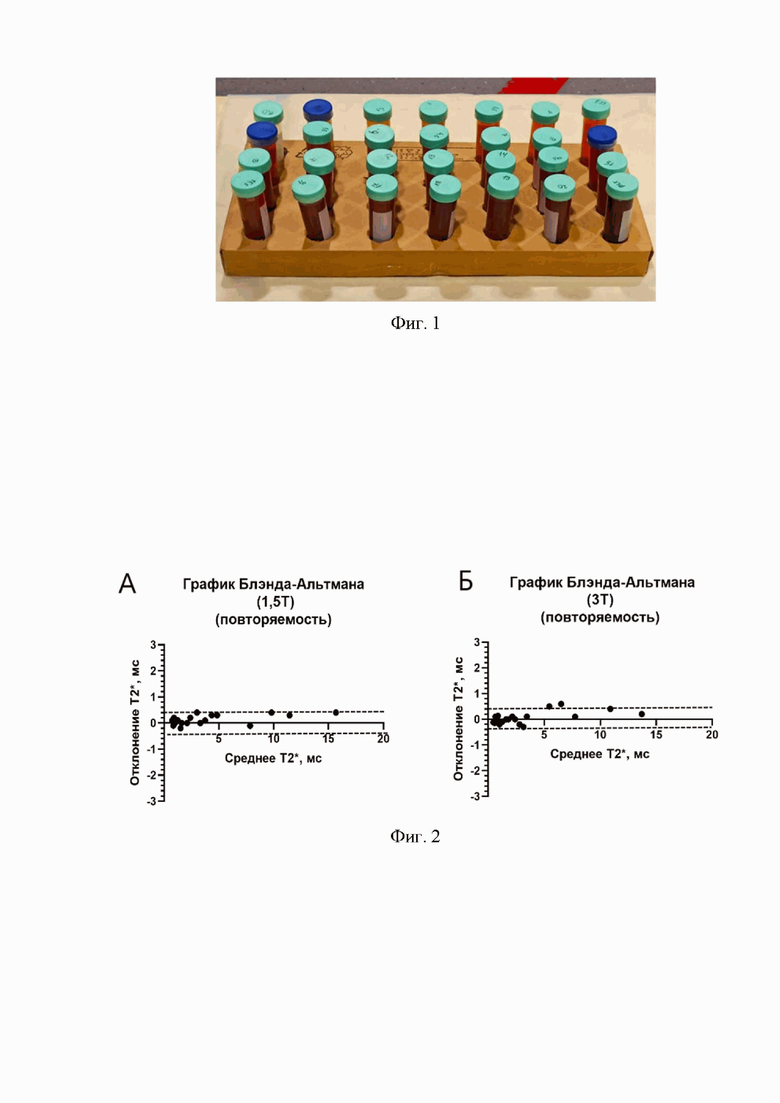
Способ стандартизации количественной магнитно-резонансной оценки содержания железа в печени проводят следующим образом: на первом этапе создается МР-совместимый фантом, состоящий из 28 пробирок объемом по 50 мл каждая (Фиг. 1), содержащих парамагнитные наночастицы сложного оксида железа (Fe3O4), полученных в результате реакции Элмора, где в качестве носителей ионов двух- и трехвалентного железа используются 6- водный хлорид железа (III) и 7-водный сульфат железа (II), для начала процесса осаждения и образования наночастиц применяется гидрат аммония, а для контроля роста и стабилизации частиц используется лимонная кислота; полученный в результате реакции раствор центрифугируется при скорости 1500 об/мин в течение 5 минут для осаждения крупных частиц; верхняя фракция раствора является искомой коллоидной взвесью наночастиц оксида железа, которые фильтруются через стандартную фильтровальную бумагу со средним диаметром пор 3-5 мкм; полученный коллоидный раствор с высокой концентрацией железа разводится с последовательным увеличением степени разведения до получения значения Т2*, соответствующего значениям в здоровой печени и при всех четырех степенях перегрузки печени железом; на втором этапе получаются референсные значения МР-сканирования фантома на двух МР-томографах различных производителей с напряженностью поля 3 и 1,5 Тл, при том, что исследовательские протоколы включают в себя получение Т2* карт с помощью методики быстрого градиентного эхо (mGRE) и на всех МР-сканерах основные параметры используемых последовательностей соответствуют тем, что используются в in vivo исследованиях – угол наклона (FA, flip angle) – 45°, время эхо (ТE, echo time) – 1,2 мс, количество эхосигналов – 20 с шагом ∆TE = 1,5 мс, время повторения (TR, repetition time) – 350 мс; разрешение – 1,5×1,5 мм, для МР-сканеров с напряженностью поля 1,5 и 3 Тл толщина среза составляет 10 и 7 мм, соответственно; на третьем этапе путем 15-17-кратного повторения МР-сканирования фантома на каждом из двух МР-сканерах разных производителей с напряженностью поля 3 и 1,5 Тл подтверждается стабильность фантома с получением референсных значений и их доверительных интервалов по графику Блэнда-Альтмана (Фиг. 2.); на четвертом этапе получаемые в результате измерения на калибруемом МР-томографе значения Т2* для каждой пробирки созданного фантома сравниваются с референсными результатами, полученными на основе предшествующих 15-17-кратных измерений на двух МР-томографах различных производителей с напряженностью поля 3 и 1,5 Тл, если результаты измерений попадают в доверительные интервалы для референсных значений, то применение формулы пересчета значений Т2* в LIC признается надежным на калибруемом аппарате, в случае отличия значений Т2* от референсных – проводится калибровка параметров МР-последовательности и протокола сканирования до достижения данного соответствия.
Описанный технический результат подтверждается в следующих примерах.
Пример 1. Апробация метода стандартизации последовательности mGRE на томографе Philips Achieva dStream (Best, The Netherlands) / 3 Тл
Сканирование фантома проводилось на томографе Philips Achieva dStream (Best, The Netherlands) / 3Тл с использованием приемной поверхностная катушки для сканирования тела dsTorso. Проводилась калибровка параметров исследования до необходимых значений: (FA, flip angle) - 45°, время эхо (ТE, echo time) – 1,2 мс, количество эхосигналов – 20 с шагом ΔTE = 1,5 мс, время повторения (TR, repetition time) – 350 мс; разрешение – 1,5×1,5 мм. Толщина среза составляла 7 мм. В результате был достигнут результат соответствия получаемых результатов референсным в переделе стандартных отклонений.
Пример 2. Апробация метода стандартизации последовательности mGRE на томографе Philips Ingenia (Best, The Netherlands) / 1.5 Тл
Сканирование фантома проводилось на томографе Philips Ingenia (Best, The Netherlands) / 1.5 Тл с использованием приемной поверхностной 16-ти канальная катушки FlexCoverage. Проводилась калибровка параметров исследования до необходимых значений: (FA, flip angle) - 45°, время эхо (ТE, echo time) – 1,2 мс, количество эхосигналов – 20 с шагом ΔTE = 1,5 мс, время повторения (TR, repetition time) – 350 мс; разрешение – 1,5×1,5 мм. Толщина среза составляла 10 мм. В результате был достигнут результат соответствия получаемых результатов референсным в переделе стандартных отклонений.
Пример 3. Апробация метода стандартизации последовательности mGRE на томографе Siemens Magnetom Trio / 3T
Сканирование фантома проводилось на Siemens Magnetom Trio / 3T. Проводилась калибровка параметров исследования до необходимых значений: (FA, flip angle) - 45°, время эхо (ТE, echo time) – 1,2 мс, количество эхосигналов – 20 с шагом ΔTE = 1,2 мс, время повторения (TR, repetition time) – 350 мс; разрешение – 1,5×1,5 мм. Толщина среза составляла 7 мм. Однако в резалтАте этого не удалось добиться желаемых результатов. Тогда были введены добавочные коэффициенты в формулу пересчета Т2* в LIC. В результате был достигнут результат соответствия получаемых результатов референсным в переделе стандартных отклонений.
Пример 4. Апробация метода стандартизации последовательности mGRE на томографе GE SIGNA Pioneer / 3.0Т
Сканирование фантома проводилось на томографе GE SIGNA Pioneer / 3.0 Т. Проводилась калибровка параметров исследования до необходимых значений: (FA, flip angle) - 45°, время эхо (ТE, echo time) – 1,2 мс, количество эхосигналов – 20 с шагом ΔTE = 1,6 мс, время повторения (TR, repetition time) – 350 мс; разрешение – 1,5×1,5 мм. Толщина среза составляла 7 мм. Однако в результате этого не удалось добиться желаемых результатов. Тогда были введены добавочные коэффициенты в формулу пересчета Т2* в LIC. В результате был достигнут результат соответствия получаемых результатов референсным в переделе стандартных отклонений.
Пример 5. Апробация метода стандартизации последовательности mGRE на томографе Siemens Magnetom Aera / 1.5Т
Сканирование фантома проводилось на томографе Siemens Magnetom Aera (Германия) / 1.5 Тл. Проводилась калибровка параметров исследования до необходимых значений: (FA, flip angle) - 45°, время эхо (ТE, echo time) – 1,3 мс, количество эхосигналов – 20 с шагом ΔTE = 1,6 мс, время повторения (TR, repetition time) – 350 мс; разрешение – 1,5×1,5 мм. Толщина среза составляла 10 мм. В результате был достигнут результат соответствия получаемых результатов референсным в переделе стандартных отклонений.
Исследование проведено в соответствии с действующими нормативными правовыми и этическими требованиями, предъявляемыми к клиническим исследованиям с участием детей (Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 г. №323-ФЗ в действующей редакции, Приказ Министерства здравоохранения Российской Федерации от 01.04.2016 г. №200н «Об утверждении правил надлежащей клинической практики») и одобрены Независимым этическим комитетом.
Таким образом, предлагаемый способ стандартизации получения значений Т2* на различных МР-томографах позволяет быстро, эффективно и неинвазивно оценивать перегрузку железом печени в любых медицинских организациях, оснащенных МР-томографами.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественной оценки степени перегрузки железом печени у детей | 2018 |
|
RU2701771C1 |
| СПОСОБ МАГНИТНО-РЕЗОНАНСНОЙ ТОМОГРАФИЧЕСКОЙ ДИАГНОСТИКИ ИШЕМИЧЕСКИХ НАРУШЕНИЙ КОРОНАРНОГО КРОВООБРАЩЕНИЯ | 2006 |
|
RU2330609C1 |
| Способ выявления очаговых изменений кортикальной, инфратенториальной и спинальной локализации при рассеянном склерозе | 2023 |
|
RU2807389C1 |
| СПОСОБ ВИЗУАЛИЗАЦИИ БАЗИЛЯРНОЙ АРТЕРИИ НА НИЗКОПОЛЬНОМ МАГНИТНО-РЕЗОНАНСНОМ ТОМОГРАФЕ | 2005 |
|
RU2286714C1 |
| Способ оценки скорости церебрального кровотока в зонах нейрональной активации | 2018 |
|
RU2702587C1 |
| СПОСОБ ИЗМЕРЕНИЯ Т2-РЕЛАКСАЦИИ, КАК КОЛИЧЕСТВЕННОГО МАРКЕРА ПАТОЛОГИЧЕСКИХ ИЗМЕНЕНИЙ | 2022 |
|
RU2808192C1 |
| СПОСОБ ИССЛЕДОВАНИЯ ФУНКЦИИ ПОЧЕК НА НИЗКОПОЛЬНОМ МАГНИТНО-РЕЗОНАНСНОМ ТОМОГРАФЕ | 2002 |
|
RU2219833C1 |
| Способ определения комплекса биомеханических параметров аорты в диагностике сердечно-сосудистых заболеваний | 2022 |
|
RU2791391C1 |
| Способ оценки количественного накопления парамагнитного контрастного препарата GDOF-Mn-DTPA для магнитно-резонансной томографии печени экспериментальных животных | 2018 |
|
RU2699334C1 |
| СПОСОБ ДИАГНОСТИКИ РАСПРОСТРАНЕНИЯ НЕОПЛАСТИЧЕСКОГО ПРОЦЕССА ПИЩЕВОДА | 2014 |
|
RU2566185C1 |
Изобретение относится к медицине, а именно к лучевой диагностике. Стандартизации метода количественного МР-определения концентрации железа в печени создается МР-совместимый фантом различных концентраций железа с заданными референсными значениями и доверительными интервалами по графику Блэнда-Альтмана; получаемые в результате измерения на калибруемом МР-томографе значения Т2* для каждого уровня концентрации железа созданного фантома сравниваются с референсными результатами, полученными на основе предшествующих многократных измерений на двух МР-томографах различных производителей с напряженностью поля 3 и 1,5 Тл; если результаты измерений попадают в доверительные интервалы для референсных значений, то применение формулы пересчета значений Т2* в LIC признается надежным на калибруемом аппарате; в случае отличия значений Т2* от референсных - проводится калибровка параметров МР-последовательности и протокола сканирования до достижения данного соответствия. Технический результат заключается в способе стандартизации количественной магнитно-резонансной оценки содержания железа в печени с использованием фантома наночастиц железа. 2 ил., 5 пр.
Способ стандартизации количественной магнитно-резонансной оценки содержания железа в печени, заключающийся в том, что для стандартизации метода количественного МР-определения концентрации железа в печени создают МР-совместимый фантом различных концентраций железа, полученных путем последовательного увеличения степени разведения исходного высококонцентрированного коллоидного раствора наночастиц железа в форме 6-водного хлорида железа (III) и 7-водного сульфата железа (II) до получения значения Т2*, соответствующих значениям концентрации железа в здоровой печени и при всех четырех степенях перегрузки печени железом, с заданными референсными значениями и доверительными интервалами по графику Блэнда-Альтмана; получаемые в результате измерения на калибруемом МР-томографе значения Т2* для каждого уровня концентрации железа созданного фантома сравнивают с референсными результатами, полученными на основе предшествующих измерений на двух МР-томографах различных производителей с напряженностью поля 3 и 1,5 Тл; если результаты измерений попадают в доверительные интервалы для референсных значений, то применение формулы пересчета значений Т2* в концентрацию железа в печени (LIC) признают надежным на калибруемом аппарате; в случае отличия значений Т2* от референсных – проводят калибровку параметров МР-последовательности и протокола сканирования до достижения соответствия.
| КАЛИБРОВКА УЛЬТРАЗВУКОВОГО, ОСНОВАННОГО НА ЭЛАСТИЧНОСТИ, ОТОБРАЖЕНИЯ ГРАНИЦЫ ОЧАГА ПОРАЖЕНИЯ | 2016 |
|
RU2702090C2 |
| Способ количественной оценки степени перегрузки железом печени у детей | 2018 |
|
RU2701771C1 |
| СПОСОБ НЕИНВАЗИВНОГО КАЧЕСТВЕННОГО И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ МАГНИТОУПРАВЛЯЕМЫХ НАНОПРЕПАРАТОВ И ОЦЕНКИ ИХ ФУНКЦИЙ В РЕАЛЬНОМ ВРЕМЕНИ У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2009 |
|
RU2427390C2 |
| Способ приготовления содержащих серу продуктов конденсации ароматического ряда | 1926 |
|
SU6643A1 |
| Титова А.М и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Радиология, том 4 N5 / 2017. | |||
Авторы
Даты
2024-05-07—Публикация
2022-07-27—Подача