Настоящее изобретение имеет приоритет патентной заявки США № 62/140672, поданной 31 марта 2015 г., которая включена сюда полностью путем ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к использованию визуализации для пространственного отображения эластичности и, более конкретно, к калибровке карты и/или обнаружению границы очага поражения.
УРОВЕНЬ ТЕХНИКИ ПО ИЗОБРЕТЕНИЮ
Способы термоабляции в качестве альтернативы радикальной хирургии являются минимально инвазивными, требуя только игл (радиочастотная (RF)), криогенная или микроволновая абляция) или неинвазивнового источника тепла, например, использующего высокоинтенсивный сфокусированный ультразвук (HIFU). В большинстве процедур злокачественная ткань нагревается до температуры свыше 55°С и коагулируется.
RF абляция (RFA) явятся в настоящее время единственным утвержденным FDA способом термоабляции в Соединенных Штатах. В нем используется зонд с активным электродным наконечником, через который пропускается переменный электрический ток с частотой 460-500 кГц. Этот ток вызывает ионное возбуждение и нагревание от трения. Тепло затем рассеивается через тепловую проводимость для осуществления абляции опухоли. RFA часто используется для лечения рака печени. Насчитывается около 500 000 новых случаев метастатического рака печени в западном мире и около 1 миллиона новых случаев первичного рака печени во всем мире (83% из которых относятся к развивающимся странам). RFA и микроволновый способы абляции также становятся более популярными в развивающихся странах вследствие сообщенного большого числа заболеваний раком печени (например, 433000 новых случаев в 2009 году только в Китае). Существующие протоколы лечения используют упрощенный объем сферической абляции, предложенный спецификациями изготовителей устройств. Действительный объем лечения значительно отличается от предложенного, что в результате приводит к большой частоте рецидивов (приблизительно 35%).
RFA обычно выполняется под визуализационным контролем и мониторингом. Одной общей причиной высокой частоты рецидивов является неспособность осуществлять мониторинг и контролировать размер абляции, чтобы адекватно убивать опухолевые клетки. Поэтому весьма важно обеспечить обратную связь в режиме реального времени для практикующего врача. В настоящее время это может быть достигнуто с приемлемой точностью термовизуализацией, основанной на магнитном резонансе (MR). Однако магнитно-резонансная визуализация (MRI) является дорогой и может быть не легко доступной. В качестве альтернативной возможности мониторинга обычно используется ультразвук для визуального контроля во время размещения иглы. Благодаря простоте использования и широкой доступности это потенциально предпочтительный способ для мониторинга очагов поражения. Однако на сегодня единственным путем его использования для мониторинга лечения является визуализация гиперэхогенных очагов поражения на изображениях в B-режиме. В большинстве случаев гиперзхогенность является следствием образования микропузырьков во время RFA, которое является временным эффектом и плохо коррелирует с границами очага поражения. Поэтому такая визуализация является только приблизительным и не хорошим индикатором эффективности лечения.
Ультразвук был использован в эластографии сдвиговой волны применительно к очагам поражения печени. Guibal, A: ʺОценка эластографии сдвиговой волны для определения характеристик локальных очагов поражения печени на ультразвукеʺ, Европейское общество радиологии (European Society of Radiology), 23:1138-1149 (2013). В Guibal исследовании описывается преимущество обеспечения в режиме реального времени двумерного количественно измеряемого изображения жесткости ткани.
Известно также, что жесткость ткани изменяется во время термоабляции.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Вследствие значительных изменений эластичности ткани с повышением температуры ультразвуковая визуализация эластичности имеет огромные потенциальные возможности в мониторинге абляции. Кода достигается пороговое значение некроза ткани, ткань начинает затвердевать и продолжает делать это под возрастающим тепловым воздействием. Отслеживая это изменение, можно оценить ход выполнения лечения и можно определить конечную точку. Жесткость ткани может быть измерена использованием построения изображения с помощью поперечных (далее - сдвиговых) волн. Это влечет за собой использование акустического лучевого импульса для генерации смещения и сдвиговых волн, которые затем прослеживаются для извлечения информации о жесткости. Сдвиговые волны распространяются быстрее с меньшим смещением в более жестких тканях тела.
Построения изображения с помощью сдвиговых волн (SWI) для пространственного отображения эластичности имеет огромные потенциальные возможности для лечения термоабляцией.
Однако известные SWI режимы, используемые в основанной на ультразвуке эластографии, не достаточно чувствительны для точного обнаружения границы подвергшегося абляции участка ткани вблизи жесткого медицинского инструмента, такого как абляционная игла или зубец, выступающий из электрода иглы. Во-первых, жесткость инструмента ограничивает смещение сдвиговой волной подвергающейся абляции ткани, окружающей иглу. Во-вторых, измерения эластичности, например, модуля упругости, страдают от низкого отношения сигнала к шуму (S/N). Кроме того, SWI чувствительность дополнительно снижается применительно к малым, глубоким очагам поражения, если низкочастотный преобразователь используется для построения изображения. Низкочастотная визуализация страдает от низкой пространственной разрешающей способности, но более высокие частоты ограничиваются в отношении глубины проникновения изображения. Ограничение является особенно строгим для абляции очага поражения более 40 миллиметров (мм) в глубину и менее 15 мм в диаметре, расположенного около критичной структуры (например, нерва или кровеносного сосуда), которая должна быть защищена от абляции. Такая структура именуется ниже защищенной структурой. Также должно быть затруднительным вычерчивать границу очага поражения при возрастающем тепловом воздействии по сравнению с первоначальным контуром опухоли.
Изображения эластичности, основанные на модуле упругости, были произведены на основе локальных скоростей сдвиговых волн, которые дополнительно определялись из времени распространения сдвиговых волн, такого как время до достижения пикового значения (TTP) или крутизна нарастания времени до достижения пикового значения (TTPS). Некоторыми из препятствий к эффективной оценке эластичности при основанном на модуле упругости мониторинге в режиме реального времени являются следующие: (1) трудно определить, где находится пик сдвиговой волны с самым малым смещением; (2) также трудно отличить пики самой быстрой сдвиговой волны между двух соседних точек; (3) существует даже меньшее смещение для подвергающейся абляции ткани, когда абляционная игла присутствует во время абляции; и (4) отражение сдвиговой волны от абляционной иглы усложняет профили сдвиговой волны более чем одним пиком.
Предложенный здесь подход обнаруживает границу очага поражения, анализируя ʺраспространение сдвиговой волны в здоровых тканяхʺ до тех пор, пока сдвиговая волна не пройдет через границу жесткого очага поражения.
Другой проблемой является то, что вводимое ультразвуком поле в SWI влияет на измерения эластичности, так как ультразвуковое поле не может быть создано с однородной амплитудой по всей глубине (тогда как может быть сфокусировано в единственную глубину).
В соответствии с тем, что предложено здесь, эффекты ультразвукового поля и/или искажения в измерении сдвиговой волны, вызванные присутствием жестких инструментов вблизи измерений, устраняются, или минимизируются, использованием вычисления разности карт, представляющих пространственные эластичности. Устойчивость к любым различиям, которые будут появляться в результате использования конкретного преобразователя/устройства отображения, является другим преимуществом. То же самое можно сказать применительно к свойствам эластичности конкретного пациента. В одном варианте осуществления даже небольшие ошибки, возникающие в гетерогенности в исследуемой среде, могут быть аннулированы через использование разностных карт.
Обычно карты эластичности представляют распределение модуля упругости. Модуль упругости, типовой показатель эластичности, пропорционален квадрату скорости распространения сдвиговой волны. В том, что предлагается здесь, динамический мониторинг устраняет необходимость в разделении на мелкие, трудно выполнимые измерения, дополнительно повышая тем самым отношение S/N. В частности, не требуется вычислять скорость распространения в качестве промежуточного значения для использования в вычислении модуля упругости.
Следует также заметить, что не требуются сложные многоканальные формирователи луча высшего порядка для предложенных способов эффективного отображения очертаний подвергаемых термоабляции очагов поражения; причем приводимые в качестве примера способы также подходят даже для более экономичных ультразвуковых сканеров, которые имеют только ограниченный ряд параллельных отслеживающих лучей или которые испускают отслеживающие лучи последовательно.
Более конкретно, принимая во внимание эти основные положения, в одном аспекте целевая среда опрашивается в соответствии с визуализацией в режиме ультразвуковой эластографии, и, основываясь на результате этого опрашивания, формируется карта пространственного распределения эластичности. Эта карта калибруется по эталонной карте пространственного распределения эластичности, которая сдержит набор разных значений эластичности. Эталонная карта выполнена с возможностью отображения ультразвуковых изображений эталонной среды, построенных с помощью сдвиговых волн. Эталонная среда не является целевой и не расположена в целевой.
В конкретном дополнительном аспекте эталонная среда является либо: a) гомогенной, если оборудование для термоабляции не находится постоянно внутри упомянутой эталонной среды, как, например, при использовании высокоинтенсивного сфокусированного ультразвука (HIFU) в качества способа абляции, или b) гомогенной за исключением оборудования, если оборудование находится постоянно внутри упомянутой эталонной среды.
В другом аспекте сдвиговые волны, которые распространяются в среде, отслеживаются опрашиванием среды. От отслеживаемых местоположений на противоположных сторонах границы подвергаемой абляции ткани измеряются задержки сдвиговой волны в среде и другой сдвиговой волны. Две сдвиговые волны образуются в результате подачи соответственно разных вталкивающих импульсов, которые испускаются раздельно. Процессор решает, основываясь на функции двух задержек, что граница пересекается между двумя этими местоположениями. Еще в одном аспекте среда опрашивается динамически. Карта пространственного распределения эластичности генерируется динамически. Разность между этой картой и предварительно сформированной картой пространственного распределения эластичности в среде генерируется динамически, чтобы тем самым динамически формировать разностную карту эластичности, которая имеет, в качестве вводимого значения, разность в задержке от одного пространственного положения до другого пространственного положения. Разностная карта и/или карта, выведенная из нее, динамически визуализируется, и/или из разностной карты динамически определяется граница подвергаемой абляции ткани.
Эти аспекты эффективно реализуются в форме машины, способа и программного обеспечения.
Подробности этих аспектов излагаются ниже со ссылкой на прилагаемые чертежи, которые выполнены не в масштабе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ. 1 - иллюстративная схема системы и иллюстративная концептуальная схема согласно настоящему изобретению;
ФИГ. 2 - иллюстративная блок-схема и концептуальная схема проводимой на стороне калибровки карты пространственного распределения эластичности согласно настоящему изобретению;
ФИГ. 3 - иллюстративная блок-схема и концептуальная схема проводимой как на стороне, так и на месте калибровки карты пространственного распределения эластичности, включающей в себя представление и интеграцию разностных карт, согласно настоящему изобретению;
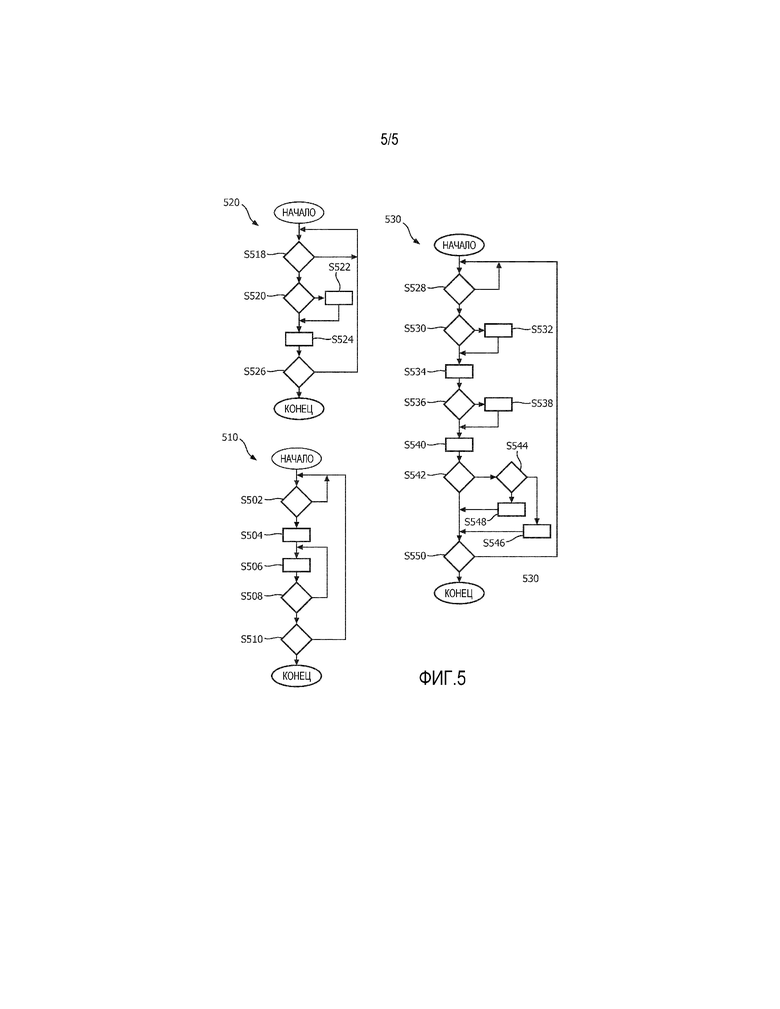
ФИГ. 4 и 5 - иллюстративная блок-схема последовательности операций в реализации и работе системы согласно настоящему изобретению.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
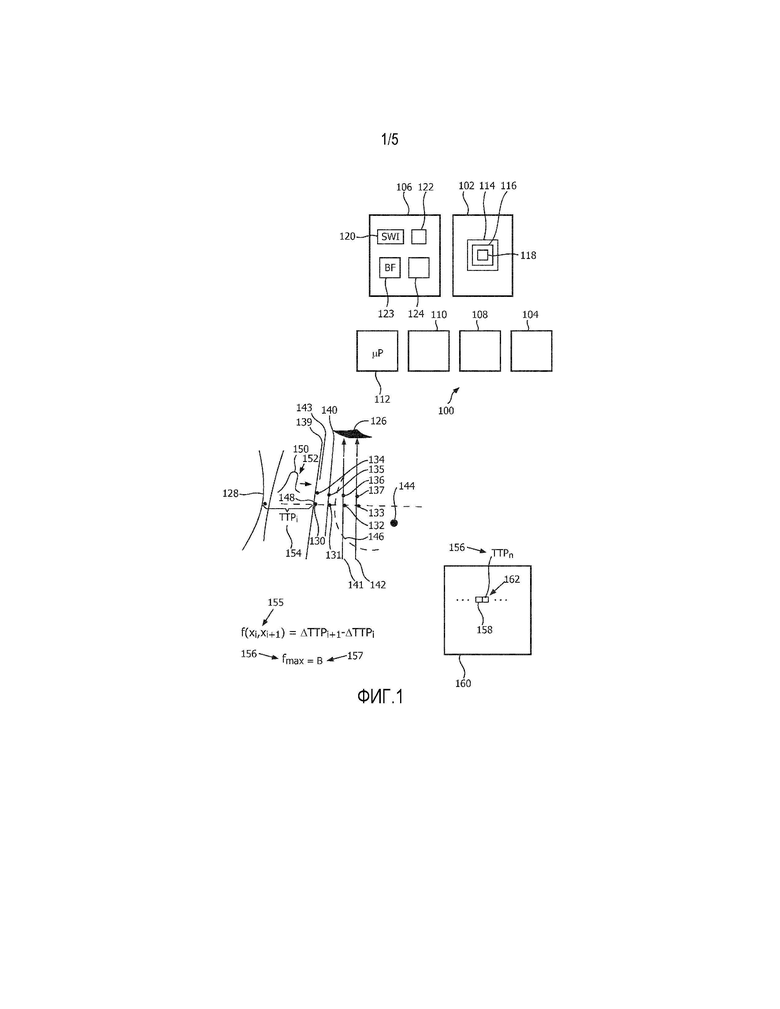
На фиг. 1 представлен, в качестве иллюстративного и не ограничивающего примера, эластографический аппарат 100 для мониторинга термоабляции в режиме реального времени. Аппарат 100 включает в себя абляционное устройство 102, источник 104 энергии, устройство 106 формирования изображений, дисплей 108, пользовательские элементы 110 управления и микропроцессор 112 или другой процессор, такой как вычислительное устройство эластографии сдвиговой волны. Функция микропроцессора реализуется в одной или более интегральных схемах. Однако она может быть реализована любым сочетанием программного обеспечения, встроенных программ и аппаратного оборудования.
Абляционное устройство 102 включает в себя, как тип абляционного оборудования, абляционную иглу 114. Последняя из упомянутых включает в себя радиочастотный (RF) электрод 116, который включает в себя один или более зубцов 118, выдвигающихся в ткань тела с целью подачи тепла для абляции. Источник 104 энергии, такой как сеть электрического тока, обеспечивает энергию для нагревания. Абляционная игла 114 вместо этого может быть иглой для криогенной или микроволновой абляции с соответственно измененной конструкцией. По желанию абляция может выполняться высокоинтенсивным сфокусированным ультразвуком (HIFU), и в этом случае обеспечивается HIFU преобразователь вместо абляционной иглы.
Устройство 106 формирования изображений включает в себя SWI модуль 120, ультразвуковой модуль 122 формирования изображений в B-режиме и формирователь 123 луча. Изображения в B-режиме могут повторяемо приобретаться для пространственной регистрации показателей эластичности на разных этапах процесса абляции. Хотя необходимость в такой регистрации ослабляется в варианте осуществления калибровки карты пространственного распределения эластичности на стороне, обсуждаемом ниже со ссылкой на фиг. 2. Изображение в B-режиме может также служить как лежащее в основе представлений, на которых могут быть нанесены цветокодированные или кодированные другим образом карты пространственного распределения эластичности (которые далее могут именоваться просто ʺкартами эластичностиʺ).
Устройство 106 формирования изображений дополнительно включает в себя один или более ультразвуковых преобразователей 124. Каждый преобразователь может быть реализован решеткой преобразователей, то есть решеткой преобразующих элементов. Хотя то, что предлагается здесь, не ограничивается отдельными преобразователями для вталкивающих импульсов и формирования изображений, отдельные преобразователи для этих двух функций позволяют отслеживать результаты вталкивании сразу же после вталкивания, обеспечивая тем самым более точные результаты.
Зонд 126 может включать в себя преобразователи 124 формирования изображений для вталкивания и отслеживания. По желанию он может также включать в себя преобразователь для HIFU терапии, который может быть размещен в отдельном зонде. Для создания сдвиговой волны вталкивающий преобразователь приводится в действие для испускания акустического лучевого вталкивающего импульса 128. Импульс фокусируется до желательной глубины построения изображения с помощью сдвиговых волн, то есть до глубины вталкивания. Вталкивание создает сдвиговую волну, которая распространяется волюметрически во всех направлениях, хотя фокус может быть выполнен с возможностью быть малым и узким, чтобы обеспечивать отслеживание на многих глубинах визуализации. Когда сдвиговая волна распространяется через ткань тела, она смещает ткань тела в поперечном направлении по отношению к направлению распространения. Это смещение может быть обнаружено в заданном отслеживаемом положении 130-137 посредством импульса 139-142 слежения, направленного в это положение. Например, импульс 139 слежения, направленный в положения 130, 134, позволяет возвратить эхо-сигналы, подлежащие измерению в соответствии с A-линией 143. Это производится повторяемо для отслеживания перемещения ткани вдоль A-линии 143. Когда пик сдвиговой волны в течение распространения сдвиговой волны прибывает на A-линию 143, обнаруживается максимальное смещение обоих положений 130, 134, соответственно, согласно кросс-корреляции A-линий 143, приобретенной из того же направления. Время между вталкиванием и соответствующим прибытием пика в контролируемое положение 130 известно как время до достижения пикового значения (TTP). Может осуществляться мониторинг отслеживаемых положений 130-137 на многих глубинах визуализации вдоль текущей плоскости визуализации. Посредством этого мониторинга можно измерить TTP для соответствующих положений 130-137. Расстояния распространения до отслеживаемых положений известны. Поскольку расстояние, деленное на время, определяет скорость, скорость распространения сдвиговой волны может быть определена по отношению к находящемуся под мониторингом положению 130. Это делается совместно для различных других таких положений в плоскости визуализации. Таким образом, могут быть вычислены разности скоростей между положениями для определения локальной скорости; однако вместо этого в соответствии с тем, что предлагается здесь, вычисляются разности во времени распространения. Кроме того, согласно данному способу, сравнения производятся не только от положения к положению, но и с эталонной картой. Обычно должно быт намного больше положений 130-137 и A-линий 143, чем показано на фиг. 1. По желанию может осуществляться мониторинг нескольких плоскостей визуализации, например, взаимно параллельных, для динамического построения трехмерных (3D) изображений. Скорость сдвиговой волны относится к модулю упругости, который является показателем эластичности ткани. Согласно тому, что предлагается здесь, разности во времени распространения вычисляются и используются в качестве индикаторов эластичности ткани в системе отслеживаемых положений известной геометрии. Например, отслеживаемые положения 130-137 могут быть расположены в эквидистантной решетке.
В радиочастотной абляции (RFA) зубец 144 или несколько зубцов размещаются внутри опухоли, например.
Тепло, создаваемое в зубце 144, осуществляет абляцию ткани, создавая тем самым границу 146 подвергшейся абляции ткани.
Кровеносный сосуд или другая защищенная структура 148, которая должна быть защищена от воздействия тепловых эффектов абляции, может находиться вблизи границы 146 подвергающейся абляции ткани. Соответственно во время абляции может осуществляться динамический мониторинг участка границы 146, расположенного у защищенной структуры 148. Способ оценки в реальном времени расширения абляции во время лечебной процедуры позволяет практикующему врачу адаптировать лечение, для того чтобы компенсировать нежелательные отклонения развивающейся границы 146 от первоначально запланированной протяженности. Это уменьшает вероятность рецидива опухоли вследствие не доведенного до конца лечения, а также вероятность нежелательного повреждения здоровой ткани.
Основываясь на мониторинге пары положений 131, 132 на противоположных сторонах границы 146, микропроцессор 112 может принять решение, что граница пресекается между двумя этими положениями.
В соответствии с продуманным, приводимым в качестве примера способом, предложенным здесь, обнаружение основывается на мониторинге многих положений на данной глубине визуализации и на сравнении с эталонными значениями. Положения на данной глубине визуализации рассматриваются попарно, два положения являются соседними. Эталонное отслеживание для каждого из двух этих положений может происходить на ранней стадии абляции, такой как пред-абляция, или может выполняться на стороне, например, на имитирующем ткани фантоме. Эталонное отслеживание, подобно текущему отслеживанию, обеспечивает измерение интервала времени между вталкиванием 128 и прибытием пика 150 сдвиговой волны 152 в первом положении 131 из пары. Этот интервал времени известен как время до достижения пикового значения (TTP) 154. Используются и другие, альтернативные значения задержки, такие как крутизна нарастания времени до достижения пикового значения (TTPS) и центр масс (COM). Значение эталонного отслеживания минус значение текущего отслеживания обозначается здесь как ΔTPi. Для следующего из пары положения 132 значение эталонного отслеживания минус значение текущего отслеживания обозначается здесь как ΔTPi+1. Если граница 146 пересекается между двумя положениями i и i+1, здесь 131 и 132, ожидается, что значение функции 155 будет положительным. Это функция f(xi, xi+1)=ΔTPi - ΔTPi+1. Кроме того, максимальное значение, или ʺмаксимум функцииʺ, 156, для всех f(xi, xi+1) на текущей глубине визуализации обозначатся на фиг. 1 как fmax. Если fmax положительно, оно пространственно соответствует положению, через которое проходит граница 146. Это представлено на фиг. 1 меткой ʺBʺ для границы 146. Микропроцессор 112 может принимать это решение, основываясь на том, положительно ли fmax. Эти положения могут быть найдены на многих глубинах визуализации, чтобы пространственно определить границу 146.
Вводимые значения 158 карты 160 эластичности являются, от положения к положению, значениями 162 задержки, такими как TTP 154. Для плоскости визуализации карта 160 является двумерной. Однако карта 160 может быть трехмерно для 3D мониторинга границы 146. Эталонная карта эластичности может быть сформирована до абляции из мониторинга среды абляции или может быть сформирована из проводимого на стороне мониторинга другой среды, которая имитирует среду абляции. Предварительная карта эластичности формируется из текущего мониторинга подвергаемой абляции среды. Эталонная и предварительная карты являются подобными наборами значений 162 задержки.
Разностная карта, или ʺD-караʺ, может быть сформирована как разность между эталонной и предварительной картами, например, эталонная карта минус предварительная карта. Вводимыми значениями D-карты являются, таким образом, ΔTPi, ΔTPi+1, и т.д.
Смещая или сдвигая D-карту на одно положение отслеживания и вычисляя разность между D-картой и сдвинутой D-картой, можно вывести карту со сдвигом положения, или ʺD2ʺ карту, с тем чтобы максимальные значения D2-карты, когда они положительны, пространственно определяли участок границы 146. D2-карта может быть цветокодированной, чтобы повысить видимость границы, когда карта воспроизводится на дисплее или распечатывается. Таким образом, полная длина границы 146 в изображении может определяться динамически, как только начинается процесс абляции, посредством последовательного мониторинга. Альтернативно частота кадров может быть увеличена локальным ограничением мониторинга просто до участка границы 146 вблизи защищенной структуры 148. В случае калибровки на месте, то есть мониторинга одного и того же физического положения в разные моменты времени или на разных этапах, используется визуализация в B-режиме, чтобы пространственно регистрировать карты эластичности компонентов в D-карте. Ряд 2D изображений в B-режиме (или 3D изображение) до абляции будет получен с указанием ориентиров (а именно, зубца 144). Изображение (изображения) в B-режиме, взятое во время или после абляции, будет сравниваться (например, через кросс-корреляцию) с изображениями до абляции для лучшего согласования RF данных в ближнем поле (снаружи зоны интенсивного нагревания). Изображения в B-режиме могут быть либо просто сформированы из следящих лучей, либо добавлены как фоновые изображения для изображений эластичности. С другой стороны, калибровка на стороне, то есть использование имитирующего ткани фантома, позволяет осуществлять мониторинг без использования визуализации в B-режиме для пространственной регистрации разных карт эластичности по отношению друг к другу. Изобретатели обнаружили, что в случае мониторинга на месте D-карта, даже без дополнительного этапа основанной на B-режиме регистрации, обычно устойчива к небольшим пространственным расхождениям двух составляющих карт.
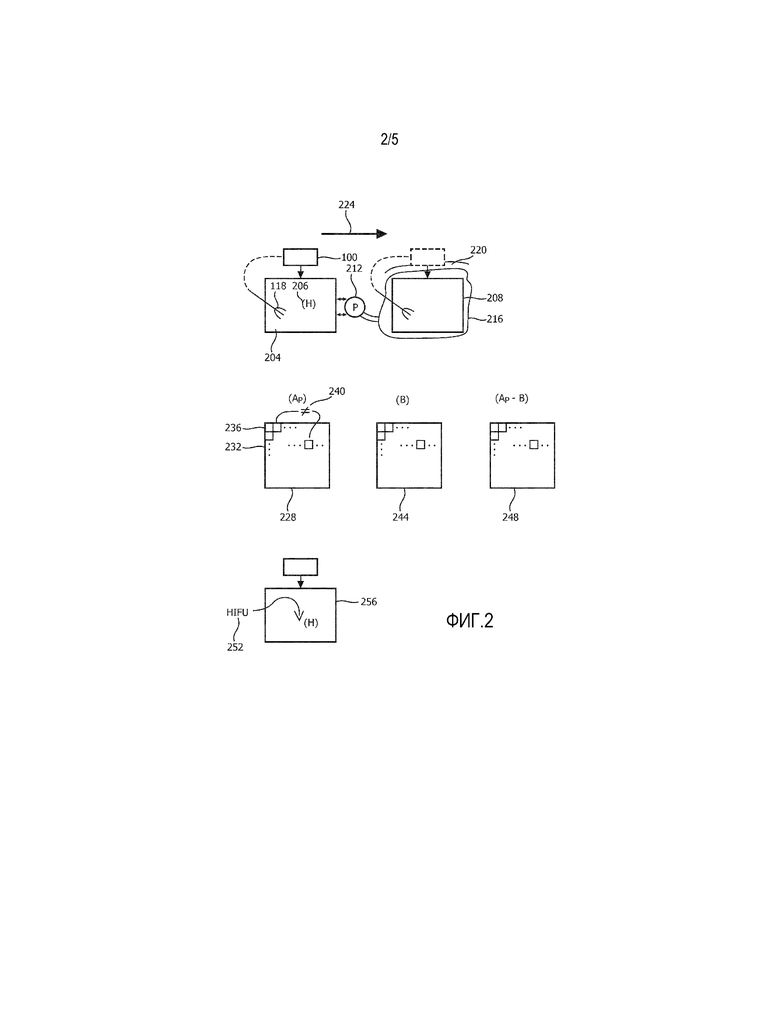
Проводимая на стороне калибровка карты эластичности использует, как показано в примере на фиг. 2, имитирующий ткани фантом 204. Материал, из которого состоит фантом 204, образован как гомогенный, что представлено на фиг. 2 (ʺHʺ) знаком 206. Свойства фантома подобраны таким образом, чтобы быть подобными свойствам здоровых тканей целевого органа. Эластографический аппарат 100, за исключением абляционного устройства 102, применяет такие же последовательности вталкивания и отслеживания на фантоме 204, которые должны быть применимы к целевой среде (MOI) 208 в клинической процедуре, которой надо следовать.
Таким образом, фантом 204 способен имитировать формирование изображений, которое должно выполняться при использовании MOI 208.
Сравнивая результаты от мониторинга фантома 204 с результатами от мониторинга MOI 208, эффекты ультразвукового поля (ʺUFEʺ) от мониторинга могут быть устранены. Вталкивающий луч узок в его фокусе, но расширяется постепенно в направлении ближнего поля и в направлении дальнего поля. Идеально сдвиговая волна должна иметь форму, подобную выгнутой наружу цилиндрической волне, с тем чтобы сдвиговая волна прибывала одновременно во все отслеживаемые положения на разных глубинах вдоль каждого направления отслеживания (параллельного направлению вталкивания). Поскольку ультразвуковой луч не имеет идеальной формы, подобной ʺузкомуʺ цилиндру, эффект несовершенного источника сдвиговой волны, то есть вталкивающего луча, требует коррекции или компенсации. Этот искажающий эффект является основной частью UFE, которая устраняется.
Чтобы дополнительно устранить искажение в эффектах сдвиговой волны, которое вызывается присутствием жесткого медицинского инструмента, фантом 204 может быт снабжен одним или более зубцами 118, располагаемыми и развертываемыми как и в плане клинической обработки. Фантом 204 сформирован с той же паренхимой 212, что и у телесного органа 216, в котором располагается MOI 208. Для RFA телесным органом часто является печень или другой орган внутри телесной ткани 220. Стрелка 224 и пунктирный контур над MOI 208 представляют временной порядок, в котором сначала осуществляется мониторинг фантома 204, для того чтобы собрать информацию, которая должна быть позже использована в динамическом мониторинге во время процедуры клинической абляции.
Сформирована изображенная ниже фантома 204 на фиг. 2 соответствующая карта 228 эластичности, то есть эталонная карта эластичности. Она обозначена как (Ap), где ʺPʺ означает фантом. Эталонная карта 228 эластичности определяет набор 232 значений 236 эластичности, которые являются задержками 162 распространения сдвиговой волны, как обсуждалось здесь выше, за исключением того, что они были выведены из мониторинга ʺна сторонеʺ, то есть на фантоме 204. Значения эластичности отличаются 240, как показано знаком неравенства, вследствие эффектов, которые устраняются достоинством основанной на фантоме калибровки клинического мониторинга.
Сформирована изображенная ниже MOI 208 на фиг. 2 соответствующая карта 228 эластичности, то есть предварительная карта 244 эластичности.
Калиброванная карта 248 эластичности является D-картой, вычисленной из эталонной и предварительной карт 228, 244
Заметим, что вместо RFA способом абляции может быть HIFU. Это представлено на фиг. 2 HIFU лучом 252. Никакого оборудования для термоабляции не требуется внутри фантома 256. В этом случае фантом 256 является гомогенным, а не гомогенным за исключением абляционного оборудования, находящегося внутри фантома.
Альтернативно эталонная карта 228 может быть получена хорошо известными способами численного моделирования на модели, которая калибруется по экспериментальным результатам, полученным при использовании фантома. См. патент США 8,118,744, Палмери (Palmery) и др., параграфы до и после Табл. 1, публикацию патента США № 2001/0130660, Клаутер (Clouter) и др., пример 1, и публикацию патента США № 2014/0180091, Мак-Аливей (McAleavey), параграф [0074]. В этом альтернативном случае численного моделирования эталонная среда не является и не расположена в MOI 208.
Что касается эталонной карты в общем случае, получатся ли она на стороне или на месте, она представляет здоровую (не подвергавшуюся абляции) телесную ткань, имеющую малые неоднородности (за пределами жестких опухолей или других жестких структур). Малые неоднородности оказывают относительно малое влияние на изменения во времени распространения сдвиговой волны (по сравнению со значительным влиянием подвергшейся абляции ткани или жесткой опухоли) и, как правило, могут не приниматься во внимание.
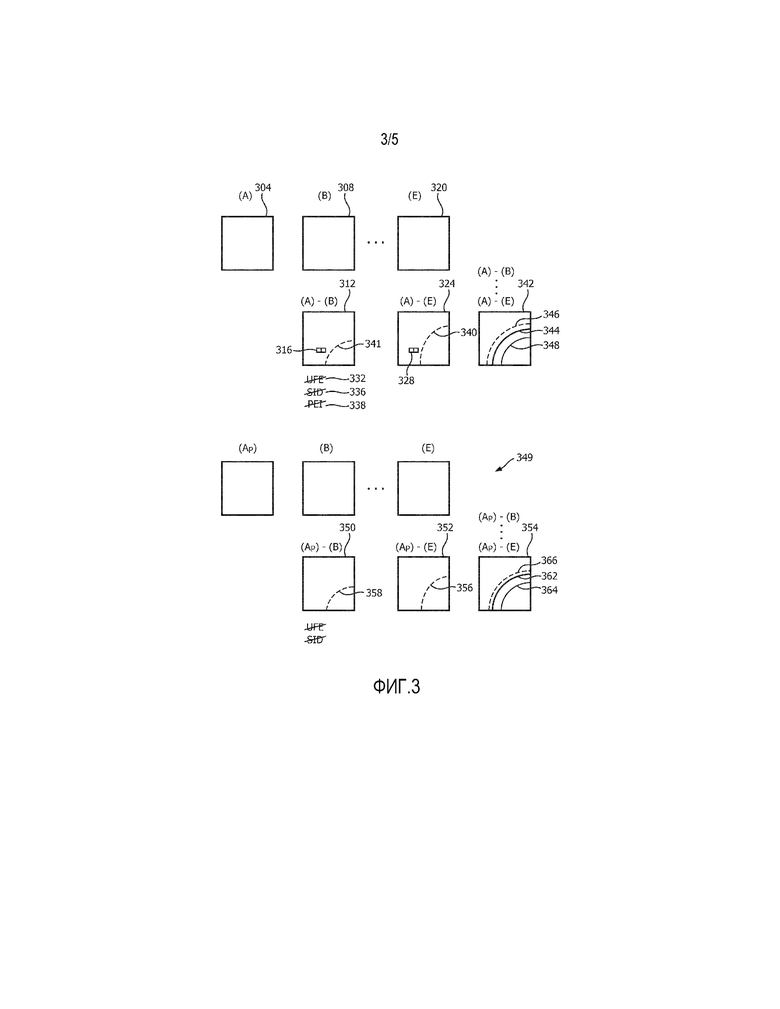
На фиг. 3 представлен пример калибровки карты эластичности и представления карты эластичности пользователю.
По отношению к калибровке на стороне формируется ряд карт эластичности во временной последовательности. Первая карта, которая может предшествовать любому приложению энергии или может предшествовать любой абляции, служит в качестве эталонной карты 304. Из эталонной карты 304 последующая карта 308 эластичности вычитается на более позднем этапе абляции. Это дает в результате первую D-карту, имеющую набор разностей задержек в виде соответствующих показателей 316 эластичности на одном этапе процедуры абляции по отношению к другому этапу этой процедуры. Эталонная карта 304 подобным образом вычитается из предварительной карты 320, представляющей этап, на котором приложение энергии завершается. Вычитание дает в результате вторую D-карту 324, имеющую соответствующий набор показателей 328 эластичности на одном этапе процедуры абляции по отношению к эластичности на другом этапе этой процедуры. В любых таких D-картах 312, 324 или D-картах промежуточных этапов абляции эффект ультразвукового поля (UFE) 332 и искажение 336 от жесткого инструмента (SID) с успехом ослабляются или исключаются вычислением разностей, которое производится, и такое ослабление/исключение представлено на фиг. 3 вычеркиванием. В качестве дополнительного преимущества существовавшие ранее неоднородности (PEI) 338 также ослабляются или исключаются. D-карты 312, 324 используются для динамического воспроизведения на дисплее или распечаток, или же для наложения или расположения вблизи текущего изображения в B-режим при мониторинге абляции. Разделение 340 пунктирной линией во второй D-карте 324 не обязательно присутствует, но представляет, где цветовое кодирование, например, предлагает участок границы 146 подвергшейся абляции ткани. Разделение 341 в полученной ранее карте 312 также показано на фиг. 3.
Альтернативно или дополнительно из одной или более D-карт 312, 324 могут быть сформированы соответствующие D2-карты и представлены пользователю.
Другое улучшение, тепловые эффекты последующего приложения энергии, может быть внесено в D-карты 312, 324 или в D2-карты продолжением отслеживания после абляции. Карта 342, сформированная в некоторый момент времени после отключения источника энергии для абляции, сохраняет разделение 340, как показано сплошной линией 344. Разделение 346 пунктирной линией соответствует предшествующему разделению 340 пунктирной линией, но показывает небольшое расширение в зоне абляции, которое произошло в период подачи энергии от источника после абляции. Другая сплошная линия 348 удерживает прежнее разделение 341 пунктирной линией. Любая из сплошных линий 344, 348 может быть представлена пользователю как графика наложений. Альтернативно интеграция следующих друг за другом карт может быть представлена визуально в виде петли кадров, причем каждый кадр представляет D-карту или D2-карту следующего этапа. Следующие друг за другом карты или сплошные линии 344, 348 могут снабжаться текущим временем абляции или другим индикатором текущего этапа абляции в качестве визуальной помощи практикующему врачу в оценке протяженности границы абляции.
Альтернативно или дополнительно может выполняться автоматическое отслеживание положения границы 340. Практикующий врач может постоянно извещаться звуковыми или выводимыми на экран сообщениями о расстоянии между границей 340 и критичной структурой 148, идентифицированной автоматически или предварительно идентифицированной практикующим врачом, в прерываемой визуализации в B-режиме в реальном времени. Генерация тепла абляционным устройством 102 может автоматически управляться микропроцессором 112, осуществляющим мониторинг абляции, в случае обнаружения близости критичной структуры. Расстояние от границы до критичной структуры может продолжать определяться при последующей генерации тепла, принимая во внимание тепловые эффекты последующего приложения энергии, то есть осуществляться мониторинг продолжающегося расширения границы 140 в течение ограниченного времени.
Для калибровки карты эластичности на стороне применимо аналогичное построение карт. Карты 349 эластичности формируются для разных этапов процедуры абляции. Карты 312, з14, сформированные на месте, соответствуют картам 350, 352, 354, сформированным на стороне. Разделения 340, 341, 346, полученные на месте, соответствуют разделениям 36, 358, 366, полученным на стороне. Сплошные линии 344, 348, полученные на месте, соответствуют сплошным линиям 362, 364, полученным на стороне.
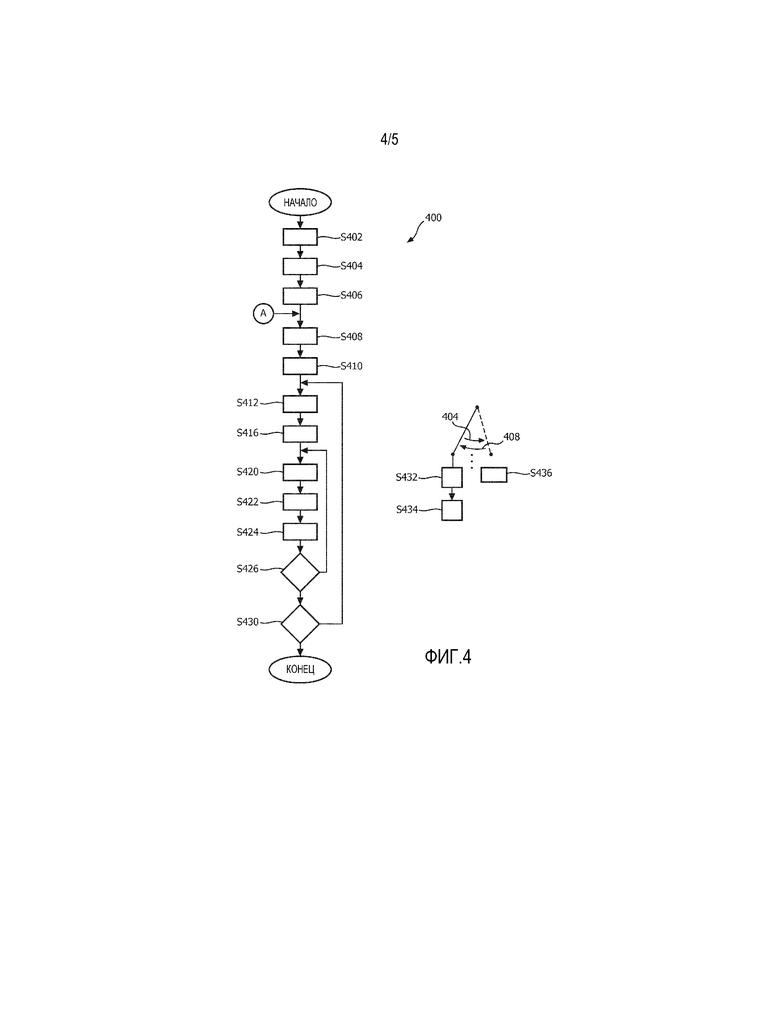
В рабочем порядке, по отношению к калибровке на стороне, выбирается телесный орган 216, подлежащий абляции (основная программа 400, этап S402). Создается гомогенный, имитирующий ткань фантом 204, который моделирует паренхиму 212 выбранного органа 216 (этап S404). Примером материала для фантома, используемого для моделирования ткани печени в ультразвуковой визуализации, является ZERDINE™ от COMPUTER IMAGING REFERENCE SYSTEMS, INC. Это твердый эластичный имитирующий ткани материал применительно к скорости звука и коэффициенту затухания. См. http://www.cirsinc.com/products/new/78/ultrasound-prostate- training-phantom/?details=specs; см. также патентную публикацию США № 2005/0054930, Рикетс (Rickets) и др., фиг. 6(a)-6(c): соноэластографические изображения с использованием фантома печени; см. также патент США № 7,462,488, Мадсен (Madsen) и др., озаглавленный ʺИмитирующие ткани фантомы для эластографииʺ, которые включены сюда полностью путем ссылки. После этих подготовительных этапов, или в качестве точки ввода, обозначенной как ʺAʺ на фиг. 4, применительно к калибровке на месте, абляционная игла 114 вводится в фантом 204 до глубины клинической обработки (этап S408). Здесь предполагается, что клинической процедурой будет RFA и что будет использована абляционная игла. Развертываются зубцы 118 (этап S410). Функция передачи в формирователе луча фокусируется на целевом положении вталкивания (этап S412). Подается вталкивающий импульс 128, чтобы создать сдвиговую волну (этап S416). Формирование луча для передачи и приема через формирователь луча регулируется для приобретения текущей A-линии 143 (этап S420). Испускается следящий импульс 136, 138 (этап S422). A-линия 143 приобретена (этап S424). Если должна быть приобретена (этап S426) другая A-линии 143, осуществляется возврат к этапу S420 приобретения A-линии. В противном случае, если не требуется приобретать (этап S426) другую A-линию 143, но должен быть излучен (этап S 430) другой вталкивающий импульс 128, осуществляется возврат к этапу S412 фокусировки вталкивания. В противном случае, если не требуется излучать (этап S430) дополнительный вталкивающий импульс 128, мониторинг завершается. В этом примере представлено последовательное формирование луч, хотя вместо этого отслеживание может происходить параллельно с использованием многоканального формирователя луча. Как было сказано выше, последовательное формирование луча в режиме приема и разреженный параллелизм более экономичных ультразвуковых систем возможны в виду вышеупомянутых показателей эффективности, которые представлены здесь выше.
Применительно к режиму или реализации работы на месте обработка чередуется, как представлено противоположно направленными стрелками 404, 408 на фиг. 4, между вталкиванием на этапе s432 и приобретением изображения в B-режиме на этап S436.
Одновременно с основной программой 400 и в соответствии с программой формирования карты эластичности, представленной на фиг. 5, когда становятся доступными данные отслеживания (этап S502), обработка нацеливается на первое отслеживаемое положение (этап S504). TTP вычисляется или извлекается из памяти (этап S506). Если имеется следующее отслеживаемое положение для обработки с целью формирования текущей предварительной карты эластичности (этап S508), осуществляется возврат к этапу S506 вычисления/извлечения. В противном случае, если отсутствует дополнительное отслеживаемое положение для формирования текущей предварительной карты эластичности (этап S508) и если мониторинг абляции должен продолжаться (этап S510), осуществляется возврат к этапу S502.
Также одновременно с основной программой 400 выполняется программа 520 формирования D-карты. Когда предварительная карта 244, 308, 320 эластичности и ее соответствующая эталонная карта 228,304 эластичности становятся доступными (этап S518), продолжение процесса зависит от того, является ли режим или реализация выполняемыми на стороне (этап S520). Если на стороне (этап S520), соответствующие изображения в B-режиме, сформированные из данных отслеживания, на которых основываются эталонная и предварительная карты, кросс-коррелированы для лучшего согласования в ближнем поле, с тем чтобы пространственно совместно регистрировать эталонную и предварительную карты (этап S522). Предварительная карта 244, 308, 320 вычитается из эталонной карты 228, 304, чтобы сформировать D-карту (этап S524). Максимальное положительное значение на каждой глубине, то есть в ряду, отслеживания D-карты может быт промаркировано для проводимой по желанию обработки или другого различения в динамическом представлении. Если мониторинг абляции должен продолжаться (этап S526), осуществляется возврат к проверке наличия карты на этапе S518.
Программа 530 представления карт также прогонятся одновременно. Когда D-карта становится доступной (этап S528), продолжение процесса зависит от того, должна ли D2-карта формироваться из нее (этап S530). Если D2-карта должна формироваться (этап S530), выводится D2-карта (этап S532). В любом случае граница 146 подвергшейся абляции ткани пространственно определяется (этап S534). Если близость находится ниже заданного порогового значения (этап S536), пользователь получает извещение (этап S538). В любом случае D-карта или D2-карта воспроизводится на дисплее или распечатывается вместе с другими выбираемыми по желанию важными признаками или отличительными особенностям текущей границы 146 подвергшейся абляции ткани (этап S540). Если должна быть представлена серия из одной или более карт, полученных на предшествующих по времени этапах (этап S542), продолжение процесса зависит от того, должен ли этап (этапы) быть представлен как графическое наложение на экране (этап S544). Если этап (этапы) должен быть представлен как графическое наложение на экране (этап S544), наложение (наложения) посылается на экран (этап S546). В противном случае, если этап (этапы) не должен быть представлен как графическое наложение на экране (этап S544), петля D-карт/D2-карт с предшествующих этапов представляется на экране (этап S548). Если на экран должна быть выведена смещенная D-карта, то D-карта, только что ставшая доступной, смещается в боковом направлении на одну A-линию, берется разность между этой D-картой и ее смещениями, и визуально представляется результирующая, или ʺD2ʺ, карта. Если полученные на предшествующем по времени этапе карты не должны быть представлены (этап S542), или по окончанию любо из этапов S546 или S548, продолжение процесса зависит от того, завершено ли отслеживание абляции (этап S550). Если отслеживание абляции не завершено (этап S550), процесс возвращается к этапу S528.
Целевая среда опрашивается в соответствии с ультразвуковой эластографической визуализацией. Формируется предварительная карта пространственного распределения эластичности. Эта карта калибруется по эталонной карте пространственного распределения эластичности, которая содержит набор разных значений эластичности. Эталонная карта выполняется с возможностью отображения изображений эталонной среды, полученных с помощью ультразвуковых сдвиговых волн. Эталонная среда не является и не располагается в целевой среде, и может быть гомогенной. Сдвиговые волны, которые распространяются в среде, отслеживаются опрашиванием среды. Из отслеживания положений на противоположных сторонах границы подвергшейся абляции ткани измеряются задержки распространения сдвиговой воны в среде и другой сдвиговой волны. Две сдвиговые волны образуются в результате соответственно разных вталкиваний, которые производятся раздельно. Процессор решает, основываясь на функции двух задержек, что граница пересекается между двумя этими положениями. Калиброванная карта динамически обновляется и может включать в себя расширение границы после абляции и предшествующие этапы с временными метками.
Хотя изобретение было представлено и описано подробно на чертежах и в приведенном выше описании, такое представление и описание должно рассматриваться как иллюстративное, пояснительное и не ограничивающее, это изобретение не ограничивается раскрытыми вариантами осуществления.
Например, мониторинг в режиме реального времени, например, малой, глубокой зоны абляции может влечь за собой мониторинг всей двух- или трехмерной границы, а не просто участка, близкого к защищенной структуре.
Другие варианты помимо представленных вариантов осуществления могут быть поняты и реализованы специалистами в данной области техники при практическом осуществлении заявленного изобретения на основе изучения чертежей, описания и прилагаемой формулы изобретения. В формуле изобретения слово ʺсодержитʺ не исключает других элементов или этапов, а артикль единственного числа (ʺaʺ или ʺanʺʺ в оригинале) не исключает множественности. Слово ʺиллюстративноеʺ, используемое здесь, означает ʺслужащее в качестве примера, образца или иллюстрацииʺ. Вариант осуществления, описанный как ʺиллюстративныйʺ, не обязательно должен быть истолкован как предпочтительный или имеющий преимущество перед другими вариантами осуществления, и/или исключающий введение признаков от других вариантов осуществления. Любые ссылочные позиции в формуле изобретения не должны пониматься как ограничивающие объем.
Компьютерная программа может запоминаться кратковременно, временно или на более долгий период времени на подходящем машиночитаемом носителе, таком как оптическое средство хранения информации или твердотельный носитель информации. Такие носители является непреходящими только в том смысле, что они не являются преходящим, распространяющими сигнал, но включают в себя другие формы машиночитаемых носителей, такие как регистровая память, кэш процессора и RAM.
Один процессор или другое устройство может выполнять функции нескольких устройств, перечисленных в формуле изобретения. Простой факт, что определенные показатели упомянуты во взаимно отличающихся зависимых пунктах формулы изобретения не означает, что сочетание этих показателей не может быть успешно использовано.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА И СПОСОБ АДАПТИВНОЙ АБЛЯЦИИ И ТЕРАПИИ НА ОСНОВАНИИ ЭЛАСТОГРАФИЧЕСКОГО МОНИТОРИНГА | 2016 |
|
RU2707037C2 |
| СПОСОБ И СИСТЕМА ДЛЯ УЛЬТРАЗВУКОВОЙ ТЕРАПИИ | 2009 |
|
RU2519378C2 |
| СИСТЕМА И СПОСОБ ЭЛАСТОГРАФИЧЕСКИХ ИЗМЕРЕНИЙ | 2014 |
|
RU2667617C2 |
| СИСТЕМА И СПОСОБ КАРТОГРАФИРОВАНИЯ ДЛЯ МЕДИЦИНСКИХ ПРОЦЕДУР | 2011 |
|
RU2577760C2 |
| НАВОДИМАЯ ПО АВТОКОРРЕЛЯЦИИ ВЗАИМНАЯ КОРРЕЛЯЦИЯ В УЛЬТРАЗВУКОВОЙ ЭЛАСТОГРАФИИ СДВИГОВОЙ ВОЛНЫ | 2015 |
|
RU2689174C2 |
| ЭНЕРГОПОДАЮЩЕЕ УСТРОЙСТВО ДЛЯ ПОДАЧИ ЭНЕРГИИ К ОБЪЕКТУ | 2011 |
|
RU2572748C2 |
| УСТРОЙСТВО И СПОСОБ КОНТРОЛЯ КАЧЕСТВА ПРИ ПЛАНИРОВАНИИ ЛУЧЕВОЙ ТЕРАПИИ НА ОСНОВЕ МАГНИТНОГО РЕЗОНАНСА | 2013 |
|
RU2637289C2 |
| УСТРОЙСТВО ВИЗУАЛИЗАЦИИ | 2010 |
|
RU2540090C2 |
| МУЛЬТИФОКУСНЫЕ СОНИКАЦИИ ДЛЯ ГИПЕРТЕРМИЧЕСКИХ ЛЕЧЕБНЫХ ВОЗДЕЙСТВИЙ С ИСПОЛЬЗОВАНИЕМ УЛЬТРАЗВУКА, СФОКУСИРОВАННОГО ПОД КОНТРОЛЕМ МАГНИТНО-РЕЗОНАНСНОЙ ТОМОГРАФИИ | 2013 |
|
RU2650598C2 |
| УСТРОЙСТВО УПРАВЛЕНИЯ АБЛЯЦИЕЙ ДЛЯ МОНИТОРИНГА В РЕАЛЬНОМ ВРЕМЕНИ СМЕЩЕНИЯ ТКАНИ В ОТВЕТ НА ПРИЛОЖЕННУЮ СИЛУ | 2009 |
|
RU2532958C2 |
Группа изобретений относится к медицинской технике, а именно к использованию визуализации для пространственного отображения эластичности. Ультразвуковое эластографическое устройство визуализации содержит ультразвуковой сканер и процессор эластографии сдвиговой волны, выполненный с возможностью управления работой ультразвукового сканера для опрашивания целевой среды и формирования предварительной карты пространственного распределения эластичности, основанной по меньшей мере частично на результате опрашивания, причем процессор эластографии сдвиговой волны дополнительно выполнен с возможностью определения калиброванной карты пространственного распределения эластичности посредством калибровки предварительной карты пространственного распределения эластичности по эталонной карте пространственного распределения эластичности, содержащей набор разных значений эластичности, соответствующих эталонной среде, которая не является упомянутой целевой средой и не располагается в ней. Аппарат для визуализации абляции ткани, подсоединенный к ультразвуковому эластографическому устройству визуализации, содержит устройство визуализации абляции и процессор визуализации абляции, выполненный с возможностью, в ответ на команды от аппарата визуализации, осуществления управления работой упомянутого устройства визуализации абляции для опрашивания упомянутой целевой среды, измерения, от отслеживаемых положений на противоположных сторонах границы подвергшейся абляции ткани, задержки распространения первой сдвиговой волны в целевой среде и второй сдвиговой волны, образующихся в результате соответствующих разных вталкиваний, которые производятся раздельно, и принятия решения, основываясь на функции задержки распространения первой сдвиговой волны и задержки распространения второй сдвиговой волны, о том, пересекается ли упомянутая граница между двумя этими положениями. Использование изобретений позволяет минимизировать искажения в измерении сдвиговой волны, вызванные присутствием жестких инструментов. 2 н. и 12 з.п. ф-лы, 5 ил.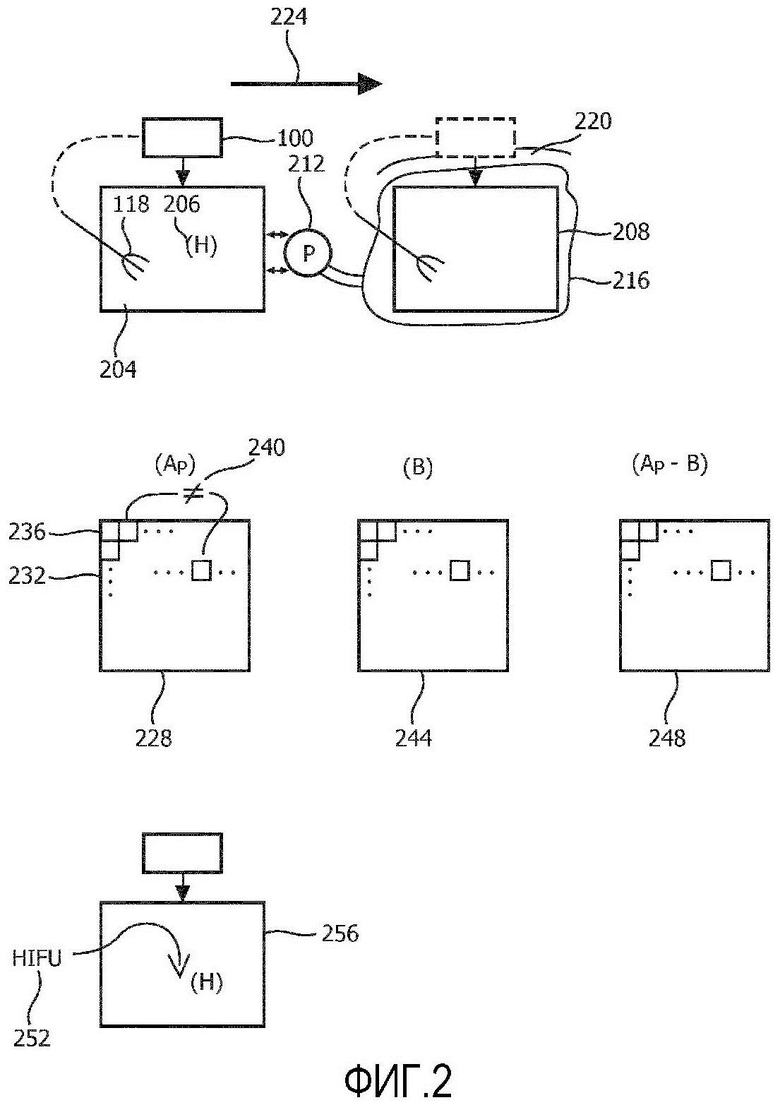
1. Ультразвуковое эластографическое устройство (100) визуализации, которое содержит:
ультразвуковой сканер (106) и
процессор (112) эластографии сдвиговой волны, выполненный с возможностью управления работой упомянутого ультразвукового сканера (106) для опрашивания целевой среды (208) и формирования предварительной карты (244, 308, 320) пространственного распределения эластичности, основанной по меньшей мере частично на результате опрашивания, причем процессор эластографии сдвиговой волны дополнительно выполнен с возможностью определения калиброванной карты (248) пространственного распределения эластичности посредством калибровки предварительной карты (244, 308, 320) пространственного распределения эластичности по эталонной карте (228, 304) пространственного распределения эластичности, содержащей набор разных значений (236) эластичности, соответствующих эталонной среде, которая не является упомянутой целевой средой (208) и не располагается в ней.
2. Устройство по п. 1, в котором упомянутая эталонная среда содержит имитирующий ткани фантом (204), выполненный с возможностью моделирования паренхимы (212) конкретного телесного органа.
3. Устройство по п. 1, в котором упомянутая эталонная среда является либо a) гомогенной (206), если оборудование для термоабляции не находится внутри упомянутой эталонной среды; либо b) гомогенной за исключением упомянутого оборудования, если упомянутое оборудование находится внутри упомянутой эталонной среды.
4. Устройство по п. 3, в котором упомянутое оборудование, находящееся внутри упомянутой эталонной среды, выполнено с возможностью моделирования присутствия упомянутого оборудования внутри упомянутой целевой среды (208).
5. Устройство по п. 1, в котором процессор (112) эластографии сдвиговой волны выполнен с возможностью калибровки за счет использования разности между упомянутой эталонной картой (228, 304) пространственного распределения эластичности и упомянутой предварительной картой (244, 308, 320) пространственного распределения эластичности для формирования калиброванной карты (248) пространственного распределения эластичности.
6. Устройство по п. 1, в котором упомянутые разностные значения (236) эластичности содержат значения задержки распространения сдвиговой волны.
7. Устройство по п. 6, в котором упомянутые значения задержки распространения сдвиговой волны содержат соответствующие периоды (154) времени в распространении сдвиговой волны к соответствующим положениям (130-137) в упомянутой эталонной среде.
8. Устройство по п. 6, в котором упомянутая предварительная карта (244, 308, 320) пространственного распределения эластичности содержит значения задержки распространения сдвиговой волны.
9. Устройство по п. 1, в котором процессор (112) эластографии сдвиговой волны дополнительно выполнен с возможностью сравнения упомянутой предварительной карты (244, 308, 320) пространственного распределения эластичности и упомянутой эталонной карты (228, 304) пространственного распределения эластичности для формирования разностной карты за счет использования разности между упомянутой эталонной картой (228, 304) пространственного распределения эластичности и упомянутой предварительной картой (244, 308, 320) пространственного распределения эластичности и динамического генерирования изображений для воспроизведения на дисплее упомянутой разностной карты, карты, выведенной (этап S532) из упомянутой разностной карты, или их сочетания.
10. Устройство по п. 9, в котором процессор эластографии сдвиговой волны дополнительно выполнен с возможностью генерирования временных рядов, содержащих карты из числа упомянутой разностной карты и/или упомянутой карты, выведенной (этап S532) из упомянутой разностной карты, для отображения абляции на разных временных этапах.
11. Аппарат для визуализации абляции ткани, подсоединенный к ультразвуковому эластографическому устройству (100) визуализации по п. 1 и содержащий:
устройство визуализации абляции, выполненное с возможностью отслеживания сдвиговых волн, которые распространяются в целевой среде (208); и
процессор визуализации абляции, выполненный с возможностью, в ответ на команды от упомянутого аппарата визуализации, осуществления:
управления работой упомянутого устройства визуализации абляции для опрашивания упомянутой целевой среды (208);
измерения, от отслеживаемых положений на противоположных сторонах границы (146) подвергшейся абляции ткани, задержки распространения первой сдвиговой волны в упомянутой целевой среде (208) и второй сдвиговой волны, образующихся в результате соответствующих разных вталкиваний, которые производятся раздельно; и
принятия решения, основываясь на функции задержки распространения первой сдвиговой волны и задержки распространения второй сдвиговой волны, о том, пересекается ли упомянутая граница между двумя этими положениями.
12. Аппарат по п. 11, выполненный с возможностью принятия решения без необходимости деления расстояния на задержку (162) распространения.
13. Аппарат по п. 11, в котором процессор визуализации абляции дополнительно выполнен с возможностью, в ответ на команды от упомянутого аппарата визуализации, отслеживания упомянутой первой сдвиговой волны для формирования упомянутой эталонной карты пространственного распределения эластичности и отслеживания второй сдвиговой волны для формирования предварительной карты пространственного распределения эластичности.
14. Аппарат по п. 13, в котором процессор визуализации абляции дополнительно выполнен с возможностью, в ответ на команды от упомянутого аппарата визуализации, сравнения эталонной карты (228, 304) пространственного распределения эластичности и предварительной карты (244, 308, 320) пространственного распределения эластичности для формирования разностной карты (248) и для осуществления (1) генерирования изображений для визуализации одной или более из упомянутой разностной карты (248) и карты, выведенной из упомянутой разностной карты (248), и/или (2) определения из упомянутой разностной карты (248) границы подвергшейся абляции ткани.
| Bastien Arnal et al, Monitoring of thermal therapy based on shear modulus changes: II | |||
| Shear wave imaging of thermal lesions, IEEE Transactions on Ultrasonics, Ferroelectrics, and Frequency Control, Volume: 58, Issue: 8, August 2011, pp.1603-1611 | |||
| US 2014187940 A1, 03.07.2014 | |||
| US 2011184287 A1, 28.07.2011 | |||
| СПОСОБ ОЦЕНКИ РЕГИОНАЛЬНЫХ УПРУГИХ СВОЙСТВ СТЕНКИ ПОЛОГО ОРГАНА | 2002 |
|
RU2217042C2 |
Авторы
Даты
2019-10-04—Публикация
2016-03-31—Подача