1. Область техники, к которой относится изобретение
Изобретение относится к области люминесцентных соединений с гетероциклическим 2,2'-бипиридиновым ядром и дипиколиламинометильным рецептором и является соединением 1, Фиг. 1. Изобретение может быть использовано в качестве люминесцентного хемосенсора (зонда) на ионы Zn2+ и может найти применение в биологии и медицине, а также в научно-исследовательских лабораториях.
2. Уровень техники
Цинк является важным компонентом многих ферментов, например, в белках карбо-ангидразы [P. Koutnik, E.G. Shcherbakova, S. Gozem, M.G. Caglayan, T. Minami, P. Anzenbacher, Fluorescence-Based Assay for Carbonic Anhydrase Inhibitors, Chem. 2 (2017) 271-282. doi:10.1016/j.chempr.2017.01.011] и «цинковых пальцах» [J.M. Berg, Zinc Finger Domains: Hypotheses and Current Knowledge, Annu. Rev. Biophys. Biophys. Chem. 19 (1990) 405 421. doi:10.1146/annurev.bb. 19.060190.002201]. Цинк играет важную роль в регуляции ферментов, экспрессии генов, нейротрансмиссии и т.д. [J. Yu, C.J. Fahrni, In Situ Imaging of Zinc with Synthetic Fluorescent Probes, in: Zinc Signal., Springer Singapore, 2019: pp.365-388. doi: 10.1007/978-981-15-0557-7_18].
Практически 2,2'-бипиридины являются многообещающими акцепторными системами, поскольку, с одной стороны, при я-сопряжении с донорными функциональными группами, энергия ВЗМО пиридинового кольца бипиридина понижается, по сравнению с энергией ВЗМО бензола, что делает бипиридин высокоэффективным акцепторным доменом лжонъюгированных флуорофоров [R. Bodapati, М. Sarma, A. Kanakati, S.K. Das. J. Org. Chem., 80, 12482 (2015). doi: 10.1021/acs.joc.5b02345]. С другой стороны, широкие возможности химической модификации бипиридинового каркаса делает данные хромофоры перспективными доменами для дизайна флуоресцентных красителей/проб с внутримолекулярным переносом заряда (ICT) под различные задачи. Несмотря на значительное число публикаций по бипиридиновым производным, в литературе не описано, за исключением нескольких статей, использование 2,2'-бипиридина в качестве хромофорной части в составе сенсоров для люминесцентного определения катионов цинка [Tian L. et al. Zinc(II)-induced color-tunable fluorescence emission in the π-conjugated polymers composed of the bipyridine unit: a way to get white-light emission // J. Phys. Chem. B. 2009. Vol.109, №15. P. 69444)947; Kopchuk D.S. et al. Design of ICT-PET fluorescent probes for zinc(II) based on 5-aryl-2,20-bipyridines // Tetrahedron Lett. Elsevier Ltd, 2012. Vol.53, №46. P. 6265-6268]. Поскольку в обозримой научной литературе не было обнаружено близкого подобия соединения 1 (Фиг. 1) нами предлагается вышеупомянутое соединение в качестве селективного хемосенсора (зонда) на ионы Zn2+ in vitro.
3. Сущность изобретения
Сущность изобретения составляет растворимый в органических растворителях 1-(4-(4-метоксифенил)-[2,2'-бипиридин]-6-ил)-N,N-бис(пиридин-2-илметил)метанамин 1, лиганд 2,2'-бипиридинового ряда, структура которого содержит дипиколиламинометильный рецептор, способный обеспечить связывание иона Zn2+ (цинк: лиганд - 1:1) с одновременным увеличением эмиссии фотовозбуждением полученного комплекса, что делает его "turn-on" хемосенсором (зондом) на ионы Zn2+.
Представляемое изобретение демонстрирует хорошие результаты при обнаружении ионов цинка в пробах, а также пригодно для качественной оценки присутствия ионов цинка in vitro.
4. Сведения, подтверждающие возможность осуществления изобретения
4.1. Для подтверждения возможности осуществления изобретения приводится способ получения соединения 1
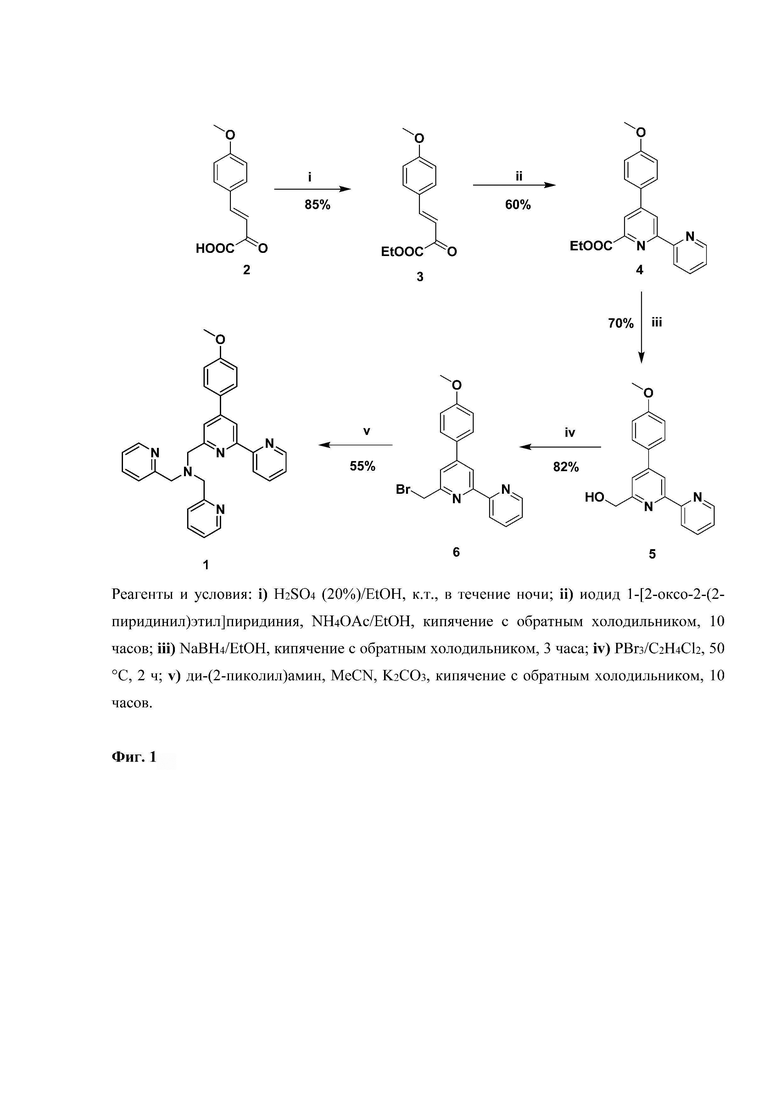
Графически схема синтеза соединения 1 представлена на Фиг. 1. 4-(4-Метоксифенил)-2-оксо-3-бутеновую кислоту 2 [Tang Z., Gao Y., Jiang S., Nie J., Sun F. Cinnamoylformate derivatives photoinitiators with excellent photobleaching ability and cyto-compatibility for visible LED photopolymerization // Prog. Org. Coat., 2022, Vol. 170, art. №106969], (4-(4-метоксифенил)-[2,2'-бипиридин]-6-ил)метанол 5 [Kopchuk D.S., Chepchugov N.V., Taniya OS., Kovalev I.S., Zyryanov G.V., Rusinov V.L., Chupakhin O.N. Effective synthetic approach to 4',5-Diaryl-2,2':6',2''-terpyridines // Russ. J. Org. Chem., 2015, Vol.51, Is. 8, P. 1162-1165], 6-(бромметил)-4-(4-метоксифенил)-2,2'-бипиридин 6 [Krinochkin A.P., Kopchuk D.S., Kim G.A., Gorbunov E.B., Kovalev I.S., Santra S., Zyryanov G.V., Majee A. Rusinov V.L., Chupakhin O.N. Synthesis and luminescence of new water-soluble lanthanide complexes of DTTA-containing 4-(4-methoxyphenyl)-2,2'-bipyridine // Inorg. Chim. Acta, 2018, Vol.478, P. 49-53] были получены по литературной методике.
Синтез этил 4-(4-метоксифенил)-2-оксо-3-бутеноата 3
4-(4-Метоксифенил)-2-оксо-3-бутеновую кислоту 2 (550 мг, 2,67 ммоль) растворяли в этаноле (45 мл) и к раствору добавляли H2SO4 (5 мл). Затем раствор выдерживали при комнатной температуре в течение ночи. К остатку добавляли воду (100 мл), продукт экстрагировали дихлорметаном (ДХМ) (2 × 30 мл). Экстракт промывали безводным сульфатом натрия. Растворитель удаляли при пониженном давлении. Неочищенный продукт использовали на следующей стадии без дополнительной очистки. Выход 420 мг (1,79 ммоль, 85%). ЯМР 1H (CDCl3) 1.47 (т, 3Н, 3J 7.2 Гц, CH2CH3), 3.86 (с, 3Н, ОСН3), 4.38 (к, 2Н, 3J 7.2 Гц, СН2), 6.92-6.96 и 7.58-7.62 (оба м, 2Н, С6НОМе), 7.24 и 7.84 (оба д, 3J 16.0 Гц, стильбен). ESI-MS, m/z: расч. 235.10, найдено 235.10 [М+Н]+.
Синтез этил 4-(4-метоксифенил)-2,2,-бипиридин-6-карбоксилата 4
(Е)-Этил-4-метоксифенил-2-оксобут-3-еноат 3 (492 мг, 2,1 ммоль) растворяли в этаноле (40 мл). Добавляли 1-(2-оксо-2-(пиридин-2-ил)этил)пиридиния иодид (978 мг, 3,0 ммоль), ацетат аммония (162 мг, 2,1 ммоль) и полученную смесь кипятили с обратным холодильником в течение 10 ч в атмосфере аргона. Затем растворитель удаляли при пониженном давлении, к остатку добавляли воду (50 мл), продукт экстрагировали ДХМ (2 × 30 мл). Остаток очищали колоночной хроматографией, элюент: смесь этилацетата и ДХМ (1:10), Rf = 0.6. Аналитический образец получали перекристаллизацией (этанол). Выход 420 мг (1,26 ммоль, 60%). ЯМР 1H (DMSO-d6): 1.47 (т, 3Н, 3J 7.2 Гц, CH2CH3), 3.88 (с, 3Н, ОСН3), 4.67 (к, 2Н, 3J 7.2 Гц, CH2), 7.07-7.12 (м, 2Н, C6HOMe), 7.43-7.48 (м, 1H, Н-5'), 7.80-7.86 (м, 2Н, C6HOMe), 7.94 (ддд, 1H, 3J 7.6 Гц, 7.6 Гц, 4J 1.6 Гц, Н-4'), 8.26 и 8.82 (оба д, 1H, 4J 1.6 Гц, Н-3 и Н-5), 8.51-8.56 (м, 1H, Н-3'), 8.67-8.71 (м, 1H, Н-6'). ESI-MS, m/z: найдено 335.14, расч. 335.13 [М+Н]+. Найдено, %: С 71.68, Н 5.27, N 8.59. C20H18N2O3. Расч., %: С 71.84, Н 5.43, N 8.38
Синтез 1-(4-(4-Метоксифенил)-2,2'-бипиридин-6-ил)-N,N-бис(пиридин-2-илметил)метанамина 1
Ди-(2-пиколил)амин (70 мг, 0,35 ммоль) растворяли в сухом ацетонитриле (40 мл), добавляли бромметилбипиридин 6 (114 мг, 0,32 ммоль) и карбонат калия (444 мг, 3,20 ммоль) и полученную смесь перемешивали с обратным холодильником в течение 10 ч в атмосфере аргона. Затем растворитель удаляли при пониженном давлении, к остатку добавляли воду (30 мл), продукт экстрагировали ДХМ (3×20 мл). Экстракт промывали безводным сульфатом натрия. Растворитель удаляли при пониженном давлении. Остаток разделяли колоночной хроматографией (силикагель, элюент: этилацетат, затем смесь этилацетат : этанол (9:1)), Rf = 0,3. Выход 84 мг (0,18 ммоль, 55%). Аналитический образец получали перекристаллизацией (ацетонитрил). ЯМР 1Н (CDCl3, δ, ppm): 3.89 (с, 2Н, ОМе), 3.97-4.10 (м, 6Н, СН2), 7.00-7.04 (м, 2Н, C6H4OMe), 7.12-7.17 (м, 2Н, Н-5(РуСН2)), 7.29-7.33 (м, 1H, Н-5'(Ру)), 7.62-7.68 (м, 4Н, Н-4(РуСН2), Н-3(РуСН2)), 7.73-7.77 (м, 2Н, С6Н4ОМе), 7.80 (д, 1H, 4J 1.6 Гц, Н-5(Ру)), 7.82 (ддд, 1H, 3J 7.6 Гц, 7.6 Гц, 4J 1.6 Гц, Н-4'(Ру)), 8.47-8.51 (м, 2Н, Н-3'(Ру), Н-3(Ру)), 8.53-8.57 (м, 2Н, Н-6(РуСН2)), 8.67-8.70 (м, 1H, Н-6'(Ру)). ЯМР 13С (CDCl3, δ, ppm): #55.4, 60.3, 60.4, 114.4, 116.8, 120.3, 121.4, 122.1, 123.0, 123.6, 128.4, 130.9, 136.5, 136.9, 149.0 (2С), 149.1, 155.9, 156.5, 159.2, 159.5, 160.5. ESI-MS, m/z: found 474.23, calculated 474.23 [M+H]+. Found, %: С 75.81, H 5.82, N 14.61. C30H27N5O. Calculated, %: С 75.92, H 5.95, N 14.76.
Заявляемое соединение представляет собой бесцветное порошкообразное вещество, умеренно растворимое в органических растворителях, нерастворимое в воде. Синтез цинкового комплекса 1⋅Zn(ClO4)2
Лиганд 1 (57 мг, 0,12 ммоль) суспендировали в 20 мл ацетонитрила, добавляли Zn(ClO4)2⋅6H2O (45 мг, 0,12 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 1 часа. Затем растворитель удаляли при пониженном давлении, остаток очищали перекристаллизацией (метанол). Выход 71 мг (0,10 ммоль, 80%). ЯМР 1Н (DMSO-d6, δ, ppm): 3.84 (с, 3Н, ОМе), 4.31 (с, 2Н, bipyCH2), 4.60 (д, 2Н, 2J 18.0 Гц, РуСН2), 4.66 (д, 2Н, 2J 18.0 Гц, РуСН2), 7.09-7.14 (м, 2Н, С6Н4ОМе), 7.47-7.52 (м, 2Н, Ш5(PyCH2)), 7.68-7.72 (H-3(PyCH2)), 7.83-7.85 (м, 1H, Н-5(Ру)), 7.93-7.97 (м, 2Н, C6H4OMe), 8.09 (ддд, 2Н, 3J.6 Гц, 7.6 Гц, 4J 1.6 Гц, H-4(PyCH2)), 8.10-8.13 (м, 1H, Н-5'(Ру)), 8.17-8.21 (м, 2Н, Н-6(PyCH2)), 8.55 (ддд, 1H, 3J 7.6 Гц, 7.6 Гц, 4J 1.6 Гц, Н-4'(Ру)), 8.77-8.80 (м, 1H, Н-3(Ру)), 9.04-9.07 (м, 1H, Н-3'(Ру)), 9.36-9.40 (м, 1H, Н-6'(Ру)). ЯМР 13С (DMSO-d6, δ, ppm): 56.0, 60.3, 61.0, 115.2, 117.9, 121.3, 124.0, 125.2, 125.5, 127.9, 128.1, 129.6, 141.4, 142.6, 147.7, 148.1, 149.6, 151.1, 152.6, 155.3, 155.5, 161.9. Found, %: С 48.89, Н 3.79, N 9.61. C30H27N5O⋅(ZnClO4)2. Calculated, %: С 48.83, Н 3.69, N 9.49. Crystal Data for C30H27Cl2N5O9Zn (M = 737.83 g/mol): orthorhombic, space group Pbca (no. 61), a = 12.464(11) Å, b = 13.404(7) Å, с = 37.721(19) Å, β = 90°, V = 6302(7) Å3, Z = 8, T = 293(2) K, μ(MoKα) = 1.012 mm-1, ρcalc = 1.555 g/cm3, F(000) = 3024. On the angles 5.516° ≤ 2Θ ≤ 56.606° total of 124525 reflections were collected, 7804 unique (Rint = 0.0401, Rsigma = 0.0186) which were used in all calculations. The final R1 = 0.0441, wR2 = 0.1043 (for reflections with I > 2σ(I)) and R1 = 0.0592, wR2 = 0.1116 (for all data), GOOF = 1.073. Largest diff. peak and hole 0.67/-0.39 eÅ-3. CCDC 2152276 содержит кристаллографические данные для этого соединения.
4.2. Подтверждение флуорофорных свойств сенсора 1 и его комплекса с ионом Zn2+
4.2.1. Флуоресцентные свойства соединения 1
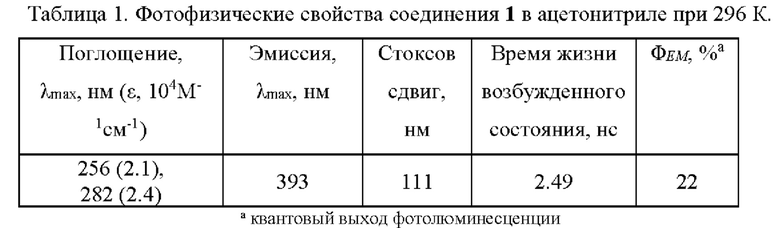
Исследованы спектрально-абсорбционные и спектрально-люминесцентные свойства полученного соединения 1 в растворе ацетонитрила при 296 К. Электронные спектры поглощения регистрировали с использованием стандартной программы Shimadzu Scan на двулучевом спектрофотометре UV-2600 ("Shimadzu", Япония) в диапазоне 190 - 700 нм с точностью установки длины волны ± 0,1 нм. Сенсор характеризуется высокой поглощательной способностью: наибольшее поглощение с молярным коэффициентом экстинкции 24000 М-1 cm-1 наблюдалось при λabs max = 282 нм (Табл. 1). Спектры возбуждения и излучения измеряли на спектрофлуориметре Horiba FluoroMax-4, в качестве импульсного источника возбуждения которого использовалась ксеноновая лампа, с точностью установки длины волны ±0.5 нм. Установлено, что максимум флуоресценции лиганда при возбуждении излучением с длиной волны 282 нм, находится при 393 нм (Табл. 1). Высокое значение Стоксова сдвига (<100 нм) и неструктурированная полоса спектра излучения свидетельствуют о наличии внутримолекулярного переноса заряда (ICT).
Процедуры измерения абсолютного квантового выхода и времени жизни возбужденного состояния флуорофора 1.
Для исследования были использованы растворители уровня очистки HPLC. Флуорофор 1 был очищен колоночной хроматографией. Для измерений применялись фирменные стандартные четырехоконные кварцевые кюветы SUPRASIL 111-QS 10 ("Hellma", Германия) объемом 4 мл, длиной оптического пути 1 см.
Измерение абсолютного квантового выхода флуорофора 1 проводилось в ацето-нитриле при 296 К с использованием спектрофлуориметра Horiba-Fluoromax-4 в интегрирующей сфере Quanta-Phi, покрытой изнутри материалом Spectralon® после калибровки монохроматора возбуждения. С целью избежать эффекта внутреннего фильтра и/или самотушения для хемосенсора измерялся спектр поглощения, чтобы выбрать длину волны возбуждения, где оптическая плотность меньше 0,1. Далее регистрировались спектры эмиссии и рэлеевского рассеяния чистого растворителя и раствора хемосенсора. Абсолютное значение квантового выхода фотолюминесценции рассчитывали с использованием стандартной программы Origin на спектрофлуориметре Horiba-Fluoromax-4.
Измерение времени жизни возбужденного состояния флуорофора 1 проводилось в ацетонитриле при 296 К с использованием однофотонного возбуждения (time-correlated single-photon counting, TCSPC) с наносекундным светодиодом (310 нм) на спектрофлуориметре Horiba-Fluoromax-4. С целью избежать эффекта внутреннего фильтра и/или самотушения для хемосенсора измерялся спектр поглощения, чтобы выбрать длину волны возбуждения, где оптическая плотность меньше 0,1. Для измерения времени жизни возбужденного состояния использовалось не менее 3-х параллелей с усреднением результатов, χ2 ≤ 1,2. Значение времени жизни рассчитывали с использованием специальной программы DataStation на спектрофлуориметре Horiba-Fluoromax-4.
Опираясь на данные таблицы 1, а именно, высокое значение Стоксова сдвига (<100 нм), долгоживущую эмиссию (<2 не), а также наличие внутримолекулярного переноса заряда (ICT) с фотолюминесцентным квантовым выходом 20%, характеризуют соединение 1, как весьма эффективный флуорофор.
4.2.2. Подтверждение насыщения координационной сферы Zn2+ соединением 1
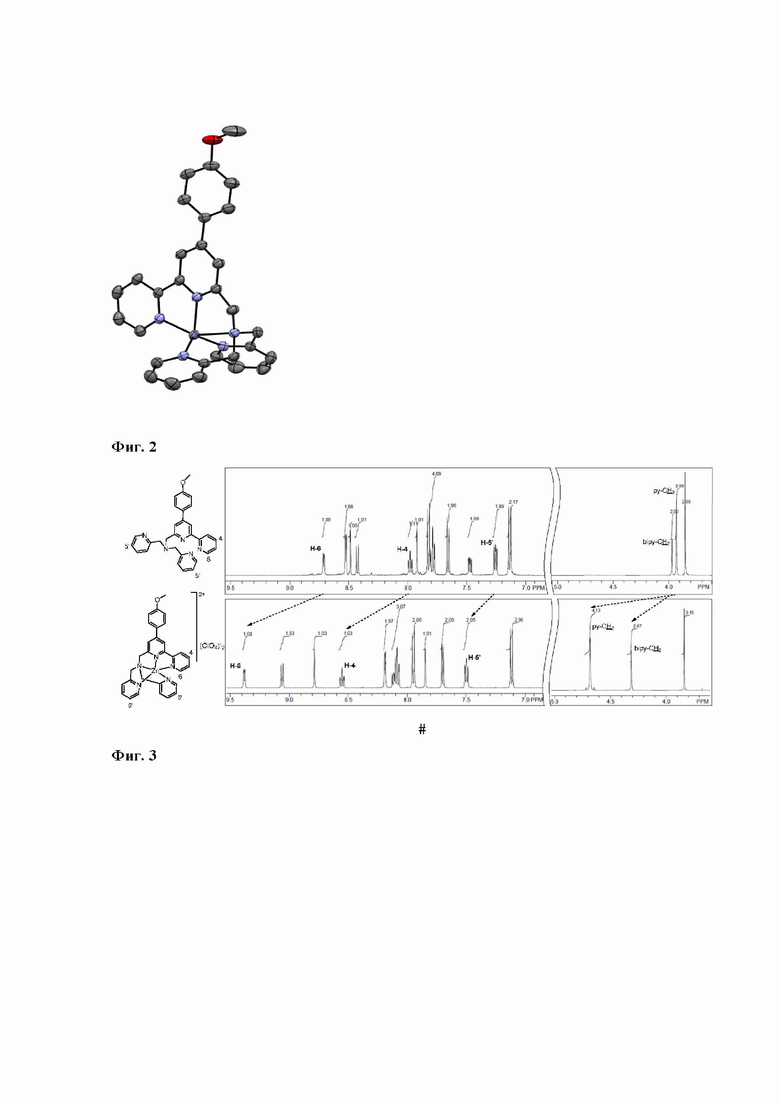
Для установления структуры металлокомплекса и определения стехиометрического соотношения металл: соединение 1 получен и исследован монокристалл [Zn(1)](ClO4)2 методом рентгеноструктурного анализа (Фиг. 2).
Кроме того, для детального изучения динамики взаимодействия лиганда 1 с Zn2+ в растворе был проведен 1Н ЯМР эксперимент на спектрометре Bruker Avance-400. Были сняты спектры 1Н ЯМР свободного лиганда 1 и цинкового комплекса в одном том же растворителе (CDCl3). Установлено, что в спектре комплекса наблюдалось смещение сигналов протонов бипиридина в положениях 4 и 6 в слабое поле с 8.0 до 8.55 ppm и с 8.7 до 9.4 ppm соответственно. Подобное смещение наблюдалось и для дипиколинового фрагмента: сигналы протонов пиридиновых колец в положениях 5 смещаются с 7.25 до 7.5 ppm (Фиг. 3).
Таким образом, показано, что структура комплекса [Zn(1)]2+ представляет собой соотношение металл: лиганд 1:1, а также доказано участие бипиридинового домена и ди-пиколиламинового фрагмента в образовании комплекса.
4.2.3. Аналитические свойства динамического комплекса Zn2+

Известно, что комплексообразование лиганда с катионами Zn2+ за счет связывания неподеленных электронных пар азотов дипиколиламинового рецептора и «выключения» процесса фото индуцированного электронного переноса (PET) приводит к усилению интенсивности флуоресценции пробы. При этом сенсор 1 является тем редким случаем, в котором сочетаются ICT и PET процессы.
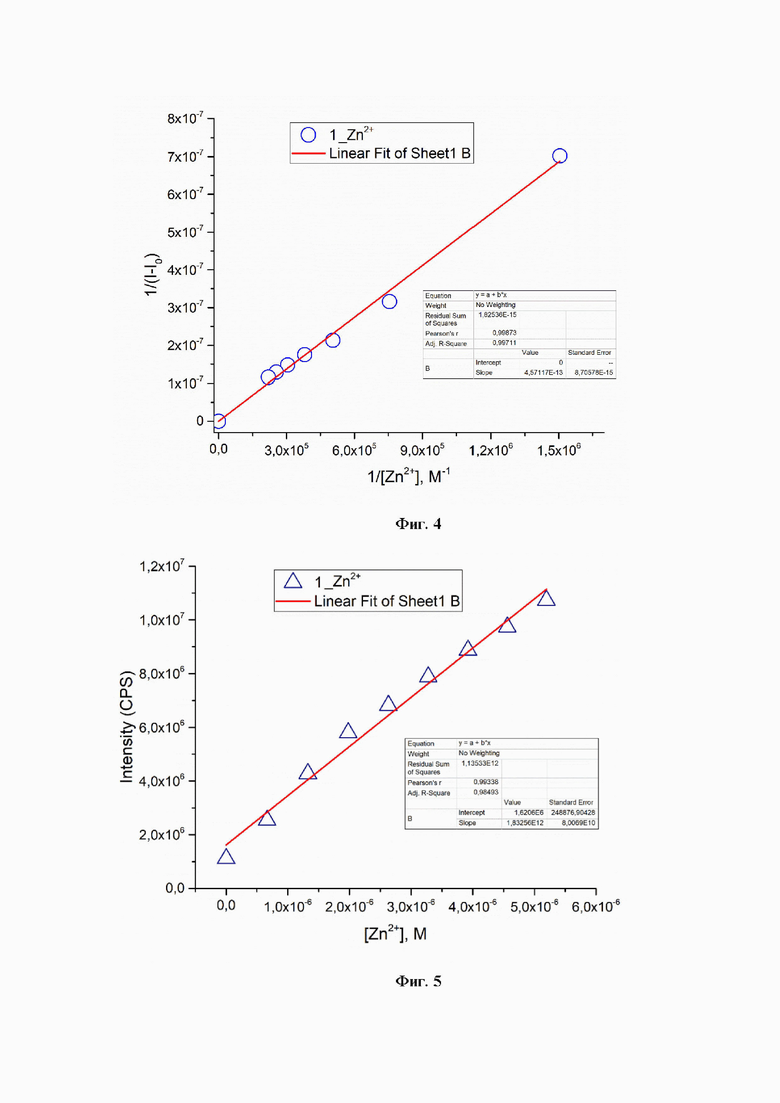
Чтобы выявить природу фотоиндуцированного процесса, дополнительно проведено тестирование координации лиганда 1 ионами Zn2+ в растворе ацетонитрила при 296 К. Для этого проведено титрование раствора лиганда 1 по насыщению координационной сферы ионами Zn2+ . Процедура титрования проводилась в кварцевой кювете с использованием метода Бенези-Хильдебранда (В-Н) с целью определения константы связывания (Ks) и заключалась в следующем [Н.А. Bene si, J.H. Hildebrand, A Spectrophotometry Investigation of the Interaction of Iodine with Aromatic Hydrocarbons, J. Am. Chem. Soc. 71 (1949) 2703-2707].
Ацетонитрильный раствор сенсора (С = 10-5М) помещали в кварцевую кювету и добавляли к нему последовательно 10-15 аликвот объемом по 5 мкл водного раствора перхлората цинка (С = 10-4 М) - Спектры эмиссии измеряли на спектрофлуориметре Horiba FluoroMax-4 при длине волны возбуждения 314 нм. Исходя из полученных данных титрования, графически была определена константа связывания (Ks) бипиридинового лиганда с Zn2+ с использованием уравнения Бенези-Хильдебранда (R2>0,99) формула (1):
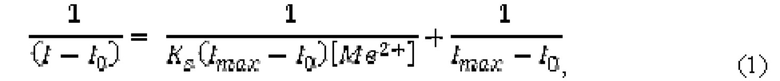
где I - текущая интенсивность эмиссии; I0 - начальная величина интенсивность эмиссии;
Imax - максимальная величина эмиссии в эксперименте; [Me2+] - текущая концентрация металла в растворе
На основе полученных данных титрования также определили предел обнаружения (LOD) ионов цинка (R2>0,99) по уравнению в соответствии с ранее описанной методикой [Shrivastava A. G. V. Methods for the determination of limit of detection and limit of quantitation of the analytical methods// Chronicles Young Sci. 2011. Vol.2, №1. P. 21-25], формула (2):

где σ - стандартное отклонение интенсивности флуорофора в отсутствие аналита и k - наклон калибровочной кривой. Исходя из данных таблицы 2, высокий порядок константы связывания (<105 М-1) (Фиг. 4, Табл. 2) при пределе обнаружения цинка, достигающем значения 10-8 М (Фиг. 5, Табл.2), определили сенсор 1, как перспективный для качественного и количественного обнаружения ионов цинка в клетках и тканях ih vitro.
4.2.4. Флуоресцентные свойства комплекса [Zn(1)]2+

Аналогично методике, описанной в п. 4.2.1, исследованы спектрально-абсорбционные и спектрально-люминесцентные свойства полученного комплекса [Zn(1)]2+ в растворе ацетонитрила при 296 К. Кроме того, осуществлены процедуры измерения абсолютного квантового выхода и времени жизни возбужденного состояния комплекса, описанные в п. 4.2.1, на базе снятых спектров абсорбции и эмиссии. При наблюдаемом батохромном смещении максимумов поглощения и эмиссии значение Стоксова сдвига для [Zn(1)]2+ возросло на 40%, а ФЕМ - на 80% (Табл. 3).
4.2.5. Подтверждение работоспособности сенсора 1 в присутствии ионов других металлов
С целью избежать перекрестной чувствительности и проверить на интерференцию ионы металлов в исследовании поведения ионов Zn2+ по отношению к соединению 1, было проведено два эксперимента.
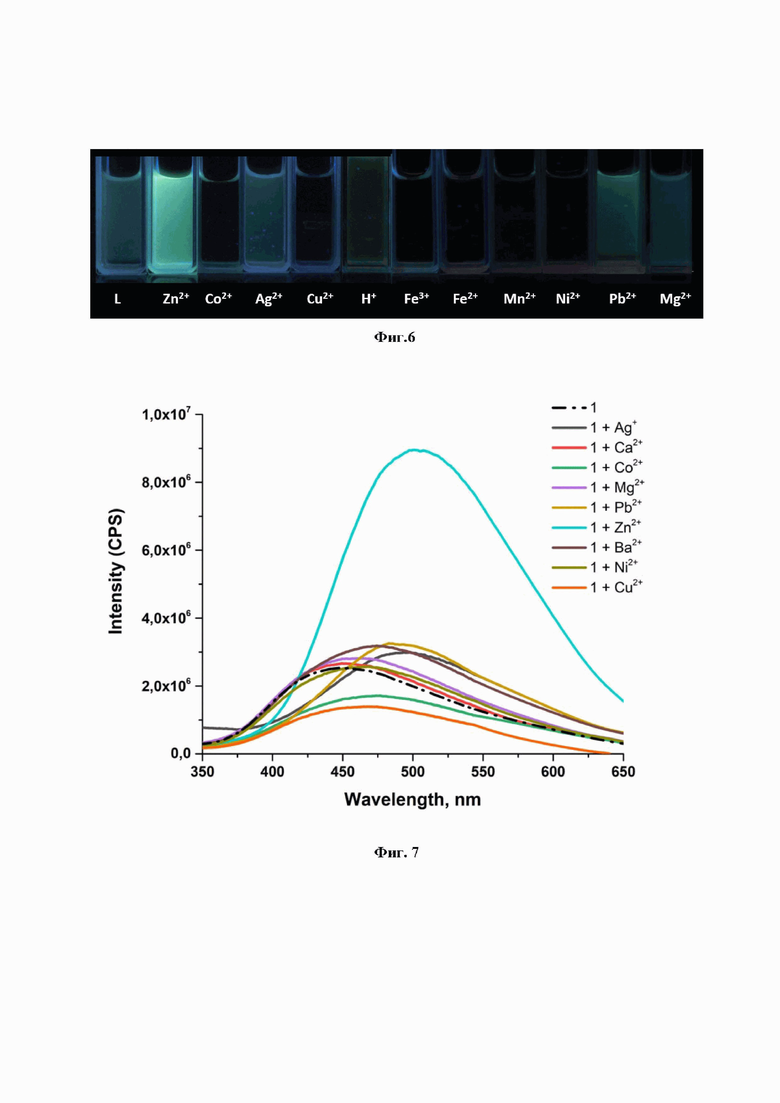
1. К ацетонитрильному раствору соединения 1 (С = 10-5 М) добавляли 50 мкл водного раствора ацетата металла (Ag+, Са2+, Со2+, Mg2+, Zn2+ , Pb2+, Ва2+, Ni2+, Cu2+) (2×10-4 M,), что составляло ~0,8 мол. экв., до полного растворения соли. Фотоснимок облучения проб УФ лампой при длине волны 365 нм выявил существенное изменение во флуоресцентном отклике сенсора 1 на присутствие ионов Zn2+ (Фиг. 6).
2. К ацетонитрильному раствору соединения 1 (С = 10-5 М) добавляли расчетный трехкратный мольный избыток ацетата металла (Ag+, Са2+, Со2+, Mg2+, Zn2+ , Pb2+, Ва2+, Ni2+, Cu2+) до полного растворения соли. Далее снимали спектры флуоресценции соединения 1 в присутствии катиона металла. У пробы 1 наблюдалась наиболее интенсивная широкая полоса излучения с максимумом 498 нм только для Zn2+ (Фиг. 7). Расчет относительного изменения интенсивности флуоресценции dI проводили по формуле: dI=I/I0, где I0 - исходная интенсивность флуоресценции раствора соединения 1; I - интенсивность флуоресценции раствора соединения 1 после добавления трехкратного мольного избытка катиона. Относительная интенсивность флуоресценции в присутствии катионов Zn2+ увеличилась в ~3,0 раза, что свидетельствует о проявлении высокой селективной сенсорной активности по отношению к катионам Zn2+ исследуемого хемосенсора 1.
4.4. Подтверждение работоспособности сенсора 1 при обнаружении цинка в клетках и тканях
Процедуры культивирования и окрашивания клеток. В работе использовали клетки рака шейки матки человека (HeLa), полученные из клеточной коллекции ООО «Био-лот» (Россия). Культуру клеток поддерживали в культуральных флаконах («Эппендорф», Германия), в среде DMEM («Sigma-Aldrich», США) с добавлением 10% фетальной телячьей сыворотки («Биолот», Россия) и 0,5% гентамицина («Биолот», Россия) в инкубаторе с атмосферой 5% СО2. Для окраски соединением 1 клетки разводили до концентрации 104 клеток/мл и переносили в чашки со стеклянным дном (Jet Biofil., Китай), где их культивировали в течение 24 часов. Затем меняли питательную среду и добавляли раствор вещества в ДМСО (в концентрации 25 ммоль/л) в количестве 50 мкл на 1 мл питательной среды.
Животные. Процедура подготовки тканей и окрашивания срезов
Крысы-самки линии Вистар (возраст 16 недель) получены из Института иммунологии и физиологии УрО РАН (Екатеринбург, Российская Федерация). Животные содержались в равных условиях (цикл 12 часов света/12 часов темноты с включением света в 9:00 утра, температура 20±2°С), по 5 животных в клетке и кормились по обычному графику со свободным доступом к воде. Животные не проявляли никаких симптомов какого-либо заболевания.
Медианная лапаротомия крыс проводилась под общим наркозом. Были извлечены желудок, селезенка и поджелудочная железа. Образцы поджелудочной ткани были отделены от жировой ткани и погружены в 10% нейтральный формалин в течение 24 часов при комнатной температуре. Затем раствор был заменен парафином.
Подготовка образцов для гистологического исследования осуществлялась на автоматическом процессоре Leica EG 1160 с последующей заливкой в парафин. Со срезов толщиной 3-4 мм удаляли парафин [Addison AW, Rao TN, Reedijk J, van Rijn J, Verschoor GC. Synthesis, structure, and spectroscopic properties of copper (II) compounds containing nitrogen-sulphur donor ligands; the crystal and molecular structure of aqua[1,7-bis(N-methylbenzimidazol-2'-yl)-2,6-dithiaheptane]copper (II). J Chem Soc, Dalton Trans 1984:1349 56. https://doi.org/10.1039/DT9840001349]. Затем, без высыхания каждый срез был окрашен раствором пробы 1 в этаноле (с = 3,8 ммоль/л) или в ДМСО (с = 6,8 ммоль/л).
Процедура микроскопического исследования.
Микроскопическое исследование проводилось с использованием оборудования Совместного научно-исследовательского центра научного оборудования Уральского филиала РАН. После окрашивания и промывания живые клетки были исследованы с помощью конфокального лазерного сканирующего микроскопа LSM-710; Carl Zeiss имеет многоканальный детектор QUASAR (34 канала). Изображения были получены с помощью погружной линзы 40х/1.3 Oil. Для получения информативного флуоресцентного изображения в специальном программном обеспечении ZEN использовался специальный лямбда-режим (λ-режим), который позволяет определить диапазон эмиссии с максимальным контрастом. Исследования проводились при возбуждении лазером с длиной волны 405 нм, и излучение было зарегистрировано во всем диапазоне конфокального микроскопа (400-750 нм).
На клеточных культурах исследование проводилось следующим образом. Фоновая флуоресценция клеток в лямбда-режиме (при возбуждении лазером с длиной волны 405 нм) была ранее удалена, после чего водный раствор ацетата цинка (с = 132 ммоль/л) добавляли в питательную среду и аккуратно смешивали.
Гистологические участки поджелудочной железы также были исследованы в лямбда-режиме. Флуоресценция изучалась в зоне островка поджелудочной железы, а также в зоне паренхимы, окружающей его.
Относительная интенсивность флуоресценции образца была определена на основе максимальной, полученной на основе изображения в лямбда-режиме. Для этого спектр интенсивности определяли в десяти точках изображения, усредняли максимальное значение и вычисляли доверительные интервалы. Так как изображения были сделаны в разных настройках, значение было скорректировано с учетом мощности лазера и высоты конфокального разреза. Изображения обрабатывались с помощью LSM Image Browser, ImageJ и GIMP.
1. Исследована способность пробы 1 окрашивать клетки, искусственно обогащенных ионами цинка, для флуоресцентной микроскопии.
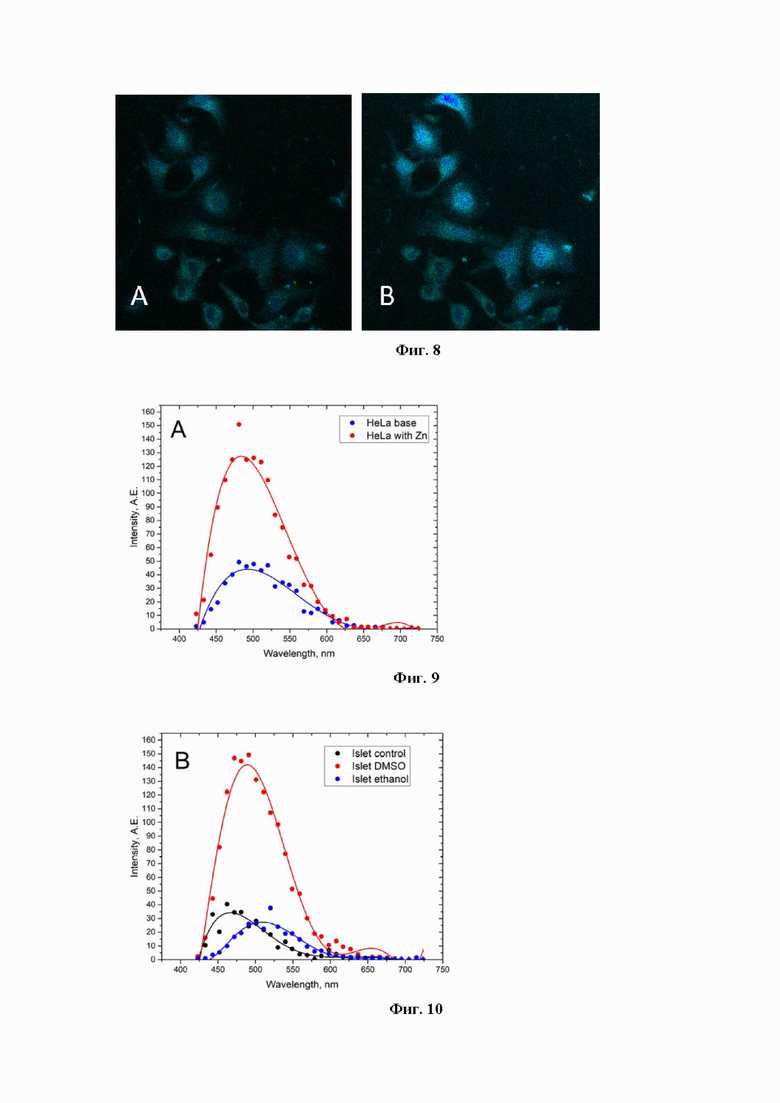
Клетки HeLa при добавлении лиганда 1 проявляли слабую автофлуоресценцию при возбуждении лазером с длиной волны 405 нм. При добавлении в клеточный раствор ацетата цинка в присутствии пробы 1 интенсивность флуоресценции клеток увеличилась примерно в 2,5 раза. При этом известно, что естественная концентрация ионов цинка в клетках составляет не более 1 × 10-10 М, и ею можно пренебречь [Qin Y, Miranda JG, Stoddard CI, Dean KM, Galati DF, Palmer AE. Direct Comparison of a Genetically Encoded Sensor and Small Molecule Indicator: Implications for Quantification of Cytosolic Zn2+ . ACS Chem Biol 2013;8:2366-71. https://doi.org/10.1021/cb4003859]. Флуоресцентное изображение клеток HeLa, искусственно обогащенных ионами цинка, до и после добавления вещества 1, представлены на Фиг. 8. Изображение получено в лямбда-режиме при возбуждении лазером с длиной волны 405 нм. Максимальная интенсивность флуоресценции в клетках, обработанных цинковой солью, при добавлении пробы 1 достигалась в течение 1-2 мин и дальнейшего изменения интенсивности не наблюдалось. Это может указывать на то, что весь лиганд 1 быстро связался с ионами цинка.
Сравнительная интенсивность максимальной флуоресценции клеток до и после добавления ионов цинка в питательную среду представлена на графике (Фиг. 9).
2. Исследована способность пробы 1 окрашивать ткани, в которых активно мета-болизируются ионы цинка.
Одним из важнейших органов, в которых активно метаболизируется цинк, является поджелудочная железа. Известно, что в β-клетках островков Лангерганса, где протекает синтез инсулина, концентрация ионов цинка составляет около 5×10-3 М. [Emdin SO, Dod-son GG, Cutfield JM, Cutfield SM. Role of zinc in insulin biosynthesis. Diabetologia 1980;19:174-82. https://doi.org/10.1007/BF00275265]. Окрашивание тканей проводили раствором вещества в ДМСО и в этаноле. Сравнительная интенсивность максимальной флуоресценции окрашенных срезов поджелудочной железы раствором ДМСО и этанола пробы 1 представлен на Фиг. 10.
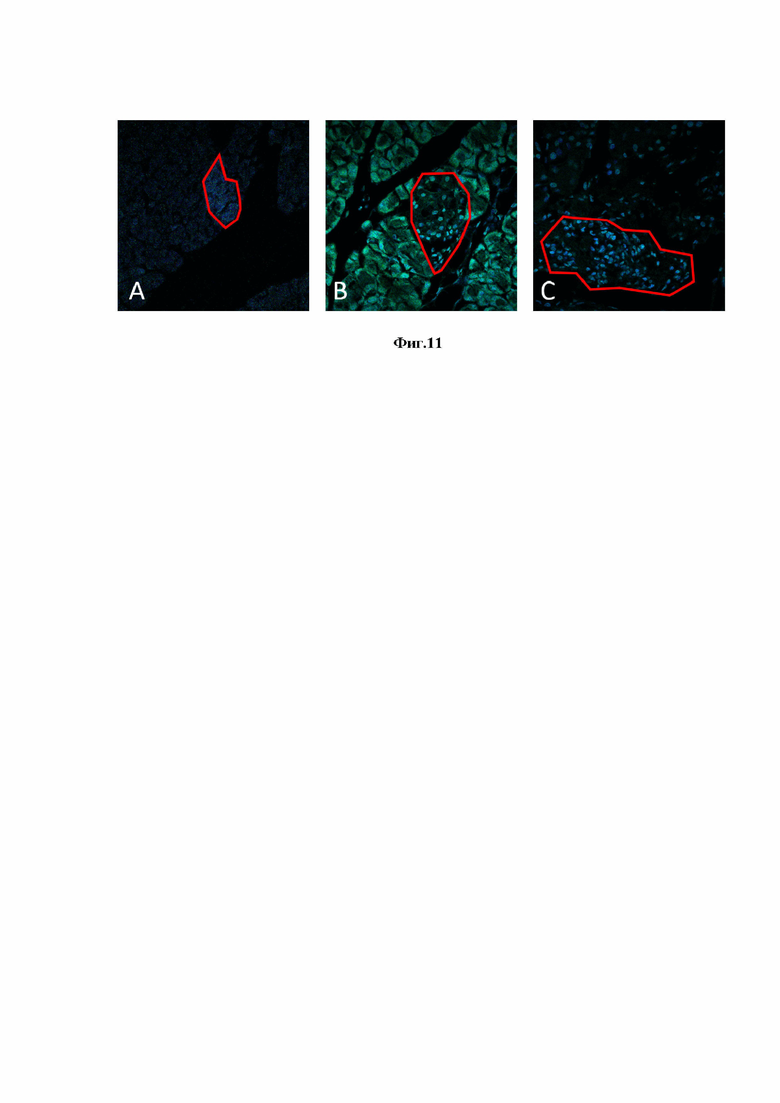
При окраске среза спиртовым раствором пробы 1 наблюдалось значительное увеличение интенсивности флуоресценции по всей ткани, но снижалась в области островков. В случае окрашивания среза раствором вещества 1 в ДМСО наблюдалась отчетливая флуоресценцию в области островка. Изображения, полученные в лямбда-режиме на волне возбуждения длиной 405 нм, показаны на Фиг. 11.
Таким образом, соединение 1 можно использовать в качестве метки/пробы для обнаружения цинка не только в живых клетках, искусственно обогащенных солями цинка, но и в фиксированных тканях, в которых катионы находятся в связанном состоянии. Высокая константа связывания соединения 1 с катионами цинка позволяет использовать его для точной локализации р-клеток поджелудочной железы (островков Лангерганса). Пригодность вещества 1 для этих целей подтверждена экспериментально.
| название | год | авторы | номер документа |
|---|---|---|---|
| 5-ФЕНИЛ-5""-п-ТОЛИЛ-2,2":6",2""-ТЕРПИРИДИН - ХЕМОСЕНСОР ДЛЯ ФЛУОРЕСЦЕНТНОГО ОПРЕДЕЛЕНИЯ КАТИОНОВ Zn В ВОДНЫХ И ПИЩЕВЫХ ОБРАЗЦАХ | 2021 |
|
RU2773238C1 |
| N-([1,1'-БИФЕНИЛ]-3-ИЛ)-4-ФЕНИЛ-1-(ПИРИДИН-2-ИЛ)-6,7-ДИГИДРО-5H-ЦИКЛОПЕНТА[C]ПИРИДИН-3-АМИН - МОНОМОЛЕКУЛЯРНЫЙ ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ НИТРОАРОМАТИЧЕСКИХ ВЗРЫВЧАТЫХ ВЕЩЕСТВ | 2022 |
|
RU2786741C1 |
| 4-(2-(ПИРИДИН-2-ИЛ)-9H-ПИРИДО[2,3-b]ИНДОЛ-8-ИЛ)АНИЛИН - КЛЕТОЧНЫЙ ФЛУОРЕСЦЕНТНЫЙ КРАСИТЕЛЬ | 2024 |
|
RU2836779C1 |
| N, N' БИС(9-АНТРИЛМЕТИЛ)ЦИКЛОГЕКСАН-1, 2-ДИАМИН-ФЛУОРЕСЦЕНТНЫЙ ХЕМОСЕНСОР НА КАТИОНЫ Zn | 2006 |
|
RU2315748C1 |
| N',N"'-((5-Гидрокси-4,7-диметил-2-оксо-2Н-хромен-6,8-диил)бис(метанилилиден))бис(4-бромбензогидразид)-амбидентатный хромогенный и флуоресцентный хемосенсор на Hg и F | 2016 |
|
RU2621701C1 |
| ДИМЕТИЛ 4-ФЕНИЛ-5-(2-ФЕНИЛ-1H-ИНДОЛ-3-ИЛ)-1-(4-ТОЛИЛ)-1H-ПИРРОЛ-2,3-ДИКАРБОКСИЛАТ - ОПТИЧЕСКИЙ ХИМИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ НИТРОАРОМАТИЧЕСКИХ ВЗРЫВЧАТЫХ ВЕЩЕСТВ | 2023 |
|
RU2820149C1 |
| ПРИМЕНЕНИЕ 2-МЕТИЛ-3-(6-(ТИОФЕН-2-ИЛ)-3-(4-ТОЛИЛ)ПИРИДИН-2-ИЛ)-1Н-ИНДОЛА В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНОГО ХИМИЧЕСКОГО СЕНСОРА ДЛЯ ОБНАРУЖЕНИЯ 2,4,6-ТРИНИТРОФЕНОЛА | 2023 |
|
RU2829733C1 |
| РЕАГЕНТ ДЛЯ ОБНАРУЖЕНИЯ КАТИОНОВ МЕТАЛЛОВ НА ОСНОВЕ 2,2’-БИПИРИДИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2668133C2 |
| ((ОКСИБИС(ЭТАН-2,1-ДИИЛ))БИС(ОКСИ))БИС(ЭТАН-2,1-ДИИЛ)БИС(ПИРЕН-1-КАРБОКСИЛАТ) - МОНОМОЛЕКУЛЯРНЫЙ ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ НИТРОАЛИФАТИЧЕСКИХ ВЗРЫВЧАТЫХ ВЕЩЕСТВ | 2022 |
|
RU2816695C1 |
| 6,7-ДИФТОР-2-(ПИРИДИН-2-ИЛ)-9H-ПИРИДО[2,3-b]ИНДОЛ - ЛЮМИНЕСЦЕНТНЫЙ ХИМИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ 2,4,6-ТРИНИТРОФЕНОЛА (ПИКРИНОВОЙ КИСЛОТЫ) | 2023 |
|
RU2828883C1 |
Изобретение относится к области люминесцентных соединений с гетероциклическим 2,2'-бипиридиновым ядром, а именно к 1-(4-(4-метоксифенил)-[2,2'-бипиридин]-6-ил)-N,N-бис(пиридин-2-илметил)метанамину
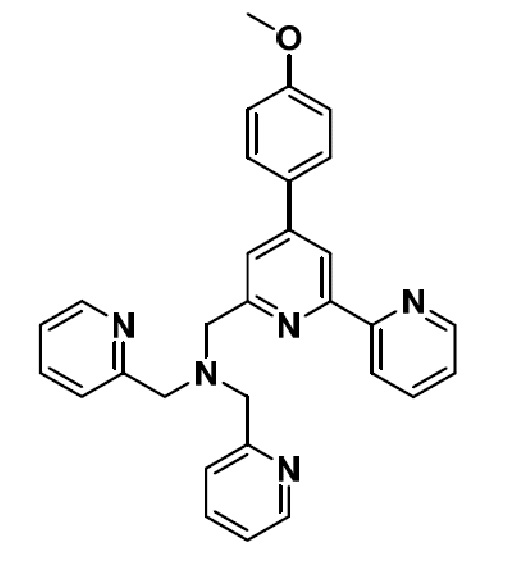
- мономолекулярному химическому сенсору для флуоресцентного определения катионов Zn2+ in vitro. Технический результат изобретения заключается в создании лиганда 2,2'-бипиридинового ряда, структура которого обеспечивает насыщение координационной сферы иона Zn2+ с одновременным увеличением эмиссии фотовозбуждением полученного металлокомплекса, что делает его "turn-on" хемосенсором (зондом) на ионы Zn2+. 11 ил., 3 табл.
1-(4-(4-Метоксифенил)-[2,2'-бипиридин]-6-ил)-N,N-бис(пиридин-2-илметил)метанамин
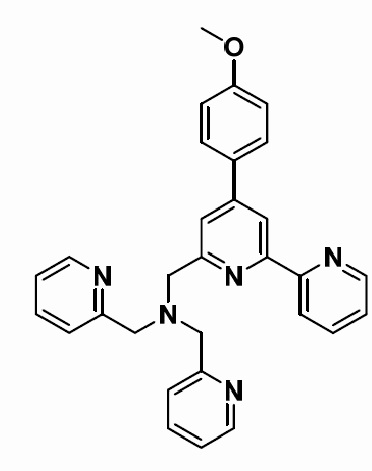 - мономолекулярный химический сенсор для флуоресцентного определения катионов Zn2+ in vitro.
- мономолекулярный химический сенсор для флуоресцентного определения катионов Zn2+ in vitro.
| TIAN L | |||
| et al., Zinc(II)-Induced Color-Tunable Fluorescence Emission in the π-Conjugated Polymers Composed of the Bipyridine Unit: A Way to Get White-Light Emission, J | |||
| Phys | |||
| Chem | |||
| B, 2005, vol.109, no.15, p.6944-6947 | |||
| KOPCHUK D.S | |||
| et al., Design of ICT-PET fluorescent probes for zinc(II) based on 5-aryl-2,20 -bipyridines, Tetrahedron Letters, |
Авторы
Даты
2024-07-01—Публикация
2023-11-10—Подача