1. Область техники, к которой относится изобретение
Изобретение относится к области люминесцентных соединений с гетероциклическим 9H-пиридо[2,3-b]индольным ядром 1, Схема 1. Изобретение может быть использовано в качестве люминесцентного красителя на органоиды живых клеток и может найти применение в биологии и медицине, а также в научно-исследовательских лабораториях.
2. Уровень техники
Пиридоиндолы (карболины или азакарбазолы) в результате планарности пиридо[2,3-b]индольного домена [Org. Biomol. Chem., 2012, 10, 5084-5093] представляют собой уникальный класс гетероциклических соединений не только из-за широкого спектра биологической активности [D. Li, R. Yang, J. Wu, В. Zhong and Y. Li, Front. Chem., 2022, 10, 988327. Z. Li, S. Chen, S. Zhu, J. Luo, Y. Zhang and Q. Weng, Molecules, 2015, 20, 13941-13957. Y. Ни, H. Shi, M. Zhou, Q. Ren, W. Zhu, W. Zhang, Z. Zhang, C. Zhou, Y. Liu, X. Ding, H. C. Shen, S. F. Yan, F. Dey, W. Wu, G. Zhai, Z. Zhou, Z. Xu, Y. Ji, H. Lv, T. Jiang, W. Wang, Y. Xu, M. Vercruysse, X. Yao, Y. Мао, X. Yu, K. Bradley and X. Tan, J. Med. Chem., 2020, 63, 9623-9649], но и благодаря многообещающим оптоэлектронным свойствам [Chem. Asian J. 2017, 12, 2501-2509] и способностью взаимодействовать с ДНК [Org. Biomol. Chem., 2012, 10, 5084-5093]. Карболины состоят из π-дефицитного пиридинового кольца, аннелированного с π-избыточным индолом, что существенно влияет на кислотно-основные свойства атомов азота пиррольного и пиридинового типа [BalonM (1997) J Org Chem 62:5104-5109], и, как следствие, приводит к проявлению ESDPT-процессов (the excited state double intramolecular proton transfer) и фототаутомерии [Chang С, Shabestary N, El-Bayoumi MA (1980) Excited-state double proton transfer in 1-azacarbazole hydrogen-bonded dimers. Chem Phys Lett 75:107 109, Waluk J, Herbich J, Oelkrug D, Uhl S (1986) Excited-state double proton transfer in the solid state: the dimers of 1-azacarbazole. J Phys Chem 90:3866-3868, Mente S, Maroncelli M (1998) Solvation and the excited-state tautomerization of 7-azaindole and 1-azacarbazole: computer simulations in water and alcohol solvents. J Phys Chem 102:3860-3878]. Хотя за последнее время спектроскопии и фотофизике различных изомеров карболина уделяется пристальное внимание [М. Balon et al. / Chemical Physics 299 (2004) 67-77], пиридоиндолы, как флуоресцентные красители для покраски живых клеток рассмотрены в литературе весьма ограниченно. Профессор Кумар и др. синтезировали ряд пиридо[1,2-а]индолов. Сильная флуоресценция одной из исследуемых пиридоиндольных проб была использована в субклеточной визуализации и демонстрировала локализацию в ядре клетки [Chem. Eur. J. 2014, 20, 14344-14350]. Группа химиков из Индии получили новый ряд флуоресцентных проб на основе алкилзамещенного пиридоиндола и тетрафе-нилэтилена, демонстрирующий легкое переключение флуоресценции, вызванное изменением рН в растворе, в виде наночастиц и в твердом состоянии. Исследования флуоресцентной микроскопии с использованием организмов, включая низшие и высшие эукариоты, выявили специфическую локализацию красителей в липидных дроплетах [Chem. Asian J. 2017, 12, 2501-2509]. В 2023 году группа немецких химиков опубликовала результаты фотометрических и флуориметрических исследований β-карболиновых производных. Пробы интеркалировали в ДНК с константами связывания Kb=1-3×104 М. Кроме того, было показано, что производное 2-бензил-6-(3-метоксифенил)гарманиума действует как флуоресцентный краситель в сложной биологической среде эукариотических клеток, а именно в фибробластах мыши NIH 3Т3 [doi.org/10.1002/ceur.202300045]. Однако при этом в литературе не было обнаружено подобие полученной нами пробы 1 в качестве флуоресцентного красителя для покраски живых клеток, таким образом нами предлагается 4-(2-(пиридин-2-ил)-9H-пиридо[2,3-B]индол-8-ил)анилин клеточный флуоресцентный краситель.
3. Сущность изобретения
Сущность изобретения составляет растворимый в органических растворителях 4-(2-(пиридин-2-ил)-9H-пиридо[2,3-b]индол-8-ил)анилин 1, который может использоваться как флуоресцентный краситель для биовизуализации ядер живых клеток.
Соединение 1 можно использовать в качестве метки/пробы для обнаружения и/или наблюдения за метаболическими процессами, протекающими в ядре и/или ядрышке живой клетки. При этом благодаря формированию комплексов с ДНК вещество 1 может быть использовано одновременно для выявления липидных дроплет (возбуждение при 405 нм), так и для ядра и/или ядрышка (возбуждение при 561 нм).
4. Сведения, подтверждающие возможность осуществления изобретения
4.1. Для подтверждения возможности осуществления изобретения приводится способ получения соединения 1
Графически схема синтеза соединения 1 представлена на Схеме 1.
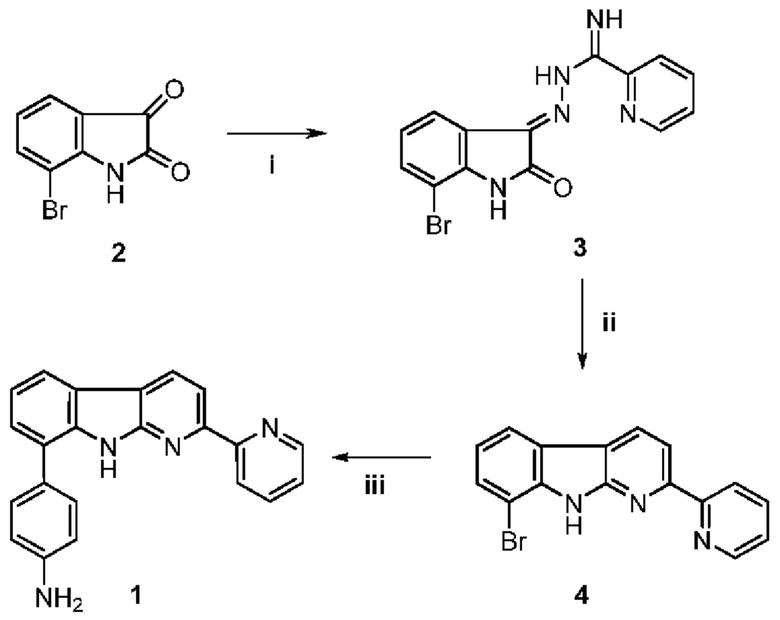
Схема 1. Реагенты и условия: i) Пиколинимидогидразид, EtOH, кипячение с обратным холодильником в течение 2 часов; ii) 2,5-норборнадиен, 1,2-дихлорбензол, в автоклаве в атмосфере аргона, 215°С, в течение 20 часов; iii) 4-аминофенилборная кислота, дихлор-бис(трифенилфосфин)палладий, трифенилфосфин, 1,4-диоксан, EtOH, кипячение в течение 15 часов.
Синтез N'-((3Z)-7-бром-2-оксо-2,3-дигидро-1H-индол-3-илиден)пиридин-2-карбоксимидогидразида 3
Смесь 7-бромоизатина (202 мг, 1 ммоль) и пиколинимидогидразид (190 мг, 1,4 ммоль) в этаноле (25 мл) кипятили в течение 2 часов. Образовавшийся осадок отфильтровывали и промывали этанолом (5 мл). Продукт использовали на следующей стадии без дополнительной очистки. Выход 233 мг (0.68 ммоль, 68%). ЯМР 1Н (400 МГц, DMSO-d6) δ 6.92-7.09 (m, 1H, CHarom), 7.41-7.48 (м, 1Н, CHarom), 7.53 (с, 1Н, NH), 7.58-7.69 (м, 1H, Н-5'(Ру)), 7.77 (с, 1H, NH), 7.96-8.10 (м, 1H, Н-4'(Ру)), 8.31-8.49 (м, 2Н, CHarom, Н-3'(Ру)), 8.67-8.80 (м, 1Н, Н-6'(Ру)), 10.82 (с, 1H, NH). ESI-MS, m/z: расч. 344.01, найдено 344.01 (М+Н)+.
Синтез 8-бром-2-(пиридин-2-ил)-9H-пиридо[2,3-b]индола 4
К суспензии N'-((3Z)-7-бром-2-оксо-2,3-дигидро-1H-индол-3-илиден)пиридин-2-карбоксимидогидразида 3 (172 мг, 0,5 ммоль) в 1,2-дихлорбензоле (15 мл) добавили 2,5-норборнадиен (0.253 мл, 2.5 ммоль). Полученную смесь перемешивали в автоклаве в атмосфере аргона при 215°С в течение 20 ч, затем растворитель удалили при пониженном давлении. Продукт реакции выделили методом колоночной хроматографии (силикагель, элюент - 1,2-дихлорметан:этилацетат (9:1)). Выход 136 мг (0.42 ммоль, 84%). ЯМР 1Н (400 МГц, CDCl3) δ 7.14 7.24 (м, 1H), 7.31-7.39 (м, 1H), 7.64 (d, J=1.1 Гц, 1H, Н-3), 7.82 -7.94 (м, 1H), 8.03 (d, J=7.7 Гц, 1H, Н-4), 8.37-8.54 (м, 3Н), 8.72-8.78 (м, 1H), 8.90 (с, 1H, NH). ЯМР 13С (101 МГц, CDCl3) δ 104.5, 114.1, 116.8, 120.1, 121.3, 121.4, 122.5, 123.6, 129.2, 129.7, 136.9, 137.9, 149.3, 151.3, 153.8, 156.5. ESI-MS, m/z: расч. 324.01, найдено 324.01 (М+Н)+.
Синтез 4-(2-(пиридин-2-ил)-9H-пиридо[2,3-b]индол-8-ил)анилина 1
Смесь 8-бром-2-(пиридин-2-ил)-9H-пиридо[2,3-b]индола 4 (100 мг, 0,3 ммоль), 4-аминофенил борной кислоты (109 мг, 0,5 ммоль), Pd(PPh3)2Cl2 (0,009 ммоль), трифенил-фосфина (0,015 ммоль), 1,4-диоксана (15 мл), этанола (10 мл) и раствора K2CO3 (3 ммоль) в воде (15 мл) перемешивали при 90°С в течение 15 ч в атмосфере аргона. После завершения (ТСХ) органическую фазу промывали водными растворами КОН и хлорида аммония, сушили безводным сульфатом натрия. Растворители удаляли при пониженном давлении. Продукт реакции выделяли методом колоночной хроматографии (силикагель, элюент - 1,2-дихлорметан:этилацетат (9:1)). Аналитические образцы получали перекристаллизацией из этанола. Выход 64 мг (0.19 ммоль, 63%). ЯМР 1Н (400 МГц, CDCl3) δ 3.85 (уш.с, 2Н, NH2), 6.84 - 6.96 (м, 2Н, C6H4NH2), 7.31-7.43 (м, 2Н, Н-5' (Ру), CHarom), 7.43-7.57 (м, 3Н, C6H4NH2, CHarom), 7.77-7.91 (м, 1H, Н-4' (Ру)), 7.98-8.11 (м, 1Н, CHarom), 8.35 (д, J=8.1 Hz, 1Н, Н-3), 8.40-8.45 (м, 1H, Н-3' (Ру)), 8.49 (д, J=8.1 Hz, 1H, Н-4), 8.69-8.79 (м, 1H, Н-6 (Ру)), 8.86 (уш.с, 1H, NH). ЯМР 13С (151 МГц, DMSO-d6) δ 112.8, 114.7, 116.5, 119.4, 120.8, 120.9, 121.6, 124.2, 125.7, 126.8, 126.8, 129.4, 129.6, 137.3, 137.6, 148.8, 149.7, 152.5, 152.7, 156.6. ESI-MS, m/z: расч. 337.14, найдено 337.14 (М+Н)+. Расч. C22H16N4: С 78.55, Н 4.79, N 16.66. Найдено: С 78.49, Н 4.71, N 16.60.
Заявляемое соединение представляет собой бесцветное порошкообразное вещество, умеренно растворимое в органических растворителях, нерастворимое в воде.
4.2. Подтверждение флуорофорных свойств пробы 1
4.2.1. Флуоресцентные свойства соединения 1
Исследованы спектрально-абсорбционные и спектрально-люминесцентные свойства полученного пробы 1 в растворе толуола и ацетонитрила при 296 К. Электронные спектры поглощения регистрировали с использованием стандартной программы Shimadzu Scan на двулучевом спектрофотометре UV-2600 ("Shimadzu", Япония) в диапазоне 190 700 нм с точностью установки длины волны ±0,1 нм. Флуорофор характеризуется высокой поглощательной способностью: наибольшее поглощение с молярным коэффициентом экстинкции 26900 М-1 cm-1 наблюдалось при λabsmax=330 нм (Табл. 1). Спектры возбуждения и излучения измеряли на спектрофлуориметре Horiba FluoroMax-4, в качестве импульсного источника возбуждения которого использовалась ксеноновая лампа, с точностью установки длины волны ±0.5 нм. Установлено, что максимум флуоресценции соединения при возбуждении излучением с длиной волны 322 нм, находится при 536 нм (Табл. 1). Высокое значение Стоксова сдвига (<100 нм), а также батохромный сдвиг спектра эмиссии (λemmax=596 нм) и существенное снижение квантового выхода в высокополярном растворителе (PLQY ~2% в ацетонитриле) свидетельствуют о наличии внутримолекулярного переноса заряда (ICT).
Процедуры измерения абсолютного квантового выхода и времени жизни возбужденного состояния флуорофора 1. Для исследования были использованы растворители уровня очистки HPLC. Флуорофор 1 был очищен колоночной хроматографией. Для измерений применялись фирменные стандартные четырехоконные кварцевые кюветы SUPRASIL 111-QS 10 ("Hellma", Германия) объемом 4 мл, длиной оптического пути 1 см.
Измерение абсолютного квантового выхода флуорофора 1 проводилось в ацетонитриле и толуоле при 296 К с использованием спектрофлуориметра Horiba-Fluoromax-4 в интегрирующей сфере Quanta-Phi, покрытой изнутри материалом Spectralon® после калибровки монохроматора возбуждения. С целью избежать эффекта внутреннего фильтра и/или самотушения для хемосенсора измерялся спектр поглощения, чтобы выбрать длину волны возбуждения, где оптическая плотность меньше 0,1. Далее регистрировались спектры эмиссии и рэлеевского рассеяния чистого растворителя и раствора хемосенсора. Абсолютное значение квантового выхода фотолюминесценции рассчитывали с использованием стандартной программы Origin на спектрофлуориметре Horiba-Fluoromax-4.
Измерение времени жизни возбужденного состояния флуорофора 1 проводилось в ацетонитриле при 296 К с использованием однофотонного возбуждения (time-correlated single-photon counting, TCSPC) с наносекундным светодиодом (310 нм) на спектрофлуориметре Horiba-Fluoromax-4. С целью избежать эффекта внутреннего фильтра и/или самотушения для хемосенсора измерялся спектр поглощения, чтобы выбрать длину волны возбуждения, где оптическая плотность меньше 0,1. Для измерения времени жизни возбужденного состояния использовалось не менее 3-х параллелей с усреднением результатов, χ2≤1,2. Значение времени жизни рассчитывали с использованием специальной программы DataStation на спектрофлуориметре Horiba-Fluoromax-4.
Опираясь на данные таблицы 1, а именно, высокое значение Стоксова сдвига (<100 нм), долгоживущую эмиссию (≤2 нс), а также наличие внутримолекулярного переноса заряда (ICT) с фотолюминесцентным квантовым выходом в толуоле 62% и ацетонитриле 2%, характеризуют соединение 1 как весьма эффективный флуорофор.
4.4. Подтверждение работоспособности сенсора 1 при покраске живых клеток
Исследование проводилось на клетках культуры Vero (клетки эпителия почки зеленой мартышки) полученных из российской коллекции клеточных культур института цитологии РАН. Клетки поддерживаются в питательной среде ДМЕМ (BioinnLabs, Russia) с добавлением 10% FBS (Biolot, Russia) в инкубаторе при температуре 37°С и атмосфере, содержащей 5% углекислого газа. Перед проведением экспериментов клетки были протестированы на отсутствие микоплазмы. Для окраски соединением 1 клетки разводили до концентрации 104 клеток/мл и переносили в чашки со стеклянным дном (Jet Biofil., Китай), где их культивировали в течение 24 часов. Затем меняли питательную среду и добавляли раствор вещества в ДМСО (в концентрации 14 ммоль/л) в количестве 50 мкл на 1 мл питательной среды.
Процедура микроскопического исследования
Микроскопическое исследование проводилось с использованием оборудования Совместного научно-исследовательского центра научного оборудования Уральского филиала РАН. После окрашивания и промывания живые клетки были исследованы с помощью конфокального лазерного сканирующего микроскопа LSM-710; Carl Zeiss имеет многоканальный детектор QUASAR (34 канала). Изображения были получены с помощью погружной линзы 40х/1.3 Oil. Клетки исследовались при помощи иммерсионного 40х объектива. Предварительно настраивался фокус при помощи 633 нм лазера, чтобы минимально воздействовать на клетки, далее снимались лямбда (полноспектральные) изображения от других лазеров. Исследования проводились при возбуждении лазером с длиной волны 405 нм, и излучение было зарегистрировано во всем диапазоне конфокального микроскопа (400-750 нм). Фоновая флуоресценция клеток в лямбда-режиме (при возбуждении лазером с длиной волны 405 нм) была ранее удалена, после чего водный раствор ацетата цинка (с=132 ммоль/л) добавляли в питательную среду и аккуратно смешивали.
Относительная интенсивность флуоресценции образца была определена на основе максимальной, полученной на основе изображения в лямбда-режиме. Для этого спектр интенсивности определяли в десяти точках изображения, усредняли максимальное значение и вычисляли доверительные интервалы. Так как изображения были сделаны в разных настройках, значение было скорректировано с учетом мощности лазера и высоты конфокального разреза. Изображения обрабатывались с помощью LSM Image Browser, ImageJ и GIMP.
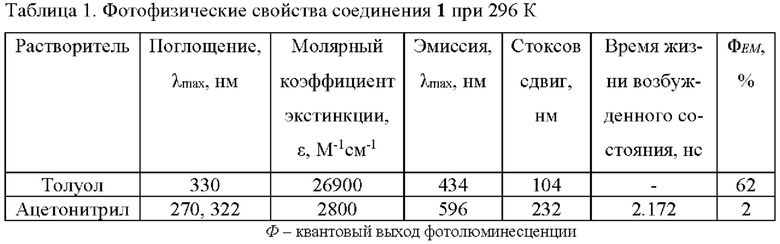
Исследована способность пробы 1 окрашивать клетки культуры Vero. Флуоресцентное изображение клеток Vero после добавления вещества 1, представлены на Фиг. 1. Флуоресцентная микроскопия клеток, окрашенных веществом 1 (лямбда режим). Отдельно представлены изображения, полученные при возбуждении (а) лазером 405 нм, (б) лазером 458 нм, (в) лазером 488 нм, (г) лазером 514 нм и (д) лазером 561 нм. На изображении (а) видны яркие вкрапления, предположительно соответствующие липидным дроплетам. На изображении (д) видно накопление красителя в ядрах и небольшое усиление флуоресценции в некоторых частях ядра, предположительно соответствующее ядрышкам.
1. При возбуждении длиной волны 405 нм соединение 1 флуоресцирует в липидных дроплетах и слегка в цитоплазме (возможно ЭПР). При возбуждении лазерами 458, 488 и 514 нм флуоресценция незначительна, что затрудняет определение части клетки, соответствующего свечению. При возбуждении того же образца лазером 561 нм наблюдается флуоресценция в ядре клетки. При этом чуть ярче флуоресценция в ядрышке.
2. Сравнение спектров испускания, полученных в ходе изучения культуры, окрашенной соединением 1, показывает существенный батохромный сдвиг. При облучении лазером 405 нм максимум испускания в липидных дроплетах 475 нм. Флуоресценции в ядре при возбуждении лазером 561 нм соответствует максимум испускания 580 нм. При этом интенсивность флуоресценции в последнем случае выше примерно в три раза. Возможной причиной является связывание с ДНК. Диаграмма сравнения спектров испускания от разных длин волн возбуждения приведена на Фиг. 2.
Таким образом, соединение 1 можно использовать в качестве метки/пробы для обнаружения и/или наблюдения за метаболическими процессами, протекающими в ядре и/или ядрышке живой клетки. При этом благодаря формированию комплексов с ДНК вещество 1 может быть использовано одновременно для выявления липидных дроплет (возбуждение при 405 нм), так и для ядра и/или ядрышка (возбуждение при 561 нм).
| название | год | авторы | номер документа |
|---|---|---|---|
| 6,7-ДИФТОР-2-(ПИРИДИН-2-ИЛ)-9H-ПИРИДО[2,3-b]ИНДОЛ - ЛЮМИНЕСЦЕНТНЫЙ ХИМИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ 2,4,6-ТРИНИТРОФЕНОЛА (ПИКРИНОВОЙ КИСЛОТЫ) | 2023 |
|
RU2828883C1 |
| 1-(4-(4-МЕТОКСИФЕНИЛ)-[2,2'-БИПИРИДИН]-6-ИЛ)-N,N-БИС(ПИРИДИН-2-ИЛМЕТИЛ)МЕТАНАМИН - МОНОМОЛЕКУЛЯРНЫЙ ХИМИЧЕСКИЙ СЕНСОР ДЛЯ ФЛУОРЕСЦЕНТНОГО ОПРЕДЕЛЕНИЯ КАТИОНОВ Zn IN VITRO | 2023 |
|
RU2822106C1 |
| ПРИМЕНЕНИЕ 2-МЕТИЛ-3-(6-(ТИОФЕН-2-ИЛ)-3-(4-ТОЛИЛ)ПИРИДИН-2-ИЛ)-1Н-ИНДОЛА В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНОГО ХИМИЧЕСКОГО СЕНСОРА ДЛЯ ОБНАРУЖЕНИЯ 2,4,6-ТРИНИТРОФЕНОЛА | 2023 |
|
RU2829733C1 |
| ДИМЕТИЛ 4-ФЕНИЛ-5-(2-ФЕНИЛ-1H-ИНДОЛ-3-ИЛ)-1-(4-ТОЛИЛ)-1H-ПИРРОЛ-2,3-ДИКАРБОКСИЛАТ - ОПТИЧЕСКИЙ ХИМИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ НИТРОАРОМАТИЧЕСКИХ ВЗРЫВЧАТЫХ ВЕЩЕСТВ | 2023 |
|
RU2820149C1 |
| N-([1,1'-БИФЕНИЛ]-3-ИЛ)-4-ФЕНИЛ-1-(ПИРИДИН-2-ИЛ)-6,7-ДИГИДРО-5H-ЦИКЛОПЕНТА[C]ПИРИДИН-3-АМИН - МОНОМОЛЕКУЛЯРНЫЙ ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ НИТРОАРОМАТИЧЕСКИХ ВЗРЫВЧАТЫХ ВЕЩЕСТВ | 2022 |
|
RU2786741C1 |
| 5-ФЕНИЛ-5""-п-ТОЛИЛ-2,2":6",2""-ТЕРПИРИДИН - ХЕМОСЕНСОР ДЛЯ ФЛУОРЕСЦЕНТНОГО ОПРЕДЕЛЕНИЯ КАТИОНОВ Zn В ВОДНЫХ И ПИЩЕВЫХ ОБРАЗЦАХ | 2021 |
|
RU2773238C1 |
| ((2-(5,6-БИС(4-ФТОРФЕНИЛ)-1,2,4-ТРИАЗИН-3-ИЛ)ХИНОЛИН)БИС(2-ФЕНИЛПИРИДИН))ИРИДИЙ(III) ХЛОРИД - КЛЕТОЧНЫЙ ФЛУОРЕСЦЕНТНЫЙ КРАСИТЕЛЬ | 2024 |
|
RU2837462C1 |
| 2-(4-МЕТОКСИФЕНИЛ)-5-(4-(4-(ПИРЕН-1-ИЛ)-1H-1,2,3-ТРИАЗОЛ-1-ИЛ)ФЕНИЛ)-1,3,4-ОКСАДИАЗОЛ-МОНОМОЛЕКУЛЯРНЫЙ ХИМИЧЕСКИЙ СЕНСОР НА НИТРОАЛИФАТИЧЕСКОЕ ВЗРЫВЧАТОЕ ВЕЩЕСТВО ТЕТРАНИТРОПЕНТАЭРИТРИТ | 2023 |
|
RU2820003C1 |
| ХИМИЧЕСКИЙ СЕНСОР ДЛЯ ОПРЕДЕЛЕНИЯ НИТРОАРОМАТИЧЕСКИХ ВЗРЫВЧАТЫХ ВЕЩЕСТВ (ВВ) - 10-(4,5-ДИ-p-ТОЛИЛ-1H-1,2,3-ТРИАЗОЛ-1-ИЛ)-2,3-ДИМЕТОКСИ-ПИРИДО[1,2-a]ИНДОЛ | 2020 |
|
RU2756790C1 |
| (ЭТАН-1,2-ДИИЛБИС(ОКСИ))БИС(ЭТАН-2,1-ДИИЛ)БИС(ПИРЕН-1-КАРБОКСИЛАТ) - МОНОМОЛЕКУЛЯРНЫЙ ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ОБНАРУЖЕНИЯ НИТРОАРОМАТИЧЕСКИХ ВЗРЫВЧАТЫХ ВЕЩЕСТВ | 2022 |
|
RU2812671C1 |
Изобретение относится к люминесцентным соединениям. Раскрыт 4-(2-(пиридин-2-ил)-9H-пиридо[2,3-b]индол-8-ил)анилин – клеточный флуоресцентный краситель. Изобретение обеспечивает возможность биовизуализации ядер живых клеток. 1 табл., 2 ил.
4-(2-(Пиридин-2-ил)-9H-пиридо[2,3-b]индол-8-ил)анилин - клеточный флуоресцентный краситель
| BELLAMRI M | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| YI S | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2025-03-21—Публикация
2024-10-02—Подача