Изобретение относится к области медицины, в частности к клинической онкологии, медицинской генетике, молекулярной диагностике, и может быть использовано для прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы.
Рак молочной железы (РМЖ) - злокачественная опухоль, исходящая из эпителия ткани молочной железы [Злокачественные новообразования в России в 2017 году (заболеваемость и смертность). / Под ред. Каприна А.Д., Старинского В.В., Петровой Г.В. - М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2018. - 250 с. [Zlokachestvennye novoobrazovaniya v Rossii v 2017 godu (zabolevaemost’ i smertnost’). Ed by Kaprin A.D., Starinsky V.V., Petrovа G.V. Moscow: MNIOI im. P. A. Herzen, branch of FSBI «NMITS radiology» of the Ministry of health of Russia; 2018. 250 p. (In Russ)].
Исследования, посвящённые этиопатогенезу РМЖ многочисленны, однако при этом не существует единой теории возникновения и развития заболевания. Реализация злокачественного фенотипа становится возможной благодаря взаимодействию различных генетических и эпигенетических нарушений, эндокринных стимулов, а также внешне-средовых воздействий в присутствии факторов риска [Łukasiewicz S, Czeczelewski M, Forma A, Baj J, Sitarz R, Stanisławek A. Breast Cancer-Epidemiology, Risk Factors, Classification, Prognostic Markers, and Current Treatment Strategies-An Updated Review. Cancers (Basel). 2021 Aug 25;13(17):4287. doi: 10.3390/cancers13174287. PMID: 34503097; PMCID: PMC8428369].
Согласно данным Cancer Research UK. Risk factors for breast cancer (2020) [Cancer Research UK. Risk factors for breast cancer. URL: https://www.cancerresearchuk.org/about-cancer/breast-cancer/risks-causes/risk-factors (дата обращения: 02.07.2022)], выделяют более 20 факторов возникновения и развития РМЖ, большинство из которых включены в современные модели расчёта рисков изучаемого заболевания (Gail, Tyrer-Cusick, Rosner Colditz BCRAT, BCPRO, and BOADICEA) [Olsson HL and Olsson ML (2020) The Menstrual Cycle and Risk of Breast Cancer: A Review. Front. Oncol. 10:21. doi: 10.3389/fonc.2020.00021].
Большинство авторов считает, что вне зависимости от конечного фенотипа и рецепторного статуса злокачественное новообразование молочной железы, начальные этапы канцерогенеза ключевым образом зависят от действия эстрогенов и прогестерона. Очевидным фактором риска является женский пол, при этом заболеваемость раком грудной железы среди мужчин составляет менее 2% от общего количества заболевших [Hilton, Heidi N.; Clarke, Christine L.; Graham, J. Dinny (2017). Estrogen and progesterone signalling in the normal breast and its implications for cancer development. Molecular and Cellular Endocrinology, (), S0303720717304331-. doi:10.1016/j.mce.2017.08.011].
В виду того, что РМЖ является гетерогенным заболеванием, имеющим несколько патогенетических разновидностей, их биологическое поведение зависит от рецепторного статуса опухоли и активации определённых сигнальных путей различными стимулами [Имянитов Е.Н. Скрининг для лиц с наследственной предрасположенностью к раку / Е.Н. Имянитов // Практическая онкология.- 2010.- т. 11, № 2.- С. 102-109].
Ключевую роль в канцерогенезе играет микроокружение опухоли: экстрацеллюлярный матрикс (ЭЦM), стромальные клетки (эндотелиальные и иммунные), фибробласты и адипоциты. Основными ферментами, регулирующими состояние ЭЦM, являются матриксные металлопротеиназы (ММРs) и их тканевые ингибиторы (TIMP) [203. Zajkowska M, Gacuta E, Kozłowska S, Lubowicka E,  EK, Chrostek L, Szmitkowski M, Pawłowski P, Zbucka-Krętowska M, Ławicki S. Diagnostic power of VEGF, MMP-9 and TIMP-1 in patients with breast cancer. A multivariate statistical analysis with ROC curve. Adv Med Sci. 2019 Mar;64(1):1-8. doi: 10.1016/j.advms.2018.07.002. Epub 2018 Sep 15. PMID: 30227310].
EK, Chrostek L, Szmitkowski M, Pawłowski P, Zbucka-Krętowska M, Ławicki S. Diagnostic power of VEGF, MMP-9 and TIMP-1 in patients with breast cancer. A multivariate statistical analysis with ROC curve. Adv Med Sci. 2019 Mar;64(1):1-8. doi: 10.1016/j.advms.2018.07.002. Epub 2018 Sep 15. PMID: 30227310].
Проведённые зарубежные исследования показали значимую роль MMPs в канцерогенезе при РМЖ [Association of matrix metalloproteinases 3 and 9 single nucleotide polymorphisms with breast cancer risk: A case control study / F.A. Ibrahim, S.E. Elfeky, M. Haroun [et al.] // Mol Clin Oncol.-2020.-N.13.-P.54-62.; Kaczorowska, A. Selected Matrix Metalloproteinases (MMP-2, MMP-7) and Their Inhibitor (TIMP-2) in Adult and Pediatric Cancer / A. Kaczorowska, N. Miękus, J. Stefanowicz [et al.] // Diagnostics (Basel).-2020.-V.10.-N.8.-P.547. doi: 10.3390/diagnostics10080547]. Показано, что дисбаланс матриксных металлопротеиназ вызывает повреждение ДНК и нестабильность генома, при этом MMPs формируют опухолевое микроокружение, открывая пути для ангиогенеза, а также воздействуя на фибробласты стромы и адипоциты, формируя условия для эпителиально-мезенхимального перехода [Candido S., Abrams S.L., Steelman L.S., Lertpiriyapong K., Fitzgerald T.L., Martelli A.M., Cocco L., Montalto G., Cervello M., Polesel J., et al. Roles of ngal and MMP-9 in the tumor microenvironment and sensitivity to targeted therapy. Biochim. Biophys. Acta. 2016;1863:438-448].
Семейство ММРs (матриксинов) представляет собой пул эндопептидаз, содержащих ионы Zn2+- и Ca2+ в своих активных сайтах. Наиболее значимые представители из них это коллагеназы, не обладающие специфичностью (например, ММР 1,8,13), желатиназы, или специфические коллагеназы коллагена 4-го типа (ММР 2 и 9), стромелизины (например, ММР 3 и 10), матрилизины (ММР 7, ММР 26) и особый тип ММР - мембранный (MMP 14, 15,16, 24) [Conlon GA, Murray GI. Recent advances in understanding the roles of matrix metalloproteinases in tumour invasion and metastasis. J Pathol. 2019 Apr;247(5):629-640. doi: 10.1002/path.5225. Epub 2019 Feb 15. PMID: 30582157].
В отдельных исследованиях показаны ассоциации с развитием РМЖ полиморфизма генов матриксных металлопротеиназ. Однако, следует отметить, что подавляющее большинство этих исследований выполнено зарубежными учеными, тогда как в Российской Федерации подобные исследования единичны. Также, следует отметить, что полученные в разных популяциях результаты нередко отличаются между собой, что может быть обусловлено как этиопатогенетическими особенностями возникновения и течения РМЖ у индивидуумов из различных этнотерриториальных групп народонаселения, так и разным дизайном исследований.
Одной из важных задач современной онкологии является изучение причин и механизмов развития 3 степени злокачественности опухолевых клеток при раке молочной железы, среди которых значимую роль играют генетические факторы.
В Российской Федерации исследования вовлеченности гена ММР-9 в формирование предрасположенности к 3 степени злокачественности опухолевых клеток при раке молочной железы фрагментарны, а данные о роли генетических вариантов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9 в развитии 3 степени злокачественности опухолевых клеток при раке молочной железы отсутствуют.
Для оценки сложившейся патентной ситуации был выполнен поиск по охранным документам за период с 1990 по 2022 гг. Анализ документов производился по направлению: способ прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы на основе молекулярно-генетических данных в зависимости от полиморфных маркеров гена ММР-9. Источники информации: сайты Федерального института промышленной собственности http://fips.ru.
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9.
Известен патент RU №2741232 (опубл. 22.01.2022) Способ прогнозирования прогрессирования рака молочной железы, включающий определение в периферической крови промежуточного метаболита витамина D 25(OH)D. При значении его содержания в сыворотке крови ≤ 18,9 нг/мл прогнозируют прогрессирование заболевания. Способ обеспечивает повышение точности прогнозирования прогрессирования рака молочной железы за счет определения промежуточного метаболита витамина D 25(OH)D в венозной крови, проявляющееся в снижении показателя промежуточного метаболита витамина D 25(OH)D, предшествующем прогрессированию заболевания. Недостатком этого способа является трудоемкость выполнения и кроме того не учитывается роль генетических полиморфизмов.
Известен патент RU 2336822 (опубл. 27.08.2008) Способ прогнозирования прогрессирования рака молочной железы, включающий исследование крови пациента. Дополнительно при обследовании определяют показатели: возраст, социальный статус, сопутствующие заболевания, количество моноцитов крови, скорость оседания эритроцитов (СОЭ), общий билирубин крови, креатинин крови, удельный вес мочи, реакцию мочи. Затем определяют прогностический коэффициент (ПК) для каждого показателя. В системе возраст при маркере до 20 лет устанавливают ПК равным (0), при маркере 20-29 лет - равным (-10), при маркере 30-39 лет - равным (-7), при маркере 40-49 лет - равным (+4), при маркере 50-59 лет - равным (+3), при маркере 60-69 лет - равным (+2), при маркере 70-79 лет - равным (+4), при маркере 80 и более лет - равным (-3). В системе социальный статус при маркере рабочие устанавливают ПК равным (+4), при маркере служащие - равным (-1), при маркере учащиеся - равным (0), при маркере безработные - равным (-12), при маркере пенсионеры и инвалиды труда (ИТР) - равным (+1). В системе сопутствующие заболевания при маркере заболевания желудочно-кишечного тракта (ЖКТ) устанавливают ПК равным (-10), при маркере заболевания сердечно-сосудистой системы - равным (+2), при маркере заболевания эндокринной системы - равным (+1,5), при маркере заболевания дыхательной системы - равным (0), при маркере заболевания опорно-двигательного аппарата - равным (0), при маркере заболевания мочеполовой системы - равным (-13), при маркере сочетание сопутствующий заболеваний - равным (-1), при маркере отсутствие сопутствующих заболеваний - равным (+2). В системе моноциты крови при маркере нет устанавливают ПК равным (0), при маркере 1-3% - равным (-2,5), при маркере 4-6% - равным (+2), при маркере 7-10% - равным (+2,5), при маркере более 10% - равным (0). В системе скорость оседания эритроцитов при маркере - 1-10 мм/ч устанавливают ПК равным (-1), при маркере 11-20 мм/ч - равным (-3), при маркере 21-30 мм/ч - равным (+7), при маркере 31-40 мм/ч - равным (0), при маркере более 40 мм/ч - равным (0). В системе общий билирубин при маркере менее 8,8 мкмоль/л устанавливают ПК равным (0), при маркере 8,8-17 мкмоль/л - равным (-1), при маркере более 17 мкмоль/л - равным (+5,5). В системе креатинин при маркере менее 0,07 ммоль/л устанавливают ПК равным (+11), при маркере 0,07-0,17 - равным (-3), при маркере более 0,17 мкмоль/л - равным (0). В системе удельный вес мочи при маркере менее 1008 устанавливают ПК равным (0), при маркере 1008-1026 - равным (+2), при маркере более 1026 - равным (+6). В системе реакция мочи при маркере кислая, устанавливают ПК равным (+3), при маркере нейтральная - равным (-3), при маркере щелочная - равным (-12). При сумме ПК от (-54,5) до (-21,5) прогнозируют низкую вероятность рака молочной железы, при сумме от (+11) до (+44,5) прогнозируют высокую вероятность рака молочной железы. Однако прогнозирование таким способом рака молочной железы спряжено с профилактическими осмотрами, при этом диспансеризация лиц из групп повышенного риска должна проводиться длительное время вплоть до возраста 55 лет.
Известен патент RU 2263319 (опубл. 27.10.2005) Способ доклинической диагностики рецидива рака молочной железы, включающий биохимическое исследование биологической жидкости пациента, отличающийся тем, что у менопаузальных женщин после комплексного лечения рака молочной железы в динамике определяют концентрацию эстриола, эстрона и эстрадиола в моче, вычисляют соотношение эстриола к эстрону и эстрадиолу и при значении его 1,68±0,23 констатируют отсутствие рецидива, а при его снижении до значений 0,74±0,12 у пациенток, проживающих без рецидива менее 1 года, до 0,65±0,13 у пациенток, проживших без рецидива от 2 до 6 лет, и до 0,50±0,10 у пациенток, проживших без рецидива от 6 до 10 лет, констатируют развитие рецидива. Недостатком данного способа является высокая стоимость анализа, что особенно важно при его многократном повторении в ходе наблюдения за больными после комплексного лечения.
Патент RU №2522501 (опубл. 20.07.2014), в котором описан способ прогнозирования наследственной предрасположенности к раку молочной железы. Сущность способа заключается в том, что проводят амплификацию коротких фрагментов гена BLM протяженностью до 200 п.о., с последующим высокоразрешающим плавлением, включающим оптимизированный для гена BLM этап формирования гетеродуплексов: быстрый нагрев до 95°С и медленное снижение температуры до 50°С; выбирают один фрагмент с аберрантным профилем плавления для секвенирования, секвенируют выбранный фрагмент и при выявлении мутации гена BLM прогнозируют наследственную предрасположенность к раку молочной железы. Недостатком этого способа является его трудоемкость, он не учитывает роль генетических полиморфизмов.
Известен патент RU 2204836 (опубл. 20.05.2003) Способ прогнозирования генерализации рака молочной железы. В данном способе проводят диагностическое наблюдение больных раком молочной железы. Определяют тромбоцитарную активность МАО-Б в плазме крови, что обеспечивает доклиническое выявление генерализации рака молочной железы. При снижении тромбоцитарной активности МАО-Б в 4-6 раз по отношению к норме прогнозируют генерализацию процесса. Недостатком предлагаемого способа является использование в качестве маркера только одного показателя - тромбоцитарной активности МАО-Б в плазме крови, применение способа в отношении уже больных раком молочной железы, преимущественная информативность предлагаемого показателя тромбоцитарной активности МАО-Б в период генерализации процесса при наличии отдаленных метастазов, что делает невозможным применение способа в ранней диагностике рака молочной железы.
Патент RU №2631940 (опубл. 28.09.2017), в котором описан способ прогнозирования рака молочной железы. Сущность способа заключается в том, что определяют факторы риска: ношение тугого бюстгальтера (Б), возраст (В), перенесенные воспалительные заболевания молочной железы (ЗМЖ), перенесенные заболевания щитовидной железы (ЗЩЖ), индекс массы тела (ИМТ), частое употребление жирной, жареной и копченой пищи (Калл), некормление ребенка грудью (НКГ), кормление ребенка грудью год и более (КГ≥1 год), позднее наступление менструации (ПНМ), длительное проживание в военных городках (ПВО), перенесенные травмы молочной железы (ТМЖ). Отсутствие каждого из указанных факторов оценивают как «0 баллов», а наличие - «1 балл». Показатели ПНМ, В, ИМТ оценивают количественно. Рассчитывают прогностический коэффициент ПК по заявленной формуле. Если значение ПК меньше 0,2197, то прогнозируют низкий риск, а если ПК от 0,2197 и более - высокий риск рака молочной железы. Недостатком способа является сложность расчетов и не учитываются генетические факторы.
Прогнозирование риска рака молочной железы на основе естественных исследований // Зиннатуллина Г.Ф., Бермишева М.А., Кононова В.А., Фарахтдинова А.Р., Хуснутдинова Э.К. // Креативная хирургия и онкология. 2009. №2. URL: https://cyberleninka.ru/article/n/prognozirovanie-vozniknoveniya-riska-raka-molochnoy-zhelezy-na-osnove-geneticheskih-issledovaniy (дата обращения: 24.07.2022), характеризуется проведением анализа распространенности двух вариантов гена NBN (c.657del5 и p.R215W) у больных раком молочной железы в Республике Башкортостан и Ханты-Мансийском автономном округе. Недостатком данного исследования является применение только для коренных жителей Республики Башкортостан и Ханты-Мансийского автономного округа.
Задачей настоящего исследования является расширение арсенала методов диагностики, а именно создание способа прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9.
Технический результат использования изобретения - получение критериев оценки риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы у женщин русской национальности, уроженок Центрально - Черноземного региона РФ, на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9, включающий:
- выделение ДНК из периферической венозной крови;
- анализ полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9;
- прогнозирование высокого риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы, при выявлении гаплотипа CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9.
Новизна и изобретательский уровень заключаются в том, что из уровня техники не известна возможность прогноза развития рака молочной железы у пациенток на основе данных о гаплотипе CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9.
Способ осуществляют следующим образом:
Выделение геномной ДНК из периферической крови осуществляют методом фенольно-хлороформной экстракции (Miller, S. A. A simple salting out procedure for extracting DNA from human nucleated cells / S. A. Miller, D. D. Dykes, H. F. Polesky // Nucleic. Acids. Res. - 1988. - Vol. 16, № 3. - P. 1215) в два этапа. На первом этапе к 4 мл крови с ЭДТА добавляют 25 мл лизирующего буфера, содержащего 320мМ сахарозы, 1% тритон Х-100, 5мМ MgCl2, 10мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4°С, 4000 об./мин. в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН=8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10мг/мл) и инкубируют образец при 37°С в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об./мин. в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. После лиофилизации полученную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -200С.
Анализ полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9 осуществлялся методом полимеразной цепной реакции (ПЦР) на термоциклере CFX-96 Real-Time System (Bio-Rad) c использованием стандартных олигонуклеотидных праймеров и зондов (синтезированы в ООО «Тест - Ген» (Ульяновск)).
Амплификация геномной ДНК производилась в реакционной смеси, суммарным объемом 10 мкл, включающей смесь для ПЦР ММР-9 - 4 мкл, Taq-полимеразу - 2 мкл, исследуемый образец (~30 нг ДНК/мкл) - 1 мкл, деионизированная вода – 3 мкл.
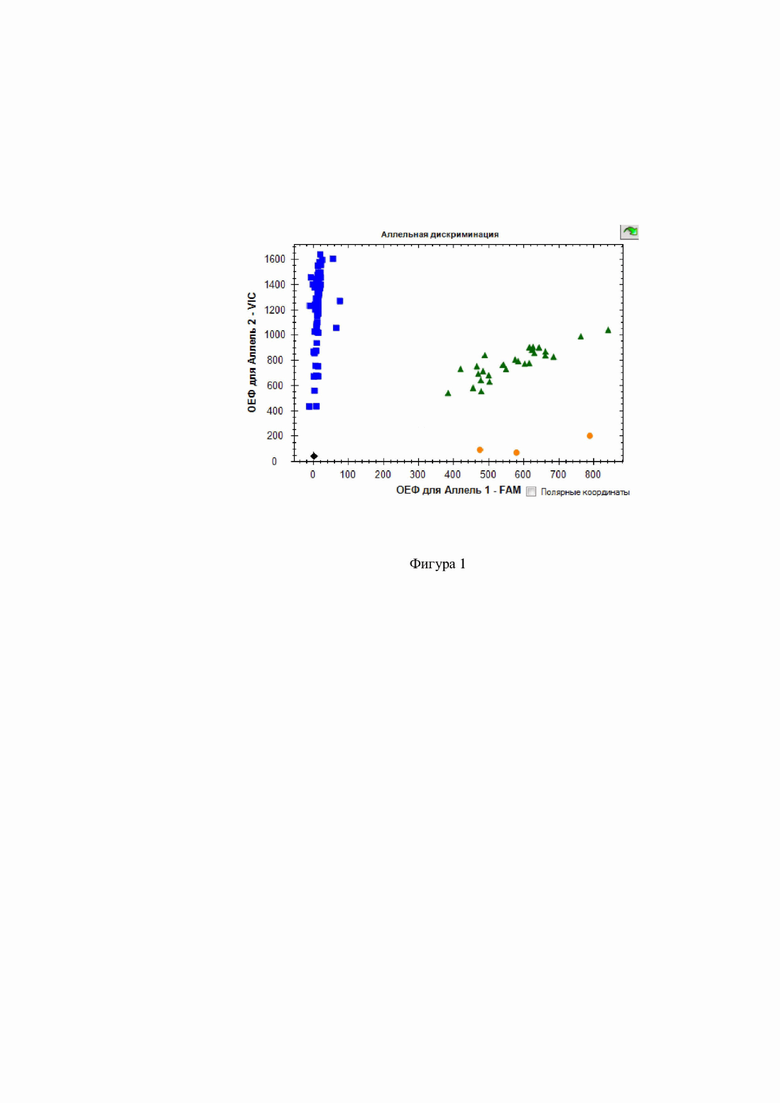
Генотипирование исследуемых образцов осуществлялось с использованием программного обеспечения «CFX-Manager™» методом дискриминации аллелей по величинам относительных единиц флуоресценции (ОЕФ) (фиг. 1, фиг. 2, фиг. 3, фиг. 4, фиг. 5, фиг. 6).
Изобретение характеризуется фигурами:
Фиг. 1. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs3918242 ММР-9 ( - TT,
- TT,  - CC,
- CC,  - CT, ■ - отриц. контр.).
- CT, ■ - отриц. контр.).
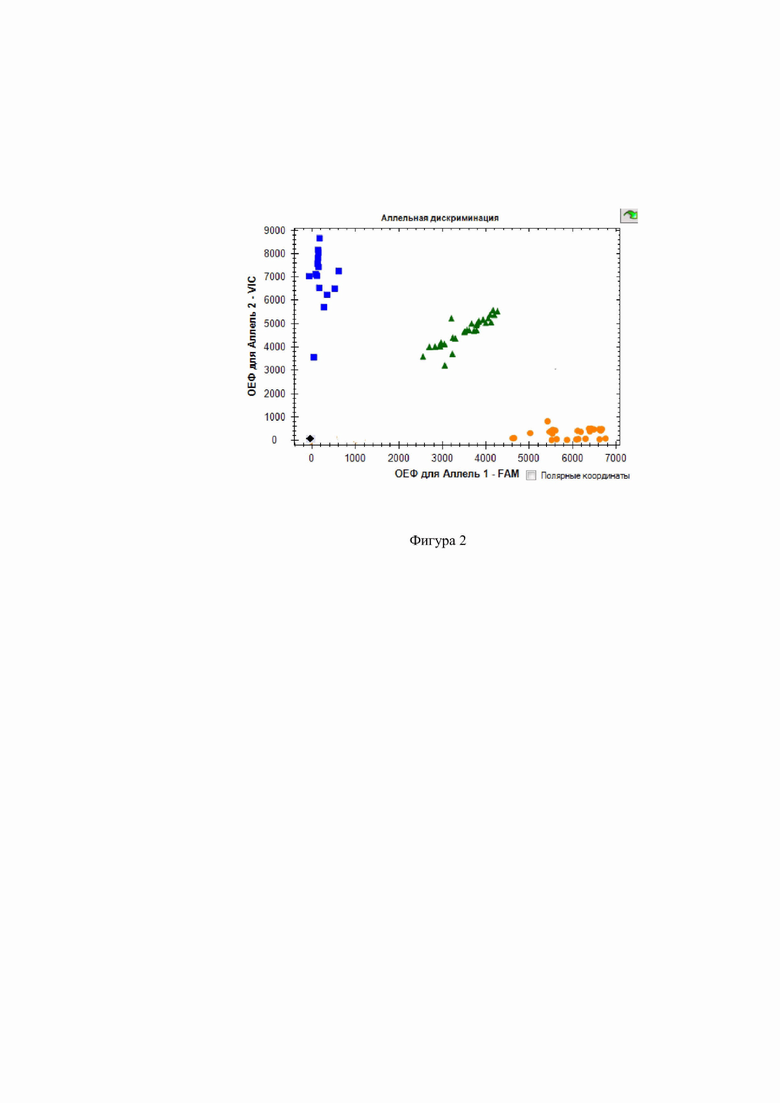
Фиг. 2. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs3918249 ММР-9 ( - TT,
- TT,  - CC,
- CC,  - TC, ■ - отриц. контр.).
- TC, ■ - отриц. контр.).
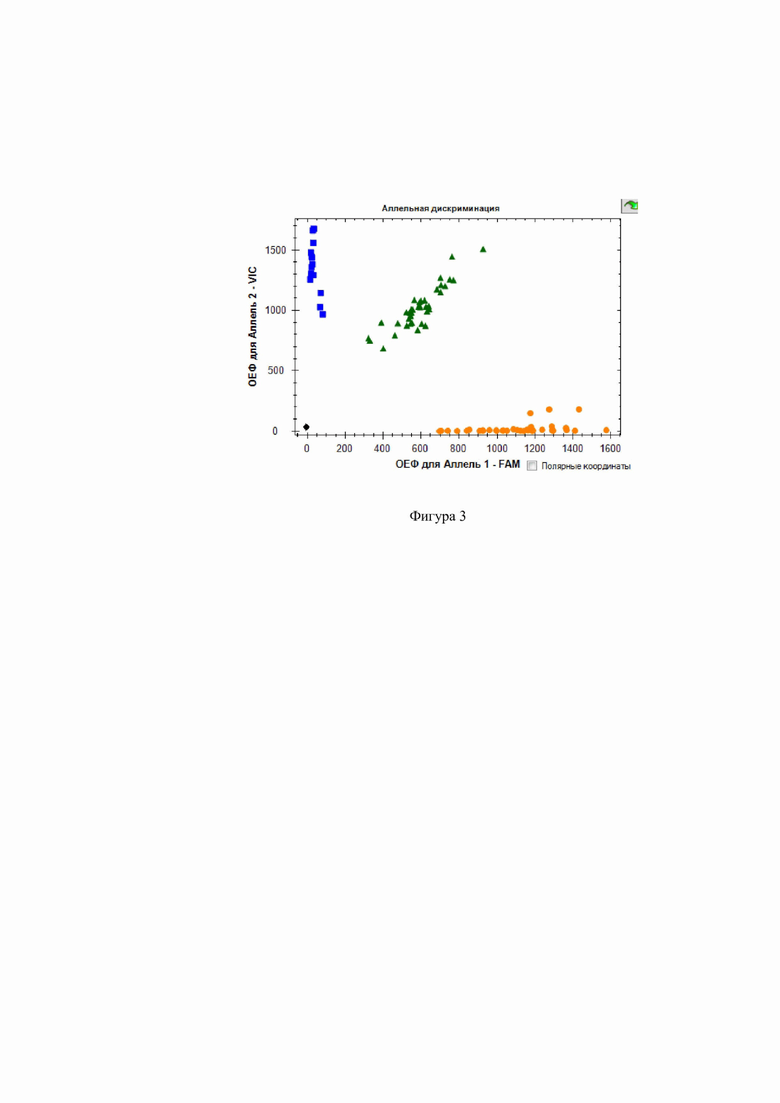
Фиг. 3. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs17576 ММР-9 ( - AA,
- AA,  - GG,
- GG,  - AG, ■ - отриц. контр.).
- AG, ■ - отриц. контр.).
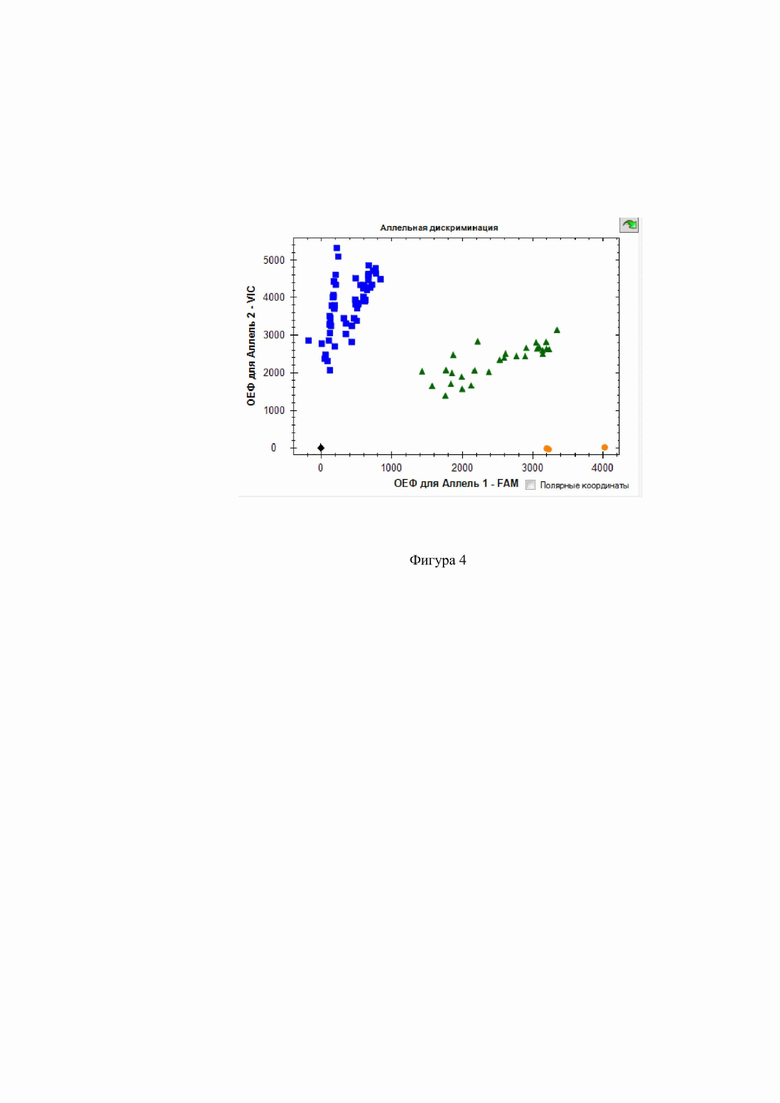
Фиг. 4. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs3787268 ММР-9 ( - AA,
- AA,  - GG,
- GG,  - GA, ■ - отриц. контр.).
- GA, ■ - отриц. контр.).
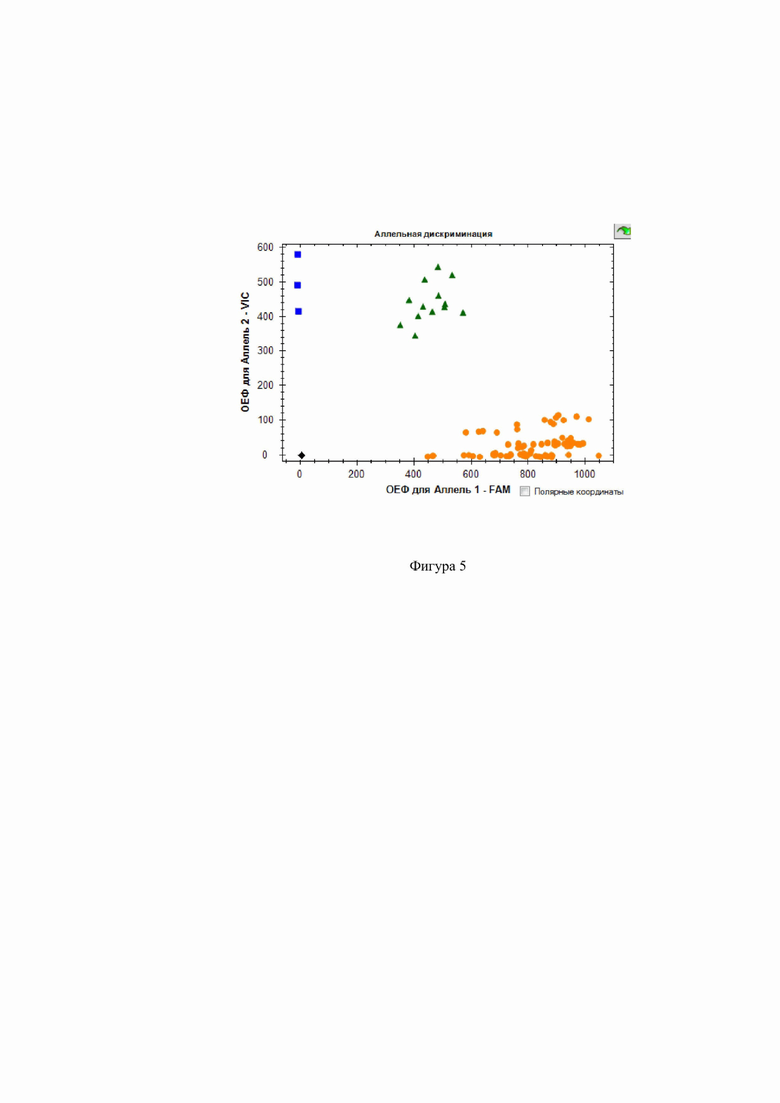
Фиг. 5. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs2250889 ММР-9 ( - CC,
- CC,  - GG,
- GG,  -CG, ■ - отриц. контр.).
-CG, ■ - отриц. контр.).
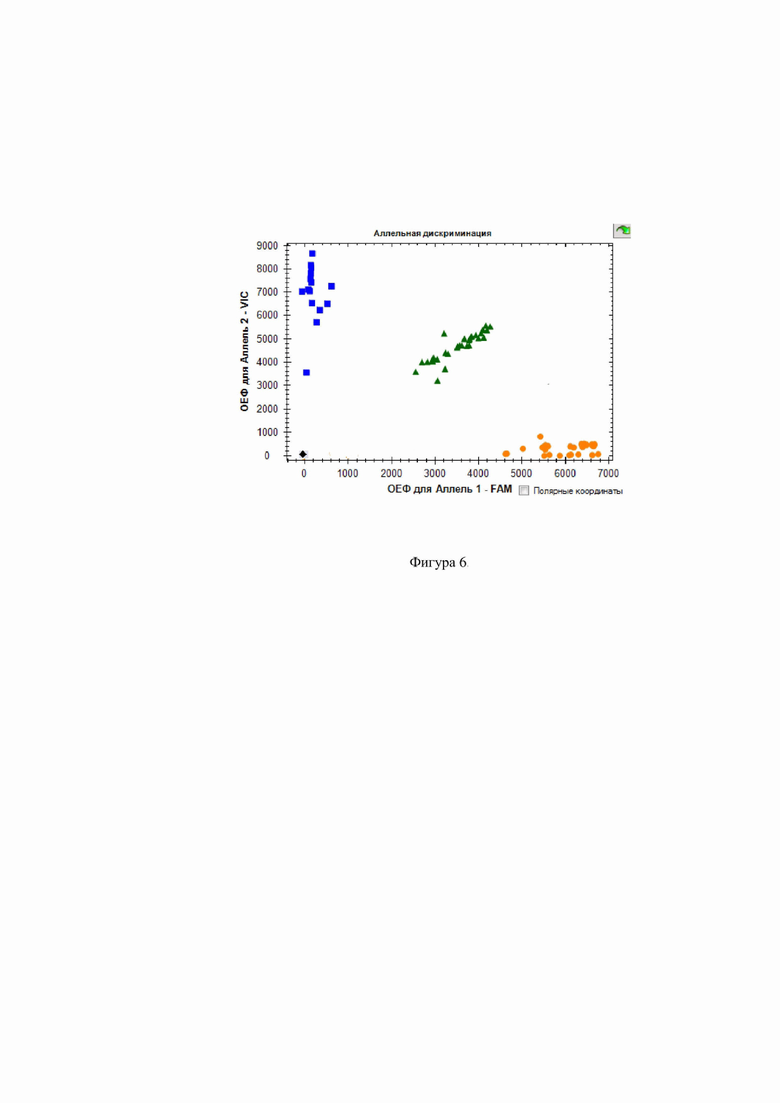
Фиг. 6. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs17577 ММР-9 ( - AA,
- AA,  - GG,
- GG,  - GA, ■ - отриц. контр.).
- GA, ■ - отриц. контр.).
Определение частот гаплотипов и анализ ассоциаций гаплотипов с развитием 3 степени злокачественности опухолевых клеток при раке молочной железы проводилось с помощью логистического регрессионного анализа в программе PLINK v. 2.050 (http://zzz.bwh.harvard.edu/plink/). При необходимости в исследование включали ковариаты (возраст, индекс массы тела). После проведения пермутационного теста (выполнялось 1000 пермутаций) за статистически значимый уровень принимали ррerm<0,05.
Возможность использования предложенного способа для оценки прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы подтверждает анализ результатов наблюдений 860 пациенток, из них 114 больные 3 степенью злокачественности опухолевых клеток при раке молочной железы и 746 женщин контрольной группы. Средний возраст больных составил 54,74±12,73 лет (варьировал от 25 до 84 лет). Возрастные характеристики больных и контроля были сопоставимы. В выборки для исследования включались (критерии включения): 1) пациентки русской национальности, являющиеся уроженками Центрального Черноземья РФ, не имеющие родства между собой и проживающие в Белгородской области (Чурносов М.И., Сорокина И.Н., Балановская Е.В. Генофонд населения Белгородской области. Динамика индекса эндогамии в районных популяциях // Генетика. 2008. Т. 44. № 8. С. 1117-1125), добровольно согласившиеся на проведение исследования; 2) в группу больных включались пациентки только после установления диагноза заболевания РМЖ, подтвержденного с помощью клинических и лабораторно-инструментальных, в т.ч. морфологических методов обследования.
Обследование больных РМЖ проводилось на базе поликлинического и химиотерапевтического отделений Белгородского областного онкологического диспансера; формирование контрольной группы без клинико-анамнестических признаков РМЖ проводилось на базе перинатального центра БОКБ Святителя Иоасафа в ходе проф. осмотров.
Все больные РМЖ и женщины контрольной группы подписали информированное согласие на участие в исследовании, проведение исследования было согласовано с этическим комитетом медицинского института НИУ «БелГУ».
Типирование молекулярно-генетических маркеров осуществлялось на кафедре медико-биологических дисциплин медицинского института НИУ «БелГУ».
При расчете частот гаплотипов и анализе их ассоциаций у пациенток установлена связь с формированием 3 степени злокачественности опухолевых клеток при раке молочной железы гаплотипа CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9. Гаплотип CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9 является фактором риска развития РМЖ 3-ей степени злокачественности (ОR=6,43).
В качестве примеров конкретного применения разработанного способа приведено обследование русских женщин, уроженок Центрально-Черноземного региона РФ и не являющихся родственницами между собой: проведено генетическое исследование по локусам rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9.
У пациентки О. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип СTAGGА полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9, что позволило отнести пациентку в группу женщин с низким риском развития РМЖ. При дальнейшем наблюдение диагноз 3 степени злокачественности опухолевых клеток при раке молочной железы у пациентки О. не подтвердился.
У пациентки Б. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9, что позволило отнести пациента в группу пациенток с повышенным риском развития РМЖ. Дальнейшее наблюдение подтвердило диагноз рака молочной железы 3-ей степени злокачественности у пациентки Б.
У пациентки Л. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип TТGАGА полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9, что позволило отнести пациентку в группу больных с пониженным риском развития РМЖ. Дальнейшее наблюдение не подтвердило диагноз 3 степени злокачественности опухолевых клеток при раке молочной железы у пациентки.
У пациентки К. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9, что позволило отнести пациентку в группу индувидуумов с повышенным риском развития РМЖ. При дальнейшем наблюдение диагноз 3 степени злокачественности опухолевых клеток при раке молочной железы у пациентки К. подтвердился.
Применение данного способа позволит на доклиническом этапе формировать среди пациенток группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития 3 степени злокачественности опухолевых клеток при раке молочной железы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования повышенного риска развития рака молочной железы 1-2 стадий у женщин на основе полиморфизма гена матриксной металлопротеиназы 9 | 2022 |
|
RU2795100C1 |
| Способ прогнозирования риска развития рака молочной железы у женщин с использованием молекулярно-генетических данных | 2022 |
|
RU2795897C1 |
| Способ прогнозирования риска развития люминального подтипа рака молочной железы | 2023 |
|
RU2795720C1 |
| Способ прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы | 2024 |
|
RU2830352C1 |
| Способ прогнозирования риска развития рака молочной железы у женщин без ожирения | 2023 |
|
RU2795726C1 |
| Способ прогнозирования риска развития рака молочной железы у женщин с ожирением | 2022 |
|
RU2795244C1 |
| Способ прогнозирования повышенного риска развития рака молочной железы 3-4 стадий заболевания у женщин | 2024 |
|
RU2830466C1 |
| Способ прогнозирования риска развития тройного негативного подтипа рака молочной железы | 2023 |
|
RU2811257C1 |
| Способ прогнозирования риска развития H. pylori-позитивной язвенной болезни двенадцатиперстной кишки с использованием данных о полиморфизме гена ММР-9 | 2022 |
|
RU2782496C1 |
| Способ прогнозирования риска развития язвенной болезни желудка на основе генетического анализа | 2022 |
|
RU2780505C1 |
Изобретение относится к медицине, а именно к клинической онкологии, медицинской генетике и молекулярной диагностике, и может быть использовано для прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы. Из периферической венозной крови выделяют ДНК. Проводят анализ генетических маркеров гена ММР-9. При выявлении гаплотипа CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9 прогнозируют высокий риск развития 3 степени злокачественности опухолевых клеток при раке молочной железы. Способ обеспечивает получение новых критериев оценки риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы у женщин русской национальности, уроженок Центрально-Черноземного региона РФ, на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9. 6 ил., 4 пр.
Способ прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы, включающий выделение ДНК из периферической венозной крови, анализ генетических маркеров гена ММР-9, и при выявлении гаплотипа CTAACG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889-rs17577 гена ММР-9 прогнозируют высокий риск развития 3 степени злокачественности опухолевых клеток при раке молочной железы.
| RU 2012120249 A, 27.01.2014 | |||
| US 20070218512 A1, 20.09.2007 | |||
| ПАВЛОВА Н.В | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Научные результаты биомедицинских исследований | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| МИРЗОЕВА Д.С | |||
| Степень злокачественности опухоли как | |||
Авторы
Даты
2024-07-23—Публикация
2023-07-14—Подача