Изобретение относится к области медицины, в частности к клинической онкологии, медицинской генетике, молекулярной диагностике, и может быть использовано для прогнозирования риска развития рака молочной железы у женщин с использованием молекулярно-генетических данных.
Рак молочной железы (РМЖ) это опухоль молочной железы злокачественного характера, имеющая эпителиальное происхождение [Gradishar W.J., Anderson B.O., Blair S.L. et al. Breast cancer version 3.2014. J Natl Compr Canc Netw 2014;12(4):542–590]. Согласно данным мировой статистики (материалы Международного агентства по изучению рака) в настоящее время ежегодно среди населения мира выявляется более 2 миллионов новых случаев РМЖ. Среди всех случаев рака (ежегодно в мире регистрируется 19,3 млн новых случаев онкопатологии) РМЖ является наиболее частым (11,7%) [Ferlay J., Colombet M., Soerjomataram I., Parkin D.M.,  , Znaor A., Bray F. Cancer statistics for the year 2020: An overview. Int. J. Cancer. 2021;149:778–789. doi: 10.1002/ijc.33588]. Среди женского населения удельный вес РМЖ среди всех онкозаболеваний составляет 24,5% [Sung H., Ferlay J., Siegel R.L., Laversanne M., Soerjomataram I., Jemal A., Bray F. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J. Clin. 2021;71:209–249. doi: 10.3322/caac.21660]. По данным Росстата в 2020 году в Российской Федерации количество женщин, у которых был впервые в жизни установлен диагноз РМЖ, составило 65,0 тысяч человек, а показатель заболеваемости был равен 82,8 на 100000 человек [Здравоохранение в России. 2021: Стат. сб./Росстат. - М., З-46 2021. – 171 с.]. Обращает на себя внимание имеющаяся тенденция к росту заболеваемости РМЖ в РФ: стандартизованный показатель заболеваемости на 100000 населения (мировой стандарт) за последние десять лет вырос с 42,83 в 2008 г. до 51,63 в 2018 г., параметр среднегодового темпа прироста заболеваемости составил 1,97%, а показатель прироста заболеваемости за данный временной период - 22,15% [5. Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2018 году. М., 2019. 250 с. [Kaprin A.D., Starinskij V.V., Petrova G.V. Malignant neoplasms in Russia in 2018. Moscow: 2019. 250 p. (in Russian)].
, Znaor A., Bray F. Cancer statistics for the year 2020: An overview. Int. J. Cancer. 2021;149:778–789. doi: 10.1002/ijc.33588]. Среди женского населения удельный вес РМЖ среди всех онкозаболеваний составляет 24,5% [Sung H., Ferlay J., Siegel R.L., Laversanne M., Soerjomataram I., Jemal A., Bray F. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J. Clin. 2021;71:209–249. doi: 10.3322/caac.21660]. По данным Росстата в 2020 году в Российской Федерации количество женщин, у которых был впервые в жизни установлен диагноз РМЖ, составило 65,0 тысяч человек, а показатель заболеваемости был равен 82,8 на 100000 человек [Здравоохранение в России. 2021: Стат. сб./Росстат. - М., З-46 2021. – 171 с.]. Обращает на себя внимание имеющаяся тенденция к росту заболеваемости РМЖ в РФ: стандартизованный показатель заболеваемости на 100000 населения (мировой стандарт) за последние десять лет вырос с 42,83 в 2008 г. до 51,63 в 2018 г., параметр среднегодового темпа прироста заболеваемости составил 1,97%, а показатель прироста заболеваемости за данный временной период - 22,15% [5. Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2018 году. М., 2019. 250 с. [Kaprin A.D., Starinskij V.V., Petrova G.V. Malignant neoplasms in Russia in 2018. Moscow: 2019. 250 p. (in Russian)].
Несмотря на активное исследование генетических основ РМЖ, которое активно проводится многочисленными научными коллективами, в течение последних десятилетий, значительная часть генетических детерминант, вовлеченных в возникновение заболевания, до настоящего времени остается неизвестной, что диктует необходимость продолжения генетико-эпидемиологических исследований РМЖ.
Среди «потенциальных» генов-кандидатов РМЖ активно изучаются гены матриксных металлопротеиназ (ММР) [Dofara SG, Chang SL, Diorio C. Gene Polymorphisms and Circulating Levels of MMP-2 and MMP-9: A Review of Their Role in Breast Cancer Risk. Anticancer Res. 2020;40(7):3619-3631. doi:10.21873/anticanres.14351]. Связь продуктов экспрессии этих генов (одноименные белки) с заболеванием в настоящее время не вызывает сомнений. За счет своей коллагеназной активности, способности расщеплять проапоптотические факторы, мобилизовывать/активировать проангиогенные факторы (факторы роста), подавлять выработку ингибиторов ангиогенеза (ангиостатин, эндостатин) ММР обеспечивают деградацию компонентов стромальной соединительной ткани и базальной мембраны ММР, что имеет «ключевое» значение в процессах ангиогенеза, инвазии и метастазирования опухоли [Radisky ES, Radisky DC. Matrix metalloproteinases as breast cancer drivers and therapeutic targets. Front Biosci (Landmark Ed). 2015;20(7):1144-1163. Published 2015 Jun 1. doi:10.2741/4364]. Повышенная экспрессия ММР (ММР1, ММР2, ММР9, др.) в очаге поражения индуцирует рост опухолевой ткани, инициирует ее инвазию и метастазирование [Baker EA, Stephenson TJ, Reed MW, Brown NJ. Expression of proteinases and inhibitors in human breast cancer progression and survival. Mol Pathol. 2002 Oct;55(5):300-4. doi: 10.1136/mp.55.5.300.]. Имеются убедительные данные о связи ММР с выживаемостью больных РМЖ [Radisky ES, Radisky DC. Matrix metalloproteinases as breast cancer drivers and therapeutic targets. Front Biosci (Landmark Ed). 2015;20(7):1144-1163. Published 2015 Jun 1. doi:10.2741/4364].
В мировой литературе представлено достаточно большое количество генетико-эпидемиологических исследований, более 50, посвященных изучению роли функционально значимого полиморфизма генов ММР в формировании РМЖ в различных этно-территориальных группах народонаселения. Однако, несмотря на это, полученные в результате проведенных исследований результаты, нередко неоднозначны, а для отдельных полиморфных локусов – противоречивы.
Одной из важных задач современной онкологии является изучение причин и механизмов развития рака молочной железы, среди которых значимую роль играют генетические факторы.
В Российской Федерации исследования вовлеченности гена ММР-9 в формирование предрасположенности к РМЖ у женщин единичны и фрагментарны, а данные о роли генетических вариантов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9 в развитии РМЖ отсутствуют.
Для оценки сложившейся патентной ситуации был выполнен поиск по охранным документам за период с 1990 по 2022 гг. Анализ документов производился по направлению: способ прогнозирования риска развития рака молочной железы на основе молекулярно-генетических данных в зависимости от полиморфных маркеров гена ММР-9. Источники информации: сайты Федерального института промышленной собственности http://fips.ru.
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития РМЖ на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9.
Известен способ прогнозирования прогрессирования рака молочной железы по патенту RU №2741232 (опубл. 22.01.2022), включающий определение в периферической крови промежуточного метаболита витамина D 25(OH)D. При значении его содержания в сыворотке крови ≤ 18,9 нг/мл прогнозируют прогрессирование заболевания. Способ обеспечивает повышение точности прогнозирования прогрессирования рака молочной железы за счет определения промежуточного метаболита витамина D 25(OH)D в венозной крови, проявляющееся в снижении показателя промежуточного метаболита витамина D 25(OH)D, предшествующем прогрессированию заболевания. Недостатком этого способа является трудоемкость выполнения и, кроме того, не учитывается роль генетических полиморфизмов.
Известен способ прогнозирования рака молочной железы по патенту RU №2336822 (опубл. 27.08.2008), включающий исследование крови пациента. Дополнительно при обследовании определяют показатели: возраст, социальный статус, сопутствующие заболевания, количество моноцитов крови, скорость оседания эритроцитов (СОЭ), общий билирубин крови, креатинин крови, удельный вес мочи, реакцию мочи. Затем определяют прогностический коэффициент (ПК) для каждого показателя. В системе возраст при маркере до 20 лет устанавливают ПК равным (0), при маркере 20-29 лет - равным (-10), при маркере 30-39 лет - равным (-7), при маркере 40-49 лет - равным (+4), при маркере 50-59 лет - равным (+3), при маркере 60-69 лет - равным (+2), при маркере 70-79 лет - равным (+4), при маркере 80 и более лет - равным (-3). В системе социальный статус при маркере рабочие устанавливают ПК равным (+4), при маркере служащие - равным (-1), при маркере учащиеся - равным (0), при маркере безработные - равным (-12), при маркере пенсионеры и инвалиды труда (ИТР) - равным (+1). В системе сопутствующие заболевания при маркере заболевания желудочно-кишечного тракта (ЖКТ) устанавливают ПК равным (-10), при маркере заболевания сердечно-сосудистой системы - равным (+2), при маркере заболевания эндокринной системы - равным (+1,5), при маркере заболевания дыхательной системы - равным (0), при маркере заболевания опорно-двигательного аппарата - равным (0), при маркере заболевания мочеполовой системы - равным (-13), при маркере сочетание сопутствующий заболеваний - равным (-1), при маркере отсутствие сопутствующих заболеваний - равным (+2). В системе моноциты крови при маркере нет устанавливают ПК равным (0), при маркере 1-3% - равным (-2,5), при маркере 4-6% - равным (+2), при маркере 7-10% - равным (+2,5), при маркере более 10% - равным (0). В системе скорость оседания эритроцитов при маркере - 1-10 мм/ч устанавливают ПК равным (-1), при маркере 11-20 мм/ч - равным (-3), при маркере 21-30 мм/ч - равным (+7), при маркере 31-40 мм/ч - равным (0), при маркере более 40 мм/ч - равным (0). В системе общий билирубин при маркере менее 8,8 мкмоль/л устанавливают ПК равным (0), при маркере 8,8-17 мкмоль/л - равным (-1), при маркере более 17 мкмоль/л - равным (+5,5). В системе креатинин при маркере менее 0,07 ммоль/л устанавливают ПК равным (+11), при маркере 0,07-0,17 - равным (-3), при маркере более 0,17 мкмоль/л - равным (0). В системе удельный вес мочи при маркере менее 1008 устанавливают ПК равным (0), при маркере 1008-1026 - равным (+2), при маркере более 1026 - равным (+6). В системе реакция мочи при маркере кислая, устанавливают ПК равным (+3), при маркере нейтральная - равным (-3), при маркере щелочная - равным (-12). При сумме ПК от (-54,5) до (-21,5) прогнозируют низкую вероятность рака молочной железы, при сумме от (+11) до (+44,5) прогнозируют высокую вероятность рака молочной железы. Однако прогнозирование таким способом рака молочной железы сопряжено с профилактическими осмотрами, при этом диспансеризация лиц из групп повышенного риска должна проводиться длительное время вплоть до возраста 55 лет.
Известен способ прогнозирования рецидива рака молочной железы по патенту RU №2263319 (опубл. 27.10.2005), включающий биохимическое исследование биологической жидкости пациента, отличающийся тем, что у менопаузальных женщин после комплексного лечения рака молочной железы в динамике определяют концентрацию эстриола, эстрона и эстрадиола в моче, вычисляют соотношение эстриола к эстрону и эстрадиолу и при значении его 1,68±0,23 констатируют отсутствие рецидива, а при его снижении до значений 0,74±0,12 у пациенток, проживающих без рецидива менее 1 года, до 0,65±0,13 у пациенток, проживших без рецидива от 2 до 6 лет, и до 0,50±0,10 у пациенток, проживших без рецидива от 6 до 10 лет, констатируют развитие рецидива. Недостатком данного способа является высокая стоимость анализа, что особенно важно при его многократном повторении в ходе наблюдения за больными после комплексного лечения.
Известен патент RU №2522501 (опубл. 20.07.2014), в котором описан способ прогнозирования наследственной предрасположенности к раку молочной железы. Сущность способа заключается в том, что проводят амплификацию коротких фрагментов гена BLM протяженностью до 200 п.о., с последующим высокоразрешающим плавлением, включающим оптимизированный для гена BLM этап формирования гетеродуплексов: быстрый нагрев до 95°С и медленное снижение температуры до 50°С; выбирают один фрагмент с аберрантным профилем плавления для секвенирования, секвенируют выбранный фрагмент и при выявлении мутации гена BLM прогнозируют наследственную предрасположенность к раку молочной железы. Недостатком этого способа является его трудоемкость, он не учитывает роль генетических полиморфизмов.
Известен способ прогнозирования генерализации рака молочной железы по патенту RU №2204836 (опубл. 20.05.2003). В данном способе проводят диагностическое наблюдение больных раком молочной железы. Определяют тромбоцитарную активность МАО-Б в плазме крови, что обеспечивает доклиническое выявление генерализации рака молочной железы. При снижении тромбоцитарной активности МАО-Б в 4-6 раз по отношению к норме прогнозируют генерализацию процесса. Недостатком предлагаемого способа является использование в качестве маркера только одного показателя - тромбоцитарной активности МАО-Б в плазме крови, применение способа в отношении уже больных раком молочной железы, преимущественная информативность предлагаемого показателя тромбоцитарной активности МАО-Б в период генерализации процесса при наличии отдаленных метастазов, что делает невозможным применение способа в ранней диагностике рака молочной железы.
Известен патент RU №2631940 (опубл 28.09.2017), в котором описан способ прогнозирования рака молочной железы. Сущность способа заключается в том, что определяют факторы риска: ношение тугого бюстгальтера (Б), возраст (В), перенесенные воспалительные заболевания молочной железы (ЗМЖ), перенесенные заболевания щитовидной железы (ЗЩЖ), индекс массы тела (ИМТ), частое употребление жирной, жареной и копченой пищи (Калл), некормление ребенка грудью (НКГ), кормление ребенка грудью год и более (КГ≥1 год), позднее наступление менструации (ПНМ), длительное проживание в военных городках (ПВО), перенесенные травмы молочной железы (ТМЖ). Отсутствие каждого из указанных факторов оценивают как «0 баллов», а наличие - «1 балл». Показатели ПНМ, В, ИМТ оценивают количественно. Рассчитывают прогностический коэффициент ПК по заявленной формуле. Если значение ПК меньше 0,2197, то прогнозируют низкий риск, а если ПК от 0,2197 и более - высокий риск рака молочной железы. Недостатком способа является сложность расчетов и не учитываются генетические факторы.
Прогнозирование риска рака молочной железы на основе естественных исследований // Зиннатуллина Г.Ф., Бермишева М.А., Кононова В.А., Фарахтдинова А.Р., Хуснутдинова Э.К. // Креативная хирургия и онкология. 2009. №2. URL: https://cyberleninka.ru/article/n/prognozirovanie-vozniknoveniya-riska-raka-molochnoy-zhelezy-na-osnove-geneticheskih-issledovaniy (дата обращения: 24.07.2022), характеризуется проведением анализа распространенности двух вариантов гена NBN (c.657del5 и p.R215W) у больных раком молочной железы в Республике Башкортостан и Ханты-Мансийском автономном округе. Недостатком данного исследования является применение только для коренных жителей Республики Башкортостан и Ханты-Мансийского автономного округа.
Задачей настоящего исследования является расширение арсенала методов диагностики, а именно создание способа прогнозирования риска развития РМЖ у женщин на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9.
Технический результат использования изобретения – получение критериев оценки риска развития рака молочной железы у женщин русской национальности, уроженок Центрально – Черноземного региона РФ, на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9, включающий:
- выделение ДНК из периферической венозной крови;
- анализ полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9;
- прогнозирование высокого риска развития рака молочной железы у женщин при выявлении гаплотипа CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9.
Новизна и изобретательский уровень заключаются в том, что из уровня техники не известна возможность прогноза развития рака молочной железы у пациенток на основе данных о гаплотипе CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9.
Способ осуществляют следующим образом:
Выделение геномной ДНК из периферической крови осуществляют методом фенольно-хлороформной экстракции (Miller, S. A. A simple salting out procedure for extracting DNA from human nucleated cells / S. A. Miller, D. D. Dykes, H. F. Polesky // Nucleic. Acids. Res. – 1988. – Vol. 16, № 3. – P. 1215) в два этапа. На первом этапе к 4 мл крови с ЭДТА добавляют 25 мл лизирующего буфера, содержащего 320 мМ сахарозы, 1% тритон Х-100, 5 мМ MgCl2, 10 мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4ºС, 4000 об/мин в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН=8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10 мг/мл) и инкубируют образец при 37°С в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об/мин в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. После лиофилизации полученную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -20°С.
Анализ полиморфных маркеров rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9 осуществлялся методом полимеразной цепной реакции (ПЦР) на термоциклере CFX-96 Real-Time System (Bio-Rad) c использованием стандартных олигонуклеотидных праймеров и зондов (синтезированы в ООО «Тест - Ген» (Ульяновск)).
Амплификация геномной ДНК производилась в реакционной смеси, суммарным объемом 10 мкл, включающей смесь для ПЦР ММР-9 – 4 мкл, Taq-полимеразу - 2 мкл, исследуемый образец (~30 нг ДНК/мкл) - 1 мкл, деионизированная вода – 3 мкл.
Генотипирование исследуемых образцов осуществлялось с использованием программного обеспечения «CFX-Manager™» методом дискриминации аллелей по величинам относительных единиц флуоресценции (ОЕФ) (фиг. 1, фиг. 2, фиг. 3, фиг. 4, фиг. 5).
Изобретение характеризуется фигурами:
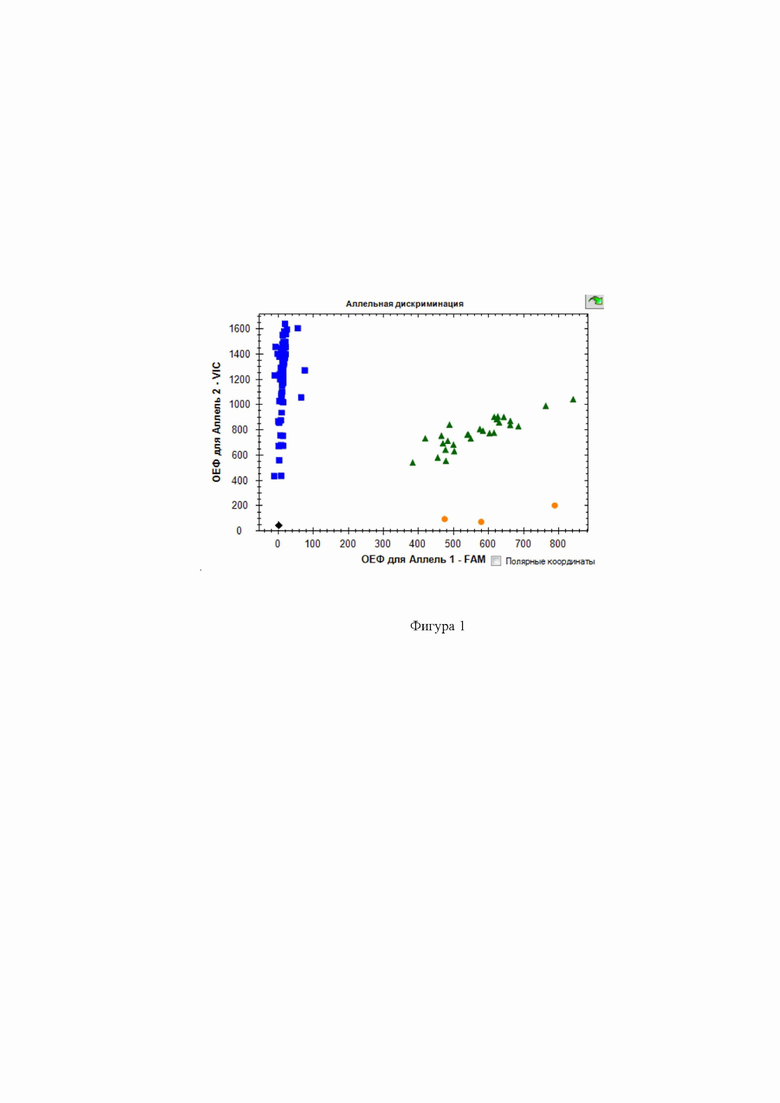
Фиг. 1 - Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs3918242 ММР-9 ( - TT,
- TT,  - CC,
- CC,  - CT, ■ - отриц. контр.).
- CT, ■ - отриц. контр.).
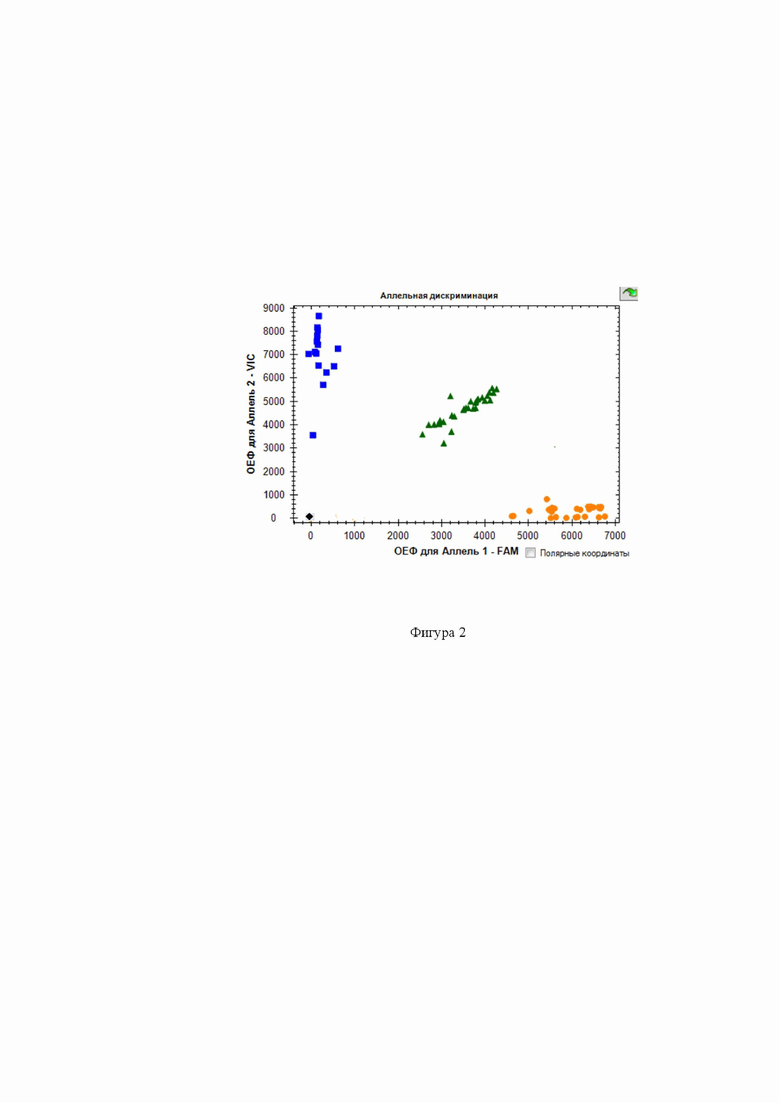
Фиг. 2 - Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs3918249 ММР-9 ( - TT,
- TT,  - CC,
- CC,  - TC, ■ - отриц. контр.).
- TC, ■ - отриц. контр.).
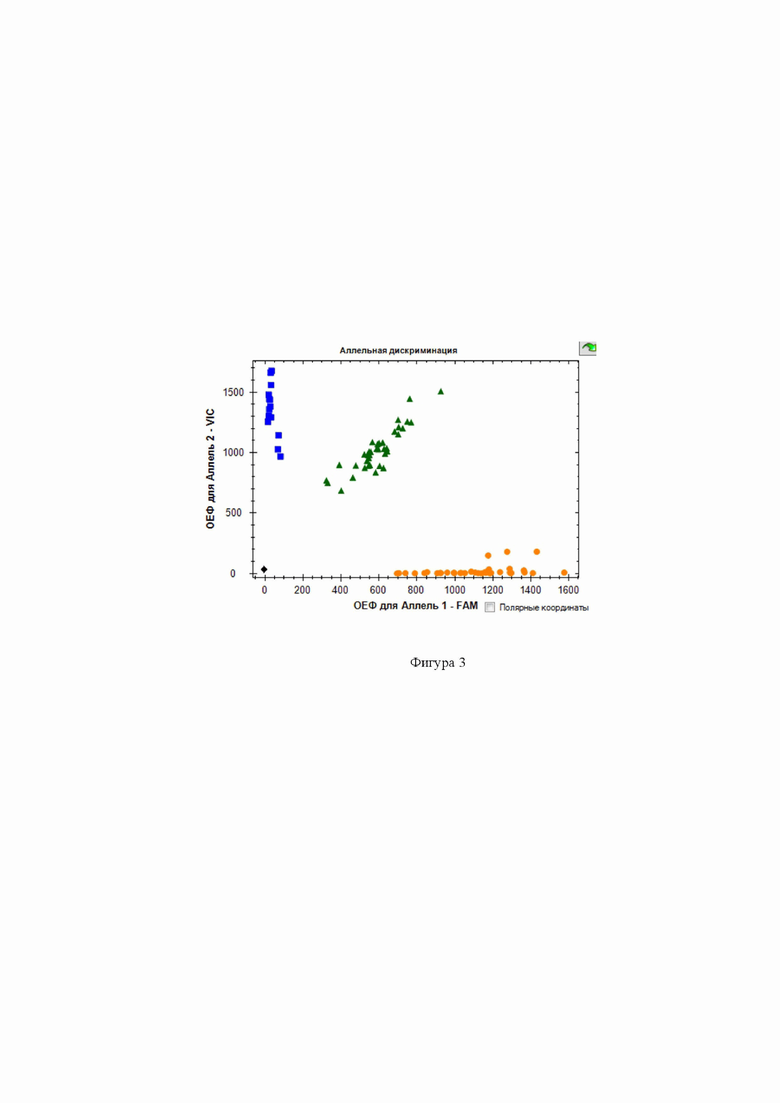
Фиг. 3 - Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs17576 ММР-9 ( - AA,
- AA,  - GG,
- GG,  - AG, ■ - отриц. контр.).
- AG, ■ - отриц. контр.).
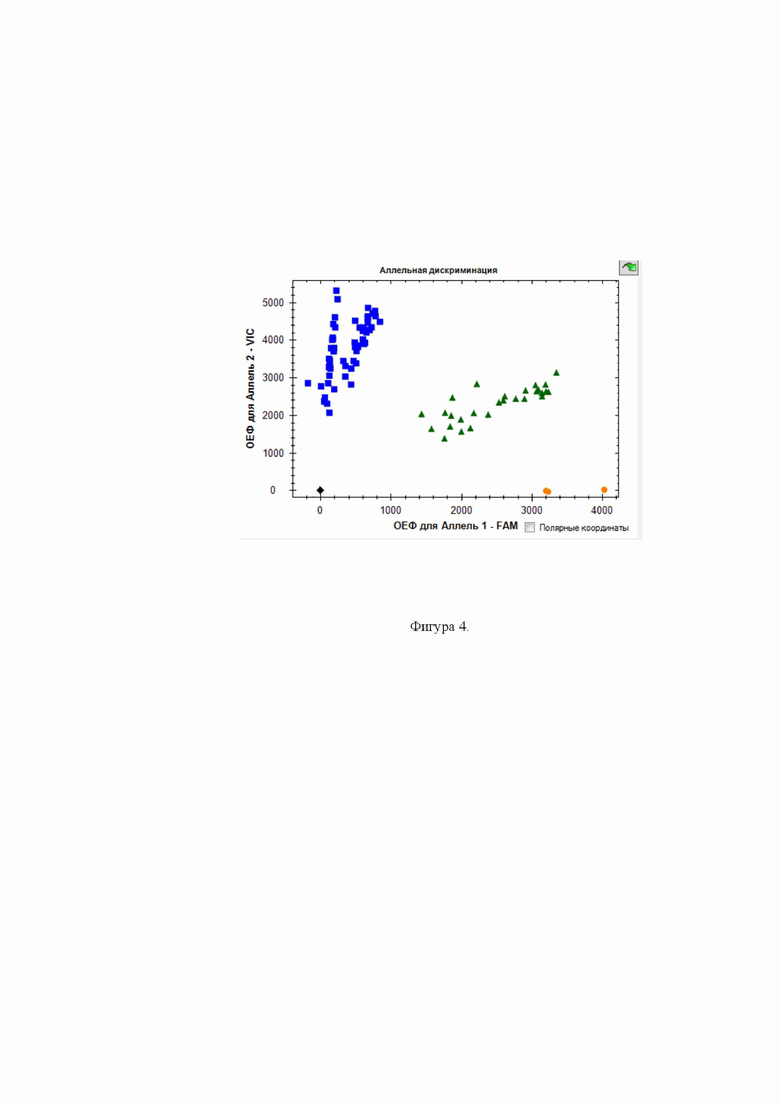
Фиг. 4 - Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs3787268 ММР-9 ( - AA,
- AA,  - GG,
- GG,  - GA, ■ - отриц. контр.).
- GA, ■ - отриц. контр.).
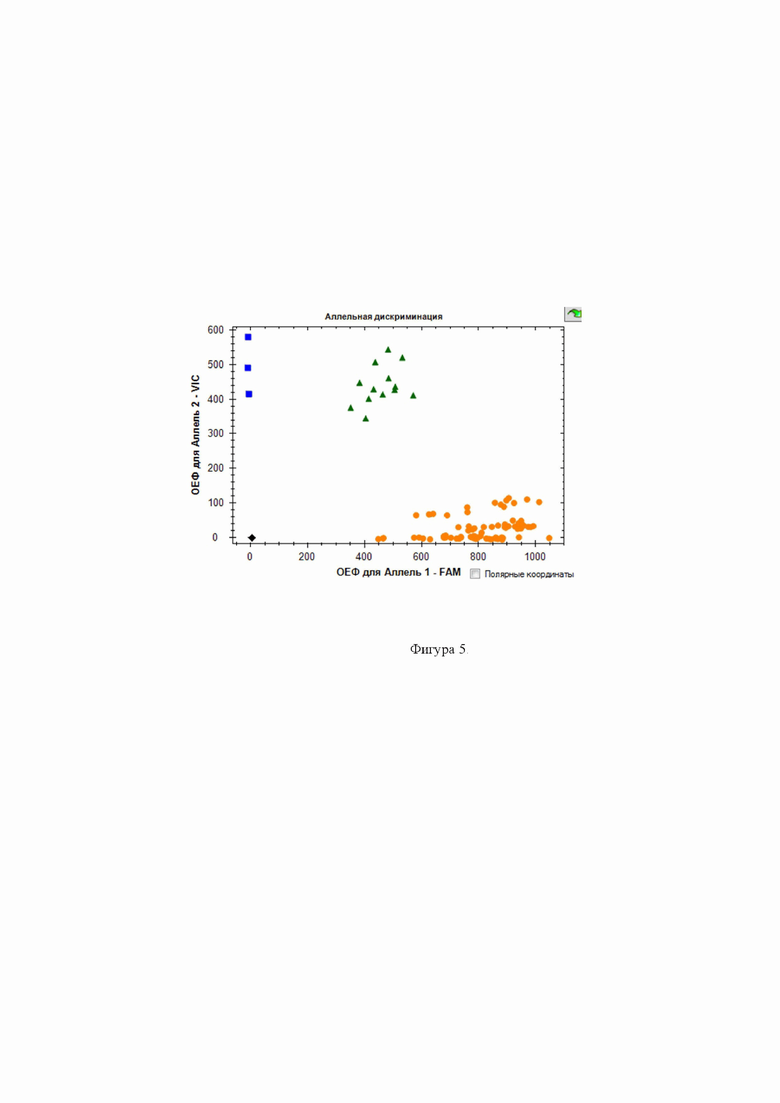
Фиг. 5 - Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма rs2250889 ММР-9 ( - CC,
- CC,  - GG,
- GG,  -CG, ■ - отриц. контр.).
-CG, ■ - отриц. контр.).
Определение частот гаплотипов и анализ ассоциаций гаплотипов с развитием РМЖ у женщин проводилось с помощью логистического регрессионного анализа в программе PLINK (версия 1.07) [Ponomarenko, I.V., Polonikov, A.V., Churnosov, M.I. Association of ESR2 RS4986938 polymorphism with the development of endometrial hyperplasia (2019) Akusherstvo i Ginekologiya (Russian Federation), 2019 (4), pp. 66-72]. При необходимости в исследование включали ковариаты (возраст, индекс массы тела). После проведения пермутационного теста (выполнялось 1000 пермутаций) за статистически значимый уровень принимали ррerm<0,05.
Возможность использования предложенного способа для оценки прогнозирования риска развития РМЖ у женщин c использованием молекулярно-генетических данных подтверждает анализ результатов наблюдений 1104 пациенток, из них 358 больные с раком молочной железы и 746 женщин контрольной группы. Средний возраст больных составил 54,74±12,73 лет (варьировал от 25 до 84 лет). Возрастные характеристики больных и контроля были сопоставимы. В выборки для исследования включались (критерии включения): 1) пациентки русской национальности, являющиеся уроженками Центрального Черноземья РФ, не имеющие родства между собой и проживающие в Белгородской области (Чурносов М.И., Сорокина И.Н., Балановская Е.В. Генофонд населения Белгородской области. Динамика индекса эндогамии в районных популяциях // Генетика. 2008. Т. 44. № 8. С. 1117-1125), добровольно согласившиеся на проведение исследования; 2) в группу больных включались пациентки только после установления диагноза заболевания РМЖ, подтвержденного с помощью клинических и лабораторно-инструментальных (в т.ч. морфологических) методов обследования.
Обследование больных РМЖ проводилось на базе поликлинического и химиотерапевтического отделений Белгородского областного онкологического диспансера; формирование контрольной группы (без клинико-анамнестических признаков РМЖ) проводилось на базе перинатального центра БОКБ Святителя Иоасафа в ходе профилактических осмотров.
Все больные РМЖ и женщины контрольной группы подписали информированное согласие на участие в исследовании, проведение исследования было согласовано с этическим комитетом медицинского института НИУ «БелГУ».
Типирование молекулярно-генетических маркеров осуществлялось на кафедре медико-биологических дисциплин медицинского института НИУ «БелГУ».
При расчете частот гаплотипов и анализе их ассоциаций у пациенток установлена связь с формированием РМЖ гаплотипа CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9. Гаплотип CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9 является фактором риска развития РМЖ у женщин с использованием молекулярно-генетических данных (ОR=3,55, р=0,002).
В качестве примеров конкретного применения разработанного способа приведено обследование русских женщин, уроженок Центрально-Черноземного региона РФ и не являющихся родственницами между собой: проведено генетическое исследование по полиморфным локусам rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9.
У пациентки Л. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип СTAGG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9, что позволило отнести пациентку в группу женщин с низким риском развития РМЖ у женщин с использованием молекулярно-генетических данных. При дальнейшем наблюдение диагноз рака молочной железы у пациентки Л. не подтвердился.
У пациентки Ш. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9, что позволило отнести женщину в группу пациенток с повышенным риском развития РМЖ с использованием молекулярно-генетических данных. Дальнейшее наблюдение подтвердило диагноз рака молочной железы у пациентки Ш.
У пациентки В. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип ТТААG полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9, что позволило отнести пациентку в группу больных с пониженным риском развития РМЖ с использованием молекулярно-генетических данных. Дальнейшее наблюдение не подтвердило диагноз рака молочной железы у пациентки.
У пациентки С. была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен гаплотип CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9, что позволило отнести пациентку в группу индувидуумов с повышенным риском развития РМЖ. При дальнейшем наблюдении диагноз рака молочной железы у пациентки С. подтвердился.
Применение данного способа позволит на доклиническом этапе формировать среди пациенток группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития РМЖ у женщин с использованием молекулярно-генетических данных.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования повышенного риска развития рака молочной железы 1-2 стадий у женщин на основе полиморфизма гена матриксной металлопротеиназы 9 | 2022 |
|
RU2795100C1 |
| Способ прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы | 2023 |
|
RU2823459C1 |
| Способ прогнозирования риска развития люминального подтипа рака молочной железы | 2023 |
|
RU2795720C1 |
| Способ прогнозирования риска развития рака молочной железы у женщин без ожирения | 2023 |
|
RU2795726C1 |
| Способ прогнозирования риска развития рака молочной железы у женщин с ожирением | 2022 |
|
RU2795244C1 |
| Способ прогнозирования риска развития тройного негативного подтипа рака молочной железы | 2023 |
|
RU2811257C1 |
| Способ прогнозирования повышенного риска развития рака молочной железы 3-4 стадий заболевания у женщин | 2024 |
|
RU2830466C1 |
| Способ прогнозирования риска развития 3 степени злокачественности опухолевых клеток при раке молочной железы | 2024 |
|
RU2830352C1 |
| Способ прогнозирования риска развития язвенной болезни желудка на основе генетического анализа | 2022 |
|
RU2780505C1 |
| Способ прогнозирования риска развития язвенной болезни у женщин по генетическим данным | 2022 |
|
RU2786314C1 |
Изобретение относится к области медицины, в частности к клинической онкологии, медицинской генетике, молекулярной диагностике, и может быть использовано для прогнозирования риска развития рака молочной железы у женщин с использованием молекулярно-генетических данных. Предложен способ прогнозирования риска развития рака молочной железы у женщин. Выделяют ДНК из периферической венозной крови, производят анализ генетических маркеров гена ММР-9, прогнозируют высокий риск развития рака молочной железы у женщин с использованием молекулярно-генетических данных при выявлении гаплотипа CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9 (ОR=3,55, р=0,002). Изобретение позволяет оценить риск развития рака молочной железы у женщин русской национальности, уроженок Центрально–Черноземного региона РФ на основе данных о полиморфных локусах rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9. 5 ил., 4 пр.
Способ прогнозирования риска развития рака молочной железы у женщин с использованием молекулярно-генетических данных, включающий выделение ДНК из периферической венозной крови, анализ генетических маркеров гена ММР-9, отличающийся тем, что высокий риск развития рака молочной железы у женщин с использованием молекулярно-генетических данных прогнозирует выявление гаплотипа CTAAC полиморфных локусов rs3918242-rs3918249-rs17576-rs3787268-rs2250889 гена ММР-9.
| VICTOR ALVES DE OLIVEIRA et al., Association between matrix metalloproteinase-9 gene polymorphism and breast cancer in Brazilian women, Clinics (Sao Paulo) | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| WIECZOREK E, et al., Genetic polymorphism of matrix metalloproteinases in breast cancer; Neoplasma, 2012;59(3):237-47, аbstract | |||
| ЗИННАТУЛЛИНА | |||
Авторы
Даты
2023-05-15—Публикация
2022-10-17—Подача