Область техники, к которой относится изобретение
Изобретение относится к области синтеза наноматериалов, точнее флуоресцентных наноматериалов, а точнее углеродных квантовых точек для различных применений – в области биомедицины, биотехнологии, диагностики, терапии, детекции различных веществ и т.д. Такие технологии полезны для получения новых типов наноматериалов с улучшенными характеристиками.
Описание предшествующего уровня техники
Углеродные квантовые точки (УКТ) представляют собой класс углеродных наноматериалов, которые сочетают в себе уникальные оптические свойства яркой флуоресценции, превосходной фотостабильности, настраиваемых спектральных характеристик, а также низкую токсичность и биоразлагаемость. УКТ широко используются в биомедицине, например, для задач детекции, биовизуализации и терапии.
Чтобы сделать УКТ или любые другие наночастицы биологически функциональными, их обычно конъюгируют с белками, нуклеиновыми кислотами, углеводами или другими полимерами. Для краткости, в рамках данной работы, мы будем называть все эти молекулы «биополимерами».
На сегодняшний день существует ряд методов конъюгации углеродных квантовых точек и биополимеров. Одним из наиболее широко применяемых методов является карбодиимидный метод, при котором формируются амидные связи между карбоновыми кислотами и аминами. Иммобилизация нуклеиновых кислот, а также различных других полимеров, таких как, например, полиэтиленгликоль или хитозан, осуществляется путем электростатической адсорбции на поверхности УКТ, легированных полиэтиленимином. Некоторые полимеры также иммобилизуются путем добавления во время синтеза УКТ.
Несмотря на то, что ковалентное присоединение используется для многих типов биомакромолекул, оно требует индивидуального подбора и оптимизации молекул линкера для каждого типа биополимера, а также, в некоторых случаях, введения дополнительных реакционноспособных групп в требуемый полимер.
Метод электростатической адсорбции является быстрым и удобным способом конъюгации биополимера с УКТ. Однако при заданном виде УКТ, имеющих, например, отрицательный заряд поверхности, этот метод применим только для сильно положительно заряженных биополимеров.
Добавление биополимера при синтезе УКТ позволяет сократить количество стадий синтеза и, в некоторых случаях, непосредственно модулировать поверхностные свойства УКТ. Однако, одной из наиболее популярных стратегий синтеза УКТ является сольвотермический путь, который включает в себя длительный нагрев реагентов при температурах 100-200 °C, чаще всего, в неводном растворителе. В таких суровых условиях выбор биополимера определяется уже не биологическим применением, а термической стабильностью и растворимостью биополимера в используемом растворителе.
Авторами был обнаружен новый универсальный способ нековалентной конъюгации углеродных квантовых точек с широким спектром биомакромолекул. Метод основан на простой двухступенчатой процедуре кратковременного нагрева и последующего осаждения полимера на поверхность УКТ методом высаливания. Примечательно, что весь процесс вместе со стадией очистки занимает менее 10 минут.
Из публикации KR101612514B1 известен близкий способ получения углеродных квантовых точек, в котором в результате нагрева жидкости с стабилизирующим агентом и источником углерода формируются углеродных квантовые точки.
Недостатком известного метода является сложность в постсинтетической модификации результирующих углеродных квантовых точек с помощью полимеров, а также сложности их очистки.
Из публикации CN112521942B известен наиболее близкий способ получения углеродных квантовых точек, в котором раствор лимонной кислоты и мочевины подвергается нагреву в микроволновой печи, в результате чего образуются углеродные квантовые точки.
Недостатком известного метода является жесткость используемых при функционализации полимером условий (такие как высокая температура), а также длительная процедура функционализации (72 часа).
Таким образом, технический результат состоит в разработке более быстрого метода синтеза функциональных (функционализированных) углеродных квантовых точек, позволяющего добиться их функционализации различными биополимерами (в т.ч. макромолекулами) в более мягких условиях и позволяющего легко их очистить от несвязавшихся молекул биополимеров.
Краткое содержание изобретения
Целью настоящего изобретения явилась разработка на основе обнаруженного явления ассоциации различных полимеров с углеродными квантовыми точками под влиянием температуры и высаливающего агента:Способа синтеза функциональных углеродных квантовых точек.Для решения перечисленных выше и других целей, которые очевидны для квалифицированного специалиста, был предложен следующий способ:
Способ синтеза функциональных углеродных квантовых точек, которые включает следующие шаги:
i) раствор лимонной кислоты и мочевины автоклавируют при температуре 150-300 градусов Цельсия,
ii) отмывают полученные углеродные квантовые точки,
отличающийся тем, что дополнительно включает следующие шаги:
iii) смешение отмытых углеродных квантовых точек с раствором полимера,
iv) нагрев полученной смеси до 50-99 градусов Цельсия,
v) повышение ионной силы полученного раствора для высаживания упомянутого полимера на поверхность углеродных квантовых точек.
Словарь
Если иное не определено, нижеследующие термины имеют следующие значения при интерпретации формулы и описания изобретения:
1) «иммунохроматографический тест» – помещение образца, в котором может находиться целевая нуклеотидная последовательность, на тест-полоску из хроматографичского материала с последующим латеральным перемещением образца по тест-полоске за счет капиллярных сил и его связывание с различными реагентами, размещенными на тест-полоске.
2) "тест-полоска" – хроматографическая среда, в которой может быть проведен анализ. Тест-полоска содержит «зону нанесения» для нанесения образца и «зону связывания» (тест-линия), содержащую иммобилизованный связывающий реагент или же связывающую нуклеотидный последовательность, способные к связыванию и иммобилизации детектируемой нуклеотидной последовательности. Зона связывания, как правило, обладает существенно меньшей площадью поверхности, чем тест-полоска и содержит иммобилизованный связывающий реагент или же иммобилизованную связывающую нуклеотидную последовательность. Зона связывания может иметь форму точки, линии, кривой, полосы или же паттерна из точек, линий, кривых, полос или же их комбинации. Как правило, направление перемещения образца по тест-полоске пересекает зону связывания. Для данного изобретения предпочтительным является формирование сигнала в зоне связывания в форме четко-очерченного паттерна, резко отличающегося от сигнала, формируемого в других частях тест-полоски. Например, зона связывания может иметь форму аббревиатуры названия или названий аналита или аналитов в исследуемом образце.
3) Термин «партнер для связывания» относится к паре молекул и/или частиц, способным распознавать друг друга (целиком или частично) и образовывать как ковалентные, так и нековалентные связи. Существует ряд часто используемых пар для связывания, а также структур на основе таких пар. Среди них можно выделить системы, основанные на взаимодействии антиген/антитело, гаптен/антигаптен, диоксигенин/антидиоксигенин F(ab’)2, фолиевая кислота/фолат-связывающий белок, биотин/стрептавидин, биотин/авидин, протеин А(G)/иммуноглобулины, комплементарные сегменты нуклеиновых кислот, вирус/клеточный рецептор, лектин/карбогидрат, фермент/ингибитор, фермент/субстрат. Также, известны системы, в которых партеры по связыванию образовывают ковалентные связи за счет наличия у таких партнеров аминореакционных групп, таких как сукцинимидиловые эфиры, изотиоционат, сульфонил галиды, или сульфгидрильные реакционные группы, включая производные галоацетатов и малеимидов. Другими партнерами для связывания могут быть галогены, стероиды и 2,4 – динитрофенилы. Для целей настоящего описания, термин «партнер для связывание» относится и к «распознающему рецептору» и его лиганду.
4) Термин «нуклеиновая кислота» обозначает полимер или олигомер, состоящий из нуклеотидов, или соединений, имитирующих их. Также термин относится к олигонуклеотидам, имеющим не встречающееся в природе участки цепи, но проявляющими такие же свойства, как и олигонуклеотиды природного происхождения. Для специалистов должно быть очевидно, что в соответствии с данным изобретением может быть осуществлено большое разнообразие анализов по детекции целевых последовательностей нуклеиновых кислот. Термин «нуклеотид» здесь относится к рибонуклеотидам, дезоксирибонуклеотидам, или аналогам нуклеотидов, имеющих химическую модификацию в одном или нескольких из строительных блоков нуклеотида (азотистых оснований - пурина или пиримидина, сахара, фосфатов). Модификации могут быть, например, проведены в пятой позиции пиримидина, или восьмой позиции пурина, в экзоциклической аминогруппе цитозина, путем замены урацила на 5-бром-урацил, замена гидроксигруппы в 2´-позиции сахара на галогруппу (либо на R, OR, SH, H, SR, NR2, NH2, NHR, CN). Термин также относится к рибонуклеиновым кислотам, встречающимся в живых организмах, либо с замененным основанием (ксантин, ионозин и т.д.) или сахаром (2´-метоксирибоза и т.п.). Также возможна модификация фосфодиэфирной связи, например, образование цепи с помощью фосфоротионатов, метилфосфонатов и пептидов. «Нуклеиновая кислота» может обозначать одно- или двуцепочечную молекулу, состоящую из мономеров (нуклеотидов), включающих в свой состав фрагменты сахаров, фосфатов и пуринов или пиримидинов. В растениях, животных, низших эукариотах и бактериях «рибонуклеиновая кислота» (РНК) выполняет функции трансляции, т.е. служит передатчиком хранящейся в «дезоксирибонуклеиновой кислоте» (ДНК) генетической информации. Термин «фрагмент» обозначает определенную часть последовательности ДНК.
5) Метод анализа и его аппаратурная реализация, относящийся к данному изобретению, может детектировать целевую нуклеиновую кислоту или другие вещества (собирательный термин – аналит), содержащиеся в различных образцах. Термин «образец» здесь относится к любой жидкости, потенциально содержащей аналиты. Образец может быть получен из человеческих или других животных тканей или жидкостей (кровь/сыворотка крови, моча, слюна, слеза, мокрота, пот, слизь, стул), из образцов культивирования клеток тканей, гистологических образцов, образцов биопсии и т.д. Образец также может быть получен из продуктов сельского хозяйства, бактерий, вирусов, либо их продуктов жизнедеятельности и обработки. Также образцом может служить различный мусор и отходы, продукты их переработки, питьевая и сточные воды, продукты питания в обработанном или сыром виде, воздух и т.д. В случае реализации данного изобретения для детектирования искомых последовательностей нуклеиновых кислот, оно может быть применено для анализа генетических отклонений и множества других заболеваний, служить для контроля протекания лечения инфекционных болезней, а также для множества других применений.
6) Термин «распознающий олигонуклеотид» обозначает НК, содержащую последовательность, комплементарную анализируемой (целевой) нуклеиновой кислоте (аналиту).
7) Термин «сигнал-генерирующий субстрат» обозначает вещество, способное взаимодействовать с сигнальным рецептором и генерировать детектируемый сигнал. Например, ABTS/TMB для пероксидазы, BCIP/MBT для щелочной фосфотазы, свет для флуоресцирующих соединений.
8) Термин «сигнальный рецептор», «сигнал-продуцируемый репортер», «репортер» обозначает вещество, способное детектировать искомый аналит через выделение энергии или путем ферментативной активности, например, флуоресцентные и хемилюминесцентные фрагменты, частицы, ферменты, радиоактивные метки, светоиспускающие домены или молекулы. Для целей этого описания, упоминание данных примеров означает возможность заменить на иные подобные вещества-«сигнальный рецепторы».
9) Термин «пористый материал» или «хроматографический материал» обозначает материал, имеющий поры не менее 0,1 мкм, предпочтительно не менее 10,0 мкм, достаточного размера для движения по нему жидкостных сред за счет капиллярных сил.
10) Термин «сигнал-продуцирующая система» обозначает совокупность реагентов необходимых для генерации детектируемого сигнала под действием внешнего воздействия. Как правило, такие системы генерируют сигнал, который может быть детектирован внешними средствами – например, путем измерения электромагнитного излучения, или путем визуального наблюдения. В основном, такие системы состоят из хромофорного субстрата и фермента, который превращает субстрат в краситель, поглощающий электромагнитное излучение определенного диапазона, фосфоресцирующие или флуоресцирующие вещества.
11) Расположение шпильки от первого или второго конца распознающего олигонуклеотида на расстоянии Х нуклеотидных оснований подразумевает собой, следующее. Местом связывания наночастицы или сигнального рецептора с распознающим олигонуклеотидом следует считать нуклеотид, с которым образована их связь (предпочтительно ковалентная). При этом, если этот нуклеотид является первым в шпильке (т.е. образовывает нековалентную связь с другим нуклеотидом), то расстояние Х=0. Если шпилька начинается с соседнего нуклеотида, то Х=1, и т.д.
12) Под первым/вторым концом одноцепочечного распознающего олигонуклеотида - имеется в виду не фактический конец молекулы, а одна или вторая его сторона. Т.е. нуклеотидное основание распознающего олигонуклеотида, соответствующее месту связи сигнального рецептора или наночастицы предпочтительно находится с краю олигонуклеотида, но может быть и не крайним основанием в олигонуклеотиде. Под нуклеотидным основанием распознающего олигонуклеотида, соответствующем месту связи сигнального рецептора (или наночастицы), подразумевается мономер нуклеиновой кислоты нуклеотид (в т.ч. нуклеозид, сахарид и остаток фосфорной кислоты), с которым связан сигнальный рецептор (или наночастица).
13) В данном описании, понятия «рецептор» и «лиганд» взаимозаменяемы и могут быть использованы для обозначения индивидуальных молекул в вышеописанном понятии «партнеров для связывания». Так, например, если часто в литературе в парах стрептавидин-биотин, антитело-антиген, под рецептором подразумевается стрептавидин и антитело, а под лигандом – биотин и антиген, то в описании данного изобретения под рецептором может подразумеваться и стрептавидин с антителом, и биотин с антигеном (при этом лигандом будет соответственно – биотин с антигеном и стрептавидин с антителом, соответственно).
14) Наночастица – подразумевает собой частицу в широком диапазоне – от 1 нм до 100 мкм, предпочтительнее от 1 нм до 10 мкм, предпочтительнее – от 1 нм до 1 мкм, предпочтительнее от 1 нм до 100 нм. При этом наночастицы могут быть металлическими, полимерными, структуры ядро-оболочка и т.п.
15) Термин «наночастицы» подразумевает надмолекулярные структуры, которые состоят из более, чем одной молекулы. При этом, хотя часто наночастицами обозначают объекты до 100 нм, в рамках описания данного изобретения подразумеваются и объекты большие чем 100 нм – предпочтительно до 5мкм, но в некоторых случаях допустим размер и до 100 мкм. Таким образом, под наночастицами подразумевают как наночастицы, так и микрочастицы, микросферы и т.п. Кроме того, подразумеваются частицы с упомянутыми размерами, как по всем измерениям, так и по хотя бы одному.
16) Терапевтические средства/молекулы/агенты. Под терапевтическими молекулами/агентами могут пониматься как вещества, субстанции, молекулы, надмолекулярные агенты, наночастицы, микрочастицы, наноагенты, микроагенты, формуляции, лекарственные формы, и т.п., которые используются как для терапии, так и диагностики различных заболеваний или состояний организма или пациента, в т.ч. включают в себя метки, контрастные агенты, компоненты с контролируемым высвобождением, парамагнитные и магнитные агенты, цитотоксические агенты, и т.п.
17) «Меткой» или «детектируемым элементом» является композиция, детектируемая спектроскопическими, фотохимическими, биохимическими, иммунохимическими, химическими или другими физическими средствами. Например, широко используемые метки включают в себя 32P, флуоресцентные красители, электронно-плотные реагенты, ферменты (например, как обычно используются в ELISA), биотин, дигоксигенин или гаптены и белки или другие сущности, которые могут быть обнаружены, например, путем включения радиоактивной метки в пептид или антитело, специфически реагирующие с целевым пептидом. Любой метод, известный в данной области для конъюгирования антитела с меткой, может быть использован, например, с использованием методов, описанных в (Hermanson, G. T., Academic press, 2013).
18) Используемый здесь термин «фармацевтический» относится к композиции, которая полезна при лечении заболевания или симптома заболевания.
19) Термин «лечение» или «терапия» (treating, treatment, therapy) относятся к любым признакам успеха при лечении или улучшении заболевания, травм, патологии или состояния, включая любые объективные или субъективные параметры, такие как уменьшение; ремиссия; уменьшение симптомов или замедление ухудшения состояния больного, патологии или состояния пациента; замедление темпов дегенерации; что делает финальную стадию заболевания менее мучительной; улучшение физического или психического благополучия пациента. Лечение или улучшение симптомов могут основываться на объективных или субъективных параметрах; включая результаты физического обследования, нейропсихиатрических экзаменов и / или психиатрической оценки. Например, определенные методы, представленные здесь, могут успешно лечить рак, уменьшая заболеваемость раком и вызывая ремиссию рака. Термин «лечение» и его продолжения включают профилактику травмы, патологии, состояния или заболевания.
20) «Болезнь» или «состояние» относятся к состоянию здоровья пациента или субъекта, подлежащему лечению различными лекарственными средствами, дисперсиями, или другими методами, представленными в настоящем документе.
21) Используемый здесь термин «контрастный агент»/«контрастное средство» относится к композиции, которая при введении субъекту улучшает предел обнаружения или способность обнаружения физического метода, техники или устройства для медицинской визуализации (например, рентгенографический инструмент, рентген, КТ, ПЭТ, МРТ (MRI), ультразвук и другие методы). Контрастный агент может усилить величину сигналов, связанных с различными структурами или жидкостями внутри субъекта.
22) «Пациент» или «нуждающийся в этом субъект» относится к живому организму, страдающему или (возможно) склонному к заболеванию или состоянию, которое можно лечить путем введения лекарства, фармацевтической композиции или агента, как указано в настоящем документе. Неограничивающие примеры включают людей, других млекопитающих, быков, крыс, мышей, собак, обезьян, коз, овец, коров, оленей и других животных, не относящихся к млекопитающим. В частности, пациент может быть человеком.
23) Используемый здесь термин «компонент с контролируемым высвобождением» или «агент активируемый внешним воздействием» относится к соединению, которое в сочетании с композицией, описанной здесь (включая варианты осуществления), высвобождает в условиях применения (в пациенте) композицию с контролируемой скоростью. Такие соединения включают высокомолекулярные, анионные мукомиметические полимеры, гелеобразующие полисахариды и тонкодисперсные субстраты носителя лекарственного средства и другие. Эти компоненты более подробно обсуждаются в патентах США 4911920; 5403841; 5212162; и 4861760. Все содержание этих патентов включено в настоящее описание посредством ссылки во всей их полноте для всех целей. В некоторых вариантах осуществление «компонента с контролируемым высвобождением» может представлять собой замедленное высвобождение, продолжительное действие, продолжительное высвобождение, высвобождение во времени, синхронизированное высвобождение, контролируемое высвобождение, модифицированное высвобождение или соединение с непрерывным высвобождением. В некоторых вариантах осуществления, соединение распадается в месте введения (например, подкожного, внутривенного) или внутри пищеварительного тракта (например, желудка, кишечника), если соединение и композицию вводят перорально. В некоторых вариантах осуществления компонент с контролируемым высвобождением является полимером и может называться «полимер с контролируемым высвобождением». Кроме того, агент, активируемые внешним воздействием может активироваться (например, высвобождать терапевтический агент или связываться с мишенью) в результате воздействия внешним магнитным/электрическим полем, ультразвуком, светом, электронным пучком, в результате радиоактивного распада каких-либо атомов, в результате взаимодействия с химическими микроокружением и т.п.
24) Используемый здесь термин «парамагнитный агент»/«парамагнитное средство» относится к парамагнитному соединению, полезному в диагностических методах визуализации (например, магнитно-резонансная томография) в качестве контрастного агента. В некоторых вариантах осуществления парамагнитный агент включает гадолиний, оксид железа, платину железа или марганец.
25) Варианты цитотоксических средств (агентов, токсинов) включают, но не ограничиваются следующими веществами: рицин, доксорубицин, даунорубицин, таксол, бромид этидия, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, дигидроксиантрациндион, актиномицин D, дифтерийный токсин, экзотоксин Pseudomonas (PE) A, PE40, абрин и глюкокортикоид и другие химиотерапевтические агенты, а также радиоизотопы. Подходящие детектируемые маркеры включают, но не ограничиваются следующими веществами, радиоизотоп, флуоресцентное соединение, биолюминесцентное соединение, хемилюминесцентное соединение, хелатор металла или фермент.
26) Неполный список иммунологических анализов включает в себя: конкурентные и неконкурентные форматы, иммуноферментные анализы в плашке (ELISA), микроточечные анализы, вестерн-блоты, гель-фильтрацию и хроматографию, иммунохроматографию, иммуногистохимию, проточную цитометрию или сортировку клеток, помеченных флуоресцентной меткой (FACS), микрочипов и т. д. Такие методы также могут быть использованы in situ, ex vivo, in vitro или in vivo, например, для диагностической визуализации.
Следует отметить, что во всей заявке альтернативы записаны в группах Маркуша, например, каждое положение терапевтического агента, может содержать более одного возможного терапевтического агента. В частности, предполагается, что каждый член группы Маркуша следует рассматривать отдельно, тем самым, содержащий другой вариант осуществления, и группа Маркуша не должна читаться как единое целое.
Подробное описание изобретения
Далее будут описаны варианты осуществления настоящего изобретения более полно со ссылкой на прилагаемые чертежи, на которых приведены лишь некоторые, но не все варианты осуществления изобретения.
В рамках данного изобретения предложен:
Способ синтеза функциональных углеродных квантовых точек, которые включает следующие шаги:
i) раствор лимонной кислоты и мочевины автоклавируют при температуре 150-300 градусов Цельсия,
ii) отмывают полученные углеродные квантовые точки,
отличающийся тем, что дополнительно включает следующие шаги:
iii) смешение отмытых углеродных квантовых точек с раствором полимера,
iv) нагрев полученной смеси до 50-99 градусов Цельсия,
v) повышение ионной силы полученного раствора для высаживания упомянутого полимера на поверхность углеродных квантовых точек.
Кроме того, способ, в котором упомянутый рецептор или второй рецептор (распознающие) являются лектином, антителом, или иным «партнером для связывания» аналита.
Кроме того, способ и/или нанометка, в которых размер или средний размер упомянутых углеродных квантовых точек (до покрытия полимером) равен 10-15, 10-20, 20-30, 10-30, 10-100, 20-40, 10-50, 50-150 нм.
Кроме того, способ и/или нанометка, в которых размер или средний размер упомянутых углеродных квантовых точек, конъюгированных с полимером, равен 20-30, 30-40, 40-50, 20-50, 30-60, 20-70, 50-100, 30-80,30-100,30-150, 20-150, 40-200,20-200,20-300,20-400,100-200,200-300,100-300 нм.
Кроме того, способ и/или нанометка, в которых размер упомянутых углеродных квантовых точек, конъюгированных с полимером, равен 30 – 250 нм.
Кроме того, способ и/или нанометка, в которых размер упомянутых углеродных квантовых точек, конъюгированных с полимером, равен 50 – 150 нм.
Кроме того, способ и/или нанометка, в которых размер упомянутых углеродных квантовых точек, конъюгированных с полимером, равен 100 – 250 нм.
Кроме того, способ и/или нанометка, в которых упомянутая соль является сульфатом аммония.
Кроме того, способ и/или нанометка, в которых упомянутая соль является NaCl, Na2SO4, MgSO4, (NH4)2SO4, КСl, MgCl2.
Кроме того, способ и/или нанометка, в которых упомянутые углеродные квантовые точки конъюгированы с антителом против молекулярного маркера за счет высаживания упомянутого антитела против молекулярного маркера на поверхность углеродных квантовых точек путем нагревания и добавления соли к раствору, содержащему упомянутое антитело против молекулярного маркера и суспензию углеродных квантовых точек.
Кроме того, способ и/или нанометка, в которых упомянутый нагрев производят до 30,40,50,60,70,80,90,95,99,40-50,50-60,60-70,70-80,80-90,90-99,90-95,80-95,70-95,60-95,50-99 градусов Цельсия.
Кроме того, способ и/или нанометка, в которых упомянутый нагрев производят до 55-65 градусов Цельсия.
Кроме того, способ и/или нанометка, в которых упомянутый нагрев производят до 85-95 градусов Цельсия.
Кроме того, способ и/или нанометка, в которых упомянутый клеточный образец является биопсийным материалом.
Кроме того, способ и/или нанометка, в которых упомянутый клеточный образец является гистологическим срезом.
Кроме того, способ и/или нанометка, в которых упомянутый клеточный образец является образцом суспендированных клеток.
Кроме того, способ и/или нанометка, в которых упомянутый флуоресцентный сигнал детектируется (сигнал от УКТ) на длинах волн испускания 360-510 нм.
Кроме того, способ и/или нанометка, в которых упомянутый флуоресцентный сигнал возбуждается на длинах волн возбуждения 300-350,350-400,400-450,450-500,500-550,550-600,600-650,650-700,750-800,800-850.
Кроме того, способ и/или нанометка, в которых упомянутый флуоресцентный сигнал детектируется (излучается) на длинах волн испускания 350-400,400-450,450-500,500-550,550-600,600-650,650-700,750-800,800-850,850-900,900-950.
Кроме того, способ и/или нанометка, в которых упомянутый флуоресцентный сигнал возбуждается на длинах волн возбуждения 360-510 нм.
Кроме того, способ и/или нанометка, в которых упомянутый флуоресцентный сигнал возбуждается на длинах волн возбуждения 510-600 нм.
Кроме того, способ и/или нанометка, в которых упомянутый флуоресцентный сигнал детектируется (излучается) на длинах волн испускания 400-525 нм.
Кроме того, способ и/или нанометка, в которых упомянутый флуоресцентный сигнал детектируется (излучается) на длинах волн испускания 525-700 нм.
Кроме того, способ и/или нанометка, в которых при облучении светом в диапазон 360-510 нм возбуждается флуоресценция.
Кроме того, способ и/или нанометка, в которых при облучении светом в диапазон 510-600 нм возбуждается флуоресценция.
Кроме того, способ и/или нанометка, в которых при возбуждении флуоресценции эмиссия находится в диапазоне 400-525 нм.
Кроме того, способ и/или нанометка, в которых при возбуждении флуоресценции эмиссия находится в диапазоне 525-700 нм.
Кроме того, способ и/или нанометка, в которых упомянутый молекулярный маркер является клеточным маркером.
Кроме того, способ и/или нанометка, в которых упомянутый клеточный маркер выбран из ряда: EGFR, HER2, PD-L1, EpCAM, CEA, PSA, CA-125, CA 19-9, CA 15-3, CA 72-4, MUC1, CD19, CD20, CD44, CD133, CD166, CD24, CD47, CD117, DR-5.
Кроме того, способ и/или нанометка, используемые в диагностике заболеваний или состояний организма.
Кроме того, способ и/или нанометка, в которых упомянутый клеточный маркер является молекулярным маркером, экспрессируемым в цитоплазме клетки.
Кроме того, способ и/или нанометка, в которых повышение ионной силы упомянутого раствора, содержащего упомянутую нуклеиновую кислоты и суспензию упомянутых углеродных квантовых точек, достигается за счет добавления к упомянутому раствору соли.
Кроме того, способ и/или нанометка, в которых упомянутый раствор, содержащий упомянутую нуклеиновую кислоты и суспензию упомянутых углеродных квантовых точек, дополнительно содержит положительно заряженный полимер.
Кроме того, способ и/или нанометка, в которых упомянутый положительно заряженный полимер является одним из группы: полиэтиленимин, полилизин, D-полилизин,L-полилизин.
Кроме того, способ и/или нанометка, в которых упомянутая нуклеиновая кислота выбирается из ряда: ДНК, РНК, плазмидная ДНК, матричная РНК, антисенс ДНК, антисенс РНК, малая интерферирующая РНК, piwiРНК, микроРНК, аптамер.
Кроме того, способ и/или нанометка, используемые в генной терапии заболеваний или состояний организма.
Кроме того способ, в котором упомянутый аналит является малой молекулой.
Кроме того способ, в котором упомянутый аналит является белком.
Кроме того способ, в котором упомянутый аналит является нуклеиновой кислотой.
Кроме того способ, в котором упомянутая тест-полоска является иммунохроматографической тест-полоской, тонкослойной или аффинной хроматографической тест-полоской.
Кроме того способ, в котором упомянутая тест-полоска содержит в себе нитроцеллюлозную мембрану.
Кроме того способ, в котором упомянутую оценку яркости осуществляют при помощи оптических методов регистрации.
Кроме того способ, в котором детектирование количества задержавщихся на тест-линии частиц упомянутых углеродных квантовых точек осуществляют в течение менее чем 2, 3, 5, 7, 10, 15, 20 минут после начала анализа.
Кроме того, способ и/или нанометка, в которых упомянутое антитело моноклональное.
Кроме того, способ и/или нанометка, в которых упомянутое антитело поликлональное.
Кроме того, способ и/или нанометка, в которых упомянутый молекулярный аналог аналита представляет собой белок-носитель, конъюгированный с молекулами аналита.
Кроме того, способ и/или нанометка, в которых регистрации количества задержавшихся на тест-линии углеродных квантовых точек производится за счет регистрации их флуоресценции.
Кроме того, способ и/или нанометка, в которых дополнительно отмывают полученные функциональные квантовые точки с упомянутым полимером, от молекул несвязавшегося полимера.
Кроме того, способ и/или нанометка, в которых упомянутое отмывание полученных углеродных квантовых точек производят растворителем из набора: этанол, метанол, вода, ацетон.
Кроме того, способ и/или нанометка, в которых в упомянутом растворе лимонной кислоты и мочевины массовое отношении лимонной кислоты и мочевины находится в диапазоне от 3:1 до 1:5.
Кроме того, способ и/или нанометка, в которых в упомянутом растворе лимонной кислоты и мочевины массовое отношении лимонной кислоты и мочевины находится в диапазоне от 1:1 до 1:3.
Кроме того, способ и/или нанометка, в которых упомянутый полимер является одним из набора: белок, углевод, нуклеиновая кислота, полиэтиленимин.
Кроме того, способ и/или нанометка, в которых упомянутый полимер является гамма-иммуноглобулином.
Кроме того, способ и/или нанометка, в которых упомянутое автоклавирование проводят при температуре 190-210 градусов Цельсия.
Кроме того, способ и/или нанометка, в которых упомянутое автоклавирование проводят при температуре 120-130,130-140,140-150,150-160,160-170,170-180,180-190,190-200,200-210,150-180,180-210,200-230,200-250 градусов Цельсия.
Кроме того, способ и/или нанометка, в которых упомянутое повышение ионной силы полученного раствора для высаживания упомянутого биополимера на поверхность углеродных квантовых точек проводят за счет добавления к упомянутому полученному раствору раствор соли.
Кроме того, способ и/или нанометка, которые дополнительно включает шаг добавления кросс-сшивающего агента.
Кроме того, способ и/или нанометка, в которых упомянутый кросс-сшивающий агент выбран из списка: эпихлоргидрин, глутаровый альдегид.
Кроме того, способ и/или нанометка, в которых упомянутое отмывание полученных конъюгатов производят ультрафильтрацией.
Кроме того, способ и/или нанометка, в которых упомянутое отмывание полученных конъюгатов производят центрифугированием.
Кроме того, способ и/или нанометка, в которых упомянутый полимер является смесью нескольких полимеров.
Кроме того, способ и/или нанометка, в которых упомянутый полимер является одним из набора: белок, углевод, нуклеиновая кислота, полиэтиленимин.
Кроме того, способ и/или нанометка, в которых упомянутый полимер является гамма-иммуноглобулином.
Кроме того, способ и/или нанометка, в которых упомянутая люцифераза является одной из ряда: люцифераза nanoLuc, люцифераза светлячка, Renilla люцифераза, Gaussia люцифераза.
Кроме того, способ и/или нанометка, в которых упомянутая люцифераза является смесью нескольких люцифераз.
Кроме того, способ и/или нанометка, в которых при облучении светом в диапазон 360-510 нм возбуждается флуоресценция.
Кроме того, способ и/или нанометка, в которых при облучении светом в диапазон 510-600 нм возбуждается флуоресценция.
Кроме того, способ и/или нанометка, в которых при возбуждении флуоресценции эмиссия находится в диапазоне 400-525 нм.
Кроме того, способ и/или нанометка, в которых при возбуждении флуоресценции эмиссия находится в диапазоне 525-700 нм.
Кроме того, способ и/или нанометка, в которых упомянутый белок является одним из ряда: трансферрин, инсулин, эндостатин, гемоглобин, миоглобин, лизоцим, иммуноглобулины, α-2-макроглобулиновый белок, фибронектин, ламинин, коллаген, желатин, белковые компоненты липопротеинов, синтетические пептиды и белки, и их комбинации.
Кроме того, способ и/или нанометка, в которых упомянутый полимер является полисахаридом.
Кроме того, способ и/или нанометка, в которых упомянутый полисахарид является одним из ряда: декстран, карбоксиметилдектран, хитозан.
Кроме того, способ и/или нанометка, в которых упомянутый полимер является смесью нескольких полимеров.
Кроме того, способ и/или нанометка, в которых упомянутые углеродные квантовые точки конъюгированы с антителом против упомянутого аналита или молекулярным аналогом аналита за счет высаживания упомянутого антитела против упомянутого аналита или молекулярного аналога аналита на поверхность углеродных квантовых точек путем добавления соли к раствору, содержащему упомянутое антитело против упомянутого аналита или молекулярный аналог аналита и суспензию углеродных квантовых точек, и его нагревания.
Кроме того, способ и/или нанометка, в которых поверхность твердой фазы является поверхностью многолуночного планшета.
Кроме того, способ и/или нанометка, в которых поверхность твердой фазы является поверхностью 96-, 384- ил 1536-луночного планшета.
Кроме того, способ и/или нанометка, в которых упомянутую регистрацию детектируемого сигнала осуществляют при помощи оптических методов регистрации, при помощью регистрации флуоресценции, люминесценции, биолюминесценции, фосфоресценции.
Кроме того, способ и/или нанометка, в которых упомянутый фермент является выбранным из группы: пероксидаза, фосфатаза, люцифераза.
Кроме того, способ и/или нанометка, в которых упомянутый фермент является нативной формой фермента, выбранного из группы: пероксидаза хрена, щелочная фосфатаза, кислая фосфатаза, люцифераза nanoLuc, люцифераза светлячка, термостабильная люцифераза, Renilla люцифераза, Gaussia люцифераза.
Кроме того, способ и/или нанометка, в которых упомянутый фермент является генно-инженерно мутированной формой фермента, выбранного из группы: пероксидаза хрена, щелочная фосфатаза, кислая фосфатаза, люцифераза nanoLuc, люцифераза светлячка, термостабильная люцифераза, Renilla люцифераза, Gaussia люцифераза.
Кроме того, способ и/или нанометка, в которых упомянутый субстрат является субстратом, выбранным из группы: хромогенный субстрат, флуорогенный субстрат, или хемилюминесцентных субстрат.
Кроме того, способ и/или нанометка, в которых упомянутое антитело является выбранным из группы: аммаиммуноглобулин, иммуноглобулин G1 (IgG1), иммуноглобулин G2 (IgG2), иммуноглобулин G3 (IgG3), иммуноглобулин G4 (IgG4), иммуноглобулин M, иммуноглобулин A, иммуноглобулин E, иммуноглобулин D, Fab-фрагмент антитела, Fab'-фрагмент антитела, Fab'2-фрагмент антитела, F(ab')2-фрагмент антитела, scFv-фрагмент антитела, нанободи, scFv-Fc фрагменты, scFv-scFv (диабоди), биспецифические scFv фрагменты, Fab-scFv-фрагмент антитела.
Кроме того, способ и/или нанометка, в которых упомянутое антитело является генно-инженерным аналогом из группы: авимеры, адгироны, аднектины, монободи, атриметры, антикалины, аффибоди, аффилины, аффимеры, аффитины, нанофитины, дарпины, кноттины, ободи, полипептиды на основе домена Кунитца, пронектины, репебоди, финомеры, центирины, ADAPT (ABD-Derived Affinity Proteins), NanoCLAMP (nano-CLostridial Antibody Mimetic Proteins), ARM (Armadillo repeat proteins), PDZ белки.
Кроме того, способ и/или нанометка, в которых упомянутый молекулярный аналог аналита представляет собой белок-носитель, конъюгированный с молекулами аналита.
Кроме того, способ и/или нанометка, в которых для уточнения точности анализа, дополнительно регистрируют флуоресцентный сигнал от углеродных квантовых точек, связавшихся с упомянутой поверхностью твердой фазы, как меру содержания аналита в образце, а затем усредняют полученные меры содержания аналита в образце для уточненной меры содержания аналита в образце.
Кроме того, способ и/или нанометка, в которых для уточнения точности анализа, дополнительно регистрируют флуоресцентный сигнал от углеродных квантовых точек, связавшихся с упомянутой поверхностью твердой фазы, как меру содержания аналита в образце, а затем усредняют полученные меры содержания аналита в образце для уточненной меры содержания аналита в образце.
Углеродные квантовые точки (УКТ) являются уникальным материалом для биомедицинских применений благодаря присущим им оптическим свойствам и биосовместимости. Однако на сегодняшний день не существует универсальной процедуры конъюгации УКТ с биополимерами, что существенно снижает их практическую ценность.
В данной работе мы открыли новый сверхбыстрый метод конъюгации УКТ с биомакромолекулами, включая белки, нуклеиновые кислоты и углеводы. Метод основан на быстром нагреве УКТ биополимерным раствором с последующим этапом высаливания, который заставляет биополимер осаждаться на поверхности УКТ и одновременно служит фазой очистки. Используя практически один и тот же протокол HSO, мы успешно использовали УКТ в иммунохроматографическом анализе (конъюгация с антителами к хлорамфениколу), в иммуноферментном анализе (одновременная конъюгация с nLuc или HRP и антихлорамфениколом), в специфическом нацеливании клеток (конъюгация с герцептином), в доставке генов (конъюгация с полиэтиленимином и плазмиодй nanoLuc).
Предложенная процедура может значительно повысить ценность УКТ для широкого спектра биомедицинских применений.
Синтез и определение характеристик УКТ
Синтез УКТ проводился сольвотермическим путем. Полученная сложная смесь продуктов после синтеза была сначала разделена по гидрофильности (с помощью осаждения этанолом и последующим центрифугированием), как и в оригинальной работе. Однако, далее, мы дополнительно удаляли крупные частицы центрифугированием; а побочные продукты низкой молекулярной массы удалялись с помощью ультрафильтрации.
Синтез УКТ проводили в соответствии со следующим протоколом. 1 г лимонной кислоты и 2 г мочевины растворяли в 8 мл формамида, а объем доводили формамидом до 10 мл. Раствор переносили в автоклав с тефлоновым покрытием, и помещали в предварительно разогретую до 160°С термостат ED56 Binder (Туттлинген, Германия) на 4 часа. Затем автоклав сразу же охлаждали под проточной водой.
Полученную темно-оранжевую смесь вместе с агрегатами переносили в пробирку объемом 50 мл, и добавляли 20 мл этилового спирта. Полученную смесь центрифугировали при 10000 g в течение 5 мин. Надосадочную жидкость выбрасывали, добавляли 2 мл воды. Пробирку обрабатывали ультразвуком до полного растворения гранулы (~ 1-2 мин), а объем доводили до 10 мл водой. Процедуру повторяют еще раз. Полученный раствор УКТ в воде центрифугировали при 10000 g в течение 5 мин для удаления крупных агрегатов. Затем полученную надосадочную жидкость переносили в новую пробирку.
Заключительным этапом промывки была ультрафильтрация через регенерированную целлюлозную мембрану MWCO 100 кДа. УКТ фильтровали под давлением около 3 бар в режиме промывки. Промывку проводили до тех пор, пока диализат не станет почти неокрашенным (в начале фильтрации диализат темно-оранжевый) примерно в течение 1 часа.
Затем ретентат аликвотировали и хранили при -20 ° С. После размораживания аликвоту центрифугировали при 15000 г в течение 5 мин, а надосадочную жидкость использовали для дальнейших опытов в течение 1-2 суток после размораживания.
Далее, мы изучили полученные УКТ с помощью просвечивающей электронной микроскопии (Рис. 1а). По микрофотографиям мы определили, что УКТ имеют околосферическую форму со средним диаметром 31 ± 7 нм.
Для изучения физико-химических свойств УКТ в растворе, мы провели исследование УКТ методом динамического светорассеяния (Рис. 1c, d). Гидродинамический размер составил (26 ± 4 нм), а дзета-потенциал -33 ± 7 мВ.
Интересно, что и гидродинамический диаметр, и размер, полученные нами по микрофотографиям ПЭМ больше соответствующих значений, описанных в оригинальной работе (1-7 нм). Возможно, это связанно с введенным нами этапом ультрафильтрации.
Далее, мы изучили наличие химических функциональных групп на поверхности УКТ с помощью ИК-спектроскопии с преобразованием Фурье (Рис. 1b).
Широкая полоса на 3122 см-1 может быть отнесена к валентной вибрации O-H как в карбоновой кислоте, так и в спирте. Пик 1657 см-1 может указывать на растяжение валентной С=О в карбоновой кислоте, амиде или альдегиде. Эти два пика подтверждают наличие групп карбоновых кислот. Далее, узкая полоса на 1098 см-1 указывает на растяжение валентного С-О в спирте или в эфире. Теперь мы можем констатировать наличие алкогольных групп в образце УКТ. Наконец, назначаем пики на 1339 и 1395 см-1 деформационным колебаниям O-H, и слабому пику на 2785 к валентным C-H вибрациям.
Далее, мы изучили оптические свойства УКТ. Спектр поглощения имеет два пика – на 370 нм и на 517 нм (Рис. 1e). Второй из этих пиков придает УКТ насыщенный фиолетовый цвет, напоминающий цвет золотых наночастиц.
Тепловая карта возбуждения/излучения флуоресценции (Рис. 1f) выявляет две различные области флуоресценции. Первый расположен в области возбуждения 350-450 нм. В этой области расположение пика излучения зависит от длины волны возбуждения. В области возбуждения 470-590 нм спектр излучения фиксирован, с пиком излучения на длине волны 636 нм. Максимальная интенсивность флуоресценции наблюдается при параметрах возбуждения/излучения 530/630.
Одним из часто используемых методов для покрытия наночастиц с помощью полимеров – это пассивная адсорбция полимера при повышенных температурах. Здесь, мы попробовали адаптировать эту стратегию для УКТ.
Мы нагрели раствор УКТ с БСА при 90 ˚C в течение 1 мин. В результате нагрева, наблюдалось значительное усиление флуоресценции УКТ (Рис 2a), видимое невооруженным глазом. Это изменение в флуоресценции указывает на то, что произошло связывание УКТ и биолполимера (в данном случае БСА).
Здесь и далее, мы используем двоеточие «:» чтобы обозначить конъюгации УКТ с биполомером. В данном случае, были полученны УКТ:БСА. Если два или более биополимера иммобилизуются на поверхности УКТ, они разделяются запятой, например УКТ:(биополимер1, биолполимер2).
Однако, получаемые покрытые УКТ обладали высокой степенью коллоидной стабильности – конъюгаты не формировали осадка при центрифугировании при 15000g в течение 30 мин. Это означает, что очистка таких конъюгатов от побочных продуктов и несвязавшегося биополимера представляет собой нетривиальную задачу.
Поэтому, мы решили применить метод высаливания, который, например, является рутинным для разделения белков плазмы крови.
Конъюгаты резко смешивались с раствором аммония сернокислого (АС) в концентрации 5-50%. Добавление АС мгновенно нарушало коллоидную стабильность наночастиц, и конъюгаты центрифугировались при 15000 g в течение 5 минут. Полученный осадок ресуспендировали в желаемом буфере.
Несмотря на то, что мы задумывали высаливание как этап очистки, далее будет показано, что оно играет ключевую роль в формировании конъюгатов.
Покрытие УКТ полисахаридами
Далее, мы применяем описанную стратегию покрытия УКТ полисахаридами. Для демонстрации концепции мы выбирали хитозан и декстран. Оба полисахарида являются популярным выбором для покрытия различных наночастиц, поскольку они, как правило, повышают стабильность, биосовместимость и биодоступность наночастиц.
Конъюгацию полисахаридов с УКТ проводили в тех же условиях, что и при БСА. Чтобы доказать наличие полимеров на поверхности точек, мы провели иммунохроматографичкий анализ. Использовались соответствующие лектины, а именно агглютинин зародышей пшеницы (WGA), связывающий N-ацетил-D-глюкозамин, являющийся ацетилированной мономером хитозана; и конканавалин А, связывающий D-глюкозу, мономер декстрана.
Лектины иммобилизовали на тестовых полосках, а полоски погружали в раствор, содержащий конъюгаты. Отрицательный контроль осуществлялся путем предварительного смешивания конъюгатов с избытком соответствующего лектина.
Оба конъюгата демонстрировали сильное связание с тест-полосками, при этом, связывание было значительно слабее для конъюгатов, предварительно смешанных с лектинами (Рис. 2b, c), что указывает на присутствие полисахаридов на поверхности УКТ.
Конъюгаты УКТ с антителами
Конъюгация антитела с наночастицей позволяет последней специфически распознавать заранее заданую биомолекулу. Такие конъюгаты лежат в основе многих лечебных и диагностических подходов.
В этом разделе мы используем HSO для получения конъюгатов УКТ с антителами к хлорамфениколу (ХАФ) и с антителами трастузумаб к рецептору эпидермального фактора роста человека 2 (HER2) и показываем их значение для диагностического и терапевтического применения.
Обнаружение ХАФ с помощью иммунохроматографии и конъюгатов УКТ:(Анти-ХАФ)
Левомицетин (ХАФ) является антибиотиком широкого спектра действия, запрещенным к применению для пищевых животных, включая коров и медоносных пчел. Разработка методов обнаружения ХАФ в пищевых продуктах в следовых количествах является важной задачей для пищевой промышленности.
Одним из популярных методов выявления ХАФ является иммунохроматографический анализ (ИХА), учитывая его быстроту и чувствительность. Схема анализа приведена на рисунке 3а.
Конъюгаты УКТ:(Анти-ХАФ) были способны специфически связываться на тестовой линии, репрезентативную фотографию тест-полосок, демонстрирующую отсутствие (слева, сильное связывание) или присутствие (справа, без связывания) ХАФ в образце (Рис. 3b, c). Предел детекции (3σ-критерий) тест-системы составил 9 нг/мл (2,1 мкМ).
Мы полагаем, что последующая оптимизация различных параметров конъюгации и анализа, таких как афинность антител, молярное отношение УКТ и антител, состав миграционного буфера, может существенно снизить предел детекции, чтобы удовлетворить высокие требования к чувствительности в реальных применениях.
Нацеливание клеток с помощью конъюгатов УКТ:(Анти-HER2)
Наноагенты, способные селективно связывать определенный тип клеток, являются мощным средством точечного воздействия на сложную биологическую систему, например, для подавления опухолевых клеток с минимальным воздействием на нормальные клетки. В этом примере часто используемой мишенью является HER2, рецептор, чрезмерно экспрессируемый раковыми клетками при многих типах рака молочной железы и почти отсутствующий на поверхности здоровых клеток. Для связывания рецептора часто используется одобренное FDA моноклональное гуманизированное антитело трастузумаб (Анти-HER2).
Используя метод HSO, мы получили конъюгаты УКТ:(Анти-HER2) и изучили их способность к специфическому связыванию in vitro с использованием клеточных линий EMT6/P (отрицательный контроль) и EMT6/P-HER2. Взаимодействие клеток и наночастиц проводили с помощью проточного цитометра, а связывание с клетками количественно оценивали с помощью флуоресценции УКТ (Рис. 3d).
Конъюгаты, связанные с HER2-положительными клетками, более чем в три раза эффективнее по сравнению с HER2-отрицательными клетками, что количественно определяется индексом окрашивания (0,56 и 0,18), что лежит в основе их потенциала в приложениях для нацеливания на клетки.
Оптимизация синтеза конъюгатов УКТ:(антитело)
Как и в случае с БСА, флуоресцентные свойства конъюгатов (продемонстрированные на УКТ:(Анти-HER2)) были значительно изменены по сравнению с исходными УКТ.
Интенсивность флуоресценции (F) на длине волны 530/630 нм усиливалась с повышением температуры синтеза (T) (Рис. 3e). Данные подгонялись степенной функцией F(T) = F0 +α (T – T 0)β, где F0, α, β трактовались как неизвестные параметры, а T0 – комнатная температура (25 °C). Наиболее подходящий β оказался равным 5.6, что указывает на резкий характер роста с более чем трехкратным усилением флуоресценции при T = 90 °C по сравнению с УКТ без покрытия.
Однако интенсивность флуоресценции при возбуждении на 350-450 нм сильно ослаблялась независимо от температурного синтеза. Это затухание, вероятно, связано с сосуществованием двух субпопуляций УКТ, одна из которых не осаждается АС и теряется на стадии промывки.
С другой стороны, температура синтеза также влияет на активность антител. Затем было изучено влияние температуры синтеза и, дополнительно, рН синтеза для конъюгатов УКТ:(Анти-ХАФ) (Рис. 3 f, g). Для количественной оценки активности антител мы измеряли связывание конъюгатов с тест-линией в МАФ. Мы предполагаем, что более сильное связывание отражает присутствие более активных молекул антител в конъюгате, и наоборот.
Конъюгаты, полученные при температуре 70 ° С и ниже, связываются с тест-полоской почти одинаково сильно. Однако при более высоких температурах связывания почти не наблюдалось. Таким образом, температуры в районе 60-70 ° С являются оптимальными с точки зрения усиления флуоресценции УКТ и активности антител.
Изучено влияние рН синтеза на активность конъюгатов. рН исследовался в нейтральной и щелочной областях, так как ожидается, что кислый рН нарушит коллоидную стабильность УКТ, поскольку они, предположительно, стабилизируются группами карбоновых кислот. Любопытно, что для исследуемой области рН 7,5 – 10 поведение конъюгатов в одном и том же тесте ИХА практически не зависело от рН.
Добавление ферментативной модальности к конхюгатам УКТ с антителами.
Далее мы стремились разработать конъюгаты УКТ:(антитело), добавив еще одну, ферментативную модальность.
Мы выбрали два фермента: пероксидазу хрена (HRP) и люциферазу nanoLuc. Окисляя соответствующий субстрат, HRP производит окрашенный продукт, легко определяемый колориметрически, а nanoLuc генерирует биолюминесценцию. Оба фермента широко используются в рутинной клинической диагностике, например, в иммуноферментном анализе (ИФА).
Методом HSO получены конъюгаты УКТ:(Анти-ХАФ, HRP) и УКТ:(Анти-ХАФ, nanoLuc). Благодаря антителу Анти-ХАФ конъюгаты способны селективно связывать антиген, и в то же время могут быть обнаружены как по ферментативной активности, так и по флуоресценции УКТ.
Такие конъюгаты могут быть естественным образом использованы в ИФА в качестве репортерных сущностей, по аналогии с конъюгированными ферментами вторичными антителами. Таким образом, мы провели прямой ИФА детектирование ХАФ (Рис. 4a), используя УКТ:(Анти-ХАФ, HRP) и УКТ:(Анти-ХАФ, nanoLuc) в качестве репортеров (Рис. 4 b, c).
Кривая «доза-реакция», полученная при флуоресцентном детектировании, как правило, имеет тот же профиль, что и при ферментативном детектировании.
Как и в случае с антителами, была исследована зависимость активности конъюгированных ферментов от рН и температуры синтеза. Оба белка были наиболее активны при более нейтральном рН и менее активны при более щелочном рН, но не теряли активности полностью.
Интересно, что для HRP-конъюгатов зависимость активности от температуры не монотонна, а имеет пик при 70 ° С. Вероятно, более высокие температуры способствуют адсорбции белка на поверхности УКТ, но, в то же время, способствуют денатурации белка и тем самым снижают его активность.
Доставка генов (трансфекция) конъюгатами УКТ:(ПЭИ, плазмида).
Далее, чтобы расширить класс биополимеров, с которыми возможна конхюгация HSO, мы применили ту же стратегию для конъюгации нулкеиновых кислот. Выбор той или иной нуклеиновой кислоты был обусловлен двумя факторами: (i) это должен быть скорее длинный полимер, чем олигомер, так как мы ожидаем, что HSO будет более эффективен для более длинных полимеров; (ii) его присутствие в живой клетке должно быть легко обнаружено; (iii) канал обнаружения должен быть ортогонален флуоресценции УКТ. Для удовлетворения этих требований была выбрана плазмидная ДНК, кодирующая белок люциферазы nanoLuc (3kb, промотор CMV).
Однако из-за электростатического отталкивания между ДНК и УКТ, которые заряжены отрицательно, процесс адсорбции ДНК на УКТ не почти не идет. Поэтому, мы также ввели в систему положительно заряженный линейный полиэтиленимин (ПЭИ), который будет служить медиатором между точками и ДНК. Таким образом, мы применили двухэтапную процедуру: УКТ сначала конъюгировали с PEI, промывали, а затем конъюгировали с плазмидой. Для любого из них использовалась температура 90 °C, чтобы максимизировать выход полимера и флуоресценцию УКТ, так как не ожидается, что плазмида потеряет функциональную активность при нагревании.
Измерение содержания ДНК на поверхности УКТ
Чтобы подтвердить успешную конъюгацию, мы измерили выход ДНК с помощью красителя SYBR gold. При анализе к образцу добавляется ДНК-краситель SYBR gold, и флуоресценция красителя увеличивается в >1000 раз при связывании ДНК, которая затем сравнивается с калибровочной кривой, и извлекается концентрация. Однако такой подход не учитывает того факта, что УКТ частично поглощает флуоресценцию SYBR, что приводит к завышению выхода.
Для решения этой проблемы каждая точка калибровочной кривой была измерена в присутствии образца УКТ:(ПЭИ, плазмида) (Рисунок 5a). Далее вычитали флуоресценцию УКТ, и находили пересечение с осью абсцисс градуировочной кривой, что соответствует искомой концентрации. Типичный выход плазмиды составил около 10%.
Трансфекция с УКТ:(ПЭИ, плазмида)
Далее мы исследовали способность конъюгатов трансфицировать живые клетки (Рис. 5b). Клетки HEK293 снабжали конъюгатами УКТ:(PEI, плазмида), содержащими 1, 5, 10, 30 или 50 нг плазмиды на лунку 96-луночной пластины. Для сравнения, также была проведена обычная трансфекция с ПЭИ с тем же содержанием плазмиды.
Зависимость эффективности трансфекции от используемой концентрации плазмиды (Рис. 5b) для конъюгатов имеет оптимум при 10 нг, и при этой концентрации конъюгаты УКТ:(PEI, плазмида) превосходят обычную трансфекцию ПЭИ почти в три раза. Однако при более высоких концентрациях УКТ имеет тенденцию к агрегации и образованию пленок вместе с крупными макроскопическими агломератами. Несмотря на то, что УКТ остается практически нетоксичным в этих концентрациях, как показал резазуриновый тест на токсичность (Рис. 5c), образующиеся пленки и агрегаты, вероятно, препятствуют проникновению новых порций трансфектанта в клетки, тем самым уменьшая количество производимого белка-репортера.
Кроме того, УКТ может помочь отслеживать конъюгаты внутри клеток (Рис. 5d). Клетки, обработанные УКТ:(PEI, плазмида), демонстрируют ярко-красную флуоресценцию (возбуждение, излучение 560/603). Флуоресценция может быть использована, например, для независимой оценки процента трансфицированных клеток.
Образование конъюгатов
В двухступенчатом процессе нагрева стадия высаливания, по видимости, является основной, а стадия нагрева необязательна, но полезна из-за значительного увеличения флуоресценции. Например, на Рис. 3f конъюгаты, полученные без нагревания, все же показали высокую функциональную активность.
Растворенный сульфат аммония сильно гидратирован и в высоких концентрациях конкурирует за молекулы воды с биополимером, что снижает растворимость полимера и способствует самоагрегации.
Масштабируемая экспериментальная установка может быть использована совместно с предлагаемой методикой конъюгации УКТ, например, раствор УКТ и биополимера может быть смешан с раствором AS в микрофлюидном чипе. Это позволит получить более точный контроль над структурой сопряжения, плотностью покрытия, конформацией биополимера на поверхности УКТ и т.д.
Эффективность очистки от соли
Основным недостатком конъюгации HSO является ее нековалентная природа, подразумевающая, что конъюгированный биополимер потенциально может десорбироваться с поверхности УКТ. Мы не смогли обнаружить воздействие несвязанного полимера в конкретных приложениях. Возможно также, что взаимодействие полимера и УКТ на самом деле может быть необратимым, несмотря на то, что оно не ковалентно.
Универсальность технологии конъбюгации в отношении биополимеров
Тем не менее, нам удалось конъюгировать УКТ с различными классами биополимеров, очевидно, что можно встретить биополимер, который не может быть конъюгирован при таком подходе. Ниже мы перечислим потенциально проблемные случаи:
А. Ожидается, что сильно отрицательно заряженные биополимеры не образуют конъюгаты с высоким выходом из-за электростатического отталкивания с поверхностью УКТ. Тем не менее, с ней можно справиться, введя положительный адаптер (как показано на примере конъюгации плазмид)
Б. Полимеры, не восприимчивые к АС, т.е. растворимые даже при высоких концентрациях АС, также могут быть трудно конъюгированы. Такого поведения мы ожидаем, например, от полимеров с короткой длиной цепи.
Общность технологии конъюгации в отношении УКТ
Помимо конъюгации биополимеров с УКТ, подробно описанных выше, данная технология конъюгации позволила конъюгировать с биополимерами большое разнообразие УКТ синтезированных по другим протоколам и методам. Из чего, можно конститировать, что данная технология универсальна по отношению к различными УКТ.
Разработанная технология получения функционализированных УКТ и конъюгации УКТ с биомполимерами представляет собой универсальный подход к функционализации углеродных квантовых точек с белками, углеводами, нуклеиновыми кислотами или другими биополимерами. Технология характерная быстротой процедуры и простотой этапа очистки.
Различные аспекты
Описанные выше детальные описания не ограничивают круг возможностей и применения изобретения, а лишь даны для удобства.
Различные биополимеры
В одном воплощении изобретения конъюгируют УКТ с полимером из группы: белками, нуклеиновыми кислотами, полисахаридами и другими. В частности, были получены конъюгаты с: иммуноглобулинами (в .ч. IgG, IgM), лектинами, пероксидазами, люциферазами, альбуминами, ДНК, РНК, плазмидной ДНК, матричной РНК, антисенс ДНК, антисенс РНК, малая интерферирующей РНК, piwiРНК, микроРНК, аптамер., антисенс-ДНК, декстраном, карбоксиметилдекстраном, хитозаном, полиэтиленимином, полиэтиленгликолем, полиакриловой кислотой.
В одном воплощении изобретения упомянутым белком может быть: сывороточный альбумин, трансферрин, голо-трансферрин, ферменты (
В одном воплощении изобретения упомянутое антитело может быть гаммаиммуноглобулин, иммуноглобулин G1 (IgG1), иммуноглобулин G2 (IgG2), иммуноглобулин G3 (IgG3), иммуноглобулин G4 (IgG4), иммуноглобулин M, иммуноглобулин A, иммуноглобулин E, иммуноглобулин D, Fab-фрагмент антитела, Fab'-фрагмент антитела, Fab'2-фрагмент антитела, F(ab')2-фрагмент антитела, scFv-фрагмент антитела, нанободи, scFv-Fc фрагменты, scFv-scFv (диабоди), биспецифические scFv фрагменты, Fab-scFv-фрагмент антитела.
Кроме того, упомянутое антитело является генно-инженерным аналогом из группы: авимеры, адгироны, аднектины, монободи, атриметры, антикалины, аффибоди, аффилины, аффимеры, аффитины, нанофитины, дарпины, кноттины, ободи, полипептиды на основе домена Кунитца, пронектины, репебоди, финомеры, центирины, ADAPT (ABD-Derived Affinity Proteins), NanoCLAMP (nano-CLostridial Antibody Mimetic Proteins), ARM (Armadillo repeat proteins), PDZ белки.
Применяемые белки для данного аспекта изобретения могут включать, но не ограничиваться следующими: альбумин, трансферрин, инсулин, эндостатин, гемоглобин, миоглобин, лизоцим, иммуноглобулины, α-2-макроглобулиновый белок, фибронектин, ламинин, коллаген, желатин, белковые компоненты липопротеинов, синтетические пептиды и белки, и их комбинации. Примеры подходящих белков включают, но не ограничиваются следующими: альбумин, трансферрин, инсулин, эндостатин, гемоглобин, миозин, лизоцим, иммуноглобулины, α-макроглобулин, фибронектин, ламин, коллаген,Apo–A1, желатин, искусственные белки и их комбинации.
Кроме того, для получения белковых наночастиц в рамках изобретения могут быть использованы сыворотка крови, плазма крови, цельная кровь.
Созданные конъюгаты с данными полимерами показали высокую специфичность связывания со своей мишенью (лигандом, партнером для связывания).
Различные соли
В одном воплощении изобретения упомянутое высаливание полимера на УКТ (высаживание) проводили различными солями. Помимо наиболее эффективного сульфата аммония, были использованы NaCl, Na2SO4, MgSO4, КСl, MgCl2.
Нагревание
В одном воплощении изобретения упомянутый нагрев производят до 45-50 градусов Цельсия, 50-60 градусов Цельсия, 60-70 градусов Цельсия, 70-80 градусов Цельсия, 80-90 градусов Цельсия, 90-99 градусов Цельсия, 90-95 градусов Цельсия, 95-99 градусов Цельсия.
В одном воплощении изобретения упомянутый нагрев производят в течение 1-5 мин, 1-10 мин, 1-20 мин, 1-30мин, 1-60мин, 1-180 мин, 1-500 мин, 1-2000 мин, 5 сек, 10 сек, 30 сек, 1 мин, 2 мин, 3 мин, 5мин, 7 мин, 10мин, 30 мин, 60 мин, 180 мин, 10 часов.
В одном воплощении изобретения упомянутый нагрев производят со скоростью повышения температуры в 0.1, 0.3, 1, 3, 10, 30, 100, 300 градус/мин.
В одном воплощении изобретения упомянутый нагрев производят в объеме (стационарной жидкости), в микрофлюидном каналя(ячейке), в потоке.
В одном воплощении изобретения упомянутый нагрев производят микроволновым облучением.
Микроскопический и цитометрический анализ
Упомянутый клеточный маркер может быть любым клинически-значимым маркером, в частности были созданы УКТ, специфично распознающие EGFR, HER2, PD-L1, EpCAM, CEA, PSA, CA-125, CA 19-9, CA 15-3, CA 72-4, MUC1, CD19, CD20, CD44, CD133, CD166, CD24, CD47, CD117, DR-5.
Регистрация сигнала
Детектируемый сигнал регистрируется качественно, полуколичественно или количественно визуально или на различном оборудовании: флуоресцентный микроскоп, цитометр, цитофлуориметр, флуориметр, люминометр.
Кросс-сшивка
В одном воплощениии метода есть дополнительный шаг кросс-сшивки наночастиц (УКТ с полимером) для стабилизации состава, предотвращения десорбции и т.п.
для кросс-сшивки наночастиц, их смешивают с бифункциональными кросс-линкерами. Это может быть глутаровый альдегид, формальдегид, диглицидиловый эфир, генипин и т.п. В одном воплощении метода, используют такой кросс-линкер, который оставляет частицы или делает их высокоспецифичными с точки зрения распознавания/связывания со своей биологической мишенью. В частности, кросс-сшивка формальдегидом или диглицидиловым эфиром предпочтительнее использования глутарового альдегида, т.к. как правило позволяет добиться более специфичных частиц. В то же время, для таких задач как неспецифическая трансфекция клеток генетическим материалом предпочтительно использовать кросс-сшивающий агент, который приводит не к избирательности частиц, а наоборот позволяет им высокоэффективно связываться с различными мишенями. Так, например, глутаровый альдегид приводит к образованию оснований Шиффа, которые обладают частичным положительным зарядом, а потому будут эффективно выполнять задачу связывания ДНК (которая заряжена отрицательно) для целей доставки генетического материала в клетки.
Методы иммобилизации связывающих рецепторов на мембране тест-полоски хорошо известны. Как правило, тестовый и контрольный связывающие рецепторы наносятся на мембрану параллельными линиями на расстоянии друг от друга. Растворы с необходимыми веществами в соответствующих буферах наносятся на тестовые полоски с помощью автоматизированных дозаторов. После высушивания на воздухе в течение необходимого времени, проводят блокировку мембраны в подходящем буфере и хранят в эксикаторе перед сборкой тест-полоски в единое целое.
Скорость проведения анализа с помощью предлагаемого изобретения значительно выше стандартных методов анализа при сохранении точности и достоверности результатов. На измерение в данном случае в среднем уходит от 10 до 300 сек. Тем не менее, возможно увеличить чувствительность, если использовать большее время проведения анализа. Кроме того, принцип данного изобретения позволяет проводить прямое измерение определяемого нуклеиновой кислоты в качестве аеалита без необходимости её амплификации при условии, что ее концентрация выше предела детекции, и связанный с ней сигнал может быть зафиксирован, например, невооруженным глазом.
Измерения с использованием метода в рамках данного изобретения могут проходить как в жестких, так и в мягких условиях. Под «жесткими» условиями подразумеваются такие значения температуры, ионной силы, а также наличие других соединений, при которых происходит гибридизация нуклеиновых кислот. В условиях «высокой жёсткости» гибридизация будет происходить только для нуклеиновых кислот, имеющих высокое содержание комплементарных азотистых оснований. Таким образом, мягкие условия требуются в том случае, когда необходима гибридизация или отжиг не полностью комплементарных нуклеиновых кислот. Специалистам известен целый ряд методов создания мягких условий для протекания гибридизации. Гибридизация же в жёстких условиях возможна только в случае полной комплементарности последовательностей. Гибридизация в менее жёстких условиях возможна для последовательностей с менее чем 100% идентичностью. Изменения условий среды, такие как снижение концентрации соли или повышение температуры, могут позволить уменьшить жёсткость условий гибридизации. Ужесточение условий гибридизации можно добиться за счет снижения ионной силы или повышения температуры гибридизации.
Таким образом, в одном из вариантов реализации данного изобретения вместо использования упомянутого антитела в качестве распознающего элемента, возможно использовать ДНК/НК рецепторы. При этом возможно проводить одностадийное, полнофункциональное определение специфических молекул ДНК или РНК в иммунохроматографическом формате анализа, при котором все необходимые реактивы находятся на тест-полоске в безводном виде. С другой стороны, данное изобретение дает возможность прямого определения НК без необходимости их амплификации и предоставляет метод их быстрого обнаружения.
Кроме того, в своих альтернативных вариантах реализации изобретение применимо и для обнаружения НК в условиях повышенной температуры, что расширяет область его использования в различных областях, например, для проведения судебно-медицинской экспертизы. В дополнении к этим преимуществам описанный метод является простым способом детекции нуклеиновых кислот и не требует серьёзных подготовки в этой области, что может облегчить проникновение методов геномного экспресс-анализа в область диагностики у постели больного и по месту оказания медицинской помощи.
Аналиты
Настоящее изобретение позволяет детектировать широкий круг молекулярных аналитов, включая нуклеиновые кислоты и полинуклеотидные последовательности, в том числе фрагменты и целые молекулы ДНК, а также транспортные, матричные, рибосомальные, микро РНК; синтетические аналоги нуклеиновых кислот, такие как пептидные НК, морфолиновые, закрытые, гликолевые и треозо-НК; а также, за счет использования особенных распознающих олигонуклеотидов (например, аптамеров) также молекулы ненуклеотидного состава, например, белки и пептиды, гормоны, низкомолекулярные физиологические регуляторы, иные гаптены, ионы металлов, и т.д.
Калибровочная кривая
В одном воплощении метода для количественной оценки содержания аналита в образце (измерения концентрации), дополнительно делают шаг сравнения полученных результатов с калибровочной кривой, измеренной для образцов с известным содержанием аналита.
Мультиплексность
Данный метод применим и для определения нескольких аналитов одновременно. В простейшем формате тестовая полоска может быть разделена на отдельные полоски, где будут нанесены отдельные зоны связывания для обнаружения различных аналитов. Кроме того, также возможно реализовать одновременную детекцию разных аналитов в одном образце. Для этого, например, отдельные зоны связывания могут быть нанесены на одну мембрану, но в её разных участках.
Специфические пары рецептор/лиганд
В рамках данного изобретения (в т.ч. вместо упомянутых антител) могут быть использованы различные специфические пары типа «рецептор/лиганд», применимые для создания сигнальных (репортерных) конъюгатов и связывающих их рецепторов, а также распознающих олигонуклеотидов или белковых рецептором с их аналитом. Компоненты таких пар, применимые в данном изобретении, могут быть как иммунного, так и неиммунного типа. Примерами иммунного связывания могут быть системы, основанные на взаимодействии антиген/антитело или гаптен/антигаптен. Поликлональные, моноклональные антитела или их иммуно-активные фрагменты могут быть подготовлены стандартными методами, известные специалистам в данной области. Термины "иммуно-активный фрагмент антитела" или "иммуно-активный фрагмент" относятся к частям молекул антител, которые содержат область специфического связывания. Такие фрагменты могут быть фрагментами Fab, которые определяются как фрагменты, лишенные части Fc, например Fab, Fab' и F(ab)2 фрагменты, или могут быть так называемыми "полумолекулярными" фрагментами, полученными восстановительным расщеплением дисульфидных связей, соединяющих тяжелые цепи исходного антитела. Если антиген, входящий в состав связывающейся пары, не является иммуногенным, например, гаптен, он может быть ковалентно связан с дополнительным белком-носителем, чтобы сделать его иммуногенным.
К неиммунным специфическим парам относятся системы, в которых два компонента проявляют естественную аффинность друг к другу, не являясь при этом антителом и антигеном. Среди известных примеров неиммунных пар можно назвать биотин и авидин, биотин и стрептавидин, фолиевая кислота и белки, связывающие фолаты, комплементарные нуклеиновые кислоты, белки А, G и иммуноглобулины и т.д. К ним также могут быть причислены пары, образующие ковалентные связи друг с другом: например, пары сульфгидрильные группы/ малеимиды и галоацетильные производные) и амино-группы/изотиоционаты, эфиры сукцинимида и сульфонилгалогениды и т.д. (M. N. Bobrow, et al., J. Immunol. Methods, 1989,125:279).
Иммунохроматографические (ИХА) тест-полоски
ИХА тест-полоска представляет собой окружение, в котором происходит анализ с помощью настоящего изобретения. Тест-полоска, как правило, состоит из хроматографического пористого материала и включает зону нанесения образца и зону связывания, как указано выше.
Хроматографические пористые материалы, из которых состоит полоска, как правило гидрофильны и/или принципиально могут быть превращены в таковые, и включают в себя следующие материалы, используемые либо по отдельности либо в сочетании с другими материалами - гранулы неорганической природы, например кремния, сульфата магния, алюминия; природные полимеры, в частности целлюлоза и материалы на ее основе (например, волокнистые полимеры - фильтровальная бумага, бумага для хроматографии и пр.); синтетические или модифицированные природные полимеры, такие как нитроцеллюлоза, ацетилцеллюлоза, поливинилхлорид, полиакриламид, кросс-сшитый декстран, агароза, полиакрилаты и др.; керамические материалы; стекло; и подобные материалы. Для описываемого изобретения предпочитаемым материалом является нитроцеллюлоза.
В предпочтительном варианте мембрана может быть как отдельной структурой в виде листа, нарезаемого на тест-полоски, либо может быть зафиксирована на подложке или твердой поверхности, как, например, при тонкослойной хроматографии.
Связывание рецепторов с поверхностью мембраны может достигаться при помощи хорошо известных методов, описанных в литературе. См. например Immobilized Enzymes, Inchiro Chibata, Halsted Press, New York (1978) и Cuatrecasas, J. Bio. Chem., 1970, 245:3059.
Подготовка тест-полоски
При подготовке тест-полоски для проведения анализа сначала наносятся необходимые реагенты, а затем тест-полоска инкубируется в необходимых буферных растворах.
Буферные растворы и растворители, используемые для описываемого изобретения известны (см. например Weng et al. (Патент США 4,740,468). Как правило значения pH буфера для проведения иммунохроматографического анализа находятся в интервале 4-11, чаще 5-10, для настоящего изобретения предпочтительно 6-9. Значения pH выбираются так, чтобы поддерживать необходимый уровень аффинности между взаимодействующими парами молекул и быть оптимальным для формирования сигнала соответствующей системой. Для достижения желаемого значения pH и его поддержания во время анализа могут использоваться различные буферы. В качестве иллюстрации могут быть приведены боратный, фосфатный, карбонатный, Tris, диэтилбарбитуровый и др. Применение определённого буферного раствора не является значимым для изобретения в целом, однако, при проведении конкретных исследований использование специфичного буферного раствора может быть предпочтительным.
Для проведения анализа в рамках данного изобретения обычно используется постоянное значение температуры. Как правило, для проведения исследования и получения детектируемого сигнала используются значения температуры в интервале 4-50 °C., обычно в промежутке 10-40 °C., а еще чаще – температуры, близкие к температуре окружающей среды, т.е. 15-25 °C.
При использовании в одном из вариантов данного изобретения распознающего олигонуклеотида и ее связывания (гибридизации) с целевой нуклеотидной последовательностью требует условий, способствующих протеканию гибридизации НК. Гибридизация как правило проводится в буферном растворе Фиколла, который также может содержать поливинилпирролидин, БСА, дрожжевую тРНК, неспецифичную ДНК, сульфат декстрана, дитиотреитол и формамид. Гибридизация может происходить как в растворе, так и на твердой фазе, при этом одна нуклеотидная цепь иммобилизуется на тест-полоске в зоне связывания.
Примеры
Далее настоящее изобретение будет подробно описано в сочетании со следующими примерами, чтобы специалисты в данной области могли лучше понять настоящее изобретение, при этом, настоящее изобретение не ограничивается следующими примерами.
Пример 1. Синтез углеродных квантовых точек.
Синтез проводили в соответствии с протоколом, описанным в работе 1, с изменениями в процессе очистки. 1 г лимонной кислоты и 2 г мочевины растворяли в 8 мл формамида, а объем доводили формамидом до 10 мл. Раствор переносили в автоклав с тефлоновым покрытием, и помещали в предварительно разогретый до 160°С термостат на 4 часа. Затем автоклав сразу же охлаждали под проточной водой.
Полученную темно-оранжевую смесь вместе с агрегатами переносили в пробирку объемом 50 мл, и добавляли 20 мл этилового спирта. Полученную смесь центрифугировали при 10000 g в течение 5 мин. Надосадочную жидкость выбрасывали, добавляли 2 мл воды. Пробирку обрабатывали ультразвуком до полного растворения гранулы (~ 1-2 мин), а объем доводили до 10 мл водой. Процедуру повторяют еще раз. Полученный раствор УКТ в воде центрифугировали при 10000 g в течение 5 мин для удаления крупных агрегатов. Затем полученную надосадочную жидкость переносили в новую пробирку.
Заключительным этапом промывки была ультрафильтрация через регенерированную целлюлозную мембрану MWCO 100 кДа. УКТ фильтровали под давлением около 3 бар в режиме промывки. Промывку проводили до тех пор, пока диализат не станет почти неокрашенным (в начале фильтрации диализат темно-оранжевый) примерно в течение 1 часа.
Затем ретентат (остаток) аликвотировали и хранили при -20 ° С. После размораживания аликвоту центрифугировали при 15000 г в течение 5 мин, а надосадочную жидкость использовали для дальнейших опытов в течение 1-2 суток после размораживания.
Пример 2. Изучение размеров и морфологии УКТ с помощью просвечивающей электронной микроскопии.
Изображения УКТ методом просвечивающей электронной микроскопии были получены при ускоряющем напряжении 200 кВ (Фиг 1а). Образцы УКТ в воде в концентрации 10 мкг/мл высушивали на воздухе на кремниевой подложке на углеродном скотче и немедленно анализировали. ТЭМ-изображения обрабатывали с использованием программного обеспечения ImageJ для получения распределения частиц по размерам. Показано, что УКТ имеют околосферическую форму со средним диаметром 31 ± 7 нм.
Пример 3. Измерение гидродинамического диаметра и дзета-потенциала УКТ
УКТ были охарактеризованы с помощью динамического светорассеяния. Образец УКТ в буфере HEPES 10 мМ pH 7.4 в концентрации 10 мг/л анализировался с помощью анализатора размера и дзета потенциала наночастиц. Измерения проводились в трех повторах и затем усреднялись. Гидродинамический размер составил (26 ± 4 нм), а дзета-потенциал -33 ± 7 мВ, соответствующие распределения представлены на Фиг. 1 В, Г.
Пример 4. Исследование УКТ с помощью ИК-спектроскопии.
Мы изучили наличие химических функциональных групп на поверхности УКТ с помощью ИК-спектроскопии с преобразованием Фурье (Фиг 1Б). 2 мг высушенных УКТ растирались в избытке KBr, а затем с помощью пресса формировалась таблетка. Спектр полученной таблетки измерялся на ИК-спектрометре с преобразованием Фурье, с использованием модуля ослабленного внутреннего отражения.
Широкая полоса на 3122 см-1 может быть отнесена к валентной вибрации O-H как в карбоновой кислоте, так и в спирте. Пик 1657 см-1 может указывать на растяжение валентной С=О в карбоновой кислоте, амиде или альдегиде. Эти два пика подтверждают наличие групп карбоновых кислот. Далее, узкая полоса на 1098 см-1 указывает на растяжение валентного С-О в спирте или в эфире. Теперь мы можем констатировать наличие алкогольных групп в образце УКТ. Наконец, мы соотносим пики на 1339 и 1395 см-1 деформационным колебаниям O-H, и слабому пику на 2785 см-1 к валентным C-H вибрациям.
Пример 5. Изучение оптических свойств УКТ
Мы изучили оптические свойства УКТ. Спектр поглощения имеет два пика – на 370 нм и на 517 нм (Фиг. 1Д). Второй из этих пиков придает УКТ насыщенный фиолетовый цвет.
Тепловая карта возбуждения/излучения флуоресценции (Фиг. 1Е) выявляет две различные области флуоресценции. Первый расположен в области возбуждения 350-450 нм. В этой области расположение пика излучения зависит от длины волны возбуждения. В области возбуждения 470-590 нм спектр излучения неизменен, с пиком излучения на длине волны 636 нм. Максимальная интенсивность флуоресценции наблюдается при параметрах возбуждения/излучения 530/630.
Пример 6. Функционализация УКТ с помощью полимеров.
В пробирке объемом 200 мкл 10 мкл биополимера в концентрации 0.1-1г/л (бычий сывороточный альбумин, хитозан, декстран, антитело против HER2-рецептора, антитело против хлорамфеникола Анти-САР, пероксидаза хрена, смесь пероксидазы хрена и антитела против хлорамфеникола в соотношении 1:1 по массе, смесь пероксидазы хрена и антитела против тропонина Анти-cTn в соотношении 1:1 по массе) смешивали с 20 мкл 0,1 М боратного буфера, рН 7-10 и 10 мкл УКТ, полученных, как описано в примере 1. Раствор тщательно перемешивали наконечником пипетки после каждого добавления.
Пробирку вставляли на 1 мин в гнездо амплификатора, предварительно нагретого до 50-90 °С, если не указано иное, с температурой крышки на 5 °С выше температуры блока. Затем пробирку сразу же перекладывали на термостат, установленный на 16 °C, и выдерживали в течение 1 минуты.
Затем раствор быстро смешивали с 40 мкл 5 или 50% аммония сульфата (АС) и перемешивали наконечником пипетки. Далее пробирку центрифугировали при 15000 г в течение 5 мин. 80 мкл воды Milli-Q очень медленно добавляли на дно пробирки, и пробирку центрифугировали еще 1 мин при 15000 g, и затем надосадочная жидкость убиралась. Наконец, конъюгаты ресуспендировали в боратном буфере 10 мМ, рН 9 и в течение 3с подвергали обработке ультразвуком
Получение УКТ:(PEI, плазмида)
На первом этапе биополимер представлял собой линейный PEI в концентрации 1 г/л. После нагревания и промывки АС, как описано выше, осадок ресуспендировали в следующем растворе: 18 мкл Milli-Q, 2 мкл плазмиды в концентрации 1 г/л, 20 мкл 0,1М боратного буфера, рН 9. Пробирку, в которой смешались реактивы, еще раз нагревали, а затем промывали с использованием АС
Пример 7. Влияние температуры синтеза и pH рабочего раствора на свойства конъюгатов УКТ:белок.
Конъюгаты УКТ:белок были получены как указано в примере 6, но при разных температурах (25 - 90 °C) и при разных pH (7.5 - 10) рабочего раствора.
Далее, исследовались спектры флуоресценции полученных конъюгатов. Интенсивность флуоресценции (F) на длине волны 530/630 нм усиливалась с повышением температуры синтеза (T) (Рис. 3e). Данные аппроксимируются степенной функцией F(T) = F0 +α (T – T 0)β, где F0, α, β трактовались как неизвестные параметры, а T0 – комнатная температура (25 °C). Наиболее подходящий β оказался равным 5.6, что указывает на резкий характер роста с более чем трехкратным усилением флуоресценции при T = 90 °C по сравнению с УКТ без покрытия (Фиг 2А).
Однако интенсивность флуоресценции при возбуждении на 350-450 нм сильно ослаблялась независимо от температурного синтеза. Это затухание, вероятно, связано с сосуществованием двух популяций УКТ, одна из которых не осаждается АС и теряется на стадии промывки (Фиг 2 Б-Д).
С другой стороны, температура синтеза также влияет на активность антител. Затем было изучено влияние температуры синтеза и, дополнительно, рН синтеза для конъюгатов УКТ:(Анти-CAP) (Фиг 2 Е, Ж). Для количественной оценки активности антител мы измеряли связывание конъюгатов с тест-линией в иммунохроматографическом анализе, описанном в примере 16. Мы предполагаем, что более сильное связывание отражает присутствие более активных молекул антител в конъюгате, и наоборот.
Конъюгаты, полученные при температуре 70 ° С и ниже, связываются с тест-полоской почти одинаково сильно. Однако при более высоких температурах связывания почти не наблюдалось. Таким образом, температуры в районе 60-70 ° С являются оптимальными с точки зрения усиления флуоресценции УКТ и активности антител.
Изучено влияние рН синтеза на активность конъюгатов. рН исследовался в нейтральной и щелочной областях, так как ожидается, что кислый рН нарушит коллоидную стабильность УКТ, поскольку они, предположительно, стабилизируются группами карбоновых кислот. Для исследуемой области рН 7,5 – 10 поведение конъюгатов в иммунохроматографическом анализе практически не зависело от рН.
Пример 8. Иммунохроматографический анализ на наличие полисахаридов в конъюгатах УКТ с полисахаридами.
На поверхность мембраны тест-полоски наносились лектины а именно агглютинин зародышей пшеницы (WGA), связывающий N-ацетил-D-глюкозамин, являющийся ацетилированной мономером хитозана; и конканавалин А, связывающий D-глюкозу, мономер декстрана.
Раствор WGA или конканавалина А в концентрации 1 г/л в буфере состава 10 мМ HEPES, pH 8,5, 0,1 мМ CaCl2 наносили на мембраны с помощью системы напыления с расходом 4 мкл/см, а затем сушили в течение ночи. Тестовые полоски были нарезаны с помощью модуля гильотинной резки и имели ширину 2 мм.
Далее, для приготовления образца смешивались 10 мкл конъюгатов УКТ:(хитозан), 5 мкл Tween 20 в 5% концентрации (w/v) и либо 5 мкл рабочего буфера, либо 5 мкл лектина при 1 г/л (в качестве отрицательного контроля)
Далее, на тестовые полоски наносили 20 мкл образца, приготовленного как описано выше, путем их погружения в этот раствор. По окончании анализа, полоски сканировали с помощью лазерного сканера с разрешением 1200 dpi. Полученные изображения в формате TIFF были проанализированы с помощью программного обеспечения ImageJ для расчета интенсивности полос.
Оба конъюгата демонстрировали сильное связывание с тест-полосками, при этом, связывание было значительно слабее для конъюгатов, предварительно смешанных с лектинами (Фиг 7 А, Б), что указывает на присутствие полисахаридов на поверхности УКТ.
Пример 9. Культивация клеточных линий.
В данных экспериментах использовались клеточные линии HEK293, EMT 6/P, EMT-HER2 (клеточная линия, стабильно экспрессирующая трансмембранный рецептор HER2, полученная из линии EMT6/P трансдукцией лентивирусной системой доставки, несущей ген, кодирующий рецептор HER2, с последующим отбором HER2-положительных клонов).
Клетки культивировали в следующих условиях: модифицированная среда Eagle Medium от Dulbecco / основная среда F12 (1:1) от Ham; 100 ЕД/мл пенициллина-стрептомицина; 10 мг/л гентамицина; 10 % фетальной бычьей сыворотки; 300 мг/л L-глютамина; 5 % CO2 при 37 °C. Клетки снимали с поверхности культурального флакона с помощью трипсина-ЭДТА.
Пример 10. Проведение микроскопического анализа клеточного образца.
20000 клеток EMT и EMT-HER2 высевали в 96-луночный планшет в 100 мкл среды и инкубировали в течение ночи. Затем к клеткам добавляли 100 мкл конъюгатов УКТ:(Anti-HER2), полученных как описано в примере 6, в концентрации 5 мг/л в среде, и инкубировали в течение ночи.
Затем, среда была заменена на 200 мкл PBS, и были получены микроскопические изображения клеток с помощью эпифлуоресцентного микроскопа в канале PerCP (возбуждение 560 нм с шириной полосы 25 нм, эмиссия 603 нм с шириной полосы 40 нм), а также в канале светлого поля.
Флуоресцентный сигнал от клеток EMT-HER2 был значительно выше, чем у клеток EMT 6/P, что подтверждает специфическое взаимодействие конъюгатов УКТ:(Anti-HER2) с клетками по рецептору HER2.
Пример 11. Цитометрический анализ клеточного образца с помощью конъюгатов УКТ.
100 000 клеток EMT 6/P и EMT-HER2 в 10 мкл среды DMEM-F12 смешивали с 2,5 мкл конъюгатов УКТ:(Анти-HER2), полученных как описано в примере 6, 5 мкл 10% BSA и 80 мкл PBS. Полученную смесь инкубировали в течение 10 мин, центрифугировали при 100 г в течение 5 мин и ресуспендировали в 100 мкл PBS.
Затем клетки сразу же анализировали с помощью проточного цитофлуориметра. Флуоресценция УКТ регистрировалась в эмиссионном канале 572-28, возбуждаемом лазером с длиной волны 488 нм. В каждом образце было собрано 5000 клеток. Стратегия отбора цитометрических событий представлена на Фиг 3А.
Индекс окрашивания для линии EMT-HER2 в три раза превышал индекс окрашивания для линии EMT 6/P, что подтверждает специфическое взаимодействие конъюгатов УКТ:(Anti-HER2) с клетками по рецептору HER2 (Фиг 3Б)
Пример 12. Измерение концентрации нуклеиновой кислоты в составе конъюгата УКТ:(ПЭИ, плазмида)
Концентрацию ДНК в составе конъюгата УКТ:(ПЭИ, плазмида) определяли с помощью красителя SYBR gold. Смешивали 10 мкл конъюгатов, разбавленных в 10 раз водой milliQ, 10 мкл плазмиды в концентрации 0, 0,5, 2 или 5 мг/л и 80 мкл красителя SYBR gold (разбавленного в 20000 раз в буфере HEPES 0.1M pH 7.4, согласно рекомендациям производителя) и измеряли флуоресценцию при параметрах возбуждения/излучения 482-16/530-40. Концентрацию определяли как пересечение градуировочной кривой с осью абсцисс. Репрезентативная градуировочная кривая представлена на Фиг. 4А, типичный выход по ДНК составлял 10%.
Пример 13. Доставка нуклеиновой кислоты в клетку
20000 клеток HEK293 высевали в 96-луночный планшет в 100 мкл среды и инкубировали в течение ночи.
Затем в лунки добавляли 100 мкл УКТ:(ПЭИ, плазмида), полученных, как описано в примере 6 с содержанием плазмиды 1, 5, 10, 30 или 50 нг в среде.
В качестве контроля в лунки добавляли 100 мкл смеси ПЭИ и плазмиды в массовом соотношении 3:1 с содержанием плазмиды 1, 5, 10, 30 или 50 нг в среде.
После этого количество белка nanoLuc, продуцируемого клетками, определяли следующим образом. Добавляли 100 мкл лизисного буфера (20 мМ Tris HCl (рН 7,5), 150 мМ NaCl, 0,5% NP-40, 5% глицерина). Через 10 мин 100 мкл лизата смешивали со 100 мкл 1 мг/л целентеразина в PBS в 96-луночном черном планшете, и сразу регистрировали люминесценцию без эмиссионного фильтра.
Зависимость эффективности трансфекции от используемой концентрации плазмиды для конъюгатов имеет оптимум при 10 нг, и при этой концентрации конъюгаты УКТ:(PEI, плазмида) превосходят обычную трансфекцию ПЭИ более, чем в два раза (Фиг 4Б). Микрофлуоресцентные фотографии клеток, трансфецированных конъюгатами (при концентрации плазмиды 10 нг) приведены на Фиг. 4Д.
Пример 14. Анализ токсичности конъюгатов УКТ:(ПЭИ, плазмида)
2000 клеток HEK293 высевали в 96-луночный планшет в 100 мкл среды и инкубировали в течение ночи.
Затем в лунки добавляли 100 мкл УКТ:(ПЭИ, плазмида) с содержанием плазмиды 1, 5, 10, 30 или 50 нг в среде.
В качестве контроля в лунки добавляли 100 мкл смеси ПЭИ и плазмиды в массовом соотношении 3:1 с содержанием плазмиды 1, 5, 10, 30 или 50 нг в среде.
Клетки инкубировали в течение 72 ч. Далее среду отбирали, добавляли 100 мкл раствора резазурина, а через 2 часа измеряли флуоресценцию при параметрах возбуждения/излучения 556-15/594-15.
При более высоких концентрациях УКТ имеют тенденцию к агрегации и образованию пленок вместе с крупными макроскопическими агломератами. Несмотря на то, что УКТ остается практически нетоксичным в этих концентрациях, как показал резазуриновый тест на токсичность (фиг. 4В), образующиеся пленки и агрегаты, вероятно, препятствуют проникновению новых порций трансфектанта в клетки, тем самым уменьшая количество производимого белка-репортера.
Пример 15. Получение конъюгата BSA-CAP
CAP-сукцинат растворяли до концентрации 100 г/л. EDC растворяли в 50 мМ MES, pH6, а затем разбавляли ДМСО в два раза для достижения конечной концентрации 100 г/л.
NHS сначала растворяли в ДМСО, а затем разбавляли в два раза 50 мМ MES, pH 6, чтобы достичь конечной концентрации 100 г/л.
50 мкл CAP-сукцината смешивали с 18,3 мкл раствора EDC, 13,6 мкл раствора NHS, 18,1 мкл смеси 50 мМ MES, рН 6 и ДМСО (1:1 по объему). Активацию проводили в течение 1 часа при комнатной температуре.
После инкубации смешивали 58,5 мкл BSA в концентрации 100 г/л, 28,7 мкл активированного CAP-сукцината и 42,8 мкл 0,1 М боратного буфера, рН 8. Пробирку центрифугировали в течение 1 мин при 10000g, и в дальнейшем использовали надосадочную жидкость.Пробирку инкубировали в течение ночи.
Для очистки конъюгата его наносили на обессоливающие колонки ZEBA (7 кДа MWCO) однократно в соответствии с рекомендациями производителя. Конъюгат хранили в воде Milli-Q.
Пример 16. Иммунохроматографический анализ для детекции хлорамфеникола в образце.
Общая схема анализа представлена на Фиг 5А.
Раствор BSA-CAP в концентрации 3 г/л наносили на мембраны с помощью системы напыления с расходом 4 мкл/см, а затем сушили в течение ночи. Тест-полоски были вырезаны с помощью модуля гильотинной резки и имели ширину 2 мм.
Далее, 2 мкл конъюгата УКТ:(Анти-CAP), полученных как описано в примере 6, смешивали с исследуемым на наличие антигена раствором следующего состава: 2 мкл CAP-сукцината в желаемой концентрации, 2 мкл 10% BSA и 12 мкл HEPES 0,1 M pH 8,5 или разбавленное этим же буфером молоко (10%) или сыворотка крови (50%).
Далее, на тестовые полоски наносили 20 мкл исследуемого раствора путем их погружения в этот раствор. По окончании анализа, полоски сканировали с помощью лазерного сканера с разрешением 1200 dpi или в флуоресцентном томографе LumoTrace FLUO (Abisense, Россия). Полученные изображения в формате TIFF были проанализированы с помощью программного обеспечения ImageJ для расчета интенсивности полос.
Конъюгаты УКТ:(Анти-CAP) были способны специфически связываться на тестовой линии, демонстрируя сильное связывание, легко наблюдаемое даже невооруженным глазом (Фиг 5Б) в отсутствии CAP, и демонстрируя отсутствие связывание в присутствии CAP. Предел детекции (3σ-критерий) тест-системы составил 9 нг/мл (2,1 мкМ), см Фиг. 5В.
Пример 17. Изучение времени циркуляции конъюгатов УКТ в кровотоке.
Мышей анестезировали и.п. введение смеси Золетила (20 мг/кг) и Рометара (1,6 мг/кг). Затем ретроорбитально вводили 200 мкг конъюгатов CQD:хитозан, полученных как описано в примере 6.. Через 1 минуту, 3 минуты, 10 минут, 30 минут, 3 часа, 8 часов, 24 часа после инъекции из ретроорбитального синуса брали 20 мкл крови и немедленно центрифугировали (5 минут, 500 g), а плазму собирали и замораживали при -20 ˚C до проведения анализа. Флуоресценцию образцов плазмы крови регистрировали при параметрах возбуждения/эмиссии 530-8/630-8 нм. Кривые выведения конъюгатов УКТ из кровотока представлены на Фиг. 5Б
Для типичного эксперимента время полувыведения конъюгатов УКТ:Хитозан составляло 2 мин.
Пример 18. Флуоресцентная биовизуализация ex vivo и биораспределение
Мышам ретроорбитально вводили 200 мкг конъюгатов УКТ:хитозан в 200 мкл PBS. Затем, через 3 часа после инъекции, мышей подвергали эвтаназии путем смещения шейных позвонков, а органы (печень, легкие, почки, селезенку, мышцы, кости, сердце, опухоль) и кровь извлекали и визуализировали с помощью возбуждающего диода 550 нм и фильтра на эмиссию 600+ нм, с использованием системы биовизуализации LumoTrace FLUO (ООО «Абисенс», Сириус, Россия). Результирующие изображения во флуоресцентном канале и в канале светлого поля приведены на Фиг 5А. Наблюдается преимущественное накопление конъюгатов в печени и селезенке, а также в опухоли.
Пример 19. Флуоресцентная биовизуализация in vivo
Мышам ретроорбитально вводили 200 мкг конъюгатов УКТ:хитозан в 200 мкл PBS. Затем, через 3 часа после инъекции, мышей анестезировали, брили, и помещали в систему биовизуализации LumoTrace FLUO (ООО «Абисенс», Сириус, Россия). Снимали флуоресцентные изображения, как в Примере 17. Регистрировали сигнал в области печени и селезенки, также был зарегистрирован сигнал в опухоли.
Пример 20. Синтез флуоресцентно-биолюминесцентных меток.
В пробирке объемом 200 мкл 10 мкл биополимера в концентрации 0.1-1г/л (люцифераза nanoLuc, смесь люциферазы nanoLuc и антитела против хлорамфеникола Анти-САР в соотношении 1:1 по массе) смешивали с 20 мкл 0,1 М боратного буфера, рН 7-10 и 10 мкл УКТ, полученных, как описано в примере 1. Раствор тщательно перемешивали наконечником пипетки после каждого добавления.
Пробирку вставляли на 1 мин в гнездо амплификатора, предварительно нагретого до 50-90 °С, если не указано иное, с температурой крышки на 5 °С выше температуры блока. Затем пробирку сразу же перекладывали на термостат, установленный на 16 °C, и выдерживали в течение 1 минуты.
Затем раствор быстро смешивали с 40 мкл 5 или 50% АС и перемешивали наконечником пипетки. Далее пробирку центрифугировали при 15000 г в течение 5 мин. 80 мкл воды Milli-Q очень медленно добавляли на дно пробирки, и пробирку центрифугировали еще 1 мин при 15000 g, и затем надосадочная жидкость убиралась. Наконец, конъюгаты ресуспендировали в боратном буфере 10 мМ, рН 9 и в течение 3с подвергали обработке ультразвуком.
Полученные, отмытые от несвязанных белков, конъюгаты УКТ:(nanoLuc), УКТ:(nanoLuc, Анти-CAP) обладали и флуоресцентными свойствами, и биолюминесцентными: при добавлении
Пример 21. Конкурентный иммуноферментный анализ на наличие хлорамфеникола в образце с помощью конъюгатов УКТ
Конъюгаты УКТ:(nanoLuc, Анти-CAP) и УКТ:(HRP, Анти-CAP) синтезировались как описано в примерах 6 и 20.
Для анализа образца подготавливался планшет: 100 мкл BSA-CAP 0,1 г/л в карбонатно-бикарбонатном буфере (0,1 М, рН 9,6) помещали в лунки 96-луночных ИФА планшетов и инкубировали при комнатной температуре в течение ночи. Далее раствор удаляли, а лунки промывали однократно 100 мкл раствора PBS(PBS с 0,05 % Tween 20). После этого в лунки добавляли 100 мкл блокирующего буфера (1% BSA в PBS). Планшет инкубировали в течение 1 ч при комнатной температуре и трижды промывали PBST.
Далее, производился непосредственно анализ образца: в лунку добавляли 100 мкл следующей смеси: 5 мкл конъюгатов УКТ:(HRP, Анти-CAP) или УКТ:(nanoLuc, Анти-CAP), 10 мкл CAP-сукцината в заданной концентрации в качестве образца, 10 мкл 10% BSA и 75 мкл PBS. Планшет инкубировали в течение 1 ч, трижды промывали PBST, а в лунки добавляли PBS. Полученный флуоресцентный сигнал измеряли при параметрах возбуждения/излучения 530-8/630-8 нм. Наконец, раствор удаляли и добавляли следующие растворы субстрата:
А. Для конъюгатов УКТ:(HRP, Анти-CAP): 0,1 г/л TMB, 0,3 г/л H2O2 в ацетатном буфере (0,1 M pH 5). Планшет инкубировали в течение 30 мин и добавляли 50 мкл H2SO4. Поглощение измерялось на длине волны 450 нм
Б. Для УКТ: (nanoLuc, Анти-CAP): 1 мг/л коэлентеразина в PBS и сразу же измеряли без фильтра эмиссии.
Кривая «доза-реакция», полученная при флуоресцентном детектировании, как правило, имеет тот же профиль, что и при ферментативном детектировании. Предел детекции составил от 1.4 до 29 нг/мл.
Пример 22. Иммуноферментный анализ (сэндвич анализ) на наличие тропонина в образце с помощью конъюгатов УКТ
Конъюгат УКТ:(HRP, Анти-cTn) синтезировались как описано в примерах 6 и 20.
Для анализа образца подготавливался планшет: 100 мкл Анти-cTn 0,1 г/л в карбонатно-бикарбонатном буфере (0,1 М, рН 9,6) помещали в лунки 96-луночных ИФА планшетов и инкубировали при температуре +4 градуса Цельсия в течение ночи. Далее раствор удаляли, а лунки промывали однократно 100 мкл раствора PBS(PBS с 0,05 % Tween 20). После этого в лунки добавляли 100 мкл блокирующего буфера (1% BSA в PBS). Планшет инкубировали в течение 1 ч при комнатной температуре и трижды промывали PBST.
Далее, производился непосредственно анализ образца: в лунки добавляли по 100 мкл образцов сыворотки крови с разными концентрациями тропонина. Планшет инкубировали в течение 1 ч при комнатной температуре и трижды промывали PBST с 1% БСА. Затем, в каждую лунку добавляли 5 мкл конъюгатов УКТ:(HRP, Анти-сTb) и 75 мкл PBS с 1% БСА. Планшет инкубировали в течение 1 ч, трижды промывали PBST, а в лунки добавляли PBS. Полученный флуоресцентный сигнал измеряли при параметрах возбуждения/излучения 530-8/630-8 нм. Наконец, раствор удаляли и добавляли раствор субстрата: 0,1 г/л TMB, 0,3 г/л H2O2 в ацетатном буфере (0,1 M pH 5). Планшет инкубировали в течение 30 мин и добавляли 50 мкл H2SO4. Поглощение измерялось на длине волны 450 нм.
Кривая «доза-реакция», полученная при флуоресцентном детектировании, как правило, имеет тот же профиль, что и при ферментативном детектировании. Предел детекции составил от 0.1 нг/мл.
Пример 23. Усреднение результатов анализа наличия аналита в образце, проведенных мультимодальными агентами.
Проводят анализ как в Примерах 21,22 затем в качестве результирующего значения концентрации аналита в образце вычисляют среднее арифметическое значение для концентрации аналита в образце, полученное по флуоресценции УКТ и по ферментативному анализу. Данный метод позволяет получить меньшую погрешность измерения концентрации при измерении одного и того же образца несколько 5 раз подряд.
Сущность изобретения поясняется чертежами фиг. 1-8.
На фиг. 1 представлены (а) ТЭМ фотографии УКТ, шкала – 100 нм. Размер частиц, согласно данной фотографии, составляет 31 ± 7 нм (среднее распределения ± стандартное отклонение распределения). (б). ИК-спектр УКТ. Обозначенные пики соотносятся с характерными линиями поглощения карбоновых кислот, спиртов, амидов, означая их присутствие в составе УКТ. (в) Распределение гидродинамических диаметров УКТ, полученное с помощью метода динамического светорассеяния. Размер составляет (26 ± 4) нм (среднее распределения ± стандартное отклонение распределения). (г) Распределение дзета-потенциалов УКТ, полученное с помощью динамического светорассеяния. Дзета-потенциал составляет –(33 ± 7) мВ (среднее распределения ± стандартное отклонение распределения). (д) Спектр поглощения УКТ в УФ и видимой областях. Наблюдается два пика – на 370 и 517 нм. Второй из этих пиков придает УКТ фиолетовый цвет. (е). Тепловая карта интенсивности флуоресценции в зависимости от длины волны возбуждения и эмиссии. Более яркие пиксели отражают более яркую флуоресценцию. Наблюдаются две основные области: в области возбуждения 350-450 нм, в которой расположение пика излучения зависит от длины волны возбуждения; и в области возбуждения 470-590 нм, в которой спектр излучения неизменен, с пиком излучения на длине волны 636 нм. Максимальная интенсивность флуоресценции наблюдается при параметрах возбуждения/излучения 530/630.
На фиг. 2 представлены фотографии тест-полосок для обнаружения полисахаридов на поверхности УКТ. (а) На тест-полоске иммобилизован Конканавалин А, распознающий глюкозу, мономер декстрана. На самой левой полоске наблюдается сильное связывание конъюгатов УКТ:декстран с тестовой линией. На средних полосках связывание конъгатов, предварительно смешанных с избытком Конканавалина А значительно слабее. На левых полосках вместо на тестовой линии иммобилизован БСА, связывания конъюгатов с этими полосками не наблюдается. (б) На тест-полоске иммобилизован лектин WGA, распознающий N-ацетил-D-глюкозамин, мономер декстрана. На самой левой полоске наблюдается сильное связывание конъюгатов УКТ:хитозан с тестовой линией. На средних полосках связывание конъгатов, предварительно смешанных с избытком WGA значительно слабее. На левых полосках вместо на тестовой линии иммобилизован БСА, связывания конъюгатов с этими полосками не наблюдается.
На фиг 3 представлены (а) Схема иммунохроматографического анализа для обнаружения аналита в образце (б) Сравнение интенсивности окрашивания тестовых линий в присутствии (справа) и отсутствии (слева) аналита, в данном случае, CAP. (в) Зависимость интенсивности окрашивания тестовых линий в зависимости от концентрации CAP в образце. Предел детекции (3σ-критерий) составляет 9 нг/мл.
На фиг. 4 представлены (а) Репрезентативная калибровочная кривая для измерения концентрации плазмиды в составе конъюгата УКТ:(ПЭИ, плазмида) с помощью красителя SYBR gold. Типичный выход по плазмиде составляет 10%. (б) Зависимость эффективности трансфекции с помощью конъюгатов УКТ:(ПЭИ, плазмида) и обычной трансфекции с помощью ПЭИ в зависимости от концентрации плазмиды. Оптимум для конъюгатов наблюдается при концентрации плазмиды 10 нг/лунку 96 луночного планшета. (в) Исследование токсичности ПЭИ и конъюгатов УКТ:(ПЭИ, плазмида) с помощью резазуринового теста. При всех концентрациях, статистически значимого отличия между контрольными и тестовыми группами и не наблюдалось (n = 3). (г) Микрофотографии клеток с добавленными УКТ:(ПЭИ, плазмида) в количестве 10 нг на лунку и контрольными клетками, полученные в канале светлого поля и во флуоресцентном канале.
На фиг 5 представлены (а) Схема отбора цитометрических событий. Вначале отсекаются события со слишком малым значением прямого светорассеяния (слева), затем события со слишком большим значением параметра FSC-A для данного значения FSC-H (в центре), и после этого анализируется гистограмма интенсивности во флуоресцентном канале PerCP-H (справа). (б) Гистограммы интенсивности во флуоресцентном канале PerCP-H для клеточных линий EMT и EMT-HER2, провзаимодействовавших с конъюгатами УКТ:(Анти-HER2). Наблюдается значительно более эффективное связывание конъюагатов с клетками линии EMT-HER2.
На фиг. 6 представлены: (а) зависимость интенсивности флуоресценции конъюгатов УКТ:(Анти-HER2) от температуры синтеза. При температуре синтеза 90 °C наблюдается более чем трехкратное усиление флуоресценции по сравнению с УКТ без покрытия. (б)-(д) тепловые карты интенсивности флуоресценции в зависимости от длины волны возбуждения и эмиссии УКТ и их конъюгатов. Наблюдается значительное усиление флуоресценции в области возбуждения 470-590 нм в процессе конъюгации, с одновременным уменьшением в области возбуждения 350-450 нм. (е, ж) Эффективность связывания конъюгатов УКТ:(Анти-CAP) с тест полосками с нанесенным BSA-CAP, в зависимости от pH рабочего раствора при синтезе (е) и от температуры синтеза (ж). pH влияет в незначительной мере, в то время как при повышении температуры эффективность связывания снижается.
На Фиг. 7 представлены (а) ex vivo биораспределение конъюгатов УКТ:Хитозан. Верхняя панель отражает флуоресцентные фотографии органов (возбуждение 550 нм, эмиссия 600+ нм), нижняя фотографии органов в светлом поле. Видно значительное накопление конъюгатов в печени, селезенке и опухоли. (б) Кинетика выведения конъюгатов УКТ:Хитозан из кровотока. Время полувыведения составляет 1.87±0.25 мин (n = 4).
На Фиг. 8 представлены результаты иммуноферментного анализа образца на наличие CAP с помощью конъюгатов УКТ. (а) Схема анализа. При наличии CAP в растворе, УКТ, модифицированные антителом к CAP не связываются с неподвижной фазой. (б, в) кривые доза-эффект, полученные с использованием УКТ:(Анти-CAP, nanoLuc). (г, д) кривые доза-эффект, полученные с использованием УКТ:(Анти-CAP, HRP). Для обоих конъюгатов на левых графиках (б, г) представлены результаты для флуоресцентной детекции сигнала, на правых – для ферментативной. Пределы детекции составляют 29, 1.4, 11.7, 3.2 нг/мл для (б, в, г, д) соответственно.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ детекции аналита в образце с помощью иммунохроматографии | 2023 |
|
RU2835200C1 |
| Способ проведения микроскопического анализа клеточного образца | 2023 |
|
RU2835203C1 |
| Способ проведения цитометрического анализа образца | 2023 |
|
RU2835213C1 |
| Способ биоимиджинга | 2023 |
|
RU2838135C1 |
| Способ доставки нуклеиновой кислоты в клетку | 2023 |
|
RU2835201C1 |
| Способ конкурентного иммуноферментного анализа для детекции аналита в образце с помощью мультимодальных наночастиц | 2023 |
|
RU2836697C1 |
| Способ твердофазного каталитического анализа содержания аналита в образце с использованием серебряных нанопроволок | 2022 |
|
RU2808559C1 |
| Способ измерения рН на основе серебряных нанопроволок | 2022 |
|
RU2808717C1 |
| Способ каталитического разложения пероксида водорода с помощью серебряных нанопроволок | 2022 |
|
RU2815436C1 |
| Флуоресцентная многоцелевая наноразмерная метка и конъюгаты на её основе | 2021 |
|
RU2777648C1 |
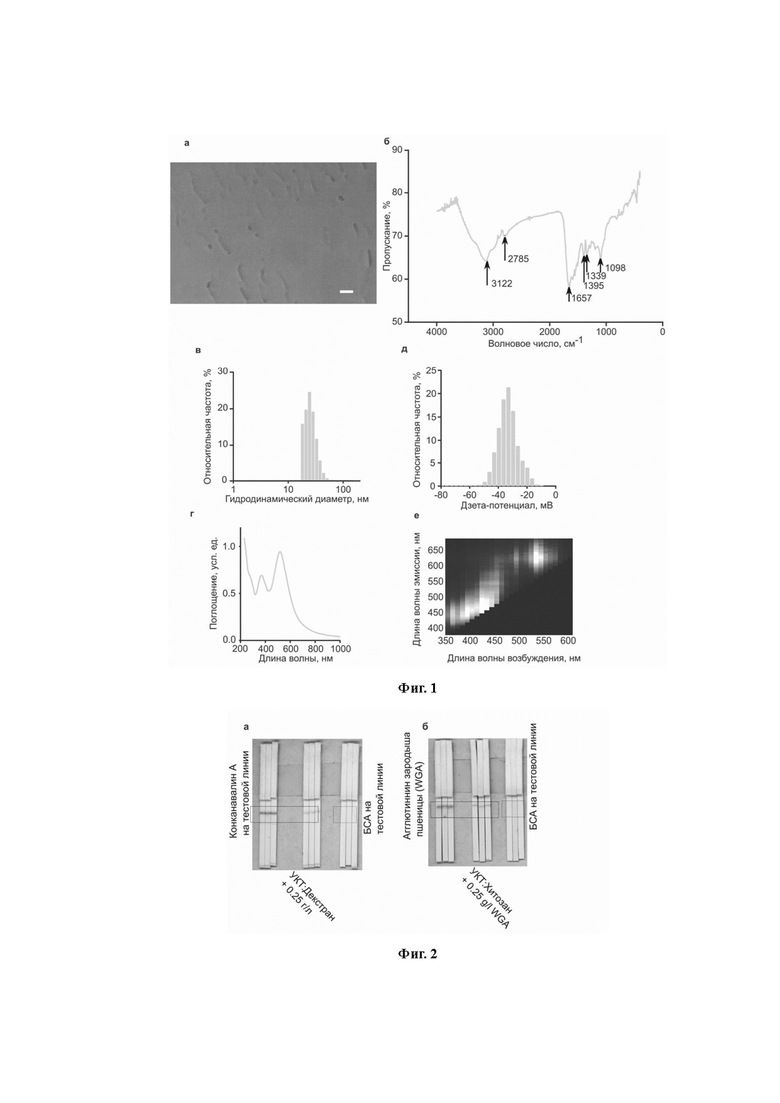
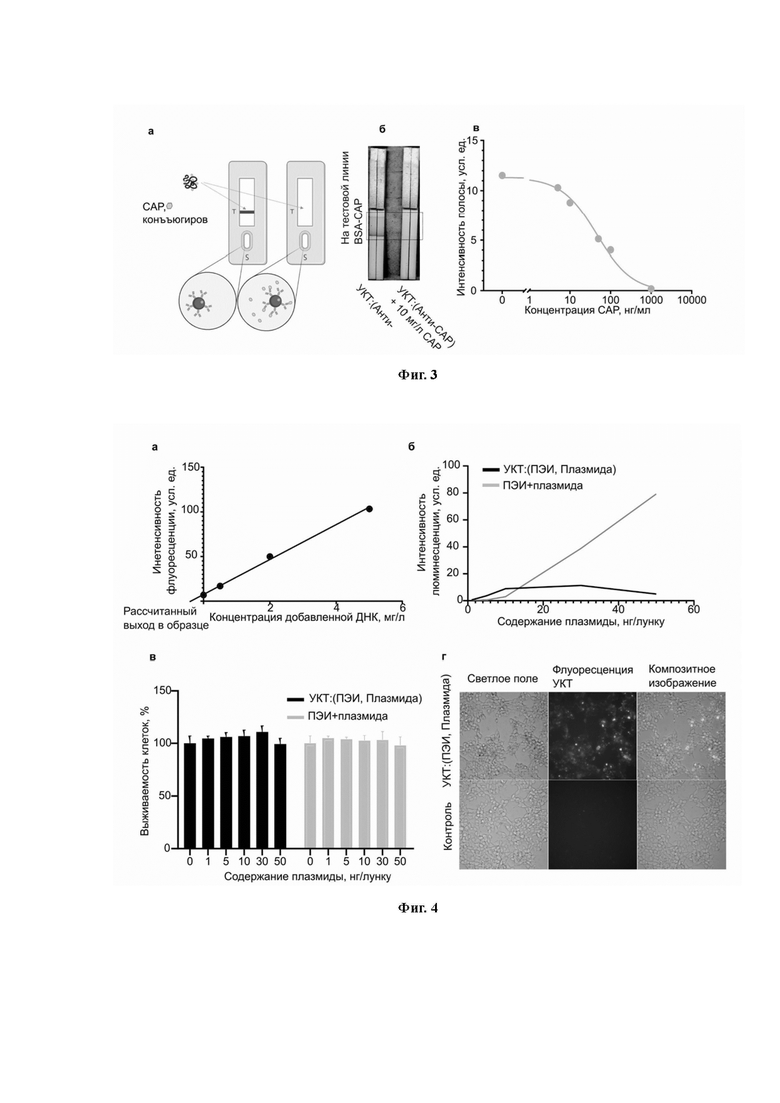
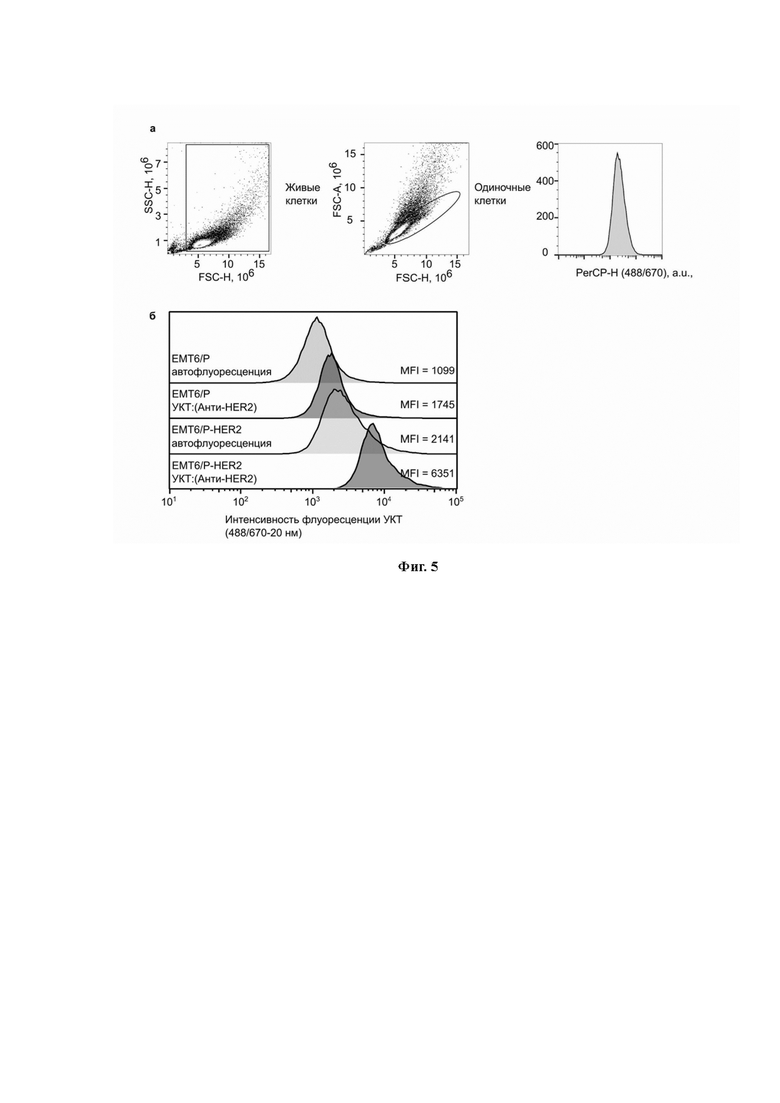

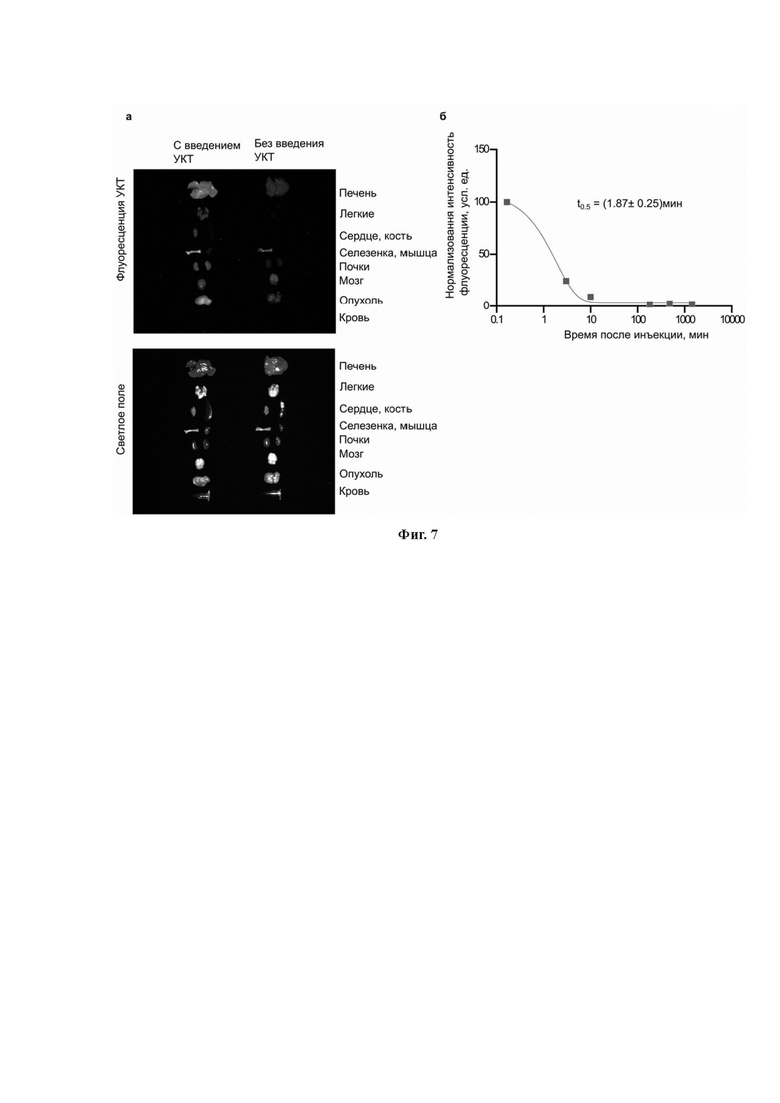
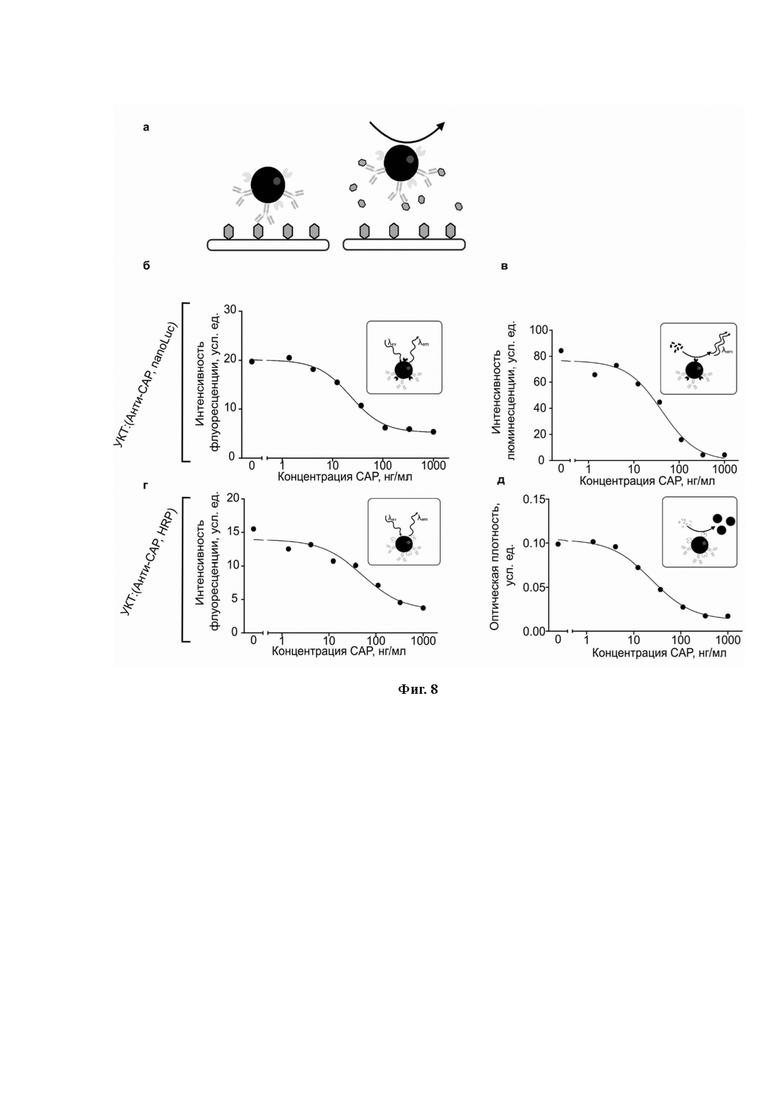
Изобретение относится к области синтеза наноматериалов, точнее флуоресцентных наноматериалов, а точнее углеродных квантовых точек для различных применений - в области биомедицины, биотехнологии, диагностики, терапии, детекции различных веществ и т.д. В частности изобретение относится к способу синтеза функциональных углеродных квантовых точек, который включает следующие шаги: i) раствор лимонной кислоты и мочевины автоклавируют при температуре 150-300 градусов Цельсия, ii) отмывают полученные углеродные квантовые точки. При этом способ характеризуется тем, что дополнительно включает следующие шаги: iii) смешение отмытых углеродных квантовых точек с раствором полимера, iv) нагрев полученной смеси до 50-99 градусов Цельсия, v) повышение ионной силы полученного раствора для высаживания упомянутого полимера на поверхность углеродных квантовых точек. Технический результат при использовании изобретения состоит в более быстром методе синтеза функциональных (функционализированных) углеродных квантовых точек, позволяющем добиться их функционализации различными биополимерами (в т.ч. макромолекулами) в более мягких условиях и позволяющем легко их очистить от несвязавшихся молекул биополимеров. 17 з.п. ф-лы, 23 пр., 8 ил.
1. Способ синтеза функциональных углеродных квантовых точек, который включает следующие шаги:
i) раствор лимонной кислоты и мочевины автоклавируют при температуре 150-300 градусов Цельсия,
ii) отмывают полученные углеродные квантовые точки,
отличающийся тем, что дополнительно включает следующие шаги:
iii) смешение отмытых углеродных квантовых точек с раствором полимера,
iv) нагрев полученной смеси до 50-99 градусов Цельсия,
v) повышение ионной силы полученного раствора для высаживания упомянутого полимера на поверхность углеродных квантовых точек.
2. Способ по п.1, в котором дополнительно отмывают полученные функциональные квантовые точки с упомянутым полимером от молекул несвязавшегося полимера.
3. Способ по п.1, в котором упомянутое отмывание полученных углеродных квантовых точек производят растворителем из набора: этанол, метанол, вода, ацетон.
4. Способ по п.1, в котором в упомянутом растворе лимонной кислоты и мочевины массовое отношении лимонной кислоты и мочевины находится в диапазоне от 3:1 до 1:5.
5. Способ по п.1, в котором в упомянутом растворе лимонной кислоты и мочевины массовое отношении лимонной кислоты и мочевины находится в диапазоне от 1:1 до 1:3.
6. Способ по п.1, в котором упомянутый полимер является одним из набора: белок, углевод, нуклеиновая кислота, полиэтиленимин.
7. Способ по п.1, в котором упомянутый полимер является гамма-иммуноглобулином.
8. Способ по п.1, в котором размер получаемых функциональных углеродных квантовых точек равен 30-250 нм.
9. Способ по п.1, в котором размер получаемых функциональных углеродных квантовых точек равен 50-150 нм.
10. Способ по п.1, в котором размер получаемых функциональных углеродных квантовых точек равен 100-250 нм.
11. Способ по п.1, в котором упомянутый нагрев полученной смеси производят до 55-65 градусов Цельсия.
12. Способ по п.1, в котором упомянутый нагрев полученной смеси производят до 85-95 градусов Цельсия.
13. Способ по п.1, в котором упомянутое автоклавирование проводят при температуре 190-210 градусов Цельсия.
14. Способ по п.1, в котором упомянутое повышение ионной силы полученного раствора для высаживания упомянутого биополимера на поверхность углеродных квантовых точек проводят за счет добавления к упомянутому полученному раствору раствора соли.
15. Способ по п.14, в котором упомянутая соль является сульфатом аммония.
16. Способ по п.14, в котором упомянутая соль является NaCl, Na2SO4, MgSO4, (NH4)2SO4, КСl, MgCl2.
17. Способ по п.1, в котором дополнительно включает шаг добавления кросс-сшивающего агента.
18. Способ по п.17, в котором упомянутый кросс-сшивающий агент выбран из списка: эпихлоргидрин, глутаровый альдегид.
| КОНЪЮГАТЫ КВАНТОВОЙ ТОЧКИ С ПЕПТИДОМ-НОСИТЕЛЕМ, ПРИГОДНЫЕ ДЛЯ ВИЗУАЛИЗАЦИИ И ДОСТАВКИ МОЛЕКУЛ В РАСТЕНИЯ | 2012 |
|
RU2609637C2 |
| CN 112209363 A, 12.01.2021 | |||
| CN 108892127 A, 27.11.2018 | |||
| CN 107500274 A, 22.12.2017 | |||
| CN 112521942 A, 19.03.2021. | |||
Авторы
Даты
2024-07-31—Публикация
2023-12-22—Подача