Область техники
Данное изобретение относится к области нанотехнологии, в частности, к созданию новых квантовых точек, визуализирующих агентов на их основе. Описываемые методы и частицы могут применяться, в частности, для специфической флуоресцентной молекулярно-нацеленной визуализации маркеров и диагностики различных заболеваний, в качестве средства для обнаружения утечек и т.д.
Уровень техники
Флуоресцентные наночастицы имеют широкое применение, например, в изготовлении различных средств для диагностики заболеваний, визуализации молекулярных маркеров, изготовлении флуоресцентных чернил и пигментов, средств для обнаружения утечек, например, хладагента в холодильных установках и системах кондиционирования воздуха, обнаружения движения жидкостей, например, выявление загрязнения нефтепластов, оптоэлектронике и т.д.
В качестве флуоресцентных меток, используемых для визуализации, особое место занимают функционализированные модифицированные коллоидные нанокристаллы (квантовые точки). Используя флуоресцентные нанокристаллы, можно подобрать флуоресцентные характеристики (варьируя материал, размер и конструкцию нанокристаллов) и осуществлять методы диагностики различных патологий. Флуоресцентные нанокристаллы имеют ряд преимуществ по сравнению с органическими красителями. Флуоресцентные нанокристаллы имеют высокий квантовый выход и большую фотостабильность и более высокий коэффициент молярного поглощения, а также большую величину стоксовского сдвига, чем у органических красителей, что проявляется в виде более высокой яркости и увеличения интенсивности аналитического сигнала. Все это упрощает диагностический процесс, повышает порог обнаружения и повышает надежность исследования. Различные способы синтеза флуоресцентных нанокристаллов (квантовых точек) были описаны, например, в патентах РФ №2497746, 2381304 и 2540385.
Описанные на сегодняшний день флуоресцентные нанокристаллы и их конъюгаты имеют ряд ограничений, не позволяющих применять их в медицине в качестве диагностических агентов. Основной проблемой, ограничивающей их применение, является большой размер, способность проникать в клетку и ядра и специфично связываться с целевыми рецепторами (Jennifer Е. Francis et all/ Evaluation of quantum dot conjugated antibodies for immunofluorescent labelling of cellular targets/ Beilstein J. Nanotechnol. 2017, 8, 1238-1249. https://doi.org/10.3782/binano.8.125), при этом известные разработки с малыми квантовыми точками не имеют подтвержденной фотостабильности и эффективности. Из уровня техники также известен флуоресцентый конъюгат, описанный в работе Здобновой Т.А., Комплексы полупроводниковых нанокристаллов и рекомбинантных антител для флуоресцентной визуализации опухолевых клеток (Автореферат диссертации на соискание ученой степени кандидата биологических наук, Москва, 2011, с. с.4-10).
Таким образом, сохраняется потребность создания флуоресцентных нанокристаллов, обладающих малым размером, высоким квантовым выходом флуоресценции, коллоидной стабильностью и возможностью применения в лабораторно-клинической практике без использования специального оборудования (с максимумом эмиссии в диапазоне 630-720 нм).
Сущность изобретения
Задачей настоящего изобретения является разработка и создания новых квантовых точек, характеризующихся малым размером, высокой интенсивностью флуоресценции в диапазоне 630-720 нм (оптический диапазон с минимальным уровнем автофлуоресценции тканей и клеток), высокой фотостабильностью, а также конъюгатов для флуоресцентного маркирования на их основе.
Технический результат настоящего изобретения заключается в разработке и получении новых квантовых точек с кристаллической структурой вюрцита, характеризующихся малым размером 6-8 нм (фигуры 1-9) при сохранении их высокой фотостабильности (более 3 часов) (таблица 1), высокой интенсивностью флуоресценции в диапазоне 630-720 нм, высоким уровнем флуоресцентного сигнала (квантовым выходом до 70%), шириной на полувысоте (FWHM) менее 65 нм. Помимо этого, технический результат настоящего изобретения заключается в разработке конъюгатов для флуоресцентного маркирования на основе квантовых точек по изобретению, которые в свою очередь характеризуются высокой интенсивностью флуоресценции и специфичностью связывания с целевыми мишенями (маркерами).
Технический результат настоящего изобретения также заключается в разработке нового способа получения квантовых точек по изобретению, который позволяет получить квантовые точки малого размера с вюрцитной структурой (фигуры 1-9); способ по изобретению позволяет эффективно наращивать полупровдниковые оболочки на ядро квантовых точек.
Указанный технический результат достигается за счет разработки и получения квантовой точки, имеющей кристаллическую структуру вюрцита и характеризующуюся размером 6-8 нм, структура которой выражается общей формулой А/Б, где:
- А - ядро квантовой точки, представляющее собой полупроводниковый материал состава CdTeSeS;
- Б - оболочка квантовой точки, покрывающая ядро и представляющая собой полупроводниковый материал состава CdS, CdZnS, CdS/ZnS, CdS/CdZnS или CdZnS/ZnS;
причем ядро квантовой точки имеет кристаллическую структуру вюрцита, размером в диапазоне 2-4 нм и с максимумом в распределении по размеру 2,5 нм, количество монослоев оболочки, покрывающей ядро, составляет от 5 до 8.
В частных вариантах воплощения изобретения квантовая точка имеет структуру CdTeSeS/CdS, CdTeSeS/CdZnS, CdTeSeS/CdS/CdZnS, CdTeSeS/CdZnS/ZnS или CdTeSeS/CdS/ZnS.
В частных вариантах воплощения изобретения молярное содержание Cd в квантовой точке составляет от 21 до 29%.
В частных вариантах воплощения изобретения молярное содержание Se в квантовой точке составляет от 14 до 20%.
В частных вариантах воплощения изобретения молярное содержание S в квантовой точке составляет от 52 до 64%.
В частных вариантах воплощения изобретения квантовые точки по изобретению характеризуются квантовым выходом от 50 до 70%.
Технический результат также достигается за счет разработки и получения флуоресцентного конъюгата для визуализации молекулярных маркеров, состоящего из фотостабильной флуоресцентной квантовой точки по изобретению, покрытой полимерной оболочкой и лиганда, обеспечивающего специфичность связывания.
В частных вариантах воплощения изобретения полимерная оболочка представляет собой сополимер метоксиполиэтиленгликольакрилата-ко-малеинового ангидрида-ко-этиленгликольдиакрилата, терминированный 1,6-гександитиолом; сополимер метоксиполиэтиленгликольакрилата-ко-малеинового ангидрида-ко-этиленгликольдиакрилата, с тиолизированным олигомером; сополимер поливинилпирролидона и акриловой кислоты, размером частиц около 1-2 нм по данным динамического рассеяния света (DLS) (фигура 18) и обеспечивающих незначительное увеличение размеров наночастиц (фигуры 16,17,19,20).
В частных вариантах воплощения изобретения лиганд конъюгирован с полимерной оболочкой через линкер.
В частных вариантах воплощения изобретения линкер представляет собой полипропиленгликоль, полиэтилен гликоль акрилат, стрептавидин или стрептавидин с His-tag.
В частных вариантах воплощения изобретения лиганды включают, но не ограничиваются ими, малые молекулы, пептиды, антитела, фрагменты антител, нанотела, нуклеиновые кислоты, причем указанные лиганды обладают специфичностью к молекулярным маркерам (мишеням), включая, но не ограничиваясь ими, фолаты, RGD-пептиды, антитела, фрагменты антител, нанотела анти-HERI, анти-HER2, анти-ЕрСАМ, анти-EGFR, анти-VEGF, анти-р16, анти-Ki-67, ЕР, анти-PR, анти-CD3, анти-CD19, анти- CD20, анти-CD33, анти-CD33, анти-CD38, анти-CD47, анти-CD-52, анти-CD79 В, анти-PD-1, анти-CD269, анти-CD274, анти-CD319, анти-CTLA-4, анти-c-Met, анти-Anti-Nectin-4, анти-TF, анти-TROP2, анти-FRα, анти-NGF, анти-CTGF, анти-TNFSF11, анти-RANKL, анти-Trop-2, анти-TIGIT, анти-IL-1, анти-IL6, анти-IL-23, анти-СЕАСАМ5, анти-VEGFR2, анти-TGF-βRII, анти-CD3, анти-TIM-3, анти-CLDN18.2, анти-СА125, анти-NKG2A, анти-LAG-3, анти-PDGF-R α, анти-IFN-gamma, анти-TIM-3, анти-PCSK9, анти-TNF, анти-GM-CSF, нуклеиновые кислоты (ДНК-зонды), комплементарные фрагментам различных онкогенов, например, онкогена HER2, ABL, c-Met и другие, для определения делеций, например, р-плеча хромосомы 12, ТР53 гена, анализа транслокации t(2;5)(p23;q35), трисомий и другие.
В частных вариантах воплощения изобретения молекулярные маркеры включают, но не ограничиваются ими, белковые структуры, входящие в состав клеток, например биомолекулы, участвующие в онкогенезе, в клеточном цикле, являющиеся сигнальными и характеризующие развитие различных заболеваний, интегрины, HER1, HER2, ЕрСАМ, EGFR, VEGF, р16, Ki-67, ЕР, PR, CD3, CD19, CD20, CD33, CD33, CD38, CD47, CD-52, CD79B, PD-1, CD269, CD274, CD319, CTLA-4, c-Met, Anti-Nectin-4, TF, TROP2, FRα, NGF, CTGF, TNFSF11, RANKL, Trop-2, TIGIT, IL-1, IL6, IL-23, CEACAM5, VEGFR2, TGF-βRII, CD3, TIM-3, CLDN18.2, CA125, NKG2A, LAG-3, PDGF-R α, IFN-gamma, TIM-3, PCSK9, TNF, GM-CSF, протоонкоген ABL и другие.
В частных вариантах воплощения изобретение может быть использовано в микроскопии (фигура 24) и цитофлуорометрии (фигура 23).
Технический результат также достигается посредством осуществления способа получения квантовой точки по изобретению, который включает следующие стадии:
а) синтез ядра квантовый точки, включающий:
- осуществление подготовки растворов прекурсоров Se, Те и S;
- смешивание при интенсивном перемешивании в атмосфере инертного газа CdO, октадецилфосфоновой кислоты и триоктилфосфин оксида при температуре 345-360°С до полного растворения CdO;
- добавление триоктилфосфина в реакционную смесь после растворения CdO;
- добавление в реакционную смесь растворов прекурсоров Se, Те и S;
- охлаждение реакционной смеси;
- очистка ядер путем двухкратного переосаждения метанолом из смеси толуол-бутанол 1:1;
б) наращивание оболочки на ядро квантовой точки.
В частных вариантах воплощения изобретения стадия смешивания при интенсивном перемешивании в атмосфере инертного газа CdO, октадецилфосфоновой кислоты и триоктилфосфин оксида осуществляется при температуре 350-355°С.
В частных вариантах воплощения изобретения инертный газ представляет собой аргон.
В частных вариантах воплощения изобретения оболочка представляет собой CdZnS, CdS/ZnS, CdS/CdZnS или CdZnS/ZnS.
В частных вариантах воплощения изобретения квантовая точка имеет структуру CdTeSeS/CdS, CdTeSeS/CdZnS, CdTeSeS/CdS/CdZnS, CdTeSeS/CdZnS/ZnS, или CdTeSeS/CdS/ZnS.
В частных вариантах воплощения изобретения для синтеза ядра используется Те с содержанием от 0,1 до 15% от общего содержания прекурсоров.
В частных вариантах воплощения изобретения для синтеза ядра используется Те с содержанием от 1,5 до 5% от общего содержания прекурсоров.
Несмотря на большой потенциал, заключенный в функциональных характеристиках квантовых точек, работающих в диапазоне, красного и пограничном к ближнему инфракрасному излучению, на сегодняшний день нерешенными остаются проблемы, связанные с их низкой фото- и коллоидной стабильностью, низким уровнем защиты квантовых точек полимерными оболочками, стабильностью самих квантовых точек, и возможности таргетирования внутриклеточных структур, обуславливающие обесцвечивание, токсичность и невозможность определения ряда молекулярных маркеров (мишеней), что существенно ограничивает диапазон их потенциальных применений. Задача, решаемая в настоящем изобретении, позволяет расширить доступный арсенал средств в данной области техники. Создаваемые квантовые точки и конъюгаты на их основе универсальны и могут применяться в составе различных средств для диагностики заболеваний, визуализации молекулярных маркеров, изготовлении флуоресцентных чернил и пигментов, средств для обнаружения утечек, например, хладагента в холодильных установках и системах кондиционирования воздуха, обнаружения движения жидкостей, например, выявление загрязнения нефтепластов, оптоэлектронике, изготовлении светодиодов, дисплеев, фотоприемников, изготовлении фотокатализаторов, нанометок для товаров и т.д.
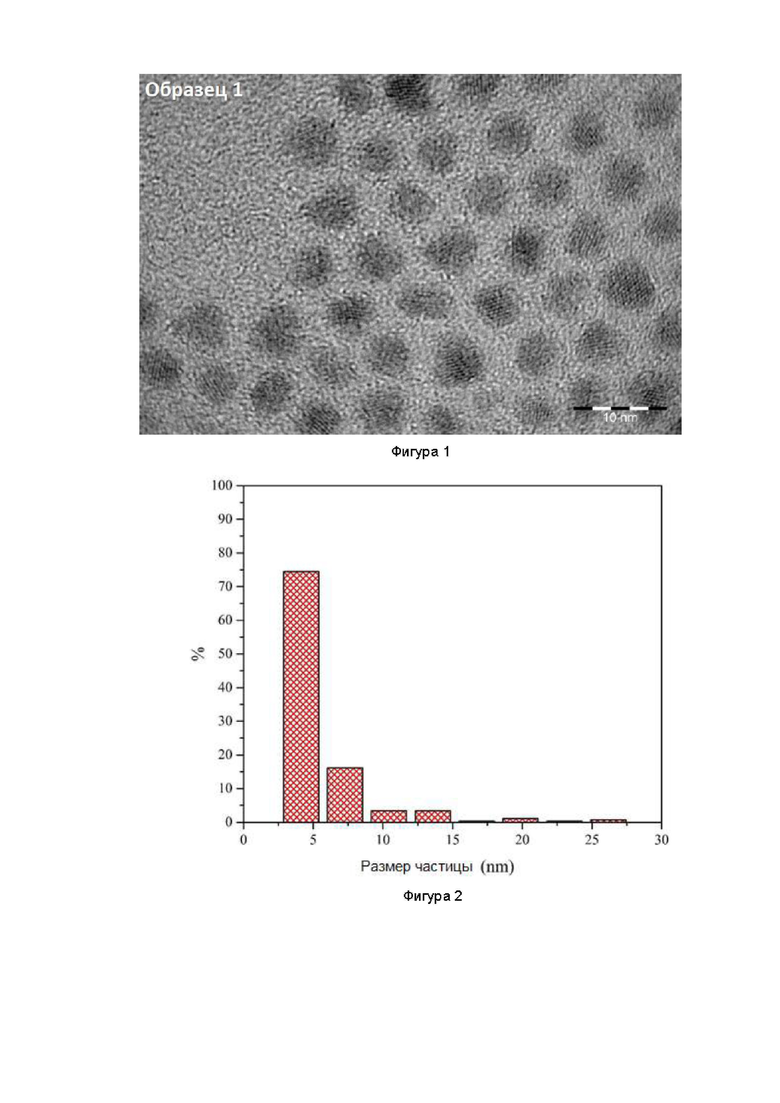
Краткое описание чертежей Фигура 1. - ПЭМ ядер квантовых точек CdTeSeS. Фигура 2. - Распределение размера ядер CdTeSeS. Фигура 3. - ПЭМ ядер квантовых точек CdTeSeS.
Фигура 4. - ПЭМ ядер квантовых точек CdTeSeS и визуализация межатомных расстояний. Согласно анализу изображений ПЭМ BP, полученные значения d соответствуют таковым для фазы P63mc, таким образом, образцы ядер содержат наночастицы вюрцита. Элементы 1-4, которые выделены на фигуре 3.
Фигура 5. Квантовые точки CdTeSeS/CdZnS.
Фигура 6. Квантовые точки CdTeSeS/CdS/ZnS.
Фигура 7. Распределение размера квантовых точек CdTeSeS/CdZnS.
Фигура 8. ПЭМ квантовых точек CdTeSeS/CdZnS.
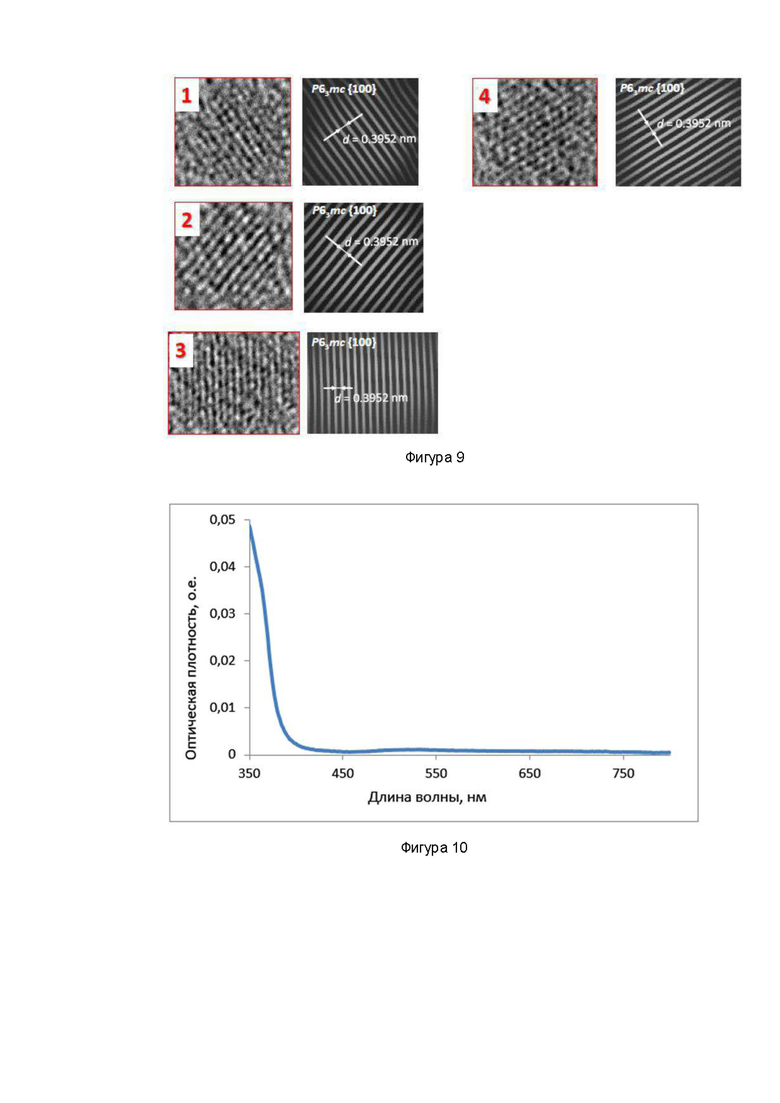
Фигура 9. ПЭМ квантовых точек CdTeSeS/CdZnS и визуализация межатомных расстояний. Согласно анализу изображений ПЭМ BP, полученные значения d (interatomic distance) соответствуют таковым для фазы P63mc, таким образом, можно сделать вывод, что все образцы содержат наночастицы вюрцита. Элементы 1-4, которые выделены на фигуре 8.
Фигура 10. Спектр оптического поглощения полимера PEGPT 1%.
Фигура 11. Спектр оптического поглощения полимера PEGPTT 1%.
Фигура 12. Спектр оптического поглощения квантовых точек (CdTeSeS/CdS/ZnS, 8 монослоев) в полимере PEGPT.
Фигура 13. Спектр оптического поглощения квантовых точек (CdTeSeS/CdS/ZnS, 8 монослоев) в полимере PEGPTT
Фигура 14. Спектр флуоресценции квантовых точек (CdTeSeS/CdS/ZnS) в полимере PEGPT.
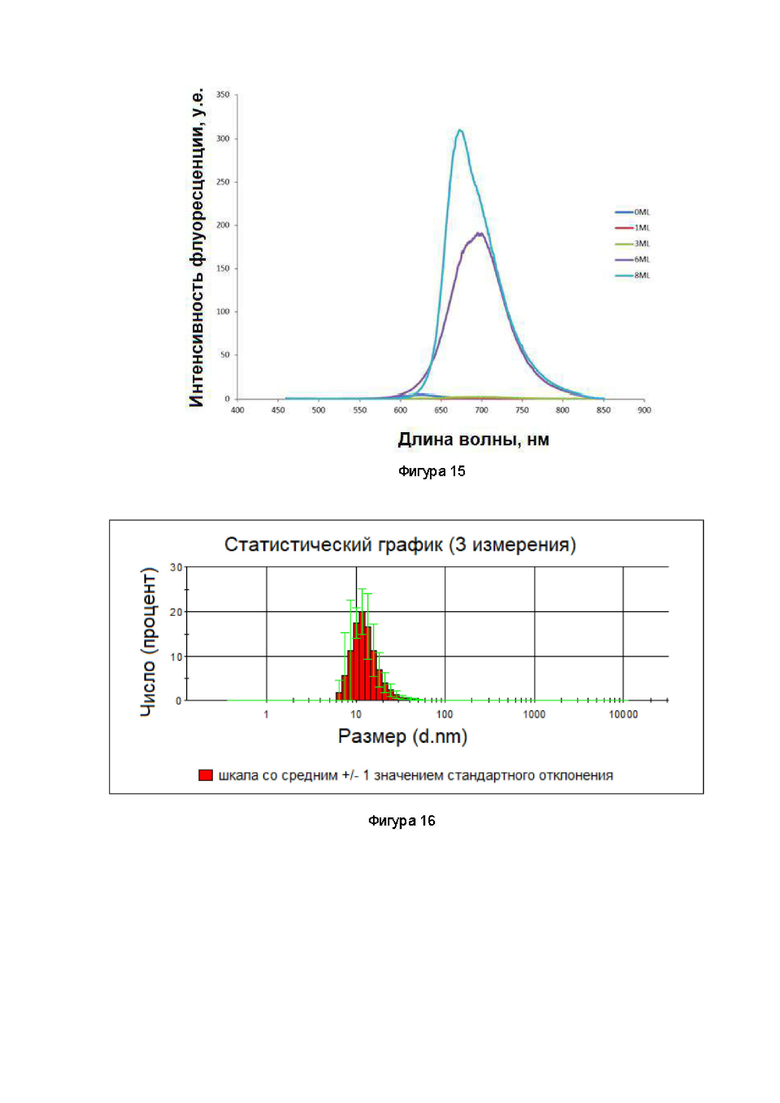
Фигура 15. Спектры флуоресценции образцов квантовых точек в полимере PEGPT с различным количеством монослоев.
Фигура 16. Гидродинамический диаметр квантовых точек CdTeSeS/CdS/ZnS в полимере PEGPT.
Фигура 17. Гидродинамический диаметр квантовых точек CdTeSeS/CdZnS в полимере PEGPT.
Фигура 18. Гидродинамический диаметр полимера PEGPT.
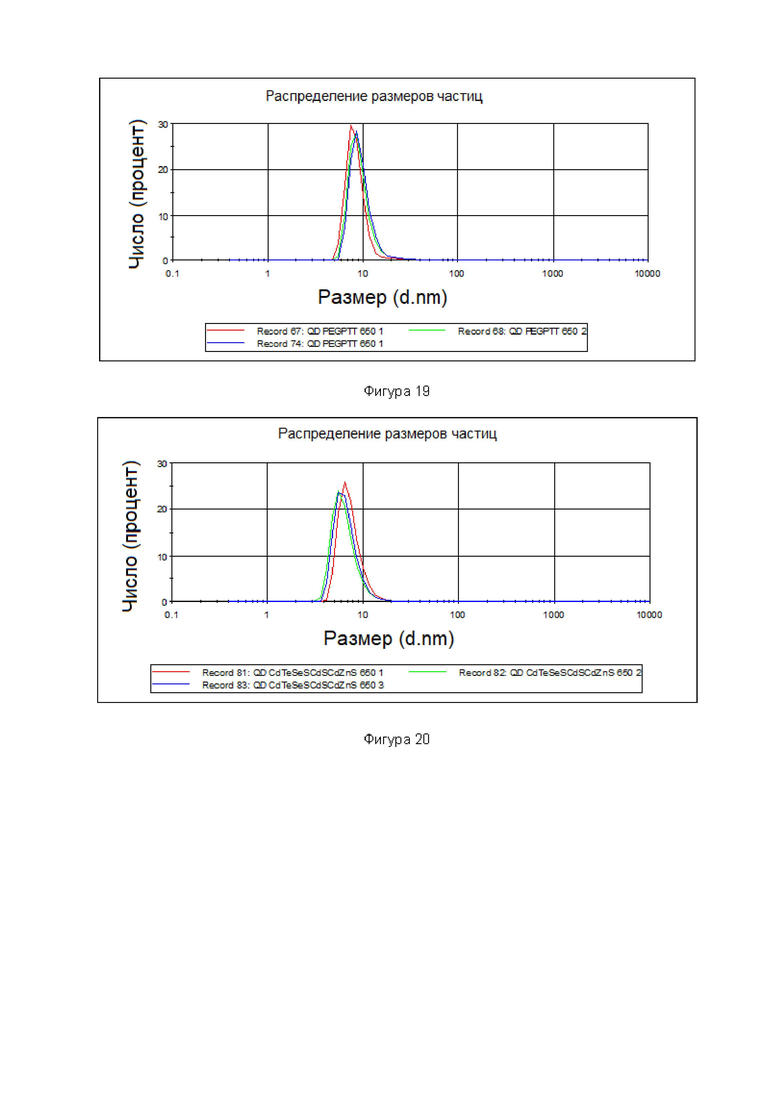
Фигура 19. Распределение размера квантовых точек по изобретению со структурой CdTeSeS/CdS/CdZnS в полимере PEGPTT, полученных с использованием МРА - со средним размером инкапсулированных квантовых точек 8 нм.
Фигура 20. Распределение размера квантовых точек по изобретению со структурой CdTeSeS/CdS/CdZnS, со средним размером 6.7 нм.
Фигура 21. Распределение размера ядер квантовых точек по изобретению со структурой CdTeSeS, средним размером 2-4 нм.
Фигура 22. Смешанная карта EDX S/Se/Cd и соответствующий профиль линии, взятый вдоль двух квантовых точек.
Фигура 23. Исследование цитометрии квантовых точек CdTeSeS/CdZnS-PEGPTT, конъюгированных с антителами против антигена CD3 человека.
Фигура 24. Иммуноцитохимическое окрашивание клеток линии НТ29 КТ CdTeSeS/CdZnS-PEGPTT, конъюгированных с антителами против антигена c-Met человека.
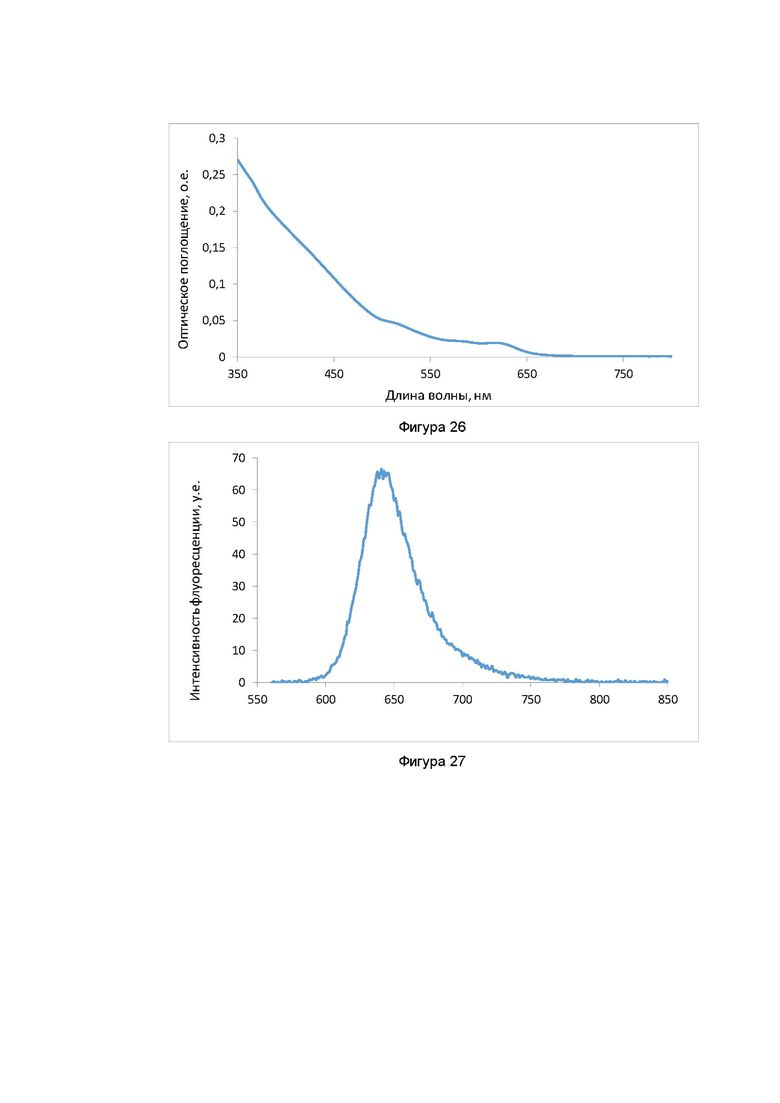
Фигура 25. Распределение размера квантовых точек CdTeSeS/CdS/CdZnS. Фигура 26. Спектр оптического поглощения квантовых точек (CdTeSeS/CdS/CdZnS) в полимере PEGPTT.
Фигура 27. Спектр флуоресценции квантовых точек (CdTeSeS/CdS/CdZnS) в полимере PEGPTT.
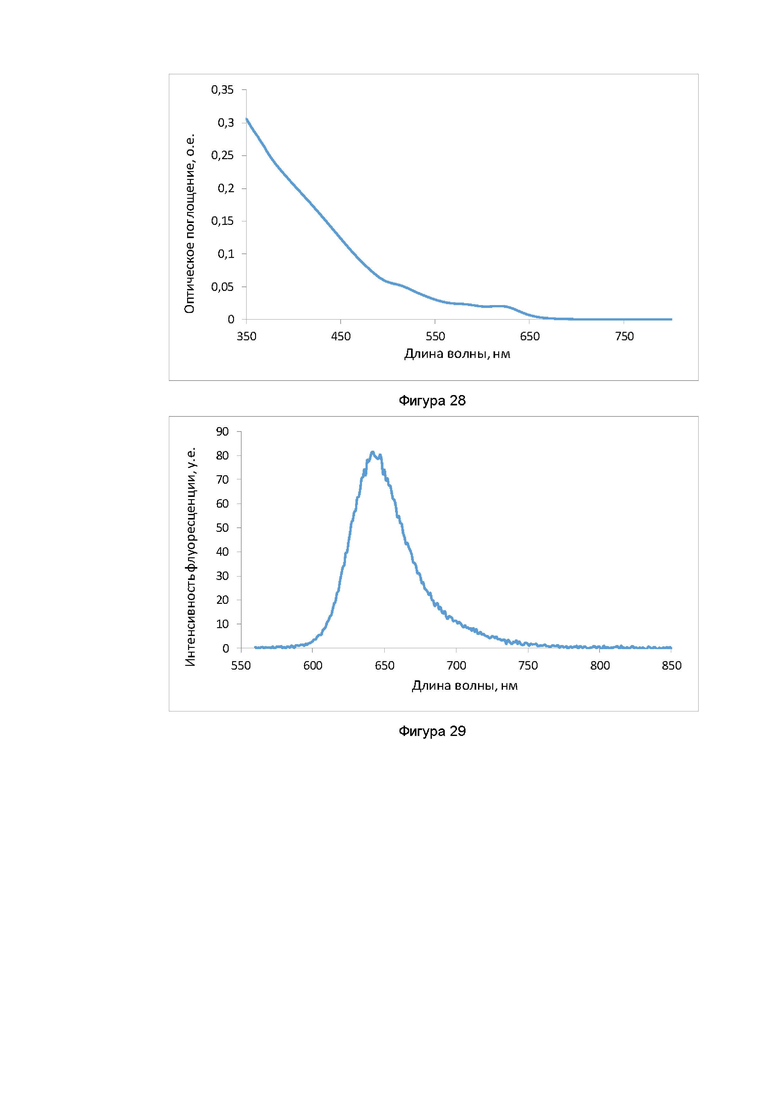
Фигура 28. Спектр оптического поглощения квантовых точек (CdTeSeS/CdS/CdZnS) в полимере PEGPTT, конъюгирован со стрептавидином (SA).
Фигура 29. Спектр флуоресценции квантовых точек (CdTeSeS/CdS/CdZnS) в полимере PEGPTT, конъюгирован со стрептавидином (SA).
Фигура 30. Спектр оптического поглощения квантовых точек (CdTeSeS/CdS/CdZnS) в полимере PEGPTT), конъюгирован со стрептавидином (SA), связанным с антителом против прогестеронового рецептора.
Фигура 31. Спектр флуоресценции квантовых точек (CdTeSeS/CdS/CdZnS) в полимере PEGPTT), конъюгирован со стрептавидином (SA), связанным с антителом против прогестеронового рецептора.
Фигура 32. Распределение размера квантовых точек CdTeSeS/CdS/CdZnS в полимере PEGPTT, полученных без использования МРА-со средним размером 16 нм.
Термины и определения
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, использованные в настоящем описании изобретения.
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из». Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
Термин «квантовая точка» (КТ) в соответствии с использованием в настоящем документе обозначает полупроводниковые нанокристаллы, которые содержат ядро и оболочку, имеют распределение по размерам 6-8 нм.
Термин «монослой» представляет собой единый, плотно упакованный слой атомов.
Термин «лиганд» - любое химическое соединение, которое способно специфически взаимодействовать с другим химическим соединением, в т.ч. с молекулярным маркером, образуя стабильный комплекс.
Термин «молекулярный маркер» - любое химическое соединение, представляющее ценность для получения информации об объекте исследования.
Термин «линкер» - химическое вещество, обеспечивающее химическую связь между КТ и лигандом и не оказывающее неблагоприятного воздействия на свойства и стабильность лиганда.
Подробное раскрытие изобретения
Квантовые точки (КТ) по изобретению без полимерного покрытия, где А-ядро/Б-полупроводниковая оболочка характеризуются, в частности, следующей структурой: CdTeSeS/CdS, CdTeSeS/CdZnS, CdTeSeS/CdS/CdZnS, CdTeSeS/CdZnS/ZnS или CdTeSeS/CdS/ZnS.
Квантовые точки по изобретению могут быть инкапсулированы в полимерное покрытие для их гидрофилизации и последующей конъюгации, в частности, полимером для гидрофилизации является:
PEGPT - сополимер метоксиполиэтиленгликольакрилата-ко-малеинового ангидрида-ко-этиленгликольдиакрилата, терминированный 1,6-гександитиолом;
PEGPTT - сополимер метоксиполиэтиленгликольакрилата-ко-малеинового ангидрида-ко-этиленгликольдиакрилата, с тиолизированным олигомером;
PTVP - сополимер поливинилпирролидона и акриловой кислоты.
На поверхность полимерной оболочки могут быть иммобилизованы лиганды, позволяющие эффективно связываться с биологическими распознаваемыми молекулами. Полимерные оболочки позволяют экранировать КТ от внешних воздействий, для целей их последующего применения в составе современных высокочувствительных биомедицинских диагностических тест-систем.
Инкапсуляция в полимерные оболочки квантовых точек преследует следующие цели: придание гидрофильных свойств и обеспечение растворимости квантовых точек и флуоресцентных конъюгатов в заданном растворителе; предотвращение агрегации и осаждения квантовых точек и флуоресцентных конъюгатов; введение необходимых функциональных групп для последующей конъюгации биокомпонентов. Общая стратегия придания флуоресцентным нанокристаллам диспергируемости в воде включает замену исходных гидрофобных лигандов лигандами, имеющими, с одной стороны, химические группы, способные связываться с поверхностью нанокристалла, с другой - полярные группы (например, гидроксильные), направленные в водную фазу. Другой подход основан на сохранении оригинальных лигандов и создании оболочки из амфифильных молекул или полимеров, имеющих гидрофобные группы для связи с оригинальными лигандами, и гидрофильные группы, обеспечивающие растворимость в воде.
Полученные образцы характеризовали спектрофотометрически (фигуры 10-13, 26, 28, 30).
Для получения КТ по настоящему изобретению используется следующая общая схема (технологическая цепочка):
1. Синтез ядер КТ.
2. Наращивание полупроводниковых оболочек.
3. Выделение и очистка КТ, их характеризация.
Для получения флуоресцентных конъюгатов на основе КТ по настоящему изобретению используется следующая общая схема (технологическая цепочка):
1. Синтез ядер квантовых точек.
2. Наращивание полупроводниковых оболочек.
3. Выделение и очистка квантовых точек, их харастеризация.
4. Синтез водорастворимого полимера для создания полимерной гидрофильной оболочки, имеющей функциональные группы для конъюгации с лигандами за счет ковалентного взаимодействия.
5. Инкапсуляция квантовых точек в полимерную оболочку. Выделение и очистка флуоресцентных нанокристаллов в оболочке, их характеризация.
6. Конъюгация квантовых точек в полимерной оболочке с лигандами, обладающими специфичностью связывания с целевыми биомолекулами.
Способ синтеза квантовых точек по изобретению характеризуется тем, что осуществляется совместное введения серы с другими прекурсорами при синтезе ядра CdTeSeS, и предназначен для получения ультрамалых ядер квантовых точек CdTeSeS, с количеством вводимого Те от 0,1 до 15% (в предпочтительных вариантах воплощения изобретения от 0,15 до 5%) от общего количества халькогенов, с максимумом в распределении размера ядра 2,5 нм, а собственно готовых квантовых точек с полупровдниковыми оболочками размером 6-8 нм и структурой, в частности, CdTeSeS/CdS, CdTeSeS/CdZnS, CdTeSeS/CdS/CdZnS, CdTeSeS/CdZnS/ZnS или CdTeSeS/CdS/ZnS.
Ключевым достижением данного изобретения является возможность формирования ядра квантовых точек размером в диапазоне 2-4 нм по данным просвечивающей электронной микроскопии (ТЕМ) (фигура 1,2) и с максимумом в распределении размера 2,5 нм по данным динамического рассеяния света (DLS) при температуре 345-360°С.
При этом, формируется вюрцитовая структура кристалла, которая подтверждена данными ТЕМ (см. фигуры 4,9). Кроме того, это также подтверждается тем фактом, что осуществляется равномерное и эффективное наращивание полупроводниковых оболочек на данные ядра и высокой фотостабильностью квантовых точек.
С целью снижения размеров наночастиц при сопоставимой длине волны эмиссии были синтезированы ядра CdTeSeS, включающие Те. Используя, в частности, 0,17 и 5% Те и снизив температуру ввода прекурсора, в частности, до 350°С, удалось получить ядра с эмиссией от 540 нм. Наращивание дополнительных полупроводниковых оболочек позволяло смещать спектр в требуемый диапазон (630-720 нм).
В стандартных, описанных в уровне техники технологиях синтеза КТ с ядрами CdTe и CdTeSe подобного размера, в которых используют температуру синтеза ниже 340°С, синтез осуществляют в водной среде (например, CN104974742A), в результате это приводит к формированию кристаллической структуры сфалерита, либо тетраподов. Последние варианты структур отличаются низкой способностью к наращиванию дополнительных полупроводниковых оболочек, поскольку рост идет неравномерно и происходит агрегация частиц. При наслаивании оболочек возникают дефекты в кристаллической структуре, которые негативно влияют на свойства наносистемы, в т.ч. на фотостабильность.
Ядра КТ по изобретению, полученные способом синтеза по изобретению, характеризуются тем, что наращивание оболочек на них осуществляется эффективно, в частности оболочки CdS, что приводит к получению КТ с максимумом эмиссии 630-720 нм, при размере 6-8 нм характеризуются высокой фотостабильностью.
В частных вариантах воплощения изобретения инкапсуляция КТ в полимер осуществляется с полимером с тиолизированным олигомером (фигура 19, 32). В предпочтительном варианте тиолизированный олигомер представляет собой политиол, в частном варианте тритиол.
Инкапсуляция КТ по изобретению в полимер с тиолизированным олигомером через замещение, в частности, с использованием 3-меркаптопропионовой кислоты дает конечный размер частиц в диапазоне 8-18 нм (см. пп 2.3.4). Инкапсуляция КТ по изобретению в полимер с тиолизированным олигомеров дает конечный размер частиц в диапазоне 10-33 нм. Такая флуоресцентная наноразмерная метка может применяться в качестве контрастирующего агента для визуализация (КТ в сополимерной оболочке, где присутствуют мономер полиэтиленгликоля и/или другие компоненты, обеспечивающие ее стабильность), может быть конъюгирована через линкер, предпочтительно -полипропиленгликоль, полиэтиленгликоль акрилат с малой молекулой, пептидом, нанотелом, фрагментами антител, антителами, нуклеиновыми кислотами.
В ходе проведенных работ были синтезированы КТ с количеством монослоев от 1 до 8. Для наращивания оболочек использовали процедуры, описанные в методиках молекулярного наслаивания [4].
В результате проведенных исследований было установлено, что в отсутствии полупроводниковых оболочек наступает агрегация частиц, что, скорее всего, связано с низким сродством поверхности ядра к полимеру. Кроме того, квантовый выход (KB) при этом не превышает 5%, что является следствием недостаточной пассивации ядра КТ.
Аналогичная ситуация наблюдается, когда монослоев 3 и менее монослоев. Оптимальная полупроводниковая оболочка, дающая KB 60%, составляет от 5 до 8 монослоев.
Примеры осуществления изобретения
Нижеследующие примеры приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Ниже приведен пример синтеза наноразмерной метки и конъюгатов на ее основе. 1. Синтез КТ.
1.1 Синтез ядер CdTeSeS.
Способ синтеза реализуется следующим образом. В каждой колбе растворяют селен и теллур в триоктилфосфине, серу в смеси октантиола с октадецен-1. Процесс растворения проводят в герметично закрытой колбе, сопровождают дегазацией и последующей продувкой инертным газом и облучением ультразвуком при температуре 60°С. После этого растворенные вещества облучают ультразвуком до исчезновения мутности.
В частных вариантах воплощения изобретения процентное содержание вводимого Те по отношению к другим прекурсорам составляет от 0,1 до 15%. В предпочтительных вариантах воплощения изобретения процентное содержание вводимого Те составляет от 0,15 до 5%. В колбу добавляют 0,6 г CdO, 4 г октадецилфосфоновой кислоты и 30 г триоктилфосфин оксида и герметично закрывают и при интенсивном перемешивании смесь дегазируют и продувают инертным газом. После полного растворения кадмия добавляют 10 мл триоктилфосфина. Температура синтеза может быть в диапазоне 350-355°С. Далее в реакционную смесь вводят 5 мл (общая концентрация халькогенидов 1М) растворенного селена, серы и теллура с молярным содержанием добавки прекурсора теллура в расчете на содержание Те в ядре от 0,15 до 5%. Реакцию ведут в течение 3 мин, после смесь охлаждают до комнатной температуры и проводят очистку путем двукратного переосаждения метанолом из смеси толуол-бутанол 1:1, конечный продукт растворяют в толуоле.
1.2 Наращивание оболочки CdS
В колбу добавляют 4,48 г CdO, 25 мл олеиновой кислоты, 75 мл октадецен-1 и 0,5 мл уксусной кислоты. Процесс растворения проводят в герметично закрытой колбе, сопровождают дегазацией и последующей продувкой инертным газом при температуре 150°С и интенсивном перемешивании до получения прозрачного раствора. Октантиол с октадецен-1 получали как описано выше. Объемы растворов рассчитывали на количество монослоев с учетом разбавления, необходимых для настройки длины волны флуоресценции. После этого производили очистку продукта по тому же протоколу
Продукт, полученный на предыдущем этапе, растворенный в гексане 100 нмоль выливают в смесь 3 мл октадецен-1 и 3 мл олеиламина. Колбу герметично закрывают и смесь вакуумируют при комнатной температуре 1 час и при 120°С 20 мин до полного удаления растворителей и газов. После раствор нагревают до 310°С со скоростью 18°С/мин в токе инертного газа и перемешивании. При достижении температуры 240°С рассчитанные количества олеата кадмия в 6 мл октадецен-1 и октантиола (1,2 эквивалента относительно олеата Cd в 6 мл октадецен-1) прибавляют по каплям со скоростью 3 мл/ч с помощью шприца. Затем быстро вливают 1 мл олеиновой кислоты и раствор нагревают далее до 310°С в течение 60 мин. Полученный продукт осаждают ацетоном, затем редиспергируют в гексане. Далее очищают дважды осаждением-редиспергированием и окончательно суспендируют в гексане или хлороформе.
Оболочки CdS наращивают послойно, поочередным введением олеата кадмия 0,1 М в октадецен-1 и серы 0,1 М в октадецен-1. Введение каждого прекурсора в реакционную смесь ведут в течение 3~5 мин. Время роста 10 мин после каждого введения. После раствор охлаждают до комнатной температуры и очищают аналогично.
1.3 Наращивание оболочки ZnS
В колбу помещают 5 мл октадецен-1, 2 мл триоктилфосфина, рассчитанное количество диэтилдитиокарбамата цинка и 0,35 М раствор Zn(OAc)2 в смеси с олеиламином и октадеценом-1 (1:2) (соотношение диэтилдитиокарбамата цинка: Zn(OAc)2=1:1 мол. экв.). Количества прекурсоров рассчитывают для настройки длины волны флуоресценции по методу молекулярного наслаивания (SILAR), исходя из количества исходных КТ [1], как описано выше. Сначала реакционную массу дегазируют при температуре 80-100°С. Затем продувают инертным газом при температуре 150°С в течение 30 мин и перемешивании. По окончанию синтеза реакционную смесь охлаждают и очищают аналогично описанному выше способу.
1.4 Наращивание оболочки CdZnS
В колбу вносят 10 г октадециламина, 30 мл октадецен-1 и рассчитанное количество КТ CdTeSeS/CdS в толуоле. Далее колбу герметично закрывали и смесь дегазировали при температуре 80-100°С при постоянном перемешивании. После вводили инертный газ и вели реакцию при 240°С проводя поочередное введение смеси кадмия 0,35 М и цинка 0,35 М (мольное соотношение 1:1) с интервалом 30 минут и 0,35 М раствора S с интервалом 60 минут. Количества прекурсоров рассчитывали по методу молекулярного наслаивания (SILAR). Смеси кадмия и цинка вводят не более, чем в течение 30 секунд, раствор серы вводят по каплям в течение 10 минут. После этого цикл наращивания повторяют. В конце синтеза смесь охлаждают и очищают аналогично описанному выше способом.
2 Инкапсуляция КТ
2.1 Вариант 1. Инкапсуляция в PTVP
2.1.1 Синтез полимера PTVP
Полимер PTVP был синтезирован по методике [3].
В 250 мл трехгорлую колбу помещают 15 мл N-винил-2-пирролидон (далее VP) (140 ммоль), 5 г (51 ммоль) малеинового ангидрида (далее MAN) в смеси 10 мл уксусной кислоты и 15 мл тетрагидрофурана. MAN растворяют при перемешивании и затем добавляют 0,66 г (2,4 ммоль) 4,4'-азобис(4-циановалериановой кислоты) (далее ABCVA). Смесь продувают инертным газом, в предпочтительном варианте аргоном, и кипятят 15 мин при перемешивании. Затем добавляют 2 мл (10,6 ммоль) этиленгликоль диметакрилат (далее EGDMA) и 0,3 г (1,2 ммоль) ABCVA, растворенных в 20 мл тетрагидрофурана. После 10 мин кипячения реакцию останавливают добавлением 1,6-гександитиола (далее НТ) (15 мл, 102 ммоль) в 20 мл тетрагидрофурана. После этого нагрев прекращают, и раствор охлаждают до комнатной температуры. Далее добавляют 3 объема диэтилового эфира для осаждения полимера. Далее полимер отделяют центрифугированием при 10000g и растворении в N,N-диметилформамиде (далее DMF). Цикл растворение/осаждение повторяют дважды, полученный продукт промывают диэтиловым эфиром.
2.1.2 Подготовка КТ к инкапсуляции в PTVP
Раствор КТ в толуоле центрифугируют с 4-кратным количеством безводного этанола (18000д, 15 мин), осадок ресуспендируют в хлороформе. Водный раствор 100 мМ 3-меркаптопропионовой кислоты (далее МРА) (800 мкл) с ТМАОН (рН 11,0), добавляют к раствору КТ в хлороформе (800 мкл) и энергично встряхивают 4 ч в темноте. Водную фазу, содержащую КТ, отделяют, и далее центрифугируют при 15000д 15 мин, супернатант диализируют 8 ч против 10 мМ фосфатного буфера (рН 7,4) в темноте в герметично закрытой колбе.
2.1.3 Инкапсуляция КТ в PTVP
К дисперсии 0,5 г КТ-МРА (МРА - 3-меркаптопропионовая кислота) в 7 мл воды при перемешивании добавляют 0,75 г PTVP-PPG-FA в 10 мл воды. Через 30 мин перемешивания смесь центрифугируют.Супернатант обрабатывают тетрагидрофураном до помутнения дисперсии. Осадок отделяют и диспергируют в 10 мл воды. Далее проводят очистку.
2.2 Вариант 2. Инкапсуляция в PEGPT 2.2.1 Синтез полимера PEGPT
В колбу помещают 40 г метилового эфира ПЭГ-акрилата 83 ммоль, 4,6 г (42 ммоль) малеинового ангидрида (далее MAN) в смеси 50 мл уксусной кислоты и 100 мл тетрагидрофурана. MAN растворяют при перемешивании и затем добавляют 1,2 г (4,2 ммоль) ABCVA. Смесь продувают инертным газом и кипятят 10 мин при перемешивании. Затем добавляют 3,5 мл (18,6 ммоль) EGDMA и 0,12 г (0,42 ммоль) ABCVA, растворенных в 20 мл тетрагидрофурана. После 10 мин кипячения реакцию останавливают добавлением НТ (15 мл, 102 ммоль) в 20 мл тетрагидрофурана. После этого смесь выдержают при температуре 75°С 1 час, и раствор охлаждают до комнатной температуры. Для осаждения полимера добавляют около 3-х объемов гексана. Полимер отделяют на делительной воронке. Дополнительно промывают 100 мл гексана и дважды 100 мл диэтилового эфира.
2.2.3 Инкапсуляция КТ в PEGPT
Полимер PEGPT 1 г растворяют в 4 мл тетрагидрофурана при перемешивании.
Вводят 0,6 мл 22% гидрофобных КТ CdTeSeS/CdS/CdZnS в хлороформе и перемешивают 20 мин, затем вводят по каплям 1 мл насыщенного раствора тетраметиламмоний гидроксид пентагидрата (далее ТМАОН) в 50% водном DMF и перемешивают 30 мин. Затем смесь разбавляют диэтиловым эфиром и осадок центрифугируют 5 мин 10000g. Далее его диспергируют в 5 мл тетрагидрофурана и процедуру осаждения повторяют. Полученный остаток сушат в вакууме для удаления остатков растворителей и диспергируют в 5 мл воды. Очистку полученного продукта от избытка лигандов и ТМАОН осуществляют ультрафильтрацией через мембрану 30000 MWCO двукратно. Остаток диспергируют в натрий-фосфатном буфере рН 8,0 до концентрации КТ 5 мкМ.
2.3 Вариант 3. Инкапсуляция в PEGPTT
2.3.1 Синтез тиолизированного олигомера ТТ - тритиол (политиол)
15 г 1,6-гександитиола (0,1 моль) растворяют в 20 мл тетрагидрофурана и после добавляли 0,05 г триоктилфосфина (0,135 ммоль) в качестве катализатора. При перемешивании вводят 8,36 г (0,02 моль) триметилолпропан этоксилат триметакрилата. Смесь разогревалась до 50°С и перемешивают еще 1 час.Затем растворители удаляют вакуумированием.
2.3.2 Синтез полимера PEGPTT
В колбу вносят 40 г метилового эфира ПЭГ-акрилата Мп 480 г/моль (83 ммоль), 4,6 г (42 ммоль) MAN в смеси 50 мл уксусной кислоты и 100 мл тетрагидрофурана. MAN растворяют при перемешивании и затем добавляют 1,2 г (4,2 ммоль) ABCVA. Смесь продувают инертным газом и кипятят 10 мин при перемешивании. Затем добавляют 3,5 мл (18,6 ммоль) EGDMA и 0,12 г (0,42 ммоль) ABCVA, растворенных в 20 мл тетрагидрофуране. После 10 мин кипячения реакцию останавливают добавлением ТТ (20 г) в 20 мл тетрагидрофурана. Затем смесь выдерживают 1 час при температуре 75°С, и после охлаждают до комнатной температуры. Добавляют 3 объема гексана и продукт отделяют на делительной воронке. Дополнительно промывают 100 мл гексана и дважды 100 мл диэтилового эфира.
2.3.3 Инкапсуляци КТ в PEGPTT, вариант 1
Полимер PEGPTT 1 г растворяют в 4 мл тетрагидрофурана.и водят 0,5 мл 22% гидрофобных КТ CdTeSeS/CdS/CdZnS в хлороформе. Смесь перемешивают 20 мин, затем вводят по каплям 1 мл насыщенного раствора ТМАОН в 50% водном ДМФА. Перемешивают еще 30 мини после разбавляют диэтиловым эфиром до помутнения. Осадок центрифугируют 5 мин 10000g. Далее его диспергируют в 5 мл тетрагидрофурана и процедуру осаждения повторяют. Полученный остаток сушат в вакууме для удаления остатков растворителей и диспергируют в 5 мл воды. Очистку полученной дисперсии от избытка лигандов и ТМАОН осуществляют ультрафильтрацией двукратно. Остаток диспергируют в натрий-фосфатном буфере рН 9,0.
2.3.4 Инкапсуляция КТ в PEGPTT, вариант 2
2.3.4.1 Подготовка полимера PEGPTT к модификации КТ 10 г PEGPTT растворяют в 30 мл дистиллята. Доводят раствор до рН 8,5 постепенным добавлением ЗМ NaOH. После этого раствор оставляют на ночь при перемешивании. Затем фракцию менее 30 кДа получают путем ультрафильтрации. Массовую концентрацию низкомолекулярной фракции определяют путем упаривания аликвоты (0,05 мл) при 100°С в течение 2 ч.
2.3.4.2 Присоединение МРА к КТ
В дисперсию 0,5 г гидрофобных КТ в 40 мл хлороформа при перемешивании вводят 30 мл 30% раствора МРА в метаноле, нейтрализованного тетраметиламмоний гидроксидом до рН 6-7. Перемешивание ведут 1-2 часа до формирования крупного, легко оседающего осадка. Осадок отделяют центрифугированием 10000g, 2 мин. КТ диспергируют в 20 мл 5% раствора тетраметиламмоний гидроксида в метаноле. Дисперсию осаждают добавлением 2-4х объемов диэтилового эфира. Осадок отделяют центрифугированием 10000g, 2 мин и подсушивают от остатков диэтилового эфира. Полученный остаток диспергируют в 2% водном растворе тетраметиламмоний гидрооксида.
2.3.4.3 Синтез КТ- PEGPTT
Подготовленный к модификации полимер по пп. 2.3.4.1 разбавляют до концентрации 5%. 5 мл КТ-МРА в концентрации 1,5% медленно добавляют к 40 мл раствора PEGPTT при эффективном перемешивании. После добавления дисперсии, смесь перемешивают еще 2 ч при комнатной температуре, затем избыток полимера и низкомолекулярные примеси отделяют путем ультрафильтрации. Очистку ультрафильтрацией проводят дважды, остаток разбавляют дистиллятом до требуемой концентрации.
3. Получение конъюгатов
3.1. Вариант 1. Получение конъюгатов с малыми молекулами
3.1.1 Синтез конъюгата KT-PTVP-PPG-FA (где КТ CdTeSeS/CdS/CdZnS; PPG -полипропиленгликоль (линкер); FA фолиевая кислота (лиганд)).
К дисперсии 0,5 г КТ-МРА в 7 мл воды при перемешивании добавляют 0,75 г PTVP-PPG-FA в 10 мл воды. Через 30 мин перемешивания смесь центрифугируют, агрегированные частицы удаляют.Супернатант обрабатывают тетрагидрофураном до помутнения дисперсии. Осадок отделяют и диспергируют в 10 мл воды и проводят очистку.
3.1.2 Блокировка -СООН групп (синтез конъюгата KT-PTVP-PPG-FA-OH)
5 мл дисперсии КТ (~20 нмоль) активируют в присутствии 500eq N-гидроксисукцинимида (далее NHS) и 1000eq N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорида (далее EDC) в течение 30 мин при комнатной температуре. Затем добавляют 10000eq диэтаноламина. Выдерживают 1 час при перемешивании и после очищают.
Блокировка карбоксигрупп обеспечивает снижение неспецифического связывания частиц.
3.2 Вариант 2. Получение конъюгатов с антителами
Примером конъюгата по изобретению являются конъгат с квантовыми точками (CdTeSeS/CdS/CdZnS) по изобретению KT-PEGPTT и лигандом (биотинилированными антителами), который может быть конъюгирован через линкер, который представляет собой стрептавидин или His-tag стрептавидин.
Биотинилированные антитела разводят PBS рН 8,5 до концентрации 0,8 мкМ. Добавляют раствор бис-аминополиэтиленгликоля до концентрации 0,2%. Затем при перемешивании вводят дисперсию KT-PEGPTT-стрептавидин 0,2 мкМ. Смесь выдерживают один час при комнатной температуре. Избыток антител удаляют методом ультрафильтрации или гель-фильтрации. Сконцентрированную дисперсию разводят в подходящем буфере с рН не менее 8,5.
3.3 Вариант 3. Получение конъюгатов с антителами карбодиимидным способом
5 мл дисперсии KT-PEGPTT (~2 нмоль) активируют в присутствии 500 мол-экв NHS и 1000 мол-экв EDC в течение 10 мин при комнатной температуре. Затем добавляют 5 мол-экв антител в натрий-фосфатном буфере рН 8,0. Выдерживают 1 час при перемешивании. Очистку полученной дисперсии от избытка низкомолекулярных продуктов осуществляют ультрафильтрацией. Остаток хроматографируют на колонке Sephadex G200 натрий-фосфатным буфером с рН 8,5. Флуоресцентную фракцию, содержащую КТ доочищают и концентрируют на мембране Advantec 20 до концентрации КТ 5 мкМ. Затем проводят центрифугирование для удаления агрегатов (5 мин 15000g).
Исследование элементного состава методом энергодисперсионного рентгеновского излучения (EDX) образцов коллоидных флуоресцентных нанокристаллов (КТ) по изобретению
1. Объект испытания: квантовые точки CdTeSeS /CdS/CdZnS
Образцы КТ наносили на сеточки с поддерживающим слоем Lacey/Formvar.
2. Ход испытания.
Проводили сканирование образцов в режиме EDX.
3. Параметры испытания:
Карты энергодисперсионного рентгеновского излучения (EDX) были получены на Titan Themis Z, работающего при 200 кВ.
4. Результаты испытания: Получены EDX-карты КТ (фигура 22), которые показывают особенности структуры ядро-оболочка КТ. Видно, что размер пятна, соответствующего Se немного меньше по размеру, чем размер пятна, соответствующего Cd, что согласуется со структурой CdTeSeS/CdS/CdZnS, т.к. Se входит в состав только ядра. Профиль линий, взятых вдоль оси, демонстрирует то, что синтез ядер проходит успешно с включением серы S в его состав. Также видны пики содержания серы вне ядра, что соответствует лиганду (октантиол) на поверхности ядра, CdS в структуре CdTeSeS/CdS/CdZnS и лиганду (октантиол) на поверхности оболочек. Дуплет Те полностью перекрывается сигналом от Cd, поэтому данный метод не подходит для обнаружения низкого содержания Те в КТ. Уровень сигнала от Zn составил значения близкие к шуму, что соответствует незначительному количеству Zn в КТ. Среднее атомное отношение, рассчитанное для КТ составило для S - 58±3%, Se - 17±3%, Cd 25±4%.
Заключение: EDX-карты КТ демонстрируют включение атомов в структуру КТ в соответствии с осуществляемым синтезом.
Исследование спектральных характеристик образцов конъюгатов коллоидных флуоресцентных нанокристаллов (КТ) по изобретению.
На первом этапе измерены спектральные характеристики полученного полимера. Изучены спектры оптического поглощения полимера PEGPT (Фиг. 10) и PEGPTT (Фиг. 11). На втором этапе определены спектры оптического поглощения инкапсулированных КТ по изобретению в PEGPT и PEGPTT (Фиг. 12 и 13 соответственно). На третьем этапе измерены спектры флуоресценции инкапсулированных КТ на длине волны возбуждения 450 нм (Фиг. 14).
Результаты исследований спектральных характеристик полученных образцов нанокристаллов и конъюгатов на их основе демонстрируют, что с помощью разработанной методики получаются наночастицы с оптимальными спектральными характеристиками для визуализации молекулярных маркеров, а именно возбуждение в синем спектре оптического диапазона (менее 450 нм) и эмиссия в красном диапазоне и пограничном к ближнему инфракрасному.
После проведены спектрофлуорометрические исследования. На первом этапе определили флуоресценцию KT-PEGPT (Фиг. 15). После изучены спектрофлуорометрические характеристики конъюгатов в зависимости от продолжительности облучения и проведено их сравнение с инкапсулированными КТ и определена их фотостабильность (Таблица 1). На последнем этапе изучены спектральные характеристики образцов КТ, которые имеют различное количество монослоев (Фиг. 15).
В результате проведенных исследований установлено, что уменьшение количества монослоев снижает квантовый выход КТ, таким образом, оптимальное количество монослоев составляет от 5 до 8.
Определены квантовые выходы образцов КТ с различным количеством монослоев.
1. Ядра CdTeSeS 0ML (0 монослоев оболочки).
В случае отсутствия оболочки происходит агрегация, KB<5%.
2. CdTeSeS/CdS/CdZnS: -1 ML KB<5%;
- 3ML KB<5%;
-5 ML KB=50-57%
- 6ML KB=54-62%;
- 8ML KB=68-72%.
В КТ с 8 ML после центрифугирования в течение 30 мин 10000g KB составляет в среднем 70%.
Результаты исследования фотостабильности КТ с полимерной оболочкой и их конъюгатов приведены в таблице 1.

В результате сравнительного анализа экспериментальных данных по методам синтеза конъюгатов и исследованию их оптических свойств может быть сделан вывод о том, что увеличение количества тиольных групп в составе полимера и более мягкие условия конъюгации обеспечивают получение фотостабильных конъюгатов.
Исследование цитометрии квантовых точек CdTeSeS/CdZnS-PEGPTT, конъюгированных с антителами против антигена CD3 человека
1. Объект испытания: конъюгат антитела CD3 с квантовыми точками CdTeSeS/CdZnS-PEGPTT.
Подготовка образцов: рабочее разведение конъюгата антитела с квантовыми точками получали путем разведения в 10, 50 и 100 раз в физиологическом растворе, забуференном фосфатами. Исходная концентрация препарата по квантовым точкам составляла 3,6 мкМ.
2. Ход испытания.
Проводили забор 5 мл венозной крови человека. В качестве антикоагулянта использовали гепарин. Фракцию мононуклеарных клеток крови выделяли путем центрифугирования в градиенте плотности фиколл-верографина (1,077 г/мл). К 1×106 выделенных лифмоцитов объеме 10 мкл добавляли 50 мкл разведенного конъюгата антитела CD3 с квантовыми точками, инкубировали 30 мин, отмывали центрифугированием и регистрировали флуоресценцию клеток.
Подготовка культуры клеток лейкоцитов крови человека с концентрацией 1×106.
3. Параметры испытания:
Флуоресценцию клеток регистрировали на проточном цитофлуориметре CytoFLEX S Beckman-Couter.
Возбуждающий свет 488 нм.
Температура проведения опыта 25±2°С.
4. Результаты испытания: при окрашивании лимфоцитов с помощью конъюгата антитела CD3 с квантовыми точками получены следующие гистограммы флуоресценции представленные на фигуре 23.
1. В канале регистрации 690/50 нм процент флуоресцирующих клеток в опыте составлял 70%, что соответствовало доле окрашенных лимфоцитов в положительном контроле при окрашивании клеток конъюгатом CD3-FITC (70%).
2. В канале регистрации 690/50 нм интенсивность флуоресценции позитивных клеток составляла 6900 отн. ед., интенсивность флуоресценции негативных клеток составляла 550 отн. ед. в канале регистрации 525/40 нм флуоресценция отсутствовала.
3. Титр коньюгата антитела CD3 с квантовыми точками составлял не менее 1:100. Заключение: конъюгат антитела CD3 с квантовыми точками демонстрирует хорошую флуоресценцию при окрашивании лимфоцитов человека. Полученный конъюгат может использоваться для определения доли Т-лимфоцитов человека при многоцветном окрашивании. Квантовые точки потенциально могут использоваться для конъюгации с другими антителами и применяться для окрашивания клеток in vitro или in vivo.
Иммуноцитохимическое исследование фрагмента человеческого антитела acMet-Fab, конъюгированного с КТ CdTeSeS/CdZnS-PEGPTT
Квантовые точки CdTeSeS/CdZnS-PEGPTT, конъюгированные с антителами против антигена c-Met человека тестировали в разведении 1:5 иммуноцитохимическим методом на клетках линии НТ29. Результаты представлены на фигуре 24 (увеличение 40х). Ярко окрашены мембраны клеток. Использование конъюгатов на основе заявленных КТ позволяет количественно и качественно оценить экспрессию целевого маркера.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
Список литературы, которая включена в настоящее описание изобретения в качестве ссылок:
[1] - P. Reiss, М. Protie're, L. Li / Small 2009, 5, No. 2, 154-168.
[2] - D.Kalinowska, I.Grabowska-Jadach, M.Drozd, M.Pietrzak Comparative studies of biological activity of cadmium-based quantum dots with different surface modifications Applied Nanoscience, 2018, Volume 8, pp 309-321.
[3] - S.V. Dezhurov, D.V. Krylsky, A.V. Rybakova, S.A. Ibragimova, P.P. Gladyshev, A.A. Vasiliev, O.S. Morenkov. One-pot synthesis of polythiol ligand for highly bright and stable hydrophilic quantum dots toward bioconjugate formation Advances in Natural Sciences: Nanoscience and Nanotechnology 2017.
[4] - P. Reiss, M. Protie're, L. Li / Core/Shell Semiconductor Nanocrystals/ Small 2009, 5, No. 2, 154-168.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ создания активной среды на основе полупроводниковых люминесцентных нанокристаллов в полимерной матрице | 2018 |
|
RU2689970C1 |
| КВАНТОВЫЕ ТОЧКИ, СПОСОБЫ ПОЛУЧЕНИЯ КВАНТОВЫХ ТОЧЕК И СПОСОБЫ ИСПОЛЬЗОВАНИЯ КВАНТОВЫХ ТОЧЕК | 2009 |
|
RU2497746C2 |
| СПОСОБ КОЛЛОИДНОГО СИНТЕЗА КВАНТОВЫХ ТОЧЕК СТРУКТУРЫ ЯДРО/МНОГОСЛОЙНАЯ ОБОЛОЧКА | 2018 |
|
RU2692929C1 |
| ЛИГАНДЫ НА ОСНОВЕ ПОЛИДИМЕТИЛСИЛОКСАНА ДЛЯ КВАНТОВЫХ ТОЧЕК В КРЕМНИЙОРГАНИЧЕСКИХ МАТЕРИАЛАХ | 2013 |
|
RU2648084C2 |
| ЛЮМИНЕСЦЕНТНЫЕ ЧЕРНИЛА ДЛЯ КРИПТОЗАЩИТЫ ДОКУМЕНТОВ И ИЗДЕЛИЙ ОТ ПОДДЕЛОК, СПОСОБ ИХ НАНЕСЕНИЯ, А ТАКЖЕ СПОСОБЫ КОНТРОЛЯ ПОДЛИННОСТИ ТАКИХ ИЗДЕЛИЙ | 2011 |
|
RU2503705C2 |
| Способ оценки состояния биоклетки | 2021 |
|
RU2755401C1 |
| Способ биоимиджинга | 2023 |
|
RU2838135C1 |
| ФЛУОРЕСЦЕНТНЫЙ ГИДРОГЕЛЬ ДЛЯ ДЕТЕКЦИИ БИОЛОГИЧЕСКИХ МОЛЕКУЛ | 2023 |
|
RU2814452C1 |
| Способ синтеза функциональных углеродных квантовых точек | 2023 |
|
RU2824005C1 |
| Способ проведения микроскопического анализа клеточного образца | 2023 |
|
RU2835203C1 |











Изобретение относится к нанотехнологии, оптоэлектронике и медицинской диагностике и может быть использовано при специфической флуоресцентной молекулярно-нацеленной визуализации маркеров, диагностике заболеваний, а также при изготовлении средств для обнаружения утечек. Квантовая точка имеет кристаллическую структуру вюрцита и размер 6-8 нм. Ядро квантовой точки имеет кристаллическую структуру вюрцита, размер 2-4 нм и состав CdTeSeS; а оболочка - CdS, CdZnS, CdS/ZnS, CdS/CdZnS или CdZnS/ZnS. Количество монослоёв оболочки от 5 до 8. Квантовая точка характеризуется молярным содержанием Cd, Se и S, %: 21-29, 14-20, 52-64, соответственно, квантовым выходом 50-70% и высокой интенсивностью флуоресценции в диапазоне 630-720 нм. Флуоресцентный конъюгат для визуализации молекулярных маркеров состоит из указанной квантовой точки, покрытой полимерной оболочкой, и лиганда, обеспечивающего специфичность связывания. Полимерная оболочка выполнена из сополимера метоксиполиэтиленгликольакрилата-ко-малеинового ангидрида-ко-этиленгликольдиакрилата, терминированного 1,6-гександитиолом; сополимера метоксиполиэтиленгликольакрилата-ко-малеинового ангидрида-ко-этиленгликольдиакрилата с тиолизированным олигомером; сополимера поливинилпирролидона и акриловой кислоты. Лиганд выбран из фолиевой кислоты, антитела или его фрагмента и конъюгирован с полимерной оболочкой через линкер, представляющий собой полипропиленгликоль, полиэтиленгликоль акрилат или стрептавидин. Молекулярный маркер представляет собой вещество белковой или нуклеиновой природы, являющееся продуктом жизнедеятельности живых клеток и входящее в их состав. Указанные конъюгаты также характеризуются высокой интенсивностью флуоресценции. 2 н. и 10 з.п. ф-лы, 32 ил., 1 табл.
1. Квантовая точка, имеющая кристаллическую структуру вюрцита и характеризующаяся размером 6-8 нм, структура которой выражается общей формулой А/Б, где:
- А - ядро квантовой точки, представляющее собой полупроводниковый материал состава CdTeSeS;
- Б - оболочка квантовой точки, покрывающая ядро и представляющая собой полупроводниковый материал состава CdS, CdZnS, CdS/ZnS, CdS/CdZnS или CdZnS/ZnS; причем ядро квантовой точки имеет кристаллическую структуру вюрцита и размер 2-4 нм, количество монослоев оболочки, покрывающей ядро, составляет от 5 до 8.
2. Квантовая точка по п. 1, в которой квантовая точка имеет структуру CdTeSeS/CdS, CdTeSeS/CdZnS, CdTeSeS/CdS/CdZnS, CdTeSeS/CdZnS/ZnS, или CdTeSeS/CdS/ZnS.
3. Квантовая точка по п. 1, в которой молярное содержание Cd в квантовой точке составляет от 21 до 29%.
4. Квантовая точка по п. 1, в которой молярное содержание Se в квантовой точке составляет от 14 до 20%.
5. Квантовая точка по п. 1, в которой молярное содержание S в квантовой точке составляет от 52 до 64%.
6. Квантовая точка по п. 1, характеризующаяся квантовым выходом от 50 до 70%.
7. Флуоресцентный конъюгат для визуализации молекулярных маркеров, состоящий из фотостабильной флуоресцентной квантовой точки по п. 1, покрытой полимерной оболочкой, и лиганда, обеспечивающего специфичность связывания.
8. Флуоресцентный конъюгат по п. 7, характеризующийся тем, что в качестве полимерной оболочки используют сополимер метоксиполиэтиленгликольакрилата-ко-малеинового
ангидрида-ко-этиленгликольдиакрилата, терминированный 1,6-гександитиолом; сополимер метоксиполиэтиленгликольакрилата-ко-малеинового ангидрида-ко-этиленгликольдиакрилата с тиолизированным олигомером; сополимер поливинилпирролидона и акриловой кислоты.
9. Флуоресцентный конъюгат по п. 7, характеризующийся тем, что лиганд представляет собой фолиевую кислоту, антитело или его фрагмент.
10. Флуоресцентный конъюгат по п. 7, характеризующийся тем, что лиганд конъюгирован с полимерной оболочкой через линкер.
11. Флуоресцентный конъюгат по п. 10, характеризующийся тем, что линкер представляет собой полипропиленгликоль, полиэтиленгликоль акрилат, стрептавидин или стрептавидин с His-tag.
12. Флуоресцентный конъюгат по п. 7, характеризующийся тем, что молекулярный маркер представляет собой вещество белковой или нуклеиновой природы, являющееся продуктом жизнедеятельности живых клеток и входящее в их состав.
| CN 104974742 A, 14.10.2015 | |||
| ЗДОБНОВА Т.А | |||
| Комплексы полупроводниковых монокристаллов и рекомбинантных антител для флуоресцентной визуализации опухолевых клеток, Автореферат диссертации на соискание учёной степени кандидата биологических наук, Москва, 2011, с.с | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| СПОСОБ СИНТЕЗА ПОЛУПРОВОДНИКОВЫХ КВАНТОВЫХ ТОЧЕК | 2008 |
|
RU2381304C1 |
| КВАНТОВЫЕ ТОЧКИ, СПОСОБЫ ПОЛУЧЕНИЯ КВАНТОВЫХ ТОЧЕК И СПОСОБЫ ИСПОЛЬЗОВАНИЯ КВАНТОВЫХ ТОЧЕК | 2009 |
|
RU2497746C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛУПРОВОДНИКОВЫХ КОЛЛОИДНЫХ КВАНТОВЫХ ТОЧЕК СУЛЬФИДА КАДМИЯ | 2013 |
|
RU2540385C2 |
Авторы
Даты
2022-08-08—Публикация
2021-08-27—Подача