Изобретение относится к медицине, а именно к хирургии, и может быть использовано для подготовки острой гнойной и ожоговой раны к аутодермопластике.
Терапия раневого ложа, создающая местные условия для гарантированного и полного приживление кожных трансплантатов в условиях острого гнойного воспаления после механического иссечения некротических тканей остается одной из фундаментальных проблем восстановительной хирургии. Несмотря на весь комплекс лечебно-профилактических мер направленных на профилактику осложненного течения раневого, риск возникновения такого грозного и витального осложнения, как лизис кожных трансплантатов после аутопластического закрытия раны достаточно велик, и по данным разных авторов составляет от 10% до 30% [1],[2].
Своей значимости для местной подготовки раневого ложа к пластическому закрытию не утратили антисептики, кислотосодержащие препараты и методы лечения, основанные на различных физических принципах[4].
Известны различные способы подготовки ран к аутодермопластике путем обработки различными антисептиками, таких как раствор фурациллина, хлоргексидина [3] в этом случае процент приживления кожных трансплантатов в среднем составляет 61%. [3]. При применении протеолитических ферментов: трипсин, хемотрипсин, хансурид, террилитин, так же отмечается осложненное приживление кожных трансплантатов, полное приживление отмечается в – 6,2%, частичное – 12,4%, отторжение в – 11,4% [4].
К причинам, препятствующим достижению указанного ниже технического результата, является то, что в результате стандартного подхода к использованию в течении нескольких десятилетий антисептиков, антибиотиков и химио препаратов бактериальная микрофлора ран выработала механизмы резистентности в виде микробных биопленок [5].
Известен способ подготовки ожоговых ран к аутодермопластике с применением 40% салициловой кислоты и последующей некрэктомией [6].
К причинам, препятствующим достижению указанного ниже технического результата при использовании известного способа относится то, что в результате его реализации удаление некротических элементов характеризуется неселективностью и нерадикальностью, что определяет потребность в последующей длительной (в течение 7-10 дней) дополнительной подготовке раневой поверхности к аппликации аутотрансплантатов.
Известен способ трофического лечения ожоговых ран с применением биодеградируемых пленок, содержащих полимеры из смесей молочной кислоты (Poly-lacticAcid (PLA) создающие влажную раневую среду [7].
К причинам, препятствующим достижению указанного ниже технического результата при использовании известного способа относится то, что лечение ожоговых ран во влажной раневой среде с помощью пленок имеет ограничения по площади их применения, их нельзя использовать на площади более 10% поверхности тела, а так же, при наличии в ране воспаления [8].
Задачей изобретения является создание способа подготовки глубокой ожоговой раны к аутодермопластике, обеспечивающего получение технического результата, состоящего в уменьшении болевого синдрома, усилении антиоксидантной защиты в условиях течения острой гнойно-некротической воспалительной реакции, подготовки в короткие сроки ожоговой раны к аутодермопластике, улучшении приживления кожных трансплантатов.
Указанный технический результат достигается тем, что способ подготовки глубокой ожоговой раны к аутодермопластике заключается в том, что осуществляют тангенциальную некрэктомию в пределах жизнеспособных тканей, иссеченные участки ожоговой раны промывают антисептическим раствором и тщательно осушают марлевыми салфетками, затем на рану наносят равномерным тонким слоем кислотосодержащую смесь порошков, состоящую из порошков 3%-й молочной кислоты, Статина и 3%-й борной кислоты, смешанных в равных долях, после этого ожоговую рану закрывают стерильными марлевыми салфетками и фиксируют марлевым бинтом, дальнейшие перевязки осуществляют с кратностью один раз в двое суток до полной готовности раневой поверхности к аутодермопластике.
Изобретение поясняется подробным описанием, клиническими примерами и иллюстрациями, на которых изображено:
На фиг. 1 – рана при поступлении (в клиническом примере 1),
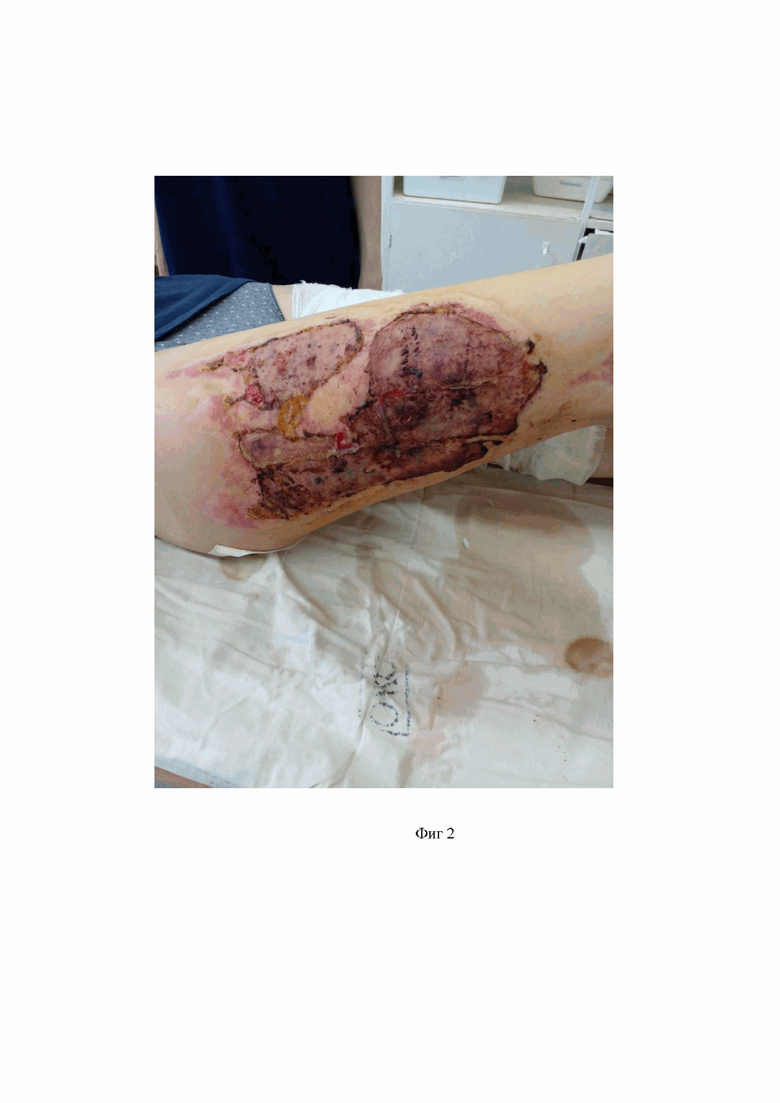
На фиг.2 – рана на седьмые сутки после аутодермопластики (в клиническом примере 1).
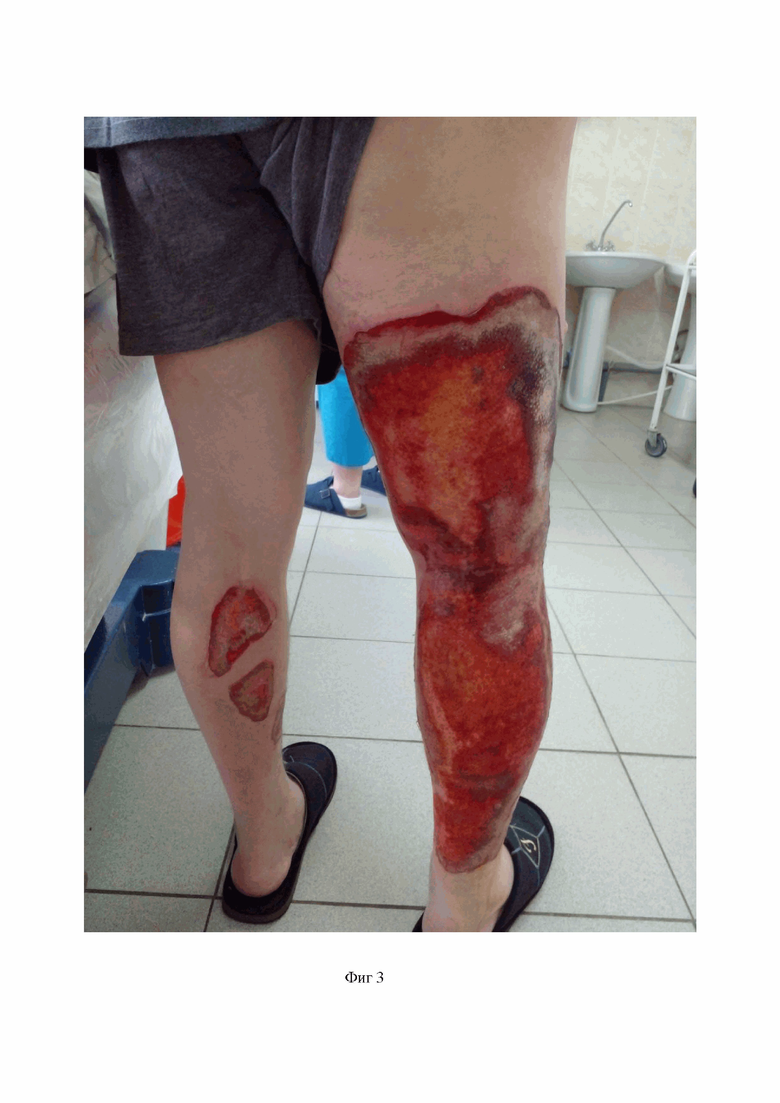
На фиг.3 – рана при поступлении (в клиническом примере 2),
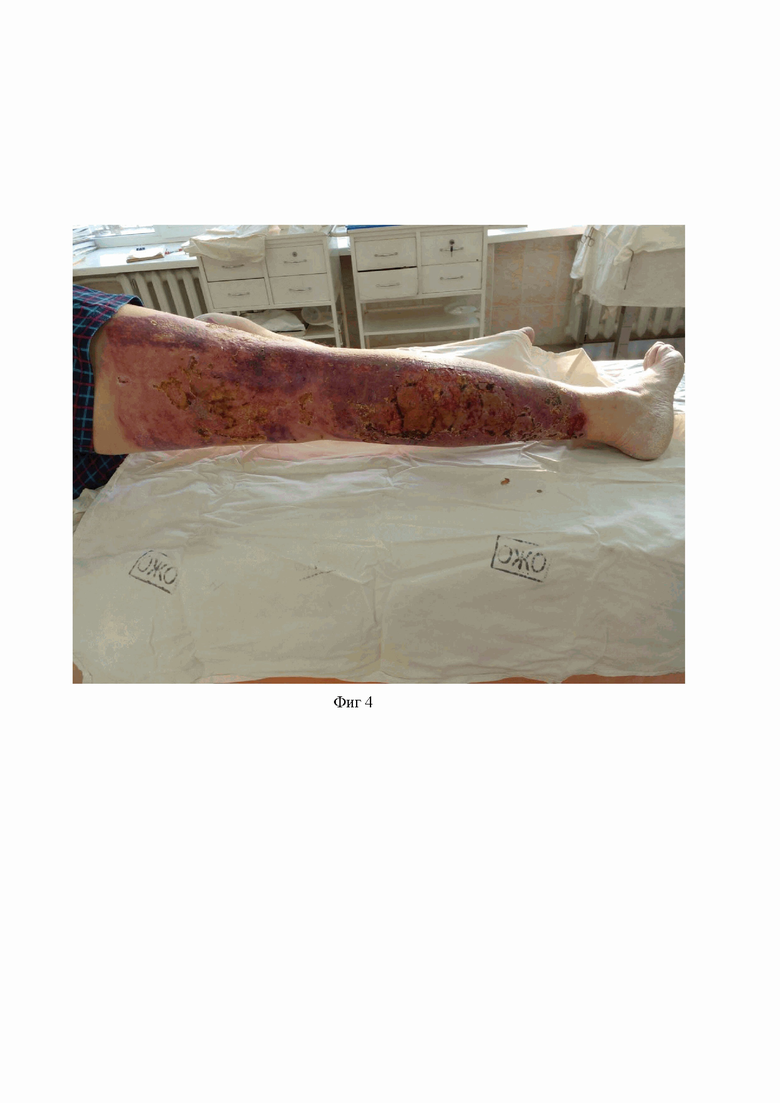
На фиг. 4 – рана после аутодермопластики (в клиническом примере 2).
Способ осуществляют следующим образом.
Для подготовки ожоговых ран к аутодермопластике на участках глубокого дермального и тотально глубокого кожного поражения (струп) под общим обезболиванием осуществляют тангенциальную некрэктомию в пределах жизнеспособных тканей. Иссеченные участки ожоговой раны промывают антисептическим раствором. Затем марлевыми салфетками ожоговая рана тщательно осушается. После иссечения некротических тканей на ожоговую рану наносят кислотосодержащую смесь порошков, состоящую из порошков 3%-й молочной кислоты, Статина и 3%-й борной кислоты, смешанных в равных долях. Кислотосодержащую смесь порошков наносят на ожоговую рану равномерным тонким слоем, закрывают ее стерильными марлевыми салфетками и фиксируют марлевым бинтом.
В послеоперационном периоде перевязки продолжают осуществлять с использованием заявленной смеси кислотосодержащих порошков с кратностью один раз в двое суток до полной готовности раневой поверхности к аутодермопластике. Раневой экссудат удаляется марлевым салфетками, рана осушается, смесь кислотосодержащих порошков тонким слоем наносится на гранулирующую рану, рана закрывается стерильными марлевыми салфетками и фиксируется марлевым бинтом.
Совместное применение порошков двух кислотосодержащих препаратов – молочной и борной кислоты, позволяет улучшить трофику и антимикробную защиту ожоговых тканей. Молочная кислота содержит клеточные метаболиты, а борная кислота обладает антисептическим и противовоспалительным действием. Лечебное действие борной кислоты в качестве составляющей порошковой смеси определялось тем, что она не только обладает широким спектром антибактериального действия, но и способствует расплавлению некротизированных. тканей. Поступление клеточных метаболитов в виде полимеров молочной кислоты помимо улучшения трофического статуса раны так же способствует повышению
антиоксидантной активности – ингибированию реакции перекисного окисления липидов и восстановлению антиоксидантного потенциала, необходимого для благоприятного и менее осложненного течения воспалительной реакции. Порошок Статин обеспечивает хороший водо- и газообмен в ожоговой ране, безболезненность перевязок и обеспечивает хороший косметический эффект, не оставляет рубцов.
В качестве перевязочного материала, фиксирующего кислотосодержащую смесь порошков на ожоговой ране, выступает хлопковая марля, обладающая достаточной адгезивной способностью механического удаления оставшихся в ране элементов некротических тканей, клеточного детрита и продуктов воспаления.
Клинический пример 1.
Пациентка Б., 35 лет, поступила в отделение 09.03.2023 г. Диагноз: Термический ожог 2-3 степени правой нижней конечности, S – 5% поверхности тела (фиг.1). Сопутствующие заболевания: Эпилепсия. Жалобы при поступлении в отделение: на ожоговую рану правого бедра, умеренной интенсивности боли в ожоговой ране. Госпитализация в отделение по направлению скорой медицинской помощи.
Проведенное оперативное лечение:
10.03.2023 г. – выполнена тангенциальная некрэктомия.
В послеоперационном периоде подготовки к кожной пластике проводились перевязки один раз в двое суток с вышеуказанной кислотосодержащей смесью порошков. Перевязки безболезненные, местное применение молочной кислоты и Статина обладает обезболивающим эффектом. Воспаление в ране серозного характера, отмечался быстрый рост грануляционной ткани. Грануляции чистые, розовые. На девятые сутки после иссечения некроза выполнено пластическое закрытие раневого дефекта.
20.03.2023 г. – выполнена свободная аутодермопластика расщепленными кожными трансплантатами. В послеоперационном периоде полное приживление кожных трансплантатов.
Обезболивающая и антибактериальная терапия не назначались в процессе подготовки раны к кожной пластике. На 17-ые сутки пациент был выписан из отделения с полным закрытием раны на амбулаторное долечивание, приживление кожных трансплантатов в полном объеме.
Клинический пример 2.
Пациент С., 65 лет, поступил в отделение 08.11.2022 г.
Диагноз: Термический ожог 2-3 степени правой кисти, обеих нижних конечностей S – 11% поверхности тела (фиг. 3). Сопутствующие заболевания: Гипертоническая болезнь. Фибриляция предсердий. Хронический простатит. Аденома предстательной железы. Сахарный диабет 2 типа впервые выявленный. Целевой уровень HB Alc< 7/5%. Госпитализация в отделение по направлению скорой медицинской помощи.
Оперативное лечение:
09.11.2022 г. Тангенциальная электродерматомная некрэктомия
11.11.2022 г. Тангенциальная электродерматомная некрэктомия.
В послеоперационном периоде подготовки к пластике, такие остро воспалительные явления, как чрезмерная обильная серозная экссудации, или “отрицательный эффект лимфляважа” купировались на 3-и сутки после операции, отмечался по клинической картине раны переход от дегенеративной к регенеративной фазе воспаления. Частота перевязок один раз в двое суток с вышеуказанной кислотосодержащей смесью порошков. Перевязки безболезненные, местное применение молочной кислоты и Cтатина обладает обезболивающим эффектом. Воспаление в ране серозного характера, отмечался быстрый рост грануляционной ткани. Грануляции чистые, розовые с отсутствием гнойного отделяемого и оживлением краевой эпителизации (фиг 4). В ране отсутствовали явления экссудативного воспаления с обильной серозной экссудацией и гнойного отделяемого. Отсутствие перифокального воспаления, быстрый рост грануляционной ткани. Стихание процессов экссудации, рост грануляций, эпителизация.
22.11.2022 г. Свободная аутодермопластика расщепленными кожными трансплантатами. В послеоперационном периоде полное приживление кожных трансплантатов. На 21-е сутки пациент был выписан из отделения с полным закрытием раны на амбулаторное долечивание, приживление кожных трансплантатов в полном объеме.
Таким образом, заявляемый способ позволяет улучшить метаболизм в тканях и усилить антиоксидантную защиту в условиях течения острой гнойно-некротической воспалительной реакции, обеспечить в короткие сроки подготовку ожоговой раны к аутодермопластике за счет быстрого роста грануляционных тканей с полным приживлением кожных аутотрансплантатов.
Литература
1. Малютина Н.Б. Рациональное применение методов раннего хирургического лечения глубоких ожогов у пациентов старших возрастных групп // Комбустиология [Электронный ресурс].-2002.-№10.- режим доступа http//.www.burn.ru.
2. Худяков В.В., Крутиков М.Г. Сравнительная оценка эффективности различных методов подготовки ожоговых ран к аутодермопластике // Комбустиология [Электронный ресурс].-2003.-№16 -17.- режим доступа http//.www.burn.ru.
3. Сафин И. А., Нартайлаков и др.//Местное лечение ран/ Материалы Всесоюзной конференции. – Москва. - 1991, - с.177-178)
4. Кузин М.И., Аничков М.Н., Золотаревский В.Я. Патогенез и лечение длительно незаживающих язв при заболеваниях сосудов конечностей // Хирургия - 1979, 3, - с. 24-31
5. Артюх Т.В., Соколова Т.Н., Островская О.Б.
Особенности резистентности клинических изолятов E.Coli и С.Аlbicans, образующих биопленку
https://cyberleninka.ru/article/n/osobennosti-rezistentnosti-klinicheskih-izolyatov-e-coli-i-c-albicans-obrazuyuschih-bioplenku/viewer
6. Б.С. Вихриев, В.М. Бурмистров // Ожоги (Руководство для врачей), 2-е изд. // Л., Медицина, 1986 - 272 с.
7. Role of Suprathel in dermal burns in children T Iqbal, U Ali, Z Iqbal , ZJ Fatima , M Rehan…-Emerg.Med, 2018 Iotusmdc.con
https://www.lotusmdc.com/katalog/UVCY/Eng-12-Suprathelin-cocuklarda-Gorulen-Derin-Dermal-Yaniklarda-Kullanimi.pdf
8.Клинические рекомендации. Ожоги термические и химические. Ожоги
солнечные. Ожоги дыхательных путей.
https://cr.minzdrav.gov.ru/schema/687_1
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОДГОТОВКИ ДЕФЕКТА КОЖНОГО ПОКРОВА К АУТОДЕРМОПЛАСТИКЕ | 2000 |
|
RU2192266C2 |
| СПОСОБ ЛЕЧЕНИЯ РАН МЯГКИХ ТКАНЕЙ РАЗЛИЧНОЙ ЭТИОЛОГИИ | 2013 |
|
RU2528905C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЛИТЕЛЬНО НЕЗАЖИВАЮЩИХ РАН У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ | 2008 |
|
RU2358757C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ТОТАЛЬНЫХ ГЛУБОКИХ ОЖОГОВ ТУЛОВИЩА | 2019 |
|
RU2701625C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГОТОВНОСТИ ОЖОГОВЫХ РАН К АУТОДЕРМОПЛАСТИКЕ | 2024 |
|
RU2841131C1 |
| Способ хирургического лечения ожоговой раны | 2019 |
|
RU2721870C1 |
| СПОСОБ КОЖНОЙ АУТОПЛАСТИКИ | 2006 |
|
RU2301636C1 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВЫХ РАН | 2005 |
|
RU2286184C2 |
| Способ оценки готовности реципиентной раны к свободной кожной пластике аутодермотрансплантатом | 2020 |
|
RU2755490C1 |
| СПОСОБ НАЛОЖЕНИЯ ВАКУУМНОЙ ПОВЯЗКИ | 2019 |
|
RU2720831C1 |

Изобретение относится к медицине, а именно к хирургии. Для подготовки глубокой ожоговой раны к аутодермопластике осуществляют тангенциальную некрэктомию в пределах жизнеспособных тканей. Раневой экссудат удаляют марлевыми салфетками. На рану наносят кислотосодержащую смесь порошков, состоящую из порошков молочной кислоты, Статина и борной кислоты, смешанных в равных долях. Ожоговую рану закрывают стерильными марлевыми салфетками, фиксируют марлевым бинтом. Перевязки осуществляют с кратностью один раз в двое суток до появления грануляций раневой поверхности. Способ позволяет уменьшить болевой синдром, усилить антиоксидантную защиту в условиях течения острой гнойно-некротической воспалительной реакции, подготовить в короткие сроки ожоговую рану к аутодермопластике, улучшить приживление кожных трансплантатов. 4 ил., 2 пр.
Способ подготовки глубокой ожоговой раны к аутодермопластике, характеризующийся тем, что осуществляют тангенциальную некрэктомию в пределах жизнеспособных тканей, раневой экссудат удаляют марлевыми салфетками, затем на рану наносят кислотосодержащую смесь порошков, состоящую из порошков молочной кислоты, Статина и борной кислоты, смешанных в равных долях, после этого ожоговую рану закрывают стерильными марлевыми салфетками и фиксируют марлевым бинтом, дальнейшие перевязки осуществляют с кратностью один раз в двое суток до появления грануляций раневой поверхности.
| RU 2009107473 A 10.09.2010 | |||
| CN102125623 A 20.07.2011 | |||
| А.Д | |||
| Фаязов и др | |||
| / Современные методы местного лечения ожоговых ран // Вестник экстренной медицины | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Nour S | |||
| et.al | |||
| / Acetic acid dressings used to treat pseudomonas colonised burn wounds: A UK national survey | |||
| Burns | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
Авторы
Даты
2024-08-26—Публикация
2023-12-20—Подача