Область техники
Настоящее изобретение относится к фармацевтической композиции, подходящей для внутривлагалищной доставки, а также к фармацевтической композиции для применения в лечении инфекционных заболеваний женской репродуктивной системы. Более конкретно, изобретение относится к фармацевтической композиции, содержащей фентиконазол совместно с антибактериальным агентом, необязательно одним или более обезболивающими или местными анестетиками и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом.
Уровень техники
Воспаление влагалища, или вагинит, вызвано разными внешними и внутренними факторами, которые изменяют микробиоту влагалища. Наиболее распространенными причинами инфекционного вагинита являются бактериальный вагиноз (БВ), вульвовагинальный кандидоз (ВВК) и трихомональный вагинит (ТВ), которые составляют примерно 90% случаев среди женщин репродуктивного возраста, посещающих клиники первого уровня. Значительное число случаев инфекционного вагинита встречается у женщин всех возрастов, как сексуально активных, так и неактивных, таким образом, многие женщины страдали от влагалищной инфекции по меньшей мере один раз в жизни.
Здоровый влагалищный тракт женщин репродуктивного возраста колонизирован нормальной микробиотой, сформированной из лактобацилл, которая защищает от патогенных штаммов бактерий, если присутствует в достаточном количестве. Наиболее распространенными причинами инфекционного вагинита являются внутренние факторы, такие как изменение микросреды влагалища и рН, и внешние факторы, такие как незащищенные половые контакты, употребление табака, спринцевание, недостаточность иммунной системы, диабет и лучевая терапия.
Указанные факторы создают дисбаланс в экосистеме влагалища и обеспечивают быстрый рост патогенных микроорганизмов, что может приводить к снижению способности нормальной микробиоты влагалища подавлять рост аэробных и анаэробных бактерий, которые вызывают повышенные влагалищные выделения, неприятный запах, воспаление и раздражение, т.е. все распространенные симптомы бактериального вагиноза.
Вульвовагинальный кандидоз вызван избыточным ростом дрожжей, главным образом, Candida albicans, которые являются ключевым компонентом влагалищной флоры. Симптомы вульвовагинального кандидоза включают влагалищные выделения, зуд, боль и отек. Несмотря на то, что Candida albicans является наиболее распространенной причиной вульвовагинального кандидоза, другие штаммы Candida, отличные от albicans, такие как Candida glabrata, Candida parapsiiosis, Candida krusei, Candida cerevisiae, Candida tropicalis, Candida lusitaniae и Trichosporon sp, все чаще идентифицируют в качестве причины вульвовагинального кандидоза.
Бактериальные и кандидозные инфекции могут сосуществовать. Смешанная бактериальная и кандидозная инфекция встречается примерно в каждом пятом случае вагинита.
Trichomonas vaginalis представляет собой жгутиковое простейшее, являющееся паразитом, который вызывает трихомониаз, характеризующийся обильными желто-зелеными выделениями и раздражением влагалища или наружных половых органов.
В данной области техники хорошо известно, что способы лечения вагинальной инфекции включают лечение противогрибковыми средствами и/или антибиотиками совместно с производными азола. Стандартные и комбинированные способы терапии (как местные, так и системные) для лечения указанных выше состояний надежно установлены.
Например, рекомендуемые режимы лечения бактериального вагиноза включают:
- Метронидазол 400-500 мг перорально два раза в день в течение 5-7 дней или 2 г перорально в одной дозе, или
- Внутривлагалищный гель метронидазола (0,75%) один раз в день в течение пяти дней, или
- Внутривлагалищный крем клиндамицина (2%) один раз в день в течение семи дней или 300 мг перорально два раза в день в течение семи дней, или
- Тинидазол 2 г перорально в одной дозе или 1 г перорально в течение пяти дней.
Рекомендуемые режимы лечения вагинального кандидоза включают:
- Флуконазол перорально 150 мг в одной дозе, или
- Итраконазол перорально 200 мг два раза в день в течение одного дня, или
- Вагинальная таблетка клотримазола 500 мг в одной дозе или 200 мг один раз в день в течение трех дней, или
- Вагинальные суппозитории миконазола 1200 мг в одной дозе или 400 мг один раз в день в течение трех дней, или
- Вагинальный пессарий эконазола 150 мг в одной дозе.
Рекомендуемые режимы терапии первой линии для лечения Trichomonas vaginalis включают:
- Метронидазол 400-500 мг перорально два раза в день в течение 5-7 дней, или
- Метронидазол 2 г перорально в одной дозе, или
- Тинидазол 2 г перорально в одной дозе.
Кроме того, растущее число случаев смешанных влагалищных инфекций представляет собой терапевтическую проблему, так как указанные инфекции требуют лечения несколькими лекарственными средствами.
В заявке на Европейский патент ЕР 1712229 А1 описаны пероральные композиции, содержащие флуконазол, тинидазол или секнидазол, для лечения влагалищных инфекций, вызванных микроорганизмами типа Gardnerella vaginalis, Actinomyces, Candida и Trichomonas vaginalis, присутствующими при вагините и бактериальном вагинозе.
В международной заявке WO 2010026469 А1 описана фармацевтическая композиция, содержащая комбинацию флуконазола, тинидазола и клиндамицина и/или их фармацевтически приемлемых солей, для лечения инфекций, передаваемых половым путем.
В заявке ЕР 910377 А1 описаны фармацевтические композиции для местного введения для лечения вагинита, содержащие комбинацию метронидазола и миконазола и один или более местных анестетиков, таких как лидокаин или бензокаин.
В заявке WO 2005087270 А1 описана фармацевтическая композиция для местного введения, содержащая терконазол и тинидазол и/или тиоконазол.
Тем не менее, пероральные способы противогрибковой терапии благоприятствуют тому, что устойчивые к лекарственным препаратам штаммы, отличные от albicans, активно растут и распространяются во влагалище, так как значительное количество лекарственного средства остается в желудочно-кишечном тракте, сокращая число С. albicans и обеспечивая рост менее восприимчивых штаммов, отличных от albicans. Кроме того, указанные выше способы терапии могут приводить к осложнениям, связанным с появлением устойчивых к лекарственным средствам дрожжей с переменной и даже полной устойчивостью к традиционно назначаемым противогрибковым лекарственным средствам, таким как флуконазол, тиоконазол, клотримазол и миконазол.
Таким образом, в данной области техники существует потребность в альтернативных фармацевтических композициях, подходящих для внутривлагалищной доставки, а также в способах лечения, которые успешно и эффективно лечат инфекции влагалища с применением фармацевтических композиций.
Краткое описание изобретения
Настоящее изобретение было реализовано с учетом известного уровня техники, описанного выше, и задачей настоящего изобретения, согласно первому аспекту, является обеспечение новой фармацевтической композиции, подходящей для внутривлагалищной доставки, содержащей фентиконазол или его фармацевтически приемлемую соль совместно с антибактериальным агентом или его фармацевтически приемлемой солью, необязательно с одним или более обезболивающими или местными анестетиками и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом.
В одном из вариантов реализации фармацевтическая композиция содержит фармацевтически эффективное количество фентиконазола в комбинации с фармацевтически эффективным количеством антибактериального агента и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом.
В другом варианте реализации фармацевтическая композиция содержит фармацевтически эффективное количество фентиконазола в комбинации с фармацевтически эффективным количеством антибактериального агента, фармацевтически эффективным количеством обезболивающего или местного анестетика и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом.
В предпочтительном варианте реализации фентиконазол присутствует в виде фентиконазола нитрата.
В предпочтительном варианте реализации антибактериальный агент представляет собой тинидазол.
В предпочтительном варианте реализации обезболивающее или местный анестетик представляет собой лидокаин или его фармацевтически приемлемую соль.
Согласно другому аспекту настоящего изобретения предложен способ получения лекарственной формы, подходящей для внутривлагалищного введения, включающий стадии смешения фентиконазола или его фармацевтически приемлемой соли в комбинации с антибактериальным агентом и необязательно с обезболивающим или местным анестетиком и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом и последующей обработки смеси для получения лекарственной формы.
Другой аспект изобретения представляет собой фармацевтическую композицию, содержащую комбинацию согласно первому аспекту, для применения в качестве лекарственного препарата для лечения инфекционных заболеваний или состояний женской репродуктивной системы, таких как вульвовагинальные инфекции.
Подробное описание изобретения
Все термины, используемые в настоящей заявке, если не утверждается иное, следует толковать в обычном значении, известном в данной области техники. Другие более конкретные определения для определенных терминов, используемых в настоящей заявке, представлены ниже и предназначены для единообразного применения в настоящем описании и формуле изобретения, если только представленное в явном виде определение не предлагает более широкое определение.
В описании и формуле изобретения слово «содержать» и формы данного слова не предназначены для исключения других технических признаков, добавок, компонентов или стадий.
Кроме того, слово «содержать» включает случай «состоять из». Дополнительные задачи, преимущества и признаки изобретения станут понятными специалистам в данной области техники после рассмотрения описания или могут быть изучены при реализации изобретения. Последующие примеры и графические материалы приведены в качестве иллюстрации и не предназначены для ограничения настоящего изобретения. Кроме того, настоящее изобретение охватывает все возможные комбинации конкретных и предпочтительных вариантов реализации, описанных в настоящем документе.
Настоящее изобретение относится к ассоциату или комбинации фентиконазола и антибактериального агента и необязательно обезболивающего или местного анестетика для применения в лечении инфекционных заболеваний и состояний женской репродуктивной системы.
Фентиконазол представляет собой производное имидазола, проявляющее широкий спектр противогрибковой активности. Он также обладает антибактериальной активностью, и спектр его действия охватывает грамположительные бактерии (Staphylococcus aureus, Staphylococcus epidermis, Streptococcus spp.) и противопаразитарное действие в отношении Triconomonas vaginalis и некоторых штаммов бактерий, таких как Gardnerella vaginalis.
Фентиконазол хорошо всасывается через стенку влагалища и удерживается в наружном слое эпидермиса (роговом слое) в течение продолжительного времени. Это обеспечивает его накопление в слизистой ткани вплоть до 72 часов, что, таким образом, позволяет поддерживать его активность в течение продолжительного периода времени и отсрочивает последующую процедуру введения. Кроме того, фентиконазол плохо всасывается на системном уровне.
Согласно одному из аспектов в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая фентиконазол или его фармацевтически приемлемую соль в качестве противогрибкового агента в комбинации с антибактериальным агентом и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом. В предпочтительном варианте реализации фентиконазол присутствует в виде фентиконазола нитрата.
В качестве иллюстрации, фентиконазол или его фармацевтически приемлемая соль может быть включен в композицию согласно изобретению в количестве от примерно 0,5% до примерно 70%, например, от примерно 5% до примерно 60% или от примерно 10% до примерно 55%, или примерно от 15% до 50% по массе. В предпочтительном варианте реализации фентиконазол присутствует в композиции согласно изобретению в количестве примерно от 20 до 50% по массе, более предпочтительно примерно от 25% до 48% по массе.
В предпочтительном варианте реализации количество фентиконазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению предпочтительно составляет от примерно 50 мг до примерно 2000 мг, более предпочтительно от примерно 100 мг до примерно 1500 мг и еще более предпочтительно от примерно 200 мг до примерно 1000 мг. В более предпочтительном варианте реализации количество фентиконазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению составляет 600 мг.
Антибактериальный агент может включать любой антибактериальный агент, известный в данной области и подходящий для лечения бактериальных инфекций вульвовагинальной системы. Иллюстративные примеры антибактериальных средств, которые могут быть подходящими, включают без ограничения акрифлавин, ампициллин, цефтриаксон, хлорамфеникол, хлорхинальдол, кетоконазол, клиндамицин, йодохинол, метронидазол, ниморазол, орнидазол, пивампициллин, секнидазол, спирамицин, тетрациклин, тинидазол, деквалиния хлорид и их фармацевтически приемлемые соли и сложные эфиры, их комбинации и т.д.
В предпочтительном варианте реализации антибактериальный агент выбран из клиндамицина, метронидазола, кетоконазола и тинидазола. В наиболее предпочтительном варианте реализации антибактериальный агент представляет собой тинидазол.
Как правило, антибактериальный агент может быть включен в композицию согласно изобретению в количестве от примерно 0,5% до примерно 70%, например, от примерно 5% до примерно 60% или от примерно 10% до примерно 55%, или примерно от 15% до 50% по массе. В предпочтительном варианте реализации фентиконазол присутствует в композиции согласно изобретению в количестве примерно от 20 до 50% по массе, более предпочтительно примерно от 25% до 48% по массе.
Следует понимать, что количество антибактериального агента или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению будет зависеть от активности конкретного применяемого антибактериального агента и используемого типа лекарственной формы внутривлагалищной композиции. Как правило, количество антибактериального агента в фармацевтических композициях согласно изобретению предпочтительно составляет от примерно 10 мг до примерно 10000 мг, более предпочтительно от примерно 100 мг до примерно 5000 мг, еще более предпочтительно от примерно 500 мг до примерно 3000 мг и еще более предпочтительно от примерно 1000 мг до примерно 2000 мг.
В одном из вариантов реализации изобретения антибактериальный агент, применяемый в фармацевтических композициях согласно изобретению, представляет собой тинидазол или его фармацевтически приемлемую соль. Как правило, количество тинидазола или его соли в фармацевтических композициях согласно изобретению составляет от примерно 200 мг до 5000 мг, более предпочтительно от 500 мг до 3000 мг. В более предпочтительном варианте реализации количество тинидазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению составляет от примерно 1000 мг до примерно 2000 мг.
В другом варианте реализации изобретения антибактериальный агент, применяемый в фармацевтических композициях согласно изобретению, представляет собой метронидазол или его фармацевтически приемлемую соль. Как правило, количество метронидазола или его соли в фармацевтических композициях согласно изобретению составляет от примерно 10 мг до 800 мг, более предпочтительно от 200 мг до 600 мг. В более предпочтительном варианте реализации количество метронидазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению составляет от примерно 300 мг до примерно 600 мг, предпочтительно примерно 500 мг.
В другом варианте реализации изобретения антибактериальный агент, применяемый в фармацевтических композициях согласно изобретению, представляет собой кетоконазол или его фармацевтически приемлемую соль. Как правило, количество кетоконазола или его соли в фармацевтических композициях согласно изобретению составляет от примерно 200 мг до 2000 мг, более предпочтительно от 500 мг до 1000 мг. В более предпочтительном варианте реализации количество кетоконазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению составляет от примерно 600 мг до примерно 900 мг, предпочтительно примерно 800 мг. В еще одном варианте реализации изобретения антибактериальный агент, применяемый в фармацевтических композициях согласно изобретению, представляет собой клиндамицин или его фармацевтически приемлемую соль. Как правило, количество клиндамицина или его соли в фармацевтических композициях согласно изобретению составляет от примерно 50 мг до 200 мг, более предпочтительно от 750 мг до 150 мг. В более предпочтительном варианте реализации количество клиндамицина или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению составляет от примерно 90 мг до примерно 120 мг, предпочтительно примерно 100 мг.
В предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая от 200 мг до примерно 1000 мг фентиконазола или его фармацевтически приемлемой соли в качестве противогрибкового агента в комбинации с 500 мг - 3000 мг тинидазола или его фармацевтически приемлемой соли в качестве антибактериального агента и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом. В более предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая 600 мг фентиконазола или его фармацевтически приемлемой соли в качестве противогрибкового агента в комбинации с примерно 1000 мг - 2000 мг тинидазола или его фармацевтически приемлемой соли в качестве антибактериального агента и фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом.
В одном из вариантов реализации отношение количества фентиконазола или его фармацевтически приемлемой соли к количеству антибактериального агента составляет в диапазоне от примерно 10:1 до примерно 1:10 по массе. В другом варианте реализации отношение количества фентиконазола или его фармацевтически приемлемой соли к количеству антибактериального агента составляет в диапазоне от примерно 7:1 до примерно 1:7, предпочтительно от 4:1 до 1:4.
Согласно дополнительному аспекту изобретения фармацевтическая композиция согласно изобретению может дополнительно содержать одно(один) или более обезболивающих или местных анестетиков.
Неограничивающие примеры обезболивающих включают буторфанол, кодеин, дигидрокодеин, фентанил, гидрокодон, леворфанол, меперидин, метадон, морфин, налоксон, оксикодон, оксиморфон, пентазоцины, пропоксифен, их фармацевтически приемлемые соли и сложные эфиры и их комбинации.
Неограничивающие примеры местных анестетиков включают бензокаин, бупивакаин, бутамбен, хлорпрокаин, лидокаин, мепивакаин, прамоксин, прилокаин, прокаин, пропаракаин, ропивакаин, тетракаин, их фармацевтически приемлемые соли и сложные эфиры и их комбинации.
В предпочтительном варианте реализации местный анестетик представляет собой лидокаин или его фармацевтически приемлемую соль.
В предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая фентиконазол или его соль в качестве противогрибкового агента, одно из тинидазола, метронидазола, кетоконазола, клиндамицина или их солей в качестве антибактериального агента, лидокаин или его соль в качестве обезболивающего или местного анестетика и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
В качестве иллюстрации, обезболивающее или местный анестетик может быть включено(-ен) в композицию согласно изобретению в количестве от примерно 0,1% до примерно 20%, например, от примерно 0,5% до примерно 5% или от примерно 1% до примерно 3% по массе. Композиции согласно изобретению, например, могут содержать от примерно 0,1% до 3,5%, предпочтительно примерно 2% по массе лидокаина и от примерно 0,1% до 3,0%, предпочтительно примерно 1,5% по массе лидокаина.
Как правило, количество лидокаина или его соли в фармацевтических композициях составляет от примерно 1 мг до 500 мг, более предпочтительно от 10 мг до 400 мг. В более предпочтительном варианте реализации количество лидокаина или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению составляет от примерно 50 мг до примерно 200 мг, предпочтительно примерно 100 мг лидокаина.
В предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая от примерно 200 мг до примерно 1000 мг фентиконазола или его соли в качестве противогрибкового агента в комбинации с примерно 500 мг - примерно 3000 мг тинидазола или его соли в качестве антибактериального агента и 50 мг -200 мг лидокаина или его соли в качестве местного анестетика, фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент. В более предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая 600 мг фентиконазола или его соли в качестве противогрибкового агента в комбинации с примерно 1000 мг - 2000 мг тинидазола или его соли в качестве антибактериального агента и 75 мг - 150 мг лидокаина или его соли и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
В другом предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая 600 мг фентиконазола или его соли в качестве противогрибкового агента в комбинации с примерно 10 мг - 800 мг метронидазола или его соли в качестве антибактериального агента и необязательно с 75 мг -150 мг лидокаина или его соли и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
В другом предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая 600 мг фентиконазола или его соли в качестве противогрибкового агента в комбинации с примерно 200 мг - 2000 мг кетоконазола или его соли в качестве антибактериального агента и необязательно с 75 мг -150 мг лидокаина или его соли и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
В более предпочтительном варианте реализации в настоящем изобретении предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, содержащая 600 мг фентиконазола или его соли в качестве противогрибкового агента в комбинации с примерно 50 мг - 150 мг клиндамицина или его соли в качестве антибактериального агента и необязательно с 75 мг - 150 мг лидокаина или его соли и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
Фармацевтическая композиция, подходящая для внутривлагалищной доставки, согласно настоящему изобретению может присутствовать в лекарственной форме, которая включает, но не ограничивается указанными, таблетки, твердые или мягкие желатиновые капсулы, кремы, суппозитории, пессарии, пенки, мази, гели, пленки, тампоны, вагинальные кольца и спринцовки. Предпочтительно, композиции имеют форму пессариев.
В предпочтительном варианте реализации фармацевтическая композиция может иметь форму пессария, содержащего фармацевтическую композицию, подходящую для внутривлагалищной доставки, согласно изобретению и основу пессария. Основа пессария может быть изготовлена из любого традиционного материала для внутривлагалищного введения, такого как глицеринизированный желатин, макроголы (полиэтиленгликоли), природные, синтетические или полусинтетические твердые жиры и фракционированное пальмоядровое масло, и их смеси. Особенно предпочтительным материалом является твердый жир, такой как триглицеридные сложные эфиры.
Как правило, количества основы пессария составляют от примерно 1% до примерно 90% по массе композиции, например, от примерно 10% до примерно 70% или от примерно 20% до примерно 60% по массе композиции.
Основа пессария также может содержать поверхностно-активное вещество, способствующее распределению активных веществ и обеспечивающее непрерывное проникновение активных веществ в слизистую оболочку.
Подходящие поверхностно-активные вещества могут быть выбраны из группы, состоящей из, но не ограничивающейся указанными, бензалкония хлорида, бензетония хлорида, цетилпиридиния хлорида, натрия докузата, глицина, гипромеллозы, фосфолипидов, полисорбатов, полоксамера, простых алкиловых эфиров полиоксиэтилена, производных полиоксиэтилена и касторового масла, сложных эфиров полиоксиэтиленсорбитана и жирных кислот, полиоксиэтиленстеаратов, натрия лаурилсульфата, сложных эфиров сорбитана, трикаприлина или их смесей. Предпочтительно, поверхностно-активное вещество представляет собой полисорбат.
Поверхностно-активное вещество может присутствовать в количестве от примерно 0% до 30% по массе, предпочтительно от примерно 0% до примерно 20%, более предпочтительно от 0% до 15% в пересчете на общую массу композиции.
Пессарий может включать по меньшей мере один или более дополнительных вспомогательных агентов для обеспечения надлежащих механических свойств и свойств высвобождения. Все указанные вспомогательные агенты должны быть совместимы с другими ингредиентами лекарственной формы и не должны наносить вред человеку. Вспомогательный агент может быть выбран из группы, состоящей из разбавителей, агентов, повышающих растворимость, эмульгаторов и антиоксидантов и/или их смесей.
Подходящие агенты, повышающие растворимость, включают кукурузное (маисовое) масло, полиэтиленгликоль, глицерин, хлопковое масло, дибутилфталат, диэтилфталат, диметиловый эфир, диметилфталат, диметилсульфоксид, диметилацетамид, этилацетат, этиловый спирт, этиллактат, этилолеат, гликофурол, изопропиловый спирт, изопропилмиристат, изопропилпальмитат, легкое минеральное масло, среднецепочечные триглицериды, метиллактат, минеральное масло, моноэтаноламин, октилдодеканол, оливковое масло, арахисовое масло, полиоксил-35-касторовое масло, пропиленкарбонат, пропиленгликоль, пирролидон, сафлоровое масло, кунжутное масло, соевое масло, подсолнечное масло, триацетин, трикаприлин, триэтаноламин, триэтилцитрат, триолеин, воду, смешиваемые с водой агенты или их смеси. Предпочтительно, агент, повышающий растворимость, представляет собой полиэтиленгликоль или глицерин, или их смеси.
Агент, повышающий растворимость, может присутствовать в количестве от примерно 0% до 80% по массе, предпочтительно от примерно 0% до примерно 50%, более предпочтительно от 0% до 30% в пересчете на общую массу композиции.
Эмульгаторы включают лецитин, экстракт юкки, экстракт коры мыльного дерева, ланолин, канделильский воск, карнаубский воск, воск жожоба, рисовые отруби, пчелиный воск, ксантановую камедь, семена айвы, глицерилолеат, глицерилстеарат, цитрат и их смеси.
Эмульгатор может присутствовать в количестве от примерно 0,05% до 20% по массе, предпочтительно от примерно 0,1% до примерно 15%, более предпочтительно от 0,2% до 10% в пересчете на общую массу композиции. Эмульгатор также можно применять в качестве агента, повышающего растворимость.
Подходящие антиоксиданты включают Pythrox LT10-IP (лецитин, аскорбилпальмитат + богатый токоферолом экстракт, подсолнечное масло), витамин Е (токоферилацетат/токоферол), аскорбиновую кислоту (витамин С) или экстракт прополиса с аскорбилпальмитатом, экстракт луковицы Allium серае (лук репчатый), экстракт корней Glycyrrhiza glabra (органическая лакрица), бутилированный гидроксианизол (БГА), бутилированный гидрокситолуол (БГТ), натрия метабисульфит, пропилгаллат и цистеин, и их смеси. Особенно предпочтительными антиоксидантами согласно настоящему изобретению являются бутилированный гидроксианизол (БГА) и бутилированный гидрокситолуол (БГТ) или их смеси.
Антиоксидант может присутствовать в количестве от примерно 0,005% до 5% по массе, предпочтительно от примерно 0,01% до примерно 4%, более предпочтительно от 0,1% до 3% в пересчете на общую массу композиции.
Помимо влагалищного пессария, фармацевтическую композицию, подходящую для внутривлагалищной доставки, согласно настоящему изобретению, можно применять и в других фармацевтических препаратах или лекарственных формах, например, в таблетках, твердых или мягких желатиновых капсулах, кремах, пенках, мазях, гелях, пленках, тампонах, вагинальных кольцах и спринцовках.
Например, фармацевтическая композиция, подходящая для внутривлагалищной доставки, согласно настоящему изобретению может иметь форму крема. Можно применять традиционную основу крема, например, содержащую масляные или воскообразные материалы, такие как жидкий парафин, белый вазелин или цетиловый спирт, воду и одно или более поверхностно-активных веществ, для получения эмульсии типа вода-в-масле.
В качестве альтернативы, фармацевтическая композиция, подходящая для внутривлагалищной доставки, согласно изобретению может иметь форму вагинальных таблеток. Таблетка содержит комбинацию фентиконазола или его фармацевтически приемлемой соли совместно с антибактериальным агентом, необязательно совместно с одним или более обезболивающими или местными анестетиками и по меньшей мере одного фармацевтически приемлемого вспомогательного вещества или носителя, при этом таблетка содержит гранулы, содержащие фентиконазол или его фармацевтически приемлемую соль и/или антибактериальный агент и фармацевтически приемлемое вспомогательное вещество и необязательно вспомогательные вещества, находящиеся вне гранул. Вспомогательные вещества, находящиеся внутри и вне гранул, могут содержать одно или более из следующих веществ: связывающее вещество, разбавитель, смазывающее вещество и разрыхлитель.
Подходящие разбавители включают кукурузный крахмал, микрокристаллическую целлюлозу, порошковую целлюлозу, силиконизированную целлюлозу, моногидрат лактозы, безводную лактозу, маннит, сорбит, сахарозу, фруктозу, декстрозу и/или их смеси. Предпочтительно, применяют моногидрат лактозы и микрокристаллическую целлюлозу.
Разбавители могут присутствовать в количестве от примерно 20% до примерно 95% по массе, предпочтительно от 35% до 90% по массе и более предпочтительно от 30 до 85% по массе от общей массы композиции.
Предпочтительно, лекарственная форма согласно изобретению содержит связывающее вещество. Связывающее вещество может быть выбрано из группы, состоящей из гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы, гидроксиэтилцеллюлозы, метилцеллюлозы, поливинилпирролидона, карбоксиметилцеллюлозы натрия, карбоксиметилцеллюлозы кальция и/или их смесей.
Связывающие вещества могут присутствовать в количестве от примерно 0,5% до примерно 20% по массе, предпочтительно от 1% до 18% по массе и более предпочтительно от 5 до 15% по массе от общей массы композиции.
Лекарственная форма согласно изобретению также может содержать разрыхлитель. Разрыхлители могут быть выбраны из группы, состоящей из гидроксипропилцеллюлозы с низкой степенью замещения, карбоксиметилцеллюлозы натрия, карбоксиметилцеллюлозы кальция, кросповидона, кроскармеллозы натрия и/или их смесей. Предпочтительно, применяют кроскармеллозу натрия.
Разрыхлители могут присутствовать в количестве от примерно 2% до примерно 50% по массе, предпочтительно от примерно 5% до примерно 45% по массе и более предпочтительно от 10% до 40% по массе от общей массы композиции.
Смазывающие вещества и агенты, препятствующие слипанию, представляют собой вспомогательные вещества, которые снижают трение между частицами и предотвращают слипание частиц лекарственного средства, а также улучшают сыпучесть гранулированных или порошкообразных композиций.
Смазывающие вещества могут быть выбраны из группы, состоящей из талька, солей щелочноземельных металлов и стеариновой кислоты, в частности, стеаратов магния и кальция, стеариновой кислоты, глицерина пальмитостеарата, стеарилфумарата и/или их смесей.
Смазывающее вещество может присутствовать в количестве от примерно 0% до 5% по массе, предпочтительно от примерно 0% до примерно 3% в пересчете на общую массу композиции.
Агент, препятствующий слипанию, может присутствовать в количестве от примерно 0% до 5% по массе, предпочтительно от примерно 0% до примерно 3% в пересчете на общую массу композиции.
В другом варианте реализации фармацевтическая композиция, подходящая для внутривлагалищной доставки, согласно изобретению может иметь форму вагинальных капсул. Вагинальная капсула содержит комбинацию фентиконазола или его фармацевтически приемлемой соли совместно с антибактериальным агентом, необязательно совместно с одним или более обезболивающими или местными анестетиками и по меньшей мере одного фармацевтически приемлемого вспомогательного вещества или носителя, таких как определено выше. Вспомогательные вещества могут включать одно или более из следующих веществ: разрыхлитель, наполнитель/разбавитель, связывающее/связующее вещество, глидант и смазывающие вещества, которые используют в абсолютных или относительных количествах, указанных выше.
Подходящие разрыхлители могут включать, но не ограничиваются указанными, натрия крахмал гликолят, кроскармеллозу натрия, кросповидон, альгины, камеди, поверхностно-активные вещества и т.д., и их смеси.
Подходящие наполнители/разбавители могут включать, но не ограничиваются указанными, дигидрат двухосновного фосфата кальция, полисахариды, главным образом, микрокристаллическую целлюлозу, лактозу, маннит, сахара, сорбит, сахарозу, неорганические соли, главным образом, соли кальция и т.д., и их смеси.
Подходящие связывающие/связующие вещества могут включать, но не ограничиваются указанными, поливинилпирролидон (повидон), желатин, сахара, глюкозу, природные камеди, синтетические целлюлозы, полиметакрилат, производные целлюлозы, такие как гид роксипропил метил целлюлоза, гидроксипропилцеллюлоза, карбоксиметилцеллюлоза, метилцеллюлоза и т.д., и их смеси.
Подходящие глиданты могут включать, но не ограничиваются указанными, коллоидный диоксид кремния, тальк, силикат алюминия и т.д., и их смеси.
Подходящие смазывающие вещества могут включать, но не ограничиваются указанными, стеарат магния, стеарилфумарат натрия, полиэтиленгликоль, стеариновую кислоту, стеараты металлов, тальк, борную кислоту, хлорид, бензоат и ацетат натрия, лаурилсульфат натрия или магния и т.д., и их смеси.
Другой аспект настоящего изобретения, таким образом, представляет собой способ получения лекарственной формы, подходящей для внутривлагалищного введения, содержащей фентиконазол или его фармацевтическую соль в комбинации с антибактериальным агентом, фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом и необязательно обезболивающим или местным анестетиком.
Согласно указанному аспекту способ включает стадии смешения фентиконазола или его фармацевтической соли, антибактериального агента и необязательно обезболивающего или местного анестетика по меньшей мере с одним фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом и последующей обработки смеси для получения лекарственной формы.
В одном из вариантов реализации смесь обрабатывают, наполняя ею капсулы или прессуя ее с получением таблеток.
Как правило, композиция подходит для введения в одной дозе в один день.
В предпочтительном варианте реализации изобретения предложен способ получения пессария, содержащего фентиконазол или его фармацевтическую соль в комбинации с антибактериальным агентом, фармацевтически приемлемым вспомогательным веществом и/или вспомогательным агентом и необязательно с обезболивающим или местным анестетиком, при этом способ включает следующие стадии:
a) Плавление твердого жира
b) Добавление поверхностно-активного вещества и/или агента, повышающего растворимость, если их используют, к расплавленному жиру
c) Добавление фентиконазола, антибактериального агента и необязательно обезболивающего или местного анестетика к расплавленному жиру, полученному на стадии а), или к смеси, полученной на стадии b), до получения гомогенного продукта
d) Наполнение подходящей упаковки конечным продуктом
Другой аспект изобретения представляет собой фармацевтическую композицию, подходящую для внутривлагалищной доставки, содержащую:
a) фентиконазол или его фармацевтически приемлемую соль, и
b) антибактериальный агент
c) необязательно одно(один) или более обезболивающих или местных анестетиков, и
d) фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент,
для применения в качестве лекарственного средства. В частности, изобретение относится к фармацевтической композиции, подходящей для внутривлагалищной доставки, для применения при лечении инфекционных заболеваний или состояний женской репродуктивной системы, таких как вульвовагинальные инфекции. Вульвовагинальные инфекции включают бактериальный вагиноз, вульвовагинальный кандидоз (инфекции, вызванные как albicans, так и штаммами, отличными от albicans), трихомональный вагинит и смешанные инфекции.
В предпочтительном варианте реализации антибактериальный агент выбран из акрифлавина, ампициллина, цефтриаксона, хлорамфеникола, хлорхинальдола, кетоконазола, клиндамицина, йодохинола, метронидазола, ниморазола, орнидазола, пивампициллина, секнидазола, спирамицина, тетрациклина, тинидазола, деквалиния хлорида и их фармацевтически приемлемых солей и сложных эфиров, и их комбинаций. В наиболее предпочтительном варианте реализации применяют клиндамицин, метронидазол, кетоконазол и тинидазол. В наиболее предпочтительном варианте реализации антибактериальный агент представляет собой тинидазол.
Композицию согласно изобретению также рассматривают как эффективную при лечении любых вторичных кандидозных, бактериальных и/или трихомональных инфекций, которые могут возникать в результате лечения указанных возбудителей. Влагалищные инфекции, вызванные стрептококками группы В и D и т.д., инфекции, связанные с микроорганизмами, вызывающими вульвит и вульвовагинит, и другие влагалищные инфекции (например, атрофический вагинит, аллергический или вызванный раздражителем вульвовагинит, генитальный псориаз (с клинически значимой инфекцией или без нее), вульвит, вызванный склерозирующим лишаем, и т.д.), также можно эффективно лечить с применением композиций, описанных в настоящем документе.
Несмотря на то, что описано, главным образом, применение композиций согласно настоящему изобретению для лечения влагалищных инфекций, они также могут найти более широкое применение при лечении первичных и/или вторичных генитальных инфекций как у мужчин, так и у женщин, включая инфекции, передаваемые половым путем, например, инфекции, вызванные хламидиями; баланит; дерматит полового члена; генитальный герпес; гонорея; и т.д.
Другой аспект изобретения относится к фармацевтической композиции, подходящей для внутривлагалищной доставки, для применения при лечении любых вторичных кандидозных, бактериальных и/или трихомональных инфекций, которые могут возникать в результате лечения указанных возбудителей, и, в общем случае, при лечении первичных и/или вторичных генитальных инфекций как у мужчин, так и у женщин, таких как инфекции, вызванные хламидиями; баланит; дерматит полового члена; генитальный герпес; гонорея; и т.д.
В предпочтительном варианте реализации антибактериальный агент выбран из клиндамицина, метронидазола, кетоконазола и тинидазола. В наиболее предпочтительном варианте реализации антибактериальный агент представляет собой тинидазол.
В качестве альтернативы фентиконазолу в составе согласно изобретению можно применять следующие противогрибковые агенты: эконазол, сертаконазол или их фармацевтически приемлемые соли, или их смеси.
Количество эконазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению предпочтительно составляет от примерно 10 мг до примерно 500 мг, более предпочтительно от примерно 20 мг до примерно 400 мг и еще более предпочтительно от примерно 50 мг до примерно 300 мг. В более предпочтительном варианте реализации количество эконазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению составляет 150 мг. Количество сертаконазола или его фармацевтически приемлемой соли в фармацевтической композиции согласно изобретению предпочтительно составляет от примерно 80 мг до 600 мг, более предпочтительно от 150 мг до 400 мг и более предпочтительно от 200 мг до 350 мг.
Фармацевтическая композиция согласно настоящему изобретению может быть обеспечена в упаковке для проведения полного курса лечения. Упаковки, содержащие по меньшей мере один состав, содержащий фармацевтическую композицию согласно настоящему изобретению, рассматривают как часть настоящего изобретения.
Следующие примеры предназначены для иллюстрации настоящего изобретения и при этом не являются ограничивающими.
Примеры
Пример 1
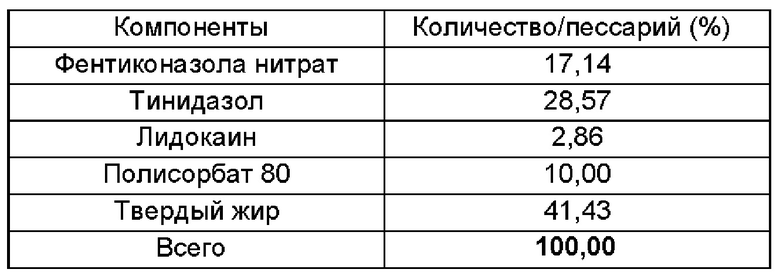
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария в соответствии со следующим составом:
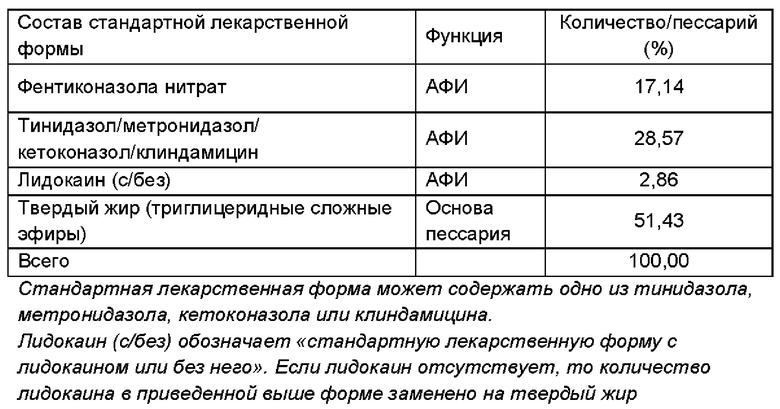
Общий способ получения:
1. Плавили твердый жир при 55°С
2. Добавляли и смешивали поверхностно-активное(-ые) вещество(-а) и/или агент(-ы), повышающий(-е) растворимость, если их использовали (в зависимости от стандартной лекарственной формы)
3. Добавляли АФИ в полученную смесь и смешивали до получения гомогенного продукта.
4. Наполняли полученной смесью формы/оболочки. Пропускали формы/оболочки через охлаждающий туннель и завершали способ герметизации
5. Завершали способ упаковки
Пример 2
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
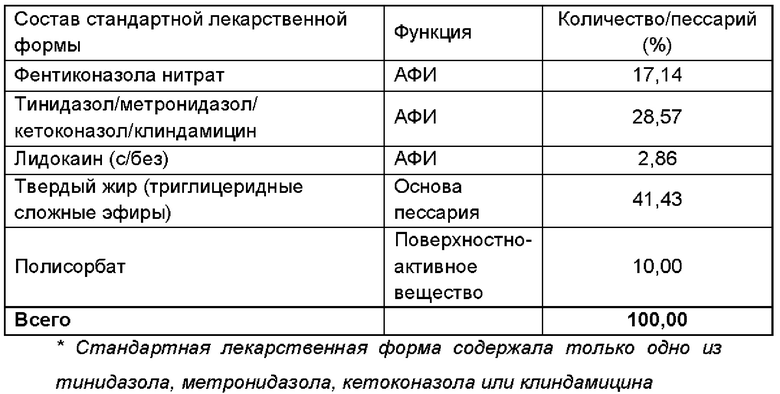
Пример 3
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
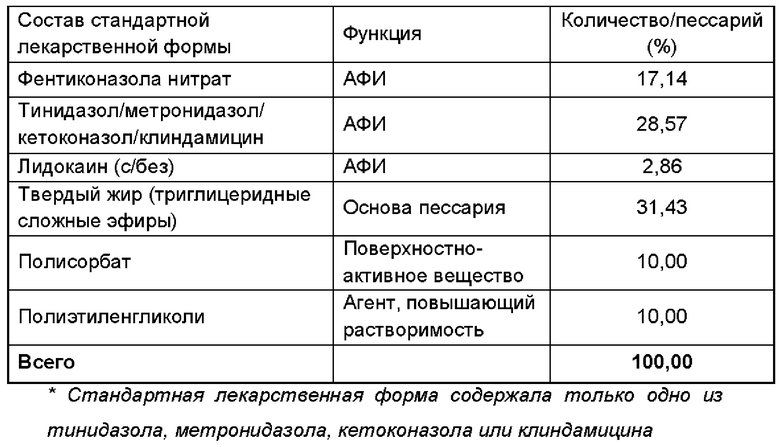
Пример 4
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
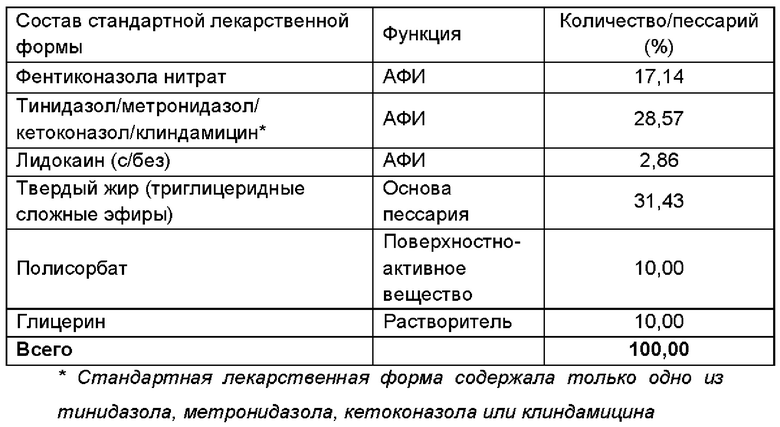
Пример 5
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
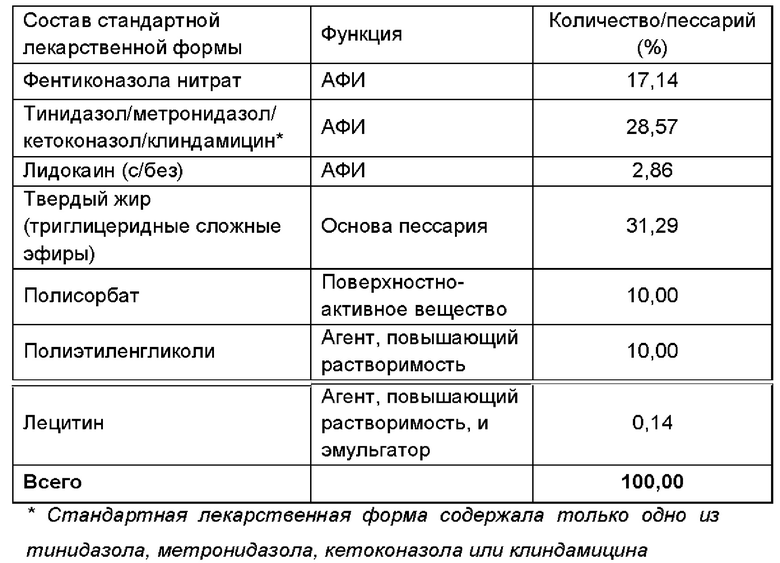
Пример 6
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
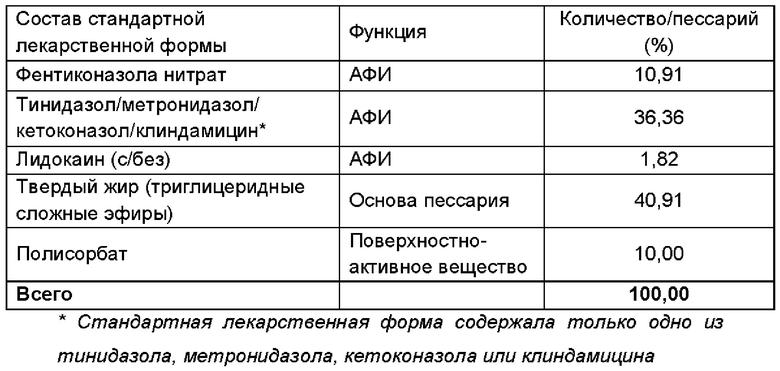
Пример 7
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
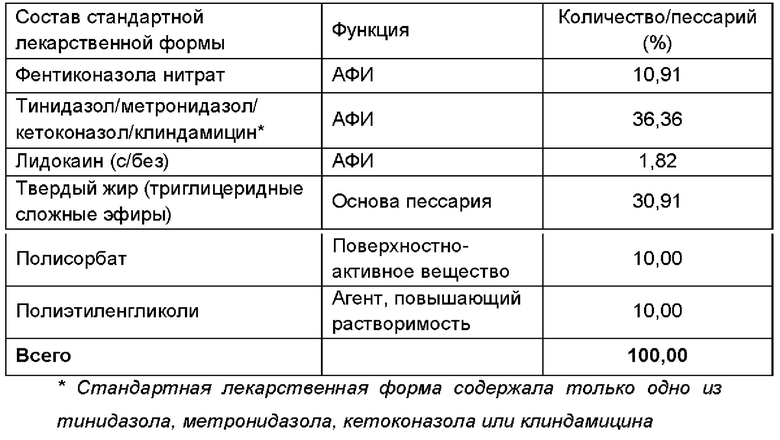
Пример 8
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
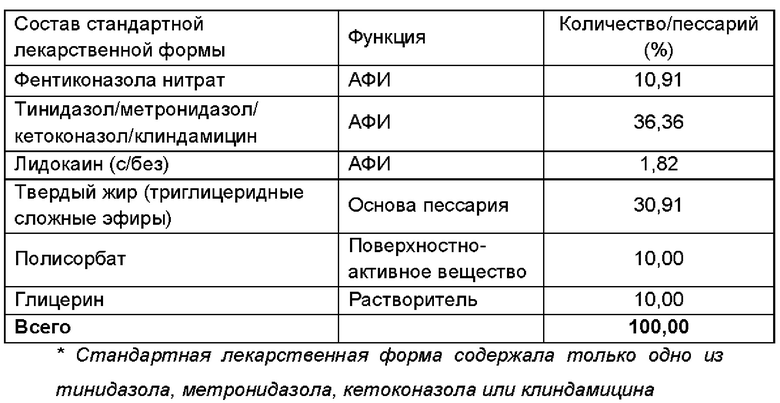
Пример 9
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
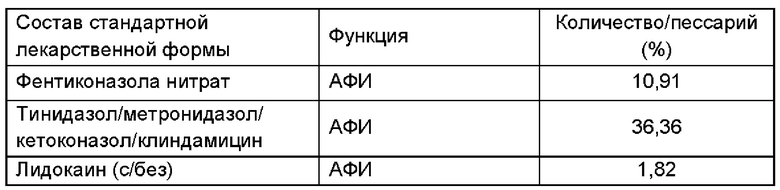

Пример 10
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде пессария согласно общему способу, описанному в примере 1, со следующим составом:
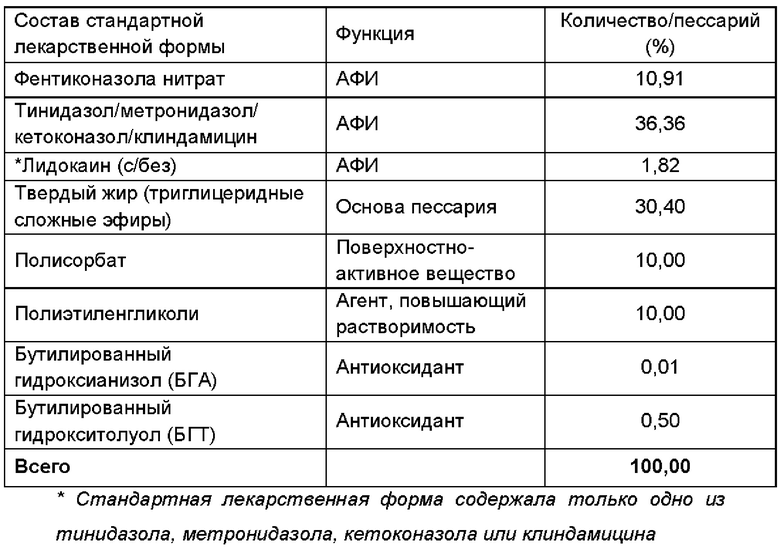
Пример 11
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде вагинальной таблетки в соответствии со следующим составом:
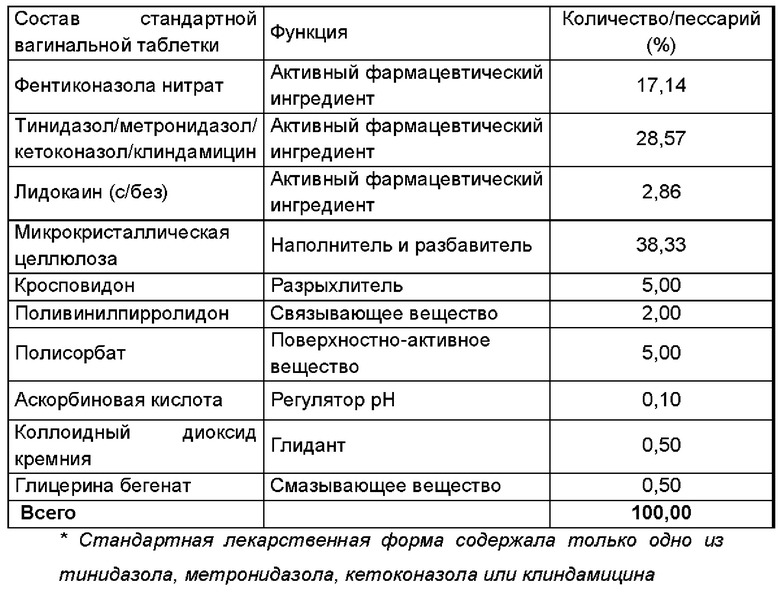
Общий способ получения вагинальных таблеток
1. Растворяли ПВП, полисорбат и аскорбиновую кислоту в надлежащем растворителе или смеси растворителей в качестве раствора для гранулирования.
2. Смешивали АФИ, МКЦ и кросповидон с получением однородного порошка и гранулировали с раствором для гранулирования.
3. Просеивали полученные гранулы и сушили.
4. Снова просеивали сухие гранулы.
5. Добавляли коллоидный диоксид кремния путем просеивания и смешивали.
6. После этого добавляли глицерина бегенат путем просеивания и смешивали в течение короткого периода времени.
7. Наконец, прессовали полученную порошковую смесь в таблетки.
Пример 12
Получали фармацевтическую композицию, включающую комбинацию фентиконазола или его соли согласно изобретению, в виде вагинальной капсулы в соответствии со следующим составом:
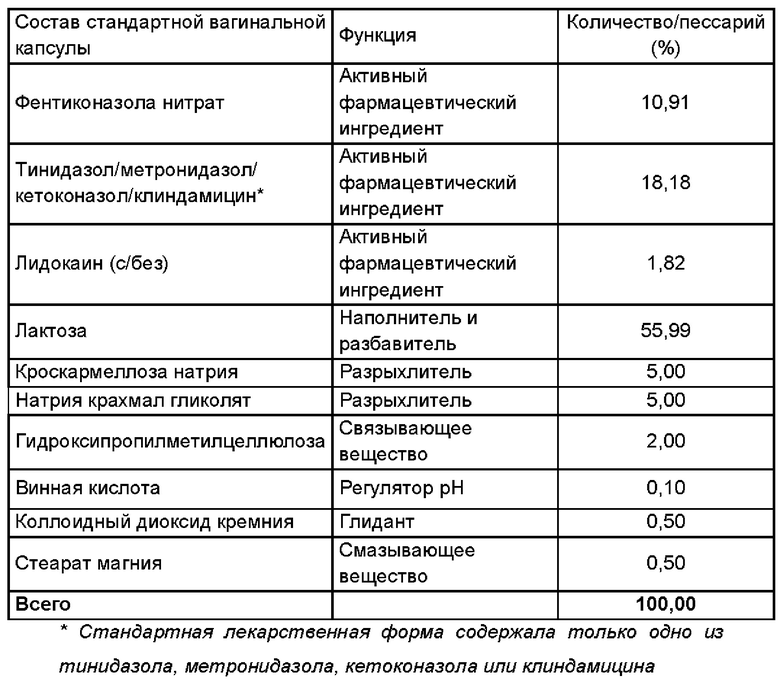
Общий способ получения вагинальных капсул
1. Просеивали АФИ, лактозу и кроскармеллозу натрия, натрия крахмал гликолят, ГПЦ и винную кислоту и смешивали с получением однородного порошка.
2. Добавляли коллоидный диоксид кремния путем просеивания и смешивали.
3. После этого добавляли стеарат магния путем просеивания и смешивали в течение короткого периода времени.
4. Наконец, наполняли смесью капсулы.
ИССЛЕДОВАНИЯ СТАБИЛЬНОСТИ
Проводили исследования стабильности фармацевтической композиции согласно настоящему изобретению. В частности, проводили исследования стабильности фармацевтической композиции согласно настоящему изобретению с лидокаином и без него.
Способы анализа ВЭЖХ для изделия в виде пессария, содержащего фентиконазола нитрат, тинидазол и лидокаин (с/без), подробно описаны ниже.
1. ХРОМАТОГРАФИЧЕСКИЕ УСЛОВИЯ ДЛЯ АНАЛИЗА НА СОДЕРЖАНИЕ ОСНОВНОГО ВЕЩЕСТВА
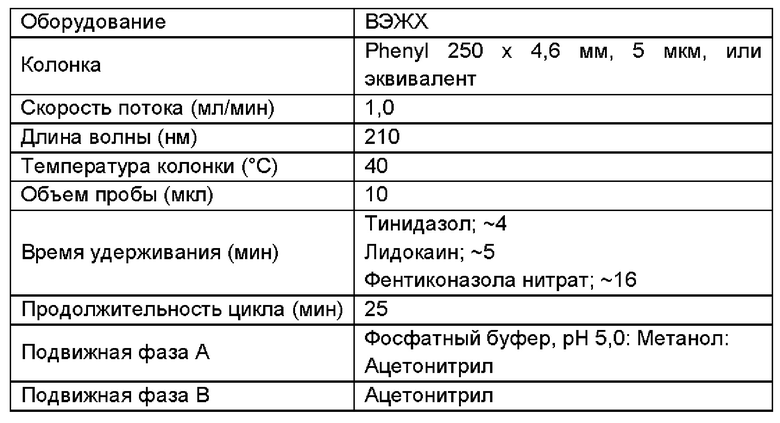
2. ХРОМАТОГРАФИЧЕСКИЕ УСЛОВИЯ ДЛЯ АНАЛИЗОВ РОДСТВЕННЫХ ПРИМЕСЕЙ ТИНИДАЗОЛА
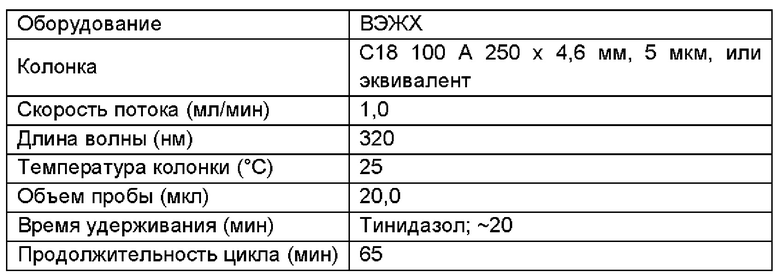

3. ХРОМАТОГРАФИЧЕСКИЕ УСЛОВИЯ ДЛЯ АНАЛИЗОВ РОДСТВЕННЫХ ПРИМЕСЕЙ ЛИДОКАИНА
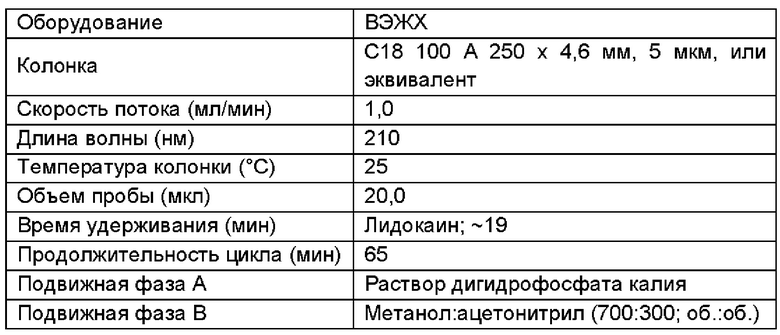
4. ХРОМАТОГРАФИЧЕСКИЕ УСЛОВИЯ ДЛЯ АНАЛИЗОВ РОДСТВЕННЫХ ПРИМЕСЕЙ ФЕНТИКОНАЗОЛА НИТРАТА
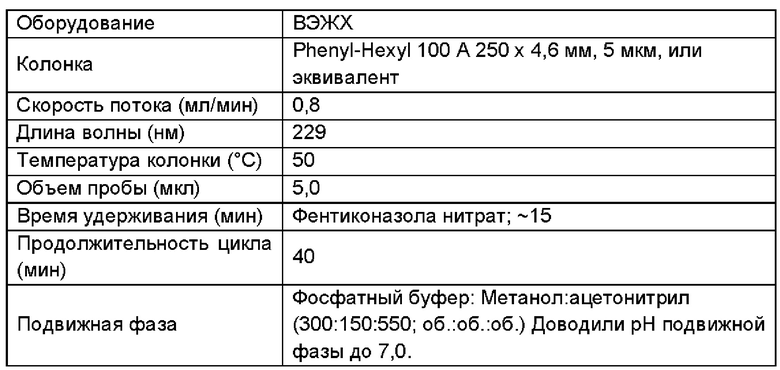
ИССЛЕДОВАНИЯ СТАБИЛЬНОСТИ для примера 2
Исследовали стабильность состава согласно примеру 2, содержащего фентиконазола нитрат, тинидазол и лидокаин в качестве активных ингредиентов, в разных условиях.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ ДОЛГОСРОЧНОЙ СТАБИЛЬНОСТИ
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 25°С ± 2°С / 60% ± 5 ОВ
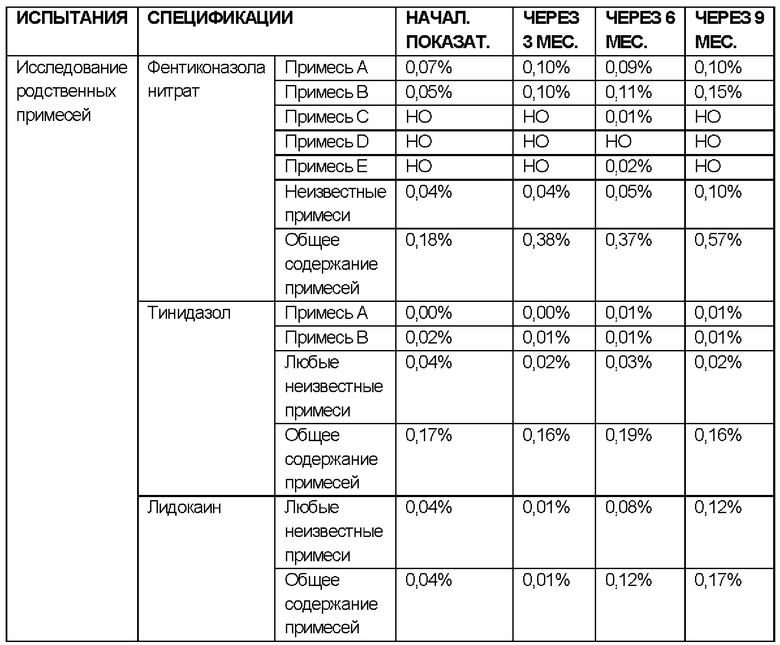
Подробную информацию о примесях А - D для фентиконазола нитрата можно найти в Европейской фармакопее 10.0, 07/2014:1211, в исправлении 10.0, стр. 2622-2624, содержание которой включено в настоящий документ посредством ссылки.
Подробную информацию о примесях А и В для тинидазола можно найти в Европейской фармакопее 10.0, 01/2017:1051, стр. 4048-4049, содержание которой включено в настоящий документ посредством ссылки.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ СТАБИЛЬНОСТИ В ПРОМЕЖУТОЧНЫХ УСЛОВИЯХ: 30°С±2°С / 65% ± 5 ОВ
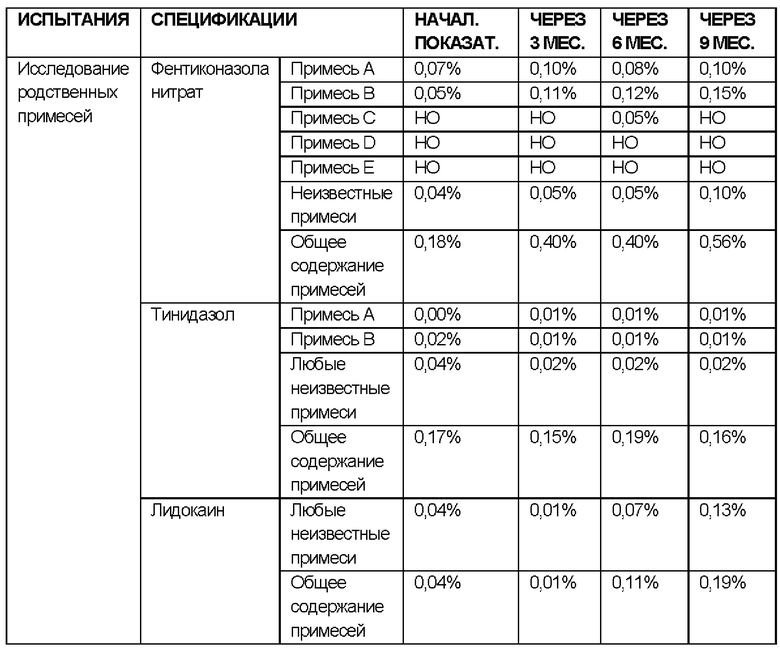
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ СТАБИЛЬНОСТИ В УСЛОВИЯХ УСКОРЕННОГО СТАРЕНИЯ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 40°С ± 2°С / 75% ± 5 ОВ
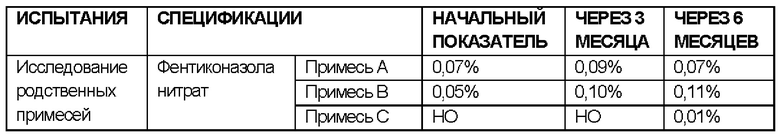
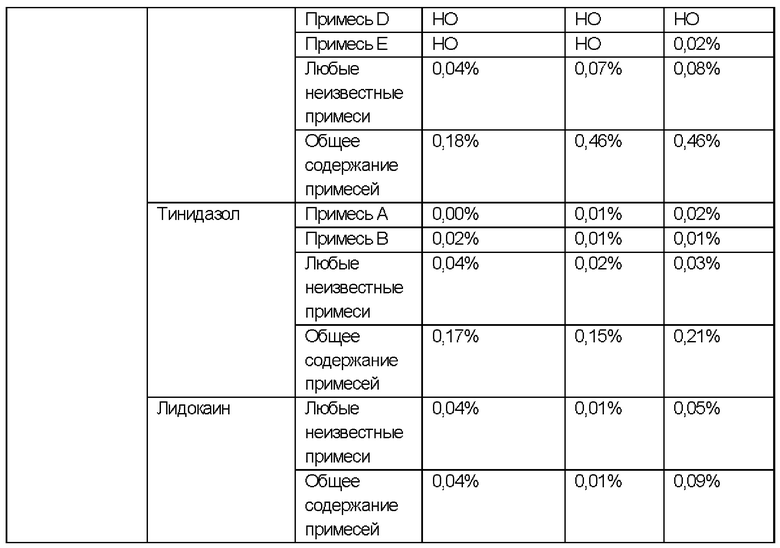
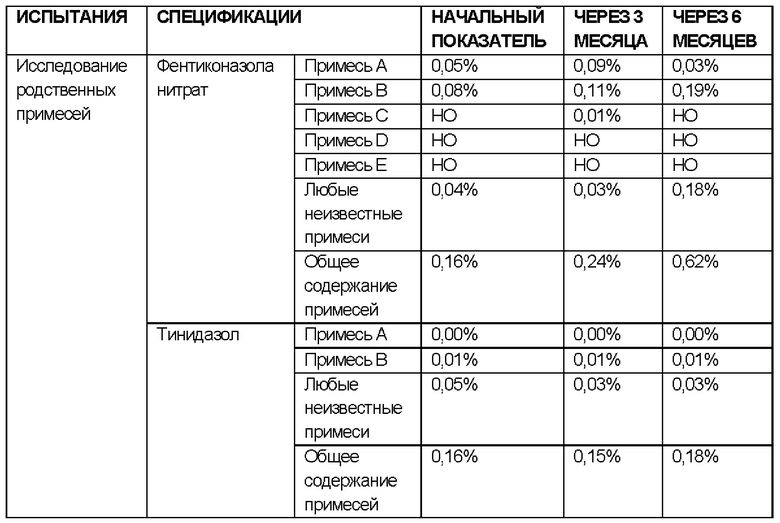
ИССЛЕДОВАНИЯ СТАБИЛЬНОСТИ для примера 2, не содержащего лидокаин
Исследовали стабильность состава согласно примеру 2, не содержащего лидокаин (количество лидокаина заменяли таким же количеством твердого жира), содержащего фентиконазола нитрат и тинидазол в качестве активных ингредиентов, в разных условиях.
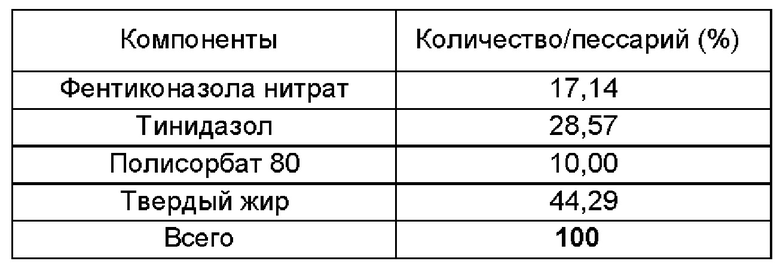
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ ДОЛГОСРОЧНОЙ СТАБИЛЬНОСТИ: УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 25°С ± 2°С / 60% ± 5 ОВ

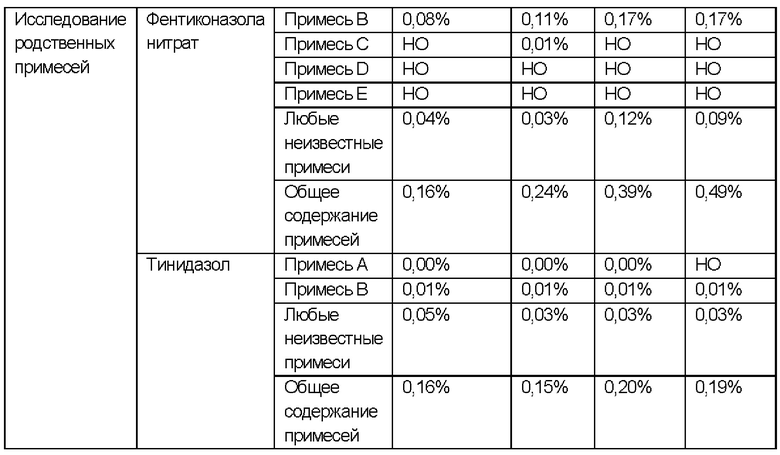
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ СТАБИЛЬНОСТИ В ПРОМЕЖУТОЧНЫХ УСЛОВИЯХ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 30°С ± 2°С / 65% ± 5 ОВ
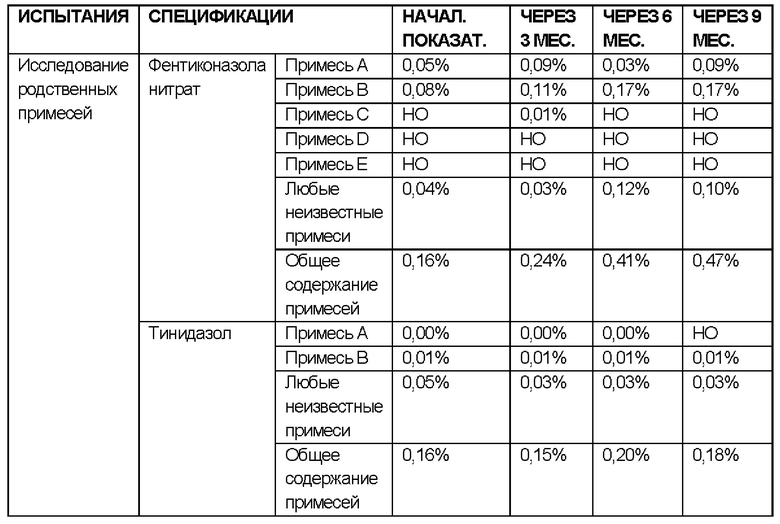
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ СТАБИЛЬНОСТИ В УСЛОВИЯХ УСКОРЕННОГО СТАРЕНИЯ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 40°С ± 2°С / 75% ± 5 ОВ
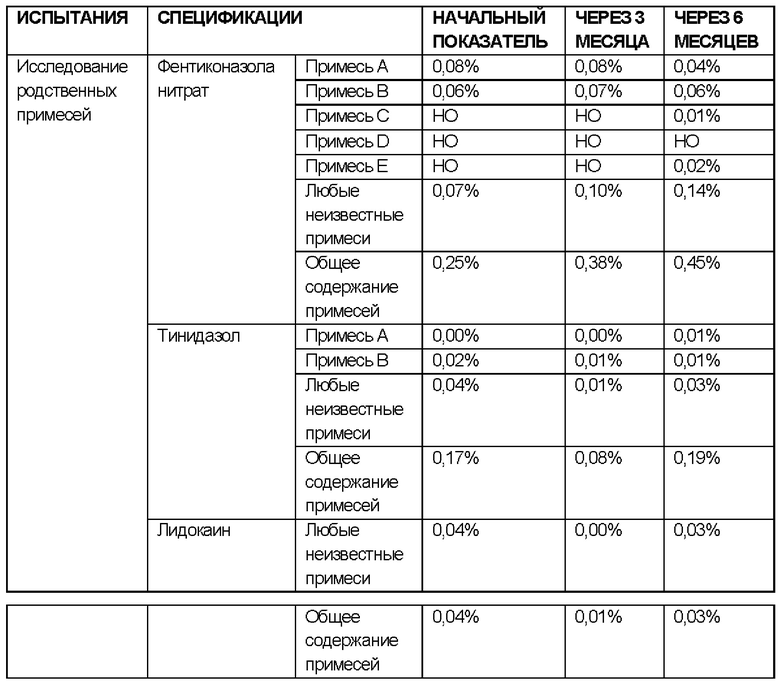
ИССЛЕДОВАНИЯ СТАБИЛЬНОСТИ для примера 6
Исследовали стабильность состава согласно примеру 6, содержащего фентиконазола нитрат, тинидазол и лидокаин в качестве активных ингредиентов, в разных условиях.
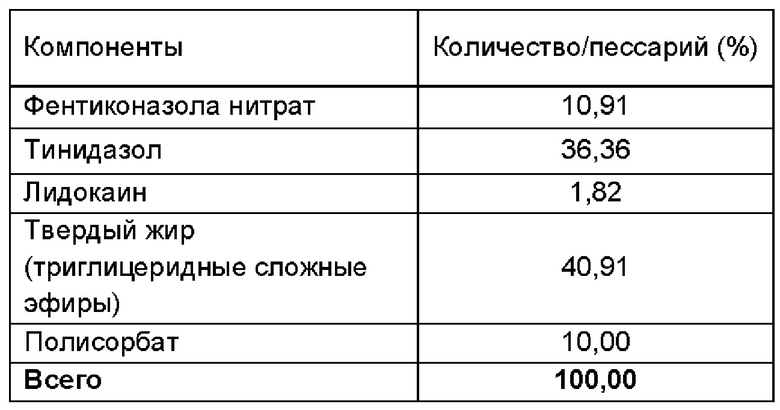
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ ДОЛГОСРОЧНОЙ СТАБИЛЬНОСТИ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 25°С ± 2°С / 60% ± 5 ОВ
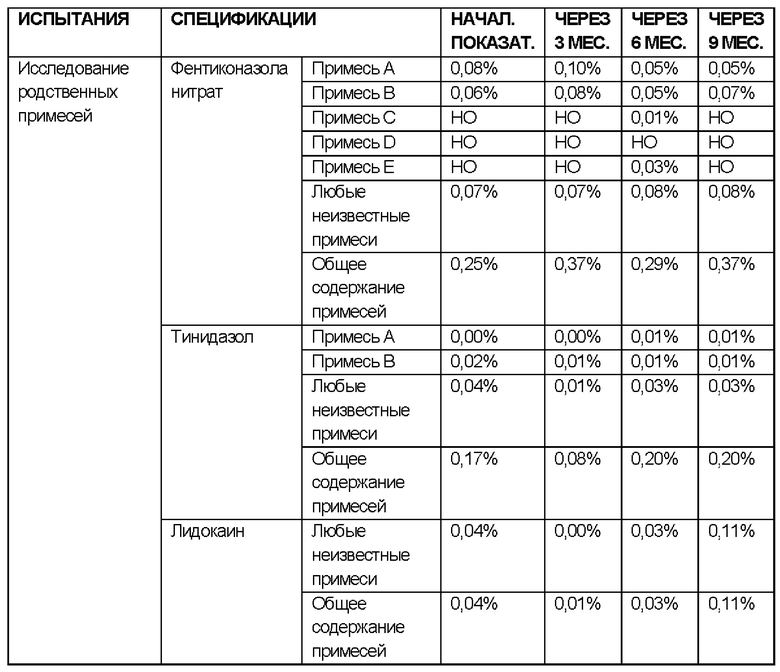
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ СТАБИЛЬНОСТИ В ПРОМЕЖУТОЧНЫХ УСЛОВИЯХ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 30°С ± 2°С / 65% ± 5 ОВ
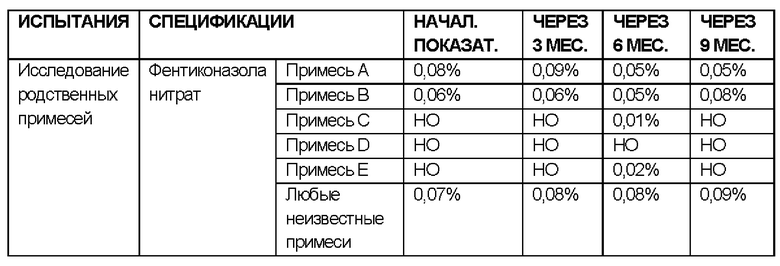
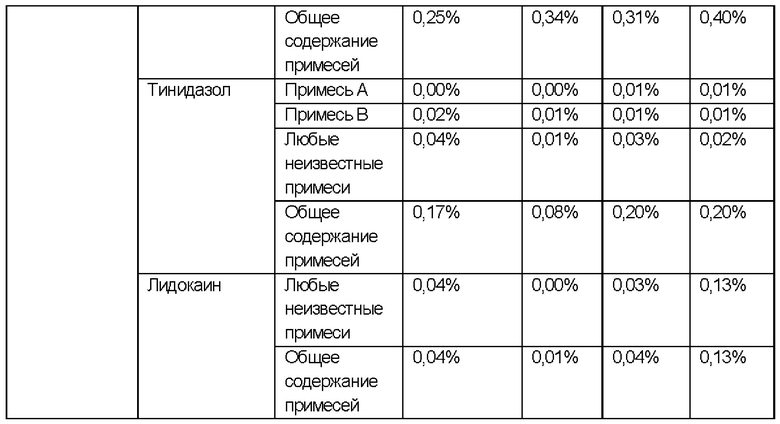
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ СТАБИЛЬНОСТИ В УСЛОВИЯХ УСКОРЕННОГО СТАРЕНИЯ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 40°С ± 2°С / 75% ± 5 ОВ
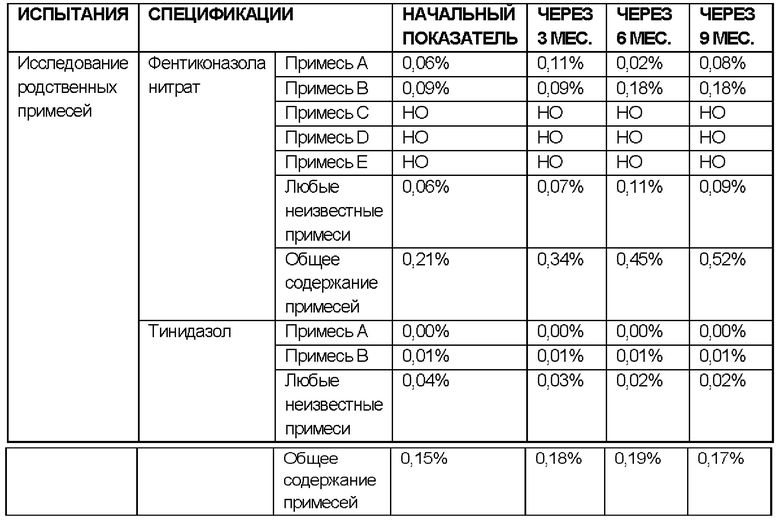
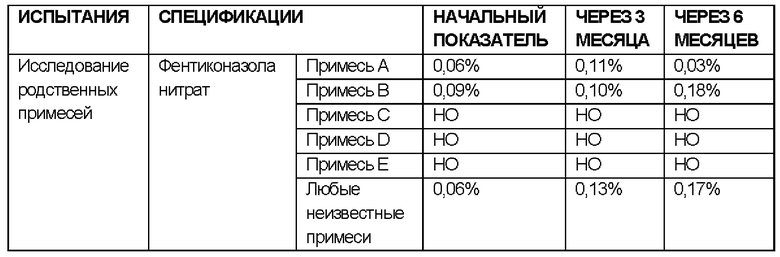
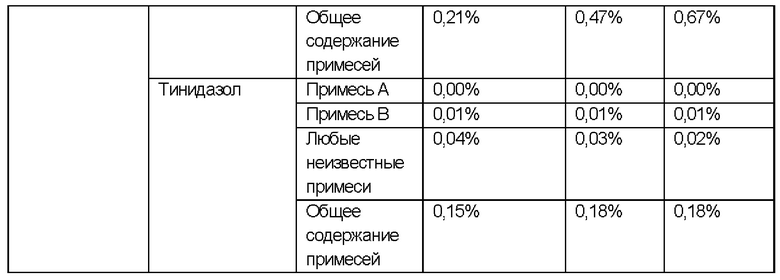
ИССЛЕДОВАНИЯ СТАБИЛЬНОСТИ для примера 6, не содержащего лидокаин
Исследовали стабильность состава согласно примеру 6, не содержащего лидокаин (количество лидокаина заменяли таким же количеством твердого жира), содержащего фентиконазола нитрат и тинидазол в качестве активных ингредиентов, в разных условиях.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ ДОЛГОСРОЧНОЙ СТАБИЛЬНОСТИ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 25°С ± 2°С / 60% ± 5 ОВ
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ СТАБИЛЬНОСТИ В ПРОМЕЖУТОЧНЫХ УСЛОВИЯХ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 30°С ± 2°С / 65% ± 5 ОВ
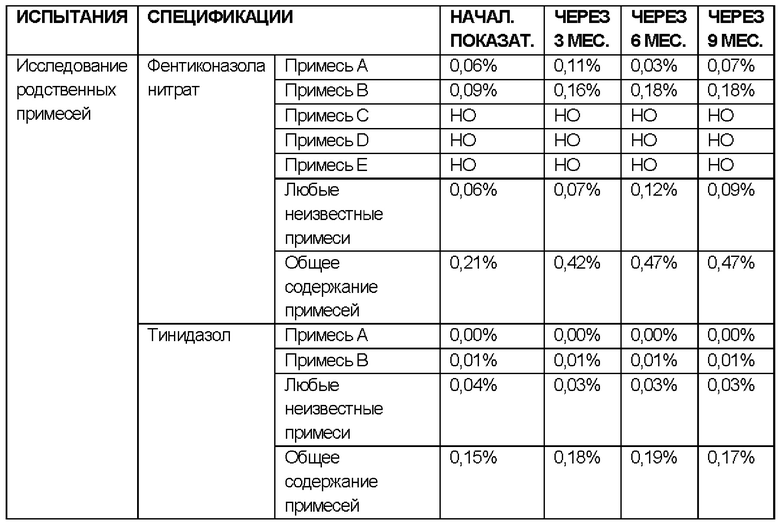
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ СТАБИЛЬНОСТИ В УСЛОВИЯХ УСКОРЕННОГО СТАРЕНИЯ:
УСЛОВИЯ ИСПЫТАНИЯ СТАБИЛЬНОСТИ: 40°С ± 2°С / 75% ± 5 ОВ
Изобретение относится к области фармацевтики и может быть использовано для лечения инфекционных заболеваний женской репродуктивной системы. Предложена фармацевтическая композиция, подходящая для внутривлагалищной доставки, для лечения инфекционных заболеваний репродуктивной системы, содержащая комбинацию фентиконазола или его фармацевтически приемлемой соли и тинидазола или его фармацевтически приемлемой соли, а также фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент. Композиция является стабильной и подходящей для внутривлагалищной доставки. 9 з.п. ф-лы, 24 табл., 12 пр.
1. Фармацевтическая композиция, подходящая для внутривлагалищной доставки для лечения инфекционных заболеваний репродуктивной системы, содержащая комбинацию:
a) фентиконазола или его фармацевтически приемлемой соли, и
b) тинидазола или его фармацевтически приемлемой соли,
и композиция дополнительно содержит
d) фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что отношение количества а) фентиконазола или его фармацевтически приемлемой соли к количеству b) тинидазола или его фармацевтически приемлемой соли в комбинации находится в диапазоне от 10:1 до 1:10 по массе.
3. Фармацевтическая композиция по п. 2, отличающаяся тем, что отношение количества а) фентиконазола или его фармацевтически приемлемой соли к количеству b) тинидазола или его фармацевтически приемлемой соли в комбинации находится в диапазоне от примерно 7:1 до примерно 1:7, предпочтительно от 4:1 до 1:4 по массе.
4. Фармацевтическая композиция по любому из предыдущих пунктов, отличающаяся тем, что фентиконазол присутствует в виде фентиконазола нитрата.
5. Фармацевтическая композиция по любому из предыдущих пунктов, содержащая от 200 до 1000 мг фентиконазола или его фармацевтически приемлемой соли и от 500 до 3000 мг тинидазола или его фармацевтически приемлемой соли и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
6. Фармацевтическая композиция по любому из предыдущих пунктов, содержащая 600 мг фентиконазола или его фармацевтически приемлемой соли и от 1000 до 2000 мг тинидазола или его фармацевтически приемлемой соли и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
7. Фармацевтическая композиция по п. 1, дополнительно содержащая:
с) одно (один) или более обезболивающих или местных анестетиков, где обезболивающее выбрано из буторфанола, кодеина, дигидрокодеина, фентанила, гидрокодона, леворфанола, меперидина, метадона, морфина, налоксона, оксикодона, оксиморфона, пентазоцинов, пропоксифена, их фармацевтически приемлемых солей и сложных эфиров и их комбинаций, или где местный анестетик выбран из группы, состоящей из бензокаина, бупивакаина, бутамбена, хлорпрокаина, лидокаина, мепивакаина, прамоксина, прилокаина, прокаина, пропаракаина, ропивакаина, тетракаина, их фармацевтически приемлемых солей и сложных эфиров и их комбинаций.
8. Фармацевтическая композиция по п. 7, отличающаяся тем, что местный анестетик, представляющий собой лидокаин или его фармацевтически приемлемую соль, присутствует в количестве от примерно 50 мг до примерно 200 мг.
9. Фармацевтическая композиция по п. 1 для лечения вульвовагинальных инфекций.
10. Фармацевтическая композиция по пп. 1 и 7, содержащая фентиконазол или его фармацевтически приемлемую соль, тинидазол, или его фармацевтически приемлемую соль или сложный эфир или их комбинации, лидокаин или его фармацевтически приемлемую соль и фармацевтически приемлемое вспомогательное вещество и/или вспомогательный агент.
| US 20180311214 A1, 01.11.2018 | |||
| WO 2006060462 A1, 08.06.2006 | |||
| WO 2005087270 A1, 22.09.2005 | |||
| CN 108210448 A, 29.06.2018 | |||
| CN 108079098 A, 29.05.2018 | |||
| Регистр лекарственных средств России РЛС Энциклопедия лекарств | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| US 20170182006 A1, 29.06.2017 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2024-10-08—Публикация
2021-01-29—Подача