Изобретение относится к области медицины, а именно к имплантируемым медицинским изделиям для детекции внеклеточных электрически потенциалов и/или возбуждения потенциалов действия путем электростимуляции.
При применении имплантируемых медицинских электродов зачастую возникает проблема несоответствия механических свойств между материалом электрода и нативной тканью, а именно в жесткости, модуле упругости и твердости. Это приводит как возникновению реакции отторжения и появлению хронического воспаления, так и к повреждению самого электрода - растрескиванию (при малом диаметре), и, как следствие, резкому возрастанию импеданса. При уменьшении размеров электрода (до десятков микрометров в сечении проводящей части - далее, микроэлектрод), проблема становится более выраженной, так как для значительного возрастания импеданса требуются меньшие повреждения, которые могут быть вызваны меньшими изгибовыми деформациями.
Известен микроэлектрод (US 20170087352 A1, опублик. 30.03.2017 г.), являющийся цилиндрической многоканальной микроэлектродной матрицей, имплантируемая часть которой имеет жесткое биодеградирующее покрытие, позволяющее выполнить точное позиционирование во время имплантации, и электропроводящего сердечника, такого как микропроволока.
Недостатками данного изобретения являются: малая биосовместимость вследствие обнажения внутренних частей микроэлектрода после растворения оболочки в долгосрочной перспективе; возможное смещение микроэлектрода при неравномерной деградации оболочки, что может быть возможно при прохождении устройства через несколько типов тканей, жидкости которых обеспечивают различную скорость растворения.
Известна электродная матрица (AU 2008208093 B2, опублик. 31.07.2008 г.) являющаяся электродной матрицей с гибкими проводящими элементами, закрепленными в жестком биодеградируюшем корпусе.
Недостатками данного изобретения являются: применение в качестве проводящих сердечников металлических проволок, что приводит к потери значительной части гибкости после растворения биодеградирующей оболочки; возможное смещение микроэлектродов в ткани при неравномерной деградации оболочки.
Наиболее близким является углеродный электрод с возможностью накопления энергии прототип (US 20170169912 А1, опублик. 15.06.2017), одним из вариантов исполнения которого может быть электрод, содержащий от 5 до 50% массовых процентов частиц одной или нескольких аллотропных модификаций углерода, в том числе в виде токопроводящего покрытия.
Недостатком данного изобретения является то, что данный электрод не обеспечивает достаточную эластичность и гибкость для использования в качестве покрытия имплантируемого в мягкие ткани микроэлектрода. Более того, такое покрытие при высокой (близкой к 50%) концентрации частиц различных фаз углерода скорее всего не будет являться биосовместимым из-за выделения множества микрочастиц тех форм углерода, что приводят к воспалению (таких как углеродные нанотрубки), при усталостной деградации материала.
Техническим результатом изобретения является приближение механических свойств всего микроэлектрода к свойствам ткани периферического нерва, а именно уменьшение модуля упругости по сравнению с необработанным углеродным волокном.
Технический результат достигается следующим образом.
Композиционный биосовместимый микроэлектрод для медицинского применения состоит из расположенного в электропроводящей матрице сердечника в виде отожженного углеродного моноволокна диаметром 5-10 мкм или пучка углеродных волокон до 100 штук и имеет внешнее изолирующее покрытие, причем матрица представляет собой композиционный материал из полидиметилсилоксана с содержанием частиц проводящего наполнителя в виде углеродных микро- и наночастиц от 30 до 70% по массе, а внешнее покрытие состоит из полидиметилсилоксана, выполненного путем смешивания диметилсилоксана и метилгидросилоксана с платиновым комплексом в качестве катализатора в массовом соотношении 10/1.
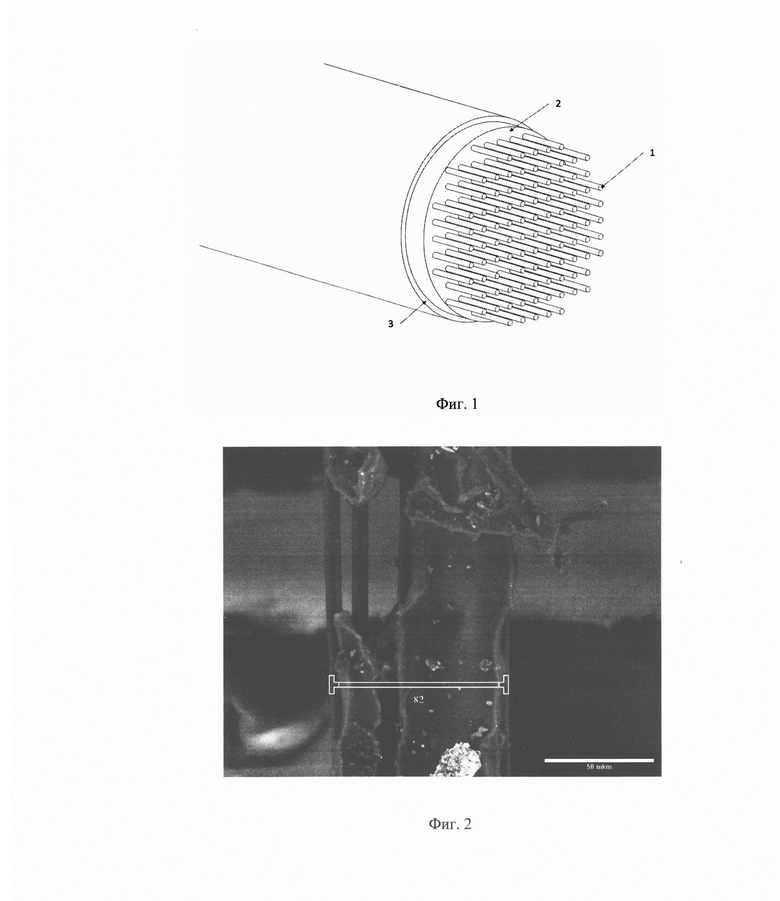
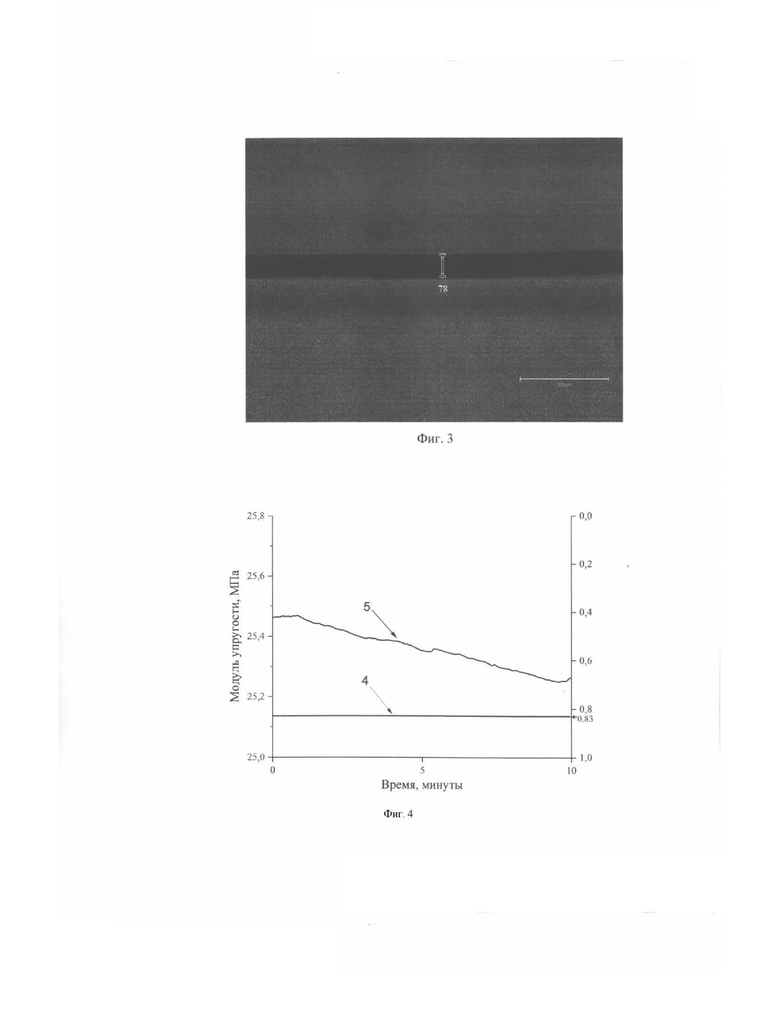
Изобретение поясняется чертежом, где на Фиг. 1 представлена схема микроэлектрода. На Фиг. 2 - СЭМ-изображение микроэлектрода. На Фиг. 3 - фотография микроэлектрода. На Фиг. 4 - график изменения модуля упругости микроэлектрода во время испытания на динамическое растяжение. На Фиг. 5 - график изменения жизнеспособности мультипотентных мезенхимальных стромальных клеток (ММСК) зуба человека после инкубации с вытяжками образцов микроэлектрода и отдельно с вытяжками образцов изолирующего покрытия.
Изобретение осуществляется следующим образом.
Микроэлектрод представляет собой углеродное волокно 1 в электропроводящей матрице 2 с изолирующим покрытием 3. Углеродное волокно 1 может представлять собой как углеродное моноволокно, так и пучок углеродных волокон до 100 штук. Электропроводящая матрица 2 состоит из полидиметилсилоксана и углеродных микро- и/или наночастиц в различных аллотропных модификациях. Изолирующее покрытие 3 состоит из полидиметилсилоксана.
Полидиметилсилоксан получается смешиванием мономера - диметилсилоксана с концевыми виниловыми группами и сшивающего агента - метилгидросилоксана с платиновым комплексом в качестве катализатора.
В первую очередь производят отжиг углеродного волокна, составляющего сердечник микроэлектрода, для удаления аппрета по ГОСТ 33598. Для аппретов, удаляемых только термическим разложением, проводят отжиг в открытом тигле в воздушной атмосфере, границы температурного интервала выбирают следующим образом: нижняя граница задается температурой разложения аппрета плюс 5°С, верхняя - не более 350°С для углеродных волокон на основе ПАН и вискозы. Отжиг производят до прекращения изменения массы образца, которое контролируют взвешиванием, производящимся по методике из раздела Б.5.2.12 по ГОСТ 32667.
Для приготовления электропроводящей матрицы мономер (диметилсилоксан) растворяют в ХЧ гексане или циклогексане, в объемном соотношении от 1/10 до 1/120, в зависимости от планируемого процента содержания проводящего наполнителя.
В непрерывно перемешиваемый раствор вводят углеродные микро- и/или наночастицы (в виде порошка или водной пасты) в массовом содержании от 30 до 80% от массы мономера (диметилсилоксана).
Сосуд с раствором помещают в термостатируемую ультразвуковую ванну, в которой в течение 0.5 - 1 часа производят обработку ультразвуком. Температуру во время обработки удерживают от 20 до 50°С.
В непрерывно перемешиваемый раствор вводят сшивающий агент (метилгидросилоксан с платиновым комплексом в качестве катализатора), после чего раствор перемешивают в течение 10 минут.
После введения сшивающего агента раствор остается пригодным к обработке пучка углеродных волокон или углеродного моноволокна в течение 1 часа.
Производят повторную обработку раствора ультразвуком в течение 10-30 минут для диспергации углеродных микро- и/или наночастиц.
В непрерывно перемешиваемый раствор вводят пучок углеродных волокон или углеродное моноволокно, закрепленный/закрепленное в натянутом состоянии на поддерживающей рамке (рамку изготавливают из нерастворимого в гексане материала). Рамку располагают таким образом, чтобы пучок углеродных волокон или углеродное моноволокно находился/находилось в середине объема раствора и не касался/касалось вращающегося магнитного якоря.
Погруженный в раствор пучок углеродных волокон или углеродное моноволокно обрабатывают ультразвуком в течение 5-10 минут, точное время выбирают таким образом, чтобы суммарное время обработки раствора после введения сшивающего агента не превышало 1 часа.
Обработанный пучок углеродных волокон или углеродное моноволокно извлекают вместе с рамкой и располагают в вертикальном состоянии в вакуумной печи.
Электропроводящую матрицу, осевшую на пучке углеродных волокон или углеродном моноволокне, отверждают в течение 1-2 часов в вакуумной печи при температуре не менее 90 и не более 170°С, поддерживая давление паров растворителя не более 50 Па.
После отверждения электропроводящей матрицы микроэлектрод можно покрыть изолирующим покрытием для электроизоляции всей поверхности за исключением концевых участков.
Для приготовления изолирующего покрытия смешивают мономер (диметилсилоксан) и сшивающий агент (метилгидросилоксан с платиновым комплексом в качестве катализатора) в массовом соотношении 10/1.
Раствор перемешивают в течение 5-10 минут, после чего вакуумируют до исчезновения пузырьков газа из жидкой смеси, что контролируют визуально.
В полученный раствор окунают рамку с закрепленным на ней микроэлектродом, после чего рамку извлекают и располагают в вертикальном положении в вакуумной печи.
Изолирующее покрытие, осевшее на микроэлектроде, отверждают в течение 1-2 часов в вакуумной печи при температуре не менее 90 и не более 170°С.
Пример 1.
Из углеродного волокна (Toray T700S, Toray Inc., 12000 моноволокон в пучке, ПАН-прекурсор) с диаметром моноволокна 10 мкм, был выделен пучок из примерно 50 углеродных моноволокон, который был отожжен в течение 20 минут при 350°С в открытом тигле в воздушной атмосфере.
Для растворения полидиметилсилоксана использовался гексан 95%. В 30 мл гексана был введен 1 г. мономера (диметилсилоксана), после чего в течение 10 мин раствор перемешивали на магнитной мешалке на средних оборотах.
Наночастицы аморфной фазы углерода предварительно просеяли на сите с ячейкой 120 мкм, после чего ввели в размешиваемый раствор в количестве 0.43 г, т.е. 30 массовых процентов. Раствор перемешивали в течение 10 мин.
Для диспергации углеродных наночастиц раствор поместили в ультразвуковую ванну и обработали ультразвуком в течение 30 мин, поддерживая постоянную температуру 30°С.
В перемешиваемый раствор ввели сшивающий агент (метилгидросилоксан с платиновым комплексом в качестве катализатора) в количестве 0.1 г., после чего раствор перемешивали в течение 5 мин.
В сосуд с перемешиваемым раствором ввели алюминиевую рамку с закрепленным на ней пучком углеродных волокон, рамку подвесили на крышке сосуда таким образом, что пучок располагался в центре объема раствора, после чего раствор перемешивали в течение 10 мин.
Для проникновения углеродных частиц в толщу пучка углеродных волокон сосуд с раствором и рамкой поместили в ультразвуковую ванну и обработали ультразвуком в течение 5 мин, под держивая постоянную температуру 30°С.
После этого рамку извлекли из раствора и закрепили в вертикальном положении в вакуумной печи. Электропроводящую матрицу отверждали с поддержанием давления паров гесана менее 50 Па в вакуумной печи в течение 3 ч при 90°С.
Для подготовки образцов для динамического механического анализа приготовили изолирующее покрытие путем смешивания 1 г. мономера (диметилсилоксана) и 0.1 г. сшивающего агента (метилгидросилоксана с платиновым комплексом в качестве катализатора). Полученную смесь перемешивали вручную в течение 5 мин, после чего вакуумировалии в течение 10 минут для удаления пузырьков газа.
Образец микроэлетрода длинной 20 мм разместили горизонтально, накрыли полимерной рамкой с отверстием размером 15 на 10 мм и 0.45 мм глубиной, после чего залили приготовленной смесью.
Рамку с залитым микроэлектродом вакуумировали в течение 15 минут для удаления пузырьков газа.
После вакуумации рамку с залитым микроэлектродом расположили в вакуумной печи горизонтально и выдержали при температуре 90°С в течение 1 часа.
На Фиг. 2 приведено СЭМ-изображение микроэлектрода, в состав которого входит пучок углеродных моноволокон, а на Фиг. 3 - фотография микроэлектрода.
Для изготовленного образца провели испытание на динамическое растяжение, при котором измерили модуль упругости при растяжении с деформацией 1%, с постоянной частотой 1 Гц, при постоянной температуре 37°С. Испытание провели на динамическом механическом анализаторе ТА Instruments Q800 (США).
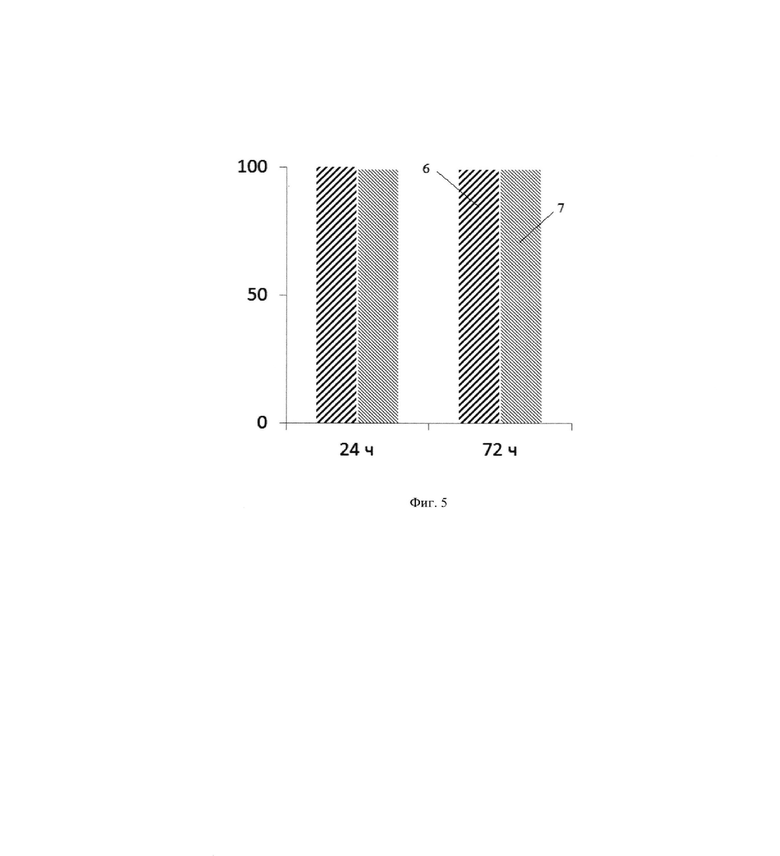
Результаты испытания показали, что модуль упругости микроэлектрода остается постоянным (кривая 4 на Фиг. 4) при растяжении и составляет 0.83 МПа. Кривая 4 является графиком изменения модуля упругости микроэлектрода, кривая 5 является графиком изменения модуля упругости углеродного волокна 1. При этом механические свойства нервной ткани известны из литературы: модуль упругости - от 10 кПа для центральной нервной системы до 5 МПа для периферических нервов [Ma, Z, Ни, S, Tan, JS, Myer, С., Njus, NM, Xia, Z. 2013. In vitro and in vivo mechanical properties of human ulnar and median nerves. J Biomed Mater Res Part A 2013: 101A: 2718- 2725.][Kerns, J., Piponov, H., Helder, C., Amirouche, F., Solitro, G. and Gonzalez, M. (2019), Mechanical Properties of the Human Tibial and Peroneal Nerves Following Stretch With Histological Correlations. Anat Rec, 302:2030-2039. https://doi.org/10.1002/ar.24250]. Таким образом, модуль упругости микроэлектрода лежит в диапазоне значений, характерном для нервной ткани.
Для установления биосовместимости микроэлектрода провели испытание на цитотоксичность для образцов самого микроэлектрода (без изолирующего покрытия) и отдельно для образцов изолирующего покрытия. Для оценки степени токсичности был проведен тест на выживаемость клеточной культуры в вытяжках образцов в водных растворах питательных сред (согласно ГОСТ ИСО-10993). Использовали мультипотентные мезенхимальные стромальные клетки (ММСК) человека, выделенные из пульпы зуба. Результаты испытания приведены на фиг.5, где Столбец 6 отражает жизнеспособность клеточной культуры после 24 и 72 часов инкубации в вытяжке образцов микроэлектрода; столбец 7 показывает жизнеспособность клеточной культуры после 24 и 72 часов инкубации в вытяжке образцов изолирующего покрытия 3.
Планшеты с клеточной культурой инкубровали в течение 24 часов при 37°С в увлажненной атмосфере с 5% CO2 для достижения монослоя. Через 24 часа в каждую лунку добавили по 200 мкл вытяжек. В контрольные добавили по 200 мкл свежей культуральной среды ДМЕМ (Gibco). Планшеты инкубировали в течение 24 и 72 часов при 37°С в увлажненной атмосфере с 5% CO2. Через 24 и 72 часа из каждой лунки отобрали по 250 мкл супернатанта, добавили по 50 мкл тест-системы CellTiter-Glo 2.0 и инкубировали на протяжении 30 минут. Для количественной оценки выживаемости провели спектрофотометрия образцов среды. Интенсивность люминесценции измеряли с помощью мультифункционального планшетного анализатора Victor Х3 (Perkin Elmer). Лунки, содержащие чистую культуральную среду без клеток, использовали для оценки фонового сигнала. Величина сигнала люминисценции от контрольных лунок приняли за 100% выживаемости, остальные значения выживаемости получили делением интенсивности люминсценции в заданной лунке на контрольную.
Результаты теста позволили сделать вывод о том, что микроэлектрод и изолирующее покрытие не оказывают цитотоксического эффекта.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НЕЙТРОНАЛЬНЫХ ИМПЛАНТОВ | 2021 |
|
RU2758972C1 |
| БЫСТРООТВЕРЖДАЕМЫЕ СИЛИКОНОВЫЕ СМАЗОЧНЫЕ ПОКРЫТИЯ | 2012 |
|
RU2630802C2 |
| СПОСОБ НАНЕСЕНИЯ ПОКРЫТИЯ НА ХИРУРГИЧЕСКИЕ ИГЛЫ | 2014 |
|
RU2674985C2 |
| СШИТЫЙ ОДНОНАПРАВЛЕННЫЙ ИЛИ МНОГООСНЫЙ АРМИРУЮЩИЙ НАПОЛНИТЕЛЬ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2616667C2 |
| ОДНОНАПРАВЛЕННЫЙ АРМИРУЮЩИЙ НАПОЛНИТЕЛЬ И СПОСОБ ПОЛУЧЕНИЯ ОДНОНАПРАВЛЕННОГО АРМИРУЮЩЕГО НАПОЛНИТЕЛЯ | 2013 |
|
RU2617484C2 |
| УГЛЕРОДНОЕ ВОЛОКНО ДЛЯ КОМПОЗИТНЫХ МАТЕРИАЛОВ С УЛУЧШЕННОЙ ЭЛЕКТРОПРОВОДНОСТЬЮ | 2012 |
|
RU2615427C1 |
| УСТРОЙСТВА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ОБЛАДАЮЩИХ АНТИПРОГЕСТИНОВЫМИ СВОЙСТВАМИ | 2000 |
|
RU2228170C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО МАТЕРИАЛА | 2011 |
|
RU2473368C1 |
| АДДИТИВНОЕ ПРОИЗВОДСТВО С ИСПОЛЬЗОВАНИЕМ РЕАКТИВНЫХ КОМПОЗИЦИЙ | 2018 |
|
RU2740061C1 |
| ВЫСОКОЭЛАСТИЧНЫЕ ПОЛИМЕРНЫЕ МЕМБРАНЫ ДЛЯ ПРОЦЕССА РАЗДЕЛЕНИЯ | 2018 |
|
RU2726354C1 |
Изобретение относится к области медицины, а именно к имплантируемым медицинским устройствам для детектирования внеклеточных электрических потенциалов и/или возбуждения потенциалов действия путем электростимуляции. Композиционный биосовместимый микроэлектрод состоит из расположенного в электропроводящей матрице сердечника в виде отожженного углеродного моноволокна диаметром 5-10 мкм или пучка углеродных волокон до 100 штук и имеет внешнее изолирующее покрытие. Матрица представляет собой композиционный материал из полидиметилсилоксана с содержанием частиц проводящего наполнителя в виде углеродных микро- и наночастиц от 30 до 70% по массе. Внешнее покрытие состоит из полидиметилсилоксана, выполненного путем смешивания диметилсилоксана и метилгидросилоксана с платиновым комплексом в качестве катализатора в массовом соотношении 10/1. Достигается приближение механических свойств всего микроэлектрода к свойствам ткани периферического нерва, а именно уменьшение модуля упругости по сравнению с необработанным углеродным волокном. 5 ил., 1 пр.
Композиционный биосовместимый микроэлектрод для медицинского применения, состоящий из расположенного в электропроводящей матрице сердечника в виде отожженного углеродного моноволокна диаметром 5-10 мкм или пучка углеродных волокон до 100 штук и имеющий внешнее изолирующее покрытие, причем матрица представляет собой композиционный материал из полидиметилсилоксана с содержанием частиц проводящего наполнителя в виде углеродных микро- и наночастиц от 30 до 70% по массе, а внешнее покрытие состоит из полидиметилсилоксана, выполненного путем смешивания диметилсилоксана и метилгидросилоксана с платиновым комплексом в качестве катализатора в массовом соотношении 10/1.
| US 2017169912 A1, 15.06.2017 | |||
| US 2014249645 A1, 04.09.2014 | |||
| US 2017347925 A1, 07.12.2017 | |||
| EA 201492080 A1, 30.06.2015 | |||
| RU 2014109864 A, 27.10.2015 | |||
| WO 2012129527 A2, 27.09.2012 | |||
| US 2012109167 A1, 03.05.2012 | |||
| JP 2009115828 A, 28.05.2009. |
Авторы
Даты
2024-11-05—Публикация
2022-12-14—Подача