Изобретение относится к области медицины, а именно к нефрологии и может использоваться с целью диагностики тяжелых когнитивных нарушений (деменции) у пациентов с хронической болезнью почек 5Д стадии.
Хроническая болезнь почек (ХБП) – это объединенное понятие, включающее любые заболевания почек, которые длятся три и более месяца, с повреждением анатомических структур почек и заменой их фиброзной тканью, приводящей к нарушению функции органа (Хроническая болезнь почек. Клинические рекомендации. М. - 2021. С. 11). ХБП имеет неуклонно прогрессирующий характер. Степень прогрессирования зависит от многих причин, но главным образом, от действия различных этиологических факторов (Хроническая болезнь почек. Клинические рекомендации. М. - 2021. С. 12). Замещение почечной ткани на фиброзную влияет на функцию почек, приводя к ее снижению. Общепринятой клинической классификацией снижения почечной функции является классификация KDIGO (Клинические практические рекомендации KDIGO 2021 по лечению гломерулярных болезней. Нефрология и диализ. 2022. - Т.24. - № 4. – С 584), которая предусматривает деление на стадии. Наиболее тяжелой является 5 стадия ХБП.
Конечным этапом прогрессирования ХБП является распространенный процесс фиброзирования, при котором почки не могут выполнять свою функцию даже на минимальном уровне. В таких случаях пациенту показано проведение заместительной почечной терапии, с использованием гемодиализа и подготовка к трансплантации почки (Хроническая болезнь почек. Клинические рекомендации. М. - 2021. С. 17). Данный этап обозначается клиническим термином – терминальная почечная недостаточность (ТПН) или ХБП 5 стадии. В то же время трансплантация почек является труднодоступным и дорогостоящим методом терапии, поэтому большинство пациентов получает терапию программным гемодиализом.
У больных, страдающих ХБП 5Д стадии, отмечается очень высокий риск развития сосудистых осложнений в виде фатального и нефатального характера (Батюшин М.М. Хроническая болезнь почек: современное состояние проблемы. Рациональная Фармакотерапия в Кардиологии 2020;16(6):938-947. DOI:10.20996/1819-6446-2020-11-06). Кроме того, больные ХБП 5Д характеризуются социальной дезадаптацией, низкой трудоспособностью и ограничением в самообслуживании. Проблема ТПН и ХБП 5Д представляет собой медико-социальную и несет большое экономическое бремя, в связи с чем актуальным представляется изучение и внедрение систем диагностики и прогнозирования развития ранних и поздних осложнений.
Одним из распространенных осложнений при ХБП 5Д является нарушение когнитивных функций пациента, которое проявляется в снижении памяти, внимания, нарушении речи, праксиса, управляющих функций, восприятия (Мухин Н.А. и др. Хроническая болезнь почек и сосудистая деменция. Терапевтический архив. 2014, 86(6), стр.7-10, Хрулёв А.Е., Студяникова С.Ф., Ланграф С.В., Садырин Р.В., Григорьева В.Н. Когнитивные нарушения у пациентов, находящихся на программном гемодиализе. Неврологический вестник. 2019 - Т. LI. - № 2. – С. 37). Нарушения когнитивных функций могут быть разной степени выраженности – от легких форм до тяжелых. При тяжелых дисфункциях (деменции) нарушается способность к социально-бытовой и профессиональной адаптации, происходит утрата привычного функционирования различной степени тяжести (Клинические рекомендации «Когнитивные расстройства у пациентов пожилого и старческого возраста». Журнал неврологии и психиатрии им. С.С. Корсакова. 2021. – Т.121. - №10-3. – С. 7). Очевидно, что развитие терминальной стадии почечной недостаточности требует высокой приверженности к лечению, частых визитов к врачу и контакта с ним, а в условии развития деменции полное соблюдение данных требований становится практически невозможным, вследствие чего снижается эффективность лечения и ухудшается прогноз заболевания таких пациентов.
Происхождение деменции при ХБП 5Д стадии носит вариабельный характер. Главной причиной развития деменции является уремия, то есть повышение в крови азотсодержащих веществ, которые накапливаются из-за критического снижения фильтрационной способности почек. Формируется эндогенная интоксикация, повышается активность провоспалительных медиаторов, то есть биологически активных веществ, участвующих в воспалении и необратимом изменении сосудистой стенки, в том числе вещества головного мозга. Следует отметить, что чем более выражена активность данных патологических процессов, тем чаще развиваются когнитивные нарушения и деменция в данной группе больных. Однако, не все пациенты с ХБП 5Д имеют тяжелые когнитивные нарушения, то есть деменцию, поскольку патологический процесс ее развития включает и другие механизмы.
В клинической практике для диагностики когнитивных нарушений и их тяжести используют различные шкалы (Клинические рекомендации «Когнитивные расстройства у пациентов пожилого и старческого возраста». Журнал неврологии и психиатрии им. С.С. Корсакова. 2021. – Т.121. - №10-3. – С. 31). Чаще всего пациенту предлагается ответить на ряд вопросов, представленных в печатном виде. При этом необходимо соблюдать определенные условия, например, проведение тестирования в утренние часы, исключение внешних раздражителей, достаточная освещенность помещения и т.д. Учитывая состояние пациента при наличии деменции получение достоверного результата нередко представляется труднодостижимым. Этот приобретает еще большее значение в условиях коморбидности, в частности, при наличии ТПН, которая характеризуется развитием и прогрессированием соответствующих симптомов (повышение артериального давления, синдром задержки жидкости и т.д.), расширяющих манифестацию патологии почек и маскирующих основной патологический процесс.
В настоящее время нет единого подхода к верификации деменции у пациентов с ХБП 5Д на основании тяжести течения основной патологии, то есть особенностей патогенетических механизмов. Стандартами диагностики наличия деменции являются оценочные шкалы, применение которых сопряжено с техническими трудностями и недостаточно точной оценкой тяжелых когнитивных расстройств. В связи с этим научный поиск в области ранней диагностики деменции у пациентов с ХБП 5Д, характеризующийся высокой чувствительностью и специфичностью метода и исключающий влияние субъективных параметров является востребованным и актуальным.
Изучение патентной и другой научной литературы не позволили определить высоко специфичные и чувствительные методы диагностики деменции у пациентов с ТПН, получающих лечение гемодиализом, с учетом патогенетических механизмов прогрессирования патологии почек, а также разработок, имеющих существенное сходство с предложенным нами методом, что позволяет определить новаторский характер изобретения.
Известен способ прогнозирования развития сосудистой субкортикальной деменции №2009146476/14 от 14.12.2009г, характеризующийся тем, что проводят магнитно-резонансную томографию головного мозга, определяют наличие артериальной гипертензии, ишемической болезни сердца, сахарного диабета, избыточной массы тела, вводят градации и числовые значения факторов риска, после чего определяют коэффициенты F1 и F2 по формулам: F1=-0,74 - 0,64·a1 - 0,59·a2 - 0,25·a3 + 0,85·a4 - 0,34·a5 + 0,84·a6 + 1,14·a7 - 1,67·a8 - 0,59·а9 - 1,68·а10 - 0,62·а11, F2=-7,75 + 2,28·a1 + 2,1·a2 + 0,9·a3 - 3,03·a4 + 1,2·a5 - 2,98·a6 - 4,05·a7 + 5,91·а8 + 2,08·а9 + 5,95·а10 + 2,2·а11, где а1 - а11 – градации факторов риска. После этого сравнивают значения полученных коэффициентов F1 и F2. При значении коэффициента F2 больше или равном F1 прогнозируют высокий риск развития субкортикальной деменции, при значении F1 больше F2 – низкий риск.
Недостатками данного способа является высокая трудозатратность и дороговизна метода, сложность вычисления коэффициентов, заявленных в способе, узкая диагностическая возможность определения деменции, связанной только с патологией субкортикальной области головного мозга, отсутствие специфичности метода в отношении пациентов с заболеванием почек.
Известен способ определения когнитивных нарушений «Адденбрукская когнитивная шкала (Addenbrooke’s Cognitive Examination, revised (ACE-R))» (Mioshi E, Dawson K, Mitchell J, Arnold R, Hodges JR. The Addenbrooke's Cognitive Examination Revised (ACE-R): a brief cognitive test battery for dementia screening. International Journal of Geriatric Psychiatry. – 2006. – V. 21. - № 11. – p. 1078-1085), характеризующийся тем, что пациенту предлагают ответить на ряд вопросов и выполнить тестовые задания, которые позволяют оценить ориентацию/внимание, запоминание, беглость речи, речь и зрительно-пространственное запоминание. По результатам ответов присваивается определенное количество баллов с максимальным значением 100 баллов. При сумме баллов от 82 до 88 устанавливалась вероятность деменции.
Известен способ определения когнитивных нарушений «Батарея тестов для оценки лобной дисфункции» [The Frontal Assessment Battery (FAB)] (Dubois B, Slachevsky A, Litvan I, Pillon B. The FAB: a frontal assessement battery at bedside. Neurology. – 2000. - № 55. – p. 1621 – 1626), характеризующийся тем, что пациенту предлагают выполнить ряд тестовых заданий, позволяющих оценить функцию обобщения, беглость речи, динамический праксис, простую и усложненную реакции выбора, хватательные рефлексы. Каждому тестовому заданию соответствует определенное количество балов. Далее производят подсчет суммы баллов пациента и определяют нарушение когнитивных функций, связанных с нарушением функции передних отделов головного мозга и лобно-подкорковых связей. Нормальными считают когнитивные функции при количестве баллов от 18 до 16, 15-12 баллов принимают за умеренное снижение когнитивных функций, при 11 баллах и меньше – признаки деменции.
Известен способ определения когнитивных нарушений «Тест свободного и ассоциированного селективного распознавания с непосредственным воспроизведением» [Free and Cued Selective Reminding Test – Immediate Recall (FCSRT-IR)] (Grober E, Buschke H, Crystal H, Bang S, Dresner R. Screening for dementia by memory testing. Neurology. – 1988. V. 38. - № 6. - p. 900 - 903, Ivnik RJ, Smith GE, Lucas JA, Tangalos EG, Kokmen E, Petersen RC. Free and cued selective reminding test: MOANS norms. J Clin Exp Neuropsychol. – 1997. – V. 19. - № 5. – p. 676 - 691), характеризующийся тем, что пациенту предлагают выполнить ряд тестовых заданий. Каждому тестовому заданию соответствует определенное количество балов. Далее производят подсчет суммы баллов, полученных после опроса больного и устанавливают нарушение когнитивной функции. При сумме баллов 27 и менее определяют прогноз развития деменции в течение двух лет. Способ основан на оценке свободного и суммарного воспроизведений, за счет индивидуальных показателей памяти и обучения.
Известен способ определения деменции «Модифицированная методика Мини-Ког» (Mini-Cog) (Borson S., Scanlan J.M., Chen P.J., et al. The Mini-Cog as a screen for dementia: Validation in a population-based sample. J Am Geriatr Soc 2003; 51: c. 1451-1454), характеризующийся тем, что пациенту предлагают выполнить ряд тестовых заданий на повторения, рисование, запоминания. Каждому заданию присваивается определенное количество баллов. По результатам теста подсчитывают количество баллов. При сумме баллов менее 3 устанавливают деменцию.
Известен способ определения тяжелых когнитивных нарушений «Тест «3 когнитивных нейропсихологических теста» (3-КТ)» (Гуторова Д.А., Васенина Е.Е., Левин О.С. Скрининг когнитивных нарушений у лиц пожилого и старческого возраста с помощью шкалы 3-КТ. Журнал неврологии и психиатрии им. СС Корсакова, Спецвыпуски. 2016; 116(6): c. 35-40), характеризующийся тем, что пациенту предлагают выполнить ряд тестовых заданий, которые позволяют определить зрительно-пространственные и регуляторные функции. Каждому заданию присваивается определенное количество баллов. Далее производят подсчет суммы баллов пациента. В случае любого отклонения от правильно выполненного теста регистрируют тяжелые когнитивные нарушения (деменцию).
Известен способ определения деменции «Клиническая рейтинговая шкала деменции» [Clinical Dementia Rating scale (CDR)] (Morris J.C. The clinical dementia rating (CDR). Current version and scoring rules. Neurology. 1993; 43: 2412-2413), характеризующийся тем, что пациенту предлагают выполнить тестовые задания, которые позволяют оценить нарушения памяти, ориентировки, мышления, социального взаимодействия, поведения и самообслуживания. По комплексу нарушений оценивается легкая, умеренная и тяжелая деменция.
Известен способ определения деменции «Опросник для скрининга деменции AD8» (Ascertain Dementia 8-item Informant Questionnaire) (Galvin J.E. et al. The AD8, a brief informant interview to detect dementia. Neurology 2005; 65: 559-564), характеризующийся тем, что пациенту предлагают ответить на тестовые задания. Каждому заданию присваивается 1 балл, при утвердительном ответе на вопрос. При сумме баллов 0-1 регистрируют нормальный когнитивный статус, а при сумме баллов выше 2 устанавливают деменцию.
Известен способ определения когнитивных нарушений «Монреальская шкала оценки когнитивных функций» (Nasreddine ZS, Phillips NA, Bédirian V, Charbonneau S, Whitehead V, Collin I, Cummings JL, Chertkow H. (2019). "The Montreal Cognitive Assessment, MoCA: A brief screening tool for mild cognitive impairment": Corrigendum. Journal of the American Geriatrics Society. – 2019. – V. 67. - № 9. – 1991. doi.org/10.1111/jgs.15925), характеризующийся тем, что пациенту предлагают набор тестов, в которых необходимо выполнить ряд заданий и ответить на вопросы в течение 10 минут. Каждому заданию присваивается определенное количество баллов. Затем проводится оценка когнитивных функций пациента методом подсчета суммы баллов – от 30 до 26 баллов принимают за норму, при 25 баллах и менее диагностируют снижение когнитивной функции. Данный способ позволяет определить нарушение когнитивных функций за счет оценки внимания и концентрации, управляющих функций, памяти, языка, зрительно-конструктивных навыков, абстрактного мышления, счета и ориентации пациента.
Известен способ определения когнитивных нарушений «Краткая шкала оценки психического статуса» [Mini Mental State Examination (MMSE)] (Folstein M.F., Folstein S.E., McHugh P.R. «Mini-mental state». A practical method for grading the cognitive state of patients for the clinician. Journal of psychiatric research. 1975; 12(3): 189-198), характеризующийся тем, что пациенту предлагают выполнить ряд тестовых заданий, оценивающих ориентацию во времени и месте, восприятие, концентрацию внимания, память, речевые функции. Каждому заданию присваивается определенное количество баллов. Затем, по результатам ответов пациента, оценивают индивидуальный балл и определяют нарушение когнитивных функций. При 25-30 баллах регистрируют недементные расстройства или норму, при 24-20 баллах – деменцию легкой степени выраженности, при 19-11 баллах – деменцию умеренной степени выраженности, а при 0-10 баллах – тяжелую деменцию.
Недостатками представленных способов являются специфичность определения деменции, связанной с заболеваниями головного мозга, субъективность оценки, зависящая от уровня образования пациента, окружающей обстановки, а также вероятности запоминания тестовых заданий при неоднократном использовании шкал, отсутствие зависимости с патогенетическими механизмами заболеваний почек.
Известны способы оценки нарушения отдельных когнитивных функций, основанных на тестовых заданиях, таких как зрительно-пространственные и управляющие функции (Тест рисования часов, The Clock Drawing Test (CDT). Nishiwaki Y., Breeze E., Smeeth L. et al. Validity of the Clock-Drawing Test as a screening tool for cognitive impairment in the elderly. Am J Epidemiol. 2004; 160(8): c. 797 – 807), память и обучение (Тест свободного и ассоциированного селективного распознавания с непосредственным воспроизведением, Free and Cued Selective Reminding Test – Immediate Recall (FCSRT-IR). Grober E. et al. Screening for dementia by memory testing. Neurology. 1988; 38(6): c. 900 – 903. Ivnik R.J., Smith G.E., Lucas J.A. et al. Free and cued selective reminding test: MOANS norms. J Clin Exp Neuropsychol. 1997; 19(5): c. 676 – 691), мнестические функции (Тест 5 (12) слов, The 5-word test. Mormont E., Jamart J., Robaye L. Validity of the five-word test for the evaluation of verbal episodic memory and dementia in a memory clinic setting. J Geriatr Psychiatry Neurol. 2012; 25(2): c. 78-84), нарушения речевой активности различного генеза (Методика «вербальных ассоциаций» (литеральных и категориальных), Word fluency test. Borkowski J.G., Benton A., Spreen O. Word fluency and brain damage. Neuropsychologia. 1976; 5: c. 135 – 140), нарушение мыслительных процессов и концентрации внимания (Тест символьно-цифрового кодирования. The Symbol Digit Modalities Test. Kiely K.M., Butterworth P., Watson N., Wooden M. The Symbol Digit Modalities Test: Normative Data from a Large Nationally Representative Sample of Australians. Archives of Clinical Neuropsychology 2014; 29(8): c. 767-775), нарушение номинативной функции речи и зрительного восприятия (Бостонский тест называния. Boston Naming Test (BNT). Kaplan E.F., Goodglass H., Weintraub S. The Boston Naming Test (2nd ed.). Lea & Febiger. Philadelphia, 1983; 120 с. Zec R.F., Burkett N.R., Markwell S.J., Larsen D.L. Normative data stratified for age, education, and gender on the Boston Naming Test. Clin Neuropsychol. 2007; 21(4): 617- 637), нарушение свойств переключения и распределения внимания, темпа и сенсомоторных реакций (Методика «Таблицы Шульте». Рубинштейн С. Я. Экспериментальные методики патопсихологии. - М.: ЗАО Изд-во ЭКСМО-Пресс, 1999. - 448 с), нарушение внимания, скорости мыслительных процессов, зрительно-моторной координации, управляющих функций (Тест слежения. Trail Making Test (TMT). Reitan R.M. Validity of the Trail Making test as an indicator of organic brain damage. Percept. Mot. Skills. 1958; 8: 271 – 276. Tombaugh T.N. Trail Making Test A and B: Normative data stratified by age and education. Archives of Clinical Neuropsychology. 2004; 19: 203 – 214).
Недостатками данных способов является специфичность для отдельных нарушений когнитивных функций, то есть, отсутствие полной диагностики когнитивных функций, включая деменцию, субъективность оценки, зависящей от уровня образования пациента, окружающей обстановки, а также вероятности запоминания тестовых заданий при неоднократном использовании шкал, отсутствие патогенетически обоснованной связи с основным заболеванием, в частности, патологией почек.
Наиболее близким способом диагностики деменции, выбранным нами за прототип в виду того, что данный способ направлен на диагностику деменции, включающую оценку патологических изменений при заболевании, является способ молекулярной диагностики состояния психосоматической функции у пациентов с дисциркуляторной энцефалопатией № 2531922 от 27.10.2014, характеризующийся тем, что у пациентов с дисциркуляторной энцефалопатией проводят стандартное терапевтическое, неврологическое и инструментальное исследование, затем определяют титры первичных антител к белку S100B в сыворотке крови. При титре антител до 150 диагностируют у пациентов с дисциркуляторной энцефалопатией 3-й степени с когнитивными нарушениями, достигающими умеренной или тяжелой деменции.
Недостатками данного способа, взятого за прототип, являются неспецифичность когорты больных, имеющих дисциркуляторную энцефалопатию, дороговизна молекулярного исследования, низкая чувствительность метода, которая характеризуется широкой специфичностью антител белка S100B к повреждениям клеток других систем организма (сосудистой и иммунной).
Таким образом, выполненный нами поиск научной и патентной литературы не позволил определить оптимальный способ диагностики деменции у пациентов ХБП 5Д стадии, который бы обладал высокой точностью и чувствительностью, при минимизации субъективности и был основан на патогенетических механизмах развития деменции при ТПН.
Задачей заявляемого нами изобретения является разработка способа диагностики деменции у пациентов с ХБП 5Д стадии, с учетом патогенетических особенностей развития когнитивных нарушений у пациентов с патологией почек и характеризующийся высокой чувствительностью и специфичностью.
Технический результат достигается следующим образом. У пациента с ХБП5Д стадии, определяется в сыворотке крови уровни общего холестерина (ОХС), холестерина липопротеидов низкой плотности (ЛПНП), эндотелина, кальция и железа. Далее определяется вероятность развития деменции по формуле:
К = 1/(1+e-z)*100%
z = -16,69+2,26 × ХЛПНП+ 2,24 × ХСa+0,27 × Хend-2,6 × ХХС+0,28 × ХFe (1)
где К – коэффициент вероятности наличия деменции,
ХЛПНП – концентрация холестерина липопротеидов низкой плотности, ммоль/л,
ХСa – уровень кальция, ммоль/л,
Хend – уровень эндотелина-1, пг/мл,
ХХС – уровень холестерина, ммоль/л,
ХFe – концентрация железа, мкмоль/л.
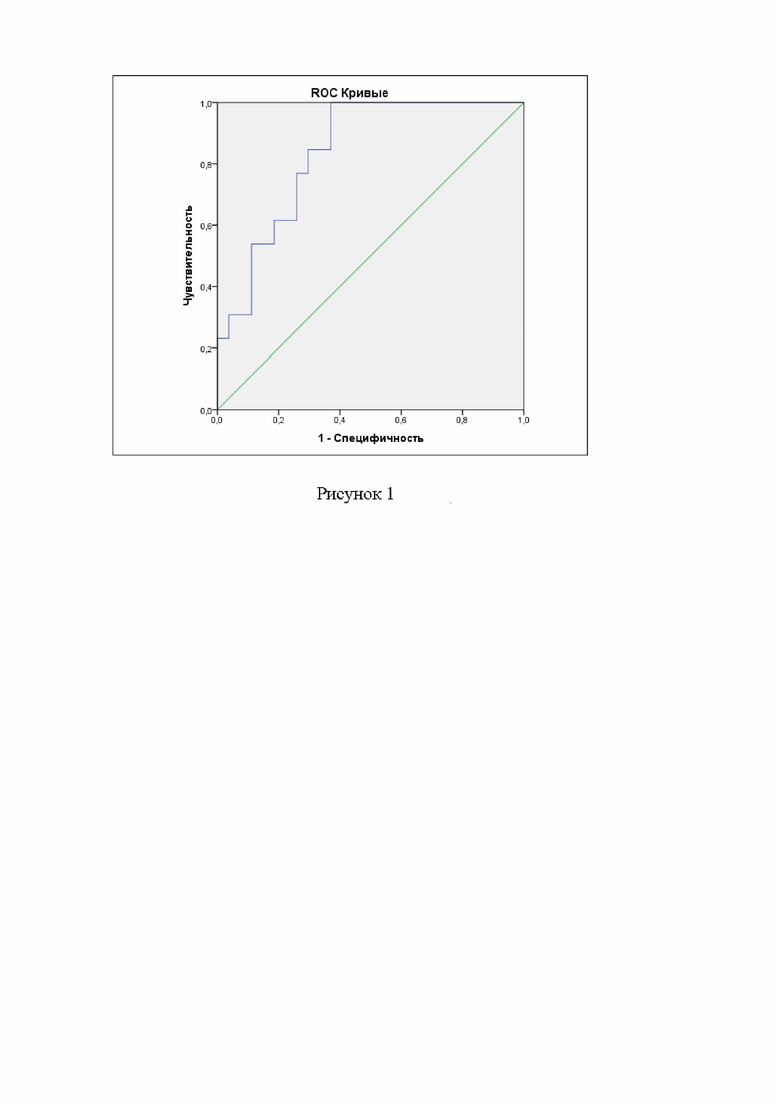
Полученная регрессионная модель является статистически значимой (p=0,01). Исходя из значения коэффициента детерминации Найджелкерка, модель (1) учитывает 44,0% факторов, определяющих вероятность развития деменции у пациентов с ХБП. Чувствительность модели составила 53,8%, специфичность – 88,9% (рис. 1). Диагностическая эффективность составила 77,5%.
Площадь под ROC-кривой, соответствующей диагностической значимости разработанной нами модели развития деменции у пациентов с ХБП 5Д, составила 0,84±0,061 с 95% ДИ: 0,72-0,96 (рис. 1). Полученная модель была статистически значимой (p=0,001). Пороговое значение коэффициента (К) – вероятности наличия деменции в точке cut-off равно 0,21. При уровне К равном или более 0,21 регистрировали наличие деменции, при значениях К менее 0,21 регистрировали отсутствие деменции.
Предложенная нами диагностическая модель была разработана следующим образом. В исследования были включены 80 больных с ХБП 5Д стадии. Всем пациентам, включенным в исследование, определяли наличие деменции согласно шкале «Краткая шкала оценки психического статуса» [Mini Mental State Examination (MMSE)]. Шкала MMSE была выбрана для диагностики деменции в исследуемой когорте пациентов, в связи с высокой распространенностью ее применения в реальной клинической практике и встречаемости в научной литературе при оценке когнитивного статуса у пациентов с ХБП. При количестве баллов менее 24 регистрируют наличие деменции и присваивают пациенту ранг 1. При количестве баллов более либо равном 24 регистрируют отсутствие деменции и присваивают пациенту ранг 2. Затем всем пациентам выполняют венепункцию с забором 5 мл венозной крови в пробирку. Далее пробирку отстаивают при комнатной температуре в течении 15-20 минут, в вертикальном положении. Затем пробирку центрифугируют в течение 12 минут при комнатной температуре на 2500 оборотах. Далее собирают сыворотку крови и разливают полученную сыворотку в эппендорфы, которые транспортируют в лабораторию для определения уровней ОХС, ЛПНП, эндотелина, кальция и железа.
Все полученные лабораторные данные, а также ранг отсутствия или наличия деменции по шкале MMSE были внесены в таблицу компьютерной прикладной программы Statistica 12.0. Далее производили статистический расчет имеющихся данных, с использованием логистической регрессии с последовательным анализом Вальда, коэффициента детерминации Найджелкерка и ROC-анализа для определения чувствительности и специфичности полученных данных. Результаты считали статистически достоверными при критерии Стьюдента (р) равном или менее 0,05, позволяющем оценить нулевые гипотезы.
В результате статистического анализа получена формула для диагностики деменции у пациентов с ХБП 5Д стадии по коэффициенту (К). При значениях К равном или более 0,21 регистрируют наличие деменции, при значениях К менее 0,21 регистрируют отсутствие деменции.
Чувствительность и специфичность метода (ROC-анализ) составили 100% и 63% соответственно.
Предложенный нами способ верификации деменции у пациентов с ХБП 5Д стадией характеризуется высокой чувствительностью и специфичностью метода, является простым, лишенным субъективного компонента диагностики, высокоинформативным и доступным, позволяющим поставить диагноз на ранней стадии и назначить лечебные и профилактические меры. Несомненным преимуществом предлагаемого способа является патогенетическая обоснованность, характеризующаяся применением лабораторных показателей, оценивающих тяжесть течения терминальной почечной недостаточности и представляющих собой объективную оценку когнитивного статуса. Более того, лабораторные показатели применяются в клинической практике при обследовании пациентов с заболеваниями почек. В то же время шкала оценки деменции MMSE является опросником, который не имеет привязки к соматическому статусу больного и не является специфичным в отношении этиологии патологического процесса.
Способ прошел апробацию в нефрологическом отделении клиники ФГБОУ ВО РостГМУ Минздрава России и в отделении диализа ФГБУЗ «Ростовская клиническая больница «ЮОМЦ ФМБА», в когорте пациентов с ХБП 5Д стадии.
Пример 1
Пациент А., 58 лет имеет диагноз хронического гломерулонефрита ХБП 5Д стадии (СКФ по CKD-EPI 14 мл/мин/1,73м2). Диагноз хронического гломерулонефрита установлен около 14 лет назад. Пациент получал лечение, согласно стандартам оказания нефрологической помощи. 4 года назад установлена ХБП 5 стадии, требующая проведения заместительной почечной терапии, в качестве которой был выбран гемодиализ. На момент обследования пациент предъявляет жалобы на выраженное снижение памяти, координации во времени, невозможность ясно выразить мысли. Установлено, что вес пациента 72 кг, индекс массы тела пациента 25,6 кг/м2. Пациент получает лечение программным гемодиализом 3 раза в неделю по 4 часа 40 минут. Пациенту выполнен тест MMSE, по результатам которого было определено 22 балла. Установлены следующие лабораторные показатели: ЛПНП – 5,36 ммоль/л, кальций – 0,9 ммоль/л, эндотелин - 52,98 пг/мл, ХС – 4,57 ммоль/л, железо – 5,13 мкмоль/л. Используя предлагаемую нами формулу для диагностики деменции было получено значение К=81,9, что свидетельствует о наличии деменции у пациента А. с ХБП 5Д стадией. Шкала MMSE также указывает на наличие деменции у данного пациента.
Пример 2
Пациент Н., 72 года имеет диагноз симптоматической артериальной гипертензии, хронического гломерулонефрита ХБП 5Д стадии (СКФ по CKD-EPI 12 мл/мин/1,73м2). Основной диагноз был установлен 3 года назад. Пациент нерегулярно получал лечение, согласно стандартам оказания нефрологической помощи, так как не был привержен к терапии. 6 месяцев назад поставлен диагноз ХБП 5 стадии, которая требовала проведения заместительной почечной терапии, в виде гемодиализа. На момент обследования пациент предъявляет жалобы на головокружения, периодическую потерю координации во времени и пространстве, выраженное снижение памяти и запоминания. Физикальный осмотр позволил определить вес пациента 70 кг, индекс массы тела пациента 24,5 кг/м2. Пациент получает лечение программным гемодиализом 3 раза в неделю по 4 часа 25 минут. Пациенту выполнен тест MMSE, по результатам которого было определено 29 баллов. Установлены следующие лабораторные показатели: ЛПНП – 5,21 ммоль/л, кальций – 1,01 ммоль/л, эндотелин – 35,44 пг/мл, ХС – 8,16 ммоль/л, железо – 11,2 мкмоль/л. Используя предлагаемую нами формулу для диагностики деменции было получено значение К=0,001 что свидетельствует об отсутствии деменции у пациента Н. с ХБП 5Д стадией. Шкала MMSE также указывает на отсутствие деменции у данного пациента.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ КОГНИТИВНЫХ НАРУШЕНИЙ У ПАЦИЕНТОВ МОЛОДОГО И ЗРЕЛОГО ВОЗРАСТА С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ | 2012 |
|
RU2504325C1 |
| СПОСОБ ДИАГНОСТИКИ САРКОПЕНИИ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ БОЛЕЗНЬЮ ПОЧЕК 5Д СТАДИИ, ПОЛУЧАЮЩИХ ЛЕЧЕНИЕ ПРОГРАММНЫМ ГЕМОДИАЛИЗОМ | 2020 |
|
RU2756154C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА, СОСУДИСТОЙ И СМЕШАННОЙ ДЕМЕНЦИИ | 2015 |
|
RU2578188C1 |
| СПОСОБ КОРРЕКЦИИ КОГНИТИВНЫХ НАРУШЕНИЙ У ПАЦИЕНТОВ С АРТЕРИАЛЬНОЙ ГИПЕРТОНИЕЙ НА ФОНЕ САХАРНОГО ДИАБЕТА 2 ТИПА | 2014 |
|
RU2555334C1 |
| Способ диагностики когнитивных нарушений у пациентов с ВИЧ-ассоциированной энцефалопатией в стадии СПИД | 2022 |
|
RU2785490C1 |
| СПОСОБ ДИАГНОСТИКИ СИНДРОМА СОСУДИСТЫХ УМЕРЕННЫХ КОГНИТИВНЫХ НАРУШЕНИЙ | 2006 |
|
RU2336531C2 |
| Способ прогнозирования вероятности развития болезни Альцгеймера (БА) | 2017 |
|
RU2663451C1 |
| Способ диагностики когнитивных нарушений у беременных с гипертензивными расстройствами | 2022 |
|
RU2792740C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ГРУППЫ ЛИЦ С ПОВЫШЕННЫМ РИСКОМ РАЗВИТИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2021 |
|
RU2781612C1 |
| Способ определения типов когнитивных расстройств у больных церебральной микроангиопатией | 2018 |
|
RU2696684C1 |
Изобретение относится к медицине, а именно к нефрологии, и может быть использовано для диагностики деменции у пациентов с хронической болезнью почек 5Д стадии. Определяют в крови уровни липопротеидов низкой плотности, кальция, эндотелина, общего холестерина, железа. Определяют коэффициент (К) по формуле: К=1/(1+e-z)*100%, z=-16,69+2,26 × ХЛПНП+2,24 × ХСa+0,27 × Хend-2,6 × ХХС+0,28 × ХFe, где К - коэффициент вероятности наличия деменции, ХЛПНП - концентрация холестерина липопротеидов низкой плотности, ммоль/л, ХCa - уровень кальция, ммоль/л, Хend - уровень эндотелина, пг/мл, ХХС - уровень холестерина, ммоль/л, ХFe - концентрация железа, мкмоль/л. При К более или равном 0,21 диагностируют деменцию. При К менее 0,21 диагностируют отсутствие деменции. Способ обеспечивает возможность диагностики деменции у пациентов с хронической болезнью почек 5Д стадии, с учетом патогенетических особенностей развития когнитивных нарушений у пациентов с патологией почек, с высокой чувствительностью и специфичностью, за счет определения в крови пациента уровней общего холестерина, холестерина липопротеидов низкой плотности, эндотелина, кальция и железа, и использования оригинального уравнения. 1 ил., 2 пр.
Способ диагностики деменции у пациентов с хронической болезнью почек 5Д стадии, заключающийся в том, что определяют в крови уровни липопротеидов низкой плотности, кальция, эндотелина, общего холестерина, железа, определяют коэффициент (К) по формуле:
К = 1/(1+e-z)*100%
z = -16,69+2,26 × ХЛПНП+2,24 × Хca+0,27 × Хend-2,6 × ХХС+0,28 × ХFe,
где К - коэффициент вероятности наличия деменции,
ХЛПНП - концентрация холестерина липопротеидов низкой плотности, ммоль/л,
ХCa - уровень кальция, ммоль/л,
Хend - уровень эндотелина, пг/мл,
ХХС - уровень холестерина, ммоль/л,
ХFe - концентрация железа, мкмоль/л,
и при К более или равном 0,21 диагностируют деменцию; при К менее 0,21 диагностируют отсутствие деменции.
| МУХИН Н.А | |||
| и др | |||
| Хроническая болезнь почек и сосудистая деменция | |||
| Терапевтический архив | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| СПОСОБ ВЫЯВЛЕНИЯ ГЕНЕТИЧЕСКИХ ФАКТОРОВ РИСКА РАЗВИТИЯ ДЕМЕНЦИЙ АЛЬЦГЕЙМЕРОВСКОГО ТИПА НА ОСНОВЕ ГИДРОГЕЛЕВОГО МАТРИЧНОГО БИОЧИПА | 2022 |
|
RU2795795C1 |
| KR 2021070847 A, 15.06.2021 | |||
| WO 2019154900 A1, 15.08.2019 | |||
| WO 2013192522 A2, 27.12.2013 | |||
| JONG G.P | |||
| et al | |||
| Risk of new-onset dementia in patients with chronic kidney disease on statin users: A population-based | |||
Авторы
Даты
2025-01-14—Публикация
2023-10-29—Подача